Vorauszusetzende Kompetenzen fachlich: Stoffeigenschaften, Stoffklasse der Metalle; Atommodell (Schalenmodell), elektrostatische Gesetze; Ionen
|
|
|
- Susanne Schumacher
- vor 8 Jahren
- Abrufe
Transkript
1 Modulbeschreibung Schulart: Fach: Zielgruppen: Autor: Zeitumfang: Realschule Fächerverbund Naturwissenschaftliches Arbeiten (RS) 6 (RS), 8 (RS) Guido Hennrich Vier Stunden Die metallische Bindung ist gekennzeichnet durch frei bewegliche Elektronen im Metallgitter, die unter anderem für die elektrische Leitfähigkeit, den metallischen Glanz und die Verformbarkeit verantwortlich sind. In der vorliegenden Unterrichtseinheit wenden die Schüler/innen unter anderem Atommodelle an, um sich dem Verständnis dieser Art chemischer Bindungen zu nähern. Anhand von kleinen Versuchsaufbauten, Präsentationen und Filmmaterial werden die relevanten Prozesse anschaulich gemacht. (Modulbild: 2010 LMZ-BW/G. Hennrich) Vorauszusetzende Kompetenzen fachlich: Stoffeigenschaften, Stoffklasse der Metalle; Atommodell (Schalenmodell), elektrostatische Gesetze; Ionen 1
2 Unterrichtsverlauf 1. Stunde: Metalle Als Einstieg in das Thema dient ein kurzes Bilderrätsel ( Dalli-Klick ) der Präsentation, bei dem nacheinander vier Gegenstände erraten werden müssen. Nachdem die Lösungen bekannt sind, werden die SuS gefragt, welche Gemeinsamkeit alle Gegenstände trotz aller Unterschiedlichkeit aufweisen. Alle Gegenstände bestehen zum größten Teil aus Metallen. Metalle bilden die überwiegende Stoffklasse innerhalb der chemischen Elemente. Viele davon sind den SuS zumindest dem Namen nach aus dem vorangegangenen NWA-Unterricht bekannt. Mit Folie 47 der Präsentation werden noch einmal bekanntere Vertreter gezeigt. In einem begleitenden Unterrichtsgespräch wird den SuS zudem klar, dass die Wahl eines Metalls als Werkstoff nicht beliebig ist, sondern meistens an die Funktion oder die Herstellungsweise des Gegenstands gebunden ist. Folie 48 führt diesen Gedanken weiter. Den SuS wird der Filmausschnitt Metalle und : chemischer Bau der Metalle spezifische Eigenschaften (1:20, aus der DVD "Chemische Bindungen I: Metalle und Salze", Verleihnummer ) gezeigt. Im Anschluss an die Filmbetrachtung erhalten die SuS die kleine Aufgabe alltägliche Verwendungsmöglichkeiten von Metallen aufzuschreiben. Denkbar wäre an dieser Stelle des Unterrichts auch die Erstellung einer Mindmap zum Thema Metalle und ihre Verwendung. Am Ende der Einführung in das Thema soll den SuS bewusst sein, dass Metalle vielfache Verwendungen finden und nicht aus unserem Alltag wegzudenken sind. Folie 49 der Präsentation formuliert diesen Gedanken. Ein Steckbrief zu einem Metall, den die SuS einzeln oder in Gruppen als Hausaufgabe erarbeiten können, rundet die Themeneinführung ab (siehe Folie 50 der Präsentation). 2. Stunde: und Metalleigenschaften Am Stundenanfang wird zunächst der Gedanke aus der vorangegangenen Stunde aufgegriffen, dass die Funktion oder Herstellungsweise eines Gegenstands für die Auswahl des Metalls bestimmend ist. Hier kann auch das Arbeitsblatt Gebrauchsmetalle eingesetzt werden. Die Frage, wieso man Metalle für bestimmte Gegenstände nutzt, führt hin zu den Eigenschaften der Metalle. Mithilfe des Vorwissens der SuS über Stoffeigenschaften, werden schnell die typischen (allgemeinen) gemeinsamen Eigenschaften der Metalle erarbeitet und notiert (vgl. Folie 51 der Präsentation ). Daran knüpft sich die Frage an, woher zahlreiche Eigenschaften der Metalle rühren und der Aufbau der Metalle wird nun genauer betrachtet. Manche SuS wissen vielleicht noch aus der Filmbetrachtung in der 1. Stunde, dass Metalle aus Kristalliten bestehen (der kurze Filmausschnitt kann noch einmal wiederholt werden Metalle und : chemischer Bau der Metalle spezifische Eigenschaften (1:20, DVD siehe 1. Stunde)). Das Bild auf Folie 52 der Präsentation oder ein mitgebrachter verzinkter Gegenstand zeigen das sehr gut. 2
3 Kristallite bestehen aus regelmäßig geordneten Metallatomen. Die kurze Filmsequenz Metalle und : chemischer Bau der Metalle Metallgitter (0:20, DVD siehe 1. Stunde) zeigt dies im Modell. Der Aufbau eines Metalls scheint also auf den ersten Blick dem von Salzen zu gleichen. Wieso beide Stoffklassen aber so unterschiedliche Eigenschaften haben, erklärt Folie 53 und die Filmsequenz Metalle und : chemischer Bau der Metalle (1:30, DVD siehe 1. Stunde). Nach Betrachtung der Filmsequenz und der Folienanimation formulieren die SuS den Sachverhalt noch einmal selbst und notieren ihn gegebenenfalls auf. Im Folgenden wird nun auf einige Eigenschaften näher eingegangen, die aus der abgeleitet werden können. Zuerst einmal die elektrische Leitfähigkeit. Im Gegensatz zu Salzen sind Metalle in festem Zustand elektrisch Leitfähig. Dies können die SuS direkt aus dem Elektronengas-Modell der ableiten. Die interaktive Schaltfläche auf Folie 54 öffnet eine Animation zur elektrische Leitfähigkeit (Schaltfläche muss verlinkt sein). Nach deren Betrachtung erklären die SuS die elektrische Leitfähigkeit mit eigenen Worten. Gefestigt werden die Erkenntnisse anschließend mit dem FilmausschnittMetalle und : Leitfähigkeit und Schmelze Warum leitet Metall Strom? (1:20, DVD siehe 1. Stunde). 3. Stunde: Verformbarkeit, Schmelzpunkte Zu Beginn der Stunde werden kurz die Erkenntnisse aus der vorangegangenen Stunde wiederholt. Dann führt Folie 55 der Präsentation zum nächsten Teilthema - die Verformbarkeit von Metallen. Zunächst sehen die SuS ein Bild, in dem modellhaft ein bekannter Vorgang beschrieben wird: Ein Salzkristall zerspringt, wenn man mechanische Gewalt auf ihn ausübt. Die SuS erklären mit ihrem Vorwissen über die Ionenbindung diesen Umstand. Eine nachfolgende Betrachtung der Filmsequenz Salze und Ionenbindungen: Eigenschaften von Salzen Warum sind Salze spröde und brüchig? (1: 50, DVD siehe 1. Stunde) bringt alle SuS auf den gleichen Wissensstand. Das zweite Bild der Folie 55 zeigt ebenfalls modellhaft das Verhalten eines Metalls, wenn man mechanische Gewalt darauf ausübt. Die SuS wissen aus eigener Erfahrung, dass Metalle sich dabei verformen und nicht wie Salze zerspringen. Um zu verstehen, wieso das so ist, wird den SuS die Animation Was passiert bei der Verformung? gezeigt. Zunächst beschreiben sie das Gezeigte. Dann versuchen sie mit ihrem Wissen von den delokalisierten Elektronen ( Elektronengas ) in Metallen und der gesehenen Animation selbst zu erklären, wieso Metalle sich verformen und nicht zerspringen. Metalle sind aber nicht immer gut verformbar. Manche sind sogar sehr brüchig, so wie z.b. Gusseisen. Dass und wie die Verformbarkeit der Metalle beeinflussbar ist, können die SuS in einem einfachen Versuch nachvollziehen. Der Versuch Formbarkeit von Metall ist auch in der Filmsequenz Metalle und : Kristallite und Formbarkeit (5:20, DVD siehe 1. Stunde) zu sehen. Bei der anschließenden Betrachtung der o. g. Filmsequenz erfahren die SuS, woher die unterschiedliche Formbarkeit herrührt. An die Filmbetrachtung schließt sich ein kurzes Unterrichtsgespräch an, in dem die wesentlichen Punkte, wann ein Metall besonders gut verformbar ist, wann es brüchig 3
4 ist und wie man die Verformbarkeit beeinflussen kann, herausgearbeitet werden. Die Ergebnisse werden stichwortartig festgehalten, bzw. fließen in das Versuchsergebnis des o. g. Versuchs ein (vgl. Formbarkeit von Metall Lösung). Die Größe der Kristallite und die Abstände zwischen ihnen erklären zwar die Verformbarkeit der Metalle, sie erklären jedoch nicht, wieso die Metalle so unterschiedliche Schmelzpunkte oder verschiedene Härten haben. In Folie 56 der Präsentation wird diese Frage gestellt. Um dies zu erklären, muss man sich noch einmal tiefer auf die Ebene der Atome begeben. Der Film Metalle und : Leitfähigkeit und Schmelze Warum haben unterschiedliche Metalle verschiedene Schmelzpunkte? (2:50, DVD siehe 1. Stunde) stellt die Zusammenhänge sehr gut dar. Nachdem die SuS ihn angesehen haben, werden sie aufgefordert einen Merksatz formulieren, in welchem die Atomgröße und Ladung des Atomrumpfs mit den Schmelzpunkten und der Härte der Metalle in Beziehung gesetzt wird. Beispiel: Ein Metall ist umso weicher und hat einen umso niedrigeren Schmelzpunkt, je geringer die Ladung seines Metallrumpfs (Metallions) ist und je größer der Metallrumpf und damit der Abstand zu den delokalisierten Elektronen ist. Der Zusammenhang, der i. d. R. zwischen Atomgröße und Schmelzpunkt/Härte herrscht, erschließt sich den SuS besonders gut anhand ihrer Kenntnisse über die Eigenschaften der Alkalimetalle. In der Elementfamilie ist das Element mit dem größten Atom auch das weichste und das mit dem niedrigsten Schmelzpunkt. Die zwei abschließenden Fragen auf Folie 56 der Präsentation dazu zeigen, ob die SuS die Zusammenhänge richtig verstanden haben. Der Atomrumpf des Quecksilbers hat eine zweifach positive Ladung. Das Atom ist mit 6 Elektronenschalen sehr groß, sodass die Anziehung zwischen den Metallionen und den delokalisierten Elektronen so schwach ist, dass es nicht für den festen Aggregatzustand reicht. Der Atomrumpf des (Halb-)Metalls Bor hat eine dreifache Ladung. Das Atom ist mit 2 Elektronenschalen sehr klein, sodass die Anziehung zwischen dem Metallion und den delokalisierten Elektronen sehr stark ist. Der Schmelzpunkt von Bor liegt bei ca C, seine Mohs-Härte hat den Wert 9,5. Es ist nach dem Diamant (Kohlenstoff) das zweithärteste Element. Folie 57 der Präsentation fasst die wichtigsten Aspekte der noch einmal kurz zusammen. 4. Stunde: Legierungen; beeinflussende Faktoren der elektrischen Leitfähigkeit 4
5 Die letzte Stunde zum Thema widmet sich den Metall-Legierungen. Folie 58 der Präsentation führt zum Thema hin. Jede/r SuS kennt Messing, eine häufig verwendete Legierung. Was aber ist Messing? Ein Metall? Vielleicht sogar ein Element? Eventuell weiß sogar der/die eine oder andere Schüler/in, dass es sich bei Messing um eine Legierung handelt. Dann wird als nächstes der Begriff Legierung geklärt: Legierungen sind Stoffgemische aus zwei oder mehr Metallen. Sie sind fest und haben metallische Eigenschaften. Manche Legierungen sind den SuS gut bekannt, ihre Zusammensetzung aber nicht. Dies könnte der Anlass sein eine kurze Rechercheaufgabe durchzuführen, wie sie Folie 59 der Präsentation formuliert. Die SuS können neben Messing z.b. nach der Zusammensetzung von Bronze, Hartblei oder Edelstahl suchen. Jedoch auch Weißgold, Lötzinn oder Neusilber bieten interessante Nachforschungsgegenstände. Folie 60 dient der Besprechung der Rechercheaufgabe. Es schließt sich die Frage an, wieso viele Gegenstände aus Legierungen hergestellt werden und nicht aus reinen Metallen worauf die SuS vermutlich selbst einige Antworten finden. Endgültige Klärung liefert die Filmsequenz Metalle und : Legierungen (3:00 DVD siehe 1. Stunde), in deren Anschluss die Gründe genannt und notiert werden. Man legiert Metalle, um je nach Anforderung, die an einen Gegenstand gestellt werden, gewünschte Eigenschaften zu erzielen: Härte, Zugfestigkeit, Verformbarkeit, Schmelzbarkeit, Korrosionsbeständigkeit usw. Hat man etwas Woodsche Legierung (Woodsches Metall) in seiner Chemikaliensammlung, kann man den Unterschied zu den reinen Metallen aus dem die Legierung besteht eindrucksvoll demonstrieren. Woodsche Legierung besteht aus 50 % Bismut, 25 % Blei, 12,5 % Zinn und 12,5 % Cadmium. Während die SuS die Schmelzpunkte der reinen Metalle heraussuchen, bringt man ein Becherglas Wasser zum Sieden. Gibt man dann eine Probe der Legierung in das nicht mehr kochende Wasser, schmilzt das Metall nach kurzer Zeit. Woodsches Metall hat einen Schmelzpunkt von ca. 71 C. Bismut hingegen schmilzt bei 271 C, Blei bei 327 C, Zinn bei 232 C und Cadmium bei 321 C. Aufgrund seines niedrigen Schmelzpunkts wird Woodsches Metall z. B. in elektrischen Sicherungen oder als Schmelzsicherung für Sprinkleranlagen genutzt. Auch die elektrische Leitfähigkeit in Metallen ist eine veränderliche Eigenschaft. Um dies zu zeigen, betrachten die SuS zunächst die Animationen Stromleitung in Metallen auf Folie 62 der Präsentation (Schaltfläche muss verlinkt sein). Sie schauen zuerst die Animation des Versuchs an und beschreiben die darin angedeuteten Veränderungen - dass durch das Erhitzen des Metalldrahts die Stromstärke sinkt und die Lampe weniger hell leuchtet. Danach betrachten die SuS die Modelldarstellung und erklären, warum die Stromstärke bei einem erwärmten Metall abnimmt. Die zwei Ergebnissätze dazu auf Folie 62 können notiert werden. Folie 63 versucht eine Parallele zwischen den schwingenden Atomrümpfen in erwärmten Metallen und den Fremdionen in Legierungen zu ziehen. Eine einfache Animation zeigt, dass die Metallionen des legierten Metalls die Elektronen beim Durchfluss bremsen. Mit Folie 64, die abschließende Informationen liefert, endet die Erarbeitung des Themas. Die Bearbeitung des Arbeitsblatts Lückentext und/oder des Arbeitsblatts Metalle Eigenschaften beschließt das Thema. 5
6 Bildungsplanbezug Realschule Fächerverbund Naturwissenschaftliches Arbeiten 1. KOMPETENZERWERB DURCH DENK- UND ARBEITSWEISEN Antworten und Erkenntnisse durch Kooperation und Kommunikation Die Schülerinnen und Schüler können mit Modellen sich selbst und anderen Phänomene beschreiben, dem Verstehen zugänglich machen und in einen Kontext einordnen 2. KOMPETENZERWERB DURCH DAS ERSCHLIESSEN VON PHÄNOMENEN, BEGRIFFEN UND STRUKTUREN Den Mikrokosmos und modellhafte Deutungen erfahren Die Schülerinnen und Schüler können ein Atommodell zur Erläuterung von Bindungsverhalten und zum Verständnis des Periodensystems der Elemente (PSE) anwenden Phänomene und Möglichkeiten ihrer Beschreibung erleben Die Schülerinnen und Schüler können elektrische Leitungsvorgänge in Metallen, Flüssigkeiten, Gasen, dem Vakuum und Halbleitern beschreiben (Aus: Bildungsplan Realschule, Klassen 5-10; Kompetenzen und Inhalte für Naturwissenschaftliches Arbeiten; Seiten 97, 100 und 101) Ausführliche Informationen zum Bildungsplan gibt es unter Bildung stärkt Menschen. 6
Grundlagen der Elektronik
 Grundlagen der Elektronik Wiederholung: Elektrische Größen Die elektrische Stromstärke I in A gibt an,... wie viele Elektronen sich pro Sekunde durch den Querschnitt eines Leiters bewegen. Die elektrische
Grundlagen der Elektronik Wiederholung: Elektrische Größen Die elektrische Stromstärke I in A gibt an,... wie viele Elektronen sich pro Sekunde durch den Querschnitt eines Leiters bewegen. Die elektrische
Vorauszusetzende Kompetenzen fachlich: Stoffeigenschaften; Atombau, Schalenmodell, elektrostatische Gesetze; Ionenbindung
 Modulbeschreibung Schulart: Fach: Zielgruppe: Autor: Zeitumfang: Realschule Fächerverbund Naturwissenschaftliches Arbeiten (RS) 10 (RS) Guido Hennrich Acht bis zehn Stunden Bei der (auch: kovalenten Bindung)
Modulbeschreibung Schulart: Fach: Zielgruppe: Autor: Zeitumfang: Realschule Fächerverbund Naturwissenschaftliches Arbeiten (RS) 10 (RS) Guido Hennrich Acht bis zehn Stunden Bei der (auch: kovalenten Bindung)
Werkstoffkunde Chemische Bindungsarten
 Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
Einen Wiederherstellungspunktes erstellen & Rechner mit Hilfe eines Wiederherstellungspunktes zu einem früheren Zeitpunkt wieder herstellen
 Einen Wiederherstellungspunktes erstellen & Rechner mit Hilfe eines Wiederherstellungspunktes zu einem früheren Zeitpunkt wieder herstellen 1 Hier einige Links zu Dokumentationen im WEB Windows XP: http://www.verbraucher-sicher-online.de/node/18
Einen Wiederherstellungspunktes erstellen & Rechner mit Hilfe eines Wiederherstellungspunktes zu einem früheren Zeitpunkt wieder herstellen 1 Hier einige Links zu Dokumentationen im WEB Windows XP: http://www.verbraucher-sicher-online.de/node/18
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
40-Tage-Wunder- Kurs. Umarme, was Du nicht ändern kannst.
 40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
Überprüfung der Bildungsstandards in den Naturwissenschaften. Chemie Marcus Mössner
 Überprüfung der Bildungsstandards in den Naturwissenschaften Bildungsstandards im Fach Chemie für den Mittleren Bildungsabschluss (Beschluss vom 16.12.2004) Die Chemie untersucht und beschreibt die stoffliche
Überprüfung der Bildungsstandards in den Naturwissenschaften Bildungsstandards im Fach Chemie für den Mittleren Bildungsabschluss (Beschluss vom 16.12.2004) Die Chemie untersucht und beschreibt die stoffliche
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Portfolio: "Die Ratten" von Gerhart Hauptmann
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Portfolio: "Die Ratten" von Gerhart Hauptmann Das komplette Material finden Sie hier: Download bei School-Scout.de Titel: man zum
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Portfolio: "Die Ratten" von Gerhart Hauptmann Das komplette Material finden Sie hier: Download bei School-Scout.de Titel: man zum
Gemeinschaftskunde (Gym) 9 (WRS/HS), 10 (WRS/HS), 10 (RS), 10 (Gym) Franco Mastrobattista Acht Stunden
 Modulbeschreibung Schularten: Fächer: Zielgruppen: Autor: Zeitumfang: Werkrealschule/Hauptschule; Realschule; Gymnasium Fächerverbund Welt-Zeit-Gesellschaft (WRS/HS); Fächerverbund Erdkunde - Wirtschaftskunde
Modulbeschreibung Schularten: Fächer: Zielgruppen: Autor: Zeitumfang: Werkrealschule/Hauptschule; Realschule; Gymnasium Fächerverbund Welt-Zeit-Gesellschaft (WRS/HS); Fächerverbund Erdkunde - Wirtschaftskunde
Vorwissen der SuS erfassen. Positive/Negative Aspekte von Online-Spielen feststellen. Urteilsfähigkeit der SuS trainieren.
 Unterrichtsverlauf Zeit/ Unterrichtsinhalt U-Phase (Lehrer- und Schüleraktivitäten) Kompetenzerwerb/Ziele Arbeitsform und Methoden Medien und weitere Materialien Stundenthema: Online-Spiele und ihre Nachteile
Unterrichtsverlauf Zeit/ Unterrichtsinhalt U-Phase (Lehrer- und Schüleraktivitäten) Kompetenzerwerb/Ziele Arbeitsform und Methoden Medien und weitere Materialien Stundenthema: Online-Spiele und ihre Nachteile
Adobe Photoshop. Lightroom 5 für Einsteiger Bilder verwalten und entwickeln. Sam Jost
 Adobe Photoshop Lightroom 5 für Einsteiger Bilder verwalten und entwickeln Sam Jost Kapitel 2 Der erste Start 2.1 Mitmachen beim Lesen....................... 22 2.2 Für Apple-Anwender.........................
Adobe Photoshop Lightroom 5 für Einsteiger Bilder verwalten und entwickeln Sam Jost Kapitel 2 Der erste Start 2.1 Mitmachen beim Lesen....................... 22 2.2 Für Apple-Anwender.........................
Angestrebte Kompetenzen/Ziele
 Unterrichtsverlauf zu: Unternehmensanalyse, 7-8 Std., Jahrgangstufe 2, Wirtschaft, WG 1. Std. Angestrebte Kompetenzen 5 Min. Stundenthema: Umweltanalyse Begrüßung und Einstieg in das Thema: Unternehmensanalyse
Unterrichtsverlauf zu: Unternehmensanalyse, 7-8 Std., Jahrgangstufe 2, Wirtschaft, WG 1. Std. Angestrebte Kompetenzen 5 Min. Stundenthema: Umweltanalyse Begrüßung und Einstieg in das Thema: Unternehmensanalyse
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Elektrische Spannung und Stromstärke
 Elektrische Spannung und Stromstärke Elektrische Spannung 1 Elektrische Spannung U Die elektrische Spannung U gibt den Unterschied der Ladungen zwischen zwei Polen an. Spannungsquellen besitzen immer zwei
Elektrische Spannung und Stromstärke Elektrische Spannung 1 Elektrische Spannung U Die elektrische Spannung U gibt den Unterschied der Ladungen zwischen zwei Polen an. Spannungsquellen besitzen immer zwei
Zahlenwinkel: Forscherkarte 1. alleine. Zahlenwinkel: Forschertipp 1
 Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
Modulbeschreibung. Erfindung: Schreibwerkzeug. Schularten: Fächer:
 Modulbeschreibung Schularten: Fächer: Zielgruppen: Autorin: Zeitumfang: Grundschule; Förderschule Fächerverbund Mensch, Natur und Kultur (GS); Fächerverbund Mensch, Natur und Kultur (FS) 4 (GS), Grundstufe
Modulbeschreibung Schularten: Fächer: Zielgruppen: Autorin: Zeitumfang: Grundschule; Förderschule Fächerverbund Mensch, Natur und Kultur (GS); Fächerverbund Mensch, Natur und Kultur (FS) 4 (GS), Grundstufe
Die Bundes-Zentrale für politische Bildung stellt sich vor
 Die Bundes-Zentrale für politische Bildung stellt sich vor Die Bundes-Zentrale für politische Bildung stellt sich vor Deutschland ist ein demokratisches Land. Das heißt: Die Menschen in Deutschland können
Die Bundes-Zentrale für politische Bildung stellt sich vor Die Bundes-Zentrale für politische Bildung stellt sich vor Deutschland ist ein demokratisches Land. Das heißt: Die Menschen in Deutschland können
Was meinen die Leute eigentlich mit: Grexit?
 Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Was meinen die Leute eigentlich mit: Grexit? Grexit sind eigentlich 2 Wörter. 1. Griechenland 2. Exit Exit ist ein englisches Wort. Es bedeutet: Ausgang. Aber was haben diese 2 Sachen mit-einander zu tun?
Zeichen bei Zahlen entschlüsseln
 Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Anwendungsbeispiele Buchhaltung
 Kostenstellen in Webling Webling ist ein Produkt der Firma: Inhaltsverzeichnis 1 Kostenstellen 1.1 Was sind Kostenstellen? 1.2 Kostenstellen in der 2 Kostenstellen in Webling 2.1 Kostenstellen erstellen
Kostenstellen in Webling Webling ist ein Produkt der Firma: Inhaltsverzeichnis 1 Kostenstellen 1.1 Was sind Kostenstellen? 1.2 Kostenstellen in der 2 Kostenstellen in Webling 2.1 Kostenstellen erstellen
Umgang mit Schaubildern am Beispiel Deutschland surft
 -1- Umgang mit Schaubildern am Beispiel Deutschland surft Im Folgenden wird am Beispiel des Schaubildes Deutschland surft eine Lesestrategie vorgestellt. Die Checkliste zur Vorgehensweise kann im Unterricht
-1- Umgang mit Schaubildern am Beispiel Deutschland surft Im Folgenden wird am Beispiel des Schaubildes Deutschland surft eine Lesestrategie vorgestellt. Die Checkliste zur Vorgehensweise kann im Unterricht
Geld Verdienen im Internet leicht gemacht
 Geld Verdienen im Internet leicht gemacht Hallo, Sie haben sich dieses E-book wahrscheinlich herunter geladen, weil Sie gerne lernen würden wie sie im Internet Geld verdienen können, oder? Denn genau das
Geld Verdienen im Internet leicht gemacht Hallo, Sie haben sich dieses E-book wahrscheinlich herunter geladen, weil Sie gerne lernen würden wie sie im Internet Geld verdienen können, oder? Denn genau das
Die Zentralheizung der Stadt Wer heizt wie?
 Die Zentralheizung der Stadt Wer heizt wie? Entwicklung der Fernwärme. Sie erheben, wie bei ihnen geheizt wird, und vergleichen mit der Situation in Wien und in den Bundesländern. Entwicklung der Zentralheizung
Die Zentralheizung der Stadt Wer heizt wie? Entwicklung der Fernwärme. Sie erheben, wie bei ihnen geheizt wird, und vergleichen mit der Situation in Wien und in den Bundesländern. Entwicklung der Zentralheizung
Anleitung zur Daten zur Datensicherung und Datenrücksicherung. Datensicherung
 Anleitung zur Daten zur Datensicherung und Datenrücksicherung Datensicherung Es gibt drei Möglichkeiten der Datensicherung. Zwei davon sind in Ges eingebaut, die dritte ist eine manuelle Möglichkeit. In
Anleitung zur Daten zur Datensicherung und Datenrücksicherung Datensicherung Es gibt drei Möglichkeiten der Datensicherung. Zwei davon sind in Ges eingebaut, die dritte ist eine manuelle Möglichkeit. In
Wie Sie mit Mastern arbeiten
 Wie Sie mit Mastern arbeiten Was ist ein Master? Einer der großen Vorteile von EDV besteht darin, dass Ihnen der Rechner Arbeit abnimmt. Diesen Vorteil sollten sie nutzen, wo immer es geht. In PowerPoint
Wie Sie mit Mastern arbeiten Was ist ein Master? Einer der großen Vorteile von EDV besteht darin, dass Ihnen der Rechner Arbeit abnimmt. Diesen Vorteil sollten sie nutzen, wo immer es geht. In PowerPoint
Sich einen eigenen Blog anzulegen, ist gar nicht so schwer. Es gibt verschiedene Anbieter. www.blogger.com ist einer davon.
 www.blogger.com Sich einen eigenen Blog anzulegen, ist gar nicht so schwer. Es gibt verschiedene Anbieter. www.blogger.com ist einer davon. Sie müssen sich dort nur ein Konto anlegen. Dafür gehen Sie auf
www.blogger.com Sich einen eigenen Blog anzulegen, ist gar nicht so schwer. Es gibt verschiedene Anbieter. www.blogger.com ist einer davon. Sie müssen sich dort nur ein Konto anlegen. Dafür gehen Sie auf
Lehrerhandbuch Unterrichtsstunde zum Mathematiklabor Thema Proportionalität. Universität Würzburg Lena Moser
 Lehrerhandbuch Unterrichtsstunde zum Mathematiklabor Thema Proportionalität Universität Würzburg Lena Moser Tafelbild Proportionalität Raupe auf Uhr r(ϕ)= ϕ Eigenschaft: Zellteilung exponentielles Wachstum
Lehrerhandbuch Unterrichtsstunde zum Mathematiklabor Thema Proportionalität Universität Würzburg Lena Moser Tafelbild Proportionalität Raupe auf Uhr r(ϕ)= ϕ Eigenschaft: Zellteilung exponentielles Wachstum
Die Dateiablage Der Weg zur Dateiablage
 Die Dateiablage In Ihrem Privatbereich haben Sie die Möglichkeit, Dateien verschiedener Formate abzulegen, zu sortieren, zu archivieren und in andere Dateiablagen der Plattform zu kopieren. In den Gruppen
Die Dateiablage In Ihrem Privatbereich haben Sie die Möglichkeit, Dateien verschiedener Formate abzulegen, zu sortieren, zu archivieren und in andere Dateiablagen der Plattform zu kopieren. In den Gruppen
Inhalt. 1 Einleitung AUTOMATISCHE DATENSICHERUNG AUF EINEN CLOUDSPEICHER
 AUTOMATISCHE DATENSICHERUNG AUF EINEN CLOUDSPEICHER Inhalt 1 Einleitung... 1 2 Einrichtung der Aufgabe für die automatische Sicherung... 2 2.1 Die Aufgabenplanung... 2 2.2 Der erste Testlauf... 9 3 Problembehebung...
AUTOMATISCHE DATENSICHERUNG AUF EINEN CLOUDSPEICHER Inhalt 1 Einleitung... 1 2 Einrichtung der Aufgabe für die automatische Sicherung... 2 2.1 Die Aufgabenplanung... 2 2.2 Der erste Testlauf... 9 3 Problembehebung...
Lichtbrechung an Linsen
 Sammellinsen Lichtbrechung an Linsen Fällt ein paralleles Lichtbündel auf eine Sammellinse, so werden die Lichtstrahlen so gebrochen, dass sie durch einen Brennpunkt der Linse verlaufen. Der Abstand zwischen
Sammellinsen Lichtbrechung an Linsen Fällt ein paralleles Lichtbündel auf eine Sammellinse, so werden die Lichtstrahlen so gebrochen, dass sie durch einen Brennpunkt der Linse verlaufen. Der Abstand zwischen
Studieren- Erklärungen und Tipps
 Studieren- Erklärungen und Tipps Es gibt Berufe, die man nicht lernen kann, sondern für die man ein Studium machen muss. Das ist zum Beispiel so wenn man Arzt oder Lehrer werden möchte. Hat ihr Kind das
Studieren- Erklärungen und Tipps Es gibt Berufe, die man nicht lernen kann, sondern für die man ein Studium machen muss. Das ist zum Beispiel so wenn man Arzt oder Lehrer werden möchte. Hat ihr Kind das
Anhand des bereits hergeleiteten Models erstellen wir nun mit der Formel
 Ausarbeitung zum Proseminar Finanzmathematische Modelle und Simulationen bei Raphael Kruse und Prof. Dr. Wolf-Jürgen Beyn zum Thema Simulation des Anlagenpreismodels von Simon Uphus im WS 09/10 Zusammenfassung
Ausarbeitung zum Proseminar Finanzmathematische Modelle und Simulationen bei Raphael Kruse und Prof. Dr. Wolf-Jürgen Beyn zum Thema Simulation des Anlagenpreismodels von Simon Uphus im WS 09/10 Zusammenfassung
Vorauszusetzende Kompetenzen methodisch: Teamarbeit; zuverlässiges und sachgerechtes Umgehen mit den Materialien; eigenständiges Arbeiten.
 Modulbeschreibung Schulart: Fächer: Zielgruppe: Autorin: Zeitumfang: Schule für Geistigbehinderte Bildungsbereich Selbstständige Lebensführung (SfGB); Bildungsbereich Natur, Umwelt, Technik (SfGB); Bildungsbereich
Modulbeschreibung Schulart: Fächer: Zielgruppe: Autorin: Zeitumfang: Schule für Geistigbehinderte Bildungsbereich Selbstständige Lebensführung (SfGB); Bildungsbereich Natur, Umwelt, Technik (SfGB); Bildungsbereich
Realschule; Gymnasium Deutsch (RS); Deutsch (Gym) 8 (RS), 8 (Gym) Dr. Jessica Lütge Zehn Stunden
 Modulbeschreibung Schularten: Fächer: Zielgruppen: Autorin: Zeitumfang: Realschule; Gymnasium Deutsch (RS); Deutsch (Gym) 8 (RS), 8 (Gym) Dr. Jessica Lütge Zehn Stunden Die Schülerinnen und Schüler erarbeiten
Modulbeschreibung Schularten: Fächer: Zielgruppen: Autorin: Zeitumfang: Realschule; Gymnasium Deutsch (RS); Deutsch (Gym) 8 (RS), 8 (Gym) Dr. Jessica Lütge Zehn Stunden Die Schülerinnen und Schüler erarbeiten
IT-Unternehmensarchitektur Übung 01: IT-Strategie
 IT-Unternehmensarchitektur Übung 01: IT-Strategie 29. April 2010 (Donnerstag) Fachgebiet Software-Architekturen, Prof. Dr. Robert Hirschfeld Dipl.-Math. Gernot Dern, Dipl.-Inform. (univ.) Wolfgang Keller,
IT-Unternehmensarchitektur Übung 01: IT-Strategie 29. April 2010 (Donnerstag) Fachgebiet Software-Architekturen, Prof. Dr. Robert Hirschfeld Dipl.-Math. Gernot Dern, Dipl.-Inform. (univ.) Wolfgang Keller,
Die Post hat eine Umfrage gemacht
 Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
Bedienungsanleitung. Matthias Haasler. Version 0.4. für die Arbeit mit der Gemeinde-Homepage der Paulus-Kirchengemeinde Tempelhof
 Bedienungsanleitung für die Arbeit mit der Gemeinde-Homepage der Paulus-Kirchengemeinde Tempelhof Matthias Haasler Version 0.4 Webadministrator, email: webadmin@rundkirche.de Inhaltsverzeichnis 1 Einführung
Bedienungsanleitung für die Arbeit mit der Gemeinde-Homepage der Paulus-Kirchengemeinde Tempelhof Matthias Haasler Version 0.4 Webadministrator, email: webadmin@rundkirche.de Inhaltsverzeichnis 1 Einführung
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Die Liebe und der Verlust
 Die Liebe und der Verlust Jeder Mensch hat in seinem Leben Zuneigung, Affinität oder Liebe zu einem anderen Menschen gehabt in einer Partnerschaft oder sogar einer Ehe. Gemeint ist eine Zeit, in der man
Die Liebe und der Verlust Jeder Mensch hat in seinem Leben Zuneigung, Affinität oder Liebe zu einem anderen Menschen gehabt in einer Partnerschaft oder sogar einer Ehe. Gemeint ist eine Zeit, in der man
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
infach Geld FBV Ihr Weg zum finanzellen Erfolg Florian Mock
 infach Ihr Weg zum finanzellen Erfolg Geld Florian Mock FBV Die Grundlagen für finanziellen Erfolg Denn Sie müssten anschließend wieder vom Gehaltskonto Rückzahlungen in Höhe der Entnahmen vornehmen, um
infach Ihr Weg zum finanzellen Erfolg Geld Florian Mock FBV Die Grundlagen für finanziellen Erfolg Denn Sie müssten anschließend wieder vom Gehaltskonto Rückzahlungen in Höhe der Entnahmen vornehmen, um
Wie sieht unsere Welt im Kleinen aus?
 Skriptum Wie sieht unsere Welt im Kleinen aus? 1 Wie sieht unsere Welt im Kleinen aus? Atom- und Quantenphysik für Kids Seminar im Rahmen der KinderUni Wien, 12. 7. 2005 Katharina Durstberger, Franz Embacher,
Skriptum Wie sieht unsere Welt im Kleinen aus? 1 Wie sieht unsere Welt im Kleinen aus? Atom- und Quantenphysik für Kids Seminar im Rahmen der KinderUni Wien, 12. 7. 2005 Katharina Durstberger, Franz Embacher,
Kreativ visualisieren
 Kreativ visualisieren Haben Sie schon einmal etwas von sogenannten»sich selbst erfüllenden Prophezeiungen«gehört? Damit ist gemeint, dass ein Ereignis mit hoher Wahrscheinlichkeit eintritt, wenn wir uns
Kreativ visualisieren Haben Sie schon einmal etwas von sogenannten»sich selbst erfüllenden Prophezeiungen«gehört? Damit ist gemeint, dass ein Ereignis mit hoher Wahrscheinlichkeit eintritt, wenn wir uns
Die Gesellschaftsformen
 Jede Firma - auch eure Schülerfirma - muss sich an bestimmte Spielregeln halten. Dazu gehört auch, dass eine bestimmte Rechtsform für das Unternehmen gewählt wird. Für eure Schülerfirma könnt ihr zwischen
Jede Firma - auch eure Schülerfirma - muss sich an bestimmte Spielregeln halten. Dazu gehört auch, dass eine bestimmte Rechtsform für das Unternehmen gewählt wird. Für eure Schülerfirma könnt ihr zwischen
Grundlagen der Elektrotechnik
 Grundlagen der Elektrotechnik Was hat es mit Strom, Spannung, Widerstand und Leistung auf sich Michael Dienert Walther-Rathenau-Gewerbeschule Freiburg 23. November 2015 Inhalt Strom und Spannung Elektrischer
Grundlagen der Elektrotechnik Was hat es mit Strom, Spannung, Widerstand und Leistung auf sich Michael Dienert Walther-Rathenau-Gewerbeschule Freiburg 23. November 2015 Inhalt Strom und Spannung Elektrischer
Die Wanderung von Ladung
 Die Wanderung von Ladung Eine lehrergesteuerte Unterrichtsstunde zum elektrischen Strom im Fach Physik Rahmen 9. Klasse mathematischer Zweig Lehrplaneinheit: 9.2 Elektrizitätslehre, bewegte elektrische
Die Wanderung von Ladung Eine lehrergesteuerte Unterrichtsstunde zum elektrischen Strom im Fach Physik Rahmen 9. Klasse mathematischer Zweig Lehrplaneinheit: 9.2 Elektrizitätslehre, bewegte elektrische
Sowohl die Malstreifen als auch die Neperschen Streifen können auch in anderen Stellenwertsystemen verwendet werden.
 Multiplikation Die schriftliche Multiplikation ist etwas schwieriger als die Addition. Zum einen setzt sie das kleine Einmaleins voraus, zum anderen sind die Überträge, die zu merken sind und häufig in
Multiplikation Die schriftliche Multiplikation ist etwas schwieriger als die Addition. Zum einen setzt sie das kleine Einmaleins voraus, zum anderen sind die Überträge, die zu merken sind und häufig in
Der Kalender im ipad
 Der Kalender im ipad Wir haben im ipad, dem ipod Touch und dem iphone, sowie auf dem PC in der Cloud einen Kalender. Die App ist voreingestellt, man braucht sie nicht laden. So macht es das ipad leicht,
Der Kalender im ipad Wir haben im ipad, dem ipod Touch und dem iphone, sowie auf dem PC in der Cloud einen Kalender. Die App ist voreingestellt, man braucht sie nicht laden. So macht es das ipad leicht,
Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium
 Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- & Medienbedarf
Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- & Medienbedarf
1 topologisches Sortieren
 Wolfgang Hönig / Andreas Ecke WS 09/0 topologisches Sortieren. Überblick. Solange noch Knoten vorhanden: a) Suche Knoten v, zu dem keine Kante führt (Falls nicht vorhanden keine topologische Sortierung
Wolfgang Hönig / Andreas Ecke WS 09/0 topologisches Sortieren. Überblick. Solange noch Knoten vorhanden: a) Suche Knoten v, zu dem keine Kante führt (Falls nicht vorhanden keine topologische Sortierung
Zukunftskonferenz. Behinderten-Sportverband Berlin e.v.
 Zukunftskonferenz Behinderten-Sportverband Berlin e.v. 27.09.2008 in Berlin - Fotoprotokoll- Führungs-Akademie, DOSB: Moderation und Planung Gabriele Freytag Klaus Schirra Protokoll: Führungs-Akademie
Zukunftskonferenz Behinderten-Sportverband Berlin e.v. 27.09.2008 in Berlin - Fotoprotokoll- Führungs-Akademie, DOSB: Moderation und Planung Gabriele Freytag Klaus Schirra Protokoll: Führungs-Akademie
Lernaufgabe Industriekauffrau/Industriekaufmann Angebot und Auftrag: Arbeitsblatt I Auftragsbeschreibung
 Angebot und Auftrag: Arbeitsblatt I Auftragsbeschreibung Ein Kunde hat Interesse an einem von Ihrem Unternehmen hergestellten Produkt gezeigt. Es handelt sich dabei um einen batteriebetriebenen tragbaren
Angebot und Auftrag: Arbeitsblatt I Auftragsbeschreibung Ein Kunde hat Interesse an einem von Ihrem Unternehmen hergestellten Produkt gezeigt. Es handelt sich dabei um einen batteriebetriebenen tragbaren
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL Modul: Versuch: Physikalische Eigenschaften I. VERSUCHSZIEL Die
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL Modul: Versuch: Physikalische Eigenschaften I. VERSUCHSZIEL Die
Frühjahr 2000, Thema 2, Der elektrische Widerstand
 Frühjahr 2000, Thema 2, Der elektrische Widerstand Referentin: Dorothee Abele Dozent: Dr. Thomas Wilhelm Datum: 01.02.2007 1) Stellen Sie ein schülergemäßes Modell für einen elektrisch leitenden bzw. nichtleitenden
Frühjahr 2000, Thema 2, Der elektrische Widerstand Referentin: Dorothee Abele Dozent: Dr. Thomas Wilhelm Datum: 01.02.2007 1) Stellen Sie ein schülergemäßes Modell für einen elektrisch leitenden bzw. nichtleitenden
Repetitionsaufgaben Wurzelgleichungen
 Repetitionsaufgaben Wurzelgleichungen Inhaltsverzeichnis A) Vorbemerkungen B) Lernziele C) Theorie mit Aufgaben D) Aufgaben mit Musterlösungen 4 A) Vorbemerkungen Bitte beachten Sie: Bei Wurzelgleichungen
Repetitionsaufgaben Wurzelgleichungen Inhaltsverzeichnis A) Vorbemerkungen B) Lernziele C) Theorie mit Aufgaben D) Aufgaben mit Musterlösungen 4 A) Vorbemerkungen Bitte beachten Sie: Bei Wurzelgleichungen
Handbuch ECDL 2003 Modul 2: Computermanagement und Dateiverwaltung Dateien löschen und wiederherstellen
 Handbuch ECDL 2003 Modul 2: Computermanagement und Dateiverwaltung Dateien löschen und wiederherstellen Dateiname: ecdl2_05_03_documentation Speicherdatum: 22.11.2004 ECDL 2003 Modul 2 Computermanagement
Handbuch ECDL 2003 Modul 2: Computermanagement und Dateiverwaltung Dateien löschen und wiederherstellen Dateiname: ecdl2_05_03_documentation Speicherdatum: 22.11.2004 ECDL 2003 Modul 2 Computermanagement
1. TEIL (3 5 Fragen) Freizeit, Unterhaltung 2,5 Min.
 EINFÜHRUNG 0,5 Min. THEMEN: Freizeit, Unterhaltung (T1), Einkaufen (T2), Ausbildung, Beruf (T3), Multikulturelle Gesellschaft (T4) Hallo/Guten Tag. (Nehmen Sie bitte Platz. Können Sie mir bitte die Nummer
EINFÜHRUNG 0,5 Min. THEMEN: Freizeit, Unterhaltung (T1), Einkaufen (T2), Ausbildung, Beruf (T3), Multikulturelle Gesellschaft (T4) Hallo/Guten Tag. (Nehmen Sie bitte Platz. Können Sie mir bitte die Nummer
Erfahrungen mit Hartz IV- Empfängern
 Erfahrungen mit Hartz IV- Empfängern Ausgewählte Ergebnisse einer Befragung von Unternehmen aus den Branchen Gastronomie, Pflege und Handwerk Pressegespräch der Bundesagentur für Arbeit am 12. November
Erfahrungen mit Hartz IV- Empfängern Ausgewählte Ergebnisse einer Befragung von Unternehmen aus den Branchen Gastronomie, Pflege und Handwerk Pressegespräch der Bundesagentur für Arbeit am 12. November
Anleitung zur Datensicherung und -rücksicherung in der VR-NetWorld Software
 Anleitung zur Datensicherung und -rücksicherung in der VR-NetWorld Software Damit Sie bei einer Neuinstallation auf Ihren alten Datenbestand zurückgreifen können, empfehlen wir die regelmäßige Anlage von
Anleitung zur Datensicherung und -rücksicherung in der VR-NetWorld Software Damit Sie bei einer Neuinstallation auf Ihren alten Datenbestand zurückgreifen können, empfehlen wir die regelmäßige Anlage von
Das große ElterngeldPlus 1x1. Alles über das ElterngeldPlus. Wer kann ElterngeldPlus beantragen? ElterngeldPlus verstehen ein paar einleitende Fakten
 Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Internet Explorer Version 6
 Internet Explorer Version 6 Java Runtime Ist Java Runtime nicht installiert, öffnet sich ein PopUp-Fenster, welches auf das benötigte Plugin aufmerksam macht. Nach Klicken auf die OK-Taste im PopUp-Fenster
Internet Explorer Version 6 Java Runtime Ist Java Runtime nicht installiert, öffnet sich ein PopUp-Fenster, welches auf das benötigte Plugin aufmerksam macht. Nach Klicken auf die OK-Taste im PopUp-Fenster
e LEARNING Kurz-Anleitung zum Erstellen eines Wikis 1. Wiki erstellen
 Kurz-Anleitung zum Erstellen eines Wikis Die Aktivität Wiki verschafft Ihnen die Möglichkeit, Wissen zu sammeln und zu strukturieren. Dabei können Sie die Teilnehmer Ihres Kurses an der Erstellung des
Kurz-Anleitung zum Erstellen eines Wikis Die Aktivität Wiki verschafft Ihnen die Möglichkeit, Wissen zu sammeln und zu strukturieren. Dabei können Sie die Teilnehmer Ihres Kurses an der Erstellung des
Informationsblatt Induktionsbeweis
 Sommer 015 Informationsblatt Induktionsbeweis 31. März 015 Motivation Die vollständige Induktion ist ein wichtiges Beweisverfahren in der Informatik. Sie wird häufig dazu gebraucht, um mathematische Formeln
Sommer 015 Informationsblatt Induktionsbeweis 31. März 015 Motivation Die vollständige Induktion ist ein wichtiges Beweisverfahren in der Informatik. Sie wird häufig dazu gebraucht, um mathematische Formeln
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 1 Einteilung der Stoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772 Nidfurn 055-654
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 1 Einteilung der Stoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772 Nidfurn 055-654
Fachbericht zum Thema: Anforderungen an ein Datenbanksystem
 Fachbericht zum Thema: Anforderungen an ein Datenbanksystem von André Franken 1 Inhaltsverzeichnis 1 Inhaltsverzeichnis 1 2 Einführung 2 2.1 Gründe für den Einsatz von DB-Systemen 2 2.2 Definition: Datenbank
Fachbericht zum Thema: Anforderungen an ein Datenbanksystem von André Franken 1 Inhaltsverzeichnis 1 Inhaltsverzeichnis 1 2 Einführung 2 2.1 Gründe für den Einsatz von DB-Systemen 2 2.2 Definition: Datenbank
Modellbildungssysteme: Pädagogische und didaktische Ziele
 Modellbildungssysteme: Pädagogische und didaktische Ziele Was hat Modellbildung mit der Schule zu tun? Der Bildungsplan 1994 formuliert: "Die schnelle Zunahme des Wissens, die hohe Differenzierung und
Modellbildungssysteme: Pädagogische und didaktische Ziele Was hat Modellbildung mit der Schule zu tun? Der Bildungsplan 1994 formuliert: "Die schnelle Zunahme des Wissens, die hohe Differenzierung und
Wie optimiert man die Werbungserkennung von Ad- Detective?
 Wie optimiert man die Werbungserkennung von Ad- Detective? Die Ad-Detective-Werbe-Erkennung von VideiReDo basiert auf der Erkennung von Schwarzwerten / scharzen Bildern, die die Werbeblöcke abgrenzen.
Wie optimiert man die Werbungserkennung von Ad- Detective? Die Ad-Detective-Werbe-Erkennung von VideiReDo basiert auf der Erkennung von Schwarzwerten / scharzen Bildern, die die Werbeblöcke abgrenzen.
Fachdidaktik der Informatik 18.12.08 Jörg Depner, Kathrin Gaißer
 Fachdidaktik der Informatik 18.12.08 Jörg Depner, Kathrin Gaißer Klassendiagramme Ein Klassendiagramm dient in der objektorientierten Softwareentwicklung zur Darstellung von Klassen und den Beziehungen,
Fachdidaktik der Informatik 18.12.08 Jörg Depner, Kathrin Gaißer Klassendiagramme Ein Klassendiagramm dient in der objektorientierten Softwareentwicklung zur Darstellung von Klassen und den Beziehungen,
Primzahlen und RSA-Verschlüsselung
 Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
3. Halbleiter und Elektronik
 3. Halbleiter und Elektronik Halbleiter sind Stoe, welche die Eigenschaften von Leitern sowie Nichtleitern miteinander vereinen. Prinzipiell sind die Elektronen in einem Kristallgitter fest eingebunden
3. Halbleiter und Elektronik Halbleiter sind Stoe, welche die Eigenschaften von Leitern sowie Nichtleitern miteinander vereinen. Prinzipiell sind die Elektronen in einem Kristallgitter fest eingebunden
In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können.
 Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Stellen Sie bitte den Cursor in die Spalte B2 und rufen die Funktion Sverweis auf. Es öffnet sich folgendes Dialogfenster
 Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
Professionelle Seminare im Bereich MS-Office
 Gegenüber PowerPoint 2003 hat sich in PowerPoint 2007 gerade im Bereich der Master einiges geändert. Auf Handzettelmaster und Notizenmaster gehe ich in diesen Ausführungen nicht ein, die sind recht einfach
Gegenüber PowerPoint 2003 hat sich in PowerPoint 2007 gerade im Bereich der Master einiges geändert. Auf Handzettelmaster und Notizenmaster gehe ich in diesen Ausführungen nicht ein, die sind recht einfach
! " # $ " % & Nicki Wruck worldwidewruck 08.02.2006
 !"# $ " %& Nicki Wruck worldwidewruck 08.02.2006 Wer kennt die Problematik nicht? Die.pst Datei von Outlook wird unübersichtlich groß, das Starten und Beenden dauert immer länger. Hat man dann noch die.pst
!"# $ " %& Nicki Wruck worldwidewruck 08.02.2006 Wer kennt die Problematik nicht? Die.pst Datei von Outlook wird unübersichtlich groß, das Starten und Beenden dauert immer länger. Hat man dann noch die.pst
Das Persönliche Budget in verständlicher Sprache
 Das Persönliche Budget in verständlicher Sprache Das Persönliche Budget mehr Selbstbestimmung, mehr Selbstständigkeit, mehr Selbstbewusstsein! Dieser Text soll den behinderten Menschen in Westfalen-Lippe,
Das Persönliche Budget in verständlicher Sprache Das Persönliche Budget mehr Selbstbestimmung, mehr Selbstständigkeit, mehr Selbstbewusstsein! Dieser Text soll den behinderten Menschen in Westfalen-Lippe,
Gimp Kurzanleitung. Offizielle Gimp Seite: http://www.gimp.org/
 Gimp Kurzanleitung Offizielle Gimp Seite: http://www.gimp.org/ Inhalt Seite 2 Seite 3-4 Seite 5-6 Seite 7 8 Seite 9 10 Seite 11-12 Ein Bild mit Gimp öffnen. Ein Bild mit Gimp verkleinern. Ein bearbeitetes
Gimp Kurzanleitung Offizielle Gimp Seite: http://www.gimp.org/ Inhalt Seite 2 Seite 3-4 Seite 5-6 Seite 7 8 Seite 9 10 Seite 11-12 Ein Bild mit Gimp öffnen. Ein Bild mit Gimp verkleinern. Ein bearbeitetes
Ebenenmasken Grundlagen
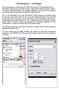 Ebenenmasken Grundlagen Was sind Ebenmasken? Was machen sie? Wofür braucht man sie? Wie funktionieren sie? Ebenmasken sind eines der sinnvollsten Tools in anspruchvollen EBV Programmen (EBV = elektronische
Ebenenmasken Grundlagen Was sind Ebenmasken? Was machen sie? Wofür braucht man sie? Wie funktionieren sie? Ebenmasken sind eines der sinnvollsten Tools in anspruchvollen EBV Programmen (EBV = elektronische
Inkrementelles Backup
 Inkrementelles Backup Im Gegensatz zu einer kompletten Sicherung aller Daten werden bei einer inkrementellen Sicherung immer nur die Dateien gesichert, die seit der letzten inkrementellen Sicherung neu
Inkrementelles Backup Im Gegensatz zu einer kompletten Sicherung aller Daten werden bei einer inkrementellen Sicherung immer nur die Dateien gesichert, die seit der letzten inkrementellen Sicherung neu
SCHRITT 1: Öffnen des Bildes und Auswahl der Option»Drucken«im Menü»Datei«...2. SCHRITT 2: Angeben des Papierformat im Dialog»Drucklayout«...
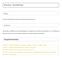 Drucken - Druckformat Frage Wie passt man Bilder beim Drucken an bestimmte Papierformate an? Antwort Das Drucken von Bildern ist mit der Druckfunktion von Capture NX sehr einfach. Hier erklären wir, wie
Drucken - Druckformat Frage Wie passt man Bilder beim Drucken an bestimmte Papierformate an? Antwort Das Drucken von Bildern ist mit der Druckfunktion von Capture NX sehr einfach. Hier erklären wir, wie
Wie oft soll ich essen?
 Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Handbuch ECDL 2003 Basic Modul 2: Computermanagement und Dateiverwaltung Dateien löschen und wiederherstellen
 Handbuch ECDL 2003 Basic Modul 2: Computermanagement und Dateiverwaltung Dateien löschen und wiederherstellen Dateiname: ecdl2_05_03_documentation.doc Speicherdatum: 16.03.2005 ECDL 2003 Modul 2 Computermanagement
Handbuch ECDL 2003 Basic Modul 2: Computermanagement und Dateiverwaltung Dateien löschen und wiederherstellen Dateiname: ecdl2_05_03_documentation.doc Speicherdatum: 16.03.2005 ECDL 2003 Modul 2 Computermanagement
lernen Sie uns kennen...
 KARRIERE lernen Sie uns kennen... Vielen Dank für Ihr Interesse an unserer Steuerberatungskanzlei. Nachfolgend möchten wir Ihnen Gelegenheit bieten, uns und unsere Denkweise näher kennenzulernen. Im Grunde
KARRIERE lernen Sie uns kennen... Vielen Dank für Ihr Interesse an unserer Steuerberatungskanzlei. Nachfolgend möchten wir Ihnen Gelegenheit bieten, uns und unsere Denkweise näher kennenzulernen. Im Grunde
UserManual. Handbuch zur Konfiguration einer FRITZ!Box. Autor: Version: Hansruedi Steiner 2.0, November 2014
 UserManual Handbuch zur Konfiguration einer FRITZ!Box Autor: Version: Hansruedi Steiner 2.0, November 2014 (CHF 2.50/Min) Administration Phone Fax Webseite +41 56 470 46 26 +41 56 470 46 27 www.winet.ch
UserManual Handbuch zur Konfiguration einer FRITZ!Box Autor: Version: Hansruedi Steiner 2.0, November 2014 (CHF 2.50/Min) Administration Phone Fax Webseite +41 56 470 46 26 +41 56 470 46 27 www.winet.ch
Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit
 Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit Frau Dr. Eva Douma ist Organisations-Beraterin in Frankfurt am Main Das ist eine Zusammen-Fassung des Vortrages: Busines
Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit Frau Dr. Eva Douma ist Organisations-Beraterin in Frankfurt am Main Das ist eine Zusammen-Fassung des Vortrages: Busines
Diese Ansicht erhalten Sie nach der erfolgreichen Anmeldung bei Wordpress.
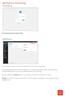 Anmeldung http://www.ihredomain.de/wp-admin Dashboard Diese Ansicht erhalten Sie nach der erfolgreichen Anmeldung bei Wordpress. Das Dashboard gibt Ihnen eine kurze Übersicht, z.b. Anzahl der Beiträge,
Anmeldung http://www.ihredomain.de/wp-admin Dashboard Diese Ansicht erhalten Sie nach der erfolgreichen Anmeldung bei Wordpress. Das Dashboard gibt Ihnen eine kurze Übersicht, z.b. Anzahl der Beiträge,
Mediale Informationen erschließen, aufbereiten, verarbeiten. Intensive Kommunikation von Schüler und Stoff
 Unterrichtsverlauf zu: UE Leasing, 6 8 Std., Jahrgangsstufe 1, Wirtschaft, Berufliches Gymnasium U- Phase 1. Std. Angestrebte Kompetenzen/Ziele Medien und weitere 5 Min. Stundenthema: Merkmale des Leasings
Unterrichtsverlauf zu: UE Leasing, 6 8 Std., Jahrgangsstufe 1, Wirtschaft, Berufliches Gymnasium U- Phase 1. Std. Angestrebte Kompetenzen/Ziele Medien und weitere 5 Min. Stundenthema: Merkmale des Leasings
GLEICH WEIT WEG. Aufgabe. Das ist ein Ausschnitt aus der Tausenderreihe:
 GLEICH WEIT WEG Thema: Sich orientieren und operieren an der Tausenderreihe Klasse: 3. Klasse (Zahlenbuch nach S. 26-27) Dauer: 3-4 Lektionen Material: Tausenderreihe, Arbeitsblatt, evt. Plättchen Bearbeitung:
GLEICH WEIT WEG Thema: Sich orientieren und operieren an der Tausenderreihe Klasse: 3. Klasse (Zahlenbuch nach S. 26-27) Dauer: 3-4 Lektionen Material: Tausenderreihe, Arbeitsblatt, evt. Plättchen Bearbeitung:
Herzlich Willkommen beim Webinar: Was verkaufen wir eigentlich?
 Herzlich Willkommen beim Webinar: Was verkaufen wir eigentlich? Was verkaufen wir eigentlich? Provokativ gefragt! Ein Hotel Marketing Konzept Was ist das? Keine Webseite, kein SEO, kein Paket,. Was verkaufen
Herzlich Willkommen beim Webinar: Was verkaufen wir eigentlich? Was verkaufen wir eigentlich? Provokativ gefragt! Ein Hotel Marketing Konzept Was ist das? Keine Webseite, kein SEO, kein Paket,. Was verkaufen
Mathematik. Lineare Funktionen. Vergleich von Handy - Tarifen
 Mathematik Lineare Funktionen Vergleich von Handy - Tarifen Thema der Unterrichtseinheit: Funktionen Thema der Unterrichtsstunde: Grafische Darstellung linearer Funktionen Bedeutung des Schnittpunktes
Mathematik Lineare Funktionen Vergleich von Handy - Tarifen Thema der Unterrichtseinheit: Funktionen Thema der Unterrichtsstunde: Grafische Darstellung linearer Funktionen Bedeutung des Schnittpunktes
Ein Hinweis vorab: Mailkonfiguration am Beispiel von Thunderbird
 Mailkonfiguration am Beispiel von Thunderbird Ein Hinweis vorab: Sie können beliebig viele verschiedene Mailkonten für Ihre Domain anlegen oder löschen. Das einzige Konto, das nicht gelöscht werden kann,
Mailkonfiguration am Beispiel von Thunderbird Ein Hinweis vorab: Sie können beliebig viele verschiedene Mailkonten für Ihre Domain anlegen oder löschen. Das einzige Konto, das nicht gelöscht werden kann,
Kurzanleitung MAN E-Learning (WBT)
 Kurzanleitung MAN E-Learning (WBT) Um Ihr gebuchtes E-Learning zu bearbeiten, starten Sie bitte das MAN Online- Buchungssystem (ICPM / Seminaris) unter dem Link www.man-academy.eu Klicken Sie dann auf
Kurzanleitung MAN E-Learning (WBT) Um Ihr gebuchtes E-Learning zu bearbeiten, starten Sie bitte das MAN Online- Buchungssystem (ICPM / Seminaris) unter dem Link www.man-academy.eu Klicken Sie dann auf
Anwendungsbeispiele. Neuerungen in den E-Mails. Webling ist ein Produkt der Firma:
 Anwendungsbeispiele Neuerungen in den E-Mails Webling ist ein Produkt der Firma: Inhaltsverzeichnis 1 Neuerungen in den E- Mails 2 Was gibt es neues? 3 E- Mail Designs 4 Bilder in E- Mails einfügen 1 Neuerungen
Anwendungsbeispiele Neuerungen in den E-Mails Webling ist ein Produkt der Firma: Inhaltsverzeichnis 1 Neuerungen in den E- Mails 2 Was gibt es neues? 3 E- Mail Designs 4 Bilder in E- Mails einfügen 1 Neuerungen
2.1 Erstellung einer Gutschrift über den vollen Rechnungsbetrag
 1. Einführung Manchmal ist es notwendig, dem Kunden eine Gutschrift zu einer bestimmten Rechnung, über einzelne Positionen oder auch völlig frei von einer Basis-Rechnung zu erstellen. Die verschiedenen
1. Einführung Manchmal ist es notwendig, dem Kunden eine Gutschrift zu einer bestimmten Rechnung, über einzelne Positionen oder auch völlig frei von einer Basis-Rechnung zu erstellen. Die verschiedenen
Selbst-Test zur Vorab-Einschätzung zum Vorkurs Chemie für Mediziner
 Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Chemische Bindung. Chemische Bindung
 Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
10.1 Auflösung, Drucken und Scannen
 Um einige technische Erläuterungen kommen wir auch in diesem Buch nicht herum. Für Ihre Bildergebnisse sind diese technischen Zusammenhänge sehr wichtig, nehmen Sie sich also etwas Zeit und lesen Sie dieses
Um einige technische Erläuterungen kommen wir auch in diesem Buch nicht herum. Für Ihre Bildergebnisse sind diese technischen Zusammenhänge sehr wichtig, nehmen Sie sich also etwas Zeit und lesen Sie dieses
Antrag für ein Schlichtungs-Verfahren
 Eingangsstempel Antrag für ein Schlichtungs-Verfahren Dieser Antrag ist in Leichter Sprache geschrieben. Das sieht man auch am gelben, runden Zeichen. Im Text finden Sie immer wieder unterstrichene Wörter.
Eingangsstempel Antrag für ein Schlichtungs-Verfahren Dieser Antrag ist in Leichter Sprache geschrieben. Das sieht man auch am gelben, runden Zeichen. Im Text finden Sie immer wieder unterstrichene Wörter.
Jeopardy and andere Quizformate im bilingualen Sachfachunterricht Tipps zur Erstellung mit Powerpoint
 Bilingual konkret Jeopardy and andere Quizformate im bilingualen Sachfachunterricht Tipps zur Erstellung mit Powerpoint Moderner Unterricht ist ohne die Unterstützung durch Computer und das Internet fast
Bilingual konkret Jeopardy and andere Quizformate im bilingualen Sachfachunterricht Tipps zur Erstellung mit Powerpoint Moderner Unterricht ist ohne die Unterstützung durch Computer und das Internet fast
