INHALTSVERZEICHNIS. 1. Allgemeine Grundlagen 2. Grundbegriffe organisch-chemischer Reaktionen 3. Stereochemie 4. Stoffgruppen
|
|
|
- Cornelia Ritter
- vor 7 Jahren
- Abrufe
Transkript
1 IALTSVERZEIIS 1. Allgemeine Grundlagen 2. Grundbegriffe organisch-chemischer Reaktionen 3. Stereochemie 4. Stoffgruppen 4.1. Alkane 4.2. Alkene, Alkine 4.3. Aromatische Systeme 4.4. alogenkohlenwasserstoffe 4.5. Alkohole 4.6. Phenole 4.7. Amine 4.8. arbonyle Aldehyde, Ketone, (hinone) 4.9. arbonsäuren und Derivate eterocyclen EMPFLEES LERBU Latscha, Kazmaier, hemie für Biologen, 3. Auflage, 2008, Springer Verlag 6
2 Biochemie Lehre der chemischen Vorgänge in Lebewesen Biomolekulare Strukturen Stoffwechsel Informationsfluss in und zwischen rganismen rganische hemie hemie der Kohlenstoffverbindungen omenklatur der Verbindungen Analytische rganische hemie z.b. Strukturaufklärung Reaktionen Anorganische hemie hemie der kohlenstoff-freien Substanze, der Kohlensäure, der Blausäure und Salze dieser Substanzen hemie der Metalle Komplexchemie Kristallographie 7
3 Zusammensetzung des menschlichen Körpers Element Massenanteil in % Sauerstoff (Element-Symbol: ) Kohlenstoff (Element-Symbol: ) alcium (Element-Symbol: a) atrium (Element-Symbol: a) Kalium (Element-Symbol: K) Magnesium (Element-Symbol: Mg) Wasserstoff (Element-Symbol: ) Phosphor (Element-Symbol: P) Stickstoff (Element-Symbol: ) Summe Rest Spurenelemente (u, o, r, Fe, usw.) 8
4 Wozu brauchen Biologen organische hemie? (1) Verständnis für Struktur und Funtkion von Biomolekülen(Proteine, ukleinsäuren, Vitamine) (2) Reaktivitäten (à Funktion) von Biomolekülen folgen Regeln derrganischen hemie Protein Vitamin DA Thiaminpyrophosphat Vitamin B 1 Vitamin D 2 9
5 Das Enzym - DA Polymerase ybridisierung, Funktionelle Gruppen (fg), Säure-Base Eigenschaften, Wechselwirkungen zwischen fg (z.b. Wasserstoff-Brücken),... 10
6 Das Enzym - DA Polymerase und die katalysierte Reaktion 2 2 DA DA P 2 DA Polymerase P 2 P + P P P 2 P P 2 Verstehen von Funktion und Reaktivität von Biomolekülen à z.b. PR (Polymerase hain Reaction, obelpreis 1993) 11
7 1. Allgemeine Grundlagen 12
8 Aufbau der Materie ATMKER Protonen und eutronen ATMÜLLE Elektronen Massenzahl Ladungszahl ELEMETSYMBL rdnungszahl zb: Fluor 19 F 0 9 Bohr sches Atommodell Ein chemisches Element ist durch die Anzahl der Protonen im Kern charakterisiert. Anzahl der Protonen =Kernladungszahl =rdnungszahl. Ein chemisches Element ist elektrisch neutral. Anzahl Protonen = Anzahl Elektronen. Die Summe der Zahl der Protonen und eutronen wird ukleonenzahl bzw. Massenzahl genannt. Quantenmechanische Betrachtung ukleonenzahl =Protonenzahl +eutronenzahl Isotopen eines chemischen Elements unterscheiden sich durch die Anzahl von eutronen, d.h. unterschiedliche Massenzahl aber gleiche Protonenzahl. Elektron Elementarteilchen Symbol LLadung Ruhemasse e - -1 (-e = x ) m e = 9.11 x kg Proton p + +1 (+e = x ) m p = x kg eutron n 0 0 m n = x kg 13
9 Periodensystem der Elemente 14
10 Atomorbitaltheorie (A-Theorie) Einführung/Wiederholung: Zustände vonelektronen eines Atoms könnenmit einer sogenannten Wellenfunktionen (WF, Ψ) beschrieben werden. Von diesen WF Ψ kann die Energie der Elektronen (Schrödinger Gleichung Ψ = EΨ) abgeleitet werden. Die Aufenthaltswahrscheinlichkeit der Elektronen ergibt sich aus Ψ 2 (à Atomorbitale). Wellenfunktionen Ψ, die Lösungen der Schrödinger Gleichung sind, heißen Eigenfunktionen. Die Energiewerte E, welche zudiesen Funktionengehören,heißen Eigenwerte. Wellenfunktionen Ψ n,l,m = f (n,l,m) n = 1,2,3,..., (ganze Zahlen) l = 0,1,2,... bis n-1 m = +l, +(l-1),...,0,...,-(l-1),-l auptquantenzahl ebenquantenzahl Magnetische Quantenzahl (maximal 2l+1 Werte) ame ausgeschrieben Wert von l Aussehen s-rbital sharp l = 0 radialsymmetrisch p-rbital principal l = 1 hantelförmig in den drei Raumachsen d-rbital diffuse l = 2 gekreuzte Doppelhantel f-rbital fundamental l = 3 rosettenförmig 15
11 Atomorbitaltheorie (A-Theorie) Wellenfunktionen Ψ n,l,m = f(n,l,m) n = 1,2,3,..., (ganzezahlen) l = 0,1,2,... bis n-1 m = +l, +(l-1),...,0,...,-(l-1),-l auptquantenzahl ebenquantenzahl MagnetischeQuantenzahl(maximal2l+1 Werte) Um die Elektronenzuständevollständig zu definieren braucht es eine vierte Quantenzahl: Spinquantenzahl s à s= +1/2 oder -1/2 Damit wird dereigendrehimpuls des Elektrons umschrieben. Durch die vier Quantenzahlen n, l, m unds ist der Zustand eines Elektrons im Atom eindeutig charakterisiert. n Schale (zb K,L, M,...),Energie, rbitalgröße l Form des rbitals (s, p,d,...) m rientierung im Raum s Richtung des Elektronen-Eigendrehimpulses 16
12 Graphische Darstellung der rbitale z y 1s-rbital:n=1, l=0, m=0: radialsymmetrisch x z z z y y y x x x 2p-rbitale:l=1, m=-1,0,+1: p x, p y, p z -rbital, hantelförmig, Vorzeichenwechsel 17
13 Mehrelektronen-Systeme Mehrelektronen-System können näherungsweise durch bisher gezeigtes wiedergegeben werden. Pauli-Verbot Zwei Elektronen dürfen nicht in allen vier Quantenzahlen übereinstimmen! Ein Atomorbital kann höchstens mit 2 Elektronen undzwar mit antiparallelen Spin (s=+1/2 unds=-1/2) besetzt werden! undsche Regel Besitzt ein Atom energetisch gleichwertige (entartete) Elektronenzustände, und werden mehrere Elektronen eingebaut, so erfolgt der Einbau derart, daß die Elektronen die rbitale zuerst mit parallelem Spin besetzen. Anschließend erfolgt die paarweise Besetzung mit antiparallelem Spin. p x p y p z 2p-rbitale:l=1, m=-1,0,+1: p x, p y, p z -rbital, hantelförmig, Vorzeichenwechsel 18
14 Bindungsarten hemische Bindung Bindungsarten 1. starke Bindungen: ionische, kovalente und metallische Bindungen à energiereich, nicht leicht zu brechen. 2. schwachebindungen: Wasserstoffbrückenbindung, Van der Waals Wechselwirkung à leicht(er) zu brechen. Kovalente Bindung (auch Atombindung) v.a. wichtig in rganischer hemie!! Kovalente (Elektronenpaar-) Bindungen bilden sich zwischen Partnern mit ähnlicher Elektronegativität (E) aus. Beispiele: 1. Elemente gleicher E: l-l (= l 2 ). Elektronenpaar-Bindungen sind gerichtet, zwischen Bindungspartner existiert erhöhte Elektronendichte). l l l l Valenzstrichformel 2. Elemente unterschiedlicher E: -F Fluorwasserstoff, 2 Kohlendioxid, 2 Wasser δ- F δ+ δ+ δ- δ- δ- δ+ δ+ 19
15 Kovalente Bindungen in organischen Verbindungen Bindung Bindende rbitale sp 3 sp 2, p z sp, p z, p y Bindungstyp σ σ, π σ, π, π Winkel zwischen den Bindungen 109, Bindungslänge / pm [10-12 m] Bindungsenergie / kj mol Drehbarkeit um - ja nein nein 20
16 Molekülorbitale in der rganischen hemie in den meisten organischen Verbindungen sind nur die Energieniveaus mit den auptquantenzahlen n=1 und 2 mit Elektronen besetzt. n=1: 1s kugelsymmetrisches rbital mit 2 Elektronen n=2: 2s kugelsymmetrisches rbital mit 2 Elektronen, 3 x 2p rbital mit 6 Elektronen 2s 1s 2p z 2p y 2p x 21
17 Molekülorbitale in der rganischen hemie Elektronenkonfiguration des Kohlenstoff-Atoms: 1s 2 2s 2 2p 2 = [e] 2s 2 2p 2 Betrachten das Kohlenstoff-Atom im Grundzustand (GZ): 4 e - in äußerer Schale à stehen zur Ausbildung von Bindungen zur Verfügung. Energie 2p Energiezufuhr Energie 2p 2s 2s Grundzustand angeregter Zustand Bei Energiezufuhr: e - aus 2s rbital in 2p rbital nun stehen 4 ungepaarte Elektronen zur Ausbildung von Bindungen zur Verfügung à -Atom bildet in der Regel 4 Bindungen aus 22!!
18 Probleme des Modells Kohlenstoff-Atom 4 x Wasserstoff-Atom Energie 2s 2p Energie 1s 1s 1s 1s Überlappung würde zu 4 Bindungen führen, eine ohne festgelegte Richtung (2s + 1s) und drei senkrecht zueinander stehenden (1s + 2p x bzw. 2p y bzw. 2p z ) Man findet aber, dass die 4 Bindungen im Methanmolekül gleichwertig (gleich lang) sind und das Molekül vollkommen symmetrisch aufgebaut ist!! Methan 23
19 Methan 4 das ybridisierungsmodell Summenformel: 4 ybridisierungs-modell: Die vier rbitale des -Atoms (2s, 2p x, 2p y, 2p z ) sind gemischt (hybridisiert) oder gekreuzt. à FLGE: 4 neue energetisch-entartete (= gleiche) sp 3 -rbitale. Energie 2p ybridisierung Energie 2s 4 x sp 3 rbitale 24
20 Die sp 3 -ybridisierung Graphische Darstellung eines sp-ybridorbitals Energie 4 x sp rbitale (sp 3 -ybridisierung) 2s 2p sp Elektron z y x Tetraedrische Anordnung durch Abstoßung der Elektronen: 2 Bindungen liegen in z/y-ebene, 1 Bindung vor der z/y-ebene (voller Keil), 1 Bindung dahinter (gestrichelter Keil) 25
21 Die σ-bindung! Beispiel: Wasserstoffmolekül 2 Darstellung: - 1s 1s! Beispiel: --Bindung Darstellung: - 1s sp Beispiel: --Bindung Darstellung: -! sp sp à Substanzen mit der größtmöglichen Anzahl von σ-bindungen (zb Methan 4 ) nennt man gesättigte Verbindungen. à wichtige Eigenschaft von σ-bindungen: Sie sind frei rotierbar entlang der Bindung. Beispiel: Ethan x sp-rbitale von 2 sp 3 -hybridisierten -Atomen 6 x s-sp -σ-bindungen 1 x sp-sp -σ-bindungen à 7 σ-bindungen 6 x 1s-rbital von -Atomen Freie Drehbarkeit 26
22 Ethan Seitenansicht Frontansicht (s. Pfeil) 27
23 Die sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p rbital Energie 3 x sp rbitale 3 x sp-rbital 1 x 2p-rbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 σ- und 1 π-)bindungen liegen in z/y-ebene 28
24 Die π-bindung Beispiel: in --Doppelbindung Darstellung: = 2p 2p à verbindungen mit Mehrfachbindungen nennt man ungesättigte Verbindungen. à wichtige Eigenschaft von π-bindungen: Sie sind IT frei rotierbar entlang der Bindung (aufgrund Vorzeichenwechsel in p-rbital). Beispiel: Ethen x sp-rbitale von 2 sp 2 -hybridisierten -Atomen 2 x p-rbitale von 2 sp2 -hybridisierten -Atomen 4 x s-sp -σ-bindungen 1 x sp-sp -σ-bindungen à 5 σ-bindungen 1 x p-p -π-bindung à 1 π-bindung 4 x 1s-rbital von -Atomen KEIE freie Drehbarkeit 29
25 Ethen Seitenansicht Frontansicht (s. Pfeil) 30
26 Die sp-ybridisierung sp-ybridisierung 2 x 2p rbital Energie 2 x sp-rbital 2 x 2p-rbital 2 x sp rbitale z y x lineare Anordnung in sp-hybridisierten -Atomen aus 2 σ- und 2 π-bindungen 31
27 Die sp-ybridisierung Beispiel Ethin 2 x s-sp -σ-bindungen 1 x sp-sp -σ-bindungen à 3 σ-bindungen 2 x p-p -π-bindungen à 2 π-bindungen 4 x sp-rbitale von 2 sp-hybridisierten -Atomen Seitenansicht 4 x p-rbitale von 2 sp-hybridisierten -Atomen 2 x 1s-rbital von -Atomen Frontansicht 32
28 Zusammenfassung Kovalente Bindungen in organischen Verbindungen sp 3 -ybridisierung aus 2s-rbital und 3 2p-rbitalen entstehen 4 sp 3 -rbitale. à gesättigterkohlenstoff: bildet rotationssymmetrische σ-bindung aus z.b. 4, 2 6, 3 8 sp 2 -ybridisierung aus 2s-rbital und 2 2p-rbitalen entstehen 3 sp 2 -rbitale und ein 2p-rbital bleibt übrig. à ungesättigter Kohlenstoff: bildet 3 σ-bindungen und eine π-bindung, d.h. wir erhalten eine Doppelbindung zu einem Bindungspartner z.b. Ethen 2 4. Durch die Doppelbindung wird die Rotationsfreiheit um die Mehrfachbindungsachse aufgehoben. 3 3 icht gleich 3 3 E-But-2-en Z-But-2-en sp-ybridisierung aus 2s-rbital und 1 2p-rbital entstehen 2 sp-rbitale und zwei 2p-rbitale bleiben übrig. à ungesättigter Kohlenstoff:bildet 2 σ-bindungen und 2 π-bindung, d.h. wir erhalten eine Dreichfachbindung zu einem Bindungspartner z.b. Ethin
29 Mesomerie Bisher: sp 3, sp 2 und sp ybridisierung à Einfach-, Doppel- und Dreichfachbindungen à kovalente Bindungen. Kovalente Bindungen: sind Elektronenpaarbindungen (aus Valenzelektronen), wobei jeweils ein Elektron von einem der Bindungspartner zur Verfügung gestellt wird (Bindung wird als Strich zwischen Atomen dargestellt) à Valenzstruktur. Bisher konnten wir die Bindungsverhältnisse eines Moleküls durch EIE Valenzstruktur angeben. Es gibt aber Fälle bei denen sich MERERE Valenzstrukturen für ein Molekül formulieren lassen à MESMERIE Essigsäure 2 gleichwertige mesomere Grenzstrukturen des Acetat-Anions 34
30 Moleküle mit mehreren Doppelbindungen 1. Isolierte Doppelbindungen:mehr als eine Einfachbindung Abstand 2. Konjugierte Doppelbindungen:Doppelbindung durch eine 'Einfachbindung' verbunden Kürzerer Abstand als erwartet für Einfachbindung 4 x sp 2 hybridisierte -Atome Elektronen sind delokalisiert 35
31 Aromatizität Besonderer Fall: cyclisch-konjugierte, planare π-systeme mit 4n+2 π Elektronen bekanntester Vertreter: Benzol 6 6 hypothetisch 2 Formen möglich mit unterschiedlichen Bindungslängen (Einfach- und Doppelbindungen) à ABER: Experimenteller Befunde: 1 Alle Bindungen in Benzol sind gleichwertig und zeigen einen Abstand von 1.39 Å (vgl. r(-) = 1.54 Å und r(=) = 1.34 Å). 2 Alle -Atome sind sp 2 -hybridisiert. 3 Bindungswinkel betragen 120. à alle zwölf Atome ( 6 6 ) bilden eine Ebene, die p-rbitale aller 6 sp 2 -hybridisierten -Atome überlappen und sind somit ober- und unterhalb der Ringebene delokalisiert! à Benzol zeichnet sich durch eine erhöhte Stabilität aus und ist in Reaktionen träger als Alkene. 36
32 Aromatizität - Benzol 37
33 Aromatizität Die ückel Regel ach ückel gilt: eine Verbindung ist aromatisch, wenn sie in einem cyclischen System (4n+2) π Elektronenaufweist! n = 0: 2 π-elektronen n = 1: 6 π-elektronen n = 2: 10 π-elektronen n = 3: 14 π-elektronen yclopropenyl- Kation Benzol yclopentadienyl- Anion aphtalin Anthracen 38
34 Systematik organischer Verbindungen rganische Verbindungen Acyclische Verbindungen (kettenförmig) yclische Verbindungen (ringförmig) Gesättigte Kohlenwasserstoffe (Alkane) Ungesättigte Kohlenwasserstoffe (Alkene, Alkine) arbocyclen eterocyclen Alicyclen ycloalkane, ycloalkene, ycloalkine Aromaten gesättigt aromatisch ungesättigt 39
35 hemische Formelsprache Beispiel: D-Glucose ( 2 ) n Verhältnisformel:gibt kleinstmögliches Verhältnis der Elemente einer organischen Verbindung Summenformel: Anzahl der einzelnen Elemente in organischer Verbindung Konstitutionsformel: Welche Atome über welche Bindung miteinander verknüpft sind, keine Information über die räumliche Anordnung. 40
36 hemische Formelsprache Beispiel: D-Glucose Konfigurationsformel: Räumliche Anordnung der Atome in einem Molekül mit bekannter Konstitution. 2 Fischer-Projektion aworth-ringformel Konformationsformel: Räumliche Anordnung der Atome in einem Molekül mit bekannter Konstitution unter Berücksichtigung von Rotationen um Einfachbindungen. Sessel 1 Sessel 2 41
37 Isomerie Definition: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen Anordnung (Stereoisomere) unterscheiden. Isomere Konstitutionsisomere Stereoisomere z.b. Pentan z.b. Enantiomere cis-/trans-isomere 42
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
Organische Chemie Chemie der Kohlenstoffverbindungen
 Organische Chemie Chemie der Kohlenstoffverbindungen Christoph Kreutz Lehrveranstaltungsnummer: 719.021 Bachelorstudium Biologie Wintersemester 2018/2019 Allgemeines zur Vorlesung Vorlesungsunterlagen
Organische Chemie Chemie der Kohlenstoffverbindungen Christoph Kreutz Lehrveranstaltungsnummer: 719.021 Bachelorstudium Biologie Wintersemester 2018/2019 Allgemeines zur Vorlesung Vorlesungsunterlagen
1. Allgemeine Grundlagen
 1. Allgemeine Grundlagen 12 Aufbau der Materie ATOMKERN Protonen und Neutronen ATOMÜLLE Elektronen Massenzahl Ladungszahl ELEMENTSYMBOL Ordnungszahl zb: Fluor 19 F 0 9 Bohr sches Atommodell Ein chemisches
1. Allgemeine Grundlagen 12 Aufbau der Materie ATOMKERN Protonen und Neutronen ATOMÜLLE Elektronen Massenzahl Ladungszahl ELEMENTSYMBOL Ordnungszahl zb: Fluor 19 F 0 9 Bohr sches Atommodell Ein chemisches
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul Rademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 7: 24.11.2004) MILESS: hemie für Biologen 126 Was
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul Rademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 7: 24.11.2004) MILESS: hemie für Biologen 126 Was
Chemie II. Vorlesung: Mo Uhr, HPT C103 Übungen: Mo Uhr, HCI H2.1, HCI J4
 hemie II Vorlesung: Mo 11-13 Uhr, PT 103 Übungen: Mo 14-16 Uhr, I 2.1, I J4 Literatur:.E. Mortimer, U. Müller: hemie, 11. Auflage Thieme-Verlag Stuttgart 2014 Dr. Wolfram Uhlig Laboratorium für Anorganische
hemie II Vorlesung: Mo 11-13 Uhr, PT 103 Übungen: Mo 14-16 Uhr, I 2.1, I J4 Literatur:.E. Mortimer, U. Müller: hemie, 11. Auflage Thieme-Verlag Stuttgart 2014 Dr. Wolfram Uhlig Laboratorium für Anorganische
Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie,
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
Aktuelle Beispiele aus der Forschung
 Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, starke, schwache Bindungen, Elektronenpaarbindung, bindende und freie Elektronenpaare, Oktettregel, Edelgaskonfiguration, Lewis-Formeln,
Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, starke, schwache Bindungen, Elektronenpaarbindung, bindende und freie Elektronenpaare, Oktettregel, Edelgaskonfiguration, Lewis-Formeln,
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. hristoffers, Vorlesung Organische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. inführung 1.1 Atomorbitale Die Atome im Molekülverband werden durch lektronen
Prof. hristoffers, Vorlesung Organische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. inführung 1.1 Atomorbitale Die Atome im Molekülverband werden durch lektronen
Chemie für Biologen SS Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 3: Kovalente Bindungen)
 Chemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische Chemie Universität Duisburg Essen (Teil 3: Kovalente Bindungen) (3) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung
Chemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische Chemie Universität Duisburg Essen (Teil 3: Kovalente Bindungen) (3) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung
Chemische Bindungen Atombindung
 Atombindung Das Lewis Modell der kovalenten Bindung Die Entstehung von Molekülen beruht auf der Bildung von gemeinsamen, bindenden Elektronenpaaren in dem Bestreben der Atome, eine energetisch stabile
Atombindung Das Lewis Modell der kovalenten Bindung Die Entstehung von Molekülen beruht auf der Bildung von gemeinsamen, bindenden Elektronenpaaren in dem Bestreben der Atome, eine energetisch stabile
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006
 Übungsaufgaben zur Vorlesung hemie für Biologen, WS 2005/2006 Themenbereiche Atombau, chemische Bindung, Stöchiometrie, Aggregatzustände 1. Ergänzen Sie folgende Tabelle: Symbol Z M Protonen eutronen Elektronen
Übungsaufgaben zur Vorlesung hemie für Biologen, WS 2005/2006 Themenbereiche Atombau, chemische Bindung, Stöchiometrie, Aggregatzustände 1. Ergänzen Sie folgende Tabelle: Symbol Z M Protonen eutronen Elektronen
Chemie-Vorkurs für Pharmaziestudenten SoSe Gerd Bendas Fachbereich Pharmazie Rheinische Friedrich Wilhelms Universität Bonn
 Chemie-Vorkurs für Pharmaziestudenten SoSe 2018 Gerd Bendas Fachbereich Pharmazie Rheinische Friedrich Wilhelms Universität Bonn gbendas@uni-bonn.de Einteilung der Veranstaltungen: die Veranstaltungen
Chemie-Vorkurs für Pharmaziestudenten SoSe 2018 Gerd Bendas Fachbereich Pharmazie Rheinische Friedrich Wilhelms Universität Bonn gbendas@uni-bonn.de Einteilung der Veranstaltungen: die Veranstaltungen
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Einführung in die Nomenklatur der organischen Chemie. Einteilung der Kohlenwasserstoffe
 organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Oktett-Theorie von Lewis
 Oktett-Theorie von Lewis Oktettregel Atome versuchen durch die Nutzung gemeinsamer Elektronenpaare möglichst ein Elektronenoktett zu erlangen. allgemeiner: Edelgasregel Atome streben durch Vereinigung
Oktett-Theorie von Lewis Oktettregel Atome versuchen durch die Nutzung gemeinsamer Elektronenpaare möglichst ein Elektronenoktett zu erlangen. allgemeiner: Edelgasregel Atome streben durch Vereinigung
Bindungskonzepte in der. Organischen Chemie. 1.1 Hybridisierung
 O:/Wiley/Organische_Chemie_Aufl_1/3d/c01.3d from 19.07.2012 09:18:28 1 Bindungskonzepte in der 1 Organischen Chemie In diesem Kapitel Die Organische Chemie wird gemeinhin als die Chemie der Kohlenstoffverbindungen
O:/Wiley/Organische_Chemie_Aufl_1/3d/c01.3d from 19.07.2012 09:18:28 1 Bindungskonzepte in der 1 Organischen Chemie In diesem Kapitel Die Organische Chemie wird gemeinhin als die Chemie der Kohlenstoffverbindungen
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen II
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen II Elektronenpaarbindung, Elektronegativität, polare Atombindung, Dipolmoment, Hybridisierung von Atomorbitalen, sp 3 -, sp 2 -, sp-hybridorbitale,
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen II Elektronenpaarbindung, Elektronegativität, polare Atombindung, Dipolmoment, Hybridisierung von Atomorbitalen, sp 3 -, sp 2 -, sp-hybridorbitale,
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Valenz-Bindungstheorie H 2 : s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie
 Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Moleküle. Zweiatomige Moleküle: H 2+
 Moleküle Zweiatomige Moleküle: 2+ : zwei Kerne, ein Elektron Der Abstand zwischen den Atomkernen wird so klein gewählt, dass die 1s-Orbitale überlappen und durch Linearkombination Molekülorbitale gebildet
Moleküle Zweiatomige Moleküle: 2+ : zwei Kerne, ein Elektron Der Abstand zwischen den Atomkernen wird so klein gewählt, dass die 1s-Orbitale überlappen und durch Linearkombination Molekülorbitale gebildet
Bindungstheorie Elektronenoktett durch Übertragung von Elektronen: Ionenbindung
 Bindungstheorie Elektronenoktett durch Übertragung von Elektronen: Ionenbindung al: (Elektronegativität: a 0.9 l 3.1) a (1s 2, 2s 2, 2p 6, 3s 1 ) a + (1s 2, 2s 2, 2p 6 ) + e eon-konfiguration l (1s 2,
Bindungstheorie Elektronenoktett durch Übertragung von Elektronen: Ionenbindung al: (Elektronegativität: a 0.9 l 3.1) a (1s 2, 2s 2, 2p 6, 3s 1 ) a + (1s 2, 2s 2, 2p 6 ) + e eon-konfiguration l (1s 2,
Inhaltsverzeichnis. 3 Gesättigte Kohlenwasserstoffe (Alkane) 3.1 Offenkettige Alkane 3.2 Cyclische Alkane
 Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Wechselwirkungen zwischen Atomen Was bisher geschah Quantenmechanisches
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Wechselwirkungen zwischen Atomen Was bisher geschah Quantenmechanisches
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
Organische Chemie. Kapitel 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Organische Verbindungen enthalten Kohlenstoff
 rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
4.Teil Kovalente Bindung
 4.Teil Kovalente Bindung Lewis-Konzept, Valenstrichformel, Oktettregel Polare Elektronenpaarbindung und Elektronegativität Gebrochene Bindungsordnung und Mesomerie Valenzschalen-Elektronenpaar-Abstoßungsmodell
4.Teil Kovalente Bindung Lewis-Konzept, Valenstrichformel, Oktettregel Polare Elektronenpaarbindung und Elektronegativität Gebrochene Bindungsordnung und Mesomerie Valenzschalen-Elektronenpaar-Abstoßungsmodell
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Grundlagen der Chemie
 Grundlagen der Chemie Angelika Brückner, Thomas Werner Leibniz-Institut für Katalyse e. V. an der Universität Rostock Bitte! 1 Informationen Vorlesung Dienstag, 11:00-12:30, LHSL Mittwoch, 11:30-13:00,
Grundlagen der Chemie Angelika Brückner, Thomas Werner Leibniz-Institut für Katalyse e. V. an der Universität Rostock Bitte! 1 Informationen Vorlesung Dienstag, 11:00-12:30, LHSL Mittwoch, 11:30-13:00,
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Organische Chemie für Technische Biologen Organische Chemie für Lehramtskandidaten Sommersemester 2005 Prof. Dr. Stephen Hashmi.
 Organische Chemie für Technische Biologen Organische Chemie für Lehramtskandidaten Sommersemester 2005 Prof Dr Gliederung des Vorlesungsstoffes I Allgemeines II Chemische Bindung III Einteilung der Organischen
Organische Chemie für Technische Biologen Organische Chemie für Lehramtskandidaten Sommersemester 2005 Prof Dr Gliederung des Vorlesungsstoffes I Allgemeines II Chemische Bindung III Einteilung der Organischen
CHE 172.1: Organische Chemie für die Life Sciences
 1 CHE 172.1: Organische Chemie für die Life Sciences Prof Dr. J. A. Robinson 1. Struktur und Bindung organischer Moleküle 1.1 Atomstruktur : Die Ordnungszahl (oder Atomzahl /Atomnummer = Atomic number)
1 CHE 172.1: Organische Chemie für die Life Sciences Prof Dr. J. A. Robinson 1. Struktur und Bindung organischer Moleküle 1.1 Atomstruktur : Die Ordnungszahl (oder Atomzahl /Atomnummer = Atomic number)
2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten
 Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Chemische Bindungen Atombindung
 Atombindung Das Lewis Modell der kovalenten Bindung Bildung von Molekülen (Einfachbindungen) Aus jeweils einem ungepaarten Elektron eines Atoms bildet sich ein gemeinsames Elektronenpaar als Molekülorbital
Atombindung Das Lewis Modell der kovalenten Bindung Bildung von Molekülen (Einfachbindungen) Aus jeweils einem ungepaarten Elektron eines Atoms bildet sich ein gemeinsames Elektronenpaar als Molekülorbital
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Organische Chemie I. OC I Lehramt F. H. Schacher 1
 Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Allgemeine Chemie I, Organische Chemie HS 2016
 Allgemeine Chemie I, rganische Chemie S 2016 Prof. elma Wennemers CAB Departement Chemie und Angewandte Biowissenschaften Freitag 7:45 09:30, CI G3 Übungen: Montag, 08.45 09.30 CI J343 Valeria Rondo-Brovetto
Allgemeine Chemie I, rganische Chemie S 2016 Prof. elma Wennemers CAB Departement Chemie und Angewandte Biowissenschaften Freitag 7:45 09:30, CI G3 Übungen: Montag, 08.45 09.30 CI J343 Valeria Rondo-Brovetto
Die chemische Bindung
 Die chemische Bindung Die Valenz-Bond Theorie Molekülorbitale Die Bänder Theorie der Festkörper bei einer ionischen Bindung bildet bildet sich ein Dipol aus ('Übertragung von Elektronen') Eine kovalente
Die chemische Bindung Die Valenz-Bond Theorie Molekülorbitale Die Bänder Theorie der Festkörper bei einer ionischen Bindung bildet bildet sich ein Dipol aus ('Übertragung von Elektronen') Eine kovalente
Übungen zur VL Chemie für Biologen und Humanbiologen Diese Aufgaben werden in der Übung besprochen.
 Übungen zur VL Chemie für Biologen und umanbiologen 03.10.2010 Diese Aufgaben werden in der Übung besprochen. Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben
Übungen zur VL Chemie für Biologen und umanbiologen 03.10.2010 Diese Aufgaben werden in der Übung besprochen. Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Das Lewis-Modell zur Erklärung kovalenter Bindungen
 Das Lewis-Modell zur Erklärung kovalenter Bindungen Erarbeiten Sie sich, innerhalb der Expertengruppe, einen Überblick über das Lewis-Modell zur Erklärung kovalenter Bindungen! Gehen Sie zusätzlich auf
Das Lewis-Modell zur Erklärung kovalenter Bindungen Erarbeiten Sie sich, innerhalb der Expertengruppe, einen Überblick über das Lewis-Modell zur Erklärung kovalenter Bindungen! Gehen Sie zusätzlich auf
Organische Chemie I SS 2018
 Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Organisation Informationen: www.wuttkegroup.de
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Organisation Informationen: www.wuttkegroup.de
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
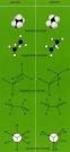 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Vom Atombau zum Königreich der Elemente
 Vom Atombau zum Königreich der Elemente Wiederholung: Elektronenwellenfunktionen (Orbitale) Jedes Orbital kann durch einen Satz von Quantenzahlen n, l, m charakterisiert werden Jedes Orbital kann maximal
Vom Atombau zum Königreich der Elemente Wiederholung: Elektronenwellenfunktionen (Orbitale) Jedes Orbital kann durch einen Satz von Quantenzahlen n, l, m charakterisiert werden Jedes Orbital kann maximal
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2014 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 4. Vorlesung, 27. 3. 2014 Molekülbindung, H2+ - Molekülion, Hybridisierung, Kohlenstoffverbindungen
Atom-, Molekül- und Festkörperphysik für LAK, SS 2014 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 4. Vorlesung, 27. 3. 2014 Molekülbindung, H2+ - Molekülion, Hybridisierung, Kohlenstoffverbindungen
1.8. Aufgaben zur Elektronenpaarbindung
 1.8. Aufgaben zur Elektronenpaarbindung Aufgabe 1: Elektronenpaarbindung a) Welche anderen Bezeichnungen gibt es für die Elektronenpaarbindung? b) Wie erreichen Nichtmetallatome die Edelgaskonfiguration,
1.8. Aufgaben zur Elektronenpaarbindung Aufgabe 1: Elektronenpaarbindung a) Welche anderen Bezeichnungen gibt es für die Elektronenpaarbindung? b) Wie erreichen Nichtmetallatome die Edelgaskonfiguration,
1.8. Aufgaben zur Elektronenpaarbindung
 1.8. Aufgaben zur Elektronenpaarbindung Aufgabe 1: Elektronenpaarbindung a) Welche anderen Bezeichnungen gibt es für die Elektronenpaarbindung? b) Wie erreichen Nichtmetallatome die Edelgaskonfiguration,
1.8. Aufgaben zur Elektronenpaarbindung Aufgabe 1: Elektronenpaarbindung a) Welche anderen Bezeichnungen gibt es für die Elektronenpaarbindung? b) Wie erreichen Nichtmetallatome die Edelgaskonfiguration,
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
CHE 172.1: Organische Chemie für die Life Sciences
 1 CHE 172.1: Organische Chemie für die Life Sciences Prof Dr. J. A. Robinson Inhaltsangabe 1. Struktur und Bindung organischer Moleküle 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen.
1 CHE 172.1: Organische Chemie für die Life Sciences Prof Dr. J. A. Robinson Inhaltsangabe 1. Struktur und Bindung organischer Moleküle 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen.
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CHE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 1. Struktur und Bindung organischer Moleküle 1.1 Atomstruktur: Die Ordnungszahl (oder Atomzahl /Atomnummer
CHE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 1. Struktur und Bindung organischer Moleküle 1.1 Atomstruktur: Die Ordnungszahl (oder Atomzahl /Atomnummer
Chemie für Mediziner. Norbert Sträter
 Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Bundesrealgymnasium Imst. Chemie Klasse 8. Aliphate
 Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Chemische Bindung in Kohlenwasserstoffen / Orbitalhybridisierung
 Quelle: www.fotocommunity.de C Methan Der einfachste Kohlenwasserstoff, das Methan, gehört zu den gasförmigen Ausscheidungsprodukten von Wiederkäuern. Das Methanmolekül weist die Struktur eines idealen
Quelle: www.fotocommunity.de C Methan Der einfachste Kohlenwasserstoff, das Methan, gehört zu den gasförmigen Ausscheidungsprodukten von Wiederkäuern. Das Methanmolekül weist die Struktur eines idealen
Allgemeine Chemie I, Organische Chemie HS 2017
 Allgemeine Chemie I, rganische Chemie S 2017 Prof. elma Wennemers CAB Departement Chemie und Angewandte Biowissenschaften Freitag 7:45 09:30, CI G3 Übungen: Montag, 08.45 09.30 CI J343 annes Ausserwöger
Allgemeine Chemie I, rganische Chemie S 2017 Prof. elma Wennemers CAB Departement Chemie und Angewandte Biowissenschaften Freitag 7:45 09:30, CI G3 Übungen: Montag, 08.45 09.30 CI J343 annes Ausserwöger
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Orbital. Atombindung, Bindung. Elektronegativität. Dipol
 GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Klausur zur Vorlesung "Grundzüge der Chemie" für Studierende des Maschinenbaus BITTE AUSFÜLLEN BITTE HALTEN SIE IHREN STUDENTAUSWEIS BEREIT
 1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
Das Periodensystem der Elemente
 Q34 LK Physik 17. November 2015 Aufbau Die ermittelten Zusammenhänge der Elektronenzustände in der Atomhülle sollen dazu dienen, den der Elemente zu verstehen. Dem liegen folgende Prinzipien zugrunde:
Q34 LK Physik 17. November 2015 Aufbau Die ermittelten Zusammenhänge der Elektronenzustände in der Atomhülle sollen dazu dienen, den der Elemente zu verstehen. Dem liegen folgende Prinzipien zugrunde:
Arbeitsblatt: Bindungsarten & ihre Beschreibung durch AOs 3 (EVA geeignet)
 Ph/Ch UE Quantenchemie Datum: Arbeitsblatt: Bindungsarten & ihre Beschreibung durch AOs 3 (EVA geeignet) 5 Ziel: Darstellung von MOs aus AOs erklärt Bindungsarten Man kann an den elektrischen Ladungsdichten
Ph/Ch UE Quantenchemie Datum: Arbeitsblatt: Bindungsarten & ihre Beschreibung durch AOs 3 (EVA geeignet) 5 Ziel: Darstellung von MOs aus AOs erklärt Bindungsarten Man kann an den elektrischen Ladungsdichten
2. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
 2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundwissen Chemie 10. Klasse NTG
 Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
Lösung 14. Allgemeine Chemie II Frühjahrsemester 2013
 Lösung 14 Allgemeine Chemie II Frühjahrsemester 2013 1. Aufgabe Bohr hat für das Wasserstoffatom ein Modell erstellt, das der klassischen Mechanik gehorcht und gewisse Ähnlichkeiten mit dem Planetenmodell
Lösung 14 Allgemeine Chemie II Frühjahrsemester 2013 1. Aufgabe Bohr hat für das Wasserstoffatom ein Modell erstellt, das der klassischen Mechanik gehorcht und gewisse Ähnlichkeiten mit dem Planetenmodell
Moleküle: mit kovalenten Bindungen verknüpfte Atome vs. Ionische Bindung
 Chemische Verbindungen Moleküle: mit kovalenten Bindungen verknüpfte Atome vs. Ionische Bindung Struktur: Atomorbitale & Molekülorbitale Hybridisierung 3D Struktur von Molekülen Funktionelle Gruppen Teile
Chemische Verbindungen Moleküle: mit kovalenten Bindungen verknüpfte Atome vs. Ionische Bindung Struktur: Atomorbitale & Molekülorbitale Hybridisierung 3D Struktur von Molekülen Funktionelle Gruppen Teile
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
EINFÜHRUNG IN DIE ORGANISCHE CHEMIE
 rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
Stereoisomerie. C 2 H 4 O 2 Schmelzpunkt 17 Grad Celcius
 3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Auf der rechten Seite sind Beispiele für kovalente Bindungen.
 Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Die Strukturabhängigkeit der chemischen Verschiebung
 Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Grundtypen der Bindung. Grundtypen chemischer Bindung. Oktettregel. A.8.1. Atombindung
 Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und Herstellung
 6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 8. Klasse NTG 1 / 48 ) ( 8. Klasse NTG 2 / 48 ) ( 8. Klasse NTG 3 / 48 )
 Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Chemie für Biologen SS Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 11: Alkine / Polyene / Aromaten)
 hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
Organische Chemie. 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8. Lehrstuhl für Organische Chemie
 Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Atommodell. Atommodell nach Bohr und Sommerfeld Für sein neues Atommodell stellte Bohr folgende Postulate auf:
 Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
