MIKROBIOLOGE DER MITTEILUNGEN DES BERUFSVERBANDES DER ÄRZTE FÜR MIKROBIOLOGIE UND INFEKTIONSEPIDEMIOLOGIE E.V. 17. Jahrgang, Heft 4 August 2007
|
|
|
- Greta Walter
- vor 6 Jahren
- Abrufe
Transkript
1 DER MIKROBIOLOGE MITTEILUNGEN DES BERUFSVERBANDES DER ÄRZTE FÜR MIKROBIOLOGIE UND INFEKTIONSEPIDEMIOLOGIE E.V. 17. Jahrgang, Heft 4 August 2007 EDITORIAL ÜBERSICHT Karin Rönnebäumer, Wolfgang Bohne, Raimond Lugert und Uwe Groß Mikrosporidien ungewöhnliche Pilze als Erreger von. opportunistischen Infektionen des Menschen DIAGNOSTIK Markus Frey Pyrosequencing: Schnelle Differenzierung und Resistenztestung H. Linde, G. Mistlbeck, H. Wolf, N. Lehn Schnellnachweis von Methicillin-resistentem Staphylococcus aureus Ökonomische Aspekte von Screening bei Aufnahme des Patienten Das komplette Inhaltsverzeichnis finden Sie auf der Seite 130
2 INHALTSVERZEICHNIS EDITORIAL ÜBERSICHT Karin Rönnebäumer, Wolfgang Bohne, Raimond Lugert und Uwe Groß Mikrosporidien ungewöhnliche Pilze als Erreger von opportunistischen Infektionen des Menschen DIAGNOSTIK Markus Frey Pyrosequencing: Schnelle Differenzierung und Resistenztestung H. Linde, G. Mistlbeck, H. Wolf, N. Lehn Schnellnachweis von Methicillin-resistentem Staphylococcus aureus Ökonomische Aspekte von Screening bei Aufnahme des Patienten BERICHT Kay Schaefer, Köln Tropenmedizinische Exkursionen für Ärzte nach Uganda und Kenia: Erfahrungsbericht nach 26 Fortbildungs-Rundreisen zwischen BUCHBESPRECHUNG QUALITÄTSSICHERUNG S. Suerbaum, S. Ziesing und G. Rademacher Mikrobiologischer Ringversuch 411 A2/2006 Abschließende Ergebnismitteilung und Besprechung BEZUGSQUELLEN FORTBILDUNGSVERANSTALTUNGEN MITTEILUNGEN Trichinellose-Gefahr durch lokal hergestellte Rohwürste aus Osteuropa TAGUNGSBERICHT Bericht über die 39. Jahrestagung der Arbeitsgruppe Klinische Mykologie der Deutschsprachigen Mykologischen Gesellschaft (DMykG ) TAGUNGSKALENDER... dritte Umschlagseite IMPRESSUM... dritte Umschlagseite 130 MIKROBIOLOGE 17.Jg. 2007
3 EDITORIAL Liebe Kolleginnen, liebe Kollegen, der Sommer (wo in unseren Breiten war es denn wirklich einer?) neigt sich schon wieder dem Ende entgegen, und ich hoffe, dass Sie sich alle einige erholsame Urlaubstage gönnen konnten. Viele Neuigkeiten gibt es nicht zu berichten, aber zumindest sind zwei Meldungen für uns doch interessant und insgesamt positiv zu werten: Zum trat das Gesetz zur Änderung medizinprodukterechtlicher und anderer Vorschriften in Kraft. Was sich zunächst nicht sonderlich aufregend anhört, erweist sich beim genauen Hinsehen aber doch als eine Änderung, die beweist, dass es sich tatsächlich lohnt, mit Sachverstand und guten Argumenten gegen unsinnige gesetzliche Regelungen vorzugehen. In 3 Nr. 21 und Nr. 22 (neu) MPG wird die In-Haus-Herstellung von Medizinprodukten und In-vitro-Diagnostika nun getrennt geregelt. Der bisher im MPG verwendete Begriff der In-Haus-Herstellung für eine Herstellung im eigenen Haus für das eigene Haus wird zukünftig durch den Begriff Eigenherstellung ersetzt. In 3 Nr. 22 wird die Eigenherstellung von In-vitro-Diagnostika neu geregelt. Hier bleibt die räumliche Beschränkung auf den Ort der Herstellung (Labor) bzw. auf Räume in unmittelbarer Nähe zu diesem bestehen. Es wird explizit erwähnt, dass für In-vitro-Diagnostika, die im industriellen Maßstab hergestellt werden, die Vorschriften über Eigenherstellung nicht anwendbar sind. Für in Blutspendeeinrichtungen hergestellte In-vitro-Diagnostika, die der Prüfung von Blutzubereitungen dienen, gelten diese Vorgaben entsprechend. Durch die neue Regelung wird die Eigenherstellung auf die Laboratorien begrenzt, die nicht im industriellen Maßstab und damit wie ein konventioneller und professioneller Hersteller agieren. Letztere müssen die allgemeinen Regelungen ohne Ausnahme beachten. Laut Begründung wird sich der Maßstab zur Begrenzung vorwiegend vom Umfang der Produktion abgrenzen lassen. Es wird jedoch keine starre Grenze vorgegeben, damit die zuständigen Landesbehörden im Einzelfall im Rahmen der Überwachung sachgerecht bewerten und entscheiden können. Diese flexible Regelung gestattet auch die notwendige, aber ggf. etwas umfangreichere, überregionale Versorgung von Kranken durch besonders qualifizierte Spezialisten oder vergleichbare Versorgungsformen, die das Privileg der Eigenversorgung beanspruchen sollen. Damit gilt für die Eigenherstellung von In-vitro-Diagnostika in Laboratorien einer Gesundheitseinrichtung folgende Begründung: Es kann davon ausgegangen werden, dass hierzulande die gesamte stationäre und ambulante Versorgung in Laboratorien von diesem Begriff erfasst ist. Neben den ärztlich geleiteten Laboratorien in Krankenhäusern und Arztpraxen sollen auch Apotheken in Kliniken sowie nationale Referenzzentren und Konsiliarlabore Reagenzien als Eigenherstellung für die jeweilige Einrichtung herstellen können soweit sie sie nicht im industriellen Maßstab produzieren. Aus meiner Sicht nennt man so etwas der Vernunft eine Bahn gebrochen. Dieser Tage erhielt ich endlich vom Vorstand der DGHM den abschließenden Entwurf für ein Curriculum Fachmikrobiologe, und ich hoffe, dass damit der letzte Schritt für eine vernünftige Regelung für ein entsprechendes Zertifikat getan ist und wir bei der DGHM-Tagung in Göttingen dieses Thema abschließen können. Wie Sie in diesem Heft der Vorankündigung für unsere Frühjahrstagung vom entnehmen können, waren wir aufgrund logistischer Probleme gezwungen, den Tagungsort zu ändern: wir werden unsere Veranstaltung in Bad Kissingen abhalten, das neben der besseren Hotel- und Tagungskapazität auch eine deutlich bessere verkehrstechnische Anbindung sowohl mit der Bahn als auch mit dem Auto bietet. Mit besten kollegialen Grüssen, Ihr H. K. Geiss MIKROBIOLOGE 17.Jg
4 ÜBERSICHT Mikrosporidien ungewöhnliche Pilze als Erreger von opportunistischen Infektionen des Menschen Karin Rönnebäumer, Wolfgang Bohne, Raimond Lugert und Uwe Groß Nationales Referenzzentrum für Systemische Mykosen am Institut für Medizinische Mikrobiologie Universitätsklinikum Göttingen, Göttingen Einleitung Mikrosporidien wurden bereits vor mehr als 100 Jahren vor allem als Pathogene von Insekten (z. B. Honigbienen) beschrieben. Erst durch ihren Nachweis als Erreger opportunistischer Infektionen bei immunsupprimierten Patienten erlangten sie auch infektiologische Aufmerksamkeit. Heute sind neben Insekten und dem Menschen zahlreiche Tierarten als Wirte für Mikrosporidien bekannt. Als unizelluläre Eukaryonten gehören sie zu den Protisten und wurden lange Zeit den Parasiten zugeordnet, weil ihr intrazellulärer Entwicklungszyklus Ähnlichkeiten mit dem von intrazellulären Protozoen aufweist. In den letzten Jahren haben aber molekulare DNA-Sequenzanalysen ergeben, dass sie phylogenetisch den Pilzen sehr viel näher stehen und nunmehr als atypische oder ungewöhnliche Pilze gelten (2, 12, 19). Auch der Nachweis von Chitin in der Sporenwand ist vereinbar mit einer potenziellen Zugehörigkeit der Mikrosporidien zu den Pilzen. Trotzdem weisen Mikrosporidien Besonderheiten auf, die sich bei anderen Pilzen nicht finden: So besitzen sie - wie Bakterien - 70S-Ribosomen, die sich aus einer 50S- und einer 30S-Untereinheit zusammensetzen. Auffällig ist das Fehlen einer separaten 5.8S rrna. Mitochondrien sind bei Mikrosporidien ebenso wie ein typischer GOLGI- Apparat nicht nachweisbar. Es konnten bei ihnen jedoch mitochondriales Hitzeschockprotein HSP70, sowie weitere mitochondriale Proteine identifiziert werden, was zunächst als Hinweis auf einen Verlust des Mitochondriums im Laufe der Evolution bewertet wurde (12, 15). Erst vor kurzem gelang dann tatsächlich der Nachweis eines Organells, das als Relikt eines Mitochondriums gewertet wird (21). Das Genom der Mikrosporidien-Art Encephalitozoon cuniculi wurde vor einigen Jahren sequenziert; es ist mit 2.9 MB, 11 Chromosomen und ungefähr offenen Leserastern das bisher kleinste sequenzierte eukaryotische Genom (12). Tabelle 1: Es wird davon ausgegangen, dass es sich bei den meisten Mikrosporidiosen des Menschen um Anthropozoonosen handelt Spezies Tierreservoir Enterocytozoon bieneusi Schweine, Hunde, Affen Encephalitozoon intestinalis (Septata intestinalis) Hunde, Schweine, Rinder, Ziegen Encephalitozoon hellem Vögel (Papageien) Encephalitozoon cuniculi Verschiedene Säugetiere Stamm I Kaninchen, Mäuse Stamm II Mäuse, Füchse Stamm III Hunde, Füchse, Katzen, Pferde, Nagetiere, Ziegen, Schafe, Schweine Nosema connori? Nosema ocularum? Nosema-ähnliche Arten? Vittaforma corneae (Nosema corneum)? Pleistophora spp. Fische Trachipleistophora hominis? Trachipleistophora anthropophtera? Microsporidia africanum? Microsporidia ceylonensis? MIKROBIOLOGE 17.Jg. 2007
5 Epidemiologie Die bisher entdeckten ungefähr 150 Mikrosporidiengattungen mit mehr als Arten spielen vor allem als weltweit vorkommende Pathogene von Insekten und Fischen eine Rolle; nur wenige sind humanpathogen. Enterocytozoon bieneusi ist die beim immunsupprimierten Menschen am häufigsten nachgewiesene Mikrosporidienart. Daneben spielen vor allem die Encephalitozoon- Arten E. intestinalis (früher Septata intestinalis), E. cuniculi und E. hellem eine wichtige Rolle bei Patienten mit stark eingeschränkter Immunität (9). Außerdem wurden die Gattungen Nosema, Vittaforma, Pleistophora, Trachipleistophora und Brachiola als Pathogene des immunsupprimierten Patienten nachgewiesen. Für die wichtigsten humanpathogenen Arten ist ein Reservoir in Tieren bekannt, so dass derzeit davon ausgegangen wird, dass es sich bei den Mikrosporidiosen des Menschen um Anthropozoonosen handelt (Tabelle 1). Für E. cuniculi sind mindestens drei verschiedenen Genotypen bzw. Stämme beschrieben, die jeweils mit tierspezifischen Wirtsreservoiren assoziiert sind und z. T. auch klinische Symptome im betroffenen Tier (v. a. im Kaninchen) hervorrufen. Infektionsbiologische Grundlagen Der ungefähr 48 Stunden dauernde Entwicklungszyklus von Mikrosporidien kann in drei Phasen unterteilt werden: Umweltphase Sporen Proliferative, obligat intrazelluläre Phase Meronten Sporogonie Sporonten Sporen Die Sporen sind in der Umwelt für mindestens sechs Monate lebensfähig und stellen daher das für die Transmission auf den Menschen verantwortliche Mikrosporidienstadium dar. Die Infektiosität der Sporen kann durch eine 30-minütige Erhitzung auf 60 C verhindert werden. Wie der Mensch sich infiziert, ist bis heute nicht vollkommen klar. Für die klinisch relevanteste Art E. bieneusi scheint. jedoch vor allem der fäkal-orale Übertragungsweg bedeutungsvoll zu sein Die Sporen der Mikrosporidien weisen folgende ultrastrukturelle Besonderheiten auf (Abb. 1, 2): Abb. 1: Schematische Darstellung einer Spore von Encephalitozoon cuniculi MIKROBIOLOGE 17.Jg
6 Abb. 2: Elektronenmikroskopische Darstellung von Encephalitozoon cuniculi. Deutlich sichtbar sind die einreihige Anordnung der sechs Windungen des Polarfilaments, der Nukleus (N), sowie der im anterioren Pol lokalisierte Polaroplast und die posteriore Vakuole 1. Die Sporenwand lässt eine Unterscheidung in eine dünne Exo- und eine dicke Endospore zu; letztere besteht u. a. aus einem Protein-α-Chitin-Komplex. 2. Am anterioren Pol befindet sich der lammellenartig aufgebaute Polaroplast mit der sogenannten Ankerscheibe. 3. Die Ankerscheibe dient der Fixierung des innerhalb der Spore spiralig aufgewickelten Polarfilaments, das in diesem Zustand speziesabhängig 4-30 Windungen bildet. Nach Extrusion kann es eine Länge von µm erreichen. 4. Am posterioren Pol ist eine Vakuole nachweisbar, die wahrscheinlich für die Extrusion des Polarfilaments von Bedeutung ist. Das Polarfilament spielt für die Invasion der Mikrosporidien in ihre Wirtszelle eine herausragende Rolle (6). Dabei scheinen verschiedenste Zellen des Menschen als Wirtszellen geeignet zu sein, wobei jedoch überwiegend Darmepithelzellen sowohl von E. bieneusi, als auch von Encephalitozoon spp. infiziert werden können. Auf einen noch unbekannten externen Stimulus hin platzt an der im anterioren Pol gelegenen Sollbruchstelle die Sporenwand und das Polarfilament wird herausgeschleudert. Als mögliche Auslöser für diese Vorgänge gelten (i) Veränderungen des ph-wertes oder des Redoxpotenzials, (ii) Veränderungen der Kalzium-, Natrium- oder Kalium-Ionenkonzentration oder (iii) ein osmotischer Stimulus, der durch Umwandlung von Trehalose in Glukose innerhalb der posterioren Vakuole eingeleitet wird. Letztere dehnt sich dadurch aus und baut einen Druck innerhalb der Spore auf, so dass es zum oben beschrieben Platzen der Sporenwand kommt. Es ist nach wie vor unklar, ob die physikalische Schleuderkraft des Polarfilaments dazu führt, dass die Zellmembran der potenziellen Wirtszelle schlicht und einfach durchbrochen wird oder ob ein Endozytoseähnlicher Mechanismus an der Invasion beteiligt ist. Anschließend wird das infektiöse Sporoplasma zusammen mit dem Nukleus durch das Polarfilament hindurch in die Wirtszelle injiziert. Die leere Spore, sowie das Polarfilament werden degradiert. Die Sporoplasmamembran verbleibt zwar in der leeren Sporenhülle, das in die Wirtszelle injizierte Sporoplasma wird aber von einer Membran umhüllt, die vom Polaroplasten stammt. Der gesamte Invasionsmechanismus findet innerhalb von nur zwei Sekunden statt (6). Die weitere intrazelluläre Entwicklung der Mikrosporidien verläuft gattungsspezifisch: Während Enterocytozoon bieneusi sich frei im Zytoplasma seiner Wirtszelle entwickelt, wird bei Encephalitozoon spp. intrazellulär eine fungiphore Vakuole gebildet, innerhalb der es zur weiteren Differenzierung des Pilzes kommt (Abb. 3). Die Ätiologie der fungiphoren Vakuolenmembran ist noch unklar, doch wird aufgrund des Invasionsmechanismus der Mikrosporidien angenommen, dass sie vom Pilz generiert wird. Die weitere Entwicklung der Mikrosporidien geht von Meronten aus, die sich über das Sporontenstadium schließlich zu Sporen differenzieren. Nach Ruptur der Wirtszelle werden diese frei und stellen das umweltresistente Transmissionsstadium dar. Bei diesem aktiven Invasionsprozess kommt es zur Bildung einer fusionsinkompetenten fungiphoren Vakuole: So ist weder eine Kolokalisation der Mikrosporidien mit endosomalen oder lysosomalen Markern, noch eine Ansäuerung der fungiphoren Vakuole zu beobachten. Die Aufnahme der Mikrosporidien scheint dabei wesentlich von der betreffenden Wirtszellart abhängig zu sein: Während bei in-vitro-kultivierung mit humanen Fibroblasten vor allem dieser aktive Invasionsmechanismus beobachtet wird, führt die Interaktion von E. cuniculi-sporen mit murinen Knochenmarksmakrophagen eher zur Phagozytose der Pathogene (3). Innerhalb der fungiphoren Vakuole findet die weitere Entwicklung dieser Mikrosporidienart in höchst koordinierter Art und Weise statt: So adhärieren die Meronten in Tight-Junction-ähnlicher Weise an der fungiphoren Vakuolenmembran und sind daher peripher lokalisiert, während die weitere Differenzierung hin zum Sporontenstadium im Zentrum der fungiphoren Vakuole beobachtet wird. 134 MIKROBIOLOGE 17.Jg. 2007
7 Polares Filament Sporoplasma Spore Sporonten und Sporen Meronten Merogonie Sporogonie Encephalitozoon: Fungiphore Vakuole Enterocytozoon: Zytoplasma Abb. 3: Schematische Darstellung des Lebenszyklus von Enterozytozoon und Encephalitozoon. Die nähere Analyse des Genoms von E. cuniculi zeigte, dass es nur sehr wenige klassische Signaltransduktionswege gibt. Durch den direkten Vergleich mit anderen Pilzen konnten auch in E. cuniculi Komponenten identifiziert werden, die bei anderen Pilzen mit Differenzierungsvorgängen assoziiert sind (z.b. Rho GTPase oder Protein). Die quantitative Bestimmung der entsprechenden. mrna-konzentrationen ergab jedoch keine signifikanten Unterschiede zwischen dem Meronten- und dem Sporontenstadium, so dass eine stadienspezifische Regulierung durch die entsprechenden Signaltransduktionskomponenten auf mrna-ebene eher unwahrscheinlich ist (Bohne und Groß, unveröffentlicht). Aus diesem Grund wird vielmehr angenommen, dass die intrazelluläre Entwicklung von E. cuniculi stark von noch unbekannten Wirtszellfaktoren abhängig ist. Die bei den Mikrosporidien nachgewiesene hohe Anzahl von Ribosomen weist dabei auf eine produktive Proteinsynthese hin Mit Hilfe klonierter Mikrosporidiengene und den von ihnen kodierten rekombinanten Proteinen konnten stadienspezifische monoklonale Antikörper generiert werden. Sie ermöglichen die Differenzierung zwischen Meronten auf der einen und Sporonten/Sporen auf der anderen Seite (1). Dabei konnten auch stadienspezifisch-exprimierte Proteine und Enzyme identifiziert werden, wie z. B. das Sporenwandprotein SWP-1, eine Endochitinase und eine Chitin-Synthase. Letztere werden verstärkt während der Entwicklung vom Meronten zum Sporontenstadium gebildet und sind ein weiteres Indiz dafür, dass es sich bei Mikrosporidien um Pilze handelt (16). Verschiedene experimentelle Ergebnisse deuten darauf hin, dass vor allem die zelluläre Immunität für die Kontrolle der Infektion von Bedeutung ist. So können z. B. athymische Mäuse durch Transfer von T-Zellen aus der Milz immunisierter Mäuse vor einer Mikrosporidiose geschützt werden. Auch für die Kontrolle der Mikrosporidiose des Menschen spielt die zelluläre Immunität eine zentrale Rolle: In der Regel ist bei AIDS-Patienten erst unterhalb einer CD4 + -T-Zellzahl von 100/µl mit dem Auftreten einer Mikrosporidiose zu rechnen. Steigt unter der antiretroviralen Therapie die CD4 + -T-Zellzahl an, so ist auch häufig eine Spontanremission der Mikrosporidiose zu beobachten (15). Klinische Manifestationen Prinzipiell muss damit gerechnet werden, dass alle humanpathogenen Mikrosporidienarten disseminierte Infektionen beim massiv immunsupprimierten Menschen (vor allem AIDS oder Transplantatempfänger) verursachen können. Die wichtigsten klinischen Manifestationen der bei diesen Patientengruppen am häufigsten nachgewiesenen Mikrosporidienarten sind in Tabelle 2 zusammengefasst. Tabelle 2: Übersicht der wichtigsten klinischen Manifestationen der beim immunsupprimierten Patienten am häufigsten nachgewiesenen Mikrosporidienarten. Enterocytozoon bieneusi chronisch wässrige Diarrhoe Encephalitozoon (Septata) intestinalis Diarrhoe, Nephritis Encephalitozoon hellem Keratokonjunktivitis, Disseminierung Encephalitozoon cuniculi Disseminierung, Encephalitis Enterocytozoon bieneusi befällt vor allem die Enterozyten des Duodenums bzw. des Jejunums und ruft daher vor allem bei AIDS-Patienten oder bei Transplantatempfängern mit therapeutisch induzierter Immunsuppression chronisch wässrige Diarrhoen ohne Fieber hervor. Als Zeichen der Dysfunktion des Dünndarms kann es zu einem abnormalen D-Xylose-Test kommen. Darüber hinaus kann diese Mikrosporidienart bei den genannten Patienten unter Umständen auch eine Cholangitis, sowie Pneumonien oder Infektionen des oberen Respirationstraktes (z.b. Sinusitis und Rhinitis) hervorrufen (7). MIKROBIOLOGE 17.Jg
8 Bei immunsupprimierten Patienten mit durch Mikrosporidien verursachter wässriger Diarrhoe ist darüber hinaus auch an Encephalitozoon intestinalis zu denken. Auch bei dieser Mikrosporidienart werden Cholangitiden, Pneumonien und Infektionen des oberen Respirationstrakts beobachtet. Aber auch Harnwegsinfektionen mit Nephritiden, sowie - in seltenen Fällen - Karatokonjunktivitiden und disseminierte Infektionen können auf eine Infektion mit E. intestinalis zurückzuführen sein. Die weitaus häufigste Mikrosporidienart, die bei einer Keratokonjunktivitis von AIDS-Patienten nachgewiesen wird, ist E. hellem. Dabei ist neben der konjunktivalen Gefäßerweiterung meistens auch eine oberflächliche, epitheliale Keratitis nachweisbar, die in der Spaltlampenuntersuchung durch punktuelle Veränderungen der Kornea imponiert. Ebenso wie die bereits genannten Arten kann E. hellem beim Immunsupprimierten auch zur Disseminierung führen und Infektionen des Respirationsoder Urogenitaltraktes hervorrufen. Darüber hinaus werden in letzter Zeit zunehmend okuläre Mikrosporidiosen auch bei immunkompetenten Patienten nachgewiesen, die bei dieser Patientenpopulation jedoch meist als tiefe, stromale Keratitis imponieren (11). Encephalitozoon cuniculi wird am häufigsten bei disseminierten Mikrosporidiosen Immunsupprimierter nachgewiesen, so dass theoretisch jedes Organ betroffen sein kann. In diesem Zusammenhang soll besonders auf Encephalitiden hingewiesen werden. Alle anderen humanpathogenen Mikrosporidienarten (Tabelle 1) werden nur in Einzelfällen bei immunsupprimierten Patienten isoliert. Klinische Manifestationen sind vor allem eine Myositis, eine Keratitis oder eine Disseminierung. In seltenen Fällen scheinen darüber hinaus Mikrosporidien auch für klinische Manifestationen bei immunkompetenten Individuen verantwortlich zu sein. So konnte zum Beispiel mit Hilfe der PCR bei 6.1% von Reiserückkehrern mit selbstlimitierender Diarrhoe vor allem E. bieneusi, aber auch Encephalitozoon spp. im Stuhl nachgewiesen werden (13). Diagnostik Bei routinemäßig durchgeführten mikroskopischen Untersuchungen von Punktaten, Biopsien, (Konjunktival- oder Hornhaut-) Abstrichen, sowie anderen klinischen Materialien können grampositiv erscheinende intrazelluläre Einschlüsse einen ersten Hinweis auf das Vorhandensein von Mikrosporidien liefern. Bei disseminierten Verläufen werden Mikrosporidien nicht selten mit dem Urin ausgeschieden und sind dann daher im Urinsediment nachweisbar. Aufgrund ihrer Größe können sie leicht mit Stäbchenbakterien verwechselt werden. Mikrosporidien zeigen jedoch eine typische Sicherheitsnadelmorphologie, die besonders deutlich in der modifizierten Trichromfärbung (17) sichtbar wird. Diese Färbung ist generell zu empfehlen, obwohl bisher in den meisten Laboratorien als Standardfärbung für den Nachweis von Mikrosporidien die Giemsa- Färbung Methanol-fixierter Präparate eingesetzt wird. Mikrosporidien stellen sich in der modifizierten Trichromfärbung als pinkfarbige, 1-4 µm große stäbchenförmige Erreger mit sicherheitsnadelartiger Morphologie (prominentere Anfärbung der Pole) dar, wobei E. bieneusi in der Regel etwas kleiner als Encephalitozoon spp. ist. Färbelösung für die modifizierte Trichromfärbung: 6.0 g Chromotrope 2R 0.5 g Anilinblau 0.25 g Wolframphosphatsäure 3 ml Essigsäure Mixtur für 30 Minuten stehen lassen, anschließend 100 ml Aqua dest. dazu geben, den ph auf 2.5 einstellen und die Färbelösung dann ohne Lichtzutritt lagern. Modifizierte Trichromfärbung: Nachdem die Objektträger mit Patientenmaterial 10 Minuten in Methanol fixiert wurden, folgt der Färbeschritt in der o. a. Trichromfärbelösung für 90 Minuten. Anschließend wird der Objektträger für 10 Sekunden in 0.45% Essigsäure/90% Äthanol und danach nochmals 10 Sekunden in 95% Äthanol gespült. Danach werden die Objekträger sequenziell für (i) 5 Minuten in 95% Äthanol, (ii) nochmals 5 Minuten in 95% Äthanol und (iii) 10 Minuten in absoluten Äthanol gegeben. Anschließend folgt eine zehnminütige Behandlung mit Histosol oder Xylol, um die Objektträger am Ende in DePeX einzudecken und zu mikroskopieren. Die Sporenhülle der Mikrosporidien besteht unter anderem - wie für Pilze üblich - aus Chitinstrukturen. Ein wichtiges Unterscheidungsmerkmal zu bakteriellen Erregern ist daher die Anfärbbarkeit der Mikrosporidiensporen mit optischen Aufhellern (z. B. Calcofluor-Weiss oder Uvitex 2B). Dabei ist zu beachten, dass dieses Pilzstadium während der späten intrazellulären Entwicklung entsteht und dann vor allem als für die Übertragung notwendiges Stadium meistens extrazellulär nachweisbar ist. Es sei darauf hingewiesen, dass im Stuhl und in Körperflüssigkeiten daher in der Regel nur Sporen gefunden werden, während in Gewebsbiopsien alle Stadien gleichermaßen nachweisbar sind (Abb. 4). Darüber hinaus stehen im NRZ für Systemische Mykosen auch monoklonale Antikörper für den Nachweis von Meronten zur Verfügung. Die kulturelle Anzucht von Mikrosporidien der Gattung Encephalitozoon gelingt innerhalb von 3-10 Wochen in verschiedenen Zellsystemen, wie z.b. mit HEp-2, MDCK, MRC-5, Caco-2 oder der E6-Affennierenzelllinie (20). Für E. bieneusi ist die routinemäßige, diagnostische Anzucht in Zellkultur bisher zwar noch nicht etabliert, neueste Ergebnisse zeigen aber, dass der vollständige Entwicklungszyklus in MDBK-Zellen innerhalb von ca. sechs Wochen gelingt (5). Eine Speziesdifferenzierung ist nur durch Elektronenmikroskopie oder durch PCR möglich. Bei ersterer ist u. a. die Anordnung des polaren Filaments oder die Konfiguration des Nukleus für die Speziesdiagnostik von Bedeutung. So stellt sich das spiralig aufgewickelte Polarfilament von E. cuniculi in der Elektronenmikroskopie einreihig mit sechs Querschnitten (Abb. 1, 2) dar, während das Polarfilament bei E. bieneusi zwei Reihen mit jeweils sechs Querschnitten bildet. 136 MIKROBIOLOGE 17.Jg. 2007
9 Abb. 4: Intrazellulärer Nachweis von Mikrosporidien mit Hilfe von optischen Aufhellern. Da diese Art der Diagnostik nur wenig verbreitet ist, wird heute vor allem die PCR zur Speziesdifferenzierung eingesetzt. Aus therapeutischen Gründen reicht dabei meistens die Zuordnung auf Gattungsebene, weil im Gegensatz zu Enterozytozoon bieneusi alle beim Menschen nachgewiesenen Mikrosporidien der Gattung Encephalitozoon in der Regel mit Albendazol therapierbar sind (s. u.). Als einfacher und praktikabler Nukleinsäurenachweis hat sich auch im NRZ für Systemische Mykosen die von Fedorko et al beschriebene PCR zum Nachweis der SSU rrna erwiesen (4). Hierbei werden gattungsspezifisch unterschiedlich große Amplifikate erzielt, deren Spezifität durch PstI-Restriktionsverdau weiter bestätigt werden kann: Während das Amplifikat von E. bieneusi keine PstI- Schnittstelle aufweist, wird jenes der Encephalitozoon- Gattung durch PstI-Restriktionsverdau in zwei Fragmente geschnitten (Tabelle 3, Abb. 5). Im Vergleich zur lichtmikroskopischen Diagnostik (Nachweisgrenze Sporen/g Stuhl) zeichnet sich die PCR-Diagnostik durch eine signifikant bessere diagnostische Sensitivität mit einer Nachweisgrenze von 10 2 Sporen/g Stuhl aus (14, 18). Die klinische Sensitivität für menschliche Patientenproben wurde für die Mikroskopie mit 80% (bei einer Spezifität von 95%) und für die PCR mit 89% (bei einer Spezifität von 98%) ermittelt (18). Das hat auch unmittelbare Konsequenzen für die klinisch-relevante Nachweisrate von Mikrosporidiosen: So konnte z. B. in einer afrikanischen Studie gezeigt werden, dass bei AIDS-Patienten mit Diarrhoe der lichtmikroskopische Nachweis von Mikrosporidien in nur 18% aus dem Stuhl der Patienten gelang. Wurden die gleichen Patientenproben mit Hilfe der PCR untersucht, waren jedoch 51% der Proben positiv (10). Abb. 5: PCR-Nachweis von Encephalitozoon cuniculi. Durch PstI-Restriktion ist eine eindeutige Abgrenzung gegenüber Enterozytozoon bieneusi möglich. (1) Marker, (2) PCR-Amplifikat, (3) PstI-Restriktion des Amplifikats MIKROBIOLOGE 17.Jg
10 Tabelle 3: PCR mit anschließendem Restriktionsverdau zur gattungsspezifischen Differenzierung der wichtigsten humanpathogenen Mikrosporidien (4) PCR-Amplifikat PstI-Fragmente E. bieneusi 250 bp 250 bp Encephalitozoon spp bp bp und 146 bp Der serologische Antikörpernachweis hat aufgrund der bei den betroffenen Patienten meist vorhandenen Immunsuppression in der Regel nur eine untergeordnete Bedeutung. Hier steht unter anderem ein Immunfluoreszentest (inhouse) zur Verfügung, bei dem in Zellkultur angezüchtete Mikrosporidien als Antigen eingesetzt werden. Unter Verwendung dieses Tests konnte gezeigt werden, dass Patienten mit nachgewiesener E. bieneusi-infektion (12.5%) im Vergleich zu gesunden Kontrollpersonen (1.9%) signifikant häufiger Antikörper mit einem Titer >1: 10 aufweisen (Groß und Weiss, unveröffentlicht). Therapie Die Therapie der Mikrosporidiose ist nach wie vor unbefriedigend. Insbesondere die am häufigsten vorkommende Infektion mit E. bieneusi ist schwierig zu therapieren. In Einzelfällen haben Fumagillin oral (3 x 20 mg/tag für 14 Tage) oder Albendazol oral (2 x 400 mg/tag für 1-2 Monate) oder Nitazoxanid (2 x 1 g/tag für 2 Monate) Erfolg gebracht. Im Gegensatz dazu sind die sich intrazellulär innerhalb einer fungiphoren Vakuole vermehrenden Encephalitozoon-Arten meistens gut mit Albendazol oral (2 x 400 mg/tag für 1-2 Monate) therapierbar. Die durch E. hellem verursachte Keratokonjunktivitis spricht meistens gut auf topisches Fumagillin (3-10 mg/ml) an (8). Literatur 1. Bohne, W., D. J. P. Ferguson, K. Kohler, and U. Groß Developmental expression of a tandemly repeated, glycine- and serine-rich spore wall protein in the microsporidian pathogen Encephalitozoon cuniculi. Infect. Immun. 68: Didier, E. S., and L. M. Weiss Microsporidiosis: current status. Curr. Opin. Infect. Dis. 19: Fasshauer, V., U. Groß, and W. Bohne The parasitophorous vacuole membrane of Encephalitozoon cuniculi lacks host cell membrane proteins immediately after invasion. Eukaryot. Cell 4: Fedorko, D. P., N. A. Nelson, C. P. Cartwright Identification of microsporidia in stool specimens by using PCR and restriction endonucleases. J. Clin. Microbiol. 33: Feng, D., A. Akiyoshi, A. Sheoran, Q. Zhang, G.Widmer, and S. Tzipori Serial propagation of Enterozytozoon bieneusi of human origin in rodents and in cell culture. IX. Int. Workshops on Opportunistic Protists, Lissabon, Juni 2006 (abstract). 6. Franzen, C Microsporidia: how can they invade other cells? Trends Parasitol. 20: Franzen, C. und A. Müller Molecular techniques for detection, species differentiation, and phylogenetic analyis of microsporidia. Clin. Microbiol. Rev. 12: Groß, U Treatment of microsporidiosis including albendazole. Parasitol. Res. 90: S14-S Groß, U., M. Weig, F.Petry Opportunistische parasitologische Infektionen bei immunsupprimierten Patienten. Med. Welt 48: Gumbo, T., S. Sarbah, I. T. Gangaidzo, Y. Ortega, C. R. Sterling, A. Carville, S. Tzipori, and P. M. Wiest Intestinal parasites in patients with diarrhea and human immunodeficiency virus infection in Zimbabwe. AIDS 13: Joseph, J., G. K. Vemuganti, and S. Sharma Microsporidia: emerging ocular pathogens. Indian J. Med. Microbiol. 23: Katinka, M. D., S. Duprat, E. Cornillot, G. Metenier, F. Thomarat, G. Prensier, V. Barbe, E. Peyretaillade, P. Brottier, P. Wincker, F. Delbac, H. El Alaoui, P. Peyret, W. Saurin, M. Gouy, J. Weissenbach, and C. P. Vivares Genome sequence and gene compaction of the eukaryote parasite Encephalitozoon cuniculi. Nature 414: Müller, A.,R. Bialek, A. Kämper, G. Fätkenheuer, B. Salzberger, and C. Franzen Detection of microsporidia in travelers with diarrhea. J. Clin. Microbiol. 39: Müller, A., K. Stellermann, P. Hartmann, M. Schrappe, G. Fätkenheuer, B. Salzberger, V. Diehl, and C. Franzen A powerful DNA extraction method and PCR for detection of microsporidia in clinical stool specimens. Clin. Diagn. Lab. Immunol. 6: Murray und Weiss, The Microsporidia and Microsporidiosis, ASM Press, Rönnebäumer, K., J. Wagener, U. Groß, and W. Bohne Identification of novel developmental regulated genes in Encephalitozoon cuniculi: an endochitinase, a chitin-synthase and two subtilisin-like proteases are induced during meront-to-sporont differentiation. J. Euk. Microbiol. 53: Ryan, N. J., G. Sutherland, K. Coughlan, M. Globan, J. Doultree, J. Marshall, R. W. Baird, J. Pedersen, and B. Dwyer A new trichrome-blue stain for detection of microsporidial species in urine, stool, and nasopharyngeal specimens. J. Clin. Microbiol. 31: Rinder, H., K. Janitschke, H. Aspöck, A. J. da Silva, P. Deplazes, D. P. Fedorko, C. Franzen, U. Futh, F. Hünger, A. Lehmacher, C. G. Meyer, J.-M. Molina, J. Sandfort, R. Weber, T. Löscher, and the Diagnostic Multicenter Study Group on Microsporidia Blinded, externally controlled multicenter evaluation of light microscopy and PCR for detection of microsporidia in stool specimens. J. Clin. Microbiol. 36: Van de Peer, Y., A. Ben Ali, and A. Meyer Microsporidia: accumulating evidence that a group of amitochondriate and suspectedly primitive eukaryotes are just curious fungi. Gene 246: Visvesvara, G. S In vitro cultivation of microsporidia of clinical importance. Clin. Microbiol. Rev. 15: Williams, B. A., R. P. Hirt, J. M. Lucocq, and T. M. Embley A mitochondrial remnant in the microsporidian Trachipleistophora hominis. Nature 418: Die Arbeiten der Autoren werden von der Deutschen Forschungsgemeinschaft (GR 906/11-2) unterstützt. Korrespondenzadresse Prof. Dr. med Uwe Groß Nationales Referenzzentrum für Systemische Mykosen am Institut für Medizinische Mikrobiologie Universitätsklinikum Göttingen Kreuzbergring Göttingen Tel: , Fax: ugross@gwdg.de 138 MIKROBIOLOGE 17.Jg. 2007
11 DIAGNOSTIK Pyrosequencing: Schnelle Differenzierung und Resistenztestung Markus Frey, Hygiene-Institut, Abt. für Hygiene und Med. Mikrobiologie, Universitätsklinikum Heidelberg Einleitung Mikroorganismen anhand ihrer DNA-Sequenz genotypisch zu identifizieren erleichtert in vielen Fällen eine schnelle und genaue Diagnostik. Vor allem die Sequenzierung der 16S-rRNA ist heute eine Standardmethode durch die Mikroorganismen unabhängig von ihrem Phänotyp eindeutig bestimmt werden können 1,2. Die Didesoxy-Methode nach Sanger 3 stellt die zur Zeit verbreitetste Sequenziertechnik dar. Durch ihre kontinuierliche Weiterentwicklung ist ein leistungsfähiges und zuverlässiges System für den Routineeinsatz entstanden. Doch machen der begrenzte Durchsatz und die Kosten dieser Technik auch alternative Sequenzierverfahren interessant. Im folgenden Artikel soll die Pyrosequenzierung 4,5 als ein, auch für die mikrobiologische Diagnostik, interessantes Verfahren vorgestellt werden. Prinzip der Pyrosequenzierung Während der Polymerase katalysierten DNA-Synthese entsteht beim Einbau eines Didesoxynukleotid- Aquivalents genau ein Äquivalent Pyrophosphat (PPi) (Abb. 1). Dieser stöchiometrische Zusammenhang erlaubt es die inkorporierten Didesoxynukleotide anhand der freigesetzten Menge an Pyrophosphat zu quantifizieren. Der Pyrophosphat-Nachweis erfolgt durch mehrere gekoppelte, simultan ablaufende Reaktionen (Abb. 2). Pyrophosphat wird durch eine Sulfurylase mit dem Substrat APS zu ATP umgesetzt. Das ATP liefert die Energie für die Oxidation von Luciferin durch eine Luciferase. Dabei entsteht ein Lichtblitz im sichtbaren Bereich (560 nm). Die entstehende Lichtmenge kann nun durch eine CCD- Kamera quantitativ detektiert werden. dntp PP i Pyrophosphat Abb. 1: Ausgehend von einem Primer (Pfeil) wird entlang ein DNA-Strangs der Gegenstrang durch eine Polymerase synthetisiert. Dabei wird durch den Einbau von Nukleotiden Pyrophosphat frei. Ob es sich bei dem eingebauten Nukleotid um ATP, GTP, CTP oder TTP handelt, kann bestimmt werden, indem die Zugabe sequenziell erfolgt. Jedem detektierten Lichtblitz kann so eine Nukleotidart zugeordnet werden. Überschüssig zugegebene Nukleotide werden durch eine Apyrase abgebaut. Danach kann das nächste Nukleotid dispensiert werden. Die Zeit, welche die Apyrase für den vollständigen Abbau der Nukleotide benötigt (1 Minute), wird für die Nukleotidzugabe zu weiteren Proben genutzt. Die Sequenzierung einer Probe benötigt so ebenso lange wie die Sequenzierung einer kompletten Mikrotiterplatte (96 Proben). 1. (DNA) n +dntp Polymerase (DNA) n+1 + PP i 2. PP i + APS Sulfurylase Pyrophosphat ATP + Sulfat Adenosine 5'- phosphosulfat 3. Luciferase ATP + Luciferin Licht + Oxyluciferin 4. überschüssige dntps/atp Apyrase dndp + P i dnmp + P i Abb. 2: Der Reaktionsablauf einer Pyrosequenzierung. Durch den Nukeotideinbau bei der DNA-Synthese wird Pyrophosphat freigesetzt (1.). Das Pyrophosphat wird über die Zwischenstufe ATP als Lichtemission detektiert (2.+3.). Überschüssige Nukleotide werden abgebaut ohne eine Lichtemission zu erzeugen (4.). MIKROBIOLOGE 17.Jg
12 In der Praxis wird das zugegebene ATP durch das Derivat ATPαS ersetzt. ATPαS inkorporiert problemlos in den DNA-Strang, kann aber nicht durch die Luciferase umgesetzt werden. Eine Interferenz mit der Detektions- Reaktion wird so vermieden. Da es mit der Zugabe der Nukleotide zu einer ständigen Verdünnung des Reaktionsansatzes kommt, sind maximal 100 Dispensierungen möglich. Dies entspricht einer Leseweite von Basen (je nach Sequenz). Einsatzgebiete in der Mikrobiologie Sowohl zur Differenzierung als auch zur genotypischen Resistenztestung sind in den letzten Jahren eine Reihe von Protokollen publiziert worden. Die Linezolid-Resistenztestung von Enterokokken 6, Rifampicin-Resistenzbestimmung von M. tuberculosis 7 und die schnelle Differenzierung von Erregern der neonatalen Sepsis 8 sollen nur einige Beispiele für den sich laufend erweiternden Einsatzbereich der Pyrosequenzierung sein. Praktische Durchführung Die Pyrosequenzierung ist ein isothermer Prozess. Die optimale Reaktionstemperatur mit der verfügbaren Reaktionschemie beträgt ca. 28 C liegt. Doppelsträngige DNA liegt bei dieser Temperatur nicht denaturiert vor. Ein Sequenzierprimer kann sich so nicht anlagern. Eine vorherige Einzelstrangpräparation ist daher notwendig. Dafür wird die zu sequenzierende Region durch eine modifizierte PCR amplifiziert. Einer der eingesetzten Primer ist dabei biotinyliert. Durch die Bindung des PCR- Produkts an eine Streptavidinmatrix und anschließendes denaturierendes Waschen erhält man so einzelsträngige DNA. Die Bindung an die Streptavidinmatrix stört die folgende Sequenzierung nicht. Nach Zugabe eines Sequenzierprimers kann die Sequenzierreaktion gestartet werden. Im Pyrosequencer werden die Proben auf die Reaktionstemperatur gebracht und anschließend die Nukleotide sequenziell und zyklisch zu den Proben dispensiert. Eine CCD-Kamera im Gerät nimmt in Echtzeit die Lichtemission der Probe auf. In Form eines PyrogrammsTM (Fa. Biotage)wird zur Auswertung die emittierte Lichtmenge (y-achse) in Bezug zum dipensierten Nukleotid (x-achse) gebracht (Abb. 3). Zusammenfassung Die Pyrosequenzierung ist eine robuste und schnelle Methode die vor allem bei hohen Durchsätzen mit geringer Leseweite Vorteile zeigt. Assays zur Typisierungen definierter Genabschnitte sind einfach zu etablieren. Die Miniaturisierbarkeit der Pyrosequenziertechnik macht sie auch für große Sequenzierprojekte interessant 9. Literatur 1. Woese CR. Bacterial evolution. Microbiol Rev 1987;51(2): Clarridge JE, 3rd. Impact of 16S rrna gene sequence analysis for identification of bacteria on clinical microbiology and infectious diseases. Clin Microbiol Rev 2004;17(4):840-62, table of contents. 3. Sanger F, Nicklen S, Coulson AR. DNA sequencing with chainterminating inhibitors. Proc Natl Acad Sci U S A 1977;74(12): Ronaghi M, Karamohamed S, Pettersson B, Uhlen M, Nyren P. Real-time DNA sequencing using detection of pyrophosphate release. Anal Biochem 1996;242(1): Ronaghi M. Pyrosequencing sheds light on DNA sequencing. Genome Res 2001;11(1): Sinclair A, Arnold C, Woodford N. Rapid detection and estimation by pyrosequencing of 23S rrna genes with a single nucleotide polymorphism conferring linezolid resistance in Enterococci. Antimicrob Agents Chemother 2003;47(11): Jureen P, Engstrand L, Eriksson S, Alderborn A, Krabbe M, Hoffner SE. Rapid detection of rifampin resistance in Mycobacterium tuberculosis by Pyrosequencing technology. J Clin Microbiol 2006;44(6): Jordan JA, Butchko AR, Durso MB. Use of pyrosequencing of 16S rrna fragments to differentiate between bacteria responsible for neonatal sepsis. J Mol Diagn 2005;7(1): Margulies M, Egholm M, Altman WE, et al. Genome sequencing in microfabricated high-density picolitre reactors. Nature 2005;437(7057): TCGATCGATCGATCGATCGATCGA GATAGGACCA TTCTGCGC Abb. 3: Ein Pyrogramm zeigt die emittierte Lichtmenge (y-achse) und das jeweils dispensierte Nukleotid (x-achse). Die Auswertung ergibt die daraus resultierende Sequenz. Korrespondenzadresse Markus Frey Hygiene-Institut Abteilung für Hygiene und Med. Mikrobiologie Universitätsklinikum Heidelberg Im Neuenheimer Feld Heidelberg 140 MIKROBIOLOGE 17.Jg. 2007
13 DIAGNOSTIK Schnellnachweis von Methicillin-resistentem Staphylococcus aureus Ökonomische Aspekte von Screening bei Aufnahme des Patienten Vortrag anlässlich der Jahresversammlung des Berufsverbands der Ärzte für Mikrobiologie und Infektionsepidemiologie, März 2004, Potsdam Aktualisierte Fassung H. Linde 1, G. Mistlbeck 2, H. Wolf 1, N. Lehn 1 1 Institut für Medizinische Mikrobiologie und Hygiene, Universität Regensburg, Regensburg 2 Fachhochschule Regensburg, Fachbereich Betriebswirtschaft, Rechnungswesen und Controlling, Regensburg Einleitung Methicillin-Resistenz bei Staphylococcus aureus (MRSA) stellt therapeutisch ein erhebliches Problem dar: Eine Reihe von Studien belegt eine längere Behandlungsdauer und eine höhere Komplikationsrate mit schlechterem Endergebnis, wenn Betalaktame als primäre Therapieform nicht wirksam sind (2;4;7;9;15). Eine weitere Einschränkung der therapeutischen Möglichkeiten droht durch das Auftreten von MRSA-Stämmen mit verminderter Empfindlichkeit bzw. Resistenz gegen Glykopeptide oder Linezolid (26). Der zunehmende Gebrauch von Glykopeptiden zur Behandlung von MRSA steht mutmaßlich im Zusammenhang mit der Selektion von Vancomycinresistenten Enterokokken (VRE), die ihrerseits als Ursprung der Glykopeptidresistenz bei MRSA gelten (5;31;34). Es ist deswegen als bedrohlich anzusehen, wenn weltweit wie auch in Deutschland eine Zunahme von MRSA bei Krankenhausisolaten von S. aureus zu verzeichnen ist (20). Deutschland wies in einer Studie der European Antimicrobial Resistance Surveillance System (EARSS; aus den Jahren 1999 bis 2002 von allen europäischen Ländern die höchsten MRSA-Zuwachsraten auf bei großen Unterschieden zwischen verschiedenen Regionen (32). In der Resistenzstudie der PEG aus dem Jahre 2004 hat der Anteil von MRSA in Deutschland und angrenzenden Ländern bereits 22,6 % erreicht ( In den USA, wo der Anteil von MRSA in Krankenhäusern landesweit 50 % beträgt ( hospital associated MRSA ; HA-MRSA), wird analog der Ausbreitung von Penicillin-resistenten S. aureus in den 50er Jahren nun eine weitere Verbreitung von MRSA aus dem Krankenhaus heraus auch außerhalb von medizinischen Einrichtungen befürchtet (30). Eine neue Bedrohung stellen MRSA-Stämme dar, die primär außerhalb von medizinischen Einrichtungen vorkommen (sog. community-associated MRSA ; CA-MRSA) (23), und wegen ihrer höheren Virulenz in medizinischen Einrichtungen ein erhebliches nosokomiales Problem darstellen können (22). Konzepte zur Eindämmung von MRSA in medizinischen Einrichtungen liegen vor, sie gründen sich auf koordinierte Maßnahmen: 1. Erkennung der Einschleppung von MRSA durch Screening-Maßnahmen, 2. Verzögerung der Evolution bzw. Selektion durch Infektionsprävention und rationalen Einsatz von Antibiotika, und 3. Verhütung der Verbreitung durch Hygienemaßnahmen. Die Maßnahmen sind beispielsweise in den Niederlanden, Dänemark und Slowenien mustergültig umgesetzt und werden als search, separate, destroy, declare -Politik bezeichnet (32;33). Aktive Suche nach MRSA durch Screening- Maßnahmen bei Aufnahme von Risiko-Patienten, nach Kontakt mit MRSA-Patienten (andere Patienten und Personal) sowie nach Sanierung des Trägerstatus ist ein fester Bestandteil des niederländischen Konzepts. Aufwändige Isolierungsmaßnahmen, die die Übertragungsrate wesentlich senken (16-18), und wie sie auch in deutschen Krankenhäusern üblich sind, können aber nur dann ihre volle Wirksamkeit erfassen, wenn sie möglichst frühzeitig angewandt werden. Eine Statusbestimmung und Konsensusempfehlung über die Indikation und den Umfang von MRSA-Screeninguntersuchungen in Deutschland wurde unter Federführung des Robert Koch-Instituts im Herbst 2005 vorgestellt (12). Offene Fragen betreffen z. B., ob alle Patienten oder nur Risikopatienten bei Aufnahme (bzw. Entlassung) untersucht werden sollten, welche Kriterien für die Einstufung als Risikopatient gelten, wie welche Untersuchungsmaterialien zu entnehmen sind (z. B. trockene oder angefeuchtete Abstrichtupfer von Nase und ggf. anderen Entnahmestellen, wenn ja: welche?, poolen von Abstrichen?), und welche Labortechniken mit welcher Sensitivität bzw. Zeitaufwand zum Einsatz kommen sollten (8). Die Einführung neuer Indikationen bzw. schneller und teurer Untersuchungsverfahren (z. B. Direktnachweis mittels PCR) muss sich dabei neben Fragen zur medizinischen Sinnhaftigkeit ganz besonders die Frage gefallen lassen, ob diese Maßnahmen kosteneffektiv sind. Eine Reihe von klinischen Studien sowie Modellrechnungen belegen einen positiven Effekt von MRSA- Screeninguntersuchungen bzgl. der Verhütung von neuen Infektionen, sowie eine Senkung der Gesamtkosten (13;19;25;27;36). Auch eine aktuelle Studie aus Deutschland kommt unter DRG-Abrechnungsbedingungen zum Schluss, dass MRSA-Screening kosteneffektiv ist (35). In vielen Institutionen stoßen die Empfehlungen zu MRSA- Screening allerdings auf Vorbehalte, schließlich werden zusätzliche Kosten nicht nur durch die Diagnostik verursacht, sondern bei positivem Nachweis auch in erhebli- MIKROBIOLOGE 17.Jg
14 chem Umfang durch die nun notwendigen Isolierungsmaßnahmen. Für die einzelne medizinische Institution erscheint eine Entscheidung schwierig, weil Kostenstrukturen aus Studien nicht einfach übertragen werden können, weil die lokale MRSA-Rate vom allgemeinen Durchschnitt stark abweicht, oder weil der Nettoeffekt wegen der außerordentlichen Komplexität der Kostenberechnungen schwer kalkulierbar ist. Der vorliegende Artikel möchte 1. die Problematik einer Kostenabschätzung diskutieren, 2. die aktuell durchgeführten Screeningmaßnahmen für MRSA mittels schneller PCR-gestützter Diagnostik am Universitätsklinikum Regensburg mit den dazugehörigen Kostenaspekten in einer sensitivity -Analyse (25) darstellen, und 3. eine solche Modellrechnung der sensitivity -Analyse für andere medizinische Institutionen zur Verfügung stellen. Material und Methode MRSA-Risikostatus von Patienten Laut Beschluss der Hygienekommission am Universitätsklinikum Regensburg vom werden Patienten in Bezug auf ihren MRSA-Risikostatus in 4 Gruppen aufgeteilt (Tab. 1). MRSA-Screening-Diagnostik Zum Screening wird routinemäßig ein Nasenabstrich (für beide Nasenvorhöfe), sowie falls vorhanden zusätzliche Proben aus Infektionsherden (Wunde, Sputum, BAL, etc.), entnommen. Anschließend wird der Nasenvorhof mit besonderer Berücksichtigung des medialen Abschnittes abgestrichen (6). Die kulturelle Diagnostik erfolgt ohne Voranreicherung auf nicht-selektiven und selektiven Festnährmedien (Columbia-Schafblutagar mit aufgelegtem Aztreonam- und Ciprofloxacin-Blättchen, Mannit-Kochsalz-Agar). Verdächtige Kolonien werden mittels Standard-Methoden identifiziert (1) und eine Resistenzbestimmung nach CLSI durchgeführt (24). In einer parallel durchgeführten Studie zum schnellen PCR-gestützten MRSA-Nachweis August bis November 2003 wurden dieselben Untersuchungsmaterialien verwendet. Nach automatisierter DNA-Isolierung (MagnaPure, Roche, Mannheim) wurde mittels LightCycler (Roche) die PCR für das meca-gen, ein S. aureusspezifisches Gen sowie ein Staphylokokken-spezifisches Gen durchgeführt. DNA-Isolierung und Inhibition wurden durch geeignete Kontrollen überprüft (28). Die Ergebnisse ließen in 86 % der Fälle eine eindeutige Aussage zu, die Sensitivität betrug 94 %, und der negative Vorhersagewert 99 % (21). Derzeit wird in der klinischen Routine ein verbesserter PCR-Test 2 mal täglich durchgeführt, sodass die Ergebnisse jeweils ca. um 13:00 bzw. 17:00 desselben Tages vorliegen (14). sensitivity -Analyse: Die Faktoren für die Berechnung der Kosten wurden in einem Excel -Arbeitsblatt erfasst. Die folgenden verschiedenen Zahlen- und Kostenblöcke wurden berücksichtigt: Block 1, Patienten mit MRSA bei Aufnahme: Anzahl der Patienten, MRSA-Prävalenz, Anteil mit MRSA kolonisierter Patienten, Anteil MRSA-infizierter Patienten, Anteil MRSA-infizierter Patienten mit schwerer (lebensbedrohlicher) Infektion, zusätzliche Mortalität durch MRSA-Infektion Block 2, Patientenscreening, erkannte Patienten: Anteil Risikogruppe insgesamt, Anteil Risikogruppe hohes Risiko, tatsächliche Screening-Rate, Sensitivität der Diagnostik, Spezifität der Diagnostik, Anzahl der Untersuchungen pro Patient, Rate der zufälligen Diagnostik, Rate der wieder aufgenommenen Patienten, Rate des spontanen Verlusts von MRSA Block 3, Übertragungsfenster: Mittlere Patientenverweildauer, mittlere Patientenverweildauer Kolonisierte, zusätzliche Verweildauer Infizierte, Zeitdauer Diagnostik, Übertragungs-Intervall vor Diagnostik Screening, Überragungs-Intervall vor Diagnostik zufällig, Übertragungs-Intervall nach Diagnostik Kolonisierte, Übertragungs-Intervall nach Diagnostik Infizierte Block 4, Neue MRSA-Patienten: Neue MRSA-Fälle/ MRSA-Pat.-Tag ohne Isolierung, Risiko-Reduktionsfaktor durch Isolierung, Neue MRSA-Fälle/MRSA-Pat.-Tag mit Isolierung Block 5: Kosten: Isolierung Kolonisierter pro Tag, Behandlung Infizierter pro Tag, alternativ: Entgangener Deckungsbeitrag (nach DRG), Material mit Anforderung Screening, Material mit Anforderung Entzündungserreger" bei Infektion, Therapiedauer Infizierte Tabelle 1: MRSA-Risikostatus von Patienten am Universitätsklinikum Regensburg Risiko Station Kriterien Maßnahmen Hoch Alle MRSA bekannt < 1 Jahr Verlegung von externer Intensivstation Screening Präventive Isolierung * Verlegung von Ausland Überdurchschnittlich Alle MRSA bekannt > 1 Jahr Screening in externem Krankenhaus > 2 Wochen innerhalb des letzten Jahres Kontakt zu MRSA-Patient** Niedrig Intensiv Verlegung aus Alten-/Pflegeheim Screening Chronische Erkrankungen Sehr niedrig Alle anderen - - *bis Ergebnis der Diagnostik bekannt; **Unterbringung in demselben Zimmer 142 MIKROBIOLOGE 17.Jg. 2007
15 Aus diesen Größen wurden u. a. die folgenden Parameter errechnet: Therapiekosten bei Infektion, Kosten der konventionellen Diagnostik bei Infektzeichen, Kosten von Screening, Kosten der präventiven Isolierung, Kosten der Isolierung nach positivem Befund, intangible Kosten: zusätzliche Mortalität, Zunahme der MRSA-Rate innerhalb eines Jahres. Es wurden die absoluten Kosten sowie der Quotient aus den aufgewendeten Kosten und den Kosten für verhütete Fälle als Maß für Kosteneffizienz gebildet. (stark mod. nach (25)). Ergebnisse Kostenabschätzung Nach S. B. Levy betreffen Infektionskrankheiten die Gesellschaft. Dies weist auf die außerordentliche Komplexität von Kosten-Nutzen-Kalkulationen hin. Durch MRSA bzw. Gegenmaßnahmen verursachte Kosten müssen für einen Vergleich in intangible Kosten (Kosten, die nicht berechnet werden können) und erfassbare Kosten (direkte und indirekte) unterschieden werden. In einer polarisierten Sicht lassen sich 2 verschiedene Strategien annehmen ( Therapie : keine Diagnostik, kalkulierte Gabe von MRSA-wirksamen Medikamenten bei jeder Infektion; Prävention : Diagnostik zur Erkennung von Trägern und Infizierten sowie entsprechende Hygienemaßnahmen), die sich in ihrer Kostenstruktur grundlegend unterscheiden (vgl. Tab. 2). Wie intangible Kosten durch Antibiotikaresistenz von S. aureus betroffen sein können, zeigt das Beispiel der Geschichte der Penicillinresistenz von S. aureus. Zwischen 1950 und 1960 kam es durch einen Anstieg der Penicillinresistenten S. aureus auf > 90 % zu einem Wiederanstieg der Letalität bei Bakteriämie durch S. aureus von % auf % (29). Schlechter beherrschbare infektiöse Komplikationen nach primärem Erfolg von high tech - Medizin (z. B. Organtransplantationen, Immunsuppression, Verbrennungen, etc.) sind in Bezug auf die Kosten- Nutzen-Analyse von Infektionen durch MRSA mit Sicherheit relevant, jedoch in ihrer Größenordnung schlecht abzuschätzen. Was es für die kalkulierte Behandlung von leichteren Infektionen außerhalb von Krankenhäusern bedeuten würde, wenn sich MRSA-Stämme dort weiter ausbreiten, ist derzeit nicht abschätzbar. Die Betrachtung und der Vergleich von Kostenaspekten werden durch unterschiedliche Strukturen und Bedingungen in verschiedenen medizinischen Einrichtungen weiter erschwert. Eine Reihe von Faktoren kann bei einer Kosten-Nutzen-Betrachtung zu höchst unterschiedlichen Ergebnissen führen (Tab. 3, ohne Anspruch auf Vollständigkeit). Die Problematik sei am Beispiel der Auswirkung von kürzeren Krankenhausverweilzeiten (durch DRGs) skizziert. Als Folge(n) wäre z. B. vorstellbar: - eine Abnahme der Anzahl der Übertragung durch ein verkleinertes Übertragungsfenster, - eine Zunahme der Übertragung durch Vernachlässigung von Basishygiene bei der möglichst schnellen Durchführung der diagnostischen und therapeutischen Maßnahmen (d. h. Erhöhung der Übertragungsrate), oder auch - eine Pseudo -Abnahme durch ausbleibende Erfassung von neu erworbenen MRSA-Stämmen bei bereits entlassenen Patienten. Tabelle 2: Gegenüberstellung von Kosten durch eine Strategie der Therapie statt Prävention bzw. Prävention statt Therapie. Therapie statt Prävention Prävention statt Therapie Erhöhung intangibler Kosten durch Erhöhte Mortalität Erhöhte Morbidität Gefährdung anderer Patienten Gefährdung des Personals Selektion von VRE, GISA, VRSA, HA-MRSA, CA-MRSA* Ausbreitung von MRSA außerhalb von medizinischen Einrichtungen Verschlechterung der Prognose der Grunderkrankung Psychische Belastung durch Isolierung Erniedrigung intangibler Kosten durch Verhütung anderer nosokomialer Infekte bzw. Erreger Erhöhung direkter/indirekter Kosten durch Therapie Verlängerte Verweildauer durch verzögertes Ansprechen Screening/Hygiene/Dekontamination Verlängerte Verweildauer durch erschwerte Behandlung der Grunderkrankung Erniedrigung direkter/indirekter Kosten durch Rationale Antibiotikatherapie *VRE: Vancomycin-resistente Enterokokken; GISA: Glykopeptid-intermediäre S. aureus; VRSA: Vancomycin-resistenter S. aureus; HA-MRSA: hospital-associated MRSA; CA-MRSA: community-associated MRSA MIKROBIOLOGE 17.Jg
16 Tabelle 3: Faktoren, die die Vergleichbarkeit von Kosten-Nutzen-Betrachtungen aus verschiedenen medizinischen Einrichtungen einschränken Art und Spektrum der vorherrschenden (Epidemie-)Klone von MRSA Prävalenz von MRSA in Normal- und Risikopatienten Anteil der MRSA-Träger mit anschließender Infektion Verweildauer der Patienten MRSA-Trägerrate von Personal, Risikofaktoren Selektionsdruck durch Antibiotika (Art und Umfang) Umsetzung von Basis-Hygiene-Maßnahmen (Rate der Händedesinfektion) Umsetzung von MRSA-spezifischen Hygiene-Maßnahmen Bauliche Bedingungen (wie viele Patienten in einem Raum?, overcrowding ) Stellenschlüssel ( understaffing )/Motivation/Ausbildung des Personals Kosten für mikrobiologische Untersuchungen Finanzielle Konsequenzen bei Überschreiten der durchschnittlichen Liegedauer durch infektionsbedingte Komplikationen Screeningmaßnahmen und Kostenüberlegungen am Universitätsklinikum Regensburg Kostenabschätzungen zur Einführung einer neuen Maßnahme können sich in einem ersten Schritt an einem Vergleich der Kosten der neuen Maßnahme und ihrem Potential zur Verhütung einer MRSA-Infektion orientieren. Wird beispielsweise einer Maßnahme das Potential zur Verhütung einer MRSA-Infektion pro Monat zugeschrieben, und sind die zusätzlichen Kosten durch eine solche Infektion bekannt, so kann daraus das Budget zur Finanzierung dieser Maßnahme abgeschätzt werden. Beispiel: Bei unter DRG-Bedingungen nicht erstatteten Kosten von 5705,75 für eine nosokomiale Infektion durch MRSA (35) könnten pro Jahr maximal 1/Monat x 12 Monate x 5.705,75 = zusätzlich ausgegeben werden (Anzahl der verhüteten Fälle x Kosten pro Fall). Für die Variable Anzahl der verhüteten Fälle kann in der Praxis eine (pessimistische) Schätzung angenommen bzw. eine Annahme getroffen werden, da genaue Daten oft nicht vorliegen. Um eine Kostenabschätzung im Sinne einer Kosten- Nutzen-Analyse für die Durchführung von MRSA- Schnelldiagnostik mittels PCR bei Aufnahmescreening von Risikopatienten auf Intensivstationen zu erhalten, wurde am Universitätsklinikum Regensburg eine sensitivity -Analyse durchgeführt. Die Fragestellung war, in welchem Maß eine PCR-gestützte Schnelldiagnostik, deren Ergebnis nach drei Stunden verfügbar ist, zur Verhütung einer weiteren MRSA-Übertragung bzw. zur Steuerung von Ressourcen auf einer Intensivstation beitragen kann. Dabei werden die Kosten der Diagnostik und die Kosten für präventive Isolierung bei Hochrisikopatienten bzw. Isolierung bei positivem Nachweis den Kosten für mögliche neue MRSA-Fälle gegenübergestellt. Es wurde darauf geachtet, dass sämtliche Rechnungsgrößen aus Daten von Intensivstationen des Universitätsklinikums Regensburg stammen. Die Zahlen zur Trägerrate von MRSA bei Aufnahme der verschiedenen Risikogruppen sowie die Übertragungsrate auf neue Patienten wurden aus aktuell durchgeführten Studien übernommen (Manuskript eingereicht). In der ersten Studie (n = 450 Patienten) betrug die Trägerrate bei neu aufgenommenen Patienten auf die Intensivstation 68/1.000 (Hochrisikopatienten 280/1.000). In einer zweiten Studie wurden Patienten (n = 285; Abstriche), die im Zimmer eines Patienten mit neu erkanntem MRSA lagen, über 14 Tage regelmäßig auf MRSA untersucht. Bei 7 % dieser Kontaktpatienten konnte ebenfalls MRSA gefunden werden. Aus der Kontaktdauer ließ sich eine Übertragungsrate von 1/100 pro Kontakttag mit einem MRSA-Patienten abschätzen, wenn man annimmt, dass bei dem neu betroffenen Patienten nicht schon vorher unerkannt MRSA vorhanden war (Manuskript eingereicht). Berechnete Modellvarianten Für die Beschreibung von unterschiedlichen klinischen Ansätzen zum Management von MRSA-Patienten wurden 4 verschiedene Handlungsmodelle angenommen, in denen Therapie, Diagnostik und hygienische Maßnahmen einen unterschiedlichen Stellenwert einnehmen. Die 4 Modelle lassen sich beschreiben als: Modell 1: Keine Screening- Diagnostik, keine Infekt-Diagnostik, kalkulierte Gabe von MRSA-wirksamen Antibiotika bei jeder Infektion, keine Isolierung; Modell 2: Keine Screening-Diagnostik, Infekt- Diagnostik, mit MRSA-infizierte Patienten werden isoliert; Modell 3: Konventionelle Screening-Diagnostik, Infektdiagnostik, asymptomatische Träger und infizierte Patienten werden isoliert; Modell 4: Schnelle Screening- Diagnostik, Infektdiagnostik, Risikopatienten, asymptomatische Träger und infizierte Patienten werden isoliert. Dabei entspricht das Modell 1 am ehesten der (radikalen) Annahme Therapie statt Diagnostik, während die Modelle 3 und 4 der Annahme Diagnostik statt Therapie entsprechen. Modell 2 dürfte für den größten Teil der Krankenhäuser in Deutschland gelten. In der Tab. 4 sind für die 4 verschiedenen Handlungsmodelle die jeweiligen Kostenblöcke aufgeführt. 144 MIKROBIOLOGE 17.Jg. 2007
17 Tabelle 4: Kostenblöcke der 4 verschiedenen Handlungsmodelle Direkte Kosten Intangibel Modell Diagnostik Infektion Diagnostik Screening Isolierung Risikopat. Isolierung nach positivem Screening Isolierung Infektion Therapie Mortalität MRSA-Rate 1 Nein Nein Nein Nein Nein Ja 2 Ja Nein Nein Nein Ja Ja 3 Ja Ja Nein Ja Ja Ja 4 Ja Ja Ja Ja Ja Ja Tabelle 5: Direkte und intangible Kosten durch Screening entsprechend der Handlungsmodelle 1-4 Modell Kosten gesamt ( ) Kosten Therapie ( ) Kosten Prävention ( ) Kosten Therapie neue Fälle* / Kosten Prävention Neue MRSA Patienten (n) Zusätzlich verstorben (n) MRSA Zins (%) Zunahme MRSA nach 1 Jahr (%) n. d. 4,4 0,059 4, n. d. 2,1 0,028 2, ,15** 1,1 0,014 1, ,15*** 0,6 0,008 0, Patienten, davon 68 mit MRSA, Intensivstationen, Universitätsklinikum Regensburg. * worst case -Annahme: alle neuen Patienten erleiden eine Infektion, durchschnittliche Kosten pro Infektion 5.705,75 (35). ** Vergleich Modell 3 vs. Modell 2; ***Vergleich Modell 4 vs. Modell 2. Die Berechnungen der verschiedenen Kostenblöcke unter den verschiedenen Modellannahmen 1-4 ergab die folgenden Ergebnisse (vgl. auch Tab. 5): Modell 1 weist mit großem Abstand die niedrigsten -Kosten auf, umgekehrt verhält es sich bei den intangiblen Kosten, die eine ungebremste Zunahme von MRSA sowie eine erhebliche zusätzliche Mortalität zeigen. Modell 2 weist bereits erhebliche -Kosten auf, die im Vergleich zu Modell 1 sich vor allem durch die zusätzlich durchgeführten Isolierungsmaßnahmen und die lange Verweildauer von infizierten Patienten ergeben. Modell 3 und in noch stärkerem Umfang Modell 4 führen bei geringfügig höheren Kosten zu einer weiteren wesentlichen Senkung der intangiblen Kosten. Der Quotient aus Kosten aus verhüteten Fällen / Kosten durch Prävention fällt in den Modellen 3 und 4 als kleiner 1 aus. In dieser isolierten Betrachtung ist die Kosteneffizienz negativ. Modellrechungen für andere Institutionen Um die sensitivity -Analyse für andere Institutionen anzuwenden, lassen sich für alle Parameter in den Excel - Arbeitsblättern leicht die entsprechenden Werte annehmen, die entweder aus eigenen Untersuchungen stammen, der Literatur entnommen sind, oder Grenzwerte von Schätzungen (höchster oder niedrigster anzunehmender Wert) darstellen. Entsprechend lassen sich für alle anderen Werte die für die jeweilige medizinische Einrichtung gültigen Werte einsetzen und per Excel -File Kosten und Nutzen errechnen. Das Excel -Arbeitsblatt zur eigenen Berechnung kann beim Autor angefordert werden. Diskussion Eine vollständige Abschätzung von finanziellen Nutzen und Kosten durch die Einführung neuer diagnostischer Verfahren ist wegen der großen Anzahl der einzubeziehenden Faktoren und der Komplexität ihrer Beziehungen untereinander schwierig. Intangible Kosten sowie der direkte medizinische Nutzen für den Patienten und die Gesellschaft müssen zudem gesondert bewertet werden. Gleichzeitig befördern in Deutschland die neuen Abrechnungsmodalitäten ein individuelles ökonomisches Verhalten von Kostenträgern, das auf eine Verschiebung von Kosten zielt (vgl. tragedy of the commons, (11)). Die Diskussion der Kostenproblematik ist nicht Gegenstand des vorliegenden Artikels. Vielmehr wird ein Rechenmodell vorgestellt, in dem Kosten und der zu erwartende Nutzen einer neuen diagnostischen Methode für die jeweils besondere Situation einer medizinischen Einrichtung abgeschätzt werden können. Aktuelle Daten zur zunehmenden Verbreitung von MRSA in Deutschland sowie die Erfahrungen anderer Länder (Hochprävalenzland USA, Niedrigprävalenzländer Niederlande, Dänemark) haben in Deutschland zu einer breiteren Diskussion über Kosten und Nutzen von Screeninguntersuchungen auf MRSA bei Aufnahme von (Risiko-) Patienten geführt (8;12). Neben Screeninguntersuchungen bei Aufnahme besteht eventuell ein weiterer Nutzen von Screeninguntersuchungen nach Kontakt von Patienten mit MRSA-Patienten, bei Entlassung, oder bei regelmäßigen Personaluntersuchungen. Evidenzbasierte Daten, die den Nutzen von MRSA-Screening zeigen, liegen leider nur begrenzt vor (35;36). Auf die Bedeutung von möglichst einfachen Definitionen wurde im Rahmen der Experten- MIKROBIOLOGE 17.Jg
18 kommission des Robert Koch-Instituts hingewiesen. Der Nachweis von MRSA direkt aus Probenmaterial mittels PCR bei Risikopatienten bei Aufnahme mit einer Verfügbarkeit des Ergebnisses innerhalb von drei Stunden verspricht zusätzlich eine Reihe von klinischen Vorteilen: - relativ sicherer (Negative Vorhersagewert > 99 %) Ausschluss einer Besiedlung von Patienten mit MRSA, bei Infektzeichen eine klare Indikation zur kalkulierten Therapie mit MRSA-wirksamen Medikamenten, sowie Durchführung von Isolierungsmaßnahmen; - frühzeitig verfügbare Entscheidung zur Fortführung der präventiven Isolierung bei Hochrisikopatienten bzw. deren Aufhebung. Damit leistet MRSA-Screening im allgemeinen und die schnelle PCR-Diagnostik im besonderen einen Beitrag zu einer rationalen Antibiotikatherapie, Verhütung von MRSA-Ausbreitung sowie Steuerung der Isolierungsressourcen. Am Universitätsklinikum Regensburg ist die Einführung der Untersuchung auf eine hohe Akzeptanz der klinischen Kollegen gestoßen, weil die Raum- und Personalplanung frühzeitig erfolgen kann. Auf der anderen Seite steht dem Nutzen ein erheblicher materieller, technischer und personeller Aufwand entgegen. Ziel der vorliegenden Überlegungen war es, unter Einbezug von möglichst lokalen epidemiologischen Daten abzuschätzen, ob in finanzieller Hinsicht ein Nutzen der finanziellen Aufwendungen besteht. Zur Abschätzung wurde in Anlehnung an Papia et al. (25) die Methode der sensitivity - Analyse gewählt und modifiziert. Die Attraktivität der Anwendung der sensitivity -Analyse in Kombination mit Excel besteht in der einfachen Möglichkeit, schnell verschiedene Werte für die einzelnen Parameter durchzuspielen. Wahlweise können eigene Daten, Literaturangaben oder pessimistische bzw. optimistische Annahmen gemacht werden. Auf diese Weise lassen sich auf einfache Art individuelle Szenarien erstellen. Unter Annahme der epidemiologischen Daten für die Situation auf Intensivstationen in Regensburg ergab sich ein differenziertes Bild. Die Werte der von uns verwendeten Rechnungsgrößen (z. B. Übertragungsrate pro Patiententag) ist mit Angaben aus aktuellen Studien vergleichbar (10;27;35). Der Quotient aus vermiedenen gegenüber den tatsächlich aufgewendeten Kosten lag für konventionelles MRSA-Screening von Risiko- und für PCR-gestütztes MRSA-Screening von Hochrisikopatienten weit unter 1. In diesem direkten monetären Vergleich kann eine Kosteneffizienz nicht festgestellt werden. Dieser Befund steht in Gegensatz zu publizierten Daten (25;36). Im Unterschied zu den genannten Studien wurden in der hier vorliegenden Berechnung die Kosten für die Isolierung von kolonisierten Patienten zusätzlich berücksichtigt. Diese Kosten machen einen erheblichen Teil der Kosten aus, und verändern deswegen das Verhältnis von aufgewendeten und eingesparten Kosten. Im Unterschied zur Kosteneffizienz belegen die Zahlen jedoch einen deutlichen Effekt der Handlungsmodelle 3 und 4 in Bezug auf die intangiblen Kosten neue MRSA-Patienten, zusätzliche Todesfälle durch MRSA- Infektion, sowie der Zunahme von MRSA. Dieser positive Effekt wird durch relativ geringfügige Mehrausgaben erreicht. Insbesondere Modell 4 scheint geeignet, langfristig die Rate von MRSA zu reduzieren. Zu diesem Ergebnis kommt auch eine Arbeitsgruppe um Marc Bonten (3). Aus infektiologisch-hygienisch-epidemiologischer Sicht erscheint die Durchführung von Screening bei Risikopatienten deswegen höchst sinnvoll. Der Vorteil des verwendeten Rechenmodells besteht darin, dass andere medizinische Einrichtungen entsprechende Abschätzungen, auch unter Verwendung von lokalen Daten, durchführen können. Der Umfang von Screening sollte für die jeweilige medizinische Einrichtung individuell festgelegt werden. Weitere klinische Studien zur Indikation und Methode von MRSA-Screening sind dringlich. Danksagung Wir danken Herrn Prof. Dr. P. Oberender, Universität Bayreuth, für die kritische Diskussion und Anregungen. Literaturverzeichnis 1. Becker K. Diagnostik von Methicillin-resistenten Staphylococcus aureus (MRSA)-Stämmen Teil 1. Taxonomische Einordnung, Anzucht und Differenzierung von Staphylococcus aureus. Mikrobiologe 2004;14: Blot SI, Vandewoude KH, Hoste EA, Colardyn FA. Outcome and attributable mortality in critically ill patients with bacteremia involving methicillin-susceptible and methicillin-resistant Staphylococcus aureus. Arch.Intern Med. 2002;162: Bootsma MC, Diekmann O, Bonten MJ. Controlling methicillinresistant Staphylococcus aureus: Quantifying the effects of interventions and rapid diagnostic testing. Proc.Natl.Acad.Sci.U.S.A. 2006;103: Chang FY, MacDonald BB, Peacock JE, Jr., Musher DM, Triplett P, Mylotte JM, O'Donnell A, Wagener MM, Yu VL. A prospective multicenter study of Staphylococcus aureus bacteremia: incidence of endocarditis, risk factors for mortality, and clinical impact of methicillin resistance. Medicine (Baltimore) 2003;82: Chang S, Sievert DM, Hageman JC, Boulton ML, Tenover FC, Downes FP, Shah S, Rudrik JT, Pupp GR, Brown WJ, Cardo D, Fridkin SK. Infection with vancomycin-resistant Staphylococcus aureus containing the vana resistance gene. N.Engl.J.Med. 2003;348: Cole AM, Tahk S, Oren A, Yoshioka D, Kim YH, Park A, Ganz T. Determinants of Staphylococcus aureus nasal carriage. Clin.Diagn. Lab Immunol. 2001;8: Cosgrove SE, Sakoulas G, Perencevich EN, Schwaber MJ, Karchmer AW, Carmeli Y. Comparison of mortality associated with methicillin-resistant and methicillin-susceptible Staphylococcus aureus bacteremia: a meta-analysis. Clin.Infect.Dis. 2003;36: Daschner FD. MRSA - Die Katastrophe droht. Klinikarzt 2004;33:7. 9. Engemann JJ, Carmeli Y, Cosgrove SE, Fowler VG, Bronstein MZ, Trivette SL, Briggs JP, Sexton DJ, Kaye KS. Adverse clinical and economic outcomes attributable to methicillin resistance among patients with Staphylococcus aureus surgical site infection. Clin. Infect.Dis. 2003;36: Forrester M, Comm B, Arts B, Anthony N, Pettitt AN. Use of stochastic epidemic modeling to quantify transmission rates of colonization with methicillin-resistant Staphylococcus aureus in an intensive care unit. Infect.Control Hosp.Epidemiol. 2005;26: Foster KR, Grundmann H. Do we need to put society first? The potential for tragedy in antimicrobial resistance. PLoS.Med. 2006;3:e Gastmeier P, Witte W. Zum Management des MRSA-Screenings. Epidemiologisches Bulletin ; Girou E, Azar J, Wolkenstein P, Cizeau F, Brun-Buisson C, Roujeau JC. Comparison of systematic versus selective screening for methicillin-resistant Staphylococcus aureus carriage in a high-risk dermatology ward. Infect.Control Hosp.Epidemiol. 2000;21: Hagen RM, Seegmuller I, Navai J, Kappstein I, Lehn N, Miethke T. Development of a real-time PCR assay for rapid identification of methicillin-resistant Staphylococcus aureus from clinical samples. Int.J.Med.Microbiol. 2005;295: Harbarth S, Rutschmann O, Sudre P, Pittet D. Impact of methicillin resistance on the outcome of patients with bacteremia caused by Staphylococcus aureus. Arch.Intern.Med. 1998;158: Heuck D, Witte W. Methicillin-resistente Staphylococcus aureus (MRSA) in deutschen Alten- und Pflegeheimen - zur Situation. Epidemiologisches Bulletin 19; 2003; Höpgen ME, Dreesmann J, Braulke C, Heuck D, Witte W. MRSA- Besiedlung in einem Alten- und Pflegeheim: Risikofaktoren und Prävalenz. Hygiene und Medizin 2001;26: Jernigan JA, Titus MG, Groschel DH, Getchell-White S, Farr BM. Effectiveness of contact isolation during a hospital outbreak of methicillin-resistant Staphylococcus aureus. Am.J.Epidemiol. 1996;143: MIKROBIOLOGE 17.Jg. 2007
19 19. Karchmer TB, Durbin LJ, Simonton BM, Farr BM. Costeffectiveness of active surveillance cultures and contact/droplet precautions for control of methicillin-resistant Staphylococcus aureus. J.Hosp.Infect. 2002;51: Kipp F, Friedrich AW, Becker K, von Eiff C. Berohliche Zunahme Methicillin-resistenter Staphylococcus aureus-stämme. Dtsch Arztebl 2004;101: Lehn N, Linde H, Schneider-Brachert W, Kaiser P, Reischl U. MRSA screening on admission by real time PCR directly from the swab within the same day th Congress of the European Society of Clinical Microbiology and Infectious Diseases, Prag. 22. Linde H, Wagenlehner F, Strommenger B, Drubel I, Tanzer J, Reischl U, Raab U, Holler C, Naber KG, Witte W, Hanses F, Salzberger B, Lehn N. Healthcare-associated outbreaks and communityacquired infections due to MRSA carrying the Panton-Valentine leucocidin gene in southeastern Germany. Eur.J.Clin.Microbiol. Infect.Dis. 2005;24: Moran GJ, Krishnadasan A, Gorwitz RJ, Fosheim GE, McDougal LK, Carey RB, Talan DA. Methicillin-resistant S. aureus infections among patients in the emergency department. N.Engl.J.Med. 2006;355: NCCLS. Performance standards for antimicrobial disk susceptibility testing. Ninth informational supplement M100-S9. National Committee for Clinical Laboratory Standards, Villanova, Pa Papia G, Louie M, Tralla A, Johnson C, Collins V, Simor AE. Screening high-risk patients for methicillin-resistant Staphylococcus aureus on admission to the hospital: is it cost effective? Infect.Control Hosp.Epidemiol. 1999;20: Peeters MJ, Sarria JC. Clinical characteristics of linezolid-resistant Staphylococcus aureus infections. Am.J.Med.Sci. 2005;330: Raboud J, Saskin R, Simor A, Loeb M, Green K, Low DE, McGeer A. Modeling transmission of methicillin-resistant Staphylococcus aureus among patients admitted to a hospital. Infect.Control Hosp.Epidemiol. 2005;26: Reischl U, Linde HJ, Metz M, Leppmeier B, Lehn N. Rapid identification of methicillin-resistant Staphylococcus aureus and simultaneous species confirmation using real-time fluorescence PCR. Journal of Clinical Microbiology 2000;38: Rubin RJ, Harrington CA, Poon A, Dietrich K, Greene JA, Moiduddin A. The economic impact of Staphylococcus aureus infection in New York City hospitals. Emerg.Infect.Dis. 1999;5: Salgado CD, Farr BM, Calfee DP. Community-acquired methicillinresistant Staphylococcus aureus: a meta-analysis of prevalence and risk factors. Clin.Infect.Dis. 2003;36: Tenover FC, Weigel LM, Appelbaum PC, McDougal LK, Chaitram J, McAllister S, Clark N, Killgore G, O'Hara CM, Jevitt L, Patel JB, Bozdogan B. Vancomycin-resistant Staphylococcus aureus isolate from a patient in Pennsylvania. Antimicrobial Agents and Chemotherapy 2004;48: Tiemersma EW, Bronzwaer SLAM, Lyytikäinen O, Degener JE, Schrijnemakers P, Bruinsma N, Monen J, Witte W, Grundmann H, European Antimicrobial Resistance Surveillance System Participants. Methicillin-resistant Staphylococcus aureus in Europe, Emerg.Infect Dis 2004;10: Vriens M, Blok H, Fluit A, Troelstra A, Van Der WC, Verhoef J. Costs Associated with a Strict Policy to Eradicate Methicillin- Resistant Staphylococcus aureus in a Dutch University Medical Center: A 10-Year Survey. Eur.J Clin.Microbiol.Infect Dis 2002;21: Weigel LM, Clewell DB, Gill SR, Clark NC, McDougal LK, Flannagan SE, Kolonay JF, Shetty J, Killgore GE, Tenover FC. Genetic analysis of a high-level vancomycin-resistant isolate of Staphylococcus aureus. Science 2003;302: Wernitz MH, Keck S, Swidsinski S, Schulz S, Veit SK. Cost analysis of a hospital-wide selective screening programme for methicillinresistant Staphylococcus aureus (MRSA) carriers in the context of diagnosis related groups (DRG) payment. Clin.Microbiol.Infect. 2005;11: Wernitz MH, Swidsinski S, Weist K, Sohr D, Witte W, Franke KP, Roloff D, Ruden H, Veit SK. Effectiveness of a hospital-wide selective screening programme for methicillin-resistant Staphylococcus aureus (MRSA) carriers at hospital admission to prevent hospitalacquired MRSA infections. Clin.Microbiol.Infect. 2005;11: Korrespondenzadresse PD Dr. med. Hans-Jörg Linde Institut für Medizinische Mikrobiologie und Hygiene Universität Regensburg Franz-Josef-Strauss-Allee Regensburg Tel.: Fax: Hans-Joerg.Linde@klinik.uni-regensburg.de MIKROBIOLOGE 17.Jg
20 BERICHT Tropenmedizinische Exkursionen für Ärzte nach Uganda und Kenia: Erfahrungsbericht nach 26 Fortbildungs-Rundreisen zwischen Kay Schaefer, Köln Abstract 26 Fortbildungs-Rundreisen auf dem Gebiet der klinischen Tropen- und Reisemedizin sind vom Autor zwischen in Uganda und Kenia durchgeführt worden. Ärzte aus Europa, USA, Kanada und Australien sind mit verschiedenen tropischen Infektionskrankheiten in den jeweiligen Endemiegebieten vertraut gemacht worden. Der Autor schreibt in diesem Bericht über seine Erfahrungen. Einleitung Immer häufiger kehren Touristen aus tropischen Ländern mit Malaria (1) und anderen tropischen Infektionskrankheiten zurück. Ärzte aus Europa und den USA sehen bei Immigranten und Asylbewerbern immer öfter Infektionskrankheiten, die sie vorher noch nie gesehen hatten (2). Die globale Erderwärmung wird in Zukunft auch zu einem Anstieg von tropischen Infektionskrankheiten in gemäßigten Breiten führen (3). Untersuchungen in europäischen und amerikanischen Krankenhäusern haben gezeigt, dass Malariainfektionen oft verkannt werden (4). Eine qualifizierte klinische Ausbildung der Ärzte auf dem Gebiet der Tropen- und Reisemedizin ist notwendig, um tropische Infektionskrankheiten im Frühstadium zu erkennen. Der Autor hat 26 Fortbildungs-Rundreisen nach Uganda und Kenia durchgeführt und berichtet über seine Erfahrungen. Design (Methode) Unter der Aufsicht von erfahrenen Tropenmedizinern der Universität Mbarara (Uganda) und Nairobi (Kenia) wurden maximal 7 Teilnehmer pro Exkursion auf dem Gebiet der klinischen Tropen- und Reisemedizin in Ostafrika ausgebildet. Während der 2 Wochen dauernden Fortbildungs-Rundreisen (Im Durchschnitt 1500 km per Geländewagen und Flugzeug) besuchten die Teilnehmer verschiedene Universitäts-Krankenhäuser, Out-Patients- Clinics und Forschungsprojekte in Uganda und Kenia. Im Rahmen von Visiten mit individuellem Bedside-Teaching, Fallvorstellungen, Laborpraktika und Vorlesungen wurden die Teilnehmer in den jeweiligen Endemiegebieten mit der Epidemiologie, Pathogenese, Klinik, Diagnostik, Therapie, Prävention und Kontrolle der dort vorkommenden tropischen Infektionskrankheiten vertraut gemacht. Das Curriculum beinhaltete unter anderem: Malaria, Afrikanische Trypanosomiasis, Viszerale Leishmaniose, Schistosomiasis, Lymphatische Filariose, Onchozerkose, Dengue Fieber, HIV/AIDS und opportunistische Infektionen, Lepra sowie charakteristische dermatologische und ophtalmologische Erkrankungen in den Tropen. Die Teilnehmer wurden auf den neusten Stand der Reisemedizin gebracht (z.b. WHO-Impfrichtlinien, DD von Fieber- und Durchfallerkrankungen bei Tropenrückkehrern) und besuchten das Flying Doctors Hauptquartier der African Medical Research Foundation (AMREF) sowie das Joint Clinical Research Center (JCRC), in dem die neusten HIV- Impfstoffstudien zum Einsatz kamen. Die Teilnahme an einer Exkursion schließt mit einem Zertifikat über 50 Lehrstunden auf dem Gebiet der Tropen- und Reisemedizin ab (Dies entspricht 50 Fortbildungspunkten im gesamten Ärztekammerbereich der BRD Referenz Kammerbereich Nordrhein) und ist ein Ermächtigungskriterium (Kenntnisse von tropischen Arbeitsplätzen) der G 35-Untersuchung. Darüber hinaus ist zusätzlich ein 9-stündiger Refresherkurs für Reisemedizin der Deutschen Tropenmedizinischen Gesellschaft (DTG) in die Reise integriert. Resultate 26 Fortbildungs-Rundreisen sind zwischen durchgeführt worden, 14 in Kenia und 12 in Uganda. Insgesamt haben 188 Ärzte an den Exkursionen teilgenommen: 144 (77%) aus Europa, 37 (20%) aus den USA/Kanada, 7 (3%) aus Australien. Darunter waren 90 Frauen (48%) und 98 Männer (52%). Das Durchschnittsalter lag bei 45 Jahren. Von den Teilnehmern waren: 80 Praktische Ärzte (43%), 46 Tropenmediziner (24%), 33 Mikrobiologen/Labormediziner (18%), 12 Arbeitsmediziner (6%), 9 Dermatologen (5%). 179 (95%) Teilnehmer gaben an, immer häufiger Impfungen, reisemedizinische Beratung und klinische Untersuchungen nach Tropenaufenthalt zu machen. 184 (98%) Ärzte nahmen an den Exkursionen vor allem Teil, um sich weiter zu bilden. Diskussion Aufgrund des wachsenden Tourismus in tropische Länder werden Ärzte aus Europa und den USA immer häufiger mit reisemedizinischer Beratung, Impfungen und medizinischen Check-Ups nach Tropenaufenthalt konfrontiert. Viele von Ihnen sind aber nur unzureichend auf dem Gebiet der klinischen Tropen- und Reisemedizin ausgebildet worden. Bei vielen Hausärzten in Großbritannien sind die tropen- und reisemedizinischen Kenntnisse unzureichend oder mangelhaft (5). In Kanada müssten 40% der Kliniken ihr Personal besser schulen, um auf den neusten Stand der klinischen Tropen- und Reisemedizin zu kommen (6). Vorlesungen und das Internet bieten Möglichkeiten, das theoretische Wissen der Ärzte auf den neusten Stand zu bringen (7). Klinische Erfahrungen auf dem Gebiet der Tropen- und Reisemedizin können jedoch nur dann erworben werden, wenn Ärzte an Visiten teilnehmen und Patienten am Krankenbett unter der Aufsicht von Experten 148 MIKROBIOLOGE 17.Jg. 2007
21 untersuchen. Einige Tropeninstitute in Europa, wie z.b. das Bernhard-Nocht Institut in Hamburg (8) und die London School of Hygiene and Tropical Medicine (Persönliche Erfahrung) haben eine angeschlossene klinische Abteilung für tropische Infektionskrankheiten. Allerdings ist dort die klinische Ausbildung aufgrund der geringen Patientenzahlen begrenzt. Zwei Wochen dauernde Tropenkurse für bis zu 10 Ärzte werden seit einigen Jahren in verschiedenen Lehrkrankenhäusern in größeren Städten in Südamerika, Afrika und Asien angeboten (9). Die Teilnehmer werden während der Visiten, Fallvorstellungen, Laborpraktika und Vorlesungen mit der Epidemiologie, Pathogenese, Klinik, Diagnostik, Therapie, Prävention und Kontrolle der wichtigsten tropischen Infektionskrankheiten vertraut gemacht. Gelegentliche Exkursionen in andere Krankenhäuser und Out- Patient-Clinics geben einen Einblick in das lokale Gesundheitssystem. Die seit 1995 jährlich stattfindenden Fortbildungs- Rundreisen nach Uganda und Kenia sind so konzipiert, dass Ärzte auf dem Gebiet der klinischen Tropen- und Reisemedizin in den jeweiligen Endemiegebieten ausgebildet werden. Zwei typische Kurstage in Uganda sehen wie folgt aus: 1. Tag: Auf dem Weg von Kampala nach Jinja reisen die Teilnehmer durch ein Gebiet, in dem die Schlafkrankheit endemisch ist. Nach einer Vorlesung über African Trypanosomiasis machen die Ärzte Visite in einem Lehrkrankenhaus in Jinja am Ufer des Viktoriasees. Sie untersuchen Trypanosomiasis Patienten und besprechen am Krankenbett die Symptomatik und Behandlung mit dem Chefarzt. Nachdem die Teilnehmer die gängigen diagnostischen Nachweismethoden für African Trypanosomiasis in einem Feldlabor erlernt haben (1. Photo), besuchen Sie mit einem Entomologen ein Tse-Tse Fly Kontrollprojekt. Der Tag endet mit einer wissenschaftlichen Exkursion durch einen National Park, in dem die Teilnehmer das Habitat von Antilopen das Haupt Reservoir der Trypanosomiasis rhodesiense Infektion kennen lernen. Kontrollmaßnahmen werden während der Exkursion mit erfahrenen Epidemiologen besprochen. Pädiatrie Kleinkinder mit zerebraler Malaria (2. Photo) im Lehrkrankenhaus der Mbarara Universität, besuchen die Ärzte ein Malaria Kontrollprojekt in dem imprägnierte Mosquito-Netze hergestellt und an die Bevölkerung verteilt werden. Eine Vorlesung am Abend über die Differenzialdiagnose von Fiebererkrankungen bei Tropenrückkehren schließt das Tagesprogramm ab. Photo 2: Behandlung der zerebralen Malaria auf der Kinderstation Das einzigartige Konzept der Fortbildungs-Rundreisen durch Uganda und Kenia ermöglicht den Teilnehmern neben der Diagnostik, Klinik und Behandlung auch die Epidemiologie, Entomologie, Prävention und Kontrolle wichtiger tropischer Infektionskrankheiten vor Ort kennen zu lernen. Fortbildungs-Rundreisen in andere tropische Länder würden die Ausbildung weiterer Ärzte auf dem Gebiet der klinischen Tropen- und Reisemedizin vertiefen und somit die Gesundheit von Tropenrückkehrern verbessern. Temine für Exkursionen Tropenmedizinische Fortbildungsreise nach Kenia 20. Januar - 1. Februar Tropenmedizinische Fortbildungsreise nach Uganda 10. Februar Februar Tropenmedizinische Fortbildungsreise nach Kenia 1. Februar Februar Tropenmedizinische Fortbildungsreise nach Uganda 22. Februar - 6. März 2009 Photo 1: Diagnostik der Schlafkrankheit in einem Feldlabor 2. Tag: Die Kurs-Teilnehmer reisen (300 km) nach Mbarara in West-Uganda, ein Malaria-Endemiegebiet. Nach Vorlesung, Laborpraktika und Bedside-Teaching auf der Literatur 1. Eliades MJ, Shah S, Nguyen-Dinh P, et al. Malaria surveillance United States, MMWR Surveill Summ 2005; 53(SS-2): Schlagenhauf P, Steffen R, Loutan L. Migrants as a major risk group for imported malaria in European countries. J Travel Med 2003; 10: McMichael AJ, Woodruff RE, Hales H. Climate change and human health: present and future risks. The Lancet 2006; 367: Meshnick SR, Alker AP. Malaria, not down and certainly not out. Am J Trop Med Hyg 2005; 73: Hoveyda N, McDonald P, Behrens RH. A Description of Travel Medicine in General Practice: A Postal Questionnaire Survey. J Travel Med 2004; 11 (5): MIKROBIOLOGE 17.Jg
Umgang mit MRSA in der Arztpraxis
 Infomarkt der Kassenärztlichen Vereinigung Berlin 06.04.2011 Umgang mit MRSA in der Arztpraxis Dr. Levke Quabeck Ärztliche Referentin im Ref. Infektionsschutz Senatsverwaltung für Gesundheit, Umwelt und
Infomarkt der Kassenärztlichen Vereinigung Berlin 06.04.2011 Umgang mit MRSA in der Arztpraxis Dr. Levke Quabeck Ärztliche Referentin im Ref. Infektionsschutz Senatsverwaltung für Gesundheit, Umwelt und
ESBL. Konsequenzen für die ambulante Pflege
 ESBL Konsequenzen für die ambulante Pflege ESBL = Extended spectrum Betalaktamase ß Laktamase: Ein Enzym, das von den Bakterien gebildet wird und den ß-Laktam Ring der folgenden ß-Laktam Antibiotika. Diese
ESBL Konsequenzen für die ambulante Pflege ESBL = Extended spectrum Betalaktamase ß Laktamase: Ein Enzym, das von den Bakterien gebildet wird und den ß-Laktam Ring der folgenden ß-Laktam Antibiotika. Diese
Infektionen des Gastrointestinaltraktes durch Parasiten
 Infektionen des Gastrointestinaltraktes durch Parasiten Andreas Müller Zentrum für Kinderheilkunde der Universität Bonn Protozoen und Diarrhoe Gardia lamblia Bis 2% bei akuter Diarrhoe* Cryptosporidium
Infektionen des Gastrointestinaltraktes durch Parasiten Andreas Müller Zentrum für Kinderheilkunde der Universität Bonn Protozoen und Diarrhoe Gardia lamblia Bis 2% bei akuter Diarrhoe* Cryptosporidium
Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor. Dr. med. Arno Köster
 Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor Dr. med. Arno Köster Definition Multiresistenz (MRE) ICD-10-GM Version 2010 U81! Bakterien mit Multiresistenz gegen
Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor Dr. med. Arno Köster Definition Multiresistenz (MRE) ICD-10-GM Version 2010 U81! Bakterien mit Multiresistenz gegen
Mikrosporidien: intrazelluläre Eukaryoten und opportunistische Krankheitserreger
 Mikrosporidien: intrazelluläre Eukaryoten und opportunistische Krankheitserreger Alexander MATHIS, Peter DEPLAZES & Rainer WEBER 1 Einleitung 266 2 Encephalitozoon cuniculi 267 3 Encephalitozoon hellem
Mikrosporidien: intrazelluläre Eukaryoten und opportunistische Krankheitserreger Alexander MATHIS, Peter DEPLAZES & Rainer WEBER 1 Einleitung 266 2 Encephalitozoon cuniculi 267 3 Encephalitozoon hellem
MRSA Typisierungen
 EUREGIO Gronau/Enschede MRSA Typisierungen 2012-2013 Ansprechpartner Dr. med. R. Köck Institut für Hygiene Universitätsklinikum Münster robin.koeck@ukmuenster.de Tel. 0251-83-55348 0 Inhaltsverzeichnis
EUREGIO Gronau/Enschede MRSA Typisierungen 2012-2013 Ansprechpartner Dr. med. R. Köck Institut für Hygiene Universitätsklinikum Münster robin.koeck@ukmuenster.de Tel. 0251-83-55348 0 Inhaltsverzeichnis
49. Fortbildungsveranstaltung für Hals-Nasen- Ohrenärzte
 Multiresistente Keime: Mikrobiologie, Hygiene Autor: Prof. Dr. med. Wolfgang Pfister, Universitätsklinikum Jena, Institut für Medizinische Mikrobiologie, Erlanger Allee 101, 07747 Jena, E-Mail: Wolfgang.Pfister@med.uni-jena.de
Multiresistente Keime: Mikrobiologie, Hygiene Autor: Prof. Dr. med. Wolfgang Pfister, Universitätsklinikum Jena, Institut für Medizinische Mikrobiologie, Erlanger Allee 101, 07747 Jena, E-Mail: Wolfgang.Pfister@med.uni-jena.de
Ambulante MRSA-Versorgung - aktuelle Situation und ungelöste Probleme
 Ambulante MRSA-Versorgung - aktuelle Situation und ungelöste Probleme 15. Göttinger Forum Krankenhaus- und Kommunalhygiene für den öffentlichen Gesundheitsdienst 24. und 25. November 2016 Dr. Jörg Herrmann
Ambulante MRSA-Versorgung - aktuelle Situation und ungelöste Probleme 15. Göttinger Forum Krankenhaus- und Kommunalhygiene für den öffentlichen Gesundheitsdienst 24. und 25. November 2016 Dr. Jörg Herrmann
MRSA-Screening. Screening am Israelitischen Krankenhaus. Abteilung Innere Medizin, IKH A. Friedrich
 MRSA-Screening Screening am Israelitischen Krankenhaus P. Schlömer Abteilung Innere Medizin, IKH A. Friedrich Institut für f r Hygiene, Universitätsklinikum tsklinikum MünsterM Notwendigkeit eines MRSA-Screenings
MRSA-Screening Screening am Israelitischen Krankenhaus P. Schlömer Abteilung Innere Medizin, IKH A. Friedrich Institut für f r Hygiene, Universitätsklinikum tsklinikum MünsterM Notwendigkeit eines MRSA-Screenings
Mikrobiologische Surveillance oder nicht, das ist hier die Frage,. Heinz Burgmann
 Mikrobiologische Surveillance oder nicht, das ist hier die Frage,. Mikrobiologische Untersuchungen auf der ICU Diagnostisch: Klinische Indikation Material aus normalerweise sterilen Bereich (Blut, Blase,
Mikrobiologische Surveillance oder nicht, das ist hier die Frage,. Mikrobiologische Untersuchungen auf der ICU Diagnostisch: Klinische Indikation Material aus normalerweise sterilen Bereich (Blut, Blase,
Die PCR-Diagnostik invasiver Mykosen
 Die PCR-Diagnostik invasiver Mykosen Dr.med. Ralf Bialek Institut für Tropenmedizin, Universitätsklinikum Tübingen Verbreitungsgebiete der Histoplasmose Kultur- und 18S rdna-pcr PCR-Ergebnisse zum
Die PCR-Diagnostik invasiver Mykosen Dr.med. Ralf Bialek Institut für Tropenmedizin, Universitätsklinikum Tübingen Verbreitungsgebiete der Histoplasmose Kultur- und 18S rdna-pcr PCR-Ergebnisse zum
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim
 MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
Multiresistente gramnegative Erreger Herausforderung für die Mikrobiologie? PD Dr. Reinhard Hoffmann Institut für Labormedizin und Mikrobiologie
 Multiresistente gramnegative Erreger Herausforderung für die Mikrobiologie? PD Dr. Reinhard Hoffmann Institut für Labormedizin und Mikrobiologie 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 2012
Multiresistente gramnegative Erreger Herausforderung für die Mikrobiologie? PD Dr. Reinhard Hoffmann Institut für Labormedizin und Mikrobiologie 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 2012
Richtlinie für Krankenhaushygiene und Infektionsprävention
 Richtlinie für Krankenhaushygiene und Infektionsprävention Inhaltsverzeichnis 21. Lieferung der Richtlinie für Krankenhaushygiene und Infektionsprävention Elsevier, Urban & Fischer Verlag München Jena
Richtlinie für Krankenhaushygiene und Infektionsprävention Inhaltsverzeichnis 21. Lieferung der Richtlinie für Krankenhaushygiene und Infektionsprävention Elsevier, Urban & Fischer Verlag München Jena
Surveillancesysteme in der Humanmedizin. Tim Eckmanns Robert Koch-Institut
 Surveillancesysteme in der Humanmedizin Tim Eckmanns Robert Koch-Institut Surveillance ist ein kontinuierlicher und systematischer Prozess der Erfassung, Analyse, Interpretation und Verbreitung beschreibender
Surveillancesysteme in der Humanmedizin Tim Eckmanns Robert Koch-Institut Surveillance ist ein kontinuierlicher und systematischer Prozess der Erfassung, Analyse, Interpretation und Verbreitung beschreibender
17. Gebiet Mikrobiologie, Virologie und Infektionsepidemiologie
 Auszug aus der Weiterbildungsordnung der Ärztekammer Niedersachsen und Richtlinien vom 01.05.2005, geändert zum 01.02.2012 (siehe jeweilige Fußnoten) 17. Gebiet Mikrobiologie, Virologie und Infektionsepidemiologie
Auszug aus der Weiterbildungsordnung der Ärztekammer Niedersachsen und Richtlinien vom 01.05.2005, geändert zum 01.02.2012 (siehe jeweilige Fußnoten) 17. Gebiet Mikrobiologie, Virologie und Infektionsepidemiologie
Befragung von Berliner Krankenhäusern zu MRSA und anderen Erregern. Irina Zuschneid Gesundheitsamt Friedrichshain-Kreuzberg
 Befragung von Berliner Krankenhäusern zu MRSA und anderen Erregern Irina Zuschneid Gesundheitsamt Friedrichshain-Kreuzberg Ziel der Befragung Erhebung des Ist-Zustands bezüglich Personal im Bereich Hygiene
Befragung von Berliner Krankenhäusern zu MRSA und anderen Erregern Irina Zuschneid Gesundheitsamt Friedrichshain-Kreuzberg Ziel der Befragung Erhebung des Ist-Zustands bezüglich Personal im Bereich Hygiene
Welche Labordaten werden gebraucht?
 Welche Labordaten werden gebraucht? A 1 Postoperative oberflächliche Wundinfektion Infektion an der Inzisionsstelle innerhalb von 3 Tagen nach der Operation, die nur Haut oder subkutanes Gewebe mit einbezieht,
Welche Labordaten werden gebraucht? A 1 Postoperative oberflächliche Wundinfektion Infektion an der Inzisionsstelle innerhalb von 3 Tagen nach der Operation, die nur Haut oder subkutanes Gewebe mit einbezieht,
8. Osnabrücker Hygienetag. 17. März 2010
 8. Osnabrücker Hygienetag aktiv für 17. März 2010 aktiv für Johann Peter Frank 1745-1821 Kann esaktiv wohl größeren Widerspruch füreinen geben als eine Spitalinfektion? Ein Übel, welches man da erst bekommt,
8. Osnabrücker Hygienetag aktiv für 17. März 2010 aktiv für Johann Peter Frank 1745-1821 Kann esaktiv wohl größeren Widerspruch füreinen geben als eine Spitalinfektion? Ein Übel, welches man da erst bekommt,
Kosten nosokomialer Pneumonien mit und ohne multiresistente Erreger (MRE)
 Kosten nosokomialer Pneumonien mit und ohne multiresistente Erreger (MRE) 2. Hygienetag Köln 12.10.2011 Häufigkeit nosokomialer Pneumonien auf Intensivstationen Gepoolter arithm. Mittelwert Pneumonie HWI
Kosten nosokomialer Pneumonien mit und ohne multiresistente Erreger (MRE) 2. Hygienetag Köln 12.10.2011 Häufigkeit nosokomialer Pneumonien auf Intensivstationen Gepoolter arithm. Mittelwert Pneumonie HWI
Dr. med. Andreas F. Wendel Institut für Hygiene. Carbapenemasen - search and detect
 Carbapenemasen - search and detect Dr. med. Andreas F. Wendel Institut für Hygiene Klinisch relevante Carbapenemase-bildende gramnegative Bakterien (CDC) Carbapenemaseproduzierende Enterobakterien (VERY)
Carbapenemasen - search and detect Dr. med. Andreas F. Wendel Institut für Hygiene Klinisch relevante Carbapenemase-bildende gramnegative Bakterien (CDC) Carbapenemaseproduzierende Enterobakterien (VERY)
ESBL. Konsequenzen für die stationäre Pflege
 ESBL Konsequenzen für die stationäre Pflege ESBL-Bildner ESBL = Extended spectrum Betalaktamase ß Laktamase: Ein Enzym, das von den Bakterien gebildet wird und den ß-Laktam Ring der folgenden ß-Laktam
ESBL Konsequenzen für die stationäre Pflege ESBL-Bildner ESBL = Extended spectrum Betalaktamase ß Laktamase: Ein Enzym, das von den Bakterien gebildet wird und den ß-Laktam Ring der folgenden ß-Laktam
Krankenhaus-Hygiene Über das Richtige berichten - Anforderungen an die Datenerfassung und das Reporting
 Krankenhaus-Hygiene Über das Richtige berichten - Anforderungen an die Datenerfassung und das Reporting Ingo Pfenning Stationäre Versorgung Techniker Krankenkasse Vortrag am 15.Mai 2012 in Berlin Hygienesymposium
Krankenhaus-Hygiene Über das Richtige berichten - Anforderungen an die Datenerfassung und das Reporting Ingo Pfenning Stationäre Versorgung Techniker Krankenkasse Vortrag am 15.Mai 2012 in Berlin Hygienesymposium
Diagnostik von Infektionen. Professor Christian Ruef Institut für Infektiologie und Spitalhygiene
 Diagnostik von Infektionen Professor Christian Ruef Institut für Infektiologie und Spitalhygiene 1 Schwerpunkte Einleitung, Uebersicht Klinische Beispiele Sepsis Pneumonie auf der Intensivstation Ausblick
Diagnostik von Infektionen Professor Christian Ruef Institut für Infektiologie und Spitalhygiene 1 Schwerpunkte Einleitung, Uebersicht Klinische Beispiele Sepsis Pneumonie auf der Intensivstation Ausblick
MRE AK Krankenhäuser Punktprävalenz-Untersuchung MRE Netzwerk Metropolregion Rhein-Neckar
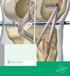 MRE AK Krankenhäuser Punktprävalenz-Untersuchung MRE Netzwerk Metropolregion Rhein-Neckar Warum sind wir hier? Wir möchten Ihnen eine Untersuchung vorstellen, die zeigt dass die Zahl der von multiresistenten
MRE AK Krankenhäuser Punktprävalenz-Untersuchung MRE Netzwerk Metropolregion Rhein-Neckar Warum sind wir hier? Wir möchten Ihnen eine Untersuchung vorstellen, die zeigt dass die Zahl der von multiresistenten
Während der Synthese synthetisiert die Polymerase den neuen Strang in 5 3 Richtung und bewegt sich in 3 5 -Richtung am Matrizenstrang entlang:
 4.4 Replikation und PCR Ablauf der Replikation in vivo: Die Replikation wird von einer DNA-abhängigen DNA- Polymerase katalysiert. Jede DNA-Polymerase synthetisiert den neuen Strang in 5 3 Richtung, hierzu
4.4 Replikation und PCR Ablauf der Replikation in vivo: Die Replikation wird von einer DNA-abhängigen DNA- Polymerase katalysiert. Jede DNA-Polymerase synthetisiert den neuen Strang in 5 3 Richtung, hierzu
MRSA Alles im Griff, Alles klar, Alles unter Kontrolle? 17. Dezember 2014
 MRSA Alles im Griff, Alles klar, Alles unter Kontrolle? Aktuelle Daten, Zahlen und die neue KRINKO-MRSA-Empfehlung 6/2014 17. Dezember 2014 Jürgen Krahn der Stadt Darmstadt und des Landkreises Themen 1.
MRSA Alles im Griff, Alles klar, Alles unter Kontrolle? Aktuelle Daten, Zahlen und die neue KRINKO-MRSA-Empfehlung 6/2014 17. Dezember 2014 Jürgen Krahn der Stadt Darmstadt und des Landkreises Themen 1.
MRSA. (Methicillin-resistenter Staphylococcus aureus)
 MRSA (Methicillin-resistenter Staphylococcus aureus) Gemeinsam auf Nummer sicher Liebe Patientin, lieber Patient, herzlich willkommen in der Fachklinik 360 Die Klinik für Orthopädie und Rheumatologie der
MRSA (Methicillin-resistenter Staphylococcus aureus) Gemeinsam auf Nummer sicher Liebe Patientin, lieber Patient, herzlich willkommen in der Fachklinik 360 Die Klinik für Orthopädie und Rheumatologie der
Übersicht. Definitionen MRSA, ca-mrsa,... Epidemiologie von ca-mrsa. Beschreibung von Virulenz, Klinik, Therapie von ca-mrsa.
 1 Übersicht Definitionen MRSA, ca-mrsa,... Epidemiologie von ca-mrsa Beschreibung von Virulenz, Klinik, Therapie von ca-mrsa Ca-MRSA Ausbrüche Prävention von Erkrankungen und Ausbrüchen 2 Staphylococcus
1 Übersicht Definitionen MRSA, ca-mrsa,... Epidemiologie von ca-mrsa Beschreibung von Virulenz, Klinik, Therapie von ca-mrsa Ca-MRSA Ausbrüche Prävention von Erkrankungen und Ausbrüchen 2 Staphylococcus
Empfehlungen der KRINKO zum Umgang mit ESBL MRGN. Prof. Dr. C. Wendt
 Empfehlungen der KRINKO zum Umgang mit ESBL MRGN Prof. Dr. C. Wendt Alle Krankenhäuser MRSA 3/4 MRGN E. coli und Klebs. Trend MRSA Trend 4/4 MRGN E. coli Klbes. 3500 3000 2500 Patienten 2000 1500 1000
Empfehlungen der KRINKO zum Umgang mit ESBL MRGN Prof. Dr. C. Wendt Alle Krankenhäuser MRSA 3/4 MRGN E. coli und Klebs. Trend MRSA Trend 4/4 MRGN E. coli Klbes. 3500 3000 2500 Patienten 2000 1500 1000
Die Novellierung des Infektionsschutzgesetzes. -Was hat sich geändert?-
 19. VKD/VDGH Führungskräfteseminar Zukunft der Patientenversorgung- Gesetzliche Herausforderungen und Best Practice in den Krankenhäusern Die Novellierung des Infektionsschutzgesetzes -Was hat sich geändert?-
19. VKD/VDGH Führungskräfteseminar Zukunft der Patientenversorgung- Gesetzliche Herausforderungen und Best Practice in den Krankenhäusern Die Novellierung des Infektionsschutzgesetzes -Was hat sich geändert?-
Aktuelle Resistenzsituation in Klinik und Praxis
 Bad Honnef-Symposium 2014 15. April 2014, Königswinter Aktuelle Resistenzsituation in Klinik und Praxis Ines Noll Robert Koch-Institut Fachgebiet Nosokomiale Infektionen, Surveillance von Antibiotikaresistenz
Bad Honnef-Symposium 2014 15. April 2014, Königswinter Aktuelle Resistenzsituation in Klinik und Praxis Ines Noll Robert Koch-Institut Fachgebiet Nosokomiale Infektionen, Surveillance von Antibiotikaresistenz
MRSA-Last in einer Universitätsklinik. Maßnahmen zur Senkung und Kontrolle
 MRSA-Last in einer Universitätsklinik Maßnahmen zur Senkung und Kontrolle Ella Ott Institut für Medizinische Mikrobiologie und Krankenhaushygiene MRSA - Bedeutung Zunahme der Morbidität Erhöhtes Risiko
MRSA-Last in einer Universitätsklinik Maßnahmen zur Senkung und Kontrolle Ella Ott Institut für Medizinische Mikrobiologie und Krankenhaushygiene MRSA - Bedeutung Zunahme der Morbidität Erhöhtes Risiko
48. Fortbildungsveranstaltung für Hals-Nasen- Ohrenärzte
 Multiresistente Keime in der Praxis von Dr. Ute Helke Dobermann Autorin: Dr. Ute Helke Dobermann, Universitätsklinikum Jena, Erlanger Allee 101, 07740 Jena, Helke.Dobermann@med.uni-jena.de Einleitung:
Multiresistente Keime in der Praxis von Dr. Ute Helke Dobermann Autorin: Dr. Ute Helke Dobermann, Universitätsklinikum Jena, Erlanger Allee 101, 07740 Jena, Helke.Dobermann@med.uni-jena.de Einleitung:
Bremer Fachtag Legionellen
 Bremer Fachtag Legionellen Grundlagen der Infektionsgefahr 25.10.2017 Dr. med. Monika Lelgemann MSc Gesundheitsamt Bremen Abteilung 2 / Sozialmedizin Erwachsene Legionellen - Hintergrund Legionärskrankheit
Bremer Fachtag Legionellen Grundlagen der Infektionsgefahr 25.10.2017 Dr. med. Monika Lelgemann MSc Gesundheitsamt Bremen Abteilung 2 / Sozialmedizin Erwachsene Legionellen - Hintergrund Legionärskrankheit
Rili-BÄK Spezieller Teil B 3. Carmen Hansen, Bio-Rad Laboratories GmbH
 Rili-BÄK Spezieller Teil B 3 Carmen Hansen, Bio-Rad Laboratories GmbH Spezieller Teil B 3 Direkter Nachweis und Charakterisierung von Infektionserregern Deutsches Ärzteblatt, Jahrgang 110, Heft 12, 22.
Rili-BÄK Spezieller Teil B 3 Carmen Hansen, Bio-Rad Laboratories GmbH Spezieller Teil B 3 Direkter Nachweis und Charakterisierung von Infektionserregern Deutsches Ärzteblatt, Jahrgang 110, Heft 12, 22.
Multiresistente Keime - Therapie
 Multiresistente Keime - Therapie Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Ted-Frage 1 Welche Erreger sind Ihrer Ansicht
Multiresistente Keime - Therapie Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Ted-Frage 1 Welche Erreger sind Ihrer Ansicht
Multiresistente Gram-negative Bakterien (MRGN) Problemkeime des 21. Jahrhunderts
 Multiresistente Gram-negative Bakterien (MRGN) Problemkeime des 21. Jahrhunderts Prävention der Ausbreitung Präzise und rasche Diagnostik Konsequente Infektionskontrolle Rationaler Antibiotika- Einsatz
Multiresistente Gram-negative Bakterien (MRGN) Problemkeime des 21. Jahrhunderts Prävention der Ausbreitung Präzise und rasche Diagnostik Konsequente Infektionskontrolle Rationaler Antibiotika- Einsatz
Zielgerichtete Therapie der Clostridium-difficile-assoziierten Diarrhoe von Anfang an
 Vancomycin Zielgerichtete Therapie der Clostridium-difficile-assoziierten Diarrhoe von Anfang an Münster (23. April 2013) Im Rahmen eines Presseroundtables diskutierten drei namhafte Experten über die
Vancomycin Zielgerichtete Therapie der Clostridium-difficile-assoziierten Diarrhoe von Anfang an Münster (23. April 2013) Im Rahmen eines Presseroundtables diskutierten drei namhafte Experten über die
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER
 Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
Clostridium difficile. Dr. med. M. Herz ZE Interne Krankenhaushygiene, UKSH, Campus Kiel
 Clostridium difficile Dr. med. M. Herz ZE Interne Krankenhaushygiene, UKSH, Campus Kiel Clostridium difficile zählt zu den häufigsten identifizierten Erregern einer nosokomial erworbenen Diarrhoe international
Clostridium difficile Dr. med. M. Herz ZE Interne Krankenhaushygiene, UKSH, Campus Kiel Clostridium difficile zählt zu den häufigsten identifizierten Erregern einer nosokomial erworbenen Diarrhoe international
Inhalt. Entdeckung und allgemeine Informationen. Klassifizierung. Genom Viren untypische Gene Tyrosyl-tRNA Synthetase. Ursprung von grossen DNA Viren
 Mimivirus Inhalt Entdeckung und allgemeine Informationen Klassifizierung Genom Viren untypische Gene Tyrosyl-tRNA Synthetase Ursprung von grossen DNA Viren Entstehung von Eukaryoten Entdeckung 1992 in
Mimivirus Inhalt Entdeckung und allgemeine Informationen Klassifizierung Genom Viren untypische Gene Tyrosyl-tRNA Synthetase Ursprung von grossen DNA Viren Entstehung von Eukaryoten Entdeckung 1992 in
Krankenhaus-Hygiene Aktuell
 Krankenhaus-Hygiene Aktuell Juni 2015 Gundi Heuschen Weltweite Situation Globaler Reiseverkehr: Schnelle Verbreitung weltweit innerhalb weniger Stunden Steigende Infektionsraten Zunehmende Antibiotikaresistenzen
Krankenhaus-Hygiene Aktuell Juni 2015 Gundi Heuschen Weltweite Situation Globaler Reiseverkehr: Schnelle Verbreitung weltweit innerhalb weniger Stunden Steigende Infektionsraten Zunehmende Antibiotikaresistenzen
Schnelle Diagnostik durch molekularbiologische und massenspektrometrische Verfahren
 Schnelle Diagnostik durch molekularbiologische und massenspektrometrische Verfahren 10.10.2017 ECMM-Symposium Priv. Doz. Dr. med. Axel Hamprecht Institut für medizinische Mikrobiologie, Immunologie und
Schnelle Diagnostik durch molekularbiologische und massenspektrometrische Verfahren 10.10.2017 ECMM-Symposium Priv. Doz. Dr. med. Axel Hamprecht Institut für medizinische Mikrobiologie, Immunologie und
Hygiene-Daten nutzen für Patientenfürsprecher. Düsseldorf 14. November Walter Popp
 Hygiene-Daten nutzen für Patientenfürsprecher Düsseldorf 14. November 2017 Walter Popp Seite 1 Daten mit Bezug zur Hygiene Hygienekommission Hygienepersonal Begehungsberichte Händehygiene OP-Hygiene Screening
Hygiene-Daten nutzen für Patientenfürsprecher Düsseldorf 14. November 2017 Walter Popp Seite 1 Daten mit Bezug zur Hygiene Hygienekommission Hygienepersonal Begehungsberichte Händehygiene OP-Hygiene Screening
Daten mit Bezug zur Hygiene
 Hygiene-Daten nutzen für Patientenfürsprecher Düsseldorf 14. November 2017 Walter Popp Seite 1 Daten mit Bezug zur Hygiene Hygienekommission Hygienepersonal Begehungsberichte Händehygiene OP-Hygiene Screening
Hygiene-Daten nutzen für Patientenfürsprecher Düsseldorf 14. November 2017 Walter Popp Seite 1 Daten mit Bezug zur Hygiene Hygienekommission Hygienepersonal Begehungsberichte Händehygiene OP-Hygiene Screening
Vortrag. Aktuelle Zahlen zu Screening und multiresistenten Erregern aus den Kliniken Mühldorf
 Vortrag Aktuelle Zahlen zu Screening und multiresistenten Erregern aus den Kliniken Mühldorf Thomas Kitzeder - 10.11.2015 (Quelle: FAZ-Net_25.08.2010_Christiane Pfohlmann_ Tag der Offenen Tür ) Der Zufall
Vortrag Aktuelle Zahlen zu Screening und multiresistenten Erregern aus den Kliniken Mühldorf Thomas Kitzeder - 10.11.2015 (Quelle: FAZ-Net_25.08.2010_Christiane Pfohlmann_ Tag der Offenen Tür ) Der Zufall
Basierend auf Publikation: Ahmadian A, Ehn M, Hober S. (2006): Pyrosequencing: history, biochemistry and future; Clin Chim Acta. 363(1-2):83-94.
 In diesem Skript wird der Versuch unternommen, der Prozess Pyrosequencing so zu erklären, dass Schüler die Chance haben Pyrosequencing zu verstehen. Es basiert auf einem Vortrag im Rahmen des Science Bridge
In diesem Skript wird der Versuch unternommen, der Prozess Pyrosequencing so zu erklären, dass Schüler die Chance haben Pyrosequencing zu verstehen. Es basiert auf einem Vortrag im Rahmen des Science Bridge
Klebsiella pneumoniae
 Enterobakterien E. coli Klebsiella spp., Klebsiella pneumoniae Enterobacter spp. (Serratia spp., Citrobacter spp., Proteus spp., Morganella morganii) Enterobakterien allgemein Natürliche Darmflora von
Enterobakterien E. coli Klebsiella spp., Klebsiella pneumoniae Enterobacter spp. (Serratia spp., Citrobacter spp., Proteus spp., Morganella morganii) Enterobakterien allgemein Natürliche Darmflora von
Multiresistente Erreger und Antibiotikaresistenzen
 Rationaler Antibiotikaeinsatz durch Information und Kommunikation Multiresistente Erreger und Antibiotikaresistenzen Professor Petra Gastmeier Dr. med. Tobias Kramer Dr. med. Florian Salm Institut für
Rationaler Antibiotikaeinsatz durch Information und Kommunikation Multiresistente Erreger und Antibiotikaresistenzen Professor Petra Gastmeier Dr. med. Tobias Kramer Dr. med. Florian Salm Institut für
BESCHLUSS. des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011
 BESCHLUSS des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 Vergütungsvereinbarung für ärztliche Leistungen
BESCHLUSS des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 Vergütungsvereinbarung für ärztliche Leistungen
Erratum BESCHLUSS. des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011
 Erratum zum Beschluss des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 In dem Beschluss des Bewertungsausschusses
Erratum zum Beschluss des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 266. Sitzung am 14. Dezember 2011 mit Wirkung zum 1. April 2012 bis zum 31. März 2014 In dem Beschluss des Bewertungsausschusses
TUBERKULOSE Ansteckungswege, Erkennung und Behandlung
 TUBERKULOSE Ansteckungswege, Erkennung und Behandlung Marie Charlotte von Heinz Gesundheitsamt Hamburg-Mitte Wohnungslose: Ganz schön krank! Hamburg, 05. November 2008 Inhalt 1. Verbreitung der Tuberkulose
TUBERKULOSE Ansteckungswege, Erkennung und Behandlung Marie Charlotte von Heinz Gesundheitsamt Hamburg-Mitte Wohnungslose: Ganz schön krank! Hamburg, 05. November 2008 Inhalt 1. Verbreitung der Tuberkulose
MRE-Typisierungsmethoden
 MRE-Typisierungsmethoden AG Krankenhaushygiene im Bezirksamt Tempelhof-Schöneberg von Berlin 08.03.2017 1 RESISTOGRAMME DIREKTVERGLEICH 2 PULSFELDGELELEKTROPHORESE (PFGE) 3 PULSFELDGELELEKTROPHORESE (PFGE)
MRE-Typisierungsmethoden AG Krankenhaushygiene im Bezirksamt Tempelhof-Schöneberg von Berlin 08.03.2017 1 RESISTOGRAMME DIREKTVERGLEICH 2 PULSFELDGELELEKTROPHORESE (PFGE) 3 PULSFELDGELELEKTROPHORESE (PFGE)
Sicherer Umgang mit multiresistenten Keimen. Informationen für Patienten und Angehörige
 Sicherer Umgang mit multiresistenten Keimen Informationen für Patienten und Angehörige Gemeinsam gegen Keime und Bakterien Räumliche Unterbringung Als Vorsichtsmaßnahme werden Sie gegebenenfalls in einem
Sicherer Umgang mit multiresistenten Keimen Informationen für Patienten und Angehörige Gemeinsam gegen Keime und Bakterien Räumliche Unterbringung Als Vorsichtsmaßnahme werden Sie gegebenenfalls in einem
Testmethoden der Molekularpathologie. im Vergleich
 Testmethoden der Molekularpathologie im Vergleich Andreas Bösl (Feldkirch) Gerlinde Winter (Graz) Testmethoden der Molekularpathologie PCR Fragmentanalyse Gelelektrophorese, Kapillarelektrophorese Sequenzierung
Testmethoden der Molekularpathologie im Vergleich Andreas Bösl (Feldkirch) Gerlinde Winter (Graz) Testmethoden der Molekularpathologie PCR Fragmentanalyse Gelelektrophorese, Kapillarelektrophorese Sequenzierung
Resistenzentwicklung -international, national, regional
 Infektiologie Update 2014 24. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Workshop der Sektion Grundlagen: Antibiotikaresistenz - Epidemiologie, Detektion & Therapiestrategie 17.
Infektiologie Update 2014 24. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Workshop der Sektion Grundlagen: Antibiotikaresistenz - Epidemiologie, Detektion & Therapiestrategie 17.
Laborinformation
 Institut für Medizinische Mikrobiologie und Krankenhaushygiene Prof. Dr. med. Dirk Schlüter Direktor Telefon: +49 391 67-13392 Telefax: +49 391 67-13384 dirk.schlueter@med.ovgu.de Laborinformation 29.06.2018
Institut für Medizinische Mikrobiologie und Krankenhaushygiene Prof. Dr. med. Dirk Schlüter Direktor Telefon: +49 391 67-13392 Telefax: +49 391 67-13384 dirk.schlueter@med.ovgu.de Laborinformation 29.06.2018
HYGIENE. Wo liegt die Grenze zwischen Krankenhaushygiene und Sauberkeit?
 Wo liegt die Grenze zwischen Krankenhaushygiene und Sauberkeit? Tagung des Bundesverbandes Beschwerdemanagement, 07.10.2016 PD Dr. med. Dr. PH Frank Kipp Institut für Hygiene HYGIENE Hygiene ist nach einer
Wo liegt die Grenze zwischen Krankenhaushygiene und Sauberkeit? Tagung des Bundesverbandes Beschwerdemanagement, 07.10.2016 PD Dr. med. Dr. PH Frank Kipp Institut für Hygiene HYGIENE Hygiene ist nach einer
Innovative Laborparameter für die urologische Praxis
 Innovative Laborparameter für die urologische Praxis Chlamydia trachomatis Antikörper Darmkrebsvorsorge M2-PK-Quick Dr. Monika Börner UCM 9. Herbstklausurtagung 21. November 2009 Kloster Seeon Innovative
Innovative Laborparameter für die urologische Praxis Chlamydia trachomatis Antikörper Darmkrebsvorsorge M2-PK-Quick Dr. Monika Börner UCM 9. Herbstklausurtagung 21. November 2009 Kloster Seeon Innovative
MRE außerhalb des Krankenhauses: wer übernimmt die Verantwortung. Constanze Wendt Hygiene-Institut Heidelberg
 MRE außerhalb des Krankenhauses: wer übernimmt die Verantwortung Constanze Wendt Hygiene-Institut Heidelberg Ärztliche Versorgung Die ärztliche Grundversorgung im ambulanten Bereich wird durch den Hausarzt
MRE außerhalb des Krankenhauses: wer übernimmt die Verantwortung Constanze Wendt Hygiene-Institut Heidelberg Ärztliche Versorgung Die ärztliche Grundversorgung im ambulanten Bereich wird durch den Hausarzt
Molekularpathologische Untersuchungen aus Paraffinmaterial. OA Dr. Martina Hassmann Institut für Pathologie und Mikrobiologie LKH HORN
 Molekularpathologische Untersuchungen aus Paraffinmaterial OA Dr. Martina Hassmann Institut für Pathologie und Mikrobiologie LKH HORN PCR-Untersuchung aus Paraffinmaterial - Bei Tumoren: K-Ras-,EGFR-Mutation,
Molekularpathologische Untersuchungen aus Paraffinmaterial OA Dr. Martina Hassmann Institut für Pathologie und Mikrobiologie LKH HORN PCR-Untersuchung aus Paraffinmaterial - Bei Tumoren: K-Ras-,EGFR-Mutation,
Mikrobiologie der Knocheninfektion mit Problematik der multiresistenten Erreger
 Mikrobiologie der Knocheninfektion mit Problematik der multiresistenten Erreger Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie Außenstelle Großhadern
Mikrobiologie der Knocheninfektion mit Problematik der multiresistenten Erreger Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie Außenstelle Großhadern
Diabetisches Fußsyndrom
 Präanalytik Interdisziplinärer Laborworkshop 13.12.2008 Mainz Dr. med. Anne-Marie Fahr Labor Limbach Heidelberg Voraussetzungen für die Materialabnahme (und für die antimikrobielle Therapie) Diagnose Wundinfektion
Präanalytik Interdisziplinärer Laborworkshop 13.12.2008 Mainz Dr. med. Anne-Marie Fahr Labor Limbach Heidelberg Voraussetzungen für die Materialabnahme (und für die antimikrobielle Therapie) Diagnose Wundinfektion
Diagnostik und Dekolonisation bei MRSA und anderen MRE. Dr. Michael Eckardt Krankenhaushygieniker Kreiskliniken Darmstadt-Dieburg
 Diagnostik und Dekolonisation bei MRSA und anderen MRE Dr. Michael Eckardt Krankenhaushygieniker Kreiskliniken Darmstadt-Dieburg Worum geht s? MRSA-Diagnostik - Warum? - Wann? - Wie? MRSA-Dekolonisation
Diagnostik und Dekolonisation bei MRSA und anderen MRE Dr. Michael Eckardt Krankenhaushygieniker Kreiskliniken Darmstadt-Dieburg Worum geht s? MRSA-Diagnostik - Warum? - Wann? - Wie? MRSA-Dekolonisation
Monitoring von Resistenzen in der Humanmedizin. Tim Eckmanns Robert Koch-Institut
 Monitoring von Resistenzen in der Humanmedizin Tim Eckmanns Robert Koch-Institut Unterschied Monitoring und Surveillance von Antibiotikaresistenzdaten Another task of epidemiology is monitoring or surveillance
Monitoring von Resistenzen in der Humanmedizin Tim Eckmanns Robert Koch-Institut Unterschied Monitoring und Surveillance von Antibiotikaresistenzdaten Another task of epidemiology is monitoring or surveillance
KISS-Definitionen des Nationalen Referenzzentrums zu postoperativen Wundinfektionen (Stand )
 Information für weiterbehandelnde Ärzte KISS-Definitionen des Nationalen Referenzzentrums zu postoperativen Wundinfektionen (Stand 01.01.2017) Zur Erfassung nosokomialer, postoperativer Wundinfektionen
Information für weiterbehandelnde Ärzte KISS-Definitionen des Nationalen Referenzzentrums zu postoperativen Wundinfektionen (Stand 01.01.2017) Zur Erfassung nosokomialer, postoperativer Wundinfektionen
Mikrosporidiosen des Menschen - Wo ist das Reservoir?
 Mitt. Österr. Ges. Tropenmed. Parasitol. 22 (2000) Abteilung für Infektions- und Tropenmedizin (Leiter: Prof. Dr. T. Löscher) der Universität München (1) Institut für Vergleichende Tropenmedizin u. Parasitologie
Mitt. Österr. Ges. Tropenmed. Parasitol. 22 (2000) Abteilung für Infektions- und Tropenmedizin (Leiter: Prof. Dr. T. Löscher) der Universität München (1) Institut für Vergleichende Tropenmedizin u. Parasitologie
50. Fortbildungsveranstaltung für Hals-Nasen- Ohrenärzte
 Expertenrunde: Informationen zu aktuellen medizinischen Themen: Evidente Therapie bei Infektionen Antibiotikaeinsatz, Indikationen für antivirale Therapie in der HNO Autor: Prof. Dr. med. Wolfgang Pfister,
Expertenrunde: Informationen zu aktuellen medizinischen Themen: Evidente Therapie bei Infektionen Antibiotikaeinsatz, Indikationen für antivirale Therapie in der HNO Autor: Prof. Dr. med. Wolfgang Pfister,
Diagnostik von CDI Verlässlichkeit kommerzieller Tests und sinnvolle Algorithmen
 Diagnostik von CDI Verlässlichkeit kommerzieller Tests und sinnvolle Algorithmen Athanasios Makristathis Klinische Abteilung für Mikrobiologie Klinisches Institut für Labormedizin 1 Pathogenetische Aspekte
Diagnostik von CDI Verlässlichkeit kommerzieller Tests und sinnvolle Algorithmen Athanasios Makristathis Klinische Abteilung für Mikrobiologie Klinisches Institut für Labormedizin 1 Pathogenetische Aspekte
STS-Verzeichnis Akkreditierungsnummer: STS 0363
 Internationale Norm: ISO/IEC 17025:2005 Schweizer Norm: SN EN ISO/IEC 17025:2005 Institut für Infektionskrankheiten der Universität Bern Abteilung für Klinische Mikrobiologie Friedbühlstrasse 51 Postfach
Internationale Norm: ISO/IEC 17025:2005 Schweizer Norm: SN EN ISO/IEC 17025:2005 Institut für Infektionskrankheiten der Universität Bern Abteilung für Klinische Mikrobiologie Friedbühlstrasse 51 Postfach
Influenza eine unterschätzte Krankheit
 Influenza eine unterschätzte Krankheit Cornelia Otto Abteilung Hygiene und Umweltmedizin, Sachgebiet Infektionshygiene/Medizinalwesen Referat für Gesundheit und Umwelt Landeshauptstadt München Infektionshygiene.rgu@muenchen.de
Influenza eine unterschätzte Krankheit Cornelia Otto Abteilung Hygiene und Umweltmedizin, Sachgebiet Infektionshygiene/Medizinalwesen Referat für Gesundheit und Umwelt Landeshauptstadt München Infektionshygiene.rgu@muenchen.de
Multiresistente Erreger (MRE)/ Clostridium difficile 5. Runder Tisch für Hygienebeauftragte in der stationären Pflege
 5. Runder Tisch für Hygienebeauftragte in der stationären Pflege 26.06.2018 Silke Hildebrandt Petra Huber Hygiene und Umweltmedizin/ Infektionshygiene Referat für Gesundheit und Umweltschutz Landeshauptstadt
5. Runder Tisch für Hygienebeauftragte in der stationären Pflege 26.06.2018 Silke Hildebrandt Petra Huber Hygiene und Umweltmedizin/ Infektionshygiene Referat für Gesundheit und Umweltschutz Landeshauptstadt
Multiresistente Erreger und Patientensicherheit
 Multiresistente Erreger und Patientensicherheit Maßnahmen und Erfahrungen im klinischen Alltag Krankenhausinfektionen Hintergründe, Gefahren und Strategien Prof. Dr. med. Julia Seifert 06.03.2015 Mehr
Multiresistente Erreger und Patientensicherheit Maßnahmen und Erfahrungen im klinischen Alltag Krankenhausinfektionen Hintergründe, Gefahren und Strategien Prof. Dr. med. Julia Seifert 06.03.2015 Mehr
Identifizierung von Zellen des mononukleären phagozytierenden Systems (MPS)
 63 Die Milzen der mit dem Adenovirus FAV1 infizierten Jungmasthühner (Positivkontrollen) wiesen unter Einsatz der Lymphozytenmarker CD3 (Dako), CD3 (Biozol), IgM und IgG deutlich oberflächengefärbte Lymphozyten
63 Die Milzen der mit dem Adenovirus FAV1 infizierten Jungmasthühner (Positivkontrollen) wiesen unter Einsatz der Lymphozytenmarker CD3 (Dako), CD3 (Biozol), IgM und IgG deutlich oberflächengefärbte Lymphozyten
Urogenitale Infektionserreger mittels PCR
 Urogenitale Infektionserreger mittels PCR Dr. Monika Börner Planegg 09. September 2009 Urogenitale Infektionserreger mittels PCR Grundlagen / Allgemeines Chlamydia trachomatis Neisseria gonorrhoeae Mykoplasmen
Urogenitale Infektionserreger mittels PCR Dr. Monika Börner Planegg 09. September 2009 Urogenitale Infektionserreger mittels PCR Grundlagen / Allgemeines Chlamydia trachomatis Neisseria gonorrhoeae Mykoplasmen
Novellierung des Infektionsschutzgesetzes - Konsequenzen für die Praxis - Christoph Huesmann. Fachkrankenpfleger für Hygiene und Infektionsprävention
 Novellierung des Infektionsschutzgesetzes - Konsequenzen für die Praxis - Christoph Huesmann Fachkrankenpfleger für Hygiene und Infektionsprävention Entwicklung Bundesseuchengesetz Bekämpfung ansteckender
Novellierung des Infektionsschutzgesetzes - Konsequenzen für die Praxis - Christoph Huesmann Fachkrankenpfleger für Hygiene und Infektionsprävention Entwicklung Bundesseuchengesetz Bekämpfung ansteckender
Die zoonotische Komponente des MRSA-Komplexes
 Die zoonotische Komponente des MRSA-Komplexes Methicillin-resistente Staphylococcus aureus bei beruflich mit dem Schwein exponierten Personen Meemken, D.; Jansen, A.; Kleinkauf, N.; Eckmanns, T.; Blaha,
Die zoonotische Komponente des MRSA-Komplexes Methicillin-resistente Staphylococcus aureus bei beruflich mit dem Schwein exponierten Personen Meemken, D.; Jansen, A.; Kleinkauf, N.; Eckmanns, T.; Blaha,
und Linezolid sind mit hohen Tagestherapiekosten verbunden und auch resistente MRSA-Stämme gegen diese Substanzen sind bereits aufgetreten [28,29].
![und Linezolid sind mit hohen Tagestherapiekosten verbunden und auch resistente MRSA-Stämme gegen diese Substanzen sind bereits aufgetreten [28,29]. und Linezolid sind mit hohen Tagestherapiekosten verbunden und auch resistente MRSA-Stämme gegen diese Substanzen sind bereits aufgetreten [28,29].](/thumbs/54/33822289.jpg) 1. EINLEITUNG Methicillin-resistente Stämme der Spezies Staphylococcus aureus (MRSA) wurden erstmals 1961 in Großbritannien beschrieben [1,2]. Das semisynthetische Penicillin Methicillin wurde erst zwei
1. EINLEITUNG Methicillin-resistente Stämme der Spezies Staphylococcus aureus (MRSA) wurden erstmals 1961 in Großbritannien beschrieben [1,2]. Das semisynthetische Penicillin Methicillin wurde erst zwei
Schnelle Tests für gute Hygiene
 Schnelle Tests für gute Hygiene Thomas Valentin Sektion für Infektiologie und Tropenmedizin Universitätsklinik für Innere Medizin LKH Universitätsklinikum Graz Sinn von Schnelltests Möglichst früh (idealerweise
Schnelle Tests für gute Hygiene Thomas Valentin Sektion für Infektiologie und Tropenmedizin Universitätsklinik für Innere Medizin LKH Universitätsklinikum Graz Sinn von Schnelltests Möglichst früh (idealerweise
Neues von Mucor & Co
 Neues von Mucor & Co Birgit Willinger Abteilung für Klinische Mikrobiologie Klinisches Institut für Labormedizin Birgit Wilinger Abteilung für Klinische Mikrobiologie, Klinisches Institut für Labormedizin1
Neues von Mucor & Co Birgit Willinger Abteilung für Klinische Mikrobiologie Klinisches Institut für Labormedizin Birgit Wilinger Abteilung für Klinische Mikrobiologie, Klinisches Institut für Labormedizin1
Entwicklung einer Multiplex-PCR zum Nachweis Enteropathogener Escherichia coli
 Charité-Universitätsmedizin Berlin Campus Benjamin Franklin Aus dem Institut für Infektionsmedizin Geschäftsführender Direktor Prof. Dr. med. Dr. h.c. Helmut Hahn Abteilung: Medizinische Mikrobiologie
Charité-Universitätsmedizin Berlin Campus Benjamin Franklin Aus dem Institut für Infektionsmedizin Geschäftsführender Direktor Prof. Dr. med. Dr. h.c. Helmut Hahn Abteilung: Medizinische Mikrobiologie
Wissenschaftlich-technische Entwicklungen im Bereich der Multiplex- und High-Throughput-Diagnostik. Karl J. Lackner
 Wissenschaftlich-technische Entwicklungen im Bereich der Multiplex- und High-Throughput-Diagnostik Karl J. Lackner Hochdurchsatzverfahren in der molekularen bzw. genetischen Diagnostik Next Generation-Sequenzierung
Wissenschaftlich-technische Entwicklungen im Bereich der Multiplex- und High-Throughput-Diagnostik Karl J. Lackner Hochdurchsatzverfahren in der molekularen bzw. genetischen Diagnostik Next Generation-Sequenzierung
Projektskizze: Studie/ Auswertung/ Publikation
 Projektskizze: Studie/ Auswertung/ Publikation Name: PD Dr. Dr. Robert Bals, CAPNetz C11 Datum: 30. 8. 2007 Institution(en)/Autor(en): Klinikum der Universität Marburg Klinik für Innere Medizin mit Schwerpunkt
Projektskizze: Studie/ Auswertung/ Publikation Name: PD Dr. Dr. Robert Bals, CAPNetz C11 Datum: 30. 8. 2007 Institution(en)/Autor(en): Klinikum der Universität Marburg Klinik für Innere Medizin mit Schwerpunkt
Intraabdominelle Pilzinfektionen in der Intensivmedizin
 Intraabdominelle Pilzinfektionen in der Intensivmedizin Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Antibiotic Stewardship-Team
Intraabdominelle Pilzinfektionen in der Intensivmedizin Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Antibiotic Stewardship-Team
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger. Prof. Dr. C. Wendt
 ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
Ausbruchsmanagement des Gesundheitsamtes Leipzig am Beispiel KPC-Erreger
 Ausbruchsmanagement des Gesundheitsamtes Leipzig am Beispiel KPC-Erreger Hygienekongress 2013 Datum: 28.09.2013 Vortrag von: Dr. med. Ingrid Möller, Leiterin der Abteilung Hygiene, Vortrag von: Stadt Leipzig,
Ausbruchsmanagement des Gesundheitsamtes Leipzig am Beispiel KPC-Erreger Hygienekongress 2013 Datum: 28.09.2013 Vortrag von: Dr. med. Ingrid Möller, Leiterin der Abteilung Hygiene, Vortrag von: Stadt Leipzig,
Fortschritte in der Diagnostik häufiger Infektionskrankheiten. Ursula Flückiger Zentrum Innere Medizin Hirslanden Klinik Aarau
 Fortschritte in der Diagnostik häufiger Infektionskrankheiten Ursula Flückiger Zentrum Innere Medizin Hirslanden Klinik Aarau Themen Maldi TOF: Identifikation von Bakterien Durchfall, Pneumonie Mulitplex
Fortschritte in der Diagnostik häufiger Infektionskrankheiten Ursula Flückiger Zentrum Innere Medizin Hirslanden Klinik Aarau Themen Maldi TOF: Identifikation von Bakterien Durchfall, Pneumonie Mulitplex
Prävalenz bei ambulanten Patienten mit ambulant erworbener Pneumonie nach Erreger
 Produktnummer: IF1250M Rev. I Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Produktnummer: IF1250M Rev. I Leistungsmerkmale Nicht für den Vertrieb in den USA ERWARTETE WERTE Patienten mit ambulant erworbener Pneumonie Zwei externe Prüfer untersuchten den Focus Chlamydia MIF IgM
Begriffsverwirrung ESBL KPC VRE MDR NDM XDR PDR
 M R G N Begriffsverwirrung VRE ESBL KPC XDR MDR PDR NDM Multiresistenz Bisher definiert nach genotypische Resistenzmechanismen, z.b. Extended-spectrum β-lactamasen (ESBL) Klebsiella pneum. Carbapenemasen
M R G N Begriffsverwirrung VRE ESBL KPC XDR MDR PDR NDM Multiresistenz Bisher definiert nach genotypische Resistenzmechanismen, z.b. Extended-spectrum β-lactamasen (ESBL) Klebsiella pneum. Carbapenemasen
Bakterielle Zoonosenerreger
 Bakterielle Zoonosenerreger Blinde Passagiere erobern eine neue Welt Prof. Dr. Dr. h.c. Helge Karch Westfälische Wilhelms-Universität Münster Berlin, 8.10.2009 Bakterielle Zoonosen auf dem Vormarsch Enger
Bakterielle Zoonosenerreger Blinde Passagiere erobern eine neue Welt Prof. Dr. Dr. h.c. Helge Karch Westfälische Wilhelms-Universität Münster Berlin, 8.10.2009 Bakterielle Zoonosen auf dem Vormarsch Enger
BfR stuft den massiven Einsatz von Antibiotika in der Tierproduktion als bedenklich ein
 Antibiotikaresistente Keime auf Hähnchenfleisch-Proben sind nichts Neues BfR stuft den massiven Einsatz von Antibiotika in der Tierproduktion als bedenklich ein Berlin (10. Januar 2012) - Eine Stichprobe
Antibiotikaresistente Keime auf Hähnchenfleisch-Proben sind nichts Neues BfR stuft den massiven Einsatz von Antibiotika in der Tierproduktion als bedenklich ein Berlin (10. Januar 2012) - Eine Stichprobe
cobas T MRSA/SA Test Zuverlässige Befunde bevor die Infektion sich ausbreitet
 cobas T MRSA/SA Test Zuverlässige Befunde bevor die Infektion sich ausbreitet Schnelle und zuverlässige Diagnostik für effiziente Hygienemaßnahmen bevor die Infektion sich ausbreitet Infektionen mit Staphylococcus
cobas T MRSA/SA Test Zuverlässige Befunde bevor die Infektion sich ausbreitet Schnelle und zuverlässige Diagnostik für effiziente Hygienemaßnahmen bevor die Infektion sich ausbreitet Infektionen mit Staphylococcus
3.1 Ergebnisse des endoskopischen Screenings. Im Zeitraum von Mai 2000 bis August 2001 wurde bei insgesamt 148 Kopf-Hals-
 32 3. Ergebnisse 3.1 Ergebnisse des endoskopischen Screenings Im Zeitraum von Mai 2000 bis August 2001 wurde bei insgesamt 148 Kopf-Hals- Tumorpatienten eine einmalige Videoösophagoskopie mit routinemäßigen
32 3. Ergebnisse 3.1 Ergebnisse des endoskopischen Screenings Im Zeitraum von Mai 2000 bis August 2001 wurde bei insgesamt 148 Kopf-Hals- Tumorpatienten eine einmalige Videoösophagoskopie mit routinemäßigen
Institut für Krankenhaushygiene & Mikrobiologie, Graz Dr. Anita Lassacher
 Steiermärkische Krankenanstaltengesellschaft m.b.h. Hygiene Bakteriologie Serologie Molekularbiologie Tbc-Diagnostik Mykologie Parasitologie Institut für Krankenhaushygiene & Mikrobiologie, Graz Dr. Anita
Steiermärkische Krankenanstaltengesellschaft m.b.h. Hygiene Bakteriologie Serologie Molekularbiologie Tbc-Diagnostik Mykologie Parasitologie Institut für Krankenhaushygiene & Mikrobiologie, Graz Dr. Anita
Krankenhaushygiene und Infektionsschutz: Gefahren erkennen: Neue Erreger auf dem Vormarsch
 Krankenhaushygiene und Infektionsschutz: Gefahren erkennen: Neue Erreger auf dem Vormarsch Petra Gastmeier Institut für Hygiene und Umweltmedizin, Charité Universitätsmedizin Berlin Die wichtigsten Erreger
Krankenhaushygiene und Infektionsschutz: Gefahren erkennen: Neue Erreger auf dem Vormarsch Petra Gastmeier Institut für Hygiene und Umweltmedizin, Charité Universitätsmedizin Berlin Die wichtigsten Erreger
Problemkeime in der niedergelassenen Praxis
 Problemkeime in der niedergelassenen Praxis Prof. Dr. med. Ines Kappstein Krankenhaushygiene Kliniken Südostbayern AG Klinikum Traunstein Cuno-Niggl-Str. 3 83278 Traunstein E-Mail: ines.kappstein@kliniken-sob.de
Problemkeime in der niedergelassenen Praxis Prof. Dr. med. Ines Kappstein Krankenhaushygiene Kliniken Südostbayern AG Klinikum Traunstein Cuno-Niggl-Str. 3 83278 Traunstein E-Mail: ines.kappstein@kliniken-sob.de
Gezielt ist besser! Optimierung von Diagnostik verbessert die Therapie von Lungeninfektionen
 Optimierung von Diagnostik verbessert die Therapie von Lungeninfektionen Herr Dr. med. Marcus Berkefeld Frau Dr. med. Ilka Engelmann Klassische Methoden des Virusnachweis 1. direkter Immun-Fluoreszenz-Test
Optimierung von Diagnostik verbessert die Therapie von Lungeninfektionen Herr Dr. med. Marcus Berkefeld Frau Dr. med. Ilka Engelmann Klassische Methoden des Virusnachweis 1. direkter Immun-Fluoreszenz-Test
Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV
 Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV Von Dr. med. Markus Rupp, MSD SHARP & DOHME GMBH, Haar München (20. September 2008) Der World-Aids-Report
Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV Von Dr. med. Markus Rupp, MSD SHARP & DOHME GMBH, Haar München (20. September 2008) Der World-Aids-Report
