3.5 Ultraphosphate MP 4 O 11 (M 2+ = Mn, Fe, Co, Ni, Cu, Zn, Cd) 87
|
|
|
- Reiner Bäcker
- vor 5 Jahren
- Abrufe
Transkript
1 3.5 Ultraphosphate MP 4 O 11 (M 2+ = Mn, Fe, Co, Ni, Cu, Zn, Cd) 87 Abbildung 3.25 Verschiedene Ultraphosphatnetzwerke in Phosphaten MP 4 O 11. a) 10/10-Netze (M = Mn, Fe, Co, Ni, Cu, Zn, Cd), b) 8/12-Netze (M = Ca, Mn), c) 6/14-Netze (M = Ni), d) 4/16-Netze (M = Ni) Tabelle 3.3 Ultraphosphate MP 4 O 11. Übersicht der verschiedenen Kombinationen von Ringgrößen in den zweidimensionalen Netzwerken. Ringgrößen Ultraphosphat 10 / / 8 14 / 6 16 / 4 MgP 4 O 11 X 1) X 2) MnP 4 O 11 X 3) X 4) X 5) FeP 4 O 11 X 6) CoP 4 O 11 X 7) X 8) NiP 4 O 11 X 9) X 10) CuP 4 O 11 X 11) ZnP 4 O 11 X 6) X 12) CdP 4 O 11 X 6) 1 (Yakubovich et al., 1993), 2 (Stachel et al., 1992), 3 (Murashova & Chudinova, 1994), 4 (Minacheva et al., 1975; Olbertz et al., 1995), 5 (Olbertz et al., 1994), 6 (Weil, 1998), 7 (Anette Schmidt, 1998), 8 (Olbertz et al., 1993), 9 (Blum, 1997), 10 (Olbertz et al., 1995), 11 (Weil, Glaum & Özalp, 1996; Olbertz et al., 1996), 12 (Baez- Doelle et al., 1993).
2 88 Für die M 2+ ergibt sich, ähnlich wie bei den bereits erwähnten (Tris)metaphosphaten M(PO 3 ) 3, eine vergleichsweise einfache Bindungssituation, welche als Grundlage zum Verständnis des spektroskopischen und magnetischen Verhaltens von weiteren wasserfreien Metall(II)- phosphaten mit variierendem Verknüpfungsgrad der Metall-Sauerstoff-Polyeder dienen kann. Auf das unterschiedliche Ligandenverhalten von (Metall-Metall) verbrückenden und "terminalen" (nur an ein Metall gebundenen) Sauerstoffatomen wird in Kapitel 4 näher eingegangen. Eine Besonderheit aller Ultraphosphate ist die Ausbildung von tertiären Phosphatgruppen mit einem sehr kurzen Abstand d(p O) 1,44 Å und drei längeren Abständen d(p O) 1,56 Å. In den sekundären Phosphatgruppen finden sich dagegen zwei kurze Abstände, d(p O) 1,465 Å und zwei sehr lange mit d(p O) 1,605 Å. Für tertiäre Phosphatgruppen wird eine Aufweitung der Winkel zwischen Sauerstoff der an M 2+ gebunden ist und den drei Sauerstoffatomen mit Phosphor als zweitem Bindungspartner gefunden. Die Aufweitung bezogen auf den idealen Tetraederwinkel beträgt ca. 6. Für die sekundären Phosphatgruppen wird eine starke Aufweitung (auf ca. 120 ) zwischen den beiden an M 2+ gebundenen Sauerstoffatomen beobachtet, während der Winkel zwischen den beiden längeren P O- Bindungen verkleinert wird (auf ca. 100 ). Hiermit ist die stereochemische Situation um Phosphor in den sekundären Phosphateinheiten mit der in SO 2 F 2 vergleichbar. Besondere Erwähnung verdienen die Verfeinerungen der Kristallstrukturen der MP 4 O 11 (M = Mn, Fe, Cu, Zn, Cd) mit den 10/10-Ringsystemen. Heizguinier-Aufnahmen belegen für diese Ultraphosphate bei Temperaturen um 100 C eine reversible Phasenumwandlung zwischen einer monoklinen Hochtemperaturform und einer triklinen, pseudo-monoklinen Elementarzelle unterhalb von T u. Hieraus ergibt sich mit sehr hoher Wahrscheinlichkeit eine Verzwilligung der Kristalle der Raumtemperaturform, wobei die zweizählige Achse (oder die Spiegelebene) aus der monoklinen Hochtemperaturform als Zwillingselement wirken sollte (Zwillingsmatrix: ). Im Verlauf der Strukturverfeinerungen bestätigte sich diese Annahme (Weil, Glaum & Özalp, 1996; Weil, 1998). Bei den im Rahmen dieser Arbeit synthetisierten Ultraphosphaten mit 10/10-Ringen spiegelt sich der Aufbau aus Phosphatschichten [// (-2 0 1)], die durch M 2+ zwischen den Schichten zusammengehalten werden im Habitus der erhaltenen Kristalle [Platten mit Plattenebene (-2 0 1)], sowie in deren leichter Spaltbarkeit wieder.
3 3.5 Ultraphosphate MP 4 O 11 (M 2+ = Mn, Fe, Co, Ni, Cu, Zn, Cd) 89 Eine interessante topologische Analogie ergibt sich zwischen den 10/10- Ultraphosphatnetzwerken und den Polyphosphidnetzen in CuP 2 (Möller & Jeitschko, 1982), MgP 4 (von Schnering & Menge, 1976) sowie dem dazu isotypen CdP 4 (Krebs, Müller & Zürn, 1956). In anderen Polyphosphiden der Zusammensetzung MP 4 wurden ebenfalls zweidimensional-unendlich kondensierte P 10 -Ringe mit allerdings unterschiedlichem Verknüpfungsmuster beobachtet (Jeitschko et al., 1982). In der Struktur von ZnP 4 (Dommann, Marsh & Hulliger, 1989) finden sich zweidimensionale Phosphid-Netzwerke aus kondensierten P 4 -Ringen und P 16 -Ringen. Auch hier ist die topologische Analogie zwischen Polyphosphid und Ultrahosphat, in diesem Falle mit 16/4-Netzwerk offensichtlich. Auf entsprechende strukturelle Zusammenhänge zwischen binären intermetallischen Phasen und den jeweiligen ternären Oxo- Verbindungen ist bereits früher hingeweisen worden (Hyde & O'Keeffe, 1985). 3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) Bislang sind drei wasserfreie Phosphate der allgemeinen Zusammensetzung M 2 O(PO 4 ) bekannt: α- und β-fe 2 O(PO 4 ) (Modaressi et al., 1981; Ijjaali et al., 1991; Ech-Chahed et al., 1988; ElKaïm et al., 1996), NiCrO(PO 4 ) (Ech-Chahed et al., 1988) und V 2 O(PO 4 ) (Glaum & Gruehn, 1989). Von diesen sind β-fe 2 O(PO 4 ), NiCrO(PO 4 ) und V 2 O(PO 4 ) isostrukturell, während α-fe 2 O(PO 4 ) trotz einiger Gemeinsamkeiten deutlich unterschiedlich aufgebaut ist. Außer den wasserfreien, im Labor synthetisierten Phosphaten existieren eine Reihe von basischen eisenhaltigen Mineralien (Lazulit, Scorzalit, Barbosalit, Lipscombit), die sich unter der allgemeinen Formel (, M 2+, M 3+ ) 2 (O, OH) (PO 4 ) zusammenfassen lassen. Die Formel deutet die Variationsmöglichkeiten in der Zusammensetzung nur an. So ist vom Eisen eine Verbindung 2 Fe 3+ 4(OH) 3 (PO 4 ) 3 sehr gut untersucht (Malaman et al., 1991). Neben der Variation der Verhältnisse Fe 2+ /Fe 3+ und O 2 /OH ist auch die Substitution von Eisen durch andere Metalle möglich. Dabei überrascht besonders, daß der Strukturtyp auch mit Ti 4+ als Kation neben P 5+ unter Ausbildung einer vergleichsweise großen Anzahl von Lücken realisiert werden kann (Reinauer & Glaum, 1998; Reinauer, 1998).
4 Vanadium(II, III)-oxidphosphat V 2 O(PO 4 ) Die Kristallstruktur von β-v 2 O(PO 4 ) ist bereits früher beschrieben worden (Glaum & Gruehn, 1989; Glaum, 1990). Als Einstieg in die Betrachtung der gesamten Strukturfamilie sollen die wesentlichen strukturellen Merkmale von β-v 2 O(PO 4 ) (I4 1 /amd; Z = 4; a = 5,362(5) Å; c = 12,378(9) Å; V = 355,9 Å 3 ) als Beispiel für den Aristotyp hier trotzdem kurz vorgestellt werden. Charakteristisch für den Strukturtyp sind unendliche Ketten aus flächenverknüpften [VO 6 ]- Oktaedern (Abbildung 3.27) entlang [1 0 0] und [0 1 0] der tetragonalen Zelle. Der sehr kurze Abstand d(v V) = 2,68 Å innerhalb der Ketten deutet auf starke Metall-Metall- Wechselwirkungen hin. Senkrecht zueinander verlaufende Ketten in unterschiedlicher Höhe z der Elementarzelle sind über gemeinsame Sauerstoffatome verbunden. Diese "oxidischen" Sauerstoffatome sind durch vier Vanadiumatome koordiniert (d(v O) = 2.05 Å). Die Winkel (V, O, V) betragen 81,8 (beide V-Atome in einer Kette) und 124,8 (V-Atome in benachbarten Ketten). Weiterhin sind die Ketten noch durch [PO 4 ]-Tetraeder miteinander verbunden (Abbildung 3.26). Die Sauerstoffatome der [PO 4 ]-Gruppen sind neben Phosphor noch durch zwei Vanadiumatome, nahezu trigonal-planar koordiniert. Der Abstand der Sauerstoffatome zur Ebene aus P und 2 V beträgt 0,09Å. Abbildung 3.26 V 2 O(PO 4 ). a) Projektion der Kristallstruktur auf die ab-ebene. [VO 6 ]: dunkelgrau, [PO 4 ]: hellgrau. b) Projektion auf die bc-ebene.
5 3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) 91 1 Abbildung 3.27 V 2 O(PO 4 ). ORTEP-Darstellung eines Ausschnitts der Ketten [ VO ] nach den Angaben bei (Glaum & Gruehn, 1989). 6/ 2 Während bei V 2 O(PO 4 ) und β-fe 2 O(PO 4 ) eine Stabilisierung der Kristallstruktur durch ausgedehnte Metall-Metall-Wechselwirkungen vorliegen könnte, sind entsprechende Effekte bei NiCrO(PO 4 ) nicht möglich. Die Existenz der Verbindung, trotz der elektrostatisch ungünstigen Flächenverknüpfung der [MO 6 ]-Oktaeder, ist deshalb überraschend. Zum kristallchemischen Existenzbereich des Strukturtyps liegen, abgesehen von einigen orientierenden Experimenten (Glaum, 1990), keine systematischen Angaben vor. Es konnte allerdings gezeigt werden, daß Titan(IV)-oxidphosphat, Ti 5 O 4 (PO 4 ) 4 (Reinauer, 1998; Reinauer & Glaum, 1998) sowie die gemischtvalenten Titan(III, IV)-oxidphosphate R1 und R2 (Reinauer, Glaum & Gruehn, 1994; Reinauer, 1998) ebenfalls der Strukturfamilie zuzurechnen sind Titan(IV)-oxidphosphat Ti 5 O 4 (PO 4 ) 4 Die Metrik der Elementarzelle von Ti 5 O 4 (PO 4 ) 4 (P , Z = 4, a = 12,8417(12) Å, b = 14,4195(13) Å, c = 7,4622(9) Å, V = 1381,8 Å 3 ) steht in einfachem Zusammenhang zur Elementarzelle von β-v 2 O(PO 4 ). a a b = b c c Ti O PO ( ) β V O( PO ) Die Symmetrieverwandschaft zwischen der Struktur von Ti 5 O 4 (PO 4 ) 4 und der des Aristotyps wird durch den Gruppe-Untergruppe-Stammbaum in Abbildung 3.28 veranschaulicht. Im Unterschied zur Struktur von β-v 2 O(PO 4 ) sind in Ti 5 O 4 (PO 4 ) 4 nicht alle Oktaederlücken
6 92 besetzt. Gemäß der Formulierung 3 Ti 5 O 4 (PO 4 ) 4 wird zum Ausgleich der Ladungen des Oxidphosphat-Gerüsts eine Besetzung von 20 der 32 Oktaederlücken je Elementarzelle benötigt. In der geordneten Struktur verteilen sich die 20 Ti 4+ auf 5 kristallographische Lagen, dadurch ergibt sich entlang der Richtung der "Ketten" ([0-1 2] bzw. [0 1 2] bezogen auf die orthorhombische Zelle von Ti 5 O 4 (PO 4 ) 4 ) eine Abfolge... L B B L B B L B L... von leeren "L" und besetzten "B" Oktaederlücken. In Abbildung 3.29 ist ein Ausschnitt einer "Kette" aus flächenverknüpften [TiO 6 ]-Oktaedern dargestellt. Innerhalb der "Ketten" ergeben sich zwei kristallographisch unabhängige [Ti 2 O 9 ]-Einheiten aus vier stark verzerrten [TiO 6 ]-Oktaedern mit Abständen d(ti O) zwischen 1,72 Å und 2,39 Å. Ähnlich wie in TiOSO 4 (Gatehouse, Platts & Williams, 1993) könnte man hier von Titanyl- Gruppen (TiO) 2+ sprechen. Das fünfte [TiO 6 ]-Oktaeder ist wesentlich weniger stark verzerrt mit Abständen 1,91 Å d(ti O) 1,98 Å. Eine detailliertere Beschreibung der Kristallstruktur mit den interatomaren Abständen findet sich in der Literatur (Reinauer & Glaum, 1998). Abbildung 3.30 vergleicht die Idealstruktur von und Ti 5 O 4 (PO 4 ) 4 mit der Struktur, die sich bei Besetzung aller Oktaerlücken ergibt. Abbildung 3.28 Gruppe-Untergruppe Beziehung zwischen den Strukturen von β-v 2 O(PO 4 ), Ti 5 O 4 (PO 4 ) und den gemischtvalente Titan(III, IV)-oxidphosphaten "R1" und "R2".
7
3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) 93
 3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) 93 Abbildung 3.29 Ti 5 O 4 (PO 4 ). ORTEP-Darstellung eines Ausschnitts der "Ketten" aus flächenverknüpften [TiO 6 ]-Oktaedern einschließlich der in der Idealstruktur
3.6 Phosphate der Strukturfamilie M 2 O(PO 4 ) 93 Abbildung 3.29 Ti 5 O 4 (PO 4 ). ORTEP-Darstellung eines Ausschnitts der "Ketten" aus flächenverknüpften [TiO 6 ]-Oktaedern einschließlich der in der Idealstruktur
Auf n-kugeln einer dichtesten Packung kommen n-oktaederlücken und 2n-Tetraederlücken
 2.1 Kugelpackungen In einer Verbindung A m X n haben die X-Atome die Anordnung einer dichtesten Kugelpackung und A-Atome besetzen die Oktaederlücken (OL). Geben Sie die resultierenden Formeln A m X n an,
2.1 Kugelpackungen In einer Verbindung A m X n haben die X-Atome die Anordnung einer dichtesten Kugelpackung und A-Atome besetzen die Oktaederlücken (OL). Geben Sie die resultierenden Formeln A m X n an,
Freiwillige Übungsaufgaben zum Stoff vorangegangener Vorlesungen zur Selbstkontrolle für den 2. April 2008 (wird nicht bewertet)
 AC II - 2. April 2008 Übungen Anke Zürn Zusammenfassung & Wiederholung Dichteste Kugelpackungen (KP) Freiwillige Übungsaufgaben zum Stoff vorangegangener Vorlesungen zur Selbstkontrolle für den 2. April
AC II - 2. April 2008 Übungen Anke Zürn Zusammenfassung & Wiederholung Dichteste Kugelpackungen (KP) Freiwillige Übungsaufgaben zum Stoff vorangegangener Vorlesungen zur Selbstkontrolle für den 2. April
Neue Untersuchungen an wasserfreien Phosphaten der Übergangsmetalle
 Robert Glaum Neue Untersuchungen an wasserfreien Phosphaten der Übergangsmetalle mit 97 Abbildungen Justus-Liebig-Universität, Gießen (1999) Dr. rer. nat. Robert Glaum Institut für Anorganische und Analytische
Robert Glaum Neue Untersuchungen an wasserfreien Phosphaten der Übergangsmetalle mit 97 Abbildungen Justus-Liebig-Universität, Gießen (1999) Dr. rer. nat. Robert Glaum Institut für Anorganische und Analytische
Methoden der Chemie III Teil 1 Modul M.Che.1101 WS 2010/11 3 Moderne Methoden der Anorganischen Chemie Mi 10:15-12:00, Hörsaal II George Sheldrick
 Methoden der Chemie III Teil 1 Modul M.Che.1101 WS 2010/11 3 Moderne Methoden der Anorganischen Chemie Mi 10:15-12:00, Hörsaal II George Sheldrick gsheldr@shelx.uni-ac.gwdg.de Das Gitter Kristalle bestehen
Methoden der Chemie III Teil 1 Modul M.Che.1101 WS 2010/11 3 Moderne Methoden der Anorganischen Chemie Mi 10:15-12:00, Hörsaal II George Sheldrick gsheldr@shelx.uni-ac.gwdg.de Das Gitter Kristalle bestehen
Magnetisches Verhalten
 Kapitel 5 5.1 Vorbemerkungen Nach den grundlegenden Arbeiten (van Vleck, 1965), die sich mit dem magnetischen Verhalten "freier" Ionen beschäftigten sind in der Folgezeit systematisch Verbindungen untersucht
Kapitel 5 5.1 Vorbemerkungen Nach den grundlegenden Arbeiten (van Vleck, 1965), die sich mit dem magnetischen Verhalten "freier" Ionen beschäftigten sind in der Folgezeit systematisch Verbindungen untersucht
AC II Übung 4 Abgabe Mittwoch, 18. März 2009
 4.1 Energieberechnungen nach Sanderson (Beispiel Prüfungsaufgabe) Berechnen Sie die polar-kovalente Bindungsenergie nach R.T. Sanderson für ein KBr-Molekül (monomer, Gas). Geben Sie alle Rechenschritte
4.1 Energieberechnungen nach Sanderson (Beispiel Prüfungsaufgabe) Berechnen Sie die polar-kovalente Bindungsenergie nach R.T. Sanderson für ein KBr-Molekül (monomer, Gas). Geben Sie alle Rechenschritte
Anorganische Strukturchemie
 Ulrich Müller Anorganische Strukturchemie 5., überarbeitete und erweiterte Auflage Teubner Inhaltsverzeichnis 1 Einleitung 9 2 Beschreibung chemischer Strukturen 11 2.1 Koordinationszahl und Koordinationspolyeder
Ulrich Müller Anorganische Strukturchemie 5., überarbeitete und erweiterte Auflage Teubner Inhaltsverzeichnis 1 Einleitung 9 2 Beschreibung chemischer Strukturen 11 2.1 Koordinationszahl und Koordinationspolyeder
Thema heute: Chemische Bindungen - Ionenbindung
 Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, Doppelbindungsregel, VSEPR-Theorie Thema heute: Chemische Bindungen - Ionenbindung Vorlesung Allgemeine Chemie, Prof. Dr. Martin Köckerling
Wiederholung der letzten Vorlesungsstunde: Chemische Bindungen, Doppelbindungsregel, VSEPR-Theorie Thema heute: Chemische Bindungen - Ionenbindung Vorlesung Allgemeine Chemie, Prof. Dr. Martin Köckerling
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Übungsaufgaben zur Kristallographie Serie 10 LÖSUNG
 1) Packungsdichte Berechnen Sie die Packungsdichte der kubisch dichtesten Kugelpackung, der hexagonal dichtesten Kugelpackung, einer kubisch primitiven Kugelpackung und einer kubisch innenzentrierten Kugelpackung.
1) Packungsdichte Berechnen Sie die Packungsdichte der kubisch dichtesten Kugelpackung, der hexagonal dichtesten Kugelpackung, einer kubisch primitiven Kugelpackung und einer kubisch innenzentrierten Kugelpackung.
AC I (AC) HS 2011 Übungen + Lösungen Serie 10
 rof. A. Togni, D-CHAB, HCI H 239 AC I (AC) HS 2011 Übungen ösungen Serie 10 Koordinationschemie A 1. rinzipiell liessen sich sechs iganden () in einem Metallkomplex M 6 nicht nur oktaedrisch sondern auch
rof. A. Togni, D-CHAB, HCI H 239 AC I (AC) HS 2011 Übungen ösungen Serie 10 Koordinationschemie A 1. rinzipiell liessen sich sechs iganden () in einem Metallkomplex M 6 nicht nur oktaedrisch sondern auch
Struktur von Festkörpern
 Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Struktur von Festkörpern Wir wollen uns zunächst mit der Struktur von Festkörpern, daß heißt mit der Geometrie in der sie vorliegen beschäftigen Kovalent gebundene Festkörper haben wir bereits in Form
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Gefüge und Eigenschaften metallischer Werkstoffe WS 17/18
 Gefüge und Eigenschaften metallischer Werkstoffe WS 7/8 Übung 5 Musterlösung 0..07 Aufgabe Welche Bravais-Gittertypen gibt es? Welche Modifikationen besitzen Sie? Nennen Sie Materialbeispiele zu jedem
Gefüge und Eigenschaften metallischer Werkstoffe WS 7/8 Übung 5 Musterlösung 0..07 Aufgabe Welche Bravais-Gittertypen gibt es? Welche Modifikationen besitzen Sie? Nennen Sie Materialbeispiele zu jedem
1 Kristallgitter und Kristallbaufehler 10 Punkte
 1 Kristallgitter und Kristallbaufehler 10 Punkte 1.1 Es gibt 7 Kristallsysteme, aus denen sich 14 Bravais-Typen ableiten lassen. Charakterisieren Sie die kubische, tetragonale, hexagonale und orthorhombische
1 Kristallgitter und Kristallbaufehler 10 Punkte 1.1 Es gibt 7 Kristallsysteme, aus denen sich 14 Bravais-Typen ableiten lassen. Charakterisieren Sie die kubische, tetragonale, hexagonale und orthorhombische
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Hybridisierung und Molekülstruktur, sp 3 -Hybridorbitale (Tetraeder), sp 2 - Hybridorbitale (trigonal planare Anordnung), sp-hybridorbitale (lineare Anordnung),
Wiederholung der letzten Vorlesungsstunde: Hybridisierung und Molekülstruktur, sp 3 -Hybridorbitale (Tetraeder), sp 2 - Hybridorbitale (trigonal planare Anordnung), sp-hybridorbitale (lineare Anordnung),
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # Elektronengas # Bändermodell Bindungsmodelle Metallbindung > Bindungsmodelle Elektronengas
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # Elektronengas # Bändermodell Bindungsmodelle Metallbindung > Bindungsmodelle Elektronengas
C. Röhr, Phosphor, WS 09/10. Phosphor Phosphane Phosphide -
 Phosphor Phosphane Phosphide - Inhalt Einleitung Elementmodifikationen Phosphane/Phosphide mit PH/P : P > 1 (Kettenstücke) Phosphane/Phosphide mit PH/P : P = 1 (Ketten und Ringe) Phosphane/Phosphide mit
Phosphor Phosphane Phosphide - Inhalt Einleitung Elementmodifikationen Phosphane/Phosphide mit PH/P : P > 1 (Kettenstücke) Phosphane/Phosphide mit PH/P : P = 1 (Ketten und Ringe) Phosphane/Phosphide mit
zweiwertige Kationen Mg V Cr Mn Fe Co Ni Cu Zn Cd
 64 Kristallchemie Tabelle 3.1 Übersicht der bislang bekannten Vertreter des Fe 7 (PO 4 ) 6 Strukturtyps. "++" Struktur aus Einkristalldaten, "+" Charakterisierung aus Pulveraufnahmen, "O" Erfolglose Syntheseversuche
64 Kristallchemie Tabelle 3.1 Übersicht der bislang bekannten Vertreter des Fe 7 (PO 4 ) 6 Strukturtyps. "++" Struktur aus Einkristalldaten, "+" Charakterisierung aus Pulveraufnahmen, "O" Erfolglose Syntheseversuche
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Kristallchemie Atome Ionen Moleküle Chemische Bindungen Metalle, Metalloide, Nichtmetalle Metalle: E-neg < 1.9 - e - Abgabe Kationen Nichtmetalle: E-neg > 2.1 - e - Aufnahme Anionen Metalloide: B, Si,
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2012/13 Christoph Wölper Universität Duisburg-Essen > Intermetallische Phasen Hume-Rothery-Phasen # späte Übergangsmetalle (Gruppe T2) und Gruppe
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2012/13 Christoph Wölper Universität Duisburg-Essen > Intermetallische Phasen Hume-Rothery-Phasen # späte Übergangsmetalle (Gruppe T2) und Gruppe
Strukturchemie. Kristallstrukturen. Elementstrukturen. Kugelpackungen. Kubisch dichte Kugelpackung. Lehramt 1a Sommersemester
 Kugelpackungen Kubisch dichte Kugelpackung Lehramt 1a Sommersemester 2010 1 Kugelpackungen: kubisch dichte Packung (kdp, ccp) C B A A C B A C B A C Lehramt 1a Sommersemester 2010 2 Kugelpackungen Atome
Kugelpackungen Kubisch dichte Kugelpackung Lehramt 1a Sommersemester 2010 1 Kugelpackungen: kubisch dichte Packung (kdp, ccp) C B A A C B A C B A C Lehramt 1a Sommersemester 2010 2 Kugelpackungen Atome
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Grundlagen der Chemie Ionenradien
 Ionenradien Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Ionenradien In einem Ionenkristall halten benachbarte
Ionenradien Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Ionenradien In einem Ionenkristall halten benachbarte
Kurs Röntgenstrukturanalyse, Teil 1: Der kristalline Zustand
 Kurs Röntgenstrukturanalyse, Teil 1: Der kristalline Zustand Beispiel 1: Difluoramin M. F. Klapdor, H. Willner, W. Poll, D. Mootz, Angew. Chem. 1996, 108, 336. Gitterpunkt, Gitter, Elementarzelle, Gitterkonstanten,
Kurs Röntgenstrukturanalyse, Teil 1: Der kristalline Zustand Beispiel 1: Difluoramin M. F. Klapdor, H. Willner, W. Poll, D. Mootz, Angew. Chem. 1996, 108, 336. Gitterpunkt, Gitter, Elementarzelle, Gitterkonstanten,
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # kubisch Fd3m # Aufbau durch nur 3 Atome -> 0 0 0 (8a) -> 5/8 5/8 5/8 (16d) -> 3/8 3/8 3/8
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 2013/14 Christoph Wölper Universität Duisburg-Essen # kubisch Fd3m # Aufbau durch nur 3 Atome -> 0 0 0 (8a) -> 5/8 5/8 5/8 (16d) -> 3/8 3/8 3/8
Wiederholung der letzten Vorlesungsstunde
 Wiederholung der letzten Vorlesungsstunde Festkörper, ausgewählte Beispiele spezieller Eigenschaften von Feststoffen, Kohlenstoffmodifikationen, Nichtstöchiometrie, Unterscheidung kristalliner und amorpher
Wiederholung der letzten Vorlesungsstunde Festkörper, ausgewählte Beispiele spezieller Eigenschaften von Feststoffen, Kohlenstoffmodifikationen, Nichtstöchiometrie, Unterscheidung kristalliner und amorpher
Thema heute: Aufbau fester Stoffe - Kristallographie
 Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Wiederholung der letzten Vorlesungsstunde
 Wiederholung der letzten Vorlesungsstunde Gitterpunkte, Gittergeraden, Gitterebenen, Weiß'sche Koeffizienten, Miller Indizes Symmetrie in Festkörpern, Symmetrieelemente, Symmetrieoperationen, Punktgruppenymmetrie,
Wiederholung der letzten Vorlesungsstunde Gitterpunkte, Gittergeraden, Gitterebenen, Weiß'sche Koeffizienten, Miller Indizes Symmetrie in Festkörpern, Symmetrieelemente, Symmetrieoperationen, Punktgruppenymmetrie,
Frage 1. Schreiben Sie die chemischen Symbole für nachfolgende Elemente an:
 Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 1 Punkte Bitte eintragen: Matrikelnummer: Name: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Schreiben Sie die
Klausuraufgaben Grundvorlesung Testat vom 27.2.02, Seite 1 Punkte Bitte eintragen: Matrikelnummer: Name: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Schreiben Sie die
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2
 Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 4 Molekülstruktur Ausnahmen von der Oktettregel Hypervalente Verbindungen VSEPR Hybridisierung Molekülorbitale
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 4 Molekülstruktur Ausnahmen von der Oktettregel Hypervalente Verbindungen VSEPR Hybridisierung Molekülorbitale
Zur Kristallstruktur von 4PbO. PbS04
 Zeitschrift fur Kristallographie, Bd. 141, S. 145-150 (1975) Zur Kristallstruktur von 4PbO. PbS04 Von K. SAHL Institut fur Mineralogie der Ruhr-Universitat, Bochum (Eingegangen am 23. August 1972; in endgiiltiger
Zeitschrift fur Kristallographie, Bd. 141, S. 145-150 (1975) Zur Kristallstruktur von 4PbO. PbS04 Von K. SAHL Institut fur Mineralogie der Ruhr-Universitat, Bochum (Eingegangen am 23. August 1972; in endgiiltiger
7 Das Reaktionssystem Co 2 (CO) 8 /[Et 4 N][Co 2 (Se i C 3 H 7 ) 5 ]/Ph 4 PCl
![7 Das Reaktionssystem Co 2 (CO) 8 /[Et 4 N][Co 2 (Se i C 3 H 7 ) 5 ]/Ph 4 PCl 7 Das Reaktionssystem Co 2 (CO) 8 /[Et 4 N][Co 2 (Se i C 3 H 7 ) 5 ]/Ph 4 PCl](/thumbs/70/63749433.jpg) Co 2 (CO) 8 /[Et 4 N][Co 2 (Se i C 3 H 7 ) 5 ]/Kat 92 7 Das Reaktionssystem Co 2 (CO) 8 /[Et 4 N][Co 2 (Se i C 3 H 7 ) 5 ]/Ph 4 PCl Der Grund für die Untersuchung des Systems Co 2 (CO) 8 /[Et 4 N][Co 2
Co 2 (CO) 8 /[Et 4 N][Co 2 (Se i C 3 H 7 ) 5 ]/Kat 92 7 Das Reaktionssystem Co 2 (CO) 8 /[Et 4 N][Co 2 (Se i C 3 H 7 ) 5 ]/Ph 4 PCl Der Grund für die Untersuchung des Systems Co 2 (CO) 8 /[Et 4 N][Co 2
Ionenbindungen, Ionenradien, Gitterenergie, Born-Haber-Kreisprozess, Madelung-Konstante
 Wiederholung der letzten Vorlesungsstunde: Ionenbindungen, Ionenradien, Gitterenergie, Born-Haber-Kreisprozess, Madelung-Konstante Thema heute: 1) Kovalente Gitter, 2) Metalle 280 Kovalente und molekulare
Wiederholung der letzten Vorlesungsstunde: Ionenbindungen, Ionenradien, Gitterenergie, Born-Haber-Kreisprozess, Madelung-Konstante Thema heute: 1) Kovalente Gitter, 2) Metalle 280 Kovalente und molekulare
2. VD, BSc. Anorganische Chemie II Herbst 2005 R. Nesper, G. Patzke. Punktgruppenbestimmung (6 Punkte)
 2. VD, BSc. Anorganische Chemie II Herbst 2005 R. Nesper, G. Patzke Aufgabe 1 Punktgruppenbestimmung (6 Punkte) Bestimmen Sie die Punktgruppensymmetrie für die folgenden Moleküle. (a): C 3 (b): C 2v (c):
2. VD, BSc. Anorganische Chemie II Herbst 2005 R. Nesper, G. Patzke Aufgabe 1 Punktgruppenbestimmung (6 Punkte) Bestimmen Sie die Punktgruppensymmetrie für die folgenden Moleküle. (a): C 3 (b): C 2v (c):
6. Die Chemische Bindung
 6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
Röntgenographische Charakterisierung der hergestellten Feststoffe mittels Pulverdiffraktion, sowie Auswertung der erhaltenen Pulverdiffraktogramme
 Röntgenographische Charakterisierung der hergestellten Feststoffe mittels Pulverdiffraktion, sowie Auswertung der erhaltenen Pulverdiffraktogramme Vorbemerkung: Wegen der umfassenden Theorie von kristallographischen
Röntgenographische Charakterisierung der hergestellten Feststoffe mittels Pulverdiffraktion, sowie Auswertung der erhaltenen Pulverdiffraktogramme Vorbemerkung: Wegen der umfassenden Theorie von kristallographischen
2.1 Translationssymmetrie
 2.1 Translationssymmetrie Die periodische Anordnung eines Kristalls entspricht mathematisch einer Translationssymmetrie. Diese wird mit Hilfe von drei fundamentalen Translationsvektoren beschrieben: T
2.1 Translationssymmetrie Die periodische Anordnung eines Kristalls entspricht mathematisch einer Translationssymmetrie. Diese wird mit Hilfe von drei fundamentalen Translationsvektoren beschrieben: T
Kristallstrukturen und (Kugel-) Packungen
 Beschreibung von Kristallstrukturen durch: Elementarzellen: Vollständige Beschreibung der Kristallstruktur durch Größe, Form und Symmetrie der Elementarzelle (translationsinvarianter Teil der Kristallstruktur)
Beschreibung von Kristallstrukturen durch: Elementarzellen: Vollständige Beschreibung der Kristallstruktur durch Größe, Form und Symmetrie der Elementarzelle (translationsinvarianter Teil der Kristallstruktur)
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
ISP-Methodenkurs. Pulverdiffraktometrie. Prof. Dr. Michael Fröba, AC Raum 114, Tel: 040 /
 ISP-Methodenkurs Pulverdiffraktometrie Prof. Dr. Michael Fröba, AC Raum 4, Tel: 4 / 4838-337 www.chemie.uni-hamburg.de/ac/froeba/ Röntgenstrahlung (I) Wilhelm Conrad Röntgen (845-93) 879-888 Professor
ISP-Methodenkurs Pulverdiffraktometrie Prof. Dr. Michael Fröba, AC Raum 4, Tel: 4 / 4838-337 www.chemie.uni-hamburg.de/ac/froeba/ Röntgenstrahlung (I) Wilhelm Conrad Röntgen (845-93) 879-888 Professor
Neue Untersuchungen an wasserfreien Phosphaten der Übergangsmetalle
 Robert Glaum Neue Untersuchungen an wasserfreien Phosphaten der Übergangsmetalle mit 97 Abbildungen Justus-Liebig-Universität, Gießen (1999) Dr. rer. nat. Robert Glaum Institut für Anorganische und Analytische
Robert Glaum Neue Untersuchungen an wasserfreien Phosphaten der Übergangsmetalle mit 97 Abbildungen Justus-Liebig-Universität, Gießen (1999) Dr. rer. nat. Robert Glaum Institut für Anorganische und Analytische
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2
 Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
Kristallstruktur und Mikrostruktur Teil I Vorlesung 2 1 Kristallstruktur und Teil I Scripte Mikrostruktur http://www.uni-stuttgart.de/mawi/aktuelles_lehrangebot/lehrangebot.html 2 Wiederholung Koordinatensysteme
3 Erstarrung. 3.1 Einphasige Erstarrung von Legierungen. 3.2 Zweiphasige Erstarrung
 Studieneinheit IV Erstarrung. Einphasige Erstarrung von Legierungen.. Planare Erstarrung Makroseigerung.. Nicht-planare dendritische Erstarrung Mikroseigerung.. Gussstrukturen. Zweiphasige Erstarrung..
Studieneinheit IV Erstarrung. Einphasige Erstarrung von Legierungen.. Planare Erstarrung Makroseigerung.. Nicht-planare dendritische Erstarrung Mikroseigerung.. Gussstrukturen. Zweiphasige Erstarrung..
Grundlagen-Vertiefung PW3. Kristalle und Kristallstrukturen Version von 15. Oktober 2013
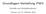 Grundlagen-Vertiefung PW3 Kristalle und Kristallstrukturen Version von 15. Oktober 2013 Kristalle besitzen einen geordneten und periodischen Gitteraufbau. Die überwiegende Mehrzahl der anorganischen Festkörper
Grundlagen-Vertiefung PW3 Kristalle und Kristallstrukturen Version von 15. Oktober 2013 Kristalle besitzen einen geordneten und periodischen Gitteraufbau. Die überwiegende Mehrzahl der anorganischen Festkörper
Einfache Kristallstrukturen
 Einfache Kristallstrukturen Konstruktion von Kristallen: Kugelpackungen - hexagonal und kubisch dichteste Packungen - kubisch einfache Packung - kubisch innenzentrierte Packung Kristallstrukturen der Metalle
Einfache Kristallstrukturen Konstruktion von Kristallen: Kugelpackungen - hexagonal und kubisch dichteste Packungen - kubisch einfache Packung - kubisch innenzentrierte Packung Kristallstrukturen der Metalle
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Röntgenstrukturanalyse von Einkristallen
 Strukturmethoden: Röntgenstrukturanalyse von Einkristallen Sommersemester 2017 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah Symmetrie,
Strukturmethoden: Röntgenstrukturanalyse von Einkristallen Sommersemester 2017 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah Symmetrie,
2.4 Metallische Bindung und Metallkristalle. Unterteilung in Metalle, Halbmetalle, Nicht metalle. Li Be B C N O F. Na Mg Al Si P S Cl
 2.4 Metallische Bindung und Metallkristalle Li Be B C N O F Na Mg Al Si P S Cl K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba Tl Pb Bi Po At Unterteilung in Metalle, Halbmetalle, Nicht metalle Metalle etwa
2.4 Metallische Bindung und Metallkristalle Li Be B C N O F Na Mg Al Si P S Cl K Ca Ga Ge As Se Br Rb Sr In Sn Sb Te I Cs Ba Tl Pb Bi Po At Unterteilung in Metalle, Halbmetalle, Nicht metalle Metalle etwa
Vorlesung Allgemeine Chemie: Chemische Bindung
 Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
Valenz-Bindungstheorie H 2 : s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie
 Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Chalkogenpolykation-Halogenidobismutate: Salzartige Verbindungen mit hoher struktureller Komplexität
 Chalkogenpolykation-Halogenidobismutate: Salzartige Verbindungen mit hoher struktureller Komplexität Dissertation zur Erlangung des Doktorgrades der Naturwissenschaften (Dr. rer. nat.) der Mathematisch-Naturwissenschaftlichen
Chalkogenpolykation-Halogenidobismutate: Salzartige Verbindungen mit hoher struktureller Komplexität Dissertation zur Erlangung des Doktorgrades der Naturwissenschaften (Dr. rer. nat.) der Mathematisch-Naturwissenschaftlichen
Übersicht. Wasserstoff-Verbindungen
 Allgemeine Chemie - Teil Anorganische Chemie II: 5. Hauptgruppe Übersicht A. Die Stellung der Elemente der 5. Hauptgruppe im Periodensystem. Stickstoff 2.1. Stickstoff-Wasserstoff Wasserstoff-Verbindungen.1.1.
Allgemeine Chemie - Teil Anorganische Chemie II: 5. Hauptgruppe Übersicht A. Die Stellung der Elemente der 5. Hauptgruppe im Periodensystem. Stickstoff 2.1. Stickstoff-Wasserstoff Wasserstoff-Verbindungen.1.1.
Z. Naturforsch. 60b, (2005); eingegangen am 06. September 2005
 K 5 [FeO 4 ] und K 17 [Fe 5 O 16 ]: Zwei neue Kalium-Oxoferrate(III) K 5 [FeO 4 ] and K 17 [Fe 5 O 16 ]: Two New Potassium Oxoferrates(III) Gero Frisch und Caroline Röhr Institut für Anorganische und Analytische
K 5 [FeO 4 ] und K 17 [Fe 5 O 16 ]: Zwei neue Kalium-Oxoferrate(III) K 5 [FeO 4 ] and K 17 [Fe 5 O 16 ]: Two New Potassium Oxoferrates(III) Gero Frisch und Caroline Röhr Institut für Anorganische und Analytische
Festk0203_ /11/2002. Neben Translationen gibt es noch weitere Deckoperationen die eine Struktur in sich überführen können:
 Festk234 37 11/11/22 2.9. Drehungen und Drehinversionen Bereits kennen gelernt: Translationssymmetrie. Neben Translationen gibt es noch weitere Deckoperationen die eine Struktur in sich überführen können:
Festk234 37 11/11/22 2.9. Drehungen und Drehinversionen Bereits kennen gelernt: Translationssymmetrie. Neben Translationen gibt es noch weitere Deckoperationen die eine Struktur in sich überführen können:
Präparation. Kapitel Vorbemerkungen
 Kapitel 2 2.1 Vorbemerkungen Die klassischen Methoden der präparativen Festkörperchemie stoßen bei der Synthese von wasserfreien Phosphaten häufig an ihre Grenzen. So ist die direkte Umsetzung von Metalloxiden
Kapitel 2 2.1 Vorbemerkungen Die klassischen Methoden der präparativen Festkörperchemie stoßen bei der Synthese von wasserfreien Phosphaten häufig an ihre Grenzen. So ist die direkte Umsetzung von Metalloxiden
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Seminar zum Praktikum Anorganische Chemie III III
 Seminar zum Praktikum Anorganische hemie III III Metallorganische hemie Dr. J. Wachter IR-Teil 4 www.chemie.uni-regensburg.de/anorganische_hemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_hemie/wachter/lehre.html
Seminar zum Praktikum Anorganische hemie III III Metallorganische hemie Dr. J. Wachter IR-Teil 4 www.chemie.uni-regensburg.de/anorganische_hemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_hemie/wachter/lehre.html
Allgemeine Chemie I Herbstsemester 2012
 Lösung 4 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Im Vorlesungsskript sind für Xenon die Werte σ(xe) = 406 pm und ε = 236 kjmol 1 tabelliert. ( ) 12 ( ) 6 σ σ E i j = 4ε (1) r i j r i j r i j
Lösung 4 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Im Vorlesungsskript sind für Xenon die Werte σ(xe) = 406 pm und ε = 236 kjmol 1 tabelliert. ( ) 12 ( ) 6 σ σ E i j = 4ε (1) r i j r i j r i j
Gliederung der Vorlesung im SS
 Gliederung der Vorlesung im SS A. Struktureller Aufbau von Werkstoffen. Atomare Struktur.. Atomaufbau und Periodensystem der Elemente.2. Interatomare Bindungen.3. Aggregatzustände 2. Struktur des Festkörpers
Gliederung der Vorlesung im SS A. Struktureller Aufbau von Werkstoffen. Atomare Struktur.. Atomaufbau und Periodensystem der Elemente.2. Interatomare Bindungen.3. Aggregatzustände 2. Struktur des Festkörpers
Vorlesung Allgemeine Chemie: Chemische Bindung
 Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
Vorlesung Allgemeine Chemie: Chemische Bindung Inhalte Gruppentendenzen: Alkalimetalle, Halogene, Reaktion mit H 2 und H 2 O, basische und saure Oxide, Ionenbindung, Gitterenergie, Tendenzen in Abhängigkeit
4. Zusammenfassung 100 H P P H
 4. Zusammenfassung 100 =XVDQIDVVXQJ Die vorliegende Arbeit beschreibt sowohl die Synthese und Komplexchemie von Zirkoniumphosphaniden sowie der homologen Systeme des Arsens, als auch die erstellung von
4. Zusammenfassung 100 =XVDQIDVVXQJ Die vorliegende Arbeit beschreibt sowohl die Synthese und Komplexchemie von Zirkoniumphosphaniden sowie der homologen Systeme des Arsens, als auch die erstellung von
Symmetrieelemente C 3 C 2 C 3 O H H N H H H
 Symmetrieelemente Ein Symmetrielement liegt vor, wenn ein Objekt (hier: Molekül) durch eine Symmetrieoperation mit sich selbst zur Deckung gebracht werden kann. neue und alter Orientierung nicht unterscheidbar
Symmetrieelemente Ein Symmetrielement liegt vor, wenn ein Objekt (hier: Molekül) durch eine Symmetrieoperation mit sich selbst zur Deckung gebracht werden kann. neue und alter Orientierung nicht unterscheidbar
Formgedächtniswerkstoffe Welche Voraussetzungen müssen für den Formgedächtniseffekt erfüllt sein?
 Welche Voraussetzungen müssen für den Formgedächtniseffekt erfüllt sein? 1. Kompatibilität: neue Phase muss sich in Matrixphase bilden können d.h. ohne Mikrobrüche Gitterähnlichkeit muss vorhanden sein!
Welche Voraussetzungen müssen für den Formgedächtniseffekt erfüllt sein? 1. Kompatibilität: neue Phase muss sich in Matrixphase bilden können d.h. ohne Mikrobrüche Gitterähnlichkeit muss vorhanden sein!
Anorganische Chemie VI Materialdesign. Heute: Röntgen-Einkristall-Strukturanalytik
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie VI Materialdesign Heute: Röntgen-Einkristall-Strukturanalytik
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie VI Materialdesign Heute: Röntgen-Einkristall-Strukturanalytik
Marc Armbrüster (Autor) Bindungsmodelle für intermetallische Verbindungen mit der Struktur des CuAl2-Typs
 Marc Armbrüster (Autor) Bindungsmodelle für intermetallische Verbindungen mit der Struktur des CuAl2-Typs https://cuvillier.de/de/shop/publications/2717 Copyright: Cuvillier Verlag, Inhaberin Annette Jentzsch-Cuvillier,
Marc Armbrüster (Autor) Bindungsmodelle für intermetallische Verbindungen mit der Struktur des CuAl2-Typs https://cuvillier.de/de/shop/publications/2717 Copyright: Cuvillier Verlag, Inhaberin Annette Jentzsch-Cuvillier,
Anorganische Chemie III - Festkörperchemie
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Chemie/Festkörperchemie Prof. Dr. Martin Köckerling Vorlesung Anorganische Chemie III - Festkörperchemie 1 Wiederholung
Physik IV Einführung in die Atomistik und die Struktur der Materie
 Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 21 30.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 21 Prof. Thorsten Kröll 30.06.2011 1 H 2
Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 21 30.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 21 Prof. Thorsten Kröll 30.06.2011 1 H 2
Abbildung 3.1: Kraftwirkungen zwischen zwei Stabmagneten
 Kapitel 3 Magnetostatik 3.1 Einführende Versuche Wir beginnen die Magnetostatik mit einigen einführenden Versuchen. Wenn wir - als für uns neues und noch unbekanntes Material - zwei Stabmagnete wie in
Kapitel 3 Magnetostatik 3.1 Einführende Versuche Wir beginnen die Magnetostatik mit einigen einführenden Versuchen. Wenn wir - als für uns neues und noch unbekanntes Material - zwei Stabmagnete wie in
Grundlagen der Chemie Metalle
 Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Übungsaufgaben zur Kristallographie Serie 8 LÖSUNG
 1) Edelgase a) Unter welchen Bedingungen kristallisieren Edelgase? Bei tiefen Temperaturen und/oder hohen Drücken. Ausnahme: Helium braucht tiefe Temperaturen und hohen Druck gleichzeitig um zu kristallisieren.
1) Edelgase a) Unter welchen Bedingungen kristallisieren Edelgase? Bei tiefen Temperaturen und/oder hohen Drücken. Ausnahme: Helium braucht tiefe Temperaturen und hohen Druck gleichzeitig um zu kristallisieren.
4.5 UV/vis-Spektren der Tris(metaphosphate) M(PO 3 ) 3 (M = V, Cr, Mn, Fe, Mo)
 4.5 UV/vis-Spektren der Tris(metaphosphate) M(PO 3 ) 3 133 4.5 UV/vis-Spektren der Tris(metaphosphate) M(PO 3 ) 3 (M = V, Cr, Mn, Fe, Mo) Am Beispiel der Titan(III)-phosphate konnte die Anisotropie im
4.5 UV/vis-Spektren der Tris(metaphosphate) M(PO 3 ) 3 133 4.5 UV/vis-Spektren der Tris(metaphosphate) M(PO 3 ) 3 (M = V, Cr, Mn, Fe, Mo) Am Beispiel der Titan(III)-phosphate konnte die Anisotropie im
2 Bindung, Struktur und Eigenschaften von Stoffen. 2.1 Ionenbindung und Ionenkristall s Modell der Ionenbindung
 2 Bindung, Struktur und Eigenschaften von Stoffen 2.1 Ionenbindung und Ionenkristall s. 0.6 Modell der Ionenbindung 8 - Bindung zwischen typischen Metallen und Nichtmetallen, EN > 1,7 - stabile Edelgaskonfiguration
2 Bindung, Struktur und Eigenschaften von Stoffen 2.1 Ionenbindung und Ionenkristall s. 0.6 Modell der Ionenbindung 8 - Bindung zwischen typischen Metallen und Nichtmetallen, EN > 1,7 - stabile Edelgaskonfiguration
Binäre und ternäre Carbid- und Nitridsysteme der Übergangsmetalle
 Herausgeber GÜNTER PETZOW Materialkundlich- Technische r* Binäre und ternäre Carbid- und Nitridsysteme der Übergangsmetalle von HELMUT HOLLECK Leiter der Abteilung Konstitution und Thermodynamik" im Institut
Herausgeber GÜNTER PETZOW Materialkundlich- Technische r* Binäre und ternäre Carbid- und Nitridsysteme der Übergangsmetalle von HELMUT HOLLECK Leiter der Abteilung Konstitution und Thermodynamik" im Institut
Bachelorprüfung. Werkstofftechnik der Metalle
 Bachelorprüfung Werkstofftechnik der Metalle 22.07.2015 Name: Matrikelnummer: Unterschrift: Aufgabe Maximalanzahl an Punkten: Punkte erreicht: Punkte nach Einsicht (nur zusätzliche Punkte) 1 6 2 5 3 9.5
Bachelorprüfung Werkstofftechnik der Metalle 22.07.2015 Name: Matrikelnummer: Unterschrift: Aufgabe Maximalanzahl an Punkten: Punkte erreicht: Punkte nach Einsicht (nur zusätzliche Punkte) 1 6 2 5 3 9.5
Zur Farbe von Phosphaten der Übergangsmetalle
 Kapitel 4 Zur Farbe von Phosphaten der Übergangsmetalle 4.1 Vorbemerkungen - Das Problem Die grundlegenden Arbeiten von Bethe zur Kristallfeldtheorie liegen inzwischen 70 Jahre zurück (Bethe, 1929). Betrachtungen
Kapitel 4 Zur Farbe von Phosphaten der Übergangsmetalle 4.1 Vorbemerkungen - Das Problem Die grundlegenden Arbeiten von Bethe zur Kristallfeldtheorie liegen inzwischen 70 Jahre zurück (Bethe, 1929). Betrachtungen
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
4.2 Kovalente Bindung. Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916)
 4.2 Kovalente Bindung Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916) Treten Atome von Nichtmetallen miteinander in Wechselwirkung, kommt es nicht zu einer Übertragung von Elektronen. Nichtmetallatome
4.2 Kovalente Bindung Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916) Treten Atome von Nichtmetallen miteinander in Wechselwirkung, kommt es nicht zu einer Übertragung von Elektronen. Nichtmetallatome
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Musterlösung. Bitte eintragen: Matrikelnummer: 0815 Name: Musterstudi.
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
4 TTF und TCNQ in Faujasit
 32 4 TTF und TCNQ in Faujasit Die vier Cyanogruppen des 7,7,8,8 Tetracyanchinodimethan (TCNQ) erniedrigen durch ihren elektronenziehenden Effekt die Elektronendichte im chinoiden System. Durch die Aufnahme
32 4 TTF und TCNQ in Faujasit Die vier Cyanogruppen des 7,7,8,8 Tetracyanchinodimethan (TCNQ) erniedrigen durch ihren elektronenziehenden Effekt die Elektronendichte im chinoiden System. Durch die Aufnahme
Konzepte der anorganischen und analytischen Chemie II II
 Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
Steckbrief Bariumcarbonat BaCO 3
 Steckbrief Bariumcarbonat BaCO 3 Bariumcarbonat ist eine thermodynamisch stabile Verbindung, die aus Ba 2+ - Ionen 2- und CO 3 - Ionen besteht. Das farblose Salz gehört zur Stoffklasse der Carbonate und
Steckbrief Bariumcarbonat BaCO 3 Bariumcarbonat ist eine thermodynamisch stabile Verbindung, die aus Ba 2+ - Ionen 2- und CO 3 - Ionen besteht. Das farblose Salz gehört zur Stoffklasse der Carbonate und
Abbildung 2.1: MoS 2 Kristall (natürliche Probe, polykristallines Material, Fundort: Prokopstollen, Tschechien)
 2 Verwendete Halbleitermaterialien 2.1 WS 2, WSe 2, MoS 2 und MoSe 2 - Schichtgitterhalbleiter aus der Gruppe der Übergangsmetalldichalkogenide Die in dieser Arbeit als Absorber eingesetzten Materialien
2 Verwendete Halbleitermaterialien 2.1 WS 2, WSe 2, MoS 2 und MoSe 2 - Schichtgitterhalbleiter aus der Gruppe der Übergangsmetalldichalkogenide Die in dieser Arbeit als Absorber eingesetzten Materialien
Thema heute: Grundlegende Ionenstrukturen
 Wiederholung der letzten Vorlesungsstunde Einfache Metallstrukturen, Dichtestpackung von "Atomkugeln", N Oktaeder-, 2N Tetraederlücken, Hexagonal-dichte Packung, Schichtfolge ABAB, hexagonale Elementarzelle,
Wiederholung der letzten Vorlesungsstunde Einfache Metallstrukturen, Dichtestpackung von "Atomkugeln", N Oktaeder-, 2N Tetraederlücken, Hexagonal-dichte Packung, Schichtfolge ABAB, hexagonale Elementarzelle,
Pulverdiffraktometrie
 Pulverdiffraktometrie Polykristallines Material Fingerprintmethode Homogenität/ Phasenanalyse Kristallsystem + Gitterparameter + Laue-Symmetrie Raumgruppe?? Zusammensetzung - quantitativ! Textur Partikelgröße
Pulverdiffraktometrie Polykristallines Material Fingerprintmethode Homogenität/ Phasenanalyse Kristallsystem + Gitterparameter + Laue-Symmetrie Raumgruppe?? Zusammensetzung - quantitativ! Textur Partikelgröße
6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser
 Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 35 6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 6.1. Natriumsilikatglas Nach dem Ionenaustausch folgten Temperaturbehandlungen zwischen
Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 35 6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 6.1. Natriumsilikatglas Nach dem Ionenaustausch folgten Temperaturbehandlungen zwischen
Typisch metallische Eigenschaften:
 Typisch metallische Eigenschaften: hohe elektrische Leitfähigkeit hohe thermische Leitfähigkeit bei Energiezufuhr (Wärme, elektromagnetische Strahlung) können Elektronen emittiert werden metallischer Glanz
Typisch metallische Eigenschaften: hohe elektrische Leitfähigkeit hohe thermische Leitfähigkeit bei Energiezufuhr (Wärme, elektromagnetische Strahlung) können Elektronen emittiert werden metallischer Glanz
10. Das Wasserstoff-Atom Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol]
![Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol] Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol]](/thumbs/49/25486820.jpg) Seite 22 22 Auflösung von Si in NaOH-Lösung Weiterführende Infos Quarzsand und Alkalicarbonate werden bei ca. 1300 C zusammengeschmolzen und das Produkt ((Na/K) 2 O* n SiO 2 ) bei 150 C und 5 bar in Wasser
Seite 22 22 Auflösung von Si in NaOH-Lösung Weiterführende Infos Quarzsand und Alkalicarbonate werden bei ca. 1300 C zusammengeschmolzen und das Produkt ((Na/K) 2 O* n SiO 2 ) bei 150 C und 5 bar in Wasser
Übungsaufgaben Metallorganische Chemie der Übergangsmetalle Teil 3
 1 Übungsaufgaben Metallorganische Chemie der Übergangsmetalle Teil 3 1. Wie viele Valenzelektronen werden für den Metallcluster [Ru6(µ6-H)(CO)18] gezählt und welche Molekülstruktur ist zu erwarten? 2.
1 Übungsaufgaben Metallorganische Chemie der Übergangsmetalle Teil 3 1. Wie viele Valenzelektronen werden für den Metallcluster [Ru6(µ6-H)(CO)18] gezählt und welche Molekülstruktur ist zu erwarten? 2.
konst. 2 e' Abbildung 6.1: Fehlordnungsmodell im Zinkoxid bei geringfügigem Zusatz von Aluminiumoxid
 6. Dotierte Oxide 57 6. Dotierte Oxide Durch Zulegieren geringer Mengen eines anderen Metalls zu einem parabolisch zunderndem Metall (oder durch Veränderungen in der Gasphase) kann die Zundergeschwindigkeit
6. Dotierte Oxide 57 6. Dotierte Oxide Durch Zulegieren geringer Mengen eines anderen Metalls zu einem parabolisch zunderndem Metall (oder durch Veränderungen in der Gasphase) kann die Zundergeschwindigkeit
Festkörperchemie SYNTHESE. Shake and bake Methode: Sol-Gel-Methode. Am Beispiel :
 Festkörperchemie SYNTHESE Shake and bake Methode: Am Beispiel : Man zerkleinert die Salze mechanisch, damit eine möglichst große Grenzfläche zwischen den beiden Komponenten entsteht und vermischt das ganze.
Festkörperchemie SYNTHESE Shake and bake Methode: Am Beispiel : Man zerkleinert die Salze mechanisch, damit eine möglichst große Grenzfläche zwischen den beiden Komponenten entsteht und vermischt das ganze.
Darstellung des Spinells ZnAl 2 O 4
 Darstellung des Spinells ZnAl 2 O 4 Andreas J. Wagner 15. Juli 2004 1 Theorie Unter den Begriff der Spinelle fallen diverse anorganische Festkörperverbindungen der allgemeinen Zusammensetzung M II M III
Darstellung des Spinells ZnAl 2 O 4 Andreas J. Wagner 15. Juli 2004 1 Theorie Unter den Begriff der Spinelle fallen diverse anorganische Festkörperverbindungen der allgemeinen Zusammensetzung M II M III
Hexagonal dichtest gepackte Struktur
 Hexagonal dichtest gepackte Struktur Auch diese Struktur ist sehr wichtig, da sie von sehr vielen Systemen angenommen wird (kein Bravaisgitter). Das einfach hexagonale Bravais-Gitter (in 3-dim): zwei-dim:
Hexagonal dichtest gepackte Struktur Auch diese Struktur ist sehr wichtig, da sie von sehr vielen Systemen angenommen wird (kein Bravaisgitter). Das einfach hexagonale Bravais-Gitter (in 3-dim): zwei-dim:
Beispielaufgaben IChO 2. Runde 2019 Koordinationschemie
 Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
