Patientenaufklärung. Geburtsdatum:... Diagnose:... durch:...
|
|
|
- Dennis Waldfogel
- vor 7 Jahren
- Abrufe
Transkript
1 Patientenaufklärung Titel der Studie: Offene multizentrische Therapieoptimierungsstudie mit Glivec (imatinib mesylate) in Kombination mit einer Chemotherapie aus Mitoxantron, Topotecan und AraC (MTC) bei Patienten mit refraktärer oder rezidivierter akuter myeloischer Leukämie (AML) (Open-label Multicenter Trial of Glivec (imatinib mesylate, formerly known as STI571) in Combination with Chemotherapy (MTC) in Patients with Refractory or Relapsed Acute Myeloid Leukemia (AML)) Patientenname (Vor- und Nachname):... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Sehr geehrte Patientin, sehr geehrter Patient! Hintergrund der Studie Bei Ihnen wurde eine schwere Knochenmarkserkrankung festgestellt. Leider konnte die Erkrankung durch die bisherige Therapie nicht so beherrscht werden, dass keine weitere Therapie notwendig ist. In der jetzigen Situation steht keine Standardtherapie zur Verfügung. Wir möchten Ihnen anbieten, an einer von uns durchgeführten experimentellen klinischen Untersuchung teilzunehmen. In dieser Studie wird das Medikament Imatinib (Glivec ), das in Deutschland für Ihre Erkrankung noch nicht zugelassen ist und von dem wir annehmen, dass es einen Fortschritt in der Therapie Ihrer Erkrankung darstellt, untersucht. Durch die Kombination von Glivec mit einer Chemotherapie wird eine effektivere Zerstörung der leukämischen Blutzellen erwartet. Die Chemotherapie mit den Substanzen Mitoxantron, Topotecan und Cytosin-Arabinosid (MTC) wurde bereits erfolgreich eingesetzt, wobei Topotecan ebenfalls für Ihre Erkrankung noch nicht zugelassen ist. Ziel dieser Untersuchung ist es, die Wirksamkeit und die Verträglichkeit von Imatinib in Kombination mit der Chemotherapie aus Mitoxantrone, Topotecan und Cytosinarabinosid (MTC) bei Patienten mit therapierefraktärer oder rezidivierter akuter myeloischer Leukämie (AML) zu untersuchen. Insbesondere soll geprüft werden, ob die Rate an kompletten Remissionen durch die Kombination verbessert werden kann. Behandlung mit Imatinib Imatinib ist eine bei der chronisch myeloischen Leukämie (CML) zugelassene hocheffektive Substanz. Es hemmt hier die Aktivität eines Enzym, die sogenannten bcr/abl-tyrosinkinase, 1
2 die für die chronisch myeloische Leukämie typisch ist. Darüberhinaus hemmt Imatinib jedoch auch andere Eiweißmoleküle, die für die Signalgebung innerhalb der Zellen wichtig sind und in Tumor- oder Leukämiezellen eine verstärkten Zellteilungsrate bedingen. Die Folge dieser Enzymhemmung ist eine Störung der Teilung von einzelnen Zellen. Dies führt dazu, dass Körperzellen, die sich relativ häufig teilen, geschädigt werden, damit an der Zellteilung und somit am Wachstum gehindert werden. Tumorzellen teilen sich in der Regel sehr häufig und sind deswegen von diesem Mechanismus besonders betroffen. Imatinib zeigt eine hohe Ansprechrate bei der CML und einem Bindegewebstumor des Darmes (sog. GIST-Tumor) sowie bei weiteren Erkrankungen des blutbildenden Systems. Bei einigen Patienten mit akuter myeloischer Leukämie (AML) wurde ebenfalls ein Ansprechen beobachtet. Die Nebenwirkungen von Imatinib sind relativ gering. Ablauf der Studie Wenn Sie der Studienteilnahme zustimmen, werden Sie mit einer Kombinationstherapie aus Imatinib und der Chemotherapie MTC bestehend aus Topotecan, Mitoxantron und Cytarabin behandelt. Dabei erhalten Sie Imatinib in einer Dosierung von 2 x 400 mg als Tabletten, die anderen Substanzen werden als Infusionen über die Vene gegeben. Die Dauer eines Chemotherapiezyklus beträgt 7 Tage. Imatinib wird fortlaufend während der gesamten Behandlungsdauer, d.h. bis nach dem letzten Chemotherapiezyklus gegeben. Abhängig vom Ansprechen Ihrer Erkrankung auf den ersten Therapiezyklus wird die Behandlung durch einen zweiten Therapiezyklus, der dem ersten entspricht, fortgesetzt. Bei einem Ansprechen Ihrer Erkrankung auf die ersten beiden Therapiezyklen ist zur Festigung des Therapieerfolges ein dritter Therapiezyklus geplant. Bei geeigneten Patienten ist zur dauerhaften Sicherung des Therapieerfolges eine allogene Knochenmarktransplantation oder periphere Blutstammzelltransplantation geplant. Sollte dieses Verfahren bei Ihnen möglich sein, werden Sie nach den ersten beiden Therapiezyklen nochmals darüber gesondert aufgeklärt. Vor Studienbeginn sind Untersuchungen geplant, die Ihren gesundheitlichen Zustand und damit die Eignung für eine solche Studie prüfen. Zu diesem Zweck werden genaue körperliche Untersuchungen durch Ihren Arzt durchgeführt. Zusätzlich werden vor Therapiebeginn virologische Untersuchungen (Hepatitisserologie, HIV-Serologie) aus dem peripheren Blut durchgeführt. Die Blutabnahmen und andere Kontrolluntersuchungen während der Therapie entsprechen der klinischen Routine. Eine Knochenmarkzytologie, das heißt, eine Entnahme von ca. 3 ml Knochenmark mit einer Spezialkanüle, ist vor Therapiebeginn sowie nach den Therapiezyklen zur Beurteilung des Erfolgs der Chemotherapie sowie im Falle des wieder Auftretens der Erkrankung notwendig. Zu diesen Zeitpunkten sind bei der Therapie Ihrer Erkrankung auch außerhalb dieser Studie Knochenmarkspunktionen vorgesehen, so dass dies keine Mehrbelastung für Sie bedeutet. Begleitmedikation Bestimmte Arzneien sollten unter Chemotherapie nur kontrolliert eingenommen werden. Insbesondere in Kombination mit Imatinib können in der Kombination mit anderen Substanzen Komplikationen auftreten. Bitte informieren Sie deshalb Ihren behandelnden Arzt über alle von Ihnen verwendeten Medikamente. Dies betrifft auch Arzneien, die Sie ohne Rezept in der Apotheke erhalten haben. Fragen Sie bitte vorher in jedem Fall Ihren Arzt, ob Sie ein bestimmtes Medikament einnehmen dürfen, um mögliche Wechselwirkungen zu vermeiden. 2
3 Mögliche Nebenwirkungen von Imatinib Imatinib wird in der Regel gut vertragen. Häufiger beobachtete Nebenwirkungen, die überwiegend milder Natur sind, sind Flüssigkeitseinlagerungen, Muskelkrämpfe, Durchfall, Erbrechen, Muskelkrämpfe bzw. Schmerzen, Kopfschmerzen, Blutungsneigung, Hautrötungen und Erschöpfungszustände. Mögliche Nebenwirkungen der Chemotherapie Unter der Chemotherapie MTC können folgende Nebenwirkungen auftreten: Verringerung der Zahl der weißen Blutkörperchen (d.h. ein erhöhtes Infektionsrisiko), außerdem kann es zu einer Abnahme der Zahl der Blutplättchen (d.h. gesteigertes Blutungsrisiko) und ebenso zur Erniedrigung der roten Blutkörperchen mit möglicher Anämiesymptomatik (d.h. Müdigkeit, Kurzatmigkeit, Herzklopfen) kommen. Die Verminderung der roten (Erythrozyten) und der weißen Blutkörperchen (Leukozyten) sowie der Blutplättchen (Thrombozyten) ist in der Regel nur von kurzer Dauer. Weitere Nebenwirkungen, die unter und nach der Chemotherapie auftreten können, sind Schwäche, Durchfall, Appetitlosigkeit, Übelkeit, Erbrechen, Haarausfall, Obstipation, Müdigkeit, Fieber, abdominelle Schmerzen, Stomatitis, Kopfschmerzen und Hautausschlag. Zu den häufigsten Nebenwirkungen zählen: Haut: Haarausfall, Haut- und Schleimhautentzündungen, lokale Reizerscheinungen Magen/Darm: Übelkeit, Erbrechen, Diarrhoe, Schleimhautentzündungen und ulzerationen Herz/Kreislauf: Erkrankungen des Herzmuskels, unregelmäßige Herzschlagfolge, akute Herzrhythmusstörungen Blut: Knochenmarkssuppression mit Leukopenie und Thrombozytämie, Anämie Nieren: Nierenschäden und Schäden der ableitenden Harnwege Stoffwechsel/ Endokrinium: erhöhter Harnsäuregehalt des Blutes, Störungen der Spermatogenese und der Ovulation, irreversible Fertilitätsstörungen Immunsystem: Immunsuppression, allergische Reaktionen, Muskel- und Knochenschmerzen Nervensystem/ Psyche: Neurotoxische Störungen, Kopfschmerzen, Denkstörungen, Lethargie, Benommenheit/Schläfrigkeit Leber/Galle: Leberschäden, Lebervenenthrombose (in Einzelfällen) In der Regel verschwinden die genannten Nebenwirkungen nach Abschluss der Behandlung und Regeneration des Knochenmarkes. Sind die bei Ihnen beobachteten Nebenwirkungen zu stark und nicht mehr zu tolerieren, wird entweder eine Dosisreduktion des Medikaments oder sogar ein Abbruch der Therapie erforderlich. 3
4 In einigen wenigen Fällen zeigt die Behandlungsanpassung nicht den gewünschten Effekt auf die Nebenwirkungen. So könnte es auch zu länger anhaltenden und bleibenden Nebenwirkungen kommen. Außerdem können verzögerte Nebenwirkungen noch Monate oder Jahre nach Beendigung der Behandlung auftreten. Die Behandlung kann Risiken nach sich ziehen, die gegenwärtig noch nicht abgeschätzt werden können. Sollte während der Behandlung festgestellt werden, dass sich Ihre Erkrankung verschlechtert, sich eine schwere Nebenwirkung einstellt, oder sollten neue wissenschaftliche Erkenntnisse gewonnen werden, die darauf hinweisen, dass die gegenwärtige Behandlung nicht optimal für Sie ist, wird die Therapie beendet und weitere Behandlungsmaßnahmen diskutiert. Die Alternative, die in diesem Fall gewählt wird, kann andere Chemotherapeutika einschließen oder bedeuten, dass die Behandlung eingestellt wird. Natürlich haben Sie auf jeden Fall die Möglichkeit, mit Ihrem behandelnden Arzt das weitere Vorgehen genau zu besprechen, sollten Sie in diese Situation kommen. Weitere Hinweise Für Kinder, die Sie zeugen, während Sie sich in Behandlung befinden, besteht das Risiko einer Erbgutschädigung. Somit besteht unter der Zytostatikatherapie das Risiko der Behinderung des Kindes im Falle einer Schwangerschaft. Daher ist während der AML- Therapie von Patienten in gebär-/zeugungsfähigem Alter auf sichere Verhütungsmittel zu achten. Versicherungsschutz Für alle Patienten besteht zum Ausgleich des durch eine Gesundheitsprüfung eingetretenen Vermögensschaden der für klinische Prüfungen gesetzlich vorgeschriebene Versicherungsschutz. Während der Dauer der klinischen Prüfung sollte eine andere medizinische Behandlung mit Ausnahme von Notfallsituationen nur im Einvernehmen mit dem Prüfarzt durchgeführt werden. Bei Verdacht auf einen studienbedingten Gesundheitsschaden ist der behandelnde Prüfarzt sofort zu benachrichtigen, damit dieser die Versicherung informieren kann. Die Versicherung wurde bei Provinzial (Westfälische Provinzial, Provinzial Allee 1, Münster) mit der Versicherungsnummer /4750 abgeschlossen. Auf die 6 (Leistungen) und 11 (Obliegenheiten) wird besonders hingewiesen. Die Versicherungsbedingungen wurden ausgehändigt. Freiwilligkeit der Teilnahme Die Teilnahme an der Studie ist freiwillig, Sie können jederzeit, auch ohne Angaben von gründen, Ihre Teilnahmebereitschaft widerrufen, ohne dass Ihnen dadurch irgendwelche Nachteile für Ihre weitere ärztliche Versorgung entstehen. Ihre Teilnahme an der Studie kann auch durch den Prüfarzt ohne Ihre Einwilligung aus wichtigen Gründen beendet werden, wenn Ihre Sicherheit und Ihr Wohlbefinden, z.b. auf Grund von schweren Nebenwirkungen der Behandlung, gefährdet wären oder Ihr Arzt der Meinung ist, dass es beim Fortschreiten Ihrer Erkrankung in Ihrem Interesse ist, nicht mehr an der Studie teilzunehmen. 4
5 Titel der Studie: Einverständniserklärung Offene multizentrische Therapieoptimierungsstudie mit Glivec (imatinib mesylate) in Kombination mit einer Chemotherapie aus Mitoxantron, Topotecan und AraC (MTC) bei Patienten mit refraktärer oder rezidivierter akuter myeloischer Leukämie (Open-label Multicenter Trial of Glivec (imatinib mesylate, formerly known as STI571) in Combination with Chemotherapy (MTC) in Patients with Refractory or Relapsed Acute Myeloid Leukemia (AML)) Ich erkläre mich bereit, an der Studie teilzunehmen. Patienten Nr. Ich bin von Herrn / Frau (Dr. med.) ausführlich und verständlich über die Studie / Behandlungsprotokoll, mögliche Belastungen und Risiken sowie über Wesen und Tragweite der Studie sowie die sich hieraus ergebenden Anforderungen aufgeklärt worden. Ich habe darüber hinaus den Text der Patientenaufklärung und dieser Einwilligungserklärung gelesen und verstanden. Aufgetretene Fragen wurden mir vom Prüfarzt verständlich und ausreichend beantwortet. Ich hatte ausreichend Zeit, Fragen zu stellen und mich zu entscheiden. Ich werde den ärztlichen Anforderungen, die für die Durchführung der Studie erforderlich sind, Folge leisten, behalte mir jedoch das Recht vor, meine freiwillige Mitwirkung jederzeit zu beenden, ohne dass mir daraus Nachteile entstehen. Über den Abschluss einer Versicherung bin ich informiert worden. Eine Kopie der Patientenaufklärung, der Einwilligungserklärung und der Information und Einwilligungserklärung zum Datenschutz habe ich erhalten. Das Original verbleibt beim Prüfarzt. Ort, Datum Unterschrift des Patienten Ort, Datum Unterschrift des Arztes 5
6 Information und Einwilligungserklärung zum Datenschutz Titel der Studie: Offene multizentrische Therapieoptimierungsstudie mit Glivec (imatinib mesylate) in Kombination mit einer Chemotherapie aus Mitoxantron, Topotecan und AraC (MTC) bei Patienten mit refraktärer oder rezidivierter akuter myeloischer Leukämie (Open-label Multicenter Trial of Glivec (imatinib mesylate, formerly known as STI571) in Combination with Chemotherapy (MTC) in Patients with Refractory or Relapsed Acute Myeloid Leukemia (AML)) Bei wissenschaftlichen Studien werden persönliche Daten und medizinische Befunde über Sie erhoben. Die Weitergabe, Speicherung und Auswertung dieser studienbezogenen Daten erfolgt nach gesetzlichen Bestimmungen und setzt vor der Teilnahme an der Studie folgende freiwillige Einwilligung voraus: 1) Ich erkläre mich damit einverstanden, dass die im Rahmen dieser Studie erhobenen Daten/Krankheitsdaten auf Fragebögen und elektronischen Datenträgern aufgezeichnet und ohne Namensnennung weitergegeben werden dürfen an - den Leiter der klinischen Studie sowie dem Monitor und den Statistiker zur wissenschaftlichen Auswertung; - die zuständige Überwachungsbehörde (Regierungspräsidium Darmstadt) oder Bundesoberbehörde (Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn) zur Überprüfung der ordnungsgemäßen Durchführung der Studie. 2) Außerdem erkläre ich mich damit einverstanden, dass ein autorisierter und zur Verschwiegenheit verpflichteter Beauftragter der zuständigen inländischen (und ausländischen) Überwachungsbehörde oder der zuständigen Bundesoberbehörde in meine beim Prüfarzt vorhandenen personenbezogenen Daten Einsicht nimmt, soweit dies für die Überprüfung der Studie notwendig ist. Für diese Maßnahme entbinde ich den Prüfarzt von der ärztlichen Schweigepflicht. Ort, Datum Unterschrift des Patienten 6
Patientenaufklärung. Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:...
 Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Chemotherapie und Zweck der Studie Sehr geehrte
Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Chemotherapie und Zweck der Studie Sehr geehrte
Patientenaufklärung. Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:...
 Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Chemotherapie und Zweck der Studie Sehr geehrte
Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Chemotherapie und Zweck der Studie Sehr geehrte
Patienteninformation zur Studie
 Patienteninformation zur Studie Rituximab-Gemcitabin/Oxaliplatin-Therapie bei indolenten Lymphomen Sehr geehrte Patientin! Sehr geehrter Patient! Sie wurden darüber aufgeklärt, dass Sie an einem niedrig
Patienteninformation zur Studie Rituximab-Gemcitabin/Oxaliplatin-Therapie bei indolenten Lymphomen Sehr geehrte Patientin! Sehr geehrter Patient! Sie wurden darüber aufgeklärt, dass Sie an einem niedrig
Patientenaufklärung. Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:...
 Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Therapie und Zweck der Studie Sehr geehrte
Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Therapie und Zweck der Studie Sehr geehrte
für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten
 PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
Fachbereich Humanmedizin / Klinikum der Johann Wolfgang Goethe-Universität Frankfurt am Main
 PATIENTENINFORMATIONSBLATT: Patientenaufklärung zur Teilnahme an einer wissenschaftlichen Studie Pilot-Studie: Anwendungsbeobachtung zur Evaluierung der therapeutischen Wirksamkeit und Sicherheit bei Durchführung
PATIENTENINFORMATIONSBLATT: Patientenaufklärung zur Teilnahme an einer wissenschaftlichen Studie Pilot-Studie: Anwendungsbeobachtung zur Evaluierung der therapeutischen Wirksamkeit und Sicherheit bei Durchführung
EUREKA-Register des Europäischen Leukämienetzes (ELN) Patienteninformation
 Universitätsklinikum Jena Prof. Dr. Andreas Hochhaus Klinik für Innere Medizin II Tel. 03641 932 4201 Abteilung Hämatologie/Onkologie Fax 03641 932 4202 Erlanger Allee 101 cml@med.uni-jena.de 07740 Jena
Universitätsklinikum Jena Prof. Dr. Andreas Hochhaus Klinik für Innere Medizin II Tel. 03641 932 4201 Abteilung Hämatologie/Onkologie Fax 03641 932 4202 Erlanger Allee 101 cml@med.uni-jena.de 07740 Jena
Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme)......
 Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme) Name und Anschrift der Einrichtung, in der die klinische Prüfung durchgeführt wird (Prüfzentrum) Name und Telefon-Nummer des/r
Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme) Name und Anschrift der Einrichtung, in der die klinische Prüfung durchgeführt wird (Prüfzentrum) Name und Telefon-Nummer des/r
- 1 - MCL younger (version 2.2 d, 7.6.2004)
 Patienten-Information zur Europäischen Mantelzell-Lymphom-Studie Wirksamkeit von 3 Doppelzyklen R-CHOP/R-DHAP mit anschließendem Ara-C-haltigem myeloablativem Regime und autologer Stammzell-Transplantation
Patienten-Information zur Europäischen Mantelzell-Lymphom-Studie Wirksamkeit von 3 Doppelzyklen R-CHOP/R-DHAP mit anschließendem Ara-C-haltigem myeloablativem Regime und autologer Stammzell-Transplantation
PATIENTEN-INFORMATION
 Leiter der klinischen Prüfung: OA PD Dr. med. Th. Fischer III. Med. Klinik und Poliklinik Univ.-Klinikum Gebäude 302 Langenbeckstraße 1 55131 MAINZ Tel: 06131-17-6544 PATIENTEN-INFORMATION zur klinischen
Leiter der klinischen Prüfung: OA PD Dr. med. Th. Fischer III. Med. Klinik und Poliklinik Univ.-Klinikum Gebäude 302 Langenbeckstraße 1 55131 MAINZ Tel: 06131-17-6544 PATIENTEN-INFORMATION zur klinischen
Patienteninformation
 AML 97 (OSHO-Protokoll #45) Rolle der allogenen Stammzelltransplantation (SCT) im Vergleich zu einer zweiten Konsolidierung auf das leukämiefreie Überleben (LFS) von Patienten über 60 Jahre in kompletter
AML 97 (OSHO-Protokoll #45) Rolle der allogenen Stammzelltransplantation (SCT) im Vergleich zu einer zweiten Konsolidierung auf das leukämiefreie Überleben (LFS) von Patienten über 60 Jahre in kompletter
Patienteninformation und Einwilligungserklärung
 Patienteninformation und Einwilligungserklärung Wirksamkeit und Sicherheit von 90Y-Ibritumomab Tiuxetan bei Patienten mit rezidiviertem oder refraktärem Mantelzell-Lymphom nach autologer Stamzelltransplantation
Patienteninformation und Einwilligungserklärung Wirksamkeit und Sicherheit von 90Y-Ibritumomab Tiuxetan bei Patienten mit rezidiviertem oder refraktärem Mantelzell-Lymphom nach autologer Stamzelltransplantation
Patienteninformation. Behandlung der akuten Promyelozytenleukämie mit Arsentrioxid (TRISENOX)
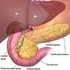 Anlage 11 Patienteninformation Behandlung der akuten Promyelozytenleukämie mit Arsentrioxid (TRISENOX) Eine Phase-IV Studie mit Arsentrioxid (ATO) zur Erfassung der Wirksamkeit und Toxizität sowie des
Anlage 11 Patienteninformation Behandlung der akuten Promyelozytenleukämie mit Arsentrioxid (TRISENOX) Eine Phase-IV Studie mit Arsentrioxid (ATO) zur Erfassung der Wirksamkeit und Toxizität sowie des
PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG
 PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG Prüfstelle: Prüfarzt: (Name) Tel.: Gegenüberstellung von Imatinib (400mg täglich) und Nilotinib (2x 300mg täglich) bei Patienten mit chronischer myeloischer
PATIENTENINFORMATION UND EINVERSTÄNDNISERKLÄRUNG Prüfstelle: Prüfarzt: (Name) Tel.: Gegenüberstellung von Imatinib (400mg täglich) und Nilotinib (2x 300mg täglich) bei Patienten mit chronischer myeloischer
Behandlung der feuchten altersabhängigen Makuladegeneration (feuchte AMD) mit VEGF-Hemmern durch operative Medikamenteneingabe in das Auge
 Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
Probandeninformation für Patienten mit Bluthochdruck
 Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Probandeninformation für Patienten mit Bluthochdruck Studie über Monoamine-produzierende Tumore The PMT-study: Prospective
Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Probandeninformation für Patienten mit Bluthochdruck Studie über Monoamine-produzierende Tumore The PMT-study: Prospective
Akute Leukämien und das Myelodysplastische Syndrom
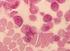 Akute Leukämien und das Myelodysplastische Syndrom Der Begriff Leukämie kommt aus dem Griechischen und bedeutet weißes Blut. Der Name rührt daher, dass bei Patienten mit Leukämie sehr viele weiße Blutzellen
Akute Leukämien und das Myelodysplastische Syndrom Der Begriff Leukämie kommt aus dem Griechischen und bedeutet weißes Blut. Der Name rührt daher, dass bei Patienten mit Leukämie sehr viele weiße Blutzellen
Teilnehmerinformation zur Vorbereitung der mündlichen Aufklärung durch den zuständigen Arzt oder Psychologen
 Teilnehmerinformation zur Vorbereitung der mündlichen Aufklärung durch den zuständigen Arzt oder Psychologen D3 Titel der Studie: Untersuchung des Einflusses einer veränderten serotonergen und dopaminergen
Teilnehmerinformation zur Vorbereitung der mündlichen Aufklärung durch den zuständigen Arzt oder Psychologen D3 Titel der Studie: Untersuchung des Einflusses einer veränderten serotonergen und dopaminergen
wir möchten Sie fragen, ob Sie bereit sind, an der von uns vorgesehenen klinischen Studie teilzunehmen.
 Universitätsklinikum Essen. Neurologische Klinik und Poliklinik. Hufelandstr. 55. 45122 Essen Sehr geehrte Dame, sehr geehrter Herr, wir möchten Sie fragen, ob Sie bereit sind, an der von uns vorgesehenen
Universitätsklinikum Essen. Neurologische Klinik und Poliklinik. Hufelandstr. 55. 45122 Essen Sehr geehrte Dame, sehr geehrter Herr, wir möchten Sie fragen, ob Sie bereit sind, an der von uns vorgesehenen
Universitätsklinikum des Saarlandes
 Universitätsklinikum des Saarlandes Merkblatt zur Patienten/innenaufklärung Studientitel: Klinische Phase I/II Dosisfindungssstudie zur Ermittlung der maximal tolerierten Dosis (MTD) von rekombinantem
Universitätsklinikum des Saarlandes Merkblatt zur Patienten/innenaufklärung Studientitel: Klinische Phase I/II Dosisfindungssstudie zur Ermittlung der maximal tolerierten Dosis (MTD) von rekombinantem
Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt [Adresse] Patienteninformation/Einwilligungserklärung
![Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt [Adresse] Patienteninformation/Einwilligungserklärung Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt [Adresse] Patienteninformation/Einwilligungserklärung](/thumbs/33/15930247.jpg) Universitätsklinikum Münster. Klinik für Transplantationsmedizin. 48149 Münster [Adresse] Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt Direktor Albert-Schweitzer-Campus
Universitätsklinikum Münster. Klinik für Transplantationsmedizin. 48149 Münster [Adresse] Klinik für Transplantationsmedizin Univ.-Prof. Dr. med. Hartmut H.-J. Schmidt Direktor Albert-Schweitzer-Campus
Ihr Wegweiser zu. Information für Patienten
 Ihr Wegweiser zu Information für Patienten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können
Ihr Wegweiser zu Information für Patienten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können
PATIENTEN - INFORMATION
 PATIENTEN - INFORMATION zur klinischen Prüfung Eine offene Phase II Studie zur Untersuchung der Durchführbarkeit, Sicherheit und Effektivität einer dosisreduzierten Stammzelltransplantation bei älteren
PATIENTEN - INFORMATION zur klinischen Prüfung Eine offene Phase II Studie zur Untersuchung der Durchführbarkeit, Sicherheit und Effektivität einer dosisreduzierten Stammzelltransplantation bei älteren
MUSTER BEM-EINLADUNG
 MUSTER BEM-EINLADUNG Sehr geehrte(r) Frau/Herr, seit dem sind Sie arbeitsunfähig erkrankt. Alternativ: Innerhalb der letzten 12 Monate sind Sie insgesamt länger als 6 Wochen arbeitsunfähig erkrankt. Aufgrund
MUSTER BEM-EINLADUNG Sehr geehrte(r) Frau/Herr, seit dem sind Sie arbeitsunfähig erkrankt. Alternativ: Innerhalb der letzten 12 Monate sind Sie insgesamt länger als 6 Wochen arbeitsunfähig erkrankt. Aufgrund
Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle,
 Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle, prospektive Kohortenstudie Protokoll: Initiator: EuroTARGET: Europäisches Forschungsprojekt
Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle, prospektive Kohortenstudie Protokoll: Initiator: EuroTARGET: Europäisches Forschungsprojekt
ANHANG NEBENWIRKUNGEN
 ANHANG NEBENWIRKUNGEN Gegenüberstellung von Imatinib (400mg täglich) und Nilotinib (2x 300mg täglich) bei Patienten mit chronischer myeloischer Leukämie (CML) in erster chronischer Phase, die unter Behandlung
ANHANG NEBENWIRKUNGEN Gegenüberstellung von Imatinib (400mg täglich) und Nilotinib (2x 300mg täglich) bei Patienten mit chronischer myeloischer Leukämie (CML) in erster chronischer Phase, die unter Behandlung
Patienteninformation
 Patienteninformation Erfassung der Komplikationsrate bei rheumaorthopädischen Eingriffen in Abhängigkeit von der eingenommenen Basistherapie. Rheumatische Erkrankungen werden medikamentös mittels sogenannter
Patienteninformation Erfassung der Komplikationsrate bei rheumaorthopädischen Eingriffen in Abhängigkeit von der eingenommenen Basistherapie. Rheumatische Erkrankungen werden medikamentös mittels sogenannter
Klinikum der Universität München
 Patienteninformation Patienten-Aufklärungsbogen zur Studie Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen wurde eine bösartige Erkrankung des Lymphsystems ein sogenanntes Non- Hodgkin-Lymphom
Patienteninformation Patienten-Aufklärungsbogen zur Studie Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen wurde eine bösartige Erkrankung des Lymphsystems ein sogenanntes Non- Hodgkin-Lymphom
De-ursil - De-ursil RR - De-ursil RR mite
 Bern, 23.10.2015 Information für Patientinnen und Patienten Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen bzw. anwenden. Dieses Arzneimittel ist Ihnen persönlich verschrieben
Bern, 23.10.2015 Information für Patientinnen und Patienten Lesen Sie diese Packungsbeilage sorgfältig, bevor Sie das Arzneimittel einnehmen bzw. anwenden. Dieses Arzneimittel ist Ihnen persönlich verschrieben
Patienteninformation zur Chemotherapie
 SLK-Kliniken Heilbronn GmbH, Klinikum Am Gesundbrunnen, Heilbronn Urologische Klinik Ärztlicher Direktor Prof. Dr. med. J. Rassweiler Am Gesundbrunnen 74064 Heilbronn Direktwahl (07131) 49-2401 Ambulanz
SLK-Kliniken Heilbronn GmbH, Klinikum Am Gesundbrunnen, Heilbronn Urologische Klinik Ärztlicher Direktor Prof. Dr. med. J. Rassweiler Am Gesundbrunnen 74064 Heilbronn Direktwahl (07131) 49-2401 Ambulanz
Chirurgische Klinik PD Dr. Daniel Weber Leitender Arzt Leiter Handchirurgie
 Chirurgische Klinik PD Dr. Daniel Weber Leitender Arzt Leiter Handchirurgie Kinderspital Zürich - Eleonorenstiftung Steinwiesstrasse 75 CH-8032 Zürich www.kispi.uzh.ch Kontakt Dr. phil. Norma Ruppen-Greeff
Chirurgische Klinik PD Dr. Daniel Weber Leitender Arzt Leiter Handchirurgie Kinderspital Zürich - Eleonorenstiftung Steinwiesstrasse 75 CH-8032 Zürich www.kispi.uzh.ch Kontakt Dr. phil. Norma Ruppen-Greeff
Plasmozytom / multiples Myelom Nebenwirkungen und Langzeitfolgen
 Plasmozytom / multiples Myelom- Selbsthilfegruppe NRW e.v. Patientenseminar, 9. November 2013 Bildungsstätte Essen, Wimberstraße 1, 45239 Essen Plasmozytom / multiples Myelom Nebenwirkungen und Langzeitfolgen
Plasmozytom / multiples Myelom- Selbsthilfegruppe NRW e.v. Patientenseminar, 9. November 2013 Bildungsstätte Essen, Wimberstraße 1, 45239 Essen Plasmozytom / multiples Myelom Nebenwirkungen und Langzeitfolgen
auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
 Seite 4 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Folsäure Heumann 5 mg Tabletten Folsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Seite 4 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Folsäure Heumann 5 mg Tabletten Folsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gesundheitstipps Fit bleiben 50plus
 Gesundheitstipps Fit bleiben 50plus Vom richtigen Umgang mit Medikamenten Gut informiert in die zweite Lebenshälfte Wenn Sie heute um die 50 Jahre alt sind, haben Sie weitere drei oder vier Lebensjahrzehnte
Gesundheitstipps Fit bleiben 50plus Vom richtigen Umgang mit Medikamenten Gut informiert in die zweite Lebenshälfte Wenn Sie heute um die 50 Jahre alt sind, haben Sie weitere drei oder vier Lebensjahrzehnte
GEHT DA MEHR? Fragen und Antworten zum Thema Erektionsstörung
 GEHT DA MEHR? Fragen und Antworten zum Thema Erektionsstörung EREKTIONSSTÖRUNGEN Gute Nachrichten: Man(n) kann was tun! Wenn die Liebe auf kleiner Flamme brennt, kann dies eine vorübergehende Abkühlung
GEHT DA MEHR? Fragen und Antworten zum Thema Erektionsstörung EREKTIONSSTÖRUNGEN Gute Nachrichten: Man(n) kann was tun! Wenn die Liebe auf kleiner Flamme brennt, kann dies eine vorübergehende Abkühlung
Anhang III. Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage
 Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
Anhang III Änderungen an relevanten Abschnitten der Fachinformation und der Packungsbeilage Hinweis: Änderungen an der Fachinformation und der Packungsbeilage müssen unter Umständen im Anschluss durch
DEUTSCHE STUDIENGRUPPE GASTROINTESTINALE LYMPHOME DSGL
 DEUTSCHE STUDIENGRUPPE GASTROINTESTINALE LYMPHOME DSGL Patienteninformation Studie DSGL 01/2003 Original für den Patienten Kopie für den Arzt Kopie für das Studiensekretariat Sehr geehrte Patientin, sehr
DEUTSCHE STUDIENGRUPPE GASTROINTESTINALE LYMPHOME DSGL Patienteninformation Studie DSGL 01/2003 Original für den Patienten Kopie für den Arzt Kopie für das Studiensekretariat Sehr geehrte Patientin, sehr
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Patienteninformation
 Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, Ihr Arzt hat Ihnen die Möglichkeit zur Teilnahme an einer klinischen Studie eröffnet. Vielleicht sind Sie auch durch eigene Initiative
Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, Ihr Arzt hat Ihnen die Möglichkeit zur Teilnahme an einer klinischen Studie eröffnet. Vielleicht sind Sie auch durch eigene Initiative
Subkutane spezifische Immuntherapie
 Subkutane spezifische Immuntherapie Eine Information für Patienten A business of Spezifische Immuntherapie Die Allergietestung durch Ihren Arzt hat ergeben, dass Sie (oder Ihr Kind) an einer Allergie leiden.
Subkutane spezifische Immuntherapie Eine Information für Patienten A business of Spezifische Immuntherapie Die Allergietestung durch Ihren Arzt hat ergeben, dass Sie (oder Ihr Kind) an einer Allergie leiden.
Angaben zur Vorgeschichte (Dieser Erhebungsbogen verbleibt im Gesundheits- und Veterinäramt)
 Kreis Siegen-Wittgenstein Gesundheits- und Veterinäramt Angaben zur Vorgeschichte (Dieser Erhebungsbogen verbleibt im Gesundheits- und Veterinäramt) Name, ggfs. auch Geburtsname Vorname Straße, Hausnummer
Kreis Siegen-Wittgenstein Gesundheits- und Veterinäramt Angaben zur Vorgeschichte (Dieser Erhebungsbogen verbleibt im Gesundheits- und Veterinäramt) Name, ggfs. auch Geburtsname Vorname Straße, Hausnummer
Ihr Wegweiser zur. Therapie mit YERVOY (Ipilimumab)
 Ihr Wegweiser zur Therapie mit YERVOY (Ipilimumab) Informationsbroschüre für Patienten Yervoy unterliegt einer zusätzlichen Überwachung. Dies ermögicht eine schnelle Identifizierung neuer Erkenntnisse
Ihr Wegweiser zur Therapie mit YERVOY (Ipilimumab) Informationsbroschüre für Patienten Yervoy unterliegt einer zusätzlichen Überwachung. Dies ermögicht eine schnelle Identifizierung neuer Erkenntnisse
Patienteninformation
 I Patientenaufklärung und Einverständniserklärung Liebe Patientin, lieber Patient! Sie leiden unter einer Erkrankung des rheumatischen Formenkreises. Dazu zählen sowohl entzündliche (Arthritis) als auch
I Patientenaufklärung und Einverständniserklärung Liebe Patientin, lieber Patient! Sie leiden unter einer Erkrankung des rheumatischen Formenkreises. Dazu zählen sowohl entzündliche (Arthritis) als auch
Klinik für Nuklearmedizin - Universitätsklinikum Aachen
 - Universitätsklinikum Aachen Patienteninformation über die Radiopeptidtherapie Zweck der Behandlung Die neuroendokrinen Tumorzellen besitzen spezielle Rezeptoren an ihrer Oberfläche, die als Andockstelle
- Universitätsklinikum Aachen Patienteninformation über die Radiopeptidtherapie Zweck der Behandlung Die neuroendokrinen Tumorzellen besitzen spezielle Rezeptoren an ihrer Oberfläche, die als Andockstelle
Multiples Myelom: Behandlungsmöglichkeiten im Rezidiv. Univ.-Doz. Dr. Eberhard Gunsilius Hämatologie & Onkologie Universitätsklinik Innsbruck
 Multiples Myelom: Behandlungsmöglichkeiten im Rezidiv Univ.-Doz. Dr. Eberhard Gunsilius Hämatologie & Onkologie Universitätsklinik Innsbruck Myelom: Therapeutisches Arsenal Verbesserung der Prognose Interferon,
Multiples Myelom: Behandlungsmöglichkeiten im Rezidiv Univ.-Doz. Dr. Eberhard Gunsilius Hämatologie & Onkologie Universitätsklinik Innsbruck Myelom: Therapeutisches Arsenal Verbesserung der Prognose Interferon,
Patientenaufklärung. Chemotherapie mit Gemcitabin (Gemzar ) und Carboplatin. Patientenaufkleber
 314 Kapitel Harnblasentumor.4.2 Gemcitabin und Carboplatin Patientenaufklärung Chemotherapie mit Gemcitabin (Gemzar ) und Carboplatin Patientenaufkleber Sehr geehrte Patientin, sehr geehrter Patient, bei
314 Kapitel Harnblasentumor.4.2 Gemcitabin und Carboplatin Patientenaufklärung Chemotherapie mit Gemcitabin (Gemzar ) und Carboplatin Patientenaufkleber Sehr geehrte Patientin, sehr geehrter Patient, bei
Frauen und HIV. Marianne Rademacher. Referentin für Prävention für Weibliche Sexarbeit/Frauen im Kontext von HIV, STI und Hepatitis der DAH e.v.
 Frauen und HIV Referentin für Prävention für Weibliche Sexarbeit/Frauen im Kontext von HIV, STI und Hepatitis der DAH e.v. BAH, Positvenplenum 29.10.2015 Effektivität und Verträglichkeit der cart Frauen
Frauen und HIV Referentin für Prävention für Weibliche Sexarbeit/Frauen im Kontext von HIV, STI und Hepatitis der DAH e.v. BAH, Positvenplenum 29.10.2015 Effektivität und Verträglichkeit der cart Frauen
1. Aushändigen der Informationsschrift an die Patientin Q
 1 universitäts Prof. Dr. med. Annegret Geipel Leitung Pränatale Medizin DEGUM Stufe III Spezielle Geburtshilfe und Perinatalmedizin Studienzentrale PraenaTest Frau Claudia Büthke Fon:+49 (0) 228-287 14728
1 universitäts Prof. Dr. med. Annegret Geipel Leitung Pränatale Medizin DEGUM Stufe III Spezielle Geburtshilfe und Perinatalmedizin Studienzentrale PraenaTest Frau Claudia Büthke Fon:+49 (0) 228-287 14728
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Wortlaut der für die Packungsbeilage vorgesehenen Angaben
 Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
Was Sie tun können, um richtig vorzusorgen Durch einen Unfall, eine schwere Krankheit oder Altersabbau kann jeder Mensch in eine Situation kommen, in
 1BUJFOUFOWFSGÛHVOH 7PSTPSHFWPMMNBDIU #FUSFVVOHTWFSGÛHVOH Was Sie tun können, um richtig vorzusorgen Durch einen Unfall, eine schwere Krankheit oder Altersabbau kann jeder Mensch in eine Situation kommen,
1BUJFOUFOWFSGÛHVOH 7PSTPSHFWPMMNBDIU #FUSFVVOHTWFSGÛHVOH Was Sie tun können, um richtig vorzusorgen Durch einen Unfall, eine schwere Krankheit oder Altersabbau kann jeder Mensch in eine Situation kommen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN ECHINACIN MADAUS -TROPFEN. Wirkstoff: Presssaft aus Purpursonnenhutkraut
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN ECHINACIN MADAUS -TROPFEN Wirkstoff: Presssaft aus Purpursonnenhutkraut Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN ECHINACIN MADAUS -TROPFEN Wirkstoff: Presssaft aus Purpursonnenhutkraut Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
Patienteninformation
 Patienteninformation Prüfzentrum (Name, Anschrift): Prüfarzt (Name/Telefon): Studienzentrale (Anschrift/Telefon): Studienleiter: Prof. Dr. med. M. Gregor, Universitätsklinikum Tübingen Dokumentationsassistentin:
Patienteninformation Prüfzentrum (Name, Anschrift): Prüfarzt (Name/Telefon): Studienzentrale (Anschrift/Telefon): Studienleiter: Prof. Dr. med. M. Gregor, Universitätsklinikum Tübingen Dokumentationsassistentin:
MORBUS FABRY Morbus Fabry ist eine seltene und schwere, aber behandelbare Krankheit
 MORBUS FABRY Morbus Fabry ist eine seltene und schwere, aber behandelbare Krankheit Diese Broschüre möchte Sie über die Entstehung, Vererbung und Behandlung der Fabry-Erkrankung informieren. Hier finden
MORBUS FABRY Morbus Fabry ist eine seltene und schwere, aber behandelbare Krankheit Diese Broschüre möchte Sie über die Entstehung, Vererbung und Behandlung der Fabry-Erkrankung informieren. Hier finden
Information zur Anschlussrehabilitation (AR) für die Patientin/den Patienten
 Information zur Anschlussrehabilitation (AR) für die Patientin/den Patienten Sehr geehrte Patientin, sehr geehrter Patient, Ihr Krankenhausarzt schlägt Ihre Weiterbehandlung in einer Rehabilitationseinrichtung
Information zur Anschlussrehabilitation (AR) für die Patientin/den Patienten Sehr geehrte Patientin, sehr geehrter Patient, Ihr Krankenhausarzt schlägt Ihre Weiterbehandlung in einer Rehabilitationseinrichtung
Fragen und Antworten zur hämatopoetischen Stammzelle
 Fragen und Antworten zur hämatopoetischen Stammzelle Grundlagen, Indikationen, therapeutischer Nutzen von Rainer Haas, Ralf Kronenwett 1. Auflage Fragen und Antworten zur hämatopoetischen Stammzelle Haas
Fragen und Antworten zur hämatopoetischen Stammzelle Grundlagen, Indikationen, therapeutischer Nutzen von Rainer Haas, Ralf Kronenwett 1. Auflage Fragen und Antworten zur hämatopoetischen Stammzelle Haas
Patienteninformation zur Behandlung der Psoriasis mit Ciclosporin
 Praxis Dr. Ralph von Kiedrowski Patienteninformation zur Behandlung der Psoriasis mit Ciclosporin Liebe Patientin, lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Ciclosporin-
Praxis Dr. Ralph von Kiedrowski Patienteninformation zur Behandlung der Psoriasis mit Ciclosporin Liebe Patientin, lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Ciclosporin-
Epilepsie erfolgreich kontrollieren
 Epilepsie pass Epilepsie erfolgreich kontrollieren Mit Epilepsie-Tagebuch Das Epilepsie-Tagebuch von Hund Name Geburtsdatum Rasse Gewicht Erster epileptischer Anfall am (Tag/Monat/Jahr) im Alter von Besitzer
Epilepsie pass Epilepsie erfolgreich kontrollieren Mit Epilepsie-Tagebuch Das Epilepsie-Tagebuch von Hund Name Geburtsdatum Rasse Gewicht Erster epileptischer Anfall am (Tag/Monat/Jahr) im Alter von Besitzer
Cefavora - Tropfen. Gebrauchsinformation: Information für Anwender
 1 von 5 Cefavora - Tropfen Gebrauchsinformation: Information für Anwender Wirkstoffe: Ginkgo biloba Ø / Viscum album Ø / Crataegus Ø Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor sie mit
1 von 5 Cefavora - Tropfen Gebrauchsinformation: Information für Anwender Wirkstoffe: Ginkgo biloba Ø / Viscum album Ø / Crataegus Ø Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor sie mit
Postfach 1660. 61406 Oberursel. Versicherungs-Nr.: Zu versichernde Person: Geburtsdatum:
 ALTE LEIPZIGER Leben Postfach 1660 Absender: 61406 Oberursel Versicherungs-Nr.: Zu versichernde Person: Geburtsdatum: Fragebogen zu psychosomatischen und psychischen Störungen/Erkrankungen 1. Welche Erkrankungen
ALTE LEIPZIGER Leben Postfach 1660 Absender: 61406 Oberursel Versicherungs-Nr.: Zu versichernde Person: Geburtsdatum: Fragebogen zu psychosomatischen und psychischen Störungen/Erkrankungen 1. Welche Erkrankungen
SPENDE VON HÄMATOPOETISCHEN STAMMZELLEN (HSZ) EINE HOFFNUNG AUF LEBEN
 IN IHRER NÄHE SIE? SPENDE VON HÄMATOPOETISCHEN STAMMZELLEN (HSZ) EINE HOFFNUNG AUF LEBEN SIND SIE KOMPATIBEL? WER KANN SICH ALS POTENTIELLER SPENDER EINTRAGEN LASSEN? Jede Person zwischen 18 und 40 Jahren,
IN IHRER NÄHE SIE? SPENDE VON HÄMATOPOETISCHEN STAMMZELLEN (HSZ) EINE HOFFNUNG AUF LEBEN SIND SIE KOMPATIBEL? WER KANN SICH ALS POTENTIELLER SPENDER EINTRAGEN LASSEN? Jede Person zwischen 18 und 40 Jahren,
Patientenverfügung. Ich Familienname:... Vorname:... Geburtsdatum:... Adresse:...
 Patientenverfügung Ich Familienname:... Vorname:... Geburtsdatum:... Adresse:... bestimme für den Fall, dass ich vorübergehend oder dauerhaft außerstande bin, meinen Willen zu bilden oder verständlich
Patientenverfügung Ich Familienname:... Vorname:... Geburtsdatum:... Adresse:... bestimme für den Fall, dass ich vorübergehend oder dauerhaft außerstande bin, meinen Willen zu bilden oder verständlich
Patienten-Information
 Patienten-Information Behandlung des hypereosinophilen Syndroms (HES), der chronischen Eosinophilenleukämie (CEL) und der systemischen Mastozytose mit Eosinophilie (SME) mit dem Tyrosinkinaseinhibitor
Patienten-Information Behandlung des hypereosinophilen Syndroms (HES), der chronischen Eosinophilenleukämie (CEL) und der systemischen Mastozytose mit Eosinophilie (SME) mit dem Tyrosinkinaseinhibitor
Klinische Studien für Kinder erklärt Eine Broschüre für Kinder ab 7 Jahre
 Forschen, um neue Medikamente zu finden Klinische Studien für Kinder erklärt Eine Broschüre für Kinder ab 7 Jahre Worum geht es hier? Liebe Kinder, liebe Eltern, in dieser Broschüre steht, wie man neue
Forschen, um neue Medikamente zu finden Klinische Studien für Kinder erklärt Eine Broschüre für Kinder ab 7 Jahre Worum geht es hier? Liebe Kinder, liebe Eltern, in dieser Broschüre steht, wie man neue
Patienteninformation und Einwilligungserklärung zur Teilnahme am Projekt Register unerwünschter Arzneimittel- Nebenwirkungen (UAW-Register)
 Patienteninformation und Einwilligungserklärung zur Teilnahme am Projekt Register unerwünschter Arzneimittel- Nebenwirkungen (UAW-Register) Sehr geehrte Patientin, sehr geehrter Patient, sehr geehrte Angehörige,
Patienteninformation und Einwilligungserklärung zur Teilnahme am Projekt Register unerwünschter Arzneimittel- Nebenwirkungen (UAW-Register) Sehr geehrte Patientin, sehr geehrter Patient, sehr geehrte Angehörige,
Briefkopf. Synopsis des Studienprotokolls
 Briefkopf Synopsis des Studienprotokolls Titel der Studie Studie LDE225 in Kombination mit Paclitaxel bei Patienten mit fortgeschrittenen soliden Tumoren. Eine multizentrische Studie der Phase I. Protokollnummer
Briefkopf Synopsis des Studienprotokolls Titel der Studie Studie LDE225 in Kombination mit Paclitaxel bei Patienten mit fortgeschrittenen soliden Tumoren. Eine multizentrische Studie der Phase I. Protokollnummer
Name: Größe: cm Vorname: Gewicht: kg. Adresse: Letzte Krebsvorsorgeuntersuchung: Letzte Blutung / Periode: Telefonnummer: Handy:
 Anamnesebogen Liebe Patientin, um einen möglichst reibungslosen Behandlungsablauf zu gewährleisten bitten wir Sie, die folgenden Fragen bereits vor dem Gespräch mit Ihrer Ärztin nach bestem Wissen zu beantworten.
Anamnesebogen Liebe Patientin, um einen möglichst reibungslosen Behandlungsablauf zu gewährleisten bitten wir Sie, die folgenden Fragen bereits vor dem Gespräch mit Ihrer Ärztin nach bestem Wissen zu beantworten.
Wirkstoff: Natriumchondroitinsulfat
 Gebrauchsinformation: Information für Anwender CONDROSULF 800 mg - Tabletten Wirkstoff: Natriumchondroitinsulfat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender CONDROSULF 800 mg - Tabletten Wirkstoff: Natriumchondroitinsulfat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Patientenaufklärung und Einverständniserklärung zur intravitrealen Injektion beim diabetischen Makulaödem
 Patientendaten Arzt-/Klinikstempel Patientenaufklärung und Einverständniserklärung zur intravitrealen Injektion beim diabetischen Makulaödem Das diabetische Makulaödem ist eine Verdickung der Netzhaut.
Patientendaten Arzt-/Klinikstempel Patientenaufklärung und Einverständniserklärung zur intravitrealen Injektion beim diabetischen Makulaödem Das diabetische Makulaödem ist eine Verdickung der Netzhaut.
Patienteninformation und Einwilligungserklärung
 Patienteninformation und Einwilligungserklärung zur PRO-Dokumentation im MS-Register der DMSG, Bundesverband e.v. Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, Sie haben Ihre Einwilligung
Patienteninformation und Einwilligungserklärung zur PRO-Dokumentation im MS-Register der DMSG, Bundesverband e.v. Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, Sie haben Ihre Einwilligung
AMLCG und German AML Intergroup MUSTER
 AMLCG und German AML Intergroup Patienteninformation MUSTER Risiko-stratifizierte Therapie primärer und sekundärer AML und MDS. Eine randomisierte Studie der AMLCG (1) zur Bedeutung von Hochdosis-AraC
AMLCG und German AML Intergroup Patienteninformation MUSTER Risiko-stratifizierte Therapie primärer und sekundärer AML und MDS. Eine randomisierte Studie der AMLCG (1) zur Bedeutung von Hochdosis-AraC
vorsorgen selbst bestimmen e.v.
 vorsorgen selbst bestimmen e.v. Patientenverfügung 1. Zu meiner Person Name: Vorname: Geburtsdatum: Wohnort: Straße: Geburtsort: 2. Reichweite dieser Patientenverfügung Die folgende Verfügung bedeutet
vorsorgen selbst bestimmen e.v. Patientenverfügung 1. Zu meiner Person Name: Vorname: Geburtsdatum: Wohnort: Straße: Geburtsort: 2. Reichweite dieser Patientenverfügung Die folgende Verfügung bedeutet
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Aciclovir Mylan 800 mg Tabletten Aciclovir
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Aciclovir Mylan 800 mg Tabletten Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Aciclovir Mylan 800 mg Tabletten Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Behandlung mit gerinnungshemmenden Substanzen Was bedeutet Blutgerinnung?
 Behandlung mit gerinnungshemmenden Substanzen Was bedeutet Blutgerinnung? In unverletzten Blutgefäßen ist das Blut beim gesunden Menschen stets dünnflüssig und gerinnt nicht. Eine nach einer Verletzung
Behandlung mit gerinnungshemmenden Substanzen Was bedeutet Blutgerinnung? In unverletzten Blutgefäßen ist das Blut beim gesunden Menschen stets dünnflüssig und gerinnt nicht. Eine nach einer Verletzung
Patienteninformation zur systemischen Behandlung mit Acitretin
 Praxis Dr. Ralph von Kiedrowski Patienteninformation zur systemischen Behandlung mit Acitretin Lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Acitretin erläutern. Noch
Praxis Dr. Ralph von Kiedrowski Patienteninformation zur systemischen Behandlung mit Acitretin Lieber Patient, dieses Informationsblatt soll Ihnen die vorgesehene Behandlung mit Acitretin erläutern. Noch
Nebenwirkungsmanagement
 Nebenwirkungsmanagement Robert Dengler Schwerpunktpraxis und Tagesklinik für Hämatologie und Onkologie, Hämostaseologie, Palliativmedizin Dr. A. Kröber, Dr. C. Stosiek, Dr. T. Zilch, PD Dr. C. Schambeck,
Nebenwirkungsmanagement Robert Dengler Schwerpunktpraxis und Tagesklinik für Hämatologie und Onkologie, Hämostaseologie, Palliativmedizin Dr. A. Kröber, Dr. C. Stosiek, Dr. T. Zilch, PD Dr. C. Schambeck,
MEDIKAMENTÖSER SCHWANGERSCHAFTSABBRUCH
 Dr. Christiane Tennhardt Berlin - Lichtenberg Internationale Erfahrungen / besondere Risiken? Legale / Abrechnungstechnische Aspekte Akzeptanz der Klientinnen bei BALANCE Praktische Durchführung Zwischenbilanz
Dr. Christiane Tennhardt Berlin - Lichtenberg Internationale Erfahrungen / besondere Risiken? Legale / Abrechnungstechnische Aspekte Akzeptanz der Klientinnen bei BALANCE Praktische Durchführung Zwischenbilanz
GEBRAUCHSINFORMATION. Wirkstoff: Acetylsalicylsäure. Z.Nr.: 3155
 Liebe Patientin, lieber Patient! Bitte lesen Sie diese Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Einnahme dieses Arzneimittels beachten sollen. Wenden
Liebe Patientin, lieber Patient! Bitte lesen Sie diese Gebrauchsinformation aufmerksam, weil sie wichtige Informationen darüber enthält, was Sie bei der Einnahme dieses Arzneimittels beachten sollen. Wenden
Bluterkrankungen bei Menschen mit Down-Syndrom
 Bluterkrankungen bei Menschen mit Down-Syndrom oder Besonderheiten des Blutbildes bei Trisomie 21 Prim. Univ.-Prof. Dr. Milen Minkov Facharzt für Kinder- und Jugendheilkunde Pädiatrische Hämatologie und
Bluterkrankungen bei Menschen mit Down-Syndrom oder Besonderheiten des Blutbildes bei Trisomie 21 Prim. Univ.-Prof. Dr. Milen Minkov Facharzt für Kinder- und Jugendheilkunde Pädiatrische Hämatologie und
Informationen zum Thema Elektronische Patientenakte (EPA)
 Gesundheitskarte AKTUELL Informationen zum Thema Elektronische Patientenakte (EPA) Röntgenbilder, Ultraschallaufnahmen, Laborbefunde, Untersuchungsberichte alles über eine Karte? Was heute noch häufig
Gesundheitskarte AKTUELL Informationen zum Thema Elektronische Patientenakte (EPA) Röntgenbilder, Ultraschallaufnahmen, Laborbefunde, Untersuchungsberichte alles über eine Karte? Was heute noch häufig
Antikoagulantien. Dieser Patient wird behandelt mit. Präparat: Straße und Hausnr.: Wohnort:
 Dieser Patient wird behandelt mit Antikoagulantien Präparat: Name: Straße und Hausnr.: Wohnort: Vorname: Mit Hinweisen und Dokumentationsmöglichkeit zur Überbrückungstherapie Stempel bzw. Anschrift des
Dieser Patient wird behandelt mit Antikoagulantien Präparat: Name: Straße und Hausnr.: Wohnort: Vorname: Mit Hinweisen und Dokumentationsmöglichkeit zur Überbrückungstherapie Stempel bzw. Anschrift des
Epilation oder Dauerhafte Haarentfernung mit IPL Laser
 DR. RICHARD NAGELSCHMITZ FACHARZT FÜR HALS-NASEN-OHRENHEILKUNDE ÄSTHETISCHE MEDIZIN Epilation oder Dauerhafte Haarentfernung mit IPL Laser Mit dieser Aufklärung möchte ich Sie vorab über die modernen Möglichkeiten
DR. RICHARD NAGELSCHMITZ FACHARZT FÜR HALS-NASEN-OHRENHEILKUNDE ÄSTHETISCHE MEDIZIN Epilation oder Dauerhafte Haarentfernung mit IPL Laser Mit dieser Aufklärung möchte ich Sie vorab über die modernen Möglichkeiten
Bei den Leukämien handelt es sich um bösartige Erkrankungen des blutbildenden Systems,
 Leukämien Bei den Leukämien handelt es sich um bösartige Erkrankungen des blutbildenden Systems, im Volksmund ist deshalb gelegentlich auch vom Blutkrebs die Rede. Die Erkrankung nimmt ihren Ausgang im
Leukämien Bei den Leukämien handelt es sich um bösartige Erkrankungen des blutbildenden Systems, im Volksmund ist deshalb gelegentlich auch vom Blutkrebs die Rede. Die Erkrankung nimmt ihren Ausgang im
Versorgung HIV-Infizierter e.v. (dagnä) und dem Berufsverband niedergelassener Gastroenterologen Deutschlands e.v. (bng).
 Patienteninformationen zur Teilnahme an der Besonderen Versorgung zur Verbesserung der Versorgungsqualität von Patienten mit einer chronischen Die BARMER GEK hat mit der Kassenärztlichen Vereinigung Westfalen-Lippe
Patienteninformationen zur Teilnahme an der Besonderen Versorgung zur Verbesserung der Versorgungsqualität von Patienten mit einer chronischen Die BARMER GEK hat mit der Kassenärztlichen Vereinigung Westfalen-Lippe
Implantation eines ICD- oder CRT-Systems
 Implantation eines ICD- oder CRT-Systems Patient: Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist die Implantation eines ICD- (implantierbarer Kadioverter- Defibrillator) oder CRT-(cardiale
Implantation eines ICD- oder CRT-Systems Patient: Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist die Implantation eines ICD- (implantierbarer Kadioverter- Defibrillator) oder CRT-(cardiale
Wiederauftreten der Erkrankung
 Wiederauftreten der Erkrankung Dr. med. Elke Keil Park-Klinik Weißensee Wie merke ich überhaupt, daß der Tumor wieder da ist? Tumormarker? Alleiniger asymptomatischer Anstieg des Tumormarkers ist kein
Wiederauftreten der Erkrankung Dr. med. Elke Keil Park-Klinik Weißensee Wie merke ich überhaupt, daß der Tumor wieder da ist? Tumormarker? Alleiniger asymptomatischer Anstieg des Tumormarkers ist kein
Selbstverständlich haben Sie das Recht auf Zugang zu Ihren Daten bzw. die Korrektur nicht korrekter Daten.
 Informationsblatt zur Datenverarbeitung mit der DaLiD (Datenbank für Leistungssport) für Kaderathleten/-innen und talentierte Nachwuchssportler/-innen (Hinweis: Im weiteren Verlauf wird zur verbesserten
Informationsblatt zur Datenverarbeitung mit der DaLiD (Datenbank für Leistungssport) für Kaderathleten/-innen und talentierte Nachwuchssportler/-innen (Hinweis: Im weiteren Verlauf wird zur verbesserten
Christliche Patientenvorsorge
 Christliche Patientenvorsorge durch Vorsorgevollmacht, Betreuungsverfügung, Behandlungswünsche und Patientenverfügung Formular der Deutschen Bischofskonferenz und des Rates der Evangelischen Kirche in
Christliche Patientenvorsorge durch Vorsorgevollmacht, Betreuungsverfügung, Behandlungswünsche und Patientenverfügung Formular der Deutschen Bischofskonferenz und des Rates der Evangelischen Kirche in
ELTERNINFORMATION Beobachtungsstudie bei Patienten mit T-Zell Immundefekt (profound combined immunodeficiency : P-CID) Studienkurztitel: P-CID
 Platzhalter Patientenetikett Stempel oder Briefkopf der Abteilung Sehr geehrte Eltern, ELTERNINFORMATION Beobachtungsstudie bei Patienten mit T-Zell Immundefekt (profound combined immunodeficiency : P-CID)
Platzhalter Patientenetikett Stempel oder Briefkopf der Abteilung Sehr geehrte Eltern, ELTERNINFORMATION Beobachtungsstudie bei Patienten mit T-Zell Immundefekt (profound combined immunodeficiency : P-CID)
Das Österreichische Stammzellregister und seine Aufgaben:
 1 Österreichische Knochenmarkspendezentrale FONDS ÖSTERREICHISCHES STAMZELLREGISTER Florianigasse 38/12 A - 1080 Wien, Austria, Europe Tel.: +43-1 403 71 93 Fax.: +43-1 408 23 21 DVR.Nr.: 5111415 Das Österreichische
1 Österreichische Knochenmarkspendezentrale FONDS ÖSTERREICHISCHES STAMZELLREGISTER Florianigasse 38/12 A - 1080 Wien, Austria, Europe Tel.: +43-1 403 71 93 Fax.: +43-1 408 23 21 DVR.Nr.: 5111415 Das Österreichische
Informationen zu Ihrer Behandlung in der Tagesklinik
 Informationen zu Ihrer Behandlung in der Tagesklinik Liebe Patientin, lieber Patient, bei Ihnen soll eine ambulante Therapie durchgeführt werden. Mit dieser Broschüre teilen wir Ihnen einige Hinweise zu
Informationen zu Ihrer Behandlung in der Tagesklinik Liebe Patientin, lieber Patient, bei Ihnen soll eine ambulante Therapie durchgeführt werden. Mit dieser Broschüre teilen wir Ihnen einige Hinweise zu
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Aciclovir Genericon 400 mg Tabletten. Wirkstoff: Aciclovir
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Aciclovir Genericon 400 mg Tabletten Wirkstoff: Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Aciclovir Genericon 400 mg Tabletten Wirkstoff: Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Universität Ulm Medizinische Fakultät
 , Anhang F Universität Ulm Medizinische Fakultät Universitätsklinikum Zentrum für Innere Medizin, D-89070 Ulm Klinik für Innere Medizin III Hämatologie, Onkologie, Rheumatologie und Infektionskrankheiten
, Anhang F Universität Ulm Medizinische Fakultät Universitätsklinikum Zentrum für Innere Medizin, D-89070 Ulm Klinik für Innere Medizin III Hämatologie, Onkologie, Rheumatologie und Infektionskrankheiten
OFT SCHLAPP, MÜDE, DEPRIMIERT? Eisenmangel weit verbreitet und vielfach unterschätzt
 OFT SCHLAPP, MÜDE, DEPRIMIERT? Eisenmangel weit verbreitet und vielfach unterschätzt Liebe Patientin, lieber Patient! Fühlen Sie sich häufig schlapp, müde, erschöpft, deprimiert? Frieren Sie leicht? Neigen
OFT SCHLAPP, MÜDE, DEPRIMIERT? Eisenmangel weit verbreitet und vielfach unterschätzt Liebe Patientin, lieber Patient! Fühlen Sie sich häufig schlapp, müde, erschöpft, deprimiert? Frieren Sie leicht? Neigen
HÄMOLYTISCH-URÄMISCHES SYNDROM (HUS)
 HÄMOLYTISCH-URÄMISCHES SYNDROM (HUS) DEFINITION eine Erkrankung der kleinen Blutgefäße, der Blutzellen und der Nieren seltene Krankheit, die vorwiegend bei Säuglingen, Kleinkindern (zwischen einem und
HÄMOLYTISCH-URÄMISCHES SYNDROM (HUS) DEFINITION eine Erkrankung der kleinen Blutgefäße, der Blutzellen und der Nieren seltene Krankheit, die vorwiegend bei Säuglingen, Kleinkindern (zwischen einem und
Ich werde als Spender gebraucht
 MB Ich werde als Spender gebraucht Informationen für Knochenmarkspender oder Spender von Blutvorläuferzellen (= Blutstammzellen), die möglicherweise bald spenden werden Das internationale Computersystem
MB Ich werde als Spender gebraucht Informationen für Knochenmarkspender oder Spender von Blutvorläuferzellen (= Blutstammzellen), die möglicherweise bald spenden werden Das internationale Computersystem
Hinweise für den Hospizdienst zur Einhaltung der datenschutzrechtlichen Bestimmungen Überarbeitung April 2011
 ServicePoints Hospiz in Baden-Württemberg Arbeitsgruppe Ambulante Hospizdienste im Ministerium für Arbeit und Sozialordnung, Familien und Senioren Baden-Württemberg Hinweise für den Hospizdienst zur Einhaltung
ServicePoints Hospiz in Baden-Württemberg Arbeitsgruppe Ambulante Hospizdienste im Ministerium für Arbeit und Sozialordnung, Familien und Senioren Baden-Württemberg Hinweise für den Hospizdienst zur Einhaltung
EURAP EUROPÄISCHES REGISTER FÜR SCHWANGERSCHAFTEN UNTER ANTIEPILEPTIKA
 EURAP EUROPÄISCHES REGISTER FÜR SCHWANGERSCHAFTEN UNTER ANTIEPILEPTIKA Aufruf zur Teilnahme an der Studie zur Pharmakokinetik in der Schwangerschaft und Stillzeit Studie zur Pharmakokinetik in Schwangerschaft
EURAP EUROPÄISCHES REGISTER FÜR SCHWANGERSCHAFTEN UNTER ANTIEPILEPTIKA Aufruf zur Teilnahme an der Studie zur Pharmakokinetik in der Schwangerschaft und Stillzeit Studie zur Pharmakokinetik in Schwangerschaft
