Versuchsprotokoll Klonierung eines amplifizierten PCR-Fragments. 0 Inhaltsverzeichnis
|
|
|
- Miriam Dressler
- vor 6 Jahren
- Abrufe
Transkript
1 0 Inhaltsverzeichnis 0 Inhaltsverzeichnis Einleitung Versuch Versuchsteil (PCR und Gel der cdna) Einleitung Durchführung Auswertung Versuchsteil (Gel des Plasmids) Einleitung Durchführung Auswertung Versuchsteil und (Extraktion aus Gel und Gel der Restriktion) Einleitung Durchführung Auswertung Versuchsteil und (Hi-Bind Säule, Konzentrationsverhältnis) Einleitung Durchführung Auswertung Versuchsteil (Ligation) Einleitung Durchführung Auswertung Versuchsteil , , und (Herstellung der Bakterienkolonien) Einführung Durchführung Auswertung Versuchsteil (PCR der weißen Kolonien) Einleitung Durchführung Auswertung Versuchsteil , , (DNA-Minipräps, Konzentration d. Plasmid) Einleitung Durchführung Auswertung Versuchsteil (Analytisches Gel Minipräp) Einleitung Durchführung Auswertung Versuchsteil (Restriktion der weißen Kolonie) Einleitung Durchführung Auswertung Versuchsteil (Orientierungsbestimmung durch PCR) Einleitung Durchführung Auswertung Diskussion Seite von 16
2 1 Einleitung Ziel des vorliegenden Versuchs ist es, eine amplifizierte cdna-sequenz in kompetente Zellen zu klonieren. Die Vorgehensweise sei nun nachfolgend kurz skizziert: Eine gp80 cdna-sequenz wird durch eine PCR amplifiziert, an ihren Schnittstellen durch das Restriktionsenzym Pst I geschnitten und dann in das Plasmid puc19 einkloniert. Das Plasmid mit Insert wird dann in zuvor kompetent gemachte Zellen (E. coli xl1blue) transformiert und somit kloniert. Durch eine nachfolgende Lyse der Zellen wird das neue Plasmid aufgereinigt und die Orientierung des Inserts festgestellt. Im nun folgenden Kapitel Versuch ist die detaillierte Vorgehensweise aufgezeigt und die daraus resultierenden Teilschritte mit Ergebnissen und Diskussionen dargestellt. 2 Versuch 2.1 Versuchsteil (PCR und Gel der cdna) Einleitung In diesem Versuchsteil wird die cdna vervielfältigt (amplifiziert) und dann auf ein Gel aufgetragen, um ihre Existenz zu beweisen und die Reinheit zu gewährleisten. Ob es sich um das gesuchte DNA-Stück handelt, kann man an der Größe feststellen, die man anhand des aufgetragenen Standarts VII ungefähr abschätzen kann Durchführung Die Durchführung des Versuchsteils wird wie im Skript Seite vorgenommen. Pipettieransatz: 25µl Hot Start Mix (dntps, Puffer, Taq-Polymerase, Magnesium) 2µl Clus-Hund-F (Forward-Primer) 2µl Clus-Hund-R2 (Reverse-Primer bei 1125bp bis 1138bp) 2µl cdna (20ng) 19µl Wasser 50µl Endvolumen Zum Auftragen des PCR-Produkts werden 5µl PCR-Produkt 5µl Wasser 2µl Autragspuffer 6fach (im Folgenden immer nur AP genannt) aufgetragen. Seite von 16
3 2.1.3 Auswertung Das amplifzierte DNA-Stück ist 785bp lang. Beim nachfolgenden Gelbild sind der Standart VII und der Standart XIV in Geltasche 6 bzw. 13 aufgetragen. Abb. 1: Gel v. PCR der cdna In der Spur 1 ist keine Bande zu erkennen. Dort hat die PCR der cdna nicht funktioniert. Auf Spur 5 ist die Bande nicht so kräftig wie bei den anderen Banden. Hier wurde eine geringere Menge PCR-Produkt aufgetragen. Ist weniger DNA aufgetragen, kann sich auch weniger Ethidiumbromid in die Furchen der DNA einlagern. Somit ist auch die Strahlung unter der UV-Lampe geringer. Die unterschiedlichen Höhen der restlichen Banden sind auf die Benutzung der 2 verschiedenen Reverse-Primer bei der PCR zurückzuführen. Bei Benutztung des Clus-Hund R ist das DNA-Fragment einige Basenpaare kleiner und läuft aus physikalischen Gründen weiter als das größere DNA-Fragment, was durch die Benutzung des Clus-Hund R2 entstanden ist. Vergleicht man die Proben mit den zwei Standarts und mit der berechneten Basenlänge, so kann man sagen, dass es sich hier wirklich um das gewollte DNA-Stück handelt. 2.2 Versuchsteil (Gel des Plasmids) Einleitung In Versuchsteil wird auf das Gel die Restriktionslösung des Plasmids (Vektors) aufgetragen. Auch dieser Schritt dient dazu eine Verunreinigung mit nicht verdautem Vektor zu vermeiden Durchführung Die Durchführung wird, wie im Skript auf Seite 90 beschrieben, vorgenommen. 10µl Restriktionsansatz (verdauter Vektor) Seite von 16
4 2µl AP (6-fach) 12µl Endvolumen Auswertung Abb. 2: Gel des restringierten Vektors Auf dem Gelbild kann man auf der Spur 7 den Standart VII erkennen. Die Spur 1 wurde freigelassen. Alle anderen Banden sind gleich weit gelaufen. Vergleicht man nun die Banden mit dem Standart VII, kann man feststellen, daß die Größe des Vektors, welche man anhand des Gels ablesen kann, mit der bekannten Größe von 2,69kb übereinstimmt. Es handelt sich somit, um den gewollten Vektor. Bei Bande 6 wurde ein ungeschnittenes Plasmid zur Kontrolle aufgetragen. Die Konzentration war jedoch zu gering gewählt, dass man die Bande nicht sehen kann. 2.3 Versuchsteil und (Extraktion aus Gel und Gel der Restriktion) Einleitung Die in den vorherigen Versuchsteilen durchgeführten Gel-Elektrophoresen haben für die Aufreinigung des DNA-Fragment und des Vektors (Plasmids) gedient. Die so aufgereinigten Substanzen müssen nun aus dem Gel ausgelöst werden, um miteinander legiert werden zu können. Das Herauslösen des Inserts und des Plasmids erfolgen durch die sogenannte HiBind-Säule. Nun erfolgt unter Versuchsteil die Restriktion des DNA-Fragments an den Schnittstellen PstI. Nach der Restriktion wird unter Versuchsteil eine erneute Gelelektrophorese durchgeführt, um das geschnittene DNA-Fragement (ab nun als Insert bezeichnet) von dem ungeschnittenen DNA-Fragmenten zu trennen. Seite von 16
5 2.3.2 Durchführung Zur Entfernung der Agarose wird ein Bindepuffer hinzugegeben. Die Menge des Bindepuffers wird über das Gewicht des herausgeschnittenen Gelstücks bestimmt. Das Gelstück wiegt 119,8mg. Somit muss 100mg = 400µl 120mg = 480µl hinzugegeben werden. Für den Restriktionsansatz ist folgendes Pipettierschema angewendet worden: 26µl DNA-Fragment 5µl Puffer H (10-fach) 18µl Wasser 1µl Restriktionsenzym PstI 50µl Endvolumen Die erneute Gelelektrophorese wird mit dem geschnittenen Insert, dem Standart XIV und den ungeschnittenen DNA-Fragmenten (Fragment mit Reverse-Primer R und Reverse-Primer R2) durchgeführt. Die restlichen Schritte können im Skript auf den Seiten nachvollzogen werden Auswertung Das nachfolgende Gel enthält bei Bande 4 das ungeschnittenen DNA-Fragment Reverse- Primer R, bei Bande 5 den Standart XIV, bei Bande 6 das ungeschnittene DNA-Fragment Reverse-Primer R2 und bei Bande 1 meine Probe. Abb. 3: Gel des geschnittenen Inserts Nur bei den Spuren 1 und 3 ist ein klarer Unterschied zwischen ungeschnittenem DNA- Fragment und dem Insert zu erkennen. Die unterschiedlichen Höhen der beiden oberen Seite von 16
6 Banden von Spur 1 und 3 kommen durch den unterschiedlichen PCR-Primer zustande (siehe Versuchsteil ). Die beiden unteren Banden entsprechen dem geschnittenen Insert. Vergleicht man die Banden mit dem Standart kann man feststellen, dass auch die Größe auf das Vorhandensein des Insert spricht. Auf Spur 9 kann man keine Bande feststellen. Hier hat die PCR der DNA erst gar nicht funktioniert. (Hier sei vermerkt, dass auch das PCR-Gel keine Bande gezeigt hat.) 2.4 Versuchsteil und (Hi-Bind Säule, Konzentrationsverhältnis) Einleitung Auch hier wird das geschnittene Insert per HiBind-Säule aus dem Gel extrahiert. Bei Versuchsteil wird eine Gelelektrophorese gemacht, um das Konzentrationsverhältnis zwischen Insert und Vektor zu bestimmen, damit man für die Ligation die geeigneten Stoffmengen einsetzen kann. ( ) Durchführung Die Extraktion wird wie unter 2.4. durchgeführt. Anleitung bitte Skript Seite 93 entnehmen. Das nun extrahierte und geschnittene Insert wird zusammen mit dem Vektor zur Konzentrationsbestimmung in gleicher Menge nebeneinander auf das Gel aufgetragen. Pipettierschema: 3µl Vektor bzw. Insert 7µl Wasser 2µl AP (6-fach) 12µl Endvolumen Auswertung Das nachfolgende Gel zeigt das Ergebnis: 2 1 Abb. 4: Gel zur Bestimmung des Konzentrationsverhältnisses zwischen Insert und Vektor Seite von 16
7 Die Helligkeit der Banden zeigt die Konzentration an. Allerdings ist dabei zu berücksichtigen, dass der Vektor ungefähr 4mal so groß ist wie das Insert. Somit entspricht die gleiche Helligkeit der beiden Banden einem Konzentrationsunterschied von 4:1 (Insert : Vektor). Da man bei der Ligation jedoch genau dieses Verhältnis einsetzen soll, ist eine gleiche Helligkeit arbeitserleichternd. Betrachtet man das Gel so kann man bei Spur 9 und 10 (Pfeil 1 und 2) genau die gleiche Helligkeit feststellen. Die Spur 9 entspricht dem Insert, die Spur 10 dem Vektor. Die ungefähren Größen, die man am Standart XIV ablesen kann, entsprechen den bekannten bzw. errechneten Größen des Inserts bzw. des Vektors. Somit ist die Stoffmenge für die Ligation bestimmt. Nachfolgende Rechnung macht dies noch einmal deutlich: Vektor (ca. 2,69kb) und Insert (ca. 650bp) gleiche Helligkeit der Banden. Konzentration bei der Ligation soll wenigstens im Bezug auf das Insert 3-fach sein. Vektor ist ca. 4mal so groß. Also nimmt man die gleiche Menge und hat somit ein Verhältnis von ca. 4: Versuchsteil (Ligation) Einleitung Bei der nachfolgenden Ligation werden Insert und Vektor vereinigt. Dies kann nur deswegen geschehen, weil beide mit dem gleichen Restriktionsenzym PstI geschnitten wurden. Somit besitzen sie die gleichen sticky ends (überhängende Enden, die die Ligation vereinfachen) und werden somit ligiert Durchführung Die Durchführung wird wie im Skript auf Seite 95 durchgeführt. Das Pipettierschema sieht wie folgt aus: 10µl Plasmid 10µl Insert 2,3µl Ligationspuffer (10-fach) 1µl Ligase 23,3µl Endvolumen Auswertung 1bp entspricht 660g/mol Seite von 16
8 642bp * 660g/mol = g/mol 2690bp *660g/mol = g/mol Die Größe des Vektors ist ca. 4mal so groß. Versuchsprotokoll Insertlänge = 642bp, Vektorlänge = 2690bp = 3332bp (Länge des puc19 mit Insert) 2.6 Versuchsteil , , und (Herstellung der Bakterienkolonien) Einführung Die Bakterien E.coli xl1blue wurden über Nacht in Overnight-Röhrchen in LB-Medium vermehrt. Aus diesem entstandenen Medium wird dann 1ml entnommen und in einem neuen LB-Medium gezüchtet, bis der OD 600 -Wert zwischen 0,5 und 0,7 liegt. Bei diesen Werten ist die Bakterienkultur im besten logarithmischen Wachsen und am geeignesten für die Transformation ( ). Die Transformation des Vektors mit dem Insert in die Bakterienzelle erfolgt durch Calciumchlorid. Die Bakterien werden mit dem Ligationsansatz leicht gemischt und durch die entstandene Permeabilität der Membran durch das Calciumchlorid gelangt das Plasmid mit Insert in die Zellen. Zusätzlich wird auch eine Positivkontrolle durchgeführt. Die genaue Vorgehensweise findet man im Skript auf den Seiten 93, 94 und Durchführung Die Durchführung geschieht laut Skript Seite 93, 94 und 96. Bei Versuchsteil werden 2mal 100µl in CaCl 2 aufgenommen und in ein Greinerröhrchen überführt. Im Versuchsteil wird folgendermaßen vorgegangen: Von der Bakterienkultur mit dem OD 600 -Wert von 0,5 bis 0,7 werden 2mal 1,5ml in Eppis gegeben und bei 4000rpm 2 Minuten zentrifugiert. Das Pellet entspricht den Bakterien mit dem neuen Plasmid. Von dem Ligationsansatz werden 100µl ausplattiert, von der Positivkontrolle (Nummer 3) 90µl und von einer 1:10 verdünnten Positivkontrolle ebenfalls 100µl auf eine Agarplatte mit LB- Medium und Ampicillin ausplattiert Auswertung Ligationansatz: Positivkontrolle: Positivkontrolle (verdünnt): Religation: gewachsen (blaue und weiße Kolonien) nicht gewachsen nicht gewachsen gewachsen Seite von 16
9 Übersicht der gesamten Versuchsgruppe: Was? Gewachsen Nicht gewachsen Religation 3 0 Ligation 7 1 Positivkontrolle Nummer Positivkontrolle Nummer Positivkontrolle Nummer Dass die Kontrollen nicht bzw. nur schlecht gewachsen sind, kann nur auf das nicht Vorhandensein eines Plasmids und somit einer Ampicillinresistenz beruhen. Dies erklärt auch das Wachsen des Ligationsansatzes und der Religation, die beide diese Resistenz besitzen. Warum weisen manche Kolonien eine blaue bzw. keine Färbung auf? Wurde bei der Ligation nur eine Religation vollzogen, also kein Insert eingebaut, so ist das lacz- Gen intakt. Dieses kodiert für die ß-Galactosidase, die das auf den Platten aufgetragene X-Gal enzymatisch abbaut. Das Abbauprodukt erscheint dann blau. Wurde hingegen ein Insert eingebaut, ist das lacz-gen nicht mehr aktiv, da es vom Insert unterbrochen wird. Ein Abbau des X-Gal ist nicht möglich. Diese Kolonien verbleiben weiß. Die Funktion des zusätzlich aufgetragenen IPPD ist die Blockierung des Repressors des lacz-gens. Kann der Repressor nicht am Operator andocken, ist eine Bildung von ß-Galactosidase erst möglich. 2.7 Versuchsteil (PCR der weißen Kolonien) Einleitung Dieser Schritt dient der Kontrolle! Hier entscheidet sich erstmals, ob die weiße Kolonie wirklich ein Plasmid mit Insert trägt. Da diese PCR der weißen Bakterienkolonie allerdings nicht als besonders sicher gilt, werden im Versuchsteil die gleichen Kolonien für die Animpfung von Minipräps genutzt, um das Ergebnis zusätzlich abzusichern Durchführung Die Durchführung wird laut Skript Seite 97 durchgeführt. Änderung des Pipettieransatzes: Seite von 16
10 12,5µl Hot start Mix 10,5µl Wasser mit Bakterien 1µl Reverse Primer 1µl Universal Primer 25µl Endvolumen Versuchsprotokoll Auswertung Theoretisch ist das Amplifikat dieser PCR ca. 746bp groß. Auf die Zahl kommt zustande, wenn man das Insert zwischen den beiden Pst I- Schnittstellen berechnet (ca. 642bp) und das Stück Plasmid zwischen dem Reverse- und Forward- Primer-Praktikum hinzurechnet (104bp). Ist das Insert nicht vorhanden, ist das Amplifikat nur 104bp groß. Abb. 5: PCR der weißen Bakterienkolonie Dies kann man eindeutig an den Spuren 8 und 9 erkennen. Die Spur 9 ist die Positivkontrolle, die das Insert scheinbar gar nicht trägt. Dies lässt sich auch später anhand den Minipräps aufzeigen ( ). Die Spur 8 entspricht der Selbstligation, die hier eindeutig das Insert trägt (Vergleich mit Standart XIV). Meine PCR (Spur 3 bzw. 4)der Selbstligation sowie Positivkontrolle hat nicht funktioniert. Mögliche Gründe sind: 1) Die PCR hat nicht funktioniert. 2) Es wurde eine blaue Bakterienkultur gepickt. Dafür spricht, dass andere Praktikanten andere vermeintlich weiße Kolonien von mir gepickt haben, deren PCR funktioniert hat. Trotzdem kann man auch bei 104bp keine Bande erkennen. Dies kann man sich vielleicht bei der Betrachtung des Gels erklären, da hier vielleicht die 104bp-große Bande schon aus dem Gel gelaufen ist. 2.8 Versuchsteil , , (DNA-Minipräps, Konzentration d. Plasmid) Einleitung Um zu überprüfen, ob die Klonierung funktioniert hat, wird eine weiße Kolonie über Nacht vermehrt ( ). Am nächsten Tag erfolgt dann die DNA-Minipräparation, bei der der vermehrte Plasmid präpariert wird. Dies erfolgt durch eine alkalische Lyse der Bakterienzelle ( ). Seite von 16
11 In dem Versuchsteil wird dann die Optische Dichte des Plasmids zur Konzentrationsbestimmung gemessen, um eine Aussage über die Reinheit des Plasmids zu machen. Dabei wird einmal bei 260nm (DNA) und bei 280nm (Proteine) gemessen und der Quotient gebildet. Dieser sollte ca. 1,7 betragen Durchführung Die Durchführung erfolgt laut Skript Seiten 98 und 99. Änderung bei : Das Pellet wird im vorletzten Schritt in 100µl Wasser aufgenommen und es werden nur 20µl für die Konzentrationsbestimmung eingesetzt Auswertung Gemessene Extinktion: Positivkontrolle Ligationsansatz DNA bei 260nm 0,484 0,325 Proteine bei 280nm 0,278 0,173 Beispiel der Berechnung der Konzentration: 1,0 OD = 50µg/ml 0,1 OD = 5µg/ml Wir haben aber nur 20µl, deswegen: 5µg = 20µl xµg = 1µl x = 5/20 c = 0,25 µg/µl für 1 OD ist c = 2,5µg/µl. Es werden nur die Konzentrationen der Positivkontrolle und des Ligationsansatzes der DNA bestimmt. Positivkontrolle: Ligationsansatz: c = 0,484 * 2,5µg/µl =1,21 µg/µl c = 0,325 * 2,5 µg/µl = 0,8125µg/µl Es sollen im Versuchsteil jedoch 2µg DNA eingesetzt werden, deswegen: Positivkontrolle: Ligationsansatz: 2µg = xµl 2µg = xµl 1,21µg = 1µl 0,8125µg = 1µl x = 1,7µl x = 2,5µl Berechnung des OD-Quotienten: OD-Quotient = 0,484 / 0,278 = 1,74 für die Positivkontrolle OD-Quotient = 0,325 / 0,173 = 1,87 für den Ligationsansatz Seite von 16
12 2.9 Versuchsteil (Analytisches Gel Minipräp) Einleitung Die oben berechnete Menge DNA wird auf dem Gel aufgetragen und somit erneut geprüft, ob das Insert einkloniert wurde Durchführung Die Proben für das Gel wurden folgendermaßen angesetzt: Positivkontrolle: Ligationsansatz: 1,7µl DNA 2,5µl DNA 8,3µl Wasser 7,5µl Wasser 2µl AP (6-fach) 2µl AP (6-fach) 12µl Endvolumen 12µl Endvolumen Auswertung Abb. 6: PCR Minipräp (keine bp angegeben, da kein Standart aufgetragen wurde) Auch hier ist bei dem Ligationsansatz und der Positivkontrolle (Spur 3 bzw. 4) keine Bande zu erkennen. Erklärung siehe Ein weiterer Grund könnte sein, dass sich die Zellen nach das Plasmid nach der Aufreinigung nicht richtig gelöst hat. Ein Beweis bleibt aus. Auf Spur 8 ist die Kontrolle aufgetragen. Betrachtet man Spur 5 (eigene Ligation) und Spur 6 (Positivkontrolle) so stellt man fest, dass die eigene Ligation das Insert beinhaltet. Die Positivkontrolle dagegen ist negativ. Diese Aussage passt zu der Aussage, die unter 2.8. getroffen wurde. Die dicken Banden entsprechen der supercoild (s.c.) Form des Plasmids, die durch ihre Komprimierung am weitesten wandert. Die darüberliegenden Banden sind nicked circled (n.c.) Form. Die lineare Form kann man hier nicht erkennen. Die Banden, die sich auf der Höhe der Geltaschen befinden, können der genomischen DNA entsprechen. Am unteren Rand des Gels kann man die RNA-Bande erkennen. Seite von 16
13 2.10 Versuchsteil (Restriktion der weißen Kolonie) Einleitung Die Restriktion der weißen Kolonie dient der Orientierungsbestimmung. Ab diesem Versuchsteil habe ich die Selbstligation von Karoline eingesetzt Durchführung Durchführung siehe Skript Seite 100. Pipettierschema des Restriktionsansatzes: 8,5µl DNA des Klons 5µl 10-fach Puffer PvuII 35,5µl Wasser 1µl PvuII-Enzym 50µl Endvolumen Danach Auftragung auf Gel mit 2µl AP (6-fach) mit 10 µl verdauter DNA Auswertung Meine Bande Abb. 7: Restriktion der weißen Kolonie Auf Spur 5 befindet sich meine Bande. Sie ist ca. 2,6kb groß. Dies entspricht dem geschnittenen Plasmid. Das herausgeschnitten Insert (plus einige Basen des Plasmids bis zur Schnittstelle PvuII) ist auf dem Gel nicht mehr zu sehen. Es ist aus dem Gel herausgelaufen. Somit ist die Bestimmung der Orientierung anhand dieses Gels nicht möglich. Seite von 16
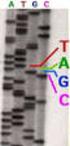
14 Insert Abb. 8: Skizze des puc 19 mit Insert und der möglichen Schnittstellen des PvuII-Restriktionsenzyms Wenn PvuII auf dem Plasmid schneidet, entsteht die bei der Abb. 7 aufgezeigte Bande. Über die Größe der kleinen Stücke könnte man die Orientierung herausfinden 2.11 Versuchsteil (Orientierungsbestimmung durch PCR) Einleitung Durch die PCR mit unterschiedlichen Primern auf dem Plasmid und dem Insert kann hiermit eine Orientierungsbestimmung gemacht werden Durchführung Die Durchführung erfolgt wie im Skript auf Seite 101 beschrieben. Pipettierschemata: PCR 1 PCR 2 PCR 3 (nochmalige Kontrolle meiner Pos.-Kontrolle) 1µl DNA 1µl DNA 5µl DNA 1µl KB3-Primer 1µl KB3-Primer 1µl Universal-Primer 1µl Reverse-Primer 1µl Forward-Primer 1µl Reverse-Primer 9,5µl Wasser 9,5µl Wasser 5,5µl Wasser 12,5µl Hot Start Mix 12,5µl Hot Start Mix 12,5µl Wasser 25µl Endvolumen 25µl Endvolumen 25µl Endvolumen Auswertung Abb. 9: PCR des Minipräps Auf der Spur 7 befindet sich der Standart XIV. Die Banden auf den Spuren 2, 6, 9, 11 und 12 sind alle gleich weit gelaufen. Es handelt sich hier der Größe nach um unser Plasmid (ca. 1000bp). Seite von 16
15 Bei den Spuren 2, 3 und 4 handelt es sich um meine Proben. Auf Spur 4 wurde noch einmal die Positivkontrolle der vorherigen Versuchsteile aufgetragen. Auch dieses Mal ist keine Bande zu erkennen. Erklärung siehe Auf Spur 2 handelt es sich um die PCR 1 (siehe Durchführung), bei Spur 3 um die PCR 2. Das Ergebnis ist somit eindeutig. Das Insert wurde richtigrum eingebaut! Die Zeichnungen werden dies erklären. Abb. 10: Orientierungseinschätzung durch Primerzugabe Das Ablesen der DNA-Stränge erfolgt immer vom 5 -Ende zum 3 -Ende. Bei der PCR sind 2 Primer notwendig. Der eine ist zum Ablesen des Sense-Stranges, der andere zum Ablesen des Antisense-Stranges verantwortlich. Gibt man zu der PCR Reverse-Primer (PRR) und KB3-Primer hinzu (PCR1), funktioniert die DNA (siehe Abbildung B, schwarze Pfeile), wenn das Insert richtigrum eingebaut wurde. Falls es falschrum eingebaut wurde, funktioniert die PCR mit diesen 2 Primern nicht (Abbildung C, roter Pfeil)! Dreht man diese Tatsache um, so erklärt sich der Fall für die Anwendung des Forward-Primers (FPP). Somit wurde hier in Sense-Richtung einkloniert. Seite von 16
16 Abb. 11: Plasmid-Orientierungsschema 3 Diskussion Zusammenfassend kann man nun feststellen, dass der Versuch funktioniert hat und somit zu einem akzeptablen Ergebnis geführt hat. Wenn ich nun den eigenen Versuchsansatz betrachte, kann man mit dem Ergebnis wohl nur halb zufrieden sein. Haben die Aufreinigung des Plasmids sowie des Inserts perfekt funktioniert, ist der Transformationsschritt absolut missglückt. Allerdings muss man auch bedenken, dass jeder nur eine einzige Probe angesetzt hat, was in einem natürlichen Laborumfeld nicht üblich ist. Nimmt man alle FI-Praktikanten zusammen, ist wohl eine normale prozentuale Erfolgschance am Ende herausgekommen. Seite von 16
Molekulare Klonierung Praktikum
 Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
Molekulare Klonierung Praktikum 2013 Praktikumsaufgabe Ligation 1. Zusammensetzung des Ligationsreaktions-ansatzes : 1 l Vektor DNA 1 l Insert DNA 2 l 10X Ligase Puffer 15 l destillertes Wasser 1 l Ligase
AUFGABENSAMMLUNG. Restriktionsenzyme. Füllen Sie den Lückentext aus. Gentechnik Schroedel, Braunschweig
 Restriktionsenzyme Füllen Sie den Lückentext aus. PCR 1a Mit dem folgenden Quiz können Sie Ihr Wissen zum Thema PCR überprüfen. Klicken Sie jeweils die richtige Antwort an. PCR 1b Mit dem folgenden Quiz
Restriktionsenzyme Füllen Sie den Lückentext aus. PCR 1a Mit dem folgenden Quiz können Sie Ihr Wissen zum Thema PCR überprüfen. Klicken Sie jeweils die richtige Antwort an. PCR 1b Mit dem folgenden Quiz
Zellbiologie und Physiologie Labormethoden der Biologie
 Zellbiologie und Physiologie Labormethoden der Biologie Molekularbiologie I Dr. Stefan Weinl > Molekularbiologie I Plasmidpräparation Transformation Restriktionsverdau Gel-Elektrophorese 1 > Experimenteller
Zellbiologie und Physiologie Labormethoden der Biologie Molekularbiologie I Dr. Stefan Weinl > Molekularbiologie I Plasmidpräparation Transformation Restriktionsverdau Gel-Elektrophorese 1 > Experimenteller
Zellbiologie und Physiologie Labormethoden der Biologie
 Zellbiologie und Physiologie Labormethoden der Biologie > Molekularbiologie I Plasmidpräparation Molekularbiologie I Transformation Gel-Elektrophorese Dr. Stefan Weinl > Plasmid-Isolierung aus E. coli
Zellbiologie und Physiologie Labormethoden der Biologie > Molekularbiologie I Plasmidpräparation Molekularbiologie I Transformation Gel-Elektrophorese Dr. Stefan Weinl > Plasmid-Isolierung aus E. coli
Gentechnologie: Klonierung und Transformation von DNA
 Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
Grundpraktikum Genetik 8. Kurstag 16.06.2005 Gentechnologie: Klonierung und Transformation von DNA Lerninhalte: Transformation, natürliche Kompetenz, Transformationseffizienz, Vektor, Plasmid, Resistenzgen,
Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen
 F2-Praktikum Genetik Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen Gruppe 4 (Susanne Duncker, Kristin Hofmann) Einleitung Wir untersuchten in diesem Versuch die Effizienz der VDJ-Rekombination
F2-Praktikum Genetik Protokoll Versuch 1: VDJ-Rekombination in humanen prä-b-zellen Gruppe 4 (Susanne Duncker, Kristin Hofmann) Einleitung Wir untersuchten in diesem Versuch die Effizienz der VDJ-Rekombination
Protokoll Versuch A1 Klonierung des Tyro3-D1D2-Fragments mittels PCR
 Protokoll Versuch A1 Klonierung des Tyro3-D1D2-Fragments mittels PCR Gruppe 8 Susanne Duncker und Friedrich Hahn Einleitung und Aufgabenstellung Ziel dieses Versuchs ist es, das Gen für ein bestimmtes
Protokoll Versuch A1 Klonierung des Tyro3-D1D2-Fragments mittels PCR Gruppe 8 Susanne Duncker und Friedrich Hahn Einleitung und Aufgabenstellung Ziel dieses Versuchs ist es, das Gen für ein bestimmtes
3 ERGEBNISSE 3.1 PLASMIDKONSTRUKTIONEN UND -PRÄPARATIONEN
 ERGEBNISSE Die Zielsetzung dieser Arbeit ist es, ein in-vitro-modell zur Bestimmung der Zyto- und Genotoxizität zu konstruieren. Zur Entwicklung des Genotoxizitätsmodells wurde der Vektor pnf-κb/neo unter
ERGEBNISSE Die Zielsetzung dieser Arbeit ist es, ein in-vitro-modell zur Bestimmung der Zyto- und Genotoxizität zu konstruieren. Zur Entwicklung des Genotoxizitätsmodells wurde der Vektor pnf-κb/neo unter
1 µl BamHI H 2 O 21 µl H 2 O 30 µl Volumen 18 µl H 2 O 30 µl Inkubation 2h @ 37 C 2h @ 37 C
 F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
F1-Praktikum Genetik Protokoll Versuch 2: Nachweis der Funktion von Promotor- und Enhancer-Sequenzen mittels Reportergen-Assay Gruppe 8, Manfred Depner & Susanne Duncker Einführung Um die Funktion von
Versuch 8. Plasmid - Isolierung
 Versuch 8 Plasmid - Isolierung Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X C. Weindel & M. Schwarz Wird benotet?: Einleitung Ein Plasmid
Versuch 8 Plasmid - Isolierung Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X C. Weindel & M. Schwarz Wird benotet?: Einleitung Ein Plasmid
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Transformation des Expressionsstammes
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein Transformation des Expressionsstammes
Genetik Praktikumsklausur SS2005
 Genetik Praktikumsklausur SS2005 1. Aufgabe: Der Genotyp AbaB wird geselbstet, dabei werden 256 Nachkommen gebildet. Davon erhalten 16 Pflanzen den Genotyp ABAB a) gekoppelt b) nicht gekoppelt c) teilweise
Genetik Praktikumsklausur SS2005 1. Aufgabe: Der Genotyp AbaB wird geselbstet, dabei werden 256 Nachkommen gebildet. Davon erhalten 16 Pflanzen den Genotyp ABAB a) gekoppelt b) nicht gekoppelt c) teilweise
Antibiotika sind oft Inhibitoren der Genexpression
 Antibiotika sind oft Inhibitoren der Genexpression Inhibitoren der Transkription: Rifampicin, Actinomycin α-amanitin Inhibitoren der Translation: Puromycin, Streptomycin, Tetracycline, Chloramphenicol
Antibiotika sind oft Inhibitoren der Genexpression Inhibitoren der Transkription: Rifampicin, Actinomycin α-amanitin Inhibitoren der Translation: Puromycin, Streptomycin, Tetracycline, Chloramphenicol
Versuchsprotokoll: Chromatographie. Gelchromatographische Trennung eines Proteingemischs
 Versuchsprotokoll: Chromatographie Gelchromatographische Trennung eines Proteingemischs 1.1. Einleitung Das Ziel der Gelchromatographie ist es ein vorhandenes Proteingemisch in die einzelnen Proteine zu
Versuchsprotokoll: Chromatographie Gelchromatographische Trennung eines Proteingemischs 1.1. Einleitung Das Ziel der Gelchromatographie ist es ein vorhandenes Proteingemisch in die einzelnen Proteine zu
Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten
 Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten erstellt vom Unterausschuß Methodenentwicklung des LAG 1. Zweck und Anwendungsbereich
Methodensammlung des LAG PCR-Nachweis von gentechnisch veränderten Organismen, die von pbr322 abgeleitete Sequenzen enthalten erstellt vom Unterausschuß Methodenentwicklung des LAG 1. Zweck und Anwendungsbereich
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Monokotylen Vorbereitung auf diesen Praktikumsteil: Organisation - Für den Bioinformatik-Teil benötigen Sie pro Gruppe einen Laptop -
Kurstage 7 und 8: Klassische Experimente der Gentechnologie
 Kurstage 7 und 8: Klassische Experimente der Gentechnologie Liga;on von DNA (Tag 7) Transforma;on von Bakterien (Tag 7) Auswertung der Transforma;on (Tag 8) Isolierung und Analyse von rekombinanter Plasmid
Kurstage 7 und 8: Klassische Experimente der Gentechnologie Liga;on von DNA (Tag 7) Transforma;on von Bakterien (Tag 7) Auswertung der Transforma;on (Tag 8) Isolierung und Analyse von rekombinanter Plasmid
3 GFP green fluorescent protein
 SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
SCHNUPPERKURS GENTECHNIK 1 ExploHeidelberg 2 Klonierung des Phagen Lambda 3 GFP green fluorescent protein 4 Gens in a bottle Vanessa Hecht 1 ExploHeidelberg Stiftung Jugend und Wissenschaft GmbH Technologiepark
Restriktion und Gentechnik
 Restriktion und Gentechnik Einteilung 1.) Restriktion - Restriktionsenzyme - Southern Blotting 2.)Gentechnik - sticky ends - blunt ends Restriktion Grundwerkzeuge der Gentechnik - Restriktionsenzymanalyse
Restriktion und Gentechnik Einteilung 1.) Restriktion - Restriktionsenzyme - Southern Blotting 2.)Gentechnik - sticky ends - blunt ends Restriktion Grundwerkzeuge der Gentechnik - Restriktionsenzymanalyse
Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA
 Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
Aufbau eines Assays zur Optimierung einer Polymerase für die Generierung hochgradig fluoreszenz-markierter DNA Von der Naturwissenschaftlichen Fakultät der Technischen Universität Carolo-Wilhelmina zu
MODULE für den SCHULKOFFER GENTECHNIK
 MODULE für den SCHULKOFFER GENTECHNIK Modul 1 - DNA-Bastel-Set Zusammenbau eines Papiermodells in Form einer Doppelhelix sehr einfach, Unterstufe, ohne Koffer möglich Modul 2 - DNA-Isolierung aus Gemüse
MODULE für den SCHULKOFFER GENTECHNIK Modul 1 - DNA-Bastel-Set Zusammenbau eines Papiermodells in Form einer Doppelhelix sehr einfach, Unterstufe, ohne Koffer möglich Modul 2 - DNA-Isolierung aus Gemüse
Modifizierte Gene Editor Mutagenese
 Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
Modifizierte Gene Editor Mutagenese zur gleichzeitigen Einführung mehrerer Punktmutationen DNA Template Präparation: 2 µg Plasmid DNA (bei 6 kb, sonst entsprechend mehr oder weniger) + 2 µl 2M NaOH, 2
Ein interessanter und arbeitsreicher Tag im livfe Biolab in Darmstadt
 Ein interessanter und arbeitsreicher Tag im livfe Biolab in Darmstadt Als einer der ersten Kurse überhaupt durfte der Biologieleistungskurs der Alfred-Delp-Schule unter Kursleitung von Sven Remdisch das
Ein interessanter und arbeitsreicher Tag im livfe Biolab in Darmstadt Als einer der ersten Kurse überhaupt durfte der Biologieleistungskurs der Alfred-Delp-Schule unter Kursleitung von Sven Remdisch das
1 Einleitung... 13. 1.1 Staphylokokken... 13. 1.2 Koagulase-negative Staphylokokken... 13. 1.4 MSCRAMM-Proteine... 16. 1.5 LPXTG-Motive...
 Inhaltsverzeichnis 1 Einleitung... 13 1.1 Staphylokokken... 13 1.2 Koagulase-negative Staphylokokken... 13 1.3 Staphylococcus saprophyticus... 14 1.4 MSCRAMM-Proteine... 16 1.5 LPXTG-Motive... 16 1.6 Oberflächenassoziierte
Inhaltsverzeichnis 1 Einleitung... 13 1.1 Staphylokokken... 13 1.2 Koagulase-negative Staphylokokken... 13 1.3 Staphylococcus saprophyticus... 14 1.4 MSCRAMM-Proteine... 16 1.5 LPXTG-Motive... 16 1.6 Oberflächenassoziierte
Gentechnologie: Isolierung und Charakterisierung von DNA
 Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Genetisches Grundpraktikum 9. Kurstag 23.06.2005 Gentechnologie: Isolierung und Charakterisierung von DNA Lerninhalte: Klonierung, Plasmid, Polylinker ( multiple cloning site ), Restriktionsendonuklease,
Überproduktion der Taq DNA Polymerase mit rekombinanten E. coli Zellen
 Überproduktion der Taq DNA Polymerase mit rekombinanten E. coli Zellen Versuchsleiter: Bernhard Eikmanns Protokollführung: Karl Varadi Gruppe: 11 Durchführung: 11.11 15.11.2002 Protokoll testiert: WS02
Überproduktion der Taq DNA Polymerase mit rekombinanten E. coli Zellen Versuchsleiter: Bernhard Eikmanns Protokollführung: Karl Varadi Gruppe: 11 Durchführung: 11.11 15.11.2002 Protokoll testiert: WS02
6. Induktion der Galactosidase von Escherichia coli
 Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 19.1.2005 6. Induktion der Galactosidase
Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 19.1.2005 6. Induktion der Galactosidase
2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
 Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
Translation of lab protocols Transformation Protocol 1) Stellen Sie die kompetenten Zellen auf Eis 2) Mischen Sie daraufhin das Ligationsprodukt zusammen. Dazu werden 50 µl Zellen und 2 µl Plasmid zusammengegeben
Hochdurchsatz Generierung und Analyse von Arabidopsis thaliana-proteinen
 MAX-PLANCK-INSTITUT FÜR MOLEKULARE GENETIK Hochdurchsatz Generierung und Analyse von Arabidopsis thaliana-proteinen Dissertation zur Erlangung der Doktorwürde des Fachbereichs Biologie, Chemie, Pharmazie
MAX-PLANCK-INSTITUT FÜR MOLEKULARE GENETIK Hochdurchsatz Generierung und Analyse von Arabidopsis thaliana-proteinen Dissertation zur Erlangung der Doktorwürde des Fachbereichs Biologie, Chemie, Pharmazie
7 Prinzipien und Methoden der DNA-Klonierung
 7 Prinzipien und Methoden der DNA-Klonierung Das Klonieren von DNA-Molekülen seien es DNA-Fragmente, komplette Gene oder sogar das ganze Genom eines Organismus stellt im Grunde genommen den Kern gentechnischer
7 Prinzipien und Methoden der DNA-Klonierung Das Klonieren von DNA-Molekülen seien es DNA-Fragmente, komplette Gene oder sogar das ganze Genom eines Organismus stellt im Grunde genommen den Kern gentechnischer
Inhaltsverzeichnis. Polymerase Chain Reaction Theoretischer Hintergrund - 2 -
 Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Inhaltsverzeichnis 1 Theoretischer Hintergrund - 2-1.1 Die Komponenten der PCR - 2-1.2 Das Verfahren der PCR - 3-1.3 Die Gelelektrophorese - 5-2 Material und Methoden - 6-3 Ergebnisse - 7-3.1 Ergebnisse
Bachelorkurs Evolutionsbiologie II WS 2016/17 Woche 2, Experiment 1: Insertions/Deletions Polymorphismus in D.
 Experiment 1: Insertions/Deletions Polymorphismus in D. melanogaster Eine der häufigsten Formen von molekularer Variabilität sind Insertionen bzw. Deletionen (abgekürzt: InDels). D.h. dass unterschiedliche
Experiment 1: Insertions/Deletions Polymorphismus in D. melanogaster Eine der häufigsten Formen von molekularer Variabilität sind Insertionen bzw. Deletionen (abgekürzt: InDels). D.h. dass unterschiedliche
Plasmide, Vektoren und Klonierung
 Biologische Übungen IV, Kurstage 3, 4 Restriktionskartierung eines Plasmids, 27./28.05.2004 Protokollant: Bernhard Schnepf Gruppe A1: Dachs Sven Schnepf Bernhard Thumann Rauno Plasmide, Vektoren und Klonierung
Biologische Übungen IV, Kurstage 3, 4 Restriktionskartierung eines Plasmids, 27./28.05.2004 Protokollant: Bernhard Schnepf Gruppe A1: Dachs Sven Schnepf Bernhard Thumann Rauno Plasmide, Vektoren und Klonierung
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers FIGURE 20.1 Biology 6/e Biotechnologie Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016
 Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 7 (11.07-15.07.) Methoden und Techniken II 1. Sie bekommen
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 7 (11.07-15.07.) Methoden und Techniken II 1. Sie bekommen
Grundlagen der Klonierung. Analytische Methoden der Biologie SS09 7 Klonierung und Gentechnik. Modul
 Restriktion und Ligation: Restriktion und Ligation: Grundlagen der Klonierung Modul 2303-021 1 Restriktion und Ligation Verknüpfung von Fragmenten unterschiedlicher DNA Herkunft Restriktion und Ligation
Restriktion und Ligation: Restriktion und Ligation: Grundlagen der Klonierung Modul 2303-021 1 Restriktion und Ligation Verknüpfung von Fragmenten unterschiedlicher DNA Herkunft Restriktion und Ligation
7 Anhang. 7.1 Herstellung der Expressionskassetten
 7 Anhang 7.1 Herstellung der Expressionskassetten Das Luciferase-Reportergen wurde über die Schnittstellen Nco I und Xba I aus dem Vektor psp-luc+ in den ebenfalls Nco I und Xba I geschnittenen Vektor
7 Anhang 7.1 Herstellung der Expressionskassetten Das Luciferase-Reportergen wurde über die Schnittstellen Nco I und Xba I aus dem Vektor psp-luc+ in den ebenfalls Nco I und Xba I geschnittenen Vektor
1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II
 Arbeitsblatt 1 Analyse von DNA 1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II Bevor Sie anfangen: Alle Reagenzien müssen vor Gebrauch vollständig aufgetaut sein und durchmischt
Arbeitsblatt 1 Analyse von DNA 1-A: Schneiden des Plasmids pucd-lacz mit dem Restriktionsenzym Ban II Bevor Sie anfangen: Alle Reagenzien müssen vor Gebrauch vollständig aufgetaut sein und durchmischt
1. EINLEITUNG Der eukaryontische Translationsinitiationsfaktor 5A (eif5a) Der Polyaminbiosyntheseinhibitor Agmatin...
 1. EINLEITUNG... 14 1.1 Lebenszyklus der Malaria Erreger Plasmodium falciparum und Plasmodium vivax... 16 1.2 Molekulares Targeting... 18 1.2.1 Die alternative Fettesäurebiosynthese II in Plasmodium falciparum...
1. EINLEITUNG... 14 1.1 Lebenszyklus der Malaria Erreger Plasmodium falciparum und Plasmodium vivax... 16 1.2 Molekulares Targeting... 18 1.2.1 Die alternative Fettesäurebiosynthese II in Plasmodium falciparum...
Cornel Mülhardt. Molekularbiologie/ Genomics
 Cornel Mülhardt Molekularbiologie/ Genomics 1 Was ist denn Molekularbiologie", bitteschön? 1 1.1 Das Substrat der Molekularbiologie, oder : Molli-World für Anfänger 2 1.2 Was brauche ich zum Arbeiten?
Cornel Mülhardt Molekularbiologie/ Genomics 1 Was ist denn Molekularbiologie", bitteschön? 1 1.1 Das Substrat der Molekularbiologie, oder : Molli-World für Anfänger 2 1.2 Was brauche ich zum Arbeiten?
MPP Multiplex 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Bioinformatik I: Grundlagen der Gentechnik
 Bioinformatik I: Grundlagen der Gentechnik Dr. Maik Böhmer Institut für Biologie und Biotechnologie der Pflanzen Schlossplatz 7 Schwerpunkte: Vorlesung 1: Einführung & Enzyme der Gentechnik Vorlesung 2:
Bioinformatik I: Grundlagen der Gentechnik Dr. Maik Böhmer Institut für Biologie und Biotechnologie der Pflanzen Schlossplatz 7 Schwerpunkte: Vorlesung 1: Einführung & Enzyme der Gentechnik Vorlesung 2:
Warum man nicht schon in der SDS- Page eine Immunfärbung machen kann. Warum bei A-Tailingzyklus die A s nich immer mehr werden
 Molbi Nachklausur 2009 Hier mal so die Fragen die mir noch so einfallen. Also es war gefragt: Warum man nicht schon in der SDS- Page eine Immunfärbung machen kann. Warum bei A-Tailingzyklus die A s nich
Molbi Nachklausur 2009 Hier mal so die Fragen die mir noch so einfallen. Also es war gefragt: Warum man nicht schon in der SDS- Page eine Immunfärbung machen kann. Warum bei A-Tailingzyklus die A s nich
Analyse des Genoms des Pseudomonas-Phagen 0CTX, insbesondere der Steuerung der späten Gene
 Analyse des Genoms des Pseudomonas-Phagen 0CTX, insbesondere der Steuerung der späten Gene Frank Wilhelm Langewische Inhaltsverzeichnis Verzeichnis der Abbildungen Verzeichnis der Tabellen Verzeichnis
Analyse des Genoms des Pseudomonas-Phagen 0CTX, insbesondere der Steuerung der späten Gene Frank Wilhelm Langewische Inhaltsverzeichnis Verzeichnis der Abbildungen Verzeichnis der Tabellen Verzeichnis
Plasmidpräparation aus Bakterien Inhalt
 Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Inhalt Einleitung... 2 Materialien... 4 Gewinnung der Bakterien... 6 Zerstörung der Bakterien... 7 Trennung von Plasmid-DNA und genomischer DNA... 8 Reinigung der Plasmid-DNA... 10 Elution der gereinigten
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016
 Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 2 (06.06. 10.06.) DNA-Schäden, Mutationen und Reparatur 1.
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 2 (06.06. 10.06.) DNA-Schäden, Mutationen und Reparatur 1.
Methodensammlung der Bund/Länder-Arbeitsgemeinschaft Gentechnik. PCR- Nachweis von E. coli B- und BL21- Stämmen
 Methodensammlung der Bund/Länder-Arbeitsgemeinschaft Gentechnik PCR- Nachweis von E. coli B- und BL21- Stämmen Erstellt vom Unterausschuss Methodenentwicklung der LAG, März 2005 1. Zweck und Anwendungsbereich
Methodensammlung der Bund/Länder-Arbeitsgemeinschaft Gentechnik PCR- Nachweis von E. coli B- und BL21- Stämmen Erstellt vom Unterausschuss Methodenentwicklung der LAG, März 2005 1. Zweck und Anwendungsbereich
Mycoplasma gallisepticum
 BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Mycoplasma gallisepticum Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Klonierung von S2P Rolle der M19-Zellen. POL-Seminar der Biochemie II 13.02.2007 Sebastian Gabriel
 Klonierung von S2P Rolle der M19-Zellen POL-Seminar der Biochemie II 13.02.2007 Sebastian Gabriel Inhalt 1. Was ist eine humane genomische DNA-Bank? 2. Unterschied zwischen cdna-bank und genomischer DNA-Bank?
Klonierung von S2P Rolle der M19-Zellen POL-Seminar der Biochemie II 13.02.2007 Sebastian Gabriel Inhalt 1. Was ist eine humane genomische DNA-Bank? 2. Unterschied zwischen cdna-bank und genomischer DNA-Bank?
Drosophila melanogaster
 Modul biol113 Zellbiologie Drosophila melanogaster Komponenten der angeborenen Immunabwehr Experimente 1) RT (Reverse Transkriptase)-PCR zum Nachweis einer AMP- Expression nach Infektion 1.1 PCR-Reaktion
Modul biol113 Zellbiologie Drosophila melanogaster Komponenten der angeborenen Immunabwehr Experimente 1) RT (Reverse Transkriptase)-PCR zum Nachweis einer AMP- Expression nach Infektion 1.1 PCR-Reaktion
Gentechnische Methoden
 Desmond S. T. Nicholl Gentechnische Methoden 2. Auflage Aus dem Englischen übersetzt von Renate FitzRoy und Kurt Beginnen Spektrum Akademischer Verlag Heidelberg Berlin Inhalt Vorwort XI 1. 1.1 1.2 1.3
Desmond S. T. Nicholl Gentechnische Methoden 2. Auflage Aus dem Englischen übersetzt von Renate FitzRoy und Kurt Beginnen Spektrum Akademischer Verlag Heidelberg Berlin Inhalt Vorwort XI 1. 1.1 1.2 1.3
VERZEICHNIS DER ABBILDUNGEN UND TABELLEN VERZEICHNIS DER ABKÜRZUNGEN UND TRIVIALNAMEN
 INHALTSVERZEICHNIS I VERZEICHNIS DER ABBILDUNGEN UND TABELLEN VII VERZEICHNIS DER ABKÜRZUNGEN UND TRIVIALNAMEN XIII 1 EINLEITUNG 1 1.1 Osmoadaption halophiler Mikroorganismen 2 1.1.1 Salt-in-cytoplasm
INHALTSVERZEICHNIS I VERZEICHNIS DER ABBILDUNGEN UND TABELLEN VII VERZEICHNIS DER ABKÜRZUNGEN UND TRIVIALNAMEN XIII 1 EINLEITUNG 1 1.1 Osmoadaption halophiler Mikroorganismen 2 1.1.1 Salt-in-cytoplasm
Borrelia burgdorferi s.l.
 BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Borrelia burgdorferi s.l. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Grundideen der Gentechnik
 Grundideen der Gentechnik Die Gentechnik kombiniert Biotechnik und Züchtung. Wie in der Züchtung wird die Erbinformation eines Lebewesen verändert. Dabei nutzte man in den Anfängen der Gentechnik vor allem
Grundideen der Gentechnik Die Gentechnik kombiniert Biotechnik und Züchtung. Wie in der Züchtung wird die Erbinformation eines Lebewesen verändert. Dabei nutzte man in den Anfängen der Gentechnik vor allem
Biochemie und. chemischer Mechanismus
 Dissertation zur Erlangung des Doktorgrades der Fakultät für Chemie und Pharmazie der Ludwig-Maximilians-Universität München Biochemie und chemischer Mechanismus der Thiomethylierung von RNA Dorothea Maria
Dissertation zur Erlangung des Doktorgrades der Fakultät für Chemie und Pharmazie der Ludwig-Maximilians-Universität München Biochemie und chemischer Mechanismus der Thiomethylierung von RNA Dorothea Maria
F-I Molekulare Zoologie: Teil I: Expressionsanalysen. Expressionsanalyse mittels RT-PCR
 F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
F-I Molekulare Zoologie: Teil I: Expressionsanalysen Expressionsanalyse mittels RT-PCR Inhalt: Seite I. Generelles 1 II. RNA-Aufreinigung mit EZNA Total RNA Kit (PeqLab)...2 III. Umschreiben von RNA in
Übersicht Sequenziermethoden
 DNA-Sequenzierung Übersicht Sequenziermethoden Sanger-Sequenzierung Pyrosequencing (Roche/454) Illumina/Solexa Pacific Biosciences (PacBio) Sanger-Sequenzierung Didesoxymethode, Kettenabruch- Synthese
DNA-Sequenzierung Übersicht Sequenziermethoden Sanger-Sequenzierung Pyrosequencing (Roche/454) Illumina/Solexa Pacific Biosciences (PacBio) Sanger-Sequenzierung Didesoxymethode, Kettenabruch- Synthese
2.5 Expression von Domänen des rgne-proteins in E.coli
 2.5 Expression von Domänen des rgne-proteins in E.coli Da die Kristallisation des rgne-gesamtproteins erfolglos verlief (2.4.5), wurde alternativ die Expression, Reinigung und Kristallisation der einzelnen
2.5 Expression von Domänen des rgne-proteins in E.coli Da die Kristallisation des rgne-gesamtproteins erfolglos verlief (2.4.5), wurde alternativ die Expression, Reinigung und Kristallisation der einzelnen
1. Beschreiben Sie die Rolle der folgenden Proteine bei der DNA- Replikation in E. coli:
 1. Beschreiben Sie die Rolle der folgenden Proteine bei der DNA- Replikation in E. coli: Übung 7 - DnaA bindet an 13 bp DNA Sequenz (DnaA Box, 5 Wiederholungen bei E. coli) im oric ori wird in AT reicher
1. Beschreiben Sie die Rolle der folgenden Proteine bei der DNA- Replikation in E. coli: Übung 7 - DnaA bindet an 13 bp DNA Sequenz (DnaA Box, 5 Wiederholungen bei E. coli) im oric ori wird in AT reicher
DNA Isolierung. Praktikum Dr. László Kredics
 Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
Isolierung Praktikum Dr. László Kredics SZTE, Inst. für Med. Biol., Praktikum -Isolierung Zellaufschluss Isolierung genomischer Isolierung von Plasmid Konzentrationsbestimmung der -Lösungen Anhand Absorptionswert
Forschung hautnah: Wissenschaftliches Schülerpraktikum vergeben durch den Förderverein der BiologieOlympiade e.v.
 Forschung hautnah: Wissenschaftliches Schülerpraktikum vergeben durch den Förderverein der BiologieOlympiade e.v. Zentrum für Medizinische Mikrobiologie und Hygiene Heidelberg AG Kubatzky PD Dr. Katharina
Forschung hautnah: Wissenschaftliches Schülerpraktikum vergeben durch den Förderverein der BiologieOlympiade e.v. Zentrum für Medizinische Mikrobiologie und Hygiene Heidelberg AG Kubatzky PD Dr. Katharina
Rekombinante Antikorperfragmente fur die. Zoonosediagnostik
 Rekombinante Antikorperfragmente fur die Zoonosediagnostik Von der Fakultat fur Lebenswissenschaften der Technischen Universitat Carolo-Wilhelmina zu Braunschweig zur Erlangung des Grades eines Doktors
Rekombinante Antikorperfragmente fur die Zoonosediagnostik Von der Fakultat fur Lebenswissenschaften der Technischen Universitat Carolo-Wilhelmina zu Braunschweig zur Erlangung des Grades eines Doktors
Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014
 Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014 Tag 1 PCR Die Polymerase-Kettenreaktion (engl. polymerase chain reaction) ermöglicht die selektive
Laborkurs des Heidelberger Life-Science Lab und des igem-teams Heidelberg 2014 2. Woche/14. 16.07.2014 Tag 1 PCR Die Polymerase-Kettenreaktion (engl. polymerase chain reaction) ermöglicht die selektive
Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele
 Versuch 1: Restriktionsenzyme als molekulare Werkzeuge Versuchsinhalt Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele Zwei
Versuch 1: Restriktionsenzyme als molekulare Werkzeuge Versuchsinhalt Restriktion zweier Plasmide zur Erstellung einer physikalischen Karte, Grundlagen der DNA- Trennung und Analyse über Agarosegele Zwei
https://cuvillier.de/de/shop/publications/2978
 Andreas Christmann (Autor) Zur bakteriellen Oberflächenpräsentation kombinatorischer Peptidbibliotheken und deren Anwendung auf Fragestellungen der Immunologie, Molekularbiologie und der Molekualren Medizin
Andreas Christmann (Autor) Zur bakteriellen Oberflächenpräsentation kombinatorischer Peptidbibliotheken und deren Anwendung auf Fragestellungen der Immunologie, Molekularbiologie und der Molekualren Medizin
Gentechnologie für Einsteiger
 T. A. Brown Gentechnologie für Einsteiger 3. Auflage Aus dem Englischen übersetzt von Sebastian Vogel Spektrum Akademischer Verlag Heidelberg Berlin Vorwort Vorwort zur dritten englischen Auflage Vorwort
T. A. Brown Gentechnologie für Einsteiger 3. Auflage Aus dem Englischen übersetzt von Sebastian Vogel Spektrum Akademischer Verlag Heidelberg Berlin Vorwort Vorwort zur dritten englischen Auflage Vorwort
Methoden der Gentechnik
 Methoden der Gentechnik *** DNA-Rekombination und Klonierung *** 1. Allgemeine Grundprinzipien 1.1. Wesen der Gentechnik 1.2. Allgemeine Ziele der Gentechnik 1.3. Molekulare Voraussetzungen 1.4. Wichtige
Methoden der Gentechnik *** DNA-Rekombination und Klonierung *** 1. Allgemeine Grundprinzipien 1.1. Wesen der Gentechnik 1.2. Allgemeine Ziele der Gentechnik 1.3. Molekulare Voraussetzungen 1.4. Wichtige
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen
 Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen Vorbereitung auf diesen Praktikumsteil: Organisation 2. Praktikumstag: - Für den Bioinformatik-Teil benötigen Sie am 2. Tag dieses
Praktikumsteil: 3 - RACE-PCR und Klonierung von MADS-Box- Genen aus Tulpen Vorbereitung auf diesen Praktikumsteil: Organisation 2. Praktikumstag: - Für den Bioinformatik-Teil benötigen Sie am 2. Tag dieses
Molekularbiologische / gentechnische Methoden
 Molekularbiologische / gentechnische Methoden MPM 1 Wie lässt sich ein spezifisches Gen/Genprodukt molekular analysieren? Fundamentales Problem: Komplexität biologischer Systeme MPM 2 Ein Ausschnitt aus
Molekularbiologische / gentechnische Methoden MPM 1 Wie lässt sich ein spezifisches Gen/Genprodukt molekular analysieren? Fundamentales Problem: Komplexität biologischer Systeme MPM 2 Ein Ausschnitt aus
Protokoll Praktikum für Humanbiologie Studenten
 Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Protokoll Praktikum für Humanbiologie Studenten Teil A: Charakterisierung der Auswirkungen von γ Interferon auf die Protein und mrna Mengen in humanen A549 Lungenepithelzellen. Studentenaufgaben Tag 1
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers
 Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein (1) Plasmidpräparation
Praktikum Biochemie Biotechnologie (Molekularbiologie & Biochemie) Bettina Siebers Protein Expression Genomische DNA PCR Vektormolekül (Plasmid) Escherichia coli Reinigung Protein (1) Plasmidpräparation
Pasteurella multocida
 BACTOTYPE PCR Amplification Kit Pasteurella multocida Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von
BACTOTYPE PCR Amplification Kit Pasteurella multocida Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von
3. Methoden. 3. Methoden RNA-Isolierung
 3. Methoden 7 3. Methoden 3.1 RNA-Isolierung Aus 250µl EDTA-Blut wurde die RNA isoliert. Dazu wurde der QIAamp RNA Blood Mini Kit (Qiagen KatNr. 52304) verwendet. Das Blut wurde mit 300 µl EL-Puffer versetzt
3. Methoden 7 3. Methoden 3.1 RNA-Isolierung Aus 250µl EDTA-Blut wurde die RNA isoliert. Dazu wurde der QIAamp RNA Blood Mini Kit (Qiagen KatNr. 52304) verwendet. Das Blut wurde mit 300 µl EL-Puffer versetzt
Anhang Anhang 8.1 Konstruktion transgener SQD1 -Pflanzen
 Anhang 92 8 Anhang 8.1 Konstruktion transgener SQD1-Pflanzen Mutagenese und ein dadurch entstehender Phänotyp eines Organismus kann Aufschluß über die Funktion eines betroffenen Gens geben. Die Erzeugung
Anhang 92 8 Anhang 8.1 Konstruktion transgener SQD1-Pflanzen Mutagenese und ein dadurch entstehender Phänotyp eines Organismus kann Aufschluß über die Funktion eines betroffenen Gens geben. Die Erzeugung
https://cuvillier.de/de/shop/publications/1657
 Christian Landmann (Autor) Funktionelle Charakterisierung von Enzymen des Sekundärstoffwechsels in Lavendel (Lavandula angustifolia) und Erdbeere (Fragaria x ananassa) https://cuvillier.de/de/shop/publications/1657
Christian Landmann (Autor) Funktionelle Charakterisierung von Enzymen des Sekundärstoffwechsels in Lavendel (Lavandula angustifolia) und Erdbeere (Fragaria x ananassa) https://cuvillier.de/de/shop/publications/1657
Mycobacterium paratuberculosis
 BACTOTYPE PCR Amplification Kit Mycobacterium paratuberculosis Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
BACTOTYPE PCR Amplification Kit Mycobacterium paratuberculosis Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS
 Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
Anwendungsbericht zur Herstellung des Proteins GST-GFP-NLS Von: Andreas Tschammer, Fachhochschule Aalen-Hochschule f. Technik und Wirtschaft, Fachbereich Chemie, Schwerpunkt Molekulare Biotechnologie Material
1. Nennt Informationen, die ein Wissenschaftler für die Durchführung des farbig markierten Schrittes benötigt. 2. Nennt zusätzliche Probleme die bei
 Wir erinnern uns 1. Nennt Informationen, die ein Wissenschaftler für die Durchführung des farbig markierten Schrittes benötigt. 2. Nennt zusätzliche Probleme die bei der Verwendung eines Gens aus einer
Wir erinnern uns 1. Nennt Informationen, die ein Wissenschaftler für die Durchführung des farbig markierten Schrittes benötigt. 2. Nennt zusätzliche Probleme die bei der Verwendung eines Gens aus einer
PRAKTISCHE ÜBUNGEN IN GENETIK FÜR FORTGESCHRITTENE. Protokoll FÜR LEHRAMTSKANDIDATEN
 Universität zu Köln Institut für Genetik 8. April 2001 PRAKTISCHE ÜBUNGEN IN GENETIK FÜR FORTGESCHRITTENE FÜR LEHRAMTSKANDIDATEN WS 2000/2001 Protokoll Versuchsleiter: Dr. Fußwinkel Dr. Kisters-Woike Dr.
Universität zu Köln Institut für Genetik 8. April 2001 PRAKTISCHE ÜBUNGEN IN GENETIK FÜR FORTGESCHRITTENE FÜR LEHRAMTSKANDIDATEN WS 2000/2001 Protokoll Versuchsleiter: Dr. Fußwinkel Dr. Kisters-Woike Dr.
Einführung in die Umweltwissenschaften
 Einführung in die Umweltwissenschaften Genetik und Gentechnologie (pro und contra) 16.11. 2012 WS 2011/12 H.P. Aubauer, P. Bajons, V. Schlosser Basen:? Purinbasen: Adenin DNA - Grundbausteine Guanin Phosphate
Einführung in die Umweltwissenschaften Genetik und Gentechnologie (pro und contra) 16.11. 2012 WS 2011/12 H.P. Aubauer, P. Bajons, V. Schlosser Basen:? Purinbasen: Adenin DNA - Grundbausteine Guanin Phosphate
Rekombinante DNA. Werkzeuge der Gentechnik
 Rekombinante DNA = im Labor neu zusammengesetzte DNA. Ein definiertes DNA Fragment (meistens ein Gen) wird aus seiner ursprünglichen Lage entnommen und in einen Vektor integriert, der gezielt in andere
Rekombinante DNA = im Labor neu zusammengesetzte DNA. Ein definiertes DNA Fragment (meistens ein Gen) wird aus seiner ursprünglichen Lage entnommen und in einen Vektor integriert, der gezielt in andere
4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd30-igg1-tnf- Fusionsproteins
 ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
ERGEBNISSE 29 4. Ergebnisse 4.1. Herstellung des CH2/CH3-trunkierten dimerisierten anti-cd3-igg1-tnf- Fusionsproteins Im vorliegenden Immunzytokin wurden die Domänen CH2/CH3 des humanen Fc-Fragmentes durch
Vorlesung LV-Nr Molekularbiologie für Agrarwissenschaften. J. Glößl, SS 2007
 Vorlesung LV-Nr. 954.104 Molekularbiologie für Agrarwissenschaften J. Glößl, SS 2007 Thematik: Molekularbiologische Methoden Teil 2 Die ppt Folien wurden freundlicherweise von Prof. Florian Rüker aus der
Vorlesung LV-Nr. 954.104 Molekularbiologie für Agrarwissenschaften J. Glößl, SS 2007 Thematik: Molekularbiologische Methoden Teil 2 Die ppt Folien wurden freundlicherweise von Prof. Florian Rüker aus der
Pflanze direkt 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.322.0250 Artikel-Nr. BS91.322.1250 250 Reaktionen in 20 μl 1250 Reaktionen in 20 μl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
GEIM- TECHIMOLOGISCHE ARBEITSMETHODEN
 GEIM- TECHIMOLOGISCHE ARBEITSMETHODEN Ein Handbuch experimenteller Techniken und Verfahren Herausgegeben von Rudolf Hagemann Bearbeitet von Frank Baldauf, Jörn Belter, Sabine Brantl, Baimund Eck, Karsten
GEIM- TECHIMOLOGISCHE ARBEITSMETHODEN Ein Handbuch experimenteller Techniken und Verfahren Herausgegeben von Rudolf Hagemann Bearbeitet von Frank Baldauf, Jörn Belter, Sabine Brantl, Baimund Eck, Karsten
Klonierung von GFP in E.coli
 Bernhard-Strigel-Gymnasium Memmingen Kollegstufe Jahrgang:...2007/2009 Leistungskurs:...Biologie Kollegiatin:...Nicole Makowski Facharbeit Klonierung von GFP in E.coli Abgegeben am: 30.01.2009 Bewertung:
Bernhard-Strigel-Gymnasium Memmingen Kollegstufe Jahrgang:...2007/2009 Leistungskurs:...Biologie Kollegiatin:...Nicole Makowski Facharbeit Klonierung von GFP in E.coli Abgegeben am: 30.01.2009 Bewertung:
SCRIPTUM HIGH PRECISE
 Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
Nur für Forschungszwecke Datenblatt Artikel BS.50.020 = 20 Reaktionen x 50 µl Artikel BS.50.100 = 100 Reaktionen x 50 µl Artikel BS.50. 500 = 500 Reaktionen x 50 µl Haltbarkeit: 12 Monate Lagerung bei
2. Konstruktion und Charakterisierung einer stx 2 -Mutante im E. coli-stamm O157:H7 86-24
 IV. Ergebnisse 90 2. Konstruktion und Charakterisierung einer stx 2 -Mutante im E. coli-stamm O157:H7 86-24 Die Konstruktion einer isogenen Toxinmutante des Stx2-produzierenden EHEC- Stamm O157:H7 86-24
IV. Ergebnisse 90 2. Konstruktion und Charakterisierung einer stx 2 -Mutante im E. coli-stamm O157:H7 86-24 Die Konstruktion einer isogenen Toxinmutante des Stx2-produzierenden EHEC- Stamm O157:H7 86-24
DNA Isolierung. Praktikum Dr. László Kredics
 Isolierung Praktikum Dr. László Kredics Aufgabe: Isolierung von Plasmid aus Bakterienzellen Plasmid : pbluescript Vektor, Gröβe: 2960 Bps 1. 1,5 ml Bakterienkultur in Eppendorf-Röhrchen pipettieren, 2
Isolierung Praktikum Dr. László Kredics Aufgabe: Isolierung von Plasmid aus Bakterienzellen Plasmid : pbluescript Vektor, Gröβe: 2960 Bps 1. 1,5 ml Bakterienkultur in Eppendorf-Röhrchen pipettieren, 2
Europaisches Patentamt European Patent Office Office europeen des brevets. Veröffentlichungsnummer: A2 EUROPAISCHE PATENTANMELDUNG C12N 9/10
 Europaisches Patentamt European Patent Office Office europeen des brevets Veröffentlichungsnummer: 0 264 805 A2 EUROPAISCHE PATENTANMELDUNG (jy Anmeldenummer: 87114995.195.1 int. Cl.«: C12N 15/00 Anmeldetag:
Europaisches Patentamt European Patent Office Office europeen des brevets Veröffentlichungsnummer: 0 264 805 A2 EUROPAISCHE PATENTANMELDUNG (jy Anmeldenummer: 87114995.195.1 int. Cl.«: C12N 15/00 Anmeldetag:
DNA-Analytik. Beispiel: Nachweis von gentechnisch veränderten Lebensmitteln
 DNA-Analytik Beispiel: Nachweis von gentechnisch veränderten Lebensmitteln rdna PCR mrna RT-PCR Protein (Enzym) Immunochemie Produkt Stoffanalytik 1. Extraktion der DNA aus den Lebensmitteln 2. DNA liegt
DNA-Analytik Beispiel: Nachweis von gentechnisch veränderten Lebensmitteln rdna PCR mrna RT-PCR Protein (Enzym) Immunochemie Produkt Stoffanalytik 1. Extraktion der DNA aus den Lebensmitteln 2. DNA liegt
Chlamydia sp. BACTOTYPE PCR Amplification Kit. Gebrauchsanweisung. Labor Diagnostik Leipzig
 BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
BACTOTYPE PCR Amplification Kit Chlamydia sp. Labor Diagnostik Leipzig Gebrauchsanweisung Technologie Die Produktgruppe BACTOTYPE PCR Amplification Kit umfasst optimierte Systeme zum Nachweis von pathogenen
Pharmakologische Untersuchungen zur Neuropeptid Y Yi-, Y 2 - und Ys-Rezeptorselektivität peptidischer und nichtpeptidischer Liganden:
 o Pharmakologische Untersuchungen zur Neuropeptid Y Yi-, Y 2 - und Ys-Rezeptorselektivität peptidischer und nichtpeptidischer Liganden: Klonierung und funktioneile Expression des humanen Ys-Rezeptors in
o Pharmakologische Untersuchungen zur Neuropeptid Y Yi-, Y 2 - und Ys-Rezeptorselektivität peptidischer und nichtpeptidischer Liganden: Klonierung und funktioneile Expression des humanen Ys-Rezeptors in
Fachverlag Köhler Giessen VETERINÄRMEDIZIN
 VETERINÄRMEDIZIN Kälteanpassung \bi\ Listeria monocytogenes: Klonierung, D^Ä-Sequenzanalyse und Funktionsstudien der Gene CS/JL, CS/JLB und flar aus dem Wildtypstamm Listeria monocytogenes EGD Eva-Maria
VETERINÄRMEDIZIN Kälteanpassung \bi\ Listeria monocytogenes: Klonierung, D^Ä-Sequenzanalyse und Funktionsstudien der Gene CS/JL, CS/JLB und flar aus dem Wildtypstamm Listeria monocytogenes EGD Eva-Maria
Molekularbiologie I. PCR Klonierung Transformation Southern Blot Hybridisierung BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN V 2.
 V 2.6 Molekularbiologie I BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN PCR Klonierung Transformation Southern Blot Hybridisierung Abteilung für Biochemie und Molekularbiologie, Fachbereich
V 2.6 Molekularbiologie I BIOCHEMISCHES ANFÄNGERPRAKTIKUM FÜR CHEMIKER UND BIOLOGEN PCR Klonierung Transformation Southern Blot Hybridisierung Abteilung für Biochemie und Molekularbiologie, Fachbereich
Induktion der β-galaktosidase von Escherichia coli
 Induktion der β-galaktosidase von Escherichia coli 1. Einleitung Das Bakterium Escherichia coli ist in der Lage verschiedene Substrate für seinen Stoffwechsel zu nutzen. Neben Glucose und Acetat kann es
Induktion der β-galaktosidase von Escherichia coli 1. Einleitung Das Bakterium Escherichia coli ist in der Lage verschiedene Substrate für seinen Stoffwechsel zu nutzen. Neben Glucose und Acetat kann es
1. Welche Auswirkungen auf die Expression des lac-operons haben die folgenden Mutationen:
 Übung 10 1. Welche Auswirkungen auf die Expression des lac-operons haben die folgenden Mutationen: a. Eine Mutation, die zur Expression eines Repressors führt, der nicht mehr an den Operator binden kann.
Übung 10 1. Welche Auswirkungen auf die Expression des lac-operons haben die folgenden Mutationen: a. Eine Mutation, die zur Expression eines Repressors führt, der nicht mehr an den Operator binden kann.
3,58 g 0,136 g. ad 100 ml
 9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
9 Anhang 9.1 Rezepturen der Puffer und Lösungen 9.1.1 Vorbereitung der Proben zur Extraktion Coon s-puffer (0,1 M, ph 7,2-7,6) Na 2 HPO 4 x 12 H 2 O KH 2 PO 4 Aqua dest. 3,58 g 0,136 g 8,77 g 9.1.2 Aufbereitung
DNA-KLONIERUNG.
 DNA-KLONIERUNG http://openpcr.org/use-it/ DNA- KLONIERUNG: Vervielvältigung eines DNA-Moleküls In vitro - PCR In vivo in unterschiedlichen Wirtszellen POLYMERASE- KETTENREAKTION (Polymerase Chain Reaction,
DNA-KLONIERUNG http://openpcr.org/use-it/ DNA- KLONIERUNG: Vervielvältigung eines DNA-Moleküls In vitro - PCR In vivo in unterschiedlichen Wirtszellen POLYMERASE- KETTENREAKTION (Polymerase Chain Reaction,
