Kapitel 11: Lebensmittelfarbstoffe
|
|
|
- Martin Fuhrmann
- vor 7 Jahren
- Abrufe
Transkript
1 Kapitel 11: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität oder Farbe zu erzielen. Zum Beispiel ersetzen Farbstoffe die bei der Verarbeitung verlorengegangene Farbe. Konservierungsmittel werden beigefügt, um die Lebensmittel vor schädlichen Bakterien und Schimmelpilzen zu schützen. Emulgatoren und Stabilisatoren ersetzen die durch die Fettreduktion verlorengegangene natürliche Sämigkeit einer Speise. Es dürfen nur gesetzlich zugelassene Zusatzstoffe bei der Lebensmittelverarbeitung verwendet werden. Diese sind in einer Positivliste zusammengefasst, d.h. nur die hier aufgeführten Stoffe dürfen Lebensmitteln zugesetzt werden. In dieser sogenannten E-Liste findet man viele Substanzen, die natürlicherweise in Lebensmitteln vorkommen, z.b. Carotine (E160a), Citronensäure (E130) oder Pektin (E140), aber auch Stoffe, die überhaupt nicht in der Natur vorkommen, so z.b. Azofarbstoffe oder die Süssstoffe Aspartam (E951) und Cyclamat (E952). Das E steht für EU, die Schweiz hat sich den europäischen Bestimmungen angeschlossen und die Nummerierung übernommen. Die Zusatzstoffe werden mit dem Buchstaben E bezeichnet, gefolgt von einer 3- bis 4-stelligen Zahl. Das E-Nummern-System dient auch dazu, um zugelassene Zusatzstoffe quer durch alle Sprachen zu kennzeichnen. Farbstoffe Als Farbstoff werden chemische Verbindungen bezeichnet, die die Eigenschaft haben, andere Materialien zu färben. Nach DIN sind es solche Farbmittel, die in ihrem Anwendungsmedium löslich sind. Unlösliche Farbmittel heissen Pigmente. Farbstoffe, die dazu verwendet werden, Lebensmittel zu färben, werden als Lebensmittelfarben bezeichnet und sind Lebensmittelzusatzstoffe. Die Farbstoffe kann man in tierische und pflanzliche oder organische und anorganische Farbstoffe einteilen. Eine weitere Einteilung unterscheidet zwischen synthetischen und natürlichen Farbstoffen. Synthetische Farbstoffe sind zum Beispiel Azofarbstoffe. Tierische Farbstoffe sind Farbstoffe, die von Tieren produziert werden. Das sind z.b. Purpur (von der Purpurschnecke) und Karmin (von der Cochenille-Schildlaus). Pflanzliche Farbstoffe sind Farbstoffe, die aus Pflanzen produziert werden, z.b. Indigo, Chlorophyll (Blattgrün), Crocetin (Safran) oder Carotin (Karotten). Anorganische Farbstoffe sind Farbstoffe ohne Kohlenstoff, z.b. Chromgelb. Weisses Licht (Spektrum im Bereich nm) ist eine Mischung von Licht mit verschiedensten Wellenlängen. Das Farbspektrum reicht hierbei von langwelligem Rotlicht (IR) (ca. 790 nm) bis zu kurzwelligem Violettlicht (UV) (ca. 380 nm). HS
2 Die Wirkungsweise von Farbstoffen beruht nun darauf, bestimmte Teile des Lichtspektrums zu absorbieren. Die Komplementärfarbe der absorbierten Wellenlänge ist die Farbe, in welcher der Farbstoff erscheint. Die Absorption von elektromagnetischer Strahlung, zu der auch Licht gehört, beruht dabei auf der Anhebung des Energieniveaus von Elektronen in Molekülen oder Atomen (Erhöhung des Abstandes zwischen Elektronen und den Atomkernen). Die hierzu nötige Energie wird der einfallenden elektromagnetischen Strahlung, dem Licht, entnommen. Da sich diese Vorgänge auf der Quantenebene abspielen, ist diese Absorption nicht kontinuierlich, sondern erfolgt nur in bestimmten Stufen, die dem energetischen Unterschied zwischen den Elektronenkonfigurationen vor und nach der Absorption entsprechen. Dieser Energieunterschied ist umgekehrt proportional zu der absorbierten Wellenlänge des einfallenden Lichts und bestimmt somit die Farbe, in der der Farbstoff erscheint. Treten in den betrachteten Molekülen oder Atomen nur einfache σ-bindungen auf, so ist die Energie, die benötigt wird, um die entsprechenden σ-elektronen auf ein höheres energetisches Niveau zu heben, zu gross, als dass es zu einer Niveauerhöhung durch den sichtbaren Teil des elektromagnetischen Spektrums kommen könnte. Im Allgemeinen findet hier eine Absorption im Bereich des UV-Lichtes oder der Röntgenstrahlung statt, so dass diese Art von Verbindungen normalerweise als Farbstoff ungeeignet sind. Leichter gelingt die Anregung der Elektronen, die in π-bindungen, z.b. ungesättigten Bindungen, auftreten. Diese absorbieren elektromagnetische Wellen im Bereich des langwelligen UV-Bereichs. Arrangiert man mehrere solche ungesättigte Bindungen (Mehrfachbindungen) abwechselnd mit einfachen Atombindungen, so kommt es zu einer Delokalisierung der π-elektronen, wodurch der Abstand zwischen dem angeregten und dem Grundzustand noch einmal verringert wird. Dem entspricht eine Verschiebung der absorbierten Wellenlängen hin zu grösseren Wellenlängen. Im Allgemeinen gilt hierbei, dass der Absorbtionsbereich umso mehr verschoben wird, je grösser die Anzahl dieser ungesättigten Bindungen ist. Eine weitere Anhebung kann erreicht werden, indem solche Stoffe mit besonders geeigneten anderen Atomgruppen oder Atomen kombiniert werden, die als Elektronenakzeptoren oder Elektronendonoren fungieren und/oder mesomeriefähig sind. Als Auxochrome (Elektronendonatoren) oder Antiauxochrome (Elektronenakzeptoren) können beispielsweise folgende funkrionelle Gruppen Verwendung finden: Auxochrome Antiauxochrome R-OH R-NH 2 R-SO 3 H R-COOH R 2 -C=O R-NO 2 R-CHO R-C=NR HS
3 Die Wirkung dieser Auxo- bzw. Antiauxochrome beruht dabei auf einer Polarisierung des Moleküls und einer daraus folgenden Verschiebung der vorhandenen delokalisierten Elektronen, die durch die ungesättigten Verbindungen im Rest des Moleküls zur Verfügung stehen. Die Gruppen, die ensprechende delokalisierte Elektronen zur Verfügung stellen, werden auch als Chromophore bezeichnet. Folgende funktionelle Gruppen können beispielsweise als Chromophore fungieren: Chromophore R-C=C-R R-N=N-R R-C=O R-C=NH R-N=O Lebensmittelfarbstoffe (E100 E180, E579, E585) Lebensmittelfarbstoffe sind natürliche oder synthetische Farbstoffe, die laut Lebensmittelgesetz zum Färben von Nahrungs-, Genuss- und Artzneimitteln zugelassen sind. Unansehnliche Waren erhalten durch Lebensmittelfarben ein verkaufsförderndes farbiges und appetitanregendes Aussehen. Bedenklich dabei ist, dass der Eindruck guter Qualität vermittelt wird, auch wenn das nicht der Fall ist. Ausserdem gewöhnen sich die Verbraucher an Färbungen, die mit dem natürlichen Aussehen der Produkte unter Umständen nicht mehr viel zu tun haben. Grundsätzlich kann man davon ausgehen, dass von Lebensmittelfarbstoffen keine Gesundheitsgefährdung ausgeht. Bei einigen Farbstoffen besteht jedoch aufgrund der chemischen Verwandtschaft mit den zum Teil giftigen Azofarbstoffen der Verdacht auf gesundheitsschädigendes Potential. Azofarbstoffe Mit über 2000 organischen Verbindungen stellen die Azofarbstoffe die grösste Gruppe der Farbstoffe. Sie zeichnen sich durch besonders lichtechte, stabile und kräftige Farben aus, die sich gut mischen lassen. Viele Azoverbindungen werden im menschlichen Körper durch Enzyme in ihre Ausgangsverbindungen aufgespalten, die als stark krebserzeugend gelten. Während Azofarbstoffe zu Beginn des 19. Jahrhunderts ein breites Anwendungsspektrum hatten, ist deshalb heute ihre Verwendung hauptsächlich auf die Färbung von Fetten, Holz und Papier beschränkt. Nur einige wenige sind auch zum Färben von Lebensmittels, Kosmetikartikeln und Textilien zugelassen. Viele Azofarbstoffe stehen noch immer unter Verdacht, Allergien und Pseudoallergien auszulösen, sowie am hyperkinetischen Syndrom (Zappelphillip) beteiligt zu sein. HS
4 Herstellung der Azofarbstoffe Diazotierung Die Diazotierung bezeichnet die Nitrosierung primärer, aromatischer Amine mit salpetriger Säure, welche zur Bildung von Diazonium-Kationen führt. Die Diazotierung findet im Prinzip auch bei primären aliphatischen Aminen statt, jedoch sind deren Diazonium-Ionen im allgemeinen so instabil, dass sie sofort unter Stickstoffabspaltung in Carbenium-Ionen übergehen. Diazoniumsalze sind wichtige Zwischenstufen für organische Synthesen, beispielsweise für die Azokupplung und Sandmeyer Reaktion. Mechanismus Durch Zugabe einer Säure wird aus Nitrit ein Nitrosonium-Ion als Elektrophil gebildet: Die Reaktion zur Diazonium-Verbindung verläuft über mehrere Stufen: Die Stabilität aromatischer Diazonium-Ionen beruht auf Resonanzstablisierung durch den aromatischen Ring: HS
5 Wässrige Lösungen von Arendiazoniumionen sind unter Eiskühlung stabil. Salze mit nicht-nucleophilen Gegenionen (Sulfate, Tetrafluoroborate, Hexafluorophosphate) sind am stabilsten, fallen aus und können sogar isoliert werden. Azokupplung Darstellung von Azoverbindungen durch Umsetzung eines Diazoniumsalzes mit einem elektronenreichen Aromaten. Mechanismus Da Aryldiazoniumsalze schwache Elektrophile sind, gehen sie nur mit aktivierten Aromaten Reaktionen ein. So sind erst Phenolate genügend reaktiv. Die Azokupplung erfolgt selektiv in para-position, ausser an dieser Stelle ist bereits ein Substituent vorhanden (dann ortho). HS
6 Synthese von Azorubin Azorubin (E122) Charakteristik: Azorubin ist ein roter, wasserlöslicher Azofarbstoff. Er ist beständig gegen Licht und Hitze, jedoch nicht gegen Fruchtsäuren. Verwendung: Azorubin wird verwendet für Getränke, Süss- und Zuckerwaren, Marzipan, Puddingpulver, Kunstspeiseeis, Biskuit, Fruchtkonserven, Fertigsuppen, braune Saucen, Paniermehl sowie bei Arzneimitteln zur Färbung von Dragees. Sicherheit: Das Risiko von Azorubin ist bis heute nicht abschliessend geklärt. Es besteht der Verdacht auf Auslösung von Pseudoallergien bei empfindlichen Menschen, besonders bei Personen, die empfindlich auf Aspirin oder Benzoesäure reagieren. Im Tierversuch wurden bei höherer Dosierung verschiedene Nebenwirkungen auf Blutbild, Lunge, Lymphsystem und Bauchspeicheldrüse beobachtet. Reaktionsgleichungen HS
7 Ansatz 0,50 g 4-Aminonaphthalin-1-sulfonsäure-Natriumsalz (2 mmol) 0,70 g 1-Naphthol-4-sulfonsäure-Natriumsalz (2 mmol) 0,20 g Natriumnitrit gelöst in H 2 O sodass w = 14% 5 ml NaOH 2M (mol L -1 ) 4,5 ml HCl 2M (mol L -1 ) Geräte 100 ml Zweihalsrundkolben Thermometer 50 ml Becherglas 25 ml Tropftrichter Durchführung Herstellung der Diazoniumsalzlösung In einem Becherglas wird das 4-Aminonaphthalin-1-sulfonsäure-Natriumsalz in 5 ml dest. H 2 O gelöst. Unter Rühren werden 1-2 Tropfen NaOH 2M hinzugegeben, bis der ph am Ende grösser als 7 ist (mit ph-papier prüfen). Anschliessend wird die Natriumnitrit-Lösung langsam mithilfe einer Pasteurpipette hinzugegeben. In einem zweiten Becherglas werden 4,5 ml HCl 2M in einem Eisbad abgekühlt. Sobald die Temperatur maximal 5 C beträgt, wird die erste Lösung unter Rühren langsam mithilfe einer Pasteurpipette hinzugegeben. Danach wird 10 min weiter gerührt. Um sicherzugehen dass die Reaktion vollständig abgelaufen ist, wird mithilfe von KI-Stärkepapier getestet, ob überschüssiges Natriumnitrit vorhanden ist: ein Tropfen aus dem zweiten Becherglas wird auf einen Teststreifen aufgetragen. Sollte sich das Papier blau/lila verfärben, deutet dies auf das Vorhandensein von Natriumnitrit hin. Die Reaktion ist abgeschlossen. Ansonsten werden noch wenige Tropfen Natriumnitrit hinzugefügt. Vorsicht: Feste Diazoniumsalze sind explosiv, gebrauchte Gegensände sofort gut waschen. Vorbereitung der Kupplungskomponente Das 1-Naphthol-4-sulfonsäure-Natriumsalz wird in 5 ml H 2 O im Zweihalsrundkolben auf C im Ölbad erwärmt. Sobald alles gelöst ist, wird die Lösung auf Raumtemperatur abgekühlt und mit 5 ml NaOH 2M versetzt. Die Lösung wird mit Eiswasser auf 5 C gekühlt. Kupplung zum Farbstoff Zur Kupplungskomponente wird unter Rühren im Eisbad die Diazoniumsalzlösung mit dem Tropftrichter zugetropft. Danach lässt man bei Raumtemperatur Minuten nachrühren. HS
8 Nachweis von Azorubin (E122) in Sirup Der Farbstoff Azorubin soll aus rotem Sirup mittels Wollfadenmethode extrahiert und qualitativ mittels Dünnschichtchromatographie (DC) bestimmt werden. Ansatz 2 Pasteurpipetten roter Sirup 10 ml Essigsäure 5%ige wässrige Lösung 10 ml Ammoniak 5%ige wässrige Lösung Geräte 50 ml Becherglas 10 ml Messzylinder Durchführung Der Sirup wird in einem Becherglas vorgelegt und 10 ml 5%ige Essigsäure werden hinzugefügt. Die Lösung wird unter Rühren auf 70 C erhitzt. Ein 50 cm langer Wollfaden wird in die Lösung gelegt und gerührt. Wenn die Lösung fast farblos ist, wird der Wollfaden mit Wasser gut gespült. Der gespülte Wollfaden wird in ein Becherglas mit 10 ml Ammoniak 5%ig gelegt und gerührt bis sich der Wollfaden wieder ganz entfärbt hat (durch Erhitzen auf 70 C). Dann wird der Wollfaden entfernt und die Lösung erhitzt, damit sie auf einige ml konzentriert. Die konzentrierte Probe wird mittels Dünnschicht-Chromatographie qualitativ bestimmt. Dünnschichtchromatographie (DC) Die Chromatographie ist eine sehr leistungsfähige und verbreitete Trennmethode. Sie wurde erstmals vom russichen Botaniker Tswett 1903 zur Trennung von Blattfarbstoffen angewendet (chroma, gr. = Farbe). Für die Dünnschichtchromatographie verwendet man Plättchen aus Kunststoff, Aluminium oder Glas, die mit einer dünnen Schicht eines sehr feinkörnigen Stoffes (z.b. Kieselgel- oder Alumiumoxidpulver) beschichtet sind. Diese Schicht nennt man stationäre Phase. Das zu trennende Gemisch wird nun in der Nähe des unteren Randes des Plättchens punktförmig aufgetragen. Anschliessend wird das Plättchen in ein Gefäss gestellt, das eine geringe Menge Flüssigkeit enthällt. Diese Flüssigkeit bezeichnet man als Fliessmittel oder mobile Phase. Der Füllstand muss tiefer als der aufgetragenen Punkt auf dem Kieselgel sein, damit das Fliessmittel das unbekannte Gemisch nicht auflöst. Das Fliessmittel steigt nun durch die Kapilarkraft in der Schicht hoch. Sobald die Flüssigkeit den Gemischfleck erreicht hat, sind die Teilchen des Gemisches der Anziehungskraft der stationären Phase einerseits und der Anziehungskraft der mobilen Phase andererseits ausgesetzt. Je nach Kräfteverhältnis bleibt ein Teilchen eher am Startpunkt oder es wandert eher mit der mobilen Phase nach oben. HS
9 Die Kräfte und somit das Wanderverhalten eines Teilchens hängen sowohl von der Art des Schichtmaterials und des Fliessmittels, als auch von der Art des Teilchens ab. In den meisten Fällen lassen sich Schichtmaterialien und Fliessmittelgemische so kombinieren, dass die verschiedenen Teilchensorten eines Gemisches verschieden weit wandern, sodass sie sich voneinander trennen lassen. HS
Kapitel 4: Lebensmittelfarbstoffe
 Kapitel 4: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
Kapitel 4: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe.
 2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
Theorie der Farbigkeit
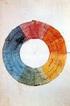 1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
Probe- und Vergleichslösungen: Trennschicht (stationäre Phase): Kieselgel. Fließmittel (mobile Phase):
 , der Allrounder aus dem Supermarkt Welche Zucker sind in enthalten? Nachweis mittels Dünnschichtchromatografie (DC) [6] 27.06.03 / 04.07.03 Jessica Bornemann Grundlagen: Für die DC verwendet man Kunststofffolien,
, der Allrounder aus dem Supermarkt Welche Zucker sind in enthalten? Nachweis mittels Dünnschichtchromatografie (DC) [6] 27.06.03 / 04.07.03 Jessica Bornemann Grundlagen: Für die DC verwendet man Kunststofffolien,
Farbigkeit bei Molekülen Fluoreszenz Phosphoreszenz
 Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Farbstoffe Zusammenfassung Klausur K2
 Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009
 Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 06.03.2009 Assistent: Esther Amstad E-Mail: zclaudio@student.ethz.ch
Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 06.03.2009 Assistent: Esther Amstad E-Mail: zclaudio@student.ethz.ch
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
Synthese des Azofarbstoff Orange II
 ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
5 Elektronenübergänge im Festkörper
 5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
Organisch-chemisches Praktikum Wintersemester 2005/06. o-chlortoluen. Stephan Steinmann
 rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
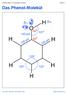 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Thema 12 Lebensmittelfarbstoffe
 Thema 12 Lebensmittelfarbstoffe Anna Bella Rohweder Inhalt: 1. Lebensmittelfarbstoffe S. 2 2. Farbigkeit S. 3 Über die Eigenschaften von Licht S. 3 Anregung von Elektronen S. 4 Absorption von Lichtquanten
Thema 12 Lebensmittelfarbstoffe Anna Bella Rohweder Inhalt: 1. Lebensmittelfarbstoffe S. 2 2. Farbigkeit S. 3 Über die Eigenschaften von Licht S. 3 Anregung von Elektronen S. 4 Absorption von Lichtquanten
Arbeitsblatt Wie entstehen Farben?
 Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Photochemische Umlagerung von Azobenzen
 Photochemische Umlagerung von Azobenzen Theorie Das Molekül Azobenzol wurde im Jahre 1863 entdeckt und bildet das Grundgerüst für die große Gruppe der Azofarbstoffe mit ihrer ungeheuren Vielfalt von Anwendungen.
Photochemische Umlagerung von Azobenzen Theorie Das Molekül Azobenzol wurde im Jahre 1863 entdeckt und bildet das Grundgerüst für die große Gruppe der Azofarbstoffe mit ihrer ungeheuren Vielfalt von Anwendungen.
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53
 Endersch, Jonas 13.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.5: Dünnschicht und Säulenchromatographie Einleitung und Theorie In diesem Versuch wurden
Endersch, Jonas 13.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.5: Dünnschicht und Säulenchromatographie Einleitung und Theorie In diesem Versuch wurden
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Konzentrationsbestimmung mit Lösungen
 Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
(±)-4-Methyl-3- heptanon
 Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Synthese von Diphenylmethanol
 FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
Die Primärreaktion der Photosynthese
 Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
Die Primärreaktion der Photosynthese
 Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
Schulversuchspraktikum. Anna Hille. Sommersemester Klassenstufen 11 & 12. Farbstoffe
 Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 11 & 12 Farbstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet zwei Lehrerversuche
Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 11 & 12 Farbstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet zwei Lehrerversuche
Coffeincitrat Coffeini citras Synonym: Coffeinum citricum
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
Nachweis von Nitrit und Nitrat
 Name: Datum: Nachweis von Nitrit und Nitrat Geräte Spatel, gekühlte Tüpfelplatte, Trichter, Faltenfilter, 1 Reagenzglas, Reagenzglasständer, Plastikschüssel mit Eis, Mörser mit Pistill Materialien Spinat,
Name: Datum: Nachweis von Nitrit und Nitrat Geräte Spatel, gekühlte Tüpfelplatte, Trichter, Faltenfilter, 1 Reagenzglas, Reagenzglasständer, Plastikschüssel mit Eis, Mörser mit Pistill Materialien Spinat,
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Wir untersuchen das Grün der Blätter
 Naturwissenschaften Kantonsschule Freudenberg Wir untersuchen das Grün der Blätter Messzylinder: Mörser: 1. Schritt: Farbe aus grünen Blättern extrahieren Jede Gruppe wählt im Park eine andere Pflanze
Naturwissenschaften Kantonsschule Freudenberg Wir untersuchen das Grün der Blätter Messzylinder: Mörser: 1. Schritt: Farbe aus grünen Blättern extrahieren Jede Gruppe wählt im Park eine andere Pflanze
Herstellung des Benzoldiazoniumchlorids aus Anilin, Natriumnitrit und Salzsäure. Benzoldiazonium-Ion
 Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Synthese von Acetylsalicylsäure (Aspirin)
 1 Grundlagen 1.1 Einleitung Synthese von Acetylsalicylsäure (Aspirin) von HRISTPH KÖLBL Acetylsalicylsäure, ist eines der weit verbreiteten Schmerz- und Entzündungshemmenden Mittel. Bekannt wurde Acetylsalicylsäure
1 Grundlagen 1.1 Einleitung Synthese von Acetylsalicylsäure (Aspirin) von HRISTPH KÖLBL Acetylsalicylsäure, ist eines der weit verbreiteten Schmerz- und Entzündungshemmenden Mittel. Bekannt wurde Acetylsalicylsäure
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Dünnschichtchromatographische Auftrennung von Salbeiöl
 Dünnschichtchromatographische Auftrennung von Salbeiöl Inhaltsverzeichnis - Einleitung - Material & Methoden - Versuchsdurchführung - Ergebnisse - Diskussion - Quellenangabe Einleitung Ätherische Öle:
Dünnschichtchromatographische Auftrennung von Salbeiöl Inhaltsverzeichnis - Einleitung - Material & Methoden - Versuchsdurchführung - Ergebnisse - Diskussion - Quellenangabe Einleitung Ätherische Öle:
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Wie zählen wir Mengen in der Chemie? Stefan
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Wie zählen wir Mengen in der Chemie? Stefan
Versuch VI.2: Komplexchemie des Nickels Auswertung von Lars Müller
 Name: Lars Müller Gruppe: Donati (HCI J196/168) Datum: 15. Jan. 2004 Versuch VI.2: Komplexchemie des ckels Auswertung von Lars Müller Ziel ckel(ii) kann sehr verschiedene Metallkomplexe bilden, die meist
Name: Lars Müller Gruppe: Donati (HCI J196/168) Datum: 15. Jan. 2004 Versuch VI.2: Komplexchemie des ckels Auswertung von Lars Müller Ziel ckel(ii) kann sehr verschiedene Metallkomplexe bilden, die meist
Chemie-Labothek zur Photochemie
 Fluoreszenz und Phosphoreszenz, Echtfarbenemissionsspektren (EFES) V1: Fluoreszenz und Phosphoreszenz Arbeitsmaterialien: Waage Mörser mit Pistill Porzellanschale Bunsenbrenner UV-Handlampe 7 Reagenzgläser
Fluoreszenz und Phosphoreszenz, Echtfarbenemissionsspektren (EFES) V1: Fluoreszenz und Phosphoreszenz Arbeitsmaterialien: Waage Mörser mit Pistill Porzellanschale Bunsenbrenner UV-Handlampe 7 Reagenzgläser
Dünnschichtchromatographie
 PB III/Seminar DC Dünnschichtchromatographie Dr. Johanna Liebl Chromatographie - Prinzip physikalisch-chemische Trennmethoden Prinzip: Verteilung von Substanzen zwischen einer ruhenden (stationären) und
PB III/Seminar DC Dünnschichtchromatographie Dr. Johanna Liebl Chromatographie - Prinzip physikalisch-chemische Trennmethoden Prinzip: Verteilung von Substanzen zwischen einer ruhenden (stationären) und
Endersch, Jonas 26./ Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 26./27.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.4a: Herstellung von 2,5 Dibrombenzochinon Reaktionsgleichung: Einleitung und Theorie: In diesem
Endersch, Jonas 26./27.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.4a: Herstellung von 2,5 Dibrombenzochinon Reaktionsgleichung: Einleitung und Theorie: In diesem
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
3 Elektronengas-Modell und Polyene
 3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
D-(+)-Biotin (Vitamin H)
 D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
8. Löslichkeit verschiedener Salze bestimmen
 Praktikum Chemie N 8 Classe : Date de la remise : Note sur 10 : Nom(s) : 8. Löslichkeit verschiedener Salze bestimmen Video Löslichkeit Die Löslichkeit eines Stoffes gibt an, in welchem Umfang ein Reinstoff
Praktikum Chemie N 8 Classe : Date de la remise : Note sur 10 : Nom(s) : 8. Löslichkeit verschiedener Salze bestimmen Video Löslichkeit Die Löslichkeit eines Stoffes gibt an, in welchem Umfang ein Reinstoff
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
Synthese: Triphenylcarbinol
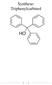 Synthese: Triphenylcarbinol 1 Inhaltsverzeichnis Synthese von Triphenylcarbinol 1.1 Allgemeine Angaben..... 3 1.2 Strukturformel...3 1.3 Reaktionsgleichung.......3 1.4 Ansatz........4 1.5 Ausbeuteberechnung.4
Synthese: Triphenylcarbinol 1 Inhaltsverzeichnis Synthese von Triphenylcarbinol 1.1 Allgemeine Angaben..... 3 1.2 Strukturformel...3 1.3 Reaktionsgleichung.......3 1.4 Ansatz........4 1.5 Ausbeuteberechnung.4
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Station 6: Aktivkohle macht s sauber! Ein Experiment
 Station 6: Aktivkohle macht s sauber! Ein Experiment Material: 1 Calcium-Brausetablette 4 Bechergläser (100 ml) Wasser Teelöffel (TL) Esslöffel (EL) Aktivkohle 3 Filter 3 Trichter 2 Abwurfbehälter (1 l)
Station 6: Aktivkohle macht s sauber! Ein Experiment Material: 1 Calcium-Brausetablette 4 Bechergläser (100 ml) Wasser Teelöffel (TL) Esslöffel (EL) Aktivkohle 3 Filter 3 Trichter 2 Abwurfbehälter (1 l)
Fette, Öle und Tenside
 Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
Herstellung von Azofarbstoffen und Färben von Textilien
 Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Stark konz., Fluoreszierend
 hemie-protokoll 28.10.02, Seite 1 von 5 Lukman Iwan, 30.10.02 Stundenprotokoll vom Montag, 28. Oktober 2002 Es fehlen: keine VB: Lösungsmittel Extraktfarbe VD: Ethanol (Brennspiritus) Blaugrün, Stark konz.,
hemie-protokoll 28.10.02, Seite 1 von 5 Lukman Iwan, 30.10.02 Stundenprotokoll vom Montag, 28. Oktober 2002 Es fehlen: keine VB: Lösungsmittel Extraktfarbe VD: Ethanol (Brennspiritus) Blaugrün, Stark konz.,
Versuche zum Thema Aminosäuren
 Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung)
 Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Synthese von 3-Aminophthalsäurehydrazid
 Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Benzol-d. Illumina-Chemie.de - Artikel
 Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
Lehrerinformation Brillantblau
 Lehrerinformation: Allgemeines zu Triarylmethylfarbstoffen Viele Gegenstände, mit denen wir tagtäglich in Berührung kommen, sind farbig. Letztlich ist aber all diese Farbenpracht auf die chemischen Verbindungen
Lehrerinformation: Allgemeines zu Triarylmethylfarbstoffen Viele Gegenstände, mit denen wir tagtäglich in Berührung kommen, sind farbig. Letztlich ist aber all diese Farbenpracht auf die chemischen Verbindungen
Welche Aufgaben haben Fette im Körper?
 Einleitung Welche Aufgaben haben Fette im Körper? 1 Fette... Einleitung Welche Aufgaben haben Fette im Körper? 2 Fette... sind wichtige Energielieferanten (38-39 kj/g) Einleitung Welche Aufgaben haben
Einleitung Welche Aufgaben haben Fette im Körper? 1 Fette... Einleitung Welche Aufgaben haben Fette im Körper? 2 Fette... sind wichtige Energielieferanten (38-39 kj/g) Einleitung Welche Aufgaben haben
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Extraktionen von Naturstoffen in Bildern: Eugenol und Eugenolacetat
 Extraktionen von Naturstoffen in Bildern: Eugenol und Eugenolacetat Hier wird die Extraktion von Eugenol und Eugenolacetat aus Gewürznelken dokumentiert. Genaue Extraktionsvorschrift: siehe Lambdasyn.
Extraktionen von Naturstoffen in Bildern: Eugenol und Eugenolacetat Hier wird die Extraktion von Eugenol und Eugenolacetat aus Gewürznelken dokumentiert. Genaue Extraktionsvorschrift: siehe Lambdasyn.
Lichtabsorption. Handout zum Vortrag am REFERAT BIOLOGIE LEISTUNGSKURS. 11 Februar 2007 Verfasst von: Daniela Luxem
 Lichtabsorption Handout zum Vortrag am 13.02.2007 REFERAT BIOLOGIE LEISTUNGSKURS 11 Februar 2007 Verfasst von: Daniela Luxem Lichtabsorption Handout zum Vortrag am 13.02.2007 Ziel dieser Arbeit ist, den
Lichtabsorption Handout zum Vortrag am 13.02.2007 REFERAT BIOLOGIE LEISTUNGSKURS 11 Februar 2007 Verfasst von: Daniela Luxem Lichtabsorption Handout zum Vortrag am 13.02.2007 Ziel dieser Arbeit ist, den
Versuche zur Untersuchung von Fruchtfarbstoffen
 Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
5 Elektronengas-Modell und Polyene
 5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Carbonsäuren und Derivate. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
8 Stevia qualitativ aus der Pflanze extrahieren
 8 Stevia qualitativ aus der Pflanze extrahieren 8.1 Vorwort Stevia ist der mit Abstand am teuersten Zuckerersatzstoff den wir untersucht haben, deshalb beschäftigte uns die Frage, wie der hohe Preis zu
8 Stevia qualitativ aus der Pflanze extrahieren 8.1 Vorwort Stevia ist der mit Abstand am teuersten Zuckerersatzstoff den wir untersucht haben, deshalb beschäftigte uns die Frage, wie der hohe Preis zu
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Echt ätzend! - Was ist und wie wirkt Abflussreiniger?
 Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften
 Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Wie wirkt sich die Zugabe von Salz auf den Schmelz- und Siedepunkt von Wasser aus?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13
 Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
CHEMIEPRAKTIKUM SPF/EGF KANTONSSCHULE BADEN. Einleitung
 EMIEPRAKTIKUM SPF/EGF KATSSULE BADE erstellung von Indigo, Färbevorgang Einleitung Indigo ist einer der ältesten und wichtigsten aturfarbstoffe, mit dem schon vor Jahrtausenden in der ganzen Welt - in
EMIEPRAKTIKUM SPF/EGF KATSSULE BADE erstellung von Indigo, Färbevorgang Einleitung Indigo ist einer der ältesten und wichtigsten aturfarbstoffe, mit dem schon vor Jahrtausenden in der ganzen Welt - in
Synthese von 1-Amino-2-naphthol
 Illumina-Chemie.de - Artikel Synthesen Synthese von Der wohl bekannteste Weg zu einer Aminogruppe ist die Nitrierung eines Kohlenwasserstoffes und anschließende Reduktion. Reaktive Aromaten wie Phenole
Illumina-Chemie.de - Artikel Synthesen Synthese von Der wohl bekannteste Weg zu einer Aminogruppe ist die Nitrierung eines Kohlenwasserstoffes und anschließende Reduktion. Reaktive Aromaten wie Phenole
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Fluoreszenz. Abb. 1: Möglicher Versuchsaufbau
 Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Synthese von 1-(p-Tolyl)butan-1,4-diol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Chemie-Labothek zur Photochemie
 Optischer Datenspeicher auf der Basis molekularer Schalter V1: Herstellung der Spiropyran-Polystyrol-Folie (Angaben für 1 DIN A4 Folie): Arbeitsmaterialien und Chemikalien: hitzebeständige Kopierfolie
Optischer Datenspeicher auf der Basis molekularer Schalter V1: Herstellung der Spiropyran-Polystyrol-Folie (Angaben für 1 DIN A4 Folie): Arbeitsmaterialien und Chemikalien: hitzebeständige Kopierfolie
Kohlenhydrate in Lebensmitteln Schokolade ist nicht gleich Schokolade!
 Kohlenhydrate in Lebensmitteln ist nicht gleich! Einführung Sicher hast du schon davon gehört, dass es verschiedene Zuckerarten gibt. So gibt es Traubenzucker (Glucose), Fruchtzucker (Fructose) und natürlich
Kohlenhydrate in Lebensmitteln ist nicht gleich! Einführung Sicher hast du schon davon gehört, dass es verschiedene Zuckerarten gibt. So gibt es Traubenzucker (Glucose), Fruchtzucker (Fructose) und natürlich
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
