Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe.
|
|
|
- Gertrud Peters
- vor 7 Jahren
- Abrufe
Transkript
1 2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die größte und bedeutendste Farbstoffgruppe dar. Ihr einfachster Vertreter ist das Azobenzol dessen langwelligster π - π*-übergang bei λ max = 33 nm liegt. Wegen der n-π*-übergänge im sichtbaren Bereich erscheint die Substanz allerdings orange gefärbt. Durch Einführung von auxochromen und antiauxochromen Gruppen wird die intensive π - π*-bande in den sichtbaren Bereich verschoben. Dann wird die Farbe im wesentlichen vom π - π*-übergang -Übergang bestimmt, da dieser sehr viel intensiver ist als der n-π*-übergang. Auf diese Weise erzielt man aber meist nur Lichtabsorptionen im kurzwelligen Bereich des sichtbaren Lichtes, so dass diese Azoverbindungen meist gelb, orange oder allenfalls rot aussehen. Durch Einführung mehrerer Azogruppen, die möglichst über aphthalinringe verknüpft sein sollen, lässt sich das delokalisierte π-system soweit ausdehnen, dass man auch blaue, grüne und sogar schwarze Azofarbstoffe erhält. Es liegen dann meist mehrere π - π*-übergänge im sichtbaren Bereich vor. Azokupplungsreaktion - Diazotierung und Kupplung Die Synthese der Azofarbstoffe geschieht meist über die Azokupplungsreaktion, bei der man zunächst ein Diazoniumsalz herstellt. Dieses Diazonium-Ion ist in der Lage, in einer Kupplungsreaktion (elektrophile Substitution) mit Aromaten zu reagieren. Aus atriumnitrit (ao 2 ) und H 3 O + -Ionen bildet sich die salpetrige Säure HO 2, die durch Protonierung und Wasserabspaltung zum O + -Ion (itrosyl-ion) wird.
2 2. Azofarbstoffe 2.2 Kurzform: + H + H 2 + HO H 2 O Anilin Salpetrige Säure Diazonium-Ion Diazotierung Da im Diazoniumkation die Struktur des stabilen molekularen Stickstoffs bereits vorgebildet" ist, spaltet dies leicht Stickstoff ab, wobei ein Carbeniumion entsteht, das dann weitere Reaktionen eingehen kann (Addition eines ucleophils, Eliminierung, Umlagerung usw.): Dies tritt immer ein, wenn R ein aliphatischer Rest ist, so dass aliphatische Diazoniumsalze praktisch nicht isolierbar sind. Ist R hingegen ein aromatischer Rest, so wird das Diazoniumkation durch die Konjugation der --π-elektronen mit dem aromatischen π-system mesomeriestabilisiert, so dass aromatische Diazoniumsalze unterhalb 5 C stabil sind. (Bei Temperaturen oberhalb 5 C findet Stickstoffabspaltung unter Bildung von Phenol in wässriger Lösung statt.) Das Diazoniumsalz besitzt am endständigen Stickstoffatom elektrophile Eigenschaften (Elektronenmangel), wie aus der Grenzstruktur II ersichtlich wird. Zu beachten ist, dass für die elektrophilen Eigenschaften nicht die Ladung, sondern das Elektronendefizit maßgebend ist. Aus diesem Grund sind die Diazoniumionen in der Lage, Aromaten unter elektrophiler Substitution anzugreifen. Wegen der starken Delokalisation der positiven Ladung (vgl. Grenzstrukturen) ist es nur ein schwaches elektrophiles Reagenz. Deshalb können nur stark aktivierte Aromaten wie z. B. aromatische Amine (starker +M-Effekt der Aminogruppe) und Phenole (starker +M-, +-Effekt des O - im Phenolatanion) mit Diazoniumionen umgesetzt werden. Die Elektrophilie des Diazoniumkations kann durch -M- und -I- Substituenten erhöht werden (z.b. O 2 usw.). Wegen der Größe des angreifenden Diazoniumions erfolgt der Angriff fast ausschließlich in para- Stellung zum Erstsubstituenten.
3 2. Azofarbstoffe 2.3 Ort der Kupplung ist ph-abhängig Für jede Kupplungsreaktion gibt es einen optimalen ph-wert. Kuppelt man mit Aminen, so arbeitet man am besten in einem ph-bereich von 4 bis 9. Im stärker sauren Bereich ist die Konzentration an freiem Amin zu gering und das protonierte Amin kann wegen des Wegfalls des + M-Effektes der ursprünglichen H 2 -Gruppe nicht angegriffen werden. Bei Phenolen als Kupplungspartner liegt der optimale ph-wert bei 9 bis 1. Das Phenolation ist wegen des starken +M- und +I-Effektes des O - wesentlich reaktiver als das Phenol selbst. Da mit steigendem ph-wert die freie Phenolationenkonzentration zunimmt, sollte die Reaktionsgeschwindigkeit mit steigendem ph-wert ansteigen. Dies nutzt man aus, wenn man aphthalinderivate, die sowohl die H 2 - als auch die OH-Gruppe enthalten, als Kupplungspartner benutzt. Bei ph 5 bis 7 dirigiert die H 2 -Gruppe, bei ph 8 bis 1 die OH-Gruppe. Azofarbstoffe als Indikatoren Manche Azofarbstoffe finden als Indikatoren Verwendung. Die Wirkung eines Indikators beruht darauf, dass Indikatorsäure und Indikatorbase unterschiedliche Farbe besitzen. Methylorange ist bei ph- Werten größer als 4 gelborange (λ max = 473 nm) gefärbt. Die zweite Grenzstruktur hat nur einen geringen Anteil an dem tatsächlichen Elektronenzustand, d. h. der Bindungsausgleich ist gering (schwache Delokalisation der π-elektronen). Bei ph-werten kleiner als 3,5 wird Methylorange an einem -Atom der Azogruppe protoniert und nimmt dabei eine rote Farbe an (λ max = 51 nm). Das protonierte Methylorange (Indikatorsäure) ist mesomeriestabilisiert, da jetzt die zweite Grenzstruktur der ersten nahezu gleichwertig ist. Das bedeutet, dass der Bindungsausgleich sehr stark ist (große Delokalisation), was nach Regel 2 eine starke bathochrome Verschiebung bewirkt.
4 2. Azofarbstoffe 2.4 Absorptionsspektren Buttergelb Absorptionsspektrum von Buttergelb (ph = 2),35,3,25,2,15,1, Absorptionsspektrum von Buttergelb (ph = 12),25,2,15,1, Methylorange Absorptionsspektrum von Methylorange (ph = 2) 1,4 1,2 1,8,6,4, Absorptionsspektrum von Methylorange (ph = 12) 1,6 1,4 1,2 1,8,6,4,
5 2. Azofarbstoffe 2.5 Weshalb sind einige Azofarbstoffe krebserzeugend? Azofarbstoffe werden zur Färbung vieler Textilien, Fette (dazu zählen auch Öle und Wachse), Stroh, Holz, Papier usw. sowie als Beschichtungsstoffe, etwa für CD-R, benutzt. Einzelne Azofarbstoffe sind als Lebensmittelfarbstoffe zugelassen. Diejenigen Azofarbstoffe, die erwiesenermaßen giftige bzw. krebserzeugende Amine freisetzen können, sind in Deutschland für Gebrauchsgegenstände wie Textilien, Schmuck oder Kosmetikartikel verboten. Des Weiteren bilden Azofarbstoffe die Grundlage für Lederfarbstoffe und finden auch einen großen Anwendungsbereich in der Medizin z.b. zum Anfärben von Krebszellen. Azofarbstoffe können aus einer Vielzahl an verschiedenen Aminen hergestellt werden. Es wurde bewiesen, dass der menschliche Körper in der Lage ist, aufgenommenen Azofarbstoff an der Azobrücke durch Darmbakterien oder Azoreduktasen der Leber wieder in die Ausgangsstoffe zu spalten. Da auch Azofarbstoffe aus karzinogenen Aminen hergestellt werden können, wurden daraufhin alle Azofarbstoffe, die aus mindestens einem dieser gesundheitsgefährdenden Aminen hergestellt wurden, in Deutschland (Bedarfsgegenständeverordnung) und später auch in der EU verboten. Durch diese Richtlinie sind zur Zeit 22 Amine verboten. Reduktive Spaltung Die Grundstruktur der Azofarbstoffe bedingt jedoch auch, dass sie durch reduktive Spaltung zu primären aromatischen Aminen gespalten werden können: O CH 3 HO O CH 3 + 4H + + 4e + H 2 H 2 HO Sudanrot G o-anisidin Beispiel eines Azofarbstoffs und seiner reduktiven Spaltung o-anisidin ist stark krebserzeugend [Krebsklasse 2 (im Tierversuch krebserzeugend)]
6 2. Azofarbstoffe 2.6 Versuche zum Thema Azofarbstoffe: Darstellung von Methylorange Becherglas (1 ml) Reagenzglas Sulfanilsäure (Xi) Dimethylanilin (T, ) Essigsäure, verd. ao2 (T) HCl, verd. aoh, verd. dest. Wasser Eine Spatelspitze Sulfanilsäure wird in dem Becherglas zu etwa 8 ml Wasser gegeben. Man versetzt mit einigen Tropfen verd. Essigsäure und fügt eine Spatelspitze atriumnitrit hinzu. In einem Reagenzglas stellt man eine Mischung aus 1 ml Dimethylanilin, einigen Tropfen verd. Salzsäure und etwa 1 ml Wasser her. Dieses Gemisch setzt man unter Umrühren langsam der Flüssigkeit im Becherglas zu. In drei Rg werden zu jeweils ca. 5 ml Wasser, bzw. aoh verd. und HCl verd. einige Tropfen des Reaktionsprodukts hinzugegeben. H 3 C CH 3 O H O S O O Sulfanilsäure H 2,-Dimethylanilin Darstellung von aphtholrot hohes Becherglas (4 ml) RG Anilin (T, ) ß-aphthol (Xn) HCl(konz) (C) ao2 aoh, verd. Eiswürfel Entsorgung: Organische Lösemittel In ein Rg gibt man etwa l ml Anilin und versetzt vorsichtig mit der gleichen Menge konzentrierter Salzsäure, fügt einige kleine Stückchen Eis zu und stellt es in das Becherglas zu Eiswasser. Zu dieser Lösung gibt man unter ständiger Kühlung portionsweise eine gut vorgekühlte Lösung aus 2 Spateln atriumnitrit in etwa 4 ml Wasser. Anschließend fügt man eine Lösung aus l Spatel ß-aphthol in l ml verdünnter atronlauge zu. H 2 OH Anilin ß-aphthol
7 2. Azofarbstoffe 2.7 Darstellung von Anilingelb hohes Becherglas (4 ml) RG Anilin (T, ) Ethanol (F) HCl(konz) (C) ao2 Eiswürfel Entsorgung: Organische Lösemittel In ein Rg. gibt man etwa l ml Anilin, versetzt vorsichtig mit der gleichen Menge konzentrierter Salzsäure und füllt mit Wasser auf die Hälfte des Rg auf. Zu dieser Lösung gibt man einige kleine Eisstückchen und stellt sie in das Becherglas zu Eiswasser. Anschließend gibt man portionsweise eine gut vorgekühlte Lösung aus 2 Spateln atriumnitrit in etwa 4 ml Wasser zu. Zu dieser Lösung gibt man eine eisgekühlte Lösung von l ml Anilin in 4 ml Ethanol. Das Gemisch wird gut durchgeschüttelt und zwischendurch wieder gekühlt (Anilin nicht mit den Fingern berühren!). H 2 Anilin Darstellung von Bismarckbraun Becherglas (1 ml) Becherglas (6 ml) RG m-phenylendiamin (T, ) HCl(konz) (C) ao2 aoh, verd. Eiswürfel Entsorgung: Organische Lösemittel l Spatel m-phenylendiamin wird im 1-ml-Becherglas zu etwa 2 ml Wasser gegeben und mit ca. 2 ml konzentrierter Salzsäure versetzt. Die entstehende Lösung wird im 6-ml-Becherglas in Eiswasser gekühlt. Im Rg wird eine Spatelspitze atriumnitrit in 1 bis 12 ml Wasser gelöst und ebenfalls im Eiswasser gekühlt. Anschließend wird die atriumnitritlösung langsam in die m-phenylendiaminlösung gerührt. Es entsteht der Farbstoff Bismarckbraun mit folgender Formel: H 2 H 2 m-phenylendiamin
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Triphenylmethanfarbstoffe
 3. Triphenylmethanfarbstoffe 3.1 Triphenylmethanfarbstoffe Diese Farbstoffklasse leitet sich vom Triphenylcarbeniumion als Chromophor ab. Durch Einführung auxochromer Gruppen in Parastellung kann man die
3. Triphenylmethanfarbstoffe 3.1 Triphenylmethanfarbstoffe Diese Farbstoffklasse leitet sich vom Triphenylcarbeniumion als Chromophor ab. Durch Einführung auxochromer Gruppen in Parastellung kann man die
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
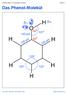 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Versuchsprotokoll. Gruppe 12, Typ: Pflichtversuch - H + Einsatz in der Schule Sulfanilsäure NH 2 C 6 H 4 SO 3 H Xi 36/38, 43 24, 37 S I
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
4. Phthaleine 4.1. Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid
 4. Phthaleine 4.1 Phthaleine Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid ausgeht. Phenolphthalein erhält man durch Zusammenschmelzen von
4. Phthaleine 4.1 Phthaleine Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid ausgeht. Phenolphthalein erhält man durch Zusammenschmelzen von
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Farbigkeit bei Molekülen Fluoreszenz Phosphoreszenz
 Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Herstellung von Azofarbstoffen und Färben von Textilien
 Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Herstellung des Benzoldiazoniumchlorids aus Anilin, Natriumnitrit und Salzsäure. Benzoldiazonium-Ion
 Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
7. Studieneinheit. Siebte Studieneinheit
 86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
Nachweis von Nitrit und Nitrat
 Name: Datum: Nachweis von Nitrit und Nitrat Geräte Spatel, gekühlte Tüpfelplatte, Trichter, Faltenfilter, 1 Reagenzglas, Reagenzglasständer, Plastikschüssel mit Eis, Mörser mit Pistill Materialien Spinat,
Name: Datum: Nachweis von Nitrit und Nitrat Geräte Spatel, gekühlte Tüpfelplatte, Trichter, Faltenfilter, 1 Reagenzglas, Reagenzglasständer, Plastikschüssel mit Eis, Mörser mit Pistill Materialien Spinat,
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Theorie der Farbigkeit
 1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
Farbstoffe Zusammenfassung Klausur K2
 Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Schulversuchspraktikum. Anna Hille. Sommersemester Klassenstufen 11 & 12. Farbstoffe
 Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 11 & 12 Farbstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet zwei Lehrerversuche
Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 11 & 12 Farbstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet zwei Lehrerversuche
Kernlehrpläne ab Schuljahr 2014/15 Schuleigener Lehrplan / FMG / Sekundarstufe II CHEMIE
 CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
Übungsaufgaben zum Kapitel Farbstoffe mit Hilfe des Lernprogramms Farbstoffermittler
 Übungsaufgaben zum Kapitel Farbstoffe mit ilfe des Tipp: Vergleiche auf der KGA-Chemie-Unterrichtsmaterialseite im Lehrplan Kapitel C 11.2 Farbstoffe - mit dem efteintrag Farbstoffe (Passwort: schuelerkga11)
Übungsaufgaben zum Kapitel Farbstoffe mit ilfe des Tipp: Vergleiche auf der KGA-Chemie-Unterrichtsmaterialseite im Lehrplan Kapitel C 11.2 Farbstoffe - mit dem efteintrag Farbstoffe (Passwort: schuelerkga11)
Grundkurs Farbstoffe 1983/II 1984/I 1984/IV 1985/IV
 Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Auswertung der Versuche mit Aminosäuren und Proteinen (Eiweiß)
 Auswertung der Versuche mit Aminosäuren und Proteinen (Eiweiß) Vorbereitung: Für die folgenden Versuche wird eine Eiweißlösung aus dem Eiklar eines ühnereis hergestellt, indem man dieses in 60 ml dest.
Auswertung der Versuche mit Aminosäuren und Proteinen (Eiweiß) Vorbereitung: Für die folgenden Versuche wird eine Eiweißlösung aus dem Eiklar eines ühnereis hergestellt, indem man dieses in 60 ml dest.
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung)
 Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
12 Organische Farbstoffe
 12 rganische Farbstoffe 12.1 Licht und Farbe vorläufige Fassung Zur Aufgabe A1 Das absorbierte Licht im Wellenlängenbereich 480 490 nm ist blau. Die Lösung hat folglich die Komplementärfarbe, d.h., sie
12 rganische Farbstoffe 12.1 Licht und Farbe vorläufige Fassung Zur Aufgabe A1 Das absorbierte Licht im Wellenlängenbereich 480 490 nm ist blau. Die Lösung hat folglich die Komplementärfarbe, d.h., sie
3. Aromatische Verbindungen Benzol(en)
 3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
Schulversuchspraktikum. Isabel Großhennig. Sommersemester Klassenstufen 11 & 12. Farbstoffe. Kurzprotokoll
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009
 Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 06.03.2009 Assistent: Esther Amstad E-Mail: zclaudio@student.ethz.ch
Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 06.03.2009 Assistent: Esther Amstad E-Mail: zclaudio@student.ethz.ch
6. Woche. Reaktionen und Nachweis der Anionen. Klasse I
 6. Woche Reaktionen und achweis der Anionen Klasse I Klassenreaktion: Die Anionen der I. Anionenklasse zeigen nach Zugabe verdünnter Salzsäure eine gut wahrnehmbare Veränderung (Gasentwicklung oder iederschlag
6. Woche Reaktionen und achweis der Anionen Klasse I Klassenreaktion: Die Anionen der I. Anionenklasse zeigen nach Zugabe verdünnter Salzsäure eine gut wahrnehmbare Veränderung (Gasentwicklung oder iederschlag
LMPG 2, ÜB21, Molekülbau & UV/VIS-Absorption LÖSUNG 1 von 11
 LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
Kapitel 11: Lebensmittelfarbstoffe
 Kapitel 11: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
Kapitel 11: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
11 Organische Farbstoffe
 Lösungen zu den Durchblick-Seiten 11.11 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 Das Phenolmolekül ist reaktiver als das unsubstituierte Benzolmolekül, da in ihm durch Mesomerie negative
Lösungen zu den Durchblick-Seiten 11.11 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 Das Phenolmolekül ist reaktiver als das unsubstituierte Benzolmolekül, da in ihm durch Mesomerie negative
3-01. Triphenylmethan
 Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Organisch-chemisches Praktikum Wintersemester 2005/06. o-chlortoluen. Stephan Steinmann
 rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
Versuchsprotokoll. ph-abhängigkeit der Getränkefarben
 AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll phabhängigkeit der Getränkefarben
AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll phabhängigkeit der Getränkefarben
Bundesrealgymnasium Imst. Chemie Klasse 8. Aromaten und deren Reaktionen
 Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Äbung Amine, Nitroverbindungen
 Ri 192 Äbung Amine, Nitroverbindungen 1. Schreiben Sie die Strukturformel fär: a) 2-Butanamin b) 2,4-Pentandiamin CH 2 CH NH 2 CH CH 2 CH NH 2 NH 2 c) N,N-Dimethyl-2-pentanamin d) 2,5-Dichlorbenzenamin
Ri 192 Äbung Amine, Nitroverbindungen 1. Schreiben Sie die Strukturformel fär: a) 2-Butanamin b) 2,4-Pentandiamin CH 2 CH NH 2 CH CH 2 CH NH 2 NH 2 c) N,N-Dimethyl-2-pentanamin d) 2,5-Dichlorbenzenamin
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau
 Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Beispiele. Polysubstituierte Benzole. Chapter 16. Organic Chemistry. Reaktionen of Substituierter Benzole. Bezeichnung durch Numerierung oder Präfix
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Beispiele Chapter 16 Reaktionen of Substituierter Benzole Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Bezeichnung durch
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Beispiele Chapter 16 Reaktionen of Substituierter Benzole Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Bezeichnung durch
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 21/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 11.2.211 Gruppe 12: Farb-, Spreng- und Wirkstoffe
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 21/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 11.2.211 Gruppe 12: Farb-, Spreng- und Wirkstoffe
Welcher Indikator ist für die Titration von Essigsäure (pks =4.76) mit Natronlauge am besten geeignet?
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
Br 1. Auch bei der folgenden Kombination, sind die Strukturen nicht identisch, sie lassen sich durch Drehung nicht ineinander überführen.
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Kunststoffe (Polykondensation)
 Kunststoffe (Polykondensation) Herstellung eines Phenoplasts 7. Stunde (13 15 14 00 Uhr) am Donnerstag, den 27. Januar 2011 Ein Chemieprotokoll von Sebastian Huber, Maximilian Mayer, Robert Bozsak und
Kunststoffe (Polykondensation) Herstellung eines Phenoplasts 7. Stunde (13 15 14 00 Uhr) am Donnerstag, den 27. Januar 2011 Ein Chemieprotokoll von Sebastian Huber, Maximilian Mayer, Robert Bozsak und
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Ableitung wieder aus einer einfachen anorganischen Verbindung, NH 3 :
 168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Dieser Schauversuch, bei dem eine Flüssigkeit mit einer Verzögerung spontan ins Sieden gerät, beruht auf einer autokalytischen Reaktion.
 Illumina-Chemie.de - Artikel Show-Experimente Dieser Schauversuch, bei dem eine Flüssigkeit mit einer Verzögerung spontan ins Sieden gerät, beruht auf einer autokalytischen Reaktion. Material/Geräte: Kelchglas
Illumina-Chemie.de - Artikel Show-Experimente Dieser Schauversuch, bei dem eine Flüssigkeit mit einer Verzögerung spontan ins Sieden gerät, beruht auf einer autokalytischen Reaktion. Material/Geräte: Kelchglas
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Versuchsprotokoll. Nitrierung von Phenol. Gruppe 4, Typ: Pflichtversuch O O - N
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Stundenübersicht über das IHF Organische Produkte Werkstoffe und Farbstoffe
 Stundenübersicht über das IHF Organische Produkte Werkstoffe und Farbstoffe Unterrichtsvorhaben I Inhaltlicher Schwerpunkt Organische Verbindungen und Reaktionswege Kontext Vom fossilen Rohstoff zum Anwendungsprodukt
Stundenübersicht über das IHF Organische Produkte Werkstoffe und Farbstoffe Unterrichtsvorhaben I Inhaltlicher Schwerpunkt Organische Verbindungen und Reaktionswege Kontext Vom fossilen Rohstoff zum Anwendungsprodukt
ATTO 565 und ATTO 590
 ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Stickstoffhaltige Verbindungen
 Stickstoffhaltige Verbindungen Nitroderivate, Amine, Diazound Azoverbindungen. Prof. Ivo C. Ivanov 1 Nitroderivate der KW CH-Acidität von Nitroverbindungen: Nitro-aci-Nitro- Tautomerie: oder: aci-form
Stickstoffhaltige Verbindungen Nitroderivate, Amine, Diazound Azoverbindungen. Prof. Ivo C. Ivanov 1 Nitroderivate der KW CH-Acidität von Nitroverbindungen: Nitro-aci-Nitro- Tautomerie: oder: aci-form
Arbeitsblatt Wie entstehen Farben?
 Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Kernlehrpläne ab Schuljahr 2014/15 Schuleigener Lehrplan / FMG / Sekundarstufe II CHEMIE
 CHEMIE QUALIFIKATIONSSPHASE 2 GRUNDKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Sequenzierung inhaltlicher Aspekte Organische Reaktionsabläufe
CHEMIE QUALIFIKATIONSSPHASE 2 GRUNDKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Sequenzierung inhaltlicher Aspekte Organische Reaktionsabläufe
Organische Chemie I Molekül der Woche - Azulen
 I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
Maßanalytische Bestimmung von Halogeniden nach Fajans
 Illumina-Chemie.de - Artikel Analytik Die Titration nach Fajans bedient sich organischer Farbstoffe als sogen. Adsorptionsindikatoren. Sie ist eine Alternative zu dem Vorgehen nach Mohr. Außerdem wird
Illumina-Chemie.de - Artikel Analytik Die Titration nach Fajans bedient sich organischer Farbstoffe als sogen. Adsorptionsindikatoren. Sie ist eine Alternative zu dem Vorgehen nach Mohr. Außerdem wird
H1 Bestimmung des Löslichkeitsprodukts von Magnesiumhydroxid
 H Löslichkeitsprodukt und Komplexgleichgewichte Auch bei den Komplex-Reaktionen beschäftigen wir uns im Wesentlichen mit Gleichgewichtsreaktionen, in denen Liganden ausgetauscht werden. Dabei sollen Kriterien
H Löslichkeitsprodukt und Komplexgleichgewichte Auch bei den Komplex-Reaktionen beschäftigen wir uns im Wesentlichen mit Gleichgewichtsreaktionen, in denen Liganden ausgetauscht werden. Dabei sollen Kriterien
Junior-Laborführerschein für die Orientierungsstufe
 Junior-Laborführerschein für die Orientierungsstufe Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in
Junior-Laborführerschein für die Orientierungsstufe Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
Synthese von 3-Aminophthalsäurehydrazid
 Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Kapitel 4: Lebensmittelfarbstoffe
 Kapitel 4: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
Kapitel 4: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
VO-5. Organische Chemie 2. Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria.
 VO-5 Organische Chemie 2 Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria. wolfgang.schoefberger@jku.at 89 Mesomerer Effekt verringert die
VO-5 Organische Chemie 2 Priv. Doz. DI Dr. Wolfgang Schoefberger Johannes Kepler Universität Linz Altenberger Str. 69, 4040 Linz, Austria. wolfgang.schoefberger@jku.at 89 Mesomerer Effekt verringert die
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Versuch: Nachweis von Salicylsäure
 Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß. Schulversuch-Protokoll Jan gr.
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
Schulversuch (Gruppe 6/Assistentenversuch): Vergleich aliphatischer Alkohole und Phenole
 Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P )
 Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Protokoll für den 6. Praktikumstag
 Protokoll für den 6. Praktikumstag http://www.biomedizinischechemie.de Autor: Werner Schwalbach Version 2.0 Quellen: Anorganisches Grundpraktikum kompakt von Gertrud Kiel Versuch 4.1 des Permanganations
Protokoll für den 6. Praktikumstag http://www.biomedizinischechemie.de Autor: Werner Schwalbach Version 2.0 Quellen: Anorganisches Grundpraktikum kompakt von Gertrud Kiel Versuch 4.1 des Permanganations
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Reak%onen an der Carbonylgruppe
 Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Dietikon, 3. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Dietikon, 3. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
AnC I Protokoll: 5.5 Simultanbestimmung von Bi/Pb! SS Analytische Chemie I. Versuchsprotokoll. 5.5 Simultanbestimmung von Bi/Pb
 Analytische Chemie I Versuchsprotokoll 5.5 Simultanbestimmung von Bi/Pb.! Theoretischer Hintergrund Bi 3+ und Pb 2+ werden nebeneinander bestimmt. Bismut(III) bildet bereits im Sauren einen EDTA-Komplex,
Analytische Chemie I Versuchsprotokoll 5.5 Simultanbestimmung von Bi/Pb.! Theoretischer Hintergrund Bi 3+ und Pb 2+ werden nebeneinander bestimmt. Bismut(III) bildet bereits im Sauren einen EDTA-Komplex,
4. Anorganisch-chemische Versuche
 4. Anorganisch-chemische Versuche o 4.4 Redoxreaktionen 4.4.1 Reduktion von Mangan(VII) in schwefelsaurer Lsg. 4.4.2 Oxidation von Mangan(II) in salpetersaurer Lsg. 4.4.3 Oxidation von Chrom(III) in alkalischer
4. Anorganisch-chemische Versuche o 4.4 Redoxreaktionen 4.4.1 Reduktion von Mangan(VII) in schwefelsaurer Lsg. 4.4.2 Oxidation von Mangan(II) in salpetersaurer Lsg. 4.4.3 Oxidation von Chrom(III) in alkalischer
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Synthese des Azofarbstoff Orange II
 ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
Prüfungsaufgaben von und zu Aromaten (incl. Aryldiazoniumsalzen)
 Prüfungsaufgaben von und zu Aromaten (incl. Aryldiazoniumsalzen) Die Aufgaben lehnen sich an Prüfungsaufgaben aus der Abschlussprüfung für Chemielaboranten der vergangenen Jahre an. äufig erstrecken sich
Prüfungsaufgaben von und zu Aromaten (incl. Aryldiazoniumsalzen) Die Aufgaben lehnen sich an Prüfungsaufgaben aus der Abschlussprüfung für Chemielaboranten der vergangenen Jahre an. äufig erstrecken sich
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
