11 Organische Farbstoffe
|
|
|
- Robert Adler
- vor 6 Jahren
- Abrufe
Transkript
1 Lösungen zu den Durchblick-Seiten Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 Das Phenolmolekül ist reaktiver als das unsubstituierte Benzolmolekül, da in ihm durch Mesomerie negative Teilladungen in den ortho-positionen und in der para-position vorliegen: O O O O Die Kupplungsreaktion ist eine elektrophile Substitution. Die negativen Teilladungen begünstigen den elektrophilen Angriff des Diazoniumions. Im alkalischen Milieu liegt Phenol hauptsächlich als Phenolation vor. Dessen negative Ladung ist durch Mesomerie über den aromatischen Ring verteilt, mit Schwerpunkten in den ortho-positionen und in der para-position: O O O O A2 Gelbliche Wäsche absorbiert blaues Licht. Wäscheblau absorbiert zusätzlich Licht der Komplementärfarbe. Die Wäsche ist daher insgesamt nicht mehr gelblich, aber sie reflektiert trotzdem nicht mehr alles Licht und sieht grau aus. Optische Aufheller absorbieren (unsichtbares) UV-Licht und fluoreszieren blau, d. h., sie ersetzen das durch die gelbliche Wäsche absorbierte Licht. Im Idealfall sieht die Wäsche weiß aus. Zusatzinformationen zu A2: Fluoreszenz ist die Eigenschaft von Stoffen, innerhalb von bis 10 7 Sekunden nach Anregung durch Licht die absorbierte Energie in Form von Strahlung gleicher oder längerer Wellenlänge wieder abzu geben. Optische Aufheller bewirken eine Aufhellung und täuschen gleichzeitig eine Bleichwirkung vor, indem sie UV-Licht (z. B. von der Sonne oder auch einem Schwarzlicht ) absorbieren und die Energie als schwach bläuliche Fluoreszenz abstrahlen, also in der Komplementärfarbe der Vergilbung. An optische Aufheller werden hohe Anforderungen gestellt. Sie müssen waschecht und beständig gegenüber Schweiß, hohen Temperaturen und Sonnenlicht sein. Außerdem kann nicht jeder optische Aufheller jedem Material zugesetzt werden. Die Einsatz gebiete sind vielfältig: Man verwendet optische Aufheller z. B. zum Weißtönen von Baumwolle, Zellwolle, Papier, Wolle, Synthesefasern, Kunststoffen, Wachsen, Seifen, Wäsche steifen, Druck farben und Fotopapieren. Allerdings ist ihr Einsatz zur Lebensmittelschönung verboten. Die vermutete Cancerogenität hat sich aber im Einzelnen nicht bestätigen lassen. Die meisten optischen Aufheller sind Derivate des Stilbens (1,2-Diphenylethen) oder analoge Verbindungen wie heteraromatische Systeme, die über eine Ethenbrücke verbunden sind. Ein Beispiel ist die Flavonsäure (4,4 -Diamino-2,2 -stilbendisulfonsäure), deren Derivate zum Weißtönen von Textilien eingesetzt werden. 1 Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
2 A3 a) Die Rylen-Farbstoffmoleküle können als miteinander verbundene aphthalinmoleküle betrachtet werden. Alternativ könnte man sie auch als Ausschnitte aus einem Graphenmolekül ansehen. Die Moleküle sind ebene Plättchen. Die Elektronen der (formalen) Doppelbindungen scheinen über das gesamte Molekül delokalisiert zu sein. Die drei abgebildeten Moleküle unterscheiden sich in der Anzahl der aphthalin-einheiten. Folglich unterscheiden sich die drei abgebildeten Moleküle durch die Fläche, die den delokalisierten Elektronen zur Verfügung steht. b) Bei den abgebildeten Molekülen nimmt die Wellenlänge der absorbierten Strahlung mit der Größe des delokalisierten Elektronensystems zu. Dies entspricht dem Merksatz in Kap. 11.4: Je ausgedehnter das delokalisierte Elektronensystem ist, desto kleiner ist die Energie der absorbierten Photonen und desto größer folglich die Wellenlänge der absorbierten Strahlung. c) Je tiefer ein Ton ist, desto größer ist die Wellenlänge der entsprechenden Schwingung, z. B. der Schwingung einer Saite. Aus diesem Grund hat eine Bratsche längere Saiten als eine Violine, und ein Violoncello hat noch längere Saiten. Außerdem ist bei tieferen Tönen (größeren Wellenlängen) der notwendige Resonanzkörper größer. Bei den Molekülen wird, je ausgedehnter (länger) das delokalisierte Elektronensystem ist, Licht größerer Wellenlängen absorbiert. inweis: Man kann dies mit dem Modell des Elektrons im eindimensionalen Kasten erklären, siehe Kap A4 a) O 3 S ao 2 Cl (aq) ao (aq) O Sulfanilsäure (4-Aminobenzolsulfonsäure) 6-ydroxy-naphthalinsulfonsäure atriumnitrit verd. Salzsäure verd. atronlauge inweis: Die amen der beiden organischen Ausgangsstoffe müssen hier nicht genannt werden; zur Lösung der Aufgabe genügen die Strukturformeln. 2 Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
3 b) Bildung der itrosylkations: Diazotierung: O 3 S + O + O 3 S + 2 O Azokupplung: O O O 3 S + O 3 S + eutralisation: O O O 3 S + 2 ao O 3S + 2 a O Bildung des itrosylkations: Das itration wird in der Salzsäure protoniert; es entsteht ein itrosylkation. Diazotierung: Das itrosylkation greift die Aminogruppe der Sulfanilsäure elektrophil an, sodass ein aromatisches itrosamin entsteht. Dieses wird in der sauren Lösung protoniert. In einer Eliminierungsreaktion wird dann ein Wassermolekül abgespalten; es bildet sich ein aromatisches Diazoniumion. Azokupplung: Das Diazoniumion reagiert in einer elektrophilen Substitution mit einem Molekül der 6-ydroxy-naphtalin-2-sulfonsäure. Anhand mesomerer Grenzformeln kann man zeigen, dass das als Zwischenprodukt entstehende Carbokation am stabilsten ist, wenn die Substitution in ortho-position zur O-Gruppe stattfindet. Die Substitution der para-position ist durch den zweiten Ring blockiert. (Als weiteres Produkt wäre ein Molekül zu erwarten, bei dem die andere ortho-position angegriffen wird. Allerdings lägen dann der Phenylring und die Sulfonsäuregruppe auf derselben Seite; dies ist evtl. räumlich ungünstig.) c) O O 3 S 3 Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
4 A5 5.1 Absorptionsspektrum: 0,7 E 0,6 0,5 0,4 0,3 0,2 0,1 0,0 450 l in nm Aus dem Absorptionsspektrum (oder aus der Wertetabelle): Das Absorptionsmaximum des Farbstoffs liegt bei l = 555 nm. Die Farbe des Farbstoffs ist Purpur (Magenta) bis Violett. Begründung: Der Farbstoff absorbiert hauptsächlich Licht im Bereich zwischen ca. 500 und 580 nm. Das übrige Licht addiert sich zu Licht der genannten Farbe. 5.3 Auftragung der Extinktion gegen die Konzentration und Ermittlung einer Ausgleichsgeraden: 0,8 E 0,7 0,6 0,5 0,4 0,3 Probelösung 0,2 0,1 0,0 c in 10 5 mol/l 0,0 0,5 1,0 1,5 2,0 a) Die Konzentration der Probelösung kann grafisch ermittelt werden. Sie ist c = 1, mol/l. b) Da die Schichtdicke d = 1 cm ist, entspricht die Steigung der Ausgleichsgerade dem molaren Extinktionskoeffizienten: e = 0, l/(mol cm) = 3, l/(mol cm) 4 Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
5 inweis: Mit dem Ergebnis der Teilaufgabe 5.3b kann man die Konzentration der Probelösung auch nach dem Lambert-Beer-Gesetz berechnen: c = E e d = 0,37 0, l/(mol cm) 1 cm = 1, mol/l 5.4 Der Transmissionsgrad bzw. die Extinktion einer Lösung bei einer bestimmten Wellenlänge hängt von den Konzentrationen der gelösten Farbstoffteilchen ab, die Licht dieser Wellenlänge absorbieren. Wenn nur ein Farbstoff gelöst ist, kann man über die Messung der Extinktion seine Konzentration bestimmen. Als Messgerät verwendet man ein Spektralfotometer. Es besteht aus den folgenden auptkomponenten: Strahlungsquelle (Lichtquelle) Eintrittsblende Monochromator: Bauteil, das nur Licht einer bestimmten (aber einstellbaren) Wellenlänge durchlässt, d. h. monochromatisches Licht erzeugt Küvette: Durchsichtiges Gefäß für die Probenlösung, das vom monochromatischen Licht durchstrahlt wird. Die Länge des Lichtwegs durch die Lösung in der Küvette bezeichnet man als Schichtdicke d. Austrittsblende Strahlungsempfänger (z. B. Fotozelle) Der Transmissionsgrad t ist der Quotient aus durchgelassener und eingestrahlter Lichtintensität. Die Extinktion E ist der negative dekadische Loraithmus des Transmissionsgrads t. ach dem Lambert-Beer-Gesetz ist (bei konstanter Schichtdicke d) die Extinktion E proportional zur Konzentration c des Farbstoffs. Bei der Fotometrie geht man folgendermaßen vor: Zunächst wird ein Absorptionsspektrum der Farbstofflösung aufgenommen, d. h., man misst die Extinktion abhängig von der Wellenlänge und trägt diese in einem Diagramm auf. Aus diesem Absorptionsspektrum wählt man eine Wellenlänge aus, bei der die Extinktion einen hohen Wert hat. Dann setzt man mehrere Lösungen mit bekannten Konzentrationen an und misst deren Extinktionen bei der ausgewählten Wellenlänge. In einem Diagramm trägt man die Extinktion gegen die Konzentration auf und ermittelt eine Kalibriergerade. un misst man die Extinktion einer Lösung des Farbstoffs, deren Konzentration man ermitteln will. Anhand der Kalibriergeraden kann man aus der Extinktion die Konzentration bestimmen. Alternativ kann man aus der Steigung der Kalibriergeraden den molaren Extinktionskoeffizienten bestimmen und dann die Konzentration der Probelösung nach dem Lambert-Beer-Gesetz berechnen (siehe inweis zur Teilaufgabe 5.3). 5 Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
6 A6 6.1 a) Methylviolett gehört zur Klasse der Triphenylmethanfarbstoffe. b) Einige Grenzformeln von Methylviolett: Die Grenzformeln zeigen, dass ein großes delokalisiertes Elekronensystem besteht. Die Methylbzw. Dimethylaminogruppen wirken durch ihren +M-Effekt als auxochrome Gruppen, indem sie die positive Ladung am zentralen C-Atom aufnehmen. Ein so großes delokalisiertes Elekronensystem kann durch elektromagnetische Strahlung im sichtbaren Bereich angeregt werden. Das Molekül absorbiert also Licht und ist daher farbig. inweis: Da die auxochromen Gruppen gleich bzw. zueinander sehr ähnlich sind, absorbiert das System bei besonders großen Wellenlängen, ähnlich wie z. B. Phenolphthalein oder Bromthymolblau in alkalischer Lösung (siehe Kap im Schülerbuch). 6.2 In neutraler Lösung ist die Farbstofflösung blauviolett. Aus dem Farbkreis (Kap. 11.2, B3) ergibt sich, dass hauptsächlich Licht der Komplementärfarbe Gelb absorbiert wird, also im Bereich nm. (inweis: Das Absorptionsmaximum liegt bei ca. 580 nm.) In stark saurer Lösung ist die Farbstofflösung gelb. Aus dem Farbkreis ergibt sich, dass hauptsächlich Licht der Komplementärfarbe Blauviolett absorbiert wird, also im Bereich nm. (inweis: Das Absorptionsmaximum liegt bei ca. 430 nm.) In schwach saurer Lösung ist die Farbstofflösung grün. Die Komplementärfarbe dazu ist Magenta; sie entspricht aber keinem Wellenlängenbereich des Lichts. Am Spektrum des sichtbaren Lichts (Kap. 11.2, B2) kann man aber erkennen, dass sich die Farbe Grün ergibt, wenn das Licht im Bereich unter ca. 500 nm und über ca. 600 nm absorbiert wird. Das Absorptionsspektrum der grünen Farbstofflösung hat folglich zwei Bereiche mit hoher Extinktion. (inweis: Die Absorptionsmaxima liegen bei ca. 420 nm und ca. 620 nm.) 6 Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
7 6.3 Beim Ansäuern werden die Farbstoffmoleküle an den Stickstoffatomen protoniert: + + violett grün gelb Bei jeder Protonierung eines Stickstoffatoms entfällt ein freies Elektronenpaar und damit eine eine auxochrome Gruppe mit +M-Effekt. Dadurch ändert sich die Farbe. inweis: Man könnte zunächst vermuten, dass jede dieser Protonierungen zu einer Verschiebung der Lichtabsorption nach kleineren Wellenlängen führt. Bei genauerer Betrachtung zeigt sich, dass es etwas komplizierter ist: Bei der violetten Form erstreckt sich das Absorptionssystem über das ganze Molekül, siehe Lösung zu 6.1b. Allerdings sind die Phenylringe aus sterischen Gründen etwas aus der Ebene gedreht (das Molekül ist verdrillt ), sodass die Elektronen der p-bindungen nicht optimal delokalisert sind. Bei der gelben Form geht das Absorptionssystem nur vom zentralen Kohlen stoff atom ( M-Effekt) bis zum unprotonierten Stickstoffatom (+M-Effekt), es ist also deutlich kleiner. Die grüne Form hat ein Absorptionsmaximum bei einer größeren Wellenlänge als die violette Form und ein zweites Absorptionsmaximum bei einer etwas kleineren Wellenlänge als die gelbe Form (siehe Lösung zu 6.2). Man kann dies folgendermaßen erklären: Bei der grünen Form ist der Phenylring mit dem protonierten Stickstoffatom stark aus der Ebene gedreht, während die beiden anderen Phenylringe annähernd in einer Ebene liegen. Das Absorptionssystem zwischen den beiden unprotonierten Stick stoff atomen hat die gleiche Länge wie das Absorp tionssystem der violetten Form und ist außerdem besser eingeebnet, d. h., die Delokalisierung der p-elektronen ist praktisch ungestört. Das System absorbiert deshalb Licht von größeren Wellenlängen als die violette Form. Der aus der Ebene herausgedrehte Phenylring bildet zusammen mit dem zentralen Kohlenstoffatom ein zweites (relativ kurzes) Absorptions system. Dieses ist für das zweite Absorptionsmaximum verantwortlich. Literatur dazu: W. Kratzert, R. Peichert: Farbstoffe. eidelberg Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
8 6.4 In alkalischer Lösung wird ein ydroxidion addiert: 3 C C 3 3 C C 3 + O 3 C C 3 3 C C 3 O C 3 C 3 violett farblos Dadurch wird das delokalisierte Elektronensystem am zentralen Kohlenstoffatom unterbrochen. Die delokalisierten Elektronensysteme der drei Phenylringe sind so klein, dass die Wellenlänge des absorbierten Lichts nicht im sichtbaren Bereich liegt. Folglich ist die Lösung farblos. 8 Elemente Chemie Oberstufe RW Ernst Klett Verlag Gmb, Stuttgart 2015
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
12 Organische Farbstoffe
 12 rganische Farbstoffe 12.1 Licht und Farbe vorläufige Fassung Zur Aufgabe A1 Das absorbierte Licht im Wellenlängenbereich 480 490 nm ist blau. Die Lösung hat folglich die Komplementärfarbe, d.h., sie
12 rganische Farbstoffe 12.1 Licht und Farbe vorläufige Fassung Zur Aufgabe A1 Das absorbierte Licht im Wellenlängenbereich 480 490 nm ist blau. Die Lösung hat folglich die Komplementärfarbe, d.h., sie
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
LMPG 2, ÜB21, Molekülbau & UV/VIS-Absorption LÖSUNG 1 von 11
 LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Farbigkeit bei Molekülen Fluoreszenz Phosphoreszenz
 Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
3-01. Triphenylmethan
 Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Arbeitsblatt Wie entstehen Farben?
 Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Farbstoffe Zusammenfassung Klausur K2
 Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
K1: Lambert-Beer`sches Gesetz
 K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Elektronenspektroskopie
 Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Farbigkeit und Theorien
 Farbigkeit und Theorien Farbigkeit von Dinah Shafry Licht ist elektromagnetische Strahlung, bei der jede Farbe eine einzelne Wellenlänge besitzt, die als unterschiedliche Farben vom Menschen wahrgenommen
Farbigkeit und Theorien Farbigkeit von Dinah Shafry Licht ist elektromagnetische Strahlung, bei der jede Farbe eine einzelne Wellenlänge besitzt, die als unterschiedliche Farben vom Menschen wahrgenommen
Physikalische Chemie: Kinetik
 Physikalische Chemie: Kinetik Prof. Thiemann SS 2002 Protokoll Versuch 2 «Die ph-abhängigkeit der Solvolysegeschwindigkeit von Malachitgrün» 1 Inhalt: 1. Theorie 2. Zusatzfragen Bau eines UV-Spektralphotometers
Physikalische Chemie: Kinetik Prof. Thiemann SS 2002 Protokoll Versuch 2 «Die ph-abhängigkeit der Solvolysegeschwindigkeit von Malachitgrün» 1 Inhalt: 1. Theorie 2. Zusatzfragen Bau eines UV-Spektralphotometers
10/6/2015. Licht IST FARBIG! DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE. Alle Objekte sind Reflektoren!
 DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE 1 WAS GENAU SIND OPTISCHE AUFHELLER? Optische Aufheller sind chemische Stoffe welche im elektromagnetischen Spektrum Licht
DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE 1 WAS GENAU SIND OPTISCHE AUFHELLER? Optische Aufheller sind chemische Stoffe welche im elektromagnetischen Spektrum Licht
Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe.
 2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
Kernlehrpläne ab Schuljahr 2014/15 Schuleigener Lehrplan / FMG / Sekundarstufe II CHEMIE
 CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Photometrie mit Pyridinnucleotiden
 Photometrie mit Pyridinnucleotiden Grundlagen der Photometrie Photometer-Arten Eppendorf-Photometer Struktur und Funktion des NADH Beispiele des optischen Tests Berechnungsverfahren Biochemie - "Photometrie
Photometrie mit Pyridinnucleotiden Grundlagen der Photometrie Photometer-Arten Eppendorf-Photometer Struktur und Funktion des NADH Beispiele des optischen Tests Berechnungsverfahren Biochemie - "Photometrie
Übungsfragen zu den Diagrammen
 Übungsfragen zu den Diagrammen 1. SONNENSPEKTRUM 2500 2000 1500 1000 idealer Schwarzer Körper (Temperatur 5900 K) extraterrestrische Sonnenstrahlung (Luftmasse AM0) terrestrische Sonnenstrahlung (Luftmasse
Übungsfragen zu den Diagrammen 1. SONNENSPEKTRUM 2500 2000 1500 1000 idealer Schwarzer Körper (Temperatur 5900 K) extraterrestrische Sonnenstrahlung (Luftmasse AM0) terrestrische Sonnenstrahlung (Luftmasse
AnC I Protokoll: 6.1 Extraktionsphotometrische Bestimmung von Cobalt mit HDEHP! SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
h-bestimmung mit LEDs
 Aufbau und Funktion der 13. März 2006 Inhalt Aufbau und Funktion der 1 Aufbau und Funktion der 2 sbeschreibung Inhalt Aufbau und Funktion der 1 Aufbau und Funktion der 2 sbeschreibung Aufbau und Funktion
Aufbau und Funktion der 13. März 2006 Inhalt Aufbau und Funktion der 1 Aufbau und Funktion der 2 sbeschreibung Inhalt Aufbau und Funktion der 1 Aufbau und Funktion der 2 sbeschreibung Aufbau und Funktion
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
3. Aromatische Verbindungen Benzol(en)
 3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
GRUNDLAGEN DER SPEKTROPHOTOMETRIE
 11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
11 GRUNDLAGEN DER SPEKTROPHOTOMETRE Materie erscheint uns farbig, wenn sie aus dem einfallenden weißen Licht einen bestimmten spektralen Teil absorbiert. Als Farbe nehmen wir den reflektierten Anteil des
UV/VIS-Spektroskopie
 UV/VIS-Spektroskopie Version 2, Gruppe M 14 Jorge Ferreiro, Studiengang Chemieingenieur, 4. Semester, fjorge@student.ethz.ch Natalja Früh, Studiengang Interdisziplinäre Naturwissenschaften, 4. Semester
UV/VIS-Spektroskopie Version 2, Gruppe M 14 Jorge Ferreiro, Studiengang Chemieingenieur, 4. Semester, fjorge@student.ethz.ch Natalja Früh, Studiengang Interdisziplinäre Naturwissenschaften, 4. Semester
Photom etrieren Photometrie Fraunhofer sche Linien
 17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
Theorie der Farbigkeit
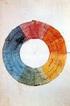 1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Fluoreszenz. Abb. 1: Möglicher Versuchsaufbau
 Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Die Natriumlinie. und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz
 Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
UV/VIS-Spektroskopie
 UV/VIS-Spektroskopie Dies ist die älteste spektroskopische Methode, die aber wegen begrenzter Aussagekraft heute in der Praxis keine allzu große Rolle mehr spielt. Es werden elektronische Übergänge angeregt,
UV/VIS-Spektroskopie Dies ist die älteste spektroskopische Methode, die aber wegen begrenzter Aussagekraft heute in der Praxis keine allzu große Rolle mehr spielt. Es werden elektronische Übergänge angeregt,
Wie Heavy Metal ist der Boden?
 Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Optische Eigenschaften fester Stoffe. Licht im neuen Licht Dez 2015
 Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Spektroskopie-Seminar SS Infrarot-Spektroskopie. Infrarot-Spektroskopie
 Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
5 Elektronenübergänge im Festkörper
 5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
Abiturprüfung auf Basis der Kernlehrpläne Beispielaufgabe 1
 Seite 1 von 4 Name: Abiturprüfung auf Basis der Kernlehrpläne Beispielaufgabe 1 Chemie, Grundkurs Vorbemerkung: Mit dem Abiturjahrgang 2017 legen die ersten Schülerinnen und Schüler ihre Abiturprüfung
Seite 1 von 4 Name: Abiturprüfung auf Basis der Kernlehrpläne Beispielaufgabe 1 Chemie, Grundkurs Vorbemerkung: Mit dem Abiturjahrgang 2017 legen die ersten Schülerinnen und Schüler ihre Abiturprüfung
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Spektroskopie-Seminar WS 17/18 3 Infrarot-Spektroskopie. Infrarot-Spektroskopie
 WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
Herstellung von Azofarbstoffen und Färben von Textilien
 Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Herstellung des Benzoldiazoniumchlorids aus Anilin, Natriumnitrit und Salzsäure. Benzoldiazonium-Ion
 Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Bilder Ton Zeit [s] Vorspann
![Bilder Ton Zeit [s] Vorspann Bilder Ton Zeit [s] Vorspann](/thumbs/62/47191146.jpg) Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Versuche zur Untersuchung von Fruchtfarbstoffen
 Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Lösungen zu den Übungen zur Einführung in die Spektroskopie für Studenten der Biologie (SS 2011)
 Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
4. Die Bedeutung der Endgruppen am Beispiel der Phenylpolyenale und ihrer Farbsalze
 4. Die Bedeutung der Endgruppen am Beispiel der Phenylpolyenale und ihrer Farbsalze 4.1 Lernziele 1. Sie können Absorptionsmessungen von Phenylpolyenalen durchführen. 2. Sie stellen die Farbsalze der Phenylpolyenale
4. Die Bedeutung der Endgruppen am Beispiel der Phenylpolyenale und ihrer Farbsalze 4.1 Lernziele 1. Sie können Absorptionsmessungen von Phenylpolyenalen durchführen. 2. Sie stellen die Farbsalze der Phenylpolyenale
Schulversuchspraktikum. Anna Hille. Sommersemester Klassenstufen 11 & 12. Farbstoffe
 Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 11 & 12 Farbstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet zwei Lehrerversuche
Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 11 & 12 Farbstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet zwei Lehrerversuche
Das Sehen des menschlichen Auges
 Das Sehen des menschlichen Auges Der Lichteinfall auf die lichtempfindlichen Organe des Auges wird durch die Iris gesteuert, welche ihren Durchmesser vergrößern oder verkleinern kann. Diese auf der Netzhaut
Das Sehen des menschlichen Auges Der Lichteinfall auf die lichtempfindlichen Organe des Auges wird durch die Iris gesteuert, welche ihren Durchmesser vergrößern oder verkleinern kann. Diese auf der Netzhaut
Versuchsprotokoll. ph-abhängigkeit der Getränkefarben
 AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll phabhängigkeit der Getränkefarben
AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll phabhängigkeit der Getränkefarben
Broschüre-Licht und Farbe
 Broschüre-Licht und Farbe Juliane Banach Juni 2008 bearbeitet mit: FreeHand 2007 Inhaltsverzeichnis Kapitel Seite Was ist Licht? 4 Das Auge 5 Stäbchen und Zapfen 6 Dispersion 7 Farbspektrum 8 Absorption
Broschüre-Licht und Farbe Juliane Banach Juni 2008 bearbeitet mit: FreeHand 2007 Inhaltsverzeichnis Kapitel Seite Was ist Licht? 4 Das Auge 5 Stäbchen und Zapfen 6 Dispersion 7 Farbspektrum 8 Absorption
Versuch K2 Photometrische Messung
 Versuch K2 Photometrische Messung Aufgaben: 1. Messung der Extinktion von Mangan(III)-oxalat bei verschiedenen Wellenlängen. 2. Bestimmung der Geschwindigkeitskonstanten des Zerfalls des komplexen Mangan(III)-oxalations
Versuch K2 Photometrische Messung Aufgaben: 1. Messung der Extinktion von Mangan(III)-oxalat bei verschiedenen Wellenlängen. 2. Bestimmung der Geschwindigkeitskonstanten des Zerfalls des komplexen Mangan(III)-oxalations
Grundkurs Farbstoffe 1983/II 1984/I 1984/IV 1985/IV
 Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Fluoreszenzspektroskopie
 A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
Extraktion/Komplexbildung
 Extraktion/Komplexbildung Inhalte dieser Lerneinheit: Quantitativer Nachweis von Eisen mit o-phenanthrolin Quantitativer Nachweis von Kupfer mit Bichinolin Dabei werden Grundlagen der: Komplexbildung und
Extraktion/Komplexbildung Inhalte dieser Lerneinheit: Quantitativer Nachweis von Eisen mit o-phenanthrolin Quantitativer Nachweis von Kupfer mit Bichinolin Dabei werden Grundlagen der: Komplexbildung und
Versuchsprotokoll: Aminosäure- und Proteinbestimmung
 Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2
 Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 10. Temperaturabhängigkeit der Reaktionsgeschwindigkeit: Arrhenius-Beziehung Thema In diesem Versuch
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 10. Temperaturabhängigkeit der Reaktionsgeschwindigkeit: Arrhenius-Beziehung Thema In diesem Versuch
Lösung: a) b = 3, 08 m c) nein
 Phy GK13 Physik, BGL Aufgabe 1, Gitter 1 Senkrecht auf ein optisches Strichgitter mit 100 äquidistanten Spalten je 1 cm Gitterbreite fällt grünes monochromatisches Licht der Wellenlänge λ = 544 nm. Unter
Phy GK13 Physik, BGL Aufgabe 1, Gitter 1 Senkrecht auf ein optisches Strichgitter mit 100 äquidistanten Spalten je 1 cm Gitterbreite fällt grünes monochromatisches Licht der Wellenlänge λ = 544 nm. Unter
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Äußerer lichtelektrischer Effekt (Äußerer Fotoeffekt; HALLWACHS-Effekt)
 Äußerer lichtelektrischer Effekt (Äußerer Fotoeffekt; HALLWACHS-Effekt) Experiment 1: Bestrahlung einer elektrisch geladene Zinkplatte mit Licht Rotlichtlampe; positive Ladung Quecksilberdampflampe; positive
Äußerer lichtelektrischer Effekt (Äußerer Fotoeffekt; HALLWACHS-Effekt) Experiment 1: Bestrahlung einer elektrisch geladene Zinkplatte mit Licht Rotlichtlampe; positive Ladung Quecksilberdampflampe; positive
SCHWEIZER JUGEND FORSCHT. Chemie und Materialwissenschaften
 SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und Pigmente Übungen mit Lösungen
 Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und Pigmente Übungen mit Lösungen Korrektorat: Dina Baars, Bern Illustrationen: Christoph Frei, Bern 1.
Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und Pigmente Übungen mit Lösungen Korrektorat: Dina Baars, Bern Illustrationen: Christoph Frei, Bern 1.
Photochemische Reaktion
 TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
Versuch Fluoreszenz-Quenching
 Versuch Fluoreszenz-Quenching Zielstellung: 1.) Aufnahme des UV-Vis-Spektrums eines Fluoreszenzfarbstoffes 2.) Aufnahme der Kennlinie des verwendeten Photon-Counting-Moduls (PCM) im Bereich von 1,9 2,9
Versuch Fluoreszenz-Quenching Zielstellung: 1.) Aufnahme des UV-Vis-Spektrums eines Fluoreszenzfarbstoffes 2.) Aufnahme der Kennlinie des verwendeten Photon-Counting-Moduls (PCM) im Bereich von 1,9 2,9
Versuchsprotokoll. Gruppe 12, Typ: Pflichtversuch - H + Einsatz in der Schule Sulfanilsäure NH 2 C 6 H 4 SO 3 H Xi 36/38, 43 24, 37 S I
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
Bundesrealgymnasium Imst. Chemie Klasse 8. Aromaten und deren Reaktionen
 Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Äußerer lichtelektrischer Effekt
 Grundexperiment 1 UV-Licht Video: 301-1 Grundexperiment 2 UV-Licht Grundexperiment 3 Rotes Licht Video: 301-2 Grundexperiment 3 UV-Licht Glasplatte Video: 301-2 Herauslösung von Elektronen aus Metallplatte
Grundexperiment 1 UV-Licht Video: 301-1 Grundexperiment 2 UV-Licht Grundexperiment 3 Rotes Licht Video: 301-2 Grundexperiment 3 UV-Licht Glasplatte Video: 301-2 Herauslösung von Elektronen aus Metallplatte
Elektromagnetische Strahlung
 Elektromagnetische Strahlung 1 Absorptionsmethoden - Grundlagen Als Absorptionsmethoden bezeichnet man die Konzentrationsbestimmung einer Substanz, indem gemessen wird, wie sie die Intensität elektromagnetischer
Elektromagnetische Strahlung 1 Absorptionsmethoden - Grundlagen Als Absorptionsmethoden bezeichnet man die Konzentrationsbestimmung einer Substanz, indem gemessen wird, wie sie die Intensität elektromagnetischer
Äußerer lichtelektrischer Effekt Übungsaufgaben
 Aufgabe: LB S.66/9 Durch eine Natriumdampflampe wird Licht der Wellenlänge 589 nm (gelbe Natriumlinien) mit einer Leistung von 75 mw ausgesendet. a) Berechnen Sie die Energie der betreffenden Photonen!
Aufgabe: LB S.66/9 Durch eine Natriumdampflampe wird Licht der Wellenlänge 589 nm (gelbe Natriumlinien) mit einer Leistung von 75 mw ausgesendet. a) Berechnen Sie die Energie der betreffenden Photonen!
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Das Spektrum elektromagnetischer Strahlung
 Druckversion: Virtuelles Labor: UV-Vis-Spektroskopie 1 Versuchsziel ufnahme eines Spektrums von Sulfanilamid (SN) und Sulfathiazol (ST) zur Ermittlung der maximalen Wellenlänge max und der entsprechenden
Druckversion: Virtuelles Labor: UV-Vis-Spektroskopie 1 Versuchsziel ufnahme eines Spektrums von Sulfanilamid (SN) und Sulfathiazol (ST) zur Ermittlung der maximalen Wellenlänge max und der entsprechenden
Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre?
 Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
Gymnasium / Realschule. Atomphysik 2. Klasse / G8. Aufnahme und Abgabe von Energie (Licht)
 Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
21-1. K=f c I=I0 e f c d
 21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
Physikalische Chemie Praktikum. Aufbau der Materie: Absorptionsspektrum eines Farbstoffes / Photometrie
 Hochschule Emden / Leer Physikalische Chemie Praktikum Vers. Nr. 22 Mai 2014 Aufbau der Materie: Absorptionsspektrum eines Farbstoffes / Photometrie Allgemeine Grundlagen Spektroskopie und prinzipieller
Hochschule Emden / Leer Physikalische Chemie Praktikum Vers. Nr. 22 Mai 2014 Aufbau der Materie: Absorptionsspektrum eines Farbstoffes / Photometrie Allgemeine Grundlagen Spektroskopie und prinzipieller
Korrektorat: Dina Baars, Bern Illustrationen: Christoph Frei, Bern. 1. Auflage 2010 Alle Rechte vorbehalten Copyright Pädagogische Hochschule PHBern
 Günter Baars (unter Mitarbeit von B. Debrunner, I. Kulakowska, T. Loosli, I. Pompizi, S. Stieger) E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Leitprogramm: Quantenchemie und organische
Günter Baars (unter Mitarbeit von B. Debrunner, I. Kulakowska, T. Loosli, I. Pompizi, S. Stieger) E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Leitprogramm: Quantenchemie und organische
Analytische Chemie. LD Handblätter Chemie. Aufnahme von Absorptionsspektren mit einem Spektrometer C Optische Analysemethoden Spektrometrie
 AW-2014-05 Analytische Chemie Optische Analysemethoden Spektrometrie LD Handblätter Chemie C3.3.1.2 Aufnahme von Absorptionsspektren mit einem Spektrometer Versuchsziele Lichtspektren betrachten und verstehen.
AW-2014-05 Analytische Chemie Optische Analysemethoden Spektrometrie LD Handblätter Chemie C3.3.1.2 Aufnahme von Absorptionsspektren mit einem Spektrometer Versuchsziele Lichtspektren betrachten und verstehen.
Grundlagen der photometrischen Messung
 Grundlagen der photometrischen Messung Teil 1: Grundlagen, Optik, AQS, Testsätze (I) 2015 WTW GmbH. [ Juni 2015] Einführung Phos (griech.) für Licht => Photometrie ist ein Messverfahren, bei dem mit Hilfe
Grundlagen der photometrischen Messung Teil 1: Grundlagen, Optik, AQS, Testsätze (I) 2015 WTW GmbH. [ Juni 2015] Einführung Phos (griech.) für Licht => Photometrie ist ein Messverfahren, bei dem mit Hilfe
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)
 Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Solubilisierung in Mizellen. hydrophobe Kette. hydrophile Kopfgruppe. -nicht-ionische. -anionische. -kationische. -zwitterionische Tenside.
 Solubilisierung in Mizellen Abstract 1 Theoretische Grundlagen Tenside sind Moleküle, die aus einem hydrophilen (polaren) und einem hydrophoben (unpolaren) Molekülteil bestehen(abbildung 1). hydrophile
Solubilisierung in Mizellen Abstract 1 Theoretische Grundlagen Tenside sind Moleküle, die aus einem hydrophilen (polaren) und einem hydrophoben (unpolaren) Molekülteil bestehen(abbildung 1). hydrophile
Zusammenhang zwischen Farbe, Wellenlänge, Frequenz und Energie des sichtbaren Spektrums
 Zusammenhang zwischen Farbe, Wellenlänge, Frequenz und Energie des sichtbaren Spektrums Farbe, die das menschliche Auge empfindet Wellenlänge [10-9 m] Frequenz [10 14 Hz] Energie [kj/ 1 mol Photonen] Rot
Zusammenhang zwischen Farbe, Wellenlänge, Frequenz und Energie des sichtbaren Spektrums Farbe, die das menschliche Auge empfindet Wellenlänge [10-9 m] Frequenz [10 14 Hz] Energie [kj/ 1 mol Photonen] Rot
Stephen. Grundvoraussetzung: Die Moleküle müssen das Licht absorbieren! E = λ = Wellenlänge. Hashmi. ν = Frequenz
 Prof Dr ashmi, Sommersemester 2002 1 rganische Chemie für Technische Biologen, Teil 24 otochemie, Farbstoffe Bedeutung in der atur: - otosynthese - Sehvorgang - Zellschädigung durch energiereiches Licht
Prof Dr ashmi, Sommersemester 2002 1 rganische Chemie für Technische Biologen, Teil 24 otochemie, Farbstoffe Bedeutung in der atur: - otosynthese - Sehvorgang - Zellschädigung durch energiereiches Licht
Inhaltlicher Schwerpunkt: Organische Verbindungen und Reaktionswege
 Unterrichtvorhaben 1: Kontext: Maßgeschneiderte Produkte aus Kunststoffen Grundkurs Qualifikationsphase 2 Unterrichtsvorhaben 2: Kontext: Wenn das Erdöl zu Ende geht UF2 Auswahl UF4 Vernetzung E3 Hypothesen
Unterrichtvorhaben 1: Kontext: Maßgeschneiderte Produkte aus Kunststoffen Grundkurs Qualifikationsphase 2 Unterrichtsvorhaben 2: Kontext: Wenn das Erdöl zu Ende geht UF2 Auswahl UF4 Vernetzung E3 Hypothesen
