Welche Atome kommen überwiegend (nach der Häufigkeit geordnet!) in organ.verbindungen
|
|
|
- Ralph Weiss
- vor 7 Jahren
- Abrufe
Transkript
1 Prüfungsvorbereitung emie 1. Teil der organishen hemie 1. Wie viele Verbindungen kennt man in der anorganishen hemie und in der organishen? Beispiel: 2. Warum gibt es so viele organishe Moleküle, obwohl nur reht wenige Atome sih verknüpfen? Welhe Atome kommen überwiegend (nah der äufigkeit geordnet!) in organ.verbindungen vor? 3. Was ist der Grund dafür, dass aus diesem reht geringen Atomvorrat so viele vershiedene Moleküle entstehen können? Das immer in organishen Molekülen vorkommende Atom hat einige herausragende Eigenshaften, die diese Fülle an organishen Molekülen ermögliht: a) es ist wertig, das heißt, es kann vier Bindungen zu vier einwertigen Atomen knüpfen (z.b. 4 ) oder zwei Bindungen zu zwei zweiwertigen Atomen z.b. 2 - dies ist aber kein organishes Molekül!) b) es kann sih mit anderen Atomen entsprehend der Wertigkeit verknüpfen : 3 l ( das ist das ), 2 (das ist das ), 3 (das ist das ). ) es kann mit anderen - Atomen sih zu einer langen Kette, Ringen oder verzweigten Molekülstrukturen verknüpfen. Beispiel : ein Kohlenwasserstoff mit sehs -Atomen Länge: Name: Name: Summenformel: Summenformel: Name: Summenformel:
2 Prüfungsvorbereitung emie 1. Teil der organishen hemie 4. Wie kann man die organishe hemie von der anorganishen hemie untersheiden? Alte Definition, die vor der synthetishen erstellung des arnstoffs galt: Moderne Definition (allgemein gültig): 5. Da ursprünglih die organishen Verbindungen tatsählih nur in Lebewesen vorkamen, findet man in Umbauprodukten von Lebewesen auh eine Vielzahl organisher Moleküle. So findet man vor allem im eine unvorstellbare Vielfalt organisher Verbindungen. Man shätzt, dass nahezu alle organishen Verbindungen darin vorkommen, die meisten sind nahgewiesen, jährlih kommen viele neuentdekte hinzu. Es ist daher ein wihtiges Argument gegen den blinden, vershwenderishen Verbrauh von Erdöl als Rohstoff, dass darin viele Stoffe enthalten sind, die einfah zu shade zum Verbrennen (Autofahren, Kunststoffherstellen...) sind und uns anderweitig wihtiger sein könnten! 6. Wie trennt man nun diese unvorstellbare Vielfalt von Stoffen im Erdöl, um ein halbwegs einheitlihes (immer noh unübershaubares! ) Stoffgemish ähnliher Eigenshaften zu erhalten. Eine Möglihkeit ist die Destillation - Stoffe mit ähnlihen Siedepunkten haben meist auh ähnlihe Eigenshaften. Atmosphärishe (oder fraktionierte) Destillation ( bei normalen Drukverhältnissen) geringster Siedepunkt : Gase < 30 Benzine um 100 Mitteldestillate: Kerosin, Peroleum 200 eizöl 300 höhster Siedepkt: shweres eizöl >400 max. 400 Vakuumdestillation ( unter reduziertem Druk) Trennung des Shweren eizöls in Shmieröle und Rükstand Bitumen Bei Drukverminderung wird der Siedepunkt bis zu 150 herabgesetzt! * * Auf dem Mount Everest (wo der Luftdruk geringer ist als bei Normalnull oder auh bei uns im Shwarzwald siedet Wasser deutlih unter 100, da die Wassermoleküle weniger stark zurükgehalten werden! 7. Warum erhitzt man zur weiteren Trennung das Shwere eizöl niht über 400? Die im shweren eizöl enthaltenen Moleküle sind lange Kohlenstoffverbindungen. Diese langen Ketten würden bei einer Erwärmung auf über 400 so sehr in Bewegung geraten, dass sie unkontrolliert in kürzere Moleküle. 8. Aufbau eines Destillationsturmes mit Glokenböden, wo die entsprehenden Stoffe der dort untershrittenen Siedetemperatur wieder flüssig werden und sih ansammeln.
3 Prüfungsvorbereitung emie 1. Teil der organishen hemie Umweltaspekt: oher Energieverbrauh bei der Destillation! äufig wird das in großen Mengen entstehende Gas (ungenutzt) abgefakelt anstatt es aufzufangen. 9. raken - Benzingewinnung aus langkettigen Alkanen (von geringem Bedarfswert; z.b. Shweres eizöl oder Bitumen) Das Argument aus Frage 7 wird nun in kontrollierter Weise genutzt: Erhitzt man langkettige Kohlenwasserstoffe ( z.b. Shweres eizöl) zerbrehen die langen Ketten in kürzere unter anderem auh in die Alkane der Benzine ( auptbestandteil z.b. eptan!) Thermishes raken bei rund 600 Nahteil: oher Energieverbrauh, geringe Ausbeute Katalytishes raken (Katalysator) <600 Vorteil: Größere Ausbeute und geringerer Nebenaspekt: Unter den rakprodukten befinden sih sowohl Alkane als auh Alkene! w Welhe rakprodukte könnten aus diesem Molekül entstehen? 10. Die homologe Reihe der ALKANE Alkane bestehen nur aus und - es gibt nur bindungen! w Zähle die homologe Reihe auf! Zustandsform Gas a) ( Summenformel: ) b) ( Summenformel: ) ) ( Summenformel: ) d) ( Summenformel: ) Flüssigkeit e) ( Summenformel: ) f) ( Summenformel: ) g) ( Summenformel: ) h) ( Summenformel: ) i) ( Summenformel: ) j) ( Summenformel: )
4 Prüfungsvorbereitung emie 1. Teil der organishen hemie Ab eptadean ( ) sind die Alkane fest! Sogenannte Paraffine (Stoffgemishe!) 11. Alkaneigenshaften : w Dihte als Wasser-----> shwimmen Fett! w Alle Alkane sind brennbar ----> doh je länger die Kette desto mehr bei der Verbrennung! w Sie sind in Wasser niht löslih (da unpolar! oder hydrophob) 12. Allgemeine Bildungsformel ALKANE: 13. Isomerie bei ALKANEN - gleihe aber untershiedlihe : Längerkettige Alkane können vershiedene Strukturen einnehmen, obwohl sie dieselbe Summenformel haben (doh leiht veränderten physikalishen Eigenshaften)! 6 14 kann folgende Strukturen haben - es sind die Isomeren des n-exans (bitte die exakte Benennung verwenden!) Wie heißen diese möglihen "Abzweige" ( ALKYL"GRUPPEN")von einer Grundkette?
5 Prüfungsvorbereitung emie 1. Teil der organishen hemie
6 Prüfungsvorbereitung emie 1. Teil der organishen hemie 17. Molekulargewihtsberehnungen bei Alkanen - Alkenen - Alkinen oder bei ALKANLEN bzw. Alkansäuren : = 12 u = 1 u = 16 u! 18 ALKENE - ein oder mehrere Doppelbindungen im Kohlenwasserstoffmolekül > größere Reaktionsbereitshaft > Nahweis über die Brom - Addition > Dibrom -ALKAN - - Br Br - - Br Br + Br > Brom ist ein farbiger Stoff, nah der Addition an das Alken zum Alkan ist diese Färbung vershwunden! Nahweis einer vormals vorhandenen Doppelbindung (Additionsmöglihkeit) am Molekül. 19 ALKENE mit mehreren Doppelbindungen im Molekül : dien dien 19. AlkineEigenshaften: Sehr reaktionsfreudige Verbindungen! in in 20. alogenalkane: Ausgehend von dem Grundalkan (z.b. Methan ) wird durh Substitution (Ersetzung eines Wasserstoffatoms durh ein alogen z.b. hlor) eine Molekülveränderung herbeigeführt.
7 Prüfungsvorbereitung emie 1. Teil der organishen hemie Energie + l > l + l Methan + hlor (molekular) > ( Mono)hlor-Methan + hlorwasserstoff l l l l l l l l l (Gas) 21. Wie heißt dieser Stoff mit dem andelsnamen (eingetragenes Warenzeihen der Bayer? AG)? l F F l 22. Von den ALKANEN führt der Weg über eine XIDATIN weiter zu den Alkoholen (ALKANLEN) + 1/ > Methan + Sauerstoff (atom)-----> Methanol Alkoholeigenshaften: bwohl von der Masse her reht kleine Moleküle, haben sie doh einen hohen Siedepunkt. Warum? unpolare Alkylgruppe polare ydroxylgruppe
8 Prüfungsvorbereitung emie 1. Teil der organishen hemie 22. Alkohole sind in Benzin löslih (unpolares Lösungsmittel). Diese Lösung vermitteln sie mit ihrem unpolaren Alkylrest, die kurzen Alkohole sind bis Butanol (einshließlih) in Wasser löslih (polares Lösungsmittel), dies vermittelt die polare -Gruppe! 23. Das Wassermolekül und seine Polarität. Beshreibe: 24. Warum ist ein so kleines und massearmes Molekül wie Wasser flüssig und niht gasförmig? Die Molekülmasse des Wassers beträgt u. Auh das Ethanmolekül hat die gleihe polare Gruppe wie das Wassermolekül, es ist an dieser Stelle der - Gruppe polar (hydrophil = wasserfreundlih oder auh lipophob= fettunfreundlih/fettunlöslih). Zusätzlih besitzt das Ethanolmolekül noh eine unpolare (hydrophobe =wasserfeindlihe oder auh lipophile= fettfreundlihe) ALKYL-Gruppe. ier ist die Elektronenverteilung völlig gleihmäßig. Bei den längerkettigen Alkoholen ab Pentanol überwiegt die polare Gruppe: Sie sind niht mehr wasserlöslih, nur noh fettlöslih (hydrophob)! 24. Isomerie bei Alkoholen (ALKANLEN): Die Lage der -Gruppe und unverzweigtes oder Verzweigtes!
9 Prüfungsvorbereitung emie 1. Teil der organishen hemie 25. Mehrwertige Alkohole - Alkohole mit mehreren -Gruppen Das 1,2 Ethandiol (Glykol) ist ein solher mehrwertiger Alkohol (ein süßlih shmekender Stoff zum Panshen von Wein shon oft verwandt! + als Frostshutzmittel!) Das 1,2,3 Propantriol (Glyzerin) ist ein solher mehrwertiger Alkohol ( Verwendung in Kosmetika und zum Geshmeidighalten von Kunststoffdihtungen) Sorbit ist ein zahnfreundliher Süßstoff, der aber leiht abführend wirkt. Sein Name ist exanhexol: Alkohole wirken reduzierend - das heißt, sie entnehmen einem anderen Stoff - und werden dabei. Ag N 3 + Alkohol > Die funktionelle Gruppe der Alkohole ist die gruppe. 27. Was bedeutet die funktionelle Gruppe? 28. Die weitere xidation der ALKANLE führt zu : Methanol + 1/ > Methandiol = instabiles Zwishenprodukt (Regel: niht mehr als eine -Gruppe an einem - Atom! Bitte wenden!!
10 Prüfungsvorbereitung emie 1. Teil der organishen hemie Wasserabspaltung > freie Bindung! Methanal oder Fromaldehyd ( ein gutes Desinfektionsmittel) funktionelle Gruppe der ALKANALE 30 Eine weitere XIDATIN der ALKANALE führt zu den Alkansäuren / arbonsäuren + 1/ > R Warum sind Alkansäuren "Säuren" im klassishen Sinne? R= Rest (z.b. bei Methansäure; 3 bei Ethansäure..) a) Sie bilden in wässriger Lösung und b) p-wert 7. ) Sie reagieren mit zu und.
11 Prüfungsvorbereitung emie 1. Teil der organishen hemie 32. Dissoziationsgleihung von in ydro(xo)nium-ionen und neg. Säurerest ( ) > neg. Säurerest-Ion 33. Langkettige Alkansäuren nennt man. Sie sind auh zunehmend (je nah Kettenlänge) fest. 34. Bei den 18 -langen arbonsäuren gibt es mehrere arbonsäuren - mit untershiedliher Summenformel und untershiedlihen physikalishen Eigenshaften: Stearinsäure ( ), Ölsäure ( ), Linolsäure( ) und der Linolensäure ( ) 35. Was versteht man unter gesättigten Fettsäuren, was unter ungesättigten Fettsäuren? 36. Ih gebe zu einer Alkansäure eine Lauge. Was passiert? Es entsteht ein und bildet sih (Neutralisationsgleihung). 37. Fülle die Reaktionsgleihungen vollständig aus! 3 + Mg > + + Magnesium > Magnesium Na > > Na > + + Natrium > Natrium- + Ih werfe Natriumbutanoat (Natriumsalz der Butansäure) in Wasser. Ih sehe die vormals feststellbaren Körnhen niht mehr. Warum?
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
 Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
1. Homologe Reihe der Alkansäuren
 1. omologe Reihe der Alkansäuren 2 Mit Zunahme der Kettenlänge verlängern sich die unpolaren Teile (Alkylgruppen) der Alkansäuremoleküle, dadurch steigen die van-der-waals-kräfte zwischen den Molekülen
1. omologe Reihe der Alkansäuren 2 Mit Zunahme der Kettenlänge verlängern sich die unpolaren Teile (Alkylgruppen) der Alkansäuremoleküle, dadurch steigen die van-der-waals-kräfte zwischen den Molekülen
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Alkohole Brüder des Wassers
 6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Organische Chemie. Maximilian Ernestus
 rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
rganische hemie Maximilian Ernestus Inhaltsverzeichnis 1 rganische hemie 2 1.1 Wichtige Eigenschaften von Kohlenstoff..................... 2 1.2 Alkane....................................... 3 1.2.1 Isomere..................................
Grundwissen 10. Klasse NTG 1
 Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Homologe Reihe der Alkane. Benennung der Alkane. Konstitutionsisomerie. Isomerie. Was versteht man unter der Homologen Reihe der Alkane?
 Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Chemie in der Einführungsphase am CFG
 Einteilung organischer Verbindungen in Stoffklassen Übersicht 1. Was ist Organische Chemie? 2. Kohlenstoffwasserstoffe/Alkane 3. Alkohole 4. Vom Alkohol zum Aromastoff - Um 1806: BERZELIUS (1779 1848):
Einteilung organischer Verbindungen in Stoffklassen Übersicht 1. Was ist Organische Chemie? 2. Kohlenstoffwasserstoffe/Alkane 3. Alkohole 4. Vom Alkohol zum Aromastoff - Um 1806: BERZELIUS (1779 1848):
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Grundwissen Chemie Jahrgangsstufe 10 (NTG)
 Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Chemiefragen 10.Klasse:
 Hausaufgaben bitte entweder: - auf Papier schriftlich erledigen oder - per email an Herrn Apelt senden: Reinhard.Apelt@web.de Chemiefragen 10.Klasse: A) Organische Verbindungen Kohlenwasserstoffe B) Erdöl
Hausaufgaben bitte entweder: - auf Papier schriftlich erledigen oder - per email an Herrn Apelt senden: Reinhard.Apelt@web.de Chemiefragen 10.Klasse: A) Organische Verbindungen Kohlenwasserstoffe B) Erdöl
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
T7 - Bestimmung der Oberflächenspannung homologer wässriger Alkohollösungen (Traubesche Regel)
 T7 - Bestimmung der Oberflähenspannung homologer wässriger Alkohollösungen (Traubeshe Regel) Aufgaben:. Messung der Oberflähenspannung von vershieden konzentrierten wässrigen Lösungen der homologen Alkohole
T7 - Bestimmung der Oberflähenspannung homologer wässriger Alkohollösungen (Traubeshe Regel) Aufgaben:. Messung der Oberflähenspannung von vershieden konzentrierten wässrigen Lösungen der homologen Alkohole
Einführung in die Nomenklatur der organischen Chemie. Einteilung der Kohlenwasserstoffe
 organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Vorlesung 5. Alkane. Experimentalchemie, Prof. H. Mayr 20 Achtung Lückentext. Nur als Begleittext zur Vorlesung geeignet. Anzahl C-Atome im n-alkan
 Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
Arbeitsheft Organische Redoxreaktionen Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse:
 Arbeitsheft Organishe Reoxreaktionen Inhalt Jakob Inhaltsverzeihnis: Seite: Vorkenntnisse: Bestimmung er OZ bei organishen Molekülen Arbeitsheft Reoxreaktionen Verbrennung von Kohlenwasserstoffen. Oxiation
Arbeitsheft Organishe Reoxreaktionen Inhalt Jakob Inhaltsverzeihnis: Seite: Vorkenntnisse: Bestimmung er OZ bei organishen Molekülen Arbeitsheft Reoxreaktionen Verbrennung von Kohlenwasserstoffen. Oxiation
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
chulportfolio 3. Schulkonzept 3.7 Kern- und Schulcurricula G9 (Klasse 5 11) Chemie Chemie Klasse 11
 Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Grundwissen der 10.Klasse NTG
 Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen Chemie Mittelstufe (10 MNG)
 Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Alkane. Name: Summenformel: vereinfachte Formel: Zustand: Methan CH 4 CH 4 g (gaseous) Ethan C 2 H 6 CH 3 CH 3 g. Propan C 3 H 8 CH 3 CH 2 CH 3 g
 Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Kohlenwasserstoffe. Homologe Reihe. Alkane. Alkene. HGA-Grundwissen Chemie-10. Klasse NTG
 GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
Ein Alkan, dem ein H-Atom fehlt, wird Alkyl-Rest genannt. Der Name ergibt sich aus dem Alkan, jedoch mit der Endung yl:
 Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Wie ist der räumliche Bau von Methan? Wie kann dies als zweidimensionale Formel dargestellte werden?
 Wie ist der räumliche Bau von Methan? Wie kann dies als zweidimensionale Formel dargestellte werden? Formeln von Methan Methan hat die ermittelte Summenformel CH 4. Dies ist eine Molekülformel. Die vier
Wie ist der räumliche Bau von Methan? Wie kann dies als zweidimensionale Formel dargestellte werden? Formeln von Methan Methan hat die ermittelte Summenformel CH 4. Dies ist eine Molekülformel. Die vier
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Inhalt. Stoffe lassen sich ordnen - Elementfamilien. Der Bau der Atome. Kopiervorlagen. Kopiervorlagen. 0 Materialien zur Sprachbildung. aufgeführt.
 Inhalt 0 Materialien zur Sprachbildung Sofern sich die in eine besondere Rubrik einordnen lassen, ist dies jeweils aufgeführt. Stoffe lassen sich ordnen - Elementfamilien Diagnosebogen I - Selbsteinschätzung
Inhalt 0 Materialien zur Sprachbildung Sofern sich die in eine besondere Rubrik einordnen lassen, ist dies jeweils aufgeführt. Stoffe lassen sich ordnen - Elementfamilien Diagnosebogen I - Selbsteinschätzung
Gruppe 06: Löslichkeit von Alkoholen in Wasser
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: Löslichkeit von Alkoholen in Wasser Reaktion bzw. hier Mischbarkeit:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: Löslichkeit von Alkoholen in Wasser Reaktion bzw. hier Mischbarkeit:
Fette und fettähnliche Substanzen
 Fette und fettähnliche Substanzen Fette und fettähnliche Substanzen (letztere wurden früher als Lipoide bezeichnet) bilden die Gruppe der Lipide. Sie sind unlöslich in Wasser, aber gut löslich in organischen
Fette und fettähnliche Substanzen Fette und fettähnliche Substanzen (letztere wurden früher als Lipoide bezeichnet) bilden die Gruppe der Lipide. Sie sind unlöslich in Wasser, aber gut löslich in organischen
Kennsilbe. -an. -en -in. -yl. -ol. -al (VI) -on. (VII) -säure (VIII)
 Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Zeitbedarf Gruppe 6: Alkohole Versuch: Mischungsexperimente
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Zeitbedarf Gruppe 6: Alkohole Versuch: Mischungsexperimente
Christian-Ernst-Gymnasium
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
Alkane als Kraftstoffe
 Alkane als Kraftstoffe Du hast bereits gelernt, dass bei der fraktionierten Destillation Alkane erhalten werden können, die geeignet sind als Kraftstoffe eingesetzt zu werden. Unterschiedliche Motoren
Alkane als Kraftstoffe Du hast bereits gelernt, dass bei der fraktionierten Destillation Alkane erhalten werden können, die geeignet sind als Kraftstoffe eingesetzt zu werden. Unterschiedliche Motoren
Halogenalkane. Radikalische Halogenierung von Alkanen. Addition von Halogenwasserstoffen an Alkene. H 3 C + HBr H C C C H.
 alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )
![Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 ) Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )](/thumbs/74/69784240.jpg) 1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
Grundwissen Chemie. 8. Jahrgangsstufe, Gruppe I
 Grundwissen Chemie 8. Jahrgangsstufe, Gruppe I Stoffe, Experimente - Stoffe und Stoffgemische unterscheiden Stoffeigenschaften, Reinstoffe, Gemische, Trennverfahren - Teilchenmodell: Atome und Moleküle
Grundwissen Chemie 8. Jahrgangsstufe, Gruppe I Stoffe, Experimente - Stoffe und Stoffgemische unterscheiden Stoffeigenschaften, Reinstoffe, Gemische, Trennverfahren - Teilchenmodell: Atome und Moleküle
Decan Homologe Reihe der Alkane, unterschiedlich lange C-Ketten mit C- C (sp 3 /sp 3 ) und C-H (sp 3 /s)-bindungen (σ-bindungen) Beispiele: Butan
 1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
Grundwissenkarten Hans-Carossa- Gymnasium
 Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 10 - MuG erstellt von der Fachschaft Chemie C 10.1 Molekülstruktur und Stoffeigenschaften Atombindung Die chemische Bindung,
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und Herstellung
 6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Alkane - eine vielseitige Stoffgruppe. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Alkane - eine vielseitige Stoffgruppe Das komplette Material finden Sie hier: School-Scout.de RAAbits Hauptschule 7 9 Naturwissenschaften
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Alkane - eine vielseitige Stoffgruppe Das komplette Material finden Sie hier: School-Scout.de RAAbits Hauptschule 7 9 Naturwissenschaften
Heinrich-Böll-Gesamtschule SILP Chemie Jahrgang 10
 Inhaltsfeld: Säuren und Basen Inhaltliche Schwerpunkte Mögliche Kontexte Basiskonzepte Eigenschaften saurer und alkalischer Lösungen Neutralisation Eigenschaften von Salzen Kompetenzen Fachwissen Erkenntnisgewinnung
Inhaltsfeld: Säuren und Basen Inhaltliche Schwerpunkte Mögliche Kontexte Basiskonzepte Eigenschaften saurer und alkalischer Lösungen Neutralisation Eigenschaften von Salzen Kompetenzen Fachwissen Erkenntnisgewinnung
Inhaltsverzeichnis VII. Vorwort... V
 VII Vorwort... V 1 Einleitung... 1 1.1 Der Begriff der Organischen Chemie... 1 1.2 Vielfalt organischer Verbindungen... 1 1.3 Ordnung in der Vielfalt... 2 2 Grundlegendes... 3 2.1 Kohlenstoff hat vier
VII Vorwort... V 1 Einleitung... 1 1.1 Der Begriff der Organischen Chemie... 1 1.2 Vielfalt organischer Verbindungen... 1 1.3 Ordnung in der Vielfalt... 2 2 Grundlegendes... 3 2.1 Kohlenstoff hat vier
Aufgaben zu Aldehyden und Ketonen
 Aufgaben zu Aldehyden und Ketonen 1. Formulieren Sie jeweils die Reaktionsgleichungen! a) erstellung von Ethanal aus einem Alkanol mit Sauerstoff (mit Ag als Katalysator) b) erstellung von yclohexanon
Aufgaben zu Aldehyden und Ketonen 1. Formulieren Sie jeweils die Reaktionsgleichungen! a) erstellung von Ethanal aus einem Alkanol mit Sauerstoff (mit Ag als Katalysator) b) erstellung von yclohexanon
Station 1: Nomenklatur von Alkanen
 Station 1: Nomenklatur von Alkanen Station 1: Nomenklatur von Alkanen 1. a) 3-Ethyl-2-methylpentan e) 2,2-Dimethylpropan b) 3-Ethyl-2-methylpentan f) 2,3,5-Trimethylhexan c) 2,3,5-Trimethylhexan g) 2,3-Dimethylbutan
Station 1: Nomenklatur von Alkanen Station 1: Nomenklatur von Alkanen 1. a) 3-Ethyl-2-methylpentan e) 2,2-Dimethylpropan b) 3-Ethyl-2-methylpentan f) 2,3,5-Trimethylhexan c) 2,3,5-Trimethylhexan g) 2,3-Dimethylbutan
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Stationenlernen Chemie im Paket. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Orbital. Elektronenpaarabstoßungsmodell. räumliche Grundstrukturen 1. räumliche Grundstrukturen 2
 Orbital Der Raum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Dieses Modell ermöglicht eine Vorhersage der räumlichen Struktur eines Moleküls. Elektronenpaarabstoßungsmodell
Orbital Der Raum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Dieses Modell ermöglicht eine Vorhersage der räumlichen Struktur eines Moleküls. Elektronenpaarabstoßungsmodell
Alkine sind aliphatische, ungesättigte Kohlenwasserstoffe die eine oder mehrere Dreifachbindungen aufweisen. CnH2n-2
 Ri 51 1.3. Alkine Alkine sind aliphatische, ungesättigte Kohlenwasserstoffe die eine oder mehrere Dreifachbindungen aufweisen. Allgemeine Summenformel der Monoalkine: CnH2n-2 Alkine sind gestreckte MolekÄle.
Ri 51 1.3. Alkine Alkine sind aliphatische, ungesättigte Kohlenwasserstoffe die eine oder mehrere Dreifachbindungen aufweisen. Allgemeine Summenformel der Monoalkine: CnH2n-2 Alkine sind gestreckte MolekÄle.
Abituraufgaben Alkohole 1978/IV 1982/II/1 1984/II/1 1984/III/1 1984/IV/4.3
 Abituraufgaben Alkohole 1978/IV 1.1 Erstellen Sie die Formel des einfachsten dreiwertigen Alkanols (Triol), das zugleich primärer, sekundärer und tertiärer Alkohol ist. Benennen Sie die Verbindung eindeutig.
Abituraufgaben Alkohole 1978/IV 1.1 Erstellen Sie die Formel des einfachsten dreiwertigen Alkanols (Triol), das zugleich primärer, sekundärer und tertiärer Alkohol ist. Benennen Sie die Verbindung eindeutig.
Summenformel Elektronenstrichformel Name Siedepunkt
 Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Schulcurriculum des Faches Chemie. für die Klassenstufen 8 10
 Schulcurriculum des Faches Chemie für die Klassenstufen 8 10 Chemie - Klasse 8 Was ist Chemie? Richtig experimentieren und Entsorgen Naturwissenschaftliche Arbeitsweise Rotkraut oder Blaukraut? Richtig
Schulcurriculum des Faches Chemie für die Klassenstufen 8 10 Chemie - Klasse 8 Was ist Chemie? Richtig experimentieren und Entsorgen Naturwissenschaftliche Arbeitsweise Rotkraut oder Blaukraut? Richtig
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Organische Chemie II Chemie am 14.01.2013
 Organische Chemie II Inhaltsverzeichnis Diskussionen über Wasserlöslichkeit und Siedetemperaturen von allen Euch bekannten Organischen Stoffen führen können... 2 Regeln zur Beeinflussung der Reaktionsgeschwindigkeit
Organische Chemie II Inhaltsverzeichnis Diskussionen über Wasserlöslichkeit und Siedetemperaturen von allen Euch bekannten Organischen Stoffen führen können... 2 Regeln zur Beeinflussung der Reaktionsgeschwindigkeit
Chemie. für die Berufsmaturität. Günter Baars. Chemie. Baars. Unter Mitarbeit von Franz Heini, Markus Isenschmid und Doris Kohler
 www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
2 Sehnen, Sekanten und Chordalen
 Sehnen, Seanten und Chordalen Übersiht.1 Sehnen- und Seantensatz................................................... 7. Chordalen.................................................................. 3 Weitere
Sehnen, Seanten und Chordalen Übersiht.1 Sehnen- und Seantensatz................................................... 7. Chordalen.................................................................. 3 Weitere
wir-sind-klasse.jimdo.com
 Alkohole Alkohole sind Kohlenwasserstoffverbindungen mit einer Hydroxylgruppe (funktionelle Gruppe). Ihre allgemeine Summenformel ist C n H 2n+n OH Alkohole können mit ihrer funktionellen Gruppe Wasserstoffbrückenbindungen
Alkohole Alkohole sind Kohlenwasserstoffverbindungen mit einer Hydroxylgruppe (funktionelle Gruppe). Ihre allgemeine Summenformel ist C n H 2n+n OH Alkohole können mit ihrer funktionellen Gruppe Wasserstoffbrückenbindungen
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Fossile Rohstoffe. Erdöl
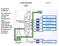 Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Rupprecht-Gymnasium München Fachschaft Chemie
 Rupprecht-Gymnasium München Fachschaft Chemie Grundwissen der 10. Klasse NTG In der Jahrgangsstufe 10 erwerben die Schüler folgendes Grundwissen: Sie kennen die wichtigsten Alkane, Alkene und Alkine, können
Rupprecht-Gymnasium München Fachschaft Chemie Grundwissen der 10. Klasse NTG In der Jahrgangsstufe 10 erwerben die Schüler folgendes Grundwissen: Sie kennen die wichtigsten Alkane, Alkene und Alkine, können
Bundesrealgymnasium Imst. Chemie Klasse 8. Aliphate
 Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1
 Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
113 Estersynthese GEFAHRENSYMBOLE SICHERHEITSRATSCHLÄGE
 113 Estersynthese GUT ZU WISSEN Die Ester sind eine große Stoffgruppe in der organischen Chemie und auch im Alltag finden haben wir häufig mit ihnen zu tun. Bekannteste Vertreter dürften wohl die Polyester
113 Estersynthese GUT ZU WISSEN Die Ester sind eine große Stoffgruppe in der organischen Chemie und auch im Alltag finden haben wir häufig mit ihnen zu tun. Bekannteste Vertreter dürften wohl die Polyester
10.1. Was versteht man unter einem Orbital? 10.2
 10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
Kohlenstoffverbindungen
 Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
10.1. Was versteht man unter einem Orbital? 10.2
 10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
2.7. Fragen zu Carbonsäuren und Estern
 Benennung Wie heißen die folgenden Verbindungen? 2.7. Fragen zu arbonsäuren und Estern NH 2 H H a) N b) H 2 a) R-2,4-Diaminobutansäure (D-Form) b) 2-Hydroxypropensäure H Struktur und Benennung Erkläre
Benennung Wie heißen die folgenden Verbindungen? 2.7. Fragen zu arbonsäuren und Estern NH 2 H H a) N b) H 2 a) R-2,4-Diaminobutansäure (D-Form) b) 2-Hydroxypropensäure H Struktur und Benennung Erkläre
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Grundwissen Chemie Klasse
 Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Versuchsprotokoll. Mischbarkeit von Alkoholen
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Aufgaben zu intermolekularen Kräften
 Aufgaben zu intermolekularen Kräften 1L ummerierung und Inhalte der gedruckten Version mit der Download-Version abgleichen! Evtl. gibt es Unterschiede. äufig enthält die Download-Version noch Bonusaufgaben.
Aufgaben zu intermolekularen Kräften 1L ummerierung und Inhalte der gedruckten Version mit der Download-Version abgleichen! Evtl. gibt es Unterschiede. äufig enthält die Download-Version noch Bonusaufgaben.
Stoffe im Alltag 8 Experimentieren in der Chemie 10
 2 Stoffe im Alltag 8 Experimentieren in der Chemie 10 Feuer und Brandbekämpfung 12 Feuer und Flamme 12 Voraussetzungen für die Verbrennung 14 Brände löschen 15 Stoffe und ihre Eigenschaften 16 Den Stoffen
2 Stoffe im Alltag 8 Experimentieren in der Chemie 10 Feuer und Brandbekämpfung 12 Feuer und Flamme 12 Voraussetzungen für die Verbrennung 14 Brände löschen 15 Stoffe und ihre Eigenschaften 16 Den Stoffen
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie
 Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Aufgabe 1 * Mischung von Flüssigkeiten 3 Gruppen mischen Spiritus mit Wasser. 3 Gruppen mischen jeweils Erbsen mit Grieß. Füllt
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Aufgabe 1 * Mischung von Flüssigkeiten 3 Gruppen mischen Spiritus mit Wasser. 3 Gruppen mischen jeweils Erbsen mit Grieß. Füllt
"Alkane, Alkene, Alkine
 Inhalt und Einsatz im Unterricht "Alkane, Alkene, Alkine Einführung in die organische Chemie" (Chemie Sek. I, Kl. 7-9) Diese DVD behandelt das Unterrichtsthema "Alkane, Alkene, Alkine" für die Klassenstufen
Inhalt und Einsatz im Unterricht "Alkane, Alkene, Alkine Einführung in die organische Chemie" (Chemie Sek. I, Kl. 7-9) Diese DVD behandelt das Unterrichtsthema "Alkane, Alkene, Alkine" für die Klassenstufen
2.5. Alkohole und Ether
 2.5. Alkohole und Ether 2.5.1. Alkohole Alkohole mit entsprechenden Alkanen vergleichen (Geruch, Aggregatzustand) Alkohole zeichnen sich durch ydroxylgruppen (-Gruppen) aus und werden durch Anhängen der
2.5. Alkohole und Ether 2.5.1. Alkohole Alkohole mit entsprechenden Alkanen vergleichen (Geruch, Aggregatzustand) Alkohole zeichnen sich durch ydroxylgruppen (-Gruppen) aus und werden durch Anhängen der
1.9. Zwischenmolekulare Kräfte
 1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
Grundwissen Chemie 10. Jahrgangsstufe
 Grundwissen Chemie 10. Jahrgangsstufe 1. Kohlenwasserstoffe - Alkane gesättigte Kohlenwasserstoffe (nur Einfachbindungen) mit der allgemeinen Summenformel C n H 2n+2 homologe Reihe (= Gruppe chemisch verwandter
Grundwissen Chemie 10. Jahrgangsstufe 1. Kohlenwasserstoffe - Alkane gesättigte Kohlenwasserstoffe (nur Einfachbindungen) mit der allgemeinen Summenformel C n H 2n+2 homologe Reihe (= Gruppe chemisch verwandter
Robert-Koch-Gymnasium Deggendorf. Grundwissen Chemie. 10. Jahrgangsstufe (WSG)
 obertkochgymnasium Deggendorf Grundwissen Chemie 10. Jahrgangsstufe (WSG) Molekülstruktur und Stoffeigenschaften rbitalmodell: Die Elektronen in der Atomhülle befinden sich in rbitalen (rt mit der höchsten
obertkochgymnasium Deggendorf Grundwissen Chemie 10. Jahrgangsstufe (WSG) Molekülstruktur und Stoffeigenschaften rbitalmodell: Die Elektronen in der Atomhülle befinden sich in rbitalen (rt mit der höchsten
CoA H C 6 H C 10. Die Trivialnamen der fett geschriebenen Carbonsäuren sollten Sie kennen.
 Vorlesung 42 Fette und Öle sind mit Glycerin veresterte arbonsäuren. Sie sind die energiereichsten Nahrungsmittel und bilden die Energiereserve des tierischen und pflanzlichen rganismus. 2 R R 2 R 1 2
Vorlesung 42 Fette und Öle sind mit Glycerin veresterte arbonsäuren. Sie sind die energiereichsten Nahrungsmittel und bilden die Energiereserve des tierischen und pflanzlichen rganismus. 2 R R 2 R 1 2
Organische Stofflehre
 Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Präparat 1: Darstellung von Essigsäurebutylester
 hristina Sauermann 1 - A- Praktikum Präparat 1: Darstellung von Essigsäurebutylester 3 3 ( 2 ) 3 2 S 4 (konz.) in l 3 3 4 9 Essigsäure Butanol Essigsäurebutylester ( 2 4 2 ) ( 4 10 ) ( 6 12 2 ) M = 60,05
hristina Sauermann 1 - A- Praktikum Präparat 1: Darstellung von Essigsäurebutylester 3 3 ( 2 ) 3 2 S 4 (konz.) in l 3 3 4 9 Essigsäure Butanol Essigsäurebutylester ( 2 4 2 ) ( 4 10 ) ( 6 12 2 ) M = 60,05
Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur
 Versuchsanweisung: Eigenschaften von Alkoholen, die ydroxylgruppe als funktionelle Gruppe Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur Organische Substanzen bestehen zum
Versuchsanweisung: Eigenschaften von Alkoholen, die ydroxylgruppe als funktionelle Gruppe Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur Organische Substanzen bestehen zum
