Achtung: dieses Antragsformular gilt nicht für Studien, die dem Arzneimittelgesetz 40ff. (AMG) oder dem Medizinproduktegesetz
|
|
|
- Marielies Althaus
- vor 7 Jahren
- Abrufe
Transkript
1 Achtung: dieses Antragsformular gilt nicht für Studien, die dem Arzneimittelgesetz 40ff. (AMG) oder dem Medizinproduktegesetz 20ff. (MPG) unterliegen! Antrag an die Ethikkommission an der Technischen Universität Dresden zur Durchführung klinischer Untersuchungen am Menschen Allgemeine Hinweise zur Antragstellung: - Einreicheschluss ist immer der 4. des Sitzungsmonats - Alle Unterlagen sind in deutscher Sprache vorzulegen. Wenn der Prüfplan englischsprachig ist, muss eine deutsche Synopse beigefügt werden. - Sämtliche Unterlagen sind 1x in Papierform, geheftet und 1x auf CD-ROM einzureichen. Papierversion und elektronische Version müssen identisch sein! Beantragung einer Beratung gemäß: 15 der Berufsordnung für Ärzte in Sachsen 1 Abs. 3 Satz 1 der Satzung der Ethikkommission an der Technischen Universität Dresden (gilt für Zahnmediziner, Psychologen, Nichtmediziner etc.) Antragsteller: Bei Einreichung der Unterlagen durch Dritte (Firmen, CRO, Studienzentrale etc.) muss zwingend eine Vollmacht des hiesigen Prüfers vorgelegt werden! Titel/Name: Vorname: Klinik/Institut: Straße: PLZ, Ort: -Adresse: Prof. Dr. med. Hohenstein Bernd Medizinische Klinik III, Bereich Nephrologie Fetscherstr Dresden bernd.hohenstein@uniklinikum-dresden.de Telefon-Nr.: Bitte beantworten Sie soweit wie möglich die einzelnen Fragen direkt - wenn der vorgesehene Platz nicht ausreicht, verweisen Sie auf zuzuordnende Anlagen. 1. Bezeichnung der Studie: Register zur Epidemiologie, Diagnostik und Therapie der C3 Glomerulopathie und der Immunkomplex vermittelten MPGN 2. Liegt oder lag die Studie in dieser oder ähnlicher Form bereits einer anderen Ethik-Kommission vor? wenn ja, welcher?
2 3. Fragestellung und Ziel der Studie: Aufgrund der gewachsenen Erkenntnis, dass es sich bei der membranoproliferativen Glomerulonephritis (MPGN) weniger um eine Erkrankungsentität, als vielmehr um ähnliche histopathologische Erscheinungsformen unterschiedlicher Nierenerkrankungen handelt [1], erfolgte im Jahr 2010 eine neue Klassifizierung in Immunkomplex und Komplement vermittelte Formen [2]. Entsprechend einem aktuellen internationalen Konsensus ist bei Letzteren der Oberbegriff einer Glomerulonephritis mit dominanten C3 Ablagerungen zu wählen [3]. Zentrales diagnostisches Kriterium dieser Komplement vermittelten Formen ist nun die alleinige oder dominante (definiert als mehr als 2 fach stärker als für Immunglobuline ausgeprägte) Ablagerung von Komplement C3 in der immunhistochemischen/immunfluoreszenz Diagnostik. Neben nicht näher definierten anderen Formen und der postinfektiösen Glomerulonephritis ist die sogenannte C3 Glomerulopathie (C3G) der wesentliche Vertreter dieser Krankheitsbilder, welche dann entsprechend der vorherrschenden histologischen Ablagerungsmuster in weitere Untergruppen (z.b. membranoproliferative C3G, mesangiale C3G, membranöse C3G = dense deposit disease) gegliedert werden können [4]. Finden sich im Rahmen der immunhistochemischen Diagnostik dagegen keine dominanten Ablagerungen von Komplement C3, sondern überwiegend IgG, so ist von einer Immunkomplex vermittelten, membranoproliferativen Glomerulonephritis (sog. sekundäre MPGN) auszugehen. Zentrale Voraussetzung für die Entstehung einer C3G ist eine Dysregulation des alternativen Komplementweges, welcher dadurch ständig übermäßig stark aktiviert wird. Die gestörte Regulation führt zur vermehrten Bildung und Aktivierung der C3 Konvertase oder/und der C5 Konvertase. Sowohl der Ausfall einzelner oder mehrerer regulatorischer Komponenten wie auch eine Stabilisierung der aktivierten C3 oder C5 Konvertase können initiierende Mechanismen sein. Pathogenetisch sind dafür einerseits Mutationen im Bereich einzelner Komponenten und andererseits Autoantikörper verantwortlich, zur Dysregulation des alternativen Komplementweg führen [5 8]. Mutationen in verschiedenen für Komplementkomponenten kodierende Gene lassen sich in etwa 20 25% der C3G Fälle nachweisen [9 13]. Bei 50 80% der Patienten mit einer C3G gelingt der Nachweis von Autoantikörpern [3]. Die Kenntnis der zu Grunde liegenden Pathophysiologie ist für die weiterführende Diagnostik zur Abklärung sekundärer Ursachen wegweisend. Eine umfassende Komplementanalytik, begleitet von Antikörperscreening und humangenetischer Analyse sollten bei diesen Patienten konsequent erfolgen. Mit dem besseren Verständnis der Pathophysiologie wurden bis heute eine Reihe therapeutischer Ansätze in unterschiedlichen Konstellationen für Patienten mit C3G eingesetzt. Bis heute existieren hierzu aber keinerlei systematische Therapiestudien, die Epidemiologie und klinischen Verläufe des Krankheitsbildes sind insbesondere in Deutschland weitgehend unklar. Aufgrund der Seltenheit der Erkrankung (ca. 1 3 pro Millionen pro Jahr) können verlässliche epidemiologische Datenerhebungen nur über eine zentrale Erfassung in Form eines Registers erfolgen. Hierzu entwickelt der Antragsteller derzeit in Zusammenarbeit mit dem Koordinierungszentrum für klinische Studien der TU Dresden ein internetbasiertes Register für die Entität dieser Krankheitsbilder, welches eine Erfassung und Dokumentation diagnostischer Befunde und klinischer Verläufe ermöglichen soll, um so die Basis für weiterführende Therapiestudien zu erstellen. Die Basis für weiterführende Studien wird durch eine explorative statistische Analyse diagnostischer Befundkonstellationen und klinischer Verläufe der Registerdaten gebildet. Parallel streben wir die Sammlung von Proben der Patienten an, um in nachfolgenden Projekten gezielt nach bisher unbekannten, pathogenetisch relevanten Faktoren suchen zu können. Dieses Register wird in deutscher und englischer Sprache zur Verfügung stehen. 4. Leiter der Studie in unserem Zuständigkeitsbereich (nur 1 Leiter zulässig!): 2
3 Prof. Dr. med. Bernd Hohenstein, Bereich Nephrologie, Medizinische Klinik III Gesamtleiter der Studie in Deutschland (nur bei multizentrischen Studien): Prof. Dr. med. Bernd Hohenstein Bereich Nephrologie, Medizinische Klinik III Universitätsklinikum Carl Gustav Carus Fetscherstrasse 74, Dresden Phone: Fax: dresden.de 5. Ausführende Ärzte in unserem Zuständigkeitsbereich: Prof. Dr. med. Bernd Hohenstein Prof. Dr. med. Christian Hugo PD Dr. med. Jens Passauer Dr. med. Mirian Opgenoorth 6. Finanzierung der Studie: Werden Drittmittel eines industriellen Sponsors eingeworben? wenn ja, Sponsorvertrag beifügen! Kostenübernahmeerklärung des Sponsors (ausgefülltes Formular beifügen!) Werden Drittmittel eines öffentlichen Geldgebers (DFG, BMBF u.ä.) eingeworben? wenn ja, bitte angeben: Antrag auf Entgeltbefreiung (ausgefülltes Formular beifügen!) Es werden keine Drittmittel eingeworben. Antrag auf Entgeltbefreiung (ausgefülltes Formular beifügen!) 7. Art der Studie: Handelt es sich um eine - offene Studie - kontrollierte Studie gegen Placebo gegen Vergleichspräparat (bitte angeben) Ist eine statistische Fallzahlschätzung erfolgt? Angaben zur Biometrie: Es handelt sich um eine offene Registerstudie, für die eine biometrische Planung nicht notwendig ist. Die Registerdaten werden einer explorativen Datenanalyse unterzogen, über die Häufigkeiten von 3
4 Befundkonstellationen und klinischen Verläufen evaluiert und als epidemiologische Datengrundlage für nachfolgende Studien verwendet werden. 8. Untersuchung an - gesunden Probanden - symptomtragenden Probanden - Patienten Sind die Personen voll geschäftsfähig? Wenn nein: nähere Angaben (z.b. Minderjährige; eingeschränkt geschäftsfähige Personen; geschäftsunfähige Personen; Personen, für die ein Betreuer bestellt wurde) 9. Unterbringung der unter 8. genannten Personen: - ambulant - stationär 10. Voraussichtliche Dauer für den Probanden/Patienten: Aufklärung über die Teilnahme an der Studie, ca. 15 bis 30 Minuten pro Patient. 11. Aufwandsentschädigung/Honorar vorgesehen? 12. Zur Anwendung kommende Geräte/Substanzen: (Beschreibung; internationaler Freiname und/oder Strukturformel) entfällt 13. Studienbedingte Maßnahmen an Probanden/Patienten - stationärer Aufenthalt - Blutentnahmen - Blasenkatheter - Endoskopie - Biopsien - radioaktive Substanzen - Therapiepausen - weitere Maßnahmen: KEINE Zwingend auszufüllen! Angaben zum möglichen Einsatz einer Strahlenanwendung (Zutreffendes ankreuzen) Bitte beachten Sie hierzu das Informationsblatt Anpassung an StrahlSchV und RöV auf der Homepage der Ethikkommission: A: Bei der klinischen Prüfung erfolgt keine Strahlenanwendung, die in den Geltungsbereich von StrlSchV oder RöV fällt, oder die Strahlenanwendung wird nur mit der sog. rechtfertigenden Indikation eines fachkundigen Arztes gemäß 80 StrlSchV bzw. 23 RöV eingesetzt. Die betroffene Person würde die gleiche Strahlenanwendung (Art, Umfang, Häufigkeit) erhalten, wenn sie nicht an der Studie teilnimmt. B: Bei der klinischen Prüfung wird die Strahlenanwendung im Rahmen der sog. Begleitdiagnostik gemäß 24 (2) Nr. 1 StrlSchV bzw. 28b (2) Nr. 1 RöV eingesetzt (z.b. Verlaufskontrolle). Dabei muss die Art der Anwendung dem medizinischen Standard entsprechen, die Art und die Häufigkeit müssen dem Zweck des Forschungsvorhabens entsprechen, die Patienten 4
5 müssen einwilligungsfähig sein. Eine Genehmigung im vereinfachten Verfahren nach 23 u. 24 (2) StrlSchV bzw. 28a u. 28b (2) RöV wird beim BfS (Bundesamt für Strahlenschutz) beantragt. C: Bei der klinischen Prüfung erfolgt eine studienbedingte Strahlenanwendung entweder zur Entwicklung / Erprobung von Strahlenanwendung in Diagnostik/Therapie oder als begleitdiagnostische Strahlenanwendung, für die nicht alle Voraussetzungen von 24 (2) Nr. 1 StrlSchV bzw. 28b (2) Nr. 1 RöV erfüllt sind. Eine Genehmigung im ausführlichen Verfahren nach 23 u. 24 (1) StrlSchV bzw. 28a u. 28b (1) RöV wird beim BfS beantragt. Bitte beachten Sie, dass die Ethik-Kommission in den Fällen B und C bestätigen muss, dass für das beantragte Forschungsvorhaben ein zwingendes Bedürfnis gemäß 24 (1) StrlSchV bzw. 28b (1) RöV besteht. Hierzu ist ein gesonderter Antrag (Download auf der Homepage der Ethikkommission) erforderlich! 14. Dient die Studie - auch unmittelbar dem Interesse des Probanden/Patienten? - einem rein wissenschaftlichen Ziel ohne unmittelbaren diagnostischen oder therapeutischen Wert für den Probanden/Patienten? 15. Zusammenfassende Bewertung des ärztlichen Leiters zur Risiko-Nutzen-Abwägung der Studie: Es handelt sich um eine Registerstudie mit dem Ziel, eine epidemiologische Datenbasis für multizentrische Therapiestudien zu etablieren. In Abwägung der Teilnahme ohne studienbedingte obligatorische Blutentnahme überwiegt der potentielle Nutzen für den einzelnen Patienten vor dem Hintergrund einer derzeit nicht therapierbaren progredient verlaufenden Erkrankung klar gegenüber dem Risiko. Welche Nebenwirkungen sind im Rahmen der Studie zu erwarten? Im Rahmen der Studie erfolgt ggf. eine Blutentnahme für nachfolgende Analysen hinsichtlich der Pathophysiologie. Die Blutentnahme beinhaltet das geringe Risiko der lokalen Infektion, Gefäß und Nervenverletzung und erfolgt im Rahmen routinemäßiger medizinischer Laborkontrollen. 16. Liegen zu der geplanten Studie bereits vor - Literatur? - Labor- (in vitro-) Versuche? - Tierversuche? - Untersuchungen am Menschen als Fallbeschreibungen über die Verträglichkeit (Phase I)? Wirksamkeit (Phase II)? Klinische Prüfung (Phase III)? (gemäß den Richtlinien über die Prüfung von Arzneimitteln) siehe Anlage Nr.: 17. Bestehender Versicherungsschutz: - für den Patienten/Probanden 5
6 Art des Versicherungsschutzes - verschuldensabhängig (Haftpflichtversicherung) - ereignisabhängig (Unfallversicherung) - Wegeunfallversicherung wenn nein, muss in der Patienten/Probandeninformation darüber aufgeklärt werden Die Studie findet ausschließlich im Rahmen notwendiger medizinischer Kontrollen statt, ebenso die Blutentnahme für die nicht obligatorischen Proben. Den Versicherungsschutz hierfür obliegt entsprechend der Haftpflichtversicherung der jeweiligen Einrichtung. 18. Darstellung der geplanten Versuchsanordnung (Versuchsprotokoll) siehe Anlage Nr.: 1 Die Datenerfassung und auswertung erfolgt pseudonymisiert (verschlüsselt). In geplanten Publikationen werden nur anonymisierte Daten verwendet. Eine Weitergabe von Daten an Dritte, die nicht an der Studie beteiligt sind, wird unter keinen Umständen erfolgen. Soweit es zur Überprüfung der Studie notwendig ist, kann ein autorisierter und zur Verschwiegenheit verpflichteter Beauftragter der Ethik Kommission in die vorhandenen Daten Einsicht nehmen. Die Erhebung im Rahmen des Registers beinhaltet keinerlei therapeutische Vorgaben oder diagnostische Maßgaben, erfasst aber sämtliche klinisch diagnostischen therapeutisch gebräuchlichen Vorgehensweisen für die Gruppe der C3 Glomerulopathie und Immunkomplex vermittelten Glomerulonephritiden. Zusätzlich werden Verlaufsparameter der Patienten in Abständen von 3 12 Monaten erhoben. Die betroffenen Patienten werden entweder in einem lokalen Schwerpunktzentrum vor Ort, oder aber nach Überweisung über den Bereich Nephrologie des Universitätsklinikums Dresden eingeschlossen. Alle Behandler/Patienten werden gebeten, dass für weiterführende Analysen insgesamt 4 Proben (2x Serum, 2x EDTA abzentrifugiert und eingefroren, insgesamt ca. 30ml) und eine Urinprobe asserviert und übereignet werden. Folgende Parameter werden erhoben: bei Diagnosestellung: egfr (ml/min/1,73m 2 ), Proteinurie (g/g Kreatinin oderg/24h), Vorhanden sein eines nephrotischen Syndroms Vorhandensein Arterielle Hypertonie, familiäres Auftreten, Vorliegen einer sekundären Ursache. Aktuelle Medikation. Histopathologische Befunde (MPGN Typ 1 od. Typ 2 od. Typ 3, Dense Deposit Disease, C3 Glomerulonephritis, C3 Glomerulopathie, Immunkomplexvermittelter MPGN), Befundender Pathologe, Schriftlicher Endbefund Komplementdiagnostik nach Diagnosestellung: Vorliegen einer funktionellen Komplementanalytik incl. Auffälligkeiten, Vorliegen einer humangenetischen Diagnostik bekannter, pathophysiologisch relevanter Gene incl. Auffälligkeiten, Pathophysiologisch relevante Auto Antikörper (C3NeF, anti C3, anti CFB, anti CFH) Klinischer Verlauf: Nierenfunktionsveränderung seit Diagnose, Zeit bis zur Halbierung der egfr / Verdopplung des Serumkreatinins, Aktuelle Medikation, Dialysepflichtigkeit (Nein, Ja), Zeit bis zur Dialysepflichtigkeit Durchführung einer Nierentransplantation (Nein, Ja), falls ja, Rezidiv im Transplantat (Nein, Ja) nach welcher Zeit, Bemerkung (Freitext) Therapie: Eine Therapie ist erfolgt (Nein, Ja), falls Ja wie (supportiv, Immunmodulation mit XY), Wirksamkeit der Therapie. 19. Aufklärung der Patienten/Probanden über die Studie: 6
7 (u.a. Ziel, Durchführung, individueller Nutzen, Risiken, Belastungen, Freiwilligkeit, Widerrufsrecht, Versicherung) - mündlich und schriftlich Die entsprechenden Unterlagen sind in jedem Fall zum Verbleib beim Probanden/Patienten auszuhändigen. siehe Anlage Nr.: Dokumentation der Einwilligung der Patienten/Probanden: siehe Anlage Nr.: Patienten-/Probanden-Dokumentationsbögen: siehe Anlage Nr.: Entfällt, da elektronisch via Datenbank Dresden, den Leiter der Studie Direktor der Klinik/des Institutes Literatur: 1. Walker, P.D., et al., Dense deposit disease is not a membranoproliferative glomerulonephritis. Mod Pathol, (6): p Fakhouri, F., et al., C3 glomerulopathy: a new classification. Nat Rev Nephrol, (8): p Pickering, M.C., et al., C3 glomerulopathy: consensus report. Kidney Int, (6): p Cook, H.T. and M.C. Pickering, Histopathology of MPGN and C3 glomerulopathies. Nat Rev Nephrol, (1): p Jozsi, M., et al., Autoantibodies to complement components in C3 glomerulopathy and atypical hemolytic uremic syndrome. Immunol Lett, (2): p Chen, Q., et al., Combined C3b and factor B autoantibodies and MPGN type II. N Engl J Med, (24): p Ohi, H. and T. Yasugi, Occurrence of C3 nephritic factor and C4 nephritic factor in membranoproliferative glomerulonephritis (MPGN). Clin Exp Immunol, (2): p Licht, C., et al., MPGN II--genetically determined by defective complement regulation? Pediatr Nephrol, (1): p Sethi, S., et al., C3 Glomerulonephritis Associated With Complement Factor B Mutation. Am J Kidney Dis, Tortajada, A., et al., C3 glomerulopathy-associated CFHR1 mutation alters FHR oligomerization and complement regulation. J Clin Invest, (6): p Deltas, C., et al., C3 glomerulonephritis/cfhr5 nephropathy is an endemic disease in Cyprus: clinical and molecular findings in 21 families. Adv Exp Med Biol, : p Lesher, A.M., B. Nilsson, and W.C. Song, Properdin in complement activation and tissue injury. Mol Immunol, (3): p Martinez-Barricarte, R., et al., Human C3 mutation reveals a mechanism of dense deposit disease pathogenesis and provides insights into complement activation and regulation. J Clin Invest, (10): p
8 8
9 Anlage 1: Prüfplan Web basierte Registerdatenbank: und Datenbankentwicklung und verwaltung: Koordinierungszentrum für Klinische Studien, Technische Universität Dresden Einschlusskriterien: Männlich/ weiblich Alter Jahre Schriftliche Einwilligung des Patienten eine der nachfolgenden Diagnosen MPGN Typ 1 MPGN Typ 2 MPGN Typ 3 Dense Deposit Disease C3 Glomerulonephritis C3 Glomerulopathie Immunkomplex vermittelte MPGN Erhebung der folgenden Daten in pseudonymisierter Form: bei Diagnosestellung: egfr (ml/min/1,73m 2 ), Proteinurie (g/g Kreatinin oder g/24h), Vorhanden sein eines nephrotischen Syndroms Vorhandensein Arterielle Hypertonie, familiäres Auftreten, Vorliegen einer sekundären Ursache. Aktuelle Medikation. Histopathologische Befunde, Befundender Pathologe, Schriftlicher Endbefund 2x Serumprobe zentrifugiert, tiefgefroren (nicht verpflichtend) 2x EDTA Probe zentrifugiert, tiefgefroren (nicht verpflichtend) 1x Urinprobe tiefgefroren (nicht verpflichtend) Komplementdiagnostik nach Diagnosestellung: Vorliegen einer funktionellen Komplementanalytik incl. Auffälligkeiten, Vorliegen einer humangenetischen Diagnostik bekannter, pathophysiologisch relevanter Gene incl. Auffälligkeiten, Pathophysiologisch relevante Auto Antikörper (C3NeF, anti C3, anti CFB, anti CFH) Klinischer Verlauf: Nierenfunktionsveränderung seit Diagnose, Zeit bis zur Halbierung der egfr / Verdopplung des Serumkreatinins, aktuelle Medikation, Dialysepflichtigkeit (Nein, Ja), Zeit bis zur Dialysepflichtigkeit Durchführung einer Nierentransplantation (Nein, Ja), falls ja, Rezidiv im Transplantat (Nein, Ja) nach welcher Zeit, Bemerkung (Freitext) Therapie: Eine Therapie ist erfolgt (Nein, Ja), falls Ja wie (supportiv, Immunmodulation mit XY), Wirksamkeit der Therapie. Nachbeobachtung alle 3 12 Monate
Register zur Epidemiologie, Diagnostik und Therapie der C3 Glomerulopathie und der Immunkomplex vermittelten MPGN
 Patienteninformation und Einwilligungserklärung inkl. Datenschutzerklärung Register zur Epidemiologie, Diagnostik und Therapie der C3 Glomerulopathie und der Immunkomplex-vermittelten MPGN Kurzbezeichnung:
Patienteninformation und Einwilligungserklärung inkl. Datenschutzerklärung Register zur Epidemiologie, Diagnostik und Therapie der C3 Glomerulopathie und der Immunkomplex-vermittelten MPGN Kurzbezeichnung:
Empfehlung für den Umgang mit multizentrischen Studien außerhalb von AMG oder MPG durch Ethik-Kommissionen I. Vorbemerkungen
 Empfehlung für den Umgang mit multizentrischen Studien außerhalb von AMG oder MPG durch Ethik-Kommissionen gemäß Beschluss des Arbeitskreises Medizinischer Ethik-Kommissionen in der Bundesrepublik Deutschland
Empfehlung für den Umgang mit multizentrischen Studien außerhalb von AMG oder MPG durch Ethik-Kommissionen gemäß Beschluss des Arbeitskreises Medizinischer Ethik-Kommissionen in der Bundesrepublik Deutschland
Novellierung der Strahlenschutz- und Röntgenverordnung
 1 Novellierung der Strahlenschutz- und Röntgenverordnung Klinische Studienzentrale (CSC) Antje Wiede Neuregelung: Genehmigungsbedürftigkeit radiologischer Untersuchungen bei palliativen medikamentösen
1 Novellierung der Strahlenschutz- und Röntgenverordnung Klinische Studienzentrale (CSC) Antje Wiede Neuregelung: Genehmigungsbedürftigkeit radiologischer Untersuchungen bei palliativen medikamentösen
der Universität Witten/Herdecke e.v. z. Hd. Herrn RA Prof. Dr. med. P. Gaidzik Alfred-Herrhausen-Straße Witten Antragsformular
 Antragsteller: Ethik-Kommission der Universität Witten/Herdecke e.v. z. Hd. Herrn RA Prof. Dr. med. P. Gaidzik Alfred-Herrhausen-Straße 50 58448 Witten Antragsformular Der Antrag ist sorgfältig in deutscher
Antragsteller: Ethik-Kommission der Universität Witten/Herdecke e.v. z. Hd. Herrn RA Prof. Dr. med. P. Gaidzik Alfred-Herrhausen-Straße 50 58448 Witten Antragsformular Der Antrag ist sorgfältig in deutscher
Antrag auf biometrische und datentechnische Unterstützung von medizinischen Forschungsprojekten
 Antrag auf biometrische und datentechnische Unterstützung von medizinischen Forschungsprojekten Angaben zur Person Anrede Frau Titel Professor Herr Doktor Name Vorname Email Telefon Klinik-/Institutsbezeichnung
Antrag auf biometrische und datentechnische Unterstützung von medizinischen Forschungsprojekten Angaben zur Person Anrede Frau Titel Professor Herr Doktor Name Vorname Email Telefon Klinik-/Institutsbezeichnung
Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer
 Prüferbewertung und Eignung von Prüfstellen Worauf achtet die Ethikkommission? Prof. Dr. Joerg Hasford Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer Die nachfolgenden Ausführungen
Prüferbewertung und Eignung von Prüfstellen Worauf achtet die Ethikkommission? Prof. Dr. Joerg Hasford Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer Die nachfolgenden Ausführungen
Antrag zur Durchführung einer epidemiologischen Studie
 Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
Anzeige einer klinischen Prüfung gemäß 67 Abs. 1 und 3 AMG und 12 Abs. 1-3 GCP-V bei der zuständigen Landesbehörde
 1. Vollständiger Titel des Prüfplans (einschl. Zielsetzung) Prüfplancode EudraCT-Nr. 2. An (Name und Anschrift der zuständigen Behörde) 3. Name (ggf. Firmenbezeichnung) und Anschrift, Telefonnummer und
1. Vollständiger Titel des Prüfplans (einschl. Zielsetzung) Prüfplancode EudraCT-Nr. 2. An (Name und Anschrift der zuständigen Behörde) 3. Name (ggf. Firmenbezeichnung) und Anschrift, Telefonnummer und
Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen und des Bundesamts für Strahlenschutz (BfS) bei Klinischen Studien
 Berlin, 17.6.2014: Pressekonferenz: Die neue EU-Verordnung zu klinischen Studien eine Chance für den Forschungsstandort Deutschland Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen
Berlin, 17.6.2014: Pressekonferenz: Die neue EU-Verordnung zu klinischen Studien eine Chance für den Forschungsstandort Deutschland Forderungen der DGHO unter Berücksichtigung der Rolle von Ethik-Kommissionen
Patienteninformation und Einwilligungserklärung. zur Teilnahme am Nephronophthise-Register
 Patienteninformation und Einwilligungserklärung zur Teilnahme am Nephronophthise-Register Auftraggeber der Studie: Prof. Dr. med. Heymut Omran Direktor der Klinik und Poliklinik für Kinder- und Jugendmedizin
Patienteninformation und Einwilligungserklärung zur Teilnahme am Nephronophthise-Register Auftraggeber der Studie: Prof. Dr. med. Heymut Omran Direktor der Klinik und Poliklinik für Kinder- und Jugendmedizin
Update Glomerulonephritis Karl Lhotta Nephrologie und Dialyse
 Update Glomerulonephritis 2012 Karl Lhotta Sicherheit und Komplikationsrate der perkutanen Nierenbiopsie (Norwegen 1988-2010) Tondel, CJASN 7:1591, 2012 Risikofaktoren für Komplikationen Risikofaktor Alter
Update Glomerulonephritis 2012 Karl Lhotta Sicherheit und Komplikationsrate der perkutanen Nierenbiopsie (Norwegen 1988-2010) Tondel, CJASN 7:1591, 2012 Risikofaktoren für Komplikationen Risikofaktor Alter
PATIENTENAUFKLÄRUNG ZWECK DER ZUSATZUNTERSUCHUNG
 Immunologische und molekularbiologische Untersuchungen im Blut und im Gewebe zur Verbesserung der Diagnostik als PATIENTENAUFKLÄRUNG Sie werden gebeten, an einer Zusatzuntersuchung zur Bestimmung Ihres
Immunologische und molekularbiologische Untersuchungen im Blut und im Gewebe zur Verbesserung der Diagnostik als PATIENTENAUFKLÄRUNG Sie werden gebeten, an einer Zusatzuntersuchung zur Bestimmung Ihres
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Anzeige einer klinischen Prüfung gemäß 67 Abs. 1 und 3 AMG und 12 Abs. 1-3 GCP-V bei der zuständigen Landesbehörde
 An (Name und Anschrift der zuständigen Behörde) Regierung von Oberbayern Zentrale Arzneimittelüberwachung Bayern (GMP/GCP) 80534 München Name (ggf. Firmenbezeichnung) und Anschrift des Anzeigenden Grund
An (Name und Anschrift der zuständigen Behörde) Regierung von Oberbayern Zentrale Arzneimittelüberwachung Bayern (GMP/GCP) 80534 München Name (ggf. Firmenbezeichnung) und Anschrift des Anzeigenden Grund
Patienteninformation zur klinischen Studie:
 UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
Patienteninformation Teil 2 Untersuchung der Erbsubstanz (genetische und epigenetische Untersuchung) der Blutproben für das
 Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten
 PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
PATIENTEN INFORMATION. Deutsches Klinisches Register. Therapie und medizinische Versorgung von Patienten mit moderater bis schwerer Neurodermitis
 PATIENTEN INFORMATION Deutsches Klinisches Register Therapie und medizinische Versorgung von Patienten mit moderater bis schwerer Neurodermitis Sehr geehrte Patientin, Sehr geehrter Patient, wir möchten
PATIENTEN INFORMATION Deutsches Klinisches Register Therapie und medizinische Versorgung von Patienten mit moderater bis schwerer Neurodermitis Sehr geehrte Patientin, Sehr geehrter Patient, wir möchten
Name, Vorname, Titel. Vertragliche Tätigkeit beantragt am für folgende Fachrichtung: Aufnahme der Tätigkeit geplant zum Tätigkeit aufgenommen am
 KV HESSEN I Europa-Allee 90 I 60486 Frankfurt Kassenärztliche Vereinigung Hessen Qualitätssicherung Europa-Allee 90 60486 Frankfurt Photodynamische Therapie am Augenhintergrund Antrag auf Genehmigung zur
KV HESSEN I Europa-Allee 90 I 60486 Frankfurt Kassenärztliche Vereinigung Hessen Qualitätssicherung Europa-Allee 90 60486 Frankfurt Photodynamische Therapie am Augenhintergrund Antrag auf Genehmigung zur
2. Um welche Art von Biomaterialien und Daten handelt es sich?
 150701 Biobank Augenklinik Version 1_modek.docx Klinik für Augenheilkunde Universitätsklinikum Freiburg Killianstraße 5 D-79106 Freiburg Spende, Einlagerung und Nutzung von Biomaterialien sowie Erhebung,
150701 Biobank Augenklinik Version 1_modek.docx Klinik für Augenheilkunde Universitätsklinikum Freiburg Killianstraße 5 D-79106 Freiburg Spende, Einlagerung und Nutzung von Biomaterialien sowie Erhebung,
Modul 2 Arbeitskreis Medizinischer Ethik-Kommissionen in Deutschland
 Modul 2 Arbeitskreis Medizinischer Ethik-Kommissionen in Deutschland Entwickelt auf der Basis der Detailed guidance on the application format and documentation to be submitted in an application for an
Modul 2 Arbeitskreis Medizinischer Ethik-Kommissionen in Deutschland Entwickelt auf der Basis der Detailed guidance on the application format and documentation to be submitted in an application for an
Klinisch wissenschaftliches Begleitprogramm
 Version 3.0; Köln, den 26.07.2010 Sponsor Code: Uni-Koeln-1167 Sponsor: Universität zu Köln Leiter der Klinischen Prüfung: Prof. Dr. A. Engert Patienteninformation Phase I Studie mit AVD plus Lenalidomid
Version 3.0; Köln, den 26.07.2010 Sponsor Code: Uni-Koeln-1167 Sponsor: Universität zu Köln Leiter der Klinischen Prüfung: Prof. Dr. A. Engert Patienteninformation Phase I Studie mit AVD plus Lenalidomid
STUDIEN PRO UND CONTRA
 V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
Antrag auf Ermächtigung zur ambulanten psychotherapeutischen und psychiatrischen Versorgung
 Achtung: Die Seiten 1-6 des Antrages aufgrund der elektronischen Erfassung bitte nur komplett einrei- chen!! Andernfalls ist eine Bearbeitung nicht möglich. An die Geschäftsstelle des Zulassungsausschusses
Achtung: Die Seiten 1-6 des Antrages aufgrund der elektronischen Erfassung bitte nur komplett einrei- chen!! Andernfalls ist eine Bearbeitung nicht möglich. An die Geschäftsstelle des Zulassungsausschusses
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Johannes Drach Medizinische Universität Wien Univ. Klinik für Innere Medizin I Klinische Abteilung
Richtlinien des Bundesausschusses der Zahnärzte und Krankenkassen
 Richtlinien des Bundesausschusses der Zahnärzte und Krankenkassen über die Einführung neuer Untersuchungs- und Behandlungsmethoden und die Überprüfung erbrachter vertragszahnärztlicher Leistungen (NUB-Richtlinien)
Richtlinien des Bundesausschusses der Zahnärzte und Krankenkassen über die Einführung neuer Untersuchungs- und Behandlungsmethoden und die Überprüfung erbrachter vertragszahnärztlicher Leistungen (NUB-Richtlinien)
Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen
 Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation. Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group
 Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Hämatologie im Wandel, Frankfurt 28. Februar 2015 2 Überblick Einführung
Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Hämatologie im Wandel, Frankfurt 28. Februar 2015 2 Überblick Einführung
Zulassungsüberschreitende Anwendung von Arzneimitteln im Rahmen klinischer Studien ( 35c SGB V)
 Zulassungsüberschreitende Anwendung von Arzneimitteln im Rahmen klinischer Studien ( 35c SGB V) Berlin, 22. September 2009 Dr. Regina Skavron Abteilung Arzneimittel, Gemeinsamer Bundesausschuss Zulassungsüberschreitende
Zulassungsüberschreitende Anwendung von Arzneimitteln im Rahmen klinischer Studien ( 35c SGB V) Berlin, 22. September 2009 Dr. Regina Skavron Abteilung Arzneimittel, Gemeinsamer Bundesausschuss Zulassungsüberschreitende
Studienprojekt Candidämie des NRZ für Systemische Mykosen
 Studienprojekt Candidämie des NRZ für Systemische Mykosen PD Dr. med. Margarete Borg-von Zepelin Institut für Medizinische Mikrobiologie; Universitätsklinikum Göttingen Nationales Referenzzentrum für systemische
Studienprojekt Candidämie des NRZ für Systemische Mykosen PD Dr. med. Margarete Borg-von Zepelin Institut für Medizinische Mikrobiologie; Universitätsklinikum Göttingen Nationales Referenzzentrum für systemische
Übung 6 im Fach "Biometrie / Q1"
 Universität Ulm, Institut für Epidemiologie und Medizinische Biometrie, D-89070 Ulm Institut für Epidemiologie und Medizinische Biometrie Leiter: Prof. Dr. D. Rothenbacher Schwabstr. 13, 89075 Ulm Tel.
Universität Ulm, Institut für Epidemiologie und Medizinische Biometrie, D-89070 Ulm Institut für Epidemiologie und Medizinische Biometrie Leiter: Prof. Dr. D. Rothenbacher Schwabstr. 13, 89075 Ulm Tel.
Antrag auf Genehmigung zur Ausführung und Abrechnung von Leistungen der Positronenemissionstomographie
 Kassenärztliche Vereinigung Hamburg Qualitätssicherung Postfach 76 06 20 22056 Hamburg Arztstempel Antrag auf Genehmigung zur Ausführung und Abrechnung von Leistungen der Positronenemissionstomographie
Kassenärztliche Vereinigung Hamburg Qualitätssicherung Postfach 76 06 20 22056 Hamburg Arztstempel Antrag auf Genehmigung zur Ausführung und Abrechnung von Leistungen der Positronenemissionstomographie
Titel der Studie: Umfrage zur Gebrauchstauglichkeit von Patientendatenmanagementsystemen (PDMS) auf deutschen Intensivstationen
 Studiensynopse Titel der Studie: Umfrage zur Gebrauchstauglichkeit von Patientendatenmanagementsystemen (PDMS) auf deutschen Intensivstationen Sponsor der Studie und Datenverarbeitende Stelle: Deutsche
Studiensynopse Titel der Studie: Umfrage zur Gebrauchstauglichkeit von Patientendatenmanagementsystemen (PDMS) auf deutschen Intensivstationen Sponsor der Studie und Datenverarbeitende Stelle: Deutsche
Patienteninformation. Sehr geehrte Patientin, sehr geehrter Patient,
 und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
Merkblatt für einen Antrag auf Ermächtigung zur Teilnahme an der vertragsärztlichen Versorgung
 Bezirksstelle Köln Ansprechpartner / Ansprechpartnerin: Geschäftsstelle Frau Raffaela Bamberg 0221 7763-6512 0221 7763-6500 Zulassungsausschuss Frau Johanna Erpelding 0221 7763-6518 0221 7763-6500 Sedanstr.
Bezirksstelle Köln Ansprechpartner / Ansprechpartnerin: Geschäftsstelle Frau Raffaela Bamberg 0221 7763-6512 0221 7763-6500 Zulassungsausschuss Frau Johanna Erpelding 0221 7763-6518 0221 7763-6500 Sedanstr.
Sammlung personenbezogener Daten Deutsche PSP-Gesellschaft e.v. Datenschutzkonzept
 Sammlung personenbezogener Daten Deutsche PSP-Gesellschaft e.v Datenschutzkonzept (Version August 2016) Projekt Sammlung personenbezogener Daten von Interessenten für Forschungs-Therapie- und Beobachtungsstudien
Sammlung personenbezogener Daten Deutsche PSP-Gesellschaft e.v Datenschutzkonzept (Version August 2016) Projekt Sammlung personenbezogener Daten von Interessenten für Forschungs-Therapie- und Beobachtungsstudien
Zeitschrift für Nephrologie und Hypertensiologie Organ der Deutschen Gesellschaft für Innere Medizin Organ des Berufsverbandes Deutscher Internisten
 Der Nephrologe Zeitschrift für Nephrologie und Hypertensiologie Organ der Deutschen Gesellschaft für Innere Medizin Organ des Berufsverbandes Deutscher Internisten Elektronischer Sonderdruck für B. Hohenstein
Der Nephrologe Zeitschrift für Nephrologie und Hypertensiologie Organ der Deutschen Gesellschaft für Innere Medizin Organ des Berufsverbandes Deutscher Internisten Elektronischer Sonderdruck für B. Hohenstein
Antrag auf Ausführung und Abrechnung von molekulargenetischen Untersuchungen bei monogenen Erkrankungen
 Kassenärztliche Vereinigung Berlin Abteilung Qualitätssicherung Masurenallee 6A 14057 Berlin Praxisstempel Telefon (030) 31003-307, Fax (030) 31003-305 Antrag auf Ausführung und Abrechnung von molekulargenetischen
Kassenärztliche Vereinigung Berlin Abteilung Qualitätssicherung Masurenallee 6A 14057 Berlin Praxisstempel Telefon (030) 31003-307, Fax (030) 31003-305 Antrag auf Ausführung und Abrechnung von molekulargenetischen
Richtlinien der Ethik-Kommission der Medizinischen Fakultät der Christian-Albrechts-Universität zu Kiel. 1 (Präambel)
 Richtlinien der Ethik-Kommission der Medizinischen Fakultät der Christian-Albrechts-Universität zu Kiel 1 (Präambel) (1) Die Medizinische Fakultät der Christian-Albrechts-Universität zu Kiel hat am 10.05.1976
Richtlinien der Ethik-Kommission der Medizinischen Fakultät der Christian-Albrechts-Universität zu Kiel 1 (Präambel) (1) Die Medizinische Fakultät der Christian-Albrechts-Universität zu Kiel hat am 10.05.1976
kontrolliert wurden. Es erfolgte zudem kein Ausschluss einer sekundären Genese der Eisenüberladung. Erhöhte Ferritinkonzentrationen wurden in dieser S
 5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
Studien in der Onkologie Bewertung und Bedeutung
 Studien in der Onkologie Bewertung und Bedeutung Referentin Annette Schuster Münchner Studienzentrum am Klinikum rechts der Isar der Technischen Universität t MünchenM 1 eigentlich wollte ich nicht an
Studien in der Onkologie Bewertung und Bedeutung Referentin Annette Schuster Münchner Studienzentrum am Klinikum rechts der Isar der Technischen Universität t MünchenM 1 eigentlich wollte ich nicht an
Hämaturie, Proteinurie und Niereninsuffizienz...
 Fallvorstellung Nephrologie Hämaturie, Proteinurie und Niereninsuffizienz... Georg Georges Fall 1 22jähriger BWL-Student Praktikum in Singapur Routineuntersuchung: Mikrohämaturie + Proteinurie Vorstellung
Fallvorstellung Nephrologie Hämaturie, Proteinurie und Niereninsuffizienz... Georg Georges Fall 1 22jähriger BWL-Student Praktikum in Singapur Routineuntersuchung: Mikrohämaturie + Proteinurie Vorstellung
Zur Anwendung radioaktiver Stoffe oder ionisierender Strahlen in der medizinischen Forschung Genehmigungsverfahren nach 28a RöV und 23 StrlSchV
 Strahlenschutzkommission Geschäftsstelle der Strahlenschutzkommission Postfach 12 06 29 D-53048 Bonn http://www.ssk.de Zur Anwendung radioaktiver Stoffe oder ionisierender Strahlen in der medizinischen
Strahlenschutzkommission Geschäftsstelle der Strahlenschutzkommission Postfach 12 06 29 D-53048 Bonn http://www.ssk.de Zur Anwendung radioaktiver Stoffe oder ionisierender Strahlen in der medizinischen
Informationsschrift. Momentum Projekt Heidelberg Aktiver Umgang mit einer Krebserkrankung
 Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Die Bedeutung der Qualitätssicherung in der klinischen Forschung
 Die Bedeutung der Qualitätssicherung in der klinischen Forschung Am Beispiel eines externen Qualitätsaudits Nadja Schachteli 1 Qualitätskontrolle und Qualitätssicherung, GCP 5.1.1 Der Sponsor ist für die
Die Bedeutung der Qualitätssicherung in der klinischen Forschung Am Beispiel eines externen Qualitätsaudits Nadja Schachteli 1 Qualitätskontrolle und Qualitätssicherung, GCP 5.1.1 Der Sponsor ist für die
Der informierte Patient als Wegbereiter der zukünftigen Forschung
 Der informierte Patient als Wegbereiter der zukünftigen Forschung Riegler S., Macheiner T., Riegler A. MedPro 2014, Brandenburg Agenda Die Rolle des informierten Patienten im Bereich Biobanking Der Einwilligungsprozess
Der informierte Patient als Wegbereiter der zukünftigen Forschung Riegler S., Macheiner T., Riegler A. MedPro 2014, Brandenburg Agenda Die Rolle des informierten Patienten im Bereich Biobanking Der Einwilligungsprozess
Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale Erkrankungen (mitonet)
 Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale Erkrankungen (mitonet) Das wesentliche Ziel des mitonet ist der Aufbau eines deutschlandweiten Netzwerks aus Klinikern
Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale Erkrankungen (mitonet) Das wesentliche Ziel des mitonet ist der Aufbau eines deutschlandweiten Netzwerks aus Klinikern
Hinweise zur Antragstellung
 ETHIK-KOMMISSION der Medizinischen Fakultät der Ruhr-Universität Bochum Vorsitzender: Prof. Dr. M. Zenz Geschäftsführende Ärztin: Christine Schnell Sekretariat: Gabriele Crüsemann Geschäftsstelle: Gesundheitscampus
ETHIK-KOMMISSION der Medizinischen Fakultät der Ruhr-Universität Bochum Vorsitzender: Prof. Dr. M. Zenz Geschäftsführende Ärztin: Christine Schnell Sekretariat: Gabriele Crüsemann Geschäftsstelle: Gesundheitscampus
Antrag auf Zulassung zur Promotion zum Doktor der Zahnmedizin
 Dekanat Medizinische Fakultät Antrag auf Zulassung zur Promotion zum Doktor der Zahnmedizin 1. Hiermit beantrage ich die Zulassung zur Promotion zum Doktor der Zahnmedizin Name Geburtsname Vorname(n)-Rufname
Dekanat Medizinische Fakultät Antrag auf Zulassung zur Promotion zum Doktor der Zahnmedizin 1. Hiermit beantrage ich die Zulassung zur Promotion zum Doktor der Zahnmedizin Name Geburtsname Vorname(n)-Rufname
INSTITUT FÜR ANGEWANDTE QUALITÄTSFÖRDERUNG UND FORSCHUNG IM GESUNDHEITSWESEN
 INSTITUT FÜR ANGEWANDTE QUALITÄTSFÖRDERUNG UND FORSCHUNG IM GESUNDHEITSWESEN SCOPING-WORKSHOP Nierenersatztherapie bei chronischem Nierenversagen QS-Datenerhebung in der Dialysepraxis Therapeutische Konsequenzen
INSTITUT FÜR ANGEWANDTE QUALITÄTSFÖRDERUNG UND FORSCHUNG IM GESUNDHEITSWESEN SCOPING-WORKSHOP Nierenersatztherapie bei chronischem Nierenversagen QS-Datenerhebung in der Dialysepraxis Therapeutische Konsequenzen
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG
 Studiennummer: - PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Registerstudie zur Proktokolektomie bei Colitis ulcerosa (ReProCu-Studie) Dokumentation zur Erforschung der Colitis ulcerosa für die verbesserte
Studiennummer: - PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Registerstudie zur Proktokolektomie bei Colitis ulcerosa (ReProCu-Studie) Dokumentation zur Erforschung der Colitis ulcerosa für die verbesserte
Antrag bei der Krankenkasse Zur Übernahme der Behandlungskosten - Off Label Therapie bei Uveitis - Patient:, geb. Datum:
 Antrag bei der Krankenkasse Zur Übernahme der Behandlungskosten - Off Label Therapie bei Uveitis - Patient:, geb. Datum: Augen-Diagnosen (bitte alle auflisten): Uveitis bekannt seit: Symptome durch die
Antrag bei der Krankenkasse Zur Übernahme der Behandlungskosten - Off Label Therapie bei Uveitis - Patient:, geb. Datum: Augen-Diagnosen (bitte alle auflisten): Uveitis bekannt seit: Symptome durch die
Zulassung von Arzneimitteln. Klinische Untersuchungen. Katalin Müllner
 Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Bekanntmachung über die Zulassung, Nachzulassung und Registrierung von Arzneimitteln (Empfehlungen der Kommission D
 Bekanntmachung über die Zulassung, Nachzulassung und Registrierung von Arzneimitteln (Empfehlungen der Kommission D nach 25 Abs. 6 und Abs. 7 des Arzneimittelgesetzes zur Planung und Durchführung homöopathischer
Bekanntmachung über die Zulassung, Nachzulassung und Registrierung von Arzneimitteln (Empfehlungen der Kommission D nach 25 Abs. 6 und Abs. 7 des Arzneimittelgesetzes zur Planung und Durchführung homöopathischer
Kassenärztliche Vereinigung Hessen. Qualitätssicherung Substitution & weitere Genehmigungen. Europa-Allee Frankfurt
 KV HESSEN I Europa-Allee 90 I 60486 Frankfurt Kassenärztliche Vereinigung Hessen Qualitätssicherung Substitution & weitere Genehmigungen Europa-Allee 90 60486 Frankfurt Substitutionsgestützte Behandlung
KV HESSEN I Europa-Allee 90 I 60486 Frankfurt Kassenärztliche Vereinigung Hessen Qualitätssicherung Substitution & weitere Genehmigungen Europa-Allee 90 60486 Frankfurt Substitutionsgestützte Behandlung
Antrag auf Zulassung zur Promotion zum Doktor der Medizin
 Dekanat Medizinische Fakultät Antrag auf Zulassung zur Promotion zum Doktor der Medizin 1. Hiermit beantrage ich die Zulassung zur Promotion zum Doktor der Medizin Name Geburtsname Vorname(n)-Rufname bitte
Dekanat Medizinische Fakultät Antrag auf Zulassung zur Promotion zum Doktor der Medizin 1. Hiermit beantrage ich die Zulassung zur Promotion zum Doktor der Medizin Name Geburtsname Vorname(n)-Rufname bitte
Wichtige Informationen zur Anforderung von Untersuchungen von somatischen Mutionen in den BRCA1 und BRCA2-Genen an Tumormaterial
 Wichtige Informationen zur Anforderung von Untersuchungen von somatischen Mutionen in den BRCA1 und BRCA2-Genen an Tumormaterial Zur Durchführung der BRCA1/2-Analysen müssen der Molekularpathologie Südbayern
Wichtige Informationen zur Anforderung von Untersuchungen von somatischen Mutionen in den BRCA1 und BRCA2-Genen an Tumormaterial Zur Durchführung der BRCA1/2-Analysen müssen der Molekularpathologie Südbayern
Landesamt für Gesundheit und Soziales Ethik-Kommission des Landes Berlin
 Landesamt für Gesundheit und Soziales Ethik-Kommission des Landes Berlin Christian v. Dewitz Leiter der Geschäftsstelle Ethik-Kommission Definition ( 3 Abs. 2c GCP-V): Ethik-Kommission ist ein unabhängiges
Landesamt für Gesundheit und Soziales Ethik-Kommission des Landes Berlin Christian v. Dewitz Leiter der Geschäftsstelle Ethik-Kommission Definition ( 3 Abs. 2c GCP-V): Ethik-Kommission ist ein unabhängiges
Anlage 1 zum Vertrag zur Verbesserung der medizinischen Versorgung in Sachsen
 Anlage 1 zum Vertrag zur Verbesserung der medizinischen Versorgung in Sachsen zwischen der Kassenärztlichen Vereinigung Sachsen (nachfolgend KVS genannt) und der DAK-Gesundheit Vertragsgebiet Sachsen (nachfolgend
Anlage 1 zum Vertrag zur Verbesserung der medizinischen Versorgung in Sachsen zwischen der Kassenärztlichen Vereinigung Sachsen (nachfolgend KVS genannt) und der DAK-Gesundheit Vertragsgebiet Sachsen (nachfolgend
Erfahrungen mit GCP Inspektionen von MPG Studien
 Erfahrungen mit GCP Inspektionen von MPG Studien Yvonne Borck, Universitätsklinik Bonn Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v Hintergrund Nach 26 MPG unterliegen Betriebe und
Erfahrungen mit GCP Inspektionen von MPG Studien Yvonne Borck, Universitätsklinik Bonn Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v Hintergrund Nach 26 MPG unterliegen Betriebe und
Inhalt des Leitfadens. Wo wird der neue Leitfaden zu finden sein?
 NEU! LEITFADEN Klinische Prüfung von Medizinprodukten (MP) und Leistungsbewertungsprüfung von In-vitro-Diagnostika (IVD) Einreichung und Durchführung Dr. med. Violetta Zmuda AGES MEA, Institut Überwachung,
NEU! LEITFADEN Klinische Prüfung von Medizinprodukten (MP) und Leistungsbewertungsprüfung von In-vitro-Diagnostika (IVD) Einreichung und Durchführung Dr. med. Violetta Zmuda AGES MEA, Institut Überwachung,
Hinweise zum Versicherungsschutz
 Hinweise zum Versicherungsschutz 1. Versicherungspflicht a) AMG- und MPG-Studien Studien am Menschen zur Prüfung von Arzneimitteln und Medizinprodukten unterliegen einer gesetzlichen Versicherungspflicht
Hinweise zum Versicherungsschutz 1. Versicherungspflicht a) AMG- und MPG-Studien Studien am Menschen zur Prüfung von Arzneimitteln und Medizinprodukten unterliegen einer gesetzlichen Versicherungspflicht
Tabellarischer Ablauf des Forschungsvorhabens
 Antrag zur Beurteilung eines Forschungsvorhabens an die Ethik-Kommission der Fachbereich 03 Rechts- und Wirtschaftswissenschaften der Johannes Gutenberg-Universität Mainz Allgemeine Angaben 1. Dem Antrag
Antrag zur Beurteilung eines Forschungsvorhabens an die Ethik-Kommission der Fachbereich 03 Rechts- und Wirtschaftswissenschaften der Johannes Gutenberg-Universität Mainz Allgemeine Angaben 1. Dem Antrag
Diagnostik und Versorgung von Patienten im Rahmen der pädiatrischen Kardiologie Anlage 3, Nr. 8
 Antrag nach 116 b SGB V Krankenhaus Diagnostik und Versorgung von Patienten im Rahmen der pädiatrischen Kardiologie Anlage 3, Nr. 8 1. Konkretisierung der Erkrankung und des Behandlungsauftrages mittels
Antrag nach 116 b SGB V Krankenhaus Diagnostik und Versorgung von Patienten im Rahmen der pädiatrischen Kardiologie Anlage 3, Nr. 8 1. Konkretisierung der Erkrankung und des Behandlungsauftrages mittels
Informationsschrift. Momentum Projekt Heidelberg Aktiver Umgang mit einer Krebserkrankung
 Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Kritische Gesichtspunkte zu Umbrella Protokollen und Adaptiven Designs aus der Sicht der Genehmigungsbehörde
 Kritische Gesichtspunkte zu Umbrella Protokollen und Adaptiven Designs aus der Sicht der Genehmigungsbehörde Heiko Preußer, BfArM Sachgebietsleiter Klinik Fachgebiet Klinische Prüfung Historischer Überblick
Kritische Gesichtspunkte zu Umbrella Protokollen und Adaptiven Designs aus der Sicht der Genehmigungsbehörde Heiko Preußer, BfArM Sachgebietsleiter Klinik Fachgebiet Klinische Prüfung Historischer Überblick
Antrag. auf Genehmigung zur Beschäftigung eines Sicherstellungsassistenten wegen belegärztlicher Tätigkeit nach 32 Abs. 2 Ärzte-ZV
 Kassenärztliche Vereinigung Bayerns Sicherstellung Elsenheimerstr. 39 80687 München Antrag auf Genehmigung zur Beschäftigung eines Sicherstellungsassistenten wegen belegärztlicher Tätigkeit nach 32 Abs.
Kassenärztliche Vereinigung Bayerns Sicherstellung Elsenheimerstr. 39 80687 München Antrag auf Genehmigung zur Beschäftigung eines Sicherstellungsassistenten wegen belegärztlicher Tätigkeit nach 32 Abs.
Anamnesebogen. Zyklusanamnese Frau. Frühere Verhütungsmethoden: letzte Vorsorgeuntersuchung bei Ihrem Frauenarzt: Familienkrankengeschichte:
 Anamnesebogen Zyklusanamnese Erste Regelblutung im Alter von ca Jahren 1. Tag der letzten Regel: Blutungsrhythmus:! regelmäßig, zwischen und Tagen! unregelmäßig zwischen und T/W/M! keine Regelblutungen
Anamnesebogen Zyklusanamnese Erste Regelblutung im Alter von ca Jahren 1. Tag der letzten Regel: Blutungsrhythmus:! regelmäßig, zwischen und Tagen! unregelmäßig zwischen und T/W/M! keine Regelblutungen
Ambulante MRSA-Versorgung Abrechnung und Vergütung seit
 Ambulante MRSA-Versorgung Abrechnung und Vergütung seit 01.04.2014 Steffen Göhring Hauptabteilungsleiter Abrechnung KV Thüringen Versorgung von MRSA im ambulanten Bereich seit 01.04.2012 Infolge der Änderungen
Ambulante MRSA-Versorgung Abrechnung und Vergütung seit 01.04.2014 Steffen Göhring Hauptabteilungsleiter Abrechnung KV Thüringen Versorgung von MRSA im ambulanten Bereich seit 01.04.2012 Infolge der Änderungen
PATIENTENINFORMATION. Caregiver Burden bei betreuenden Angehörigen schwer betroffener Parkinsonpatienten
 Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Die Antragstellung erfolgt für mich persönlich (gilt nicht für angestellte Ärzte) LANR: (lebenslange Arztnummer, falls diese bekannt ist) LANR: LANR:
 Antrag auf Genehmigung zur Durchführung und Abrechnung von Leistungen der MR-Angiographie gemäß der Vereinbarung von Qualitätssicherungsmaßnahmen nach 135 Abs. 2 SGB V (Qualitätssicherungsvereinbarung
Antrag auf Genehmigung zur Durchführung und Abrechnung von Leistungen der MR-Angiographie gemäß der Vereinbarung von Qualitätssicherungsmaßnahmen nach 135 Abs. 2 SGB V (Qualitätssicherungsvereinbarung
Entscheidungen vor dem Hintergrund des Patientenrechtegesetzes
 Entscheidungen vor dem Hintergrund des Patientenrechtegesetzes Juristische Aspekte Johannes Schopohl 9. Landespsychotherapeutentag Berlin Berlin, 9. März 2013 Überblick 1. Juristischer Hintergrund von
Entscheidungen vor dem Hintergrund des Patientenrechtegesetzes Juristische Aspekte Johannes Schopohl 9. Landespsychotherapeutentag Berlin Berlin, 9. März 2013 Überblick 1. Juristischer Hintergrund von
Probandeninformation für Patienten mit Bluthochdruck
 Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Probandeninformation für Patienten mit Bluthochdruck Studie über Monoamine-produzierende Tumore The PMT-study: Prospective
Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Probandeninformation für Patienten mit Bluthochdruck Studie über Monoamine-produzierende Tumore The PMT-study: Prospective
Sehr geehrte Ratsuchende!
 Genetische Beratung Sehr geehrte Ratsuchende! Sie möchten sich über die Risiken einer erblichen Erkrankung informieren, die bei Ihnen selbst, Ihren Kindern oder Verwandten aufgetreten ist? Sie möchten
Genetische Beratung Sehr geehrte Ratsuchende! Sie möchten sich über die Risiken einer erblichen Erkrankung informieren, die bei Ihnen selbst, Ihren Kindern oder Verwandten aufgetreten ist? Sie möchten
PROGRAMM. 1. Schulungstag: Mittwoch, von 09:00-16:30 Uhr 2. Schulungstag: Mittwoch, von 09:00-16:30 Uhr
 PROGRAMM GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG mit Wissensprüfung* ) + Teilnahmezertifikat 1. Schulungstag: Mittwoch, 30.09.2015 von 09:00-16:30
PROGRAMM GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG mit Wissensprüfung* ) + Teilnahmezertifikat 1. Schulungstag: Mittwoch, 30.09.2015 von 09:00-16:30
Pharmaökonomiestudien (PÖS) unter Praxisbedingungen. Ein realistischer Weg zur Kosten-Effektivitäts-Bewertung von Arzneimitteln.
 Pharmaökonomiestudien (PÖS) unter Praxisbedingungen Ein realistischer Weg zur Kosten-Effektivitäts-Bewertung von Arzneimitteln. 6 Kernfragen der Wirtschaftlichkeitsbewertung einer Arzneimittelverordnung
Pharmaökonomiestudien (PÖS) unter Praxisbedingungen Ein realistischer Weg zur Kosten-Effektivitäts-Bewertung von Arzneimitteln. 6 Kernfragen der Wirtschaftlichkeitsbewertung einer Arzneimittelverordnung
Europäische Verfahren
 Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Patientenfragebogen zur Indikationsstellung der Lipoproteinapherese nach Anlage I 1 Richtlinie Methoden vertragsärztlicher Versorgung
 Antragsversendung an: KVN, Unternehmensbereich Vertragsärztliche Versorgung, Berliner Allee 22, 30175 Hannover Patientenfragebogen zur Indikationsstellung der Lipoproteinapherese nach Anlage I 1 Richtlinie
Antragsversendung an: KVN, Unternehmensbereich Vertragsärztliche Versorgung, Berliner Allee 22, 30175 Hannover Patientenfragebogen zur Indikationsstellung der Lipoproteinapherese nach Anlage I 1 Richtlinie
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v.
 Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Die medizinische Einrichtung. erfüllt die Voraussetzungen für die Erbringung der folgenden Methoden:
 Checkliste des Gemeinsamen Bundesausschusses zur Abfrage der Qualitätskriterien zum Beschluss über Maßnahmen zur Qualitätssicherung bei interstitieller Low-Dose- Rate-Brachytherapie zur Behandlung des
Checkliste des Gemeinsamen Bundesausschusses zur Abfrage der Qualitätskriterien zum Beschluss über Maßnahmen zur Qualitätssicherung bei interstitieller Low-Dose- Rate-Brachytherapie zur Behandlung des
zur Durchführung und Abrechnung von Leistungen der invasiven Kardiologie (Vereinbarung zur invasiven Kardiologie)
 Abteilung Qualitätssicherung Bismarckallee 1-6 23795 Bad Segeberg Tel.: 04551/883-533 Fax: 04551/883-7533 email: christine.sancion@kvsh.de ANTRAG zur Durchführung und Abrechnung von Leistungen der invasiven
Abteilung Qualitätssicherung Bismarckallee 1-6 23795 Bad Segeberg Tel.: 04551/883-533 Fax: 04551/883-7533 email: christine.sancion@kvsh.de ANTRAG zur Durchführung und Abrechnung von Leistungen der invasiven
Patienteninformation:
 Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
Das bürgerliche Probandenrecht ein vernachlässigtes Thema? unter Berücksichtigung der neuen Verordnung (EU) 536/2014
 Das bürgerliche Probandenrecht ein vernachlässigtes Thema? unter Berücksichtigung der neuen Verordnung (EU) 536/2014 über klinische Prüfung mit Humanarzneimitteln Arbeitskreis Ärzte und Juristen der AWMF
Das bürgerliche Probandenrecht ein vernachlässigtes Thema? unter Berücksichtigung der neuen Verordnung (EU) 536/2014 über klinische Prüfung mit Humanarzneimitteln Arbeitskreis Ärzte und Juristen der AWMF
WILLKOMMEN im virtuellen Konferenzraum
 DLR-PT.de Folie 1 WILLKOMMEN im virtuellen Konferenzraum Klinische Studien mit hoher Relevanz für die Versorgung älterer und hochaltriger Patientinnen und Patienten Das Web-Seminar beginnt um 10:00 Uhr.
DLR-PT.de Folie 1 WILLKOMMEN im virtuellen Konferenzraum Klinische Studien mit hoher Relevanz für die Versorgung älterer und hochaltriger Patientinnen und Patienten Das Web-Seminar beginnt um 10:00 Uhr.
Institut für Klinische Chemie (Zentrallabor) Zur Studienanmeldung, möchten wir Sie bitten dieses Formular auszufüllen.
 Studienanmeldung Zur Studienanmeldung, möchten wir Sie bitten dieses Formular auszufüllen. Bitte beachten Sie bei Ihrer Planung, dass für die Studienanmeldung eine Mindestbearbeitungszeit von 8 Wochen
Studienanmeldung Zur Studienanmeldung, möchten wir Sie bitten dieses Formular auszufüllen. Bitte beachten Sie bei Ihrer Planung, dass für die Studienanmeldung eine Mindestbearbeitungszeit von 8 Wochen
Analyse der Ergebnisse Mukoviszidose Register. Marguerite Honer Qualitätsmanagement Mukoviszidose Institut
 Analyse der Ergebnisse Mukoviszidose Register Marguerite Honer Qualitätsmanagement Mukoviszidose Institut Fakten Finanzierung des CF Registers ausschließlich durch Spenden des Mukoviszidose e.v und der
Analyse der Ergebnisse Mukoviszidose Register Marguerite Honer Qualitätsmanagement Mukoviszidose Institut Fakten Finanzierung des CF Registers ausschließlich durch Spenden des Mukoviszidose e.v und der
Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid
 10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
Antrag. Name, Vorname Ich bin in Einzelpraxis/Berufsausübungsgemeinschaft zugelassener Vertragsarzt seit/ab: tt.mm.jj
 Kassenärztliche Vereinigung Bayerns Qualitätssicherung Vogelsgarten 6 90402 Nürnberg Antrag auf Genehmigung zur Ausführung und Abrechnung von ärztlichen Leistungen zur Diagnostik und ambulanten Eradikationstherapie
Kassenärztliche Vereinigung Bayerns Qualitätssicherung Vogelsgarten 6 90402 Nürnberg Antrag auf Genehmigung zur Ausführung und Abrechnung von ärztlichen Leistungen zur Diagnostik und ambulanten Eradikationstherapie
1 von :09
 1 von 5 09.06.2011 15:09 2 von 5 09.06.2011 15:09 Klinische Studien CAI Prüfplancode ISRCTN EudraCT Clinicaltrials.gov DRKS CAI n/a NCT00126321 Therapie von Patienten mit rezidivierter akuter myeloischer
1 von 5 09.06.2011 15:09 2 von 5 09.06.2011 15:09 Klinische Studien CAI Prüfplancode ISRCTN EudraCT Clinicaltrials.gov DRKS CAI n/a NCT00126321 Therapie von Patienten mit rezidivierter akuter myeloischer
Ultraschallgesteuerte Punktion der Niere und von Gefäßen zur Katheteranlage
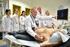 3. Brandenburger Nephrologie Kolleg 06. Juni 2013 Ultraschallgesteuerte Punktion der Niere und von Gefäßen zur Katheteranlage Karsten Schlieps St. Joseph Krankenhaus, Berlin Tempelhof Nierenbiopsie Indikationen
3. Brandenburger Nephrologie Kolleg 06. Juni 2013 Ultraschallgesteuerte Punktion der Niere und von Gefäßen zur Katheteranlage Karsten Schlieps St. Joseph Krankenhaus, Berlin Tempelhof Nierenbiopsie Indikationen
Förderung Klinischer Studien durch die Deutsche Forschungsgemeinschaft
 Förderung Klinischer Studien durch die Deutsche Forschungsgemeinschaft Dr. Eckard Picht Deutsche Forschungsgemeinschaft Gruppe Medizin Übersicht des Vortrags Die Deutsche Forschungsgemeinschaft Förderung
Förderung Klinischer Studien durch die Deutsche Forschungsgemeinschaft Dr. Eckard Picht Deutsche Forschungsgemeinschaft Gruppe Medizin Übersicht des Vortrags Die Deutsche Forschungsgemeinschaft Förderung
Membranoproliferative Glomerulonephritis (MPGN)
 Membranoproliferative Glomerulonephritis (MPGN) Die membranoproliferative Glomerulonephritis (MPGN) ist eine seltene Nierenerkrankung, die klinisch durch Hämaturie, Proteinurie, Hypertension und histologisch
Membranoproliferative Glomerulonephritis (MPGN) Die membranoproliferative Glomerulonephritis (MPGN) ist eine seltene Nierenerkrankung, die klinisch durch Hämaturie, Proteinurie, Hypertension und histologisch
Studienvereinbarung / Study Agreement
 Studienwerberin/Studienwerber Matrikelnummer Akad. Grad, Vorname/n, Familienname geb. am in (Ort) Kennzeichnung des Studiums: Q794445202 Clinical PhD Studium Studienadresse (Straße) PLZ, Ort Telefonnummer:
Studienwerberin/Studienwerber Matrikelnummer Akad. Grad, Vorname/n, Familienname geb. am in (Ort) Kennzeichnung des Studiums: Q794445202 Clinical PhD Studium Studienadresse (Straße) PLZ, Ort Telefonnummer:
BESCHLUSS. des Erweiterten Bewertungsausschusses nach 87 Abs. 4 SGB V in seiner 53. Sitzung am 19. Dezember Teil A
 BESCHLUSS des Erweiterten Bewertungsausschusses nach 87 Abs. 4 SGB V in seiner 53. Sitzung am 19. Dezember 2017 Teil A zur Änderung des Einheitlichen Bewertungsmaßstabes (EBM) mit Wirkung zum 1. Januar
BESCHLUSS des Erweiterten Bewertungsausschusses nach 87 Abs. 4 SGB V in seiner 53. Sitzung am 19. Dezember 2017 Teil A zur Änderung des Einheitlichen Bewertungsmaßstabes (EBM) mit Wirkung zum 1. Januar
DFV Deutsche Familienversicherung AG Reuterweg Frankfurt. Schadenanzeige Unfallversicherung
 DFV Deutsche Familienversicherung AG Reuterweg 47 60323 Frankfurt Schadenanzeige Unfallversicherung Sehr geehrter Versicherungsnehmer, eine schnelle Bearbeitung des Versicherungsfalles ist nur möglich,
DFV Deutsche Familienversicherung AG Reuterweg 47 60323 Frankfurt Schadenanzeige Unfallversicherung Sehr geehrter Versicherungsnehmer, eine schnelle Bearbeitung des Versicherungsfalles ist nur möglich,
auf Genehmigung zur Durchführung von Leistungen der nuklearmedizinischen Diagnostik und Therapie im Rahmen der vertragsärztlichen Versorgung
 und Therapie im Rahmen der vertragsärztlichen Versorgung gemäß der Vereinbarung zur Strahlendiagnostik und -therapie nach 135 Abs. 2 SGB V Antragsteller/-in: (Vertragsarzt, ermächtigter Arzt, MVZ und Name
und Therapie im Rahmen der vertragsärztlichen Versorgung gemäß der Vereinbarung zur Strahlendiagnostik und -therapie nach 135 Abs. 2 SGB V Antragsteller/-in: (Vertragsarzt, ermächtigter Arzt, MVZ und Name
Workshop 1 AMNOG stratifizierte Medizin. Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH
 Workshop 1 AMNOG stratifizierte Medizin Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH 1. Welche Chancen und Risiken sind mit einer Stratifizierung in der Arzneimitteltherapie für
Workshop 1 AMNOG stratifizierte Medizin Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH 1. Welche Chancen und Risiken sind mit einer Stratifizierung in der Arzneimitteltherapie für
