Institut für Energiespeicherung Prof. Dr. André Thess. Praktikum. Betrieb eines Batterie-Brennstoffzellen- Hybridsystems
|
|
|
- Rainer Richter
- vor 7 Jahren
- Abrufe
Transkript
1 Praktikum Betrieb eines Batterie-Brennstoffzellen- Hybridsystems
2 Einleitung Der zunehmende Leistungsbedarf mobiler und portabler Anwendungen erfordert Energiespeicher- und Ernergiewandlersysteme mit hohem Wirkungsgrad, hoher spezifischer Energie und großer Energiedichte. Des Weiteren wird auf Grund der knapper werdenden fossilen Brennstoffe der Betrieb mit regenerativ gewinnbaren Rohstoffen (z.b. Wasserstoff oder Bio-Ethanol ) in absehbarer Zukunft eine gesteigerte Rolle spielen. Neben den sich weiter entwickelnden Batterien, v. a. Lithium-Systeme, erfüllen Brennstoffzellen (BSZ) diese Anforderungen sehr gut. Aufgrund der spezifischen Charakteristika von Brennstoffzellen wird deren alleiniger Einsatz nur in Ausnahmefällen erfolgen. Daraus resultiert die Notwendigkeit so genannte Hybridsysteme zu entwickeln und zu testen. Dabei wird einem BSZ-System eine Pufferkomponente, wie z.b. Kondensatoren oder sekundäre Batterien, zur Seite gestellt, die kurzfristige Lastsprünge und Spitzenlasten abdecken. Abb. 1: Nexa-Stack von Ballard mit 1,2 kw Nominalleistung Das vorgestellte System der Firma Heliocentris kombiniert dabei einen 1,2 kw-pefc-stack von Ballard (Abb. 1) mit Blei-Akkus. Zur Demonstration sind verschiedene Einstellungen zwischen beiden Komponenten möglich, die die unterschiedlichen Betriebsarten abbilden. Die Extremfälle stellen dabei der reine Batterie- bzw. der reine BSZ-Betrieb dar. Die elektrische Verschaltung ist in Abb. 2 dargestellt. Abb. 2: Verschaltung des Hybridsystems ( Power In entspricht dem BSZ-Stack)
3 Grundlagen Brennstoffzellen Der Fokus dieses Praktikumversuchs liegt auf dem Verhalten von Brennstoffzellen, konkret den Polymer-Elektrolyt-BSZ (PEFC). Dieser Typ funktioniert bei relativ niedrigen Temperaturen von unter 100 C, benötigt allerdings eine ausreichende Befeuchtung der Gase im Betrieb. Aktuelle Forschungen beschäftigen sich mit der Anhebung dieser Betriebstemperatur auf bis zu 180 C um zum einen die Vergiftungsanfälligkeit des Katalysators zu verringern und um zum anderen das Wassermanagement zu minimieren. Abb. 3: Aufbau einer PEFC [1] und eines Stacks In Abb. 3 ist der schematische Aufbau dargestellt, wobei der Grundaufbau aller BSZ, unabhängig vom Typ, identisch ist und dem aller galvanischen Elemente, einschließlich Batterien, entspricht. Es gibt die Anode, an der das Brenngas reagiert, eine gasdichte und ionenleitende Membran, die beide Elektroden voneinander trennt sowie eine Kathode, an der das Oxidationsmittel reduziert wird. Beide Elektroden sind über einen äußeren elektrischen Kreis verbunden, an dem ein Verbraucher angeschlossen werden kann. Die Komponenten einer PEFC und die am häufigsten eingesetzten Materialien sind in Tabelle 1 zusammengefasst. Ebenso sind die Aufgaben und Anforderungen aufgeführt. Komponente Material Aufgaben Anforderungen Graphit Abdichten der Zelle nach Außen gasdicht Bipolarplatte Metall Stromabnehmer elektrisch leitfähig Festigkeit/Stabilisierung mechanisch stabil Gasdiffusions- beschichtetes Kohlegewebe elektrische Kontaktierung elektrisch leitfähig schicht Kohlepapier (z. B. Toray) gleichmäßige Verteilung der Gase hydrophob Metall Wasserhaushalt porös katalytisch Elektroden Katalysator und Additive chemische Reaktionszone porös (Pt, C, PTFE, Ionomer) elektrische und ionische Leitfähigkeit Elektrolyt Ionomer (z.b. Nafion) Trennung Elektrodenräume gasdicht Ionenleitung Ionenleitend Tabelle 1: Komponenten einer PEFC [2]
4 Für den Betrieb einer Wasserstoff/Sauerstoff-Zelle ergeben sich vereinfacht folgende Reaktionen: Anode: Kathode: Gesamtreaktion: H 2 2 2H e (Gl. 1) 1 O2 2H 2e H 2O 2 (Gl. 2) 1 O2 H O (Gl. 3) 2 H 2 2 Anhand der chemischen Reaktionspartner lässt sich mit Hilfe der Nernst-Gleichung E 0,5 R * T p H 2 R * T po2 Erev ln ln 0, (Gl. 4) 2 * F po2 2 * F p0 5 die maximal erreichbare Spannung in einer solchen Zelle errechnen. Diese ist bei Normalbedingungen: E0=1,229 V Allerdings stellt dieser Wert lediglich eine theoretische Größe dar, da keinerlei Verluste durch einen technischen Aufbau berücksichtigt werden. Daher werden in realen Systemen lediglich offene Zellspannungen, also ohne Belastung der Zellen, von rund 1 V erreicht. Um einen Verbraucher anzutreiben ist jedoch ein Stromfluss notwendig. Dieser ergibt sich anhand der Polarisationskurve, auch U(j)-Kennlinie genannt. Darin wird ein Zusammenhang zwischen Stromdichte und Spannung bzw. Leistung(-sdichte) hergestellt. Eine typische Kurve ist in Abb. 4 dargestellt. Die Stromdichte errechnet sich als Quotient aus Stromstärke und der Elektrodenfläche der verwendeten Zelle, wodurch eine bessere Vergleichbarkeit einzelner Zellen möglich wird. Bei Stacks wird hingegen im Normalfall die Stackspannung in Abhängigkeit von der Stackstromstärke aufgetragen (dann als U(I)-Kennlinie bezeichnet), da dort die Gesamtleistung im Vordergrund steht und das Verhalten der Einzelzellen eine untergeordnete Rolle spielt. Spannung / mv Stromdichte / ma*cm -2 Abb. 4: Polarisationskurve einer PEFC im H2/O2-Betrieb 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 Leistungsdichte / W*cm -2
5 Die U(j)-Kennlinie kann in drei Abschnitte eingeteilt werden, die durch unterschiedliche Mechanismen dominiert werden. Im Bereich 1 sind vor allem die Aktivierungsverluste zu finden, die aufgrund der technischen Komponenten entstehen. So ist die Membran nicht absolut gasdicht, es gibt einen geringen Durchtritt von H2, der zu einer Mischpotentialbildung führt. Des Weiteren sind die Hemmungen durch den nicht idealen Katalysator abgebildet. Im zweiten Abschnitt dominieren die ohm schen Verluste, die aufgrund von Kontakt- und Durchtrittswiderständen auftreten. Im Sinne von einfachen Widerständen bezeichnen sie die Behinderung der Elektronen bzw. Ionen in der Zelle. Ein wichtiger Aspekt dabei ist der Wasserhaushalt, der bei einer PEFC eine entscheidende Rolle spielt. Aktuelle Membranen, meistens aus Nafion, stellen nur im feuchten Zustand einen ausreichend guten Ionenleiter dar. Daher muss immer Wasser in der Zelle vorhanden sein, wobei zu viel H2O zu einer Verstopfung des Drei-Phasen-Gebietes führt. Dadurch kann die Reaktionszone nicht mehr mit ausreichend Gas versorgt werden. Ein zu geringer Wasseranteil führt logischerweise zu einem Austrocknen der Membran und damit zu einem erhöhten Innenwiderstand. Die Wasserbalance stellt also einen kritischen Aspekt in der Betriebsführung einer PEFC dar und beeinflusst vor allem den ohm schen Bereich der Polarisationskurve sehr deutlich. Der dritte Bereich schließlich zeigt die Diffusionslimitierung der BSZ. Aufgrund der physikalischen Randbedingungen kann nur eine begrenzte Menge an Gas transportiert werden. Die notwendige Menge an Brenngas für eine einzelne Brennstoffzelle (bei gegebener Stromstärke) kann mit Hilfe des Farraday-Gesetzes bestimmt werden: m Q * z * F I * t (Gl. 5) M Die Menge an Oxidationsmittel (z. B. Sauerstoff aus der Luft) errechnet sich dann anhand von Gl. 3. Übersteigt der Gasbedarf die zur Verfügung stehende Menge an Brennstoff, kommt es zu einem starken Leistungsabfall. Die Erhöhung des Druckes und/oder des Durchflusses kann diese Limitierung zu höheren Stromstärken verschieben, eine andere Möglichkeit ist die Veränderung der Kanalstruktur bzw. der Gasdiffusionsschichten. Die Erfahrung hat gezeigt, dass eine PEFC deutlich bessere Leistungen bringt, wenn die Gasflüsse höher als notwendig liegen, also ein sogenannter überstöchiometrischer Betrieb vorliegt. Daher werden die Ergebnisse aus Gl. 5 mit einem Stöchiometriefaktor λ multipliziert, üblicherweise 1,5 für das Brenngas und 2 für das Oxidationsmittel. Im Ballard-Stack wird anodenseitig ein so genannter Dead-End -Betrieb betrieben. Das heißt, dass es auf der Anode nur eine Gaszufuhr gibt, aber keinen Abgasstrang. Dadurch wird die Ausbeute verbessert, da der gesamte Wasserstoff verbraucht wird und nur soviel nachgeführt wird, wie Bedarf vorhanden ist. Problematisch ist der Wasserhaushalt, weil kein Abtransport des sich sammelnden Wassers erfolgt. Gelöst wird dieses Problem durch regelmäßiges Spülen der Anode. Auf der Kathode wird Umgebungsluft als Oxidationsmittel verwendet. Neben der Polarisations- und Leistungskennlinie spielt der Wirkungsgrad in den Betrachtungen zu Energiewandlern eine zentrale Rolle. In der Literatur finden sich viele Ansätze die Effizienz einer BSZ zu beurteilen. An dieser Stelle sollen lediglich zwei genannt werden. Das ist zum einen der theoretisch maximale (Gl. 6) und zum anderen ein technisch relevanter (Gl. 7) Wirkungsgrad, der die abgreifbare elektrische Leistung in Relation zur zugeführten chemischen Energie setzt: G ideal (Gl. 6) H
6 und el U * V H 2 Institut für Energiespeicherung P BSZ (Gl. 7) H Beim Ersteren ergibt sich für die Reaktion aus Gl. 3 unter Standardbedingungen ein Wert von 83 %. Für technische reale Systeme werden unter optimalen Bedingungen gemäß Gl. 7 Wirkungsgrade von rund 50 % erzielt. Batterien Auf den Aufbau und die Funktionsweise von Batterien und speziell Akkumulatoren soll an dieser Stelle nicht konkret eingegangen werden. Sie dienen in diesem Fall lediglich der beispielhaften Darstellung des Hybridbetriebs. Um die Arbeitsweise des Systems zu verstehen ist allerdings eine kurze Betrachtung der Betriebsweise einer Batterie unumgänglich. In Abb. 5 sind einige Entladekurven in Abhängigkeit von der Zeit dargestellt. Dabei wird der Lade- und Entladestrom einer Batterie als C-Koeffizient bezeichnet. Die meisten tragbaren Batterien sind eingestellt für 1 C. Das heißt, dass eine Batterie mit 1000 mah einen Strom von 1000 ma während einer Stunde abgeben kann, wenn der Koeffizient 1 C beträgt. Wenn dieselbe Batterie mit 0,5 C entladen wird, gibt sie 500 ma während 2 Stunden ab. Bei 2 C liefert die 1000 mah Batterie 2000 ma während 30 Minuten. 1 C wird oft bezeichnet als 1-Stunden-Entladung, eine 0,5 C würde eine 2-Stunden- und eine 0,1 C eine 10-Stunden-Entladung bedeuten [3]. Bei dem Versuch werden zwei Blei-Akkus vom Typ WP 18-12, mit einer Kapazität von 18 Ah bei einer Entladung mit 0,1 C und von 8,1 Ah bei einem Entladung mit 1 C, eingesetzt. Die Nennspannung liegt jeweils bei 12 V, im Betrieb werden die Batterien allerdings bis zu einem Maximum von 15 V geladen [4]. Abb. 5: Entladekurve Batterie unter verschiedenen Belastungen [3]
7 Versuchsdurchführung Die Versuche sollen den Unterschied zwischen Batterie und Brennstoffzelle verdeutlichen, des Weiteren sollen die Vorteile einer Kopplung beider Techniken demonstriert werden. Zu diesem Zweck werden statische und dynamische Belastungen beider Systeme miteinander verglichen. Versuch 1 Nach dem Start wird das System so eingestellt, dass ein reiner Batteriebetrieb zu verzeichnen ist. Um die technische Handhabbarkeit zu verdeutlichen wird ein konstanter Strom von 35 A durch die elektronische Last angelegt, gleichzeitig wird der Verlauf der Spannung aufgezeichnet. Um eine aussagekräftiges Ergebnis zu bekommen, sollte diese Einstellung für rund 5 Minuten beibehalten werden. Wird ein definierter Ladezustand unterschritten schaltet das Heliocentris-System selbstständig den BSZ-Stack zu. Die BSZ-Parameter (Leistung, Strom, ) werden dabei im Vorhinein definiert und werden nicht verändert. Mit Hilfe dieser Einstellungen kann der Anwender das System seinen Bedürfnissen anpassen und entsprechend seiner Anforderungen betreiben. Versuch 2 Als zweiter Versuch wird eine vollständige Belastungskennlinie der Batterie abgefahren. Aufgrund der sich ändernden Stromstärken (siehe Tabelle) liegt eine quasi-dynamische Belastung vor, da das System auf die Lastsprünge reagieren muss. Die Haltezeit pro Stufe sollte ca. 1 Minute betragen. Während der U(I)-Kennlinie befindet sich die BSZ im Ruhezustand. Versuch 3 Nach einem Umbau der Anlage ist der Betrieb des BSZ-Stacks ohne Akku-Unterstützung und DC/DC-Wandler möglich. Um einen Vergleich mit der Batterie zu ermöglichen werden die gleichen Aufgaben gestellt. Zuerst wird bei einem konstanten Strom (35 A) die Spannung überwacht. Analog zu Versuch 1 ist eine Haltezeit von 5 Minuten vorgesehen. Mit Hilfe der Datenerfassung lassen sich die verschiedenen Parameter des Stacks überwachen und bewerten, so die Stacktemperatur, der Verbrauch an Wasserstoff und der Systemdruck. Versuch 4 Zu den wichtigsten Untersuchungsmethoden für Brennstoffzellen gehört die U(j)- bzw. U(I)- Kennlinie, wie bereits dargestellt wurde. Basierend auf den gleichen Parametern wie in Versuch 2 wird im reinen BSZ-Betrieb eine U(I)-Kurve aufgenommen. Versuch 5 Den Abschluss der Versuche bildet der Hybridbetrieb. In diesem Fall laufen BSZ und sekundäre Batterie parallel und die Auswirkungen auf die U(I)-Kennlinie soll aufgezeigt werden. Der Stack wird auf einen konstanten Betrieb eingestellt, während eine quasi dynamische Belastung angelegt wird. Auch hier sollen wieder die Kennwerte aus der Tabelle verwendet werden.
8 Auswertung Für die Auswertung sind verschiedene Punkte abzuarbeiten: A) Stellen Sie den Versuchsaufbau vor. Versuch 1 1.a) Graphische Auswertung des Versuchs: zeitliche Verläufe (min) der wichtigsten Größen (Stromstärke/EL Current (A), Spannung/EL Voltage (V), H2-Durchfluß). 1.b) Zu welchem Zeitpunkt wurde in Versuch 1 die BSZ zugeschaltet? Woran ist dieser Umstand zu erkennen? Versuch 2 Graphische Auswertung des Versuchs: 2.a) zeitliche Verläufe (min) der wichtigsten Größen 2.b) Strom-Spannungs-Kennlinie (U(I)-Kennlinie). Versuch 3 3.a) Graphische Auswertung des Versuchs: zeitliche Verläufe (min) der wichtigsten Größen. 3.b) Welche Unterschiede zwischen Batterie (Versuch 1) und BSZ (Versuch 3) ergeben sich im stationären Verhalten? Was ist die Ursache für diesen Unterschied? 3.c) Wie ändert sich die Stacktemperatur mit zunehmender Belastung? Warum? Versuch 4 4.a) Graphische Auswertung des Versuchs: zeitliche Verläufe (min) der wichtigsten Größen. 4.b) Graphische Auswertung des Versuchs: Strom-Spannungs-Kennlinie (U(I)-Kennlinie). 4.c) Wie und warum unterscheiden sich die U(I)-Kennlinien von Batterie und BSZ? 4.d) Herleitung und Berechnung des notwendigen H2-Durchflusses unter Normalbedingungen (siehe Tabelle unten). Daten Stack: 46 Brennstoffzellen, aktive Fläche: 100cm 2 Stromstärke (A) (EL Current) Spannung (V) (EL Voltage) Leistung (W) (EL Power) H2-Durchflusses errechnet (nl) (nl/min) H2-Durchflusses gemessen (nl) (nl/min)
9 4.e) Vergleich des in d) berechneten H2-Durchflusses mit dem gemessenen Gasfluss (H2 Flow). Wie ist der Unterschied zu erklären? 4.f) Wie und warum ändert sich der Wirkungsgrad des Stacks über den Lastbereich? Versuch 5 5.a) Graphische Auswertung des Versuchs: zeitliche Verläufe (min) der wichtigsten Größen. 5.b) Graphische Auswertung des Versuchs: Strom-Spannungs-Kennlinie (U(I)-Kennlinie).5.c) Wie verläuft der Ladestrom der Batterie? Welche Schlussfolgerungen können daraus gezogen werden? B) Was sind die Vorteile einer Hybridisierung zwischen Batterie und Brennstoffzelle? C) Warum werden heutzutage in der Automobilindustrie bzw. für stationäre Anwendungen praktisch nur noch Hybridsysteme entwickelt?
10 Formelzeichen, Konstanten und Abkürzungen e - H2 H + H2O O2 Elektron Wasserstoff Wasserstoffion / Proton Wasser Sauerstoff C C-Koeffizient (Entladungsfaktor) [-] E Hu I j M m Pel p Q T t V Potential / Spannung [mv] unterer Heizwert [MJ/kg] Stromstärke [A] Stromdichte [A/cm²] molare Masse [g/mol] Masse [kg] elektrische Leistung [W] Druck [MPa] Ladung [C] Temperatur [K] Zeit [s] Durchfluss [nl/min] z Elektronenzahl (der Reaktion) [-] G freie Reaktionsenthalpie / Gibb sche Enthalpie [J/mol] H Reaktionsenthalpie [J/mol] F Faraday-Konstante (F= 9,6485*10 7 C/kmol) R Gaskonstante (R=8,31441 J/mol*K) BSZ nl PEFC Brennstoffzelle Normliter Polymer-Elektrolyt-Brennstoffzelle
11 Größe Messdatei Bedeutung Name in Abb. 2 Date Datum Time Uhrzeit Ambient Temperature Umgebungstemperatur Nexa Oxygen Concentration Sauerstoffkonzentration Nexa Hydrogen Concentration Wasserstoffkonzentration Nexa Hydrogen Pressure Wasserstoffdruck (Versorgung) Nexa Stack Temperature Stack-Temperatur Nexa Stack Voltage Stack-Spannung Nexa Stack Current Stack-Strom Nexa Output Voltage Eingangsspannung DC/DC-Wandler (vom Stack) DCDC Output Voltage Ausgangsspannung DC/DC-Wandler DCDC Output Current Ausgangsstrom DC/DC-Wandler IOut EL Voltage fehlt (Spannung elektronische Last) EL Current Strom elektronische Last Iload EL Power Leistung elektronische Last H2 Flow Wasserstoffdurchfluss (-verbrauch) DCDC Battery Current Batteriestrom IBat Quellen 1. Wagner, N. Impedance Spectroscopy in Electrochemical Porous Systems. in Electrochemistry Days Erlangen. 2. Friedrich, K.A., Vorlesung Brennstoffzellentechnik. 3. Buchmann, I. Battery University [cited; Available from: 4. Heliocentris, Bedienungsanleitung Nexa-Lernsystem. 2008, Heliocentris Energiesysteme GmbH. Für weitere Informationen zum Thema Brennstoffzelle: 1. Vorlesung Brennstoffzellentechnik Prof. Dr. K. Andreas Friedrich (ITW) 2. Brennstoffzellentechnik Peter Kurzweil ISBN: Fuel Cell Handbook U.S. Department of Energy 0cells/FCHandbook7.pdf
Praktikum Betrieb eines Batterie-Brennstoffzellen- Hybridsystems
 Praktikum Betrieb eines Batterie-Brennstoffzellen- Hybridsystems Kontakt: altmann@itw.uni-stuttgart.de Einleitung Der zunehmende Leistungsbedarf mobiler und portabler Anwendungen erfordert Energiespeicher-
Praktikum Betrieb eines Batterie-Brennstoffzellen- Hybridsystems Kontakt: altmann@itw.uni-stuttgart.de Einleitung Der zunehmende Leistungsbedarf mobiler und portabler Anwendungen erfordert Energiespeicher-
HappyEvening am Brennstoffzellen zur mobilen Energiebereitstellung
 HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
Elektrizität. = C J m. Das Coulomb Potential φ ist dabei:
 Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Einführung in Technik und Funktionsweise von Brennstoffzellen und Batterieantrieben Prof. Dr. K. Andreas Friedrich
 Einführung in Technik und Funktionsweise von Brennstoffzellen und Batterieantrieben Prof. Dr. K. Andreas Friedrich Folie 1 > Friedrich, Ungethüm > Institut für Technische Thermodynamik, Institut für Fahrzeugkonzepte
Einführung in Technik und Funktionsweise von Brennstoffzellen und Batterieantrieben Prof. Dr. K. Andreas Friedrich Folie 1 > Friedrich, Ungethüm > Institut für Technische Thermodynamik, Institut für Fahrzeugkonzepte
Inhalt. History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ. Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell.
 Brennstoffzellen Inhalt History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell o Stacks o Anwendung o Fazit History Erste BZ vor
Brennstoffzellen Inhalt History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell o Stacks o Anwendung o Fazit History Erste BZ vor
5. Funktionsweise. Bild 1: Prinzip der Entladung. Chemische Reaktionen [1][6][10] positive Elektrode PbSO 4 + 2H 2 O
![5. Funktionsweise. Bild 1: Prinzip der Entladung. Chemische Reaktionen [1][6][10] positive Elektrode PbSO 4 + 2H 2 O 5. Funktionsweise. Bild 1: Prinzip der Entladung. Chemische Reaktionen [1][6][10] positive Elektrode PbSO 4 + 2H 2 O](/thumbs/88/116958020.jpg) 5. Funktionsweise Bild 1: Prinzip der Entladung Chemische Reaktionen [1][6][10] PbO 2 + 3 H + + HSO 4 - + 2e - Pb + HSO 4 - positive Elektrode PbSO 4 + 2H 2 O Negative Elektrode PbSO 4 + H + + 2e - Zellenreaktion
5. Funktionsweise Bild 1: Prinzip der Entladung Chemische Reaktionen [1][6][10] PbO 2 + 3 H + + HSO 4 - + 2e - Pb + HSO 4 - positive Elektrode PbSO 4 + 2H 2 O Negative Elektrode PbSO 4 + H + + 2e - Zellenreaktion
Die Wirkungsweise einer Brennstoffzelle. Ein Vortrag von Bernard Brickwedde
 Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12
 Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Dynamik des lokalen Strom/Spannungsverhaltens von Nafion-Membranen
 Dynamik des lokalen Strom/Spannungsverhaltens von Nafion-Membranen Präsentation der Ergebnisse der Aversumsprojekte 2009 Steffen ink a Wolfgang G. Bessler, b A. Masroor, b Emil Roduner a a Universität
Dynamik des lokalen Strom/Spannungsverhaltens von Nafion-Membranen Präsentation der Ergebnisse der Aversumsprojekte 2009 Steffen ink a Wolfgang G. Bessler, b A. Masroor, b Emil Roduner a a Universität
IEE. Modellierung und Simulation der Zelleigenschaften auf Basis von zeitvarianten Stoffdaten (GEENI)
 Problem: Eine erfolgreiche Modellierung von Lithium-Ionen-Batterien muss alle physikalischen und elektrochemischen Vorgänge, wie beispielsweise die elektrochemischen Reaktionen an den Elektroden, die Diffusion
Problem: Eine erfolgreiche Modellierung von Lithium-Ionen-Batterien muss alle physikalischen und elektrochemischen Vorgänge, wie beispielsweise die elektrochemischen Reaktionen an den Elektroden, die Diffusion
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL SEKUNDARSTUFE II Modul: Versuch: Elektrochemie 1 Abbildung 1:
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL SEKUNDARSTUFE II Modul: Versuch: Elektrochemie 1 Abbildung 1:
Power, der die Puste nie ausgeht!
 Fuel Cells Die Brennstoffzelle im Westerwald-Treff Power, der die Puste nie ausgeht! Die Brennstoffzelle im Westerwald-Treff Die Projektpartner Das Brennstoffzellen-Projekt im Hotelpark Westerwald-Treff
Fuel Cells Die Brennstoffzelle im Westerwald-Treff Power, der die Puste nie ausgeht! Die Brennstoffzelle im Westerwald-Treff Die Projektpartner Das Brennstoffzellen-Projekt im Hotelpark Westerwald-Treff
Simulation elektrochemischer Abläufe in Direkt-Methanolbrennstoffzellen
 Simulation elektrochemischer Abläufe in Direkt-Methanolbrennstoffzellen Torsten Köhler Mohrenstr. 39 10117 Berlin +49 30 2 03 72 0 www.wias-berlin.de Februar 2005 1/19 Inhalt 1. Elektrochemische Grundlagen
Simulation elektrochemischer Abläufe in Direkt-Methanolbrennstoffzellen Torsten Köhler Mohrenstr. 39 10117 Berlin +49 30 2 03 72 0 www.wias-berlin.de Februar 2005 1/19 Inhalt 1. Elektrochemische Grundlagen
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 3 Wirkungsgrad der Brennstoffzelle Versuchszweck
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 3 Wirkungsgrad der Brennstoffzelle Versuchszweck
Technische Universität München. Brennstoffzelle. Roland Fuchsberger
 Brennstoffzelle Roland Fuchsberger Inhalt Elektrochemische Grundlagen Elektrochemische Zelle Faradaysches Gesetz Nernstsche Gleichung Brennstoffzelle Geschichte Verschiedene Typen Marktanalyse Portabel
Brennstoffzelle Roland Fuchsberger Inhalt Elektrochemische Grundlagen Elektrochemische Zelle Faradaysches Gesetz Nernstsche Gleichung Brennstoffzelle Geschichte Verschiedene Typen Marktanalyse Portabel
Strömungssimulation in Li-Dualinsertationszellen
 Strömungssimulation in Li-Dualinsertationszellen Christoph Wiesian, Dennis Dieterle, Sven Wagner c.wiesian@uni-muenster.de dennis.dieterle@uni-muenster.de sven.wagner@uni-muenster.de 22.12.2009 Wiesian,
Strömungssimulation in Li-Dualinsertationszellen Christoph Wiesian, Dennis Dieterle, Sven Wagner c.wiesian@uni-muenster.de dennis.dieterle@uni-muenster.de sven.wagner@uni-muenster.de 22.12.2009 Wiesian,
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle. Inhaltsfeld: Elektrochemie
 Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Kennlinie der Methanol- Brennstoffzelle
 E m1 Kennlinie der Methanol- Brennstoffzelle Material: Methanol-Brennstoffzelle Flasche mit 1M Methanol-Lösung Spritztülle Verbraucher-Messbox 4 Kabel Verschlussstopfen Tank Zusätzliche Komponenten: Methanol
E m1 Kennlinie der Methanol- Brennstoffzelle Material: Methanol-Brennstoffzelle Flasche mit 1M Methanol-Lösung Spritztülle Verbraucher-Messbox 4 Kabel Verschlussstopfen Tank Zusätzliche Komponenten: Methanol
Das Wort Kondensator leitet sich vom lateinischen condensare (= verdichten, dicht zusammenpressen) her.
 3.1 Aufbau Das Wort Kondensator leitet sich vom lateinischen condensare (= verdichten, dicht zusammenpressen) her. In der Elektrotechnik handelt es sich bei einem Kondensator um ein Bauelement, dass in
3.1 Aufbau Das Wort Kondensator leitet sich vom lateinischen condensare (= verdichten, dicht zusammenpressen) her. In der Elektrotechnik handelt es sich bei einem Kondensator um ein Bauelement, dass in
Die elektrische Energie wird durch Ionen transportiert. Ionen sind elektrisch geladene Atome bzw. Elektrolyt
 Galvanische Elemente Galvanische (Galvani ital.physiker) Elemente wandeln chemische in elektrische um. Sie bestehen aus zwei Elektroden (Anode, Kathode) und einer elektrisch leitenden Flüssigkeit, dem
Galvanische Elemente Galvanische (Galvani ital.physiker) Elemente wandeln chemische in elektrische um. Sie bestehen aus zwei Elektroden (Anode, Kathode) und einer elektrisch leitenden Flüssigkeit, dem
Versuchsplanung und Standardmeßzelle zur umfassenden Charakterisierung von MT-PEM Brennstoffzellen
 Versuchsplanung und Standardmeßzelle zur umfassenden Charakterisierung von MT-PEM Brennstoffzellen B. Lutter, M. Heinen, V. Peinecke 4. Workshop AIF-Brennstoffzellenallianz ZBT, Duisburg, 3. Mai 2011 Elektrochemie
Versuchsplanung und Standardmeßzelle zur umfassenden Charakterisierung von MT-PEM Brennstoffzellen B. Lutter, M. Heinen, V. Peinecke 4. Workshop AIF-Brennstoffzellenallianz ZBT, Duisburg, 3. Mai 2011 Elektrochemie
GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN
 10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
Fachbereich Ingenieurwissenschaften und Mathematik. Praktikum Dezentrale Energiesysteme. DEZ 1 Brennstoffzellen
 Fachbereich Ingenieurwissenschaften und Mathematik Praktikum Dezentrale Energiesysteme DEZ 1 Brennstoffzellen Lehrgebiet Regenerative Energiesysteme und Elektrotechnik Prof.-Dr.-Ing. Jens Haubrock Inhalt
Fachbereich Ingenieurwissenschaften und Mathematik Praktikum Dezentrale Energiesysteme DEZ 1 Brennstoffzellen Lehrgebiet Regenerative Energiesysteme und Elektrotechnik Prof.-Dr.-Ing. Jens Haubrock Inhalt
Brennstoffzelle. Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes. Schüler-Skript und Versuchsanleitung
 Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
E 3 Brennstoffzelle. 1 Aufgabenstellung
 E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
Aufgabenblatt Z/ 01 (Physikalische Größen und Einheiten)
 Aufgabenblatt Z/ 01 (Physikalische Größen und Einheiten) Aufgabe Z-01/ 1 Welche zwei verschiedenen physikalische Bedeutungen kann eine Größe haben, wenn nur bekannt ist, dass sie in der Einheit Nm gemessen
Aufgabenblatt Z/ 01 (Physikalische Größen und Einheiten) Aufgabe Z-01/ 1 Welche zwei verschiedenen physikalische Bedeutungen kann eine Größe haben, wenn nur bekannt ist, dass sie in der Einheit Nm gemessen
Der Elektrik-Trick für die Mittelstufe. Das Wort Kondensator leitet sich vom lateinischen condensare (= verdichten, dicht zusammenpressen) her.
 Der Kondensator 1. Aufbau Das Wort Kondensator leitet sich vom lateinischen condensare (= verdichten, dicht zusammenpressen) her. In der Elektrotechnik handelt es sich bei einem Kondensator um ein Bauelement,
Der Kondensator 1. Aufbau Das Wort Kondensator leitet sich vom lateinischen condensare (= verdichten, dicht zusammenpressen) her. In der Elektrotechnik handelt es sich bei einem Kondensator um ein Bauelement,
Messung des Stromverbrauchs der E-10 und der Entladekurve von NiMH Akkus. Autor: Klaus Schraeder
 Messung des Stromverbrauchs der E-10 und der Entladekurve von NiMH Akkus Autor: Klaus Schraeder Zahlreiche Postings in diesem Forum haben sich mit den Fragen des Stromverbrauchs, der optimalen Akkus und
Messung des Stromverbrauchs der E-10 und der Entladekurve von NiMH Akkus Autor: Klaus Schraeder Zahlreiche Postings in diesem Forum haben sich mit den Fragen des Stromverbrauchs, der optimalen Akkus und
Lithium (-Ionen) -Polymer Akkus
 Geschichte und Aufbau Aufstellung der sogenannten Voltaschen Spannungsreihe (1794) Batterien gehören zu den elektrochemischen Stromquellen. Eigentlich ist Batterie der Oberbegriff für mehrere in Serie
Geschichte und Aufbau Aufstellung der sogenannten Voltaschen Spannungsreihe (1794) Batterien gehören zu den elektrochemischen Stromquellen. Eigentlich ist Batterie der Oberbegriff für mehrere in Serie
METTLER TOLEDO Prozessanalytik. Online-Prozessund Reinwassersysteme. Leitfaden für Online-Leitfähigkeitsmessungen Theorie und Praxis
 Leitfaden Schulexperimente Leitfähigkeit METTLER TOLEDO Prozessanalytik Online-Prozessund Reinwassersysteme Leitfaden für Online-Leitfähigkeitsmessungen Theorie und Praxis Inhaltsverzeichnis 1 Einleitung
Leitfaden Schulexperimente Leitfähigkeit METTLER TOLEDO Prozessanalytik Online-Prozessund Reinwassersysteme Leitfaden für Online-Leitfähigkeitsmessungen Theorie und Praxis Inhaltsverzeichnis 1 Einleitung
kann elektrische Energie durch Umwandlung in chemische Energie speichern und diese durch Rückumwandlung wieder abgeben Laden Entladen
 1 BATTERIEN-ABCABC Batterien-ABC 2 Akkumulator (Akku) kann elektrische Energie durch Umwandlung in chemische Energie speichern und diese durch Rückumwandlung wieder abgeben elektrische Energie Laden Entladen
1 BATTERIEN-ABCABC Batterien-ABC 2 Akkumulator (Akku) kann elektrische Energie durch Umwandlung in chemische Energie speichern und diese durch Rückumwandlung wieder abgeben elektrische Energie Laden Entladen
E7 Elektrolyse. Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch. Münster, den
 E7 Elektrolyse Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch Münster, den 18.12.2000 INHALTSVERZEICHNIS 1. Einleitung 2. Theoretische Grundlagen 2.1 Elektrolyse 2.2 Die FARADAYschen Gesetze der
E7 Elektrolyse Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch Münster, den 18.12.2000 INHALTSVERZEICHNIS 1. Einleitung 2. Theoretische Grundlagen 2.1 Elektrolyse 2.2 Die FARADAYschen Gesetze der
1. Elektroanalytik-I (Elektrochemie)
 Instrumentelle Analytik SS 2008 1. Elektroanalytik-I (Elektrochemie) 1 1. Elektroanalytik-I 1. Begriffe/Methoden (allgem.) 1.1 Elektroden 1.2 Elektrodenreaktionen 1.3 Galvanische Zellen 2 1. Elektroanalytik-I
Instrumentelle Analytik SS 2008 1. Elektroanalytik-I (Elektrochemie) 1 1. Elektroanalytik-I 1. Begriffe/Methoden (allgem.) 1.1 Elektroden 1.2 Elektrodenreaktionen 1.3 Galvanische Zellen 2 1. Elektroanalytik-I
TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in. Reihenschaltung/Parallelschaltung
 TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in V17 Fachgebiet Chemie Reihenschaltung/Parallelschaltung 1. Aufgabe Bauen Sie die Anordnung nach Bild 1 oder Bild 2 auf. Nehmen Sie
TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in V17 Fachgebiet Chemie Reihenschaltung/Parallelschaltung 1. Aufgabe Bauen Sie die Anordnung nach Bild 1 oder Bild 2 auf. Nehmen Sie
Bedienungsanleitung. F109 Fuel Cell Stack 5. F110 Fuel Cell Stack 10
 Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Einführung in die Elektrochemie
 Einführung in die Elektrochemie > Grundlagen, Methoden > Leitfähigkeit von Elektrolytlösungen, Konduktometrie > Elektroden Metall-Elektroden 1. und 2. Art Redox-Elektroden Membran-Elektroden > Potentiometrie
Einführung in die Elektrochemie > Grundlagen, Methoden > Leitfähigkeit von Elektrolytlösungen, Konduktometrie > Elektroden Metall-Elektroden 1. und 2. Art Redox-Elektroden Membran-Elektroden > Potentiometrie
Grundlagen: Galvanische Zellen:
 E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
6.3 Stromerzeugung mit galvanischen Zellen. Aufbauprinzip + Kontakte Abdichtung
 6.3 Stromerzeugung mit galvanischen Zellen Aufbauprinzip + Kontakte Abdichtung Elektrolyt Anode Stromkollektor Kathode Behälter Separator (Diaphragma) Anode: Kathode: Elektrolyt: Separator: Oxidation eines
6.3 Stromerzeugung mit galvanischen Zellen Aufbauprinzip + Kontakte Abdichtung Elektrolyt Anode Stromkollektor Kathode Behälter Separator (Diaphragma) Anode: Kathode: Elektrolyt: Separator: Oxidation eines
Strömungssimulation in Li-Dualinsertationszellen
 Strömungssimulation in Li-Dualinsertationszellen Julius Sewing, Nikolaus Krause, Dennis Dieterle j.sewing@gmx.net nikokrause@gmx.de dennis.dieterle@uni-muenster.de 22. Juni 2010 Sewing, Krause, Dieterle
Strömungssimulation in Li-Dualinsertationszellen Julius Sewing, Nikolaus Krause, Dennis Dieterle j.sewing@gmx.net nikokrause@gmx.de dennis.dieterle@uni-muenster.de 22. Juni 2010 Sewing, Krause, Dieterle
Brenstoffzelle (BRZ)
 Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
Was ist Elektrochemie?
 Was ist Elektrochemie? Eine elektrochemische Reaktion erfüllt folgende vier Eigenschaften: Sie findet an Phasengrenzen statt. Die einzelnen Phasen sind unterschiedlich geladen. (unterschiedliche elektrische
Was ist Elektrochemie? Eine elektrochemische Reaktion erfüllt folgende vier Eigenschaften: Sie findet an Phasengrenzen statt. Die einzelnen Phasen sind unterschiedlich geladen. (unterschiedliche elektrische
-1 (außer in Verbindung mit Sauerstoff: variabel) Sauerstoff -2 (außer in Peroxiden: -1)
 1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
Entladung eines Kondensators
 3.11.5 Entladung eines Kondensators Im Gegensatz zu einer Batterie kann mit einem Kondensator innerhalb von kurzer Zeit eine hohe Stromstärke erzeugt werden. Dies wird zum Beispiel beim Blitz eines Fotoapparates
3.11.5 Entladung eines Kondensators Im Gegensatz zu einer Batterie kann mit einem Kondensator innerhalb von kurzer Zeit eine hohe Stromstärke erzeugt werden. Dies wird zum Beispiel beim Blitz eines Fotoapparates
Erich Tag Elektrochemie
 STUDIENBÜCHER CHEMIE Erich Tag Elektrochemie Eine Einführung in die Theorie elektrochemischer Gleichgewichte und elektrochemischer Prozesse Herausgegeben von W. Botsch, E. Höfling und J. Mauch VERLAG MORITZ
STUDIENBÜCHER CHEMIE Erich Tag Elektrochemie Eine Einführung in die Theorie elektrochemischer Gleichgewichte und elektrochemischer Prozesse Herausgegeben von W. Botsch, E. Höfling und J. Mauch VERLAG MORITZ
Experimentalphysik 2
 Repetitorium zu Experimentalphysik 2 Ferienkurs am Physik-Department der Technischen Universität München Gerd Meisl 5. August 2008 Inhaltsverzeichnis 1 Übungsaufgaben 2 1.1 Übungsaufgaben....................................
Repetitorium zu Experimentalphysik 2 Ferienkurs am Physik-Department der Technischen Universität München Gerd Meisl 5. August 2008 Inhaltsverzeichnis 1 Übungsaufgaben 2 1.1 Übungsaufgaben....................................
Das Brennstoffzellen-Radio
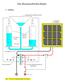 Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
Elektrotechnik: Zusatzaufgaben
 Elektrotechnik: Zusatzaufgaben 1.1. Aufgabe: Rechnen Sie die abgeleiteten Einheiten der elektrischen Spannung, des elektrischen Widerstandes und der elektrischen Leistung in die Basiseinheiten des SI um.
Elektrotechnik: Zusatzaufgaben 1.1. Aufgabe: Rechnen Sie die abgeleiteten Einheiten der elektrischen Spannung, des elektrischen Widerstandes und der elektrischen Leistung in die Basiseinheiten des SI um.
Vorlesung 3: Elektrodynamik
 Vorlesung 3: Elektrodynamik, georg.steinbrueck@desy.de Folien/Material zur Vorlesung auf: www.desy.de/~steinbru/physikzahnmed georg.steinbrueck@desy.de 1 WS 2015/16 Der elektrische Strom Elektrodynamik:
Vorlesung 3: Elektrodynamik, georg.steinbrueck@desy.de Folien/Material zur Vorlesung auf: www.desy.de/~steinbru/physikzahnmed georg.steinbrueck@desy.de 1 WS 2015/16 Der elektrische Strom Elektrodynamik:
Wir schaffen Wissen heute für morgen
 Wir schaffen Wissen heute für morgen Paul Scherrer Institut Prof. Dr. Petr Novák Aktuelle und zukünftige Batterien: Realität vs. Wunschdenken Bild: David Horsey, Internet Energiespeicherung ist eine gut
Wir schaffen Wissen heute für morgen Paul Scherrer Institut Prof. Dr. Petr Novák Aktuelle und zukünftige Batterien: Realität vs. Wunschdenken Bild: David Horsey, Internet Energiespeicherung ist eine gut
Stefan Reißmann ANORGANISCH-CHEMISCHES TUTORIUM WS 2000/2001
 7. ELEKTROCHEMIE Im Prinzip sind alle chemischen Reaktionen elektrischer Natur, denn an allen chemischen Bindungen sind Elektronen beteiligt. Unter Elektrochemie versteht man jedoch vorrangig die Lehre
7. ELEKTROCHEMIE Im Prinzip sind alle chemischen Reaktionen elektrischer Natur, denn an allen chemischen Bindungen sind Elektronen beteiligt. Unter Elektrochemie versteht man jedoch vorrangig die Lehre
ZIELKONFLIKTE BEI DER BRENNSTOFFZELLENAUSLEGUNG
 ZIELKONFLIKTE BEI DER BRENNSTOFFZELLENAUSLEGUNG DR. INGO DRESCHER KONZERNFORSCHUNG BRENNSTOFFZELLE HYBRIDTAGUNG BRAUNSCHWEIG 21. FEBRUAR 2017 MÖGLICHE ENTWICKLUNG NACHHALTIGER ENERGIEN IM AUTOMOBILSEKTOR
ZIELKONFLIKTE BEI DER BRENNSTOFFZELLENAUSLEGUNG DR. INGO DRESCHER KONZERNFORSCHUNG BRENNSTOFFZELLE HYBRIDTAGUNG BRAUNSCHWEIG 21. FEBRUAR 2017 MÖGLICHE ENTWICKLUNG NACHHALTIGER ENERGIEN IM AUTOMOBILSEKTOR
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 2 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 2 Kennlinien der Brennstoffzelle Versuchszweck
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 2 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 2 Kennlinien der Brennstoffzelle Versuchszweck
Thema: Die Luftbatterie
 Klasse: 9/10 Name: Datum: Thema: Die Luftbatterie Gefahrenstoffe Natriumchlorid - - Materialien: Graphit-Elektrode, Aluminium-Folie, Küchenpapier oder Handpapier, Pipette Chemikalien: Durchführung: Natriumchlorid-Lösung
Klasse: 9/10 Name: Datum: Thema: Die Luftbatterie Gefahrenstoffe Natriumchlorid - - Materialien: Graphit-Elektrode, Aluminium-Folie, Küchenpapier oder Handpapier, Pipette Chemikalien: Durchführung: Natriumchlorid-Lösung
Simultane Elektrochemische Impedanzspektrometrie und Kalorimetrie an Lithium-Ionen-Akkumulatoren
 Physikalisch-Technische Bundesanstalt Braunschweig und Berlin Nationales Metrologieinstitut Simultane Elektrochemische Impedanzspektrometrie und Stefan M. Sarge Physikalisch-Technische Bundesanstalt Bundesallee
Physikalisch-Technische Bundesanstalt Braunschweig und Berlin Nationales Metrologieinstitut Simultane Elektrochemische Impedanzspektrometrie und Stefan M. Sarge Physikalisch-Technische Bundesanstalt Bundesallee
Wasserstoff als Energieträger Gliederung:
 Wasserstoff als Energieträger Gliederung: Wasserstoff: Energie speichern und verteilen Die Brennstoffzelle Wasserstoff aus der Ptm6 Alge Wasserstoff als Energiespeicher Der umweltfreundliche Akku: Um Wasserstoff
Wasserstoff als Energieträger Gliederung: Wasserstoff: Energie speichern und verteilen Die Brennstoffzelle Wasserstoff aus der Ptm6 Alge Wasserstoff als Energiespeicher Der umweltfreundliche Akku: Um Wasserstoff
MEMATEC PRODUCTS GEBRAUCH VON AKKUS. Mematec Products GmbH August-Müller-Straße 24 D Freiberg Neckar
 28.10.2016 MEMATEC PRODUCTS GEBRAUCH VON AKKUS Mematec Products GmbH August-Müller-Straße 24 D- 71691 Freiberg Neckar Liebe Kunden, wir haben dieses Merkblatt für Sie zusammengestellt, weil wir festgestellt
28.10.2016 MEMATEC PRODUCTS GEBRAUCH VON AKKUS Mematec Products GmbH August-Müller-Straße 24 D- 71691 Freiberg Neckar Liebe Kunden, wir haben dieses Merkblatt für Sie zusammengestellt, weil wir festgestellt
6.2.6 Ohmsches Gesetz ******
 6..6 ****** Motivation Das Ohmsche Gesetz wird mithilfe von verschiedenen Anordnungen von leitenden Drähten untersucht. Experiment 6 7 8 9 0 Abbildung : Versuchsaufbau. Die Ziffern bezeichnen die zehn
6..6 ****** Motivation Das Ohmsche Gesetz wird mithilfe von verschiedenen Anordnungen von leitenden Drähten untersucht. Experiment 6 7 8 9 0 Abbildung : Versuchsaufbau. Die Ziffern bezeichnen die zehn
Präsentation Technologie
 Präsentation Technologie 1 Einführung fortu PowerCell entwickelt und produziert ein neuartiges Akku-System auf Basis anorganischer Komponenten Die neue Technologie ermöglicht höchste Energiedichten (über
Präsentation Technologie 1 Einführung fortu PowerCell entwickelt und produziert ein neuartiges Akku-System auf Basis anorganischer Komponenten Die neue Technologie ermöglicht höchste Energiedichten (über
Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle
 Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 1 Kennlinie des Elektrolyseurs Versuchszweck Beim
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 1 Kennlinie des Elektrolyseurs Versuchszweck Beim
White Paper: Möglicher Einsatz von bidirektionalen DC/DC Wandlern im Bereich mobile Anwendungen
 White Paper: Möglicher Einsatz von bidirektionalen DC/DC Wandlern im Bereich mobile Anwendungen Einleitung DC/DC-Wandler dienen der Anpassung von zwei verschiedenen Gleichspannungen. Unter anderem in mobilen
White Paper: Möglicher Einsatz von bidirektionalen DC/DC Wandlern im Bereich mobile Anwendungen Einleitung DC/DC-Wandler dienen der Anpassung von zwei verschiedenen Gleichspannungen. Unter anderem in mobilen
Elektrolyseure Typ EV
 Elektrolyseure Typ EV Kurzbeschreibung Die Elektrolyseure der Baureihe EV Y / n z (Y = Baugröße, n z = Zellenzahl) sind atmosphärische Wasserstofferzeuger mit Kapazitäten bis zu 250 m N ³ H 2 /h. Sie bestehen
Elektrolyseure Typ EV Kurzbeschreibung Die Elektrolyseure der Baureihe EV Y / n z (Y = Baugröße, n z = Zellenzahl) sind atmosphärische Wasserstofferzeuger mit Kapazitäten bis zu 250 m N ³ H 2 /h. Sie bestehen
Praktikum II TR: Transformator
 Praktikum II TR: Transformator Betreuer: Dr. Torsten Hehl Hanno Rein praktikum2@hanno-rein.de Florian Jessen florian.jessen@student.uni-tuebingen.de 30. März 2004 Made with L A TEX and Gnuplot Praktikum
Praktikum II TR: Transformator Betreuer: Dr. Torsten Hehl Hanno Rein praktikum2@hanno-rein.de Florian Jessen florian.jessen@student.uni-tuebingen.de 30. März 2004 Made with L A TEX and Gnuplot Praktikum
Aufbau und Charakterisierung eines O 2 -Sensors auf Basis der Laserspektroskopie für PEM-Elektrolysesysteme
 Aufbau und Charakterisierung eines O 2 -Sensors auf Basis der Laserspektroskopie für PEM-Elektrolysesysteme Aversumergebnis 2009 Sebastian Rau 1, Benjamin Scherer 2 1 Fraunhofer-Institut für Solare Energiesysteme
Aufbau und Charakterisierung eines O 2 -Sensors auf Basis der Laserspektroskopie für PEM-Elektrolysesysteme Aversumergebnis 2009 Sebastian Rau 1, Benjamin Scherer 2 1 Fraunhofer-Institut für Solare Energiesysteme
Physikalisches Anfängerpraktikum Teil 2 Elektrizitätslehre. Protokollant: Versuch 27 Solarzellen
 Physikalisches Anfängerpraktikum Teil 2 Elektrizitätslehre Protokoll Versuch 27 Solarzellen Harald Meixner Sven Köppel Matr.-Nr. 3794465 Matr.-Nr. 3793686 Physik Bachelor 2. Semester Physik Bachelor 2.
Physikalisches Anfängerpraktikum Teil 2 Elektrizitätslehre Protokoll Versuch 27 Solarzellen Harald Meixner Sven Köppel Matr.-Nr. 3794465 Matr.-Nr. 3793686 Physik Bachelor 2. Semester Physik Bachelor 2.
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 6 Kalorimetrie Aufgabe: Mittels eines Flüssigkeitskalorimeters ist a) die Neutralisationsenthalpie von säure b) die ösungsenthalpie
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 6 Kalorimetrie Aufgabe: Mittels eines Flüssigkeitskalorimeters ist a) die Neutralisationsenthalpie von säure b) die ösungsenthalpie
Elektrotechnik: Übungsblatt 2 - Der Stromkreis
 Elektrotechnik: Übungsblatt 2 - Der Stromkreis 1. Aufgabe: Was zeichnet elektrische Leiter gegenüber Nichtleitern aus? In elektrischen Leitern sind die Ladungen leicht beweglich, in Isolatoren können sie
Elektrotechnik: Übungsblatt 2 - Der Stromkreis 1. Aufgabe: Was zeichnet elektrische Leiter gegenüber Nichtleitern aus? In elektrischen Leitern sind die Ladungen leicht beweglich, in Isolatoren können sie
Abiturprüfung Physik, Grundkurs
 Seite 1 von 6 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Entladung eines Kondensators In dieser Aufgabe geht es um die Entladung eines Kondensators. Im ersten Teil (Teilaufgabe 1)
Seite 1 von 6 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Entladung eines Kondensators In dieser Aufgabe geht es um die Entladung eines Kondensators. Im ersten Teil (Teilaufgabe 1)
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
Der elektrische Widerstand R. Auswirkung im Stromkreis Definition Ohmsches Gesetz
 Der elektrische Widerstand R Auswirkung im Stromkreis Definition Ohmsches Gesetz Kennlinie Wir wissen, am gleichen Leiter bewirken gleiche Spannungen gleiche Ströme. Wie ändert sich der Strom, wenn man
Der elektrische Widerstand R Auswirkung im Stromkreis Definition Ohmsches Gesetz Kennlinie Wir wissen, am gleichen Leiter bewirken gleiche Spannungen gleiche Ströme. Wie ändert sich der Strom, wenn man
Kritische Parameter und neue Konzepte für HTPEM Bipolarplatten und Dichtungen
 Kritische Parameter und neue Konzepte für HTPEM Bipolarplatten und Dichtungen 21.Juni 2016 Workshop AiF-Brennstoffzellenallianz, Duisburg Isabel Kundler, Rouven Henkel, Thorsten Hickmann Eisenhuth GmbH
Kritische Parameter und neue Konzepte für HTPEM Bipolarplatten und Dichtungen 21.Juni 2016 Workshop AiF-Brennstoffzellenallianz, Duisburg Isabel Kundler, Rouven Henkel, Thorsten Hickmann Eisenhuth GmbH
Elektrochemische Zellen zur Energie-Speicherung und Energie-Umwandlung. Terminology
 Kapitel 5: Elektrochemische Zellen zur Energie-Speicherung und Energie-Umwandlung 5.1 Brennstoffzellen 5.2 Batterien 5.2.1 Lithium-Ionen-Batterie 5.2.2 Redox-Flow-Batterien 1 Terminology Specific energy:
Kapitel 5: Elektrochemische Zellen zur Energie-Speicherung und Energie-Umwandlung 5.1 Brennstoffzellen 5.2 Batterien 5.2.1 Lithium-Ionen-Batterie 5.2.2 Redox-Flow-Batterien 1 Terminology Specific energy:
Moderne und zukünftige elektrische Energiespeicher im Überblick
 Moderne und zukünftige elektrische Energiespeicher im Überblick 11. Solartagung Rheinland-Pfalz, Umwelt-Campus Birkenfeld Jonas Keil 09.12.2015 Energiespeichertechnik an der Technischen Universität München
Moderne und zukünftige elektrische Energiespeicher im Überblick 11. Solartagung Rheinland-Pfalz, Umwelt-Campus Birkenfeld Jonas Keil 09.12.2015 Energiespeichertechnik an der Technischen Universität München
6.1 Elektrodenpotenzial und elektromotorische Kraft
 6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
Die Modellierung einer Lithium-Batterie Zwischenpräsentation zum Praktikum Nichtlineare Modellierung in den Naturwissenschaften
 MÜNSTER Die Modellierung einer Lithium-Batterie Zwischenpräsentation zum Praktikum Nichtlineare Modellierung in den Naturwissenschaften Christoph Fricke, Natascha von Aspern, Carla Tameling 12.06.2012
MÜNSTER Die Modellierung einer Lithium-Batterie Zwischenpräsentation zum Praktikum Nichtlineare Modellierung in den Naturwissenschaften Christoph Fricke, Natascha von Aspern, Carla Tameling 12.06.2012
ELEKTROCHEMIE. Elektrischer Strom: Fluß von elektrischer Ladung. elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie.
 ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
Elektrofahrzeugakkumulatoren auf Basis der fortu Technologie
 Elektrofahrzeugakkumulatoren auf Basis der fortu Technologie 1 Aktuelle Situation Die Elektrotraktion stellt immer noch eine Nische dar. Als Grund für mangelnde Marktdurchdringung werden oft unzureichende
Elektrofahrzeugakkumulatoren auf Basis der fortu Technologie 1 Aktuelle Situation Die Elektrotraktion stellt immer noch eine Nische dar. Als Grund für mangelnde Marktdurchdringung werden oft unzureichende
Ladegerät. Martin Glunz 24. Februar 2001
 Ladegerät Martin Glunz Martin@Wunderkis.de 24. Februar 2001 1 Allgemeines Das Ladegerät benötigt zur Versorgung eine Gleichspannung von 10... 28V. Im Ladebetrieb kann der Versorgungsstrom bis zu ca. 30A
Ladegerät Martin Glunz Martin@Wunderkis.de 24. Februar 2001 1 Allgemeines Das Ladegerät benötigt zur Versorgung eine Gleichspannung von 10... 28V. Im Ladebetrieb kann der Versorgungsstrom bis zu ca. 30A
Modellierung und Simulation von Lithium-Ionen Akkus
 MÜNSTER und Simulation von Lithium-Ionen Akkus C. Ascheberg C. Benndorf D. Brüning 14.12.2010 C. Holtschulte M. Wentker K. Wenzel > Übersicht MÜNSTER und Simulation von Lithium-Ionen Akkus 2/18 Theoretische
MÜNSTER und Simulation von Lithium-Ionen Akkus C. Ascheberg C. Benndorf D. Brüning 14.12.2010 C. Holtschulte M. Wentker K. Wenzel > Übersicht MÜNSTER und Simulation von Lithium-Ionen Akkus 2/18 Theoretische
Die Brennstoffzelle. Von: Ismail Nasser
 Die Brennstoffzelle Gliederung Was ist eine Brennstoffzelle? Geschichte der Brennstoffzelle Aufbau und Funktionsweise der Brennstoffzelle Unterschiedliche Arten Gesamtwirkungsgrad Kosten Was ist eine Brennstoffzelle?
Die Brennstoffzelle Gliederung Was ist eine Brennstoffzelle? Geschichte der Brennstoffzelle Aufbau und Funktionsweise der Brennstoffzelle Unterschiedliche Arten Gesamtwirkungsgrad Kosten Was ist eine Brennstoffzelle?
TR Transformator. Blockpraktikum Herbst Moritz Stoll, Marcel Schmittfull (Gruppe 2b) 25. Oktober 2007
 TR Transformator Blockpraktikum Herbst 2007 (Gruppe 2b) 25 Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 11 Unbelasteter Transformator 2 12 Belasteter Transformator 3 13 Leistungsanpassung 3 14 Verluste
TR Transformator Blockpraktikum Herbst 2007 (Gruppe 2b) 25 Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 11 Unbelasteter Transformator 2 12 Belasteter Transformator 3 13 Leistungsanpassung 3 14 Verluste
Dielektrizitätskonstante
 Dielektrizitätskonstante Spannung am geladenen Plattenkondensator sinkt, wenn nichtleitendes Dielektrikum eingeschoben wird Ladung bleibt konstant : Q = C 0 U 0 = C D U D Q + + + + + + + + + + + - - -
Dielektrizitätskonstante Spannung am geladenen Plattenkondensator sinkt, wenn nichtleitendes Dielektrikum eingeschoben wird Ladung bleibt konstant : Q = C 0 U 0 = C D U D Q + + + + + + + + + + + - - -
Reformierung von Kohlenwasserstoffen PEM-Elektrolyse
 Bereitstellung von Wasserstoff Reformierung von Kohlenwasserstoffen PEM-Elektrolyse Ursula Wittstadt Fraunhofer-Institut für Solare Energiesysteme ISE Wasserstoff Expo 2002 Hamburg, 10.10.2002 Fraunhofer
Bereitstellung von Wasserstoff Reformierung von Kohlenwasserstoffen PEM-Elektrolyse Ursula Wittstadt Fraunhofer-Institut für Solare Energiesysteme ISE Wasserstoff Expo 2002 Hamburg, 10.10.2002 Fraunhofer
Test zum Begriff Spannung Ein grundlegender Begriff der Elektrizitätslehre
 Test zum Begriff Spannung Ein grundlegender Begriff der Elektrizitätslehre Kontakt: Dr. Hermann Härtel Gastwissenschaftler am Institut für Theoretische Physik und Astrophysik Leibnizstr. 15-24098 Kiel
Test zum Begriff Spannung Ein grundlegender Begriff der Elektrizitätslehre Kontakt: Dr. Hermann Härtel Gastwissenschaftler am Institut für Theoretische Physik und Astrophysik Leibnizstr. 15-24098 Kiel
Vorlesung Allgemeine Chemie 30. November 2010
 Vorlesung Allgemeine Chemie 30. November 2010 Daniell-Element E (Cu 2+ /Cu = +0.337 E (Zn 2+ /Zn = 0.763 Fig. 22.5 22.8 Machen wir teilweise, folgt. Definitionen, nochmals: Freie Enthalpie oder Freie Reaktionsenthalpie
Vorlesung Allgemeine Chemie 30. November 2010 Daniell-Element E (Cu 2+ /Cu = +0.337 E (Zn 2+ /Zn = 0.763 Fig. 22.5 22.8 Machen wir teilweise, folgt. Definitionen, nochmals: Freie Enthalpie oder Freie Reaktionsenthalpie
E2: Wärmelehre und Elektromagnetismus 15. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 15. Vorlesung 11.06.2018 Wissenschaftliche Instrumente aus dem 18. und 19. Jahrhundert aus der Sammlung des Teylers Museum in Haarlem, Niederlande Heute: - Reihen-
E2: Wärmelehre und Elektromagnetismus 15. Vorlesung 11.06.2018 Wissenschaftliche Instrumente aus dem 18. und 19. Jahrhundert aus der Sammlung des Teylers Museum in Haarlem, Niederlande Heute: - Reihen-
Inhalt. 1. Erläuterungen zum Versuch 1.1. Aufgabenstellung und physikalischer Hintergrund 1.2. Messmethode und Schaltbild 1.3. Versuchdurchführung
 Versuch Nr. 02: Bestimmung eines Ohmschen Widerstandes nach der Substitutionsmethode Versuchsdurchführung: Donnerstag, 28. Mai 2009 von Sven Köppel / Harald Meixner Protokollant: Harald Meixner Tutor:
Versuch Nr. 02: Bestimmung eines Ohmschen Widerstandes nach der Substitutionsmethode Versuchsdurchführung: Donnerstag, 28. Mai 2009 von Sven Köppel / Harald Meixner Protokollant: Harald Meixner Tutor:
SCHREINER LERN-APP: «3.1.1 ELEKTRIZITÄT»
 Wo sind die Einsatzgebiete bürstenloser Gleichstrommotoren (BLDC)? Was bedeutet BLDC? Spannung Wie ist die Abkürzung für Formeln und die Einheit? Widerstand Wie ist die Abkürzung für Formeln und die Einheit?
Wo sind die Einsatzgebiete bürstenloser Gleichstrommotoren (BLDC)? Was bedeutet BLDC? Spannung Wie ist die Abkürzung für Formeln und die Einheit? Widerstand Wie ist die Abkürzung für Formeln und die Einheit?
Nanotechnologie in der Brennstoffzelle
 Nanotechnologie in der Brennstoffzelle Vortrag zur Vorlesung Nanostrukturphysik WS 10/11 Nicolas Jäckel 1 Übersicht Wie Funktioniert eine Brennstoffzelle? Arten von Brennstoffzellen Nanotechnologische
Nanotechnologie in der Brennstoffzelle Vortrag zur Vorlesung Nanostrukturphysik WS 10/11 Nicolas Jäckel 1 Übersicht Wie Funktioniert eine Brennstoffzelle? Arten von Brennstoffzellen Nanotechnologische
Galvanoplastik. Elektrochemie B. Lukas Woolley, Rafael Adamek, Peter Krack. 24 Februar ETH Zürich
 Elektrochemie B Lukas Woolley Rafael Adamek Peter Krack ETH Zürich 24 Februar 2017 Programm 1 2 3 4 Garfield Elektrolysezelle + - e e Anode Kathode e Cu CuSO 4 Cu 2+ Cu 2+ e Programm 1 2 3 4 Zelltypen
Elektrochemie B Lukas Woolley Rafael Adamek Peter Krack ETH Zürich 24 Februar 2017 Programm 1 2 3 4 Garfield Elektrolysezelle + - e e Anode Kathode e Cu CuSO 4 Cu 2+ Cu 2+ e Programm 1 2 3 4 Zelltypen
Zusammenfassung v09 vom 28. Mai 2013
 Zusammenfassung v09 vom 28. Mai 2013 Ohm sche Widerstände sind durch die Befolgung des Ohm schen Gesetzes charakterisiert. Dies beinhaltet in (idealisierten Fällen) die Linearität zwischen Strom und Spannung,
Zusammenfassung v09 vom 28. Mai 2013 Ohm sche Widerstände sind durch die Befolgung des Ohm schen Gesetzes charakterisiert. Dies beinhaltet in (idealisierten Fällen) die Linearität zwischen Strom und Spannung,
Themengebiet: Thermodynamik. Brennstoffzelle, Wirkungsgrad, Durchtrittsüberspannung, Diffusionsüberspannung,
 Seite 1 Themengebiet: Thermodynamik Stichwörter, Wirkungsgrad, Durchtrittsüberspannung, Diffusionsüberspannung, Literatur [1] A. Macdonald and M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris,
Seite 1 Themengebiet: Thermodynamik Stichwörter, Wirkungsgrad, Durchtrittsüberspannung, Diffusionsüberspannung, Literatur [1] A. Macdonald and M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris,
Aufgaben zur Elektrizitätslehre
 Aufgaben zur Elektrizitätslehre Elektrischer Strom, elektrische Ladung 1. In einem Metalldraht bei Zimmertemperatur übernehmen folgende Ladungsträger den Stromtransport (A) nur negative Ionen (B) negative
Aufgaben zur Elektrizitätslehre Elektrischer Strom, elektrische Ladung 1. In einem Metalldraht bei Zimmertemperatur übernehmen folgende Ladungsträger den Stromtransport (A) nur negative Ionen (B) negative
Speichertechniken für die zukünftige Energieversorgung Energiespeicher-Symposium Stuttgart 06./07. März Ulrich Wagner
 Speichertechniken für die zukünftige Energieversorgung Energiespeicher-Symposium Stuttgart 06./07. März 2012 Ulrich Wagner Energiespeicher strategische Elemente des zukünftigen Energiesystems - Energiekonzept
Speichertechniken für die zukünftige Energieversorgung Energiespeicher-Symposium Stuttgart 06./07. März 2012 Ulrich Wagner Energiespeicher strategische Elemente des zukünftigen Energiesystems - Energiekonzept
