Blut,Plasma,Serum, Künstl. Niere bis 2,00 mmol/l Messparameter: Na + Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff
|
|
|
- Bella Arnold
- vor 6 Jahren
- Abrufe
Transkript
1 Messparameter: H Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser, Glaziologie Messparameter: H Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser Messparameter: H Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser, Tränenflüssigkeit Messparameter: Na Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Blut, Plasma, Serum, Künstliche Niere Messparameter: Na Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser, künstliche Niere Messparameter: Na Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Blut, Plasma, Serum Blut,Plasma,Serum, Künstl. Niere bis 2,00 mmol/l Messparameter: Na Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Acetat in den Dialyselösungen Messparameter: Na Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser mit phwerten >8 Drastisches Unterscheidungsvermögen gegenüber Messparameter: Na Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff K und Li Blut, Plasma, Serum, Fermenter, Wasser auch bei Messparameter: K Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff einem ph >10 Blut, Plasma, Serum, Urin, Künstliche Niere, Messparameter: K Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Fermenter, Wasser Blut, Plasma, Serum, Urin, Künstliche Niere, Messparameter: K Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser Analytik auch bei hohen RubidiumAktivitäten bzw. Messparameter: Rb Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Konzentrationen >0,1M Messparameter: Rb Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Rb Elektroanalytik auch bei einem phwert <1 Messparameter: Rb Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Rb Elektroanalytik auch bei phwerten >10 Analytik auch bei hohen CäsiumionenAktivitäten Messparameter: Cs Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff bzw. Konzentrationen >0,1M Messparameter: Cs Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wässrige Lösungen Hauptstr Röslau 1/6
2 Messparameter: Cs Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Cs Elektroanalytik auch bei phwerten >10 Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser, Fermenter Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff NH4 Elektroanalytik auch bei phwerten >10 Messparameter: Ca Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Blut, Plasma, Serum, Urin, Wasser, Fermenter Blut, Plasma, Serum, Urin, Wasser, Fermenter, Messparameter: Ca Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Künstl. Niere bis 2,00 mmol/l Ac Messparameter: Ca Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser mit phwerten >8 Messparameter: Cl Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Blut, Plasma, Serum Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Wasser Wasser, hochselektiv gegenüber SulfatIonen, Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff großer Meßbereich Messparameter: OAn Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff Sensor zur Messung organischer Anionen Messparameter: Ag Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff neu Messparameter: Li Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff neu Messparameter: Ba 2 Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff neu Messparameter: Cu 2 Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff neu Messparameter: Zn 2 Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff neu Messparameter: NO 2 Potentiometrisch Ionenselektiv Membran Tubulär, Kunststoff neu Messparameter: H Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser, in CO 2 Sensoren Hauptstr Röslau 2/6
3 Messparameter: H Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser Messparameter: Na Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Künstliche Niere Messparameter: Na Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser Messparameter: Na Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Spezialanwendung Künstliche Niere bis 2,00 mmol/l Acetat in den Messparameter: Na Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Dialyselösungen Messparameter: Na Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser mit phwerten >8 Drastisches Unterscheidungsvermögen gegenüber Messparameter: Na Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff K und Li Messparameter: K Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Fermenter, Wasser auch bei einem ph >10 Messparameter: K Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Künstliche Niere, Fermenter, Wasser Messparameter: K Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Künstliche Niere, Wasser Analytik auch bei hohen RubidiumAktivitäten bzw. Messparameter: Rb Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Konzentrationen >0,1M Messparameter: Rb Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Rb Elektroanalytik auch bei einem phwert <1 Messparameter: Rb Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Rb Elektroanalytik auch bei phwerten >10 Messparameter: Cs Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Spezialanwendung Messparameter: Cs Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Cs Elektroanalytik auch bei phwerten >10 Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser, Fermenter Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff NH 4 Elektroanalytik auch bei phwerten >10 Hauptstr Röslau 3/6
4 Messparameter: Ca Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser, Fermenter Messparameter: Ca Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser mit phwerten >8 Messparameter: Ca Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser, Fermenter Messparameter: Cl Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Spezialanwendung Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff Wasser, hochselektiv gegenüber SulfatIonen Wasser, hochselektiv gegenüber SulfatIonen, Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff großer Meßbereich Messparameter: J Potentiometrisch Ionenselektiv Membran wechselbar, flach, Kunststoff hochselektiv für die Wasseranalytik Potentiometrisch Ionenselektiv Membran Kunststoff, MSSerie Wasser, hochselektiv gegenüber SulfatIonen Messparameter: Harnstoff Messparameter: Harnstoff Potentiometrisch Potentiometrisch Membran wechselbar, Enzym, NH4 selektiv. Membran wechselbar, Enzym, NH4 selektiv. Künstliche Niere Spezialanwendung Messparameter: pco 2 Potentiometrisch Gas Membran wechselbar Wasser, Blut, Luft, Gase Messparameter: ßDGlucose Messparameter: ßDGlucose Messparameter: LLactat Messparameter: Methanol Messparameter: Methanol Fermenter, Künstliche Niere Blut, Plasma, Serum, Künstliche Niere, Fermenter Blut, Plasma, Serum, Künstliche Niere, Fermenter LeckageÜberwachung von MethanolTanks, Meßbereich 160mg/l Messung in wäßrigen Lösungen Hauptstr Röslau 4/6
5 Messparameter: Ethanol Messparameter: Ethanol Messparameter: Isopropanol Messparameter: Formaldehyd Messparameter: Glutardialdehyd Messparameter: LAscorbat Messparameter: Oxalat Messparameter: Oxalat Membran wechselbar, Enzym, H 2 O 2 selektiv. Bier, Wein, Sekt, Liköre usw. Bier, Wein, Sekt, Korn usw. Druckereien (korrekte Bezeichnung: 2Propanol oder Isopropylalkohol) Spezialanwendung Glutardialdehyd = Glutaraldehyd Vitamin C ist LAscorbinsäure. Spezialanwendung zur Messung im mikromolaren Bereich Wasser Wasser, Waschmittellösungen, Bleichen in der Papierindustrie hochempfindlicher H 2 O 2 Sensor für wässrige Lösungen Messparameter: ßDGlucose Glucosemessung im mikromolaren Bereich Messparameter: ph Potentiometrisch Ionenselektiv Membran Tubulär, Glas Blut, Tränenflüssigkeit, Wasser, Fermenter Messparameter: ph Potentiometrisch Ionenselektiv Membran Tubulär, Glas Blut, Wasser, Fermenter Messparameter: ph Potentiometrisch Ionenselektiv Membran Tubulär, Glas Wasser Messparameter: Na Potentiometrisch Ionenselektiv Membran Tubulär, Glas Blut, Wasser, Fermenter Messparameter: Cl Potentiometrisch Ionenselektiv Membran Festkörper Wasser Hauptstr Röslau 5/6
6 Messparameter: J Potentiometrisch Ionenselektiv Membran Festkörper Wasser Messparameter: Br Potentiometrisch Ionenselektiv Membran Festkörper neu Messparameter: S 2 Potentiometrisch Ionenselektiv Membran Festkörper neu Messparameter: Ag Potentiometrisch Ionenselektiv Membran Festkörper neu Membran wechselbar Membran wechselbar Wasser Membran wechselbar Wasser: Grenzwertkontrolle 0,1 mg/l H 2 O 2, Auflösung: 0,001 mg/l H 2 O 2 Wasseraufbereitung, Bleichen in der Textil und Papierindustrie Membran wechselbar Prozeßkontrolle in der Textilindustrie Messparameter: po 2 Gas Membran wechselbar Blut, Wasser, Luft, Gase Messparameter: ph 2 Gas Membran wechselbar Gase, Lösungen Hinweis: Aufgrund steter Entwicklung neuer Sensoren, ist diese Liste keineswegs vollständig, sondern nur als repräsentatives Beispiel zu verstehen. Weitere Parameter auf Anfrage! Hauptstr Röslau 6/6
Wasserchemie Modul 4
 Wasserchemie Modul 4 Ionenchromatographie / HPLC Plausibilitätstests tstests Ionensensitive Elektroden Chromatographie Trennung von Stoffgemischen Zwei nicht mischbare Phasen - stationäre Phase (Ionentauscher)
Wasserchemie Modul 4 Ionenchromatographie / HPLC Plausibilitätstests tstests Ionensensitive Elektroden Chromatographie Trennung von Stoffgemischen Zwei nicht mischbare Phasen - stationäre Phase (Ionentauscher)
Produktekatalog. Ionenselektive Elektroden
 Produktekatalog Ionenselektive Elektroden Inhalt Inhalt Inhalt... 1 Übersicht... 2 1. Ionenselektive Elektroden... 3 Festkörper (IS 550)... 4 Plastikmembran (IS 561)... 7 Glasmembran (G 15)... 9 2. Gassensitive
Produktekatalog Ionenselektive Elektroden Inhalt Inhalt Inhalt... 1 Übersicht... 2 1. Ionenselektive Elektroden... 3 Festkörper (IS 550)... 4 Plastikmembran (IS 561)... 7 Glasmembran (G 15)... 9 2. Gassensitive
CITSens Ion. Ionenselektive Elektroden, Ionenselektive Membranen, Ionenmeter (Potentiometer) und mehr
 CITSens Ion Ionenselektive Elektroden, Ionenselektive Membranen, Ionenmeter (entiometer) und mehr Inhaltsverzeichnis CITSens Ion...1 CITSens Ion entiometer...3 CITSens Ion Ministab-Elektroden...5 Art.
CITSens Ion Ionenselektive Elektroden, Ionenselektive Membranen, Ionenmeter (entiometer) und mehr Inhaltsverzeichnis CITSens Ion...1 CITSens Ion entiometer...3 CITSens Ion Ministab-Elektroden...5 Art.
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Vergleichbarkeitsklassen
 ÖQUASTA Seite: 1/ 5 Parameter: ph 1.Wert Roche / AVL C Parameter: ph 2.Wert 5 9 Parameternummer,name ÖQUASTA Seite: 2/ 5 Parameter: ph 2.Wert Roche / AVL C Parameter: po2 1.Wert Roche / AVL 5 9 5 Parameternummer,name
ÖQUASTA Seite: 1/ 5 Parameter: ph 1.Wert Roche / AVL C Parameter: ph 2.Wert 5 9 Parameternummer,name ÖQUASTA Seite: 2/ 5 Parameter: ph 2.Wert Roche / AVL C Parameter: po2 1.Wert Roche / AVL 5 9 5 Parameternummer,name
Titration Sensors. Titrations-Sensoren DS800-TwoPhase DS500 DP5 Phototrode. Titration verschiedenster Tenside schnell, genau und verlässlich
 Titration Sensors TitrationsSensoren DS800TwoPhase DS500 DP5 Phototrode Titration verschiedenster Tenside schnell, genau und verlässlich Zweiphasen TensidTitrationen DS800TwoPhase Überlegene Leistung für
Titration Sensors TitrationsSensoren DS800TwoPhase DS500 DP5 Phototrode Titration verschiedenster Tenside schnell, genau und verlässlich Zweiphasen TensidTitrationen DS800TwoPhase Überlegene Leistung für
Analysenservice FM-VEA-AS
 Analysenservice FM-VEA-AS Preisliste 2015 Analytik von Wasser, Abwasser, Böden, Schlämmen, Abfällen, Sonderproben Art der Leistung Probennahme nach Aufwand nach Aufwand Aufbereitung von Feststoffen Brechen
Analysenservice FM-VEA-AS Preisliste 2015 Analytik von Wasser, Abwasser, Böden, Schlämmen, Abfällen, Sonderproben Art der Leistung Probennahme nach Aufwand nach Aufwand Aufbereitung von Feststoffen Brechen
Potentiometrische Messungen
 Potentiometrische Messungen Vorlesungsreihe: Analytische Chemie (WS 2011 / 2012) Vorlesungsgliederung Messaufbau potentiometrischer Methoden Klassifizierung potentiometrischer Elektroden Charakterisierung
Potentiometrische Messungen Vorlesungsreihe: Analytische Chemie (WS 2011 / 2012) Vorlesungsgliederung Messaufbau potentiometrischer Methoden Klassifizierung potentiometrischer Elektroden Charakterisierung
SS 2010. Thomas Schrader. der Universität Duisburg-Essen. (Teil 7: Säuren und Basen, Elektrolyte)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 7: Säuren und Basen, Elektrolyte) Definition Säure/Base Konjugierte Säure/Base-Paare Konjugierte
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 7: Säuren und Basen, Elektrolyte) Definition Säure/Base Konjugierte Säure/Base-Paare Konjugierte
Im Wasser sind ph-werte von ca bis 15 möglich.
 8 Superbasen 8.1 Basizität im System Wasser 2 H 2 O H 3 O + + OH pk =14 Säurestärken (pk S ): pk S HClO 4 10 saurer als H 3 O + HCl 7 H 2 SO 4 3 H 3 O + 0 H 3 PO 4 2.2 H 3.2 HCN 9.2 H 2 O 2 11.6 H 2 O
8 Superbasen 8.1 Basizität im System Wasser 2 H 2 O H 3 O + + OH pk =14 Säurestärken (pk S ): pk S HClO 4 10 saurer als H 3 O + HCl 7 H 2 SO 4 3 H 3 O + 0 H 3 PO 4 2.2 H 3.2 HCN 9.2 H 2 O 2 11.6 H 2 O
Kleine Formelsammlung Chemie
 Karl Schwister Kleine Forelsalung Cheie ISBN-1: 3-446-41545-9 ISBN-13: 978-3-446-41545-4 Leseprobe Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-41545-4 sowie i Buchhandel.
Karl Schwister Kleine Forelsalung Cheie ISBN-1: 3-446-41545-9 ISBN-13: 978-3-446-41545-4 Leseprobe Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-41545-4 sowie i Buchhandel.
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Bezeichnung Messbereich Best.Nr. WT % UEG adrig, abgeschirmt
 WT0238 für brennbare Gase Messverfahren: Wärmetönung kabel: 3-adrig, abgeschirmt, z.b. 3 x 1,5 mm 2 LiYCY Kalibrierung: Methan (CH 4 ), brennbare Gase und Dämpfe Ausgangssignal: 0,2.. 1 ma Bezeichnung
WT0238 für brennbare Gase Messverfahren: Wärmetönung kabel: 3-adrig, abgeschirmt, z.b. 3 x 1,5 mm 2 LiYCY Kalibrierung: Methan (CH 4 ), brennbare Gase und Dämpfe Ausgangssignal: 0,2.. 1 ma Bezeichnung
Analytische Chemie. B. Sc. Chemieingenieurwesen. 03. Februar 2010. Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 03. Februar 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 03. Februar 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Qualitative Analyse. - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch,
 - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
- Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
6. Seminar. Prof. Dr. Christoph Janiak. Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 6. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 6. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
Anorganische Chemie I/II
 Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 11. Februar 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 11. Februar 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Anorganische-Chemie. Michael Beetz Arbeitskreis Prof. Bein. Grundpraktikum für Biologen 2017
 Michael Beetz Arbeitskreis Prof. Bein Butenandstr. 11, Haus E, E 3.027 michael.beetz@cup.uni-muenchen.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Trennungsgänge und Nachweise # 2 Trennungsgänge
Michael Beetz Arbeitskreis Prof. Bein Butenandstr. 11, Haus E, E 3.027 michael.beetz@cup.uni-muenchen.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Trennungsgänge und Nachweise # 2 Trennungsgänge
Trennungsgang. AC-I Seminar, B.
 Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Analytische Chemie. B. Sc. Chemieingenieurwesen. 02. Februar Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 02. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 02. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Normalwerte: 1-3% < 1%: Verminderung des effektiv zirkulierenden Volumen (prärenales ANV) >3%: renaler Natriumverlust (z.b. akuter Tubulusschaden)
 Erklärungen Formel 1: Fraktionelle Natriumexkretion (%) Fe (Natrium) = (Natrium (Harn) *Kreatinin (Serum) )/((Natrium (Blut) *Kreatinin (Serum) )*100 Normalwerte: 1-3% < 1%: Verminderung des effektiv zirkulierenden
Erklärungen Formel 1: Fraktionelle Natriumexkretion (%) Fe (Natrium) = (Natrium (Harn) *Kreatinin (Serum) )/((Natrium (Blut) *Kreatinin (Serum) )*100 Normalwerte: 1-3% < 1%: Verminderung des effektiv zirkulierenden
Sauerstoff. Vorkommen:
 Vorkommen: Sauerstoff a) O 2 : Atmosphäre: 23% (21 Vol-%) O 2 der Atmosphäre ist biolog. Ursprungs: (Chlorophyll, Enzyme, hν) H 2 O + CO 2 O 2 + {CH 2 O} b) H 2 O: Meerwasser 86% c) gebunden als Oxide,
Vorkommen: Sauerstoff a) O 2 : Atmosphäre: 23% (21 Vol-%) O 2 der Atmosphäre ist biolog. Ursprungs: (Chlorophyll, Enzyme, hν) H 2 O + CO 2 O 2 + {CH 2 O} b) H 2 O: Meerwasser 86% c) gebunden als Oxide,
Das Formelpuzzle Kopiervorlage
 Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
Physiologie der Atmung. Cem Ekmekcioglu
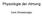 Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Homöostase der Mineralstoffe
 Mineralstoffversorgung auf dem Milchviehbetrieb Vetsuisse-Fakultät Zürich 24. November 2015 Homöostase der Mineralstoffe Maren Feldmann Klinik für Rinder Tierärztliche Hochschule Hannover Rindergesundheitsdienst
Mineralstoffversorgung auf dem Milchviehbetrieb Vetsuisse-Fakultät Zürich 24. November 2015 Homöostase der Mineralstoffe Maren Feldmann Klinik für Rinder Tierärztliche Hochschule Hannover Rindergesundheitsdienst
7. Woche. Gesamtanalyse (Vollanalyse) einfacher Salze. Qualitative Analyse anorganischer Verbindungen
 7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
Übung zu den Vorlesungen Organische und Anorganische Chemie
 Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 12.11.08 1. Stellen sie die Reaktionsgleichung für die Herstellung von Natriumsulfid aus den Elementen auf. Wieviel
Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 12.11.08 1. Stellen sie die Reaktionsgleichung für die Herstellung von Natriumsulfid aus den Elementen auf. Wieviel
Allgemeine Grundlagen 2
 Allgemeine Grundlagen 2 1 Reaktionen und Bindung 1) Redox - Reaktionen 1. Semester 2) Säure - Base - Reaktionen 1. Semester 3) Komplexreaktionen (eigentlich kein neuer Reaktionstyp, sondern eine Säure
Allgemeine Grundlagen 2 1 Reaktionen und Bindung 1) Redox - Reaktionen 1. Semester 2) Säure - Base - Reaktionen 1. Semester 3) Komplexreaktionen (eigentlich kein neuer Reaktionstyp, sondern eine Säure
Elektrochemisches Gleichgewicht
 Elektrochemisches Gleichgewicht - Me 2 - Me Me 2 - Me 2 - Me 2 Oxidation: Me Me z z e - Reduktion: Me z z e - Me ANODE Me 2 Me 2 Me 2 Me 2 Me Oxidation: Me Me z z e - Reduktion: Me z z e - Me KATHODE Instrumentelle
Elektrochemisches Gleichgewicht - Me 2 - Me Me 2 - Me 2 - Me 2 Oxidation: Me Me z z e - Reduktion: Me z z e - Me ANODE Me 2 Me 2 Me 2 Me 2 Me Oxidation: Me Me z z e - Reduktion: Me z z e - Me KATHODE Instrumentelle
Lösung Sauerstoff: 1s 2 2s 2 2p 4, Bor: 1s 2 2s 2 2p 1, Chlor: 1s 2 2s 2 2p 6 3s 2 3p 5 Neon: 1s 2 2s 2 2p 6
 1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
Proteine I. Fällung Konzentrationsbestimmung. Dr. Richard Weiss
 Proteine I Fällung Konzentrationsbestimmung Dr. Richard Weiss Praktikumsaufbau Tag 1: Konzentrieren Denaturierende und native Fällung Protein Konzentrationsbestimmung Tag 2: Entsalzen Gelchromatographie
Proteine I Fällung Konzentrationsbestimmung Dr. Richard Weiss Praktikumsaufbau Tag 1: Konzentrieren Denaturierende und native Fällung Protein Konzentrationsbestimmung Tag 2: Entsalzen Gelchromatographie
Übungsklausur - Lösung
 Übungsklausur - Lösung Das Benutzen eines Periodensystems zur Lösung der Klausur ist selbstverständlich erlaubt. 1. Geben Sie die Verhältnisformel von folgenden Verbindungen an (8P): a) Kaliumiodid KI
Übungsklausur - Lösung Das Benutzen eines Periodensystems zur Lösung der Klausur ist selbstverständlich erlaubt. 1. Geben Sie die Verhältnisformel von folgenden Verbindungen an (8P): a) Kaliumiodid KI
Produktekatalog. ph Elektroden
 Produktekatalog ph Elektroden Inhalt Inhalt Inhalt... 1 Übersicht... 2 Allgemeines... 3 1. ph Elektroden... 5 ph Glaselektroden (GA Reihe)... 6 Kombinierte ph Elektroden (CA Reihe)... 9 1 Übersicht Übersicht
Produktekatalog ph Elektroden Inhalt Inhalt Inhalt... 1 Übersicht... 2 Allgemeines... 3 1. ph Elektroden... 5 ph Glaselektroden (GA Reihe)... 6 Kombinierte ph Elektroden (CA Reihe)... 9 1 Übersicht Übersicht
6,
 ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome. Chemische Reaktionen. Verbindungen
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 92 Grundlagen der Allgemeinen und Anorganischen Chemie 3. Das Periodensystem der Elemente 93
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 92 Grundlagen der Allgemeinen und Anorganischen Chemie 3. Das Periodensystem der Elemente 93
Probenahme. Nachbarschaftstag Marburg Biedenkopf
 Probenahme Nachbarschaftstag Marburg Biedenkopf 17.09.2009 Probenahme Nachbarschaftstag Marburg Biedenkopf 17.09.2009 Wesentlicher Baustein einer aussagekräftigen Analytik Entnahme einer repräsentativen
Probenahme Nachbarschaftstag Marburg Biedenkopf 17.09.2009 Probenahme Nachbarschaftstag Marburg Biedenkopf 17.09.2009 Wesentlicher Baustein einer aussagekräftigen Analytik Entnahme einer repräsentativen
Parameter zur Bewertung von Betriebsproblemen bei Faulbehältern. Karl Svardal
 Parameter zur Bewertung von Betriebsproblemen bei Faulbehältern Karl Svardal Institut für Wassergüte, Ressourcenmanagement und Abfallwirtschaft Technische Universität Wien Einleitung mesophile Schlammfaulung
Parameter zur Bewertung von Betriebsproblemen bei Faulbehältern Karl Svardal Institut für Wassergüte, Ressourcenmanagement und Abfallwirtschaft Technische Universität Wien Einleitung mesophile Schlammfaulung
Themen heute: Säuren und Basen, Redoxreaktionen
 Wiederholung der letzten Vorlesungsstunde: Massenwirkungsgesetz, Prinzip des kleinsten Zwangs, Löslichkeitsprodukt, Themen heute: Säuren und Basen, Redoxreaktionen Vorlesung Allgemeine Chemie, Prof. Dr.
Wiederholung der letzten Vorlesungsstunde: Massenwirkungsgesetz, Prinzip des kleinsten Zwangs, Löslichkeitsprodukt, Themen heute: Säuren und Basen, Redoxreaktionen Vorlesung Allgemeine Chemie, Prof. Dr.
SS Thomas Schrader. der Universität Duisburg-Essen. (Teil 8: Redoxprozesse, Elektrochemie)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Küvetten-Test LCK 320 Eisen 2+/3+
 ACHTUNG NEU! Das aktuelle Ausgabedatum finden Sie bei dem Arbeitsgang bzw. der. Küvetten-Test /3+ Prinzip Eisen(II)-Ionen bilden mit 1.10-Phenantrolin eine orangerote Komplexverbindung. Eisen(III)-Ionen
ACHTUNG NEU! Das aktuelle Ausgabedatum finden Sie bei dem Arbeitsgang bzw. der. Küvetten-Test /3+ Prinzip Eisen(II)-Ionen bilden mit 1.10-Phenantrolin eine orangerote Komplexverbindung. Eisen(III)-Ionen
_ED_Anhang.qxd :38 Seite 1557 Anhang Appendix
 Anhang Appendix Maße und Gewichte Weights and Measures Anhang Appendix I. Längenmaße I. Linear Measures 1. Amerikanische Längenmaße 1. American Linear Measure 1 yard = 3 feet = 0,9144 m = 91,44 cm 1 foot
Anhang Appendix Maße und Gewichte Weights and Measures Anhang Appendix I. Längenmaße I. Linear Measures 1. Amerikanische Längenmaße 1. American Linear Measure 1 yard = 3 feet = 0,9144 m = 91,44 cm 1 foot
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
Messung von Kohlendioxid CO 2 und flüchtigen organischen Verbindungen (VOCs) im Innenraum
 Sensorik in der Innenraumklimatisierung S. Kittelmann, O. Kiesewetter, R. Traute, A. Krausser UST Umweltsensortechnik GmbH Messung von Kohlendioxid CO 2 und flüchtigen organischen Verbindungen (VOCs) im
Sensorik in der Innenraumklimatisierung S. Kittelmann, O. Kiesewetter, R. Traute, A. Krausser UST Umweltsensortechnik GmbH Messung von Kohlendioxid CO 2 und flüchtigen organischen Verbindungen (VOCs) im
Sehr geehrter Auftraggeber, anbei erhalten Sie den Prüfbericht zu den Proben: Probenummer Entnahmestelle Probenahme
 / S-NA-LB, Strom- und Wasserversorgung info@stw-toelz.de Besucheranschrift S-NA-LB Gebäude G (Labor) Emmy-Noether-Str. 2 Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner: Hr. Bader Telefon / -Fax 089 / 2361-3462/
/ S-NA-LB, Strom- und Wasserversorgung info@stw-toelz.de Besucheranschrift S-NA-LB Gebäude G (Labor) Emmy-Noether-Str. 2 Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner: Hr. Bader Telefon / -Fax 089 / 2361-3462/
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7
 AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser
 REPORT Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. YVE & BIO GmbH, Bremen 4 Otmar Plank 5 HET August 2014
REPORT Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. YVE & BIO GmbH, Bremen 4 Otmar Plank 5 HET August 2014
Rationale Basisdiagnostik bei Elektrolytstörungen
 Rationale Basisdiagnostik bei Elektrolytstörungen Siegfried Waldegger Kindernephrologie Innsbruck Department für Kinder und Jugendheilkunde Elektrolytstörungen in Zusammenhang mit angeborenen Erkrankungen
Rationale Basisdiagnostik bei Elektrolytstörungen Siegfried Waldegger Kindernephrologie Innsbruck Department für Kinder und Jugendheilkunde Elektrolytstörungen in Zusammenhang mit angeborenen Erkrankungen
Lösungen zu den Übungen zur Experimentalvorlesung AC
 Lösungen zu den Übungen zur Experimentalvorlesung AC 1. Stöchiometrisches Rechnen 1.1. n (S = mol n (S 8 = 0,5 mol 1.. n (P = 8 mol n (P = mol 1.3. m (P =,8 g m (P =,8 g m (P = 1, g 1.. m (1/3 As 3+ =
Lösungen zu den Übungen zur Experimentalvorlesung AC 1. Stöchiometrisches Rechnen 1.1. n (S = mol n (S 8 = 0,5 mol 1.. n (P = 8 mol n (P = mol 1.3. m (P =,8 g m (P =,8 g m (P = 1, g 1.. m (1/3 As 3+ =
Anhang Zustand Solothurner Gewässer_Inhalt_def.indd :15
 Anhang Beurteilungskriterien für Oberflächengewässer und Grundwasser Beurteilungskriterien für Oberflächengewässer Biochemischer Sauerstoffbedarf (BSB 5 2 bis 4 mg/l O 2 Gelöster organischer Kohlenstoff
Anhang Beurteilungskriterien für Oberflächengewässer und Grundwasser Beurteilungskriterien für Oberflächengewässer Biochemischer Sauerstoffbedarf (BSB 5 2 bis 4 mg/l O 2 Gelöster organischer Kohlenstoff
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
9. Das Messen von Potentialen, die elektrochemische Zelle
 Analytik 9.1 9. Das Messen von Potentialen, die elektrochemische Zelle 9.1. Die elektrochemische Zelle Die elektrochemische Zelle erlaubt es, die freie Energie einer chemischen Reaktion direkt in elektrische
Analytik 9.1 9. Das Messen von Potentialen, die elektrochemische Zelle 9.1. Die elektrochemische Zelle Die elektrochemische Zelle erlaubt es, die freie Energie einer chemischen Reaktion direkt in elektrische
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Periodensystem. Physik und Chemie. Sprachkompendium und einfache Regeln
 Periodensystem Physik und Chemie Sprachkompendium und einfache Regeln 1 Begriffe Das (neutrale) Wasserstoffatom kann völlig durchgerechnet werden. Alle anderen Atome nicht; ein dermaßen komplexes System
Periodensystem Physik und Chemie Sprachkompendium und einfache Regeln 1 Begriffe Das (neutrale) Wasserstoffatom kann völlig durchgerechnet werden. Alle anderen Atome nicht; ein dermaßen komplexes System
2. Woche. Anorganische Analysenmethodik
 2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
C. Röhr, Phosphor, WS 09/10. Phosphor Phosphane Phosphide -
 Phosphor Phosphane Phosphide - Inhalt Einleitung Elementmodifikationen Phosphane/Phosphide mit PH/P : P > 1 (Kettenstücke) Phosphane/Phosphide mit PH/P : P = 1 (Ketten und Ringe) Phosphane/Phosphide mit
Phosphor Phosphane Phosphide - Inhalt Einleitung Elementmodifikationen Phosphane/Phosphide mit PH/P : P > 1 (Kettenstücke) Phosphane/Phosphide mit PH/P : P = 1 (Ketten und Ringe) Phosphane/Phosphide mit
Das Chemische Gleichgewicht
 II. Gleichgewichte von Säuren S und Basen 13 Puffer-Lösungen Definition: Lösungen, die einen definierten ph-wert haben, der konstant bleibt, auch wenn Säuren S oder Basen in begrenzten Mengen zugesetzt
II. Gleichgewichte von Säuren S und Basen 13 Puffer-Lösungen Definition: Lösungen, die einen definierten ph-wert haben, der konstant bleibt, auch wenn Säuren S oder Basen in begrenzten Mengen zugesetzt
Enthalpie, Entropie und Temperatur des Phasenübergangs flüssig-gasförmig. eine Analyse von Elementen und chemischen Verbindungen
 Bayerisches Zentrum für Angewandte Energieforschung e.v. Enthalpie, Entropie und Temperatur des Phasenübergangs flüssiggasförmig eine Analyse von Elementen und chemischen Verbindungen Harald Mehling Berater
Bayerisches Zentrum für Angewandte Energieforschung e.v. Enthalpie, Entropie und Temperatur des Phasenübergangs flüssiggasförmig eine Analyse von Elementen und chemischen Verbindungen Harald Mehling Berater
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Säure - Base - Theorien
 Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Säure Base Theorien S. Arrhenius (1887) Säuren sind Stoffe, die in wässriger Lösung H + (aq) Ionen bilden, während Basen OH (aq) Ionen bilden. H 2 SO 4, HNO 3, HCl, NaOH, Ba(OH) 2, aber: NH 3, CH 3, OCH
Strukturchemie. Kristallstrukturen. Elementstrukturen. Kugelpackungen. Kubisch dichte Kugelpackung. Lehramt 1a Sommersemester
 Kugelpackungen Kubisch dichte Kugelpackung Lehramt 1a Sommersemester 2010 1 Kugelpackungen: kubisch dichte Packung (kdp, ccp) C B A A C B A C B A C Lehramt 1a Sommersemester 2010 2 Kugelpackungen Atome
Kugelpackungen Kubisch dichte Kugelpackung Lehramt 1a Sommersemester 2010 1 Kugelpackungen: kubisch dichte Packung (kdp, ccp) C B A A C B A C B A C Lehramt 1a Sommersemester 2010 2 Kugelpackungen Atome
Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s 2 3p 6. Geben Sie isoelektronische Ionen zu den folgenden Atomen an
 Übung 05.11.13 Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 Ne / F - / O 2- / N 3- / Na + / Mg 2+ / Al 3+. Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s
Übung 05.11.13 Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 Ne / F - / O 2- / N 3- / Na + / Mg 2+ / Al 3+. Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s
Phalloidin-Färbung an kultivierten adhärenten Säugerzellen. Formaldehyd-Fixierung
 Phalloidin-Färbung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen. Hier
Phalloidin-Färbung an kultivierten adhärenten Säugerzellen Formaldehyd-Fixierung 2 Materialien Pinzetten Für das Handling der Zellen ist es empfehlenswert Pinzetten mit sehr feiner Spitze zu nutzen. Hier
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Atombau, Periodensystem der Elemente
 Seminar zum Brückenkurs Chemie 2015 Atombau, Periodensystem der Elemente Dr. Jürgen Getzschmann Dresden, 21.09.2015 1. Aufbau des Atomkerns und radioaktiver Zerfall - Erläutern Sie den Aufbau der Atomkerne
Seminar zum Brückenkurs Chemie 2015 Atombau, Periodensystem der Elemente Dr. Jürgen Getzschmann Dresden, 21.09.2015 1. Aufbau des Atomkerns und radioaktiver Zerfall - Erläutern Sie den Aufbau der Atomkerne
O H H 3 C. Methanol. Molekulargewicht Siedepunkt Löslichkeit in Wasser H 3 C-OH. unbegrenzt H 3 C-Cl. 7.4 g/l H 3 C-CH 3 -24/C -88/C
 Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Tintometer -Group. CHECKIT Comparator. Highlights. mit kontinuierlichen Farbskalen (Discs) kostengünstig genau zuverlässig
 Tintometer -Group Highlights Einfache Handhabung, exakte Reagenzdosierung Mindesthaltbarkeit von 5/10 Jahren auf Tabletten in Aluminium-Folie Hohe Analysegenauigkeit Problemloser Versand und sichere Lagerung
Tintometer -Group Highlights Einfache Handhabung, exakte Reagenzdosierung Mindesthaltbarkeit von 5/10 Jahren auf Tabletten in Aluminium-Folie Hohe Analysegenauigkeit Problemloser Versand und sichere Lagerung
Weiterbildungskurs: «Messtechnik: Eine Reise vom Messwert zur wertvollen Information»
 Funktionsprinzipien und Grenzen der häufigst eingesetzten Sensoren TS NH 4 -N mg/l NO 3 -N g/l ph O 2 ppm W-18, 2013 / 2014 Martina Hofer Seite 1 Ablauf Inhalt Messverfahren Sensoren Zeit [min] Ionen Selektiv
Funktionsprinzipien und Grenzen der häufigst eingesetzten Sensoren TS NH 4 -N mg/l NO 3 -N g/l ph O 2 ppm W-18, 2013 / 2014 Martina Hofer Seite 1 Ablauf Inhalt Messverfahren Sensoren Zeit [min] Ionen Selektiv
Anorganische Chemie I
 Anorganische Chemie I PRÜFUNG B. Sc. Chemieingenieurwesen 14. Juli 2014 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie I PRÜFUNG B. Sc. Chemieingenieurwesen 14. Juli 2014 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
(Atommassen: Ca = 40, O = 16, H = 1;
 1.) Welche Molarität hat eine 14,8%ige Ca(OH) 2 - Lösung? (Atommassen: Ca = 40, O = 16, H = 1; M: mol/l)! 1! 2! 2,5! 3! 4 M 2.) Wieviel (Gewichts)%ig ist eine 2-molare Salpetersäure der Dichte 1,100 g/cm
1.) Welche Molarität hat eine 14,8%ige Ca(OH) 2 - Lösung? (Atommassen: Ca = 40, O = 16, H = 1; M: mol/l)! 1! 2! 2,5! 3! 4 M 2.) Wieviel (Gewichts)%ig ist eine 2-molare Salpetersäure der Dichte 1,100 g/cm
1.6. Die Ionenbindung
 1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
Chemische Bindung. Ue Mol 1. fh-pw
 Ue Mol 1 Chemische Bindung Periodensystem - Atome - Moleküle Periodensystem(e) 3 Nichtmetalle - Metalloide 5 Eigenschaften der Elemente 6 Bindungstypen 7 Ionenbindung 8 Kovalente, homöopolare Bindung 10
Ue Mol 1 Chemische Bindung Periodensystem - Atome - Moleküle Periodensystem(e) 3 Nichtmetalle - Metalloide 5 Eigenschaften der Elemente 6 Bindungstypen 7 Ionenbindung 8 Kovalente, homöopolare Bindung 10
Akkreditierungsumfang der Prüfstelle (EN ISO/IEC 17025:2005) Seibersdorf Labor GmbH Chemische Analytik / (Ident.Nr.: 0312)
 Chemische Analytik / (Ident.: 031 1 2 3 4 5 6 7 8 9 10 11 12 AA E03 AA G01 AA_L10 AA_L16 D04 D05 D11 D17 D18 D19 DIN 38405-13 DIN 38405-21 2008-02 Quantitative Bestimmung von Chlorid in wässrigen Lösungen
Chemische Analytik / (Ident.: 031 1 2 3 4 5 6 7 8 9 10 11 12 AA E03 AA G01 AA_L10 AA_L16 D04 D05 D11 D17 D18 D19 DIN 38405-13 DIN 38405-21 2008-02 Quantitative Bestimmung von Chlorid in wässrigen Lösungen
Redoxreaktionen. Elektrochemische Spannungsreihe
 Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
Teil F: Übersicht über die obligatorischen und fakultativen Parameter der BZE- und Level I+II-Erhebungen. Inhaltsverzeichnis Teil F
 F Boden Humus Inhaltsverzeichnis Teil F BZE Level I+II F. Übersicht über die optionalen und fakultativen der BZE- und Level I+II-Erhebungen 1. BZE 1.1 BZE (1) 1.2 BZE (2) 2. Level I+II 2.1 Level I+II (1)
F Boden Humus Inhaltsverzeichnis Teil F BZE Level I+II F. Übersicht über die optionalen und fakultativen der BZE- und Level I+II-Erhebungen 1. BZE 1.1 BZE (1) 1.2 BZE (2) 2. Level I+II 2.1 Level I+II (1)
Messmethoden. Die Bestimmung von Ammonium-N und Nitrat-N erfolgt durch fraktionierte Destillation
 Messmethoden Probenvorbereitung 5 ml/l Dünger in 1000 ml entionisiertem Wasser; Filtration mit Ederol 13 P oder S&S 513 1/2. Bestimmung von NH 4 -N und NO 3 -N Die Bestimmung von Ammonium-N und Nitrat-N
Messmethoden Probenvorbereitung 5 ml/l Dünger in 1000 ml entionisiertem Wasser; Filtration mit Ederol 13 P oder S&S 513 1/2. Bestimmung von NH 4 -N und NO 3 -N Die Bestimmung von Ammonium-N und Nitrat-N
FTIR zur Bestimmung von Alkoholen in Spirituosen
 FTIR zur Bestimmung von Alkoholen in Spirituosen Dr. Martin Geßner Fachzentrum Analytik oenologische und pflanzliche Analytik Inhaltsstoffe von Spirituosen Hauptinhaltsstoffe sind Wasser und Ethanol. Methanol
FTIR zur Bestimmung von Alkoholen in Spirituosen Dr. Martin Geßner Fachzentrum Analytik oenologische und pflanzliche Analytik Inhaltsstoffe von Spirituosen Hauptinhaltsstoffe sind Wasser und Ethanol. Methanol
Umwelthygiene Marburg GmbH & Co KG
 1305431 Umwelthygiene Marburg GmbH & Co KG Rudolf Breitscheidstr. 24, D35037 Marburg Umwelthygiene Marburg GmbH & Co KG Staatlich anerkannte Untersuchungsstelle nach 15 Abs. 4 Amtsgericht Marburg: HRB
1305431 Umwelthygiene Marburg GmbH & Co KG Rudolf Breitscheidstr. 24, D35037 Marburg Umwelthygiene Marburg GmbH & Co KG Staatlich anerkannte Untersuchungsstelle nach 15 Abs. 4 Amtsgericht Marburg: HRB
KliChi. Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik. Dr. med. Bernhard Schlüter - 1 -
 Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Säure-Basen-Analytik und Blutgasanalytik Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium Universitätsklinikum
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot
 Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Die Blutgasanalyse Was ist außerklinisch tolerabel? KAI 2014 Dr. med. Günter Schrot Normale Blutgasanalyse ph 7,36-7,44 po2 >80 mmhg pco2 35-45 mmhg HCO3-22 -26 mmol/l berechnet Das Säure-Basen-System
Ammonium Gasdiffusion / ph-indikator DIN EN ISO (Ammoniak)
 FIA Methodenliste Stand: 24.03.2016 Gesamt- Brenzcatechinviolett APHA 3500 Al modifiziert Aluminium 0,01 mg/l 0,05... 0,5 mg/l Al-T Wasser / Abwasser 0,2... 2 mg/l Al-T Ammonium Gasdiffusion / ph-indikator
FIA Methodenliste Stand: 24.03.2016 Gesamt- Brenzcatechinviolett APHA 3500 Al modifiziert Aluminium 0,01 mg/l 0,05... 0,5 mg/l Al-T Wasser / Abwasser 0,2... 2 mg/l Al-T Ammonium Gasdiffusion / ph-indikator
Analytische Methoden und Verfahren zur Überwachung und Optimierung von Biogasanlagen. Prof. Dr. Thomas Kirner
 Analytische Methoden und Verfahren zur Überwachung und Optimierung von Biogasanlagen Prof. Dr. Thomas Kirner 21.07.2015 Voraussetzungen Fermentation von Biomasse Mikroorganismen interagieren in einem komplexen
Analytische Methoden und Verfahren zur Überwachung und Optimierung von Biogasanlagen Prof. Dr. Thomas Kirner 21.07.2015 Voraussetzungen Fermentation von Biomasse Mikroorganismen interagieren in einem komplexen
5. Periodensystem der Elemente 5.1. Aufbauprinzip 5.2. Geschichte des Periodensystems 5.3. Ionisierungsenergie 5.4. Elektronenaffinität 5.5.
 5. Periodensystem der Elemente 5.1. Aufbauprinzip 5.2. Geschichte des Periodensystems 5.3. Ionisierungsenergie 5.4. Elektronenaffinität 5.5. Atomradien 5.6. Atomvolumina 5.7. Dichte der Elemente 5.8. Schmelzpunkte
5. Periodensystem der Elemente 5.1. Aufbauprinzip 5.2. Geschichte des Periodensystems 5.3. Ionisierungsenergie 5.4. Elektronenaffinität 5.5. Atomradien 5.6. Atomvolumina 5.7. Dichte der Elemente 5.8. Schmelzpunkte
Das chemische Gleichgewicht
 1 Grundlagen Viele Substanzen sind in Wasser praktisch nicht löslich, l d.h. sie sind nur sehr geringfügig gig löslich. (Tatsächlich nicht lösliche Stoffe gibt es nicht! Schwerlösliche Verbindungen In
1 Grundlagen Viele Substanzen sind in Wasser praktisch nicht löslich, l d.h. sie sind nur sehr geringfügig gig löslich. (Tatsächlich nicht lösliche Stoffe gibt es nicht! Schwerlösliche Verbindungen In
Prüfbericht über Wasseruntersuchungen gemäß TrinkwV 2001
 Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
1.1.1 DOSAControl Mess- und Regelgerät DCW 330
 1.1.1 DOSAControl Mess- und Regelgerät DCW 330 3-Kanal-Regler, für potentiostatische und amperometrische Sensoren, zur Messung von: ph-, Redox-Wert und freiem Chlor, -gesamt Chlor, -Chlordioxid, -Brom,
1.1.1 DOSAControl Mess- und Regelgerät DCW 330 3-Kanal-Regler, für potentiostatische und amperometrische Sensoren, zur Messung von: ph-, Redox-Wert und freiem Chlor, -gesamt Chlor, -Chlordioxid, -Brom,
Innovative Grundwassersanierung mittels einer Reaktiven Wand Hans-Joachim Betko Immissionsschutz und Umwelt aktuell, München, 25.10.
 Innovative Grundwassersanierung mittels einer Reaktiven Wand Hans-Joachim Betko Immissionsschutz und Umwelt aktuell, München, 25.10.2010 TÜV SÜD Industrie Service GmbH Herkunft Eisen TÜV SÜD Industrie
Innovative Grundwassersanierung mittels einer Reaktiven Wand Hans-Joachim Betko Immissionsschutz und Umwelt aktuell, München, 25.10.2010 TÜV SÜD Industrie Service GmbH Herkunft Eisen TÜV SÜD Industrie
Kapiteltest 1.1. Kapiteltest 1.2
 Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Chemische und Mikrobiologische Untersuchung von mittels EVA -Wasserfiltersystem aufbereitetem Leitungswasser
 REPORT Chemische und Mikrobiologische Untersuchung von mittels EVA -Wasserfiltersystem aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. Aquadec GmbH, Bremen 4 Otmar Plank 5 HET Berichtsnummer:
REPORT Chemische und Mikrobiologische Untersuchung von mittels EVA -Wasserfiltersystem aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. Aquadec GmbH, Bremen 4 Otmar Plank 5 HET Berichtsnummer:
Platin Substrat Heizung
 CO 2 -Messung in Luft mit Festelektrolytzellen 1 Motivation e Kenntnis der Konzentration von CO 2 als ubiquitäres biogenes Gas ist für die Bestimmung der Aktivität biologischer Prozesse, wie bei der tierischen
CO 2 -Messung in Luft mit Festelektrolytzellen 1 Motivation e Kenntnis der Konzentration von CO 2 als ubiquitäres biogenes Gas ist für die Bestimmung der Aktivität biologischer Prozesse, wie bei der tierischen
Was ist Elektrochemie?
 Was ist Elektrochemie? Eine elektrochemische Reaktion erfüllt folgende vier Eigenschaften: Sie findet an Phasengrenzen statt. Die einzelnen Phasen sind unterschiedlich geladen. (unterschiedliche elektrische
Was ist Elektrochemie? Eine elektrochemische Reaktion erfüllt folgende vier Eigenschaften: Sie findet an Phasengrenzen statt. Die einzelnen Phasen sind unterschiedlich geladen. (unterschiedliche elektrische
Einteilung der Maßanalyse
 Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
Einteilung der Maßanalyse Neutralisation (Säure-Base-Titration Acidimetrie Alkalimetrie Fällungstitration Redoxtitration Iodometrie Dichromatometrie Manganometrie etc. Komplexometrie Säure/Basen Theorien
CHEMIE KAPITEL 4 SÄURE-BASE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
Blut, Urin, Leben: NMR-Analytik macht Verborgenes sichtbar
 Blut, Urin, Leben: NMR-Analytik macht Verborgenes sichtbar Einleitung Blut und Urin Paracelsus: Seit Antike üblich: Schmecken und Riechen des Urins Gut zugängliche Körperflüssigkeiten Routinemäßig zu erhalten
Blut, Urin, Leben: NMR-Analytik macht Verborgenes sichtbar Einleitung Blut und Urin Paracelsus: Seit Antike üblich: Schmecken und Riechen des Urins Gut zugängliche Körperflüssigkeiten Routinemäßig zu erhalten
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung
 Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
Proteine in wässriger Lösung
 Proteine in wässriger Lösung Struktur von Proteinen in wässriger Lösung: außen hydrophobe Bereiche, im Inneren hydrophobe Bereiche, hydrophobic collapse Proteine in wässriger Lösung - + + - Hydrathülle
Proteine in wässriger Lösung Struktur von Proteinen in wässriger Lösung: außen hydrophobe Bereiche, im Inneren hydrophobe Bereiche, hydrophobic collapse Proteine in wässriger Lösung - + + - Hydrathülle
Anorganisch-chemisches Praktikum für Human- und Molekularbiologen
 Anorganisch-chemisches Praktikum für Human- und Molekularbiologen 4. Praktikumstag Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Flammenfärbung
Anorganisch-chemisches Praktikum für Human- und Molekularbiologen 4. Praktikumstag Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Flammenfärbung
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Stoffe oder Teilchen, die Protonen abgeben kånnen, werden als SÄuren bezeichnet (Protonendonatoren).
 5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
