Bestimmung der pflanzlichen oder fossilen Herkunft von L- Weinsäure durch Ermittlung ihrer 14 C -Aktivität
|
|
|
- Claudia Dressler
- vor 6 Jahren
- Abrufe
Transkript
1 RESOLUTION OENO 12/2008 BESTIMMUNG DER PFLANZLICHEN ODER FOSSILEN HERKUNFT VON L-WEINSÄURE DURCH ERMITTLUNG IHRER 14 C -AKTIVITÄT DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf 2 IV des Gründungsübereinkommens vom 3. April 2001 der internationalen Organisation für Rebe und Wein und auf Vorschlag der Unterkommission für Analysemethoden BESCHLIESST, den Anhang A des Internationalen Sammelwerks für Analysemethoden durch folgende Typ-IV-Methode zu ergänzen: Titel Bestimmung der pflanzlichen oder fossilen Herkunft von L- Weinsäure durch Ermittlung ihrer 14 C -Aktivität Typ der Methode IV 1. GEGENSTAND UND ANWENDUNGSBEREICH Die Methode kann dazu benutzt werden, die pflanzliche oder fossile Herkunft von Weinsäure festzustellen und bei einer Mischung der Verbindungen unterschiedlichen Ursprungs ihren jeweiligen Anteil zu ermitteln. Dabei lässt sich fossile L-Weinsäure (L+-Weinsäure) bereits in Mengen von weniger als 10 % bestimmen. 2. PRINZIP Die im Handel erhältliche Weinsäure pflanzlichen Ursprungs ist in den meisten Fällen ein Erzeugnis des Weinbaus. Das im Hefetrub vorhandene Kaliumhydrogentartrat wird extrahiert und als L-Weinsäure in Verkehr gebracht. Der 14 C - Gehalt der Säure hängt daher, wie beim Weinalkohol, vom 14 C -Gehalt des Kohlendioxids der zu Grunde liegenden Weine des jeweiligen Jahrgangs ab. Diese Aktivität ist auf Grund des Herstellungsprozesses relativ hoch. Synthetische Weinsäure aus fossilen Produkten hat hingegen einen wesentlich niedrigeren bzw. fast zu vernachlässigenden 14 C -Gehalt. Durch die Messung der 14 C -Aktivität in dpm/g Kohlenstoff (decays per minute = Zerfälle pro Minute) durch Flüssigszintillationszählung können die Herkunft und jegliche Mischungen beider Formen ermittelt werden. 1
2 3. REAGENZIEN UND PRODUKTE 3.1 Reagenzien Szintillationsflüssigkeit, z. B. Instagel Plus C-Toluol, dessen Aktivität von einem Labor zertifiziert wurde, als Referenz zur Berechnung der Effizienz des Geräts und seines Wirkungsgrads durch Erstellen der Quenchkurve C-, 3 H-Standards und 12 C-Toluol zum Kalibrieren des Szintillationszählers bezüglich des Untergrundrauschens %iges Nitromethan ultrareines Wasser (> 18 MΩ) C-Toluollösung mit ca. 430 dpm/ml durch Verdünnen der 14 C-Standardstammlösung in 12 C- Toluol 3.2 Standards Erstellen der Quenchkurve Nach dem Kalibrieren des Szintillators mit jeweils zertifiziertem 14 C-, 3 H- und 12 C- Toluol die Quenchkurve gemäß folgendem Protokoll erstellen. Zwölf Kolben mit 10 ml einer Lösung mit 500 g/l fossiler L-Weinsäure in Wasser beschicken, anschließend soviel 14 C- Toluolstandard hinzugeben, dass man insgesamt auf dpm pro Kolben kommt (bei Bedarf eine Zwischenlösung der Standardlösung in Toluol vorbereiten). Zunächst steigende Konzentrationen Nitromethan, z. B. in 12 Reagenzgläsern 0, 0, 0, 5, 10, 15, 20, 35, 50, 100, 200 und 400 µl hinzugeben und anschließend 10 ml Szintillationsflüssigkeit. Mindestens 3 Proben müssen ohne Nitromethan bleiben. Die Quenchkurve einmal im Jahr erstellen und dazu die Reagenzgläser in der Reihenfolge zunehmenden Gehalts an Nitromethan analysieren. Mit der Quenchkurve kann man die Effizienz bzw. den durchschnittlichen Wirkungsgrad (Meaneff) ermitteln Bestimmung des Untergrundrauschens (Messung des Nulleffekts) Anhand von fossiler L-Weinsäure, z. B. der zur Berechnung des Wirkungsgrads verwendeten Weinsäure, das Untergrundrauschen ermitteln bzw. eine Messung des Nulleffekts durchführen. Diese Analyse muss unmittelbar nach der Quenchkurve erstellt werden und anschließend ungefähr einmal im Monat. 2
3 3.2.3 Erstellen der Kalibrierkurve Vor der Szintillationsmessung muss die Reinheit der fossilen und der pflanzlichen L- Weinsäure durch HPLC geprüft werden. Kalibrieren mit einer Mischung aus Weinsäure pflanzlichen Ursprungs (mit garantierter Herkunft) mit der fossilen Form zwischen 0 % und 100 %. Herstellen der Lösungen mit 500 g/l Nullmessung bzw. Untergrundrauschen Standards Kontrollmessung jeweils in 50 ml-messkolben Wiegen 25 g fossile L- 25 g bekannte Blindlösung Weinsäure Mischungen aus fossiler und pflanzlicher L- Weinsäure Auflösen verschließen Mischung gut durch Schütteln und/oder auf Kopf stellen homogenisieren Herstellen der Szintillationsmischungen In Kunststoffkolben jeweils hinzufügen Testbeginn ausgehend v. Lösungen mit 500 g/l 10 ml mit Hilfe von Messpipetten Zusatz ///////////////////////// ///////////////////////// 100 µl Zugabe 10 ml mit Hilfe eines Automaten Szintillationsflüssigkeit gut verschließen und stark schütteln 15 Min. warten und während 500 Min. analysieren 3.3 Kontrollmessung Art der für die Kontrollmessung verwendeten Substanz Eine fossile L-Weinsäurelösung mit 500 g/l wird mit 14 C Toluol (dpm < 100) dotiert. Die Bestimmung des Untergrundrauschens muss zusammen mit der gleichen fossilen L- Weinsäure vorgenommen werden Art der Kontrollmessung Durch die Kontrollmessung wird sichergestellt, dass im Untersuchungsmedium keine fremde Aktivität vorhanden ist. 3
4 3.3.3 Maximal zulässiger Nullwert Der maximal zulässige Nullwert hängt vom verwendeten Material ab, ein Wert von 5% ist annehmbar Häufigkeit und Verfahren der Nullwertmessung Bei normalem Gebrauch wird einmal im Monat bzw. bei jeder Analysenreihe eine Nullwertmessung am Szintillatinsmessgerät durchgeführt. Diese Kontrolle wird auch bei jedem Wechsel der Szintillationsflüssigkeit bzw. nach Erstellen einer neuen Quenchkurve durchgeführt Entscheidungsregeln in Abhängigkeit von den Ergebnissen der Nullwertmessung Wenn die Ergebnisse nach Überprüfen des Messprotokolls außerhalb der Kontrollgrenzen liegen, müssen eine Kalibrierung des Szintillatinsmessgerät und anschließend eine neue Kontrollmessung vorgenommen werden. Wenn die Kalibrierung richtig ist, die Messung der neuen Kontrollmessung hingegen nicht, eine neue Quenchkurve erstellen und erneut eine Kontrollmessung durchführen. 4. GERÄTE 4.1 Mehrkanal-Flüssigszintillationsspektrometer mit Rechner, Drucker und voreingestellter Kalibrierung der Auswerteeinheit, dessen Quenchkurve zum Beispiel mit Nitromethan ermittelt wurde 4.2 Kaliumarme Kolben ( 40 K) mit Schraubverschlüssen, mit schwachem und identischem Hintergrundrauschen ml-pipetten mit 2 Messstrichen 4.4 Automatische Bürette mit einer Gewindeverbindung, passend für die Scintillationsgefäße 4.5 Laborgläser 4
5 5. PROBEN Die Reinheit der Proben kann erforderlichenfalls vor der Analyse durch Szintillation per HPLC überprüft werden. In ultrareinem Wasser eine Lösung mit 500 g/l zu analysierender Probe herstellen. Herstellung der Lösungen mit 500 g/l Analytische Nullmessung bzw. Untergrundrauschen Standards Kontrollmessung Probe jeweils in 50 ml-messkolben Wiegen 25 g fossile L-) 25 g bekannte Nulllösung Weinsäure Mischungen aus verwenden fossiler und 25 g pflanzlicher L- Weinsäure Auflösen verschließen Mischung gut durch Schütteln und/oder auf Kopf stellen homogenisieren Herstellung der Szintillationsmischungen In Kunststoffkolben jeweils hinzufügen Testbeginn ausgehend v. Lösungen mit 500 g/l 10 ml mit Hilfe von Messpipetten Zusatz ///////////////////////// ///////////////////////// 100 µl ///////////////////////// Zugabe 10 ml mit Hilfe eines Automaten Szintillationsflüssigkeit gut verschließen und kräftig schütteln 15 Min. warten und während 500 Min. analysieren Anmerkungen Nach jeweils 5 bis 10 analysierten Proben eine Probe mit 0 % natürlicher Weinsäure, d. h. 10 ml fossile Weinsäure und 10 ml Szintillationsflüssigkeit verwenden. Am Ende jeder Analysereihe das Untergrundrauschen bestimmen. 6. BERECHNUNG Die Messungen werden direkt in Stöße pro Minute (cpm) angegeben, müssen aber in dpm/g Kohlenstoff umgerechnet werden. 6.1 Ergebnisse Berechnung der spezifischen 14 C-Aktivität der Probe in dpm/g Kohlenstoff: 5
6 A = ( X X' ) , ( 1) Rm m - A: Aktivität in Zerfälle/Minute und pro Gramm Kohlenstoff - X: Impulse pro Minute der Probe - X : cpm der für das Untergrundrauschen benutzten fossilen L-Weinsäure - m: Masse der Weinsäure in der 10 ml Lösung bei Testbeginn mit 500 g/l, d. h. 5 g Säure - Rm: entspricht dem durchschnittlichen Wirkungsgrad in Prozent (1) es sind 3,125 Gramm Weinsäure pro Gramm Kohlenstoff (Verhältnis des Molekulargewichts der Säure (150 g/mol) in Bezug auf die Gesamtmasse an Kohlenstoff (d. h. 4 * 12 = 48 g/mol) vorhanden. Das Ergebnis wird mit einer Dezimalstelle angegeben. 6.2 Überprüfung der Ergebnisse durch die Kontrollmessung Das Ergebnis muss durch den Vergleich des in Punkt 6.1 erhaltenen Werts mit dem Ergebnis aus dem Zusatz verglichen werden. Bei einer großen Differenz (> 5%) muss der Wert in dpm ausgehend vom Wert in cpm wie folgt neu berechnet werden: dpm korrigiert= cpm/ Rm mit einem durchschnittlichen Wirkungsgrad (Rm) ausgehend von der Quenchkurve. Die beiden Ergebnisse dürfen nicht um mehr als 5 % vom Durchschnittswert abweichen. Ansonsten muss die Probe erneut analysiert und dazu die Menge des Zusatzes verdoppelt werden. Die 2 erzielten Ergebnisse mit den Standards vergleichen. Wenn sie nicht um mehr als 5 % vom Mittelwert von einander abweichen, das durchschnittliche Ergebnis angeben. Anmerkung: Das bedeutet, in diesem Fall liegt ein solches Quenching der Probe vor, dass die direkte Analyse nicht verwendbar ist. 6.3 Unsicherheit Die bei unseren Analysebedingungen erreichte Unsicherheit beträgt ± 0,7 dpm/g Kohlenstoff. 6
7 7. VALIDIERUNG DURCH VERGLEICH MIT EINER REFERENZMETHODE 7.1 Prinzip Die Weinsäure wird durch einen Verbrennungsprozess in CO 2 und anschließend in Benzolumgewandelt. Die Messung erfolgt dann durch Flüssigszintillation. Nach einer Vorbehandlung zur Beseitigung von Verunreinigungen wird das CO 2 der Probe gemäß folgender Reaktionskette in Benzol umgewandelt: C + O 2 CO 2 (1) CaCO HCl CO 2 + H 2 O + Ca Cl - (2) 800 C 2 CO Li Li 2 C Li 2 O (3) Li 2 C H 2 O C 2 H LiOH (4) Al 2 O 3 mit Cr 3+ und V 3 C 2 H 2 C 6 H 6 (5) (1) Organische Probe: Der Kohlenstoff der Probe wird unter Sauerstoffspülung und Hitze (oder einer Verbrennung unter Sauerstoffdruck ) zu Kohlendioxid (CO 2 ) umgewandelt. (2) Mineralische Probe (Karbonate marinen, terrestrischen, oder aquatischen Ursprungs, usw.): Das Karbonat wird durch Salzsäure (HCl) in Kohlendioxid (CO 2 ), Wasser und Kalziumionen zersetzt. (3) Durch Reaktion des Kohlendioxids (CO 2 ) mit auf +600 C bis +800 C erhitztem Lithiummetall entsteht Lithiumcarbid (Li 2 C 2 )und Lithiumoxid (Li 2 O). (4) Die Hydrolyse von Lithiumcarbid mit Wasser ergibt Acetylen (C 2 H 2 ) und Lithiumhydroxid (LiOH). Es muss tritium- und radonfreies Wasser verwendet werden. (5) Die Trimerisation von Acetylen an einem Aluminiumkatalysator, der mit Chrom- Vanadium überzogenen ist, bei ca. 185 C ergibt Benzol (C 6 H 6 ). 7.2 Vorgehensweise: Das entweder nach Abbrennen, Verbrennen oder Säureangriff einer Probe erzielte Kohlendioxid (CO 2 ) wird in einem Gaszylinder aufbewahrt. Man gibt die nötige Menge Lithium ( = Katalysator in eine Nickelschale und stellt anschließend das Ganze auf den Boden eines Wärmereaktors. Man erzeugt im Reaktor ein Vakuum und erhitzt den unteren Bereich, wobei gleichzeitig der obere Bereich an der Wandung mit Wasser gekühlt wird. 7
8 7.2.1 Herstellung des Carbids Nach ca. einer Stunde Erhitzen erreicht die Temperatur ca. 650 C. Nun kann das CO 2 mit dem geschmolzenen Lithium zusammengebracht werden. Die Lithiummenge liegt im Vergleich zur Kohlenstoffmenge der Probe immer im Überschuss vor. Der in Bezug auf die stöchiometrischen Bedingungen zu verwendende Lithiumüberschuss variiert nach verschiedenen Literaturangaben zwischen 20 und 100 %. Die chemische Reaktion (Herstellung des Carbids oder Einfangen ) findet praktisch unmittelbar danach statt, sodass die ersten Minuten für die Reaktion entscheidend sind. Diese Reaktion ist exotherm (Temperaturanstieg um 200 C). Die Umsetzung erfolgt ziemlich schnell und ist bereits nach den ersten 20 Minuten abgeschlossen, während das Erhitzen noch weitere 45 bis 50 Minuten fortgesetzt wird, um Radonspuren (aus Uran), die eventuell im Kohlendioxid enthalten sein können, zu entfernen Abkühlen Nach Abschluss der Behandlung (Erhitzen) lässt man den Reaktor bis auf Raumtemperatur (25 30 C) abkühlen Hydrolyse des Lithiumcarbids Man gibt Wasser im Überschuss (1,5 l) in den Reaktor. Die chemische Reaktion findet sofort statt und gleichzeitig wird Acetylen freigesetzt. Auch diese Reaktion ist exotherm (Temperaturanstieg von +80 bis zu +100 C). Das entstandene Acetylen wird dann verdampft, um mit dem Aluminiumkatalysator mit Vanadium-Chrom (Cr 3+ ) in Kontakt zu treten. Dieser wird vorab mindestens drei Stunden lang luftgetrocknet und dann weitere zwei Stunden unter Vakuum und Erhitzen auf +380 C. Dies ist von größter Bedeutung, um das gesamte auf dem Katalysator verbliebene Wasser zu entfernen Trimerisation Katalytische Polymerisation von Acetylen zu Benzol Vor der Trimerisation muss die Temperatur des Katalysators wieder auf +60 bis +70 C abgefallen sein. Da diese Reaktion ebenfalls exotherm ist, wird diese Temperatur von alleine aufrechterhalten. Anschließend wird der Katalysator während 1,5 Stunden erneut auf +180 C erhitzt und das Benzol desorbiert, um in einer Röhre, die mit flüssigem Stickstoff umgeben ist, aufgefangen zu werden. Das Desorbieren erfolgt unter Vakuum. Am Ende des Versuchs lässt man das kristallisierte Benzol sich wieder auf Raumtemperatur erwärmen, damit es vor der Verwendung zur Szintillationsmessung seine flüssige Form zurück erhält. 8
9 7.3 Apparatur für die Synthese von Benzol Vorrat C 2 H 2 Vorrat CO 2 OFEN PUMPE PUMPE Wasserkreislauf zur Abkühlung HEIZREAKTOR AUFFANGEN DES BENZOLS OFEN 750 C 7.4 Referenzlösung für die Szintillationsmessung Als Referenz für die Flüssigszintillationszählung wird eine auf 4 ml festgelegte Menge Lösung verwendet. Diese Lösung enthält idealer Weise 3,52 g Benzol als Probe in der Szintillationsflüssigkeit, die aus einem primären und sekundären Szintillanten besteht. Es gilt, dass die Dichte von Benzol 0,88 g/liter beträgt, d.h. 0,88 X 4 ml = 3,52 g. 9
10 Primäre Szintillationsflüssigkeit Chemische Bezeichnung Maximale Fluoreszenzwellenlänge Sekundäre Szintillationsflüssigkeit Chemische Bezeichnung Fluoreszenzwellenlänge Optische Absorptions- und Emissionseigenschaften der beiden szintillierenden Stoffe: Wellenlänge der maximalen Absorption Wellenlänge der maximalen Emission Butyl-PBD (2-(4-Biphenylyl)-5-(4-Tert-Butyl- Phenyl)-1,3,4-Oxadiazol) 367 nm bis-msb 1,4-Di-(2-Methylstyryl)-Benzol 415 nm 409 nm 412 nm 7.5 Korrektur des Delta 13 C-Werts für die isotopische Fraktionierung Die Messung erfordert eine Korrektur für die Isotopenfraktionierung mit einem 13 C PDB Standard und einem Wert von -25 o / oo. 8. VERFAHRENSKENNZAHLEN DER METHODE 8.1 Durchführung Zur Herstellung der Weinsäuretestlösungen mit 500 g/l wurden eine Weinsäureprobe aus dem Weinbau und eine synthetische Weinsäureprobe verwendet. Der Gehalt an Weinsäure aus dem Weinbau in den Testlösungen variierte zwischen 0 % und 100 %. Herkunft und Reinheit der beiden Ausgangsproben wurden mit Hilfe der Referenzmethode geprüft. 10
11 8.2 Ergebnisse: Die Ergebnisse sind in der folgenden Tabelle und der Grafik aufgeführt: TATSÄCHLICHER GEHALT % WEINSÄURE AUS DEM WEINBAU ERGEBNISSE DER ERGEBNISSE DER ALTERNATIVEN REFERENZMETHODE METHODE 0 0 und ,5 und 6, ,4 und ,6 und 25, ,7 und ,4 und 50, ,8 und 58, und 63,
12 Activité Aktivität du Kohlenstoff carbone (in dpm/g Kohlenstoff) (en dpm/g de C) Alternative Methode C 14 -Aktivität entsprechend Gehalt an fossiler (L+) Weinsäure Méthode Alternative Activité C 14 en fonction de la teneur en acide tartrique (L+) fossile y = 0,159x + 0,2543 R 2 = 0,9917 % natürliche Weinsäure % de l'acide tartrique naturel 8.3 Genauigkeit, Präzision Die Genauigkeit beträgt 6,9 %. Die Standardabweichung für die Wiederholbarkeit der Alternativmethode beträgt 2,86 % pflanzliche Weinsäure. 9. LITERATUR Sammlung der internationalen Methoden zur Analyse von Spirituosen, Alkohol und des aromatischen Anteils der Getränke, Internationale Organisation für Rebe und Wein, offizielle Ausgabe, Juni 1994, Seite 201, 204, 210 und 307. EG-Analysemethoden für neutralen Alkohol, geltend für den Weinbereich, Verordnung der Kommission (EG) Nr. 625/2003 vom 02. April 2003 (ABl. Nr. L90 S.4 vom )] J. GUERAIN et S. TOURLIERE, Radioactivité carbone et tritium dans les alcools, Industries Alimentaires et Agricoles 92. Jahrgang, Juli - August 1975, Nr. 7-8 S. COHEN, B. CRESTO, S. NACHAMPASSAK, T. PAYOT, B. MEDINA, S. CHAUVET, Détermination de l origine de l acide tartrique L(+): naturelle ou fossile par la détermination de son activité C 14 - Document OIV FV 1238,
RESOLUTION OENO 20/2004
 ZUCKERCOULEUR DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf 2 IV des Gründungsübereinkommens vom 3. April 2001 der Internationalen Organisation für Rebe und Wein auf Vorschlag der Unterkommission
ZUCKERCOULEUR DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf 2 IV des Gründungsübereinkommens vom 3. April 2001 der Internationalen Organisation für Rebe und Wein auf Vorschlag der Unterkommission
BESTIMMUNG DER FÄHIGKEIT EINES ENZYMPRÄPARATS, PEKTINKETTEN ZU TRENNEN MITTELS VISKOSITÄTSMESSUNG
 RESOLUTION OIV/OENO 351/2009 BESTIMMUNG DER FÄHIGKEIT EINES ENZYMPRÄPARATS, PEKTINKETTEN ZU TRENNEN MITTELS VISKOSITÄTSMESSUNG DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf 2 IV des
RESOLUTION OIV/OENO 351/2009 BESTIMMUNG DER FÄHIGKEIT EINES ENZYMPRÄPARATS, PEKTINKETTEN ZU TRENNEN MITTELS VISKOSITÄTSMESSUNG DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf 2 IV des
RESOLUTION OIV-OENO gestützt auf die Arbeiten der Expertengruppen Spezifikationen önologischer Erzeugnisse und Mikrobiologie
 RESOLUTION OIV-OENO 496-2013 MONOGRAPHIE ÜBER HEFEAUTOLYSATE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz iv des Übereinkommens vom 3. April 2001 zur Gründung der Internationalen Organisation
RESOLUTION OIV-OENO 496-2013 MONOGRAPHIE ÜBER HEFEAUTOLYSATE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz iv des Übereinkommens vom 3. April 2001 zur Gründung der Internationalen Organisation
SIMULTANER NACHWEIS VON L-ASCORBINSÄURE UND D-ISOASCORBINSÄURE (ERYTHROBINSÄURE ) IN WEIN DURCH HPLC UND UV-DETEKTION
 RESOLUTION OENO 11/008 SIMULTANER NACHWEIS VON L-ASCORBINSÄURE UND D-ISOASCORBINSÄURE (ERYTHROBINSÄURE ) IN WEIN DURCH HPLC UND UV-DETEKTION Die GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel, Paragraf
RESOLUTION OENO 11/008 SIMULTANER NACHWEIS VON L-ASCORBINSÄURE UND D-ISOASCORBINSÄURE (ERYTHROBINSÄURE ) IN WEIN DURCH HPLC UND UV-DETEKTION Die GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel, Paragraf
RESOLUTION OIV-OENO ANALYSE FLÜCHTIGER VERBINDUNGEN IN WEIN MITTELS GASCHROMATOGRAPHIE
 RESOLUTION OIV-OENO 553-2016 ANALYSE FLÜCHTIGER VERBINDUNGEN IN WEIN MITTELS GASCHROMATOGRAPHIE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz 2 iv des Übereinkommens vom 3. April 2001 zur Gründung
RESOLUTION OIV-OENO 553-2016 ANALYSE FLÜCHTIGER VERBINDUNGEN IN WEIN MITTELS GASCHROMATOGRAPHIE DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz 2 iv des Übereinkommens vom 3. April 2001 zur Gründung
RESOLUTION OIV/OENO 427/2010 KRITERIEN FÜR METHODEN ZUR QUANTIFIZIERUNG VON POTENTIELL ALLERGENEN RÜCKSTÄNDEN EIWEISSHALTIGER SCHÖNUNGSMITTEL IM WEIN
 RESOLUTION OIV/OENO 427/2010 KRITERIEN FÜR METHODEN ZUR QUANTIFIZIERUNG VON POTENTIELL ALLERGENEN RÜCKSTÄNDEN EIWEISSHALTIGER SCHÖNUNGSMITTEL IM WEIN Die GENERALVERSAMMLUNG, unter Berücksichtigung des
RESOLUTION OIV/OENO 427/2010 KRITERIEN FÜR METHODEN ZUR QUANTIFIZIERUNG VON POTENTIELL ALLERGENEN RÜCKSTÄNDEN EIWEISSHALTIGER SCHÖNUNGSMITTEL IM WEIN Die GENERALVERSAMMLUNG, unter Berücksichtigung des
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Versuch 6
 Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 6 Herstellung einer Titerbestimmung von 500mL einer Salzsäure Maßlösung mit der Äquivalentkonzentration c(hcl) = 0,1 mol/l Fachbereich MT 1 Wintersemester
Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 6 Herstellung einer Titerbestimmung von 500mL einer Salzsäure Maßlösung mit der Äquivalentkonzentration c(hcl) = 0,1 mol/l Fachbereich MT 1 Wintersemester
RESOLUTION OENO 33/2004 BESTIMMUNG VON SHIKIMISÄURE IN WEIN MITTELS HPLC UND UV-DETEKTION
 BESTIMMUNG VON SHIKIMISÄURE IN WEIN MITTELS HPLC UND UV-DETEKTION DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel, Paragraf IV des Gründungsübereinkommens der Internationalen Organisation für Rebe
BESTIMMUNG VON SHIKIMISÄURE IN WEIN MITTELS HPLC UND UV-DETEKTION DIE GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel, Paragraf IV des Gründungsübereinkommens der Internationalen Organisation für Rebe
RESOLUTION OIV-OENO
 RESOLUTION OIV-OENO 506-2016 MONOGRAPHIE ÜBER SELEKTIVE ZEOLITHE (FAUJASIT) DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz 2 iv des Übereinkommens vom 3. April 2001 zur Gründung der Internationalen
RESOLUTION OIV-OENO 506-2016 MONOGRAPHIE ÜBER SELEKTIVE ZEOLITHE (FAUJASIT) DIE GENERALVERSAMMLUNG, gestützt auf Artikel 2 Absatz 2 iv des Übereinkommens vom 3. April 2001 zur Gründung der Internationalen
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
LEE2: 2. Messung der Molrefraktion der Flüssigkeiten für die Bestimmung der Qualität des Rohmaterials
 ŠPŠCH Brno Erarbeitung berufspädagogischer Konzepte für die beruflichen Handlungsfelder Arbeiten im Chemielabor und Operator Angewandte Chemie und Lebensmittelanalyse LEE2: 2. Messung der Molrefraktion
ŠPŠCH Brno Erarbeitung berufspädagogischer Konzepte für die beruflichen Handlungsfelder Arbeiten im Chemielabor und Operator Angewandte Chemie und Lebensmittelanalyse LEE2: 2. Messung der Molrefraktion
RESOLUTION OIV-OENO
 RESOLUTION OIV-OENO 552-2016 BESTIMMUNG VON ZUCKERN IN MOST UND WEIN MITTELS HOCHLEISTUNGSFLÜSSIGKEITSCHROMATOGRAPHIE - AKTUALISIERUNG DER METHODE OIV-MA- AS311-03 DIE GENERALVERSAMMLUNG, gestützt auf
RESOLUTION OIV-OENO 552-2016 BESTIMMUNG VON ZUCKERN IN MOST UND WEIN MITTELS HOCHLEISTUNGSFLÜSSIGKEITSCHROMATOGRAPHIE - AKTUALISIERUNG DER METHODE OIV-MA- AS311-03 DIE GENERALVERSAMMLUNG, gestützt auf
METHODE ZUR BESTIMMUNG DER α-dicarbonylverbindungen IM WEIN DURCH HPLC NACH DERIVATISIERUNG MIT 1,2-DIAMINOBENZOL
 RESOLUTION OIV/OENO 386A/2010 METHODE ZUR BESTIMMUNG DER α-dicarbonylverbindungen IM WEIN DURCH HPLC NACH DERIVATISIERUNG MIT 1,2-DIAMINOBENZOL Die GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf
RESOLUTION OIV/OENO 386A/2010 METHODE ZUR BESTIMMUNG DER α-dicarbonylverbindungen IM WEIN DURCH HPLC NACH DERIVATISIERUNG MIT 1,2-DIAMINOBENZOL Die GENERALVERSAMMLUNG, unter Bezugnahme auf Artikel 2, Paragraf
Versuch 1: Extraktion von ß-Carotin aus Lebensmitteln
 Name Datum Versuch 1: Extraktion von aus Lebensmitteln Geräte: 4 Reagenzgläser, 4 Gummistopfen, Reagenzglasständer, 1 Erlenmeyerkolben mit Stopfen, Messer, Mörser, Spatel, Messpipette, 1 kleine Petrischale,
Name Datum Versuch 1: Extraktion von aus Lebensmitteln Geräte: 4 Reagenzgläser, 4 Gummistopfen, Reagenzglasständer, 1 Erlenmeyerkolben mit Stopfen, Messer, Mörser, Spatel, Messpipette, 1 kleine Petrischale,
Einfache DOC- und TOC-Bestimmung im Abwasser
 Vollzug Umwelt MITTEILUNGEN ZUM GEWÄSSERSCHUTZ NR. 28 Einfache DOC- und TOC-Bestimmung im Abwasser Bundesamt für Umwelt, Wald und Landschaft BUWAL Herausgeber Bundesamt für Umwelt, Wald und Landschaft
Vollzug Umwelt MITTEILUNGEN ZUM GEWÄSSERSCHUTZ NR. 28 Einfache DOC- und TOC-Bestimmung im Abwasser Bundesamt für Umwelt, Wald und Landschaft BUWAL Herausgeber Bundesamt für Umwelt, Wald und Landschaft
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion:
 Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Standardabweichung und Variationskoeffizient. Themen. Prinzip. Material TEAS Qualitätskontrolle, Standardabweichung, Variationskoeffizient.
 Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Übungsaufgaben Chemie Nr. 3
 Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie
 Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Text Anlage. Heparin-Calcium
 Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Metrologie = Wissenschaft vom Messen. Messunsicherheit von Analysenergebnissen. VU Chemisch Rechnen
 Metrologie = Wissenschaft vom Messen Messunsicherheit von Analysenergebnissen Wer mißt, mißt Mist!! Metrologie Meteorologie Kräht der Hahn am Mist, Ändert sich das Wetter oder es bleibt, wie es ist!! Inhalt
Metrologie = Wissenschaft vom Messen Messunsicherheit von Analysenergebnissen Wer mißt, mißt Mist!! Metrologie Meteorologie Kräht der Hahn am Mist, Ändert sich das Wetter oder es bleibt, wie es ist!! Inhalt
Typische Fragen für den Gehschul-Teil: Typ 1: Mengen und Konzentrationen:
 Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Aus organisatorischen Gründen wird dieser Test gleichzeitig mit der Prüfung aus Grundlagen der Biochemie angeboten. Das Abschneiden
Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Aus organisatorischen Gründen wird dieser Test gleichzeitig mit der Prüfung aus Grundlagen der Biochemie angeboten. Das Abschneiden
Katalysator vor und nach der Reaktion
 Katalysator vor und nach der Reaktion Braunstein als Katalysator bei der Zersetzung von Wasserstoffperoxid Wasserstoffperoxid ist wenig stabil und zerfällt leicht. Dabei entsteht Sauerstoff, der mit Hilfe
Katalysator vor und nach der Reaktion Braunstein als Katalysator bei der Zersetzung von Wasserstoffperoxid Wasserstoffperoxid ist wenig stabil und zerfällt leicht. Dabei entsteht Sauerstoff, der mit Hilfe
Versuch 03: Enzyme. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
 Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
Bestimmung des Stickstoffgehalts von Erde
 Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
AnC I Protokoll: 6.1 Extraktionsphotometrische Bestimmung von Cobalt mit HDEHP! SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie. Allgemeine Chemie. Rückblick auf vorherige Übung
 Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan
 Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Ansatzwerte: SurTec 691 I Ansatzlösung 8 Vol% (7-9 Vol%) SurTec 691 II Ansatzadditiv 2 Vol% (1,5-3 Vol%)
 SurTec 691 Schwarzpassivierung für alkalische Zinküberzüge Eigenschaften Chrom(VI)-freie Schwarzpassivierung auf Basis von dreiwertigem Chrom speziell entwickelt für die Beschichtung von Massenware erzeugt
SurTec 691 Schwarzpassivierung für alkalische Zinküberzüge Eigenschaften Chrom(VI)-freie Schwarzpassivierung auf Basis von dreiwertigem Chrom speziell entwickelt für die Beschichtung von Massenware erzeugt
3.5 Hydrolyse von Salzen. Aufgabe. Reagieren wässrige Salzlösungen neutral? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Probe und Probenmenge Wassermenge Auftragspuffermenge 5 µl Kaninchenmuskelextrakt 50 µl 100 µl
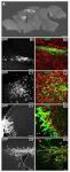
 Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
Arbeitsgruppe D 6 Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs 3: Proteinanalysen Im heutigen Kurs extrahierten wir zum einen Proteine aus verschiedenen Geweben eines Kaninchens und führten
Bradford Reagent, 5x
 GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Bradford Reagent, 5x Reagenz für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39222) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 HeidelbergPhone +49-6221-138400, Fax +49-6221-1384010
SingleQuant Assay Kit
 GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG SingleQuant Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39226) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
Liebigkühler. Rundkolben Vorstoß. Becherglas
 Die Destillation 1 1 Allgemeines Bei der Destillation werden Stoffe mit unterschiedlichen Siedetemperaturen durch Erhitzen voneinander getrennt. Aus Rotwein kann auf diese Weise der Alkohol (Ethanol, Sdp.
Die Destillation 1 1 Allgemeines Bei der Destillation werden Stoffe mit unterschiedlichen Siedetemperaturen durch Erhitzen voneinander getrennt. Aus Rotwein kann auf diese Weise der Alkohol (Ethanol, Sdp.
AnC I Protokoll: 3.4 Iodometrische Bestimmung von Ascorbinsäure (Vitamin C)" SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 3.4 Iodometrische Bestimmung von Ascorbinsäure (Vitamin C) 1.! Theoretischer Hintergrund Bei dieser Redoxtitration wird Ascorbinsäure mit Hilfe von Triiodid oxidiert.
Analytische Chemie I Versuchsprotokoll 3.4 Iodometrische Bestimmung von Ascorbinsäure (Vitamin C) 1.! Theoretischer Hintergrund Bei dieser Redoxtitration wird Ascorbinsäure mit Hilfe von Triiodid oxidiert.
Kurztitel. Kundmachungsorgan. /Artikel/Anlage. Inkrafttretensdatum. Text. Bundesrecht. Kosmetik - Analysenverordnung
 Kurztitel Kosmetik - Analysenverordnung Kundmachungsorgan BGBl. Nr. 95/1995 zuletzt geändert durch BGBl. Nr. 546/1996 /Artikel/Anlage Anl. 37 Inkrafttretensdatum 09.10.1996 Text Anlage 37 -------------
Kurztitel Kosmetik - Analysenverordnung Kundmachungsorgan BGBl. Nr. 95/1995 zuletzt geändert durch BGBl. Nr. 546/1996 /Artikel/Anlage Anl. 37 Inkrafttretensdatum 09.10.1996 Text Anlage 37 -------------
RICHTLINIE 1999/4/EG DES EUROPÄISCHEN PARLAMENTS UND DES RATES vom 22. Februar 1999 über Kaffee- und Zichorien-Extrakte
 1999L0004 DE 18.11.2013 003.001 1 Dieses Dokument ist lediglich eine Dokumentationshilfe, für deren Richtigkeit die Organe der Union keine Gewähr übernehmen B RICHTLINIE 1999/4/EG DES EUROPÄISCHEN PARLAMENTS
1999L0004 DE 18.11.2013 003.001 1 Dieses Dokument ist lediglich eine Dokumentationshilfe, für deren Richtigkeit die Organe der Union keine Gewähr übernehmen B RICHTLINIE 1999/4/EG DES EUROPÄISCHEN PARLAMENTS
Tritium und Radiokohlenstoff in der Umwelt
 in der Umwelt Roland Tesch, Rudolf Engelbrecht H-3 natürliches Isotop des Wasserstoffs niederenerg. - -Emitter E max = 18,6 kev T ½ = 4500 ± 8 Tage 1 TU = 1100 10-19 mol/g = 0,119 Bq/L natürliches Isotop
in der Umwelt Roland Tesch, Rudolf Engelbrecht H-3 natürliches Isotop des Wasserstoffs niederenerg. - -Emitter E max = 18,6 kev T ½ = 4500 ± 8 Tage 1 TU = 1100 10-19 mol/g = 0,119 Bq/L natürliches Isotop
Was haben wir gelernt?
 Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Gruppe I : Darstellung und Nachweis von Säuren
 Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 2,
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau
 Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Präzision in der Analytik Ein unentbehrlicher Teil der Methodenvalidierung
 Abacus Validation Systems Präzision in der Analytik Ein unentbehrlicher Teil der Methodenvalidierung Joachim Pum, MMed (Univ. Pretoria) 2008 Definition Präzision ist das Maß für die Streuung von Analysenergebnissen
Abacus Validation Systems Präzision in der Analytik Ein unentbehrlicher Teil der Methodenvalidierung Joachim Pum, MMed (Univ. Pretoria) 2008 Definition Präzision ist das Maß für die Streuung von Analysenergebnissen
¾ Kb / A. Analyse von Bier
 Analyse von Bier Zielsetzung: Bestimmung des Aschegehalts, des Dichte - und Alkohol- und Maltosegehaltes, des ph-wertes, der flüchtigen Säure sowie der Extrakte und Stammwürze durch jene im Schweizer Lebensmittelbuch
Analyse von Bier Zielsetzung: Bestimmung des Aschegehalts, des Dichte - und Alkohol- und Maltosegehaltes, des ph-wertes, der flüchtigen Säure sowie der Extrakte und Stammwürze durch jene im Schweizer Lebensmittelbuch
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Ist der Aufschluss für eine Gesamtphosphatbestimmung auch im Hochtemperaturthermostat (HT) möglich?
 FAQ Laboranalytik Chemie Parameter Phosphat Was bedeutet in der Formel PO4 P der Buchstabe P? Ist eine Berechnung von PO4 ( Phosphat Phosphor) nach PO4 3- ( Phosphat) möglich? Gesamt- oder Orthophosphat?
FAQ Laboranalytik Chemie Parameter Phosphat Was bedeutet in der Formel PO4 P der Buchstabe P? Ist eine Berechnung von PO4 ( Phosphat Phosphor) nach PO4 3- ( Phosphat) möglich? Gesamt- oder Orthophosphat?
Leonardo da Vinci Innovationstransferprojekt TraWi. Projektnummer: DE/13/LLP-LdV/TOI/147629
 ŠPŠCH Pardubice Erarbeitung berufspädagogischer Konzepte für das berufliche Handlungsfeld Operator Chemist operator LEE 2b: 2. ph-wert-bestimmung Sie sind chemischer Operator in einem chemischen Betrieb,
ŠPŠCH Pardubice Erarbeitung berufspädagogischer Konzepte für das berufliche Handlungsfeld Operator Chemist operator LEE 2b: 2. ph-wert-bestimmung Sie sind chemischer Operator in einem chemischen Betrieb,
Vergleich verschiedener Verfahren zur Bestimmung der schwefligen Säure
 Vergleich verschiedener Verfahren zur Bestimmung der schwefligen Säure Dr. Martin Pour Nikfardjam Staatliche Lehr- u. Versuchsanstalt für Wein- u. Obstbau Weinsberg Dr. Martin Pour Nikfardjam Inhalt Möglichkeiten
Vergleich verschiedener Verfahren zur Bestimmung der schwefligen Säure Dr. Martin Pour Nikfardjam Staatliche Lehr- u. Versuchsanstalt für Wein- u. Obstbau Weinsberg Dr. Martin Pour Nikfardjam Inhalt Möglichkeiten
Anhang C Jährliche Überprüfung der Vorgaben
 Anhang C Jährliche Überprüfung der Vorgaben Verfahren und Softwareanforderungen zur Auswahl der Vorgabenstammblätter, die zur jährlichen Überprüfung der Vorgaben anstehen. Für allgemeine (grundlegende)
Anhang C Jährliche Überprüfung der Vorgaben Verfahren und Softwareanforderungen zur Auswahl der Vorgabenstammblätter, die zur jährlichen Überprüfung der Vorgaben anstehen. Für allgemeine (grundlegende)
Merkblatt für die ökologische Weinbereitung
 Merkblatt für die ökologische Weinbereitung Herausgegeben von der Gesellschaft für Ressourcenschutz mbh Nr. 20: Regelungen zur Herstellung von Bio-Wein Mit der Verordnung (EU) Nr. 203/2012 vom 08. März
Merkblatt für die ökologische Weinbereitung Herausgegeben von der Gesellschaft für Ressourcenschutz mbh Nr. 20: Regelungen zur Herstellung von Bio-Wein Mit der Verordnung (EU) Nr. 203/2012 vom 08. März
Versuch: Siedediagramm eines binären Gemisches
 Versuch: Siedediagramm eines binären Gemisches Aufgaben - Kalibriermessungen Bestimmen Sie experimentell den Brechungsindex einer gegebenen Mischung bei unterschiedlicher Zusammensetzung. - Theoretische
Versuch: Siedediagramm eines binären Gemisches Aufgaben - Kalibriermessungen Bestimmen Sie experimentell den Brechungsindex einer gegebenen Mischung bei unterschiedlicher Zusammensetzung. - Theoretische
Verbrennungstechnik. 1. Brennstoffe. 1.Brennstoffe. 2.Heizwert. 2.1 Oberer Heizwert 2.2 Unterer Heizwert. 3.Verbrennungsvorgang
 Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
Reaktion von Marmor mit Salzsäure (Reaktionskinetik)
 Prinzip Marmor reagiert mit Salzsäure. Das dabei entweichende Kohlenstoffdioxid führt zu einem Massenverlust, der über eine bestimmte Zeit verfolgt und unter reaktionskinetischen Aspekten ausgewertet wird.
Prinzip Marmor reagiert mit Salzsäure. Das dabei entweichende Kohlenstoffdioxid führt zu einem Massenverlust, der über eine bestimmte Zeit verfolgt und unter reaktionskinetischen Aspekten ausgewertet wird.
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Protokoll Grundpraktikum I: T6 Thermoelement und newtonsches Abkühlungsgesetz
 Protokoll Grundpraktikum I: T6 Thermoelement und newtonsches Abkühlungsgesetz Sebastian Pfitzner 5. Juni 03 Durchführung: Sebastian Pfitzner (553983), Anna Andrle (55077) Arbeitsplatz: Platz 3 Betreuer:
Protokoll Grundpraktikum I: T6 Thermoelement und newtonsches Abkühlungsgesetz Sebastian Pfitzner 5. Juni 03 Durchführung: Sebastian Pfitzner (553983), Anna Andrle (55077) Arbeitsplatz: Platz 3 Betreuer:
Verbrennungsrechnung als kinetischer Simulationsansatz
 Verbrennungsrechnung als kinetischer Simulationsansatz Simulationsansatz mit CHEMCAD Die Daten für Flammpunkt, Zündtemperatur, Explosionsgrenzen diverser Stoffe sind weitestgehend bekannt. Methoden zur
Verbrennungsrechnung als kinetischer Simulationsansatz Simulationsansatz mit CHEMCAD Die Daten für Flammpunkt, Zündtemperatur, Explosionsgrenzen diverser Stoffe sind weitestgehend bekannt. Methoden zur
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Ammoniaksynthese nach Haber-Bosch
 Sarah Kiefer, Thomas Richter Ammoniaksynthese nach Haber-Bosch 1. Allgemeine Einführung 2. Chemisches Grundprinzip 3. Industrielle Umsetzung 4. Anwendung und Auswirkungen 1. Allgemeine Einführung Steckbrief:
Sarah Kiefer, Thomas Richter Ammoniaksynthese nach Haber-Bosch 1. Allgemeine Einführung 2. Chemisches Grundprinzip 3. Industrielle Umsetzung 4. Anwendung und Auswirkungen 1. Allgemeine Einführung Steckbrief:
Für enzymkinetische Untersuchungen legen Sie 0.2 ml einer 5 mm Substratlösung vor. Der fertige Inkubationsansatz hat ein Volumen von 2 ml.
 Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
Die Gehschule ist ein Teil der Biochemischen Übungen für das Bakkalaureat LMBT. Der Test wird im Anschluss an die Prüfung aus Grundlagen der Biochemie angeboten, welche 90 min dauert (also bei der Türe
Versuch 412: Photometrische Bestimmung von Phosphatspuren als "Phosphormolybdänblau"
 Instrumentelle Bestimmungsverfahren 131 Versuch 412: Photometrische Bestimmung von Phosphatspuren als "Phosphormolybdänblau" Phosphationen reagieren mit Molybdat MoO 4 in saurer Lösung zur 2 gelben Dodekamolybdatophosphorsäure
Instrumentelle Bestimmungsverfahren 131 Versuch 412: Photometrische Bestimmung von Phosphatspuren als "Phosphormolybdänblau" Phosphationen reagieren mit Molybdat MoO 4 in saurer Lösung zur 2 gelben Dodekamolybdatophosphorsäure
. = Standardabweichung, berechnet aus Ergebnissen, die unter Vergleichsbedingungen erhalten worden sind.
 RESOLUTION OIV/OENO 427/2010 Geändert Durch OIV-COMEX 502-2012 1 Definitionen der Verfahrenskriterien Richtigkeit r = Grad der Übereinstimmung zwischen dem aus einer großen Serie von Testergebnissen erhaltenen
RESOLUTION OIV/OENO 427/2010 Geändert Durch OIV-COMEX 502-2012 1 Definitionen der Verfahrenskriterien Richtigkeit r = Grad der Übereinstimmung zwischen dem aus einer großen Serie von Testergebnissen erhaltenen
Online Projektlabor Chemie. Durchführung für die Spurenanalytik in Wasser
 Online Projektlabor Chemie Technische Universität Berlin Durchführung für die Spurenanalytik in Wasser Leitung des Projektlabores: Prof. Dr. Th. Friedrich Ersteller des Dokumentes: Daniel Christian Brüggemann
Online Projektlabor Chemie Technische Universität Berlin Durchführung für die Spurenanalytik in Wasser Leitung des Projektlabores: Prof. Dr. Th. Friedrich Ersteller des Dokumentes: Daniel Christian Brüggemann
8. Simultane UV/VIS-Zweikomponentenanalyse
 Simultane UV/VIS-Zweikomponentenanalyse 89 8. Simultane UV/VIS-Zweikomponentenanalyse Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb
Simultane UV/VIS-Zweikomponentenanalyse 89 8. Simultane UV/VIS-Zweikomponentenanalyse Einleitung Polycyclische Aromaten treten als Begleiter des bei der Verbrennung entstehenden Rußes, z. B. beim Betrieb
Arbeitskreis Kappenberg Reaktion von Marmor mit Salzsäure H 02 Computer im Chemieunterricht (Reaktionskinetik) Gravimetrie
 Computer im Chemieunterricht (Reaktionskinetik) Gravimetrie Prinzip: Marmor reagiert mit Salzsäure. Das dabei entweichende Kohlenstoffdioxid führt zu einem Massenverlust, der über eine bestimmte Zeit verfolgt
Computer im Chemieunterricht (Reaktionskinetik) Gravimetrie Prinzip: Marmor reagiert mit Salzsäure. Das dabei entweichende Kohlenstoffdioxid führt zu einem Massenverlust, der über eine bestimmte Zeit verfolgt
Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen.
 1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2009/10 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2009/10 vom 18.09.2009 A1 A2 A3 A4 A5 Σ Note 10 10 10 10 10 NAME:... VORNAME:...MUSTERLÖSUNG... Pseudonym für Ergebnisveröffentlichung:... Schreiben
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2009/10 vom 18.09.2009 A1 A2 A3 A4 A5 Σ Note 10 10 10 10 10 NAME:... VORNAME:...MUSTERLÖSUNG... Pseudonym für Ergebnisveröffentlichung:... Schreiben
!!! NEUE ÖAB-MONOGRAPHIE!!!
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende neue Monographie ist für die Aufnahme in das ÖAB (österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.05.2014 an folgende
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende neue Monographie ist für die Aufnahme in das ÖAB (österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.05.2014 an folgende
2. Teilklausur zum Chemischen Grundpraktikum im WS 2015/16 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2015/16 vom 20.01.2016 A1 A2 A3 F4 R5 E6 Note 10 9 6 8 9 8 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben Sie
2. Teilklausur zum Chemischen Grundpraktikum im WS 2015/16 vom 20.01.2016 A1 A2 A3 F4 R5 E6 Note 10 9 6 8 9 8 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben Sie
Wasser à. Nachweis: Wasser ist
 Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Hopfen. 3. Lëtzebuerger Naturwëssenschaftsolympiad. Finalrunde: Donnerstag, den 28. Januar 2010. und Malz... Antwortbogen
 3. Lëtzebuerger Naturwëssenschaftsolympiad Finalrunde: Donnerstag, den 28. Januar 2010 Lycée Michel-Rodange, Luxembourg Hopfen und Malz... Antwortbogen Versuch I: Beobachtung von Hefe unter dem Mikroskop
3. Lëtzebuerger Naturwëssenschaftsolympiad Finalrunde: Donnerstag, den 28. Januar 2010 Lycée Michel-Rodange, Luxembourg Hopfen und Malz... Antwortbogen Versuch I: Beobachtung von Hefe unter dem Mikroskop
Klausur : Allgemeine und Anorganische Chemie. Name...Fachrichtung... Matr.-Nr...
 Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
Experimente mit Brausetabletten
 Experimente mit Brausetabletten Beim Auflösen von Brausetabletten reagiert Natriumhydrogencarbonat NaHCO 3 mit der ebenfalls in der Tablette enthaltener Säure (meist Wein- oder Citronensäure; allgemein
Experimente mit Brausetabletten Beim Auflösen von Brausetabletten reagiert Natriumhydrogencarbonat NaHCO 3 mit der ebenfalls in der Tablette enthaltener Säure (meist Wein- oder Citronensäure; allgemein
Synthese von tert-butylchlorid (2-Chloro-2-methylpropan)
 Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Lösung Sauerstoff: 1s 2 2s 2 2p 4, Bor: 1s 2 2s 2 2p 1, Chlor: 1s 2 2s 2 2p 6 3s 2 3p 5 Neon: 1s 2 2s 2 2p 6
 1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
Chemie mit Signalwirkung: Fluoreszenzfarbstoffe
 Schlussbericht Studienwoche Forschen in der Chemie 2012 Autorin: Firma: Betreuer: Clariant Produkte (Schweiz) AG Dr. Ulrich Geiger Chemie mit Signalwirkung: Fluoreszenzfarbstoffe Fragestellung und Ziel
Schlussbericht Studienwoche Forschen in der Chemie 2012 Autorin: Firma: Betreuer: Clariant Produkte (Schweiz) AG Dr. Ulrich Geiger Chemie mit Signalwirkung: Fluoreszenzfarbstoffe Fragestellung und Ziel
Praktikum Physik. Protokoll zum Versuch 5: Spezifische Wärme. Durchgeführt am Gruppe X
 Praktikum Physik Protokoll zum Versuch 5: Spezifische Wärme Durchgeführt am 10.11.2011 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
Praktikum Physik Protokoll zum Versuch 5: Spezifische Wärme Durchgeführt am 10.11.2011 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
AWA Amt für Wasser und Abfall. OED Office des eaux et des déchets
 OED Office des eaux et des déchets 1 1 Aufschlüsse von wässrigen Proben Basel, 17.11.2010 R. Ryser, Fachbereichsleiter Anorganische Umweltanalytik 2 Aufbau des Referates Gesetzliche Anforderungen betreffend
OED Office des eaux et des déchets 1 1 Aufschlüsse von wässrigen Proben Basel, 17.11.2010 R. Ryser, Fachbereichsleiter Anorganische Umweltanalytik 2 Aufbau des Referates Gesetzliche Anforderungen betreffend
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
5- HYDROXYMETHYL-2-FURANSÄURE ERARBEITUNG EINES MODELLSYSTEMS ZUR BILDUNG IN GERÖSTETEM KAFFEE. T. Golubkova, M. Murkovic
 5- HYDROXYMETHYL-2-FURANSÄURE ERARBEITUNG EINES MODELLSYSTEMS ZUR BILDUNG IN GERÖSTETEM KAFFEE T. Golubkova, M. Murkovic Institut für Biochemie Technische Universität, Graz, Österreich Einleitung Während
5- HYDROXYMETHYL-2-FURANSÄURE ERARBEITUNG EINES MODELLSYSTEMS ZUR BILDUNG IN GERÖSTETEM KAFFEE T. Golubkova, M. Murkovic Institut für Biochemie Technische Universität, Graz, Österreich Einleitung Während
Reaktionsgleichungen und was dahinter steckt
 Reaktionsgleichungen und was dahinter steckt Prinzipien Bestehende Formeln dürfen nicht verändert werden. Bei Redoxreaktionen kann H, OH oder H 2 O ergänzt werden. Links und rechts vom Reaktionspfeil muss
Reaktionsgleichungen und was dahinter steckt Prinzipien Bestehende Formeln dürfen nicht verändert werden. Bei Redoxreaktionen kann H, OH oder H 2 O ergänzt werden. Links und rechts vom Reaktionspfeil muss
Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 (MOL)
 Seite 1 Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 1 Literatur W. Walcher, Praktikum der Physik, Teubner Themengebiet: Thermodynamik Bundesanstalt für Arbeitsschutz und
Seite 1 Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 1 Literatur W. Walcher, Praktikum der Physik, Teubner Themengebiet: Thermodynamik Bundesanstalt für Arbeitsschutz und
7. Woche. Gesamtanalyse (Vollanalyse) einfacher Salze. Qualitative Analyse anorganischer Verbindungen
 7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
Bereiten Sie bitte die folgenden Fragen für die Vorlesung am 03.12.2015 schriftlich vor:
 Fragenkatalog 11 Bereiten Sie bitte die folgenden Fragen für die Vorlesung am 03.12.2015 schriftlich vor: 1. Geben Sie zwei Möglichkeiten an, mit denen Sie Untergrundkompensation in der AAS betreiben können
Fragenkatalog 11 Bereiten Sie bitte die folgenden Fragen für die Vorlesung am 03.12.2015 schriftlich vor: 1. Geben Sie zwei Möglichkeiten an, mit denen Sie Untergrundkompensation in der AAS betreiben können
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Prof. Dr. J. Gmehling Universität Oldenburg, Institut für Reine und Angewandte Chemie, Technische Chemie, D Oldenburg
 Abschlussbericht an die Max-Buchner-Forschungsstiftung (FKZ: 277) Messung der Gleichgewichtslage und der Kinetik ausgewählter Veretherungsreaktionen und Überprüfung der Vorhersagbarkeit der Lösungsmitteleffekte
Abschlussbericht an die Max-Buchner-Forschungsstiftung (FKZ: 277) Messung der Gleichgewichtslage und der Kinetik ausgewählter Veretherungsreaktionen und Überprüfung der Vorhersagbarkeit der Lösungsmitteleffekte
Massenwirkungsgesetz (MWG) und Reaktionskombinationen
 Massenwirkungsgesetz (MWG) und Reaktionskombinationen Das Massenwirkungsgesetz stellt den Zusammenhang zwischen Aktivitäten (bzw. Konzentrationen) der Produkte und der Edukte einer chemischen Reaktion,
Massenwirkungsgesetz (MWG) und Reaktionskombinationen Das Massenwirkungsgesetz stellt den Zusammenhang zwischen Aktivitäten (bzw. Konzentrationen) der Produkte und der Edukte einer chemischen Reaktion,
Versuchsprotokoll Kapitel 6
 Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
SurTec 691 Schwarzpassivierung für alkalische Zinküberzüge
 Protection upgraded SurTec 691 Schwarzpassivierung für alkalische Zinküberzüge Eigenschaften Chrom(VI)-freie Schwarzpassivierung auf Basis von dreiwertigem Chrom speziell entwickelt für die Beschichtung
Protection upgraded SurTec 691 Schwarzpassivierung für alkalische Zinküberzüge Eigenschaften Chrom(VI)-freie Schwarzpassivierung auf Basis von dreiwertigem Chrom speziell entwickelt für die Beschichtung
Klausur zur Vorlesung "Grundzüge der Chemie" für Studierende des Maschinenbaus BITTE AUSFÜLLEN BITTE HALTEN SIE IHREN STUDENTAUSWEIS BEREIT
 1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Versuch 8
 Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 8 Bestimmung des Schwefelsäuregehaltes einer Schwefelsäurelösung mit unbekannter Massekonzentration und Herstellung einer Lösung mit c(h2 S04)
Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 8 Bestimmung des Schwefelsäuregehaltes einer Schwefelsäurelösung mit unbekannter Massekonzentration und Herstellung einer Lösung mit c(h2 S04)
E1 Ein Modellversuch zum chemischen Gleichgewicht
 Chemische Reaktionen verlaufen keineswegs immer zu 100% von den Edukten zu den Produkten. Für ein Verständnis der Akzeptor-Donator Theorien (Säure/Base, Redox) sind eingehende Kenntnisse über die Ursachen
Chemische Reaktionen verlaufen keineswegs immer zu 100% von den Edukten zu den Produkten. Für ein Verständnis der Akzeptor-Donator Theorien (Säure/Base, Redox) sind eingehende Kenntnisse über die Ursachen
man sagt : Phosphor + Sauerstoff reagieren Tetraphosphorzu dekaoxid
 Die Luft 1.Versuch Wir entzünden eine Kerze und stülpen ein Becherglas darüber. Beobachtung : Nach kurzer Zeit erlischt die Flamme. Feststellung : Für die Verbrennung in unserer Umwelt ist Luft notwendig.
Die Luft 1.Versuch Wir entzünden eine Kerze und stülpen ein Becherglas darüber. Beobachtung : Nach kurzer Zeit erlischt die Flamme. Feststellung : Für die Verbrennung in unserer Umwelt ist Luft notwendig.
TÜV SÜD Industrie Service GmbH
 Rohstoff, Produkt oder Abfall Problem der Definition TÜV SÜD Industrie Service GmbH Dr. Johann R. Mandl Immissionsschutz und Umwelt aktuell, München, 13.10.2009 Problem der Definition Ist ein Produktionsrückstand
Rohstoff, Produkt oder Abfall Problem der Definition TÜV SÜD Industrie Service GmbH Dr. Johann R. Mandl Immissionsschutz und Umwelt aktuell, München, 13.10.2009 Problem der Definition Ist ein Produktionsrückstand
2. Bestimmen Sie die Geschwindigkeitskonstante k der Rohrzuckerinversion in s -1.
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 33 Spezifische Drehung von gelöstem Rohrzucker - Rohrzuckerinversion Aufgabe: 1. Bestimmen Sie den Drehwinkel α für Rohrzucker für
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 33 Spezifische Drehung von gelöstem Rohrzucker - Rohrzuckerinversion Aufgabe: 1. Bestimmen Sie den Drehwinkel α für Rohrzucker für
Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände
 Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände 7. Multimethoden-Methoden für einzelne Stoffgruppen, die in mehreren Laboratorien erprobt
Methoden zur Untersuchung von Papier, Karton und Pappe für Lebensmittelverpackungen und sonstige Bedarfsgegenstände 7. Multimethoden-Methoden für einzelne Stoffgruppen, die in mehreren Laboratorien erprobt
Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14
 Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14 Teil des Moduls MN-C-AlC S. Sahler, M. Wolberg Inhalt Mittwoch, 08.01.2014, Allgemeine Einführung in die Quantitative Analyse Glasgeräte und
Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14 Teil des Moduls MN-C-AlC S. Sahler, M. Wolberg Inhalt Mittwoch, 08.01.2014, Allgemeine Einführung in die Quantitative Analyse Glasgeräte und
Von Bekir Ada & Edin Terzic ANORGANISCHE PEROXIDE & RADIKALE
 Von Bekir Ada & Edin Terzic ANORGANISCHE PEROXIDE & RADIKALE THEMEN Radikale Was sind Radikale Verwendung Stickstoffmonoxid Wasserstoffperoxid Halogen Polymerisation Peroxide Was sind Peroxide Natriumperoxid
Von Bekir Ada & Edin Terzic ANORGANISCHE PEROXIDE & RADIKALE THEMEN Radikale Was sind Radikale Verwendung Stickstoffmonoxid Wasserstoffperoxid Halogen Polymerisation Peroxide Was sind Peroxide Natriumperoxid
