Entscheidungsgrundlagen. vom 15. November C. Ermittlung der Vergleichsgrößen gemäß 35 Abs.1 Satz 5 SGB V 10
|
|
|
- Gesche Geier
- vor 6 Jahren
- Abrufe
Transkript
1 Entscheidungsgrundlagen vom 15. November 2005 A. Einführung 2 B. Entscheidungsgrundlagen zur Festbetragsgruppenbildung 3 C. Ermittlung der Vergleichsgrößen gemäß 35 Abs.1 Satz 5 SGB V 10 D. Anpassung und Aktualisierung der Festbetragsgruppen 17 1
2 Entscheidungsgrundlagen des Unterausschusses Arzneimittel zur Festbetragsgruppenbildung nach 35 Abs.1 Satz 2 Nr.2 SGB V und zur Konkretisierung des Ausnahmetatbestandes nach 35 Abs.1 Satz 3 2. HS SGB V zur Gruppenbildung unter Einbeziehung von Arzneimitteln mit patentgeschützten Wirkstoffen nach 35 Abs. 1 Satz 2 Nr. 2 i. V. m. 35 Abs. 1 Satz 3 und Abs. 1a SGB V A. Einführung Nach 35 Abs. 1 SGB V bestimmt der Gemeinsame Bundesausschuss in den Richtlinien nach 92 Abs. 1 S. 2 Nr. 6, für welche Gruppen von Arzneimitteln Festbeträge festgesetzt werden können. In den Gruppen sollen Arzneimittel mit 1. denselben Wirkstoffen, 2. pharmakologisch-therapeutisch vergleichbaren Wirkstoffen, insbesondere mit chemisch verwandten Stoffen, 3. therapeutisch vergleichbarer Wirkung, insbesondere Arzneimittelkombinationen zusammengefasst werden; unterschiedliche Bioverfügbarkeiten wirkstoffgleicher Arzneimittel sind zu berücksichtigen, sofern sie für die Therapie bedeutsam sind. Die nach S. 2 Nr. 2 und 3 gebildeten Gruppen müssen gewährleisten, dass Therapiemöglichkeiten nicht eingeschränkt werden und medizinisch notwendige Verordnungsalternativen zur Verfügung stehen; ausgenommen von diesen Gruppen sind Arzneimittel mit patentgeschützten Wirkstoffen, deren Wirkungsweise neuartig ist und die eine therapeutische Verbesserung, auch wegen geringerer Nebenwirkungen, bedeuten. Als neuartig gilt ein Wirkstoff, solange derjenige Wirkstoff, der als Erster dieser Gruppe in Verkehr gebracht worden ist, unter Patentschutz steht. Der Gemeinsame Bundesausschuss ermittelt auch die nach Absatz 3 notwendigen rechnerischen mittleren Tages- oder Einzeldosen oder anderen geeigneten Vergleichsgrößen. 2
3 B. Entscheidungsgrundlagen zur Festbetragsgruppenbildung Diese Entscheidungsgrundlagen sichern ein einheitliches Verfahren bei der Bildung von Festbetragsgruppen nach 35 Abs.1 Satz 2 Nr. 2 SGB V unter Berücksichtigung der Ausnahmeregelungen nach 35 Abs.1 Satz 3 2. HS und Abs. 1a SGB V auf der Grundlage des allgemein anerkannten Standes der medizinischen Erkenntnisse i. S. d. 2 Abs. 1 Satz 3 SGB V. Sie gewährleisten ein objektives, transparentes und nachprüfbares Verfahren der Festbetragsgruppenbildung auch unter Berücksichtigung der evidenzbasierten Medizin Konkretisierung der gesetzlichen Kriterien zur Gruppierung auf Wirkstoff- Ebene (Stufe 2) Bei der Gruppenbildung nach 35 Abs.1 Satz 2 Nr. 2 SGB V sind folgende Kriterien zu beachten: 1. nach 35 Abs. 1 Satz 2 Nr. 2 SGB V pharmakologisch-therapeutische Vergleichbarkeit chemische Verwandtschaft 2. nach 35 Abs. 1 Satz 3 SGB V neuartige Wirkungsweise therapeutische Verbesserung (auch 35 Abs. 1a SGB V) 1 Feststellung der pharmakologisch-therapeutischen Vergleichbarkeit, chemische Verwandtschaft Für die pharmakologisch-therapeutische Vergleichbarkeit kommt es auf die pharmakologischen und therapeutischen Eigenschaften der Wirkstoffe an. Nach der Gesetzessystematik erfolgt die Gruppenbildung auf der Ebene von Wirkstoffen. Als Ausgangspunkt für die Feststellung der Vergleichbarkeit von Wirkstoffen eignet sich die anatomisch-therapeutisch-chemische Klassifikation 3
4 der WHO (ATC-Code) nach Maßgabe des 73 Abs.8 S. 5 SGB V. Danach können Festbetragsgruppen gebildet werden für Wirkstoffe, die einem Wirkprinzip (4. Ebene) zugeordnet sind, auch wenn sie sich in übergeordneten Klassifikationsmerkmalen unterscheiden. Allerdings ist bei auf dieser Grundlage vorgeschlagenen Festbetragsgruppen ergänzend zu prüfen, ob unter pharmakologisch-therapeutischen Gesichtspunkten bestimmte Wirkstoffe (5. Ebene) auch wegen einer relevanten therapeutischen Verbesserung oder wegen therapeutisch relevanter geringerer Nebenwirkungen von der Gruppenbildung auszuschließen oder in Untergruppen zusammenzufassen sind. Maßgebend für die Prüfung der pharmakologisch-therapeutischen Vergleichbarkeit von Wirkstoffen, insbesondere unter dem Gesichtspunkt der chemischen Verwandtschaft, sind die folgenden Kriterien: 1. Ebenen der pharmakologisch-therapeutischen Vergleichbarkeit 1.1 pharmakologische Vergleichbarkeit Für die Vergleichbarkeit von Wirkstoffen unter pharmakologischen Gesichtspunkten sind die Pharmakokinetik und Pharmakodynamik wesentlich Pharmakokinetik Pharmakokinetische Eigenschaften, durch Wirkstoff und/oder Galenik bedingt, finden u. a. Ausdruck in der Bioverfügbarkeit (absolute Bioverfügbarkeit, gemessen gegen eine parenterale Applikation), aber auch z. B. in einer unterschiedlichen Eliminationshalbwertszeit und Wirkungsdauer. Pharmakokinetische Parameter sind für die Festbetragsgruppenbildung dann relevant, wenn sie hinsichtlich der therapeutischen Verbesserung, auch wegen geringerer Nebenwirkungen, nachweislich von erheblicher Bedeutung sind Pharmakodynamik 4
5 Allgemeine Voraussetzung für die Wirkung eines Arzneistoffs (Pharmakon) ist z. B: die Interaktion mit einem Rezeptor, der bestimmte physiologische Abläufe im Organismus steuert. Unter pharmakologischen Rezeptoren versteht man intrazelluläre oder membranständige Proteine, die nach Bindung eines Liganden an eine für diesen spezifische Rezeptorbindungsstelle einen Effekt hervorrufen. Ein vergleichbarer Wirkungsmechanismus ist Voraussetzung für die pharmakologische Vergleichbarkeit. 1.2 Chemische Verwandtschaft Wirkstoffe sind chemisch verwandt, wenn sie eine vergleichbare chemische Grundstruktur aufweisen und sich durch eine räumliche Struktur auszeichnen, die eine spezifische Pharmakon-Rezeptor-Wechselwirkung ermöglicht. Eine chemische Verwandtschaft erstreckt sich nicht nur auf Molekülvariationen aus kombinatorischen Syntheseverfahren, sondern schließt auch Strukturformen ein, die auf Verfahren der Gentechnik oder des molecular modeling beruhen. Chemisch verwandt sind z. B aktive Stereoisomere und Razemate sowie prodrugs. Chemische Verwandtschaft ist grundsätzlich auch bei unterschiedlichen Herstellungsverfahren gegeben. 1.3 Pharmakologisch-therapeutische Vergleichbarkeit Wirkstoffe sind pharmakologisch-therapeutisch vergleichbar, wenn sie über einen vergleichbaren Wirkungsmechanismus hinaus eine Zulassung für ein oder mehrere gemeinsame Anwendungsgebiete besitzen. 5
6 2 Ausnahmeregelungen nach 35 Abs.1 Satz 3 und Abs.1 a Satz 2 SGB V Ausgenommen von der Gruppenbildung nach 35 Abs.1 Satz 2 Nr. 2 und 3 SGB V sind Arzneimittel mit patentgeschützten Wirkstoffen, deren Wirkungsweise neuartig ist und die eine therapeutische Verbesserung, auch wegen geringerer Nebenwirkungen, bedeuten. 35 Abs. 1 a Satz 2 SGB V bestimmt, dass von der Gruppenbildung nach 35 Abs.1 a Satz 1 SGB V patentgeschützte Wirkstoffe ausgenommen sind, die eine therapeutische Verbesserung, auch wegen geringerer Nebenwirkungen, bedeuten. 1. Neuartige Wirkungsweise Als neuartig gilt ein Wirkstoff, solange derjenige Wirkstoff, der als Erster dieser Gruppe in Verkehr gebracht worden ist, unter Patentschutz steht. Die Neuartigkeit der Wirkungsweise ist nur relevant für Festbetragsgruppen nach 35 Abs. 1 Satz 2 Nr. 2 SGB V i. S. des 35 Abs. 1 Satz 3 und 4 SGB V. 2. Therapeutische Verbesserung Ein Arzneimittel mit einem patentgeschützten Wirkstoff zeigt im Vergleich zu anderen Arzneimitteln derselben Festbetragsgruppe eine therapeutische Verbesserung i. S. des 35 Abs. 1 Satz 3 und Abs. 1a Satz 2 SGB V, wenn in dem (den) gemeinsamen Anwendungsgebiet(en) ein Zusatznutzen mit einem therapeutisch relevanten Ausmaß nach dem allgemein anerkannten Stand der medizinischen Erkenntnisse besteht. Eine therapeutische Verbesserung kann sich insbesondere daraus ergeben, dass a) das Arzneimittel eine überlegene Wirksamkeit gegenüber Standardmitteln in der Vergleichsgruppe nach dem allgemein anerkannten Stand der medizinischen Erkenntnisse zeigt, b) das Arzneimittel über besondere Leistungsmerkmale verfügt, z. B. 6
7 Wechsel des Applikationsortes (z.b. systemisch, topisch), Wechsel des Applikationsweges (z.b. oral, parenteral) oder für die Therapie bedeutsame andere Galenik (z.b. retardiert/normal freisetzend) c) das Arzneimittel geringere Nebenwirkungen aufweist. Als Nebenwirkung1 bezeichnet man eine Reaktion, die schädlich und unbeabsichtigt ist und bei Dosierungen auftritt, wie sie normalerweise beim Menschen zur Prophylaxe, Diagnose oder Therapie von Krankheiten oder für die Änderung einer physiologischen Funktion verwendet werden.2 Die Nebenwirkungen werden in der Regel der Organklassensystematik der WHO zugeordnet und nach Häufigkeitsklassen3 quantifiziert. Art und Ausmaß beschreiben den Schweregrad der Nebenwirkungen. Eine Nebenwirkung ist schwerwiegend, wenn sie tödlich oder lebensbedrohend ist, zu Arbeitsunfähigkeit führt oder einer Behinderung oder hat eine stationären Behandlung oder Verlängerung einer stationären Behandlung zur Folge hat.4 Geringere Nebenwirkung i. S. des 35 Abs. 1 Satz 3 und Abs. 1a SGB V ist im Vergleich zu den anderen Wirkstoffen der Vergleichsgruppe der Wegfall oder 1 Das Nebenwirkungs- wie auch das Interaktionspotential jedes einzelnen in einer Festbetragsgruppe zusammengefassten Wirkstoffs ist Bestandteil der arzneimittelgesetzlichen Zulassung und in der Fachinformation, als Grundlage für den bestimmungsgemäßen Gebrauch, beschrieben. 2 Kloesel/Cyran, Kommentar zum Arzneimittelgesetz (AMG), 4 Rn. 48 lit.a); 3. Bekanntmachung zur Anzeige von Nebenwirkungen, Wechselwirkungen mit anderen Mitteln und Arzneimittelmissbrauch, nach 29 Abs. 1 Satz 2 bis 8 AMG, BAnz. Nr.97 v.25.mai 1996, S SPC-Guideline (Guideline on Summary of Product Characteristics, Guideline on the Readabbility of the Label and Package Leaflet) -sehr häufig (>=10%), -häufig (>=1%-<10%), -gelegentlich (>=0,1%-<1%), -selten (>=0,01%-<0,1%) bis -sehr selten (<0,01%) und Einzelfällen. 4 Kloesel/Cyran, AMG, 4 Rn. 48 lit. b); 3. Bekanntmachung zur Anzeige von Nebenwirkungen, Wechselwirkungen mit anderen Mitteln und Arzneimittelmissbrauch, nach 29 Abs. 1 Satz 2 bis 8 AMG, BAnz. Nr.97 v.25.mai 1996, S
8 die erhebliche Verringerung des Häufigkeitsgrades einer therapierelevanten Nebenwirkung. Eine Nebenwirkung ist therapierelevant, wenn sie schwerwiegend ist oder ein Wirkstoff aufgrund des Ausmaßes der Verringerung von Nebenwirkungen regelmäßig über den Einzelfall hinaus zweckmäßige Therapie im Sinne des 12 SGB V ist und deshalb aus Gründen der therapeutischen Notwendigkeit den anderen Wirkstoffen vorzuziehen ist. 3 Nachweis der therapeutischen Verbesserung Maßstab für die Beurteilung einer therapeutischen Verbesserung ist der allgemein anerkannte Stand der medizinischen Erkenntnisse gemäß 2 Abs.1 Satz 3 SGB V. 1. Allgemein anerkannter Stand der medizinischen Erkenntnisse 5 Der allgemein anerkannte Stand der medizinischen Erkenntnisse wird auf der Basis der arzneimittel-gesetzlichen Zulassung festgestellt. Darüber hinaus kann eine therapeutische Verbesserung dem allgemein anerkannten Stand der medizinischen Erkenntnisse entsprechen, wenn sie von der großen Mehrheit der einschlägigen Fachleute (Ärzte, Wissenschaftler) befürwortet wird. Von einzelnen, nicht ins Gewicht fallenden Gegenstimmen abgesehen, muss über die Zweckmäßigkeit der therapeutischen Verbesserung Konsens bestehen. Das setzt im Regelfall voraus, dass über Qualität und Wirksamkeit der therapeutischen Verbesserung zuverlässige, wissenschaftlich nachprüfbare Aussagen gemacht werden können. Die therapeutische Verbesserung muss in einer für die sichere Beurteilung ausreichenden Zahl von Behandlungsfällen erfolgreich gewesen sein. Der Erfolg muss sich aus wissenschaftlich einwandfrei geführten Statistiken über die Zahl der behandelten Fälle und die Wirksamkeit der therapeutische Verbesserung ablesen lassen. 5 Die nachfolgende Definition entspricht der ständigen Rechtsprechung des BSG zur Auslegung des 2 Abs.1 Satz 3 SGB V, der als Leitnorm den Versorgungsstandard für die Leistungspflicht der GKV festlegt; vgl. zum Ganzen BSG, Urt. v , Az.: B 1 KR 16/00 R 8
9 2. Unterlagen für den Nachweis einer therapeutischen Verbesserung Die Feststellung, ob eine therapeutische Verbesserung dem allgemeinen anerkannten Stand der medizinischen Erkenntnisse entspricht, erfolgt grundsätzlich auf der Basis a) der arzneimittelgesetzlichen Zulassung nach 25 AMG unter Berücksichtigung der Angaben der amtlichen Fachinformation sowie b) unter Berücksichtigung valider Endpunktstudien 2.1 Vergleichsstudien a) Die therapeutische Verbesserung soll in randomisierten, doppelblinden und kontrollierten direkten Vergleichsstudien guter Qualität anhand relevanter klinischer Endpunkte nachgewiesen sein und ein therapeutisch bedeutsames Ausmaß aufweisen. b) Die Studien sollen eine positive Beeinflussung klinisch bedeutsamer Endpunkte zeigen. c) Sie sollen an Populationen oder unter Bedingungen durchgeführt sein, die für die übliche Behandlungssituation repräsentativ und relevant sind. d) Sie sollen gegenüber Standardmitteln der Vergleichsgruppe durchgeführt werden, um die mögliche Überlegenheit der therapeutischen Verbesserung mit ausreichender Sicherheit prüfen zu können. 2.2 Placebo-kontrollierte Studien Liegen direkte Vergleichsstudien nicht vor, ist zu prüfen, ob placebokontrollierte Studien verfügbar sind, die sich für einen indirekten Nachweis einer therapeutischen Verbesserung eignen und den unter 2.1. b) und 2.1. c) beschriebenen Qualitätsanforderungen entsprechen. 9
10 2.3 Entscheidung des Unterausschusses Der Unterausschuss prüft die nach 2.1 und 2.2 vorgelegten Studien hinsichtlich ihrer Planungs-, Durchführungs- und Auswertungsqualität und entscheidet über ihre Aussagekraft zur Relevanz der therapeutischen Verbesserung unter Berücksichtigung der aktuellen Fachinformation. C. Ermittlung der Vergleichsgrößen gemäß 35 Abs.1 Satz 5 SGB V Gemäß 35 Abs.3 Satz 5 SGB V hat der Gemeinsame Bundesausschuss die für die Festsetzung von Festbeträgen nach 35 Abs.3 SGB V notwendigen mittleren Tages- oder Einzeldosen oder andere geeignete Vergleichsgrößen zu ermitteln. 1 Vergleichsgröße für Wirkstoffe mit vergleichbarer Applikationsfrequenz Als geeignete Vergleichsgröße im Sinne des 35 Abs.1 Satz 5 wird die verordnungsgewichtete durchschnittliche Einzelwirkstärke bestimmt. Sie wird nach Maßgabe der folgenden Methodik ermittelt. 1. Ermittlung der gewichteten Einzelwirkstärke Grundsätzlich ist davon auszugehen, dass nur therapeutisch sinnvolle Wirkstärken zugelassen werden. Um der therapeutischen Relevanz der einzelnen Wirkstärken angemessen Rechnung zu tragen, ist ihre jeweilige Verordnungshäufigkeit zu berücksichtigen. Zu diesem Zweck werden für jeden einzelnen Wirkstoff die zu den im Markt verfügbaren Einzelwirkstärken ausgewiesenen Verordnungen anhand der zum Stichtag zuletzt verfügbaren Jahresdaten des GKV - Arzneimittelindex herangezogen. 10
11 Jeder wirkstärkenbezogen ermittelte prozentuale Verordnungsanteil wird zunächst abgerundet und zu diesem Ergebnis der Wert 1 addiert. Der Gewichtungswert ist also stets die nächst größere ganze Zahl. Jede Einzelwirkstärke wird dann mit ihrem Gewichtungswert multipliziert und als gewichtete Einzelwirkstärke ausgewiesen. 2. Ermittlung der durchschnittlichen Einzelwirkstärke Anschließend werden für jeden einzelnen Wirkstoff die gewichteten Einzelwirkstärken addiert und durch die Summe der Gewichtungswerte des Wirkstoffes dividiert. Die so ermittelte durchschnittliche Einzelwirkstärke ergibt die Vergleichsgröße. Diese berücksichtigt die Verordnungsrelevanz der einzelnen Einzelwirkstärken und erlaubt einen quantitativen Vergleich der therapeutischen Einsatzbreite des jeweiligen Wirkstoffes. VG= Ø VO - gewichtete Einzelwirkstärke (Wirkstärke pro abgeteilte Einheit) 2 Vergleichsgröße für Wirkstoffe mit unterschiedlicher Applikationsfrequenz Als geeignete Vergleichsgröße im Sinne des 35 Abs.1 Satz 5 wird die verordnungsgewichtete durchschnittliche Einzelwirkstärke für Wirkstoffe mit Dauertherapie oder Mischformen aus Dauertherapie und zyklischer Therapie bestimmt, die eine unterschiedliche Applikationsfrequenz innerhalb von 24 Stunden besitzen. Sie wird nach Maßgabe der folgenden Methodik ermittelt: 1. Ermittlung der gewichteten Einzelwirkstärke Grundsätzlich ist davon auszugehen, dass nur therapeutisch sinnvolle Wirkstärken zugelassen werden. Um der therapeutischen Relevanz der einzelnen Wirkstärken angemessen Rechnung zu tragen, ist ihre jeweilige 11
12 Verordnungshäufigkeit zu berücksichtigen. Zu diesem Zweck werden für jeden einzelnen Wirkstoff die zu den im Markt verfügbaren Einzelwirkstärken ausgewiesenen Verordnungen anhand der zum Stichtag zuletzt verfügbaren Jahresdaten des GKV-Arzneimittelindex herangezogen. Jeder wirkstärkenbezogen ermittelte prozentuale Verordnungsanteil wird zunächst abgerundet und zu diesem Ergebnis der Wert 1 addiert. Der Gewichtungswert ist also stets die nächst größere ganze Zahl. Jede Einzelwirkstärke wird dann mit ihrem Gewichtungswert multipliziert und als gewichtete Einzelwirkstärke ausgewiesen. 2. Ermittlung der durchschnittlichen Einzelwirkstärke Anschließend werden für jeden einzelnen Wirkstoff die gewichteten Einzelwirkstärken addiert und durch die Summe der Gewichtungswerte des Wirkstoffes dividiert. Die so ermittelte durchschnittliche Einzelwirkstärke ergibt die vorläufige Vergleichsgröße (vvg). Diese berücksichtigt die Verordnungsrelevanz der einzelnen Einzelwirkstärken. vvg = Ø VO-gewichtete Einzelwirkstärke (Wirkstärke pro abgeteilte Einheit) 3. Ermittlung der applikationsbezogenen Vergleichsgröße Bei den hier gruppierten Wirkstoffen unterscheiden sich die durchschnittlichen täglichen Einnahmefrequenzen der Wirkstoffe. Um die Vergleichsgröße sachgerecht berechnen zu können, werden die täglichen Applikationsfrequenzen einbezogen. Liegt für den Wirkstoff ein Mustertext des Bundesinstituts für Arzneimittel und Medizinprodukte vor, werden die Angaben der Applikationsfrequenzen entsprechend diesem übernommen. Liegt kein wirkstoffbezogener Mustertext vor, werden zur Ermittlung der Applikationsfrequenzen die jeweils aktuellsten verfügbaren Fachinformationen herangezogen. 12
13 Die Applikationsfrequenzen sind pro Wirkstoff ggf. je nach gruppenspezifischen Besonderheiten, entsprechend der verschiedenen Anwendungsgebiete und/oder Applikationssysteme zu kategorisieren. Liegen pro Kategorie mehrere Angaben vor, wird für diese Kategorie die jeweils kleinste ganze Applikationsfrequenz berücksichtigt. Aus den für die Kategorien eines Wirkstoffes vorliegenden kleinstmöglichen Applikationsfrequenzen werden pro Wirkstoff die verschiedenen Ausprägungen ermittelt. Der Durchschnittswert dieser Ausprägungen Ø APF-Wirkstoff ist der Applikationsfaktor (APF) des Wirkstoffes. APF = Ø APF-Wirkstoff Sofern gruppenbezogen eine Standardisierung des Durchschnittswertes erforderlich ist, wird zu diesem Zweck die Standardapplikationsfrequenz der Festbetragsgruppe bestimmt. Die Standardapplikationsfrequenz der Festbetragsgruppe (APF-Standard) ist die Applikationsfrequenz in der Festbetragsgruppe, die am häufigsten vorkommt, unabhängig von ihrer absoluten Größe. Der Applikationsfaktor APF ergibt sich dann aus dem Verhältnis des Durchschnittswertes und der Standardapplikationsfrequenz: APF = Ø APF-Wirkstoff APF-Standard Der berechnete Applikationsfaktor (APF) wird anschließend mit der vorläufigen Vergleichsgröße multipliziert und ergibt die endgültige Vergleichsgröße VG = vvg x APF 3 Vergleichsgröße für Wirkstoffe mit unterschiedlichen Applikationsfrequenzen und Behandlungszeiten Als geeignete Vergleichsgröße im Sinne des 35 Abs.1 Satz 5 wird die verordnungsgewichtete durchschnittliche Gesamtwirkstärke für Wirkstoffe mit 13
14 zyklischer Therapie bestimmt. Sie wird nach Maßgabe der folgenden Methodik ermittelt: 1. Ermittlung der gewichteten Gesamtwirkstärke Grundsätzlich ist davon auszugehen, dass nur therapeutisch sinnvolle Wirkstärken zugelassen werden. Bei Wirkstoffen, die in zyklischen Therapien Anwendung finden, ist die Packungsgröße im allgemeinen sowohl dem Anwendungsgebiet als auch der Anwendungsdauer angemessen. Sie ist somit Ausdruck der unterschiedlichen Behandlungszeiten und der unterschiedlichen Applikationsfrequenzen der Wirkstoffe. Um der therapeutischen Relevanz der einzelnen Gesamtwirkstärken je Packung angemessen Rechnung zu tragen, ist ihre jeweilige Verordnungshäufigkeit zu berücksichtigen. Zu diesem Zweck werden für jeden einzelnen Wirkstoff die zu den im Markt verfügbaren Gesamtwirkstärken ausgewiesenen Verordnungen anhand der zum Stichtag zuletzt verfügbaren Jahresdaten des GKV-Arzneimittelindex herangezogen. Jeder gesamtwirkstärkenbezogen ermittelte prozentuale Verordnungsanteil wird zunächst abgerundet und zu diesem Ergebnis der Wert 1 addiert. Der Gewichtungswert ist also stets die nächst größere ganze Zahl. Jede Gesamtwirkstärke wird dann mit ihrem Gewichtungswert multipliziert und als gewichtete Gesamtwirkstärke ausgewiesen. 2. Ermittlung der durchschnittlichen Gesamtwirkstärke Anschließend werden für jeden einzelnen Wirkstoff die gewichteten Gesamtwirkstärken addiert und durch die Summe der Gewichtungswerte des Wirkstoffes dividiert. Die so ermittelte durchschnittliche Gesamtwirkstärke ergibt die Vergleichsgröße, Diese berücksichtigt die Verordnungsrelevanz der einzelnen Gesamtwirkstärken und erlaubt einen quantitativen Vergleich der therapeutischen Einsatzbreite des jeweiligen Wirkstoffes. VG= Ø VO - gewichtete Gesamtwirkstärke (Wirkstärke pro Packung) 14
15 4 Vergleichsgröße für Wirkstoffe mit unterschiedlichen Applikationsfrequenzen und Intervallen, unterschiedlichen Behandlungszeiten und unterschiedlicher Anzahl therapiefreier Tage Als geeignete Vergleichsgröße im Sinne des 35 Abs.1 Satz 5 wird die verordnungsgewichtete durchschnittliche intervallbezogene Gesamtwirkstärke für Wirkstoffe mit lntervalltherapie oder Mischformen aus lntervalltherapie und Dauertherapie bestimmt. Sie wird nach Maßgabe der folgenden Methodik ermittelt: 1. Ermittlung der gewichteten Gesamtwirkstärke Grundsätzlich ist davon auszugehen, dass nur therapeutisch sinnvolle Wirkstärken zugelassen werden. Bei Wirkstoffen, die in den oben genannten Therapieformen angewendet werden, ist die Packungsgröße Ausdruck der Therapietage und der unterschiedlichen Applikationsfrequenzen der Wirkstoffe. Um der therapeutischen Relevanz der einzelnen Gesamtwirkstärken je Packung angemessen Rechnung zu tragen, ist ihre jeweilige Verordnungshäufigkeit zu berücksichtigen. Zu diesem Zweck werden für jeden einzelnen Wirkstoff die zu den im Markt verfügbaren Gesamtwirkstärken ausgewiesenen Verordnungen anhand der zum Stichtag zuletzt verfügbaren Jahresdaten des GKV - Arzneimittelindex herangezogen. Jeder gesamtwirkstärkenbezogen ermittelte prozentuale Verordnungsanteil wird zunächst abgerundet und zu diesem Ergebnis der Wert 1 addiert. Der Gewichtungswert ist also stets die nächst größere ganze Zahl. Jede Gesamtwirkstärke wird dann mit ihrem Gewichtungswert multipliziert und als gewichtete Gesamtwirkstärke ausgewiesen. 2. Ermittlung der durchschnittlichen Gesamtwirkstärke Anschließend werden für jeden einzelnen Wirkstoff die gewichteten Gesamtwirkstärken addiert und durch die Summe der Gewichtungswerte des Wirkstoffes dividiert. Die so ermittelte durchschnittliche Gesamtwirkstärke ergibt die vorläufige Vergleichsgröße. Diese berücksichtigt die Verordnungsrelevanz der einzelnen Gesamtwirkstärken. 15
16 vvg= Ø VO gewichtete Gesamtwirkstärke (Wirkstärke pro Packung) 3. Ermittlung der intervallbezogenen Vergleichsgröße Bei den hier betroffenen Therapieformen bildet die Packungsgröße allein nicht im ausreichenden Maß die Reichweite einer Packung im Rahmen der Intervalltherapie ab. Spezifische Ausprägungen des Therapieintervalls müssen wirkstoffbezogen in die Vergleichsgröße einbezogen werden. Ein Therapieintervall (Tl) lässt sich als Summe der Therapietage (TT) und der therapiefreien Tage (TF) abbilden: Tl =TT+TF Das Verhältnis aus durchschnittlichen Therapieintervallen (Ø TI) und den durchschnittlichen therapiefreien Tagen (Ø TF): Ø TI Ø TF drückt die spezifischen Ausprägungen des wirkstoffbezogenen Therapieintervalls aus. Durch Multiplikation dieses Quotienten mit den verordnungsgewichteten Gesamtwirkstärken erhält man die intervallbezogene Vergleichsgröße. VG = Ø VO gewichtete Gesamtwirkstärke x Ø TI Ø TF (Wirkstärke pro Packung sowie Berücksichtigung von Therapieintervall und therapiefreien Tagen) 16
17 D. Anpassung und Aktualisierung der Festbetragsgruppen Festbetragsgruppen als Bestandteil der Arzneimittel-Richtlinien des Gemeinsamen Bundesausschusses müssen dem allgemein anerkannten Stand der medizinischen Erkenntnisse entsprechen und deshalb in geeigneten Zeitabständen überprüft werden. Dies gilt auch für signifikante Änderungen der prozentualen Verordnungsanteile einzelner Wirkstärken eines bestimmten Wirkstoffes. 17
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Tragende Gründe. Vom 28. Mai Inhaltsverzeichnis. 1. Rechtsgrundlagen. 2. Eckpunkte der Entscheidung. 3. Beratungsverlauf
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über einen Antrag zur Verordnungsfähigkeit der zulassungsüberschreitenden Anwendung eines Arzneimittels zu Lasten der gesetzlichen Krankenkassen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über einen Antrag zur Verordnungsfähigkeit der zulassungsüberschreitenden Anwendung eines Arzneimittels zu Lasten der gesetzlichen Krankenkassen
1. Rechtsgrundlage. 2. Eckpunkte der Entscheidung
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Verfahrensordnung (VerfO):Änderung im 5.Kapitel Anpassung der Regelungen zur frühen Nutzenbewertung an Gesetzesänderungen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Verfahrensordnung (VerfO):Änderung im 5.Kapitel Anpassung der Regelungen zur frühen Nutzenbewertung an Gesetzesänderungen
Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG)
 Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
Gesetzliche Regelungen für Arzneimittel Wozu ein Gesetz, das Arzneimittel behandelt? Arzneimittelgesetz (AMG) 1 Zweck des Gesetzes Es ist der Zweck dieses Gesetzes, im Interesse einer ordnungsgemäßen Arzneimittelversorgung
Krankenversicherungsrecht
 Krankenversicherungsrecht Rechtliche Voraussetzungen für die Leistungspflicht der gesetzlichen Krankenversicherung (gkv) zur Behandlung von Transsexualismus Übersicht A. Grundfragen B. Einzelfragen, Kasuistik
Krankenversicherungsrecht Rechtliche Voraussetzungen für die Leistungspflicht der gesetzlichen Krankenversicherung (gkv) zur Behandlung von Transsexualismus Übersicht A. Grundfragen B. Einzelfragen, Kasuistik
S D M K D M KV G ONKOLOGIE C üsseldorf D
 MDS MDK GKV ONKOLOGIE C Düsseldorf München 19. September 2007 Leistungsumfang der GKV bei Behandlungen unter Teilnahme an klinischen Studien - Prüfung durch den MDK Prof. Dr. Axel Heyll Leiter des Kompetenz
MDS MDK GKV ONKOLOGIE C Düsseldorf München 19. September 2007 Leistungsumfang der GKV bei Behandlungen unter Teilnahme an klinischen Studien - Prüfung durch den MDK Prof. Dr. Axel Heyll Leiter des Kompetenz
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission
 Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
13. Wahlperiode
 13. Wahlperiode 03. 12. 2002 Kleine Anfrage der Abg. Heike Dederer GRÜNE und Antwort des Sozialministeriums Ambulante Rehabilitation in Baden-Württemberg nach Einführung des SGB IX Kleine Anfrage Ich frage
13. Wahlperiode 03. 12. 2002 Kleine Anfrage der Abg. Heike Dederer GRÜNE und Antwort des Sozialministeriums Ambulante Rehabilitation in Baden-Württemberg nach Einführung des SGB IX Kleine Anfrage Ich frage
Eingangsformel. 1 Geltungsbereich. 2 Begriffsbestimmungen. AM-NutzenV. Ausfertigungsdatum: 28.12.2010. Vollzitat:
 Verordnung über die Nutzenbewertung von Arzneimitteln nach 35a Absatz 1 SGB V für Erstattungsvereinbarungen nach 130b SGB V (Arzneimittel-Nutzenbewertungsverordnung - AM- NutzenV) AM-NutzenV Ausfertigungsdatum:
Verordnung über die Nutzenbewertung von Arzneimitteln nach 35a Absatz 1 SGB V für Erstattungsvereinbarungen nach 130b SGB V (Arzneimittel-Nutzenbewertungsverordnung - AM- NutzenV) AM-NutzenV Ausfertigungsdatum:
Nutzenbewertung. von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V. Wirkstoff: Nepafenac. nach 2 Abs. 2 VerfO des G-BA
 Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Wirkstoff: Nepafenac nach 2 Abs. 2 VerfO des G-BA Datum der Veröffentlichung: 1. Oktober 2013 1 Nepafenac Zugelassenes Anwendungsgebiet
Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Wirkstoff: Nepafenac nach 2 Abs. 2 VerfO des G-BA Datum der Veröffentlichung: 1. Oktober 2013 1 Nepafenac Zugelassenes Anwendungsgebiet
Themen. Insulinanaloga - Fragen und Antworten
 Themen Insulinanaloga - Fragen und Antworten Was sind Insulinanaloga? Als Humaninsulin wird die synthetische Nachbildung des körpereigenen, natürlichen Hormons Insulin bezeichnet. Insulinanaloga sind Abwandlungen
Themen Insulinanaloga - Fragen und Antworten Was sind Insulinanaloga? Als Humaninsulin wird die synthetische Nachbildung des körpereigenen, natürlichen Hormons Insulin bezeichnet. Insulinanaloga sind Abwandlungen
Thema: Stellenwert von Leitlinien und antizipierten Sachverständigengutachten
 Leitlinien Workshop der DGAUM am 19. Juni 2009 in Rostock Thema: Stellenwert von Leitlinien und antizipierten Sachverständigengutachten aus Sicht der Sozialgerichtsbarkeit Dr. Peter Becker, Richter am
Leitlinien Workshop der DGAUM am 19. Juni 2009 in Rostock Thema: Stellenwert von Leitlinien und antizipierten Sachverständigengutachten aus Sicht der Sozialgerichtsbarkeit Dr. Peter Becker, Richter am
Überprüfung der Qualifikation des Personals nach 14, 52a, 63a, 72 Abs. 2 und 74a AMG
 Seite 2 von 5 1 Zweck Diese Verfahrensanweisung regelt das Verfahren zur Feststellung der erforderlichen Qualifikation bei Personen, die eine oder mehrere der folgenden Tätigkeiten auszuüben beabsichtigen:
Seite 2 von 5 1 Zweck Diese Verfahrensanweisung regelt das Verfahren zur Feststellung der erforderlichen Qualifikation bei Personen, die eine oder mehrere der folgenden Tätigkeiten auszuüben beabsichtigen:
6.). Verschiedene Salze, Ester, Ether, Isomere, Mischungen von Isomeren,
 Regelungen des GKV-Spitzenverbandes nach 130a Abs. 3a Satz 10 SGB V zum Herstellerabschlag nach 130a Abs. 3a Satz 3 und 4 SGB V im Konsens mit den Verbänden der pharmazeutischen Unternehmer Grundsätzliches
Regelungen des GKV-Spitzenverbandes nach 130a Abs. 3a Satz 10 SGB V zum Herstellerabschlag nach 130a Abs. 3a Satz 3 und 4 SGB V im Konsens mit den Verbänden der pharmazeutischen Unternehmer Grundsätzliches
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Vortioxetin wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Apixaban wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Dokumentationshilfe Einzelhändler - Arzneimittelrecht
 Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
BAnz AT 11.11.2014 B1. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Tragende Gründe. Vom 2. August Inhalt 1. Rechtsgrundlage Eckpunkte der Entscheidung Verfahrensablauf... 6
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
(Orthopädische) Hilfsmittelversorgung aus Sicht des MDK
 (Orthopädische) Hilfsmittelversorgung aus Sicht des MDK Dr. Lothar Kern Fachbereich Hilfsmittel und Medizinprodukte MDK Bayern 17. Wissenschaftliche Tagung des ASBH Beirates 21. November 2015 Wer ist der
(Orthopädische) Hilfsmittelversorgung aus Sicht des MDK Dr. Lothar Kern Fachbereich Hilfsmittel und Medizinprodukte MDK Bayern 17. Wissenschaftliche Tagung des ASBH Beirates 21. November 2015 Wer ist der
Richtlinien der Stadt Uelzen zu den Elternbeiträgen in den Kindertagesstätten in Uelzen ab dem 01.08.2014
 Richtlinien der Stadt Uelzen zu den Elternbeiträgen in den Kindertagesstätten in Uelzen ab dem 01.08.2014 Die nachfolgenden Richtlinien gelten für den Besuch der Kindertagesstätten in der Stadt Uelzen,
Richtlinien der Stadt Uelzen zu den Elternbeiträgen in den Kindertagesstätten in Uelzen ab dem 01.08.2014 Die nachfolgenden Richtlinien gelten für den Besuch der Kindertagesstätten in der Stadt Uelzen,
Behandlung der feuchten altersabhängigen Makuladegeneration (feuchte AMD) mit VEGF-Hemmern durch operative Medikamenteneingabe in das Auge
 Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
2. Anzahl der Patienten bzw. Abgrenzung der für die Behandlung infrage kommenden Patientengruppen
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
BAnz AT 06.08.2014 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme
 Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme unter Verwendung der ICD und der Alpha-ID Manfred Criegee-Rieck Ein paar Zahlen: Blick
Integration der gesetzlich authorisierten Arzneimittelinformation in rechnergestützte klinische Arbeitsplatzsysteme unter Verwendung der ICD und der Alpha-ID Manfred Criegee-Rieck Ein paar Zahlen: Blick
Richtlinie zur Abkürzung und Verlängerung der Ausbildungszeit, zur Teilzeitberufsausbildung sowie zur vorzeitigen Zulassung zur Abschlussprüfung
 Richtlinie zur Abkürzung und Verlängerung der Ausbildungszeit, zur Teilzeitberufsausbildung sowie zur vorzeitigen Zulassung zur Abschlussprüfung A. Grundsätze (1) Diese Richtlinie soll die Auslegung der
Richtlinie zur Abkürzung und Verlängerung der Ausbildungszeit, zur Teilzeitberufsausbildung sowie zur vorzeitigen Zulassung zur Abschlussprüfung A. Grundsätze (1) Diese Richtlinie soll die Auslegung der
Abgrenzung aus Sicht der Lebensmittelwirtschaft
 Abgrenzung aus Sicht der Lebensmittelwirtschaft Antje Preußker Wissenschaftliche Leitung BfArM im Dialog: Abgrenzung von Arzneimitteln 19. September 2016 Schwerpunkt Nahrungsergänzungsmittel steht für
Abgrenzung aus Sicht der Lebensmittelwirtschaft Antje Preußker Wissenschaftliche Leitung BfArM im Dialog: Abgrenzung von Arzneimitteln 19. September 2016 Schwerpunkt Nahrungsergänzungsmittel steht für
Patentverletzung von Pharmapatenten durch Fach- oder Gebrauchsinformation
 Patentverletzung von Pharmapatenten durch Fach- oder Gebrauchsinformation Dr. Anna Wolters 29. September 2010 Universität Augsburg Institut für Bio-, Gesundheits- und Medizinrecht (IBGM) Vorbereitung Patentverletzungsprozess
Patentverletzung von Pharmapatenten durch Fach- oder Gebrauchsinformation Dr. Anna Wolters 29. September 2010 Universität Augsburg Institut für Bio-, Gesundheits- und Medizinrecht (IBGM) Vorbereitung Patentverletzungsprozess
Wichtige Änderungen im GKV-WSG für Krebspatienten
 Wichtige Änderungen im GKV-WSG für Krebspatienten Versorgung von Krebspatienten, Qualität quo vadis? Berlin 9./10. März 2007 Dr. Johannes Bruns Kosten Krankheitsklassen in Euro je Einwohner 2002 2004 600
Wichtige Änderungen im GKV-WSG für Krebspatienten Versorgung von Krebspatienten, Qualität quo vadis? Berlin 9./10. März 2007 Dr. Johannes Bruns Kosten Krankheitsklassen in Euro je Einwohner 2002 2004 600
17. März 2011 Deutsches Patent- und Markenamt. Dr. Christopher Brückner
 Definition des Erzeugnisses in Abhängigkeit von der pharmakologischen Wirkung Verhältnis zu Erwägungsgrund 14 der EG-Verordnung 1610/96 und Auswirkungen für die pharmazeutische Industrie 17. März 2011
Definition des Erzeugnisses in Abhängigkeit von der pharmakologischen Wirkung Verhältnis zu Erwägungsgrund 14 der EG-Verordnung 1610/96 und Auswirkungen für die pharmazeutische Industrie 17. März 2011
Wortlaut der für die Packungsbeilage vorgesehenen Angaben
 Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
Zulassungsnummer: 6312395.00.00 Seite 1 von 5 Apothekenpflichtig TUSSISANA Mischung 20 und 50 ml Stoff Darreichungsform Menge Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation:
Leitfaden zur Definition des Generikaabschlages nach 130a Abs. 3b SGB V
 Leitfaden zur Definition des Generikaabschlages nach 130a Abs. 3b SGB V Anknüpfend an die im Bundesgesundheitsministerium getroffenen Absprachen zur Anwendung des Generikaabschlages vom 6. März 2006 haben
Leitfaden zur Definition des Generikaabschlages nach 130a Abs. 3b SGB V Anknüpfend an die im Bundesgesundheitsministerium getroffenen Absprachen zur Anwendung des Generikaabschlages vom 6. März 2006 haben
3 BetrSichV: Konkretisierungen der Pflicht aus 5 ArbSchG
 Anlage 9 3 BetrSichV: Konkretisierungen der Pflicht aus 5 ArbSchG Vorgabe von Beurteilungsmaßstäben: 1. Anhänge 1-5 BetrSichV 2. 16 GefStoffV (Ermittlungspflicht des Arbeitgebers bzgl. Umgang mit Gefahrstoffen)
Anlage 9 3 BetrSichV: Konkretisierungen der Pflicht aus 5 ArbSchG Vorgabe von Beurteilungsmaßstäben: 1. Anhänge 1-5 BetrSichV 2. 16 GefStoffV (Ermittlungspflicht des Arbeitgebers bzgl. Umgang mit Gefahrstoffen)
Wie funktioniert eine klinische Studie?
 Wie funktioniert eine klinische Studie? Bernhard Saller 3. Süddeutscher Hypophysen- und Nebennierentag München, 5. Mai 2007 Definitionen Ablauf klinischer Studien Klinische Arzneimittelprüfungen Zulassungsprozess
Wie funktioniert eine klinische Studie? Bernhard Saller 3. Süddeutscher Hypophysen- und Nebennierentag München, 5. Mai 2007 Definitionen Ablauf klinischer Studien Klinische Arzneimittelprüfungen Zulassungsprozess
BAnz AT 07.07.2016 B4. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
18. Januar Gesetzlicher Auftrag Eckpunkte der Entscheidung Beratungsverlauf 4
 Tragende Gründe zum Beschluss über eine Änderung der Arzneimittel-Richtlinie in Anlage 2: Festbetragsgruppenneubildung (Stufe 3) Bisphosphonate und Kombinationen von Bisphosphonaten mit Additiva 18. Januar
Tragende Gründe zum Beschluss über eine Änderung der Arzneimittel-Richtlinie in Anlage 2: Festbetragsgruppenneubildung (Stufe 3) Bisphosphonate und Kombinationen von Bisphosphonaten mit Additiva 18. Januar
Verwaltungsvorschrift des Ministeriums für Wirtschaft, Bau und Tourismus Mecklenburg-Vorpommern vom 1. August 2016
 Richtlinie für die Beurteilung der bevollmächtigten Bezirksschornsteinfegerinnen und bevollmächtigten Bezirksschornsteinfeger in Mecklenburg-Vorpommern Verwaltungsvorschrift des Ministeriums für Wirtschaft,
Richtlinie für die Beurteilung der bevollmächtigten Bezirksschornsteinfegerinnen und bevollmächtigten Bezirksschornsteinfeger in Mecklenburg-Vorpommern Verwaltungsvorschrift des Ministeriums für Wirtschaft,
Zusammenfassende Dokumentation
 Zusammenfassende Dokumentation über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage IX Festbetragsgruppenbildung Antipsychotika, andere, Gruppe 1, in Stufe 2 nach 35 Abs. 1 SGB V Vom 17. Dezember
Zusammenfassende Dokumentation über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage IX Festbetragsgruppenbildung Antipsychotika, andere, Gruppe 1, in Stufe 2 nach 35 Abs. 1 SGB V Vom 17. Dezember
BAnz AT 20.11.2014 B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Management im Gesundheitswesen Industrie. Preisbildung. Reinhard Busse, Prof. Dr. med. MPH FFPH
 Management im Gesundheitswesen Industrie Preisbildung Reinhard Busse, Prof. Dr. med. MPH FFPH FG Management im Gesundheitswesen, Technische Universität Berlin (WHO Collaborating Centre for Health Systems
Management im Gesundheitswesen Industrie Preisbildung Reinhard Busse, Prof. Dr. med. MPH FFPH FG Management im Gesundheitswesen, Technische Universität Berlin (WHO Collaborating Centre for Health Systems
Die Gymnasiale Oberstufe. Englisch 5-stündig schriftliche Abiturprüfung. Geschichte + Gemeinschaftskunde 3-stündig Präsentationsprüfung
 Die Gymnasiale Oberstufe Klasse III IV (Jahrgangsstufe 1 2) Pflichtkernfächer Deutsch 5-stündig schriftliche Abiturprüfung Englisch 5-stündig schriftliche Abiturprüfung Mathematik 5-stündig schriftliche
Die Gymnasiale Oberstufe Klasse III IV (Jahrgangsstufe 1 2) Pflichtkernfächer Deutsch 5-stündig schriftliche Abiturprüfung Englisch 5-stündig schriftliche Abiturprüfung Mathematik 5-stündig schriftliche
Anhaltspunkt für erheblichen Zusatznutzen
 Pertuzumab Anhaltspunkt für erheblichen Zusatznutzen - Überlebensvorteil bei bestimmten Patientinnen - Keine Aussagen zum Schaden möglich Köln (1. Juli 2013) - Pertuzumab (Perjeta ) ist seit März 2013
Pertuzumab Anhaltspunkt für erheblichen Zusatznutzen - Überlebensvorteil bei bestimmten Patientinnen - Keine Aussagen zum Schaden möglich Köln (1. Juli 2013) - Pertuzumab (Perjeta ) ist seit März 2013
Richtlinie zur Abkürzung und Verlängerung der Ausbildungszeit, zur Teilzeitberufsausbildung sowie zur vorzeitigen Zulassung zur Abschlussprüfung
 Richtlinie zur Abkürzung und Verlängerung der Ausbildungszeit, zur Teilzeitberufsausbildung sowie zur vorzeitigen Zulassung zur Abschlussprüfung A. Grundsätze (1) Diese Richtlinie soll die Auslegung der
Richtlinie zur Abkürzung und Verlängerung der Ausbildungszeit, zur Teilzeitberufsausbildung sowie zur vorzeitigen Zulassung zur Abschlussprüfung A. Grundsätze (1) Diese Richtlinie soll die Auslegung der
Keine CE-Kennzeichnung ohne klinische Bewertung
 Seite 1 von 5 Keine CE-Kennzeichnung ohne klinische Bewertung Medizinprodukte können in der Regel nicht ohne klinische Daten und deren Bewertung auf den Markt gelangen. Zudem besteht für Medizinprodukte
Seite 1 von 5 Keine CE-Kennzeichnung ohne klinische Bewertung Medizinprodukte können in der Regel nicht ohne klinische Daten und deren Bewertung auf den Markt gelangen. Zudem besteht für Medizinprodukte
.04.201. Diese Erläuterungen beziehen sich auf die Vorschläge des Vorstandes des GKV-Spitzenverbandes zur Festbetragsfestsetzung vom 22.02.2013.
 01.03.2013 Arzneimittel-Festbeträge: en zum Stellungnahmeverfahren vom 04.0.03.201.2013 bis 02.0.04.201.2013 Diese en beziehen sich auf die Vorschläge des Vorstandes des GKV-Spitzenverbandes zur Festbetragsfestsetzung
01.03.2013 Arzneimittel-Festbeträge: en zum Stellungnahmeverfahren vom 04.0.03.201.2013 bis 02.0.04.201.2013 Diese en beziehen sich auf die Vorschläge des Vorstandes des GKV-Spitzenverbandes zur Festbetragsfestsetzung
KLINISCHE PRÜFUNG EINE EINFÜHRUNG. ATA Conference 2003 - Elke Vogt-Arendt
 KLINISCHE PRÜFUNG EINE EINFÜHRUNG ATA Conference 2003 - Elke Vogt-Arendt Was ist eine klinische Prüfung? Überprüfung von Wirkung, Nebenwirkung, Dosierung usw. eines neuen Arzneimittels vor Markteinführung.
KLINISCHE PRÜFUNG EINE EINFÜHRUNG ATA Conference 2003 - Elke Vogt-Arendt Was ist eine klinische Prüfung? Überprüfung von Wirkung, Nebenwirkung, Dosierung usw. eines neuen Arzneimittels vor Markteinführung.
Die regulatorischen Strukturen in der Steuerung der Arzneimittelversorgung
 Die regulatorischen Strukturen in der Steuerung der Arzneimittelversorgung Vortrag bei dem Symposium der Deutschen Gesellschaft für Kassenarztrecht am 30. März 2006 in Berlin zu dem Thema Arzneimittelsteuerung
Die regulatorischen Strukturen in der Steuerung der Arzneimittelversorgung Vortrag bei dem Symposium der Deutschen Gesellschaft für Kassenarztrecht am 30. März 2006 in Berlin zu dem Thema Arzneimittelsteuerung
Fachliche Hinweise SGB II. Zweites Buch Sozialgesetzbuch SGB II Fachliche Hinweise. 41 SGB II Berechnung der Leistungen
 Fachliche Hinweise SGB II Zweites Buch Sozialgesetzbuch SGB II Fachliche Hinweise 41 SGB II Berechnung der Leistungen BA Zentrale GS 21 Wesentliche Änderungen Fassung vom 20.10.2014 Rz. 41.11a, 41.11b
Fachliche Hinweise SGB II Zweites Buch Sozialgesetzbuch SGB II Fachliche Hinweise 41 SGB II Berechnung der Leistungen BA Zentrale GS 21 Wesentliche Änderungen Fassung vom 20.10.2014 Rz. 41.11a, 41.11b
Z U L A S S U N G S O R D N U N G. für den Weiterbildungsstudiengang Mergers & Acquisitions
 Z U L A S S U N G S O R D N U N G für den Weiterbildungsstudiengang Mergers & Acquisitions Z U L A S S U N G S O R D N U N G für den Weiterbildungsstudiengang Mergers & Acquisitions an der Westfälischen
Z U L A S S U N G S O R D N U N G für den Weiterbildungsstudiengang Mergers & Acquisitions Z U L A S S U N G S O R D N U N G für den Weiterbildungsstudiengang Mergers & Acquisitions an der Westfälischen
Empfehlungen der Bundesapothekerkammer. für Richtlinien zum Erwerb des Fortbildungszertifikats
 Empfehlungen der Bundesapothekerkammer für Richtlinien zum Erwerb des Fortbildungszertifikats für pharmazeutisch-technische Assistenten, Apothekerassistenten, Pharmazieingenieure, Apothekenassistenten
Empfehlungen der Bundesapothekerkammer für Richtlinien zum Erwerb des Fortbildungszertifikats für pharmazeutisch-technische Assistenten, Apothekerassistenten, Pharmazieingenieure, Apothekenassistenten
Fachprüfungsordnung. für den Master-Studiengang. Angewandte Informatik. an der Otto-Friedrich-Universität Bamberg. Vom 31.
 Fachprüfungsordnung für den Master-Studiengang Angewandte Informatik an der Otto-Friedrich-Universität Bamberg Vom 31. März 2008 (Fundstelle: http://www.uni-bamberg.de/fileadmin/uni/amtliche_veroeffentlichungen/2008/2008-63.pdf)
Fachprüfungsordnung für den Master-Studiengang Angewandte Informatik an der Otto-Friedrich-Universität Bamberg Vom 31. März 2008 (Fundstelle: http://www.uni-bamberg.de/fileadmin/uni/amtliche_veroeffentlichungen/2008/2008-63.pdf)
Tragende Gründe. Vom 18. September 2014
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage IX Festbetragsgruppenbildung Humaninsulin, Gruppe 1 bis 3, in Stufe 1 nach
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage IX Festbetragsgruppenbildung Humaninsulin, Gruppe 1 bis 3, in Stufe 1 nach
Vom 20. Oktober Inhaltsverzeichnis. A. Tragende Gründe und Beschluss. B. Bewertungsverfahren
 Zusammenfassende Dokumentation zum Beschluss des Gemeinsamen Bundesausschusses über eine Nichtänderung der Arzneimittel-Richtlinie: Anlage VI (Off-Label-Use) Intravenöse Immunglobuline (IVIG) bei der Multiplen
Zusammenfassende Dokumentation zum Beschluss des Gemeinsamen Bundesausschusses über eine Nichtänderung der Arzneimittel-Richtlinie: Anlage VI (Off-Label-Use) Intravenöse Immunglobuline (IVIG) bei der Multiplen
ONKOLOGIE C. Düsseldorf
 MDS MDK GKV ONKOLOGIE C Düsseldorf Wiesbaden 09. April 2013 Relevanz klinischer Studien für die Versorgung onkologischer Patienten Sicht des MDK Prof. Dr. med. Axel Heyll Kompetenz Centrum Onkologie der
MDS MDK GKV ONKOLOGIE C Düsseldorf Wiesbaden 09. April 2013 Relevanz klinischer Studien für die Versorgung onkologischer Patienten Sicht des MDK Prof. Dr. med. Axel Heyll Kompetenz Centrum Onkologie der
Katalog zur Inhaltsanalyse von Fachinformationen bezüglich Therapeutischem Drug Monitoring (TDM)
 Katalog zur Inhaltsanalyse von Fachinformationen bezüglich Therapeutischem Drug Monitoring (TDM) Einleitung Fachinformationen (engl. Summary of Product Characteristics, SPC) können Informationen über Therapeutisches
Katalog zur Inhaltsanalyse von Fachinformationen bezüglich Therapeutischem Drug Monitoring (TDM) Einleitung Fachinformationen (engl. Summary of Product Characteristics, SPC) können Informationen über Therapeutisches
Corrigenda. Handbuch, REKOLE 4. Ausgabe 2013
 Version 0.6 Februar 2016 Corrigenda Handbuch, REKOLE 4. Ausgabe 2013 Die Referenzen der Corrigenda beziehen sich immer auf die Papierversion in der jeweiligen Sprache. Die en/ergänzungen sind in roter
Version 0.6 Februar 2016 Corrigenda Handbuch, REKOLE 4. Ausgabe 2013 Die Referenzen der Corrigenda beziehen sich immer auf die Papierversion in der jeweiligen Sprache. Die en/ergänzungen sind in roter
Vorschlag der Bundesregierung
 Vorschlag der Bundesregierung für eine neue Fassung von Artikel 38 (Verhaltensregeln) und für einen neuen Artikel 38a (Einrichtungen der Freiwilligen Selbstkontrolle) der Datenschutz-Grundverordnung (Entwurf)
Vorschlag der Bundesregierung für eine neue Fassung von Artikel 38 (Verhaltensregeln) und für einen neuen Artikel 38a (Einrichtungen der Freiwilligen Selbstkontrolle) der Datenschutz-Grundverordnung (Entwurf)
Vergleich 130a SGV V alt vs neu
 In der folgenden Gegenüberstellung finden Sie in der linken Spalte den alten Text des 130a SGB V und in der rechten Spalte den neuen Text des 130a SGB V, der ab dem 1.8.2010 in Kraft tritt. Die Änderungen
In der folgenden Gegenüberstellung finden Sie in der linken Spalte den alten Text des 130a SGB V und in der rechten Spalte den neuen Text des 130a SGB V, der ab dem 1.8.2010 in Kraft tritt. Die Änderungen
BAnz AT 12.10.2015 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Daimler AG 4T /04/2013
 Daimler AG 4T 2012 29/04/2013 DAG Konzern Prüfungsbericht Konzernabschluss zum 31.12.2012 und zusammengefasster Lagebericht Bestätigungsvermerk des Abschlussprüfers An die Daimler AG, Stuttgart Vermerk
Daimler AG 4T 2012 29/04/2013 DAG Konzern Prüfungsbericht Konzernabschluss zum 31.12.2012 und zusammengefasster Lagebericht Bestätigungsvermerk des Abschlussprüfers An die Daimler AG, Stuttgart Vermerk
Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren
 Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums für Gesundheit 1 Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren Politische Ebene Bundesbehörden Ministerien, insbesondere
Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums für Gesundheit 1 Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren Politische Ebene Bundesbehörden Ministerien, insbesondere
HANSAINVEST Hanseatische Investment GmbH. Besteuerungsgrundlagen gemäß 5 Abs. 1 S. 1 Nr. 1 und Nr. 2 InvStG. Privatvermögen
 Ohne Gewähr. Allein verbindlich sind die Angaben aus den jeweiligen Jahresberichten. Besteuerungsgrundlagen gemäß 1 und 2 Name des Investmentvermögens: SI SafeInvest ISIN: DE000A0MP292 1 c cc) i.s.d. 3
Ohne Gewähr. Allein verbindlich sind die Angaben aus den jeweiligen Jahresberichten. Besteuerungsgrundlagen gemäß 1 und 2 Name des Investmentvermögens: SI SafeInvest ISIN: DE000A0MP292 1 c cc) i.s.d. 3
Regelung der Kassenärztlichen Bundesvereinigung zur Fortbildungsverpflichtung der Vertragsärzte und Vertragspsychotherapeuten nach 95d SGB V
 Regelung der Kassenärztlichen Bundesvereinigung zur Fortbildungsverpflichtung der Vertragsärzte und Vertragspsychotherapeuten nach 95d SGB V Der Vorstand der Kassenärztlichen Bundesvereinigung hat auf
Regelung der Kassenärztlichen Bundesvereinigung zur Fortbildungsverpflichtung der Vertragsärzte und Vertragspsychotherapeuten nach 95d SGB V Der Vorstand der Kassenärztlichen Bundesvereinigung hat auf
Verordnung über den Arbeitszeitschutz - AZSchVO (Anlage 7d zur AVO)
 Verordnung über den Arbeitszeitschutz - AZSchVO (Anlage 7d zur AVO) (VO vom 9. Dezember 1997 ABl. 1997, S. 253, geändert durch VO vom 29. November 2005, ABl. 2005, S. 228, 27. Juni 2008, ABl. 2008, S.
Verordnung über den Arbeitszeitschutz - AZSchVO (Anlage 7d zur AVO) (VO vom 9. Dezember 1997 ABl. 1997, S. 253, geändert durch VO vom 29. November 2005, ABl. 2005, S. 228, 27. Juni 2008, ABl. 2008, S.
Gesetz zur Änderung von bau- und enteignungsrechtlichen Vorschriften sowie der Baumschutzverordnung
 BREMISCHE BÜRGERSCHAFT Drucksache 18/1355 Landtag 18. Wahlperiode 22.04.2014 Mitteilung des Senats vom 22. April 2014 Gesetz zur Änderung von bau- und enteignungsrechtlichen Vorschriften sowie der Baumschutzverordnung
BREMISCHE BÜRGERSCHAFT Drucksache 18/1355 Landtag 18. Wahlperiode 22.04.2014 Mitteilung des Senats vom 22. April 2014 Gesetz zur Änderung von bau- und enteignungsrechtlichen Vorschriften sowie der Baumschutzverordnung
Methodische Fragen zur frühen Nutzenbewertung nach 35a SGB V
 Die frühe Nutzenbewertung nach AMNOG Rechtssymposium des G-BA, Berlin, 16. Nov. 2010 Methodische Fragen zur frühen Nutzenbewertung nach 35a SGB V Jürgen Windeler AMNOG Nutzenbewertung für Arzneimittel
Die frühe Nutzenbewertung nach AMNOG Rechtssymposium des G-BA, Berlin, 16. Nov. 2010 Methodische Fragen zur frühen Nutzenbewertung nach 35a SGB V Jürgen Windeler AMNOG Nutzenbewertung für Arzneimittel
!!!! Sachverständigenauskunft zum Entwurf der Verordnung zur Förderung der Transparenz auf dem Telekommunikationsmarkt
 Verbraucherrechte im Telekommunikationsmarkt stärken Sachverständigenauskunft zum Entwurf der Verordnung zur Förderung der Transparenz auf dem Telekommunikationsmarkt Alexander Leefmann, Linus Neumann,
Verbraucherrechte im Telekommunikationsmarkt stärken Sachverständigenauskunft zum Entwurf der Verordnung zur Förderung der Transparenz auf dem Telekommunikationsmarkt Alexander Leefmann, Linus Neumann,
Tragende Gründe. Vom 21. Juni 2012
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII- Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII- Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
Verfahrenstechnische und methodische Anforderungen an die Bewertung einer Untersuchungs- u. Behandlungsmethode
 Informationsblatt Verfahrenstechnische und methodische Anforderungen an die Bewertung einer Untersuchungs- u. Behandlungsmethode (Bezug zu 2. Kapitel der Verfahrensordnung des G-BA (VerfO), Anlage II,
Informationsblatt Verfahrenstechnische und methodische Anforderungen an die Bewertung einer Untersuchungs- u. Behandlungsmethode (Bezug zu 2. Kapitel der Verfahrensordnung des G-BA (VerfO), Anlage II,
Gliederung Vortrag Patientenrechte: 1. Recht auf Aufklärung
 Gliederung Vortrag Patientenrechte: 1. Recht auf Aufklärung 2. Freie Arztwahl 3. Freie Krankenhauswahl 4. Recht auf Zweitmeinung und Arztwechsel 5. Recht auf Behandlungsdokumentation 1 6. Recht auf Einsicht
Gliederung Vortrag Patientenrechte: 1. Recht auf Aufklärung 2. Freie Arztwahl 3. Freie Krankenhauswahl 4. Recht auf Zweitmeinung und Arztwechsel 5. Recht auf Behandlungsdokumentation 1 6. Recht auf Einsicht
BAnz AT 25.04.2014 B4. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Ordnung über die Zulassung und über die Eignungsprüfung
 Ordnung über die Zulassung und über die Eignungsprüfung für die Studiengänge an der Berufsakademie für Gesundheits- und Sozialwesen Saarland (BA GSS) Gem. 2 des Saarländischen Berufsakademiegesetzes (Saarl.
Ordnung über die Zulassung und über die Eignungsprüfung für die Studiengänge an der Berufsakademie für Gesundheits- und Sozialwesen Saarland (BA GSS) Gem. 2 des Saarländischen Berufsakademiegesetzes (Saarl.
Stellungnahme der Bundesärztekammer
 Stellungnahme der Bundesärztekammer gemäß 91 Abs. 5 SGB V zur Änderung von Anlage I der Richtlinie Methoden vertragsärztliche Versorgung (MVV-RL): Berlin, 27.07.2011 Bundesärztekammer Herbert-Lewin-Platz
Stellungnahme der Bundesärztekammer gemäß 91 Abs. 5 SGB V zur Änderung von Anlage I der Richtlinie Methoden vertragsärztliche Versorgung (MVV-RL): Berlin, 27.07.2011 Bundesärztekammer Herbert-Lewin-Platz
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie
 AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
AMNOG: Wenn Innovation aufs System trifft: Ist das AMNOG System fit für Innovation- Beispiel Onkologie Dr. Jutta Wendel-Schrief Direktor Market Access MSD SHARP & DOHME GMBH Was sind Innovationen? Neue
Der Deutsche Bundestag hat die Petition am 09.06.2011 abschließend beraten und beschlossen:
 Michael Pohl Namensrecht Der Deutsche Bundestag hat die Petition am 09.06.2011 abschließend beraten und beschlossen: Das Petitionsverfahren abzuschließen, weil dem Anliegen nicht entsprochen werden konnte.
Michael Pohl Namensrecht Der Deutsche Bundestag hat die Petition am 09.06.2011 abschließend beraten und beschlossen: Das Petitionsverfahren abzuschließen, weil dem Anliegen nicht entsprochen werden konnte.
Zusammenfassende Dokumentation
 Zusammenfassende Dokumentation über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage IX Festbetragsgruppenbildung Tolperison, Gruppe 1, in Stufe 1 nach 35 Abs. 1 SGB V Vom 19. Dezember 2013 Inhalt
Zusammenfassende Dokumentation über die Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage IX Festbetragsgruppenbildung Tolperison, Gruppe 1, in Stufe 1 nach 35 Abs. 1 SGB V Vom 19. Dezember 2013 Inhalt
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic )
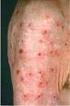 Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Calcineurininhibitoren zur topischen Anwendung: Pimecrolimus und Tacrolimus (Elidel, Douglan und Protopic ) Ergebnisse der europäischen Risiko- Bewertungs-Verfahren Anlass für die Risikobewertungsverfahren
Entwurf einer Verordnung
 Entwurf einer Verordnung des Bundesministeriums für Wirtschaft und Technologie Zweite Verordnung zur Änderung der Arzneimittelpreisverordnung A. Problem Der Festzuschlag, den Apotheken bei der Abgabe verschreibungspflichtiger
Entwurf einer Verordnung des Bundesministeriums für Wirtschaft und Technologie Zweite Verordnung zur Änderung der Arzneimittelpreisverordnung A. Problem Der Festzuschlag, den Apotheken bei der Abgabe verschreibungspflichtiger
Verwaltungsbetriebswirt/in (HVSV)
 Prüfungsordnung (vom 1. Januar 2012, StAnz. vom 09.04.2012, S. 447 ff.) 1 Ziel des Lehrgangs 2 Zulassung zum Lehrgang 3 Art, Dauer und Durchführung des Lehrgangs 4 Teilgebiete und Stoffplan 5 Leistungsnachweise
Prüfungsordnung (vom 1. Januar 2012, StAnz. vom 09.04.2012, S. 447 ff.) 1 Ziel des Lehrgangs 2 Zulassung zum Lehrgang 3 Art, Dauer und Durchführung des Lehrgangs 4 Teilgebiete und Stoffplan 5 Leistungsnachweise
Antrag auf Entlassung aus der Verschreibungspflicht. -Doramectin-
 Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Antrag auf Entlassung aus der Verschreibungspflicht Antrag auf Entlassung von Doramectin aus der Verschreibungspflicht für die topische Anwendung bei Königspython, Abgottschlange und Bartagame bei einem
Workshop Perspektiven einer soziale gerechten Beschaffung in Nordrhein-Westfalen 27. Januar 2015, Düsseldorf
 Workshop Perspektiven einer soziale gerechten Beschaffung in Nordrhein-Westfalen 27. Januar 2015, Düsseldorf CORNELIUS BARTENBACH HAESEMANN & PARTNER Rechtsanwältin Katharina Strauß Köln 2 I Cornelius,
Workshop Perspektiven einer soziale gerechten Beschaffung in Nordrhein-Westfalen 27. Januar 2015, Düsseldorf CORNELIUS BARTENBACH HAESEMANN & PARTNER Rechtsanwältin Katharina Strauß Köln 2 I Cornelius,
BAnz AT 23.04.2015 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Zusammenfassung. 5 Zusammenfassung
 5 Zusammenfassung Die Diskussion über den optimalen Operationszeitpunkt der frakturierten Hüfte wird seit langem kontrovers geführt. Ziel dieser Arbeit war zu überprüfen, ob die in Deutschland derzeit
5 Zusammenfassung Die Diskussion über den optimalen Operationszeitpunkt der frakturierten Hüfte wird seit langem kontrovers geführt. Ziel dieser Arbeit war zu überprüfen, ob die in Deutschland derzeit
Evaluationskonzepte bei neuen Methoden. Analyse und Konsequenz des GKV.SV
 Evaluationskonzepte bei neuen Methoden Analyse und Konsequenz des GKV.SV Dr. Diedrich Bühler Dr. Diedrich Bühler Überblick I) Situation und Position des GKV SV II) Methodenbewertung, Selbstverwaltung /
Evaluationskonzepte bei neuen Methoden Analyse und Konsequenz des GKV.SV Dr. Diedrich Bühler Dr. Diedrich Bühler Überblick I) Situation und Position des GKV SV II) Methodenbewertung, Selbstverwaltung /
Entwurf eines Gesetzes zur Änderung des Zweiten Buches Sozialgesetzbuch und des Finanzausgleichsgesetzes
 Deutscher Bundestag Drucksache 16/3269 16. Wahlperiode 07.11.2006 Gesetzentwurf der Fraktionen der CDU/CSU und SPD Entwurf eines Gesetzes zur Änderung des Zweiten Buches Sozialgesetzbuch und des Finanzausgleichsgesetzes
Deutscher Bundestag Drucksache 16/3269 16. Wahlperiode 07.11.2006 Gesetzentwurf der Fraktionen der CDU/CSU und SPD Entwurf eines Gesetzes zur Änderung des Zweiten Buches Sozialgesetzbuch und des Finanzausgleichsgesetzes
Rabatte bei Arzneimitteln: Hohe Qualität, ohne Zuzahlung für Sie. Bosch BKK. Gesetzliche Krankenund Pflegeversicherung
 Rabatte bei Arzneimitteln: Hohe Qualität, ohne Zuzahlung für Sie. Bosch BKK Gesetzliche Krankenund Pflegeversicherung Hohe Qualität zu günstigeren Preisen. Als Versicherte der Bosch BKK erhalten Sie die
Rabatte bei Arzneimitteln: Hohe Qualität, ohne Zuzahlung für Sie. Bosch BKK Gesetzliche Krankenund Pflegeversicherung Hohe Qualität zu günstigeren Preisen. Als Versicherte der Bosch BKK erhalten Sie die
Abschlussarbeiten am Lehrstuhl für ABWL, Absatzwirtschaft und Marketing. Handreichung für Interessenten
 Abschlussarbeiten am Lehrstuhl für ABWL, Absatzwirtschaft und Marketing Handreichung für Interessenten 05. Juli 2016 Voraussetzungen Neben einem inhaltlichen Interesse an Marketing und damit verwandten
Abschlussarbeiten am Lehrstuhl für ABWL, Absatzwirtschaft und Marketing Handreichung für Interessenten 05. Juli 2016 Voraussetzungen Neben einem inhaltlichen Interesse an Marketing und damit verwandten
Marktentwicklung: Umsatz-, Mengen- und Strukturentwicklung bei Fertigarzneimitteln
 Faktenblatt Thema: Arzneimittelmarkt Ausgaben Arzneimittel (Quelle: Amtliche Statistik KV 45) 2014: 33,3 Mrd. Euro 2013: 30,4 Mrd. Euro 2012: 29,6 Mrd. Euro 2011: 29,2 Mrd. Euro Ausgaben für Arzneimittel
Faktenblatt Thema: Arzneimittelmarkt Ausgaben Arzneimittel (Quelle: Amtliche Statistik KV 45) 2014: 33,3 Mrd. Euro 2013: 30,4 Mrd. Euro 2012: 29,6 Mrd. Euro 2011: 29,2 Mrd. Euro Ausgaben für Arzneimittel
Therapeutisches Drug Monitoring der Antidepressiva Amitriptylin, Clomipramin, Doxepin und Maprotilin unter naturalistischen Bedingungen
 Aus der Klinik und Poliklinik für Psychiatrie, Psychosomatik und Psychotherapie der Universität Würzburg Direktor: Professor Dr. med. J. Deckert Therapeutisches Drug Monitoring der Antidepressiva Amitriptylin,
Aus der Klinik und Poliklinik für Psychiatrie, Psychosomatik und Psychotherapie der Universität Würzburg Direktor: Professor Dr. med. J. Deckert Therapeutisches Drug Monitoring der Antidepressiva Amitriptylin,
Die Kombination von Medizinprodukten. SystemCheck
 Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
Die Kombination von Medizinprodukten SystemCheck Fachtagung der FKT 12.06.2008 Untertitel Die Prüfung und Bewertung von medizinischen elektrischen Systemen mit rechtssicherer Dokumentation zum Schutz von
Qualität des ambulanten Pflegedienstes
 Qualität des ambulanten Pflegedienstes Häusliche Alten- und Krankenpflege Volker Krause KG Tel.: 0214-26004500 Fax: 0214-260045130 info@volker-krause-kg.de www.volker-krause-kg.de Gesamtergebnis Pflegerische
Qualität des ambulanten Pflegedienstes Häusliche Alten- und Krankenpflege Volker Krause KG Tel.: 0214-26004500 Fax: 0214-260045130 info@volker-krause-kg.de www.volker-krause-kg.de Gesamtergebnis Pflegerische
Ordnung über den Zugang für den konsekutiven Master- Studiengang Chemie.
 Verwaltungshandbuch Ordnung über den Zugang für den konsekutiven Master- Studiengang Chemie an der Technischen Universität Clausthal, Fakultät für Natur- und Materialwissenschaften Vom 04. November 2008
Verwaltungshandbuch Ordnung über den Zugang für den konsekutiven Master- Studiengang Chemie an der Technischen Universität Clausthal, Fakultät für Natur- und Materialwissenschaften Vom 04. November 2008
Landessozialgericht Berlin-Brandenburg
 Landessozialgericht Berlin-Brandenburg Die in den Beschlüssen des Beklagten vom 26. August 2009 und vom 9. Mai 2012 enthaltenen Festbetragsfestsetzungen für den Wirkstoff Paliperidon werden aufverkündet
Landessozialgericht Berlin-Brandenburg Die in den Beschlüssen des Beklagten vom 26. August 2009 und vom 9. Mai 2012 enthaltenen Festbetragsfestsetzungen für den Wirkstoff Paliperidon werden aufverkündet
Professor Dr. Peter Krebs. Unlauterkeit irreführender geschäftlicher Handlungen, 5 UWG
 Professor Dr. Peter Krebs Arbeitsgliederung UWG Unlauterkeit irreführender geschäftlicher Handlungen, 5 UWG (Achtung: Markenrecht kann nach h.m Sperrwirkung entfalten) A Vorrangige Prüfung von 3 Abs. 3
Professor Dr. Peter Krebs Arbeitsgliederung UWG Unlauterkeit irreführender geschäftlicher Handlungen, 5 UWG (Achtung: Markenrecht kann nach h.m Sperrwirkung entfalten) A Vorrangige Prüfung von 3 Abs. 3
zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie: Anlage III Nummer 2 Alkoholentwöhnungsmittel
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der -Richtlinie: Anlage III Nummer 2 Alkoholentwöhnungsmittel Vom 20. Februar 2014 Inhalt 1. Rechtsgrundlage... 2 2. Eckpunkte
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der -Richtlinie: Anlage III Nummer 2 Alkoholentwöhnungsmittel Vom 20. Februar 2014 Inhalt 1. Rechtsgrundlage... 2 2. Eckpunkte
Johanniskraut Metaanalyse 2005
 Johanniskraut Metaanalyse 2005 Seit 1983 wurden 37 randomisierte klinische Studien mit Johanniskraut-Präparaten publiziert Davon: 26 Placebo-kontrolliert, 14 Verum-kontrolliert Studiendauer: 4 Wochen (10
Johanniskraut Metaanalyse 2005 Seit 1983 wurden 37 randomisierte klinische Studien mit Johanniskraut-Präparaten publiziert Davon: 26 Placebo-kontrolliert, 14 Verum-kontrolliert Studiendauer: 4 Wochen (10
Überwachungsprogramm gemäß 52a Bundes-Immissionsschutzgesetz und 9 Industriekläranlagen-Zulassungs- und Überwachungsverordnung
 Überwachungsprogramm gemäß 52a Bundes-Immissionsschutzgesetz und 9 Industriekläranlagen-Zulassungs- und Überwachungsverordnung Gemäß 52a Bundes-Immissionsschutzgesetz (BImSchG) und 9 Industriekläranlagen-Zulassungs-
Überwachungsprogramm gemäß 52a Bundes-Immissionsschutzgesetz und 9 Industriekläranlagen-Zulassungs- und Überwachungsverordnung Gemäß 52a Bundes-Immissionsschutzgesetz (BImSchG) und 9 Industriekläranlagen-Zulassungs-
