Lernkontrollen Medizinerpraktikum LK 3. - eine kleine Sammlung verschiedener, alter Lernkontrollen mit Lösungen -
|
|
|
- Otto Frank
- vor 5 Jahren
- Abrufe
Transkript
1 Lernkontrollen Medizinerpraktikum LK 3 - eine kleine Sammlung verschiedener, alter Lernkontrollen mit Lösungen -
2 Lernkontrollen zur Übung - LK 3a SS ) (2.5) Welche absolute Konfiguration (R oder S) besitzt folgende Verbindung? Geben Sie bitte auch die Priorität für die einzelnen Substituenten an! 2 N Br N C 3 Benennen Sie bitte folgende Verbindung nach IUPAC-Nomenklatur! C 3 3 C C 3 C 3 3 C C 3 Wie ist der Retentionsfaktor definiert? Zeichnen Sie bitte zwei Konstitutionsisomere der Summenformel C 5 10, die aus unterschiedlichen Substanzklassen stammen! 5.) (1.5) Bitte vervollständigen Sie folgende Reaktionsgleichung! N N 2 N N 2
3 1.) Prioritäten: 1. Br 2. N C 3 3. N absolute Konfiguration: (S) Ethyl-2,4,6-trimethylnonan 2.0 R f = Laufstrecke Subs tanz Laufstrecke Laufmittel und und 5.) 2 N 2 N + N N N N N N 2
4 Lernkontrollen zur Übung - LK 3a SS ) (2.5) Falsch oder richtig? Bitte geben Sie nur Antworten, wenn Sie sich sicher sind! Falsche Antworten führen zu Punktabzug! Aussage falsch oder richtig? Die stationäre Phase bei der Chromatographie ist immer ein fester Stoff! Enantiomere besitzen immer gleiche Siedepunkte! Diastereomere besitzen immer gleiche Schmelzpunkte! Cycloalkane haben die Formel C n 2n! Sekundäre Alkohole werden durch Kaliumdichromat nicht oxidiert! (3.5) (3.5) Sie geraten in der Sylvesternacht in eine Polizeikontrolle und müssen in das berühmtberüchtigte Röhrchen blasen. Dabei wird Ethanol durch Reaktion mit Kaliumdichromat nachgewiesen. Welche Farbreaktion beobachtet man? Zeigen Sie bitte anhand der Reaktionsgleichungen, was passiert! Erklären Sie bitte kurz, wie Sie 1-Butanol, Essugsäure und eptan-4-on mit ilfe der Dünnschichtchromatographie unterscheiden können! () Geben Sie bitte ein Beispiel für ein Nucleophil!
5 1.) Aussage Die stationäre Phase bei der Chromatographie ist immer ein fester Stoff! Enantiomere besitzen immer gleiche Siedepunkte! Diastereomere besitzen immer gleiche Schmelzpunkte! Cycloalkane haben die Formel C n 2n! Sekundäre Alkohole werden durch Kaliumdichromat nicht oxidiert! falsch oder richtig? FALSC RICTIG FALSC RICTIG FALSC je orange d grün 3C Cr d Cr C 3 C 3C 3 C + Cr d Cr C 3 C Gleichung Stöchiometrie polar Essigsäure stat. Phase: polar > 1-Butanol > unpolar eptan-4-on mob. Phase: unpolar 1.5 je Rf-Wert: Ac < 1-Butanol < eptan-4-on )
6 Lernkontrollen zur Übung - LK 3b SS ) (4.0) (3.0) (1.0) a) Zeichen Sie bitte alle Konstitutionsisomere von Butanol! b) Welche dieser Verbindungen ist chiral? Zeichen Sie bitte das R-Enantiomer dieser Verbindung so, daß dessen Stereochemie eindeutig erkennbar ist (z.b. als Keilstrichformel)! Zeigen Sie bitte anhand des Kästchenschemas der Elektronenkonfiguration des Kohlenstoffs, wie man sich das Zustandekommen der sp-ybridisierung vorzustellen hat! Erläutern Sie bitte kurz (nur ein Satz!) das allgemeine Prinzip der Chromatographie! Zeichnen Sie bitte die möglichen Sesselkonformationen von cis-1,3--dihydroxycyclohexan!
7 1.) chiral: 1.5 Diagramm Grundzustand d Diagramm angeregt d Diagramm hybridisiert unterschiedliche Verfahren zur Stofftrennung durch Verteilung der zu trennenden Stoffe zwischen einer stationären und einen mobilen Phase 1.0 je 1.0
8 Lernkontrollen zur Übung - LK 3a WS 1997/98 1.) (4.0) Vervollständigen Sie bitte die folgende Tabelle! Zeichnen Sie optisch aktive Substanzen so, dass deren Stereochemie erkennbar ist (z.b. Keilstrichformel)! Substanzklasse Name der Verbindung Strukturformel 2-Methylpropansäure S-3-Amino-2-Methylpentan (3.0) Zeichnen Sie bitte die Strukturformel von 2-Methyl-1-buten-3-in! Geben Sie für jedes C-Atom die ybridisierung an! Welche der folgenden Aussagen sind richtig, welche falsch? Aussage Konformationen sind Energieminima Die stationäre (unbewegliche) Phase bei der Chromatographie ist immer ein Feststoff Retentionsfaktoren liegen zwischen 0 und 1 Diastereomere besitzen gleiche chemische und physikalische Eigenschaften richtig oder falsch? (1.0) Sie haben ein Diastereomer mit 3 asymetrischen C-Atomen vorliegen. Wieviele Stereoisomere dieser Verbindung sind möglich (Formel und Endwert)?
9 1.) Substanzklasse Name der Verbindung Strukturformel ALKEN 2,5-DIMETYL-TRANS-3-EXEN Name: trans: CARBNSÄURE 2-Methylpropansäure AMIN S-3-Amino-2-Methylpentan N 2 Struktur: Stereoformel richtig richtige Strukturformel pro richtige ybridisierung 1 falsch 2 falsch 3 richtig 4 falsch N = 2 n e 8 Stereoisomere
10 Lernkontrollen zur Übung - LK 3b WS 1997/98 1.) (2.5) (1.0) (3.0) Geben Sie bitte die Reaktionsgleichung (nicht den vollständigen Mechanismus) für die Umsetzung von 2-Butanon mit 2,4-Dinitrophenylhydrazin an! Um welchen Reaktionstyp handelt es sich? Was verstehen Sie unter Mesomerie? Zeichnen Sie das R-Enantiomer von 1-Brom-1-chlorethan stereochemisch eindeutig (z.b. als Keilstrichformel) und geben Sie die Reihenfolge der Prioritäten der Substituenten an! Geben Sie die Strukturformeln für zwei Konstitutionsisomere Ihrer Wahl an und benennen Sie die von Ihnen gewählten Verbindungen nach IUPAC! 5.) (1.5) Warum geht Toluol (Methylbenzol) keine elektrophile Addition (A E ) mit Br 2 ein?
11 1.) N-N-Ph(N 2 ) N 2 2 N Ph(N 2 ) 2 Kondensationsreaktion oder A N realer elektronischer Zustand eines Moleküls läßt sich nicht mit nur einer Valenzstrukturformel beschreiben Br 3 C Cl R Br 2. Cl 3. C 3 4. pro Struktur je pro Namen je 5.) keine freien Doppelbindungen aromatisches -System 1.0 (im Gegenteil zu Alkenen)
12 Lernkontrollen zur Übung - LK 3c WS 1997/98 1.) (3.0) Bitte benennen Sie folgende Verbindungen nach IUPAC! a) b) c) Br (2.5) Geben Sie bitte den Namen und die Strukturformel der Produkte an, die bei der xidation von 1-Butanol mit Kaliumdichromat entstehen! a) Zeichnen Sie die Strukturformel von 4-Iod-2-methylheptan! b) Kennzeichnen Sie das asymetrische C-Atome in Ihrer Strukturformel! c) Zeichnen Sie das S-Enantiomer, so daß seine Stereochemie eindeutig zu erkennen ist (z.b. Keilstrichformel)! (1.5) 5.) (1.0) Was sind Isomere? Nennen Sie bitte ein Reagenz zum Nachweis von Aminen!
13 1.)a) trans-4-methyl-2-penten Name trans b) 3-Methylbutanal 1.0 c) 5-Brom-3,3-dimethyl-2-pentanol 1.0 richtiges auptfragment bei b) und c): noch Butanal Butansäure a) Formel b) I * c) (C 3 ) 2 C- 2 C I C 2 -C 2 5 Zeichnung 1.0 S-Enantiomer Verbindungen (gl. Summenformel) mit unterschiedlicher (Sequenz) oder (räumlicher Anordnung) der Atome bzw. untersch. physikalischen und chemischen Eigenschaften 5.) Benzolsulfonsäurechlorid / Na oder Pikrinsäure oder alogenalkan oder...
14 Lernkontrollen zur Übung - LK 3a SS ) Benennen Sie folgende Verbindungen nach IUPAC! a) b) N 2 (1.0) (3.0) 5.) Auf welchem Prinzip beruht die Trennwirkung in der Chropmatographie? Sie setzen Diethylamin und Triethylamin in wässriger Natronlauge mit Benzolsulfonsäurechlorid um. Geben Sie jeweils die Reaktionsgleichung an! Welche strukturelle Voraussetzung im Amin ist für den Ablauf der Reaktion entscheidend? Zeichnen Sie für eines der Isomere von 3,4-Dichlorhexan die Fischer-Projektion. Wie viele Isomere dieser Verbindung gibt es (kurze Begründung)? Welche Bedingungen müssen erfüllt sein, damit ein Molekül als aromatisch bezeichnet werden kann?
15 1.)a) trans-2,5-dimethyl-3-hexen 1.0 b) 3-Methylpentansäureamid 1.0 (Verteilung) der zu trennenden Stoffe zwischen einer (stationären und einer mobilen Phase). + Na N + PhS 2 Cl NaCl N-S 2 -Ph 1.0 N + PhS 2 Cl + Nah 1.0 N-Atom des Amins muß mind. 1 -Atom tragen, da die Reaktion sonst nicht abläuft. 1.0 ein beliebiges Isomer in Fischer-Projektion Isomere, da eine meso-verbindung möglich ist ) 4n + 2] -Elektronen (cyclisches) Molekül mit (konjugierten DB) planar
16 Lernkontrollen zur Übung - LK 3b SS ) (2.5) (1.0) (3.5) (3.0) Geben Sie bitte die Reaktionsgleichung (nicht den volständigen Mechanismus!) für die Umsetzung von 2-Butanon mit 1-Propanal zum albacetal im basischen Medium an! Um welchen Reaktionstyp handelt es sich? Wie lassen sich Enantiomere physikalisch unterscheiden? Zeichnen Sie die Strukturformel von 3-Brom-2-methylpentan und kennzeichnen Sie dasasymetrische Kohlenstoffatom! Zeichnen Sie das R-Enantiomer sterisch eindeutig (z.b. als Keilstrichformel) und geben Sie die Prioritäten der Substituenten an! Geben Sie jeweils ein Beispile für folgende Substanzklassen an (Strukturformel und Name): a) dreiwertiger Alkohol b) sekundäres Amin c) Carbonsäureester
17 1.) A N Drehwert des linear polarisierten Lichtes besitzt ein anderes Vorzeichen nach dem Durchlaufen der Proben der reinen Enantiomere 1.0 * Br Br C 3 7 C Br C 3 7 C 2 5 wenn die Substanzklasse richtig ist: je
18 Lernkontrollen zur Übung - LK 3c SS ) (1.0) (3.0) 5.) Geben Sie die Strukturformel und den Namen des Reduktions- sowie des xidationsproduktes von Ethanal an! Was ist en rbital? Zeichnen Sie die Strukturformel von 2-Brom-4-methyl-3-hexanol und kennzeichnen Sie alle asymetrischen Kohlenstoffatome! Wie viele Isomere dieser Verbindung gibt es? rdnen Sie die folgenden Verbindungen nach zunehmender Polarität: Ethanol, n-pentan, Essigsäure und Trichlormethan! Geben Sie jeweils ein Beispiel (Strukturformel!) an für: a) ein Enantiomerenpaar! b) zwei geometrische Isomere!
19 1.) Reduktion: Ethanol xidation Ethansäure / Essigsäure mathematisch: rbital ist die Wellenfkt. eines Elektrons in einem Atom/Molekül anschaulich: rbital beschreibt die Aufenthaltswahrscheinlichkeit eines Elektrons in einem Atom/Molekül 1.0 Br * * * 1.0 pro richtigem asy. C-Atom Isomere: 2 3 = 8 n-pentan Trichlormethan Ethanol Essigsäure < Zunahme 5.) pro Paar, wenn die Isomerie stimmt 1.0 pro Strukturformel
20 Lernkontrollen zur Übung - LK 3a WS 1998/99 1.) (2.5) (2.5) Die elektrophile Addition von Brom an cis-2-buten liefert 2 mögliche Produkte. Zeichnen Sie diese in der Sägebock-Projektion! Um welche Art von Isomeren handelt es sich? Wie lassen sich 1-Propanol und 2-Propanol durch eine chemische Reaktion unterscheiden? Geben Sie die jeweiligen Reakionsgleichungen an! (3.0 Zeichnen Sie das S-Enantiomer von 2-Chlor-2-butanol stereochemisch eindeutig (z.b. als Keilstrichformel) und geben Sie die Reihenfolge der Prioritäten der Substituenten an! Welche Aussage über einen aromatischen Kohlenwasserstoff trifft nicht zu? Begründen Sie bitte kurz Ihre Antwort! a) Ein aromatischer Kohlenwasserstoff ist immer cyclisch. b) Ein aromatischer Kohlenwasserstoff ist immer planar. c) Ein aromatischer Kohlenwasserstoff besitzt immer konjugierte Doppelbindungen. d) Ein aromatischer Kohlenwasserstoff besitzt immer sechs -Elektronen.
21 1.) Enantiomere Br 3 C C 3 Br Br 3 C C 3 Br x. x. x. 3 C Cl S C Cl C 2 5 C 3 d) 1.0 ückel-regel: Elektronen 1.0 (4n + 2)
22 Lernkontrollen zur Übung - LK 3a SS ) (2.5) Geben Sie bitte den vollständigen Mechanismus für die Umsetzung von 2-Propanon mit Wasser in saurer Lösung an! Zu welcher Substanzklasse gehörtdie entstehende Verbindung? (1.5) Welche der folgenden Verbindungen ist kein ückel-aromat? Begründen Sie kurz Ihre Antwort! a) b) c) (2.5) (3.0) a) Zeichnen Sie bitte die Strukturformel von 2-Butanol! b) Kennzeichnen Sie das asymetrische C-Atom in Ihrer Strukturformel! c) Zeichnen Sie das R-Enantiomer, so dass seine Stereochemie eindeutig zu erkennen ist (z.b. als Keilstrichformel)! Zeichnen Sie das rbitalbild von Acetylen (Ethin) und kennzeichnen Sie alle Bindungstypen eindeutig! 5.) () Nennen Sie bitte ein Nachweisreagens für Aldehyde!
23 1.) C (Carbonyl-) ydrat c 4n + 2] -Elektronen-Regel für c) nicht erfüllt 1.0 N 2 * N 2 C C 2 5 (R) Bild CC 2 CC CC C 5.) Name oder Formel
24 Lernkontrollen zur Übung - LK 3b SS ) (3.5) (1.0) (3.0) (2.5) Geben Sie die stöchiometrische Gleichung für die xidation von 2-Pentanol mit Dichromat-Ionen an! Was versteht man in der organischen Chemie unter dem Begriff Tautomerie? Zeichnen Sie die Strukturformel von a) 3-Methylcyclobuten b) N-Ethyl-N-methylbutanamin c) 4-Brom-5-ethyl-2-octanon! Zeichnen Sie bitte das rbitalbild von Ethen und kennzeichnen Sie alle Bindungstypen eindeutig. Wie sind die Kohlenstoffatome hybridisiert?
25 1.) 3 +Cr d 2Cr plus für richtige Stöchiometrie Umwandlung zweier Konstitutionsisomere ineinander durch Umlagerung eines -Atoms unter gleichzeitiger Verschiebung einer Doppelbindung a) b) N c) Br Bild CC CC C sp 2
26 Lernkontrollen zur Übung - LK 3c SS ) (2.5) (1.0) (3.5) Geben Sie bitte ein Beispiel für eine meso-verbindung an! Zeichnen Sie die von Ihnen gewählte Verbindung in der Fischer-Projektion und benennen Sie die Verbindung! Warum zeigen meso-verbindungen keine optische Aktivität? Zeichnen Sie bitte die Strukturformel von 4-ydroxypentanal! Geben Sie bitte die stöchiometrisch richtige Gleichung für die Umsetzung von Butanal mit Fehling-Lösung an! (1.5) Benennen Sie die folgende Verbindung nach IUPAC! 5.) (1.5) Auf welchem Prinzip berucht die Trennwirkung in der Chromatographie?
27 1.) 5.)
28 Lernkontrollen zur Übung - LK 3a WS 1999/00 1.) (4.0) Vervollständigen Sie bitte die folgende Tabelle! Substanzklasse Name der Verbindung Strukturformel sekundärer Alkohol R 3 Chlor 1 buten (2.5) (2.5) Geben Sie bitte die Reaktionsgleichung (nicht Mechanismus) für die Kondensationsreaktion von Cyclohexanon mit 2,4-Dinitrophenylhydrazin an! Warum bezeichnet man diese Reaktion als Kondensationsreaktion? Zeichnen Sie das rbitalbild von Ethen und kennzeichnen Sie alle Bindungstypen! Wie sind die Kohlenstoffatome hybridisiert? (1.0) Nennen Sie bitte zwei Nucleophile!
29 1.) Substanzklasse Name der Verbindung Strukturformel sekundärer Alkohol ALKEN R 3 Chlor 1 buten Cl Cl 1.0 ALDEYD 2-ETYL-3-METYLPENTANAL + N 2 -NPh(N 2 ) 2 N + N Ph(N 2 ) 2 2 Wasserabspaltung: Bild CC CC C sp 2 je
30 Lernkontrollen zur Übung - LK 3a WS 2000/01 1.) (1.5) (3.0) 5.) (1.5) Zeichnen Sie 1,2-Butadien und geben Sie die ybridisierugn aller Kohlenstoffatome an! Für viele aromatische Verbindungen werden Trivialnamen verwendet. Geben Sie zwei Beispiele (Strukturformel und Name)! Zeichnen Sie die Strukturformeln von 2-Chlor.3.penten-1-ol und 2,3-Dimethylpentan und kennzeichnen Sie jeweils das asymetrische C-Atom! Zeichnen Sie von beiden Verbindungen das R-Enantiomer stereochemisch eindeutig in der Keilstrichformel! Geben Sie die Reaktionsgleichung für die Umsetzung von 1-Propanol mit Propanal in saurer Lösung an! Zu welcher Substanzklasse gehört das Produkt? Geben Sie ein Beispiel für ein mesomeriestabilisiertes Ion (Strukturformeln) und erklären Sie kurz die Bedeutung!
31 1.) sp sp 3 Zeichnung 2 richtige (jedoch nicht 2 * sp 2 ) je Beispiel je Name * Cl * je R-Enantiomer + + Vollacetal 5.) 2 richtige Grenzstrukturen je Erklärung: realer elektr. Zustand eines Moleküls läßt sich exakt nicht mit einer Valenzformel beschreiben
32 Lernkontrollen zur Übung - LK 3a SS ) a) Zeichnen Sie eine Verbindung, in welcher sp 3 -, sp 2 - und sp-hybridisierte C-Atome vorkommen! b) Benennen Sie die Verbindung und kennzeichnen Sie je ein sp 3 -, sp 2 - und sp-hybridi siertes C-Atom! Zeichnen Sie je zwei mögliche Konstititionsisomere der Summenformel a) C 4 10 und b) C 5 10! (3.0) 5.) (1.0) Wie reagiert eine Carbonylverbindung mit ydrazin? Geben Sie die Reaktionsgleichung für eine Carbonylverbindung Ihrer Wahl und der Namen für die entstehende Substanzklasse an! Zeichnen Sie S-2-Iodbutan, R-2-ydroxy-2-methylbutanal und S-3-Methyl-1-penten- 4-in stereochemisch eindeutig in der Keilstrichformel! Gegeben sind Phenol und Ethanol. Welche Verbindung reagiert saurer? Begründen Sie Ihre Antwort kurz in Worten (keine Strukturen notwendig)!
33 1.) Zeichnung Name ybridisierung 2* je + 2 N-N 2 N - 2 N 2 ydrazon I je R / S richtg 5.) Phenol Anion ist mesomeriestabilisiert
34 Lernkontrollen zur Übung - LK 3b SS ) (3.0) a) Zeichnen Sie 2-Butinal und geben Sie die ybridisierung für alle C-Atome an! b) Benennen Sie die folgenden Verbindungen! N 2 Br N Br (2.5) 5.) () Setzen Sie Propanon mit einem primären Amin Ihere Wahl unter Kondensation zum Imin um (Reaktionsgleichung)! Wie ist das N-Atom im Edukt hybridisiert? a) Gegeben ist 2-Methyl-4-hexin-3-ol (zeichen!). b) Zeichnen Sie ein Enantiomer Ihrer Wahl und entscheiden Sie, ob esr- oder S-Konfiguration hat! c) Durch welche Eigenschaft läßt sich ein R-Enantiomer von einem S-Enantiomer unterscheiden? Zeichnen Sie Toluol und Methylcyclohexan und nennen Sie drei Punkte, in welchen sich die beiden Verbindungen unterscheiden! Zeichnen Sie die energetisch günstigste Anordnung von 1,2-Dibromethan in der Newmanprojektion!
35 1.)a) sp 3 sp sp 2 Zeichnung ybridisierung 2* b) cis-1,2-dibromcyclopentan N-Ethyl-3-pentanamin Anilin N: sp 3 -hybridisiert + 2 NR N + 2 R Zeichnung R-/S- Zeichnung R / S polarisiertes Licht Zeichnung je Unterschiede je 5.)
36 Lernkontrollen zur Übung - LK 3c SS ) Zeichen bzw. benennen Sie folgende Verbindungen! a) b) Cl Cl Cl Cl (2.5) c) N,N-Diethyl-2-hexanamin d) 1,2,3-Propantriol a) Was versteht man unter Diastereomeren (Erklärung in Worten)? b) Zeichen Sie ein Diastereomerenpaar (Strukturen in Fischer-Projektion) und benennen Sie die von Ihnen gewählte Verbindung! a) Zeichnen Sie das Kästchenmodell für den Grundzustand des Kohlenstoffatoms (beschriften!). b) Im Methan existieren 4 gleichartige C--Bindungen. Wie nennt man das Modell zur Erklärung dieser Eigenschaft (Name)? c) Wie groß ist der Winkel zwischen C--Bindungen im Methan? (1.0) Bei der abgebildeten Verbindung handelt es sich um β-pinen. Welche Aussage trifft nicht zu (kurze Begründung)? a) β-pinen enthält kein sp-hybridisiertes C-Atom b) β-pinen ist ein cyclischer Kohlenwasserstoff c) β-pinen enthält 3 asymetrische C-Atome d) Bromwasser entfärbt sich bei Zugabe von β-pinen 5.) (2.5) Gegeben ist 2-Chlorpropanal. a) Von welcher Verbindung ist die 2-Chlorpropanal das xidationsprodukt (Name oder Struktur)? b) Setzen Sie 2-Chlorpropanal mit 2-Butanol zum Vollacetal um (Reaktionsgleichung)! In welchem Medium arbeiten Sie?
37 1.) 5.)
38 Lernkontrollen zur Übung - LK 3d SS ) (2.5) (3.0) a) Zeichnen Sie ein sp 2 -hybridisiertes Kohlenstoffatom und beschriften Sie die jeweiligen rbitale! b) Wie gross ist der Winkel zwischen den ybridorbitalen? c) Welche Substanzklasse enthält sp 2 -hybridisierte C-Atome? Sie setzen N-Ethyl-1-butanamin mit Benzolsulfonsäurechlorid in wässriger Na um. a) Name der Reaktion? b) Reaktionsgleichung? c) Beobachtung? Zeichnen Sie R-3-Chlor-1-penten, S-3-Butin-2-ol und R-4-Ethyl-3-iod-3-methylhexan stereochemisch eindeutig in der Keilstrichformel! a) Zeichnen Sie einen aromatischen Kohlenwasserstoff und benennen Sie ihn! b) Welche Aussage über aromatische Kohlenwasserstoffe trifft nicht zu (Begründung!)? I II III IV Ein aromatischer Kohlenwasserstoff enthält sp 2 -hybridisierte C-Atome. Ein aromatischer Kohlenwasserstoff besitzt immer sechs -Elektronen. Ein aromatischer Kohlenwasserstoff ist immer cyclisch. Ein aromatischer Kohlenwasserstoff besitzt konjugierte Doppelbindungen. 5.) () Nennen Sie ein Nucleophil!
39 1.) 5.)
Prof. Dr. Th. K. Lindhorst, SS 2003, Übungsklausur. Übungsklausur. zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, OC I
 Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
b) Zeichnen Sie die beiden möglichen Isomere der Aldol-Kondensation und bezeichnen Sie die Stereochemie der Produkte.
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik und der Lehrämter (
 Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik und der Lehrämter ( 01.10.2010, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th. Russ Vorname:...
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik und der Lehrämter ( 01.10.2010, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th. Russ Vorname:...
Übung 9: Aufbau und Struktur organischer Verbindungen Übung für Medizinische Biologen - Jun.-Prof. Dr. Michael Giese.
 Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und Nebenfächer (
 Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
Aufgabe S. 2/a (2 Punkte) Wodurch können Sie 2-Hexen von 2-Methylpentan unterscheiden?
 16-2 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
16-2 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 30.07.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel CH 2 O ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 30.07.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel CH 2 O ein, die die folgenden Eigenschaften
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 4 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung zeigt eine positive Fehling-Probe. -
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 4 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung zeigt eine positive Fehling-Probe. -
Die Verwendung von Rot- und Bleistift sowie Tipp-Ex ist untersagt!!!
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Aufgabe S. 2/a (2 Punkte) Wodurch können Sie Cyclopenten von Benzol unterscheiden?
 14-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
14-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
Aufgabe S. 2/a (2 Punkte) Wodurch können Sie Acetaldehyd von Pentan unterscheiden?
 14-2 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
14-2 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
Aufgabe S. 2/b (2 Punkte) Wobei kann es sich um ein Derivat (gleiche Oxidationsstufe des Carboxyl-C-Atoms) einer Carbonsäure handeln?
 14-3 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
14-3 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Organische Chemie der Freien Universität Berlin. Klausur WS 2003/04 Teil 1
 rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 201a) Klausur WS 2003/04 Teil 1 Verfasser: Prof. Dr. H.-U. Reißig Datum: 09.01.2004 Semester: WS 03/04 Höchstpunktzahl
rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 201a) Klausur WS 2003/04 Teil 1 Verfasser: Prof. Dr. H.-U. Reißig Datum: 09.01.2004 Semester: WS 03/04 Höchstpunktzahl
Aufgabe S. 2/a (2 Punkte) Wodurch können Sie Cyclohexan von Cyclohexen unterscheiden?
 16-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
16-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Es gibt meist 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 16.05.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 16.05.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 06.07.2013 NAME;
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 06.07.2013 NAME;
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O 3 ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist vollständig mit Wasser mischbar.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O 3 ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist vollständig mit Wasser mischbar.
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 05.07.2014 NAME;
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 05.07.2014 NAME;
Stereoisomerie. C 2 H 4 O 2 Schmelzpunkt 17 Grad Celcius
 3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Vorlesung Chemie für Biologen: Klausur 1 WS Sa
 1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.03.2017 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 7 H 8 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.03.2017 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 7 H 8 ein, die die folgenden Eigenschaften
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester am
 Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und Nebenfächer (
 Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (OC) vom 15.07.2013 NAME;
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (OC) vom 15.07.2013 NAME;
alte Klausur; von 1999 ÜBUNGSKLAUSUR
 alte Klausur; von 1999 ÜBUNGSKLAUSUR Name: Bitte nicht mit Bleistift und nicht mit Rotstift ausfüllen! Telefonnummer: Studienfach: Fachsemester: Matrikelnummer: Ausweisnummer: Unterschrift:...... Diese
alte Klausur; von 1999 ÜBUNGSKLAUSUR Name: Bitte nicht mit Bleistift und nicht mit Rotstift ausfüllen! Telefonnummer: Studienfach: Fachsemester: Matrikelnummer: Ausweisnummer: Unterschrift:...... Diese
Übungsbeispiele Kapitel Organische Verbindungen
 Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.02.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 4 O 2 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.02.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 4 O 2 ein, die die folgenden Eigenschaften
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Institut für Chemie und Biochemie
 Institut für Chemie und Biochemie der Freien Universität Berlin 1. Klausur zur Vorlesung OC I 06.12.2013 Prof. Dr. Christoph Schalley Höchstpunktzahl: 100 Davon erreicht Bitte füllen Sie den nachfolgenden
Institut für Chemie und Biochemie der Freien Universität Berlin 1. Klausur zur Vorlesung OC I 06.12.2013 Prof. Dr. Christoph Schalley Höchstpunktzahl: 100 Davon erreicht Bitte füllen Sie den nachfolgenden
Organische Chemie. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie Name: Fachprüfung Vorname: 11. März 2002, 8 00-10 00 h Matr.-Nr.: Raum 204 + 206 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
Organische Chemie Name: Fachprüfung Vorname: 11. März 2002, 8 00-10 00 h Matr.-Nr.: Raum 204 + 206 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
Klausur zur Vorlesung Grundlagen der Organischen Chemie
 Prof. Dr. Jens Christoffers 16. Februar 2017 Universität Oldenburg Klausur zur Vorlesung Grundlagen der Organischen Chemie Vorname: Name: Matrikelnummer: Studiengang: 1,0 1,3 1,7 2,0 2,3 2,7 3,0 3,3 3,7
Prof. Dr. Jens Christoffers 16. Februar 2017 Universität Oldenburg Klausur zur Vorlesung Grundlagen der Organischen Chemie Vorname: Name: Matrikelnummer: Studiengang: 1,0 1,3 1,7 2,0 2,3 2,7 3,0 3,3 3,7
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1
 Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
1 Stoffklasse Alkane : C n H 2n+2 Namensendung an
 rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
Grundkurs Optische Aktivität 1983/I/1 1992/I/1 1994/III/3 1998/I/1
 Grundkurs Optische Aktivität 1983/I/1 1.1 Definieren Sie den Begriff "optische Aktivität"! 2BE 1.2 Erläutern Sie am Beispiel des Bromchloriodmethans, welche Form von Isomerie bei dieser Verbindung auftritt
Grundkurs Optische Aktivität 1983/I/1 1.1 Definieren Sie den Begriff "optische Aktivität"! 2BE 1.2 Erläutern Sie am Beispiel des Bromchloriodmethans, welche Form von Isomerie bei dieser Verbindung auftritt
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
LÖSUNGSBOGEN... Name Vorname Matr.-Nr.
 Christian-Albrechts-Universität zu Kiel Kiel, 16. 07. 2004 Institut für rganische Chemie Klausur zur Vorlesung Allgemeine Chemie II (rg.chem.) Sommersemester 2004 FÜR STUDIENFAC (Zutreffendes bitte ankreuzen)
Christian-Albrechts-Universität zu Kiel Kiel, 16. 07. 2004 Institut für rganische Chemie Klausur zur Vorlesung Allgemeine Chemie II (rg.chem.) Sommersemester 2004 FÜR STUDIENFAC (Zutreffendes bitte ankreuzen)
Klausur zur Vorlesung Allgemeine Chemie II (Organische Chemie) für Studierende der Agrarwissenschaften und der Ökotrophologie. Wintersemester 2002/03
 Klausur zur Vorlesung Allgemeine hemie II (rganische hemie) für Studierende der Agrarwissenschaften und der Ökotrophologie Wintersemester 2002/03 Name: Studienfach: Korrekturbogen Matrikelnummer: Ich versichere,
Klausur zur Vorlesung Allgemeine hemie II (rganische hemie) für Studierende der Agrarwissenschaften und der Ökotrophologie Wintersemester 2002/03 Name: Studienfach: Korrekturbogen Matrikelnummer: Ich versichere,
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Chemie Alkohole, Aldehyde & Ketone, Carbonsäuren
 Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Alkohole hemie Alkohole, Aldehyde & Ketone, arbonsäuren Alkohole erkennt man aufgrund ihrer funktionellen Gruppe, die ydroxy-gruppe. Diese ist Polar, der Rest ist unpolar. Benannt wird der Alkohol nach
Modul: BS Chemie II Organische Chemie Klausur zum Organisch-Chemischen Grundpraktikum für. Studierende der Biologie
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Klausur zum
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Klausur zum
Beuth Hochschule für Technik Berlin, Studiengang Pharma- und Chemietechnik Tutorium Organische Chemie 1 (SS 2011), Tutor: Sascha Behne
 IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist zu Propansäure oxidierbar. - Die
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist zu Propansäure oxidierbar. - Die
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
Aufgabe S. 2/a (6 Punkte) Zeichnen Sie die Strukturformeln der folgenden Verbindungen! 3-Ethylheptan-2-on
 15-3 2 Aufgabe S. 2/a (6 Punkte) Zeichnen Sie die Strukturformeln der folgenden Verbindungen! Anilin Propionsäure Phenol 3-Ethylheptan-2-on Glycerin Formaldehyd Aufgabe S. 2/b (6 Punkte) Zeichnen Sie jeweils
15-3 2 Aufgabe S. 2/a (6 Punkte) Zeichnen Sie die Strukturformeln der folgenden Verbindungen! Anilin Propionsäure Phenol 3-Ethylheptan-2-on Glycerin Formaldehyd Aufgabe S. 2/b (6 Punkte) Zeichnen Sie jeweils
Organische Chemie. 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8. Lehrstuhl für Organische Chemie
 Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Aufgabe S. 2/a (6 Punkte) Zeichnen Sie die Strukturformeln der folgenden Verbindungen! 3-Ethylheptan-2-on
 15-2 2 Aufgabe S. 2/a (6 Punkte) Zeichnen Sie die Strukturformeln der folgenden Verbindungen! Pyridin Acetylchlorid p-xylol 3-Ethylheptan-2-on Glycol Ölsäure Aufgabe S. 2/b (6 Punkte) Zeichnen Sie jeweils
15-2 2 Aufgabe S. 2/a (6 Punkte) Zeichnen Sie die Strukturformeln der folgenden Verbindungen! Pyridin Acetylchlorid p-xylol 3-Ethylheptan-2-on Glycol Ölsäure Aufgabe S. 2/b (6 Punkte) Zeichnen Sie jeweils
Abschlussklausur zur Grundvorlesung Organische Chemie im SS 2007 Nachholtermin -
 Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Wo wird am meisten Alkohol abgebaut in unserem Körper? Antworten: a) Ausscheidung durch Schweiss (=> Posten 12d) b) Abbau in Leber (=> Posten 7t)
 Posten 1a Wo wird am meisten Alkohol abgebaut in unserem Körper? a) Ausscheidung durch Schweiss (=> Posten 12d) b) Abbau in Leber (=> Posten 7t) c) Ausscheidung durch Lunge (=> Posten 16n) d) Kann nicht
Posten 1a Wo wird am meisten Alkohol abgebaut in unserem Körper? a) Ausscheidung durch Schweiss (=> Posten 12d) b) Abbau in Leber (=> Posten 7t) c) Ausscheidung durch Lunge (=> Posten 16n) d) Kann nicht
4. Stereochemie. Das wichtigste Kriterium für Chiralität ist, dass sich Objekt und Spiegelbild nicht zur Deckung bringen lassen.
 4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Konfigurationsisomerie
 Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.01.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 2 O 2 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 15.01.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 2 H 2 O 2 ein, die die folgenden Eigenschaften
Dritte Klausur zur Vorlesung Grundlagen der Organischen Chemie
 Prof. Dr. Jens Christoffers 10. März 2008 Universität Oldenburg Dritte Klausur zur Vorlesung Grundlagen der Organischen Chemie (für Studierende der Chemie ist dies die zweite Klausur, für Umweltwissenschaftler
Prof. Dr. Jens Christoffers 10. März 2008 Universität Oldenburg Dritte Klausur zur Vorlesung Grundlagen der Organischen Chemie (für Studierende der Chemie ist dies die zweite Klausur, für Umweltwissenschaftler
Basisprüfung Allgemeine Chemie (Teil OC) Montag, 3. September 2007
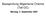 Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. Nomenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B C D N 1.2 (10
Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. Nomenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B C D N 1.2 (10
Organische Chemie der Freien Universität Berlin. Klausur SS 2007 Teil 2
 rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 21a) Klausur SS 27 Teil 2 Verfasser: Prof. Dr..-U. Reißig Datum: 21.7.27 Semester: SS 7 öchstpunktzahl: 2 (in
rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 21a) Klausur SS 27 Teil 2 Verfasser: Prof. Dr..-U. Reißig Datum: 21.7.27 Semester: SS 7 öchstpunktzahl: 2 (in
Basisprüfung Allgemeine Chemie (Teil OC) Montag, 3. September 2007
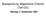 Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Organische Chemie I/II. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Decan Homologe Reihe der Alkane, unterschiedlich lange C-Ketten mit C- C (sp 3 /sp 3 ) und C-H (sp 3 /s)-bindungen (σ-bindungen) Beispiele: Butan
 1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
Wiederholung Grundlagen OC
 Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Summenformel. Strukturformel. Halbstrukturformel. Fossile Energieträger. ( 10. Klasse NTG 1 / 47 ) ( 10. Klasse NTG 2 / 47 ) ( 10. Klasse NTG 3 / 47 )
 Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Organische Chemie der Freien Universität Berlin. Klausur SS 2008 Teil 1
 rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 201a) Klausur SS 2008 Teil 1 Verfasser: Datum: 07.06.2008 Prof. Dr. H.-U. Reißig Semester: SS 08 Höchstpunktzahl:
rganische Chemie der Freien Universität Berlin C I Grundlagen der rganischen Chemie (LV 21 201a) Klausur SS 2008 Teil 1 Verfasser: Datum: 07.06.2008 Prof. Dr. H.-U. Reißig Semester: SS 08 Höchstpunktzahl:
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
3. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 3. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Beschreiben Sie den Reaktionsmechanismus einer S N 1- und einer S N 2- Reaktion. 2.
Allgemeine und Anorganische Chemie 3. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Beschreiben Sie den Reaktionsmechanismus einer S N 1- und einer S N 2- Reaktion. 2.
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Name, Vorname: Matrikelnummer: Studienrichtung: Fragen auf den folgenden Seiten: Musterlösung zur Klausur zur Experimentalvorlesung Organische Chemie
 rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 12.07.10
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 12.07.10
Name: Matrikelnummer: Geburtsdatum: Hilfsmittel: Formelsammlung (beigefügt), Periodensystem (beigefügt), Taschenrechner
 Chemie für Physiker B. Sc. Physikalische Technik XXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXX Prof. Dr. Thomas Jüstel / Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Chemie für Physiker B. Sc. Physikalische Technik XXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXX Prof. Dr. Thomas Jüstel / Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Zweite Klausur zur Vorlesung Grundlagen der Organischen Chemie
 Prof. Dr. Jens Christoffers 18. Februar 2008 Universität Oldenburg Zweite Klausur zur Vorlesung Grundlagen der Organischen Chemie (für Studierende der Chemie ist dies die erste Klausur, für Umweltwissenschaftler
Prof. Dr. Jens Christoffers 18. Februar 2008 Universität Oldenburg Zweite Klausur zur Vorlesung Grundlagen der Organischen Chemie (für Studierende der Chemie ist dies die erste Klausur, für Umweltwissenschaftler
Bachelorprüfung im Fach Biologie, Teilfach Chemie am
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 14.03.2014 2 Aufgabe 1 a) Skizzieren Sie bitte unten die Strukturformel eines aromatischen Aldehyds mit der Summenformel C 8 H 8 3 b) Zeichnen Sie bitte
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 14.03.2014 2 Aufgabe 1 a) Skizzieren Sie bitte unten die Strukturformel eines aromatischen Aldehyds mit der Summenformel C 8 H 8 3 b) Zeichnen Sie bitte
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
