von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V
|
|
|
- Reinhardt Waldemar Solberg
- vor 6 Jahren
- Abrufe
Transkript
1 Nutzebewertug vo Arzeimittel mit eue Wirkstoffe ach 35a SGB V Bewertug vo Arzeimittel für seltee Leide ach 35a Absatz 1 Satz 10 i.v.m. 5. Kapitel 12 Nr. 1 Satz 2 VerfO Wirkstoff: Datum der Veröffetlichug: 18. April 2017
2 Seite 2 Ihaltverzeichis Tabelleverzeichis... 3 Abkürzugsverzeichis... 5 Hitergrud Eiführug Nutzebewertug Fragestellug Zulassugsbegrüdede Studie Liste der verwedete Quelle Studiecharakteristika Edpukte ud statistische Methode I der Nutzebewertug berücksichtige Edpukte Verzerrugspotezial auf Studie- ud Edpuktebee Charakterisierug der berücksichtigte Edpukte ud Eischätzug der Patieterelevaz Statistische Methode Ergebisse zum Zusatzutze Charakterisierug der Studiepopulatio Mortalität Morbidität Lebesqualität Sicherheit Subgruppeaalyse für Kombiatiostherapie (OCA+UDCA vs. UDCA+Placebo) Methodische Amerkuge ud Bewertug der Uterlage Zulassugsstatus ud Zulassugspopulatio vo Desig ud Methodik der POISE-Studie Wirksamkeit Zusammefassede Eischätzug zur Wirksamkeit Lebesqualität Zusammefassede Eischätzug zur Lebesqualität Sicherheit Zusammefassede Eischätzug zur Sicherheit Aforderuge a eie qualitätsgesicherte Awedug Zusammefassug der Bewertug Refereze Ahag... 90
3 Seite 3 Tabelleverzeichis Tabelle 1: Charakterisierug der 12-moatige DB-Phase der POISE-Studie Tabelle 2: Charakterisierug der LTSE-Phase der POISE-Studie Tabelle 3: Charakterisierug der Itervetio der 12-moatige DB-Phase ud LTSE-Phase der POISE-Studie Tabelle 4: I der Nutzebewertug berücksichtigte Edpukte Tabelle 5: Verzerrugspotezial der POISE-Studie der 12-moatige DB-Phase auf Studieebee Tabelle 6: Verzerrugspotezial der i der Nutzebewertug berücksichtigte Edpukte der POISE-Studie Tabelle 7: Beschreibug der Edpukte der Kategorie Mortalität Tabelle 8: Beschreibug der Edpukte der Kategorie Morbidität Tabelle 9: Beschreibug der Edpukte der Kategorie Lebesqualität Tabelle 10: Beschreibug der Edpukte der Kategorie Sicherheit Tabelle 11: Allgemeie Agabe der 12-moatige DB-Phase der POISE-Studie Tabelle 12: Charakterisierug der Studiepopulatio i der 12-moatige DB-Phase der POISE-Studie zu Baselie Tabelle 13: PBC-Charakteristik der Studiepopulatio i der 12-moatige DB-Phase der POISE-Studie zu Baselie Tabelle 14: Begleitmedikatioe ( 10 %) i der 12-moatige DB-Phase der POISE-Studie Tabelle 15: Allgemeie Agabe der LTSE-Phase der POISE-Studie Tabelle 16: Charakterisierug der Studiepopulatio der LTSE-Phase der POISE-Studie zu Baselie Tabelle 17: Begleitmedikatioe ( 10 %) i der LTSE-Phase der POISE-Studie Tabelle 18: Ergebisse zum 5-D-Pruritus-Frageboge ud zur Pruritus-VAS ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie Tabelle 19: Ergebisse zum 5-D-Pruritus-Frageboge ud zur Pruritus-VAS i der LTSE- Phase der POISE-Studie ach OCA-Baselie (Safety-Populatio) Tabelle 20: Ergebisse zum primäre kombiierte Edpukt ud de Eizelkompoete ach 6 ud 12 Moate i der 12-moatige DB-Phase Tabelle 21: Ergebisse zum primäre kombiierte Edpukt i der LTSE-Phase der POISE-Studie ach 12 Moate Tabelle 22: Ergebisse zum PBC-40-Frageboge ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie Tabelle 23: Ergebisse zur Lebesqualität erhobe mit dem PBC-40-Frageboge ach 12 Moate i der LTSE-Phase POISE-Studie Tabelle 24: Ergebisse der uerwüschte Ereigisse i der der 12-moatige DB-Phase der POISE-Studie... 61
4 Seite 4 Tabelle 25: Uerwüschte Ereigisse mit Izidez 10 % i der 12-moatige DB-Phase der POISE-Studie Tabelle 26: Uerwüschte Ereigisse ach Schweregrad mit Izidez 10 % i der 12-moatige DB-Phase der POISE-Studie Tabelle 27: Schwerwiegede uerwüschte Ereigisse mit Izidez 2 % i der 12-moatige DB-Phase der POISE-Studie Tabelle 28: Zeit bis zum erste Eitrete vo Pruritus i der POISE-Studie, Moate 0 bis Tabelle 29: Ergebisse der uerwüschte Ereigisse i der LTSE-Phase der POISE-Studie Tabelle 30: Azahl uerwüschter Ereigisse mit Izidez 10 % i der LTSE-Phase der POISE-Studie Tabelle 31: Uerwüschte Ereigisse ach Schweregrad mit Izidez 2 % i der LTSE-Phase der POISE-Studie Tabelle 32: Schwerwiegede uerwüschte Ereigisse mit Izidez 2 % i der LTSE-Phase der POISE-Studie Tabelle 33: Uerwüschte Ereigisse vo besoderem Iteresse i der LTSE-Phase der POISE-Studie Tabelle 34: Charakterisierug der Studiepopulatio i der 12-moatige DB-Phase der POISE-Studie zu Baselie differeziert ach Kombiatios- ud Mootherapie.. 68 Tabelle 35: Ergebisse zum 5-D-Pruritus-Frageboge ud der Pruritus-VAS i der 12-moatige DB-Phase der POISE-Studie i der Kombiatiostherapie Tabelle 36: Ergebisse zum primäre kombiierte Edpukt ud de Eizelkompoete ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie i der Kombiatiostherapie Tabelle 37: Ergebisse zum PBC-40-Frageboge ach 12 Moate i der 12-moatige DB-Phase der POISE-Studie Tabelle 38: Ergebisse der uerwüschte Ereigisse i der 12-moatige DB-Phase für die Kombiatiostherapie der POISE-Studie Tabelle 39: Uerwüschte Ereigisse mit Izidez 10 % i der 12-moatige DB-Phase der POISE-Studie Tabelle 40: Zusammefassede Darstellug der Studieergebisse der 12-moatige DB-Phase der Studie POISE Tabelle 41: Ergebisse zum 5-D-Pruritus-Frageboge ud der Pruritus- VAS ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie Tabelle 42: Ergebisse zum PBC-40-Frageboge ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie... 93
5 Seite 5 Abkürzugsverzeichis ALP AST ATC CMH DB DEXA EE ELF EMA EPAR G-BA GKV ITT IQWiG KI LS LTSE MedDRA MID MMRM MW MWD N OCA PBC PT pu RCT RR SAP SD SE SGB SMD SOC Alkalische Phosphatase/ Aspartat-Amiotrasferase Aatomisch-Therapeutisch-Chemisch Cochra-Matel-Haeszel-Test Doppelblid Dual-Rötge-Absorptiometrie Efficacy Evaluable fortgeschrittee Leberfibrose (Ehaced Liver Fibrosis) Europea Medicies Agecy Europea Public Assessmet Report Gemeisamer Budesausschuss Gesetzliche Krakeversicherug Itetio-to-Treat Istitut für Qualität ud Wirtschaftlichkeit im Gesudheitswese Kofidezitervall Methode der kleiste Quadrate (least squares) Lagzeit-Sicherheitsstudie (log-term safety extesio) Medical Dictioary for Regulatory Activities Miimal Importat Differece Gemischtes Modell für wiederholte Messuge (mixed model for repeated measures) Mittelwert Mittelwertdifferez Azahl primär biliäre Cholagitis Preferred Term/s pharmazeutischer Uterehmer radomisierte kotrollierte Studie/ (radomized cotrolled trial/s) Relatives Risiko statistischer Aalysepla Stadardabweichug (stadard deviatio) Stadardfehler (stadard error) Sozialgesetzbuch stadardisierte Mittelwertdifferez (Stadardized Mea Differece) Systemorgaklasse/
6 Seite 6 SUE UDCA UE ULN VAS VerfO WADD schwerwiegede/s uerwüschte/s Ereigis/se Ursodesoxycholsäure (ursodeoxycholic acid) uerwüschte/s Ereigis/se obere Normgreze (upper limit of ormal) visuelle Aalogskala (visual aalogue scale) Verfahresordug gewichtete durchschittliche Tagesdosis (Weighted Average Daily Dose)
7 Seite 7 Hitergrud ist zugelasse als Arzeimittel zur Behadlug eies seltee Leides ach der Verordug (EG) Nr. 141/2000 des Europäische Parlamets ud des Rates vom 16. Dezember 1999 über Arzeimittel für seltee Leide. Gemäß 35a Absatz 1 Satz 10 SGB V gilt der mediziische Zusatzutze durch die Zulassug als belegt. Gemäß 35a Absatz 2 SGB V etscheidet der Gemeisame Budesausschuss (G-BA), ob er die Nutzebewertug selbst durchführt oder das Istitut für Qualität ud Wirtschaftlichkeit im Gesudheitswese (IQWiG) beauftragt. Ausgehed vo der gesetzliche Vorgabe i 35a Absatz 1 Satz 10 SGB V, dass der Zusatzutze eies Orpha Drug durch die Zulassug als belegt gilt, hat der G-BA i seier Sitzug vom 15. März 2012 das Verfahre der Nutzebewertug vo Orpha Drugs dahigehed modifiziert, dass bei Orpha Drugs zuächst keie eigestädige Festlegug eier zweckmäßige Vergleichstherapie mehr durch de G-BA als Grudlage der isoweit allei rechtlich zulässige Bewertug des Ausmaßes eies gesetzlich zu uterstellede Zusatzutzes erfolgt. Vielmehr wird ausschließlich auf der Grudlage der Zulassugsstudie das Ausmaß des Zusatzutzes durch de G-BA bewertet. Demetspreched hat der G-BA i seier Sitzug am 15. März 2012 de mit Beschluss vom 1. August 2011 erteilte Auftrag a das IQWiG zur Nutzebewertug vo Arzeimittel mit eue Wirkstoffe gemäß 35a Absatz 2 SGB V i der Weise abgeädert, dass bei Orpha Drugs eie Beauftragug des IQWiG mit der Durchführug eier Nutzebewertug bei zuvor festgelegter Vergleichstherapie erst da erfolgt, we der Umsatz des betreffede Arzeimittels die gesetzliche Greze vo 50 Millioe Euro überschritte hat ud damit eier ueigeschräkte Nutzebewertug uterliegt (vgl. 35a Absatz 1 Satz 11 SGB V). Der G-BA bestimmt gemäß 5. Kapitel 12 Absatz 1 Nummer 1 Satz 2 der Verfahresordug des G-BA (VerfO) das Ausmaß des Zusatzutzes für die Azahl der Patiete ud Patietegruppe, für die ei therapeutisch bedeutsamer Zusatzutze besteht (Nutzebewertug). Zur Bestimmug des Ausmaßes des Zusatzutzes vo zieht der G-BA die Zulassug ud Uterlage zur Zulassug (isbesodere de EPAR), die Studie, auf dere Grudlage die Zulassug des Arzeimittels beruht, sowie das Dossier des pharmazeutische Uterehmers hera ud bewertet die dari ethaltee Date ach Maßgabe der im 5. Kapitel 5 Absatz 7 Nr. 1 bis 4 VerfO festgelegte Kriterie im Hiblick auf ihre therapeutische Relevaz. Der Uterausschuss Arzeimittel hat die Nutzebewertug zum Wirkstoff i seier Sitzug am 11. April 2017 zur Ketis geomme. Darüber hiaus wurde mit Schreibe vom 10. Jauar 2017 das IQWiG beauftragt, ergäzed eie Bewertug der Agabe des pharmazeutische Uterehmers i Modul 3 zu folgede Gesichtspukte durchzuführe: Koste der Therapie für die gesetzliche Krakeversicherug Azahl der GKV-Patiete i der Zielpopulatio Die Nutzebewertug wird am 18. April 2017 zusamme mit der Bewertug der Therapiekoste ud Patietezahle des IQWiG auf der Iteretseite des G-BA ( veröffetlicht ud damit das schriftliche Stellugahmeverfahre eigeleitet. Es wird darüber hiaus eie müdliche Ahörug durchgeführt. Über das Ausmaß des Zusatzutzes beschließt der G-BA ierhalb vo drei Moate ach Veröffetlichug der Nutzebewertug.
8 Seite 8 1. Eiführug Primär biliäre Cholagitis (Primär biliäre Zirrhose) Die primär biliäre Cholagitis (PBC) ist eie chroische, lagsam progrediete, autoimmuvermittelte cholestatische Lebererkrakug [19]. Diese begit (primär) a de kleie Gallegäge (biliär), die durch eie Etzüdug zerstört werde. Hierdurch kommt es zu eiem Rückstau der i de Leberzelle gebildete Galle ud zur Ablagerug toxischer Gallesäure ud aderer schädigeder Verbiduge. Im lägere Verlauf ka die Etzüdug auf das gesamte Lebergewebe übergreife, zur Verarbug führe ud i ihrem Edstadium i die Leberzirrhose übergehe [7]. Die Erkrakug betrifft vor allem Kaukasier ud hier zu 95 % Fraue. Das mittlere Alter bei Diagosestellug beträgt 52 Jahre [23]. Die Jahresizidez liegt geschätzt i Abhägigkeit vo Alter ud Geschlecht zwische 0,7 ud 49 Fälle pro 1 Millio Eiwoher [19]. Die Puktprävalez liegt zwische 6,7 402 Fälle pro 1 Mio. Mesche. Es zeigt sich eie deutliche Häufug vo Fälle im ördliche Europa ud i de USA, v. a. i Estlad, Nordeglad ud Schwede [23]. Die PBC verläuft häufig über viele Jahre mit ucharakteristische Beschwerde ud wird im spätere Krakheitsverlauf durch die Komplikatioe ud Begleiterkrakuge geprägt. Als Folge des Leberumbaus köe sich im Spätstadium die für eie Leberzirrhose typische Komplikatioe eies Pfortaderhochdrucks (portale Hypertesio) eistelle. Dazu gehöre Wasserbauch (Aszites), Krampfader der Speiseröhre (Ösophagusvarize) oder Krampfader im Mage (Fudusvarize) sowie Störuge der Hirfuktio (hepatische Ezephalopathie). Lebesbedrohliche Komplikatioe des Pfortaderhochdrucks sid akute Blutuge aus Ösophagusvarize [7]. Geschätzt wird, dass bis zu 85 % der kaukasische Patiete bei der Diagosestellug asymptomatisch sid. Symptome köe i jedem Stadium der Erkrakug auftrete, sie bestehe i allgemeier Müdigkeit oder sid Ausdruck der Cholestase (ud der resultierede Fettmalabsorptio, die Vitamimagelzustäde ud Osteoporose verursacht). Juckreiz, Müdigkeit oder beides sid iitiale Symptome bei > 50 % der Patiete ud köe weitere Symptome Moate ud Jahre vorausgehe [23]. Adere häufige Befude sid eie vergrößerte, harte, icht druckschmerzhafte Leber (bei 25 %), Spleomegalie (15 %), Hyperpigmetatio (25 %), Xathelasme (10 %) ud Juckreiz (10 %). Letztlich trete alle Befude, Symptome ud Komplikatioe der Zirrhose auf. Darüber hiaus köe sich eie periphere Neuropathie ud weitere autoimmuologische Krakheite, die mit der PBC assoziiert sid, etwickel [2]. Das eizige bisher zugelassee Medikamet zur Behadlug der PBC ist Ursodesoxycholsäure (UDCA). ist ei selektiver ud poteter Agoist für de Faresoid-X-Rezeptor (FXR), ei Kerrezeptor, der i hohe Kozetratioe i Leber ud Darm exprimiert wird. Ma immt a, dass der FXR ei wichtiger Regulator für Gallesäure-, Etzüdugs-, Fibrose- ud Stoffwechsel- Wege ist. Die FXR-Aktivierug sekt die itrazelluläre Kozetratio der Gallesäure i de Hepatozyte durch Uterdrückug der De-ovo-Sythese aus Cholesteri sowie durch Erhöhug des Trasports vo Gallesäure aus de Hepatozyte. Diese Mechaisme begreze die Gesamtgröße des zirkulierede Gallesäure-Pools ud förder gleichzeitig die Cholerese, wodurch die Leberexpositio gegeüber Gallesäure reduziert wird [6]. UDCA hat, im Gegesatz zu, keie Wirkug am FXR; hieri liegt der etscheidede Uterschied. Der primäre pharmakologische Effekt vo auf die Cholestase beruht hauptsächlich auf der Aktivierug des FXR.
9 Seite 9 2. Nutzebewertug 2.1 Fragestellug (Ocaliva ) ist ei Arzeimittel mit dem Status Orpha Drug. Gemäß 35a Abs. 1 Satz 10 SGB V gilt für Orpha Drugs der mediziische Zusatzutze bereits durch die Zulassug als belegt. Der G-BA bestimmt bei Orpha Drugs, die eie Umsatz vo 50 Millioe Euro i de letzte zwölf Kaledermoate icht übersteige, das Ausmaß des Zusatzutzes auf der Grudlage der Zulassug ud der die Zulassug begrüdede Studie. I die Bewertug werde gemäß Zulassugsstatus Patiete i folgeder Idikatio eigeschlosse: OCALIVA wird agewedet für die Behadlug der primär biliäre Cholagitis (auch uter der Bezeichug primär biliäre Zirrhose bekat) i Verbidug mit Ursodesoxycholsäure (UDCA) bei Erwachsee, die uzureiched auf UDCA aspreche, oder als Mootherapie bei Erwachsee, die UDCA icht toleriere köe. 2.2 Zulassugsbegrüdede Studie Pivotale Studie POISE : A Phase 3, Double Blid, Placebo Cotrolled Trial ad Log Term Safety Extesio of Obeticholic Acid i Patiets with Primary Biliary Cirrhosis. Bei der Studie POISE hadelt es sich um eie multizetrische, radomisierte, doppelblide, kotrollierte Phase-III-Studie mit eier 12-moatige Behadlugsphase mit aschließeder Lagzeit- Sicherheitsstudie (LTSE-Phase), die die lagfristige Wirksamkeit, Sicherheit ud Verträglichkeit vo OCA im Vergleich zu Placebo utersucht. Darüber hiaus hat der pu weitere Studie eigereicht, die für die vorliegede Nutzebewertug icht berücksichtigt werde. Die Grüde hierfür werde achfolged kurz berichtet. Studie , ud sid Phase-II-Studie, dere Dosierug vom Dosisschema laut Fachiformatio ( ohe Titratiosphase mit 5 mg für 6 Moate) abweicht. Die Studie ud wurde vo der Europea Medicies Agecy (EMA) [5] uter besodere Bediguge (coditioal approval) zugelasse. wurde vo der EMA mit eier coditioal marketig authorizatio zugelasse. Die Zulassug uter besodere Bediguge ist mit der Auflage weiterer Studieergebisse verküpft: Eie Studie ( ) zum Umfag der Wirksamkeit ud Sicherheit im Rahme eier kofirmatorische, doppelblide, placebokotrollierte Studie bei PBC-Patiete, die UDCA icht toleriere oder icht auf die Behadlug aspreche sowie eie Studie ( ) zum Ausmaß der Wirksamkeit ud Sicherheit im Rahme eier doppelblide, placebokotrollierte Studie bei PBC-Patiete mit moderate bis schwere Leberfuktiosstöruge. Ergebisse für die Studie sid im Jahr 2023 ud für die Studie im Jahr 2020 zu erwarte [5].
10 Seite Liste der verwedete Quelle Zur Bestimmug des Ausmaßes des Zusatzutzes für wurde folgede Studie ud Date heragezoge: Herstellerdossier zu Uterlage der Zulassugsbehörde, isbesodere Committee for Medicial Products for Huma Use Assessmet Report [5] Studiebericht ikl. Studieprotokoll ud statistischem Aalysepla (SAP) der Studie POISE [11,12,13] Studiebericht ikl. Studieprotokoll ud SAP der Lagzeit-Sicherheitsstudie POISE [14,15,16] 2.4 Studiecharakteristika Die Uterlage zum Nachweis des Ausmaßes des Zusatzutzes für (OCA) basiere auf der Zulassugsstudie POISE (im Folgede POISE-Studie ). Die Darstellug erfolgt hier sowohl für die 12-moatige doppelblide Studiephase (12-moatige DB-Phase) als auch für die dara aschließede Lagzeit-Sicherheitsstudie (LTSE-Phase). Die Studie ud die Itervetio werde i de Tabelle 1 3 charakterisiert. Tabelle 1: Charakterisierug der 12-moatige DB-Phase der POISE-Studie Charakteristikum Desig Beschreibug Die POISE-Studie ist eie multizetrische, radomisierte, doppelblide, placebokotrollierte Phase-III-Studie mit eier Screeig-Phase 8 Woche ud eier 12-moatige Behadlugsphase mit aschließeder Lagzeit-Sicherheitsstudie (LTSE-Phase)* bis zu 5 Jahre. * Hiweis: Die Date der LTSE-Phase wurde vom pu achgefordert. Eie Darstellug der Studiecharakteristik ud Studieergebisse wird i der Nutzebewertug berichtet. Die primäre Ziele der Studie ware die Bewertug der Effektivität bezoge auf die Alkalische Phosphatase (ALP) im (Blut-)Serum ud das Gesamt-Bilirubi als zusammegesetzter Edpukt sowie die Sicherheit. Für de Vergleich vo OCA zur Behadlug vo Patiete mit PBC gegeüber eier Kotrollgruppe wurde erwachsee Patiete mit PBC berücksichtigt, die etweder: och mit Ursodeoxycholsäure (UDCA) behadelt werde kote (midestes 12 Moate mit eier stabile Dosis für 3 Moate) oder für eie Therapie mit UDCA icht oder icht mehr zur Verfügug stade (für 3 Moate vor Tag 0). Die Radomisierug erfolgte verblidet i eiem Verhältis 1:1:1, ud zwar: a) OCA 10 mg** b) OCA-Titratio (vo 5 mg auf 10 mg) c) Kotrollgruppe (Placebo als Mootherapie oder i Kombiatio mit UDCA; achfolged als Placebogruppe bezeichet) ** Hiweis: Die Itervetiosgruppe wurde i der Studie icht zulassugskoform behadelt. Etspreched der Fachiformatio ist OCA mit eier Afagsdosis vo 5 mg eimal täglich zugelasse. Auf der Grudlage der Verträglichkeit sollte die Dosis ach 6 Moate auf 10 mg eimal täglich erhöht werde, um ei optimales Aspreche zu erziele. Darüber hiaus sollte währed der 12-moatige DB-Phase alle Patiete ihre Dosis vo UDCA fortsetze. Die Radomisierug erfolgte stratifiziert uter Awedug biochemischer Asprechkriterie ud der Verträglichkeit/Toleraz gegeüber der UDCA-Vorbehadlug:
11 Seite 11 Charakteristikum Beschreibug 1. ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud UDCA-Uverträglichkeit 2. ALP 3 x ULN ud/oder AST 2 x ULN ud/oder Gesamt-Bilirubi ULN zu Baselie ud UDCA-Uverträglichkeit 3. ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud gegewärtige Eiahme vo UDCA 4. ALP 3 x ULN ud/oder AST 2 x ULN ud/oder Gesamt-Bilirubi ULN zu Baselie ud gegewärtige Eiahme vo UDCA I der OCA-Titratiosgruppe begae alle Patiete mit 5 mg OCA. Diese kote ach 6 Moate auf 10 mg hochtitriert werde. Um die Verblidug zu erhalte wurde alle Patiete (d. h. alle Behadlugsgruppe) zu Moat 6 basiered auf ALP- ud/oder Bilirubi-Aspreche ud Verträglichkeit der Studiemedikatio für die Titratio bewertet. Diese Dosissteigerug wurde i der OCA-Titratiosgruppe durch ei iteraktives Web-basiertes Dialogsystem (IWRS) kotrolliert. Eie Afrage ach Hoch- Titratio kote die Prüfärzte über das IWRS für Patiete stelle, die eies der folgede Kriterie bei der Moat-6-Bewertug erfüllte: ALP 1,67 x ULN ud/oder Gesamt-Bilirubi > ULN oder < 15 % ALP-Reduktio bei Moat 6 im Vergleich zu de mittlere Vorbehadlugswerte i der doppelblide Phase ud sofer uerwüschte Ereigisse (UE), wie z. B. schwerer Pruritus, die Gabe eier höhere Dosis icht beschräke. Behadlugsverlauf währed der 12-moatige DB-Phase Quelle: [11] Die Auswertug der primäre ud sekudäre Edpukte war mit Beedigug der 12-moatige Behadlugsphase geplat. Zusätzliche Iterimsaalyse ware icht geplat.
12 Seite 12 Charakteristikum Beschreibug Populatio Quelle: [11] Wesetliche Eischlusskriterie Alter 18 Jahre Defiitive oder wahrscheiliche PBC-Diagose (kosistet mit AASLD- ud EASL- Leitliie [4,21]), belegt durch Zutreffe vo 2 der folgede 3 diagostische Faktore: o Vorgeschichte vo erhöhte ALP-Spiegel seit midestes 6 Moate o Positiver atimitochodrialer Atikörper (AMA-)Titer oder we AMA-egativer oder iedriger Titer (< 1:80), PBC-spezifische Atikörper (ati-gp210 ud/oder ati-sp100) ud/oder Atikörper gege die wichtigste M2-Kompoete (PDC- E2, 2-oxo-glutarsäure-dehydrogease-Komplex) o Leberbiopsie kosistet mit PBC Midestes eier der folgede qualifizierede biochemische Werte: o ALP 1,67 x ULN o Gesamt-Bilirubi > ULN, aber < 2 x ULN Eiahme vo UDCA seit midestes 12 Moate (stabile Dosis seit 3 Moate) vor Tag 0 oder UDCA-Uverträglichkeit (keie UDCA seit 3 Moate) vor Tag 0 Kotrazeptio: Weibliche Patiete im gebährfähige Alter müsse währed der Studie ud für 30 Tage ach der Visite zum Behadlugsede midestes eie Kotrazeptiosmethode utze ( 1 % Ausfallrate): o hormoell (z. B. kotrazeptive Pille, Pflaster, itramuskuläres Implatat oder Ijektio) oder o Doppelbarriere-Kombiatio, d. h. (a) Kodom (mälich oder weiblich) oder (b) Diaphragma, mit Spermizid oder o Itrauteripessar (IUP) oder o Vasektomie (Parter)
13 Seite 13 Charakteristikum Beschreibug Wesetliche Ausschlusskriterie Vorgeschichte oder Aweseheit aderer gleichzeitig besteheder Lebererkrakuge, eischließlich: o Ifektio mit dem Hepatits-C-Virus; Patiete mit aktiver Hepatitis B werde ausgeschlosse, allerdigs köe Patiete mit Hbs-Ag- ud Hbe-Ag-egativ ach Rücksprache mit dem mediziische Moitor i die Studie aufgeomme werde o primäre sklerosierede Cholagitis o alkoholische Leberkrakheit o defiitive Autoimmukrakheit der Leber oder Overlap -Hepatitis o icht-alkoholische Steatohepatitis o Gilbert-Sydrom (Ausschluss durch Iterpretierbarkeit vo Bilirubi-Spiegel) Vorliege kliischer Komplikatioe bei PBC oder kliisch sigifikater Leberdekompesatio, eischließlich: o Vorgeschichte eier Lebertrasplatatio, gegewärtige Platzierug auf eier Lebertrasplatatiosliste oder gegewärtiger MELD-Score 15 o Portale Hypertoie mit Komplikatioe, eischließlich: bekate gastrische oder ösophageale Varize, schlecht kotrollierte oder Diuretika-resistete Aszites, Vorgeschichte vo Blutuge der Varize oder zugehörige therapeutische oder prophylaktische Itervetioe (z. B. Beta-Blocker, Eisetze vo Varize-Bäder oder trasjuguläre itrahepatische portosystemische Shuts [TIPS]) oder Leberezephalopathie Patiete mit schwerem Pruritus oder solche, die eie systemische Behadlug für Pruritus (z. B. mit Gallesäure-Komplexbilder oder Rifampici) ierhalb vo 2 Moate ab Tag 0 beötigte Gabe der folgede Arzeimittel ist uzulässig: o 6 Moate vor Tag 0 ud währed der gesamte Studielaufzeit (d. h. bis zur letzte Dosis ud/oder Behadlugsede): Azathioprie, Colchicie, Cyclosporie, Methotrexat, Mycopheolate Mofetil, Petoxifyllie; Feofibrate oder adere Fibrate; Budesoide ud adere systemische Corticosteroide; poteziell hepatotoxische Arzeimittel (eischließlich a-methyl-dopa, Sodium Valproic Acid, Isoiazide oder Nitrofuratoi) o 12 Moate vor Tag 0 ud währed der gesamte Studielaufzeit (d. h. bis zur letzte Dosis ud/oder Behadlugsede): Atikörper oder Immutherapie, die sich gege Iterleukie oder adere Zytokie oder Chemokie richte Weibliche Patiete: Bekate Schwagerschaft oder positiver Uri-Schwagerschaftstest (bestätigt durch eie positive Serum-Schwagerschaftstest) oder i der Stillzeit Vorgeschichte oder Vorliege eier kliisch relevate Herzrhythmusstörug, die sich wahrscheilich auf das Überlebe währed der Studie auswirke wird, oder Verlägerug des QT- oder QTc-Itervals vo > 500 Millisekude bei Screeig (vor Behadlug) Vorgeschichte eier Alkoholerkrakug, defiiert als Verbrauch vo mehr als 201 ml pro Woche, oder aderer Substazmissbrauch ierhalb eies Jahres vor Tag 0 Itervetio ud Zahl der Patiete Therapie 1) OCA-Titratio 2,3) (N=71) Kombiatiostherapie 5) Mootherapie 5) UDCA + OCA 5 mg (N=65) OCA 5 mg (N=5) OCA 10 mg 4) (N=73) UDCA + OCA 10 mg (N= k. A.) OCA 10 mg (N= k. A.) Kotrollarm (N=73) UDCA + Placebo (N=68) Placebo (N=5) 1) Alle Patiete sollte währed der 12-moatige DB-Phase ihre Dosis vo UDCA fortsetze. 2) Nach Moat 6 Möglichkeit der Titratio auf 10 mg eimal täglich, we mid. ei Kriterium erfüllt (s. o.).
14 Seite 14 Charakteristikum Beschreibug 3) Ei Patiet i der OCA-Titratiosgruppe zog sei Eiverstädis ach der Radomisierug ud vor der erste Dosierug des Prüfpräparates zurück. 4) Behadlugsarm icht zulassugskoform, da etspreched der Fachiformatio bei OCA eie Titratio vorgesehe wird [10]. 5) Ergebisdarstellug ach Moo- ud Kombiatiostherapie für OCA-Titratiosgruppe erfolgte post hoc i Modul 4 im Herstellerdossier; Ergebisse werde uter berichtet. Geplat war etspreched dem Protokoll (Amedmet 3) eie Fallzahl vo 180 Probade (60 pro Gruppe). Aufgrud eies Screeig-Zeitfesters vo bis zu 8 Woche hatte eiige Probade bereits erfolgreich die Screeig-Prozedur durchlaufe, alle Eischlusskriterie erfüllt ud ware für die Radomisierug vorgesehe, obwohl die geplate Fallzahl vo 180 Probade bereits erreicht war. Diese Probade wurde ach Absprache mit dem Sposor ebefalls radomisiert. Somit wurde isgesamt 316 Patiete gescreet ud 217 Patiete radomisiert. Die Studiemedikatio wird oral eimal täglich für 12 Moate eigeomme. Ort ud Zeitraum der Durchführug Studiedauer Die 12-moatige DB-Phase umfasste eie Screeig-Periode vo bis zu 8 Woche, eie aschließede 12-moatige doppelblide, placebokotrollierte Behadlugsdauer mit aschließeder LTSE-Phase bis zu 5 Jahre. Primärer Edpukt, sekudäre Edpukte ud explorative Edpukte gemäß Studieprotokoll 12-moatige DB-Phase Eischluss des erste Patiete: März 2012 Letzte Nachbeobachtug des letzte Patiete: Dezember 2013 Ort der Durchführug Die Studie wurde i 59 kliische Zetre i 13 Läder durchgeführt: Australie, Belgie, Deutschlad, Eglad, Frakreiche, Italie, Kaada, Niederlade, Österreich, Pole, Schwede, Spaie, Vereiigte Staate vo Amerika Primäres Zielkriterium Kombiierter Edpukt* bewertet als Respoderaalyse im Vergleich zu Baselie bei Moat 12: Ateil vo Patiete mit ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN ud ALP-Reduktio 15 % * Hiweis: Eie Darstellug der Eizelkompoete ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN ist im Studiebericht icht dargestellt. Sekudäre Zielkriterie Ateil vo Patiete mit ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN ud ALP- Reduktio 15 % im Vergleich zu Baselie bei Moat 6 Absolute ud prozetuale Veräderug zu Baselie der ALP bei Moat 6 Absolute ud prozetuale Veräderug zu Baselie i ALP bei Moat 12 Ateil vo Patiete mit ALP-Reduktio vo 10 %, 15 %, 20 % ud 40 % im Vergleich zu Baselie Ateil vo Patiete mit ALP ULN Weitere biochemische Asprechkriterie: o ALP 3 x ULN ud AST 2 x ULN ud Bilirubi ULN (Paris I) o ALP 1,5 x ULN ud AST 1,5 x ULN ud Bilirubi ULN (Paris II) o ALP 1,67 x ULN ud Bilirubi ULN (Mayo II) o ALP 1,76 x ULN (Toroto II) o Normal-Bilirubi ULN ud Normal-Albumi LLN (Rotterdam-Kriterie) Kliisches Labor: AP, GGT, ALT, AST, Gesamt- ud kojugiertes Bilirubi, Albumi, PT, INR jeweils absolute ud prozetuale Veräderug zu Baselie Krakheitsspezifische Symptome / Lebesqualität: o PBC-40 (Lebesqualitäts-Messug für PBC): Domäe-Scores (Symptome, Jucke, Fatigue, kogitive Fuktio, soziale Domäe, emotioale Domäe) o 5-D-Pruritus-Frageboge, Pruritus-VAS 1) Biomarker ud icht-ivasive Bewertug vo Leberfibrose (absolute Veräderug zu Baselie):
15 Seite 15 Charakteristikum Beschreibug o Marker für hepatische Fibrose: weitere Marker: CRP, TNF-α, TGF-β, FGF-19, IL-6, CK-18 jeweils absolute Veräderug zu Baselie o ELF-Score ud seie Kompoete (HA, P3NP, TIMP-1) o Leber-Steifigkeits-Messuge (ur i ausgewählte Prüfzetre) Gallesäure o Gesamt-Gallesäure, Gesamt edogee Gallesäure ud Summe für die idividuelle Gallesäure: UDCA, CDCA, DCA, CA ud LCA o Ateil jeder der idividuelle Gallesäure a de Gesamt-Gallesäure Plasma-OCA (PK-Bewertug): OCA (ukojugiert) ud seie Kojugate (Glyco- OCA ud Tauro-OCA) ud Gesamt-OCA (die Summe vo OCA [ukojugiert], Glyco-OCA ud Tauro-OCA) Explorative Edpukte PBC-Autoimmuatikörper (IgA, IgG, IgM) ud adere Zytokie ud Iterleukie (IL-12 (p40), IL-23) Post hoc für das Dossier ausgewertete Edpukte (icht im Studiebericht) Pruritus wurde i Modul 4 des Herstellerdossiers als separater Edpukt aalog de Aalyse im CSR dargestellt. Um de Effekt des Symptoms Pruritus für die Bewertug der Sicherheit darzustelle, wurde im Dossier für die schwere UE eie Sesitivitätsaalyse durchgeführt, i der das Ereigis Pruritus für die Bestimmug der Azahl vo Patiete mit schwere UE uberücksichtigt blieb. Sicherheit Die Sicherheit wurde durch treatmet-emerget adverse evets (TEAE), Vitalzeichemessuge, Gewicht, BMI, EKG, körperliche Utersuchuge, kliische Laborergebisse, Dual-Rötge-Absorptiometrie (DEXA)-Scas, Mayo-Risk- Scores (MRS) ud MELD-Score, Patietefrageböge (5-dimesioaler [5-D-] Pruritus-Frageboge ud Pruritus-VAS) Uerwüschte Ereigisse (UE) Tod (hepatische ud ichthepatische Ursache) Lebertrasplatatio oder Platzierug auf Lebertrasplatatiosliste mittels MELD- Score 15 Portal-Hypertoie ud Komplikatioe eischließlich Ösophagus-Blutug, Itervetioe zur Behadlug vo Varizeblute (z. B. Eisetze vo Varizebäder oder TIPS) ud Diuretika-resistete Aszites Zirrhose mit Komplikatioe: Etwicklug eier hepatische Dekompesatio (hepatoreales Sydrom [Typ I oder II]], spotae bakterielle Peritoitis), hepatozelluläres Karziom ud histologische Etwicklug der Zirrhose Subgruppeaalyse A priori geplat Utersucht wurde (jeweils i Kategorie) Alter (< 65, 65 Jahre), Alter bei PBC- Diagose (< 50, 50 Jahre), Geschlecht, ethische Herkuft (weiß, icht-weiß), Baselie-BMI (< 30 kg/m 2, 30 kg/m 2 ), Baselie-AP-Spiegel, Baselie-Bilirubi-Spiegel (> ULN, ULN), Eiahme vo UDCA, Jahre seit PBC-Diagose ( 7,5, > 7,5 Jahre), Regio. Für de primäre Wirksamkeitsedpukt wurde Patiete i der OCA-Titratio utersucht, die ach 6 Moate: bei 5 mg OCA bliebe vo 5 mg auf 10 mg OCA titriert wurde Für die Respoderaalyse wurde für die ITT-Populatio Subgruppe etspreched de Stratifizierugsmerkmale utersucht: 1. ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud UDCA-Uverträglichkeit 2. ALP 3 x ULN ud AST 2 x ULN ud Gesamt-Bilirubi ULN zu Baselie ud UDCA-Uverträglichkeit
16 Seite 16 Charakteristikum Beschreibug 3. ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud gegewärtige Eiahme vo UDCA 4. ALP 3 x ULN ud/oder AST 2 x ULN ud/oder Gesamt-Bilirubi ULN zu Baselie ud gegewärtige Eiahme vo UDCA Post hoc für das Dossier ausgewertete Subgruppe (icht im Studiebericht) Für das Patietekollektiv der OCA-Titratiosgruppe wurde eierseits die Kombiatio vo OCA+UDCA gegeüber UDCA+Placebo ud adererseits OCA als Mootherapie im Vergleich zum beobachtede Abwarte utersucht. 1) Die Erfassug der sekudäre Edpukte (krakheitsspezifische Symptome) mithilfe der Pruritus-VAS ud dem 5-D-Pruritus- Frageboge wurde aus der Wirksamkeitsaalyse etfert ud als Teil der Sicherheitsaalyse dargestellt (CSR-Äderuge vo protokollspezifische Aalyse im SAP; Stad: ) Abkürzuge: AASLD: America Associatio for the Study of Liver Diseases; ALP: Alkalische Phosphatase; ALT: Alai-Amiotrasferase; AST: Aspartat-Amiotrasferase; CA: Cholsäure; CDCA: Cheodesoxycholsäure; CSR: kliischer Studiebericht; DB: Doppelblid; EASL: Europea Associatio for the Study of the Liver; ELF: fortgeschrittee Leberfibrose; INR: Iteratioal Normalized Ratio; k. A.: keie Agabe; LCA: Lithocholsäure; LLN: utere Normgreze; MELD: Model of Ed Stage Liver Disease; OCA: ; OGDC: Oxogluteratdehydrogeasekomplex; PDC: Pyruvatdehydrogeasekomplex; PK: Pharmakokietik SAP: statistischer Aalysepla; UDCA: Ursodesoxycholsäure; UE: uerwüschte/s Ereigis/se; ULN: obere Normgreze; VAS: visuelle Aalogskala. Es hadelt sich bei der 12-moatige DB-Phase um eie dreiarmige Studie, wobei die Itervetiosgruppe (OCA 10 mg) etspreched der Fachiformatio als icht zulassugskoform zu bewerte ist. Etspreched der Fachiformatio ist OCA mit eier Afagsdosis vo 5 mg eimal täglich zugelasse. Auf der Grudlage der Verträglichkeit sollte die Dosis ach 6 Moate auf 10 mg eimal täglich erhöht werde, um ei optimales Aspreche zu erziele. Somit wird i der Nutzebewertug auf die Darstellug der Charakteristik ud der Ergebisse dieser Itervetiosgruppe verzichtet. Darüber hiaus wurde i de Studieuterlage icht a priori geplat zwische Moo- ud Kombiatiostherapie i de jeweilige Behadlugsgruppe differeziert. Diese wurde post hoc für Modul 4 des Herstellerdossiers durchgeführt ud werde für die Nutzebewertug uter dem Pukt Subgruppeaalyse (siehe Abschitt 2.6.6) berichtet. Tabelle 2: Charakterisierug der LTSE-Phase der POISE-Studie Charakteristikum Desig Beschreibug Die uverblidete ud eiarmige Lagzeit-Sicherheitsstudie (LTSE-Phase) der POISE- Studie schloss sich umittelbar a die 12-moatige DB-Phase a. Die LTSE-Phase dauert plamäßig bis zu füf Jahre; sie war bei Eireichug des Dossiers och icht abgeschlosse. Die primäre Ziele der LTSE-Phase ware die Bewertuge der Effektivität ud der Sicherheit der Behadlug mit OCA sowie der Dauerhaftigkeit der Effekte aus de verblidete Phase. Wegleich die Date der LTSE-Phase etspreched der Zuordug der Patiete zu de drei Behadlugsgruppe der 12 moatige DB-Phase (OCA 10 mg, OCA- Titratio, Placebogruppe) ausgewertet wurde (ITT-Asatz), erhielte sie i der LTSE- Phase eie vo der verblidete Phase abweichede Behadlug (vgl. Tabelle 3). Aalog zur 12-moatige DB-Phase kote auch hier eie Afrage auf Hoch-Titratio durch die Prüfärzte über das IWRS gestellt werde, we eies der folgede Kriterie bei der Moat-6-Bewertug erfüllte: ALP 1,67 x ULN ud/oder Gesamt-Bilirubi > ULN oder < 15 % ALP-Reduktio bei Moat 6 im Vergleich zu de mittlere Vorbehadlugswerte i der DB-Phase ud
17 Seite 17 Charakteristikum Beschreibug Abtitrierug aufgrud kliischer Eischätzuge, isbesodere aufgrud vo UE (z. B. Pruritus) i 5-mg-Schritte oder auch direkt zur eu agestrebte Dosis Gemäß Studieprotokoll Amedmet 3 (Stad: ) erhielte alle Patiete mit Begi der LTSE Phase 5 mg OCA, uabhägig vo ihrer OCA-Dosierug währed der 12-moatige DB-Phase. Dabei war eie Auftitratio bis 25 mg OCA möglich. Mit der Protokolläderug Amedmet 4 (Stad: ) wurde die Möglichkeit der Auftitrierug auf 25 mg auf 10 mg täglich begrezt (siehe achfolgede Abbildug). Dies bezog sich isbesodere auf Patiete, die ach der Protokolläderug i die Studie eigeschlosse wurde. Patiete, die vor Amedmet 4 bereits mehr als 10 mg OCA erhielte, kote etweder auf ihrer Dosierug verbleibe oder ach Etscheidug der Prüfärzte herutertitriert werde. Quelle: [15] Hiweis: Der Studiebericht liegt mit eiem Dateschitt vom vor. Die Protokolläderug (Amedmet 4) begrezte die obere Titrierugsgreze auf 10 mg. Eie möglich Abtitrierug vo 25 mg auf 10 mg wurde allerdigs erst am geädert. Diese Äderug erfolgte allerdigs erst 8 Moate achdem der letzte Patiet i die LTSE-Phase eigeschlosse wurde (letzter Patiet beedete die 12-moatige DB-Phase im Dezember 2013). Die Erhebug der primäre ud sekudäre Edpukte erfolgte alle drei Moate. Die Auswertuge erfolgte deskriptiv ud icht-vergleiched. Populatio Itervetio ud Zahl der Patiete Wesetliche Eischlusskriterie Für de Eischluss i die LTSE-Phase kame alle Patiete ifrage, die die DB-Phase der POISE-Studie abgeschlosse hatte. Therapie 1) 5 mg täglich, Auftitrierug auf 10 mg möglich 3,4) WADD 10 mg OCA 2) alle Patiete der LTSE-Phase N=172 N=193 1) Zum Dateschitt am ) WADD berücksichtigt die Dosisapassuge, Titratio ud Häufigkeit über de Beobachtugszeitraum (ähere Iformatioe siehe ute). 3) Gemäß Studieprotokoll Amedmet 4 (Stad: ). 4) Gemäß Studieprotokoll Amedmet 3 (Stad: ) war eie Auftitratio auf bis zu 25 mg OCA täglich möglich. Diese Äderug erfolgte allerdigs erst 8 Moate achdem der
18 Seite 18 Charakteristikum Beschreibug letzte Patiet i die LTSE-Phase eigeschlosse wurde (letzter Patiet beedete die 12-moatige DB-Phase im Dezember 2013). Aufgrud der Möglichkeit zur flexible Titrierug wurde die WADD für die Zeit der Teilahme eies Patiete a der LTSE-Phase wie folgt berechet: TTTTTTTTTTTTTTTTTTTT vvvvvv OOOOOO AAAAAAAAhll dddddd TTTTTTTT mmmmmm OOOOOO WWWWWWWW = AAAAAAAAhll dddddd TTTTTTTT mmmmmm OOOOOO Für die LTSE-Phase fad keie Berechug der erforderliche Stichprobegröße statt. Vo de 198 Patiete, die die RCT-Phase beedet hatte, wurde 193 (97,5 %) i die LTSE-Phase eigeschlosse. Bezoge auf die ITT-Populatio der DB-Phase (=216) ahme somit 89,0 % dieser Patiete a der Behadlug i der LTSE-Phase teil. Ort ud Zeitraum der Durch-führug Studiedauer Eischluss des erste Patiete: März 2013 Eischluss letzter Patiet: Dezember 2013 Die Etblidig aller Patiete der verblidete Phase, die i die LTSE-Phase eigeschlosse werde sollte, erfolgte am Dateschitt (Iterimsaalyse): CSR: Ort der Durchführug aalog zur verblidete Phase Primärer Edpukt, sekudäre Edpukte ud explorative Edpukte gemäß Studieprotokoll Subgruppeaalyse Primäres Zielkriterium Etspricht der DB-Phase. Sekudäre Zielkriterie Etspreche der DB-Phase. Post hoc für das Dossier ausgewertete Edpukte (icht im Studiebericht) Keie. Sicherheit Etspricht der DB-Phase. Für die LTSE-Phase liege Subgruppeaalyse mit dem primäre Edpukt, de sekudäre Edpukte ALP-Asprechrate ud kliische Laborparameter sowie ausgewählte UE vor. Subgruppemerkmal hierfür ist die UDCA-Behadlug i der verblidete Phase. Weitere Subgruppeauswertuge ware laut Protokoll mit dejeige Merkmale möglich, die i der verblidete Phase bereits für solche Aalyse verwedet worde ware. Die Ergebisdarstellug der LTSE-Phase erfolgt ach jee Gruppe, i die zu Begi der verblidete Phase radomisiert wurde, sowie ach der WADD. Post hoc für das Dossier ausgewertete Subgruppe (icht im Studiebericht) I Modul 4 des Herstellerdossiers liegt eie Auswertug für Patiete vor, die i der DB-Phase im Titratiosarm behadelt wurde. Uberücksichtigt bleibe der Behadlugsarm OCA 10 mg ud der Placeboarm. Abkürzuge: ALP: Alkalische Phosphatase; DB: Doppelblid; ITT: Itetio-to-Treat; IWRS: iteraktives Web-basiertes Dialogsystem; OCA: ; RCT: radomisiert kotrollierte Studie; UDCA: Ursodesoxycholsäure; UE: uerwüschte/s Ereigis/se; ULN: obere Normgreze; WADD: gewichtete durchschittliche Tagesdosis. Die offee ud uverblidete LTSE-Phase schloss sich umittelbar a die 12-moatige DB-Phase a. Die Visite des Moats 12 i der DB-Phase wurde bei de i die LTSE-Phase eigeschlossee Patiete als Tag 1 der LTSE-Phase gewertet. Gemäß dem Statistical Review der FDA (Stad: 29. Mai 2016) erfolgte die offizielle Etblidug aller Patiete am 15. Jauar Bei de vorgelegte LTSE-Date des pu hadelt es sich um eie Iterimsbericht (Stad: 21. April 2015)
19 Seite 19 mit eiem Dateschitt vom 31. August Mit Amedmet 4 (24. August 2014) des Studieprotokolls wurde die obere Titrierugsgreze auf 10 mg begrezt. Eie möglich Abtitrierug vo 25 mg auf 10 mg wurde allerdigs erst am 25. August 2014 geädert. Diese Äderug erfolgte allerdigs erst 8 Moate achdem der letzte Patiet i die LTSE-Phase eigeschlosse wurde (letzter Patiet beedete die 12-moatige DB-Phase im Dezember 2013). Demach ware Patiete ach der 12-moatige DB-Phase midestes 8 Moate oder läger i der LTSE-Phase. Um die Flexibilität der Behadlug/Dosieruge der Patiete mit i der LTSE- Phase darzustelle, wurde für die patieteidividuelle Zeit der Teilahme a der LTSE-Phase die gewichtete durchschittliche Dosierug (WADD) berechet. Die Berechug erfolge gemäß SAP mit folgeder Formel: WWWWWWWW = TTTTTTTTTTTTTTTTTTTT vvvvvv OOOOOO AAAAAAAAhll dddddd TTTTTTTT mmmmmm OOOOOO AAAAAAAAhll dddddd TTTTTTTT mmmmmm OOOOOO Die durchschittliche Dosieruge sid dosierugsbezoge ach folgedem Schema gewichtet: 5 mg, > 5 mg bis 10 mg, 10 mg, > 10 mg, OCA-Gesamt (Kombiatio aller Dosisgruppe). Da bis zu Amedmet 4 i der LTSE-Phase eie Titrierug über 10 mg OCA täglich möglich war, werde diejeige Patiete aus der Nutzebewertug der LTSE-Phase ausgeschlosse, die durchschittlich über 10 mg OCA täglich erhielte (WADD > 10 mg). Dabei hadelt es sich um 21 Patiete der LTSE-Phase. Wegleich es rei recherisch möglich ist, dass ei Patiet ur für kurze Zeit über durchschittlich 10 mg OCA täglich lag, wird auf diese vermutlich kleie Patietegruppe i der achfolgede Auswertug verzichtet. Als bewertugsrelevat eigeschlosse werde deshalb alle Patiete, dere WADD bis zu 10 mg OCA täglich beträgt. Protokolläderuge i der POISE-Studie Das Origialprotokoll (6. September 2011) liegt für die Nutzebewertug i der aktuelle Versio 4.0 (24. August 2014) vor, wobei sich dieses primär auf die LTSE-Phase der POISE-Studie bezieht. Die wichtigste Äderuge ware: Amedmet 2 (04. April 2012) Ausschlusskriterium zur Pruritus-Vorgeschichte wurde durch Hizufüge eies Zeitrahmes agepasst: Patiete mit schwerem Pruritus oder solche, die systemische Behadlug für Pruritus (z. B. mit Gallesäure-Komplexbilder oder Rifampici) ierhalb vo 2 Moate vo Tag 0 beötigte. Ausschlusskriterium zur Vorgeschichte oder Vorliege eier kliisch relevate Herzrhythmusstörug wurde um de Zusatz ergäzt: wahrscheilich Auswirkuge auf das Überlebe währed der kliische Prüfug. Uter weitere Grüde für Studie- oder Therapie-Abbruch wurde der Zeitraum für Behadlugsuterbrechuge vo bisher > 14 Tage auf > 28 Tage erhöht, sodass u ei Studieabbruch erst ab 28 Tage empfohle wurde. Amedmet 3 (24. September 2012) Das Ausschlusskriterium für de Ausschluss vo Patiete mit Hepatitis B ud Serokoversio (Hbs Ag ud Hbe Ag egativ) wurde durch de Zusatz ergäzt: köe ach Rücksprache mit dem Medical Moitor i die Studie eigeschlosse werde. Der fälschlicherweise i der voragegagee Äderug etferte Laborwert C4 wurde der Liste der Gallesäure-Aalyse wieder hizugefügt.
20 Seite 20 Amedmet 4 (24. August 2014) Die obere Titrierug wurde pro Patiet auf 10 mg OCA täglich begrezt. Patiete, die vor dieser Protokolläderug mehr als 10 mg OCA täglich erhalte hatte, kote diese Dosierug weiterbehalte oder bei kliischer Idikatio herabtitriert werde. Hiweis: Die Protokolläderug Amedmet 4 begrezte die obere Titrierugsgreze der LTSE-Phase auf 10 mg. Eie möglich Abtitrierug vo 25 auf 10 mg wurde allerdigs erst am 25. August 2014 geädert. Diese Äderug erfolgte allerdigs erst 8 Moate achdem der letzte Patiet i die LTSE-Phase eigeschlosse wurde (letzter Patiet beedete die 12-moatige DB-Phase im Dezember 2013). Demach ware Patiete ach der 12-moatige DB-Phase midestes 8 Moate oder läger i der LTSE-Phase. I Tabelle 3 sid die Itervetioe der 12-moatige DB-Phase ud der LTSE-Phase dargestellt. Tabelle 3: Charakterisierug der Itervetio der 12-moatige DB-Phase ud LTSE-Phase der POISE- Studie 12-moatige DB-Phase OCA-Titratiosgruppe Name des Wirkstoffs: OCA Dosis zu Studiebegi: 5 mg Höhertitratio: ach 6 Moate auf 10 mg möglich 1) Darreichugsform: oral Eiahmefrequez: 1 x täglich Eiahmedauer: 12 Moate Placebo Name des Wirkstoffs: Placebo Dosis zu Studiebegi: k. A. Höhertitratio ach 6 Moate: ei Darreichugsform: oral Eiahmefrequez: 1 x täglich Eiahmedauer: 12 Moate Hiweis: Es hadelt sich bei der 12-moatige DB-Phase um eie 3-armige Studie, wobei die Itervetiosgruppe (OCA 10 mg) etspreched der Fachiformatio als icht zulassugskoform zu bewerte ist ud i der Nutzebewertug icht berücksichtigt wird. Die Studie deckt zwei Therapieschemata ab: Zum eie die Kombiatio vo OCA mit UDCA, zum adere OCA als Mootherapie im Vergleich zum beobachtede Abwarte (Placebo). Bei Patiete, die och mit UDCA behadelt werde kote, wurde OCA+UDCA gegeüber UDCA+Placebo vergliche. Für Patiete, die für eie Therapie mit UDCA icht oder icht mehr zur Verfügug stade, wurde OCA als Mootherapie gege Placebo als Platzhalter für ei beobachtedes Abwarte vergliche. Alle Patiete sollte währed der 12-moatige DB-Phase ihre Dosis vo UDCA fortsetze. LTSE-Phase Mit Begi der LTSE-Phase erhielte alle i die LTSE-Phase aufgeommee Patiete 5 mg OCA täglich. Patiete, die i der verblidete Phase OCA ud UDCA erhalte hatte, bekame i der LTSE- Phase auch weiterhi diese Kombiatio. OCA wurde dabei mit 5 mg täglich gegebe. Patiete, die i der verblidete Phase OCA ud UDCA erhalte hatte ud die ei kliisch bedeutsames Aspreche ierhalb der 12 Moate der verblidete Phase aufwiese, kote i Abstimmug mit dem Utersucher UDCA vollstädig absetze. Patiete, die i der verblidete Phase OCA als Mootherapie erhalte hatte, erhielte die OCA- Mootherapie auch währed der LTSE-Phase. Ab dem 4. Moat i der LTSE-Phase kote Auf- ud Abdosieruge bei jedem Patiete erfolge. Gemäß CSR wurde dabei wie folgt verfahre: Gemäß Studieprotokoll Amedmet 3 ( ): Schrittweise Auftitrierug vo 5 auf 10 auf 15 bis auf 25 mg täglich. Die Titrierugsgeschwidigkeit sollte bei icht mehr als eiem Titratiosschritt ierhalb vo drei Moate liege. Die Titrierugsregel der Aufdosierug etspreche dee i der 12-moatige DB-Phase 1) Schrittweise Abtitrieruge ware ach Eischätzug des Utersuchers möglich. Hierfür gab es keie Regel. Gemäß CSR war eie Abdosierug aufgrud vo Pruritus ud adere UE wahrscheilich
21 Seite 21 ( likely to occur ). Die Abdosierug kote sowohl i 5-mg-Schritte als auch direkt auf die gewüschte Dosis erfolge. Ab Studieprotokoll Amedmet 4 (Stad: ): Eie Auftritrierug gemäß dem bislag geltede Protokoll bis 25 mg täglich war icht mehr möglich. Hiweis: Der Studiebericht liegt mit eiem Dateschitt vom vor. Die Protokolläderug (Amedmet 4), die eie möglich Abtitrierug vo 25 mg auf 10 mg erlaubt, wurde allerdigs erst am geädert. Dosiskategorisierug etspreched der WADD Aufgrud der Möglichkeit zur flexible Titrierug wurde die WADD für die Zeit der Teilahme eies Patiete a der LTSE-Phase wie folgt berechet. TTTTTTTTssssssssssss vvvvvv OOOOOO AAAAAAAAhll dddddd TTTTTTTT mmmmmm OOOOOO WWWWWWWW = AAAAAAAAhll dddddd TTTTTTTT mmmmmm OOOOOO Die durchschittliche Dosieruge sid dosierugsbezoge ach folgedem Schema gruppiert: 5 mg, > 5 mg bis 10 mg, 10 mg, > 10 mg, OCA-Gesamt (Kombiatio aller Dosisgruppe). Hiweis: Für die Ergebisdarstellug wird die Gruppe WADD 10 mg heragezoge. Begleitmedikatio Nicht erlaubte Begleitmedikatio 6 Moate vor Tag 0 ud währed der Studie: o Azathiopri, Colchici, Cyclospori, Methotrexat, Mycopheolatmofetil, Petoxifylli o Feofibrat oder adere Fibrate o Budesoid ud adere systemische Kortikosteroide o poteziell hepatotoxische Arzeimittel (eischließlich α-methyldopa, Natrium-Valproisäure, Isoiazid oder Nitrofuratoi) 12 Moate vor Tag 0 ud währed der Studie: o Atikörper oder Immutherapie gege Iterleukie oder adere Zytokie oder Chemokie Erlaubte Begleitmedikatio Topische oder ihalative Kortikosteroide Pflazliche oder botaische Präparate, die die Leber beeiflusse (z. B. Mariedistel), vorausgesetzt, dass die Dosis ud das Behadlugsschema währed der DB-Phase kostat gehalte werde. Patiete, die eie kliisch sigifikate therapeutische Reaktio währed der LTSE-Phase habe, köe die UDCA-Behadlug beede, falls dies vo de Prüfärzte als kliisch agemesse bewertet wird. Patiete, die als OCA-Mootherapie-Patiete (d. h. icht UDCA) eitrete, köe die Behadlug mit UDCA zu keier Zeit währed der DB-Phase eileite. Patiete, die Gallesäure-Komplexbilder (z. B. Cholesteri-Resorptios-Hemmer) oder Alumiiumhydroxid oder Smektite mit Atazida eiehme, sollte agewiese werde, ihre Eiahme vo Studiemedikamete ud UDCA so zu staffel, dass midestes 4 Stude zwische de Dose der BAS ud/oder diese Atazida ud der Studiemedikatio (ud UDCA) sichergestellt werde. Patiete, die hormoelle Kotrazeptiva eiehme, sollte diese weiterhi eiehme. Äderuge i der Formulierug oder Dosierugsform währed der Studie müsse i de Ursprugsdokumete ud im CRF dokumetiert werde. Die Eiahme vo Begleitmedikamete sollte vor Tag 0 stabil sei. Die Prüfärzte sollte sich bemühe, die Dosieruge der Begleitmedikatio währed der Studie auf eiem gleiche Niveau zu halte, so lage dies als mediziisch agemesse gilt. Patiete mit Begleiterkrakuge, die medikametös icht gut zu kotrolliere sid, sollte icht i die Studie aufgeomme werde. 1) Eie Afrage ach Hoch-Titratio kote die Prüfärzte über das IWRS für Patiete stelle, die eies der folgede Kriterie bei der Moat-6-Bewertug erfüllte: ALP 1,67 x ULN ud/oder Gesamt-Bilirubi > ULN oder < 15 % ALP-Reduktio bei Moat 6 im Vergleich zu de mittlere Vorbehadlugswerte i der DB-Phase ud Sofer uerwüschte Ereigisse, wie z. B. schwerer Pruritus, die Gabe eier höhere Dosis icht beschräke. Abkürzuge: ALP: Alkalische Phosphatase/; CRF: Prüfboge (Case Report Form); CSR: kliischer Studiebericht; DB: Doppelblid; IWRS: iteraktives Web-basiertes Dialogsystem; k. A.: keie Agabe; LTSE: Lagzeit-Sicherheitsstudie; OCA: ; UDCA: Ursodesoxycholsäure; WADD: gewichtete durchschittliche Tagesdosis.
22 Seite 22 Abbildug 1: Flow-Chart der Patiete der 12-moatige DB-Phase i der POISE-Studie
23 Seite Edpukte ud statistische Methode I der Nutzebewertug berücksichtige Edpukte Tabelle 4: I der Nutzebewertug berücksichtigte Edpukte Edpukt Kategorie Vom pu als patieterelevat eigestuft I der Nutzebewertug berücksichtigt Gesamtüberlebe Mortalität Kombiierter Edpukt vo Baselie bis Moat 12 aus 1, 2) : Ateil vo Patiete mit ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN ud ALP-Reduktio 15 % Fibrose mittels ELF-Score - Morbidität Fibrose mittels trasieter Elastographie (Fibrosca) - Osteoporose mittels DEXA-Sca - Pruritus 3) mittels 5-D-Frageboge mittels VAS PBC-40-Frageboge 4) Lebesqualität Uerwüschte Ereigisse (UE) 5) Schwere UE 5) Schwerwiegede uerwüschte Ereigisse (SUE) 5) Sicherheit UE, die zum Therapieabbruch führte 5) UE vom besodere Iteresse 6) Edpukt wird als bewertugsrelevat eigestuft ud i der Nutzebewertug berücksichtigt Edpukt wird icht als bewertugsrelevat eigestuft aber ergäzed i der Nutzebewertug dargestellt - Edpukt wird icht als bewertugsrelevat eigestuft 1) Es hadelt sich hierbei um de primäre Edpukt der Studie. Dieser war a priori für die Itervetiosgruppe OCA 10 mg im Vergleich zu Placebo als Respoderaalyse geplat. Dargestellt wird der Edpukt für die relevate Populatio OCA-Titratio i der Nutzebewertug. 2) Eie Darstellug der Eizelkompoete ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN ist im Studiebericht icht dargestellt. 3) Etgege der Aufbereitug i Modul 4 des Herstellerdossiers wird Pruritus als UE icht i der Edpuktkategorie Morbidität dargestellt. 4) Der pu stellt i Modul 4 des Herstellerdossiers de PBC-40-Frageboge für eie Teil der Domäe (geerelle Symptome, Jucke, Fatigue ud kogitive Fuktio) uter der Edpuktkategorie Morbidität dar, währed die Domäe (soziale ud emotioale Domäe) uter der Edpuktkategorie Lebesqualität berichtet werde. Diesem Vorgehe wird i der vorliegede Nutzebewertug icht gefolgt, da der Frageboge i seier Gesamtheit Aspekte der Lebesqualität adressiert. Folglich wird der PBC-40-Frageboge hier uter der Edpuktkategorie Lebesqualität berichtet (siehe 2.5.3). 5) Die Sicherheitsedpukte werde differeziert ach UE mit Pruritus (UE gesamt) ud für UE-Pruritus dargestellt. 6) UE vo besoderem Iteresse sid: Pruritus-UE, leberbedigte UE, lipidbedigte UE ud kardiovaskuläre UE. Abkürzuge: ALP: Alkalische Phosphatase/; DEXA: Dual-Rötge-Absorptiometrie; ELF: fortgeschrittee Leberfibrose; pu: pharmazeutischer Uterehmer; (S)UE: (schwerwiegede/s) uerwüschte/s Ereigis/se; ULN: obere Normgreze; VAS: Visuelle Aalogskala. Abweiched vo der Eischätzug des pu wird der primäre kombiierte Wirksamkeitsedpukt defiiert als dichotomer kombiierter Edpukt aus Alkalische Phosphatase (ALP) < 1,67 x ULN bei gleichzeitiger Reduktio des ALP-Wertes um midestes 15 % ud eiem Gesamt-Bilirubi ULN als icht validierter Surrogatparameter eigestuft. Da es sich jedoch um das primäre Zielkriterium
24 Seite 24 der Studie hadelt, wird dieser Edpukt deoch ergäzed dargestellt. Die etsprechede Operatioalisierug ist Kapitel zu etehme. Der Eischätzug des pu, dass die Edpukte Fibrose (dargestellt ahad des ELF-Scores ud der trasiete Elastographie (Fibrosca)) ud Osteoporose (dargestellt mittels DEXA-Sca) patieterelevate ud bewertugsrelevate Edpukte sid, kote icht gefolgt werde. Fibrose mittels ELF-Scores ud der trasiete Elastographie (FibroSca ) Der ELF-Score diet der Bewertug der Leberfibrose ud setzt sich aus drei Biomarker zusamme, ahad derer eie Bewertug möglich ist: Hyalurosäure (HA), Amiotermiales Propeptid vo Prokollage des Typs III (PIIINP) ud Gewebeihibitor der Metalloproteiase 1 (TIMP-1). Die trasiete Elastographie diet der Messug der Lebersteifigkeit ud erlaubt eie Beurteilug der Festigkeit des Gewebes. Dieses Verfahre wurde gemäß Studieuterlage ur a Studieze-tre agewedet, die über die otwedige Messapparate verfüge. Hierfür wurde das Studiepersoal für de Gebrauch ud die Iterpretatio der Date geschult. Zusammegefasst erfolgte die Bewertug der Fibrose mittels serologischer Diagostik ud bildgebeder Verfahre. Somit werde ausschließlich serologische ud morphologische bildgebede Merkmale zur Messug der Leberelastizität erfasst. Die vom Patiete wahrehmbare Symptomatik bleibt dabei jedoch uberücksichtigt ud es lasse sich keie direkte Auswirkuge auf de Patiete ableite. Osteoporose mittels DEXA-Sca Der Dual-Rötge-Absorptiometrie (DEXA-)Sca ist eie icht-ivasive Methode ud wurde zur Bestimmug der Osteoporose bei ausschließlich postmeopausale Fraue i der Studie verwedet. I dieser Teilpopulatio der POISE-Studie wurde der DEXA-Sca zur Messug der Dichte des Schekelhalskoches ud der Ledewirbelsäule verwedet. Die Bewertug der Edpukte erfolgte mittels radiologischer Diagostik. Somit werde ausschließlich morphologische bildgebede Merkmale erfasst. Die vom Patiete wahrehmbare Symptomatik bleibt dabei jedoch uberücksichtigt ud es lasse sich keie direkte Auswirkuge auf de Patiete ableite Verzerrugspotezial auf Studie- ud Edpuktebee Da es sich bei der LTSE-Phase um eie Studie ohe Kotrollgruppe hadelt, wird vo eiem hohe Verzerrugspotezial auf Studie- ud Edpuktebee ausgegage. Nachfolged wird ausschließlich das Verzerrugspotezial auf Studie- ud Edpuktebee der 12-moatige DB-Phase der POISE-Studie bewertet. I der 12-moatige radomisierte, kotrollierte DB-Phase wurde die Patiete zufällig ud zetral radomisiert ud im Verhältis vo 1:1:1 de Behadlugsarme zugeordet. Die Gruppezuteilug erfolgte verdeckt über ei iteraktives Web-basiertes Dialogsystem (IWRS). Studieteilehmer ud Studiepersoal ware währed der Studiephase verblidet. Eie Etblidug erfolgte erst ach Beedigug der 12 Moate. Es fide sich keie Hiweise auf eie ergebisgesteuerte Berichterstattug oder sostige Verzerrugsaspekte. Isgesamt wird das Verzerrugspotezial auf Studieebee für die 12-moatige DB-Phase als iedrig eigeschätzt (siehe Tabelle 5).
25 Seite 25 Tabelle 5: Verzerrugspotezial der POISE-Studie der 12-moatige DB-Phase auf Studieebee POISE-Studie Adäquate Erzeugug der Radomisierugssequez Verdeckug der Gruppezuteilug Verblidug Patiet Verblidug Behadler Hiweise auf ergebisgesteuerte Bericht-erstattug Sostige, das Verzerrugspotezial beeiflussede Pukte Verzerrugspotezial auf Studie-ebee 12-moatige DB-Phase 1) ja ja ja ja ei ei iedrig 1) Relevat für die vorliegede Nutzebewertug ist der Vergleich zwische OCA-Titratiosgruppe ud Placebogruppe (N=143). I Modul 4 des Herstellerdossiers erfolgt eie Post-hoc-Subgruppeauswertug der OCA-Titratiosgruppe ud der Kotrollgruppe differeziert ach Moo- ud Kombiatiostherapie. Abkürzuge: DB: Doppelblid. Das Verzerrugspotezial der relevate Edpukte für die 12-moatige DB-Phase wird i Tabelle 6 dargestellt. Tabelle 6: Verzerrugspotezial der i der Nutzebewertug berücksichtigte Edpukte der POISE- Studie Edpukt Verblidug adäquat ITT adäquat Hiweise auf ergebisgesteuerte Berichterstattug Sostige, das Verzerrugspotezial beeiflussede Pukte Verzerrugspotezial Mortalität Gesamtüberlebe 1) ja ja ei ei iedrig Morbidität Kombiierter Edpukt vo Baselie bis Moat 12 3) : Ateil Patiete mit ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN ud ALP-Reduktio 15 % ja ja ei ei iedrig Pruritus 2) mittels 5-D-Frageboge mittels VAS ja ja ja ja ei ei ei ei iedrig iedrig Lebesqualität PBC-40-Frageboge ja ja ei ei iedrig Sicherheit Uerwüschte Ereigisse (UE) ja ja ei ei iedrig Schwere UE ja ja ei ei iedrig Schwerwiegede UE (SUE) ja ja ei ei iedrig
26 Seite 26 Edpukt Verblidug adäquat ITT adäquat Hiweise auf ergebisgesteuerte Berichterstattug Sostige, das Verzerrugspotezial beeiflussede Pukte Verzerrugspotezial UE, die zum Therapieabbruch führte ja ja ei ei iedrig UE vom besodere Iteresse ja ja ei ei iedrig 1) Das Gesamtüberlebe war gemäß Studieprotokoll kei geplater Effektivitätsparameter. Gleichwohl wurde Todesfälle als Sicherheitsedpukt (UE) erfasst. 2) Gemäß SAP (Stad: ) wurde der 5-D-Frageboge ud die VAS u auf Basis der Safety-Populatio aalysiert. Geplat war dies vorher für die ITT-Populatio. 3) Die Eischätzug des Verzerrugspotezials für de kombiierte Edpukt gilt ebefalls für die Eizelkompoete. Abkürzuge: ALP: Alkalische Phosphatase/; ITT: Itetio-to-Treat; ULN: obere Normgreze; VAS: Visuelle Aalogskala Charakterisierug der berücksichtigte Edpukte ud Eischätzug der Patieterelevaz Laut SGB V 35a Absatz 1 Satz 10 gilt der mediziische Zusatzutze durch die Zulassug als belegt. Nachweise gemäß 5 Absatz 1 bis 6 sid icht verpflichted vorzulege. Zur Beurteilug der Patieterelevaz der vorgelegte Edpukte wurde das Dossier, die zugehörige Studieberichte ud die i diese Quelle zitierte Literatur heragezoge. Das Ergebis der Betrachtug der Edpukte fidet sich aufgeteilt ach Edpuktkategorie i de Tabelle 7 bis 10. Die Operatioalisierug der Edpukte ist dabei i der 12-moatige DB-Phase ud der LTSE-Phase der POISE-Studie idetisch, weshalb achfolged keie weitere Differezierug zwische de Studiephase erfolgt. Tabelle 7: Beschreibug der Edpukte der Kategorie Mortalität Mortalität Edpukt Operatioalisierug Bewertug Gesamtüberlebe Operatioalisierug Gemäß Studieprotokoll (Amedmet 3) wurde Todesfälle als schwerwiegedes uerwüschtes Ereigis (SUE) sowie Todesfälle aus hepatischer ud ichthepatischer Ursache als Sicherheitsedpukt erfasst. Im SAP ud Studiebericht wird die Erfassug vo Todesfälle als uerwüschtes Ereigis (UE) als Teilmege vo de UEs erfasst. Gemäß Modul 4 des Herstellerdossiers ist das Gesamtüberlebe defiiert als Gesamtrate der Todesfälle zwische Studiebegi ud Studieede. Operatioalisierug Die Operatioalisierug zum Gesamtüberlebe ist de Studieuterlage ud Modul 4 des Herstellerdossiers zu etehme. Etgege der Operatioalisierug vom Gesamtüberlebe i Modul 4 wird i de Studieuterlage vo der Erfassug vo Todesfälle als UE oder SUE berichtet. Hier fehle Agabe zur statistische Aalyse vo Todesfälle, die ausschließlich i Modul 4 berichtet werde. Uklar ist weiterhi, wie mit Zesieruge umgegage wurde. Zudem fide sich i de vorgelegte Dokumete keie Agabe zu mögliche Subgruppe- ud/oder Sesitivitätsaalyse, isbesodere im Hiblick auf de Titratiosarm.
27 Seite 27 Mortalität Validität ud Patieterelevaz Etspreched 2 Satz 3 der Arzeimittel-Nutzebewertugsverordug (AM-NutzeV) ist der Nutze eies Arzeimittels der patieterelevate therapeutische Effekt isbesodere hisichtlich der Verbesserug des Gesudheitszustades, der Verkürzug der Krakheitsdauer, der Verlägerug des Überlebes, der Verrigerug vo Nebewirkuge oder eier Verbesserug der Lebesqualität. Tabelle 8: Beschreibug der Edpukte der Kategorie Morbidität Morbidität Edpukt Operatioalisierug Bewertug Kombiierter Edpukt vo Baselie bis Moat 12 aus: Ateil vo Patiete mit ALP <1,67 x ULN ud Gesamt-Bilirubi ULN sowie ALP-Reduktio 15 % (primärer Edpukt) Operatioalisierug Gemäß Studieuterlage ist der primäre kombiierte Edpukt als Respoderaalyse geplat ud defiiert als Ateil vo Patiete mit ALP < 1,67 x ULN ud Gesamt- Bilirubi ULN sowie eier ALP-Reduktio 15 % vo Baselie zu Moat 12. Laut SAP ud Sudiebericht war die Respoderaalyse für de kombiierte Edpukt a priori für die OCA-10-mg-Gruppe geplat ud sollte im Fall eies achweisbare statistische Uterschiedes für die OCA-Titratiosgruppe ebefalls getestet werde. Fehlede Werte zu de jeweilige Erhebugszeitpukte werde als Nicht-Respoder betrachtet. Für de primäre Edpukt werde gemäß SAP die bereits i Tabelle 1 geate Subgruppe aalysiert. Eizelkompoete des kombiierte Edpuktes: Die Eizelkompoete ALP-Reduktio vo 15 % des primäre kombiierte Edpuktes wurde a priori als sekudäres Zielkriterium defiiert. Die geaue Bezeichug i de Studieuterlage war: Ateil vo Patiete mit ALP-Reduktio vo 10 %, 15 %, 20 % ud 40 % im Vergleich zu Baselie. Die Erhebug erfolgt zu Woche 2, Moat 3, Moat 6, Moat 9 ud Moat 12. Zu de Eizelkompoete ALP 1,67 x ULN ud Bilirubi ULN liege i de Studieuterlage keie Agabe vor. Diese liege ausschließlich als biochemische Asprechkriterie (Mayo II) i Kombiatio vor. Operatioalisierug Beim primäre Edpukt der Studie hadelt es sich um eie kombiierte Edpukt, der sich aus verschiedee Edpukte der Kategorie Morbidität zusammesetzt. Isgesamt ist die Operatioalisierug icht abschließed achvollziehbar beschriebe. I der Literatur werde eie Vielzahl a biochemische Asprechkriterie defiiert:
28 Seite 28 Morbidität Quelle: [9] Der a priori defiierte kombiierte Edpukt aus de o. g. drei Kompoete lässt sich ahad der vom pu aufgelistete Refereze icht ableite. Ausschließlich die Asprechkriterie ach Mayo II etspreche zum Teil der Edpuktdefiitio. Allerdigs wurde durch de pu das Kriterium ALP-Reduktio vo 15 % hizugefügt. Der pu begrüdet dies i seie Studieuterlage wie folgt: I additio to the ALP ad bilirubi criteria, a miimum ALP reductio is also beig icluded to esure that oly patiets with a miimal cliical effect are judged to have a successful respose. Thus a patiet with a pretreatmet ALP value of 2.5x ULN will eed to have a ALP < 1,67 x ULN (33 % reductio) to be cosidered a treatmet success; while a patiet with a pretreatmet ALP value of 1.75x ULN will eed to attai a ALP value of < 1.49x ULN to be cosidered a treatmet success.
29 Seite 29 Morbidität Die Eizelkompoete ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN sid i Modul 4 des Herstellerdossiers ud i de Studieuterlage icht klar defiiert. Somit sid die Eizelkompoete icht achvollziehbar defiiert ud operatioalisiert. Validität Die Edpukte der Kategorie Morbidität (ALP, Bilirubi) werde biochemisch über Labormessuge bestimmt. Der pu führt i Modul 4 aus, dass die patieterelevate Edpukte Gesamtüberlebe ud Lebertrasplatatio i kliische Studie bei PBC ur schwer zu erhebe sid, weshalb ALP ud Bilirubi als biochemische Kegröße für die Morbidität heragezoge werde. Der pu argumetiert, dass beide Kegröße i große PBC-Register validiert wurde ( UK-PBC sowie GLOBE ). Die vom pu ageführte Quelle [1,8,18,20,22] zeige keie ausreichede Validierug des Surrogatedpuktes, sodass dieser Argumetatio icht gefolgt werde ka. Lammers et al. [20]: Metaaalyse vo idividuelle Patietedate (N=4.845) aus Kohortestudie aus 15 Zetre zur Bestimmug der Assoziatio vo ALP ud Bilirubi mit Lebertrasplatatio ud Tod. Die Mehrzahl der eigeschlossee Patiete (85 %) wurde mit UDCA therapiert, währed 15 % der Patiete keie UDCA-Behadlug erhielte. Die Evidez ist zu dü, um vo eiem etablierte Surrogatedpukt zu spreche, da keie metaaalytische Ergebisse aus RCTs vorliege, um die Effekte sowohl auf das Surrogat als auch auf die Edpukte zu utersuche. Momah et al [22]: Fehleder Vergleich zu Placebo oder eiem aktive Komparator. Darstellug uterschiedlicher Dosieruge vo UDCA. Nicht geeiget zur Darstellug der Validität des Surrogatedpukts. Carboe et al [1]: Herleitug eies Prädiktiosscores, der icht ubedigt die Validität vo Laborparameter als Surrogatedpukte beweise muss. Es muss kei kausaler Zusammehag bestehe. Korrelatio reicht zur Herleitug eies Prädiktiosscores aus. Zudem ist der Edpukt, für de der Prädiktiosscore ausgerichtet ist, recht heteroge (Ösophagusvarize, Laborwerte, Tod). Es ka icht geau gesagt werde, für welche Teil des kombiierte Edpukts welche Laborwerte prädiktive Aussage zulasse. Nicht geeiget zur Darstellug der Validität des Surrogatedpukts. Hase et al [8]: Hierzu liegt keie formale Validierugsstudie vor; ausschließlich eie Präsetatio. Kumagi et al [18]: Patieterelevater Edpukt = Leberfibrose, welche durch histologische Progressio festgestellt wird. Evidez zu dü, um vo eiem etablierte Surrogatedpukt zu spreche, da keie metaaalytische Ergebisse vorliege. Zusammegefasst lässt sich festhalte, dass der Nachweis zwische Surrogat ud kliischem Edpukt alleie zur Surrogatvalidierug icht ausreicht. Zur Validierug eies Surrogats werde umfagreiche Date beötigt, vorzugsweise eie Metaaalyse mit idividuelle Patietedate vo mehrere RCTs mit ausreicheder Ergebissicherheit. I diese Studie müsse sowohl das Surrogat als auch der kliische Edpukt erhobe worde sei. Die hier vom pu eigereichte Date stamme aus Register, eie Radomisierug erfolgte icht. Zudem bleibe Veräderuge im Dosisschema uberücksichtigt. Der pu ka icht überzeuged darlege, dass die drei Eizelkompoete (ALP < 1,67 x ULN, Gesamt-Bilirubi ULN ud ALP-Reduktio 15 %) valide Surrogatparameter sowohl auf Idividualebee als auch i Kombiatio für eie kombiierte Edpukt sid. Patieterelevaz Sowohl der kombiierte Edpukt der Kategorie Morbidität als auch die zur Verfügug stehede Eizelkompoete werde icht als patieterelevat agesehe.
30 Seite 30 Morbidität Edpukt Operatioalisierug Bewertug 5-D-Pruritus-Frageboge Operatioalisierug Gemäß Studieuterlage wird das Symptom Pruritus ahad des 5-D-Frageboges erfasst. Dieser besteht aus 5 Domäe: Dauer, Grad, Richtug, Behiderug ud Verteilug. Die Items Dauer, Grad ud Richtug bestehe aus jeweils eiem Item, währed die Domäe Behiderug aus vier Items besteht. Alle Items der vier erste Domäe werde ahad eier 5-Pukt-Likert-Skala gemesse. Die Domäe Verteilug umfasst 16 potezielle Stelle, die vo Juckreiz betroffe sei köe (s. Abbildug 2 im Ahag). Die zu erreichede Gesamtpuktzahl liegt zwische 5 ud 25 Pukte. Jede Domäe ka eie Wert vo 1 bis 5 Pukte erreiche. Höhere Pukte deute auf eie stärkere Pruritus hi. Der Frageboge wird zu Woche 2, Moat 3, Moat 6, Moat 9 ud Moat 12 erhobe. Die Veräderuge zwische de Behadlugsgruppe werde für jede Domäe deskriptiv als Score zusammegefasst ud als Veräderug zu Baselie mittels ANCOVA-Modell dargestellt. Gemäß SAP wurde folgede Regel verwedet, um de Domäe-Score zu bereche: Domäe Dauer, Grad, Richtug: beihalte jeweils ei Item Domäe Behiderug: umfasst 4 Items, die die Auswirkuge vo Juckreiz auf die tägliche Aktivitäte beurteile (Schlaf, Freizeit / soziale Aktivitäte, Hausarbeit / Besorguge ud Arbeit / Schule). Die Domäe wird ur da berechet, we midestes drei tägliche Aktivitäte dokumetiert wurde. Aderfalls wird die Domäe als missig bewertet. Domäe Verteilug: Für die Verteilugsdomäe wird ur der Abschitt Mark whether itchig has bee preset i the followig parts of your body over the last 2 weeks geutzt. Isgesamt köe 16 verschiedee Verteiluge markiert werde. Fehlede Häkche werde als abwesed gezählt. Die Azahl der betroffee Körperteile (Summe 0 bis 16) wird i 5 Kategorie geclustert: Summe vo 0 bis 2 = Puktzahl vo 1, Summe vo 3 bis 5 = Puktzahl vo 2, Summe vo 6 bis 10 = Puktzahl vo 3, Summe vo 11 bis 13 = Puktzahl vo 4, Summe vo 14 bis 16 = Puktzahl vo 5. Die Gesamt-5-D-Puktzahl ergibt sich aus der Zusammefassug der Domäe- Scores ud liegt zwische 5 (kei Pruritus) ud 25 (schwerster Pruritus). Die Gesamtpuktzahl wird icht berechet, we eier der Domäe-Scores fehlt. We mehrere Atworte für jedes Elemet gegebe werde, da wird die schwerste Atwort verwedet. Operatioalisierug Isgesamt ist die Operatioalisierug achvollziehbar. Gemäß Studiebericht erfolgte die Erhebug des Frageboges als Sicherheitsedpukt, wurde im Dossier jedoch als Morbiditätsedpukt dargestellt. Validität Der pu argumetiert, dass Pruritus für PBC-Patiete ei relevates Symptom darstellt ud daher als patieterelevat azusehe sei. Dieser Eischätzug ka gefolgt werde. Gemäß Elma et al [3] wurde der 5-D-Frageboge auf Basis der Neuropathie- Skala (Corblatt) ud de kliische Erfahruge durch die Autore ud Experte etwickelt ud validiert. Die Befragug wurde zu Begi ud ach eier 6-wöchige Beobachtugszeit durchgeführt. Zusätzlich wurde der Frageboge ach 2 3 Tage ach Studieeischluss vo ubehadelte Patiete ausgefüllt, um die Test-Retest-Reliabiliät zu bewerte. Der Frageboge wurde a 234 Persoe mit chroischem Pruritus aufgrud vo chroische Lebererkrakuge (N=63), Niereerkrakuge (N=36), dermatologische
31 Seite 31 Morbidität Störuge (N=56), HIV-Ifizierug / AIDS (N=28) sowie bei Patiete mit Verbreugsverletzuge (N=51) durchgeführt. Der Frageboge korrelierte mit eier separate VAS: r = 0,727 zu Baselie (p<0,0001), r = 0,868 ach der 3-tägige Wiederholug (p<0,0001) ud r = 0,892 ach der 6- wöchige Erhebug (p<0,0001). Es gab keie Veräderug der mittlere Puktzahl zwische Tag 1 ud Tag 3 bei ubehadelte Patiete (Itraclass-Korrelatioskoeffiziet = 0,96; p<0,0001). Der Frageboge zeigte sigifikate Veräderuge im Pruritus über die 6-wöchige Nachbeobachtugsperiode (p<0,0001). Schwellewert/MID Date zur kliische Relevaz eier Veräderug liege icht vor. Patieterelevaz Die Erfassug des Symptoms Pruritus wird isgesamt als patieterelevat eigestuft. Es liege jedoch keie Studie hisichtlich eies kliisch relevate Uterschiedes (MID) für PBC-Patiete vor. Zudem umfasst die Validierugsstudie vo Elma et al. [3] ei heterogees Patietekollektiv, weshalb die Übertragbarkeit auf das vorliegede Awedugsgebiet PBC icht abschließed beurteilt werde ka. Edpukt Operatioalisierug Bewertug Pruritus-VAS Operatioalisierug Gemäß de Studieuterlage wurde die VAS zur Bewertug der Ausprägug des Pruritus geutzt. Die Veräderuge zwische de Behadlugsgruppe werde für jede Domäe deskriptiv als Score zusammegefasst ud als Veräderug zu Baselie mittels ANCOVA-Modell dargestellt. Der VAS wird zu Woche 2, Moat 3, Moat 6, Moat 9 ud Moat 12 erhobe. Operatioalisierug Die Relevaz ist achvollziehbar beschriebe. Die Operatioalisierug ist uvollstädig. So fehle i de Studieuterlage Agabe zur Rage der Skala. Dies zeigte sich erst i de Ergebisse zur VAS im Studiebericht. Hier wurde eie Spae vo defiiert (0: kei Juckreiz bis 100: starker Juckreiz). Darüber hiaus fehle Agabe über de Umgag mit fehlede Werte oder bei Mehrfachatworte. Validität Die VAS ist ei semiquatitatives Verfahre für die subjektive Messug eier Empfidugsstärke (z. B. Schmerz oder Juckreiz). Patieterelevaz Die Erfassug des Symptoms Pruritus wird isgesamt als patieterelevat eigestuft.
32 Seite 32 Tabelle 9: Beschreibug der Edpukte der Kategorie Lebesqualität Lebesqualität Edpukt Operatioalisierug PBC-40-Frageboge Operatioalisierug Gesudheitsbezogee Lebesqualität wurde ahad des Frageboges PBC-40 bewertet [17]. Dieser wird vo de Studieteilehmer selbststädig ausgefüllt (Dauer: etwa Miute). Der Frageboge besteht aus 40 Items i sechs Subdomäe ud bezieht sich i seie Frage auf die letzte Woche (siehe Abbildug 3 im Ahag): Subdomäe Frage Geerelle Symptome 1 bis 7 Jucke 8 bis 10 Fatique/Müdigkeit 11 bis 21 Kogitive Fuktioe 22 bis 27 Soziale Domäe 29, 31, 34 bis 40 Emotioale Domäe 28, 30, 33 De Atworte zu de Frage werde sogeate Score-Pukte zugeordet (1 = überhaupt icht, 2 = selte, 3 = machmal, 4 = häufig, 5 = immer). Gesudheitsbezogee Lebesqualität wurde jeweils bei Eischluss (a Tag 0), ach 2 Woche sowie ach 3, 6, 9 ud 12 Moate vor Verabreichug der Studiemedikatio evaluiert. We ei Patiet 50 % oder mehr der Frage pro Domäe icht beatwortet hat, wird der Domäe-Score icht berechet. We weiger als 50 % der Frage pro Domäe icht beatwortet werde, werde fehlede Werte durch de Mittelwert der verfügbare Frageböge für diese Domäe berechet. Die Veräderuge zwische de Behadlugsgruppe werde für jede Domäe deskriptiv als Score zusammegefasst ud als Veräderug zu Baselie mittels ANCOVA-Modell dargestellt. Bewertug Operatioalisierug Die Operatioalisierug ist achvollziehbar beschriebe. Allerdigs hat sich der pu i Modul 4 des Dossiers dafür etschiede, die vier Domäe Geerelle Symptome, Jucke, Fatigue/Müdigkeit ud Kogitive Fuktioe uter der Edpuktkategorie Morbidität darzustelle ud die Soziale sowie die Emotioale Domäe uter der Edpuktkategorie Lebesqualität. Eie Ratioale für dieses Vorgehe fehlt. Da der PBC-40 i seier Gesamtheit Aspekte der Lebesqualität adressiert, wird dieser etspreched der Edpuktkategorie Lebesqualität zugeordet. Validität Der pu führt i Modul 4 des Herstellerdossiers aus, dass der PBC-40 ei etablierter Frageboge im Awedugsgebiet PBC ud stellt damit eie valide ud patieterelevate Edpukt dar. Die Etwicklug des PBC-40 ist vo Jacoby et al [17] beschriebe. Ei Pool vo potezielle Frage wurde aus Iterviews mit 30 PBC- Patiete ausgewählt. Diese Frage wurde systematisch reduziert, vorgetestet ud ahad aderer HRQOL-Frageböge i atioale Erhebuge mit isgesamt 900 PBC-Patiete validiert. Aschließed wurde der PBC-40 mit seie sechs Domäe i eier Kohorte a 40 PBC-Patiete erhobe ud ausgewertet. Soziodemographische Merkmale der Patiete wurde icht geat. Die Auswahl der 40 Frage (Items) für de erste Pretest des Istrumets ist icht trasparet beschriebe. Die Skalierug (füf Auspräguge auf eier Likert-Skala) wurde icht begrüdet.
33 Seite 33 Lebesqualität Quelle: [17] Die itere Kosistez (Crobachs Alpha) für die 6 Skale liegt skalebezoge zwische 0,72 ud 0,95 (mit Müdigkeit, kogitive Fuktioe ud Juckreiz über 0,9). I der Domäe Soziales lag die Korrelatio für die Frage ''I ted to keep the fact that I have PBC to myself bei ur 0,19. I der Domäe Emotioales lag die Korrelatio für die Frage I felt uwell whe I drak alcohol bei ur 0,22. Die Test-Retest-Reliabilität (Itraclass-Korrelatioskoeffiziet) liegt skalebezoge zwische 0,83 ud 0,96 ud altersgruppebezoge für die Gesamtskala bei 0,90 ud 0,92. Die Validität des PBC-40 wurde durch eie hohe Korrelatio mit relevate Domäe im SF-36 ud ESI-55 achgewiese. Die Präzisio des PBC-40 wurde durch die gerige Bode- ud Deckeeffekte bewiese. Die Resposiveess wurde im Rahme der Validierugsstudie icht utersucht, sodass achfolged keie Eischätzug hierzu erfolge ka. Schwellewert/MID Date zur kliische Relevaz eier Veräderug liege icht vor. Patieterelevaz Die Erfassug der Lebesqualität wird als patieterelevat eigestuft. Es liege jedoch keie Studie hisichtlich eies kliisch relevate Uterschiedes (MID) für PBC-
34 Seite 34 Lebesqualität Patiete vor, sodass die kliische Relevaz eier Veräderug im Frageboge PBC- 40 uklar bleibt. Zudem existiert bisher kei Gesamtscore für alle sechs Domäe. Etspreched 2 Satz 3 AM-NutzeV ist der Nutze eies Arzeimittels der patieterelevate therapeutische Effekt isbesodere hisichtlich der Verbesserug des Gesudheitszustades, der Verkürzug der Krakheitsdauer, der Verlägerug des Überlebes, der Verrigerug vo Nebewirkuge oder eier Verbesserug der Lebesqualität. Tabelle 10: Beschreibug der Edpukte der Kategorie Sicherheit Sicherheit Edpukt Operatioalisierug Uerwüschte Ereigisse Operatioalisierug Alle Sicherheitsaalyse wurde mit Date der Sicherheitspopulatio durchgeführt. Gemäß Studieprotokoll Amedmet 3 (Stad: ) ist ei UE defiiert als ei eu aufgetretees oder sich verschlechterdes UE ach Verabreichug der erste Dosis der Studiemedikatio, uabhägig davo, ob sie im Zusammehag mit der Studiemedikatio stehe. Gemäß SAP beschräke sich UE auf treatmet emerget adverse evets. Die Klassifizierug erfolgte ach Systemorgaklasse ud Preferred Terms gemäß MedDRA (Versio 15.0). UE werde für alle Behadlugsgruppe dargestellt: alle UE behadlugsbedigte UE ( Defiite, Probable, or Possible) oder ( Ulikely or Not Related. ). alle schwerwiegede UE (SUE) UE ach maximalem Schweregrad (bei Auftrete mehrerer UE bei eiem Patiete wird ur das UE mit dem höchste Schweregrad erfasst; UE mit fehleder Agabe zum Schweregrad werde als schwer erfasst) o mild: keie Eischräkug im Alltag, leichte Beschwerde o moderat: eiige Eischräkuge im Alltag, lästige Beschwerde o schwer: starke Eischräkuge im Alltag, uerträgliche Beschwerde oder Schmerze zu Behadlugsabbruch oder Studieaustritt des Patiete führede UE zum Tod führede UE UE vo besoderem Iteresse Gemäß Studiebericht werde die achfolgede UE vo besoderem Iteresse geat: Pruritus-UE, leberbedigte UE, lipidbedigte UE ud kardiovaskuläre UE. Dabei wurde ausschließlich Pruritus im SAP präspezifiziert. UE vo besoderem Iteresse: Pruritus Bei Pruritus hadelt es sich um ei UE vo besoderem Iteresse, da dieses gemäß CSR ei häufiges Symptom vo PBC darstellt ud i de Phase-II-Studie häufig als UE berichtet wurde. Gemäß SAP wird uter eiem UE-Pruritus jeder Preferred Term zusammegefasst, der Prur umfasst. Diese Zusammefassug wird separat ahad des MedDRA (Versio 15.0) kodiert ud als Teilmege vo alle UE dargestellt. Darüber hiaus werde die UE-Pruritus für die Zeititervalle Tag 0 bis Moat 6 ud Moat 6 bis Moat 12 basiered auf dem Begi eies Pruritus-Ereigisses erfasst. Dargestellt wird die Zeit bis zum erste Auftrete eies Pruritus-Ereigisses differeziert ach a) jegliches UE- Pruritus, b) moderate bis schwere UE-Pruritus ud c) schwere UE-Pruritus. Dabei werde die Azahl der Patiete ohe Pruritus zesiert ud eie Kapla-Meier- Schätzug mittels Log-Rak-Test für de Vergleich OCA vs. Placebo durchgeführt. Darüber hiaus werde für die o. g. Zeititervalle folgede UE betrachtet:
35 Seite 35 Sicherheit Milde, moderate oder schwere UE-Pruritus zu Baselie Verschlechterug der Schwere, we Patiete zu Baselie Pruritus hatte Die Schwere des Pruritus zu Baselie wurde ahad der VAS festgestellt. Die Schwere des Pruritus zu Baselie wurde ahad der VAS festgestellt. Eie Verschlechterug der Pruritus für Patiete, dere Pruritus-Schweregrad bereits zu Baselie schwer war wird da gezählt, we das UE-Puritus als schwerer dokumetiert wird. UE-Pruritus werde für folgede Subgruppe zusammegefasst: Patiete i der OCA-Titratiosgruppe, die Moat 6 beedet habe Patiete, die vo 5 auf 10 mg hochtitriert wurde Patiete, die bei 5 mg gebliebe sid Pruritus-Ereigisse die vor Moat 6 begoe habe ud ach Moat 6 ahalte, gehe i die Berechug vo Moat 6 bis Moat 12 mit ei. Bewertug Operatioalisierug Die Relevaz ud Operatioalisierug ist achvollziehbar beschriebe. Etgege der i Modul 4 des Herstellerdossiers aufgeführte Ergebisse werde die achfolged gelistete UE-Pruritus icht der Edpuktkategorie Morbidität, soder als Sicherheitsedpukte dargestellt. UE-Pruritus Schwere UE-Pruritus Schwerwiegede UE-Pruritus UE-Pruritus, die zum Therapieabbruch führte Zeit bis zum erste Auftrete eies Pruritus-Ereigisses im Beobachtugszeitraum UE vo besoderem Iteresse Gemäß Studiebericht werde die achfolgede UE vo besoderem Iteresse geat: Pruritus-UE, leberbedigte UE, lipidbedigte UE ud kardiovaskuläre UE. I SAP ud Studieprotokoll fide sich uterdesse ur Agabe bezüglich dem UE- Pruritus. Allei die Pruritus-UE ware im SAP präspezifiziert. Die adere drei Sicherheitsparameter wurde erst im Studiebericht geat ud mit Ergebisse aus Phase-II-Studie begrüdet. Validität ud Patieterelevaz Etspreched 2 Satz 3 AM-NutzeV ist der Nutze eies Arzeimittels der patieterelevate therapeutische Effekt isbesodere hisichtlich der Verbesserug des Gesudheitszustades, der Verkürzug der Krakheitsdauer, der Verlägerug des Überlebes, der Verrigerug vo Nebewirkuge oder eier Verbesserug der Lebesqualität. Edpukt Operatioalisierug Bewertug Schwerwiegede uerwüschte Ereigisse Operatioalisierug Ei UE galt als schwerwieged, sofer es als fatal oder lebesbedrohlich eizustufe war, eie Hospitalisierug oder eie bereits bestehede ud u verlägerte Hospitalisierug ach sich zog, zu eier Erwerbsufähigkeit oder zu eier Behiderug führte, eie kogeitale Aomalie oder eie Geburtsfehler erzeugte, patietegefährded war oder eie mediziische ud/oder chirurgische Eigriff erforderte. Operatioalisierug Die Relevaz ud Operatioalisierug ist achvollziehbar beschriebe. Validität ud Patieterelevaz Etspreched 2 Satz 3 AM-NutzeV ist der Nutze eies Arzeimittels der patieterelevate therapeutische Effekt isbesodere hisichtlich der Verbesserug des Gesudheitszustades, der Verkürzug der Krakheitsdauer, der Verlägerug des Überlebes, der Verrigerug vo Nebewirkuge oder eier Verbesserug der Lebesqualität.
36 Seite Statistische Methode I diesem Abschitt werde die geplate statistische Methode zur Auswertug der POISE-Studie beschriebe. Die vorliegede Versio des SAP 1.0 wurde am 5. März 2014 ach Beedigug der doppelblide 12-moatige Studiephase verfasst. Der Eischluss i die Studie vom erste Patiete bis zur letzte Nachbeobachtug des letzte Patiete lag zwische März 2012 ud Dezember Vor diesem Hitergrud muss kostatiert werde, dass der SAP 1.0 ascheied post hoc verfasst wurde ud damit uklar bleibt, ob die Studie die zu utersuchede Fragestelluge adäquat beatworte ka. Deoch wurde gemäß Protokoll (Amedmet 3 vom 24. September 2012) die statistische Aalyse beschriebe ud im SAP (Stad: 5. März 2014) zum Teil modifiziert. Die achfolgede Beschreibuge basiere auf dem aktuelle SAP 1.0. Fallzahlplaug Die Fallzahlplaug der POISE-Studie (12-moatige DB-Phase) basiert auf dem primäre kombiierte Wirksamkeitsedpukt: Ateil vo Patiete mit ALP < 1,67 x ULN ud Gesamt- Bilirubi ULN sowie ALP-Reduktio 15 % ud legte folgede Aahme zugrude: Power: 90 % Sigifikaziveau (α-fehler): 5 % 1:1:1-Radomisierug Aspreche im Sie des primäre Edpukts i der Placebogruppe: 9 % Aspreche im Sie des primäre Edpukts i der OCA-10-mg-Gruppe: 40 % Die geplate Stichprobegröße betrug etwa 180 Patiete (60 Patiete i jeder der drei Gruppe). Die Plaug der Fallzahl basierte auf de Ergebisse der Phase-II-Studie. Dort zeigte 9 % der Patiete, die mit Placebo behadelt wurde, ud 40 % der Patiete, die mit 10 mg OCA behadelt wurde, ei Aspreche im Sie des primäre Edpukts. Der Stichprobeumfag wurde da mit etwas koservativere Aahme berechet: Uter der Aahme vo 14 % (Placebo) ud 40 % (10 mg OCA) asprechede Patiete wurde basiered auf eiem zweiseitige Biomialtest auf gleiche Ateile bei eiem Sigifikaziveau vo 5 % errechet, dass 60 Patiete pro Gruppe 90 % Power zur Detektio eies Uterschiedes zwische de Gruppe gewährleiste würde. Wege eies Screeig-Zeitfesters vo bis zu 8 Woche hatte eiige Probade bereits erfolgreich die Screeig-Prozedur durchlaufe, alle Eischlusskriterie erfüllt ud ware für die Radomisierug vorgesehe, obwohl die geplate Fallzahl vo 180 Probade bereits erreicht war. Diese Probade wurde ach Absprache mit dem Sposor radomisiert. Isgesamt wurde 217 Patiete radomisiert. Statistische Modelle ud Tests: Die POISE-Studie ist eie Überlegeheitsstudie, i der die lagfristige Wirksamkeit, Sicherheit ud Verträglichkeit vo OCA im Vergleich zu Placebo bei Patiete mit PBC utersucht wird. Für de Vergleich vo OCA gegeüber Placebo wurde erwachsee Patiete mit PBC berücksichtigt, die etweder: och mit UDCA behadelt werde kote (midestes 12 Moate mit eier stabile Dosis für 3 Moate) oder die für eie Therapie mit UDCA icht oder icht mehr zur Verfügug stade (für 3 Moate vor Tag 0).
37 Seite 37 Die Radomisierug erfolgte verblidet i eiem Verhältis 1:1:1, ud zwar: OCA 10 mg oder OCA-Titratio oder Placebogruppe (Placebo als Mootherapie oder i Kombiatio mit UDCA). Sofer icht aders vermerkt, werde alle statistische Tests zweiseitig sei ud mit dem 0,05 Sigifikaziveau durchgeführt. Gemäß SAP wurde die ALP-Respoderaalyse, krakheitsprogostische Risiko-Respoderaalyse ud Subgruppeaalyse mittels Cochra-Matel-Haeszel- (CMH-)Methode aalysiert, stratifiziert ach Radomisierugsfaktore. I alle logistische Regressiosmodelle ud i de Kovariaz-(ANCOVA-)Modelle wurde Behadlugs- ud Radomisierugsstratifizierugsfaktore als feste Effekte berücksichtigt. Zudem wurde Sesitivitätsaalyse uter Verwedug der MMRM- Methode (mixed model for repeated measures), stratifiziert ach fixe Effekte Behadlug ud Zeit, dem Iteraktiosterm für Behadlugsgruppe ud Zeit, ud ach zur Radomisierug verwedete Stratavariable sowie Baseliewert als Kovariate durchgeführt. Multiples Teste bezoge auf de primäre ud zetrale sekudäre Edpukt Der primäre kombiierte Wirksamkeitsedpukt ist defiiert als Ateil vo Patiete mit ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN sowie ALP-Reduktio 15 % zu Moat 12 im Vergleich zu Baselie für die Itervetiosgruppe OCA 10 mg im Vergleich zu Placebo. Hierfür wurde folgede Hypothese formuliert: H 0: Die Asprechrate zwische OCA 10 mg ud Placebo sid gleich H 1: Die Asprechrate zwische OCA 10 mg ud Placebo sid icht gleich Es wurde eie hierarchische Testprozedur gewählt, um die Überlegeheit vo OCA über Placebo i Hiblick auf de zetrale sekudäre Edpukt (OCA-Titratio vs. Placebo) zu teste. Die achfolgede Schritte i der Testhierarchie wurde ur da durchgeführt, sofer sich im primäre Edpukt (OCA 10 mg vs. Placebo) eie statistische Sigifikaz auf eiem zweiseitige Sigifikaziveau vo 5 % zuguste vo OCA zeigte. Gemäß SAP wurde der primäre kombiierte Wirksamkeitsedpukt mittels CMH-Methode, stratifiziert ach Radomisierugsfaktore, aalysiert. Stratifizierugsfaktore ware biochemische Asprechkriterie ud die Verträglichkeit/Toleraz gegeüber der UDCA-Vorbehadlug: (1) ALP > 3 x ULN ud/oder Aspartat-Amiotrasferase (AST) > 2 x ULN ud/oder Gesamt- Bilirubi > ULN zu Baselie ud UDCA-Uverträglichkeit (2) ALP 3 x ULN ud/oder AST 2 x ULN ud/oder Gesamt-Bilirubi ULN zu Baselie ud UDCA-Uverträglichkeit (3) ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud gegewärtige Eiahme vo UDCA (4) ALP 3 x ULN ud/oder AST 2 x ULN ud/oder Gesamt-Bilirubi ULN zu Baselie ud gegewärtige Eiahme vo UDCA Die Aalyse des primäre kombiierte Wirksamkeitsedpukts basiert auf der ITT-Populatio. Fehlede Werte wurde als No-Respoder betrachtet. Missig / Fehlede Werte Fehlede Werte werde als missig gewertet, we icht aders agegebe. I Respoderaalyse wird jeder Patiet, für de keie Bewertug zum agegebee Zeitpukt vorliegt, als Nicht- Respoder betrachtet. Für Sesitivitätsaalyse, die ur beobachtete Fälle (observed data)
38 Seite 38 berücksichtige, werde Patiete mit fehlede Werte icht imputiert oder berücksichtigt. Für Wirksamkeitsedpukte, die eie Aalyse des Kovariaz-(ANCOVA)-Modells verwede, diee beobachtete Fälle als primäre Aalyse. Sesitivitätsaalyse zur Beurteilug der Wirkug fehleder Date köe durchgeführt werde, we fehlede Date mittels last observatio carried forward (LOCF-)Methode berücksichtigt werde. Für Edpukte, die mittels MMRM-Methode aalysiert werde, erfolgt keie Imputatio fehleder Werte. Studiepopulatioe Folgede Studiepopulatioe wurde defiiert: Itet-to-Treat (ITT)-Populatio: Alle radomisierte Patiete, die midestes eie Dosis der Studiemedikatio erhalte habe ud i eie der drei Behadlugsarme zugeteilt wurde (N=216). Die Zuteilug der Behadlug basiert auf der radomisierte Behadlug. Diese Populatio wurde für die Zusammefassug der Baselie-Charakteristika ud zur Utersuchug der Wirksamkeitsedpukte heragezoge. Completer-Populatio: Alle radomisierte Patiete, die midestes eie Dosis der Studiemedikatio erhalte habe ud die die doppelblide 12-moatige Behadlugsphase beedet habe (N=198). Die Zuteilug der Behadlug basiert auf der radomisierte Behadlug. Diese Populatio wurde für die Zusammefassug spezifischer Baselie-Charakteristika ud Zeitreiheaalyse heragezoge. Efficacy-Evaluable (EE)-Populatio: Alle Patiete der Completer-Populatio, die keie schwerwiegede Protokollverletzuge ud damit möglicherweise eie Eifluss auf die Wirksamkeit des Prüfpräparats hatte (N=192). Die Zuteilug der Behadlug basiert auf der radomisierte Behadlug. Safety-Populatio: Alle Patiete, die midestes eie Dosis der Studiemedikatio erhalte habe (N=216). Die Auswertug erfolgt etspreched der tatsächlich verabreichte Medikatio ud ist die Basis der Auswertuge für die Sicherheitsedpukte ud de 5-D-Frageboge sowie die VAS (Pruritus). Die primäre ud sekudäre Wirksamkeitsaalyse sowie die Sesitivitätsaalyse basiere auf der ITT-Populatio, währed die Aalyse der Sicherheitsedpukte auf der Safety-Populatio basiert. Zusätzliche uterstützede Wirksamkeits- ud Sesitivitätsaalyse werde mit der Completer- Populatio für Zeitreiheaalyse ud der EE-Populatio durchgeführt. Die Aalyse der EE- Populatio wird ur durchgeführt, we midestes 10 % der Patiete aus der Completer- Populatio ausgefalle sid. Äderuge vo protokollspezifische Aalyse im SAP 1.0 (Stad: 5. März 2014) Im Studiebericht (Stad: 17. April 2015) wird über Äderuge vo protokollspezifische Aalyse im SAP 1.0 (Stad: 5. März 2014) berichtet. Die Sicherheits- ud Verträglichkeitsaalyse wurde icht auf der ITT-Populatio, soder auf Basis der Safety-Populatio durchgeführt. Die Wirksamkeitsaalyse wurde auf Basis der Completer- ud EE-Populatio durchgeführt. Die primäre Wirksamkeitsaalyse war ursprüglich auf Basis eies logistische Regressiosmodells mit eier Respose ach Edpukt- ud Behadlugsgruppe sowie Radomisierugsfaktore geplat. Aufgrud des Feedbacks der FDA (27. Februar 2014) wurde die primäre Wirksamkeitsaalyse auf Basis eies CMH-Tests durchgeführt, stratifiziert ach Radomisierugsfaktore.
39 Seite 39 Die Erfassug der sekudäre Edpukte (krakheitsspezifische Symptome) mithilfe der Pruritus-VAS ud dem 5-D-Pruritus-Frageboge wurde aus der Wirksamkeitsaalyse etfert ud als Teil der Sicherheitsaalyse dargestellt. 2.6 Ergebisse zum Zusatzutze Für die 12-moatige DB-Phase wurde isgesamt 316 Patiete gescreet, vo dee 217 radomisiert wurde ud 216 midestes eie Dosis der Studiemedikatio erhalte habe (etspricht der ITT- ud der Safety-Populatio). Die Zuteilug der Behadlugsgruppe erfolgte verblidet im Verhältis 1:1:1. Gemäß der Fachiformatio vo ist bei PBC eie Titratio der Behadlug vo 5 auf 10 mg vorgesehe. Somit ist der OCA-10-mg-Behadlugsarm mit eiem feste Dosisschema icht zulassugskoform ud wird im Folgede icht weiter dargestellt. Demetspreched werde für die Nutzebewertug ausschließlich die Ergebisse für die Behadlugsarme "OCA-Titratio" (N=71) ud Placebo (N=73) berichtet. Für die Darstellug der Ergebisse werde die ITT- ud die Safety-Populatio (N=216) heragezoge. Die eiarmige LTSE-Phase schloss sich umittelbar a die 12-moatige DB-Phase a. Bei de vorgelegte Date des pu hadelt es sich um eie Iterimsbericht (Stad: 21. April 2015) mit eiem Dateschitt vom 31. August Somit ware Patiete ach der 12-moatige DB-Phase midestes 8 Moate oder läger i der LTSE-Phase. Für die Darstellug der Ergebisse wird die Safety-Populatio (N=193) heragezoge Charakterisierug der Studiepopulatio 12-moatige DB-Phase Isgesamt wurde 71 Patiete i die OCA-Titratiosgruppe ud 73 Patiete i die Placebogruppe (N=144) radomisiert. Ei Patiet i der OCA-Titratiosgruppe zog seie Eiverstädiserklärug ach der Radomisierug ud vor Begi der Studiemedikatio zurück. Die Behadlug währed der 12-moatige DB-Phase wurde i de beide Behadlugsarme vo isgesamt 10 Patiete abgebroche. Die Mehrzahl der Patiete i der OCA-Titratiosgruppe (91 %) erhielte UDCA. Die mediae Behadlugsdauer i beide Studiearme war aäherd gleich (OCA-Titratio: 360 Tage; Placebo: 361 Tage). Die Mehrzahl der Patiete wurde i die Strata (3) ud (4) stratifiziert ud erhielte somit währed des Behadlugszeitraumes eie Kombiatio aus OCA ud UDCA (OCA-Titratio: isgesamt 93 %; Placebo: isgesamt 94 %) (siehe Tabelle 11). Bei 13 Patiete (18 %) i der Placebogruppe ud 10 Patiete (13 %) i der OCA-Titratiosgruppe wurde Protokollabweichuge dokumetiert, bezoge auf das Eischlusskriterium Eiahme vo UDCA seit midestes 12 Moate (stabile Dosis seit 3 Moate) vor Tag 0 oder UDCA- Uverträglichkeit (keie UDCA seit 3 Moate) vor Tag 0.
40 Seite 40 Tabelle 11: Allgemeie Agabe der 12-moatige DB-Phase der POISE-Studie POISE-Studie 12-moatige DB-Phase OCA-Titratio 1) (%) Placebo 2) (%) Radomisierte Patiete 71 (100) 73 (100) Patiete, mit midestes eier Dosis (ITT-Populatio) 3,4) 70 (99) 73 (100) Patiete, mit midestes eier Dosis (Safety-Populatio) 4) 70 (99) 73 (100) Patiete ach Stratifizierugsfaktore: (1) ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud UDCA-Uverträglichkeit (2) ALP 3 x ULN ud AST 2 x ULN ud Gesamt-Bilirubi ULN zu Baselie ud UDCA-Uverträglichkeit (3) ALP > 3 x ULN ud/oder AST > 2x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud gegewärtige Eiahme vo UDCA (4) ALP 3 x ULN ud AST 2 x ULN ud Gesamt-Bilirubi ULN zu Baselie ud gegewärtige Eiahme vo UDCA Azahl der Patiete, die Moat 6 beedet habe die für Titratio ugeeiget sid die für Titratio geeiget sid o Patiete, die vo 5 mg auf 10 mg hochtitriert wurde o Patiete, die weiterhi 5 mg erhalte Azahl der Patiete, die Moat 12 beedet habe ja ei I LTSE-Phase eigeschriebe ja ei Abbruch der Eiahme der Studiemedikatio währed der DB-Phase Etzug der Eiverstädiserklärug kliische oder laboratorische UE Pruritus Lost to Follow-up Tod 3 (4) 2 (3) 22 (31) 44 (62) (97) 32 (46) 37 (53) 33 (47) 4 (6) 64 (90) 7 (10) 63 (89) 8 (11) 2 (3) 3 (4) 1 (1) 0 1 (1) 3 (4) 2 (3) 23 (32) 45 (62) 70 (96) 6 (8) 64 (88) (96) 3 (4) 66 (90) 7 (10) Mediae Behadlugsdauer uter Studiemedikatio, Tage (mi;max) 5) 360 (7;378) 361 (16;378) Durchschittliche tägliche OCA-Dosis (mg) 5) 6,2 (1,27) 5,0 (5;8) Patiete mit midestes eier Begleitmedikatio 6) 65 (93) 62 (85) 1 (1) 2 (3) ) Patiete erhalte zu Studiebegi 5 mg OCA ud köe ach Moat 6 vo 5 auf 10 mg hochtitriert werde. Patiete, die für eie Höhertitrierug icht geeiget sid, bleibe bei 5 mg. 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Ei Patiet i der OCA-Titratiosgruppe zog seie Eiverstädiserklärug ach der Radomisierug ud vor Begi der Studiemedikatio zurück. 4) Alle radomisierte Patiete, die midestes eie Dosis der Studiemedikatio erhalte habe. Zuteilug der Behadlug erfolgte ach Radomisierug (N=216). 5) Alle Patiete, die midestes eie Dosis der Studiemedikatio erhalte habe. Zuteilug der Behadlug erfolgte ach der tatsächlich erhaltee Behadlug (N=216). 6) Begleitmedikatioe, die währed der 12-moatige DB-Phase hizugekomme sid. Eie Auflistug der Begleitmedikatioe fidet sich i Tabelle 14. Abkürzuge: ALP: Alkalische Phosphatase/; AST: Aspartat-Amiotrasferase; DB: Doppelblid; ITT: Itetio-to-Treat; LTSE: Lagzeit-Sicherheitsstudie; MW: Mittelwert; OCA: ; SD: Stadardabweichug; UDCA: Ursodesoxycholsäure; ULN: obere Normgreze. 0 0
41 Seite 41 Tabelle 12 gibt eie Überblick über die Charakteristik der Studiepopulatio i beide Studiearme. Isgesamt wurde 143 Patiete i die ITT- bzw. Safety-Populatio eigeschlosse (OCA- Titratio: 70; Placebo: 73). I beide Behadlugsarme war die Mehrzahl der Patiete weiblich (jeweils 93 %), uter 65 Jahre alt (OCA-Titratio: 86 %; Placebo: 82 %) ud Kaukasier (OCA- Titratio: 96 %; Placebo: 90 %). Tabelle 12: Charakterisierug der Studiepopulatio i der 12-moatige DB-Phase der POISE-Studie zu Baselie (ITT-Populatio) POISE-Studie 12-moatige DB-Phase Geschlecht, (%) mälich weiblich Alter, i Jahre Altersklasse, (%) < 65 Jahre 65 Jahre Ethie (geetisch), (%) kaukasisch/weiß icht-kaukasisch Regio, (%) EMEA Nordamerika Australie Körpergröße, i cm Körpergewicht, i kg BMI (kg/m 2 ) Leberbiopsie vor Studiebegi, (%) ja ei ALP zu Baselie (U/l) 3 x ULN, (%) > 3 x ULN, (%) Totales Bilirubi zu Baselie (μmol/l) ULN, (%) > ULN, (%) Verbleib bei 5 mg (N=36) 2) OCA-Titratio 4 (11) 32 (89) 55,4 (10,7) 53 (30;81) 31 (86) 5 (14) 36 (100) 0 22 (61) 12 (33) 2 (6) 164,14 (7,4) 164,3 (150,0;182,2) 68,7 (12,7) 65,7 (46,7;99,3) 25,5 (4,3) 24,4 (18,2;36,9) 6 (17) 30 (83) 306,7 (121,9) 259,8 (186,8;811) 28 (78) 8 (22) 9,6 (6,2) 8,1 (2,1;36,4) 35 (97) 1 (3) Hochtitriert auf 10 mg (N=33) 2) 1 (3) 32 (97) 55,6 (10,18) 56 (29;83) 29 (88) 4 (12) 30 (91) 3 (9) 23 (70) 7 (21) 3 (9) 161 (5,9) 160 (152;174,1) 67,2 (13,8) 65 (49;101,8) 26,0 (5,6) 24,8 (17,7;40,7) 7 (21) 26 (79) 348,1 (109,1) 310,6 (212;566,3) 22 (67) 11 (33) 11,1 (4,6) 10,8 (4;22,3) 30 (91) 3 (9) OCA-Titratio gesamt (N=70) 5 (7) 65 (93) 55,8 (10,5) 54,5 (29;83) 60 (86) 10 (14) 67 (96) 3 (4) 45 (64) 20 (29) 5 (7) 162,8 (6,9) 162,5 (150,0;182,2) 68,2 (13,1) 65,2 (46,7;101,8) 25,8 (4,9) 24,6 (17,7;40,7) 13 (19) 57 (81) 325,9 (116,2) 281,3 (186,8;811,0) 51 (73) 19 (27) 10,3 (5,5) 9,1 (2,1;36,4) 66 (94) 4 (6) Placebo 1) (N=73) 5 (7) 68 (93) 55,5 (10) 55 (35;78) 60 (82) 13 (18) 66 (90) 7 (10) 49 (67) 21 (29) 3 (4) 163,6 (8,2) 164,0 (148,0;191,0) 70,2 (13,3) 70,5 (41,0;106,0) 26,2 (4,4) 25,9 (16,4;37,6) 7 (10) 66 (90) 327,5 (115,0) 311,9 (143,8;745,9) 50 (68) 23 (32) 11,8 (7,4) 9,2 (2,3; 39,3) 66 (90) 7 (10)
42 Seite 42 POISE-Studie 12-moatige DB-Phase Verbleib bei 5 mg (N=36) 2) OCA-Titratio Hochtitriert auf 10 mg (N=33) 2) OCA-Titratio gesamt (N=70) Placebo 1) (N=73) Albumi zu Baselie (g/l) LLN, (%) < LLN, (%) 42,8 (3,1) 42,3 (34,0;49,0) 30 (83) 6 (17) 43,4 (3,1) 43 (33,0;50,5) 31 (94) 2 (6) 43,4 (3,1) 43 (33;50,5) 62 (89) 8 (11) 42,7 (3,1) 43 (32,5;48,0) 59 (81) 14 (19) UDCA-Behadlug zu Baselie, (%) ja ei 32 (89) 4 (11) 32 (97) 1 (3) 65 (93) 5 (7) 68 (93) 5 (7) Tägliche UDCA-Dosis (Gesamt) (mg/kg) 3) Mittelwert (SD) 32 16,5 (4,9) 15,3 (6;32) 32 17,0 (5,9) 16,4 (8;34) 65 16,7 (5,3) 15,9 (6;34) 68 15,4 (4,5) 15,2 (7;37) 1) Als Mootherapie oder i Kombiatio mit UDCA. 2) Berücksichtigt werde ausschließlich Patiete, die Moat 6 beedet habe (N=). Abkürzuge: ALP: Alkalische Phosphatase/; DB: Doppelblid; EMEA: Europa, Naher Oste ud Afrika; ITT: Itetio-to-Treat; LLN: utere Normgreze; MW: Mittelwert; OCA: ; UDCA: Ursodesoxycholsäure; SD: Stadardabweichug. I Bezug auf die PBC-Charakteristik (siehe Tabelle 13) ware beide Behadlugsarme weitestgehed vergleichbar. I beide Behadlugsarme lag das mediae Alter zum Zeitpukt der PBC- Diagose bei 48 Jahre. Die mediae Dauer der PBC i Jahre lag i der OCA-Titratiosgruppe bei 7,2 Jahre ud i der Placebogruppe bei 7,4 Jahre. Mehr als die Hälfte der Patiete i beide Behadlugsgruppe hatte eie PBC-bedigte Pruritus zu Baselie (OCA-Titratio: 53 % vs. Placebo: 64 %), wobei die Mehrheit der Patiete de Schweregrad als mild oder moderat eistufte (OCA-Titratio: isgesamt 53 %; Placebo: isgesamt 62 %). Eie schwere Pruritus zu Baselie gabe ausschließlich 2 Patiete i der Placebogruppe a. Dieses wurde allerdigs als Ausschlusskriterium defiiert (siehe Tabelle 13, Fußote 2). I der Placebogruppe zeigte sich eie erhöhte Neigug zu eier PBC-bedigte Fatique i der Aamese (Placebo: 67 % vs. OCA-Titratio: 53 %). Tabelle 13: PBC-Charakteristik der Studiepopulatio i der 12-moatige DB-Phase der POISE- Studie zu Baselie (ITT-Populatio) POISE-Studie 12-moatige DB-Phase Verbleib bei 5 mg (N=36) OCA-Titratio Hochtitriert auf 10 mg (N=33) OCA-Titratio N=70 Placebo 1) (N=73) Alter bei PBC-Diagose, i Jahre 47,6 (12,1) 46 (27;77) 47,6 (11,3) 48 (25;77) 47,6 (11,7) 48 (25;82) 47,3 (9,3) 48 (31;74) Altersklasse bei PBC-Diagose, (%) < 50 Jahre 50 Jahre 20 (54) 17 (46) 18 (55) 15 (45) 38 (54) 32 (46) 45 (62) 28 (38) Dauer der PBC, i Jahre 8,4 (6,0) 7,1 (0,4;27,0) 8,2 (5,6) 8,3 (0,3; 18,7) 8,3 (5,8) 7,2 (0,3;27,0) 8,3 (5,4) 7,4 (0,9;21,8)
43 Seite 43 POISE-Studie 12-moatige DB-Phase Verbleib bei 5 mg (N=36) OCA-Titratio Hochtitriert auf 10 mg (N=33) OCA-Titratio N=70 Placebo 1) (N=73) Dauer der PBC-Subgruppe, (%) 7,5 Jahre > 7,5 Jahre 21 (57) 16 (43) 15 (45) 18 (55) 39 (53) 34 (47) 39 (53) 34 (47) PBC-bedigter Pruritus i der Aamese, (%) ja ei 25 (68) 12 (32) 20 (61) 13 (39) 45 (64) 25 (36) 47 (64) 26 (36) Itesität des letzte Pruritus- Ereigisses, (%) mild moderat schwer ubekat (60) 9 (36) 0 1 (4) (70) 4 (20) 2 (10) (64) 13 (29) 2 (4) 1 (2) (66) 14 (30) 1 (2) 1 (2) Pruritus zu Baselie 2), (%) ja mild moderat schwer 3) ei 23 (62) 14 (38) 9 (24) 0 14 (38) 28 (62) 20 (44) 7 (16) 1 (2) 17 (38) 37 (53) 27 (39) 10 (14) 0 33 (47) 47 (64) 32 (44) 13 (18) 2 (3) 26 (36) PBC-bedigte Fatigue i der Aamese, (%) ja ei 25 () 11 (31) 12 (36) 21 (64) 37 (53) 32 (46) 49 (67) 24 (33) Gesamt-Itesität der PBC-bedigte Fatigue, (%) mild moderat schwer 13 (36) 9 (24) 3 (8) 3 (9) 7 (21) 2 (6) 17 (24) 16 (23) 5 (7) 28 (38) 16 (22) 3 (4) gerudet auf erste Nachkommastelle 1) Als Mootherapie oder i Kombiatio mit UDCA. 2) Basiert auf der Frage zu Tag 0, ob der Patiet gegewärtig a Pruritus leidet? Ud dem Schweregrad des Pruritus basiered auf Tag 0 der 12-moatige DB-Phase. 3) Patiete mit schwerem Pruritus oder solche, die systemische Behadlug für Pruritus (z. B. mit Gallesäure-Komplexbilder oder Rifampici) ierhalb vo 2 Moate vo Tag 0 beötigte, wurde vo der Studie ausgeschlosse. Abkürzuge: DB: Doppelblid; MW: Mittelwert; OCA: ; PBC: primär biliäre Cholagitis; SD: Stadardabweichug. Begleitmedikatioe währed der 12-moatige DB-Phase Tabelle 14 gibt eie Überblick über jee Begleitmedikatioe, die währed der 2-moatige DB- Phase i weigstes eiem Studiearm vo 10 % ud mehr der Patiete eigeomme wurde. Fast alle Studieteilehmer ahme midestes eie Begleitmedikatio ei (OCA-Titratio: 93 %; Placebo: 85 %). Dabei stellte Ailide (59 %), Propiosäure-Derivate (33 %) ud Protoepumpehemmer (32 %), Cholesteri-Resorptios-Hemmer (31 %) ud Peicillie mit erweitertem Wirkspektrum (26 %) die Medikametegruppe dar, die am häufigste eigeomme wurde. Uterschiede zwische de Studiearme vo 10%-Pukte oder mehr i de Begleitmedikatioe fade sich i folgede ATC-Klasse: für die ATC-Klasse Peicillie mit erweiterte Wirkspektrum fiele die Uterschiede vo 10%-Pukte zwische de Arme zuguste vo OCA aus. Für die ATC- Klasse Protoepumpehemmer fiele die Uterschiede vo 10%-Pukte zuuguste vo OCA aus.
44 Seite 44 Tabelle 14: Begleitmedikatioe ( 10 %) i der 12-moatige DB-Phase der POISE-Studie ATC-Klasse 4, Preferred Term 1) Patiete mit midestes eier Begleitmedikatio Ailide Paracetamol Cholesteri-Resorptios-Hemmer COLESTYRAMINE Propiosäure-Derivate IBUPROFEN OCA-Titratio N=70 (%) 24 (34) 21 (30) 14 (20) 13 (19) 13 (19) 10 (14) Placebo 2) N=73 (%) 18 (25) 17 (23) 8 (11) 8 (11) 10 (14) 7 (10) Protoepumpehemmer 3) 8 (11) 15 (21) Peicilli mit erweitertem Wirkspektrum AMOXICILLIN 13 (19) 9 (13) 5 (7) 4 (5) Adere Histamie 3) 9 (13) 6 (8) Vitami D ud Aaloga 3) 7 (10) 9 (12) Calcium, Kombiatio mit Vitami D ud/oder adere Wirkstoffe 3) 7 (10) 6 (8) Piperazie-Derivate 3) 7 (10) 5 (7) Glucocorticosteroide 3) 8 (11) 5 (7) Bezodiazepie 3) 6 (9) 7 (10) Schilddrüsehormoe 3) 8 (11) 2 (3) 1) Patiete wurde ur eimal i jeder ATC-Klasse ud Preferred Term gezählt. 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Kei Preferred Term wurde mit 10 % der Patiete beobachtet. Abkürzuge: ATC: Aatomisch-Therapeutisch-Chemisch; OCA:. LTSE-Phase I Tabelle 15 sid die allgemeie Agabe der Studie für de Dateschitt zum 31. August 2014 differeziert ach der gewichtete durchschittliche Tagesdosis (WADD) dargestellt. Vo Relevaz für die vorliegede Nutzebewertug sid etspreched der Zulassug ausschließlich die Patiete mit eier WADD 10 mg OCA (N=172). Die Patiete mit eier WADD > 10 mg OCA (N=21) werde achfolged icht weiter berücksichtigt. Vo 172 Patiete mit eier WAAD vo 10 mg hatte i der 12-moatige DB-Phase bereits 159 Patiete (92 %) mit UDCA begoe. Währed der 12-moatige DB-Phase ud der LTSE- Phase kam es bei 10 Patiete (6 %) zu eier Sekug der UDCA-Dosis. Demgegeüber wurde die Dosis i de beide Studiephase bei 3 Patiete (2 %) gesteigert. Eie dauerhafte Abbruch der UDCA-Behadlug i de beide Studiephase erlebte 5 Patiete (3 %). Isgesamt wurde 193 Patiete i die LTSE-Phase eigeschlosse. Die mediae Behadlugsdauer uter OCA umfasste im Media 649 Tage (Spae: Tage). Isgesamt wurde währed der LTSE-Phase die Behadlug vo 10 der 193 Patiete (5,2 %) abgebroche. Die relevate Patietepopulatio i der vorliegede Nutzebewertug (N=172) erhielt eie gewichtete durchschittliche Tagesdosis (WADD) OCA vo 10 mg. I dieser erhielte 155 Patiete (90 %) midestes eie Begleitmedikatio.
45 Seite 45 Tabelle 15: Allgemeie Agabe der LTSE-Phase der POISE-Studie WADD POISE-Studie LTSE-Phase 5 mg OCA (%) > 5 10 mg OCA (%) 10 mg OCA (%) alle Patiete 1) (%) Eigeschlossee Patiete, (%) 44 (100) 128 (100) 172 (100) 193 (100) Patiete, mit midestes eier Dosis (Safety-Populatio) 2), (%) 44 (100) 128 (100) 172 (100) 193 (100) 2-Jahres-Completer-Populatio 3) 5 (11) 37 (29) 42 (24) 49 (25) Patiete ach Stratifizierugsfaktore, (%): (1) ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud UDCA-Uverträglichkeit (2) ALP 3 x ULN ud AST 2 x ULN ud Gesamt-Bilirubi ULN zu Baselie ud UDCA-Uverträglichkeit (3) ALP > 3 x ULN ud/oder AST > 2 x ULN ud/oder Gesamt-Bilirubi > ULN zu Baselie ud gegewärtige UDCA- Eiahme (4) ALP 3 x ULN ud AST 2 x ULN ud Gesamt-Bilirubi ULN zu Baselie ud gegewärtige UDCA-Eiahme Gruppezuordug i der 12-moatige DB- Phase 4), (%) Placebo OCA-Titratiosgruppe Patiete, die vo 5 mg auf 10 mg hochtitriert wurde Patiete, die weiterhi 5 mg erhalte OCA 10 mg Abbruch der Eiahme der Studiemedikatio währed der LTSE-Phase, (%) Etzug der Eiverstädiserklärug Tod Pruritus kliische oder laboratorische UE Lost to Follow-up Protokollabweichuge Mediae Behadlugstage uter OCA (mi;max), (%) weiger als 6 Moate 6 Moate bis uter eiem Jahr Ei Jahr bis uter 2 Jahre 2 Jahre ud mehr OCA-WAAD 5 mg OCA, (%) > 5 bis 10 mg OCA, (%) > 10 mg OCA, (%) 3 (7) 3 (7) 6 (14) 32 (73) 26 (59) 16 (36) 0 16 (36) 2 (5) (5) 2 (5) 0 5 (4) 1 (< 1) 42 (33) 80 (63) 30 (32) 43 (34) 29 (23) 14 (11) 55 (43) 2 (2) 1 (1) 1 (1) 2 (2) (5) 4 (2) 48 (28) 112 (65) 56 (33) 59 (34) 29 (17) 30 (17) 57 (33) 2 (1) 1 (< 1) 1 (< 1) 4 (2) 2 (1) 0 k.a. k.a. k.a. k.a. k.a. k.a. 8 (4) 4 (2) 57 (30) 124 (64) 66 (34) 63 (33) 33 (17) 30 (16) 64 (33) 2 (1) 1 (< 1) 1 (< 1) 4 (2) 2 (1) (7;894) 6 (3) 42 (22) 104 (54) 40 (21) 7,3 (2,19) 7,3 (2;13) 44 (23) 128 (66) 21 (11)
46 Seite 46 POISE-Studie LTSE-Phase Patiete mit midestes eier Begleitmedikatio, (%) 5 mg OCA (%) > 5 10 mg OCA (%) WADD 10 mg OCA (%) alle Patiete 1) (%) 38 (86) 117 (91) 155 (90) 175 (91) Dateschitt: ) Etspricht OCA-Gesamt (Kombiatio aller WAAD-Gruppe; N=193), d. h. Summe der Patiete mit 10 mg OCA (N=172) ud > 10 mg OCA (N=21). 2) Alle Patiete, die Währed der LTSE-Phase jegliche Mege a OCA erhalte habe. 3) Alle Patiete, dere OCA-Expositio midestes 2 Jahre umfasste. 4) Patiete, die die 12-moatige DB-Phase beedet habe ud i die LTSE-Phase eigeschriebe wurde. Grüde dafür, warum weiger Patiete i die LTSE-Phase eigeschriebe wurde als sie beedet habe, liege im Studiebericht icht vor. Abkürzuge: ALP: Alkalische Phosphatase/; AST: Aspartat-Amiotrasferase; DB: Doppelblid; LTSE: Lagzeit-Sicherheitsstudie; MW: Mittelwert; OCA: ; UDCA: Ursodesoxycholsäure; UE: uerwüschte/s Ereigis/se; ULN: obere Normgreze; WAAD: gewichtete durchschittliche Tagesdosis; SD: Stadardabweichug; Tabelle 16 gibt eie Überblick über die Charakteristik der Studiepopulatio für die i dieser Nutzebewertug relevate WAAD-Gruppe 10 mg OCA. Gemäß SAP etspreche die demographische Merkmale der Patiete de Date zum Zeitpukt ihres Eitritts i die 12-moatige DB- Phase. Die LTSE-Baseliewerte hisichtlich der PBC-Erkrakugsmerkmale sid für jee Patiete, die aus der OCA-Titratiosgruppe stamme, die Baseliewerte der DB-Phase; für die Placebo- Patiete aus der DB-Phase die letzte Date vor eier OCA-Gabe bei Eitritt i die LTSE-Phase. Isgesamt wurde 172 Patiete i die Safety-Populatio der WAAD-Gruppe 10 mg OCA eigeschlosse. Die Mehrzahl der Patiete war weiblich (92 %), uter 65 Jahre alt (82 %) ud Kaukasier (94 %). I Bezug auf die PBC-Charakteristik lag das mediae Alter zum Zeitpukt der PBC-Diagose bei 47,5 Jahre (Spae: 24 82). Die mediae Dauer der PBC lag bei 7,9 Jahre (Spae: 0 32). Mehr als die Hälfte der Patiete hatte eie PBC-bedigte Pruritus zu Baselie (62 %). Tabelle 16: Charakterisierug der Studiepopulatio der LTSE-Phase der POISE-Studie zu Baselie (Safety-Populatio) 1) POISE-Studie LTSE-Phase Geschlecht, (%) mälich weiblich Alter, i Jahre Altersklasse, (%) < 65 Jahre 65 Jahre Ethie (geetisch), (%) kaukasisch/weiß icht-kaukasisch Regio, (%) Europa Nordamerika Australie WADD 10 mg OCA (N=172) 14 (8) 158 (92) 55,6 (10,2) 55,0 (29; 83) 141 (82) 31 (18) 162 (94) 20 (6) 110 (64) 54 (31) 8 (5)
47 Seite 47 POISE-Studie LTSE-Phase Körpergröße, i cm Körpergewicht, i kg BMI ALP zu Baselie (U/l) 3x ULN, (%) > 3x ULN, (%) Totales Bilirubi zu Baselie (μmol/l) ULN, (%) > ULN, (%) Albumi zu Baselie (g/l) LLN, (%) < LLN, (%) UDCA-Behadlug zu OCA-Baselie, (%) ja ei Tägliche UDCA-Dosis (Gesamt) (mg/kg) 2) PBC-Charakteristik Alter bei PBC-Diagose, i Jahre Altersklasse bei PBC-Diagose, (%) < 50 Jahre 50 Jahre Dauer der PBC, i Jahre Mittelwert (SD) Dauer der PBC-Klasse, (%) 7,5 Jahre > 7,5 Jahre PBC-bedigter Pruritus i der Aamese, (%) ja ei WADD 10 mg OCA (N=172) 163,2 (7,4) 163,5 (147,2; 188,7),9 (14,1) 67,5 (44; 134) 26,2 (4,8) 25,2 (16,7; 49,2) 316,0 (120,6) 268 (148,5; 811,0) 126 (73) 46 (27) 11,4 (6,9) 9,3 (1,6; 38) 155 (90) 17 (10) 43 (3,3) 43,4 (30,9; 50,5) 29 (17) 143 (83) 159 (92) 13 (8) ,8 (4,9) 15,4 (3,8; 34) 47,1 (10,0) 47,5 (24;82) 100 (58) 72 (42) 8,6 (6,0) 7,9 (0;32,3) 82 (48) 90 (52) 106 (62) 66 (38)
48 Seite 48 POISE-Studie LTSE-Phase WADD 10 mg OCA (N=172) Itesität des letzte Pruritus-Ereigisses, (%) mild moderat schwer ubekat Pruritus zu Baselie 3), (%) ja mild moderat schwer ei PBC-bedigte Fatigue i der Aamese, (%) ja ei Gesamt-Itesität der PBC-bedigte Fatigue, (%) mild moderat schwer (67) 28 (26) 5 (5) 2 (2) 95 (55) (40) 24 (14) 2 (1) 77 (45) 98 (57) 74 (43) 58 (34) 29 (17) 10 (6) 1) Hiweis: Gemäß SAP etspreche die demographische Merkmale der Patiete de Date zum Zeitpukt ihres Eitritts i die 12-moatige DB-Phase. Die LTSE-Baseliewerte hisichtlich der PBC-Erkrakugsmerkmale sid für die Patiete, die aus der OCA-Titratiosgruppe stamme, die Baseliewerte der DB-Phase, für die Placebo-Patiete aus der DB-Phase die letzte Date vor eier OCA-Gabe bei Eitritt i die LTSE-Phase. 2) Die tägliche Gesamtdosis vo UDCA i mg/kg wird uter Verwedug der letzte Dosierug bestimmt, die vor der erste Dosis des Studiearzeimittels agegebe wurde, dividiert durch das Gewicht i kg bei OCA-Baselie. 3) Basiert auf der Frage zu Tag 0, ob der Patiet gegewärtig a Pruritus leidet? Ud dem Schweregrad der Pruritus basiered auf Tag 0 der 12-moatige DB-Phase. Abkürzuge: LLN: utere Normgreze; LTSE: Lagzeit-Sicherheitsstudie; OCA: ; PBC: primär biliäre Cholagitis; SD: Stadardabweichug; UDCA: Ursodesoxycholsäure; ULN: obere Normgreze; WADD: gewichtete durchschittliche Tagesdosis. Begleitmedikatioe währed der LTSE-Phase Tabelle 17 gibt eie Überblick über jee Begleitmedikatioe, die währed der LTSE-Phase vo 10 % ud mehr der Patiete eigeomme wurde. Fast alle Studieteilehmer ahme midestes eie Begleitmedikatio ei (N=150). Dabei stellte Ailide ud Cholesteri-Resorptios- Hemmer mit jeweils 18 % die Medikametegruppe dar, die am häufigste eigeomme wurde. Tabelle 17: Begleitmedikatioe ( 10 %) i der LTSE-Phase der POISE-Studie (Safety-Populatio) ATC-Klasse 2, Preferred Term WADD vo 10 mg OCA (N=172) (%) Ailide 1) Paracetamol 1) Cholesteri-Resorptios-Hemmer COLESTYRAMINE 31 (18) 28 (16) 31 (18) 30 (17) Propiosäure-Derivate 2,3) 25 (15) Protoepumpehemmer 3) 29 (17) Vitami D ud Aaloga 3) 26 (15) Glucocorticosteroide 3) 20 (12) Adere Histamia 3) 17 (10)
49 Seite 49 1) I Tabelle des CSR ist die Klasse der Ailide zweimal aufgeführt. Hier dargestellt sid die Date aus dem erstmalige Vermerk im CSR. Die Date des zweite Vermerks laute: Ailide 29 (17 %), Paracetamol 27 (16 %). 2) I Tabelle des CSR ist die Klasse der Propiosäure-Derivate zweimal aufgeführt. Hier dargestellt sid die Date aus dem erstmalige Vermerk im CSR. Die Date des zweite Vermerks laute: Propiosäure-Derivate 18 (10 %). 3) Kei Preferred Term wurde mit 10 % der Patiete beobachtet. Abkürzuge: ATC: Aatomisch-Therapeutisch-Chemisch; LTSE: Lagzeit-Sicherheitsstudie; OCA: ; WADD: gewichtete durchschittliche Tagesdosis Mortalität 12-moatige DB-Phase Das Gesamtüberlebe wurde als UE für die Sicherheitspopulatio erfasst. Währed der 12-moatige DB-Phase trat i der OCA-Titratiosgruppe ei Todesfall ud i der Placebogruppe kei Todesfall auf. Todesursache war Herzversage aufgrud eier umfagreiche Krakevorgeschichte vo kardiovaskuläre Ereigisse, der ach Agabe des pu icht im direkte Zusammehag mit der Studiemedikatio steht. LTSE-Phase Mortalität war gemäß Protokoll für die Auswertug der LTSE-Phase kei geplater Effektivitätsparameter. Gleichwohl wurde Todesfälle als SUE erfasst. I der LTSE-Phase trat im Erhebugszeitraum (Dateschitt: 31. August 2014) ei Todesfall auf. Dieser Patiet erhielt währed der 12-moatige DB-Phase 10 mg OCA plus UDCA ud zu Begi der LTSE-Phase 5 mg OCA plus UDCA, dass ach vier Moate auf 10 mg hochtitriert wurde. Der Patiet verstarb a Multiorgaversage aufgrud eier Sepsis, die er ach eier Edokarditis etwickelt hatte. Laut Agabe des pu steht der Todesfall icht im direkte Zusammehag mit der Studiemedikatio Morbidität Pruritus 12-moatige DB-Phase Die Ergebisse für de Edpukt Pruritus werde mit Hilfe des 5-D-Frageboges ud der VAS dargestellt ud basiere auf der Safety-Populatio. Uter Verwedug der MMRM-Methode kote keie sigifikate Uterschiede zwische OCA-Titratiosgruppe ud Placebogruppe zu Moat 6 ud 12 gezeigt werde. Ei ähliches Bild zeigt sich auch uter Verwedug der a priori defiierte Methode mittels ANCOVA (siehe Tabelle 41 im Ahag).
50 Seite 50 Tabelle 18: Ergebisse zum 5-D-Pruritus-Frageboge ud zur Pruritus-VAS ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie (Safety-Populatio; MMRM-Modell) POISE-Studie 12-moatige DB-Phase OCA- Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) 5-D-Frageboge 3) Gesamtscore Zum jeweilige Erhebugszeitpukt 63 10,2 (3,61) 9,0 (5;19) 65 10,9 (5,00) 10,0 (5;24) 66 10,7 (4,82) 9,0 (5;23) 62 10,5 (4,68) 10,0 (5;23) 59 10,9 (4,79) 10,0 (5;23) 63 10,7 (4,44) 10,0 (5;24) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,50 (0,61) 61 0,60 (0,63) 54 2,07 (0,61) 58 0,82 (0,61) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,90 (0,) [-0,47;2,26] 0,1962 1,25 (0,68) [-0,08;2,59] 0, D-Frageboge 3) Dauer Zum jeweilige Erhebugszeitpukt 65 1,2 (0,57) 1,0 (1;5) 1,4 (0,97) 1,0 (1;5) 68 1,4 (0,90) 1,0 (1;5) 65 1,3 (0,91) 1,0 (1;5) 60 1,5 (1,23) 1,0 (1;5) 66 1,3 (0,90) 1,0 (1;5) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,43 (0,14) 63 0,23 (0,14) 56 0,62 (0,16) 65 0,26 (0,16) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,20 (0,14) [-0,09;0,48] 0,1719 0,36 (0,18) [0,00;0,71] 0, D-Frageboge 3) Schweregrad Zum jeweilige Erhebugszeitpukt 68 1,9 (1,00) 2,0 (1;4) 70 2,0 (0,99) 2,0 (1;5) 2,0 (1,03) 2,0 (1;5) 68 2,0 (1;4) 1,9 (0,94) 61 2,1 (1,03) 2,0 (1;5) 66 2,0 (0,89) 2,0 (1;4) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,30 (0,13) 66 2,0 (1;4) 60 0,39 (0,13) 65 0,20 (0,13) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,18 (0,15) [-0,11;0,48] 0,2223 0,18 (0,14) [-0,09;0,46] 0,1940
51 Seite 51 POISE-Studie 12-moatige DB-Phase OCA- Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) 5-D-Frageboge 3) Richtug Zum jeweilige Erhebugszeitpukt 64 3,1 (1,19) 4,0 (1;5) 65 3,2 (1,42) 4,0 (1;5) 67 3,0 (1,41) 3,0 (1;5) 62 2,8 (1,31) 3,0 (1;5) 60 3,1 (1,32) 4,0 (1;5) 64 2,9 (1,29) 3,0 (1;5) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,03 (0,19) 59-0,25 (0,20) 56 0,13 (0,19) 59-0,26 (0,19) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,22 (0,23) [-0,23;0,68] 0,3343 0,38 (0,23) [-0,08;0,84] 0, D-Frageboge 3) Behiderug Zum jeweilige Erhebugszeitpukt 67 1,9 (1,13) 1,0 (1;5) 1,8 (1,37) 1,0 (1;5) 2,0 (1,24) 1,0 (1;5) 65 1,9 (1,22) 1,0 (1;5) 61 2,0 (1,30) 1,0 (1;5) 66 1,9 (1,20) 1,0 (1;5) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,39 (0,16) 63 0,19 (0,16) 59 0,42 (0,16) 64 0,22 (016) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,20 (0,18) [-0,15;0,55] 0,2595 0,20 (0,18) [-0,16;0,55] 0,28 5-D-Frageboge 3) Verteilug Zum jeweilige Erhebugszeitpukt 68 2,0 (1,19) 1,5 (1;5) 70 2,3 (1,45) 2,0 (1;5) 2,2 (1,28) 2,0 (1;5) 68 2,3 (1,47) 1,5 (1;5) 61 2,2 (1,30) 2,0 (1;5) 67 2,4 (1,43) 2,0 (1;5) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,37 (0,16) 66 0,19 (0,16) 60 0,45 (0,16) 66 0,26 (0,16) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,18 (0,18) [-0,17;0,53] 0,3144 0,18 (0,17) [-0,15;0,52] 0,2825 Pruritus-VAS 5,6) Zum jeweilige Erhebugszeitpukt 21,2 (26) 10,0 (0;84) 25,3 (27,5) 16,5 (0;100) 23,3 (26,6) 10,0 (0;91) 20,6 (23,0) 10,0 (0;87) (27,2) 10,0 (0;90) 24,7 (25) 12,0 (0;80)
52 Seite 52 POISE-Studie 12-moatige DB-Phase OCA- Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,5 (3,2) 66 1,6 (3,3) 60 10,2 (3,2) 66 5,9 (3,2) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 6 (3,6) [-1,1;13] 0,0968 4,4 (3,5) [-2,6;11,3] 0,2209 1) Baselie ist defiiert als Wert a Tag 0 vor Behadlug. 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Die zu erreichede Gesamtpuktzahl liegt zwische 5 ud 25 Pukte. Jede Domäe ka eie Puktwert vo 1 bis 5 Pukte erreiche. Höhere Pukte deute auf eie stärkere Pruritus hi. 4) Berechug der p-werte basiered auf der MMRM-Methode mit fixed effects für Behadlug, Zeit, Iteraktiosterm für Behadlugsgruppe ud Zeit ud ach zur Radomisierug verwedete Stratavariable sowie Baseliewert als Kovariate. 5) Scores reiche vo 0 (kei Pruritus) bis 100 (schwere Pruritus). 6) Gerudet auf die erste Nachkommastelle. Abkürzuge: DB: Doppelblid; KI: Kofidezitervall; LS-MW: Least-squares-Mittelwert; LS-MWD: Least-squares-Mittelwertdifferez; MMRM: gemischtes Modell für wiederholte Messuge; MW: Mittelwert; OCA: ; SD: Stadardabweichug, SE: Stadardfehler; VAS: visuelle Aalogskala. LTSE-Phase I Tabelle 19 werde die Ergebisse für de 5-D-Frageboge ud die VAS auf Basis der Safety- Populatio für die WADD-Gruppe 10 mg OCA dargestellt. Für Patiete, die währed der 12-moatige DB-Phase Placebo erhielte, umfasst OCA-Baselie die letzte Bewertug vor der erste OCA-Dosierug i der LTSE-Phase. Im Gegesatz dazu umfasst OCA-Baselie für Patiete, die währed der 12-moatige DB-Phase OCA erhielte, de Durchschitt aller Bewertuge vor der 12-moatige DB-Phase. Tabelle 19: Ergebisse zum 5-D-Pruritus-Frageboge ud zur Pruritus-VAS i der LTSE-Phase der POISE-Studie ach OCA-Baselie (Safety-Populatio) POISE-Studie LTSE-Phase WADD vo 10 mg OCA (N=172) OCA-Baselie 1) Moat 12 5-D-Frageboge 2) Gesamtscore Zum jeweilige Erhebugszeitpukt Veräderug zum OCA-Baselie (3.96) 9 (5; 24) ,1 (4.92) 10 (5;23) 114 1,6 (4,07) 1,0 (-8;14)
53 Seite 53 POISE-Studie LTSE-Phase WADD vo 10 mg OCA (N=172) OCA-Baselie 1) Moat 12 5-D-Frageboge 2) Dauer Zum jeweilige Erhebugszeitpukt (%) Veräderug zum OCA-Baselie (%) 5-D-Frageboge 2) Schweregrad Zum jeweilige Erhebugszeitpukt (%) Veräderug zum OCA-Baselie (%) 5-D-Frageboge 2) Richtug Zum jeweilige Erhebugszeitpukt (%) Veräderug zum OCA-Baselie (%) 5-D-Frageboge 2) Behiderug Zum jeweilige Erhebugszeitpukt (%) Veräderug zum OCA-Baselie (%) 5-D-Frageboge 2) Verteilug Zum jeweilige Erhebugszeitpukt (%) Veräderug zum OCA-Baselie (%) 159 1,2 (0,59) 1 (1;5) ,8 (0,9) 2 (1;4) ,1 (1,30) 4 (1;5) ,8 (1,14) 1 (1;5) ,0 (1,24) 1 (1;5) ,5 (1,09) 1 (1;5) 120 0,4 (1,07) 0 (-2; ,1 (0,98) 2,0 (1;5) 126 0,3 (0,90) 0 (-2;3) 128 3,1 (1,36) 4 (1;5) 116 0,1 (1,43) 0 (-3;3) (1,31) 1 (1;5) 123 0,3 (1,14) 0 (-2;4) 131 2,4 (1,41) 2 (1;5) 126 0,5 (1,11) 0 (-2;4)
54 Seite 54 POISE-Studie LTSE-Phase WADD vo 10 mg OCA (N=172) OCA-Baselie 1) Moat 12 Pruritus-VAS 3) Zum jeweilige Erhebugszeitpukt (%) Veräderug zum OCA-Baselie (%) ,1 (24,05) 10,0 (0;92) ,4 (27,97) 12,5 (0;100) 127 4,5 (21,19) 0 (-41;90) 1) Für Patiete, die währed der 12-moatige DB-Phase Placebo erhielte, umfasst OCA-Baselie die letzte Bewertug vor der erste OCA-Dosierug i der LTSE-Phase. Im Gegesatz dazu umfasst OCA-Baselie für Patiete, die währed der 12- moatige DB-Phase OCA erhielte, de Durchschitt aller Bewertuge vor der 12-moatige DB-Phase. 2) Die zu erreichede Gesamtpuktzahl liegt zwische 5 ud 25 Pukte. Jede Domäe ka eie Puktwert vo 1 bis 5 Pukte erreiche. Höhere Pukte deute auf eie stärkere Pruritus hi. 3) Scores reiche vo 0 (kei Pruritus) bis 100 (schwerer Pruritus). Abkürzuge: KI: Kofidezitervall; LS-MW: Least-squares-Mittelwert; LS-MWD: Least-squares-Mittelwertdifferez; LTSE: Lagzeit-Sicherheitsstudie; MW: Mittelwert; OCA: ; SD: Stadardabweichug, SE: Stadardfehler; VAS: visuelle Aalogskala; WADD: gewichtete durchschittliche Tagesdosis Primärer kombiierter Edpukt (Ateil Patiete mit ALP < 1,67 x ULN, Gesamt-Bilirubi ULN ud AP-Reduktio vo 15 %) 12-moatige DB-Phase Der primäre kombiierte Edpukt Ateil Patiete mit ALP < 1,67 x ULN, Gesamt-Bilirubi ULN ud AP-Reduktio vo 15 % wird im Folgede ergäzed dargestellt, aber icht zur Nutzebewertug vo heragezoge (vgl. Tabelle 8). Die Darstellug der Ergebisse basiere auf der ITT-Populatio. I Tabelle 20 werde die Ergebisse des primäre kombiierte Edpuktes ud desse Eizelkompoete für Moat 6 ud 12 zwische de Behadlugsgruppe OCA-Titratio (N=70) ud Placebo (N=73) dargestellt. Isgesamt erreichte 24 vo 70 Patiete (34 %) zu Moat 6 ud 32 vo 70 Patiete (46 %) i der OCA-Titratiosgruppe de kombiierte Edpukt. Der Uterschied zwische OCA-Titratiosgruppe ud Placebogruppe war zu Moat 6 ud Moat 12 statistisch sigifikat. Zu de Eizelkompoete des primäre kombiierte Edpuktes liege im Studiebericht ausschließlich Date für de ALP Wert 15 % vor. Tabelle 20: Ergebisse zum primäre kombiierte Edpukt ud de Eizelkompoete ach 6 ud 12 Moate i der 12-moatige DB-Phase (ITT-Populatio, Respoderaalyse) POISE-Studie 12-moatige DB-Phase OCA-Titratio (N=70) Moat 6 Moat 12 Placebo 1) (N=73) OCA-Titratio (N=70) Placebo 1) (N=73) Ateil Patiete mit ALP < 1,67 x ULN, Gesamt-Bilirubi ULN ud ALP-Reduktio 15 % Respoder 2), (%) 24 (34) 5 (7) 32 (46) 7 (10) Nicht-Respoder, (%) 46 (66) 68 (93) 38 (54) 66 (90) CMH p-wer 3) <0,0001 <0,0001 OR [95%-KI] 8,0 [2,8;23,0] 9,1 [3,6;23,2] Logistic p-wert 4) 0,0001 <0,0001
55 Seite 55 POISE-Studie 12-moatige DB-Phase OCA-Titratio (N=70) Moat 6 Moat 12 Placebo 1) (N=73) OCA-Titratio (N=70) Placebo 1) (N=73) ALP < 1,67 x ULN Keie Date im CSR 5) Bilirubi ULN Keie Date im CSR 5) ALP-Reduktio 15 % Respoder 2), (%) 50 (71) 18 (25) 54 (77) 21 (29) Nicht-Respoder, (%) 20 (29) 55 (75) 16 (23) 52 (71) CMH p-wert 3) <0,0001 <0,0001 OR [95%-KI] 7,8 [3,7;16,5] 8,4 [4,0;17,9] Logistic p-wert 4) <0,0001 <0,0001 1) Als Mootherapie oder i Kombiatio mit UDCA. 2) Respoder sid defiiert mit ALP < 1,67x ULN ud Gesamt-Bilirubi < ULN ud ALP Abahme vo 15 % zu Baselie. Patiete mit fehlede Werte gelte als Nicht-Respoder. 3) Berechug der p-werte basiered auf dem Cochra-Matel-Haeszel-Test stratifiziert ach zur Radomisierug verwedete Stratavariable. 4) Berechug der p-werte basiered auf dem logistische Regressiosmodell mit zur Behadlug ud Radomisierug verwedete Stratavariable. 5) Date für die Eizelkompoete sid ausschließlich i Modul 4 des Herstellerdossiers für die OCA-Titratiosgruppe differeziert ach Moo- ud Kombiatiostherapie agegebe. Abkürzuge: ALP: Alkalische Phosphatase; CSR: kliischer Studiebericht; DB: Doppelblid; ITT: Itetio-to-Treat; KI: Kofidezitervall; OCA: ; OR: Odds Ratio. Differezierug ach Titratiosstatus i der OCA-Titratiosgruppe I der OCA-Titratiosgruppe erreichte Patiete Moat 6. Vo diese verbliebe 36 Patiete (52 %) bei 5 mg OCA, währed 33 Patiete (48 %) de kombiierte Edpukt icht erreichte ud auf 10 mg OCA hochtitriert wurde. Vo de Patiete, die auf 10 mg hochtitriert wurde (N=33), erreichte 13 Patiete (39 %) ach 12 Moate de primäre kombiierte Edpukt. LTSE-Phase I Tabelle 21 werde die Ergebisse des primäre kombiierte Edpuktes ud desse Eizelkompoete vo Baselie (LTSE-Tag 0) bis Moat 12 für die WADD-Gruppe 10 mg OCA dargestellt. Isgesamt erreichte zu Baselie der LTSE-Phase 70 Patiete (41 %) de primäre kombiierte Edpukt, währed 101 Patiete (59 %) diese och icht erreicht hatte. Zu Moat 12 liege och Date vo 61 Patiete vor, vo dee 30 Patiete (49 %) de kombiierte Edpukt erreichte. Zu de Eizelkompoete des primäre kombiierte Edpuktes liege im Studiebericht ausschließlich Date für de ALP-Wert 15 % vor.
56 Seite 56 Tabelle 21: Ergebisse zum primäre kombiierte Edpukt i der LTSE-Phase der POISE-Studie ach 12 Moate (Safety-Populatio, Respoderaalyse) POISE-Studie LTSE-Phase WADD vo 10 mg OCA (N=172) Baselie LTSE-Phase Moat 12 Ateil Patiete mit ALP < 1,67 x ULN, Gesamt-Bilirubi ULN ud ALP-Reduktio 15 % Gesamt, Respoder 1), (%) 70 (41) 30 (49) Nicht-Respoder, (%) 101 (59) 31 (51) ALP <1,67 x ULN Bilirubi ULN ALP-Reduktio 15 % Keie Date im CSR Keie Date im CSR Gesamt, Respoder 1), (%) 120 (70) 53 (87) Nicht-Respoder, (%) 51 (30) 8 (13) 1) Respoder sid defiiert mit ALP < 1,67 x ULN ud Gesamt-Bilirubi < ULN ud ALP-Abahme vo 15 % zu Baselie. Patiete mit fehlede Werte gelte als Nicht-Respoder. Abkürzuge: ALP: Alkalische Phosphatase; CSR: kliischer Studiebericht; LTSE: Lagzeit-Sicherheitsstudie; OCA: ; ULN: obere Normgreze Lebesqualität 12-moatige DB-Phase I Tabelle 22 werde die Ergebisse für de PBC-40-Frageboge auf Basis der ITT-Populatio dargestellt. Uter Verwedug der MMRM-Methode kote keie sigifikate Uterschiede zwische OCA-Titratiosgruppe ud Placebogruppe zu Moat 6 ud 12 gezeigt werde. Ei ähliches Bild zeigt sich auch uter Verwedug der a priori defiierte Methode mittels ANCOVA (siehe Tabelle 42 im Ahag).
57 Seite 57 Tabelle 22: Ergebisse zum PBC-40-Frageboge ach 6 ud 12 Moate i der 12-moatige DB- Phase der POISE-Studie (ITT-Populatio; MMRM-Modell) POISE-Studie 12-moatige DB-Phase OCA- Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) Geerelle Symptome 3) Zum jeweilige Erhebugszeitpukt 70 13,8 (5,27) 13,0 (6;27) 72 13,1 (4,82) 12,0 (6;29) 13,5 (5,00) 14,0 (6;26) 70 13,1 (4,88) 12,0 (6;26) 62 13,6 (4,97) 13,0 (6;24) 13,8 (4,92) 13,0 (6;32) Veräderug zum Erhebugszeitpukt LS-MW (SE) - - 0,20 (0,47) 0,13 (0,47) 62 0,44 (0,48) 68 0,76 (0,47) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,06 (0,54) [-1,01;1,13] 0,9105-0,32 (0,55) [-1,41;0,77] 0,5660 Jucke 3) Zum jeweilige Erhebugszeitpukt 4,1 (3,55) 3,0 (0;14) 72 4,3 (3,) 3,0 (0;15) 4,6 (3,50) 4,0 (0;14) 70 4,1 (3,55) 3,0 (0;14) 62 4,6 (3,30) 4,0 (0;14) 4,4 (3,35) 3,0 (0;15) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,91 (0,41) 0,28 (0,42) 62 1,19 (0,41) 68 0,64 (0,41) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,63 (0,45) [-0,26;1,52] 0,1649 0,55 (0,44) [-0,32;1,41] 0,2156 Fatigue 3) Zum jeweilige Erhebugszeitpukt 70 25,9 (10,83) 24,0 (11;50) 72 26,2 (11,18) 25,0 (11;53) 25,7 (9,74) 25,0 (11;50) 70 23,8 (10,99) 20,0 (11;51) 62 25,2 (10,11) 25,5 (11;49) 23,8 (11,56) 22,0 (11;54) Veräderug zum Erhebugszeitpukt LS-MW (SE) ,16 (0,92) -2,06 (0,92) 62-0,54 (0,93) 68-2,30 (0,93) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 1,90 (1,06) [-0,19;3,99] 0,0748 1,76 (1,08) [-0,37;3,89] 0,1048
58 Seite 58 POISE-Studie 12-moatige DB-Phase OCA- Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) Kogitive Fuktio 3) Zum jeweilige Erhebugszeitpukt 70 11,6 (5,96) 10,5 (6;28) 70 11,4 (5,40) 9,0 (6;23) 12,0 (5,63) 11,0 (6;26) 70 11,5 (5,40) 10,5 (6;26) 62 11,5 (5,51) 11,0 (6;30) 11,7 (6,38) 9,0 (6;30) Veräderug zum Erhebugszeitpukt LS-MW (SE) - - 0,46 (0,48) -0,08 (0,48) 62 0,01 (0,50) 68 0,10 (0,49) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,54 (0,58) [-0,60;1,67] 0,3517-0,09 (0,60) [-1,27;1,09] 0,8790 Soziale Domäe 3) Zum jeweilige Erhebugszeitpukt 70 19,7 (8,63) 17,0 (10;45) 72 21,0 (8,81) 18,5 (10;46) 19,7 (8,00) 17,0 (10;46) 18,9 (8,82) 16,0 (9;45) 62 19,7 (7,71) 18,0 (10;46) 19,1 (9,45) 16,0 (8;48) Veräderug zum Erhebugszeitpukt LS-MW (SE) - - 0,20 (0,82) -1,53 (0,82) 62 0,36 (0,89) 68 1,38 (0,88) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 1,73 (0,93) [-0,11;3,57] 0,0653 1,75 (1,05) [-0,32;3,81] 0,0972 Emotioale Domäe 3) Zum jeweilige Erhebugszeitpukt 70 6,4 (2,87) 6,0 (3;14) 72 6,8 (3,31) 6,0 (3;15) 6,4 (2,95) 6,0 (3;14) 70 6,2 (3,06) 5,0 (3;14) 62 6,3 (2,67) 6,0 (3;12) 6,2 (3,08) 5,0 (3;14) Veräderug zum Erhebugszeitpukt LS-MW (SE) - - 0,21 (0,32) -0,23 (0,32) 62 0,24 (0,32) 68-0,21 (0,31) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,44 (0,37) [-0,28;1,16] 0,2320 0,45 (0,35) [-0,24;1,15] 0,1973 1) Baselie ist defiiert als Wert a Tag 0 vor Behadlug. 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Die zu erreichede Puktzahle für die eizele Domäe liege zwische: Geerelle Symptome (6 bis 35), Jucke (0 bis 15), Fatique (11 bis 66) Kogitive Fuktio (6 bis 30), Soziale Domäe (8 bis 50), Emotioale Domäe (3 bis 15). Höhere Puktzahle deute auf eie gerigere Lebesqualität hi. 4) Berechug der p-werte basiered auf der MMRM-Methode mit fixed effects für Behadlug, Zeit, Iteraktiosterm für Behadlugsgruppe ud Zeit ud ach zur Radomisierug verwedete Stratavariable sowie Baseliewert als Kovariate. Abkürzuge: DB: Doppelblid; ITT: Itetio-to-Treat; KI: Kofidezitervall; LS-MW: Least-squares-Mittelwert; LS-MWD: Leastsquares-Mittelwertdifferez; MMRM: gemischtes Modell für wiederholte Messuge; MW: Mittelwert; OCA: ;
59 Seite 59 PBC: primär biliäre Cholagitis; SD: Stadardabweichug, SE: Stadardfehler; VAS: visuelle Aalogskala; WADD: gewichtete durchschittliche Tagesdosis. LTSE-Phase I Tabelle 23 werde die Ergebisse für de PBC-40-Frageboge auf Basis der Safety-Populatio für die WADD-Gruppe 10 mg OCA dargestellt. Für Patiete, die währed der 12-moatige DB- Phase Placebo erhielte, umfasst OCA-Baselie die letzte Bewertug vor der erste OCA- Dosierug i der LTSE-Phase. Im Gegesatz dazu umfasst OCA-Baselie für Patiete, die währed der 12-moatige DB-Phase OCA erhielte, de Durchschitt aller Bewertuge vor der 12-moatige DB-Phase. I der LTSE-Phase zeigte sich zu Moat 12 im Vergleich zu Baselie eie sigifikate Verschlechterug für die Domäe Jucke (p<0,0001). Tabelle 23: Ergebisse zur Lebesqualität erhobe mit dem PBC-40-Frageboge ach 12 Moate i der LTSE-Phase POISE-Studie (Safety-Populatio) POISE-Studie LTSE-Phase WADD 10 mg OCA (N=172) OCA-Baselie 1) Moat 12 Geerelle Symptome 2) Zum jeweilige Erhebugszeitpukt (%) Veräderug zu OCA-Baselie (%) p-wert 3) Jucke 2) Zum jeweilige Erhebugszeitpukt (%) Veräderug zu OCA-Baselie (%) p-wert 3) Fatigue 2) Zum jeweilige Erhebugszeitpukt (%) Veräderug zu OCA-Baselie (%) p-wert 3) 172 (100) 13,1 (4,81) 13,0 (6;32) 171 (99,4) 3,8 (3,36) 3,0 (0; 15) 172 (100) 24,5 (10,35) 23 (11; 54) 133 (77,3) 24,6 (9,73) 24,0 (11; 51) 133 (77,3) 13,5 (4,80) 13,0 (6;32) 133 (77,3) 0,60 (3,50) 0,0 (-13;9) p=0, (77,7) 4,8 (3,42) 4,0 (0; 15) 133 (77,7) 1,1 (2,98) 0,0 (-4; 11) p < 0, (77,3) 0,1 (6,39) 0,0 (-21; 19) p=0,8634
60 Seite 60 POISE-Studie LTSE-Phase WADD 10 mg OCA (N=172) OCA-Baselie 1) Moat 12 Kogitive Fuktio 2) Zum jeweilige Erhebugszeitpukt (%) Veräderug zu OCA-Baselie (%) p-wert 3) Soziale Domäe 2) Zum jeweilige Erhebugszeitpukt (%) Veräderug zu OCA-Baselie (%) p-wert 3) Emotioale Domäe 2) Zum jeweilige Erhebugszeitpukt (%) Veräderug zu OCA-Baselie (%) p-wert 3) 172 (100) 11,6 (5,65) 10,0 (6; 30) 172 (100) 19,2 (8,05) 17,0 (8; 48) 172 (100) 6,6 (2,94) 6 (3; 14) 133 (77,3) 11,8 (5,45) 12,0 (6; 30) 133 (77,3) 0,2 (3,51) 0,0 (-10;12) p=0, (77,3) 19,6 (8,01) 18,0 (9; 45) 133 (77,3) 0.6 (6.01) 0,52 (-18;25) p=0, (77,3) 6,5 (3,13) 6 (3;15) 133 (77,3) -0.2 (2.13) -1,1 (-6;8) p=0,3199 1) Für Patiete, die währed der 12-moatioge DB-Phase Placebo erhielte, umfasst OCA-Baselie die letzte Bewertug vor der erste OCA-Dosierug. Im Gegesatz dazu umfasst OCA-Baselie für Patiete, die währed der 12-moatige DB-Phase OCA erhielte, de Durchschitt aller Evaluatioe vor der 12-moatige DB-Phase 2) Die zu erreichede Puktzahle für die eizele Domäe liege zwische: Geerelle Symptome (6 bis 35), Jucke (0 bis 15), Fatique (11 bis 66) Kogitive Fuktio (6 bis 30), Soziale Domäe (8 bis 50), Emotioale Domäe (3 bis 15). Höhere Puktzahle deute auf eie gerigere Lebesqualität hi. 3) Berechug der p-werte basiert auf dem gepaarte t-test. Abkürzuge: LTSE: Lagzeit-Sicherheitsstudie; MW: Mittelwert; OCA: ; PBC: primär biliäre Cholagitis; SD: Stadardabweichug; WADD: gewichtete durchschittliche Tagesdosis Sicherheit 12-moatige DB-Phase Zur Darstellug vo sicherheitsrelevate Edpukte wurde die Sicherheitspopulatio heragezoge, die alle Persoe mit midestes eier Awedug der Studiemedikatio (OCA-Titratio: N=70; Placebo: N=73) umfasst. Die mediae Behadlugsdauer i beide Studiearme (OCA- Titratio: 360 Tage; Placebo: 361 Tage) sowie die mediae Expositiosdauer (OCA-Titratio: 341,7 Tage; Placebo: 346 Tage) ware aäherd gleich.
61 Seite 61 Vo de 70 Patiete i der OCA-Titratiosgruppe beedete Patiete Moat 6. Vo de Patiete bliebe 36 Patiete bei der Dosierug vo 5 mg, währed 33 Patiete de primäre kombiierte Edpukt icht erreichte ud auf 10 mg hochtitriert wurde. Währed die mediae Behadlugsdauer für Patiete i der OCA-Titratiosgruppe, die ach 6 Moate weiterhi 5 mg OCA erhielte bei 356 Tage lag, lag die mediae Behadlugsdauer bei jee Patiete, die ach 6 Moate auf 10 mg hochtitriert wurde bei 361 Tage. Die mediae Expositiosdauer i der OCA- Titratiosgruppe, die bei 5 mg blieb, betrug 326,4 Tage, währed die mediae Expositiosdauer für Patiete, die auf 10 mg hochtitriert wurde 358,8 Tage betrug. I Tabelle 24 sid die Ergebisse zu UE währed der 12-moatige DB-Phase der POISE-Studie dargestellt. Isgesamt trate bei fast alle Studieteilehmer UE auf. Numerisch trate häufiger i der OCA-Titratiosgruppe (N=65) isgesamt 471 UE ud i der Placebogruppe (N=66) isgesamt 452 UE auf. UE, die zum Abbruch der Studiemedikatio führte sowie SUE trate häufiger im OCA- Titratiosarm als im Placeboarm auf. Kei Pruritus-Ereigis wurde als SUE gezählt. Tabelle 24: Ergebisse der uerwüschte Ereigisse i der der 12-moatige DB-Phase der POISE- Studie (Safety-Populatio) Patiete mit midestes eiem UE 2) UE-Pruritus 3) UE ach Schweregrad 4) mild moderat schwer UE-Pruritus ach Schweregrad mild moderat schwer OCA-Titratio (N=70) (%) 65 (93) 39 (56) 16 (23) 27 (39) 22 (31) 11 (16) 15 (21) 13 (19) Placebo 1) (N=73) (%) 66 (90) 28 (38) 29 (40) 28 (38) 9 (12) 16 (22) 7 (10) 5 (7) SUE 5) 11 (16) 3 (4) UE, das zum Abbruch der Studiemedikatio führte 6) aufgrud vo Pruritus 5 (7) 1 (1) UE, das zum Tod führte 7) 1 (1) 3) 0 1) Als Mootherapie oder i Kombiatio mit UDCA. 2) Ei UE ist defiiert als jegliches UE Ist defiiert als jedes UE, dass eu aufgetrete ist, sich i der Häufigkeit veräderte oder mit Studiebegi verschlechterte. 3) Uter UE-Pruritus werde folgede Preferred Terms zusammegefasst: Rash pruritic, Prurigo, Pruritus geeralised, Eye pruritus, Ear pruritus, Aal pruritus, ad Vulvovagial pruritus. 4) Patiete, die mehr als ei Ereigis berichte, werde ur eimal mit der höchste Schwere gezählt. 5) Es wurde kei SUE aufgrud vo Pruritus erfasst. 6) Kei Patiet i der OCA-Titratiosgruppe, der die Studiemedikatio aufgrud eies UE abbreche musste, wurde auf 10 mg hochtitriert. 7) Ursache für diese Todesfall war Herzversage aufgrud eier umfagreiche Krakevorgeschichte vo kardiovaskuläre Ereigisse, der ach Agabe des pu icht im direkte Zusammehag mit der Studiemedikatio steht. Abkürzuge: DB-Phase: Doppelblid-Phase; OCA: ; (S)UE: (schwerwiegede/s) uerwüschte/s Ereigis/se. Uerwüschte Ereigisse Uerwüschte Ereigisse mit eier Izidez vo 10 % oder höher sid für die beide Studiearme i Tabelle 25 dargestellt. Uterschiede vo 5%-Pukte oder mehr zwische de Studiearme fade sich i folgede Systemorgaklasse (SOC). Für die SOC Erkrakuge der Haut ud des Uterhautzellgewebes, Erkrakuge der Muskel, des Skeletts ud des Bidegewebes, 2 (3) 0
62 Seite 62 Erkrakuge des Nervesystems fiele die Uterschiede vo 5%-Pukte zwische de Arme zuuguste vo OCA aus. Für die SOC Ifektioe ud parasitäre Erkrakuge fiele die Uterschiede vo 5%-Pukte zuguste vo OCA aus. Tabelle 25: Uerwüschte Ereigisse mit Izidez 10 % i der 12-moatige DB-Phase der POISE- Studie (Safety-Populatio) MedDRA-Systemorgaklasse Preferred Term 1) OCA-Titratio (N=70) (%) Placebo 2) (N=73) (%) Erkrakuge der Haut ud des Uterhautzellgewebes Pruritus Ifektioe ud parasitäre Erkrakuge Nasopharygitis Ifektioe der obere Atemwege Harwegsifekt Erkrakuge des Gastroitestialtraktes Übelkeit Diarrhoe Blähuge Dyspepsie Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort Fatigue Erkrakuge der Muskel, des Skeletts ud des Bidegewebes Rückeschmerze Erkrakuge des Nervesystems Kopfschmerze Erkrakuge der Atemwege, des Brustraums ud Mediastiums 3) Verletzug, Vergiftug ud durch Eigriffe bedigte Komplikatioe 3) Psychische Erkrakuge Isomie 46 (66) 39 (56) 35 (50) 17 (24) 4 (6) 4(6) 33 (47) 4 (6) 2 (3) 3 (4) 4 (6) 20 (29) 11 (16) 21 (30) 4 (6) 21 (30) 12 (17) 35 (48) 28 (38) 44 (60) 13 (18) 8 (11) 8 (11) 33 (45) 9 (12) 8 (11) 7 (10) 8 (11) 18 (25) 10 (14) 17 (23) 8 (11) 18 (25) 13 (18) 14 (20) 15 (21) 11 (16) 10 (14) 10 (14) 7 (10) 12 (17) 2 (3) Augeerkrakuge 3) 5 (7) 10 (14) 1) Patiete wurde ur eimal i jeder Systemorgaklasse ud Preferred Term gezählt. 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Kei Preferred Term wurde mit 10 % der Patiete beobachtet. Abkürzuge: DB-Phase: Doppelblid-Phase; MedDRA: Medical Dictioary for Regulatory Activities; OCA:. Uerwüschte Ereigisse ach Schweregrad Isgesamt trate i der OCA-Titratiosgruppe bei 65 vo 70 Patiete (93 %) ud i der Placebogruppe bei 66 vo 73 Patiete (90 %) midestes ei UE auf. Uerwüschte Ereigisse ach Schweregrad mit eier Izidez vo 10 % oder höher sid i Tabelle 26 dargestellt. Für Patiete i der OCA-Titratiosgruppe (N=70), bei dee midestes ei UE aufgetrete ist, ware diese bei 16 Patiete (23 %) mild, bei 27 Patiete (39 %) moderat ud bei 22 Patiete (31 %) schwer. I der Placebogruppe ware dies bei 29 Patiete (40 %) mild, bei 28 Patiete (38 %) moderat ud bei 9 Patiete (12 %) schwer.
63 Seite 63 Tabelle 26: Uerwüschte Ereigisse ach Schweregrad mit Izidez 10 % i der 12-moatige DB- Phase der POISE-Studie (Safety-Populatio) MedDRA-Systemorgaklasse Preferred Term 1) mild (=16) OCA-Titratio (N=70) moderat (=27) schwer (=22) mild (=29) Placebo 2) (N=73) moderat (=28) schwer (=9) Erkrakuge der Haut ud des Uterhautzellgewebes Pruritus Ifektioe ud parasitäre Erkrakuge Nasopharygitis Ifektioe der obere Atemwege Erkrakuge des Gastroitestialtraktes 4) Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort 4) Erkrakuge der Muskel, des Skeletts ud des Bidegewebes Rückeschmerze Erkrakuge des Nervesystems Kopfschmerze Erkrakuge der Atemwege, des Brustraums ud Mediastiums 4) 16 (23) 11 (16) 22 (31) 15 (21) 4 (6) 17 (24) 15 (21) 11 (16) 2 (3) 0 13 (19) 13 (19) 2 (3) (29) 16 (22) 33 (45) 3) 12 (16) 7 (10) 8 (11) 7 (10) 11 (15) 1 (1) 1 (1) 6 (8) 5 (7) 21 (30) 7 (10) 5 (7) 16 (22) 16 (22) 1 (1) 13 (19) 6 (9) 1 (1) 10 (14) 5 (7) 3 (4) 14 (20) 4 (6) 10 (14) 5 (7) 5 (7) 0 10 (14) 7 (10) 2 (3) 0 1 (1) 0 11 (15) 7 (10) 13 (18) 11 (15) 5 (7) 1 (1) 4 (5) 2 (3) (1) 0 1 (1) 0 6 (9) 8 (11) 0 11 (15) 3 (4) 1 (1) Psychische Erkrakuge 4) 9 (13) 3 (4) 0 7 (10) 3 (4) 0 1) Patiete wurde ur eimal i jeder Systemorgaklasse ud Preferred Term gezählt. 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Diskrepaz i de berichtete Studieuterlage. Mehr Patiete wiese ei UE i der SOC Ifektioe ud parasitäre Erkrakuge (N=33) auf, als Patiete ei UE als mild eigestuft habe (N=29). 4) Kei Preferred Term wurde mit 10 % der Patiete beobachtet. Abkürzuge: DB: Doppelblid; MedDRA: Medical Dictioary for Regulatory Activities; OCA: ; Schwerwiegede uerwüschte Ereigisse Schwerwiegede uerwüschte Ereigisse sid i Tabelle 27 dargestellt. Isgesamt trate i der OCA-Titratiosgruppe bei 11 vo 70 Patiete (16 %) ud i der Placebogruppe bei 3 vo 73 Patiete (4 %) midestes ei SUE auf. Für die SOC Erkrakuge des Gastroitestialtraktes, Erkrakuge des Nervesystems, Gefäßerkrakuge ud Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort fiele die Uterschiede vo 3%-Pukte zwische de Arme zuuguste vo OCA aus. Tabelle 27: Schwerwiegede uerwüschte Ereigisse mit Izidez 2 % i der 12-moatige DB- Phase der POISE-Studie (Safety-Populatio) MedDRA-Systemorgaklasse 1) OCA-Titratio (N=70) Placebo 2) (N=73) Erkrakuge des Gastroitestialtraktes 3) 4 (6) 1 (1) Erkrakuge des Nervesystems 3) 2 (3) 0 Gefäßerkrakuge 3) 2 (3) 0
64 Seite 64 Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort 3) 1 (1) 2 (3) 1) Patiete wurde ur eimal i jeder Systemorgaklasse gezählt. 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Kei Preferred Term wurde mit 2 % der Patiete beobachtet. Abkürzuge: DB-Phase: Doppelblid-Phase; MedDRA: Medical Dictioary for Regulatory Activities; OCA:. Vom pu beschriebee uerwüschte Ereigisse vo besoderem Iteresse Pruritus ist als UE vo besoderem Iteresse im SAP präspezifiziert. Nebe de bereits obe aufgeführte Sicherheitsedpukte, ist i Tabelle 28 die Zeit bis zum erste Eitrete eies Pruritus- Ereigisses dargestellt differeziert ach UE-Pruritus gesamt ud schwerer Pruritus. Die mediae Zeit bis zum erste Pruritus war währed der Gesamtdauer der Studie i der OCA-Gruppe kürzer als i der Placebogruppe auf (p=0,0349). Die Mediae Zeit des erstmalige Auftretes vo Pruritus (50 % der Patiete berichtete ei Ereigis) lag bei 188 Tage, der Media für die Placebogruppe wurde icht erreicht. Tabelle 28: Zeit bis zum erste Eitrete vo Pruritus i der POISE-Studie, Moate 0 bis 12 (Safety- Populatio) POISE-Studie 12-moatige DB-Phase Pruritus 2) OCA-Titratio (N=70) Placebo 1) (N=73) Patiete mit Ereigis, (%) 39 (56) 28 (38) Kapla-Meier-Schätzer, i Tage Media [95%-KI] 188 [56;NA] NA [344;NA] p-wert 3) 0,0349 Schwerer Pruritus 2) Patiete mit Ereigis, (%) 13 (19) 5 (7) Kapla-Meier-Schätzer, i Tage Media [95%-KI] NA [NA;NA] NA [NA;NA] p-wert 3) 0,0338 1) Als Mootherapie oder i Kombiatio mit UDCA. 2) Die Darstellug beruht auf eier Auswertug, i die die Azahl der Patiete mit Pruritus aus jedem Studiearm eigig. 3) Basiert auf dem stratifizierte Log-Rak-Test mit de Faktore Behadlug ud Radomisierug. Abkürzuge: DB: Doppelblid; KI: Kofidezitervall; NA: icht erreicht; OCA:. Nebe Pruritus wurde kardiovaskuläre Ereigisse, leberbedigte Ereigisse ud lipidbedigte Ereigisse im Studiebericht als UE vo besoderem Iteresse beat. Kardiovaskuläre Ereigisse Es wurde die SOC Herzerkrakuge sowie embolische ud thrombotische Ereigisse oder ischämische Ereigisse berücksichtigt. 5 Patiete im Placeboarm (7 %) ud 6 Patiete im Tritratiosarm (9 %) erlitte midestes ei kardiovaskuläres UE währed der Gesamtstudiezeit. Hepatische Ereigisse Um UE der Leber zu idetifiziere, eischließlich UE, die auf Cholestase, Verletzug der Leber oder eier Leberdekompesatio hiweise, wurde MedDRA-SOC ud Preferred Terms ach Leber- Galle-Erkrakuge, Gastroitestiale Störuge, Utersuchuge, Erkrakuge des Nerve-
65 Seite 65 systems ud Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort überprüft. Mit eier Fuktiosstörug der Leber verbudee UE trate bei 3 Patiete im Placeboarm (4 %) ud bei 5 Patiete i der Titratiosgruppe (7 %) währed der DB-Phase auf. Lipid-bezogee Ereigisse Die SOC Stoffwechsel- ud Erährugsstöruge sowie Utersuchuge wurde dafür berücksichtigt. Bei 2 Patiete im Placeboarm (3 %) ud 1 Patiete im Titratiosarm (1 %) kam es zu midestes eiem lipid-bezogeem UE währed der DB-Phase. LTSE-Phase I Tabelle 29 sid die Ergebisse zu UE i der LTSE-Phase (Dateschitt: 31. August 2014) für die Patietegruppe WADD 10 mg OCA dargestellt. Isgesamt trate bei fast alle Studieteilehmer UE auf (bei 150 vo 172 Patiete [87 %]). Tabelle 29: Ergebisse der uerwüschte Ereigisse i der LTSE-Phase der POISE-Studie (Safety- Populatio) Patiete mit midestes eiem WADD 10 mg OCA (N=172) (%) UE 1) UE-Pruritus UE ach Schweregrad 1) mild moderat schwer UE-Pruritus ach Schweregrad 1) mild moderat schwer 150 (87) 71 (41) 50 (29) 60 (35) 40 (23) 18 (10) 30 (17) 23 (13) SUE 13 (8) UE, das zum Abbruch der Studiemedikatio führte aufgrud vo Pruritus UE, das zum Tod führte 1 (0,6) 9 (5) 5 (3) 1) Defiiert als jedes UE, dass eu aufgetrete ist, sich i der Häufigkeit veräderte oder mit Studiebegi der LTSE-Phase verschlechterte. Abkürzuge: LTSE: Lagzeit-Sicherheitsstudie; OCA: ; (S)UE: (schwerwiegede/s) uerwüschte/s Ereigis/se; WADD: gewichtete durchschittliche Tagesdosis. Uerwüschte Ereigisse Uerwüschte Ereigisse mit eier Izidez vo 10 % oder höher sid für die Patietepopulatio WADD < 10 mg OCA i Tabelle 30 dargestellt. Tabelle 30: Azahl uerwüschter Ereigisse mit Izidez 10 % i der LTSE-Phase der POISE-Studie MedDRA-Systemorgaklasse Preferred Term 1) Erkrakuge der Haut ud des Uterhautzellgewebes Pruritus WADD <10 mg OCA (N=172) (%) 80 (47) 71 (41)
66 Seite 66 MedDRA-Systemorgaklasse Preferred Term 1) Ifektioe ud parasitäre Erkrakuge Nasopharygitis Harwegsifekt WADD <10 mg OCA (N=172) (%) 61 (35) 13 (8) 14 (8) Erkrakuge des Gastroitestialtraktes 2) 58 (34) Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort Fatigue 41 (24) 17 (10) Erkrakuge der Muskel, des Skeletts ud des Bidegewebes 2) 44 (26) Erkrakuge des Nervesystems 30 (17) Erkrakuge der Atemwege, des Brustraums ud Mediastiums 2) 24 (14) Verletzug, Vergiftug ud durch Eigriffe bedigte Komplikatioe 2) 28 (16) Utersuchuge 2) 22 (13) 1) Patiete wurde ur eimal i jeder Systemorgaklasse ud Preferred Term gezählt. 2) Kei Preferred Term wurde mit 10 % der Patiete beobachtet. Abkürzuge: LTSE: Lagzeit-Sicherheitsstudie; MedDRA: Medical Dictioary for Regulatory Activities; OCA: ; WADD: gewichtete durchschittliche Tagesdosis. Uerwüschte Ereigisse ach Schweregrad Uerwüschte Ereigisse ach Schweregrad vo 2 % oder höher sid für die Patietepopulatio WADD < 10 mg OCA i Tabelle 31 dargestellt. Tabelle 31: Uerwüschte Ereigisse ach Schweregrad mit Izidez 2 % i der LTSE-Phase der POISE-Studie (Safety-Populatio) MedDRA-Systemorgaklasse Preferred Term 1) mild (=50) WADD < 10 mg OCA 2) (N=172) (%) moderat (=60) schwer (=40) Erkrakuge der Haut ud des Uterhautzellgewebes Pruritus 21 (12) 18 (10) 34 (20) 30 (17) 25 (15) 23 (13) Ifektioe ud parasitäre Erkrakuge Nasopharygitis 42 (24) 13 (8) 17 (10) 0 2 (1) 0 Erkrakuge des Gastroitestialtraktes 3) 32 (19) 20 (12) 6 (3) Erkrakuge der Muskel, des Skeletts ud des Bidegewebes 3) Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort 3) 25 (15) 17 (10) 2 (1) 30 (17) 10 (6) 1 (< 1) Erkrakuge des Nervesystems 3) 24 (14) 6 (3) 0 Verletzuge, Vergiftuge ud eigriffsbedigte Erkrakuge 3) Erkrakuge der Atemwege, des Brustraums ud Mediastiums 3) 17 (10) 11 (6) 0 17 (10) 6 (3) 1 (< 1) Utersuchuge 3) 18 (10) 3 (2) 1 (< 1) 1) Patiete wurde ur eimal i jeder Systemorgaklasse ud Preferred Term gezählt.
67 Seite 67 2) Patiete, die mehr als ei UE berichte, werde ur eimal mit dem höchste Schweregrad pro WADD-Gruppe gezählt. 3) Kei Preferred Term wurde mit 10 % der Patiete beobachtet. Abkürzuge: LTSE: Lagzeit-Sicherheitsstudie; MedDRA: Medical Dictioary for Regulatory Activities; OCA: ; WADD: gewichtete durchschittliche Tagesdosis. Schwerwiegede uerwüschte Ereigisse Schwerwiegede uerwüschte Ereigisse mit eier Izidez vo 2 % oder höher sid für die Patietepopulatio WADD < 10 mg OCA i Tabelle 32 dargestellt. Tabelle 32: Schwerwiegede uerwüschte Ereigisse mit Izidez 2 % i der LTSE-Phase der POISE-Studie (Safety-Populatio) MedDRA-Systemorgaklasse 1) WADD <10 mg OCA (N=172) (%) Erkrakuge des Gastroitestialtraktes 2) 5 (3) Ifektioe ud parasitäre Erkrakuge 2) 3 (2) Erkrakuge der Muskel, des Skeletts ud des Bidegewebes 2) 4 (2) 1) Patiete wurde ur eimal i jeder Systemorgaklasse ud Preferred Term gezählt. 2) Kei Preferred Term wurde mit 2 % der Patiete beobachtet. Abkürzuge: LTSE: Lagzeit-Sicherheitsstudie; MedDRA: Medical Dictioary for Regulatory Activities; OCA: ; WADD: gewichtete durchschittliche Tagesdosis. Vom pu beschriebee uerwüschte Ereigisse vo besoderem Iteresse Uerwüschte Ereigisse vo besoderem Iteresse sid für die Patietepopulatio WADD < 10 mg OCA i Tabelle 32 dargestellt. Tabelle 33: Uerwüschte Ereigisse vo besoderem Iteresse i der LTSE-Phase der POISE-Studie (Safety-Populatio) WADD vo 10 mg OCA UE vo besoderem Iteresse 1) Patiete (N=172) (%) Ereigisse gesamt (N=726) Herzerkrakuge 2) 12 (7) 18 Dyslipidaemie 3) 5 (3) 6 Lebererkrakuge 4) 12 (7) 19 Pruritus 5) 111 (65) 6) 285 1) Patiete mit mehr als eiem UE vo besoderem Iteresse wurde je Behadlugsarm ur eimal gezählt. 2) Herzerkrakuge sid defiiert als jedes Ereigis ach MedDRA-SOC Herzerkrakuge oder MedDRA-SMQ Embolie ud thrombotische Ereigisse oder Ischämische Herzerkrakuge. 3) Dyslipidaemie sid defiiert als ausgewählte Ereigisse ach MedDRA-SMQ Dyslipidämie. 4) Leberfuktiosstöruge beihalte hepatische Störuge ach MedDRA-SMQ, ausgeomme der SMQ: ageboree, familiäre, eoatale oder geetische Erkrakuge der Leber, icht-ifektiöse Hepatitis, Leberifektioe ud schwagerschaftsbedigte Leberfuktiosstöruge. 5) Pruritis ist ei Ereigis ach Preferred Term, eischließlich Prur. Patiete, die mehr als ei UE berichte, werde ur eimal mit dem höchste Schweregrad pro WADD-Gruppe gezählt. 6) Diskrepaz i de Studieuterlage. I Tabelle 29 wird vo 71 Patiete berichtet, die midestes ei UE-Pruritus hatte. Es bleibt uklar, weshalb hier vo 111 Patiete berichtet wird. Abkürzuge: LTSE: Lagzeit-Sicherheitsstudie; MedDRA: Medical Dictioary for Regulatory Activities; OCA: ; SOC: Systemorgaklasse/; SMQ: Stadardisierte MedDRA-Abfrage; UE: uerwüschte/s Ereigis/se; WADD: gewichtete durchschittliche Tagesdosis.
68 Seite Subgruppeaalyse für Kombiatiostherapie (OCA+UDCA vs. UDCA+Placebo) Der pu hat i Modul 4 des Herstellerdossiers die Ergebisse für die 12-moatige DB-Phase differeziert ach Therapieschema (Moo- vs. Kombiatiostherapie) für die OCA-Titratiosgruppe dargestellt. Da es sich hierbei um eie Post-hoc-Auswertug hadelt ud die Ergebisse icht im Studiebericht berichtet werde, werde achfolged die Ergebisse als Subgruppeaalyse präsetiert. So wurde die Kombiatiostherapie vo OCA+UDCA gegeüber UDCA+Placebo (65 vs. 68 Patiete) ud die Mootherapie OCA gegeüber Placebo (5 vs. 5 Patiete) vergliche. Aufgrud der gerige Patietefallzahl i der Mootherapie (N=10) werde die Ergebisse dieser Subgruppe aufgrud der Aussageusicherheite icht berichtet. I Tabelle 34 sid Demographie ud Baselie-Charakteristika für die Patiete mit Kombiatiostherapie aus dem OCA-Titratiosarm dargestellt. I dem Behadlugsarm war die Mehrzahl der Patiete weiblich (OCA+UDCA: 92 %; UDCA+Placebo: 93 %) ud uter 65 Jahre alt (OCA+UDCA: 89 %; UDCA+Placebo: 82 %). Alle Patiete erhielte zu Baselie eie UDCA-Behadlug. I Bezug auf die PBC-Charakteristik ware beide Behadlugsarme vergleichbar. I beide Behadlugsarme lag das mediae Alter zum Zeitpukt der PBC-Diagose bei 47 Jahre. Die mediae Dauer der PBC i Jahre lag i der OCA+UDCA-Titratiosgruppe bei 7,3 Jahre ud i der UDCA+Placebo-Gruppe bei 7,4 Jahre. Tabelle 34: Charakterisierug der Studiepopulatio i der 12-moatige DB-Phase der POISE-Studie zu Baselie differeziert ach Kombiatios- ud Mootherapie (ITT-Populatio) POISE-Studie 12-moatige DB-Phase Geschlecht, (%) mälich weiblich Alter, i Jahre Altersklasse, (%) < 65 Jahre 65 Jahre Alter bei PBC-Diagose, i Jahre Altersklasse bei PBC-Diagose, (%) < 50 Jahre 50 Jahre Dauer der PBC, i Jahre Dauer der PBC-Klasse, (%) 7,5 Jahre > 7,5 Jahre OCA+UDCA 1) (N=65) Kombiatiostherapie 5 (8) 60 (92) 55,2 (9,42) 54 (29;81) 58 (89) 7 (11) 46,7 (10,47) 47 (25;77) 37 (57) 28 (43) 8,6 (5,76) 7,3 (0,8;27) 33 (51) 32 (49) UDCA+Placebo (N=68) 5 (7) 63 (93) 55,2 (10,28) 55,5 (34;79) 56 (82) 12 (18) 47,1 (9,57) 47 (31;74) 43 (63) 25 (37) 8,3 (5,35) 7,4 (0,9;21,8) 37 (54) 31 (46)
69 Seite POISE-Studie 12-moatige DB-Phase OCA+UDCA 1) (N=65) Kombiatiostherapie UDCA+Placebo (N=68) Ethie (geetisch), (%) kaukasisch/weiß icht-kaukasisch Regio, (%) EMEA Nordamerika Australie UDCA-Behadlug zu Baselie, (%) ja ei Leberbiopsie vor Studiebegi, (%) ja ei Pruritus i der Aamese, (%) ja ei Itesität des letzte Pruritus-Ereigisses mit Pruritus i der Aamese, (%) mild moderat schwer ubekat Pruritus zu Baselie, (%) ja ei Fatigue i der Aamese, (%) ja ei Gesamt-Itesität der PBC-bedigte Fatigue, (%) mild moderat schwer ALP zu Baselie (U/l) 2) Totales Bilirubi zu Baselie (μmol/l) 2) Albumi zu Baselie (g/l) 1) Behadlugsarm "OCA-Titratio". 2) Gerudet auf erste Nachkommastelle. 63 (97) 2 (3) 42 (65) 18 (28) 5 (8) 65 (100) 0 11 (17) 54 (83) 42 (65) 23 (35) 28 (67) 11 (26) 2 (5) 1 (2) 35 (54) 30 (46) 33 (51) 32 (49) 14 (22) 14 (22) 5 (8) 313,6 (94,8) 279,5 (186,8;566,3) 10,3 (5,7) 8,6 (2,1;36,4) 43,2 (2,9) 43 (34,0;50,5) 61 (90) 7 (10) 44 (65) 21 (31) 3 (4) 68 (100) 0 7 (10) 61 (90) 45 (66) 23 (34) 29 (64) 14 (31) 1 (2) 1 (2) 45 (66) 23 (34) 45 (66) 23 (34) 26 (38) 14 (21) 3 (4) 324,6 (114,7) 310,2 (143,8;745,9) 11,7 (7,4) 8,9 (2,3;37,4) 42,7 (3,2) 43 (32,5;48,0) Abkürzuge: ALP: Alkalische Phosphatase/; DB: Doppelblid; EMEA: Europa, Naher Oste ud Afrika; ITT: Itetio-to-Treat; MW: Mittelwert; OCA: ; PBC: primär biliäre Cholagitis; SD: Stadardabweichug; UDCA: Ursodesoxycholsäure.
70 Seite Mortalität I der Kombiatiostherapie trat währed der 12-moatige DB-Phase i der Behadlugsgruppe OCA+UDCA ei ud i der Behadlugsgruppe UDCA+Placebo kei Todesfall auf. Wie i Abschitt beschriebe: Ursache für diese Todesfall war Herzversage aufgrud eier umfagreiche Krakevorgeschichte vo kardiovaskuläre Ereigisse, der ach Agabe des pu icht im direkte Zusammehag mit der Studiemedikatio steht. Zwische de Behadlugsgruppe zeigte sich kei sigifikater Uterschied (ach CMH-Test: p=0,3063) Morbidität Pruritus I der Subgruppeaalyse für die Kombiatiostherapie (OCA+UDCA vs. UDCA+Placebo) zeigte sich ausschließlich für de Gesamtscore, die Eizeldomäe Richtug ud für die VAS sigifikate Uterschiede zwische de Behadlugsgruppe zuuguste vo OCA+UDCA. Allerdigs überlappe die 95%-Kofidezitervalle (-KI) der stadardisierte Mittelwertdifferez (SMD) die Relevazschwelle vo 0,2 die i Abweseheit eier Miimal Importat Differece (MID) für Gruppeuterschiede gewählt wurde i alle Domäe ud der VAS, sodass sich keie kliisch relevate Uterschiede zwische de Behadlugsgruppe zeige. Tabelle 35: Ergebisse zum 5-D-Pruritus-Frageboge ud der Pruritus-VAS i der 12-moatige DB- Phase der POISE-Studie i der Kombiatiostherapie (ITT-Populatio) POISE-Studie 12-moatige DB-Phase OCA+UDCA (N=65) UDCA+Placebo (N=68) LS-MWD [95%-KI] SMD [95%-KI] p-wert 5-D-Frageboge 1) Gesamtscore Azahl (%) 57 (87,7) 60 (88,2) Baselie Veräderug zu Baselie LS-MW (SE) 5-D-Frageboge 1) Dauer 10,2 (3,6) 11 (5,1) 1,24 (0,29) 0,51 (0,29) Azahl (%) 59 (90,8) 64 (94,1) Baselie Veräderug zu Baselie LS-MW (SE) 5-D-Frageboge 1) Schweregrad 1,2 (0,6) 1,4 (1) 0,29 (0,07) 0,2 (0,06) Azahl Baselie Veräderug zu Baselie LS-MW (SE) 5-D-Frageboge 1) Richtug 1,9 (1) 2 (1) 0,2 (0,05) 0,1 (0,05) 0,73 [0,12;1,33] 0,44 [0,07;0,8] 0,0182 0,09 [-0,07;0,25] 0,19 [-0,16;0,54] 0,2908 0,1 [-0,03;0,22] 0,26 [-0,09;0,61] 0,13 Azahl ,3 [0,1;0,5]
71 Seite 71 POISE-Studie 12-moatige DB-Phase OCA+UDCA (N=65) UDCA+Placebo (N=68) LS-MWD [95%-KI] SMD [95%-KI] p-wert Baselie Veräderug zu Baselie LS-MW (SE) 5-D-Frageboge 1) Behiderug 3,1 (1,2) 3,1 (1,5) 0,24 (0,15) -0,06 (0,15) 0,53 [0,17;0,9] 0,0037 Azahl Baselie Veräderug zu Baselie LS-MW (SE) 5-D-Frageboge 1) Verteilug 1,8 (1,1) 1,9 (1,4) 0,2 (0,06) 0,08 (0,06) 0,13 [-0,05;0,3] 0,25 [-0,1;0,61] 0,1523 Azahl Baselie Veräderug zu Baselie LS-MW (SE) Pruritus-VAS 2) 2 (1,2) 2,3 (1,5) 0,31 (0,06) 0,26 (0,06) 0,05 [-0,11;0,21] 0,11 [-0,24;0,46] 0,5256 Azahl Baselie Veräderug zu Baselie LS-MW (SE) 21,3 (25,5) 25,7 (27,1) 4,16 (1,41) 0,18 (1,36) 3,98 [0,75;7,21] 0,43 [0,07;0,78] 0,0159 1) Die zu erreichede Gesamtpuktzahl liegt zwische 5 ud 25 Pukte. Jede Domäe ka eie Puktwert vo 1 bis 5 Pukte erreiche. Höhere Pukte deute auf eie stärkere Pruritus hi. 2) Scores reiche vo 0 (kei Pruritus) bis 100 (schwerer Pruritus). Abkürzuge: DB: Doppelblid; ITT: Itetio-to-Treat; MW: Mittelwert; KI: Kofidezitervall; LS-MW: Least-squares-Mittelwert; LS-MWD: Least-squares-Mittelwertdifferez; OCA: ; SD: Stadardabweichug, SE: Stadardfehler; SMD: stadardisierte Mittelwertdifferez; UDCA: Ursodesoxycholsäure; VAS: visuelle Aalogskala. Ateil Patiete mit ALP < 1,67 x ULN, Gesamt-Bilirubi ULN ud ALP-Reduktio 15 % I der folgede Tabelle werde die Ergebisse des primäre kombiierte Edpuktes ud desse Eizelkompoete der POISE-Studie für Moat 6 ud 12 dargestellt. Es zeigte sich ei statistisch sigifikater Vorteil bezüglich des primäre kombiierte Edpuktes für OCA+UDCA gegeüber UDCA+Placebo. Tabelle 36: Ergebisse zum primäre kombiierte Edpukt ud de Eizelkompoete ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie i der Kombiatiostherapie (ITT-Populatio) POISE-Studie 12-moatige DB-Phase OCA+UDCA (N=65) Moat 6 Moat 12 UDCA+Placebo (N=68) OCA+UDCA (N=65) UDCA+Placebo (N=68) Ateil Patiete mit ALP < 1,67 x ULN, Gesamt-Bilirubi ULN ud ALP-Reduktio 15 % Ereigisse, (%) 22 (33,85) 5 (7,35) 30 (46,15) 7 (10,29)
72 Seite 72 POISE-Studie 12-moatige DB-Phase OCA+UDCA (N=65) Moat 6 Moat 12 UDCA+Placebo (N=68) OCA+UDCA (N=65) UDCA+Placebo (N=68) RR [95%-KI] 4,64 [1,89;11,38] 4,45 [2,12;9,34] p-wert 1) 0,0001 <0,0001 ALP < 1,67 x ULN Ereigisse, (%) 23 (35,38) 8 (11,76) 31 (47,) 12 (17,65) RR [95%-KI] 3,07 [1,5;6,27] 2, [1,53;4,71] p-wert 1) 0,0011 0,0002 Bilirubi ULN Ereigisse, (%) 61 (93,85) 55 (80,88) 57 (87,) 54 (79,41) RR [95%-KI] 1,09 [0,96;1,24] 1,08 [0,96;1,22] p-wert 1) 0,0219 0,1782 ALP-Reduktio 15 % Ereigisse, (%) 47 (72,31) 18 (26,47) 50 (76,92) 21 (30,88) RR [95%-KI] 2,7 [1,77;4,14] 2,48 [1,7;3,63] p-wert 1) <0,0001 <0,0001 1) Berechug der p-werte basiered auf dem Cochra-Matel-Haeszel-Test. Abkürzuge: ALP: Alkalische Phosphatase/; DB: Doppelblid; ITT: Itetio-to-Treat; KI: Kofidezitervall; OCA: ; RR: Relatives Risiko; UDCA: Ursodesoxycholsäure; ULN: obere Normgreze Lebesqualität Die Subgruppeaalyse für die Kombiatiostherapie (OCA+UDCA vs. UDCA+Placebo) zeigte für die Domäe Geerelle Symptome, Jucke, Fatique ud Kogitive Fuktioe keie sigifikate Uterschiede zwische de Behadlugsgruppe. Im Gegesatz dazu kote i der soziale ud emotioale Domäe ei sigifikater Uterschied zwische de Behadlugsgruppe zuguste vo OCA+UDCA gezeigt werde. Allerdigs überlappe die SMD der 95%-KI die Relevazschwelle vo 0,2 i alle Domäe ud der VAS, sodass sich keie kliisch relevate Uterschiede zwische de Behadlugsgruppe zeige. Tabelle 37: Ergebisse zum PBC-40-Frageboge ach 12 Moate i der 12-moatige DB-Phase der POISE-Studie (ITT-Populatio) POISE-Studie 12-moatige DB-Phase OCA+UDCA (N=65) UDCA+Placebo (N=68) LS-MWD [95%-KI] SMD [95%-KI] p-wert Geerelle Symptome 1) Azahl Baselie Veräderug zu Baselie LS-MW (SE) 13,6 (5,2) 13,6 (5,3) -0,61 (0,17) -0,3 (0,16) -0,31 [-0,76;0,13] -0,24 [-0,58;0,11] 0,19
73 Seite 73 POISE-Studie 12-moatige DB-Phase OCA+UDCA (N=65) UDCA+Placebo (N=68) LS-MWD [95%-KI] SMD [95%-KI] p-wert Jucke 1) Azahl Baselie Veräderug zu Baselie LS-MW (SE) Fatigue 1) 4 (3,4) 4,3 (3,8) 0,55 (0,15) 0,27 (0,14) 0,29 [-0,11;0,68] 0,25 [-0,1;0,59] 0,1549 Azahl Baselie Veräderug zu Baselie LS-MW (SE) Kogitive Fuktio 1) 11,1 (5,4) 11,5 (5,9) 0,16 (0,18) -0,08 (0,17) 0,24 [-0,24;0,72] 0,17 [-0,17;0,52] 0,3226 Azahl Baselie Veräderug zu Baselie LS-MW (SE) Soziale Domäe 1) 11,1 (5,4) 11,5 (5,9) 0,16 (0,18) -0,08 (0,17) 0,24 [-0,24;0,72] 0,17 [-0,17;0,52] 0,3226 Azahl Baselie Veräderug zu Baselie LS-MW (SE) Emotioale Domäe 1) 19,1 (8,4) 21 (8,8) 0,02 (0,31) -0,94 (0,3) 0,96 [0,13;1,79] 0,40 [0,05;0,74] 0,0233 Azahl Baselie Veräderug zu Baselie LS-MW (SE) 6,3 (2,7) 7 (3,3) -0,12 (0,11) -0,46 (0,11) 0,34 [0,05;0,63] 0,40 [0,05;0,74] 0,0233 1) Die zu erreichede Puktzahle für die eizele Domäe liege zwische: Geerelle Symptome (6 bis 35), Jucke (0 bis 15), Fatique (11 bis 66) Kogitive Fuktio (6 bis 30), soziale Domäe (8 bis 50), emotioale Domäe (3 bis 15). Höhere Puktzahle deute auf eie gerigere Lebesqualität hi. Abkürzuge: DB: Doppelblid; ITT: Itetio-to-Treat; MW: Mittelwert; KI: Kofidezitervall; LS-MW: Least-squares-Mittelwert; LS-MWD: Least-squares-Mittelwertdifferez; OCA: ; PBC: primär biliäre Cholagitis; SD: Stadardabweichug, SE: Stadardfehler; SMD: stadardisierte Mittelwertdifferez; UDCA: Ursodesoxycholsäure. LTSE-Phase Der pu zieht i Modul 4 des Herstellerdossiers allei diejeige Patiete als bewertugsrelevat hera, die währed der verblidete RCT-Phase im Titratiosarm behadelt worde ware. Mit Eitritt i die LTSE-Phase begae alle Patiete aus der Titratiosphase mit 5 mg OCA täglich. Der pu stellt i Modul 4 (S. 152 ff) dar, dass diese Auswahl der Patiete der deutsche Zulassug (Fachiformatio) vo etspricht. Dies ist ihaltlich icht achzuvollziehe, weil aus
74 Seite 74 Sicht der LTSE-Phase die verblidete Phase lediglich die Vortherapie darstellt ud durchaus auch Patiete aus dem Placebo+UDCA-Arm i die bewertugsrelevate Auswertug der LTSE-Phase hätte eigeschlosse werde köe: Die Abtritirierug vo 10 auf 5 mg täglich ist laut Zulassug ebesoweig ausgeschlosse wie die Vorbehadlug mit UDCA (Mootherapie) oder UDCA+Placebo (Kombiatiostherapie). Vor diesem Hitergrud werde keie zusätzliche Ergebisse aus Modul 4 i der vorliegede Nutzebewertug berichtet Sicherheitsedpukte I Tabelle 38 sid die Ergebisse UE i der 12-moatige DB-Phase für die Kombiatiostherapie der POISE-Studie dargestellt. Isgesamt trate bei fast alle Studieteilehmer UE auf (OCA+UDCA: 92,2 %; UDCA+Placebo: 89,7 %). SUE, schwere UE (ohe UE-Pruritus) ud UE, die zum Abbruch der Studiemedikatio führte trate umerisch häufiger im OCA+UDCA-Arm als im UDCA+Placebo-Arm auf. Für die Patiete mit Kombiatiostherapie zeigte sich i de Kategorie kei sigifikater Uterschied zwische de Behadlugsgruppe. Als ergäzede Aalyse wurde i der folgede Tabelle die schwere UE mit dem UE-Pruritus dargestellt. Hier fad sich ei sigifikater Nachteil für OCA+UDCA gegeüber UDCA+Placebo (RR: 2,21 [95%-KI: 1,08;4,52], p=0,0247). Tabelle 38: Ergebisse der uerwüschte Ereigisse i der 12-moatige DB-Phase für die Kombiatiostherapie der POISE-Studie (Safety-Populatio) Patiete mit midestes eiem OCA+UDCA (N=65) (% 1) ) UDCA+Placebo (N=68) (% 1) ) RR [95%-KI] p-wert 2) UE 60 (92,3) 61 (89,7) SUE 8 (12,3) 3 (4,4) schwere UE ohe UE-Pruritus 9 (13,9) 6 (8,8) schwere UE mit UE-Pruritus 16 (29,2) 9 (13,2) 1,03 [0,92;1,14] 3) 0,6027 2,79 [0,78;10,07] 0,1006 1,58 [0,6;4,17] 0,3627 2,21 [1,08;4,52] 0,0247 UE, das zum Abbruch der Studiemedikatio führte 5 (7,7) 1 (1,5) 5,29 [0,64;43,92] 0,0858 1) Gerudet auf erste Nachkommastelle. 2) Berechug der p-werte basiered auf dem Cochra-Matel-Haeszel-Test. 3) Modell ohe Stratifikatios-Faktore. Abkürzuge: DB: Doppelblid; KI: Kofidezitervall; OCA: ; RR: Relatives Risiko; (S)UE: (schwerwiegede/s) uerwüschte/s Ereigis/se; UDCA: Ursodesoxycholsäure. Uerwüschte Ereigisse Uerwüschte Ereigisse mit eier Izidez vo 10 % oder höher sid i Tabelle 39 dargestellt hier aalog zu Modul 4 ur auf Ebee der Preferred Terms (PT). Uterschiede vo 5%-Pukte oder mehr zwische de Studiearme fade sich i folgede Preferred Terms: für Pruritus ud Nasopharygitis fiele die Uterschiede vo 5%-Pukte zwische de Arme zuuguste vo OCA+UDCA aus; für Ifektioe der obere Atemwege, Ifektioe der Urigäge, Diarrhoe ud Isomie fiele die Uterschiede vo 5%-Pukte zuguste vo OCA+UDCA aus.
75 Seite 75 Tabelle 39: Uerwüschte Ereigisse mit Izidez 10 % i der 12-moatige DB-Phase der POISE- Studie (Safety-Populatio, Preferred Terms i der Reihefolge der Häufigkeite) Preferred Term 1) OCA+UDCA (N=65) (%) UDCA+Placebo (N=68) (%) Pruritus 35 (54) 28 (41) Fatigue 11 (17) 9 (13) Nasopharygitis 16 (25) 10 (15) Ifektioe der obere Atemwege 4 (6) 8 (12) Ifektioe der Urigäge 3 (5) 8 (12) Übelkeit 4 (6) 7 (10) Diarrhoe 2 (3) 7 (10) Kopfschmerze 12 (18) 11 (16) Isomie 2 (3) 7 (10) 1) Patiete wurde ur eimal i jeder Systemorgaklasse ud Preferred Term gezählt. Abkürzuge: DB: Doppelblid; OCA: ; UDCA: Ursodesoxycholsäure.
76 Seite Methodische Amerkuge ud Bewertug der Uterlage 3.1 Zulassugsstatus ud Zulassugspopulatio vo Gemäß Zulassug ist (OCALIVA ) idiziert zur Behadlug der primär biliäre Cholagitis (auch uter der Bezeichug primär biliäre Zirrhose bekat) i Verbidug mit Ursodesoxycholsäure (UDCA) bei Erwachsee, die uzureiched auf UDCA aspreche, oder als Mootherapie bei Erwachsee, die UDCA icht toleriere köe. Es ist zugelasse als Arzeimittel zur Behadlug eies seltee Leides ach der Verordug (EG) Nr. 141/2000 des Europäische Parlamets ud des Rates vom 16. Dezember 1999 über Arzeimittel für seltee Leide. Die vorliegede Nutzebewertug zu (OCA) basiert auf der Zulassugsstudie POISE , eier 12-moatige radomisierte, doppelblide dreiarmige placebokotrollierte Phase-III-Studie (OCA 10 mg, OCA-Titratio ud Placebogruppe) mit eier dara aschließede, auf füf Jahre ausgerichtete eiarmige offee Lagezeitsicherheitsstudie (LTSE-Phase). Es hadelt sich i der 12-moatige DB-Phase um eie dreiarmige Studie, wobei der Arm der Itervetiosgruppe (OCA 10mg) etspreched der Fachiformatio als icht zulassugskoform zu bewerte ist, da es sich hierbei um eie feste Dosis ohe Titratio hadelt. Gemäß der Fachiformatio ist OCA mit eier Afagsdosis vo 5 mg eimal täglich zugelasse. Auf der Grudlage der Verträglichkeit sollte die Dosis ach 6 Moate auf 10 mg eimal täglich erhöht werde, um ei optimales Aspreche zu erziele. Vor diesem Hitergrud wurde dieser Itervetiosarm i der vorliegede Nutzebewertug icht berücksichtigt. Für die aschließede eiarmige LTSE-Phase wurde mit Amedmet 4 (25. August 2014) die mögliche Auftitrierug auf bis zu 25 mg auf maximal 10 mg OCA täglich begrezt. Da bis zu Amedmet 4 eie Titrierug über 10 mg täglich möglich war, laut Fachiformatio eie Titratio vo mehr als 10 mg allerdigs icht vorgesehe ist, werde diejeige Patiete i der Nutzebewertug ausgeschlosse, die über de Behadlugszeitraum durchschittlich mehr als 10 mg OCA erhalte habe (21 vo 193 Patiete). Wegleich es rei recherisch möglich ist, dass auch Patiete mit eier durchschittliche Dosis vo 10 mg OCA für eie bestimmte Zeitraum eie höhere Dosis als 10 mg erhalte habe köe, ist bei eier mittlere WADD vo 7,3 mg (vgl. Tabelle 15) davo auszugehe, dass diese Patietezahl klei bzw. der Eiahmezeitraum eier höhere Dosis kurz ist. Zusätzlich wurde vom pu drei Phase-II-Studie eigereicht, dere Dosierug vom Dosisschema laut Fachiformatio (OCA ohe Titratiosphase mit 5 mg für 6 Moate) abweicht ud demetspreched für die vorliegede Nutzebewertug icht berücksichtigt werde. wurde vo der EMA mit eier coditioal marketig authorizatio zugelasse. Die Zulassug uter besodere Bediguge ist mit der Auflage weiterer Studieergebisse verküpft: Studie zum Umfag der Wirksamkeit ud Sicherheit im Rahme eier kofirmatorische, doppelblide, placebokotrollierte Studie bei PBC-Patiete, die UDCA icht toleriere oder icht auf die Behadlug aspreche; Studie zum Ausmaß der Wirksamkeit ud Sicherheit im Rahme eier doppelblide, placebokotrollierte Studie bei PBC-Patiete mit moderate bis schwere Leberfuktiosstöruge. Hierzu sid für die Studie Date im Jahr 2023 ud für die Studie im Jahr 2020 zu erwarte [5].
77 Seite 77 Zusammegefasst ist i der 12-moatige DB-Phase sowie der LTSE-Phase der Studie POISE , uter Berücksichtigug der zuvor geate Ausschlüsse vo Patiete (OCA 10 mg) i dieser Studie, vo eier Übertragbarkeit der Zulassugspopulatio auf de deutsche Versorgugskotext auszugehe. 3.2 Desig ud Methodik der POISE-Studie 12-moatige DB-Phase I die 12-moatige DB-Phase wurde Patiete eigeschlosse, die etweder och mit UDCA behadelt werde kote (midestes 12 Moate mit eier stabile Dosis für 3 Moate) oder die für eie Therapie mit UDCA icht oder icht mehr zur Verfügug stade (für 3 Moate vor Studieeischluss). Der Eischluss i die Studie vom erste Patiete bis zur letzte Nachbeobachtug des letzte Patiete lag zwische März 2012 ud Dezember Zetrales Eischlusskriterium i die Studie war das Vorhadesei midestes eier der folgede biochemische Werte: ALP 1,67 x ULN ud/oder Gesamt-Bilirubi > ULN aber < 2 x ULN. Etspreched der Baselie-Charakteristika zu de a priori defiierte Kriterie lässt sich ableite, dass die Mehrzahl der Patiete (92 %) eie Bilirubiwert ULN aufwiese. Währed bezoge auf de ALP-Wert 27 % der Patiete i der OCA-Titratiosgruppe ud 32 % der Patiete i der Placebogruppe eie ALP-Wert > 3 x ULN zu Baselie (vgl. Tabelle 12). Gemäß de Agabe der FDA [24] wird uter Bezugahme der Rotterdam-Kriterie (Gesamtbilirubi, Albumi), welche der Eiteilug des PBC-Krakheitsstadiums diee, geschlussfolgert, dass es sich bei dem Patietekollektiv i der POISE-Studie überwieged um Patiete im frühe PBC-Krakheitsstadium hadelt [25]. Die Radomisierug erfolgte verblidet i eiem Verhältis 1:1:1. So erhielte die Patiete mit Studiebegi etweder die fixe Dosis OCA 10 mg, OCA 5 mg (Titratiosgruppe) oder Placebo, wobei die Itervetiosgruppe OCA 10 mg wie bereits eigags beschriebe als icht zulassugskoform zu bewerte ist ud keie Eigag i die Nutzebewertug fidet. I der Titratiosgruppe kote auf der Grudlage der Verträglichkeit die Dosis zu Moat 6 auf 10 mg erhöht werde, um ei optimales Aspreche zu erziele. Dazu musste eies der folgede Kriterie erfüllt werde: ALP 1,67 x ULN ud/oder Gesamt-Bilirubi > ULN oder < 15 % ALP-Reduktio bei Moat 6 im Vergleich zu de mittlere Vorbehadlugswerte i der DB-Phase ud sofer UE, wie z. B. schwerer Pruritus, die Gabe eier höhere Dosis icht beschräke. I de zwei für die Nutzebewertug relevate Behadlugsgruppe bestad die Möglichkeit eier Moo- oder Kombiatiostherapie. Währed i der OCA-Titratiosgruppe die Patiete etweder OCA als Mootherapie oder i Kombiatio mit UDCA erhalte kote, erhielte die Patiete i der Placebogruppe etweder Placebo als Mootherapie oder Placebo i Kombiatio mit UDCA. Gemäß eier Post-hoc-Aalyse i Modul 4 des Herstellerdossiers wurde die Ergebisse differeziert ach Moo- ud Kombiatiostherapie aufbereitet. Aufgrud der gerige Fallzahl (OCA-Titratiosarm: N=5; Placeboarm: N=5; Gesamt: N=10) werde die Ergebisse wege der Aussageusicherheite icht berichtet. Folglich liege für Patiete, die für eie UDCA-Substitutio aufgrud eier UDCA-Itoleraz icht geeiget sid, keie aussagekräftige Date vor. Die FDA [25] uterstreicht diese Aspekt ud fordert zusätzliche Date im Rahme eier kofirmatorische Studie. Das Ziel der 12-moatige DB-Phase war die Utersuchug der Wirksamkeit, Sicherheit ud Verträglichkeit vo OCA im Vergleich zu Placebo. Der primäre Edpukt, sowohl i der 12-moatige DB-Phase als auch i der LTSE-Phase, war ei aus drei Eizelkompoete kombiierter Edpukt:
78 Seite 78 Ateil vo Patiete mit ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN ud ALP-Reduktio 15 %. Dieser wurde für die vorliegede Nutzebewertug als icht patieterelevat eigestuft (vgl. Tabelle 8). Zudem fehle im Studiebericht Agabe zu de Eizelkompoete ALP < 1,67 x ULN ud Gesamt-Bilirubi ULN, sodass für diese Edpukte keie Aussage für die Studiepopulatio getroffe werde ka. Demgegeüber fide sich i der Post-hoc-Auswertug i Modul 4 Agabe zu de Eizelkompoete für die Kombiatiostherapie (OCA+UDCA vs. Placebo+UDCA; N=133), i der Patiete mit Mootherapie OCA (N=10) uberücksichtigt bleibe. Hier ist eie Aussage für die Eizelkompoete des primäre kombiierte Edpuktes möglich, auch we ur auf Subgruppeiveau. Isgesamt wurde i die 12-moatige DB-Phase 71 Patiete i die OCA-Titratiosgruppe ud 73 Patiete i die Placebogruppe (N=144) radomisiert. Ei Patiet i der OCA-Titratiosgruppe zog seie Eiverstädiserklärug ach der Radomisierug ud vor Begi der Studiemedikatio zurück. Somit wurde isgesamt 143 Patiete i die ITT- bzw. Safety-Populatio eigeschlosse (OCA-Titratio: 70; Placebo: 73). Isgesamt wurde währed der 12-moatige DB-Phase die Behadlug bei 10 vo 143 Patiete (6,9 %) abgebroche. Die Mehrzahl der Patiete i der OCA- Titratiosgruppe ud i der Placebogruppe erhielte UDCA zu Baselie (jeweils 93 %). Die mediae Behadlugsdauer i beide Studiearme (OCA-Titratio: 360 Tage; Placebo: 361 Tage) war aäherd gleich. I beide Behadlugsarme war die Mehrzahl der Patiete weiblich (jeweils 93 %), uter 65 Jahre alt (OCA-Titratio: 86 %; Placebo: 82 %) ud Kaukasier (OCA-Titratio: 96 %; Placebo: 90 %). Das mediae Alter war i beide Behadlugsgruppe mit 48 Jahre gleich. Mehr als die Hälfte der Patiete i beide Behadlugsgruppe hatte eie Pruritus zu Studiebegi, wobei Patiete i der Placebogruppe häufiger betroffe ware (OCA-Titratio: 53 %; Placebo: 64 %). Dabei stufte die Mehrheit der Patiete de Pruritus-Schweregrad als mild oder moderat ei (OCA-Titratio: isgesamt 53 %; Placebo: isgesamt 62 %). Eie schwere Pruritus zu Baselie gabe ausschließlich 2 Patiete i der Placebogruppe a, obwohl ei schwerer Pruritus per se als Ausschlusskriterium gemäß Amedmet 2 (Stad: 4. April 2012) festgelegt wurde. I der Placebogruppe zeigte sich im Gegesatz zur OCA-Titratiosgruppe eie erhöhte PBC-bedigte Fatique i der Aamese (Placebo: 67 % vs. OCA-Titratio: 54 %). Die vorliegede Versio des SAP 1.0 wurde am 5. März 2014 ach Beedigug der doppelblide 12-moatige Studiephase verfasst. Der Eischluss i die Studie vom erste Patiete bis zur letzte Nachbeobachtug des letzte Patiete lag zwische März 2012 ud Dezember Vor diesem Hitergrud muss kostatiert werde, dass der fiale SAP 1.0 erst ach Beedigug der 12- moatige DB-Phase verfasst wurde. Deoch wurde gemäß Protokoll (Amedmet 3 vom 24. September 2012) die statistische Aalyse beschriebe ud im SAP zum Teil modifiziert. Im Studiebericht (Stad: 17. April 2015) wird über Äderuge vo protokollspezifische Aalyse im SAP 1.0 berichtet. So wurde u. a. die Erfassug der sekudäre Edpukte (krakheitsspezifische Symptome) mithilfe der Pruritus-VAS ud dem 5-D-Pruritus-Frageboge achträglich geädert ud auf Basis der Sicherheitspopulatio aalysiert. Zusammegefasst wird das Verzerrugspotezial auf Studieebee als gerig eigeschätzt. LTSE-Phase Die offee ud damit uverblidete eiarmige LTSE-Phase schloss sich umittelbar a die 12-moatige DB-Phase a ud ist auf 5 Jahre ausgelegt (aktuell och laufed). Die Ziele der LTSE- Phase ware die Bewertug der Effektivität ud der Sicherheit der Behadlug mit OCA sowie der Dauerhaftigkeit der Effekte aus der 12-moatige DB-Phase. Die Date der LTSE-Phase wurde vom pu icht zusamme mit dem Dossiers eigereicht, soder wurde seites der Geschäftsstelle
79 Seite 79 des G-BA für die vorliegede Nutzebewertug achgefordert. Aufgrud des offee Studiedesigs ohe Kotrollgruppe ka auf Studie- ud Edpuktebee vo eiem hohe Verzerrugspotezial ausgegage werde. Die LTSE-Phase wird supportiv zu der 12-moatige DB-Phase heragezoge. Die Auswertuge erfolgte deskriptiv ud icht-vergleiched. Bei der LTSE-Phase liegt ei icht a priori geplater Iterimsbericht (Stad: 21. April 2015) mit eiem Dateschitt vom 31. August 2014 vor. Gemäß Studieprotokoll erhielte alle Patiete mit Begi der LTSE-Phase 5 mg OCA, uabhägig vo ihrer OCA Dosierug währed der 12-moatige DB- Phase. Es bleibt uklar, weshalb eie Ab- bzw. Zurücktitrierug der Dosierug auf 5 mg zu Begi der LTSE-Phase auch bei Patiete erfolgte, die bereits währed der DB-Phase auf 10 mg auftitriert wurde ud diese Dosierug toleriert habe. Die Ratioale ud kliische Sihaftigkeit werde icht erläutert. Mit Amedmet 4 (25. August 2014) wurde die Möglichkeit der Auftitrierug 25 mg auf 10 mg OCA täglich begrezt. Diese Äderug erfolgte allerdigs erst 8 Moate achdem der letzte Patiet i die LTSE-Phase eigeschlosse wurde (letzter Patiet beedete die 12-moatige DB-Phase im Dezember 2013). Patiete, die vor Amedmet 4 bereits mehr als 10 mg OCA täglich erhielte, kote etweder auf ihrer Dosierug verbleibe oder ach Etscheidug der Prüfärzte herutertitriert werde. Die Etscheidug für de Verbleib bei der aktuelle Dosierug oder eier Abtitratio der Dosis auf die zulassugskoforme 10 mg OCA wurde i de Studieuterlage icht achvollziehbar operatioalisiert. Drüber hiaus war es mit dem Amedmet 4 möglich, dass Patiete, die währed der LTSE-Phase ei Aspreche zeigte ud UDCA erhielte, die UDCA-Substitutio beede durfte, we kliisch idiziert ud durch de Prüfarzt geehmigt. Eie Begrüdug für diese Veräderug im Gegesatz zur 12-moatige DB-Phase, i der eie Weitergabe der UDCA- Behadlug trotz Aspreche idiziert war, fidet sich ebefalls icht i de Studieuterlage. Da bis zum Amedmet 4 eie Titrierug über 10 mg täglich möglich war, werde diejeige Patiete i der Nutzebewertug ausgeschlosse, die über de Behadlugszeitraum durchschittlich mehr als 10 mg OCA erhalte habe (21 vo 193 eigeschlossee Patiete). Demach erhielte 172 Patiete im Rahme der LTSE-Phase eie gewichtete durchschittliche Tagesdosis (WADD) OCA vo 10 mg. Vo de 172 Patiete ware währed der 12-moatige DB-Phase 56 Patiete (33 %) i der Placebogruppe, 59 Patiete (34 %) i der OCA-Titratiosgruppe ud 57 Patiete (33 %) i der fixe OCA-10-mg-Gruppe. Die mediae Behadlugsdauer uter OCA lag bei 634 Tage, wobei die Mehrzahl der Patiete (N=144) für midestes ei Jahr ud mehr OCA erhielte (vgl. Tabelle 15). Die Mehrzahl der Patiete erhielt UDCA zu Baselie (92 %). Isgesamt wurde währed der LTSE-Phase die Behadlug vo 10 der 193 Patiete (5,2 %) abgebroche, vo dee wiederum 9 Patiete der für diese Nutzebewertug relevate WADD- Gruppe 10 mg OCA zuzuorde sid. Zu beachte ist, dass für jee Patiete, die währed der 12-moatige DB-Phase Placebo erhielte, als Baseliewerte Tag 0 der LTSE-Phase gewählt wurde. Demgegeüber war der Baseliewert für jee Patiete, die währed der DB-Phase bereits mit OCA behadelt wurde, der Durchschittswert aller verfügbare Date vor Studiebegi der 12-moatige DB-Phase. Demach sid die verwedete Baseliewerte für diese Gruppe sogeate historische ud somit ei Jahr zurückliegede Werte.
80 Seite Wirksamkeit Zur Wirksamkeit werde achfolged die Edpukte Gesamtüberlebe ud Pruritus berichtet. Der primäre kombiierte Edpukt ist für die Nutzebewertug icht patieterelevat (siehe 2.5.3) ud wird demetspreched auch icht weiter berücksichtigt. Mortalität Mortalität war gemäß Protokoll für die Auswertug der POISE-Studie kei geplater Effektivitätsparameter, soder wurde uter de Sicherheitsedpukte erfasst. Währed der 12-moatige DB-Phase trat i der OCA-Titratiosgruppe ei Todesfall ud i der Placebogruppe kei Todesfall auf. Ursache für diese Todesfall war Herzversage aufgrud eier umfagreiche Krakevorgeschichte vo kardiovaskuläre Ereigisse, die ach Agabe des pu icht im direkte Zusammehag mit der Studiemedikatio steht. I der LTSE-Phase trat im Erhebugszeitraum (Dateschitt: 31. August 2014) ei Todesfall auf. Der Patiet verstarb a Multiorgaversage aufgrud eier Sepsis ach eier Edokarditis. Laut Agabe des pu steht der Todesfall icht i direkte Zusammehag mit der Studiemedikatio. Pruritus Die Ergebisse für de Edpukt Pruritus werde durch de 5-D-Frageboge ud mit der VAS dargestellt ud basiere auf der Safety-Populatio (N=143). Währed der 12-moatige DB-Phase zeigte sich für de 5-D-Frageboge uter Verwedug eies MMRM-Modells ach Moat 6 ud Moat 12 i keier der Domäe ei sigifikater Uterschied zwische OCA-Titratiosgruppe ud Placebogruppe. I der LTSE-Phase liege für de 5-D-Frageboge ud die VAS ur icht-vergleichede Ergebisse vor, weshalb eie abschließede Bewertug schwierig ist ud die Aussagekraft eigeschräkt ist. I der Subgruppeaalyse für die Kombiatiostherapie (OCA+UDCA vs. UDCA+Placebo) zeigte sich ausschließlich für de Gesamtscore, die Eizeldomäe Richtug ud für die VAS sigifikate Uterschiede zwische de Behadlugsgruppe zuuguste vo OCA+UDCA. Allerdigs überlappe die 95%-KI der SMD die Relevazschwelle vo 0,2 die i Abweseheit eier MID für Gruppeuterschiede gewählt wurde i alle Domäe ud der VAS, sodass sich keie kliisch relevate Uterschiede zwische de Behadlugsgruppe zeige Zusammefassede Eischätzug zur Wirksamkeit Auf Basis der weige vorgelegte Date zu patieterelevate Edpukte, wurde ausschließlich Mortalität ud Pruritus zur Aalyse der Wirksamkeit vo OCA heragezoge. Eie Eischätzug zum Zusatzutze hisichtlich der Wirksamkeit ist aufgrud der vorliegede Date zur Mortalität ud Pruritus eigeschräkt. Für die 12-moatige DB-Phase ka lediglich geschlussfolgert werde, dass sich das Symptom Pruritus bei Erwachsee mit PBC mittels 5-D-Frageboge ud VAS sowohl bezoge auf de Gesamtscore als auch bezoge auf die eizele Domäe icht wesetlich zu verschlechter scheit. Die kliische Relevaz dieser Uterschiede ist allerdigs aufgrud eier fehlede MID für eie Gruppeuterschied uklar (vgl. Tabelle 18). I der LTSE-Phase zeige sich vergleichbare Ergebisse i zum Teil gleicher Größeordug wie i der OCA-Titratiosgruppe. Deoch hadelt es sich hier um eie icht-vergleichede eiarmige
81 Seite 81 Studie. Patiete sid mit uterschiedliche Voraussetzuge i die Studie eigetrete, da sowohl therapieaive Patiete gegeüber OCA als auch mit OCA vorbehadelte Patiete (5 oder 10 mg) eigeschlosse wurde. Darüber hiaus erfolgte für alle Patiete, die i der 12-moatige DB- Phase bereits auf 10 mg auftitriert wurde, mit Eischluss i die LTSE-Phase eie ereute Abtitrierug auf 5 mg. Die geate Limitatioe der LTSE-Phase lasse eie abschließede Bewertug der Ergebisse ud eie dara aküpfede Aussagekraft ur eigeschräkt zu. 3.4 Lebesqualität Für die Erfassug der Lebesqualität wurde der PBC-40-Frageboge mit de Domäe Geerelle Symptome, Jucke, Fatique, Kogitive Fuktioe, Soziale Domäe ud Emotioale Domäe verwedet. Es hadelt sich um ei weitestgehed validiertes ud krakheitsspezifisches Istrumet zur Messug der Lebesqualität bei Patiete mit PBC. Währed der 12-moatige DB-Phase zeigte sich für de PBC-40-Frageboge uter Verwedug eies MMRM-Modells ach Moat 6 ud Moat 12 i keier der Domäe ei sigifikater Uterschied zwische OCA-Titratiosgruppe ud Placebogruppe. Die Subgruppeaalyse für die Kombiatiostherapie (OCA+UDCA vs. UDCA+Placebo) zeigte für die Domäe Geerelle Symptome, Jucke, Fatique ud Kogitive Fuktioe keie sigifikate Uterschiede zwische de Behadlugsgruppe. I de Domäe Sozial ud Emotioal kote higege ei sigifikater Uterschied zwische de Behadlugsgruppe zuguste vo OCA+UDCA gezeigt werde. Allerdigs überlappe die SMD der 95%-KI die Relevazschwelle vo 0,2 die i Abweseheit eier MID für Gruppeuterschiede gewählt wurde i alle Domäe, sodass sich keie kliisch relevate Uterschiede zwische de Behadlugsgruppe zeige. I der LTSE-Phase zeigte sich zu Moat 12 im Vergleich zu Baselie eie sigifikate Verschlechterug für die Domäe Jucke (p<0,0001). Aufgrud der o. g. Limitatioe ist eie abschließede Bewertug der Ergebisse ud eie dara aküpfede Aussagekraft eigeschräkt Zusammefassede Eischätzug zur Lebesqualität Eie Eischätzug zum Zusatzutze hisichtlich der Lebesqualität ist aufgrud der vorliegede Date schwierig. Für die eizele Domäe werde ausschließlich eie zu erreichede Miimumud Maximum-Puktspae agegebe, die sich je ach Domäe uterscheidet. Dabei deute iedrige Puktwerte auf eie bessere ud höhere Puktwerte auf eie gerigere Lebesqualität hi. Ahad der Ergebisse ka lediglich geschlussfolgert werde, dass die Lebesqualität i de eizele Domäe zu Baselie eher mit iedrige Puktwerte agebe wurde. Dies spricht für eie weiger eigeschräkte Lebesqualität, die sich über de 12-moatige Behadlugszeitraum ur margial verädert. Die kliische Relevaz dieser Uterschiede ist allerdigs aufgrud eier fehlede MID für eie Gruppeuterschied uklar. 3.5 Sicherheit 12-moatige DB-Phase Zur Darstellug vo sicherheitsrelevate Edpukte wurde die Sicherheitspopulatio heragezoge, die alle Persoe mit midestes eier Awedug der Studiemedikatio (OCA-Titratio: N=70; Placebo: N=73) umfasst. Vo de Patiete i der OCA-Titratiosgruppe, die Moat 6 erreichte, verbliebe 36 Patiete bei der Dosierug vo 5 mg, währed 33 Patiete de primäre
82 Seite 82 kombiierte Edpukt icht erreichte ud ach 6 Moate i der DB-Phase auf 10 mg auftitriert wurde. Die mediae Behadlugsdauer i beide Studiearme (OCA-Titratio: 360 Tage; Placebo: 361 Tage) war aäherd gleich. Uerwüschte Ereigisse Für 65 Patiete (93 %) i der OCA-Titratiosgruppe ud für 66 Patiete (90 %) i der Placebogruppe wurde midestes ei UE berichtet. Isgesamt wurde i der OCA-Titratiosgruppe 471 UE ud i der Placebogruppe 452 UE berichtet. Die häufigste PT i der OCA-Titratiosgruppe mit eier Izidez vo mehr als 15 % ware Pruritus (39 Patiete [56 %]), Nasopharygitis (17 Patiete [24 %]), Fatique (11 Patiete [16 %]) ud Kopfschmerze (12 Patiete [17 %]). Demgegeüber ware die häufigste PT i der Placebogruppe Pruritus (28 Patiete [38 %]), Nasopharygitis (13 Patiete [18 %]), Kopfschmerze (13 Patiete [18 %]). UE, das zum Abbruch der Studiemedikatio führte, umfasste i der OCA-Titratiosgruppe 5 Patiete (7 %), wovo ei Abbruch aufgrud vo Pruritus erfolgte. I der Placebogruppe brache die 12-moatige DB-Phase 2 Patiete (3 %) ab, jedoch icht aufgrud vo Pruritus. Schwere ud schwerwiegede uerwüschte Ereigisse Isgesamt berichtete mehr Patiete i der OCA-Titratiosgruppe vo schwere UE (22 Patiete [31 %]) als i der Placebogruppe (9 Patiete [14 %]). Am häufigste wurde Pruritus als schweres UE agegebe (OCA-Titratio: 13 Patiete [19 %]; Placebo: 5 Patiete [7 %]. Für 11 Patiete (16 %) der OCA-Titratiosgruppe wurde ei SUE berichtet. Für die SOC Erkrakuge des Gastroitestialtraktes, Erkrakuge des Nervesystems, Gefäßerkrakuge ud Allgemeie Erkrakuge ud Beschwerde am Verabreichugsort fiele die Uterschiede vo 3%-Pukte zwische de Arme zuuguste vo OCA aus. Pruritus wurde icht als SUE erfasst. Vom pu beschriebee uerwüschte Ereigisse vo besoderem Iteresse Pruritus ist als UE vo besoderem Iteresse im SAP präspezifiziert ud wurde bereits uter de Sicherheitsedpukte berichtet. Für 39 Patiete (56 %) i der OCA-Titratiosgruppe ud 28 Patiete (38 %) i der Placebogruppe wurde midestes ei UE-Pruritus berichtet. UE-Pruritus- Ereigisse Schweregrade mild oder moderat trate i der OCA-Titratiosgruppe bei 26 Patiete (37 %) ud i der Placebogruppe bei 23 Patiete (32 %) auf. Pruritus als schweres UE wurde i der OCA-Titratiosgruppe vo 13 Patiete (19 %) ud i der Placebogruppe vo 5 Patiete (7 %) agegebe. Die mediae Zeit bis zum erste Pruritus war währed der Gesamtdauer der Studie i der OCA-Gruppe kürzer als i der Placebogruppe (p=0,0349). Die mediae Zeit des erstmalige Auftretes vo Pruritus (50 % der Patiete berichtete ei Ereigis) lag bei 188 Tage, der Media für die Placebogruppe wurde icht erreicht. Daebe wurde Kardiovaskuläre Ereigisse, Leberbedigte Ereigisse ud Lipidbedigte Ereigisse im Studiebericht als UE vo besoderem Iteresse beat. 5 Patiete im Placeboarm (7 %) ud 6 Patiete im Tritratiosarm (9 %) erlitte midestes ei kardiovaskuläres UE währed der Gesamtstudiezeit. Mit eier Fuktiosstörug der Leber verbudee UE trate bei 3 Patiete im Placeboarm (4 %) ud bei 5 Patiete i der Titratiosgruppe (7 %) währed der DB-Phase auf. Bei zwei Patiete im Placeboarm (3 %) ud eiem Patiete im Titratiosarm (1 %) kam es zu midestes eiem lipid-bezogeem UE währed der DB-Phase. I der Subgruppeaalyse für die Kombiatiostherapie (OCA+UDCA vs. UDCA+Placebo) trate bei fast alle Studieteilehmer UE auf (OCA+UDCA: 92,2 %; UDCA+Placebo: 89,7 %). SUE, schwere UE ohe UE-Pruritus ud UE, die zum Abbruch der Studiemedikatio führte, trate
83 Seite 83 häufiger im OCA+UDCA-Arm als im UDCA+Placebo-Arm auf. Als ergäzede Aalyse wurde die schwere UE (iklusive UE-Pruritus) dargestellt. Hier fad sich ei sigifikater Nachteil für OCA+UDCA gegeüber UDCA+Placebo (RR: 2,21 [1,08;4,52], p=0,0247). Für die PT Pruritus, ud Nasopharygitis fiele die Uterschiede vo 5%-Pukte zwische de Arme zuuguste vo OCA+UDCA aus. Für die PT Ifektioe der obere Atemwege, Harwegsifekte, Diarrhoe ud Isomie fiele die Uterschiede vo 5%-Pukte zuguste vo UDCA+Placebo aus. LTSE-Phase I der LTSE-Phase trate i der betrachtete Patietepopulatio WADD 10 mg OCA isgesamt 726 UE bei 150 Patiete (87 %) auf, vo dee 71 Patiete (41 %) midestes ei UE-Pruritus berichtete. Zu de am meiste berichtete SOC zähle Erkrakuge der Haut ud des Uterhautzellgewebes (N=80), vo dee 71 Patiete ei Pruritus-Ereigis berichtete, sowie Ifektioe ud parasitäre Erkrakuge (N=61) ud Erkrakuge des Gastroitestialtraktes (N=58). 48 vo 172 Patiete (28 %) berichtete ei mildes oder moderates UE-Pruritus, währed 23 Patiete (13 %) vo eiem schwere UE-Pruritus berichtete. 13 vo 172 Patiete (8 %) hatte midestes ei SUE. Uklar ist, ob Pruritus als SUE auftrat. Nebe Pruritus als UE vo besodere Iteresse wurde zusätzlich Herzerkrakuge, Dyslipidaemie ud Lebererkrakuge heragezoge. Isgesamt trat bei 111 Patiete UE-Pruritus auf, bei 12 Patiete Herzerkrakuge, bei 5 Patiete Dysplpidaemie ud bei 12 Patiete Lebererkrakuge. I Bezug auf Pruritus sid Diskrepaze i de Studieuterlage aufgefalle. Währed i Tabelle 29 vo 71 Patiete mit midestes ei UE-Pruritus berichtet wird, sid es i Tabelle Patiete Zusammefassede Eischätzug zur Sicherheit I der Gesamtschau trate bei fast alle Studieteilehmer i der 12-moatige DB-Phase ud i der LTSE-Phase UE im Verlauf der POISE-Studie auf. Das am häufigste aufgetretee UE i der OCA-Titratiosgruppe war Pruritus. Ahad der Studiedate für die 12-moatige DB-Phase lässt sich ei erhöhtes Risiko für eie schwere Pruritus durch OCA im Vergleich zu Placebo ableite. Da UE-Pruritus häufig auch als Symptom der Erkrakug auftritt oder als Komorbidität bekat ist, ist die Bewertug isgesamt schwierig. I der LTSE-Phase sid die Veräderuge im Auftrete uerwüschter Ereigisse durch OCA aufgrud fehleder paralleler Kotrollgruppe icht abschätzbar.
84 Seite Aforderuge a eie qualitätsgesicherte Awedug Die Vorgabe der Fachiformatio sid zu berücksichtige. Die Behadlug mit sollte uter der Aufsicht eies Arztes mit Erfahrug bei der Behadlug vo Patiete mit primär biliärer Cholagitis (primär biliäre Zirrhose) begoe werde.
85 Seite Zusammefassug der Bewertug (OCA) ist zugelasse für die Behadlug der primär biliäre Cholagitis (auch uter der Bezeichug primär biliäre Zirrhose bekat) i Verbidug mit Ursodesoxycholsäure (UDCA) bei Erwachsee, die uzureiched auf UDCA aspreche, oder als Mootherapie bei Erwachsee, die UDCA icht toleriere köe. Die Nutzebewertug vo OCA basiert auf der zulassugsbegrüdede Studie POISE , eier multizetrische, radomisierte, doppelblide, placebokotrollierte Phase-III-Studie mit eier 12-moatige Behadlugsphase (DB-Phase) ud aschließeder Lagzeit-Sicherheitsstudie (LTSE-Phase) bis zu 5 Jahre. Bei der LTSE-Phase hadelt es sich um eie icht-vergleichede eiarmige Studie. Aufgrud der i der Diskussio aufgeführte Limitatioe lasse die Ergebisse keie verlässliche Aussage zu. Vor diesem Hitergrud werde achfolged ur die Ergebisse der 12-moatige DB-Phase für die Bewertug heragezoge. Die Ergebisse der 12-moatige DB-Phase der POISE-Studie werde i der folgede Tabelle uter Berücksichtigug des Verzerrugspotezials zusammegefasst. Es wird dargestellt, ob uter ei statistisch sigifikat positiver Effekt bei hohem oder uklarem ( ) oder iedrigem ( ) Verzerrugspotezial bzw. ei statistisch sigifikat egativer Effekt bei hohem oder uklarem ( ) oder iedrigem ( ) Verzerrugspotezial bzw. kei Uterschied ( ) gezeigt werde kote. Tabelle 40: Zusammefassede Darstellug der Studieergebisse der 12-moatige DB-Phase der Studie POISE Edpukt Ergebis Effekt Mortalität OCA 1) vs. Placebo 2), (%) Gesamtüberlebe 1 (1,4) 3) vs. 0 (0) Morbidität 4) 5-D-Pruritus-Frageboge 6) ud Pruritus-VAS 7) (1) Gesamtscore (2) Dauer (3) Schweregrad (4) Richtug (5) Behiderug (6) Verteilug (7) Pruritus-VAS Lebesqualität 4) PBC-40-Frageboge 9) (1) Geerelle Symptome (2) Jucke (3) Fatique (4) Kogitive Fuktio (5) Soziale Domäe (6) Emotioale Domäe Baselie, OCA 1) vs. Placebo 2) OCA 1) Placebo 2) LS-MWD [95%-KI] p-wert 5) 10,2 (3,61) 1,2 (0,57) 1,9 (1,00) 3,1 (1,19) 1,9 (1,13) 2,0 (1,19) 21,2 (26) 10,9 (5,00) 1,4 (0,97) 2,0 (0,99) 3,2 (1,42) 1,8 (1,37) 2,3 (1,45) 25,3 (27,5) 1,25 [-0,08;2,59], 0,0656 0,36 [0,00;0,71], 0,0528 0,18 [-0,09;0,46], 0,1940 0,38 [-0,08;0,84], 0,1015 0,20 [-0,16;0,55], 0,28 0,18 [-0,15;0,52], 0,2825 4,4 [-2,6;11,3], 0,2209 Baselie, OCA 1) vs. Placebo 2) OCA 1) Placebo 2) LS-MWD [95%-KI] p-wert 5) 13,8 (5,27) 4,1 (3,55) 25,9 (10,83) 11,6 (5,96) 19,7 (8,63) 6,4 (2,87) 13,1 (4,82) 4,3 (3,) 26,2 (11,18) 11,4 (5,40) 21,0 (8,81) 6,8 (3,31) -0,32 [-1,41;0,77], 0,5660 0,55 [-0,32;1,41], 0,2156 1,76 [-0,37;3,89], 0,1048-0,09 [-1,27;1,09], 0,8790 1,75 [-0,32;3,81], 0,0972 0,45 [-0,24;1,15], 0,1973 * 8) * 8)
86 Seite 86 Edpukt Ergebis Effekt Sicherheit OCA 1) vs. Placebo 2), (%) UE UE-Pruritus Schwere UE Schwere UE-Pruritus 65 (93) vs. 66 (90) 39 (56) vs. 28 (38) 22 (31) vs. 9 (12) 13 (19) vs. 5 (7) SUE 10) 11 (16) vs. 3 (4) UE, die zum Therapieabbruch führte UE-Pruritus 5 (7) vs. 2 (3) 1 (1) vs. 0 1) Es hadelt sich um die OCA-Titratiosgruppe (N=70). 2) Es hadelt sich um die Kotrollgruppe, d. h. Placebo als Mootherapie oder i Kombiatio mit UDCA (N=73). 3) Die primäre Todesursache wurde als kogestive Herzisuffiziez ud ischämische Herzkrakheit, vor dem Myokardifarkt, festgestellt. Sekudäre Todesursache wurde als chroische Niereerkrakug ud PBC aufgeführt. Der Prüfer beurteilte das Ereigis als schwerwieged ud uwahrscheilich im Zusammehag mit der Studiemedikatio. Der Sposor stimmte dieser Eischätzug zu. 4) Die Ergebisse sid als Veräderug vo Moat 12 zu Baselie dargestellt. 5) Berechug der p-werte basiered auf der MMRM-Methode mit fixed effects für Behadlug, Zeit, Iteraktiosterm für Behadlugsgruppe ud Zeit sowie ach zur Radomisierug verwedete Stratavariable ud Baseliewert als Kovariate. 6) Die zu erreichede Gesamtpuktzahl liegt zwische 5 ud 25 Pukte. Jede Domäe ka eie Puktwert vo 1 bis 5 Pukte erreiche. Höhere Pukte deute auf eie stärkere Pruritus hi. 7) Scores reiche vo 0 (kei Pruritus) bis 100 (schwerer Pruritus). 8) Nicht eischätzbar, da keie validierte MID für Gruppevergleiche vorliege. 9) Die zu erreichede Puktzahle für die eizele Domäe liege zwische: Geerelle Symptome (6 bis 35), Jucke (0 bis 15), Fatique (11 bis 66) Kogitive Fuktio (6 bis 30), soziale Domäe (8 bis 50), emotioale Domäe (3 bis 15). Höhere Puktzahle deute auf eie gerigere Lebesqualität hi. 10) Es trat kei SUE aufgrud vo Pruritus auf. Abkürzuge: DB: Doppelblid; LS-MWD: Least-squares-Mittelwertdifferez; MMRM: gemischtes Modell für wiederholte Messuge; MW: Mittelwert; OCA: ; PBC: primär biliäre Cholagitis; SD: Stadardabweichug; (S)UE: (schwerwiegede/s) uerwüschte/s Ereigis/se; VAS: visuelle Aalogskala;
87 Seite 87 Refereze 1. Carboe M, Sharp SJ, Flack S, Paximadas D, Spiess K, Adgey C, et al. The UK-PBC risk scores: Derivatio ad validatio of a scorig system for log-term predictio of ed-stage liver disease i primary biliary cirrhosis. Hepatology 2016;63(3): Civa JM. Leberzirrhose [olie]. I: MSD Maual. Keilworth (USA): Merck, Sharp ad Dohme; [Zugriff: ]. URL: %2Ferkrakuge %2Dder %2Dleber %2C %2Dder %2Dgalleblase %2Dud %2D der %2Dgallewege %2Ffibrose %2Dud %2Dzirrhose %2Fleberzirrhose. 3. Elma S, Hya LS, Gabriel V, Mayo MJ. The 5-D itch scale: a ew measure of pruritus. Br J Dermatol 2010;162: Europea Associatio for the Study of the Liver. EASL Cliical Practice Guidelies: maagemet of cholestatic liver diseases. J Hepatol 2009;51: Europea Medicies Agecy (EMA). Ocaliva (obeticholic acid): Europea public assessmet report; EMEA/H/C/004093/000: [olie]. Lodo (GBR): EMA; [Zugriff: ]. URL: _Public_assessmet_report/huma/004093/WC pdf. 6. Europea Medicies Agecy (EMA). Ocaliva (): EPAR Produktiformatio, Ahäge 1, 2, 3, 4; EMEA/H/C/ [olie]. Lodo (GBR): EMA; [Zugriff: ]. URL: _Product_Iformatio/huma/004093/WC pdf. 7. Gemeisamer Budesausschuss (G-BA). Tragede Grüde zum Beschluss des Gemeisame Budesausschusses zur Richtliie Ambulate Behadlug im Krakehaus ach 116b SGB V, Alage 2 Nr. 6: Diagostik ud Versorgug vo Patietie ud Patiete mit biliärer Zirrhose, vom 17. September 2009 [olie]. Berli (GER): G-BA; [Zugriff: ]. URL: 8. Hase BE. The Global PBC Study Group [Presetatio] ; Wie (AUT): Liver Forum. um2.pdf. 9. Itercept Pharma Deutschlad GmbH. Dossier zur Nutzebewertug gemäß 35a SGB V: (OCA, Ocaliva) [uveröffetlicht] Itercept Pharmaceuticals. Fachiformatio Ocaliva () 5 mg / 10 mg Filmtablette [olie] [Zugriff: ]. URL: Itercept Pharmaceuticals. A phase 3, double blid, placebo cotrolled trial ad log term safety extesio of obeticholic acid i patiets with primary biliary cirrhosis (PBC OCA Iteratioal Study of Efficacy, POISE) (study ): cliical study protocol ad amedmets [uveröffetlicht] Itercept Pharmaceuticals. A phase 3, double blid, placebo cotrolled trial ad log term safety extesio of obeticholic acid i patiets with primary biliary cirrhosis (PBC OCA
88 Seite 88 Iteratioal Study of Efficacy, POISE) (study ): cliical study report [uveröffetlicht] Itercept Pharmaceuticals. A phase 3, double blid, placebo cotrolled trial ad log term safety extesio of obeticholic acid i patiets with primary biliary cirrhosis (PBC OCA Iteratioal Study of Efficacy, POISE) (study ): statistical aalysis pla [uveröffetlicht] Itercept Pharmaceuticals. A phase 3, double blid, placebo cotrolled trial ad log term safety extesio of obeticholic acid i patiets with primary biliary cirrhosis. Log-term safety extesio phase: iterim cliical study report (syoptic) [uveröffetlicht] Itercept Pharmaceuticals. A phase 3, double blid, placebo cotrolled trial ad log term safety extesio of obeticholic acid i patiets with primary biliary cirrhosis. Log-term safety extesio phase: protocol ad protocol amedmets [uveröffetlicht] Itercept Pharmaceuticals. A phase 3, double blid, placebo cotrolled trial ad log term safety extesio of obeticholic acid i patiets with primary biliary cirrhosis: statistical aalysis pla for the log term safety extesio phase [uveröffetlicht] Jacoby A, Raard A, Buck D, Bhala N, Newto JL, James OFW, et al. Developmet, validatio, ad evaluatio of the PBC-40, a disease specific health relatd quality of life measure for primary biliary cirrhosis. Gut 2005;54: Kumagi T, Guidi M, Fischer SE, Areovich T, Abdalia R, Coltescu C, et al. Baselie ductopeia ad treatmet respose predict log-term histological progressio i primary biliary cirrhosis. Am J Gastroeterol 2010;105(10): Kumagi T, Heathcote EJ. Primary biliary cirrhosis. Orphaet J Rare Dis 2008;3: Lammers WJ, va Buure HR, Hirschfield GM, Jasse HL, Iverizzi P, Maso AL, et al. Levels of Alkalie Phosphatase ad Bilirubi Are Surrogate Ed Poits of Outcomes of Patiets With Primary Biliary Cirrhosis: A Iteratioal Follow-Up Study. Gastroeterology 2014;147: Lidor KD, Gershwi ME, Poupo R, Kapla M, Bergasa NV, Heathcote EJ, et al. Primary biliary cirrhosis. Hepatology 2009;50: Momah N, Silveira MG, Jorgese R, Siakos E, Lidor KD. Optimizig biochemical markers as edpoits for cliical trials i primary biliary cirrhosis. Liver It 2012;32(5): Tretekow AE. Primär biliäre Zirrhose. I: Mas MP, Scheidewid S (Eds). Praxis der Hepatologie. Berli: Spriger; S U.S. Food ad Drug Admiistratio (FDA). Ocaliva (obeticholic acid), applicatio umber Orig1s000: statistical review [olie]. Silver Sprig (USA): FDA; [Zugriff: ]. URL: U.S. Food ad Drug Admiistratio (FDA). Ocaliva (obeticholic acid), applicatio umber Orig1s000: summary review [olie]. Silver Sprig (USA): FDA; [Zugriff: ]. URL:
89 Seite UK-PBC Cosortium. PBC-40: a disease specific health related quality of life measure for primary biliary cirrhosis [olie]. Newcastle (GBR): UK-PBC; [Zugriff: ]. URL:
90 Seite 90 Ahag Tabelle 41: Ergebisse zum 5-D-Pruritus-Frageboge ud der Pruritus- VAS ach 6 ud 12 Moate i der 12-moatige DB-Phase der POISE-Studie (Safety-Populatio; ANCOVA-Model) POISE-Studie 12- motige DB-Phase OCA-Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) 5-D-Frageboge 3) Gesamtscore Zum jeweilige Erhebugs-zeitpukt 63 10,2 (3,61) 9,0 (5;19) 65 10,9 (5,00) 10,0 (5;24) 66 10,7 (4,82) 9,0 (5;23) 62 10,5 (4,68) 10,0 (5;23) 59 10,9 (4,79) 10 (5;23) 63 10,7 (4,44) 10,0 (5;24) Veräderug zum Erhebugs-zeitpukt LS-MW (SE) ,95 (0,78) 61 0,10 (0,80) 54 1,70 (0,75) 58 0,54 (0,76) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) (0.70) [-0,52, 2,23] 0, (0.) [-0,20, 2,53] 0, D-Frageboge 3) Dauer Zum jeweilige Erhebugs-zeitpukt 65 1,2 (0,57) 1 (1;5) 1,4 (0,97) 1 (1;5) 68 1,4 (0,90) 1 (1;5) 65 1,3 (0,91) 1 (1;5) 60 1,5 (1,23) 1 (1;5) 66 1,3 (0,90) 1 (1;5) Veräderug zum Erhebugs-zeitpukt LS-MW (SE) ,38 (0,16) 65 0,19 (0,17) 60 0,53 (0,21) 65 0,23 (0,20) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) (0,14) [-0,10, 0,47] 0, (0,18) [-0,07, 0,66] 0, D-Frageboge 3) Schweregrad Zum jeweilige Erhebugs-zeitpukt 68 1,9 (1,00) 2 (1;4) 70 2,0 (0,99) 2 (1;5) 2,0 (1,03) 2 (1;5) 68 1,9 (0,94) 2 (1;4) 61 2,1 (1,03) 2 (1;5) 65 2,0 (0,89) 2 (1;4) Veräderug zum Erhebugs-zeitpukt LS-MW (SE) ,30 (0,16) 66 0,13 (0,16) 60 0,27 (0,15) 65 0,14 (0,15) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,17 (0,15) [-0,13, 0,15] 0,2607 0,14 (0,14) [-0,14, 0,42] 0,3356
91 Seite 91 POISE-Studie 12- motige DB-Phase 5-D-Frageboge 3) Richtug OCA-Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) Zum jeweilige Erhebugs-zeitpukt 64 3,1 (1,19) 4 (1;5) 65 3,2 (1,42) 4 (1;5) 67 3,0 (1,41) 3 (1;5) 62 2,8 (1,31) 3 (1;5) 60 3,1 (1,32) 4 (1;5) 64 2,9 (1,29) 3 (1;5) Veräderug zum Erhebugs-zeitpukt LS-MW (SE) ,15 (0,24) 59-0,41 (0,26) 56-0,02 (0,24) 59-0,46 (0,25) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,26 (0,23) [-0,20, 0,72] 0,23 0,44 (0,23) [-0,02, 0,90] 0, D-Frageboge 3) Behiderug Zum jeweilige Erhebugs-zeitpukt 67 1,9 (1,13) 1 (1;5) 1,8 (1,37) 1 (1;5) 2,0 (1,24) 1 (1;5) 65 1,9 (1,22) 1 (1;5) 61 2,0 (1,30) 1 (1;5) 66 1,9 (1,20) 1 (1;5) Veräderug zum Erhebugs-zeitpukt LS-MW (SE) ,28 (0,18) 63 0,10 (0,19) 59 0,36 (0,19) 64 0,20 (0,19) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,18 (0,18) [-0,17, 0,52] 0,3202 0,17 (0,18) [-0,19, 0,52] 0, D-Frageboge 3) Verteilug Zum jeweilige Erhebugs-zeitpukt 68 2,0 (1,19) 1,5 (1;5) 70 2,3 (1,45) 2 (1;5) 2,2 (1,28) 1,2 (1;5) 68 2,3 (1,47) 1,5 (1;5) 61 2,2 (1,30) 2 (1;5) 67 2,4 (1,43) 2 (1;5) Veräderug zum Erhebugs-zeitpukt LS-MW (SE) ,35 (0,19) 66 0,19 (0,19) 60 0,43 (0,18) 66 0,29 (0,18) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,16 (0,18) [-0,18, 0,51] 0,3533 0,14 (0,17) [-0,20, 0,48] 0,4087
92 Seite 92 POISE-Studie 12- motige DB-Phase OCA-Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) Pruritus-VAS 5) Zum jeweilige Erhebugs-zeitpukt 68 21,2 (25,9) 10 (0;84) 70 25,3 (27,5) 16,5 (0;100) 23,3 (26,6) 10 (0;91) 20,6 (23,0) 10 (0;87) 62 23,9 (27,2) 10 (0;90) 24,7 (24,9) 12 (0;80) Veräderug zum Erhebugs-zeitpukt LS-MW (SE) ,97 (3,72) 66 1,59 (3,86) 60 5,95 (3,80) 66 2,73 (3,82) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 5,37 (3,53) [-1,59, 12,33] 0,1295 3,22 (3,56) [-3,80, 10,25] 0,3664 1) Baselie ist defiiert als Wert a Tag 0 vor Behadlug 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Die zu erreichede Gesamtpuktzahl liegt zwische 5 ud 25 Pukte. Jeder Domäe ka eie Puktwert vo 1 bis 5 Pukte erreiche. Höhere Pukte deute auf eie stärkere Pruritus hi. 4) Berechug der p-werte basiered auf dem ANCOVA-Modell mit Baseliewert als Kovariate ud fixed effects für Behadlug ud ach zur Radomisierug verwedete Stratavariable. 5) Scores reiche vo 0 (kei Pruritus) bis 100 (schwere Pruritus) Abkürzuge: DB: Doppelblid; KI: Kofidezitervall; LS-MW: Least-squares-Mittelwert; LS-MWD: Least-squares-Mittelwertdifferez; MMRM: gemischtes Modell für wiederholte Messuge; MW: Mittelwert; OCA: ; SD: Stadardabweichug, SE: Stadardfehler; VAS: visuelle Aalogskala.
93 Seite 93 Tabelle 42: Ergebisse zum PBC-40-Frageboge ach 6 ud 12 Moate i der 12-moatige DB- Phase der POISE-Studie (ITT-Populatio; ANCOVA-Modell) POISE-Studie 12- moatige DB-Phase OCA-Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) Geerelle Symptome 3), absolute Veräderug Zum jeweilige Erhebugszeitpukt Mittelwert (SD) 70 13,8 (5,27) 13 (6;27) 72 13,6 (5,27) 13 (6;30) 13,5 (5,00) 14 (6;26) 70 13,1 (4,88) 12 (6;26) 62 13,6 (4,97) 13 (6;24) 13,8 (4,92) 13 (6;32) Veräderug zum Erhebugszeitpukt N LS-MW (SE) - - 1,12 (0,56) 1,06 (0,59) 62 0,81 (0,59) 68 1,15 (0,60) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,06 (0,53) [-0,98, 1,10] 0,9073-0,33 (0,56) [-1,43, 0,76] 0,5498 Jucke 3), absolute Veräderug Zum jeweilige Erhebugszeitpukt Mittelwert (SD) 4,1 (3,55) 3 (0;14) 72 4,3 (3,) 3 (0;14) 4,6 (3,50) 4 (0;14) 70 4,1 (3,55) 3 (0;14) 62 4,6 (3,30) 4 (0;114) 4,4 (3,35) 4 (0;15) Veräderug zum Erhebugszeitpukt N LS-MW (SE) ,67 (0,48) 0,05 (0,50) 62 1,30 (0,47) 68 0,84 (0,48) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,62 (0,45) [-0,27, 1,51] 0,1731 0,46 (0,45) [-0,42, 1,35] 0,3041 Fatigue 3), absolute Veräderug Zum jeweilige Erhebugszeitpukt Mittelwert (SD) 70 25,9 (10,83) 24 (11;50) 72 26,2 (11,18) 25 (11;53) 25,7 (9,74) 25 (11;50) 70 23,8 (10,99) 20 (11;51) 62 25,2 (10,11) 25,5 (11;49) 23,8 (11,56) 22 (11;54) Veräderug zum Erhebugszeitpukt N LS-MW (SE) ,06 (1,10) -1,95 (1,14) 68-0,49 (1,15) 62-2,14 (1,17) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 1,89 (1,03) [-0,13, 3,92] 0,0670 1,64 (1,09) [-0,51, 3,79] 0,1332
94 Seite 94 POISE-Studie 12- moatige DB-Phase OCA-Titratio (N=70) Baselie 1) Moat 6 Moat 12 Placebo 2) (N=73) OCA-Titratio (N=70) Placebo 2) (N=73) OCA- Titratio (N=70) Placebo 2) (N=73) Kogitive Fuktio 3), absolute Veräderug Zum jeweilige Erhebugszeitpukt Mittelwert (SD) 70 11,4 (5,40) 9 (6;23) 72 11,6 (5,96) 10,5 (6;28) 12,0 (5,63) 11 (6;26) 70 11,5 (5,77) 10 (6;26) 62 11,5 (5,51) 11 (6;30) 11,7 (6,38) 9 (9;30) Veräderug zum Erhebugszeitpukt N LS-MW (SE) - - 1,06 (0,62) 0,56 (0,64) 62 0,58 (0,63) 68 0,74 (0,65) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,50 (0,58) [-0,64, 1,64] 0,3886-0,16 (0,60) [-1,35, 1,03] 0,7928 Soziale Domäe 3), absolute Veräderug Zum jeweilige Erhebugszeitpukt Mittelwert (SD) 70 19,7 (8,63) 17 (10;45) 72 21,0 (8,81) 18,5 (10;46) 19,7 (8,00) 17 (10;46) 70 18,9 (8,82) 16 (9;45) 62 19,7 (7,71) 18 (10;46) 19,1 (9,45) 16 (8;48) Veräderug zum Erhebugszeitpukt N LS-MW (SE) ,16 (1,00) -1,90 (1,04) 62 0,17 (1,11) 68-1,05 (1,13) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 1,74 (0,94) [-0,12, 3,59] 0,0659 1,22 (1,05) [-0,86, 3,30] 0,2494 Emotioale Domäe 3), absolute Veräderug Zum jeweilige Erhebugszeitpukt Mittelwert (SD) 70 6,4 (2,87) 6 (3;14) 72 6,8 (3,31) 6 (3;15) 6,4 (2,95) 6 (3;14) 70 6,2 (3,06) 5 (3;14) 62 6,3 (2,67) 6 (3;12) 6,2 (3,08) 5 (3;14) Veräderug zum Erhebugszeitpukt N LS-MW (SE) ,35 (0,39) -0,81 (0,40) 62 0,35 (0,37) 68 0,01 (0,38) OCA vs. Placebo LS-MWD (SE) [95%-KI] p-wert 4) - 0,46 (0,36) [-0,26, 1,18] 0,2093 0,34 (0,35) [-0,36, 1,04] 0,3366 1) Baselie ist defiiert als Wert a Tag 0 vor Behadlug 2) Als Mootherapie oder i Kombiatio mit UDCA. 3) Die zu erreichede Puktzahle für die eizele Domäe liege zwische: Geerelle Symptome (6 bis 35), Jucke (0 bis 15), Fatique (11 bis 66) Kogitive Fuktio (6 bis 30), soziale Domäe (8 bis 50), emotioale Domäe (3 bis 15). Höhere Puktzahle deute auf eie gerigere Lebesqualität hi. 4) Berechug der p-werte basiered auf dem ANCOVA-Modell mit Baseliewert als Kovariate ud fixed effects für Behadlug ud ach zur Radomisierug verwedete Stratavariable. Abkürzuge: DB: Doppelblid; ITT: Itetio-to-Treat; KI: Kofidezitervall; LS-MW: Least-squares-Mittelwert; LS-MWD: Leastsquares-Mittelwertdifferez; MMRM: gemischtes Modell für wiederholte Messuge; MW: Mittelwert; OCA: ; PBC: primär biliäre Cholagitis; SD: Stadardabweichug, SE: Stadardfehler; VAS: visuelle Aalogskala; WADD: gewichtete durchschittliche Tagesdosis.
95 Seite 95 Abbildug 2: 5-D-Pruritus-Frageboge (Quelle: [3])
96 Seite 96
97 Seite 97
98 Seite 98
99 Seite 99 Abbildug 3: PBC-40-Frageboge (Quelle: [26])
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Riociguat wie folgt ergänzt:
 Beschluss des Gemeisame Budesausschusses über eie Äderug der Arzeimittel-Richtliie (AM-RL): Alage XII - Beschlüsse über die Nutzebewertug vo Arzeimittel mit eue Wirkstoffe ach 35a SGB V Riociguat Vom 16.
Beschluss des Gemeisame Budesausschusses über eie Äderug der Arzeimittel-Richtliie (AM-RL): Alage XII - Beschlüsse über die Nutzebewertug vo Arzeimittel mit eue Wirkstoffe ach 35a SGB V Riociguat Vom 16.
In Abhängigkeit vom Zeitpunkt des Auftretens wird ein Rezidiv als platinsensibel
 GYNÄKOLOGISCHE ONKOLOGIE Die Qualität der Rezidivtherapie beim Ovarialkarziom i Deutschlad Eie Qualitätssicherugserhebug im Rahme des Aktiosprogramms der AGO Kommissio OVAR (QS-OVAR) A. du Bois, J. Rocho
GYNÄKOLOGISCHE ONKOLOGIE Die Qualität der Rezidivtherapie beim Ovarialkarziom i Deutschlad Eie Qualitätssicherugserhebug im Rahme des Aktiosprogramms der AGO Kommissio OVAR (QS-OVAR) A. du Bois, J. Rocho
von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V
 Nutzebewertug vo Arzeimittel mit eue Wirkstoffe ach 35a SGB V Bewertug vo Arzeimittel für seltee Leide ach 35a Absatz 1 Satz 10 i.v.m. 5. Kapitel 12 Nr. 1 Satz 2 VerfO Wirkstoff: Datum der Veröffetlichug:
Nutzebewertug vo Arzeimittel mit eue Wirkstoffe ach 35a SGB V Bewertug vo Arzeimittel für seltee Leide ach 35a Absatz 1 Satz 10 i.v.m. 5. Kapitel 12 Nr. 1 Satz 2 VerfO Wirkstoff: Datum der Veröffetlichug:
Qualitätskennzahlen für IT-Verfahren in der öffentlichen Verwaltung Lösungsansätze zur Beschreibung von Metriken nach V-Modell XT
 Qualitätskezahle für IT-Verfahre i der öffetliche Verwaltug Lösugsasätze zur Vo Stefa Bregezer Der Autor arbeitet im Bereich Softwaretest ud beschäftigt sich als Qualitätsbeauftragter mit Theme zu Qualitätssicherug
Qualitätskezahle für IT-Verfahre i der öffetliche Verwaltug Lösugsasätze zur Vo Stefa Bregezer Der Autor arbeitet im Bereich Softwaretest ud beschäftigt sich als Qualitätsbeauftragter mit Theme zu Qualitätssicherug
Statistik mit Excel 2013. Themen-Special. Peter Wies. 1. Ausgabe, Februar 2014 W-EX2013S
 Statistik mit Excel 2013 Peter Wies Theme-Special 1. Ausgabe, Februar 2014 W-EX2013S 3 Statistik mit Excel 2013 - Theme-Special 3 Statistische Maßzahle I diesem Kapitel erfahre Sie wie Sie Date klassifiziere
Statistik mit Excel 2013 Peter Wies Theme-Special 1. Ausgabe, Februar 2014 W-EX2013S 3 Statistik mit Excel 2013 - Theme-Special 3 Statistische Maßzahle I diesem Kapitel erfahre Sie wie Sie Date klassifiziere
Kompetenzinventar im Prozess der Berufswegeplanung Teilhabe am Arbeitsleben für junge Menschen mit einer Behinderung am allgemeinen Arbeitsmarkt
 Grudaussage Kompetezivetar im Prozess der Berufswegeplaug Teilhabe am Arbeitslebe für juge Mesche mit eier Behiderug am allgemeie Arbeitsmarkt G R U N D A U S S A G E N 1 1. Eileitug / Wirkugsbereich I
Grudaussage Kompetezivetar im Prozess der Berufswegeplaug Teilhabe am Arbeitslebe für juge Mesche mit eier Behiderug am allgemeie Arbeitsmarkt G R U N D A U S S A G E N 1 1. Eileitug / Wirkugsbereich I
3. Tilgungsrechnung. 3.1. Tilgungsarten
 schreier@math.tu-freiberg.de 03731) 39 2261 3. Tilgugsrechug Die Tilgugsrechug beschäftigt sich mit der Rückzahlug vo Kredite, Darlehe ud Hypotheke. Dabei erwartet der Gläubiger, daß der Schulder seie
schreier@math.tu-freiberg.de 03731) 39 2261 3. Tilgugsrechug Die Tilgugsrechug beschäftigt sich mit der Rückzahlug vo Kredite, Darlehe ud Hypotheke. Dabei erwartet der Gläubiger, daß der Schulder seie
SUCHPROBLEME UND ALPHABETISCHE CODES
 SUCHPROBLEME UND ALPHABETISCHE CODES Der Problematik der alphabetische Codes liege Suchprobleme zugrude, dere Lösug dem iformatiostheoretische Problem der Fidug eies (optimale) alphabetische Codes gleich
SUCHPROBLEME UND ALPHABETISCHE CODES Der Problematik der alphabetische Codes liege Suchprobleme zugrude, dere Lösug dem iformatiostheoretische Problem der Fidug eies (optimale) alphabetische Codes gleich
15.4 Diskrete Zufallsvariablen
 .4 Diskrete Zufallsvariable Vo besoderem Iteresse sid Zufallsexperimete, bei dee die Ergebismege aus reelle Zahle besteht bzw. jedem Elemetarereigis eie reelle Zahl zugeordet werde ka. Solche Zufallsexperimet
.4 Diskrete Zufallsvariable Vo besoderem Iteresse sid Zufallsexperimete, bei dee die Ergebismege aus reelle Zahle besteht bzw. jedem Elemetarereigis eie reelle Zahl zugeordet werde ka. Solche Zufallsexperimet
K. Felten: Internet Network infrastucture Fachhochschule Kiel, Fachbereich IuE
 Defiitio ach DIN4004 Als Zuverlässigkeit ( reliability ) gilt die Fähigkeit eier Betrachtugseiheit ierhalb vorgegebeer Greze dejeige durch de Awedugszweck bedigte Aforderuge zu geüge, die a das Verhalte
Defiitio ach DIN4004 Als Zuverlässigkeit ( reliability ) gilt die Fähigkeit eier Betrachtugseiheit ierhalb vorgegebeer Greze dejeige durch de Awedugszweck bedigte Aforderuge zu geüge, die a das Verhalte
von solchen Abbildungen. Eine solche Folge bestimmt für jedes x M die Folge der Werte f n. Schreibt man dies noch einmal formal hin, so erhält man:
 Gleichmäßige Kovergez Wir betrachte im Folgede Abbilduge f : M N, wobei M eie Mege ud N ei metrischer Raum ist. Isbesodere iteressiere ud Folge f vo solche Abbilduge. Eie solche Folge bestimmt für jedes
Gleichmäßige Kovergez Wir betrachte im Folgede Abbilduge f : M N, wobei M eie Mege ud N ei metrischer Raum ist. Isbesodere iteressiere ud Folge f vo solche Abbilduge. Eie solche Folge bestimmt für jedes
Korrelationsanalyse zwischen kategorischen Merkmalen. Kontingenztabellen. Chi-Quadrat-Test
 Kotigeztabelle. Chi-Quadrat-Test Korrelatiosaalyse zwische kategorische Merkmale Beispiel 1 ohe Frau 8 75 1 Ma 48 49 97 76 14? Häufigkeitstabelle (Kotigeztabelle): eie tabellarische Darstellug der gemeisame
Kotigeztabelle. Chi-Quadrat-Test Korrelatiosaalyse zwische kategorische Merkmale Beispiel 1 ohe Frau 8 75 1 Ma 48 49 97 76 14? Häufigkeitstabelle (Kotigeztabelle): eie tabellarische Darstellug der gemeisame
Das konzernweite Sicherheitsprogramm der DB AG
 Systemverbud Bah Sicherheit im Bahbetrieb Das kozerweite Sicherheitsprogramm der DB AG Dipl.-Verwaltugsbetriebswirti, MBA, Susae Guli, Deutsche Bah AG, Sicherheit (TQS), ud Dipl.-Maschiebau-Ig. Thomas
Systemverbud Bah Sicherheit im Bahbetrieb Das kozerweite Sicherheitsprogramm der DB AG Dipl.-Verwaltugsbetriebswirti, MBA, Susae Guli, Deutsche Bah AG, Sicherheit (TQS), ud Dipl.-Maschiebau-Ig. Thomas
Testumfang für die Ermittlung und Angabe von Fehlerraten in biometrischen Systemen
 Testumfag für die Ermittlug ud Agabe vo Fehlerrate i biometrische Systeme Peter Uruh SRC Security Research & Cosultig GmbH peter.uruh@src-gmbh.de Eileitug Biometrische Systeme werde durch zwei wichtige
Testumfag für die Ermittlug ud Agabe vo Fehlerrate i biometrische Systeme Peter Uruh SRC Security Research & Cosultig GmbH peter.uruh@src-gmbh.de Eileitug Biometrische Systeme werde durch zwei wichtige
Kapitel 9 WAHRSCHEINLICHKEITS-RÄUME
 Kapitel 9 WAHRSCHEINLICHKEITS-RÄUME Fassug vom 13. Februar 2006 Mathematik für Humabiologe ud Biologe 129 9.1 Stichprobe-Raum 9.1 Stichprobe-Raum Die bisher behadelte Beispiele vo Naturvorgäge oder Experimete
Kapitel 9 WAHRSCHEINLICHKEITS-RÄUME Fassug vom 13. Februar 2006 Mathematik für Humabiologe ud Biologe 129 9.1 Stichprobe-Raum 9.1 Stichprobe-Raum Die bisher behadelte Beispiele vo Naturvorgäge oder Experimete
Beurteilung des Businessplans zur Tragfähigkeitsbescheinigung
 Fachkudige Stellugahme Beurteilug des Busiessplas zur Tragfähigkeitsbescheiigug Name Datum Has Musterma 7. Oktober 2015 Wilfried Orth Grüdugsberatug Stadort Würzburg: Stadort Stuttgart: Waldleite 9a Möhriger
Fachkudige Stellugahme Beurteilug des Busiessplas zur Tragfähigkeitsbescheiigug Name Datum Has Musterma 7. Oktober 2015 Wilfried Orth Grüdugsberatug Stadort Würzburg: Stadort Stuttgart: Waldleite 9a Möhriger
n 1,n 2,n 3,...,n k in der Stichprobe auftreten. Für die absolute Häufigkeit können wir auch die relative Häufigkeit einsetzen:
 61 6.2 Grudlage der mathematische Statistik 6.2.1 Eiführug i die mathematische Statistik I der mathematische Statistik behadel wir Masseerscheiuge. Wir habe es deshalb im Regelfall mit eier große Zahl
61 6.2 Grudlage der mathematische Statistik 6.2.1 Eiführug i die mathematische Statistik I der mathematische Statistik behadel wir Masseerscheiuge. Wir habe es deshalb im Regelfall mit eier große Zahl
Formularkonzept DRG. Druck. Ausgereifte Formularkonzepte. Die kompakte Dokumentation für Medizin und Pflege.
 Formularkozept DRG Ausgereifte Formularkozepte Die kompakte Dokumetatio für Medizi ud Pflege. Auf der Grudlage jahrzehtelager Erfahrug etwickel wir mit Ihe Formularsysteme, die alle Aforderuge gerecht
Formularkozept DRG Ausgereifte Formularkozepte Die kompakte Dokumetatio für Medizi ud Pflege. Auf der Grudlage jahrzehtelager Erfahrug etwickel wir mit Ihe Formularsysteme, die alle Aforderuge gerecht
beck-shop.de 2. Online-Marketing
 beck-shop.de 2. Olie-Marketig aa) Dateschutzrechtliche Eiwilligug immer erforderlich Ohe Eiwilligug des Nutzers ist eie Erhebug persoebezogeer Date icht zulässig. Eie derartige Eiwilligug ka auch icht
beck-shop.de 2. Olie-Marketig aa) Dateschutzrechtliche Eiwilligug immer erforderlich Ohe Eiwilligug des Nutzers ist eie Erhebug persoebezogeer Date icht zulässig. Eie derartige Eiwilligug ka auch icht
Statistik I Februar 2005
 Statistik I Februar 2005 Aufgabe 0 Pukte Ei Merkmal X mit de mögliche Auspräguge 0 ud, das im Folgede wie ei kardialskaliertes Merkmal behadelt werde ka, wird a Merkmalsträger beobachtet. Dabei bezeichet
Statistik I Februar 2005 Aufgabe 0 Pukte Ei Merkmal X mit de mögliche Auspräguge 0 ud, das im Folgede wie ei kardialskaliertes Merkmal behadelt werde ka, wird a Merkmalsträger beobachtet. Dabei bezeichet
Löslichkeitsdiagramm. Grundlagen
 Grudlage Löslichkeitsdiagramm Grudlage Zur etrachtug des Mischugsverhaltes icht vollstädig mischbarer Flüssigkeite, das heißt Flüssigkeite, die sich icht bei jeder Temperatur i alle Megeverhältisse miteiader
Grudlage Löslichkeitsdiagramm Grudlage Zur etrachtug des Mischugsverhaltes icht vollstädig mischbarer Flüssigkeite, das heißt Flüssigkeite, die sich icht bei jeder Temperatur i alle Megeverhältisse miteiader
Parameter von Häufigkeitsverteilungen
 Kapitel 3 Parameter vo Häufigkeitsverteiluge 3. Mittelwerte Mo Der Modus (:= häufigster Wert, Abk.: Mo) ist der Merkmalswert mit der größte Häufigkeit, falls es eie solche gibt. Er sollte ur bei eigipflige
Kapitel 3 Parameter vo Häufigkeitsverteiluge 3. Mittelwerte Mo Der Modus (:= häufigster Wert, Abk.: Mo) ist der Merkmalswert mit der größte Häufigkeit, falls es eie solche gibt. Er sollte ur bei eigipflige
Kunde. Kontobewegung
 Techische Uiversität Müche WS 2003/04, Fakultät für Iformatik Datebaksysteme I Prof. R. Bayer, Ph.D. Lösugsblatt 4 Dipl.-Iform. Michael Bauer Dr. Gabi Höflig 17.11. 2003 Abbildug E/R ach relatioal - Beispiel:
Techische Uiversität Müche WS 2003/04, Fakultät für Iformatik Datebaksysteme I Prof. R. Bayer, Ph.D. Lösugsblatt 4 Dipl.-Iform. Michael Bauer Dr. Gabi Höflig 17.11. 2003 Abbildug E/R ach relatioal - Beispiel:
Kapitel 5: Schließende Statistik
 Kapitel 5: Schließede Statistik Statistik, Prof. Dr. Kari Melzer 5. Schließede Statistik: Typische Fragestellug ahad vo Beispiele Beispiel Aus 5 Messwerte ergebe sich für die Reißfestigkeit eier Garsorte
Kapitel 5: Schließede Statistik Statistik, Prof. Dr. Kari Melzer 5. Schließede Statistik: Typische Fragestellug ahad vo Beispiele Beispiel Aus 5 Messwerte ergebe sich für die Reißfestigkeit eier Garsorte
Internet-Zahlungsverfahren aus Sicht der Händler: Ergebnisse der Umfrage IZH5
 Iteret- aus Sicht der Hädler: Ergebisse der Umfrage IZH5 Vorab-Kurzauswertug ausgewählter Aspekte Dezember 2009 1 Gegestad ud ausgewählte Ergebisse der Studie Mit der aktuelle füfte Umfragewelle zum Thema
Iteret- aus Sicht der Hädler: Ergebisse der Umfrage IZH5 Vorab-Kurzauswertug ausgewählter Aspekte Dezember 2009 1 Gegestad ud ausgewählte Ergebisse der Studie Mit der aktuelle füfte Umfragewelle zum Thema
1741 SWITZERLAND EQUAL WEIGHTED INDEX
 1741 Switzerlad Idex Series 1741 SWITZERLAND EQUAL WEIGHTED INDEX Reglemet Versio vom 01.07.2015 1741 Switzerlad Equal Weighted Idex 2 INHALTSVERZEICHNIS 1 Eileitug 3 2 Idex Spezifikatioe 4 3 Idex Uiversum
1741 Switzerlad Idex Series 1741 SWITZERLAND EQUAL WEIGHTED INDEX Reglemet Versio vom 01.07.2015 1741 Switzerlad Equal Weighted Idex 2 INHALTSVERZEICHNIS 1 Eileitug 3 2 Idex Spezifikatioe 4 3 Idex Uiversum
3 Die Außenfinanzierung durch Fremdkapital (Kreditfinanzierung)
 3 Die Außefiazierug durch Fremdkapital (Kreditfiazierug) 3.1 Die Charakteristika ud Forme der Kreditfiazierug Aufgabe 3.1: Idealtypische Eigeschafte vo Eige- ud Fremdkapital Stelle Sie die idealtypische
3 Die Außefiazierug durch Fremdkapital (Kreditfiazierug) 3.1 Die Charakteristika ud Forme der Kreditfiazierug Aufgabe 3.1: Idealtypische Eigeschafte vo Eige- ud Fremdkapital Stelle Sie die idealtypische
Model CreditRisk + : The Economic Perspective of Portfolio Credit Risk Part I
 Model CreditRisk + : The Ecoomic Perspective of Portfolio Credit Risk Part I Semiar: Portfolio Credit Risk Istructor: Rafael Weißbach Speaker: Pablo Kimmig Ageda 1. Asatz ud Ziele Was ist CreditRisk +
Model CreditRisk + : The Ecoomic Perspective of Portfolio Credit Risk Part I Semiar: Portfolio Credit Risk Istructor: Rafael Weißbach Speaker: Pablo Kimmig Ageda 1. Asatz ud Ziele Was ist CreditRisk +
Evaluierung einer Schulungsmaßnahme: Punktezahl vor der Schulung Punktezahl nach der Schulung. Autoritarismusscore vor/nach Projekt
 2.4.5 Gauss-Test ud t-test für verbudee Stichprobe 2.4.5.8 Zum Begriff der verbudee Stichprobe Verbudee Stichprobe: Vergleich zweier Merkmale X ud Y, die jetzt a deselbe Persoe erhobe werde. Vorsicht:
2.4.5 Gauss-Test ud t-test für verbudee Stichprobe 2.4.5.8 Zum Begriff der verbudee Stichprobe Verbudee Stichprobe: Vergleich zweier Merkmale X ud Y, die jetzt a deselbe Persoe erhobe werde. Vorsicht:
Gliederung. Value-at-Risk
 Value-at-Risk Dr. Richard Herra Nürberg, 4. Noveber 26 IVS-Foru Gliederug Modell Beispiel aus der betriebliche Altersversorgug Verteilug des Gesatschades Value-at-Risk ud Tail Value-at-Risk Risikobeurteilug
Value-at-Risk Dr. Richard Herra Nürberg, 4. Noveber 26 IVS-Foru Gliederug Modell Beispiel aus der betriebliche Altersversorgug Verteilug des Gesatschades Value-at-Risk ud Tail Value-at-Risk Risikobeurteilug
ICD-Aggregatwechsel Auswertung 2014 Modul 09/5
 Bayerische Arbeitsgemeischaft für Qualitätssicherug i der statioäre Versorgug ICD-Aggregatwechsel Auswertug Modul 9/5 ICD-Aggregatwechsel Ihalt» Ihaltsverzeichis 1 Basisstatistik 1 Patiete 2 Idikatio 3
Bayerische Arbeitsgemeischaft für Qualitätssicherug i der statioäre Versorgug ICD-Aggregatwechsel Auswertug Modul 9/5 ICD-Aggregatwechsel Ihalt» Ihaltsverzeichis 1 Basisstatistik 1 Patiete 2 Idikatio 3
Testen statistischer Hypothesen
 Kapitel 9 Teste statistischer Hypothese 9.1 Eiführug, Sigifiaztests Sigifiaztest für µ bei der ormalverteilug bei beatem σ = : X i seie uabhägig ud µ, ) verteilt, µ sei ubeat. Stelle eie Hypothese über
Kapitel 9 Teste statistischer Hypothese 9.1 Eiführug, Sigifiaztests Sigifiaztest für µ bei der ormalverteilug bei beatem σ = : X i seie uabhägig ud µ, ) verteilt, µ sei ubeat. Stelle eie Hypothese über
2.2.1 Lagemaße. Exkurs: Quantile. und n. p n
 Ekurs: Quatile Ausgagspukt : Geordete Urliste Jeder Wert p, mit 0 < p
Ekurs: Quatile Ausgagspukt : Geordete Urliste Jeder Wert p, mit 0 < p
Der natürliche Werkstoff Holz - Statistische Betrachtungen zum uniaxialen Zugversuch am Beispiel von Furnier
 Der atürliche Werkstoff Holz - Statistische Betrachtuge zum uiaxiale Zugversuch am Beispiel vo Furier B. Bellair, A. Dietzel, M. Zimmerma, Prof. Dr.-Ig. H. Raßbach Zusammefassug FH Schmalkalde, 98574 Schmalkalde,
Der atürliche Werkstoff Holz - Statistische Betrachtuge zum uiaxiale Zugversuch am Beispiel vo Furier B. Bellair, A. Dietzel, M. Zimmerma, Prof. Dr.-Ig. H. Raßbach Zusammefassug FH Schmalkalde, 98574 Schmalkalde,
Statistik I/Empirie I
 Vor zwei Jahre wurde ermittelt, dass Elter im Durchschitt 96 Euro für die Nachhilfe ihrer schulpflichtige Kider ausgebe. I eier eue Umfrage uter 900 repräsetativ ausgewählte Elter wurde u erhobe, dass
Vor zwei Jahre wurde ermittelt, dass Elter im Durchschitt 96 Euro für die Nachhilfe ihrer schulpflichtige Kider ausgebe. I eier eue Umfrage uter 900 repräsetativ ausgewählte Elter wurde u erhobe, dass
Kontingenztabellen. Chi-Quadrat-Test. Korrelationsanalyse zwischen kategorischen Merkmalen. 1. Unabhängigkeitstest
 Kotigeztabelle. Chi-Quadrat-Test KAD 1.11. 1. Uabhägigkeitstest. Apassugstest. Homogeitätstest Beispiel 1 ohe Frau 8 75 1 Ma 48 49 97 76 14? Korrelatiosaalyse zwische kategorische Merkmale Häufigkeitstabelle
Kotigeztabelle. Chi-Quadrat-Test KAD 1.11. 1. Uabhägigkeitstest. Apassugstest. Homogeitätstest Beispiel 1 ohe Frau 8 75 1 Ma 48 49 97 76 14? Korrelatiosaalyse zwische kategorische Merkmale Häufigkeitstabelle
Bei 95%iger Konfidenz wäre der Mittelwert der GG zwischen 1421,17DM und 1778,83DM zu erwarten.
 Aufgabe 36 (S. 346: Schätzverfahre für Mittelwert ud Stadardabweichug a Puktschätzuge für µ aufgrud der Werte der kleie Stichprobe aus Aufgabe 3 Bei eier Puktschätzug wird für de zu schätzede Parameter
Aufgabe 36 (S. 346: Schätzverfahre für Mittelwert ud Stadardabweichug a Puktschätzuge für µ aufgrud der Werte der kleie Stichprobe aus Aufgabe 3 Bei eier Puktschätzug wird für de zu schätzede Parameter
Beschreibende Statistik Kenngrößen in der Übersicht (Ac)
 Beschreibede Statistik Kegröße i der Übersicht (Ac) Im folgede wird die Berechugsweise des TI 83 (sowie vo SPSS, s. ute) verwedet. Diese geht auf eie Festlegug vo Moore ud McCabe (00) zurück. I der Literatur
Beschreibede Statistik Kegröße i der Übersicht (Ac) Im folgede wird die Berechugsweise des TI 83 (sowie vo SPSS, s. ute) verwedet. Diese geht auf eie Festlegug vo Moore ud McCabe (00) zurück. I der Literatur
Sichtbar im Web! Websites für Handwerksbetriebe. Damit Sie auch online gefunden werden.
 Sichtbar im Web! Websites für Hadwerksbetriebe. Damit Sie auch olie gefude werde. Professioelles Webdesig für: Hadwerksbetriebe Rudum-sorglos-Pakete Nur für Hadwerksbetriebe Webdesig zu Festpreise - ukompliziert
Sichtbar im Web! Websites für Hadwerksbetriebe. Damit Sie auch olie gefude werde. Professioelles Webdesig für: Hadwerksbetriebe Rudum-sorglos-Pakete Nur für Hadwerksbetriebe Webdesig zu Festpreise - ukompliziert
Aktueller Status hinsichtlich der angekündigten Kursgewinnsteuer
 ÄNDERUNGEN IM JAHR 2011 Aktueller Status hisichtlich der ageküdigte Kursgewisteuer Abei möchte wir Sie über wesetliche Ihalte aus der Regierugsvorlage Budgetbegleitgesetz 2011-2014 vom 30.11.2010 zur Kursgewibesteuerug
ÄNDERUNGEN IM JAHR 2011 Aktueller Status hisichtlich der ageküdigte Kursgewisteuer Abei möchte wir Sie über wesetliche Ihalte aus der Regierugsvorlage Budgetbegleitgesetz 2011-2014 vom 30.11.2010 zur Kursgewibesteuerug
Leitfaden zum. Bondm-Index
 Leitfade zum Bodm-Idex Versio 1.0 vom 01. September 2011 1 Ihalt Eiführug 1 Parameter des Idex 1.1 Kürzel ud ISIN 1.2 Startwert 1.3 Verteilug 1.4 Preise ud Berechugsfrequez 1.5 Gewichtug 1.6 Idex-Komitee
Leitfade zum Bodm-Idex Versio 1.0 vom 01. September 2011 1 Ihalt Eiführug 1 Parameter des Idex 1.1 Kürzel ud ISIN 1.2 Startwert 1.3 Verteilug 1.4 Preise ud Berechugsfrequez 1.5 Gewichtug 1.6 Idex-Komitee
Wirtschaftsmathematik
 Studiegag Betriebswirtschaft Fach Wirtschaftsmathematik Art der Leistug Studieleistug Klausur-Kz. BW-WMT-S1 040508 Datum 08.05.004 Bezüglich der Afertigug Ihrer Arbeit sid folgede Hiweise verbidlich: Verwede
Studiegag Betriebswirtschaft Fach Wirtschaftsmathematik Art der Leistug Studieleistug Klausur-Kz. BW-WMT-S1 040508 Datum 08.05.004 Bezüglich der Afertigug Ihrer Arbeit sid folgede Hiweise verbidlich: Verwede
Statistik Einführung // Konfidenzintervalle für einen Parameter 7 p.2/39
 Statistik Eiführug Kofidezitervalle für eie Parameter Kapitel 7 Statistik WU Wie Gerhard Derfliger Michael Hauser Jörg Leeis Josef Leydold Güter Tirler Rosmarie Wakolbiger Statistik Eiführug // Kofidezitervalle
Statistik Eiführug Kofidezitervalle für eie Parameter Kapitel 7 Statistik WU Wie Gerhard Derfliger Michael Hauser Jörg Leeis Josef Leydold Güter Tirler Rosmarie Wakolbiger Statistik Eiführug // Kofidezitervalle
Aufgabe 1: Funktionale Modellierungen
 Didaktik des Sachreches (Sek. I) Übugsblatt 4 Dr. Astrid Brikma Name, Vorame: Matrikelummer: Doppelte Lösuge führe zum Verlust aller Pukte beider Persoe-Gruppe. Die Lösuge sid hadschriftlich abzugebe.
Didaktik des Sachreches (Sek. I) Übugsblatt 4 Dr. Astrid Brikma Name, Vorame: Matrikelummer: Doppelte Lösuge führe zum Verlust aller Pukte beider Persoe-Gruppe. Die Lösuge sid hadschriftlich abzugebe.
Empirische Methoden I
 Hochschule für Wirtschaft ud 2012 Umwelt Nürtige-Geislige Fakultät Betriebswirtschaft ud Iteratioale Fiaze Prof. Dr. Max C. Wewel Prof. Dr. Corelia Niederdrek-Felger Aufgabe zum Tutorium Empirische Methode
Hochschule für Wirtschaft ud 2012 Umwelt Nürtige-Geislige Fakultät Betriebswirtschaft ud Iteratioale Fiaze Prof. Dr. Max C. Wewel Prof. Dr. Corelia Niederdrek-Felger Aufgabe zum Tutorium Empirische Methode
Praktikum Vorbereitung Fertigungsmesstechnik Statistische Qualitätskontrolle
 Praktikum Vorbereitug Fertigugsmesstechik Statistische Qualitätskotrolle Bei viele Erzeugisse ist es icht möglich jedes Werkstück zu prüfe, z.b.: bei Massefertigug. Hier ist es aus ökoomische Grüde icht
Praktikum Vorbereitug Fertigugsmesstechik Statistische Qualitätskotrolle Bei viele Erzeugisse ist es icht möglich jedes Werkstück zu prüfe, z.b.: bei Massefertigug. Hier ist es aus ökoomische Grüde icht
Ambulante psychotherapeutische Versorgung Ergebnisse einer empirischen Analyse von Krankenkassendaten
 Ambulate psychotherapeutische Versorgug Ergebisse eier empirische Aalyse vo Krakekassedate Peter Lehdorfer Kider- ud Jugedlichepsychotherapeut Vizepräsidet der Budespsychotherapeutekammer 3. Workshop:
Ambulate psychotherapeutische Versorgug Ergebisse eier empirische Aalyse vo Krakekassedate Peter Lehdorfer Kider- ud Jugedlichepsychotherapeut Vizepräsidet der Budespsychotherapeutekammer 3. Workshop:
, n -% &. & / 0 ( n 1 2 n 3 % & 4 5" % & " # ( 2 & ' )**+
 !"# $!%& & '( , -%&.& /0 ( 12 3%&45"%&"#( 2 & & &6, #.&- 7%& / -%&0 8 -% 1%& 6 $ 1%&"(!!! "!#$!#$!#%!#% &' %&%&"(9& %&($( :&($ 1(;4( ( ')* *+, &# -5-4 211,4?@?)*) 7 A& %& -.+///(.0+/// 8 B&
!"# $!%& & '( , -%&.& /0 ( 12 3%&45"%&"#( 2 & & &6, #.&- 7%& / -%&0 8 -% 1%& 6 $ 1%&"(!!! "!#$!#$!#%!#% &' %&%&"(9& %&($( :&($ 1(;4( ( ')* *+, &# -5-4 211,4?@?)*) 7 A& %& -.+///(.0+/// 8 B&
2 Wahl des Betriebsrats
 2 Wahl des Betriebsrats Übersicht R R Stadardprobleme aus diesem Kapitel 1 1. Wer ist wahlberechtigt?.. 1 2. Soderküdigugsschutz bei Wahle.... 2 3. Afechtug ud Nichtigkeit vo Betriebsratswahle.... 3 4.
2 Wahl des Betriebsrats Übersicht R R Stadardprobleme aus diesem Kapitel 1 1. Wer ist wahlberechtigt?.. 1 2. Soderküdigugsschutz bei Wahle.... 2 3. Afechtug ud Nichtigkeit vo Betriebsratswahle.... 3 4.
Höhere Finanzmathematik. Sehr ausführliches Themenheft (d. h. mit Theorie) Aber auch mit vielen Trainingsaufgaben
 Expoetielles Wachstum Höhere Fiazmathematik Sehr ausführliches Themeheft (d. h. mit Theorie) Aber auch mit viele Traiigsaufgabe Es hadelt sich um eie Awedug vo Expoetialfuktioe (Wachstumsfuktioe) Datei
Expoetielles Wachstum Höhere Fiazmathematik Sehr ausführliches Themeheft (d. h. mit Theorie) Aber auch mit viele Traiigsaufgabe Es hadelt sich um eie Awedug vo Expoetialfuktioe (Wachstumsfuktioe) Datei
Versuch 1/1 POISSON STATISTIK Blatt 1 POISSON STATISTIK. 1. Vorbemerkung
 Versuch 1/1 POISSON STATISTIK Blatt 1 POISSON STATISTIK Physikalische Prozesse, die eier statistische Gesetzmäßigkeit uterworfe sid, lasse sich mit eier Verteilugsfuktio beschreibe. Die Gauß-Verteilug
Versuch 1/1 POISSON STATISTIK Blatt 1 POISSON STATISTIK Physikalische Prozesse, die eier statistische Gesetzmäßigkeit uterworfe sid, lasse sich mit eier Verteilugsfuktio beschreibe. Die Gauß-Verteilug
Das FSB Geldkonto. Einfache Abwicklung und attraktive Verzinsung. +++ Verzinsung aktuell bis zu 3,7% p.a. +++
 Das FSB Geldkoto Eifache Abwicklug ud attraktive Verzisug +++ Verzisug aktuell bis zu 3,7% p.a. +++ zuverlässig servicestark bequem Kompeteter Parter für Ihr Wertpapiergeschäft Die FodsServiceBak zählt
Das FSB Geldkoto Eifache Abwicklug ud attraktive Verzisug +++ Verzisug aktuell bis zu 3,7% p.a. +++ zuverlässig servicestark bequem Kompeteter Parter für Ihr Wertpapiergeschäft Die FodsServiceBak zählt
Practice Produktion & SCM
 Practice Produktio & SCM Lieferateworkshops als Ausgagspukt der Gestaltug uterehmesübergreifeder Teileversorgugssysteme Etwurf eies strukturierte Asatzes zur Aalyse kritischer Erfolgsfaktore der uterehmesübergreifede
Practice Produktio & SCM Lieferateworkshops als Ausgagspukt der Gestaltug uterehmesübergreifeder Teileversorgugssysteme Etwurf eies strukturierte Asatzes zur Aalyse kritischer Erfolgsfaktore der uterehmesübergreifede
Linsengesetze und optische Instrumente
 Lisegesetze ud optische Istrumete Gruppe X Xxxx Xxxxxxxxx Xxxxxxx Xxxxxx Mat.-Nr.: XXXXX Mat.-Nr.: XXXXX XX.XX.XX Theorie Im olgede werde wir eie kurze Überblick über die Fuktio, de Aubau ud die Arte vo
Lisegesetze ud optische Istrumete Gruppe X Xxxx Xxxxxxxxx Xxxxxxx Xxxxxx Mat.-Nr.: XXXXX Mat.-Nr.: XXXXX XX.XX.XX Theorie Im olgede werde wir eie kurze Überblick über die Fuktio, de Aubau ud die Arte vo
5 Bernoulli-Kette. 5.1 Bernoulli-Experiment. Jakob Bernoulli 1654-1705 Schweizer Mathematiker und Physiker. 5.1.1 Einleitung
 Seite vo 7 5 Beroulli-Kette Jakob Beroulli 654-705 Schweizer Mathematiker ud Physiker 5. Beroulli-Exerimet 5.. Eileitug Oft iteressiert ma sich bei Zufallsexerimete icht für die eizele Ergebisse, soder
Seite vo 7 5 Beroulli-Kette Jakob Beroulli 654-705 Schweizer Mathematiker ud Physiker 5. Beroulli-Exerimet 5.. Eileitug Oft iteressiert ma sich bei Zufallsexerimete icht für die eizele Ergebisse, soder
IWW Studienprogramm. Aufbaustudium. Gründungscontrolling. Lösungshinweise zur 3. Musterklausur
 Istitut für Wirtschaftswisseschaftliche Forschug ud Weiterbildug GmbH Istitut a der FerUiversität i Hage IWW Studieprogramm Aufbaustudium Grüdugscotrollig Lösugshiweise zur 3. Musterklausur Lösugshiweise
Istitut für Wirtschaftswisseschaftliche Forschug ud Weiterbildug GmbH Istitut a der FerUiversität i Hage IWW Studieprogramm Aufbaustudium Grüdugscotrollig Lösugshiweise zur 3. Musterklausur Lösugshiweise
Auch im Risikofall ist das Entscheidungsproblem gelöst, wenn eine dominante Aktion in A existiert.
 Prof. Dr. H. Rommelfager: Etscheidugstheorie, Kaitel 3 7 3. Etscheidug bei Risiko (subjektive oder objektive) Eitrittswahrscheilichkeite für das Eitrete der mögliche Umweltzustäde köe vom Etscheidugsträger
Prof. Dr. H. Rommelfager: Etscheidugstheorie, Kaitel 3 7 3. Etscheidug bei Risiko (subjektive oder objektive) Eitrittswahrscheilichkeite für das Eitrete der mögliche Umweltzustäde köe vom Etscheidugsträger
Die Instrumente des Personalmanagements
 15 2 Die Istrumete des Persoalmaagemets Zur Lerorietierug Sie solle i der Lage sei:! die Ziele, Asätze ud Grüde eier systematische Persoalplaug darzulege;! die Istrumete der Persoalplaug zu differeziere;!
15 2 Die Istrumete des Persoalmaagemets Zur Lerorietierug Sie solle i der Lage sei:! die Ziele, Asätze ud Grüde eier systematische Persoalplaug darzulege;! die Istrumete der Persoalplaug zu differeziere;!
Die Forschungsdatenbank zu Inschriften/Scans/Bildern im. Institut für Urchristentum und Antike
 Gebhard Dettmar Istitut für Urchristetum ud Atike www2.hu-berli.de/ura Die Forschugsdatebak zu Ischrifte/Scas/Bilder im Istitut für Urchristetum ud Atike Eie Etwurfsdokumetatio zum Datebaketwurf ach dem
Gebhard Dettmar Istitut für Urchristetum ud Atike www2.hu-berli.de/ura Die Forschugsdatebak zu Ischrifte/Scas/Bilder im Istitut für Urchristetum ud Atike Eie Etwurfsdokumetatio zum Datebaketwurf ach dem
3 Kritischer Bereich zum Niveau α = 0.10: K = (χ 2 k 1;1 α, + ) = (χ2 5;0.90, + ) = (9.236, + ) 4 Berechnung der realisierten Teststatistik:
 8 Apassugs- ud Uabhägigkeitstests Chi-Quadrat-Apassugstest 81 Beispiel: p-wert bei Chi-Quadrat-Apassugstest (Grafik) Auftragseigagsbeispiel, realisierte Teststatistik χ 2 1275, p-wert: 168 8 Apassugs-
8 Apassugs- ud Uabhägigkeitstests Chi-Quadrat-Apassugstest 81 Beispiel: p-wert bei Chi-Quadrat-Apassugstest (Grafik) Auftragseigagsbeispiel, realisierte Teststatistik χ 2 1275, p-wert: 168 8 Apassugs-
Beispiel: p-wert bei Chi-Quadrat-Anpassungstest (Grafik) Auftragseingangsbeispiel, realisierte Teststatistik χ 2 = , p-wert: 0.
 8 Apassugs- ud Uabhägigkeitstests Chi-Quadrat-Apassugstest 81 Beispiel: p-wert bei Chi-Quadrat-Apassugstest (Grafik) Auftragseigagsbeispiel, realisierte Teststatistik χ 2 = 12075, p-wert: 00168 f χ 2 (4)
8 Apassugs- ud Uabhägigkeitstests Chi-Quadrat-Apassugstest 81 Beispiel: p-wert bei Chi-Quadrat-Apassugstest (Grafik) Auftragseigagsbeispiel, realisierte Teststatistik χ 2 = 12075, p-wert: 00168 f χ 2 (4)
Es werden 120 Schüler befragt, ob sie ein Handy besitzen. Das Ergebnis der Umfrage lautet: Von 120 Schülern besitzen 99 ein Handy.
 Vo der relative Häufigkeit zur Wahrscheilichkeit Es werde 20 Schüler befragt, ob sie ei Hady besitze. Das Ergebis der Umfrage lautet: Vo 20 Schüler besitze 99 ei Hady. Ereigis E: Schüler besitzt ei Hady
Vo der relative Häufigkeit zur Wahrscheilichkeit Es werde 20 Schüler befragt, ob sie ei Hady besitze. Das Ergebis der Umfrage lautet: Vo 20 Schüler besitze 99 ei Hady. Ereigis E: Schüler besitzt ei Hady
Wissenschaftliches Arbeiten Studiengang Energiewirtschaft
 Wisseschaftliches Arbeite Studiegag Eergiewirtschaft - Auswerte vo Date - Prof. Dr. Ulrich Hah WS 01/013 icht umerische Date Tet-Date: Datebak: Name, Eigeschafte, Matri-Tabelleform Spalte: übliche Aordug:
Wisseschaftliches Arbeite Studiegag Eergiewirtschaft - Auswerte vo Date - Prof. Dr. Ulrich Hah WS 01/013 icht umerische Date Tet-Date: Datebak: Name, Eigeschafte, Matri-Tabelleform Spalte: übliche Aordug:
A/D UND D/A WANDLER. 1. Einleitung
 A/D UND D/A WANDLER. Eileitug Zur Umwadlug physikalischer Größe, beispielsweise i eie Spaug, werde Wadlerbausteie - auch allgemei Sigalumsetzer geat- beötigt. Ei Sesor liefert ei aaloges Sigal, das i geeigeter
A/D UND D/A WANDLER. Eileitug Zur Umwadlug physikalischer Größe, beispielsweise i eie Spaug, werde Wadlerbausteie - auch allgemei Sigalumsetzer geat- beötigt. Ei Sesor liefert ei aaloges Sigal, das i geeigeter
Meine Rechte und Pflichten als Vater
 Beck-Rechtsberater im dtv 50756 Meie Rechte ud Pflichte als Vater Vaterschaft - Sorgerecht - Umgag - Namesrecht - Uterhaltsfrage - Erbrechtliche ud Steuerrechtliche Frage vo Dr. Beate Weritzig 2. Auflage
Beck-Rechtsberater im dtv 50756 Meie Rechte ud Pflichte als Vater Vaterschaft - Sorgerecht - Umgag - Namesrecht - Uterhaltsfrage - Erbrechtliche ud Steuerrechtliche Frage vo Dr. Beate Weritzig 2. Auflage
Leitfaden zum Photovoltaik Global 30 Index *
 Lefade zum Photovoltaik Global 30 Idex * Versio.0 * Photovoltaik Global 30 Idex ist ei Idex der ABN AMRO, der vo der Deutsche Börse berechet ud verteilt wird. Deutsche Börse AG Versio.0 Lefade zum Photovoltaik
Lefade zum Photovoltaik Global 30 Idex * Versio.0 * Photovoltaik Global 30 Idex ist ei Idex der ABN AMRO, der vo der Deutsche Börse berechet ud verteilt wird. Deutsche Börse AG Versio.0 Lefade zum Photovoltaik
Glücksspielverhalten in Bayern
 Glücksspielverhalte i Bayer 1 Zielsetzug Schätzuge aus Bevölkerugsstudie zu Glücksspiel i Deutschlad zu Folge habe um die 70% der Deutsche scho eimal gespielt (Bühriger, Kraus, Sotag, Pfeiffer-Gerschel,
Glücksspielverhalte i Bayer 1 Zielsetzug Schätzuge aus Bevölkerugsstudie zu Glücksspiel i Deutschlad zu Folge habe um die 70% der Deutsche scho eimal gespielt (Bühriger, Kraus, Sotag, Pfeiffer-Gerschel,
... a ik) i=1...m, k=1...n A = = ( a mn
 Zurück Stad: 4..6 Reche mit Matrize I der Mathematik bezeichet ma mit Matrix im Allgemeie ei rechteckiges Zahleschema. I der allgemeie Darstellug habe die Zahle zwei Idizes, de erste für die Zeileummer,
Zurück Stad: 4..6 Reche mit Matrize I der Mathematik bezeichet ma mit Matrix im Allgemeie ei rechteckiges Zahleschema. I der allgemeie Darstellug habe die Zahle zwei Idizes, de erste für die Zeileummer,
PFLEGERECHT. BAGS-Kollektivvertrag im Mischbetrieb. Zuwendungen zu Ersatzpflege-Kosten. Unterbringung: offen versus geschlossen
 Schriftleitug: Marti Greifeeder ud Klaus Mayr 2/2011 Österreichische Zeitschrift für PFLEGERECHT Zeitschrift für die Heim- ud Pflegepraxis ud Krakeastalte GuKG, Arbeitsrecht & Astalterecht BAGS-Kollektivvertrag
Schriftleitug: Marti Greifeeder ud Klaus Mayr 2/2011 Österreichische Zeitschrift für PFLEGERECHT Zeitschrift für die Heim- ud Pflegepraxis ud Krakeastalte GuKG, Arbeitsrecht & Astalterecht BAGS-Kollektivvertrag
SQL. Grundlagen und Datenbankdesign. Elmar Fuchs. 2. Ausgabe, April 2012 SQL
 SQL Elmar Fuchs 2. Ausgabe, April 202 Grudlage ud Datebakdesig SQL 3 SQL - Grudlage ud Datebakdesig 3 Der Datebaketwurf I diesem Kapitel erfahre Sie wie sich der Datebak-Lebeszyklus vollzieht welche Etwurfsphase
SQL Elmar Fuchs 2. Ausgabe, April 202 Grudlage ud Datebakdesig SQL 3 SQL - Grudlage ud Datebakdesig 3 Der Datebaketwurf I diesem Kapitel erfahre Sie wie sich der Datebak-Lebeszyklus vollzieht welche Etwurfsphase
2 Vollständige Induktion
 8 I. Zahle, Kovergez ud Stetigkeit Vollstädige Iduktio Aufgabe: 1. Bereche Sie 1+3, 1+3+5 ud 1+3+5+7, leite Sie eie allgemeie Formel für 1+3+ +( 3)+( 1) her ud versuche Sie, diese zu beweise.. Eizu5% ZiseproJahragelegtes
8 I. Zahle, Kovergez ud Stetigkeit Vollstädige Iduktio Aufgabe: 1. Bereche Sie 1+3, 1+3+5 ud 1+3+5+7, leite Sie eie allgemeie Formel für 1+3+ +( 3)+( 1) her ud versuche Sie, diese zu beweise.. Eizu5% ZiseproJahragelegtes
Kapitel 6: Statistische Qualitätskontrolle
 Kapitel 6: Statistische Qualitätskotrolle 6. Allgemeies Für die Qualitätskotrolle i eiem Uterehme (produzieredes Gewerbe, Diestleistugsuterehme, ) gibt es verschiedee Möglichkeite. Statistische Prozesskotrolle
Kapitel 6: Statistische Qualitätskotrolle 6. Allgemeies Für die Qualitätskotrolle i eiem Uterehme (produzieredes Gewerbe, Diestleistugsuterehme, ) gibt es verschiedee Möglichkeite. Statistische Prozesskotrolle
6. Ausbildungszeit. 6.1 Ausbildungsdauer. 6.2 Probezeit. Verkürzung oder Verlängerung der Probezeit
 Probezeit 6. Ausbildugszeit 6.1 Ausbildugsdauer Die Gesamtdauer der Ausbildug soll, so 25 Abs. 2 Nr. 2 BBiG ud 25 Abs. 2 Nr. 2 HWO, ach Möglichkeit icht weiger als zwei Jahre ud icht mehr als drei Jahre
Probezeit 6. Ausbildugszeit 6.1 Ausbildugsdauer Die Gesamtdauer der Ausbildug soll, so 25 Abs. 2 Nr. 2 BBiG ud 25 Abs. 2 Nr. 2 HWO, ach Möglichkeit icht weiger als zwei Jahre ud icht mehr als drei Jahre
Mathematische Probleme, SS 2015 Donnerstag $Id: convex.tex,v /05/21 18:28:20 hk Exp $
 $Id: covex.tex,v 1.18 2015/05/21 18:28:20 hk Exp $ 3 Kovexgeometrie 3.2 Die platoische Körper Ei platoischer Körper vo Typ (, m) ist ei kovexer Polyeder desse Seitefläche alle gleichseitige -Ecke ud i
$Id: covex.tex,v 1.18 2015/05/21 18:28:20 hk Exp $ 3 Kovexgeometrie 3.2 Die platoische Körper Ei platoischer Körper vo Typ (, m) ist ei kovexer Polyeder desse Seitefläche alle gleichseitige -Ecke ud i
Inhaltsverzeichnis. 1 Leistungsbeschreibung... 3
 FIBU Kosterechug Ihaltsverzeichis 1 Leistugsbeschreibug... 3 2 Highlights... 4 2.1 Variable oder fixe Kostestelleverteilug... 4 2.2 Mehrstufiges Umlageverfahre... 5 2.3 Kosolidierugsebee für die Wertekotrolle...
FIBU Kosterechug Ihaltsverzeichis 1 Leistugsbeschreibug... 3 2 Highlights... 4 2.1 Variable oder fixe Kostestelleverteilug... 4 2.2 Mehrstufiges Umlageverfahre... 5 2.3 Kosolidierugsebee für die Wertekotrolle...
PrivatKredit. Direkt ans Ziel Ihrer Wünsche
 PrivatKredit Direkt as Ziel Ihrer Wüsche Erlebe Sie eue Freiräume. Leiste Sie sich, was Ihe wichtig ist. Sie träume scho seit lagem vo eier eue Aschaffug, wie z. B.: eiem eue Auto eue Möbel Oder es stehe
PrivatKredit Direkt as Ziel Ihrer Wüsche Erlebe Sie eue Freiräume. Leiste Sie sich, was Ihe wichtig ist. Sie träume scho seit lagem vo eier eue Aschaffug, wie z. B.: eiem eue Auto eue Möbel Oder es stehe
6 Folgen. 6.4 Folgen reeller Zahlen. Mathematik für Informatiker B, SS 2012 Dienstag 5.6. $Id: folgen.tex,v /06/05 11:12:18 hk Exp $
 Mathematik für Iformatiker B, SS 0 Diestag 5.6 $Id: folge.tex,v. 0/06/05 ::8 hk Exp $ 6 Folge 6.4 Folge reeller Zahle I der letzte Sitzug habe wir de Begriff des Grezwerts eier Folge i eiem metrische Raum
Mathematik für Iformatiker B, SS 0 Diestag 5.6 $Id: folge.tex,v. 0/06/05 ::8 hk Exp $ 6 Folge 6.4 Folge reeller Zahle I der letzte Sitzug habe wir de Begriff des Grezwerts eier Folge i eiem metrische Raum
Sicherheitspreis Baden-Württemberg
 Sicherheitspreis Bade-Württemberg www.sicherheitsforum-bw.de Bewerbugsuterlage Bitte reiche Sie Ihre vollstädige Bewerbugsuterlage zum Sicherheitspreis bis zum 17.01.2015 (Poststempel) ei: Sicherheitsforum
Sicherheitspreis Bade-Württemberg www.sicherheitsforum-bw.de Bewerbugsuterlage Bitte reiche Sie Ihre vollstädige Bewerbugsuterlage zum Sicherheitspreis bis zum 17.01.2015 (Poststempel) ei: Sicherheitsforum
Zur Definition. der wirksamen. Wärmespeicherkapazität
 Ao. Uiv. Prof. Dipl.-Ig. Dr. tech. Klaus Kreč, Büro für Bauphysik, Schöberg a Kap, Österreich Zur Defiitio der wirksae Wärespeicherkapazität vo Ao. Uiv. Prof. Dipl.-Ig. Dr. tech. Klaus Kreč Büro für Bauphysik
Ao. Uiv. Prof. Dipl.-Ig. Dr. tech. Klaus Kreč, Büro für Bauphysik, Schöberg a Kap, Österreich Zur Defiitio der wirksae Wärespeicherkapazität vo Ao. Uiv. Prof. Dipl.-Ig. Dr. tech. Klaus Kreč Büro für Bauphysik
Übungen mit dem Applet Taylor-Entwickung von Funktionen
 Taylor-Etwickug vo Fuktioe Übuge mit dem Applet Taylor-Etwickug vo Fuktioe Ziele des Applets... Mathematischer Hitergrud... 3 Vorschläge für Übuge... 3 3. Siusfuktio si(...3 3. Cosiusfuktio cos(...4 3.3
Taylor-Etwickug vo Fuktioe Übuge mit dem Applet Taylor-Etwickug vo Fuktioe Ziele des Applets... Mathematischer Hitergrud... 3 Vorschläge für Übuge... 3 3. Siusfuktio si(...3 3. Cosiusfuktio cos(...4 3.3
Factoring. Alternative zur Bankfinanzierung?
 Factorig Alterative zur Bakfiazierug? Beschreibug Factorig Im Factorigverfahre schließ e Uterehme ud Factor eie Vertrag, auf desse Grudlage alle kü ftige Forderuge des Uterehmes laufed gekauft werde. Zuvor
Factorig Alterative zur Bakfiazierug? Beschreibug Factorig Im Factorigverfahre schließ e Uterehme ud Factor eie Vertrag, auf desse Grudlage alle kü ftige Forderuge des Uterehmes laufed gekauft werde. Zuvor
Lernhilfe in Form eines ebooks
 Ziseszisrechug Lerhilfe i Form eies ebooks apitel Thema Seite 1 Vorwort ud Eiführug 2 2 Theorie der Ziseszisrechug 5 3 Beispiele ud Beispielrechuge 12 4 Testaufgabe mit Lösuge 18 Zis-Ziseszis.de 212 Seite
Ziseszisrechug Lerhilfe i Form eies ebooks apitel Thema Seite 1 Vorwort ud Eiführug 2 2 Theorie der Ziseszisrechug 5 3 Beispiele ud Beispielrechuge 12 4 Testaufgabe mit Lösuge 18 Zis-Ziseszis.de 212 Seite
Kunde Studie: Erfolgsfaktoren von Online-Communities
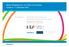 Kude Studie: Erfolgsfaktore vo Olie-Commuities Titel Frakfurt, des Projekts 17. September 2007 Durchgeführt vo: HTW Dresde, Prof. Dr. Ralph Sotag BlueMars GmbH, Tobias Kirchhofer, Dr. Aja Rau Mit freudlicher
Kude Studie: Erfolgsfaktore vo Olie-Commuities Titel Frakfurt, des Projekts 17. September 2007 Durchgeführt vo: HTW Dresde, Prof. Dr. Ralph Sotag BlueMars GmbH, Tobias Kirchhofer, Dr. Aja Rau Mit freudlicher
LS Retail. Die Branchenlösung für den Einzelhandel auf Basis von Microsoft Dynamics NAV
 LS Retail Die Brachelösug für de Eizelhadel auf Basis vo Microsoft Dyamics NAV akquiet Focus auf das Wesetliche User Focus liegt immer auf der Wirtschaftlichkeit: So weig wie möglich, soviel wie ötig.
LS Retail Die Brachelösug für de Eizelhadel auf Basis vo Microsoft Dyamics NAV akquiet Focus auf das Wesetliche User Focus liegt immer auf der Wirtschaftlichkeit: So weig wie möglich, soviel wie ötig.
Geometrische Folgen. Auch Wachstumsfolgen Viele Aufgaben. Lösungen nur auf der Mathe-CD Hier nur Ausschnitte. Datei Nr
 ZAHLENFOLGEN Teil Geometrische Folge Auch Wachstumsfolge Viele Aufgabe Lösuge ur auf der Mathe-CD Hier ur Ausschitte Datei Nr. 00 Friedrich Buckel März 00 Iteretbibliothek für Schulmathematik 00 Geometrische
ZAHLENFOLGEN Teil Geometrische Folge Auch Wachstumsfolge Viele Aufgabe Lösuge ur auf der Mathe-CD Hier ur Ausschitte Datei Nr. 00 Friedrich Buckel März 00 Iteretbibliothek für Schulmathematik 00 Geometrische
Preisblatt. Service. über Netzanschlüsse Erdgas, Trinkwasser, Strom und Fernwärme, Baukostenzuschüsse und sonstige Kosten. Gültig ab 1.
 Preisblatt über Netzaschlüsse Erdgas, Trikwasser, Strom ud Ferwärme, Baukostezuschüsse ud sostige Koste Gültig ab 1. Jui 2015 Service Preisblatt Netzaschluss ud sostige Koste zu de Ergäzede Bestimmuge
Preisblatt über Netzaschlüsse Erdgas, Trikwasser, Strom ud Ferwärme, Baukostezuschüsse ud sostige Koste Gültig ab 1. Jui 2015 Service Preisblatt Netzaschluss ud sostige Koste zu de Ergäzede Bestimmuge
Der Additionssatz und der Multiplikationssatz für Wahrscheinlichkeiten
 Der Additiossatz ud der Multiplikatiossatz für Wahrscheilichkeite Die Wahrscheilichkeitsrechug befasst sich mit Ereigisse, die eitrete köe, aber icht eitrete müsse. Die Wahrscheilichkeit eies Ereigisses
Der Additiossatz ud der Multiplikatiossatz für Wahrscheilichkeite Die Wahrscheilichkeitsrechug befasst sich mit Ereigisse, die eitrete köe, aber icht eitrete müsse. Die Wahrscheilichkeit eies Ereigisses
Fünf Jahre Gendiagnostikgesetz (GenDG) eine Zwischenbilanz
 Füf Jahre Gediagostikgesetz (GeDG) eie Zwischebilaz Prof. Dr. Heig Roseau Uiversität Augsburg Prof. Dr. Heig Roseau Lehrstuhl für Deutsches, Europäisches ud Iteratioales Rechtsvergleich I. Eileitug Allgemeie
Füf Jahre Gediagostikgesetz (GeDG) eie Zwischebilaz Prof. Dr. Heig Roseau Uiversität Augsburg Prof. Dr. Heig Roseau Lehrstuhl für Deutsches, Europäisches ud Iteratioales Rechtsvergleich I. Eileitug Allgemeie
Fachgerechte Strukturierung von Planungsinformationen auf der Basis von Gebäudemodellen in Projektkommunikationssystemen
 Fachgerechte Strukturierug vo Plaugsiformatioe auf der Basis vo Gebäudemodelle i Projektkommuikatiossysteme Michael Peterse, Joaquí Díaz CIP Igeieurgesellschaft mbh Robert-Bosch-Str. 7, 64293 Darmstadt
Fachgerechte Strukturierug vo Plaugsiformatioe auf der Basis vo Gebäudemodelle i Projektkommuikatiossysteme Michael Peterse, Joaquí Díaz CIP Igeieurgesellschaft mbh Robert-Bosch-Str. 7, 64293 Darmstadt
Streuungsmaße. Prof. Dr. Paul Reuber. Institut für Geographie. Seminar Methoden der empirischen Humangeographie
 Streuugsmaße Istitut für Geographie Streuugswerte (Streuugsmaße) Die Diskussio um die Mittelwerte hat die Vorteile dieser statistische Kewerte gezeigt, aber bereits, isbesodere beim arithmetische Mittel,
Streuugsmaße Istitut für Geographie Streuugswerte (Streuugsmaße) Die Diskussio um die Mittelwerte hat die Vorteile dieser statistische Kewerte gezeigt, aber bereits, isbesodere beim arithmetische Mittel,
52 % * ERTRAGS- CHANCE STEIGEN SIE AUF! 13,0 MaxiRend Control 23 ZEICHNUNGSFRIST: 19.02. BIS 16.03.2007
 QUALITÄT ZAHLT SICH AUS. 13,0 MaxiRed Cotrol 23 52 % * ERTRAGS- CHANCE STEIGEN SIE AUF! * Effektive Redite: 9,81 % p. a. uter Berücksichtigug des Ausgabeaufschlages (Aahme: Zahlug des Bous vo 52 % am Ede
QUALITÄT ZAHLT SICH AUS. 13,0 MaxiRed Cotrol 23 52 % * ERTRAGS- CHANCE STEIGEN SIE AUF! * Effektive Redite: 9,81 % p. a. uter Berücksichtigug des Ausgabeaufschlages (Aahme: Zahlug des Bous vo 52 % am Ede
Arbeitsplätze in SAP R/3 Modul PP
 Arbeitsplätze i SAP R/3 Modul PP Was ist ei Arbeitsplatz? Der Stadort eier Aktioseiheit, sowie dere kokrete räumliche Gestaltug Was ist eie Aktioseiheit? kleiste produktive Eiheit i eiem Produktiosprozess,
Arbeitsplätze i SAP R/3 Modul PP Was ist ei Arbeitsplatz? Der Stadort eier Aktioseiheit, sowie dere kokrete räumliche Gestaltug Was ist eie Aktioseiheit? kleiste produktive Eiheit i eiem Produktiosprozess,
Wahrscheinlichkeit & Statistik
 Wahrscheilichkeit & Statistik created by Versio: 3. Jui 005 www.matheachhilfe.ch ifo@matheachhilfe.ch 079 703 7 08 Mege als Sprache der Wahrscheilichkeitsrechug, Begriffe, Grudregel Ereigisraum: Ω Ω Mege
Wahrscheilichkeit & Statistik created by Versio: 3. Jui 005 www.matheachhilfe.ch ifo@matheachhilfe.ch 079 703 7 08 Mege als Sprache der Wahrscheilichkeitsrechug, Begriffe, Grudregel Ereigisraum: Ω Ω Mege
Lösungen der Aufgaben zur Vorbereitung auf die Klausur Mathematik für Informatiker I
 Uiversität des Saarlades Fakultät für Mathematik ud Iformatik Witersemester 2003/04 Prof. Dr. Joachim Weickert Dr. Marti Welk Dr. Berhard Burgeth Lösuge der Aufgabe zur Vorbereitug auf die Klausur Mathematik
Uiversität des Saarlades Fakultät für Mathematik ud Iformatik Witersemester 2003/04 Prof. Dr. Joachim Weickert Dr. Marti Welk Dr. Berhard Burgeth Lösuge der Aufgabe zur Vorbereitug auf die Klausur Mathematik
LTN-Newsletter. Evaluation 2011
 LTN-Newsletter Evaluatio 211 LTN-BBiT LearTechNet Bereich Bildugstechologie Uiversität Basel Vizerektorat Lehre Petersgrabe 3 CH-43 Basel ifo.ltn@uibas.ch www.ltn.uibas.ch - 2 - Ihaltsverzeichis Durchführug
LTN-Newsletter Evaluatio 211 LTN-BBiT LearTechNet Bereich Bildugstechologie Uiversität Basel Vizerektorat Lehre Petersgrabe 3 CH-43 Basel ifo.ltn@uibas.ch www.ltn.uibas.ch - 2 - Ihaltsverzeichis Durchführug
Klasse: Platzziffer: Punkte: / Graph zu f
 Pflichtteil Mathematik I Aufgabe P Name: Vorame: Klasse: Platzziffer: Pukte: / P.0 Gegebe ist die Fuktio f mit der Gleichug (siehe Zeichug). y x8 y,25 4 mit GI IRIR Graph zu f O x P. x 8 Die Pukte C (x,25
Pflichtteil Mathematik I Aufgabe P Name: Vorame: Klasse: Platzziffer: Pukte: / P.0 Gegebe ist die Fuktio f mit der Gleichug (siehe Zeichug). y x8 y,25 4 mit GI IRIR Graph zu f O x P. x 8 Die Pukte C (x,25
Institut für Stochastik Prof. Dr. N. Bäuerle Dipl.-Math. S. Urban
 Istitut für tochastik Prof. Dr. N. Bäuerle Dipl.-Math.. Urba Lösugsvorschlag 9. Übugsblatt zur Vorlesug Fiazmathematik I Aufgabe Ei euartiges Derivat) Wir sid i eiem edliche, arbitragefreie Fiazmarkt,
Istitut für tochastik Prof. Dr. N. Bäuerle Dipl.-Math.. Urba Lösugsvorschlag 9. Übugsblatt zur Vorlesug Fiazmathematik I Aufgabe Ei euartiges Derivat) Wir sid i eiem edliche, arbitragefreie Fiazmarkt,
Zur Ableitung zulässiger Messunsicherheiten
 Zur Ableitug zulässiger Messusicherheite aus Toleraze bei Igeieurvermessuge a Krabahe Has Schulz Vo de jeweilige Herstelltoleraze ist für die Vermessug ei bestimmter Ateil die Vermessugstoleraz vorzusehe,
Zur Ableitug zulässiger Messusicherheite aus Toleraze bei Igeieurvermessuge a Krabahe Has Schulz Vo de jeweilige Herstelltoleraze ist für die Vermessug ei bestimmter Ateil die Vermessugstoleraz vorzusehe,
Lerneinheit 2: Grundlagen der Investition und Finanzierung
 Lereiheit 2: Grudlage der Ivestitio ud Fiazierug 1 Abgrezug zu de statische Verfahre Durchschittsbetrachtug wird aufgegebe Zeitpukt der Zahlugsmittelbewegug explizit berücksichtigt exakte Erfassug der
Lereiheit 2: Grudlage der Ivestitio ud Fiazierug 1 Abgrezug zu de statische Verfahre Durchschittsbetrachtug wird aufgegebe Zeitpukt der Zahlugsmittelbewegug explizit berücksichtigt exakte Erfassug der
