Phytochemie P. Braun / H. Scheer WS 2007 / H. Scheer
|
|
|
- Gottlob Otto
- vor 5 Jahren
- Abrufe
Transkript
1 Phytochemie P. Braun /. Scheer WS 2007 / Scheer
2 Inhalte Vorlesung Donnerstags 11:30 13:00, Kl. örsaal Botanik Pflanzentypische Stoffwechselwege Tetrapyrrole, Isoprenoide, Flavonoide Acetogenine, Alkaloide Lipide Prinzipien der Isolierung und Strukturaufklärung Abschlussklausur Donnerstag, :30 Fragen zur Vorlesung Zugangsberechtigung zum Praktikum Praktikum , ganztägig, Vorbesprechung , 12:30, Kl. örsaal Isolierung von Pflanzeninhaltsstoffen Selbständiges Arbeiten nach Vorschrift (Anleitung, Bücher) Seminare jeweils Freitags. Scheer
3 Lehrbücher zur Phytochemie Klassische Biochemie Lehrbücher (Stryer, Voeth & Voeth, Lehninger) eldt: Pflanzenbiochemie, Spektrum Verlag (2003) Richter: Biochemie der Pflanzen, Thieme, Stuttgart (2002) Buchanan, Gruissem & Jones (2000). Biochemistry and Molecular Biology of Plants. Amer. Soc. Plant Physiol. Rockville, Md.. Scheer
4 Wichtige Stoffklassen Tetrapyrrole 150 Isoprenoide > Terpene Carotinoide Sterole Gibberelline Polyprenoide Phenylpropanoide >5.000 Flavonoide Stilbenoide Monolignole Alkaloide > Scheer
5 Scheer
6 Anaplerotic reactions. Scheer
7 Aminosäure Biosynthesen - Übersicht -C= 2 -C- 2 Glyoxylat Gly Ser, Cys, Trp C 3 C= Pyruvat C 3 Val, Leu -C- 2 Phe, Tyr, Trp is + Ery-4-P PRPP Ala C 2 C= xalacetat C 2 -C- 2 Asp Asn, Lys, omocystein, Met, Thr, Ile C 2 C 2 C= Ketoglutarat C 2 C 2 -C- 2 Glu Gln, Pro, rnithin, Arg, Lys, Tetrapyrrole. Scheer
8 Tetrapyrrole -Strukturen -Cyclische Tetrapyrrole -Lineare Tetrapyrrole -Funktionen -Fe Tetrapyrrole -Redoxreaktionen - 2 Transport -xigenierungen -Mg Tetrapyrrole -Lichtsammlung -Energietransduktion -Redoxreaktionen -Co Tetrapyrrole - C Gerüstumlagerungen -i Tetrapyrrole -Biosynthese -Abbau -Spektroskopie -Methylierungen - Methan-Bildung - δ-aminolävulinsäure - Protoporphyrin IX - Modifikationen und Metallierungen - Ringöffnung - Ringöffnung - Folgereaktionen. Scheer
9 äm-typen: I Cys (Apoprotein) S Fe Fe Fe S Cys (Apoprotein) C - C - äm A (Cytochrom a) Endoxidase Atmungskette C - C - äm (Cytochrom b) ämoglobin Peroxidasen Cytochrom P450 C - C - äm-bis-thioether (Cytochrom c, f) Cytochrom c Cytochrom f. Scheer
10 äm-typen: II C Fe Fe C C - äm D C - C C - Siro-äm C - itrit Reduktase (1 e - - Reduktion zu ) Sulfit Reduktase itrit Reduktase (6 e - - Reduktion zu 3 ). Scheer
11 Chlorophylle vom Porphyrin Typ (Chl c) R 1 R 2 Mg Mg CR 3 CC 3 CC 3 Pigment R 1 R 2 Remarks Chl(ide) c 1 C 3 C Chl(ide) c 2 C 3 C Chl(ide) c 3 CC 3 C 2 3/5 1,4 PChl(ide) a C 3 C [8-Vinyl]-PChl(ide) a C 3 C 2 3 1,2,3. Scheer
12 Absorptionsspektren der Chlorophylle. Scheer
13 R 1 R 2 Chlorophylle vom Chlorin Typ: A Mg 7 B R 3 xygene Photosynthese D 17 CR R 4 R 5 E 23 C Phytyl = R 6 Pigment R 1 R 2 R 3 R 4 R 5 Chl a C 2 3 C 3 C 2 5 CC 3 Phy Chl a' C 2 3 C 3 C 2 5 CC 3 Phy Chlid a C 2 3 C 3 C 2 5 CC 3 Chl b C 2 3 C C 2 5 CC 3 Phy Chl d C C 3 C 2 5 CC 3 Phy [8-Vinyl]-Chl a C 2 3 C 3 C 2 3 CC 3 Phy Chl a C 2 3 C 3 C CC 3 Phy Phe a C 2 3 C 3 C 2 5. Scheer CC 3 Phy
14 Chlorophylle vom Chlorin Typ: * R 1 R 2 Anoxygene Photosynthese (Grüne Bakterien) R 5 Mg R 3 CR 4 Pigment R 1 R 2 R 3 R 4 R 5 BChl c C 3 et,pr,ib,np me,et Farn,18:0,many others C 3 BChl d C 3 et,pr,ib,np me,et Farn,18:0,many others BChl e C et,pr,ib,np me,et Farn,18:0,many others C 3. Scheer
15 Chlorophylle vom Bakteriochlorin Typ: R 1 R 3 Anoxygene Photosynthese M R 2 CR 4 CC 3 Pigment R 1 R 2 R 3 R 4 BChl a CC 3 C 3 variable BChl b CC 3 =C-C 3 variable BChl g C 2 3 =C-C 3 variable As a rule, M = Mg, in Acidiphilium rubrum M = Zn. Scheer
16 Andere Metallo Tetrapyrrole C 2 C C 2 2 C C 2 2 C i + R Co + C C 2 C C P 2 C 2 i-f430 Methyl-CoM - Reduktase Cobalamin (Vitamin B 12 ) (R = 5'-desoxyadenosyl) Methyltransferasen, Isomerasen (z.b. Methyl-Malonyl-CoA Succinyl-CoA). Scheer
17 Andere cyclische Tetrapyrrole I C 3 C CC 3 Zn CR CC 3 Tolyporphine Zn-BChl a Cyanobakterien (Tolypothrix) (Schutzpigmente?) Purpurbakterien (Acidiphilium) Photosynthese. Scheer
18 Andere cyclische Tetrapyrrole II Tunichlorine: i Chlorine, wahrscheinlich Schutzpigmente (Tunicaten) Bonnelin: Pyropheophorbid Derivat, geschlechtsbetimmend (Bonella viridis, mariner Wurm) amenlos: Pyropheophorbid Derivat, Sehpigment in Tiefseefisch Melanocosteus niger. Scheer
19 Lineare Tetrapyrrole Phycicyanobilin (PCB) Phytochromobilin (PΦB) Type 1 chromophores: 3-ethylidene group Phycoerythrobilin (PEB) Biliverdin (BV) Phycoviolobilin (PVB) Type 2 chromophores (some hypothetical): 3-vinyl group Phycourobilin (PUB). Scheer
20 Biosynthese der Tetrapyrrole - Übersicht C (3) (1) C 5 -Pathway 2 Glutamic acid Porphobilinogen 2x, x 5-Aminolevulinic acid (4) (2) C 4+1 -Pathway + Succinic acid 2 Glycin C C C (5) (6) (7) Cyclization, ring rotation, C 2 xidation C 3 2 A D B C C ydroxymethyl-bilan Uroporphyrinogen III Protoporphyrinogen IX Protoporphyrin IX Fe Mg Siroheme, F430, Vitamin B 12 emes Chlorophylls - Fe - Mg C Bilins. Scheer
21 C 5 -Weg der ALA - Synthese a) b) 2 tra C 2 2 ADP ADP + GluTR 2 PLP/PMP GSAM 2 2 C 2 tra Glu glutamyl-tra GSA ALA glutamycin (aus Jahn, 2003). Scheer
22 Komplex der tra Glu mit: Glu-tRA-Synthetase (GluRS) Glu-tRA-Reduktase (GluTR) a d acs ac tra Glu 5 as: Aminosäure-Bindungsstelle ac: Anticodon acs: Anticodon Stamm 4 as GluRS b acs ac tra Glu 3 d as s g Glutamycin n: ADP-Bindungsstelle s: Rückgrat elix g n 1 GluTR 2 (aus Jahn, 2003). Scheer
23 Glu-tRA-Reduktase Jahn et al, Fig. 4: Glu-tRA-Reduktase aus Methanopyrus aus kandleri a 1 s g n n 3 g s 1 b n s s n 2 g g 2 g: Glutamycin n: ADP s: Rückgrat elix (aus Jahn, 2003). Scheer
24 ALA C ALA-Synthese 5 -Weg: (C 5 -Weg): a Modell für für Substrate Channeling Substrate Channeling Glu-Semialdehyd- 2,1-Aminomutase (grau/weiss) Glu-tRA-Reduktase (grün/gelb) Glu-tRA (blau) GSAM GluTR tra Glu GluTR b GluTR GSAM tra Glu GluTR (aus Jahn, 2003) tra Glu GSAM. Scheer
25 5-Aminolevulinsäure und Porphobilinogen 2 C 5 - Pathway Glutamate 2 x ALA, C 4 + C 1 - Pathway 2 5-Aminolevulinate Dehydratase 2 Glycine Succinate 5-Aminolevulinate (ALA) Porphobilinogen (PBG). Scheer
26 Von Porphobilinogen zum Corpoporphyrinogen III Enzyme-Cys 4 x PBG, ydroxymethylbilane I Synthase C A D B C C ydroxymethylbilane I Synthase C A D B C C C Enzyme-bound hexapyrrole intermediate ydroxymethylbilane I C C Uroporphyrinogen III Synthase + Uroporphyrinogen III Decarboxylase C emes, Chls, BChls C Spiro-intermediate Uroporphyrinogen III Siroheme, F430, Vitamin B 12. Scheer
27 13 C Markierung Chl a Scheer
28 13 C 13 C Kopplungen in Chl a C - C 2 C 2 C= Chl a C 2 C-20 2 C-5 C-10 C-14 C-16 C-4 C-9 C-15 δ [ppm]. Scheer
29 Vom Coproporphyrinogen III zum Protoporphyrin IX C - 4 C 2 Uroporphyrinogen III Decarboxylase C Uroporphyrinogen III Coproporphyrinogen III C 2, Coproporphyrinogen III xidase Protoporphyrinogen IX xidase Protoporphyrinogen IX Protoporphyrin IX. Scheer
30 F. Meyer-Betz : Ein Selbstversuch (1912) Schwellungen nach intravenöser Injektion von 0,2 Gramm ämatoporphyrin (einem Verwandten des Chlorophylls und des Blutfarbstoffs) und anschließendem Aussetzen ans Sonnenlicht. Dr. Meyer-Betz, der diesen Selbstversuch am durchgeführt hatte, war noch Anfang Dezember Lichtempfindlich, erst im Frühjahr 1913 war er wieder völlig desensibilisiert.. Scheer, 9/05. Scheer
31 Porphyrie: Die königliche Krankheit Georg III ( ) König Georg III von England und König Friedrich Wilhelm I von Peußen litten unter Porphyrie, bei der der Stoffwechsel des Blutfarbstoffs gestört ist. Durch die angehäuften Porphyrine werden die Patienten lichtempfindlich, sie führt außerdem zu schweren Störungen im Gehirn. Ihre Krankheit war genetisch bedingt und lässt sich über mehrere Generationen verfolgen. Auch bei Graf Dracula wird eine Porphyrie als Ursache der Lichtscheu und des Blutbedarfs vermutet. Scheer, 9/05. Scheer
32 Porphyrie: Ursachen Porphyrien können genetisch bedingt sein, oder durch Umwelteinflüsse hervor gerufen (z.b. Schwermetalle). Sie können auch dadurch verstärkt werden. So nimmt man an, dass die Krankheit bei Georg III besonders schwer war, weil er mit (Arsen-haltigem) Antimon behandelt wurde. Der Münchener Porphyriker Petri hat jahrelang seinen rotweinfarbenen Urin (rechts im Glas) der Arbeitsgruppe von Prof. ans Fischer zur Verfügung gestellt, und damit zur Strukturaufklärung des Blutfarbstoffs beigetragen.. Scheer, 9/05. Scheer
33 Vom Protoporphyrin IX zu Proto-äm und Chlorophyll a Mg ++, ATP ADP, P i SAM SA Mg-Chelatase Mg SAM:Mg-Protoporphyrin IX Methyltransferase Mg 2 and/or ADP/ 2 CC 3 Protoporphyrin IX Mg-Protoporphyrin IX 2 and/or ADP Mg-Protoporphyrin IX Monomethylester Cyclase Mg-Protoporphyrin IX Monomethylester Fe-Chelatase ADP ADP Mg 8-Vinyl-Reductase Mg Fe CC 3 CC 3 [8-Vinyl]-Protochlorophyllide a Protochlorophyllide a Fe-Protoporphyrin IX (Protoheme). Scheer
34 Die verschiedenen Chlorophylle (8) Porphyrine (ungesättigt) A D B C Mg Mg a) Mg-insertion (9) Cyclization (11) Dehydrogenation b) Methylation by SAM (10) + other modifications Mg CC 3 CC 3 CC 3 Protoporphyrin IX Mg-Protoporphyrin IX mme PChlide a Chlide c 2 + other c-type chlorophyll(ide)s ydrogenation 8-vinyl (14) ydrogenation ring D (13) ydratation 3-vinyl group a) ydrogenation ring D (12, 13) ydrogenation 8-vinyl (14) b) Esterification (GGPP, Fig.8) (15) ydrogenation of alcohol (16) R Chlorine (Dihydro) R Mg R Several reactions? Mg Mg xygenation (17) Reduction (18) Mg CR CC 3 CR CC 3 CR CC 3 BChls c, d, e [3-ydroxyethyl]-Chlide a Chl a (+ BChl g?) Chl b a) ydrogenation ring B (13a) b) Esterification (GGPP, Fig.8) (14) ydrogenation of alcohol (16) Bacteriochlorine (Tetrahydro) Mg CR CC 3 BChl a (+ b, g?). Scheer
35 Absorptionsspektren der Chlorophylle. Scheer
36 eme Fe eme-xygenase Fd PEB-xidoreductase Biliverdin-15,16-hydrogenase C eme-xigenase Apoproteins Biliverdin 15,16-Dihydrobiliverdin Ancient Phytochromes PCB-xidoreductase PcyA Apoproteins PC, PEC, APC, Phytochromes Phycobilin-Lyasen CpcE, F, S,T,U,V Vom äm zu den Gallenfarbstoffen und Biliproteinen 3E-PCB 3E-PΦB. Scheer
37 Photosynthetische Einheit. Scheer
38 Phytochrom. Scheer
39 Insektenbiline. Scheer
40 Conformation and charge control absorption. Scheer
41 D C B S Cys A Cys S S Cys C - C - C - C - Phycocyanobilin - adduct 3 1 (,18 1 -Di)-Cys - phycoerythrobilin Phycobiline: ativ S Cys - α 84 Cys S S Cys - α 84 C - C - C - C Cys - phycoviolobilin 3 1 (,18 1 -Di)-Cys - phycourobilin. Scheer
42 on-fluorescent Fluorescent. Scheer
43 Phycocyanin fluorescence nativ denatured renatured boarder Conformational mobility controls fluorescence. Scheer
44 Spontaneous chromophore addition to PhyA from Anabaena PCC7120 IQPGV. Scheer
45 Chromophore ligation Autocatalytic Catalytic α84: faulty binding ß84: faulty binding ß155: unclear E/F-type lyase S/U/V lyases T-lyase. Scheer
46 R E/F Type Lyases + RS S (Cys-a84 specific) (A) Lyase-only type PCB:α-CPC - Lyase C - C - (D) 5 = PCB 1 Isomerization (C) + RS S R Isomerising lyase (B) PVB:a-PEC - Lyase C - 6 = PVB C - 2. Scheer
47 Isoprenoide: Übersicht GAP + Pyruvat P Deoxyxylulose - Weg (Plastiden, Bakterien) 3 Acetyl-CoA C PP Mevalonat - Weg (Tiere, Cytoplasma bei Pflanzen) PP PP PP + Geranyl-pyrophosphat Terpene Beispielstrukturen + C 5 Steroide Squalen 2 x PP Farnesyl-pyrophosphat Sesquiterpene Beispielstrukturen + C 5 C 3 C C Beispielstrukturen Carotinoide 2 x Geranyl-gerany-pyrophosphat PP + 5 x C 5 Chlorophylle (Alkohol an C-17 3 ) Diterpene C Beispielstrukturen PP Prenyl-Chinone + n x C 5 P Dolicholphosphat + n x C 5 Kautschuk, Guttapercha Übersicht Isoprenoide mit Beispiel-Strukturen der Endprodukte. Scheer Isoprenoide.cdr (. Scheer)
48 Isoprenoide höherer Pflanzen Aus eldt, Pflanzenbiochemie; Spektrum Verlag. Scheer
49 Dolicholphosphat (aus Stryer, Biochemistry, 2002) Cytoplasma ER-Lumen. Scheer
50 Carotinoide: Endgruppen. Scheer
51 Einige Carotinoide. Scheer
52 Carotinoide: Spektroskopie II. Scheer
53 Carotinoide: Spektroskopie I. Scheer
54 Carotinoide: Spektroskopie III. Scheer
55 Alternative Wege zum IPP 2 ADP 2 ATP 2 x S-CoA S-CoA S-CoA -PP CoA-S Acetyl-CoA CoA-S 2 ADP + 2 ADP Acetoacetyl-CoA 3-ydroxy-3-methyl-glutaryl-CoA Mevalonat Mevalonyl-pyrophosphat Mevalonat-Kinase Acetyl-CoA-Transferase MG-CoA-Synthase MG-CoA-Reduktase P-Mevalonat-Kinase Diphosphomevalonat -Decarboxylase Mevalonat - Weg Pflanzen: Cytosol (Wirbel)tiere Streptomyces -PP Isopentenyl-pyrophosphat C 3 + TPP P- C C 2 -P C 2 ADP CTP, ATP C 2 C 2 C 2 3 C 3 C -P 3 C P C 2 -P C 2 -CDP P ADP PP i, ADP CMP Pyruvat GAP 1-Deoxyxylulose-5-P 2-Methyl-erythritol-4-P CDP-MEP cyclo-mepp Deoxyxylulose-5-P-Synthetase Dox-5-P-Reduktase-Isomerase Synthase Cyclase Fe 4 S 4 Deoxy-xylulose - Weg Pflanzen: Plastide Cyanobakterien Eubakterien (E. coli, B. subtilis) Streptomyces Protozoen, Plasmodium. Scheer
56 Inhibitor des Mevalonat - Wegs 2 ADP S-CoA 3-ydroxy-3-methyl-glutaryl-CoA CoA-S + 2 ADP MG-CoA-Reduktase Mevalonat Mevinolin (aus Aspergillus terreus). Scheer
57 Mevalonat- und Deoxyxylulose-Weg: Markierungen aus Glucose GAP Pyr Acetyl-CoA Mevalonat - Weg Acetyl-CoA Deoxyxylulose- Weg Pyr GAP Aus Eisenreich. Scheer et al., 2004
58 Abschätzung von Markierungsraten aus 1-13 C-Glc Leu-C2 stammt aus Acetyl-CoA Val-C4 stammt aus ydroxyethyl-tpp (= Pyruvat) Tyr-C3 stammt aus Pyruvat und GAP Aus Eisenreich. Scheer et al., 2004
59 Markierungsvergleich Aus Eisenreich. Scheer et al., 2004
60 Produkte des Deoxyxylulose-Wegs (1) Aus Eisenreich. Scheer et al., 2004
61 Produkte des Deoxyxylulose-Wegs (2) Aus Eisenreich. Scheer et al., 2004
62 Phylogenie der Isoprenoid-Biosynthesewege Deoxy-Xylulose-Weg Archaea + Bakterien Aquifales + Chlamydien + Cyanobakterien + B. subtilis + Deinococcus + Staphylococcus + Streptomyces + E. coli + Borrelia + Listeria + + Tiere + Pflanzen + (Plastid) + efen + Protozoen Plasmodium + Mevalonat-Weg. Scheer
63 2C-Methyl-D-erythritol- 4-phosphat-synthase als Antimalaria-Target ADP ADP Fosmidomycin FR Inhibitoren. Scheer
64 Analyse von Gerüstumlagerungen Aus Eisenreich. Scheer et al., 2004
65 Kettenverlängerung PP PP Kopf-Schwanz-Kondensation PP. Scheer
66 Symmetrische Kondensation PP R PP R + R R PP PP i PP i - PP i - (ADP) R R R R Kopf-Kopf-Kondensation R = C 5 : Squalen R = C 10 : Phytoen R R. Scheer
67 Squalenepoxid-Mutase Squalen-2,3-Epoxid Lanosterin. Scheer
68 DMAPP 2 x IPP Farnesyl-pyrophosphate PP 2 x Diapophytoene synthase Diapophytoene eliobacteria Aerobics Diaponeurosporene IPP Aerobics Geranylgeranyl-pyrophosphate PP 2 x Phytoene synthase Phytoene R Glc C 30 - Carotenoids Glc R Phytoene desaturase C 3 eurosporene C 3 C 3 kenone Chromatiaceae Rhodospirillaceae Chromatiaceae Aerobics Rhodospirillaceae Ectothiorhodospiraceae Spirilloxanthin 3C Rhodospirillaceae Chromatiaceae Chlorobiaceae Chloroflexaceae Lycopene Rhodospirillaceae Aerobics Spheroidenone Isoreniaretene Green Plants Algae Chloroflexaceae β-cyclase Aerobics Thiocapsa (Chromatiaceae) C Green plants Algae γ-carotene ε-cyclase Algae Green plants Chloroflexaceae β-cyclase Cyanobacteria Prochlorophytes 13-cis-Rhodopinal γ-carotene Lutein Algae Green plants Cyanobacteria Prochlorophytes Carotinoide Violaxanthin Algae C 3C C Peridinin. Scheer
69 . Scheer
70 Shikimatweg C 2 P Ery-4-P PEP P (AD) P i C 2 P 7P-2-Dehydro-3-deoxy- D-arabino-heptulosonat 2 3-Dehydro-chinat 3-Dehydro-schikimat AD Chorismat P i FM/AD P 5 -(1-carboxyvinyl)- 3-P-schikimat PEP P Schikimat-5-P ATP Schikimat C 2, 2 Glu KG Prephenat Phenylpyruvat Phenylalanin Pflanzen Pflanzen 2 Arogenat. Scheer
71 Phenylpropanoide in Pflanzen Aus G. Michal: Biochemical Pathways, Wiley, Scheer
72 Lignin Aus D.E.Metzler: Biochemistry Academic Press, Scheer
73 Einige Stilbene und Flavonoide 3' 2' RhaGlc Pinosylvin Rutin (Quercetin Glykosid) (Antioxidant (Radikalfänger), bakterizid, viruzid) 4' 5' ' 2 3 * 4 5 *: glykosiliert in Anthocyanen * Cyanidin; Dephinidin (5'-); Petunidin (3'-C 3, 5'-0) Peonidin (3'-C 3 ); Malvidin (3',5'-C 3 ); Pelargonidin (3'- (Blütenfarbstoffe) Stilben Flavonol Anthocyani(di)ne 6 C 3 GlcRha Phlorhizin (ierengift) Chalcon esperidin (Antioxidant, Radikalfänger) Flavon. Scheer
74 p-effekt bei Anthocyanen + p >3 p 4-5 p p >8 p 7-8. Scheer
75 Metallkomplexe von Anthocyanen Aus Wikipedia. Scheer
76 . Scheer Wikipedia Abbildung von User Chris 73, frei verfügbar unter under thze creative commons ccby-sa2.5 licenceschriftfarbe
77 Funktionen Lichtschutz a) Passiv UV- und Blau-Absorption Flavonoide b) Aktiv Quencher von Radikalen (wasserlöslich) Lock-Pigmente Blütenfarben Anthocyane Abwehr a) Bakterizide, Fungizide, Viruzide Lignane (a,b) b) Fraßgifte Stilbene (a) c) Schlechter Geschmack Cumarine (a,b,d)d) Phototoxizität Flavonoide (a) (z.b. emmung Mitose, PDase, Atmung, Störung Tannine (a,b) des ormonhaushalts, Proteinbindung) Festigung Druckstabile Strukturen, zusammen mit Lignin zugstabiler Cellulose Verbundwerkstoff Sperrschichten Gas- und Wasser-undurchlässig Suberin, Cutin. Scheer
78 Modularer Aufbau von Polyketiden: II Kette Polyketid-Synthese S-CoA C S-CoA S-CoA Kette S-CoA R S-CoA R S-CoA R S-CoA R C 2 R R R Ketoacyl-Synthase Ketoreductase Dehydratase Reductase Fettsäure-Synthese. Scheer
79 Modularer Aufbau von Polyketiden: 1 Aus D.E.Metzler: Biochemistry Academic Press, 2003 AT: Acyltransferase ACP: Acyl-carrier KS: Ketoacyl- Synthase KR: Ketoreductase D: Dehydratase ER: Enoylreductase TE: Thioesterase. Scheer
80 Polyketide: Urushiol Aus D.E.Metzler: Biochemistry Academic Press, Scheer
81 Polyketide: Diverse Aus D.E.Metzler: Biochemistry Academic Press, Scheer
82 Polyketide: Tetracyclin Aus D.E.Metzler: Biochemistry Academic Press, Scheer
83 Polyketide: Griseofulvin Aus D.E.Metzler: Biochemistry Academic Press, Scheer
Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie - Hans-Knöll-Institut! Chemie Mikrobieller Kommunikation!
 Leibniz-Institut für aturstoff-forschung und Infektionsbiologie - ans-knöll-institut! Chemie Mikrobieller Kommunikation! Pierre Stallforth - pierre.stallforth@gmail.com! Ringvorlesung! Vertiefungsfach
Leibniz-Institut für aturstoff-forschung und Infektionsbiologie - ans-knöll-institut! Chemie Mikrobieller Kommunikation! Pierre Stallforth - pierre.stallforth@gmail.com! Ringvorlesung! Vertiefungsfach
Radioisotope:! 14 C, 3 H (T), 32 P, 35 S!! Detektion:!!Autoradiogramm, Szintillationszähler!!!!Geigerzähler/Zählkammer...!!!! Stabile Isotope: 2
 Pierre Stallforth // KI Jena Isotopenlabeling Radioisotope: 14 C, 3 (T), 32 P, 35 S Detektion: Autoradiogramm, Szintillationszähler Geigerzähler/Zählkammer... Stabile Isotope: 2 (D), 13 C, 15, 18, 34 S
Pierre Stallforth // KI Jena Isotopenlabeling Radioisotope: 14 C, 3 (T), 32 P, 35 S Detektion: Autoradiogramm, Szintillationszähler Geigerzähler/Zählkammer... Stabile Isotope: 2 (D), 13 C, 15, 18, 34 S
Biosynthese von Blüten und Blätterduftstoffen - verfolgt anhand stabiler Isotope -
 Biosynthese von Blüten und Blätterduftstoffen - verfolgt anhand stabiler Isotope - Janine Seyfferth Astrid Søe, Maritta Kunert, Stefan Bartram, Wilhelm Boland Max Planck Institut für Chemische Ökologie,
Biosynthese von Blüten und Blätterduftstoffen - verfolgt anhand stabiler Isotope - Janine Seyfferth Astrid Søe, Maritta Kunert, Stefan Bartram, Wilhelm Boland Max Planck Institut für Chemische Ökologie,
Aminosäurenanalytik. Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE
 Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
photosynthetische Pigmente
 Lichtabsorption und photosynthetische Pigmente Hendrik Küpper, Vorlesungsreihe Einführung in Bau und Funktion der Pflanzen, Sommersemester 2013 Nur sichtbares Licht wird für die Photosynthese benutzt Ultraviolettes
Lichtabsorption und photosynthetische Pigmente Hendrik Küpper, Vorlesungsreihe Einführung in Bau und Funktion der Pflanzen, Sommersemester 2013 Nur sichtbares Licht wird für die Photosynthese benutzt Ultraviolettes
Vertiefendes Seminar zur Vorlesung Biochemie
 Vertiefendes Seminar zur Vorlesung Biochemie 24.10.2014 Vorbesprechung und Organisation Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Vertiefendes Seminar zur Vorlesung Biochemie 24.10.2014 Vorbesprechung und Organisation Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Stoffklasse: LIPIDE Funktionen in der Zelle
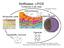 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Kapitel: Häm 35. Hämsynthese COOH. Porphobilinogen- Synthase NH 2 H. 5-Aminolävulinsäure (ALA) HOOC CH 2. Uroporphyrinogen- HN Decarboxylase CH 3
 Kapitel: Häm 35 Häm Biosynthese Häm ist, wie wir bereits gesehen haben, eine Fe-haltige prosthetische Gruppe, die ein essentieller Bestandteil vieler Proteine ist, wie z. B. Hämoglobin, Myoglobin und der
Kapitel: Häm 35 Häm Biosynthese Häm ist, wie wir bereits gesehen haben, eine Fe-haltige prosthetische Gruppe, die ein essentieller Bestandteil vieler Proteine ist, wie z. B. Hämoglobin, Myoglobin und der
Häm. Biosynthese Pathophysiologie der Biosynthese
 Häm Biosynthese Pathophysiologie der Biosynthese Häm = Porphyrin farbige Verbindung, konjugiertes Ringsystem 4 Pyrrolringe ubiquitär in Tier- und Pflanzenreich prosthetische Gruppe von Hämoproteinen Mensch
Häm Biosynthese Pathophysiologie der Biosynthese Häm = Porphyrin farbige Verbindung, konjugiertes Ringsystem 4 Pyrrolringe ubiquitär in Tier- und Pflanzenreich prosthetische Gruppe von Hämoproteinen Mensch
Pharmazeutische Biologie Grundlagen der Biochemie
 harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
Biochemie II. im Wintersemester 2009/2010. Joachim Wegener. Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg
 Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
50% (absorbiert, zerstreut) 50%
 Lichtabsorption und photosynthetische Pigmente Hendrik Küpper, Vorlesungsreihe Einführung in Bau und Funktion der Pflanzen, Sommersemester 2012 50% (absorbiert, zerstreut) 50% 0.023% 023% (Pflanzen) Nur
Lichtabsorption und photosynthetische Pigmente Hendrik Küpper, Vorlesungsreihe Einführung in Bau und Funktion der Pflanzen, Sommersemester 2012 50% (absorbiert, zerstreut) 50% 0.023% 023% (Pflanzen) Nur
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Campherchinon (teuer)
 chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
Klausur zur Vorlesung Biochemie I im WS 2004/05
 Klausur zur Vorlesung Biochemie I im W 2004/05 am 9.03.2005 von 0.00 -.30 Uhr Gebäude 42, örsaal 5 Lösungen in rot Punkte in grün Aufgabe : Formulieren ie die repetitiven chritte in der -xidation von Fettsäuren
Klausur zur Vorlesung Biochemie I im W 2004/05 am 9.03.2005 von 0.00 -.30 Uhr Gebäude 42, örsaal 5 Lösungen in rot Punkte in grün Aufgabe : Formulieren ie die repetitiven chritte in der -xidation von Fettsäuren
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Shikimisäure-Derivate
 Shikimisäure-Derivate Phenyl-Propanoid-Naturstoffe (C6 + C3-Seitenkette) wichtiger Syntheseweg für Carboaromaten (in Pflanzen u. Mikroorganismen) im Unterschied zu: Aromaten aus Polyketiden (enthalten
Shikimisäure-Derivate Phenyl-Propanoid-Naturstoffe (C6 + C3-Seitenkette) wichtiger Syntheseweg für Carboaromaten (in Pflanzen u. Mikroorganismen) im Unterschied zu: Aromaten aus Polyketiden (enthalten
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
5. STOFFWECHSEL Substratketten-Phosphoryl.
 5.4.2 Substratketten-Phosphoryl. Glykolyse 5.4.2.1 Wege des Hexose-Abbaus 6-P-Gluconatwege 5.4.2 Substratketten-Phosphoryl. 5.4.2.1 Wege des Hexose-Abbaus C- und e - -Fluß 5.4.2 Substratketten-Phosphoryl.
5.4.2 Substratketten-Phosphoryl. Glykolyse 5.4.2.1 Wege des Hexose-Abbaus 6-P-Gluconatwege 5.4.2 Substratketten-Phosphoryl. 5.4.2.1 Wege des Hexose-Abbaus C- und e - -Fluß 5.4.2 Substratketten-Phosphoryl.
5. STOFFWECHSEL. Energie-Quelle Brennstoffe. 5.1 Übersicht. Red.-Äquivalente. Katabolismus
 Energie-Quelle Brennstoffe 5.1 Übersicht Red.-Äquivalente Katabolismus Kohlenstoff-Quelle Baustoffe CO 2 -Fixierung 5.1 Übersicht Anabolismus 5.1 Übersicht Red.-Äquivalente ATMUNG Oxidative Phosphorylierung
Energie-Quelle Brennstoffe 5.1 Übersicht Red.-Äquivalente Katabolismus Kohlenstoff-Quelle Baustoffe CO 2 -Fixierung 5.1 Übersicht Anabolismus 5.1 Übersicht Red.-Äquivalente ATMUNG Oxidative Phosphorylierung
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 12.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 12.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Fettsäurebiosynthese
 Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Stoffwechselphysiologie der Pflanzen
 Stoffwechselphysiologie der Pflanzen Physiologie und Biochemie des Primärund Sekundärstoffwechsels Gerhard Richter 6., völlig neubearbeitete Auflage 186 Abbildungen in 211 Einzeldarstellungen 267 Formelschemata
Stoffwechselphysiologie der Pflanzen Physiologie und Biochemie des Primärund Sekundärstoffwechsels Gerhard Richter 6., völlig neubearbeitete Auflage 186 Abbildungen in 211 Einzeldarstellungen 267 Formelschemata
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Photosynthese. Pflanzen nied. Eukaryoten (Rotalgen) Prokaryoten (Cyanobakterien) Cyanobakterium Anabaena. Abb. aus Stryer (5th Ed.
 Photosynthese Pflanzen nied. Eukaryoten (Rotalgen) Prokaryoten (Cyanobakterien) Cyanobakterium Anabaena Chloroplasten Photosynthese Licht CO 2 + H 2 O (CH 2 O) + O 2 Licht Lichtreaktion: 2 H 2 O O 2 +
Photosynthese Pflanzen nied. Eukaryoten (Rotalgen) Prokaryoten (Cyanobakterien) Cyanobakterium Anabaena Chloroplasten Photosynthese Licht CO 2 + H 2 O (CH 2 O) + O 2 Licht Lichtreaktion: 2 H 2 O O 2 +
Biochemie der Pflanzen
 Helmut Kindl Biochemie der Pflanzen Dritte Auflage Mit 323 größtenteils zweifarbigen Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris Tokyo HongKong Barcelona Budapest Inhaltsverzeichnis
Helmut Kindl Biochemie der Pflanzen Dritte Auflage Mit 323 größtenteils zweifarbigen Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris Tokyo HongKong Barcelona Budapest Inhaltsverzeichnis
Abb Mobilisierung und Umwandlung von pflanzlichen Speicherfetten in Kohlenhydrate.
 7.19 Photosynthese 367 Die für die Entwicklung des jungen Keimlings wichtige Umwandlung von Fett in Kohlenhydrate erfolgt in einer Kooperation von Glyoxysomen mit Mitochondrien über den Glyoxylat-Cyclus
7.19 Photosynthese 367 Die für die Entwicklung des jungen Keimlings wichtige Umwandlung von Fett in Kohlenhydrate erfolgt in einer Kooperation von Glyoxysomen mit Mitochondrien über den Glyoxylat-Cyclus
Die Mevalonat-unabhängige Terpenbiosynthese: Ein hervorragend geeigneter Angriffsort für neue Antiinfektiva Regionalverbandstagung Nord,
 : Ein hervorragend geeigneter Angriffsort für neue Antiinfektiva Regionalverbandstagung Nord, Dr. Tobias Gräwert Dr. Boris Illarionov Prof. Dr. Markus Fischer www.hsfs.org Inhalt Warum sind neue Antibiotika
: Ein hervorragend geeigneter Angriffsort für neue Antiinfektiva Regionalverbandstagung Nord, Dr. Tobias Gräwert Dr. Boris Illarionov Prof. Dr. Markus Fischer www.hsfs.org Inhalt Warum sind neue Antibiotika
Es gibt 3 Ketonkörper:
 KETONKÖRPER Es gibt 3 Ketonkörper: O II CH3-C-CH2-COO ACETOACETAT CH3-C-CH2-COO I OH ß-HYDROXYBUTTERSÄURE O II CH3-C-CH3 ACETON (LYENENZYKLUS) Der Sinn der Ketogenese liegt darin, die s aus der ß-Oxidation
KETONKÖRPER Es gibt 3 Ketonkörper: O II CH3-C-CH2-COO ACETOACETAT CH3-C-CH2-COO I OH ß-HYDROXYBUTTERSÄURE O II CH3-C-CH3 ACETON (LYENENZYKLUS) Der Sinn der Ketogenese liegt darin, die s aus der ß-Oxidation
Vorlesung Rechtskunde und Toxikologie Biotransformation
 Vorlesung Rechtskunde und Toxikologie Biotransformation Prof. Dr. W. Dekant Institut für Toxikologie Universität Würzburg Biotransformationsenzyme Phase I! Cytochrom P-450! Flavin-abhängige Monooxygenasen!
Vorlesung Rechtskunde und Toxikologie Biotransformation Prof. Dr. W. Dekant Institut für Toxikologie Universität Würzburg Biotransformationsenzyme Phase I! Cytochrom P-450! Flavin-abhängige Monooxygenasen!
Biosynthese und Metabolismus von Nukleotiden
 Biosynthese und Metabolismus von ukleotiden Biochemie Die beiden Möglichkeiten... Zwei Möglichkeiten zur Bereitstellung von ukleotiden: 1) De-novo Synthese: Purine: ausgehend von Glycin (ca. 10 20 %) Pyrimidine:
Biosynthese und Metabolismus von ukleotiden Biochemie Die beiden Möglichkeiten... Zwei Möglichkeiten zur Bereitstellung von ukleotiden: 1) De-novo Synthese: Purine: ausgehend von Glycin (ca. 10 20 %) Pyrimidine:
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Mitochondriale Elektronentransportkette (Atmungskette)
 Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
Mitochondriale Elektronentransportkette (Atmungskette) Mitochondriale Elektronentransportkette (Atmungskette) Komplex I und II übetragen Elektronen auf Coenzym Q (Ubichinon) Gekoppelte Elektronen-Protonen
Biochemie von Pflanzeninhaltsstoffen
 Biochemie von Pflanzeninhaltsstoffen für Studierende der Agrar-, Lebensmittel- und Umweltnaturwissenschaften im 3.Semester WS 2004/5 nikolaus.amrhein@ipw.biol.ethz.ch Programm 12.01.2005: Sekundär- vs.
Biochemie von Pflanzeninhaltsstoffen für Studierende der Agrar-, Lebensmittel- und Umweltnaturwissenschaften im 3.Semester WS 2004/5 nikolaus.amrhein@ipw.biol.ethz.ch Programm 12.01.2005: Sekundär- vs.
BIOCHEMIE DER ERNÄHRUNG II Oxidation von Lipiden. Gastrointestinaltrakt. Fettsäureoxidation zu Acetyl-CoA
 xidation von Lipiden ß-xidation: Fettsäureoxidation zu Acetyl-oA BIEMIE DER ERNÄRUNG II 07.05.2012 wichtigste Fettsäurequelle in Nahrung: Triacylglyceride Import freier Fettsäuren ins ytosol oder Erzeugung
xidation von Lipiden ß-xidation: Fettsäureoxidation zu Acetyl-oA BIEMIE DER ERNÄRUNG II 07.05.2012 wichtigste Fettsäurequelle in Nahrung: Triacylglyceride Import freier Fettsäuren ins ytosol oder Erzeugung
Beispiele für Prüfungsfragen zu den Einheiten. 2, 3, 5, 9-12, 15, 16, und 21 (Hartig)
 Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Warnung: diese Klausur enthält nur die Fragen von Büchel und Sandmann, die Fragen von Schleiff/Scharf fehlen
 Klausurfragen Pflanzenphysiologie 19 Feb 2009 Warnung: diese Klausur enthält nur die Fragen von Büchel und Sandmann, die Fragen von Schleiff/Scharf fehlen Pkt. 1. a) In welchen der genannten Proteine liegen
Klausurfragen Pflanzenphysiologie 19 Feb 2009 Warnung: diese Klausur enthält nur die Fragen von Büchel und Sandmann, die Fragen von Schleiff/Scharf fehlen Pkt. 1. a) In welchen der genannten Proteine liegen
Inhaltsverzeichnis. Einleitung...1
 Inhaltsverzeichnis Einleitung...1 1 Terpene...5 1.1 Monoterpene...6 1.2 Sesquiterpene...19 1.3 Diterpene...26 1.4 Sesterterpene...33 1.5 Triterpene...33 1.6 Tetraterpene...39 1.7 Polyisoprene...42 1.8
Inhaltsverzeichnis Einleitung...1 1 Terpene...5 1.1 Monoterpene...6 1.2 Sesquiterpene...19 1.3 Diterpene...26 1.4 Sesterterpene...33 1.5 Triterpene...33 1.6 Tetraterpene...39 1.7 Polyisoprene...42 1.8
Biosynthese und Enzymfamilien
 Biosynthese und Enzymfamilien The vast array of plant natural products can be viewed as the current status of nature s activities in combinatorial chemistry. R.A. Dixon Kombinatorische Chemie Technologie
Biosynthese und Enzymfamilien The vast array of plant natural products can be viewed as the current status of nature s activities in combinatorial chemistry. R.A. Dixon Kombinatorische Chemie Technologie
S. 45 Abbildung 3.11: Die Orientierung der Kernporenkomplexe ist hier versehentlich invertiert worden. Eine korrigierte Darstellung finden Sie hier:
 Liebe Leserin, lieber Leser, auf dieser Seite werden wir Sie kontinuierlich über im Buch entdeckte inhaltliche Fehler informieren; dabei sind in der aktuellen Liste insbesondere solche Fehler aufgelistet,
Liebe Leserin, lieber Leser, auf dieser Seite werden wir Sie kontinuierlich über im Buch entdeckte inhaltliche Fehler informieren; dabei sind in der aktuellen Liste insbesondere solche Fehler aufgelistet,
- Biochemieklausur Name: Matrikelnr.:
 07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Evolutionärer Vorteil als Grundlage zum Leben? Von Nadine Körtel Konrad-Adenauer Straße , Hainburg
 Phototrophe Lebensweise Evolutionärer Vorteil als Grundlage zum Leben? Von Nadine Körtel Konrad-Adenauer Straße 50 63512, Hainburg Gliederung Phototrophe Bakterien Endosymbiontentheorie Chloroplasten Pigmente
Phototrophe Lebensweise Evolutionärer Vorteil als Grundlage zum Leben? Von Nadine Körtel Konrad-Adenauer Straße 50 63512, Hainburg Gliederung Phototrophe Bakterien Endosymbiontentheorie Chloroplasten Pigmente
Oxidative Phosphorylierung
 BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
4. WACHSTUM. 4.1 Messung
 4. WACHSTUM 4. WACHSTUM 4.1 Messung 4. WACHSTUM 4.2 math. Beschreibung expon. Wachstum statische Kultur 4. WACHSTUM 4.3 Wachstumskurve kontinuierliche Kultur 4. WACHSTUM 4.5 Verfahren Chemostat Turbidostat
4. WACHSTUM 4. WACHSTUM 4.1 Messung 4. WACHSTUM 4.2 math. Beschreibung expon. Wachstum statische Kultur 4. WACHSTUM 4.3 Wachstumskurve kontinuierliche Kultur 4. WACHSTUM 4.5 Verfahren Chemostat Turbidostat
Photosystem=Antenne + Reaktionszentrum
 Lichtsammelkomplexe Hendrik Küpper, Vorlesungsreihe Einführung in Bau und Funktion der Pflanzen, Sommersemester 2012 Photosystem=Antenne + Reaktionszentrum Die Antennen absorbieren die Photonen und leiten
Lichtsammelkomplexe Hendrik Küpper, Vorlesungsreihe Einführung in Bau und Funktion der Pflanzen, Sommersemester 2012 Photosystem=Antenne + Reaktionszentrum Die Antennen absorbieren die Photonen und leiten
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Nach Terpenen und Kohlenhydraten nun eine weitere große Klasse an Naturstoffen
 260 17. Aminosäuren, Peptide ach Terpenen und Kohlenhydraten nun eine weitere große Klasse an aturstoffen 17.1 Übersicht Analog zu ydroxycarbonsäuren α-, β-, γ- Aminocarbonsäuren möglich: 2 3 2 2 α-amino-essigsäure
260 17. Aminosäuren, Peptide ach Terpenen und Kohlenhydraten nun eine weitere große Klasse an aturstoffen 17.1 Übersicht Analog zu ydroxycarbonsäuren α-, β-, γ- Aminocarbonsäuren möglich: 2 3 2 2 α-amino-essigsäure
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
1a. Welche Pigmente enthält der Lichtsammelkomplex II (LHCII) höherer Pflanzen? (Namen aller Pigmente für volle Punktzahl)
 1a. Welche Pigmente enthält der Lichtsammelkomplex II (LHCII) höherer Pflanzen? (Namen aller Pigmente für volle Punktzahl) 2,5 P. 1b. Wozu dienen Carotinoide in den Proteinkomplexen der Thylakoidmembran?
1a. Welche Pigmente enthält der Lichtsammelkomplex II (LHCII) höherer Pflanzen? (Namen aller Pigmente für volle Punktzahl) 2,5 P. 1b. Wozu dienen Carotinoide in den Proteinkomplexen der Thylakoidmembran?
Klausur zur Vorlesung Biochemie I im WS 2002/03 Lösungen
 Klausur zur Vorlesung Biochemie I im W 00/03 Lösungen am 17.0.003 von 14.15 15.45 Uhr Gebäude 4, aum 115 (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte amen (in Druckbuchstaben), Matrikelnummer
Klausur zur Vorlesung Biochemie I im W 00/03 Lösungen am 17.0.003 von 14.15 15.45 Uhr Gebäude 4, aum 115 (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte amen (in Druckbuchstaben), Matrikelnummer
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
Application Notes. Aracus
 Application Notes Aracus membrapure GmbH Wolfgang Küntscher Str. 14 16761 Hennigsdorf / Berlin Mail: info@membrapure.de Tel.: 03302 / 201 20 0 Fax: 03302 / 201 20 21 Index Physiological Extended 54 amino
Application Notes Aracus membrapure GmbH Wolfgang Küntscher Str. 14 16761 Hennigsdorf / Berlin Mail: info@membrapure.de Tel.: 03302 / 201 20 0 Fax: 03302 / 201 20 21 Index Physiological Extended 54 amino
Dendrogramm der Primaten
 Arbeitsblatt 1 Dargestellt ist ein Ausschnitt der DNA-Sequenz für das Enzym NAD- Polymerase, dass bei den Primatenarten Mensch(M), Schimpanse(S), Gorilla(G), Orang-Utan(O) und Gibbon(Gi) vorhanden ist.
Arbeitsblatt 1 Dargestellt ist ein Ausschnitt der DNA-Sequenz für das Enzym NAD- Polymerase, dass bei den Primatenarten Mensch(M), Schimpanse(S), Gorilla(G), Orang-Utan(O) und Gibbon(Gi) vorhanden ist.
Kapitel: C 1 -Stoffwechsel 28
 Kapitel: 1 -Stoffwechsel 28 Bedeutung des 1 -Stoffwechsels Viele biosynthetische Vorgänge erfordern die Addition einer 1 -Einheit an eine metabolische Vorstufe. Bei den meisten arboxylierungsreaktionen
Kapitel: 1 -Stoffwechsel 28 Bedeutung des 1 -Stoffwechsels Viele biosynthetische Vorgänge erfordern die Addition einer 1 -Einheit an eine metabolische Vorstufe. Bei den meisten arboxylierungsreaktionen
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Anhang 6.2.2: Gesamtliste der Microarray-Ergebnisse
 Anhang 6.2.2: Gesamtliste der Microarray-Ergebnisse Experimente mit n Wiederholungen und Standardabweichung () sind oberhalb der Tabelle angegeben. Experimente mit den flia- und flgm -Mutanten wurden mit
Anhang 6.2.2: Gesamtliste der Microarray-Ergebnisse Experimente mit n Wiederholungen und Standardabweichung () sind oberhalb der Tabelle angegeben. Experimente mit den flia- und flgm -Mutanten wurden mit
Vertiefendes Seminar zur Vorlesung Biochemie I Bearbeitung Übungsblatt 4
 Vertiefendes Seminar zur Vorlesung Biochemie I 20.11.2015 Bearbeitung Übungsblatt 4 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 20.11.2015 Bearbeitung Übungsblatt 4 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Glutamat auf Abwegen: Die trna-abhängige Tetrapyrrol-Biosynthese
 133 Glutamat auf Abwegen: Die trna-abhängige Tetrapyrrol-Biosynthese Jürgen Moser 1, Frederic Frère 1, Dirk W. Heinz 2, Dieter Jahn 1 & Wolf-Dieter Schubert 2 1 Institut für Mikrobiologie, Technische Universität
133 Glutamat auf Abwegen: Die trna-abhängige Tetrapyrrol-Biosynthese Jürgen Moser 1, Frederic Frère 1, Dirk W. Heinz 2, Dieter Jahn 1 & Wolf-Dieter Schubert 2 1 Institut für Mikrobiologie, Technische Universität
Bio und Anorganik? Thauer-Versuch. Rosenberg-Versuch. cytostatische Wirkung durch 8 ppm Platin in Lösung
 Bio und Anorganik? Rosenberg-Versuch ~ ähr-und Pufferlösung (Glukose, MgCl 2, 4 Cl) Platinelektroden Thauer-Versuch 4 2 + C 2 Archaeen C 4 + 2 2 Escherichia coli- Bakterien cytostatische Wirkung durch
Bio und Anorganik? Rosenberg-Versuch ~ ähr-und Pufferlösung (Glukose, MgCl 2, 4 Cl) Platinelektroden Thauer-Versuch 4 2 + C 2 Archaeen C 4 + 2 2 Escherichia coli- Bakterien cytostatische Wirkung durch
Vorlesung Zell- und Molekularbiologie von Naturstoffen
 Vorlesung Zell- und Molekularbiologie von Naturstoffen Inhalte Vorkommen und Biosynthese ausgewählter Beispiele Analyse von Naturstoffen Transport Evolution der Biosynthesewege von Naturstoffen Gentechnik/Biotechnologie
Vorlesung Zell- und Molekularbiologie von Naturstoffen Inhalte Vorkommen und Biosynthese ausgewählter Beispiele Analyse von Naturstoffen Transport Evolution der Biosynthesewege von Naturstoffen Gentechnik/Biotechnologie
Tetraether Lipide thermophiler Archaebakterien
 Tetraether Lipide thermophiler Archaebakterien GlycerolDialkylnoninol Synthese der Phytanyl-Gruppe aus Geranylgeranyl-PP (isoprenoid) C40 Kette mit verzweigten Methylgruppen und Cyclopentanringen Phospholipide,
Tetraether Lipide thermophiler Archaebakterien GlycerolDialkylnoninol Synthese der Phytanyl-Gruppe aus Geranylgeranyl-PP (isoprenoid) C40 Kette mit verzweigten Methylgruppen und Cyclopentanringen Phospholipide,
Biosynthese, Charakterisierung und Funktion von Chlorophyll-Vorstufen in der lichtabhängig ergrünenden Mutante C-2A' von Scenedesmus obliquus
 3 Biosynthese, Charakterisierung und Funktion von Chlorophyll-Vorstufen in der lichtabhängig ergrünenden Mutante C-2A' von Scenedesmus obliquus DISSERTATION Zur Erlangung des Doktorgrades der Naturwissenschaften
3 Biosynthese, Charakterisierung und Funktion von Chlorophyll-Vorstufen in der lichtabhängig ergrünenden Mutante C-2A' von Scenedesmus obliquus DISSERTATION Zur Erlangung des Doktorgrades der Naturwissenschaften
Inhaltsverzeichnis. Vorwort. Stoffe in Zellen 1 Wasser
 V Vorwort XI Stoffe in Zellen 1 Wasser 2 Bau- und Inhaltsstoffe der Zelle 3 Ribose und Desoxyribose 4 UV-Absorption von Tyrosin 5 Anthocyan-Blütenfarbstoffe 6 Rotkraut - Blaukraut 7 Warum ist die Kornblume
V Vorwort XI Stoffe in Zellen 1 Wasser 2 Bau- und Inhaltsstoffe der Zelle 3 Ribose und Desoxyribose 4 UV-Absorption von Tyrosin 5 Anthocyan-Blütenfarbstoffe 6 Rotkraut - Blaukraut 7 Warum ist die Kornblume
Biochemie II - Tutorium
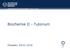 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Stoffwechselphysiologie der Pflanzen
 Stoffwechselphysiologie der Pflanzen I II Stoffwechselphysiologie der Pflanzen Physiologie und Biochemie des Primärund Sekundärstoffwechsels III Gerhard Richter 6., völlig neubearbeitete Auflage 186 Abbildungen
Stoffwechselphysiologie der Pflanzen I II Stoffwechselphysiologie der Pflanzen Physiologie und Biochemie des Primärund Sekundärstoffwechsels III Gerhard Richter 6., völlig neubearbeitete Auflage 186 Abbildungen
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Organische Chemie der biologischen Stoffwechselwege
 Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Springer-Lehrbuch. Naturstoffchemie. Eine Einführung. von Gerhard Habermehl, Peter Hammann, Hans Christoph Krebs, W. Ternes. erweitert, überarbeitet
 Springer-Lehrbuch Naturstoffchemie Eine Einführung von Gerhard Habermehl, Peter Hammann, Hans Christoph Krebs, W. Ternes erweitert, überarbeitet Naturstoffchemie Habermehl / Hammann / Krebs / et al. schnell
Springer-Lehrbuch Naturstoffchemie Eine Einführung von Gerhard Habermehl, Peter Hammann, Hans Christoph Krebs, W. Ternes erweitert, überarbeitet Naturstoffchemie Habermehl / Hammann / Krebs / et al. schnell
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Photosynthese, Teil 2
 Photosynthese, Teil 2 1 4. Synthese von Endprodukten der Kohlendioxid- Assimilation bzw. Verwertung der Assimilate primär entstehen Hexosen; ausgehend von den Triosen, Hexosen und verschiedenen Zwischenprodukten
Photosynthese, Teil 2 1 4. Synthese von Endprodukten der Kohlendioxid- Assimilation bzw. Verwertung der Assimilate primär entstehen Hexosen; ausgehend von den Triosen, Hexosen und verschiedenen Zwischenprodukten
52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat
 2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
Folsäure. Struktur = Pteroylglutamat; PteGLU n
 Folsäure Struktur = Pteroylglutamat; PteGLU n Biochemische Wirkungsweise Übertragung von C1-Einheiten; Wirksame Form ist das Tetrahydrofolat (H 4 -Folat), das durch Serin in das N 5,N 10 -Methylentetrahydrofolat
Folsäure Struktur = Pteroylglutamat; PteGLU n Biochemische Wirkungsweise Übertragung von C1-Einheiten; Wirksame Form ist das Tetrahydrofolat (H 4 -Folat), das durch Serin in das N 5,N 10 -Methylentetrahydrofolat
eine Vorlesung von Helmut Guttenberger
 eine Vorlesung von Helmut Guttenberger Allgemeine Biologie Einführung mit Geschichte Wichtigsten Baustoffe Zelle Anatomie Spross Blatt Wurzel Physiologie Wasserhaushalt Nährelemente Düngung Transport Fließgleichgewicht
eine Vorlesung von Helmut Guttenberger Allgemeine Biologie Einführung mit Geschichte Wichtigsten Baustoffe Zelle Anatomie Spross Blatt Wurzel Physiologie Wasserhaushalt Nährelemente Düngung Transport Fließgleichgewicht
Isoprenoids are involved in vital processes of all organisms. Their biosynthesis proceeds via two C 5 -building
 GcpE und LytB: Enzyme der Isoprenoid-Biosynthese als Angriffsziele für Wirkstoffe gegen Malaria und Tuberkulose GcpE and LytB: Enzymes of isoprenoid biosynthesis as targets for drugs against malaria and
GcpE und LytB: Enzyme der Isoprenoid-Biosynthese als Angriffsziele für Wirkstoffe gegen Malaria und Tuberkulose GcpE and LytB: Enzymes of isoprenoid biosynthesis as targets for drugs against malaria and
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
9. Übung zur Einführung in die Informatik (HaF) (Abschnitt IV: Rechnerstrukturen und Betriebssysteme) Musterlösung
 INFO V Bayerische Julius Maximilians Universität Würzburg Lehrstuhl für Technische Informatik Am Hubland 9774 Würzburg Tel. 93 888 7 Fax: 93 888 7 9. Übung zur Einführung in die Informatik HaF Abschnitt
INFO V Bayerische Julius Maximilians Universität Würzburg Lehrstuhl für Technische Informatik Am Hubland 9774 Würzburg Tel. 93 888 7 Fax: 93 888 7 9. Übung zur Einführung in die Informatik HaF Abschnitt
LIPIDE. Periphere Gruppe mit Cysteinylrest. FS-Synthase. Zentrale Gruppe Phosphopanthetinarm kovalente Bindung
 Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
Verfahren zu Strukturvorhersagen in vereinfachten Modellen. Tobias Voigt Sommerakademie 2002 St. Johann
 Verfahren zu Strukturvorhersagen in vereinfachten Modellen Tobias Voigt Sommerakademie 2002 St. Johann Einführung! Sequenzierung von Proteinen und Nukleinsäuren ist heute Routine! Die räumliche Struktur
Verfahren zu Strukturvorhersagen in vereinfachten Modellen Tobias Voigt Sommerakademie 2002 St. Johann Einführung! Sequenzierung von Proteinen und Nukleinsäuren ist heute Routine! Die räumliche Struktur
Biochemie Übungsblatt Nr Fettsäuresynthese:
 Fettsäuresynthese: 1) Mit Hilfe des mitochondriale ACP? AcetylCoA Carrboxylase (Biothin als prosth. Gruppe) AcetylCoA + Kohlendioxid + ATP MalonylCoA + ADP + P 2)? Reguliert durch Insulin (Insulin hemmt
Fettsäuresynthese: 1) Mit Hilfe des mitochondriale ACP? AcetylCoA Carrboxylase (Biothin als prosth. Gruppe) AcetylCoA + Kohlendioxid + ATP MalonylCoA + ADP + P 2)? Reguliert durch Insulin (Insulin hemmt
Gesundheitserziehung
 Gesundheitserziehung Lehrgang für BiologInnen Innsbruck, 09. - 10. November 2012 Ingo Wartusch Saurer Regen Problem: S-haltige Brennstoffe S + O 2 SO 2 SO 2 + 2 O 2 SO 3 2 SO 3 + 1/2 O 2 2 SO 4 --> pic
Gesundheitserziehung Lehrgang für BiologInnen Innsbruck, 09. - 10. November 2012 Ingo Wartusch Saurer Regen Problem: S-haltige Brennstoffe S + O 2 SO 2 SO 2 + 2 O 2 SO 3 2 SO 3 + 1/2 O 2 2 SO 4 --> pic
ORGANISCHE CHEMIE. Aminosäuren und Proteine
 RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
Ressourceneffiziente Produktionsverfahren für PHB- Biokunststoffe
 Projektverbund Ressourcenschonende Biotechnologie in Bayern Projektpräsentation Ressourceneffiziente Produktionsverfahren für PHB- Biokunststoffe Prof. Dr. Thomas Brück Dr. Norbert Mehlmer Technische Universität
Projektverbund Ressourcenschonende Biotechnologie in Bayern Projektpräsentation Ressourceneffiziente Produktionsverfahren für PHB- Biokunststoffe Prof. Dr. Thomas Brück Dr. Norbert Mehlmer Technische Universität
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Aliphatische Aminosäuren. Aromatische Aminosäuren
 Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte)
 Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
STOFFE (Physikalische, synthetische, analytische und theoretische Chemie)
 STOFFE (Physikalische, synthetische, analytische und theoretische Chemie) NATURSTOFFE (Organische, pharmazeutische, biologische Chemie, Biochemie) MINERALIEN (Anorganische Chemie, Geochemie, Mineralogie)
STOFFE (Physikalische, synthetische, analytische und theoretische Chemie) NATURSTOFFE (Organische, pharmazeutische, biologische Chemie, Biochemie) MINERALIEN (Anorganische Chemie, Geochemie, Mineralogie)
Michael Koch. Strukturanalyse der mitochondrialen Protoporphyrinogen IX Oxidase aus Nicotiana tabacum und von zwei weiteren Proteinen:
 Michael Koch Strukturanalyse der mitochondrialen Protoporphyrinogen IX xidase aus icotiana tabacum und von zwei weiteren Proteinen: Blaues Cupredoxin Umecyanin aus Meerrettich (Armoracia rusticana) Lumazinsynthase-W27Y-Mutante
Michael Koch Strukturanalyse der mitochondrialen Protoporphyrinogen IX xidase aus icotiana tabacum und von zwei weiteren Proteinen: Blaues Cupredoxin Umecyanin aus Meerrettich (Armoracia rusticana) Lumazinsynthase-W27Y-Mutante
1. Biochemie-Klausur Zahnmediziner, WS 03/04
 1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
Peptide. Peptidbindung. (Adapted from the handouts of Prof. AG Beck-Sickinger, Leipzig)
 Peptide Peptidbindung Alanin Glycin (Adapted from the handouts of Prof. AG Beck-Sickinger, Leipzig) Peptidbindung Bindungslänge in Å = - Kristallverband Gasphase 1,241 1,219 1,318 1,352 Dieder Winkel Φ
Peptide Peptidbindung Alanin Glycin (Adapted from the handouts of Prof. AG Beck-Sickinger, Leipzig) Peptidbindung Bindungslänge in Å = - Kristallverband Gasphase 1,241 1,219 1,318 1,352 Dieder Winkel Φ
Chemiosmotische Theorie Dunkelreaktionen Calvin-Zyklus, reduktiver Pentosephosphatzyklus,
 Wiederholung Lichtreaktionen 2 Photoreaktionen Chemiosmotische Theorie Dunkelreaktionen Calvin-Zyklus, reduktiver Pentosephosphatzyklus, C 3 -Zyklus Ribulose-1,5-bisphosphat, (C 6 ), 3-Phosphorglycerinsäure,
Wiederholung Lichtreaktionen 2 Photoreaktionen Chemiosmotische Theorie Dunkelreaktionen Calvin-Zyklus, reduktiver Pentosephosphatzyklus, C 3 -Zyklus Ribulose-1,5-bisphosphat, (C 6 ), 3-Phosphorglycerinsäure,
-Klausur Biochemie Name: Matrikelnr.:
 25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
