ICH Q7A Good Manufacturing Practice for Active Pharmaceutical Ingredients
|
|
|
- Josef Junge
- vor 5 Jahren
- Abrufe
Transkript
1 ICH Q7A GMP fur Wirkstoffe International Conference on Harmonization (ICH) ICH Q7A Good Manufacturing Practice for Active Pharmaceutical Ingredients CPMP/ICH/4106/00 Englisches Original und deutsche Ubersetzung Korrigierte 2. Auflage Ubersetzung: Stefanie Wnuck, Berlin Lektorat: Dr. Johanna Meske, Berlin
2 1 Einleitung Zielsetzung Anwendbarkeit Geltungsbereich 19 2 Qualitatsmanagement Prinzipien Verantwortlichkeiten der Qualitatssicherungseinheit(en) Verantwortung fur Produktionsaktivitaten Interne Audits (Selbstinspektion) Uberpriifung der Produktqualitat 39 3 Personal Personalqualifikation Personalhygiene Berater 43 4 Gebaude und Anlagen Design und Bauart Betriebsmittel Wasser Separate Bereiche Beleuchtung Abwasser und Abfall Betriebshygiene und Instandhaltung 55 5 Prozessausriistung Design und Bauart Wartutig und Reinigung der Ausriistung Kalibrierung Computergestutzte Systeme 67
3 INHALT 6 Dokumentation und Aufzeichnungen Dokumentationssysteme und Spezifikationen Aufzeichnungen zu Ausrustungsreinigung und -verwendung Aufzeichnungen zu Rohmaterialien, Zwischenprodukten, Wirkstoff-Etikettier- und Verpackungsmaterialien Muster-Herstellungsvorschriften (Master-Herstellungs- und Kontrollanweisungen) Chargenprotokoll (Chargenherstellungs- und -prufprotokolle) Prufprotokolle Uberprufung der Chargenherstellungsprotokolle 89 7 Materialmanagement Allgemeine Kontrollen Wareneingang und Quarantine Probenahme und Priifung eingehender Materialien fur die Produktion Lagerung Nachbewertung 99 8 Produktion und Inprozesskontrollen Produktionsaktivitaten Zeitbegrenzungen Inprozessprobenahme und-kontrollen Mischen von Zwischenprodukt- oder Wirkstoffchargen Kontaminationskontrolle Verpackung und Kennzeichnung zur Identifikation von Wirkstoffen und Zwischenprodukten Allgemeine Hinweise 115
4 9.2 Verpackungsmaterialien Vergabe und Kontrolle von Etiketten Verpackungs- und Kennzeichnungsvorgange Lagerung und Vertrieb Lagerverfahren Vertriebsverfahren Laborkontrollen Allgemeine Kontrollen Testen von Zwischenprodukten und Wirkstoffen Validierung von Priifverfahren - vgl. Abschnitt Analysenzertifikate Stabilitatsmonitoring bei Wirkstoften Festlegen von Verfalls- und Retestdaten Ruckstellmuster Validierung Validierungspolitik Validierungsdokumentation Qualifizierung Vorgehensweisen bei der Prozessvalidierung Prozessvalidierungsprogramm Periodische Uberprufung validierter Systeme Reinigungsvalidierung Validierung von Analysenmethoden Anderungskontrolle Zuriickweisung und Wiederverwendung von Materialien Zuruckweisung Aufarbeitung (reprocessing) 165
5 14.3 Umarbeitung (reworking) Ruckgewinnung von Materialien und Losungsmitteln Retouren Beanstandungen und Ruckrufe Lohnhersteller (einschlieglich Labors) Vertreter, Makler, Handler, GroBhandler, Umverpacker und Umetikettierer Anwendbarkeit Ruckverfolgbarkeit vertriebener Wirkstoffe Qualitatsmanagement Umverpackung, Umetikettierung und Lagerung von Wirkstoffen und Zwischenprodukten Stabilitat Weitergabe von Informationen Umgang mit Beanstandungen und Ruckrufen Umgang mit Retouren Spezif ische Anleitung fur Wirkstoffe, die mit Hilfe von Zellkulturen/Fermentation hergestellt werden Allgemeine Hinweise Zellbankwartung und -protokollierung Zellkultur/Fermentation Ernte, Isolation und Reinigung Schritte zur Virusbeseitigung und -inaktivierung Wirkstoffe fur klinische Prufungen Allgemeine Hinweise Qualitat Ausrustung und Anlagen Rohmaterialkontrolle 211
6 19.5 Produktion Validierung Anderungen Laborkontrollen Dokumentation Glossar 217 Stichworter 239
ICH Q7A Good Manufacturing Practice for Active Pharmaceutical Ingredients
 ICH Q7A GMP für Wirkstoffe International Conference on Harmonization (ICH) ICH Q7A Good Manufacturing Practice for Active Pharmaceutical Ingredients CPMP/ICH/4106/00 Englisches Original und deutsche Übersetzung
ICH Q7A GMP für Wirkstoffe International Conference on Harmonization (ICH) ICH Q7A Good Manufacturing Practice for Active Pharmaceutical Ingredients CPMP/ICH/4106/00 Englisches Original und deutsche Übersetzung
EU-GMP-LEITFADEN. Stand: Februar 2007 inkl. Aktualisierungs- und Erganzungslieferung
 EU-GMP-LEITFADEN Stand: Februar 2007 inkl. Aktualisierungs- und Erganzungslieferung Inhalt Inhalt Stichworter Gesamtglossar CD-ROM 1 Vorwort 2 Installationsvorgehen 3 Start des EU-GMP-LEITFADENS 1 Vorwort
EU-GMP-LEITFADEN Stand: Februar 2007 inkl. Aktualisierungs- und Erganzungslieferung Inhalt Inhalt Stichworter Gesamtglossar CD-ROM 1 Vorwort 2 Installationsvorgehen 3 Start des EU-GMP-LEITFADENS 1 Vorwort
Übersicht der Umstrukturierung
 F Regularien Schweiz und Österreich N.1 F.1 Regularien Schweiz N.1.1 F.1.1 Bundesgesetz über Arzneimittel und Medizinprodukte (Heilmittelgesetz, HMG) N.1.2 F.1.2 Verordnung über die Bewilligungen im Arzneimittelbereich
F Regularien Schweiz und Österreich N.1 F.1 Regularien Schweiz N.1.1 F.1.1 Bundesgesetz über Arzneimittel und Medizinprodukte (Heilmittelgesetz, HMG) N.1.2 F.1.2 Verordnung über die Bewilligungen im Arzneimittelbereich
EG-Leitfaden der Guten Herstellungspraxis
 pharmind serie dokumentation EG-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe / mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) von Gert Auterhoff Neuausgabe EG-Leitfaden
pharmind serie dokumentation EG-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe / mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) von Gert Auterhoff Neuausgabe EG-Leitfaden
Fragebogen Wirkstoffhersteller
 Firmenname: Produkt : Produktcode : 1. Allgemeine Fragen zum Wirkstoff Stellen Sie uns eine Wirkstoff- Spezifikation zur Verfügung? Existiert für den Wirkstoff ein Drug Master File (DMF)? Falls ja, kann
Firmenname: Produkt : Produktcode : 1. Allgemeine Fragen zum Wirkstoff Stellen Sie uns eine Wirkstoff- Spezifikation zur Verfügung? Existiert für den Wirkstoff ein Drug Master File (DMF)? Falls ja, kann
Leitfaden der Guten Herstellungspraxis. Teil II
 Anlage 3 zur Bekanntmachung des Bundesministeriums für Gesundheit zu 2 Nr. 3 der Arzneimittel- und Wirkstoffherstellungsverordnung vom 27. Oktober 2006 (Banz. S. 6887) Leitfaden der Guten Herstellungspraxis
Anlage 3 zur Bekanntmachung des Bundesministeriums für Gesundheit zu 2 Nr. 3 der Arzneimittel- und Wirkstoffherstellungsverordnung vom 27. Oktober 2006 (Banz. S. 6887) Leitfaden der Guten Herstellungspraxis
Name Bereich Information V.-Datum Bundesministerium für Gesundheit
 Page 1 of 70 Suchen Name Bereich Information V.-Datum Bundesministerium für Gesundheit Amtlicher Teil Bekanntmachung zu 2 Nummer 3 der Arzneimittel- und Wirkstoffherstellungsverordnung AMWHV vom: 21.04.2015
Page 1 of 70 Suchen Name Bereich Information V.-Datum Bundesministerium für Gesundheit Amtlicher Teil Bekanntmachung zu 2 Nummer 3 der Arzneimittel- und Wirkstoffherstellungsverordnung AMWHV vom: 21.04.2015
EG-Leitfaden einer Guten Herstellungspraxis fur Arzneimittel und Wirkstoffe
 EG-Leitfaden einer Guten Herstellungspraxis fur Arzneimittel und Wirkstoffe mit Betriebsverordnung fur pharmazeutische Unternehmer und GMP fur Wirkstoffe (ICH Q7A) Siebente, iiberarbeitete und erweiterte
EG-Leitfaden einer Guten Herstellungspraxis fur Arzneimittel und Wirkstoffe mit Betriebsverordnung fur pharmazeutische Unternehmer und GMP fur Wirkstoffe (ICH Q7A) Siebente, iiberarbeitete und erweiterte
EG-Leitfaden der Guten Herstellungspraxis
 pharmind serie dokumentation EG-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe / mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) von Gert Auterhoff Neuausgabe EG-Leitfaden
pharmind serie dokumentation EG-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe / mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) von Gert Auterhoff Neuausgabe EG-Leitfaden
EG-Leitfaden einer Guten Herstellungspraxis für Arzneimittel und Wirkstoffe
 pharmind Serie EG-Leitfaden einer Guten Herstellungspraxis für Arzneimittel und Wirkstoffe Mit Betriebsverordnung für pharmazeutische Unternehmer von G. Auterhoff erweitert, überarbeitet EG-Leitfaden einer
pharmind Serie EG-Leitfaden einer Guten Herstellungspraxis für Arzneimittel und Wirkstoffe Mit Betriebsverordnung für pharmazeutische Unternehmer von G. Auterhoff erweitert, überarbeitet EG-Leitfaden einer
ICH Q7A: Wirkstoffe aus natürlichen Quellen für klinische und kommerzielle Zwecke
 ICH Q7A: Wirkstoffe aus natürlichen Quellen für klinische und kommerzielle Zwecke Dr. Eric J.M. Meier 1 Pentapharm Ltd 2005 Wirkstoffe aus natürlichen Quellen Einführung Wirkstoffe für kommerzielle Zwecke
ICH Q7A: Wirkstoffe aus natürlichen Quellen für klinische und kommerzielle Zwecke Dr. Eric J.M. Meier 1 Pentapharm Ltd 2005 Wirkstoffe aus natürlichen Quellen Einführung Wirkstoffe für kommerzielle Zwecke
QUALITATSSICHERUNC. der fiktiven Firma Muster" für die Arzneimittelherstellung. einschl. verwandter Produkte. Dritte Auflage 1998
 QUALITATSSICHERUNC Qualitätssicherungshandbuch der fiktiven Firma Muster" für die Arzneimittelherstellung einschl. verwandter Produkte Dritte Auflage 98 Bundesfachverband der Arzneimittelhersteller e.v.
QUALITATSSICHERUNC Qualitätssicherungshandbuch der fiktiven Firma Muster" für die Arzneimittelherstellung einschl. verwandter Produkte Dritte Auflage 98 Bundesfachverband der Arzneimittelhersteller e.v.
Medizinische Dokumentare in der pharmazeutischen Produktion: GMP Good Manufacturing Practice und eine Ganze Menge Papier!
 Medizinische Dokumentare in der pharmazeutischen Produktion: GMP Good Manufacturing Practice und eine Ganze Menge Papier! Medizinisches Informationsmanagement 3.0 11. DVMD Fachtagung in Hannover 17. Februar
Medizinische Dokumentare in der pharmazeutischen Produktion: GMP Good Manufacturing Practice und eine Ganze Menge Papier! Medizinisches Informationsmanagement 3.0 11. DVMD Fachtagung in Hannover 17. Februar
Änderungskontrolle. Anforderungen / Zitate aus den Rechtsvorschriften
 Änderungskontrolle Anforderungen / Zitate aus den Rechtsvorschriften Definition im Glossar zum Annex 15 (Qualifizierung und Validierung) des EU-GMP-Leitfadens: Die Änderungskontrolle ist ein formales System,
Änderungskontrolle Anforderungen / Zitate aus den Rechtsvorschriften Definition im Glossar zum Annex 15 (Qualifizierung und Validierung) des EU-GMP-Leitfadens: Die Änderungskontrolle ist ein formales System,
Inhaltsverzeichnis IVZ. Vorwort der Herausgeber zur 1. Auflage 5. Die Autoren 7. 1 Audits und Inspektionen 17
 Vorwort der Herausgeber zur 1. Auflage 5 Die Autoren 7 1 Audits und Inspektionen 17 1.A Grundsätze 21 1.A.1 Begriffe 21 1.A.2 Rechtliche Aspekte 23 1.A.3 Anlässe für Audits 23 1.A.4 Kernforderungen an
Vorwort der Herausgeber zur 1. Auflage 5 Die Autoren 7 1 Audits und Inspektionen 17 1.A Grundsätze 21 1.A.1 Begriffe 21 1.A.2 Rechtliche Aspekte 23 1.A.3 Anlässe für Audits 23 1.A.4 Kernforderungen an
Leitfaden der Guten Herstellungspraxis
 Leitfaden der Guten Herstellungspraxis Teil II Wirkstoffe Grundlegende Anforderungen für Wirkstoffe zur Verwendung als Ausgangsstoffe Status des Dokuments: Überarbeitung Begründung der Änderungen: Überarbeitung
Leitfaden der Guten Herstellungspraxis Teil II Wirkstoffe Grundlegende Anforderungen für Wirkstoffe zur Verwendung als Ausgangsstoffe Status des Dokuments: Überarbeitung Begründung der Änderungen: Überarbeitung
Dipl.-Phys. Dr. Horst Weißsieker
 1 ULG Reinraumtechnik Modul «Reinraumbetrieb» Block 16: Reinraumbetrieb - Grundlagen Eine Übersicht und Einordnung VDI 2083 Reinraumtechnik Status heute Laufende Projekte VDI 2083/9.2 Verbrauchsmaterialien
1 ULG Reinraumtechnik Modul «Reinraumbetrieb» Block 16: Reinraumbetrieb - Grundlagen Eine Übersicht und Einordnung VDI 2083 Reinraumtechnik Status heute Laufende Projekte VDI 2083/9.2 Verbrauchsmaterialien
GMP-Konformität ausländischer Wirkstoffhersteller
 GMP-Konformität ausländischer Wirkstoffhersteller Michel Keller, Swissmedic März 2005: GMP-Konformität 1 Überblick Gesetzliche Anforderungen in der CH Infos zum GMP-Status ausländischer Hersteller Situation
GMP-Konformität ausländischer Wirkstoffhersteller Michel Keller, Swissmedic März 2005: GMP-Konformität 1 Überblick Gesetzliche Anforderungen in der CH Infos zum GMP-Status ausländischer Hersteller Situation
GDP-Audit-Checkliste. GMP-Audit-Checkliste. für Lagerung und Transport von Arzneimitteln
 GDP-Audit-Checkliste für Lagerung und Transport von Arzneimitteln Über 700 Fragen mit Referenzen zu GMP-Regelwerken zur Vorbereitung und Durchführung von GDP-Audits PDF Download GMP-Audit-Checkliste Wichtiger
GDP-Audit-Checkliste für Lagerung und Transport von Arzneimitteln Über 700 Fragen mit Referenzen zu GMP-Regelwerken zur Vorbereitung und Durchführung von GDP-Audits PDF Download GMP-Audit-Checkliste Wichtiger
Ansicht Anzeigen Haken bei Führungslinien setzten Start Folien Zurücksetzen Basiswissen GMP
 Basiswissen GMP Inhalt: Vorgaben Gesetzliche Grundlagen Vorschriften B-CH SRK Vereinbarungen mit Fraktionierern GMP Bedeutung/Definition Was ist GMP? Was regelt GMP? Was machen wir damit? Swiss Transfusion
Basiswissen GMP Inhalt: Vorgaben Gesetzliche Grundlagen Vorschriften B-CH SRK Vereinbarungen mit Fraktionierern GMP Bedeutung/Definition Was ist GMP? Was regelt GMP? Was machen wir damit? Swiss Transfusion
Inhaltsverzeichnis. I Auditierung nach IFS 5. Vorwort...5 Hinweis zum Umgang mit der Broschüre...6 Autorenverzeichnis...7
 Inhaltsverzeichnis Vorwort...5 Hinweis zum Umgang mit der Broschüre...6 Autorenverzeichnis...7 I Auditierung nach IFS 5 1 Änderungen des IFS, Version 5...15 1.1 Ab wann muss der neue Standard verwendet
Inhaltsverzeichnis Vorwort...5 Hinweis zum Umgang mit der Broschüre...6 Autorenverzeichnis...7 I Auditierung nach IFS 5 1 Änderungen des IFS, Version 5...15 1.1 Ab wann muss der neue Standard verwendet
Anlage der Bekanntmachung zu 2 Nummer 3 der Arzneimittel- und Wirkstoffherstellungsverordnung AMWHV im Bundesanzeiger vom 27. Mai 2015.
 Anlage der Bekanntmachung zu 2 Nummer 3 der Arzneimittel- und Wirkstoffherstellungsverordnung AMWHV im Bundesanzeiger vom 27. Mai 2015 EudraLex Vorschriften für Arzneimittel in der Europäischen Union,
Anlage der Bekanntmachung zu 2 Nummer 3 der Arzneimittel- und Wirkstoffherstellungsverordnung AMWHV im Bundesanzeiger vom 27. Mai 2015 EudraLex Vorschriften für Arzneimittel in der Europäischen Union,
Intensivseminar. Der GMP-Spezialist - für QS, QK, Produktion und Technik -
 Intensivseminar Der GMP-Spezialist - für QS, QK, Produktion und Technik - DER GMP-SPEZIALIST Zielsetzung: Die Anforderungen der Good Manufacturing Practices stellen ein komplexes und stark interpretierbares
Intensivseminar Der GMP-Spezialist - für QS, QK, Produktion und Technik - DER GMP-SPEZIALIST Zielsetzung: Die Anforderungen der Good Manufacturing Practices stellen ein komplexes und stark interpretierbares
Prof. Dr. Werner Fresenius / Vorsitzender AG AAMP. Tierarzneimittelbereich: Dr. Heinrich Bottermann / Vorsitzender AG AfAM. <Oberste Landesbehörde>
 Dokumenten-Nr.: 07110702 Verfahrensanweisung Gültig ab: Zentralstelle der Länder für Gesundheitsschutz bei Arzneimiteln und Medizinprodukten 1/5 Titel: Site Master File (SMF) Geltungsbereich: Inspektorat
Dokumenten-Nr.: 07110702 Verfahrensanweisung Gültig ab: Zentralstelle der Länder für Gesundheitsschutz bei Arzneimiteln und Medizinprodukten 1/5 Titel: Site Master File (SMF) Geltungsbereich: Inspektorat
Inhaltsverzeichnis. I Auditierung nach IFS 5. Vorwort 5 Hinweis zum Umgang mit der Broschüre 6 Autorenverzeichnis 7
 Vorwort 5 Hinweis zum Umgang mit der Broschüre 6 Autorenverzeichnis 7 I Auditierung nach IFS 5 1 Änderungen des IFS, Version 5 15 1.1 Ab wann muss der neue Standard verwendet werden? 15 1.2 Was sind die
Vorwort 5 Hinweis zum Umgang mit der Broschüre 6 Autorenverzeichnis 7 I Auditierung nach IFS 5 1 Änderungen des IFS, Version 5 15 1.1 Ab wann muss der neue Standard verwendet werden? 15 1.2 Was sind die
Unterschiede zwischen Wirkstoffund Arzneimittelherstellung
 Unterschiede zwischen Wirkstoffund Arzneimittelherstellung Teil 2: Materialmanagement, Analysenzertifikate, Validierung und Qualifizierung* ) Dr. Rainer Gnibl Zentrale Arzneimittelüberwachung Bayern (ZAB),
Unterschiede zwischen Wirkstoffund Arzneimittelherstellung Teil 2: Materialmanagement, Analysenzertifikate, Validierung und Qualifizierung* ) Dr. Rainer Gnibl Zentrale Arzneimittelüberwachung Bayern (ZAB),
Problematische Punkte bei Inspektionen aus Sicht der Behörden
 Problematische Punkte bei Inspektionen aus Sicht der Behörden Dr. Josiane Tinguely Casserini, stv. Kantonsapothekerin Agieren statt reagieren Punkte, die dem KAPA besonders am Herzen liegen, weil es z.t.
Problematische Punkte bei Inspektionen aus Sicht der Behörden Dr. Josiane Tinguely Casserini, stv. Kantonsapothekerin Agieren statt reagieren Punkte, die dem KAPA besonders am Herzen liegen, weil es z.t.
QUALITÄTSSICHERUNGSHANDBUCH
 Abteilung Erstellungsdatum: 22.10.2008 Seite 1 von 23 QUALITÄTSSICHERUNGSHANDBUCH Heinrich Klenk GmbH & Co. KG D ASCHENHOF 35 97525 Schwebheim Tel.: 0049 9723 60941 Fax.: 0049 9723 60935 www.klenk-herbline.de
Abteilung Erstellungsdatum: 22.10.2008 Seite 1 von 23 QUALITÄTSSICHERUNGSHANDBUCH Heinrich Klenk GmbH & Co. KG D ASCHENHOF 35 97525 Schwebheim Tel.: 0049 9723 60941 Fax.: 0049 9723 60935 www.klenk-herbline.de
Anhang 19 zum EG-Leitfaden der Guten Herstellungspraxis 1
 Anhang 19 Anlage 2 zur Bekanntmachung des Bundesministeriums für Gesundheit zu 2 Nr. 3 der Arzneimittel- und Wirkstoffherstellungsverordnung vom 18. April 2007 (BAnz. S. 4826) Anhang 19 zum EG-Leitfaden
Anhang 19 Anlage 2 zur Bekanntmachung des Bundesministeriums für Gesundheit zu 2 Nr. 3 der Arzneimittel- und Wirkstoffherstellungsverordnung vom 18. April 2007 (BAnz. S. 4826) Anhang 19 zum EG-Leitfaden
Johann Harer ANFORDERUNGEN AN MEDIZINPRODUKTE. Praxisleitfaden für Hersteller und Zulieferer. 2., überarbeitete Auflage HANSER
 Johann Harer ANFORDERUNGEN AN MEDIZINPRODUKTE Praxisleitfaden für Hersteller und Zulieferer 2., überarbeitete Auflage HANSER Inhalt 1 QM-Systeme 1 1.1 Einleitung 1 1.2 Die wesentlichen Anforderungen der
Johann Harer ANFORDERUNGEN AN MEDIZINPRODUKTE Praxisleitfaden für Hersteller und Zulieferer 2., überarbeitete Auflage HANSER Inhalt 1 QM-Systeme 1 1.1 Einleitung 1 1.2 Die wesentlichen Anforderungen der
Stellenbeschreibung Fachtechnisch verantwortliche Person (FvP) Pharmalogistik
 Stellenbeschreibung (FvP) Pharmalogistik Funktionsbezeichnung: Vorgesetzte Stelle: Stellvertreter: Frau Monika Muster Herr Markus Muster Anforderungen an die Schweizer Gesetzgebung Die FvP respektiert
Stellenbeschreibung (FvP) Pharmalogistik Funktionsbezeichnung: Vorgesetzte Stelle: Stellvertreter: Frau Monika Muster Herr Markus Muster Anforderungen an die Schweizer Gesetzgebung Die FvP respektiert
Dokumentenübersicht Revision vom Ersteller/-in Verteiler Grund der letzten Änderung
 Handbuch Kapitel 1 und 2 Anwendungsbereich & Normative Verweise 0 BdoL BdoL Kapitel 3 Begriffe Abkürzungen 0 BdoL BdoL Kapitel 4 Qualitätsmanagementsystem 0 BdoL BdoL Kapitel 5 Verantwortung der Leitung
Handbuch Kapitel 1 und 2 Anwendungsbereich & Normative Verweise 0 BdoL BdoL Kapitel 3 Begriffe Abkürzungen 0 BdoL BdoL Kapitel 4 Qualitätsmanagementsystem 0 BdoL BdoL Kapitel 5 Verantwortung der Leitung
Richtlinien der IKS betreffend die Herstellung von Arzneimitteln (Herstellungs-Richtlinien)
 Herstellungs-Richtlinien 812.22 Richtlinien der IKS betreffend die Herstellung von Arzneimitteln (Herstellungs-Richtlinien) (vom 18. Mai 1995). 1 Von der Konferenz der Interkantonalen Vereinigung für die
Herstellungs-Richtlinien 812.22 Richtlinien der IKS betreffend die Herstellung von Arzneimitteln (Herstellungs-Richtlinien) (vom 18. Mai 1995). 1 Von der Konferenz der Interkantonalen Vereinigung für die
Anforderungen an die gebindeweise Garantierung der Identität von Ausgangsstoffen
 Anforderungen an die gebindeweise Garantierung der Identität Dokument gültig ab: 9. Mai 2014 Dokumentennummer: I-SMI.TI.10 Version 03 Klassifizierung: öffentlich Ersetzt Dokument: I-SMI.TI.10_02 vom: 01.11.2007
Anforderungen an die gebindeweise Garantierung der Identität Dokument gültig ab: 9. Mai 2014 Dokumentennummer: I-SMI.TI.10 Version 03 Klassifizierung: öffentlich Ersetzt Dokument: I-SMI.TI.10_02 vom: 01.11.2007
Teil A Rili-BÄK 2008 Vertiefungsmodul. Peter Ackermann, Bio-Rad Laboratories GmbH
 Teil A Rili-BÄK 2008 Vertiefungsmodul Peter Ackermann, Bio-Rad Laboratories GmbH Neue Rili-BÄK Teil A Beschreibt die grundlegenden Anforderungen an die Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
Teil A Rili-BÄK 2008 Vertiefungsmodul Peter Ackermann, Bio-Rad Laboratories GmbH Neue Rili-BÄK Teil A Beschreibt die grundlegenden Anforderungen an die Qualitätssicherung laboratoriumsmedizinischer Untersuchungen
ISO Qualitätsmanagement prozessorientiert umsetzen
 ISO 9001 - Qualitätsmanagement prozessorientiert umsetzen Bearbeitet von Michael Cassel 1. Auflage 2007. Buch. XII, 283 S. Hardcover ISBN 978 3 446 22731 6 Format (B x L): 17,4 x 24,7 cm Gewicht: 678 g
ISO 9001 - Qualitätsmanagement prozessorientiert umsetzen Bearbeitet von Michael Cassel 1. Auflage 2007. Buch. XII, 283 S. Hardcover ISBN 978 3 446 22731 6 Format (B x L): 17,4 x 24,7 cm Gewicht: 678 g
Die Qualitätspolitik von Heinrich KLENK
 Abteilung Erstellungsdatum: 11.09.2008 Seite 1 von 9 INHALT 1. Zweck und Zielsetzung 2 2. Anwendungsbereich 2 3. Definitionen 4. Verantwortlichkeiten SEITE 5. Durchführung 4 5.1. Vorgehen und Abläufe 4
Abteilung Erstellungsdatum: 11.09.2008 Seite 1 von 9 INHALT 1. Zweck und Zielsetzung 2 2. Anwendungsbereich 2 3. Definitionen 4. Verantwortlichkeiten SEITE 5. Durchführung 4 5.1. Vorgehen und Abläufe 4
Noch ausführlicher als dieses Gesamtinhaltsverzeichnis sind die Kapitelinhaltsverzeichnisse vor den einzelnen Kapitel 1 bis 23 und A bis L.
 sverzeichnis sverzeichnis Noch ausführlicher als dieses Gesamtinhaltsverzeichnis sind die Kapitelinhaltsverzeichnisse vor den einzelnen Kapitel 1 bis 23 und A bis L. Die Autoren Informationen Glossar Abkürzungen
sverzeichnis sverzeichnis Noch ausführlicher als dieses Gesamtinhaltsverzeichnis sind die Kapitelinhaltsverzeichnisse vor den einzelnen Kapitel 1 bis 23 und A bis L. Die Autoren Informationen Glossar Abkürzungen
Stellenbeschreibung Fachtechnisch verantwortliche Person (FvP) Pharmalogistik
 Stellenbeschreibung Fachtechnisch verantwortliche Person (FvP) Pharmalogistik Funktionsbezeichnung: Stellvertreter: Fachtechnisch verantwortliche Person Herr Markus Muster Anforderungen an die Schweizer
Stellenbeschreibung Fachtechnisch verantwortliche Person (FvP) Pharmalogistik Funktionsbezeichnung: Stellvertreter: Fachtechnisch verantwortliche Person Herr Markus Muster Anforderungen an die Schweizer
Kapitel 6 Qualitätskontrolle
 Kapitel 6 Qualitätskontrolle Rechtsgrundlage zur Veröffentlichung des Leitfadens: Artikel 47 der Richtlinie 2001/83/EG zur Schaffung eines Gemeinschaftskodexes für Humanarzneimittel und Artikel 51 der
Kapitel 6 Qualitätskontrolle Rechtsgrundlage zur Veröffentlichung des Leitfadens: Artikel 47 der Richtlinie 2001/83/EG zur Schaffung eines Gemeinschaftskodexes für Humanarzneimittel und Artikel 51 der
GMP Entwicklung 2012/ GMP-Gesprächskreis in Niedersachsen 20. Februar 2013
 GMP Entwicklung 2012/2013 5. GMP-Gesprächskreis in Niedersachsen 20. Februar 2013 EU Neue Leitlinien und Regeln (Auswahl) GMP-Leitfaden Kapitel 1 Pharmaceutical Quality System Kapitel 3 Räume und Einrichtungen
GMP Entwicklung 2012/2013 5. GMP-Gesprächskreis in Niedersachsen 20. Februar 2013 EU Neue Leitlinien und Regeln (Auswahl) GMP-Leitfaden Kapitel 1 Pharmaceutical Quality System Kapitel 3 Räume und Einrichtungen
R H I. R e g i o n a l e s H e i l m i t t e l i n s p e k t o r a t d e r N o r d w e s t s c h w e i z
 R H I R e g i o n a l e s H e i l m i t t e l i n s p e k t o r a t d e r N o r d w e s t s c h w e i z Checkliste zur Vorbereitung der Inspektion in Praxisapotheken von Ärzten und Ärztinnen 1. Einführungsgespräch
R H I R e g i o n a l e s H e i l m i t t e l i n s p e k t o r a t d e r N o r d w e s t s c h w e i z Checkliste zur Vorbereitung der Inspektion in Praxisapotheken von Ärzten und Ärztinnen 1. Einführungsgespräch
(Rechtsakte ohne Gesetzescharakter) VERORDNUNGEN
 25.11.2014 L 337/1 II (Rechtsakte ohne Gesetzescharakter) VERORDNUNGEN LEGIERTE VERORDNUNG (EU) Nr. 1252/2014 R KOMMISSION vom 28. Mai 2014 zur Ergänzung der Richtlinie 2001/83/EG des Europäischen Parlaments
25.11.2014 L 337/1 II (Rechtsakte ohne Gesetzescharakter) VERORDNUNGEN LEGIERTE VERORDNUNG (EU) Nr. 1252/2014 R KOMMISSION vom 28. Mai 2014 zur Ergänzung der Richtlinie 2001/83/EG des Europäischen Parlaments
ISO 9001: Einleitung. 1 Anwendungsbereich. 2 Normative Verweisungen. 4 Qualitätsmanagementsystem. 4.1 Allgemeine Anforderungen
 DIN EN ISO 9001 Vergleich ISO 9001:2015 und ISO 9001:2015 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe 4 Kontext der Organisation 4.1 Verstehen der Organisation und ihres Kontextes
DIN EN ISO 9001 Vergleich ISO 9001:2015 und ISO 9001:2015 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe 4 Kontext der Organisation 4.1 Verstehen der Organisation und ihres Kontextes
Kapitel 2 Personal. Grundsätze. Allgemeine Anforderungen
 Kapitel 2 Personal Rechtsgrundlage zur Veröffentlichung des Leitfadens: Artikel 47 der Richtlinie 2001/83/EG zur Schaffung eines Gemeinschaftskodexes für Humanarzneimittel und Artikel 51 der Richtlinie
Kapitel 2 Personal Rechtsgrundlage zur Veröffentlichung des Leitfadens: Artikel 47 der Richtlinie 2001/83/EG zur Schaffung eines Gemeinschaftskodexes für Humanarzneimittel und Artikel 51 der Richtlinie
Neue Verpackungsstandards. IFS PACsecure und FSSC Verpackungen
 Neue Verpackungsstandards IFS PACsecure und FSSC 22000 Verpackungen 22.3.2013 Hygienemanagementsysteme für Verpackungen Die wichtigsten Verpackungsstandards.. BRC Global Standard for Packaging and Packaging
Neue Verpackungsstandards IFS PACsecure und FSSC 22000 Verpackungen 22.3.2013 Hygienemanagementsysteme für Verpackungen Die wichtigsten Verpackungsstandards.. BRC Global Standard for Packaging and Packaging
Kanton Bern. Heiminspektorat. Dr. pharm. Josiane Tinguely Casserini, Stv. Kantonsapothekerin. Gesundheits- und Fürsorgedirektion des Kantons Bern
 Heiminspektorat Dr. pharm. Josiane Tinguely Casserini, Stv. Kantonsapothekerin 1.a Organisation des Inspektorates Millizinspektorat Inspektoren sind Apotheker und Apothekerinnen, die vom Regierungsrat
Heiminspektorat Dr. pharm. Josiane Tinguely Casserini, Stv. Kantonsapothekerin 1.a Organisation des Inspektorates Millizinspektorat Inspektoren sind Apotheker und Apothekerinnen, die vom Regierungsrat
ISO/TS Qualitätsmanagement in der Automobilindustrie umsetzen
 ISO/TS 16949 - Qualitätsmanagement in der Automobilindustrie umsetzen Michael Cassel ISBN 3-446-22729-6 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/3-446-22729-6
ISO/TS 16949 - Qualitätsmanagement in der Automobilindustrie umsetzen Michael Cassel ISBN 3-446-22729-6 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/3-446-22729-6
Medizinische Gase. Arzneimittel und Medizinprodukte der Westfalen AG.
 Medizinische Gase. Arzneimittel und Medizinprodukte der Westfalen AG. Fertigarzneimittel der Westfalen AG. Sauerstoff für medizinische Zwecke (gasförmig) Hierzu nutzt die Westfalen AG die Standardzulassung
Medizinische Gase. Arzneimittel und Medizinprodukte der Westfalen AG. Fertigarzneimittel der Westfalen AG. Sauerstoff für medizinische Zwecke (gasförmig) Hierzu nutzt die Westfalen AG die Standardzulassung
Verwendung (zertifizierter) Referenzmaterialien zur Bestimmung von Mykotoxinen. Dr. Irene Hahn
 Verwendung (zertifizierter) Referenzmaterialien zur Bestimmung von Mykotoxinen Dr. Irene Hahn Begriffe und Definitionen Referenzmaterial (RM) Ausreichend homogen Stabil hinsichtlich einer oder mehrerer
Verwendung (zertifizierter) Referenzmaterialien zur Bestimmung von Mykotoxinen Dr. Irene Hahn Begriffe und Definitionen Referenzmaterial (RM) Ausreichend homogen Stabil hinsichtlich einer oder mehrerer
Für maximale Sicherheit. GMP-Ethanol. BrüggemannAlcohol Heilbronn GmbH
 Für maximale Sicherheit GMP-Ethanol BrüggemannAlcohol Heilbronn GmbH Unser GMP-Ethanol maximale Sicherheit für Sie! Unter GMP ( Good Manufacturing Practice ) versteht man die Gute Herstellungspraxis. Wesentliche
Für maximale Sicherheit GMP-Ethanol BrüggemannAlcohol Heilbronn GmbH Unser GMP-Ethanol maximale Sicherheit für Sie! Unter GMP ( Good Manufacturing Practice ) versteht man die Gute Herstellungspraxis. Wesentliche
1 Einführung. Gerd Kutz und Armin Wolff. 1.1 Zielsetzungen
 1 1 Einführung Gerd Kutz und Armin Wolff 1.1 Zielsetzungen Neue Arzneistoffe zu finden oder bekannte zu optimieren, ist die schwerste Aufgabe innerhalb der pharmazeutischen Forschung. Ebenso ist es eine
1 1 Einführung Gerd Kutz und Armin Wolff 1.1 Zielsetzungen Neue Arzneistoffe zu finden oder bekannte zu optimieren, ist die schwerste Aufgabe innerhalb der pharmazeutischen Forschung. Ebenso ist es eine
Prüfbericht. Geprüfte Qualität -
 Seite 1 von 7 Name Straße PLZ Ort Ansprechpartner Tel.- Fax E-Mail Erstkontrolle Folgekontrolle Nachkontrolle Stichprobenkontrolle Kontrolle nicht durchgeführt, weil Zeichennutzung Zulassungs- des Betriebs:
Seite 1 von 7 Name Straße PLZ Ort Ansprechpartner Tel.- Fax E-Mail Erstkontrolle Folgekontrolle Nachkontrolle Stichprobenkontrolle Kontrolle nicht durchgeführt, weil Zeichennutzung Zulassungs- des Betriebs:
Dienstleistung Produktion, Lagerung, Kommissionierung und Logistik
 Julius Hoesch GmbH & Co. KG Dienstleistung Produktion, Lagerung, Kommissionierung und Logistik Leistungs- /Serviceangebot Julius Hoesch Düren GmbH & Co. KG Birkesdorfer Straße 5 52353 Düren-Hoven Tel +49
Julius Hoesch GmbH & Co. KG Dienstleistung Produktion, Lagerung, Kommissionierung und Logistik Leistungs- /Serviceangebot Julius Hoesch Düren GmbH & Co. KG Birkesdorfer Straße 5 52353 Düren-Hoven Tel +49
Die Kontrolle durch die Lebensmittelaufsicht. Die geltende VA - K Steppert Stefan Lebensmittelinspektor
 Die Kontrolle durch die Lebensmittelaufsicht Die geltende VA - K 0211.06 Steppert Stefan Lebensmittelinspektor Lebensmittelkontrolle in NÖ Aufbau der NÖ Lebensmittelaufsicht: Bundesministerium für Gesundheit
Die Kontrolle durch die Lebensmittelaufsicht Die geltende VA - K 0211.06 Steppert Stefan Lebensmittelinspektor Lebensmittelkontrolle in NÖ Aufbau der NÖ Lebensmittelaufsicht: Bundesministerium für Gesundheit
Produktvorstellung. Seiler. Musterbeispiel Medizin mit DIN EN ISO 13485:2015
 Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel Medizin mit DIN EN ISO 13485:2015 en Zielgruppe: Medizinprodukteherstellung Inverkehrbringung von Medizinprodukten Egal was Du tust, mach es
Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel Medizin mit DIN EN ISO 13485:2015 en Zielgruppe: Medizinprodukteherstellung Inverkehrbringung von Medizinprodukten Egal was Du tust, mach es
Prüfbericht. Geprüfte Qualität -
 Seite 1 von 7 Name Straße PLZ Ort Ansprechpartner Tel.- Fax E-Mail Erstkontrolle Folgekontrolle Nachkontrolle Stichprobenkontrolle Kontrolle nicht durchgeführt, weil Zeichennutzung Regionalsiegel Geprüfte
Seite 1 von 7 Name Straße PLZ Ort Ansprechpartner Tel.- Fax E-Mail Erstkontrolle Folgekontrolle Nachkontrolle Stichprobenkontrolle Kontrolle nicht durchgeführt, weil Zeichennutzung Regionalsiegel Geprüfte
Herzlich Willkommen!!! zum IWL Pharma Workshop am in Ulm. Referent: Peter Norheimer
 Herzlich Willkommen!!! zum IWL Pharma Workshop am 27.06.2008 in Ulm Referent: Peter Norheimer Unternehmensgruppe Frigo-Trans Unternehmensgruppe Frigo-Trans GmbH Frigo-Trans East GmbH Frigo-Trans Hellas
Herzlich Willkommen!!! zum IWL Pharma Workshop am 27.06.2008 in Ulm Referent: Peter Norheimer Unternehmensgruppe Frigo-Trans Unternehmensgruppe Frigo-Trans GmbH Frigo-Trans East GmbH Frigo-Trans Hellas
Inhaltsverzeichnis. Celeitwort Storhas V. Celeitwort Behrendt. Abkiirzungsverzeichnis. 1 Einfuhrung 1
 Inhaltsverzeichnis Celeitwort Storhas V Celeitwort Behrendt VII Vorwort XVII Abkiirzungsverzeichnis XXIII 1 Einfuhrung 1 2 GMP-Grundlagen 7 2.1 Der BegriffGMP 7 2.2 Geltungsbereich von GMP 10 2.2.1 GMP
Inhaltsverzeichnis Celeitwort Storhas V Celeitwort Behrendt VII Vorwort XVII Abkiirzungsverzeichnis XXIII 1 Einfuhrung 1 2 GMP-Grundlagen 7 2.1 Der BegriffGMP 7 2.2 Geltungsbereich von GMP 10 2.2.1 GMP
1 Zielsetzung und Bedeutung der Computervalidierung 7
 1 Inhaltsverzeichnis 1 Zielsetzung und Bedeutung der Computervalidierung 7 2 Regulatorische Anforderungen und Leitlinien für die Validierung computergestützter Systeme 14 2.1 Deutschland 14 2.2 Europa
1 Inhaltsverzeichnis 1 Zielsetzung und Bedeutung der Computervalidierung 7 2 Regulatorische Anforderungen und Leitlinien für die Validierung computergestützter Systeme 14 2.1 Deutschland 14 2.2 Europa
Das (neue) Lebensmittelrecht Alles wird neu und bleibt beim Alten. Dr. Silvio Arpagaus Kantonschemiker
 Das (neue) Lebensmittelrecht Alles wird neu und bleibt beim Alten Dr. Silvio Arpagaus Kantonschemiker Glace Forum 07.11.2017 Unsere Kunden * ohne Gebrauchsgegenstände amtliche Kontrolle Prozesskontrollen
Das (neue) Lebensmittelrecht Alles wird neu und bleibt beim Alten Dr. Silvio Arpagaus Kantonschemiker Glace Forum 07.11.2017 Unsere Kunden * ohne Gebrauchsgegenstände amtliche Kontrolle Prozesskontrollen
Michael Cassel ISO 9001. Qualitätsmanagement prozessorientiert umsetzen. it 81 Abbildungen HANSER
 Michael Cassel ISO 9001 Qualitätsmanagement prozessorientiert umsetzen it 81 Abbildungen HANSER Inhalt 1 Projektplanung und Durchführung 1 1.1 Einleitung 1 1.2 Projektdurchführung 3 1.2.1 Projektvorbereitung
Michael Cassel ISO 9001 Qualitätsmanagement prozessorientiert umsetzen it 81 Abbildungen HANSER Inhalt 1 Projektplanung und Durchführung 1 1.1 Einleitung 1 1.2 Projektdurchführung 3 1.2.1 Projektvorbereitung
0 Inhaltverzeichnis. 1 Ziel. 2 Geltungsbereich
 Seite 1 von 5 0 Inhaltverzeichnis 0 Inhaltverzeichnis 1 1 Ziel 1 2 Geltungsbereich 1 3 Begriffe und Abkürzungen 2 4 Vorgehensweise und Zuständigkeiten 2 4.1 Textbaustein: 1 (für alle produktberührenden
Seite 1 von 5 0 Inhaltverzeichnis 0 Inhaltverzeichnis 1 1 Ziel 1 2 Geltungsbereich 1 3 Begriffe und Abkürzungen 2 4 Vorgehensweise und Zuständigkeiten 2 4.1 Textbaustein: 1 (für alle produktberührenden
Die Durchführung von GLP Inspektionen in Deutschland Handbuch Anhang 1: Standardarbeitsanweisungen
 Die Durchführung von GLP Inspektionen in Deutschland Handbuch Anhang 1: Standardarbeitsanweisungen Bund/Länder Arbeitsgemeinschaft Chemikaliensicherheit Ausschuss GLP und andere Qualitätssicherungs Systeme
Die Durchführung von GLP Inspektionen in Deutschland Handbuch Anhang 1: Standardarbeitsanweisungen Bund/Länder Arbeitsgemeinschaft Chemikaliensicherheit Ausschuss GLP und andere Qualitätssicherungs Systeme
Qualifizierung im Überblick
 Qualifizierung im Überblick Ein Auszug aus Praxisbuch GMP-Anlagenqualifizierung in der Pharmaindustrie von Thomas Peither, Dr. Petra Rempe, Winfried Büßing Grundlegende GMP-Anforderung Die Qualifizierung
Qualifizierung im Überblick Ein Auszug aus Praxisbuch GMP-Anlagenqualifizierung in der Pharmaindustrie von Thomas Peither, Dr. Petra Rempe, Winfried Büßing Grundlegende GMP-Anforderung Die Qualifizierung
BETRIEBSBESCHREIBUNG FÜR BOR-BEWERTUNG
 Checkliste CL - K 0215.06 Version 6.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle
Checkliste CL - K 0215.06 Version 6.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle
Gegenüberstellung von DIN EN ISO 9001:2015. und DIN EN ISO 9001:2008
 Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 IN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 IN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Inhalt. 2 Umsetzung der Einzelanforderungen Einleitung 49
 1 Projektplanung und Durchführung 1 1.1 Einleitung 1 1.2 Projektdurchführung, 4 1.2.1 Projektvorbereitung 5 1.2.1.1 Ziele des Projekts definieren 5 1.2.1.2 Projektteam bilden 6 1.2.2 Vorgehensplanung und
1 Projektplanung und Durchführung 1 1.1 Einleitung 1 1.2 Projektdurchführung, 4 1.2.1 Projektvorbereitung 5 1.2.1.1 Ziele des Projekts definieren 5 1.2.1.2 Projektteam bilden 6 1.2.2 Vorgehensplanung und
Gegenüberstellung von DIN EN ISO 9001:2015. und DIN EN ISO 9001:2008
 Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 DIN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 DIN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Neue Verpackungsstandards. IFS PACsecure und FSSC Verpackungen
 Neue Verpackungsstandards IFS PACsecure und FSSC 22000 Verpackungen 12.1.2018 Hygienemanagementsysteme für Verpackungen Die wichtigsten Verpackungsstandards.. BRC Global Standard for Packaging and Packaging
Neue Verpackungsstandards IFS PACsecure und FSSC 22000 Verpackungen 12.1.2018 Hygienemanagementsysteme für Verpackungen Die wichtigsten Verpackungsstandards.. BRC Global Standard for Packaging and Packaging
Gegenüberstellung DIN EN 9100:2018 DIN EN 9100:2010
 Gegenüberstellung DIN EN 9100:2018 DIN EN 9100:2010 DIN EN 9100:2018 DIN EN 9100:2010 4 Kontext der 4 Qualitätsmanagementsystem 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse
Gegenüberstellung DIN EN 9100:2018 DIN EN 9100:2010 DIN EN 9100:2018 DIN EN 9100:2010 4 Kontext der 4 Qualitätsmanagementsystem 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse
Hygienemanagement HACCP Getränk GmbH
 Hygienemanagement HACCP Inhalt 1. Produktion Getränk... 2 Schritt 1: Ermittlung von Gefahren... 2 Schritt 2: Bestimmung der kritischen Kontrollpunkte... 3 Schritt 3: Festlegen von Grenzwerten... 4 Schritt
Hygienemanagement HACCP Inhalt 1. Produktion Getränk... 2 Schritt 1: Ermittlung von Gefahren... 2 Schritt 2: Bestimmung der kritischen Kontrollpunkte... 3 Schritt 3: Festlegen von Grenzwerten... 4 Schritt
Leitung der Herstellung und Produktionsabweichungen kompakt, in Köln
 Leitung der Herstellung und Produktionsabweichungen kompakt, 11.05.2016 in Köln Verantwortlichkeiten der Leitung der Herstellung Verantwortungsabgrenzungen Ablauf der Bearbeitung von Abweichungen, CAPAs
Leitung der Herstellung und Produktionsabweichungen kompakt, 11.05.2016 in Köln Verantwortlichkeiten der Leitung der Herstellung Verantwortungsabgrenzungen Ablauf der Bearbeitung von Abweichungen, CAPAs
BETRIEBSBESCHREIBUNG FÜR BOR-BEWERTUNG
 Checkliste CL - K 0203 Version 5.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle im
Checkliste CL - K 0203 Version 5.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle im
Bewilligungsanforderungen an die Lagerung von Arzneimitteln durch Logistikunternehmen
 Bewilligungsanforderungen an die Lagerung von Arzneimitteln durch Logistikunternehmen Dokument gültig ab: 31. Januar 2012 Dokumentennummer: I-SMI.TI.11 Version 01 Klassifizierung: Öffentlich Ersetzt Dokument:
Bewilligungsanforderungen an die Lagerung von Arzneimitteln durch Logistikunternehmen Dokument gültig ab: 31. Januar 2012 Dokumentennummer: I-SMI.TI.11 Version 01 Klassifizierung: Öffentlich Ersetzt Dokument:
4.2.3 Liste der Dokumente MH Gesundheitsvorsorge
 Interne Dokumente Kapitel- und Dokumentenbeschreibung Version vom Seitenanzahl 0 Einführung Deckblatt Musterhandbuch 1 Vorwort 2 Deckblatt Allgemeine Informationen 1 Abkürzungsverzeichnis 1 1 Managementhandbuch
Interne Dokumente Kapitel- und Dokumentenbeschreibung Version vom Seitenanzahl 0 Einführung Deckblatt Musterhandbuch 1 Vorwort 2 Deckblatt Allgemeine Informationen 1 Abkürzungsverzeichnis 1 1 Managementhandbuch
Inspektionen von Einrichtungen der Advanced Therapies
 Inspektionen von Einrichtungen der Advanced Therapies Mag. Gabriela Romierer Institut Inspektionen, Medizinprodukte & Hämovigilanz 6. Mai 2009 Diese Präsentation stellt Auszüge über die gesetzlichen Anforderungen
Inspektionen von Einrichtungen der Advanced Therapies Mag. Gabriela Romierer Institut Inspektionen, Medizinprodukte & Hämovigilanz 6. Mai 2009 Diese Präsentation stellt Auszüge über die gesetzlichen Anforderungen
EN ISO/IEC 17025:2017 Neue Anforderungen an die Kontaminantenanalytik
 EN ISO/IEC 17025:2017 Neue Anforderungen an die Kontaminantenanalytik Ronald Stelzer Qualitätsmanagement Lebensmittelsicherheit Struktur 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe 4 Allgemeine
EN ISO/IEC 17025:2017 Neue Anforderungen an die Kontaminantenanalytik Ronald Stelzer Qualitätsmanagement Lebensmittelsicherheit Struktur 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe 4 Allgemeine
Sinn und Problematik qualitätssichernder Massnahmen
 Sinn und Problematik qualitätssichernder Massnahmen Infotag 2009 Autor Barbara Glock Qualität ist der Grad, in dem inhärente Merkmale Anforderungen erfüllen (nach ISO 9000:2005) 2 Was ist Qualität? (GESCHÄFTS)ERFOLG
Sinn und Problematik qualitätssichernder Massnahmen Infotag 2009 Autor Barbara Glock Qualität ist der Grad, in dem inhärente Merkmale Anforderungen erfüllen (nach ISO 9000:2005) 2 Was ist Qualität? (GESCHÄFTS)ERFOLG
TEIL 1 allgemeiner Teil
 TEIL 1 allgemeiner Teil Einleitung 0 Einleitung 0 Einleitung 0 Einleitung Einleitung 0 Allgemeines 0.1 Hintergrund 0.1 Hintergrund 0.1 Allgemeines 0.1 Grundsätze des Qualitätsmanagements 0.2 Ziel eines
TEIL 1 allgemeiner Teil Einleitung 0 Einleitung 0 Einleitung 0 Einleitung Einleitung 0 Allgemeines 0.1 Hintergrund 0.1 Hintergrund 0.1 Allgemeines 0.1 Grundsätze des Qualitätsmanagements 0.2 Ziel eines
QM nach DIN EN ISO 9001:2015. copyright managementsysteme Seiler Tel:
 QM nach DIN EN ISO 9001:2015 1 copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 2 Prozessplanung copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 3 Kennzahlen im Unternehmen 48 Lieferzeit
QM nach DIN EN ISO 9001:2015 1 copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 2 Prozessplanung copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 3 Kennzahlen im Unternehmen 48 Lieferzeit
Validierung hausinterner Aufbereitungsschritte bei Outsourcing
 Validierung hausinterner Aufbereitungsschritte bei Outsourcing Ulrike Prüfert-Freese Leiterin des Hygienelabors der MA 39 Folie 1 Validierung jener Teilprozesse der Aufbereitungsprozesse für Medizinprodukte
Validierung hausinterner Aufbereitungsschritte bei Outsourcing Ulrike Prüfert-Freese Leiterin des Hygienelabors der MA 39 Folie 1 Validierung jener Teilprozesse der Aufbereitungsprozesse für Medizinprodukte
Eingesetzte Mittel Anlagen, Methoden, Fähigkeiten, Techniken, Geld, Kapital PROZESS. Bündel oder Folge von Aktivitäten
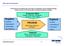 Was ist ein Prozess? Ein Prozess ist ein Bündel oder eine Folge von Aktivitäten, für die Vorgaben benötigt werden und die ein für den Kunden verwertbares Ergebnis erzeugen. Vorgaben Rohstoffe Halbfertigteile
Was ist ein Prozess? Ein Prozess ist ein Bündel oder eine Folge von Aktivitäten, für die Vorgaben benötigt werden und die ein für den Kunden verwertbares Ergebnis erzeugen. Vorgaben Rohstoffe Halbfertigteile
R H I. R e g i o n a l e s H e i l m i t t e l i n s p e k t o r a t d e r N o r d w e s t s c h w e i z
 R H I R e g i o n a l e s H e i l m i t t e l i n s p e k t o r a t d e r N o r d w e s t s c h w e i z Inspektionscheckliste für Praxisapotheken von Komplementärmediziner/innen Praxis: Fachtechnisch verantwortliche/r
R H I R e g i o n a l e s H e i l m i t t e l i n s p e k t o r a t d e r N o r d w e s t s c h w e i z Inspektionscheckliste für Praxisapotheken von Komplementärmediziner/innen Praxis: Fachtechnisch verantwortliche/r
GM P-Qualifizierung und Validierung von Wirkstoffanlagen
 Ralf Gengenbach Mit Beiträgen von Dr. Hans-Georg Eckert und Wolfgang Hähnel GM P-Qualifizierung und Validierung von Wirkstoffanlagen Ein Leitfaden für die Praxis 6B WILEY YCH WI LEY-VCH Verlag GmbH & Co.
Ralf Gengenbach Mit Beiträgen von Dr. Hans-Georg Eckert und Wolfgang Hähnel GM P-Qualifizierung und Validierung von Wirkstoffanlagen Ein Leitfaden für die Praxis 6B WILEY YCH WI LEY-VCH Verlag GmbH & Co.
1.C.1 Ziele des Qualitätsmanagementsystems im Produktlebenszyklus
 Elemente eines QM-Systems.1 Ziele des Qualitätsmanagementsystems im Produktlebenszyklus Autor: Dr. Heinrich Prinz / Ergänzungslieferung 17 Hier finden Sie Antworten auf folgende Fragen Welche Ziele hat
Elemente eines QM-Systems.1 Ziele des Qualitätsmanagementsystems im Produktlebenszyklus Autor: Dr. Heinrich Prinz / Ergänzungslieferung 17 Hier finden Sie Antworten auf folgende Fragen Welche Ziele hat
Aktualisierte Leitlinie für die Validierung der maschinellen Reinigung und Desinfektion (in der Fassung von 2017)
 Aktualisierte Leitlinie für die Validierung der maschinellen Reinigung und Desinfektion (in der Fassung von 2017) Arbeitskreis Infektionsprophylaxe, Markus Hoppe, 13./14.03.2018 Historie der Leitlinie
Aktualisierte Leitlinie für die Validierung der maschinellen Reinigung und Desinfektion (in der Fassung von 2017) Arbeitskreis Infektionsprophylaxe, Markus Hoppe, 13./14.03.2018 Historie der Leitlinie
Hygiene in der modernen Grossküche
 Hygiene in der modernen Grossküche Christine Siegrist & Karl Suter Bau und Betrieb von Großküchen und moderner Betriebsgastronomie Quelle: Google Bundesgesetz über Lebensmittel und Gebrauchsgegenstände
Hygiene in der modernen Grossküche Christine Siegrist & Karl Suter Bau und Betrieb von Großküchen und moderner Betriebsgastronomie Quelle: Google Bundesgesetz über Lebensmittel und Gebrauchsgegenstände
VERANTWORTUNGSABGRENZUNGSVERTRAG (VAV)
 VERANTWORTUNGSABGRENZUNGSVERTRAG (VAV) für die Herstellung von Arzneimitteln in kleinen Mengen im Lohnauftrag 1. Gegenstand und Inhalt 1.1 Dieser VAV bildet den vertraglichen Rahmen zwischen Elvetix Pharma
VERANTWORTUNGSABGRENZUNGSVERTRAG (VAV) für die Herstellung von Arzneimitteln in kleinen Mengen im Lohnauftrag 1. Gegenstand und Inhalt 1.1 Dieser VAV bildet den vertraglichen Rahmen zwischen Elvetix Pharma
Prüfbericht Geprüfte Qualität Bayern Eier. Packstelle
 Seite 1 von 7 Name Straße PLZ Ort Ansprechpartner Tel.- Fax email: Balis- 09- -: Printcodes: Erstkontrolle Folgekontrolle Nachkontrolle Stichprobenkontrolle Kontrolle nicht durchgeführt, weil Packstelle
Seite 1 von 7 Name Straße PLZ Ort Ansprechpartner Tel.- Fax email: Balis- 09- -: Printcodes: Erstkontrolle Folgekontrolle Nachkontrolle Stichprobenkontrolle Kontrolle nicht durchgeführt, weil Packstelle
BETRIEBSBESCHREIBUNG FÜR BOR-BEWERTUNG
 Checkliste CL - K 0219 Version 4.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle im
Checkliste CL - K 0219 Version 4.0 Seite 1 von 5 BETRIEB (Stampiglie des Betriebes) DATUM DER KONTROLLE UHRZEIT (Beginn - Ende) Unterschrift des Anwesenden des Betriebes über die Dauer der Kontrolle im
Musterhandbuch Qualitätsmanagementplan
 Musterhandbuch Leseprobe DIN ISO 10005:2009 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-25-5 Auflage 1 Grundlagen... 2 Gültigkeit... 2 Ziel und Grund... 2 Abkürzungen... 2 Informationen...
Musterhandbuch Leseprobe DIN ISO 10005:2009 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-25-5 Auflage 1 Grundlagen... 2 Gültigkeit... 2 Ziel und Grund... 2 Abkürzungen... 2 Informationen...
Lohnherstellung nicht zulassungspflichtiger Arzneimittel gemäss HMG Art. 9 Abs. 2 Bst. a und c
 Positionspapier H 006.02: Kantonsapotheker-Vereinigung Nordwestschweiz Lohnherstellung nicht zulassungspflichtiger Arzneimittel gemäss HMG Art. 9 Abs. 2 Bst. a und c Geltungsbereich: Dieses Positionspapier
Positionspapier H 006.02: Kantonsapotheker-Vereinigung Nordwestschweiz Lohnherstellung nicht zulassungspflichtiger Arzneimittel gemäss HMG Art. 9 Abs. 2 Bst. a und c Geltungsbereich: Dieses Positionspapier
LIEFERANTEN- Selbstauskunft
 Seite: 1 von 6 Firmenname: Firmenadresse: Dieser Fragebogen wurde ausgefüllt durch: Name: Funktion: Telefon: Fax: E-mail: Für erlenbacher backwaren hergestellte Produkte Datum: Unterschrift Lieferant:
Seite: 1 von 6 Firmenname: Firmenadresse: Dieser Fragebogen wurde ausgefüllt durch: Name: Funktion: Telefon: Fax: E-mail: Für erlenbacher backwaren hergestellte Produkte Datum: Unterschrift Lieferant:
Checkliste Inspektion einer Drogerie
 Checkliste Inspektion einer Drogerie Eröffnungsbesprechung 1. Zweck, Auftrag Basisinspektion, Nachinspektion spez. Inspektion 2. Vorstellung Inspektor(en) 3. Inspektionsprogramm 4. Gesetzliche Grundlagen
Checkliste Inspektion einer Drogerie Eröffnungsbesprechung 1. Zweck, Auftrag Basisinspektion, Nachinspektion spez. Inspektion 2. Vorstellung Inspektor(en) 3. Inspektionsprogramm 4. Gesetzliche Grundlagen
pro-k Fachgruppe Bedarfsgegenstände aus Kunststoff im Technisches Merkblatt Rückverfolgbarkeit von Mehrwegbehältern im Lebensmittelkontakt
 pro-k Fachgruppe Bedarfsgegenstände aus Kunststoff im Lebensmittelkontakt Technisches Merkblatt Rückverfolgbarkeit von Mehrwegbehältern im Lebensmittelkontakt Vorwort Die in der Fachgruppe Bedarfsgegenstände
pro-k Fachgruppe Bedarfsgegenstände aus Kunststoff im Lebensmittelkontakt Technisches Merkblatt Rückverfolgbarkeit von Mehrwegbehältern im Lebensmittelkontakt Vorwort Die in der Fachgruppe Bedarfsgegenstände
Erfahrungen aus der Zertifizierung
 DGSV-Kongress 2010 08.10.2010, Fulda Erfahrungen aus der Zertifizierung von Qualitätsmanagement-Systemen nach DIN EN ISO 13485 für die Aufbereitung von Medizinprodukten Dr. Thomas Kießling Sachverständiger
DGSV-Kongress 2010 08.10.2010, Fulda Erfahrungen aus der Zertifizierung von Qualitätsmanagement-Systemen nach DIN EN ISO 13485 für die Aufbereitung von Medizinprodukten Dr. Thomas Kießling Sachverständiger
EU-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe. mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV)
 EU-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) EU-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe
EU-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) EU-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe
