Humanforschungsgesetz
|
|
|
- Nele Michel
- vor 8 Jahren
- Abrufe
Transkript
1 Humanforschungsgesetz Inhalt und Änderungen zum bisherigen Recht PD Dr. med. Gabriela Senti, Leitung CTC
2 Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge aus dem HFG Das Verordnungsrecht zum HFG Änderungen zum bisherigen Recht Übergangsbestimmungen 1
3 Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge aus dem HFG Das Verordnungsrecht zum HFG Änderungen zum bisherigen Recht Übergangsbestimmungen 2
4 Humanforschungsgesetz (HFG) Art. 118b Bundesverfassung 2010: Humanforschungsgesetz (HFG) 2011: Verordnungsrecht (KlinV, HFV, OV) 2013: 1. Januar 2014: Inkrafttreten 2014: Graphik C.Jenny, BAG; Nov
5 Ziel des HFG Artikel 118b der Bundesverfassung beauftragt den Bund, die Forschung am Menschen gezielt in jenen Bereichen zu regeln, in denen eine Gefahr für die Würde und Persönlichkeit des Menschen besteht, der zugleich aber mit der bestehenden allgemeinen Rechtsordnung nicht ausreichend begegnet werden kann. Daneben soll die Forschungsfreiheit gewahrt bleiben und der Bedeutung der Forschung für die Gesellschaft Rechnung getragen werden. 4 4
6 Zweck des HFG (HFG Art. 1) Würde, Persönlichkeit und Gesundheit des Menschen in der Forschung schützen Günstige Rahmenbedingungen für die Forschung am Menschen schaffen Qualität der Forschung am Menschen sicherstellen Transparenz der Forschung am Menschen gewährleisten 5
7 Geltungsbereich des HFG (HFG Art. 2 und 3) Forschung Methodengeleitete Suche nach verallgemeinerbaren Erkenntnissen (Abgrenzung zum klinischen Handeln) Forschung zu Krankheiten klinische Versuche (z.b. mit Heilmittel, Psychologie, Chirurgie, Transplantation, Pflege, Physiotherapie etc.) Forschung zu Aufbau und Funktion des Körpers Forschung zu Anatomie, Physiologie, Genetik, Forschung zu Eingriffen und Einwirkungen auf den Körper (z.b. Schönheitschirurgie, Blutentnahme, Röntgen etc.) 6 6
8 Forschungsgegenstände (HFG Art. 2) Das HFG gilt für Forschung mit: Personen Gesundheitsbezogenen Personendaten Herkunft: z.b. Forschungsprojekte, Klinik (Krankengeschichten etc.), Register Biologischem Material Herkunft: z.b. Forschungsprojekte, Klinik (verworfenes Material), Biobanken Verstorbenen, Embryonen, Föten 7
9 Aufbau des HFG HFG KlinV Klinische Versuche HFV Nicht-klinische Versuche OV-HFG Arzneimittel Transplantatprodukt Gentherapie Entnahme biologischen Materials bzw. Erhebung Personendaten Ethikkommissionen Medizinprodukt Weiterverwendung biologischen Materials bzw. Personendaten Koordinationsstelle Transplantation Verstorbene Personen Übrige klinische Versuche Tote Embryonen und 8 Föten
10 Nicht im Geltungsbereich des HFG Fragestellung betrifft weder Krankheiten noch Forschung (Grundlagenforschung) z.b. schulische Leistungen (Pädagogik), Wohlfühlen am Arbeitsplatz (Arbeitspsychologie), Einkaufsverhalten (Ökonomie) Gegenausnahme: Forschungsprojekt mit Eingriff und Einwirkung auf den Körper (z.b. Operationen, Blutproben, CT, MRI) fallen unter das HFG 9
11 Nicht im Geltungsbereich des HFG Anonymisiertes Material oder Daten kein Schutzbedarf Embryonen in vitro Stammzellenforschungsgesetz Case Studies, Heilversuche nur Forschung, sofern verallgemeinerbare Erkenntnisse beabsichtigt sind Tierversuche in der Präklinik Tierschutzgesetz 10
12 Anonymisierung (HFV Art. 25) = irreversibles unkenntlich Machen oder Löschen aller Angaben, die in ihrer Kombination die Wiederherstellung des Bezugs zur Person ohne unverhältnismässig grossen Aufwand erlauben (Name, Adresse, Geburtsdatum, eindeutige Identifikationsnummern) solange ein Schlüssel vorhanden ist, handelt es sich nicht um anonymisierte, sondern um verschlüsselte Daten! 11
13 Anonymisierung Datenfeld Patient 1 Patient 2 ID P.M. - Wohnort Musterweg 1, Adlikon (577 Einwohner) Zürich ( Einwohner) Diagnose Trisomie 21 Bluthochdruck Geb.-Datum Sterbedatum Aufwand für Rückführung Klein Sehr gross Anonymisierung? Nein Ja Folie nach C.Jenny, BAG; Nov
14 Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge aus dem HFG Das Verordnungsrecht zum HFG Änderungen zum bisherigen Recht Übergangsbestimmungen 13
15 Wissenschaftlich relevante Fragestellung (HFG Art. 5) Forschung am Menschen darf nur durchgeführt werden, wenn eine wissenschaftlich relevante Fragestellung gegeben ist: a. zum Verständnis von Krankheiten des Menschen; b. zum Aufbau und zur Funktion des menschlichen Körpers; oder c. zur öffentlichen Gesundheit 14
16 Wissenschaftliche Anforderungen (HFG Art. 10) Forschung am Menschen darf nur durchgeführt werden, wenn: die anerkannten Regelungen über die wissenschaftliche Integrität eingehalten werden, insbesondere bezüglich des Umgangs mit Interessenkonflikten; die Anforderungen an die wissenschaftliche Qualität erfüllt sind die anerkannten internationalen Regeln der Guten Praxis über die Forschung am Menschen eingehalten werden die verantwortlichen Personen fachlich hinreichend qualifiziert sind. 15
17 Zusätzliche Anforderungen an die Forschung mit besonders verletzbaren Personen (HFG Art ) Forschung mit Kindern und Jugendlichen Forschung mit urteilsunfähigen Erwachsenen Forschung mit schwangeren Frauen Forschung an Embryonen und Föten in vivo Forschungsprojekte über Methoden des Schwangerschaftsabbruchs Forschung mit Personen im Freiheitsentzug Forschung in Notfallsituationen 16
18 Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge aus dem HFG Das Verordnungsrecht zum HFG Änderungen zum bisherigen Recht Übergangsbestimmungen 17
19 Das Verordnungsrecht zum HFG Humanforschungsverordnung KlinV Verordnung über klinische Versuche gemäss Definition HFG Art. 3 lit. l Humanforschungsverordnung HFV Verordnung über die Humanforschung mit Ausnahme der klinischen Versuche Organisationsverordnung zum HFG OV-HFG EKs, Koordinationsstelle, Datenschutz 18
20 Das Verordnungsrecht zum HFG Forschung am Menschen Klinischer Versuch Nichtklinischer Versuch KlinV HFV 19
21 Definition klinischer Versuch (HFG Art. 3 lit. l) Forschungsprojekt mit Personen, das diese prospektiv einer gesundheitsbezogenen Intervention zuordnet, um deren Wirkungen auf die Gesundheit oder auf den Aufbau und die Funktion des menschlichen Körpers zu untersuchen. 20
22 Definition gesundheitsbezogene Intervention (KlinV Art. 2 lit. a) Präventive, diagnostische, therapeutische, palliative oder rehabilitative Handlung, die im Rahmen eines klinischen Versuchs untersucht wird. 21
23 Verordnung über klinische Versuche (KlinV) Generelle Regelungen Begriffe, Grundsätze, Patientenaufklärung & Einwilligung, Haftung/Versicherung Klinische Versuche mit Heilmitteln und Transplantatprodukten Inkl. Gentherapie, gentechnisch veränderte oder pathogene Organismen Klinische Versuche mit Transplantationen Übrige klinische Versuche Öffentliche Registrierung klinischer Versuche 22
24 Verordnung über die Humanforschung mit Ausnahme der klinischen Versuche (HFV) Allgemeine Bestimmungen Forschung (mit Personen) zur Entnahme biologischen Materials oder gesundheitsbezogener Personendaten Weiterverwendung biologischen Materials und gesundheitsbezogener Personendaten Forschung an Verstorbenen Forschung an Embryonen und Föten aus Aborten 23
25 Weiterhin geltende Gesetze und Verordnungen Heilmittelgesetz, Medizinprodukteverordnung Transplantationsgesetz, -verordnung Strahlenschutzgesetz, -verordnung Datenschutzgesetz, -verordnung Bundesgesetz über genetische Untersuchungen beim Menschen Stammzellenforschungsgesetz Strafgesetzbuch Patienteninnen- und Patientengesetz Kanton Zürich 24
26 Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge aus dem HFG Das Verordnungsrecht zum HFG Änderungen zum bisherigen Recht Übergangsbestimmungen 25
27 Änderungen zum bisherigen Recht Risikokategorisierung: Bewilligungsverfahren, Versicherung, Meldepflichten je nach Gefahrenpotential abgestuft Bewilligungsverfahren bei Ethikkommission und Swissmedic Multizentrische Forschungsprojekte: Leitkommissionsverfahren Transparenz: Registrierung der klinischen Versuche 26
28 Änderungen zum bisherigen Recht Risikokategorisierung: Bewilligungsverfahren, Versicherung, Meldepflichten je nach Gefahrenpotential abgestuft Bewilligungsverfahren bei Ethikkommission und Swissmedic Multizentrische Forschungsprojekte: Leitkommissionsverfahren Transparenz: Registrierung der klinischen Versuche 27
29 Risikobasierte Kategorisierung in der Forschung Risk Categorisation High risk C B Low risk A 28
30 Definition Minimale Risiken und Belastungen KlinV Art. 2b Risiken und Belastungen, die sich unter Berücksichtigung der Verletzbarkeit der teilnehmenden Personen und der konkreten Umstände in ihrer Intensität und Qualität nur geringfügig und vorübergehend auf die Gesundheit der teilnehmenden Personen auswirken; Objektive Beurteilung durch Prüfperson unter Berücksichtigung des konkreten Zustandes und dem Grad der Vulnerabilität der teilnehmenden Person 29
31 Definition Minimale Risiken und Belastungen KlinV Art. 2b Befragungen und Beobachtungen periphere venöse oder kapillare Blutentnahmen Speichel-, Urin- und Stuhlproben sowie Abstriche MRT ohne Kontrastmittel, Sonographie, Elektrogramme Untersuchungen mit CE-markiertem Medizinprodukt ohne Kontrastmittel Untersuchungen mit zugelassenem Arzneimittel mit ionisierenden Strahlen < 5mSv pro Projekt und Person 30
32 Kategorisierung der Klinische Versuche Klinischer Versuch Arzneimittel Transplantatprodukt Gentherapie Medizinprodukt Transplantation Übrige klinische Versuche Kategorie Kategorie Kategorie Kategorie A, B, C A, C A, C A, B KlinV KlinV KlinV KlinV Kapitel 2 Kapitel 2 Kapitel 3 Kapitel 4 31
33 Kategorisierung der Nicht klinischen Versuche Nicht klinischer Versuch Entnahme von biologischem Material bzw. Erhebung von Personendaten Weiterverwendung biologischen Materials bzw. Personendaten Verstorbene Personen Tote Embryonen und Föten Kategorie A, B Keine Kategorisierung Keine Kategorisierung Keine Kategorisierung HFV HFV HFV HFV Kapitel 2 Kapitel 3 Kapitel 4 Kapitel 5 32
34 Änderungen zum bisherigen Recht Günstige Rahmenbedingungen für die Forschung in der Schweiz durch gefährdungsbezogenen Regelungsansatz Kategorisierung : Erleichterung des administrativen Aufwands Differenzierte Bewilligungsverfahren bei der EK (ordentlich, vereinfacht, Präsidialentscheid) Unterschiedlich strenge Meldepflichten bzgl. AEs/SAEs Risiko-adaptiertes Monitoring (Qualitätskontrolle) 33
35 Risikokategorisierung Arzneimittel, Transplantatprodukt A Zugelassen in der Schweiz Gemäss Fachinformation Oder Abweichung von der Fachinformation gemäss vorgegebenen Kriterien B Zugelassen in der Schweiz Abweichung von der Fachinformation ausserhalb vorgegebener Kriterien C Nicht zugelassen in der Schweiz 34
36 Risikokategorisierung Medizinprodukt A CE markiert Zugelassen in der Schweiz Anwendung gemäss Gebrauchsanweisung C Nicht CE markiert in der Schweiz Anwendung nicht gemäss Gebrauchsanweisung In der Schweiz verboten 35
37 Risikokategorisierung Transplantation A C Standardtherapie Keine Standardtherapie Transplantation embryonaler, fötaler Gewebe und Zellen 36
38 Risikokategorisierung Übrige klinische Versuche A Gesundheitsbezogene Intervention mit minimalen Risiken und Belastungen Standardbehandlung B Gesundheitsbezogene Intervention mit mehr als minimalen Risiken und Belastungen Keine Standardbehandlung 37
39 Risikokategorisierung (HFV Art. 7) Forschungsprojekte gemäss HFV A Massnahmen zur Entnahme von biologischem Material oder zur Erhebung von Personendaten mit minimalen Risiken und Belastungen verbunden B Massnahmen zur Entnahme von biologischem Material oder zur Erhebung von Personendaten mit mehr als minimalen Risiken und Belastungen verbunden 38
40 Regulatorische Konsequenzen gemäss Kategorie Kategorie A nur EK Bewilligung, vereinfachtes Verfahren bei der EK Meldung Studienende (90d), Studienreport (1 Jahr) keine Adverse Event (AE) Dokumentation Standardisierte Dokumentation und Meldung von SAEs und SUSARs, die in der Schweiz vorkommen. (SUSAR Meldung für registrierte Produkte gemäss HMG Art. 59) Reduzierte Sicherstellungspflicht Risikobasiertes Qualitätskontrolle(Monitoring) 39
41 Regulatorische Konsequenzen gemäss Kategorie Kategorie B und C EK (Ordentliches Verfahren) und Swissmedic Bewilligung Meldung Studienende (90d), Studienreport (1 Jahr) Standardisierte Adverse Event (AE) Dokumentation Standardisierte Dokumentation und Meldung von SAEs und SUSARs, die in der Schweiz vorkommen. ( SUSAR Meldung für registrierte Produkte gemäss HMG Art. 59) Volle Sicherstellungspflicht Risikobasiertes Qualitätskontrolle (Monitoring) 40
42 Änderungen zum bisherigen Recht Risikokategorisierung: Bewilligungsverfahren, Versicherung, Meldepflichten je nach Gefahrenpotential abgestuft Bewilligungsverfahren bei Ethikkommission und Swissmedic Multizentrische Forschungsprojekte: Leitkommissionsverfahren Transparenz: Registrierung der klinischen Versuche 41
43 Welche Forschung muss bewilligt werden? Bewilligung durch Ethikkommission und Swissmedic/BAG (je nach Risikokategorie/Strahlenbelastung) Alle Projekte der Forschung am Menschen Weiterverwendung von biologischem Material und gesundheitsbezogenen Personendaten 42
44 Prüfbereiche der EK Kanton Zürich Gesundheitsdirektion 43 Vollständigkeit der Gesuchsunterlagen Einstufung und Risiko-Kategorisierung Angaben für die Registrierung Relevanz der Fragestellung Eignung der Methodik Einhaltung der Guten Klinischen Praxis Schutz der Versuchspersonen Qualifikation des verantwortlichen Prüfers Infrastruktur am Durchführungsort Umgang mit Daten und Proben Finanzierung inkl. Studienverträge Folie KEK ZH März 2015
45 Bewilligungsverfahren Parallele Einreichung Prüfperson Dossier Sponsor Dossier Clock stop Formale Prüfung des Dossiers innert 7 Tagen Clock stop Ethikkommission Rückfragen Bewilligung Swissmedic Rückfragen Bewilligung 30 Tage 30 Tage Studienbeginn 44
46 Bewilligungsverfahren Einreichung EK KlinV Art. 24 Absatz 3, HFV Art. 14 Absatz 3 Anstelle der Prüfperson kann der Sponsor das Gesuch einreichen. Er übernimmt alle Melde- und Berichterstattungspflichten der Prüfperson gegenüber der EK. (auch bei Multizenter-Projekte, Untersuchungen mit Strahlenquellen) Safety, Änderungen, Abbruch, Abschluss, Unterbruch 45
47 Klinische Versuche der Transplantation KlinV Art. 54, Anhang 4 Prüfperson Dossier Sponsor Dossier Clock stop Formale Prüfung des Dossiers innert 7 Tagen Clock stop Ethikkommission Rückfragen BAG Rückstellung Bewilligung Bewilligung 30 Tage 30 Tage/ max. 60 Tage Studienbeginn 46
48 Klinische Versuche der Gentherapie, gentechnisch veränderten oder pathogenen Organismen KlinV Art. 35, Anhang 4 Ziffer 4 Sponsor Dossier 60Tage Eidg. Fachkommission für biologische Sicherheit Beurteilung von Qualität und biologischer Sicherheit des Präparats Swissmedic Bundesamt für Umwelt Beurteilung der Umweltdaten Bundesamt für Gesundheit Beurteilung der Umweltdaten 47
49 Nicht-klinische Versuche (HFV Art. 14, 16, 35) ausser Untersuchungen mit Strahlenquellen Projektleitung Dossier Sponsor Dossier Formale Prüfung des Dossiers innert 7 Tagen Ethikkommission Clock stop Rückfragen Bewilligung 30 Tage 48
50 Kanton Zürich Gesundheitsdirektion 49 Neuerungen bezüglich Weiterverwendung von Proben und Daten für die Forschung ( retrospektiver Personendatenstudien) Weiterverwendung von Personendaten und Proben für ein konkretes Forschungsprojekt wird generell bewilligungspflichtig Vorhandenes Einverständnis der Betroffenen für die Weiterverwendung von Personendaten zu Forschungszwecken entbindet nicht mehr von der Ethikpflicht! Vortrag KEK ZH November 2013
51 Kanton Zürich Gesundheitsdirektion 50 Neuerungen bezüglich Weiterverwendung von Proben und Daten für die Forschung ( retrospektiver Personendatenstudien) Aufhebung der Eidgenössische Expertenkommission für das Berufsgeheimnis in der medizinischen Forschung d.h. Generelle Bewilligungen dieser Kommission und Antrag für den Zugriff auf den Patientendaten zu Forschungszwecken verlieren Ihre Gültigkeit Aufgaben der genannten Kommission wird von den kantonalen EK übernommen Sogenannte Eigenforschung (keine Arztgeheimnisverletzung) entbindet nicht mehr von der Ethikpflicht! Vortrag KEK ZH November 2013
52 Bewilligungen für die Offenbarung des Berufsgeheimnisses in der med. Forschung bleiben bis zum Ablauf der Bewilligungsfrist gültig. Ist die Bewilligung unbefristet, so ist der zuständigen EK innerhalb eines Jahres nach Inkrafttreten des Gesetzes ein Gesuch um Erteilung einer Bewilligung nach HFG Artikel 45 Abs. 1 einzureichen. 51
53 Weiterverwendung von biologischem Material und gesundheitsbezogenen Personendaten HFV Art = jeder Umgang zu Forschungszwecken mit bereits entnommenem biologischem Material oder erhobenen Daten jedes Sammeln, Beschaffen, Zusammenführen Registrieren, Katalogisieren Aufbewahren und Erfassen in Bio- oder Datenbanken Bereitstellen, Zugänglichmachen oder Übermitteln 52
54 Weiterverwendung von biologischem Material und gesundheitsbezogenen Personendaten HFV Art Start Forschungsprojekt Register/ Biobank Einverständnis und/oder Vetorecht durch betroffene Person* Bewilligung durch EK für konkretes Forschungsprojekt Auswertung des Forschungsprojekts *Bei fehlendem Einverständnis: Einverständnis KEK notwendig (Expertenkommission zur Wahrung des Berufsgeheimnisses abgeschafft) 53
55 Weiterverwendung von biologischem Material und genetischen Daten HFG Art. 32, HFV Art. 28, 29, 30 In unverschlüsselter Form : Einwilligung nach hinreichender Aufklärung für ein Projekt In verschlüsselter Form : Einwilligung nach hinreichender Aufklärung für Forschungszwecke Anonymisierung erlaubt nach Information und kein Widerspruch erhoben explizite Einwilligung nicht notwendig 54
56 Weiterverwendung von nichtgenetischen gesundheitsbezogenen Daten HFG Art. 33, HFV Art.31, 32 In unverschlüsselter Form : Einwilligung nach hinreichender Aufklärung zu Forschungszwecken In verschlüsselter Form : vorgängige Information und kein Widerspruch erhoben 55
57 Fehlende Einwilligung und Information HFG Art. 34 Biologisches Material und gesundheitsbezogene Personendaten dürfen verwendet werden, wenn: a. es unmöglich oder unverhältnismässig schwierig ist, oder der betroffenen Person nicht zugemutet werden kann. b. keine dokumentierte Ablehnung vorliegt, und c. das Interesse der Forschung dem Interesse der betroffenen Person,, überwiegt. 56
58 Aufgabenverteilung Swissmedic-EK für Arzneimittel, Transplantatprodukte Swissmedic / Bewilligung EK EC/ / Bewilligung Qualität (Zusammensetzung und Qualität) Sicherheit (Präklinik und Sicherheit Patientensicherheit) des Teilnehmers) Nutzen / Risiko, Wirksamkeit, Ethik, etc. (Medizin / GCP) 57
59 Aufgabenverteilung Swissmedic-EK für Medizinprodukte Swissmedic / Bewilligung Anforderungen gemäss aktuellen Direktiven Risiken Performance des Medizinproduktes EC / Bewilligung Nutzen / Risiko Ethik Patienteninformation und Patientenrecht 58
60 Das Dossier ab 2014 (KlinV/OClin Anhang 4) Register 1: Register 2: Register 3: Register 4: Register 5: Register 6: Register 7: Register 8: Register X: Register X: Register 9: Register 10: Register 11: Register 12: Register 13: Register 13: Register 13: Register X: Begleitbrief Einreichungsformular Liste der Prüfer bei Multizenterstudien Befürwortende Stellungnahme der EK inkl. Korrespondenz Protokoll inklusive Amendments, mit Unterschriftenseiten Information und Einverständniserklärung für Versuchspersonen Investigator's Brochure / Fachinformation Dokumentation zu den Versuchspräparaten Entscheide von Behörden anderer Länder Hängige EK-Entscheide in der Schweiz Nachweis der Schadensdeckung für allfällig auftretende Schäden Verträge Inseratetext (für die Rekrutierung von Versuchspersonen) Curriculum Vitae des Hauptprüfers bzw. der Hauptprüferin Datenerfassungsbogen (CRF, Case Report Form) Alle Dokumente, welche den Versuchspersonen abgegeben werden Allfällige weitere, von der Ethikkommission genehmigte Dokumente Allfällige weitere Dokumente und Informationen gemäss Art. 31.2; (KlinV/Oclin) Folie V.Gafner, Swissmedic November
61 Einreichung der Unterlagen KEK Zürich Vorgehen bei Gesucheinreichung: Swissmedic Vorgehen bei Gesucheinreichung: BAG Strahlenschutz, Information HFG: Anhänge der Verordnungen (KlinV, HFV) 60
62 Dokumentation und Meldungen in klinischen Versuchen und Forschungsprojekten 61
63 Dokumentation von AEs bei klinischen Versuchen mit Arzneimitteln (KlinV Art. 39) Kategorie C: in standardisierter Weise dokumentieren (in KG und im CRF) Kategorie B: in standardisierter Weise dokumentieren, wenn in Prüfplan vorgesehen oder von Bewilligungsbehörde gefordert Kategorie A: keine Dokumentationspflicht (nur Spontanmeldungen) 62
64 Meldung von Sicherheits- und Schutzmassnahmen für alle Forschungsprojekte KlinV Art. 37, 57, 62 resp. HFV Art. 20 Prüfperson/ Projektleitung Sponsor 7 Tage Kat. B, C 7 Tage Ethikkommission Swissmedic/BAG 63
65 Meldung von Sicherheits- und Schutzmassnahmen für Projekte mit Medizinprodukten (KlinV Art. 37) Prüfperson Sponsor 2 Tage Kat. C 2 Tage Ethikkommission Swissmedic 64
66 Meldung von SAEs (KlinV Art. 40, 57) Klinische Versuche mit Arzneimitteln, Transplantation Prüfperson 24 Stunden alle SAEs Sponsor 7 Tage Tod (SAE) Ethikkommission Führt Liste der Ereignisse 65
67 Meldung von SUSAR (KlinV Art. 41, 57) Arzneimittel, Transplantation Tödliche SUSARs Prüfperson 24 Stunden Information aller Prüfpersonen Sponsor 7 Tage 7 Tage Kat. B, C Ethikkommission Swissmedic/BAG 66
68 Meldung von SUSAR (KlinV Art. 41, 57) Arzneimittel, Transplantation lebensbedrohliche und alle anderen SUSARs Prüfperson 24 Stunden Information aller Prüfpersonen Sponsor 15 Tage 15 Tage Kat. B, C Ethikkommission Swissmedic/BAG 67
69 Meldung von SAEs klinische Versuche Medizinprodukte (KlinV Art. 42) Prüfperson 24 Stunden alle SAEs Sponsor Kat. C SAE in Schweiz mit möglichem Zusammenhang Kat. C 7 Tage SAE In- und Ausland mit möglichem Zusammenhang 7 Tage Ethikkommission führt Liste der Ereignisse Swissmedic 68
70 Meldung Schwerwiegendes Ereignis (KlinV Art. 63) Übrige klinische Versuche Prüfperson 24 Stunden alle SAEs Sponsor 15 Tage SAEs mit möglichem Zusammenhang Ethikkommission Führt Liste der Ereignisse 69
71 Schwerwiegendes unerwünschtes Ereignis (SAE) Definition für übrige klinische Versuche (KlinV Art. 63) Ereignis, das eine stationäre Behandlung oder deren Verlängerung erforderlich macht zu einer bleibenden oder schwerwiegenden Behinderung oder Invalidität führt lebensbedrohend ist oder zum Tode führt eine angeborene Anomalie oder ein Geburtsdefekt zur Folge hat 70
72 Meldung von Schwerwiegendem Ereignis bei Forschungsprojekten gemäss HFV (Art. 19, 21) Projektleitung 24 Stunden Sponsor 7 Tage Ereignisse mit möglichem Zusammenhang Untersuchung mit Strahlenquellen 7 Tage Ethikkommission BAG 71
73 Schwerwiegendes Ereignis (gemäss HFV Art. 21) Definition für Forschungsprojekte gemäss HFV Nachteiliges Ereignis, bei dem nicht ausgeschlossen werden kann, dass es auf die Entnahme des biologischen Materials oder die Erhebung der gesundheitsbezogenen Personendaten zurückzuführen ist, und das: eine stationäre Behandlung oder deren Verlängerung erforderlich macht zu einer bleibenden oder schwerwiegenden Behinderung oder Invalidität führt lebensbedrohend ist oder zum Tode führt 72
74 Meldung von Schwerwiegendem Ereignis bei Forschungsprojekten gemäss HFV (Art. 19, 21) Vorgehen bei Forschungsprojekten gemäss HFV: Unterbruch des Forschungsprojektes Meldung an: - EK (inkl. Bericht über den Zusammenhang und Vorschläge für das weitere Vorgehen) - BAG (bei einer Untersuchung mit Strahlenquellen) EK entscheidet innerhalb von 30 Tagen über die Fortführung des Forschungsprojektes 73
75 Änderungen zum bisherigen Recht Risikokategorisierung: Bewilligungsverfahren, Versicherung, Meldepflichten je nach Gefahrenpotential abgestuft Bewilligungsverfahren bei Ethikkommission und Swissmedic Multizentrische Forschungsprojekte: Leitkommissionsverfahren Transparenz: Registrierung der klinischen Versuche 74
76 Multizentrische Forschungsprojekte: Leitkommissionsverfahren Leitkommission Beteiligte EK zuständige EK am Tätigkeitsort der koordinierenden Prüfperson zuständig für fachliche und betriebliche Voraussetzungen der beteiligten Prüfpersonen/Zentren in den anderen Kantonen 75
77 Genehmigungsverfahren bei Multizenter-Projekten HFG Art. 47; KlinV Art.27; HFV Art. 17 Sponsor Bewilligung innert 45 Tagen Swissmedic (klinische Versuche Kat. B und C) Koordinierende Prüfperson Auf Aufforderung der Leit-EK Dossier nach Anhang 3 Ziff. 4 KlinV Formalprüfung innert 7 Tagen Leitkommission Bewertung innert 15 Tagen Beteiligte EK Beteiligte EK Information Beteiligte EK 76
78 Ablauf der Meldung von SAEs, SUSARs bei multizentrischen klinischen Versuchen KlinV Art. 40, 41, 42 Sponsor Prüfperson Kat. B und C Koordinierende Prüfperson Swissmedic beteiligte EK Leit-EK 77
79 Änderungen zum bisherigen Recht Multizentrische Forschungsprojekte: Leitkommissionsverfahren Risikokategorisierung: Bewilligungsverfahren, Versicherung, Meldepflichten je nach Gefahrenpotential abgestuft Bewilligungsverfahren bei Ethikkommission und Swissmedic Transparenz: Registrierung der klinischen Versuche 78
80 Registrierung klinische Versuche Warum? Reduktion des Publikationsbias (selektives Publizieren) Identifizieren von Wissenslücken Bessere wissenschaftliche Qualität Sicherstellen von Nachvollziehbarkeit und Rückverfolgbarkeit Reduktion von Doppelspurigkeiten Vertrauen in die klinische Forschung schaffen durch Transparenz 79
81 Registrierung klinische Versuche Wann? Vor der Durchführung des klinischen Versuches Bei klinischen Versuchen der Phase I bis spätestens ein Jahr nach Abschluss Mind. 1x jährlich aktualisieren Sponsor verantwortlich 80
82 Registrierung klinische Versuche Register Register WHO-Primär- register clinicaltrials.g ov Studienportal.non-ch Registrierfunktionen Suchfunktionen Clinicaltrialsportal.gov Registrierfunktionen Suchfunktionen registrieren Ergänzende Datenbank Gesuchsteller (Sponsor/Prüfperson) Swiss National Clinical Trial Portal Gesuchseingabe Suchfunktionen prüfen Behörden (EK/Swissmedic/BAG) sich informieren Interessierte Öffentlichkeit 81 Quelle BAG Sektion Forschung am Menschen und Ethik A.Christen PhD, Juni 2013
83 82
84 83
85 84
86 SNCTP Swiss Clinical Trials Portal Via kofam-webseite aufrufbar SNCTP steht in vier Sprachen (E, D, F, I) zur Verfügung Ein elektronischer Wizard hilft bei der Bestimmung des Forschungsprojekttyps und der Risikokategorie Die WHO-Parameter lassen sich als XML exportieren für die Registrierung im ClinicalTrials.gov 85
87 Gesuchs Einreichung Einreichung über SNCTP per 14. April 2014 eingestellt Ab April 2014 Einreichung über den Postweg mit angepasstem Basisformular und CD oder Memory Stick direkt an die zuständige Ethikkommission (siehe neues Portal BASEC - Start bis Ende 2015 Einreichung im herkömmlichen Modus möglich obligatorisch ab
88 Gesuchs Einreichung via BASEC 87
89 88
90 Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge aus dem HFG Das Verordnungsrecht zum HFG Änderungen zum bisherigen Recht Übergangsbestimmungen 89
91 Übergangsbestimmungen klinische Versuche Bereits bewilligte Projekte mit Heilmitteln und Transplantatprodukten/ Transplantation gelten als klinische Versuche der Kategorie C Übrige bewilligte klinische Versuche gelten als klinische Versuche der Kategorie B Auf Gesuch kann Behörde diese Projekte auch in andere Kategorie einstufen 90
92 Übergangsbestimmungen klinische Versuche Bisher nicht bewilligungspflichtige Projekte: Gesuch an EK für Bewilligung innerhalb von sechs Monaten. Verlängerte EK-Bearbeitungsfrist von 6 Monaten. Bewilligte klinische Versuche, die nicht bis abgeschlossen sind, müssen innert 6 Monaten (bis 01. Juli 2014) in ein Register eingetragen werden. 91
93 Übergangsbestimmungen nicht-klinische Versuche Bewilligungen für die Offenbarung des Berufsgeheimnisses in der med. Forschung bleiben bis zum Ablauf der Bewilligungsfrist gültig. Ist die Bewilligung unbefristet, so ist der zuständigen EK innerhalb eines Jahres nach Inkrafttreten des Gesetzes ein Gesuch um Erteilung einer Bewilligung nach HFG Artikel 45 Abs. 1 einzureichen. 92
94 Übergangsbestimmungen nicht-klinische Versuche Bereits bewilligte Forschungsprojekte mit Massnahmen zur Entnahme biologischen Materials oder Erhebung von Personendaten gelten als Projekte der Kategorie B. Auf Gesuch kann Behörde diese Projekte auch in Kategorie A einstufen 93
95 Take home message Alle Forschung am Menschen geregelt Erleichterungen durch Risikokategorisierung Parallele Einreichung Ethik / Swissmedic Zentrale Registrierung der klinischen Versuche Gesuchs Einreichung via BASEC ab Jan 2016 obligatorisch 94
96 Danke für Ihre Aufmerksamkeit 95
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz
 Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
Was bedeutet die neue Gesetzgebung für mein Forschungsprojekt? Das neue Humanforschungsgesetz 6. Juni 2013 Brigitte Meier Leitung Sektion Forschung am Mensch und Ethik Bundesamt für Gesundheit Inhalt 1.
Änderungen mit dem Humanforschungsgesetz Neue Vorlagen
 Departement Klinische Forschung Clinical Trial Unit Änderungen mit dem Humanforschungsgesetz Neue Vorlagen HFG News 3 Astrid Mattes 09. Januar 2014 -Seite 5 revidiert am 24.01.2014- Werkzeug zur Risikoklassifizierung
Departement Klinische Forschung Clinical Trial Unit Änderungen mit dem Humanforschungsgesetz Neue Vorlagen HFG News 3 Astrid Mattes 09. Januar 2014 -Seite 5 revidiert am 24.01.2014- Werkzeug zur Risikoklassifizierung
Humanforschungsgesetz
 Humanforschungsgesetz dffg Inhalt und Änderungen zum bisherigen Recht PD Dr. med. Gabriela Senti, Leitung CTC Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge
Humanforschungsgesetz dffg Inhalt und Änderungen zum bisherigen Recht PD Dr. med. Gabriela Senti, Leitung CTC Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG Auszüge
Humanforschungsgesetz
 Humanforschungsgesetz dffg Inhalt und Änderungen zum bisherigen Recht Prof. Dr. med. Gabriela Senti, Leitung CTC Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG
Humanforschungsgesetz dffg Inhalt und Änderungen zum bisherigen Recht Prof. Dr. med. Gabriela Senti, Leitung CTC Agenda Entstehung, Ziel, Zweck und Geltungsbereich des neuen Humanforschungsgesetzes HFG
Erläuterungen Angaben zur Anzahl im Vollzugsjahr 2017 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts
 Name Ethikkommission: KEK Zürich Erläuterungen Angaben zur Anzahl im Vollzugsjahr 217 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts 2 3 Anzahl im Vollzugsjahr 217 als lokale Ethikkommission
Name Ethikkommission: KEK Zürich Erläuterungen Angaben zur Anzahl im Vollzugsjahr 217 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts 2 3 Anzahl im Vollzugsjahr 217 als lokale Ethikkommission
Das neue Humanforschungsgesetz Die wichtigsten Neuerung für Forschende
 Departement Klinische Forschung Clinical Trial Unit Das neue Humanforschungsgesetz Die wichtigsten Neuerung für Forschende Research Lunch Kardiologie Christiane Pauli-Magnus und Barbara Peters Das neuehumanforschungsgesetz
Departement Klinische Forschung Clinical Trial Unit Das neue Humanforschungsgesetz Die wichtigsten Neuerung für Forschende Research Lunch Kardiologie Christiane Pauli-Magnus und Barbara Peters Das neuehumanforschungsgesetz
Klinische Versuche in der Schweiz Die Versicherungsdeckung
 Klinische Versuche in der Schweiz Die Versicherungsdeckung SGHVR 12. November 2014 1 Agenda Bisherige Situation Die neue Versicherungslösung 2 Bisherige Situation Grundlage bildeten das Heilmittelgesetz
Klinische Versuche in der Schweiz Die Versicherungsdeckung SGHVR 12. November 2014 1 Agenda Bisherige Situation Die neue Versicherungslösung 2 Bisherige Situation Grundlage bildeten das Heilmittelgesetz
Angaben zur Art und Anzahl im Vollzugsjahr 2016 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts
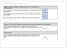 Angaben zur Anzahl im Vollzugsjahr 216 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts Anzahl im Vollzugsjahr 216 als lokale Ethikkommission erhaltene Gesuche zur Bewilligung eines multizentrischen
Angaben zur Anzahl im Vollzugsjahr 216 eingereichten Gesuche zur Bewilligung eines Forschungsprojekts Anzahl im Vollzugsjahr 216 als lokale Ethikkommission erhaltene Gesuche zur Bewilligung eines multizentrischen
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV)
 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) Vom 20. Dezember 2001, BGBl. I S. 3854 geändert am 4. Dezember 2002, BGBl I S. 4456 zuletzt geändert am 13. Februar 2004, BGBl I S. 216
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) Vom 20. Dezember 2001, BGBl. I S. 3854 geändert am 4. Dezember 2002, BGBl I S. 4456 zuletzt geändert am 13. Februar 2004, BGBl I S. 216
DATENSCHUTZ IN DER FORSCHUNG
 DATENSCHUTZ IN DER FORSCHUNG PERSONENBEZUG, ZWECKÄNDERUNG UND -ANPASSUNG, GESUNDHEITSDATEN, GENETISCHE DATEN Dr. Jens Schwanke KAIROS GMBH BOCHUM/BERLIN, conhit-satellitenveranstaltung, Berlin, 18.04.2016
DATENSCHUTZ IN DER FORSCHUNG PERSONENBEZUG, ZWECKÄNDERUNG UND -ANPASSUNG, GESUNDHEITSDATEN, GENETISCHE DATEN Dr. Jens Schwanke KAIROS GMBH BOCHUM/BERLIN, conhit-satellitenveranstaltung, Berlin, 18.04.2016
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV)
 05.07.2005 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 13. Februar 2004 (BGBl. I S. 216)
05.07.2005 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 13. Februar 2004 (BGBl. I S. 216)
Patientenmobilität an der schweizerischen Grenze
 Patientenmobilität an der schweizerischen Grenze Deutsch-französisch-schweizerische Konferenz, Baden-Baden, 17. 18. November 2014 Susanne Jeker Siggemann, stellvertretende Leiterin Sektion Rechtliche Aufsicht
Patientenmobilität an der schweizerischen Grenze Deutsch-französisch-schweizerische Konferenz, Baden-Baden, 17. 18. November 2014 Susanne Jeker Siggemann, stellvertretende Leiterin Sektion Rechtliche Aufsicht
Registration von bereits bewilligten klinischen Versuchen
 SNCTP - Anleitung Teil 2: Registration von bereits bewilligten klinischen Versuchen Version 1.2 Wichtige Hinweise: 1. Es müssen nur klinische Versuche (vgl. Definition Art. 3 Bst. l HFG) gemäss Art. 56
SNCTP - Anleitung Teil 2: Registration von bereits bewilligten klinischen Versuchen Version 1.2 Wichtige Hinweise: 1. Es müssen nur klinische Versuche (vgl. Definition Art. 3 Bst. l HFG) gemäss Art. 56
Das neue Portal für klinische Studien
 Das neue Portal für klinische Studien & Stephanie Züllig, PhD Sektion Forschung am Menschen und Ethik Hintergrund Forderung nach mehr Transparenz bei klinischen Studien (Motion Hubmann, 005) Registrierungspflicht
Das neue Portal für klinische Studien & Stephanie Züllig, PhD Sektion Forschung am Menschen und Ethik Hintergrund Forderung nach mehr Transparenz bei klinischen Studien (Motion Hubmann, 005) Registrierungspflicht
Abschnitt 1 Anwendungsbereich und Allgemeine Anforderungen an die Konformitätsbewertung 1 Anwendungsbereich
 13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
Investigator Initiated Trials
 Investigator Initiated Trials Die Universität in der Rolle des Sponsors nach AMG - Rechtliche Aspekte - Alexander May, LL.M. Seite 1 Überblick Rechtliche Rahmenbedingungen 12. AMG-Novelle Der Sponsor und
Investigator Initiated Trials Die Universität in der Rolle des Sponsors nach AMG - Rechtliche Aspekte - Alexander May, LL.M. Seite 1 Überblick Rechtliche Rahmenbedingungen 12. AMG-Novelle Der Sponsor und
Co-Marketing von Arzneimitteln. Version 07/2015
 Version 07/2015 Art. 14 HMG Das Schweizerische Heilmittelinstitut ist befugt, für bestimmte Kategorien von Arzneimitteln vereinfachte Zulassungsverfahren vorzusehen, sofern dies mit den Anforderungen an
Version 07/2015 Art. 14 HMG Das Schweizerische Heilmittelinstitut ist befugt, für bestimmte Kategorien von Arzneimitteln vereinfachte Zulassungsverfahren vorzusehen, sofern dies mit den Anforderungen an
Verordnung, mit der die Gewebeentnahmeeinrichtungsverordnung geändert wird. Vorblatt. Ziele. Inhalt
 1 von 5 Verordnung, mit der die Gewebeentnahmeeinrichtungsverordnung geändert wird Einbringende Stelle: BMG Laufendes Finanzjahr: 2014 Inkrafttreten/ Wirksamwerden: 2014 Vorblatt Ziele - Erhöhung der Sicherheit
1 von 5 Verordnung, mit der die Gewebeentnahmeeinrichtungsverordnung geändert wird Einbringende Stelle: BMG Laufendes Finanzjahr: 2014 Inkrafttreten/ Wirksamwerden: 2014 Vorblatt Ziele - Erhöhung der Sicherheit
IHR PATIENTENDOSSIER IHRE RECHTE
 IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
07.072. Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA
 07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
07.072 Forschung am Menschen. Verfassungsbestimmung ARGUMENTARIEN CONTRA Verfassungsartikel über die Forschung am Menschen Art. 118b Hauptkritikpunkt: Abs 2,Bst c «Fremdnützige Forschung an urteilsunfähigen
10 IDG (Gesetz über die Information und den Datenschutz, LS 170.4) 24 IDV (Verordnung über die Information und den Datenschutz, LS 170.
 M erkblatt Vorabkontrolle 1 Einleitung Öffentliche Organe des Kantons Zürich müssen Projekte und Vorhaben dem Datenschutzbeauftragten zur Prüfung unterbreiten, wenn diese Datenbearbeitungen beinhalten,
M erkblatt Vorabkontrolle 1 Einleitung Öffentliche Organe des Kantons Zürich müssen Projekte und Vorhaben dem Datenschutzbeauftragten zur Prüfung unterbreiten, wenn diese Datenbearbeitungen beinhalten,
Monitoring. Lucia Kacina. CTU Bern
 Monitoring Lucia Kacina CTU Bern Themen Einverständniserklärung Protokoll & Dokumentation (e)crf-einträge: Dos & Don ts Monitoringvisiten: Teilnehmer & Ablauf Monitoring: Aufgaben des Zentrums Monitoring
Monitoring Lucia Kacina CTU Bern Themen Einverständniserklärung Protokoll & Dokumentation (e)crf-einträge: Dos & Don ts Monitoringvisiten: Teilnehmer & Ablauf Monitoring: Aufgaben des Zentrums Monitoring
Das BASG / AGES PharmMed
 CMI-WORKSHOP Dipl.-Ing. Meinrad Guggenbichler Institut Inspektionen, Medizinprodukte und Hämovigilanz Das BASG / AGES PharmMed Das Bundesamt für Sicherheit im Gesundheitswesen (BASG) ist die Aufsichtsbehörde
CMI-WORKSHOP Dipl.-Ing. Meinrad Guggenbichler Institut Inspektionen, Medizinprodukte und Hämovigilanz Das BASG / AGES PharmMed Das Bundesamt für Sicherheit im Gesundheitswesen (BASG) ist die Aufsichtsbehörde
Dienstvereinbarung zur Einführung und Anwendung des Internetportals der Universität München
 Dienstvereinbarung zur Einführung und Anwendung des Internetportals der Universität München Zur Gewährleistung der schutzwürdigen Belange der Beschäftigten sowie zur Wahrung der berechtigten Interessen
Dienstvereinbarung zur Einführung und Anwendung des Internetportals der Universität München Zur Gewährleistung der schutzwürdigen Belange der Beschäftigten sowie zur Wahrung der berechtigten Interessen
vom 15. Januar 1991 (ABl. 1991 S. 36), geändert durch Verordnung vom 17. Januar 1995 (ABl. S. 41) Inhaltsverzeichnis
 Verordnung zum Schutz von Patientendaten DSVO KH-Pfalz 50.02 Verordnung der Evangelischen Kirche der Pfalz (Protestantische Landeskirche) zum Schutz von Patientendaten in kirchlichen Krankenhäusern (DSVO
Verordnung zum Schutz von Patientendaten DSVO KH-Pfalz 50.02 Verordnung der Evangelischen Kirche der Pfalz (Protestantische Landeskirche) zum Schutz von Patientendaten in kirchlichen Krankenhäusern (DSVO
Verordnung über Investitionshilfe für Berggebiete
 Verordnung über Investitionshilfe für Berggebiete (IHV) 901.11 vom 26. November 1997 (Stand am 1. Februar 2000) Der Schweizerische Bundesrat, gestützt auf die Artikel 8 Absatz 3 und 21 Absatz 3 des Bundesgesetzes
Verordnung über Investitionshilfe für Berggebiete (IHV) 901.11 vom 26. November 1997 (Stand am 1. Februar 2000) Der Schweizerische Bundesrat, gestützt auf die Artikel 8 Absatz 3 und 21 Absatz 3 des Bundesgesetzes
gestützt auf die Artikel 14, 23 Absatz 3 und 40 Absatz 3 des Bundesgesetzes vom 23. März 2001 über den Konsumkredit (KKG) 1,
 Verordnung zum Konsumkreditgesetz (VKKG) Entwurf vom... Der Schweizerische Bundesrat, gestützt auf die Artikel 14, 23 Absatz 3 und 40 Absatz 3 des Bundesgesetzes vom 23. März 2001 über den Konsumkredit
Verordnung zum Konsumkreditgesetz (VKKG) Entwurf vom... Der Schweizerische Bundesrat, gestützt auf die Artikel 14, 23 Absatz 3 und 40 Absatz 3 des Bundesgesetzes vom 23. März 2001 über den Konsumkredit
EU-Verordnung Nr. 1907/2006 (REACH)
 Was bedeutet REACH? REACH ist die EG-Verordnung Nr. 1907/2006 zur Registration, Evaluation, Authorization and Restriction of CHemicals (Registrierung, Bewertung und Zulassung von Chemikalien). Mit dieser
Was bedeutet REACH? REACH ist die EG-Verordnung Nr. 1907/2006 zur Registration, Evaluation, Authorization and Restriction of CHemicals (Registrierung, Bewertung und Zulassung von Chemikalien). Mit dieser
AGAH Workshop. Befreiung von der AMG Versicherungspflicht: Voraussetzungen und Implikationen. Markus Ambrosius
 AGAH Workshop 4. Juli 2012 Befreiung von der AMG Versicherungspflicht: Voraussetzungen und Implikationen Rechtsanwalt Markus Ambrosius Sträter Rechtsanwälte Kronprinzenstraße 20 Fon: +49 (0) 228-934 54-0
AGAH Workshop 4. Juli 2012 Befreiung von der AMG Versicherungspflicht: Voraussetzungen und Implikationen Rechtsanwalt Markus Ambrosius Sträter Rechtsanwälte Kronprinzenstraße 20 Fon: +49 (0) 228-934 54-0
Gleichwertigkeitsanerkennung nach Art. 119b AVIV
 Gleichwertigkeitsanerkennung nach Art. 119b AVIV Anleitung 23. Dezember 2014 www.vsaa.ch www.aost.ch www.ausl.ch info@vsaa.ch info@aost.ch info@ausl.ch Genfergasse 10 3011 Bern 031 310 0890 Inhalt 1 Einleitung...
Gleichwertigkeitsanerkennung nach Art. 119b AVIV Anleitung 23. Dezember 2014 www.vsaa.ch www.aost.ch www.ausl.ch info@vsaa.ch info@aost.ch info@ausl.ch Genfergasse 10 3011 Bern 031 310 0890 Inhalt 1 Einleitung...
1. Hamburger Pharma Tag 17. April 2012. Pharmakovigilanzregelungen Ein wirkliches Plus für die Arzneimittelsicherheit?
 1. Hamburger Pharma Tag 17. April 2012 Pharmakovigilanzregelungen Ein wirkliches Plus für die Arzneimittelsicherheit? Simone Winnands Agenda Definitionen zur Pharmakovigilanz Pharmakovigilanz im Zulassungsumfeld
1. Hamburger Pharma Tag 17. April 2012 Pharmakovigilanzregelungen Ein wirkliches Plus für die Arzneimittelsicherheit? Simone Winnands Agenda Definitionen zur Pharmakovigilanz Pharmakovigilanz im Zulassungsumfeld
Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren
 Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums für Gesundheit 1 Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren Politische Ebene Bundesbehörden Ministerien, insbesondere
Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums für Gesundheit 1 Verteilung der Verantwortlichkeiten zuvor, Anzeigeverfahren Politische Ebene Bundesbehörden Ministerien, insbesondere
Reglement. zum. Öffentlichkeitsprinzip. und. Datenschutz
 Reglement zum Öffentlichkeitsprinzip und Datenschutz Der Gemeinderat, gestützt auf 10, Abs. 3 und 31, Abs. 3 des Informations- und Datenschutzgesetzes (Info DG), sowie 5, Abs. 1.1. und 1.2. der Gemeindeordnung,
Reglement zum Öffentlichkeitsprinzip und Datenschutz Der Gemeinderat, gestützt auf 10, Abs. 3 und 31, Abs. 3 des Informations- und Datenschutzgesetzes (Info DG), sowie 5, Abs. 1.1. und 1.2. der Gemeindeordnung,
Reglement betreffend den Zugriff auf Personendaten zu Forschungszwecken
 Stadt Zürich Stadtspital Waid Zürich Medizinische Direktion Tièchestrasse 99 8037 Zürich Daniel Grob, Dr.med. MHA Zürich, 12. Oktober 2012 /Gr Reglement betreffend den Zugriff auf Personendaten zu Forschungszwecken
Stadt Zürich Stadtspital Waid Zürich Medizinische Direktion Tièchestrasse 99 8037 Zürich Daniel Grob, Dr.med. MHA Zürich, 12. Oktober 2012 /Gr Reglement betreffend den Zugriff auf Personendaten zu Forschungszwecken
Vereinbarung zur Sicherstellung des Schutzauftrages bei Kindeswohlgefährdung gem. 8a SGB VIII
 Die Senatorin für Bildung und Wissenschaft Vereinbarung zur Sicherstellung des Schutzauftrages bei Kindeswohlgefährdung gem. 8a SGB VIII zwischen dem Amt für Soziale Dienste / Jugendamt und der Senatorin
Die Senatorin für Bildung und Wissenschaft Vereinbarung zur Sicherstellung des Schutzauftrages bei Kindeswohlgefährdung gem. 8a SGB VIII zwischen dem Amt für Soziale Dienste / Jugendamt und der Senatorin
Studienregister für die Schweizer Öffentlichkeit welche Information ist (nicht) verfügbar?
 Studienregister für die Schweizer Öffentlichkeit welche Information ist (nicht) verfügbar? Forum Klinische Forschung Schweizerischer Nationalfonds Mittwoch, 30.01.2013, Bern Andri Christen, PhD Epidemiologist
Studienregister für die Schweizer Öffentlichkeit welche Information ist (nicht) verfügbar? Forum Klinische Forschung Schweizerischer Nationalfonds Mittwoch, 30.01.2013, Bern Andri Christen, PhD Epidemiologist
Newsletter: Februar 2016
 1 ASR GmbH www.asr-security.de Newsletter: Februar 2016 Neue behördliche Vorgaben für Onlineschulungen Seit dem 01. Februar 2016 gelten neue behördliche Anforderungen an Online- Luftsicherheitsschulungen.
1 ASR GmbH www.asr-security.de Newsletter: Februar 2016 Neue behördliche Vorgaben für Onlineschulungen Seit dem 01. Februar 2016 gelten neue behördliche Anforderungen an Online- Luftsicherheitsschulungen.
10. Keine Annahme weiterer Arbeiten
 Allgemeine Geschäftsbedingungen (AGB) Perle 1. Grundsätzliches 2. Zielsetzung 3. Dienstleistungsumfang 4. Dienstleistung 5. Dienstleistungsgrenzen 6. Tarife und Rechnungsstellung 7. Kündigung 8. Schweigepflicht
Allgemeine Geschäftsbedingungen (AGB) Perle 1. Grundsätzliches 2. Zielsetzung 3. Dienstleistungsumfang 4. Dienstleistung 5. Dienstleistungsgrenzen 6. Tarife und Rechnungsstellung 7. Kündigung 8. Schweigepflicht
Verordnung zur Änderung medizinprodukterechtlicher Vorschriften vom 16. Februar 2007
 26.02.2007 Verordnung zur Änderung medizinprodukterechtlicher Vorschriften vom 16. Februar 2007 Auf Grund des 37 Abs. 1, 9, 10 und 11 Satz 1 des Medizinproduktegesetzes in der Fassung der Bekanntmachung
26.02.2007 Verordnung zur Änderung medizinprodukterechtlicher Vorschriften vom 16. Februar 2007 Auf Grund des 37 Abs. 1, 9, 10 und 11 Satz 1 des Medizinproduktegesetzes in der Fassung der Bekanntmachung
InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
 Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
13.11.2015. Transparenz und Datenschutz: Gedanken aus Schweizer Sicht
 Transparenz und Datenschutz: Gedanken aus Schweizer Sicht 16. forumsante.ch David Rosenthal, 3. Februar 2015 1 In der Schweiz ist es einfacher Im privaten Bereich genügen im Datenschutzgesetz (DSG) ein
Transparenz und Datenschutz: Gedanken aus Schweizer Sicht 16. forumsante.ch David Rosenthal, 3. Februar 2015 1 In der Schweiz ist es einfacher Im privaten Bereich genügen im Datenschutzgesetz (DSG) ein
Gemeinsame Ausführungsordnung zum Madrider Abkommen 1 über die internationale Registrierung von Marken und zum Protokoll 2 zu diesem Abkommen
 BGBl. III - Ausgegeben am 9. März 2015 - Nr. 32 1 von 7 (Übersetzung) Gemeinsame Ausführungsordnung zum Madrider Abkommen 1 über die internationale Registrierung von Marken und zum Protokoll 2 zu diesem
BGBl. III - Ausgegeben am 9. März 2015 - Nr. 32 1 von 7 (Übersetzung) Gemeinsame Ausführungsordnung zum Madrider Abkommen 1 über die internationale Registrierung von Marken und zum Protokoll 2 zu diesem
Checkliste «Datenbekanntgabe»
 Checkliste «Datenbekanntgabe» 21 Abs. 1 des Informations- und Datenschutzgesetzes 1 regelt die Bekanntgabe von Personendaten wie folgt: 21 Bekanntgabe von Personendaten 1 Das öffentliche Organ gibt Personendaten
Checkliste «Datenbekanntgabe» 21 Abs. 1 des Informations- und Datenschutzgesetzes 1 regelt die Bekanntgabe von Personendaten wie folgt: 21 Bekanntgabe von Personendaten 1 Das öffentliche Organ gibt Personendaten
D i e n s t e D r i t t e r a u f We b s i t e s
 M erkblatt D i e n s t e D r i t t e r a u f We b s i t e s 1 Einleitung Öffentliche Organe integrieren oftmals im Internet angebotene Dienste und Anwendungen in ihre eigenen Websites. Beispiele: Eine
M erkblatt D i e n s t e D r i t t e r a u f We b s i t e s 1 Einleitung Öffentliche Organe integrieren oftmals im Internet angebotene Dienste und Anwendungen in ihre eigenen Websites. Beispiele: Eine
04.061 s Bundesgesetz über die Krankenversicherung. Teilrevision. Spitalfinanzierung (Differenzen)
 Wintersession 007 e-parl 18.1.007 09:08 04.061 s Bundesgesetz über die Krankenversicherung. Teilrevision. Spitalfinanzierung (Differenzen) für soziale Sicherheit und Gesundheit des es Bundesgesetz über
Wintersession 007 e-parl 18.1.007 09:08 04.061 s Bundesgesetz über die Krankenversicherung. Teilrevision. Spitalfinanzierung (Differenzen) für soziale Sicherheit und Gesundheit des es Bundesgesetz über
Richtlinie. des Gemeinsamen Bundesausschusses. zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie )
 Richtlinie des Gemeinsamen Bundesausschusses zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie ) in der Fassung vom 22. Januar 2004 veröffentlicht im Bundesanzeiger
Richtlinie des Gemeinsamen Bundesausschusses zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie ) in der Fassung vom 22. Januar 2004 veröffentlicht im Bundesanzeiger
Kanton St.Gallen Amt für Soziales Adoptiv- und Pflegekinder
 Kanton St.Gallen Amt für Soziales Adoptiv- und Pflegekinder Departement des Innern Impressum Herausgeber Kanton St.Gallen Departement des Innern Amt für Soziales Spisergasse 41 9001 St.Gallen T 058 229
Kanton St.Gallen Amt für Soziales Adoptiv- und Pflegekinder Departement des Innern Impressum Herausgeber Kanton St.Gallen Departement des Innern Amt für Soziales Spisergasse 41 9001 St.Gallen T 058 229
Appenzell Ausserrhoden
 Appenzell Ausserrhoden : Quellen / Unterlagen Appenzell Ausserrhoden Quellen PrüfR Prüfungsreglement für Heilpraktikerinnen und Heilpraktiker vom 29. April 2008, Stand am 1. Mai 2009, http://www.lexfind.ch/dta/21624/2/811.11.1.pdf.
Appenzell Ausserrhoden : Quellen / Unterlagen Appenzell Ausserrhoden Quellen PrüfR Prüfungsreglement für Heilpraktikerinnen und Heilpraktiker vom 29. April 2008, Stand am 1. Mai 2009, http://www.lexfind.ch/dta/21624/2/811.11.1.pdf.
BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH. Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II
 1 von 5 BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II 57. Verordnung: Konformitätsbewertung von Medizinprodukten [CELEX-Nr.: 32000L0070, 32001L0104,
1 von 5 BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II 57. Verordnung: Konformitätsbewertung von Medizinprodukten [CELEX-Nr.: 32000L0070, 32001L0104,
Das digitale Klassenund Notizbuch
 Das digitale Klassenund Notizbuch Datenschutzrechtliche Rahmenbedingungen Tel.: 0431/9881207 Fax: 0431/9881223 Email:ULD21@datenschutzzentrum.de www.datenschutz.de 30 Abs. 2 SchulG Die Daten der Schulverwaltung
Das digitale Klassenund Notizbuch Datenschutzrechtliche Rahmenbedingungen Tel.: 0431/9881207 Fax: 0431/9881223 Email:ULD21@datenschutzzentrum.de www.datenschutz.de 30 Abs. 2 SchulG Die Daten der Schulverwaltung
Veterinärdienst Hauptgasse 72 4509 Solothurn. Gesuch für die Haltung eines bewilligungspflichtigen Hundes 4 Ziff. 1 Gesetz über das Halten von Hunden
 Amt für Landwirtschaft Veterinärdienst Hauptgasse 72 4509 Solothurn Telefon 032 627 25 02 Telefax 032 627 25 09 Veterinärdienst Hauptgasse 72 4509 Solothurn Gesuch für die Haltung eines bewilligungspflichtigen
Amt für Landwirtschaft Veterinärdienst Hauptgasse 72 4509 Solothurn Telefon 032 627 25 02 Telefax 032 627 25 09 Veterinärdienst Hauptgasse 72 4509 Solothurn Gesuch für die Haltung eines bewilligungspflichtigen
1 Abs. 1 a Satz 2 Nr. 1 a KWG definiert die Anlageberatung als die
 Die gesetzliche Definition der Anlageberatung 1 Abs. 1 a Satz 2 Nr. 1 a KWG definiert die Anlageberatung als die Abgabe von persönlichen Empfehlungen an Kunden oder deren Vertreter, die sich auf Geschäfte
Die gesetzliche Definition der Anlageberatung 1 Abs. 1 a Satz 2 Nr. 1 a KWG definiert die Anlageberatung als die Abgabe von persönlichen Empfehlungen an Kunden oder deren Vertreter, die sich auf Geschäfte
Antrag'auf'Hilfeleistungen'aus'dem'Fonds'Sexueller'' Missbrauch'im'familiären'Bereich' '' A)'Zweck'des'Fonds'Sexueller'Missbrauch'
 Antrag'auf'Hilfeleistungen'aus'dem'Fonds'Sexueller'' Missbrauch'im'familiären'Bereich' '' A)'Zweck'des'Fonds'Sexueller'Missbrauch' Der Fonds Sexueller Missbrauch im familiären Bereich will Betroffenen
Antrag'auf'Hilfeleistungen'aus'dem'Fonds'Sexueller'' Missbrauch'im'familiären'Bereich' '' A)'Zweck'des'Fonds'Sexueller'Missbrauch' Der Fonds Sexueller Missbrauch im familiären Bereich will Betroffenen
Grundsätzliche Informationen zu SpAz
 Grundsätzliche Informationen zu SpAz SpAz steht Ihnen zur Eingabe der Personen- und Leistungsdaten Ihrer Absolventen zur Verfügung. Die erforderlichen Daten zur Eingabe entsprechen dabei den Angaben von
Grundsätzliche Informationen zu SpAz SpAz steht Ihnen zur Eingabe der Personen- und Leistungsdaten Ihrer Absolventen zur Verfügung. Die erforderlichen Daten zur Eingabe entsprechen dabei den Angaben von
Verordnung über die Zulassung zur nichtärztlichen psychotherapeutischen und psychologischen Berufstätigkeit (PsychV)
 8.005 Verordnung über die Zulassung zur nichtärztlichen psychotherapeutischen und psychologischen Berufstätigkeit (PsychV) vom 7. Dezember 996 Der Regierungsrat des Kantons Schaffhausen, gestützt auf Art.
8.005 Verordnung über die Zulassung zur nichtärztlichen psychotherapeutischen und psychologischen Berufstätigkeit (PsychV) vom 7. Dezember 996 Der Regierungsrat des Kantons Schaffhausen, gestützt auf Art.
1. Allgemeine Bestimmungen... 2. 2. Arbeitszeit... 2. 3. Schwankungen in der wöchentlichen Arbeitszeit... 3. 4. Überstunden... 3. 5. Überzeit...
 1. Allgemeine Bestimmungen... 2 1.1. Geltungsbereich...2 1.2. Sprachregelung...2 2. Arbeitszeit... 2 2.1. Vertrauensarbeitszeit...2 2.2. Wöchentliche Arbeitszeit...2 2.3. Service Zeit...2 2.4. Individuelle
1. Allgemeine Bestimmungen... 2 1.1. Geltungsbereich...2 1.2. Sprachregelung...2 2. Arbeitszeit... 2 2.1. Vertrauensarbeitszeit...2 2.2. Wöchentliche Arbeitszeit...2 2.3. Service Zeit...2 2.4. Individuelle
Dieses Gesetz regelt die Aktenführung, die Archivierung und die Benutzung der Unterlagen
 Anhang 5. ENTWURF Gesetz über die Archivierung (Archivierungsgesetz) Vom Der Landrat des Kantons Basel-Landschaft beschliesst: A Allgemeine Bestimmungen Zweck Dieses Gesetz dient der Nachvollziehbarkeit
Anhang 5. ENTWURF Gesetz über die Archivierung (Archivierungsgesetz) Vom Der Landrat des Kantons Basel-Landschaft beschliesst: A Allgemeine Bestimmungen Zweck Dieses Gesetz dient der Nachvollziehbarkeit
Vollziehungsverordnung zum Bundesgesetz über den Konsumkredit (VVzKKG)
 933.00 Vollziehungsverordnung zum Bundesgesetz über den Konsumkredit (VVzKKG) Vom. Februar 006 (Stand. April 006) gestützt auf Art. 39 und 40 des Bundesgesetzes über den Konsumkredit (KKG) ), Art. 4 ff.
933.00 Vollziehungsverordnung zum Bundesgesetz über den Konsumkredit (VVzKKG) Vom. Februar 006 (Stand. April 006) gestützt auf Art. 39 und 40 des Bundesgesetzes über den Konsumkredit (KKG) ), Art. 4 ff.
WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht. Mittwoch, 13. Januar 2010. Pandemie - Teil X
 Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 13. Januar 2010 Pandemie - Teil X -Dr. Michael Cramer-2010-01-13 Folie 1 Ministerium für,,, und Klinische Prüfungen
Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 13. Januar 2010 Pandemie - Teil X -Dr. Michael Cramer-2010-01-13 Folie 1 Ministerium für,,, und Klinische Prüfungen
Reglement. Entlastungsleistungen bei der Pflege zu Hause
 Reglement über Entlastungsleistungen bei der Pflege zu Hause vom 0. Februar 995 Revision vom. September 998 5. Januar 999 3. Januar 005 6. Dezember 03 Inhaltsverzeichnis Seite A. Allgemeines Ziel Grundsatz
Reglement über Entlastungsleistungen bei der Pflege zu Hause vom 0. Februar 995 Revision vom. September 998 5. Januar 999 3. Januar 005 6. Dezember 03 Inhaltsverzeichnis Seite A. Allgemeines Ziel Grundsatz
Reglement über Gemeindebeiträge an die schulergänzenden Betreuungsangebote der Gemeinde Allschwil
 REGLEMENT ÜBER GEMEINDEBEITRÄGE E I N W O H N E R G E M E I N D E Reglement über Gemeindebeiträge an die schulergänzenden Betreuungsangebote der Gemeinde Allschwil Reglementssammlung der Einwohnergemeinde
REGLEMENT ÜBER GEMEINDEBEITRÄGE E I N W O H N E R G E M E I N D E Reglement über Gemeindebeiträge an die schulergänzenden Betreuungsangebote der Gemeinde Allschwil Reglementssammlung der Einwohnergemeinde
WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE
 WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE Nabelschnurblut ist wertvoll! Wenn sich Eltern dafür entscheiden, das Nabelschnurblut ihres Kindes aufzubewahren, können sie damit dem Kind selbst,
WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE Nabelschnurblut ist wertvoll! Wenn sich Eltern dafür entscheiden, das Nabelschnurblut ihres Kindes aufzubewahren, können sie damit dem Kind selbst,
14.046 s Bundesgesetz über den Wald. Änderung (Differenzen)
 Ständerat Wintersession 05 eparl 3..05 5:43 4.046 s Bundesgesetz über den Wald. Änderung (Differenzen) Geltendes Recht Entwurf des Bundesrates Beschluss des Ständerates Beschluss des es Anträge der Kommission
Ständerat Wintersession 05 eparl 3..05 5:43 4.046 s Bundesgesetz über den Wald. Änderung (Differenzen) Geltendes Recht Entwurf des Bundesrates Beschluss des Ständerates Beschluss des es Anträge der Kommission
ISO 9001:2015 REVISION. Die neue Struktur mit veränderten Schwerpunkten wurde am 23. September 2015 veröffentlicht und ist seit 15.09.
 ISO 9001:2015 REVISION Die neue Struktur mit veränderten Schwerpunkten wurde am 23. September 2015 veröffentlicht und ist seit 15.09.2015 in Kraft 1 Präsentationsinhalt Teil 1: Gründe und Ziele der Revision,
ISO 9001:2015 REVISION Die neue Struktur mit veränderten Schwerpunkten wurde am 23. September 2015 veröffentlicht und ist seit 15.09.2015 in Kraft 1 Präsentationsinhalt Teil 1: Gründe und Ziele der Revision,
Forschung. 6.1. Forschung am Menschen
 92 KAPITEL 6 Forschung 6.1. Forschung am Menschen Mit dem im März 2010 von Volk und Ständen angenommenen Verfassungsartikel Art. 118b BV wurde der Bund ermächtigt, die Forschung am Menschen umfassend zu
92 KAPITEL 6 Forschung 6.1. Forschung am Menschen Mit dem im März 2010 von Volk und Ständen angenommenen Verfassungsartikel Art. 118b BV wurde der Bund ermächtigt, die Forschung am Menschen umfassend zu
Verschreibungsfreie Arzneimittel wieder in der Erstattung
 Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
CHECKLISTE für KRANKENANSTALTEN
 CHECKLISTE für KRANKENANSTALTEN 12 Schritte zur nutritionday Teilnahme (nd.h) 6 Monate bis 1 Woche vor nutritionday 1 2 3 4 5 6 7 8 9 10 11 12 Registrieren und Kodes bestellen Beachten Sie nationale Richtlinien
CHECKLISTE für KRANKENANSTALTEN 12 Schritte zur nutritionday Teilnahme (nd.h) 6 Monate bis 1 Woche vor nutritionday 1 2 3 4 5 6 7 8 9 10 11 12 Registrieren und Kodes bestellen Beachten Sie nationale Richtlinien
Liechtensteinisches Landesgesetzblatt
 Liechtensteinisches Landesgesetzblatt 952.11 Jahrgang 2015 Nr. 250 ausgegeben am 25. September 2015 Verordnung vom 22. September 2015 über die Abänderung der Sorgfaltspflichtverordnung Aufgrund von Art.
Liechtensteinisches Landesgesetzblatt 952.11 Jahrgang 2015 Nr. 250 ausgegeben am 25. September 2015 Verordnung vom 22. September 2015 über die Abänderung der Sorgfaltspflichtverordnung Aufgrund von Art.
Verordnung des VBS über den Flugdienst der Gruppe Rüstung
 Verordnung des VBS über den Flugdienst der Gruppe Rüstung 510.211.3 vom 15. Mai 2003 (Stand am 3. Juni 2003) Das Eidgenössische Departement für Verteidigung, Bevölkerungsschutz und Sport (VBS), gestützt
Verordnung des VBS über den Flugdienst der Gruppe Rüstung 510.211.3 vom 15. Mai 2003 (Stand am 3. Juni 2003) Das Eidgenössische Departement für Verteidigung, Bevölkerungsschutz und Sport (VBS), gestützt
Exkurs: Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen
 Exkurs: Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen 139a SGB V Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (1) Der Gemeinsame Bundesausschuss nach 91 gründet
Exkurs: Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen 139a SGB V Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (1) Der Gemeinsame Bundesausschuss nach 91 gründet
Wholesale und FTTH. Handbuch Abrechnung 1/5. Ausgabedatum 01.05.2015 Ersetzt Version 2-0. Swisscom (Schweiz) AG CH-3050 Bern
 Ausgabedatum 005.2015 Ersetzt Version 2-0 Gültig ab 005.2015 Gültig ab 005.2015 1/5 Inhaltsverzeichnis 1 Einleitung... 3 2 Rechnungsstellung... 3 3 Rechnungen... 3 4 Zahlungen... 4 5 Widerspruch gegen
Ausgabedatum 005.2015 Ersetzt Version 2-0 Gültig ab 005.2015 Gültig ab 005.2015 1/5 Inhaltsverzeichnis 1 Einleitung... 3 2 Rechnungsstellung... 3 3 Rechnungen... 3 4 Zahlungen... 4 5 Widerspruch gegen
Nr. 866a Verordnung zum Gesetz über die Verbilligung von Prämien der Krankenversicherung (Prämienverbilligungsverordnung)
 Nr. 866a Verordnung zum Gesetz über die Verbilligung von Prämien der Krankenversicherung (Prämienverbilligungsverordnung) vom. Dezember 995* (Stand. Januar 00) Der Regierungsrat des Kantons Luzern, gestützt
Nr. 866a Verordnung zum Gesetz über die Verbilligung von Prämien der Krankenversicherung (Prämienverbilligungsverordnung) vom. Dezember 995* (Stand. Januar 00) Der Regierungsrat des Kantons Luzern, gestützt
von Einstufungsprüfungen gem. 6 Abs. 1 Nr. 2 Satz 2 der Polizeilaufbahnverordnung
 Prüfungsordnung der Hochschule für Öffentliche Verwaltung Bremen für die Durchführung von Einstufungsprüfungen zum Erwerb der fachgebundenen Hochschulreife gemäß 6 Abs. 1 Nr. 2 der Polizeilaufbahnverordnung
Prüfungsordnung der Hochschule für Öffentliche Verwaltung Bremen für die Durchführung von Einstufungsprüfungen zum Erwerb der fachgebundenen Hochschulreife gemäß 6 Abs. 1 Nr. 2 der Polizeilaufbahnverordnung
Off-Label Use Ärztliche Therapiefreiheit und Haftungsrisiken im Spannungsfeld
 Off-Label Use Ärztliche Therapiefreiheit und Haftungsrisiken im Spannungsfeld 12. November 2015 Dr. iur. et dipl. sc. nat. ETH Stefan Kohler, Rechtsanwalt, VISCHER AG Inhalt Worum geht es? Sorgfaltspflichten
Off-Label Use Ärztliche Therapiefreiheit und Haftungsrisiken im Spannungsfeld 12. November 2015 Dr. iur. et dipl. sc. nat. ETH Stefan Kohler, Rechtsanwalt, VISCHER AG Inhalt Worum geht es? Sorgfaltspflichten
Zwischen Deutschland, Liechtenstein, Österreich und der Schweiz abgestimmte deutsche Übersetzung
 Zwischen Deutschland, Liechtenstein, Österreich und der Schweiz abgestimmte deutsche Übersetzung ÄNDERUNG DES ÜBEREINKOMMENS ÜBER DEN ZUGANG ZU INFORMATIONEN, DIE ÖFFENTLICHKEITSBETEILIGUNG AN ENTSCHEIDUNGSVERFAHREN
Zwischen Deutschland, Liechtenstein, Österreich und der Schweiz abgestimmte deutsche Übersetzung ÄNDERUNG DES ÜBEREINKOMMENS ÜBER DEN ZUGANG ZU INFORMATIONEN, DIE ÖFFENTLICHKEITSBETEILIGUNG AN ENTSCHEIDUNGSVERFAHREN
Die Betriebssicherheitsverordnung (BetrSichV) TRBS 1111 TRBS 2121 TRBS 1203
 Die Betriebssicherheitsverordnung (BetrSichV) TRBS 1111 TRBS 2121 TRBS 1203 Achim Eckert 1/12 Am 3. Oktober 2002 ist die Betriebssicherheitsverordnung in Kraft getreten. Auch für den Gerüstbauer und den
Die Betriebssicherheitsverordnung (BetrSichV) TRBS 1111 TRBS 2121 TRBS 1203 Achim Eckert 1/12 Am 3. Oktober 2002 ist die Betriebssicherheitsverordnung in Kraft getreten. Auch für den Gerüstbauer und den
Tutorium Klinische Psychologie I. Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie
 Tutorium Klinische Psychologie I Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Oswald David
Tutorium Klinische Psychologie I Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Fragen zur Ausbildung und rechtlichen Grundlagen in der Klinischen Psychologie Oswald David
Zypern. Mehrwertsteuererstattungen nach der 13. MwSt-Richtlinie (86/560/EWG)
 Zypern Mehrwertsteuererstattungen nach der 13. MwSt-Richtlinie (86/560/EWG) I. GEGENSEITIGKEITSABKOMMEN Artikel 2 Absatz 2 1. Hat Ihr Land Gegenseitigkeitsabkommen abgeschlossen? Ja, Zypern hat zwei Gegenseitigkeitsabkommen
Zypern Mehrwertsteuererstattungen nach der 13. MwSt-Richtlinie (86/560/EWG) I. GEGENSEITIGKEITSABKOMMEN Artikel 2 Absatz 2 1. Hat Ihr Land Gegenseitigkeitsabkommen abgeschlossen? Ja, Zypern hat zwei Gegenseitigkeitsabkommen
VLK NRW 2013. Rechtsanwalt und Fachanwalt f. Medizin-, Steuer- und Arbeitsrecht Norbert H. Müller
 VLK NRW 2013 Rechtsanwalt und Fachanwalt f. Medizin-, Steuer- und Arbeitsrecht Norbert H. Müller Haftpflichtversicherung Wie verhält sich der leitende Krankenhausarzt richtig? Haftpflichtversicherung Differenzierung
VLK NRW 2013 Rechtsanwalt und Fachanwalt f. Medizin-, Steuer- und Arbeitsrecht Norbert H. Müller Haftpflichtversicherung Wie verhält sich der leitende Krankenhausarzt richtig? Haftpflichtversicherung Differenzierung
6 Schulungsmodul: Probenahme im Betrieb
 6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
6 Schulungsmodul: Probenahme im Betrieb WIEDNER Wie schon im Kapitel VI erwähnt, ist die Probenahme in Betrieben, die Produkte nach dem Lebensmittel- und Futtermittelgesetzbuch herstellen oder in den Verkehr
Stellen Gesundheits- und Medizin Apps ein Sicherheitsrisiko dar?
 Stellen Gesundheits- und Medizin Apps ein Sicherheitsrisiko dar? 04.06.2013 Medical Apps 2013 Kathrin Schürmann, Rechtsanwältin 1 2013 ISiCO Datenschutz GmbH All rights reserved 2 1 Chancen und Risiken
Stellen Gesundheits- und Medizin Apps ein Sicherheitsrisiko dar? 04.06.2013 Medical Apps 2013 Kathrin Schürmann, Rechtsanwältin 1 2013 ISiCO Datenschutz GmbH All rights reserved 2 1 Chancen und Risiken
Der Schutz von Patientendaten
 Der Schutz von Patientendaten bei (vernetzten) Software-Medizinprodukten aus Herstellersicht 18.09.2014 Gerald Spyra, LL.M. Kanzlei Spyra Vorstellung meiner Person Gerald Spyra, LL.M. Rechtsanwalt Spezialisiert
Der Schutz von Patientendaten bei (vernetzten) Software-Medizinprodukten aus Herstellersicht 18.09.2014 Gerald Spyra, LL.M. Kanzlei Spyra Vorstellung meiner Person Gerald Spyra, LL.M. Rechtsanwalt Spezialisiert
Datenschutz und Qualitätssicherung
 Datenschutz und Qualitätssicherung AQC-Tagung 2015 David Rosenthal 19. November 2015 1 Datenschutz? Personendaten? Jede Angabe, die sich auf eine bestimmte oder bestimmbare Person bezieht. Bestimmbarkeit?
Datenschutz und Qualitätssicherung AQC-Tagung 2015 David Rosenthal 19. November 2015 1 Datenschutz? Personendaten? Jede Angabe, die sich auf eine bestimmte oder bestimmbare Person bezieht. Bestimmbarkeit?
6 Informationsermittlung und Gefährdungsbeurteilung
 Verordnung zum Schutz vor Gefahrstoffen TK Lexikon Arbeitsrecht 6 Informationsermittlung und Gefährdungsbeurteilung HI2516431 (1) 1 Im Rahmen einer Gefährdungsbeurteilung als Bestandteil der Beurteilung
Verordnung zum Schutz vor Gefahrstoffen TK Lexikon Arbeitsrecht 6 Informationsermittlung und Gefährdungsbeurteilung HI2516431 (1) 1 Im Rahmen einer Gefährdungsbeurteilung als Bestandteil der Beurteilung
Schweizerische Vereinigung für Kleintiermedizin SVK. Ordnung für die Bezeichnung "Spezialtierarzt FVH für Kleintiere"
 Schweizerische Vereinigung für Kleintiermedizin SVK Ordnung für die Bezeichnung "Spezialtierarzt FVH für Kleintiere" 1 Spezialtierarztbezeichnung Für das Gebiet der Kleintiermedizin wird die Bezeichnung
Schweizerische Vereinigung für Kleintiermedizin SVK Ordnung für die Bezeichnung "Spezialtierarzt FVH für Kleintiere" 1 Spezialtierarztbezeichnung Für das Gebiet der Kleintiermedizin wird die Bezeichnung
Kapitel I: Registrierung im Portal
 Kapitel I: Registrierung im Portal Um zu unserem Portal zu gelangen, rufen Sie bitte die folgende Internetseite auf: www.arag-forderungsmanagement.de Bei Ihrem ersten Besuch des ARAG Portals ist es notwendig,
Kapitel I: Registrierung im Portal Um zu unserem Portal zu gelangen, rufen Sie bitte die folgende Internetseite auf: www.arag-forderungsmanagement.de Bei Ihrem ersten Besuch des ARAG Portals ist es notwendig,
Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Wiederholungsverordnung
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Stand der Revision: 13.11.2013
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Stand der Revision: 13.11.2013
4.05 Leistungen der IV Vergütung der Reisekosten in der IV
 4.05 Leistungen der IV Vergütung der Reisekosten in der IV Stand am 1. Januar 2015 1 Auf einen Blick Die Invalidenversicherung vergütet die Reisekosten, die sie für die Umsetzung der von ihr angeordneten
4.05 Leistungen der IV Vergütung der Reisekosten in der IV Stand am 1. Januar 2015 1 Auf einen Blick Die Invalidenversicherung vergütet die Reisekosten, die sie für die Umsetzung der von ihr angeordneten
Ergänzungsbericht zum Tätigkeitsbericht 2013 über die Ergebnisse der externen vergleichenden Qualitätssicherung
 Ergänzungsbericht zum Tätigkeitsbericht 2013 über die Ergebnisse der externen vergleichenden Qualitätssicherung Transplantationszentrum Deutsches Herzzentrum Berlin nach 11 Abs. 5 TPG - veröffentlicht
Ergänzungsbericht zum Tätigkeitsbericht 2013 über die Ergebnisse der externen vergleichenden Qualitätssicherung Transplantationszentrum Deutsches Herzzentrum Berlin nach 11 Abs. 5 TPG - veröffentlicht
Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel
 Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel Das Schweizer Volk soll sich selber äussern bezüglich der Gesetzgebung zur embryonalen Stammzellenforschung. Die ethische Bedeutung
Die Forschung mit embryonalen Stammzellen ist ethisch nicht akzeptabel Das Schweizer Volk soll sich selber äussern bezüglich der Gesetzgebung zur embryonalen Stammzellenforschung. Die ethische Bedeutung
Informationen zum Begleiteten Fahren ab 17
 Informationen zum Begleiteten Fahren ab 17 Ausbildung Darf auch ein Bewerber ausgebildet werden, der in einem Bundesland seinen ersten Wohnsitz hat, wenn dieses Bundesland das Begleitete Fahren nicht eingeführt
Informationen zum Begleiteten Fahren ab 17 Ausbildung Darf auch ein Bewerber ausgebildet werden, der in einem Bundesland seinen ersten Wohnsitz hat, wenn dieses Bundesland das Begleitete Fahren nicht eingeführt
Zwei Schwerpunkte aus Sicht der ärzteeigenen Datensammlung. Tarifdelegierten-Tag Bern, 23. Oktober 2013
 Zwei Schwerpunkte aus Sicht der ärzteeigenen Datensammlung Tarifdelegierten-Tag Bern, 23. Oktober 2013 Themen Pseudonymisierung Übersicht Datensammlung Datenschutz & Umgang mit Patientendaten Wie wird
Zwei Schwerpunkte aus Sicht der ärzteeigenen Datensammlung Tarifdelegierten-Tag Bern, 23. Oktober 2013 Themen Pseudonymisierung Übersicht Datensammlung Datenschutz & Umgang mit Patientendaten Wie wird
Schulzahnpflege Reglement (Inkraftsetzung am 20. August 2007)
 Schulzahnpflege Reglement (Inkraftsetzung am 20. August 2007) 1. Ziel und allgemeine Bestimmungen Das Ziel der Schulzahnpflege besteht darin, durch Massnahmen zur Erhaltung einer gesunden Mundhöhle einen
Schulzahnpflege Reglement (Inkraftsetzung am 20. August 2007) 1. Ziel und allgemeine Bestimmungen Das Ziel der Schulzahnpflege besteht darin, durch Massnahmen zur Erhaltung einer gesunden Mundhöhle einen
zum Bundesgesetz über die Neuordnung der Pflegefinanzierung
 GSD/Vorentwurf vom 6.05.00 Ausführungsgesetz vom zum Bundesgesetz über die Neuordnung der Pflegefinanzierung Der Grosse Rat des Kantons Freiburg gestützt auf das Bundesgesetz vom 3. Juni 008 über die Neuordnung
GSD/Vorentwurf vom 6.05.00 Ausführungsgesetz vom zum Bundesgesetz über die Neuordnung der Pflegefinanzierung Der Grosse Rat des Kantons Freiburg gestützt auf das Bundesgesetz vom 3. Juni 008 über die Neuordnung
Vertrag zwischen. der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV)
 Vertrag zwischen der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV) über die Abgrenzung, Vergütung und Abrechnung der stationären vertragsärztlichen Tätigkeit 1) Dem
Vertrag zwischen der AOK Berlin - Die Gesundheitskasse - und der Kassenärztlichen Vereinigung Berlin (KV) über die Abgrenzung, Vergütung und Abrechnung der stationären vertragsärztlichen Tätigkeit 1) Dem
Vortrag. Elektronische Rechnungslegung
 Vortrag 29. November 2007 ecomm Berlin Dag Klimas Ihr Vortragender Jahrgang 1961 Werdegang Ausbildung Bankkaufmann Weiterbildung Bankfachwirt Ausbildereignung Kommunikationstrainer und Berater... Basisinformationen
Vortrag 29. November 2007 ecomm Berlin Dag Klimas Ihr Vortragender Jahrgang 1961 Werdegang Ausbildung Bankkaufmann Weiterbildung Bankfachwirt Ausbildereignung Kommunikationstrainer und Berater... Basisinformationen
POINT. of Reha Sport e.v. Reha-Sport. Der Wegweiser zum. Eine Information für Patientinnen, Patienten und Angehörige
 POINT of Reha Sport e.v. Der Wegweiser zum Reha-Sport Eine Information für Patientinnen, Patienten und Angehörige Was ist Reha Sport? Reha Sport wird in Form von Wirbelsäulengymnastik und Bewegungsschule,
POINT of Reha Sport e.v. Der Wegweiser zum Reha-Sport Eine Information für Patientinnen, Patienten und Angehörige Was ist Reha Sport? Reha Sport wird in Form von Wirbelsäulengymnastik und Bewegungsschule,
DOKUMENTATION. Verfahren bei Schliessungen und Verlegungen von Poststellen und Postagenturen (Art. 34 VPG)
 Eidgenössische Postkommission PostCom Commission fédérale de la poste PostCom Commissione federale delle poste PostCom Federal Postal Services Commission PostCom DOKUMENTATION Verfahren bei Schliessungen
Eidgenössische Postkommission PostCom Commission fédérale de la poste PostCom Commissione federale delle poste PostCom Federal Postal Services Commission PostCom DOKUMENTATION Verfahren bei Schliessungen
