5.2.8 Schalenaufbau der Atomhülle und Periodensystem der Elemente; Röntgenspektren
|
|
|
- Wilhelmine Franke
- vor 7 Jahren
- Abrufe
Transkript
1 5..8 Schalenaufbau der Atomhülle und Periodensystem der Elemente; Röntgenspektren Der Schalenaufbau der Atomhülle Für die Beschreibung eines Elektrons im dreidimensionalen Raum braucht man auch drei voneinander unabhängige Quantenzahlen. Sie werden im folgenden nicht vom dreidimensionalen Potentialtopf übernommen, sondern experimentell zugänglichen Eigenschaften des Atoms angepasst, nämlich der Energie, dem Drehimpuls und dem magnetischen Verhalten. Diese Größen sind wesentlich zur Beschreibung des Bohr-Sommerfeld-Modells; ihre möglichen Werte werden ohne Beweis beschrieben:. Die Hauptquantenzahl n bestimmt im wesentlichen die Energie des Elektrons im betreffenden Zustand.. Die Drehimpulsquantenzahl l gibt an, welcher Bahndrehimpuls im Bohrschen Modell einem um einen ern kreisenden Elektrons zukommt. Für l gilt: l n Die magnetische Quantenzahl m erklärt das Aufspalten von Spektrallinien in starken magnetischen Feldern (Zeeman-Effekt). Liegt die Bahnquantenzahl l vor, dann kann m folgende Werte annehmen: -l, -l+,, -, 0,,, l-, l 4. Die Spinquantenzahl s verhilft zu einer Erklärung der noch größeren Vielfalt der Spektren als man sie mit den drei Quantenzahlen n, l und m beschreiben kann. Beispielsweise kann der Stern-Gerlach-Versuch nur mit der enntnis von s verstanden werden. s nimmt nur diese beiden Werte an: s =!. Der österreichische Physiker Wolfgang Pauli ( , NP 945) erkannte 94 einen wichtigen Zusammenhang zwischen den Quantenzahlen, der für das Verständnis des Atomaufbaus äußerst wichtig ist, das sog. Pauli-Prinzip. Pauli-Prinzip: In einem Atom oder Molekül können nie zwei Elektronen in allen vier Quantenzahlen übereinstimmen. Die vorhandenen Elektronen besetzen vielmehr die durch die Quantenzahlen festgelegten Energiestufen von unten her, falls sie nicht durch Energiezufuhr vorübergehend in höhere Niveaus gehoben werden. Mit Hilfe des Pauli-Prinzips ergibt sich ein einfaches Bauprinzip für das sog. Periodensystem der Elemente. In der nachfolgenden Tabelle sind die ombinationen von n, l, m und s, bei denen nie alle vier Quantenzahlen übereinstimmen, für n = bis n = 4 zusammengestellt. Tabelle: Seite 5--8-
2 Verteilung der Elektronen auf die Haupt- und Unterschalen der Atomhüllen -Schale L-Schale M-Schale N-Schale Hauptquantenzahl n Nebenquantenzahl l 0 (s-elektronen) 0 (s-elektronen (p-elektronen 3 0 (s-elektronen) (p-elektronen) (d-elektronen) Magnetische Quantenzahl m 0 ± / - ± / 0 ± / + ± / 0 ± / - ± / 0 ± / + ± / Spin- Quantenzahl s 0 ± / ± / ± / ± / ± / ± / Zahl der möglichen Zustände 0 Gesamtzahl der möglichen Zustände Man erkennt, dass zur Hauptquantenzahl n unter Berücksichtigung des Spins insgesamt n verschiedene Zustände existieren. Sowohl beim Bohr-Sommerfeldschen als auch beim wellenmechanischen Atommodell nimmt der mittlere Abstand des Elektrons vom ern mit der Hauptquantenzahl n zu. Es liegt daher nahe, sich vorzustellen, dass die Atomhülle aus Schalen besteht, in denen sich die Elektronen mit der gleichen Hauptquantenzahl n befinden. Die Schalen, die zu den Hauptquantenzahlen n = bis n = 7 gehören, werden mit den großen Buchstaben, L, M, N, O und P bezeichnet. Ein Zustand mit l = 0 heißt s-zustand, mit l = p-zustand usw. Ein 4f-Elektron hat z. B. n = 4 und l = Tabelle: Seite 5--8-
3 Hauptschalen L M N O Energie stufen s s p 3s 3p 3d 4s 4p 4d 4f 5s Vorperiode H He Erste urzpe riode Li Be B C 7 N 3 8 O 4 9 F 5 0 Ne Zweite urzpe riode 3 Na Mg Al 4 Si 5 P 3 S 4 7 Cl 5 8 Ag Erste Langpe riode 9 0 Ca Sc Periodizität der Ionisierungsenergie und des Atomvolumens Das Periodensystem der Elemente wurde im Jahr 89 durch Mendelejew und unabhängig davon durch L. Meyer entdeckt. Es zeigte sich dabei, dass man die chemischen Elemente in Spalten und Zeilen so anordnen kann, dass in jeder Spalte chemisch verwandte Elemente stehen und dass die "Atomgewichte", von wenigen Ausnahmen abgesehen, zeilenweise von links nach rechts ansteigen. Die Ordnungszahl wurde 93 durch verschiedene Forscher als die ernladungszahl der Elemente erkannt. Da die ernladungszahl im Periodensystem monoton ansteigt, muss die Periodizität im chemischen Verhalten auf Besonderheiten im Aufbau der Seite
4 Elektronenhülle zurückzuführen sein. Dies zeigt sich auch bei einer Reihe von physikalischen Eigenschaften der Atome, zum Beispiel der Ionisierungsenergie für das am leichtesten ablösbare Elektron und dem Atomvolumen. Abbildungen: 5 He Ne 50 Rb 0 Ar 40 5 H r 30 Na 0 0 H Li 5 Li Na Rb Erste Ionisierungsspannung _Atomvolumen in cm3/mol in ev Die Skizzen sind sehr stark vereinfacht! Man erkennt eine auffallende Periodizität. In der ersten Hauptgruppe z. B. nehmen die Atomvolumina jeweils ein Maximum, die Ionisierungsenergien dagegen ein Minimum gegenüber den Nachbarelementen ein. Aus der geringen Ionisationsenergie lässt sich folgern, dass die positive ernladung weitgehend durch die übrigen Elektronen der Hülle abgeschirmt ist. Sie umschließen den ern offensichtlich wie "Schalen". Die relativ großen Atomvolumina bei denselben Atomen weisen dagegen darauf hin, dass das abzutrennende Elektron einem neuen, ausgedehnten Aufenthaltsraum zuzurechnen ist. Es befindet sich in einer neuen "Schale". Röntgenemissionsspektren, Moseley-Gesetz Röntgenstrahlen entstehen, wenn Elektronen mit genügend hoher Energie auf Materie treffen. Eine genauere Untersuchung zeigt, dass diese nicht einheitlich ist, sondern aus zwei Bestandteilen besteht, die sich in Bezug auf ihre Entstehung und ihre Zusammensetzung erheblich voneinander unterscheiden. a) Die Röntgenbremsstrahlung: Seite
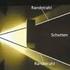
5 Die Bremsstrahlung entsteht bei der Abbremsung hochenergetischer Elektronen im Anodenmaterial einer Röntgenröhre. Die Bremsung (Beschleunigung) der Elektronen auf einem sehr kurzen Weg ist mit der Aussendung elektromagnetischer Wellen verbunden. Da die abgebremsten Elektronen beliebige Restenergien haben, erhält man ein kontinuierliches Spektrum, das an seinem kurzwellen Ende scharf abbricht. Diese Grenzwellenlänge λ g bzw. Grenzfrequenz f g ist aus dem Energiesatz leicht verständlich: Wird ein Elektron der kinetischen Energie W = e U gänzlich abgebremst und seine kinetische Energie vollständig in Strahlungsenergie umgesetzt, erhält man den Zusammenhang W = e $ U = h $ f g bzw. f g = e$u h (Duane-Hunt-Gesetz). Der Mechanismus der Entstehung der Röntgenbremsstrahlung hat zur Folge, dass die Bremsstrahlung vom Material, auf das die Elektronen treffen, unabhängig ist. Die Entstehung der Röntgenbremsstrahlung kann als Umkehrung des Fotoeffekts angesehen werden. b) Die charakteristische Röntgenstrahlung: Versuch: Ein gebündelter Röntgenstrahl aus einer Molybdän-Anode fällt unter dem einstellbaren Winkel φ auf einen NaCl-ristall mit dem wirksamen Netzebenenabstand d = 8 pm. Ein unter dem Winkel φ gegen die Einstrahlrichtung eingestelltes Zählrohr kann am ristall reflektierte Strahlen registrieren. Mit Hilfe der sog. Bragg-Bedingung k $ = $ d $ sin können den einzelnen Reflexionswinkeln φ leicht die Wellenlängen der auftreffenden Röntgenstrahlen zugeordnet werden. Skizze: Intensität U φ φ φ Zählrohr e φ Uh Ergebnis: Dem kontinuierlichen Spektrum sind einige scharfe Linien überlagert (vgl. Skizze!). Seite
6 Berechnung: Deutet man versuchsweise die verschiedenen Maxima der Zählrate als Maxima derselben Wellenlänge, aber verschiedener Ordnung, so erhält man für die Wellenlänge λ = 7 pm. Anmerkungen:. Im durchgeführten Versuch wurden weitere Wellenlängen durch Einbringen eines Zirkonfilters in den Strahlengang absorbiert; die in vielen Graphiken erkennbare weitere Wellenlänge kann mit der verwendeten Nachweisapparatur nicht separiert werden.. Die Graphik bezieht sich auf eine Cu-Anode; im tatsächlich durchgeführten Experiment mit der Molybdän-Antokathode erscheint das erste Maximum unter dem Ablenkwinkel φ = 7,5 0. Erklärung: Diskrete Spektrallinien konnten bislang durch Übergänge der Leuchtelektronen zwischen diskreten Niveaus zufrieden stellend erklärt werden. Es liegt nahe, diesen Ansatz - wenngleich modifiziert - auch für die Erklärung des charakteristischen Röntgenspektrums zu machen. Eine grobe Vorstellung kann so aussehen: Die inneren Schalen der Anodenatome sind alle voll besetzt. Durch Wechselwirkung mit einem "anfliegenden" Elektron wird die Elektronenhülle des Atoms in einen angeregten Zustand gebracht, bei dem ein Zustand in einer inneren Schale frei wird. Es entsteht eine Lücke in der sonst voll besetzten Schale, die in einem Quantensprung durch ein Elektron einer äußeren Schale aufgefüllt wird. Dabei wird die Energiedifferenz als Photon emittiert. Skizze: e e e 8 Elektronen M-Schale 8 Elektronen M-Schale L-Schale -Schale Loch in der -Schale Κα Κα -Übergang L-Schale -Schale Zur Prüfung dieser Vorstellung muss die Bohrsche Gleichung für die Emissionsfrequenz des Wasserstoffatoms bei einem Quantensprung - wie weiter oben angekündigt - modifiziert werden: n n f = m$e4 $. 8$ 0 $h 3 n n = f R $ Der Term e 4 ist beim Wasserstoff aus dem Quadrat der Elektronenladung (-e) und dem Quadrat der ernladung (+e) entstanden. In jedem Fall muss letzterer durch (Z e) ersetzt werden. Zudem wird die ernladung Z durch Seite 5--8-
7 die besetzten tieferliegenden Energiezustände teilweise abgeschirmt, so dass nicht die volle ernladungszahl Z, sondern eine um eine Abschirmzahl a verminderte ernladungszahl (Z - a) wirksam wird. Für die Frequenzen von Röntgenstrahlen sollte also gelten: f = (Z a) $ f R $ n n. Dieser Zusammenhang wurde von dem englischen Physiker Henry Moseley (887-95) gefunden und nach ihm Moseleysches Gesetz genannt. Für den Übergang von der L- (n = ) auf die -Schale (n = ) hat die Abschirmzahl den Wert a =, da das verbliebene -Elektron im wesentlichen eine ernladung abschirmt. Das Moseley-Gesetz für diese α -Strahlung nimmt dann die Form f = (Z ) $ f R $ = 3 4 $ (Z ) $ f R an. Für die im Experiment verwendete Mo-Anode (Z = 4) folgt daraus die α -Emissionsfrequenz f = 0, 75 $ 4 $ f R = 4, 4 $ 0 8 Hz bzw. die Wellenlänge = c f = 7, $ 0 m in Übereinstimmung mit der im Experiment erhaltenen Wellenlänge. Bei dieser handelt es sich daher offenbar um die Wellenlänge der α -Strahlung der Mo-Anode. Das Moseley-Gesetz bringt einen einfachen und interessanten Zusammenhang zwischen f und Z: Radiziert man die Moseley-Gleichung auf beiden Seiten, so erhält man für feste n und n f = const. $ (Z a) bzw. f i (Z a). Wird f über Z aufgetragen, so liegen alle Punkte des Graphen auf einer Geraden. Mit dieser Geraden konnten Chemiker Lücken und Unklarheiten in der Reihenfolge des Periodensystems der Elemente beseitigen. Zusammenfassung: Wird eine kernnahes inneres Elektron eines schweren Atoms durch den Stoß schneller Fremdelektronen aus seinem Niveau entfernt, so kann ein Elektron in die frei gewordene Lücke fallen; dabei wird ein Röntgenquant hoher Energie emittiert. Es entstehen die diskreten Linien des charakteristischen Röntgenspektrums. Die Frequenzen der charakteristischen Linien des Röntgenspektrums gehorchen dem Moseleyschen Gesetz f = (Z a) $ f R $ n n. Dabei ist Z die Ordnungszahl, a die zu dem Übergang vom n in den n -Zustand gehörende Abschirmzahl und f R die Rydbergfrequenz. Für die Frequenzen der α -Linien gilt a =. f ist eine lineare Funktion von (Z-a). Röntgenabsorption Seite
8 Es ist zu erwarten, dass Röntgenstrahlen von den Atomen absorbiert werden können. Dabei ist zu beachten, dass wegen des Pauli-Prinzips Absorption nur auftritt, wenn die Elektronen der vollbesetzten Schalen in Niveaus von teilweise besetzten oder unbesetzten Schalen oder in das Grenzkontinuum der freien Elektronen gehoben werden können (vgl. Skizze). Sind also die L- M- und M-Schalen eines Atoms besetzt, so tritt die in Emission gezeigte Röntgenstrahlung der α -, β -, γ - bzw. L α -Linie usw. in Absorption nicht auf. Prinzipskizze: mehrere kev a) b) c) ontinuum M teilweise oder L nicht besetzte Schale vollständig besetzte Schale Erläuterung: a) Anhebung eines -Elektrons in ein unbesetztes Niveau wenige ev unterhalb der Ionisationsgrenze: Photonenenergie h f E (-ante). b) Anhebung eines -Elektrons in ontinuum: Photonenenergie h f > E. c) Anhebung eines L-Elektrons in ein unbesetztes Niveau wenige ev unterhalb der Ionisationsgrenze: Photonenenergie h f E L (L-ante). Die energetischen Abstände zwischen inneren Niveaus liegen wegen der geringeren Abschirmung der ernladung durch äußere Elektronen im kev-bereich; ein äußeres Elektron auf einem ersten unbesetzten oder nur teilweise besetzten Niveau ist dagegen (vgl. Bild zur Ionisierungsenergie!) weniger als 5 ev von der Ionisierungsgrenze entfernt. Die Anregung innerer Elektronen auf ein unbesetztes Niveau kommt daher praktisch einer Ionisierung gleich. Die Absorption von Röntgenstrahlen kann durch Messung des Absorptionskoeffizienten α (Gleichung: I = I 0 exp(-α x), [α] = m - ) als Funktion der Wellenlänge λ bzw. der Frequenz f der Röntgenstrahlung untersucht werden. Man erhält dabei das nachfolgend skizzierte Ergebnis: Seite
9 -Gruppe Emissions β α α Absorptionsspektrum Absorptionskonstante α 00 mm -ante L-Gruppe -0 λ in 0 m Energie in ev Anmerkungen:. Röntgenabsorptionsspektren sind keine Linienspektren. Die sog. Absorptionskanten zeigen, dass bei ganz bestimmten Energien die Absorption sprunghaft ansteigt, um dann nach hohen Energien hin kontinuierlich abzunehmen. Die Absorption kommt wie im optischen Bereich dadurch zustande, dass ein Elektron von einem niederen auf ein höheres Energieniveau gehoben wird. Im Unterschied zu optischen Emissions- und Absorptionsspektren fallen aber die Absorptionskanten nicht mit den charakteristischen Linien der Emission zusammen (Begründung siehe oben!).. Wird ein Lichtquant aus der - oder L-Schale herausgeschlagen, so wird es praktisch aus dem Atom entfernt. Die Energie eines freien Elektrons ist aber nicht gequantelt. 3. In dem sprunghaften Ansteigen der Absorption an den einzelnen anten zeigt sich, dass für alle Energiequanten, die eine bestimmte Mindestenergie überschreiten, Absorption möglich ist. Wegen der größeren Absorptionsenergien liegen die Absorptionskanten bei kleineren Wellenlängen als die Emissionslinien. Seite
31. Lektion. Röntgenstrahlen. 40. Röntgenstrahlen und Laser
 31. Lektion Röntgenstrahlen 40. Röntgenstrahlen und Laser Lerhnziel: Röntgenstrahlen entstehen durch Beschleunigung von Elektronen oder durch die Ionisation von inneren Elektronenschalen Begriffe Begriffe:
31. Lektion Röntgenstrahlen 40. Röntgenstrahlen und Laser Lerhnziel: Röntgenstrahlen entstehen durch Beschleunigung von Elektronen oder durch die Ionisation von inneren Elektronenschalen Begriffe Begriffe:
Die Abbildung zeigt eine handelsübliche Röntgenröhre
 Die Röntgenstrahlung Historische Fakten: 1895 entdeckte Röntgen beim Experimentieren mit einer Gasentladungsröhre, dass fluoreszierende Kristalle außerhalb der Röhre zum Leuchten angeregt wurden, obwohl
Die Röntgenstrahlung Historische Fakten: 1895 entdeckte Röntgen beim Experimentieren mit einer Gasentladungsröhre, dass fluoreszierende Kristalle außerhalb der Röhre zum Leuchten angeregt wurden, obwohl
Atommodell. Atommodell nach Bohr und Sommerfeld Für sein neues Atommodell stellte Bohr folgende Postulate auf:
 Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Anfängerpraktikum D11 - Röntgenstrahlung
 Anfängerpraktikum D11 - Röntgenstrahlung Vitali Müller, Kais Abdelkhalek Sommersemester 2009 1 Messung des ersten Spektrums 1.1 Versuchsaufbau und Hintergrund Es sollte das Spektrum eines Röntgenapparates
Anfängerpraktikum D11 - Röntgenstrahlung Vitali Müller, Kais Abdelkhalek Sommersemester 2009 1 Messung des ersten Spektrums 1.1 Versuchsaufbau und Hintergrund Es sollte das Spektrum eines Röntgenapparates
2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten
 Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
10.6. Röntgenstrahlung
 10.6. Röntgenstrahlung Am 8. November 1895 entdeckte Wilhelm Conrad Röntgen in Würzburg die Röntgenstrahlung. Seine Entdeckung zählt zu den wohl bedeutendsten Entdeckungen in der Menschheitsgeschichte.
10.6. Röntgenstrahlung Am 8. November 1895 entdeckte Wilhelm Conrad Röntgen in Würzburg die Röntgenstrahlung. Seine Entdeckung zählt zu den wohl bedeutendsten Entdeckungen in der Menschheitsgeschichte.
Versuch 20: Charakteristische Röntgenstrahlung
 Versuch 20: Charakteristische Röntgenstrahlung 1. Einordung in den Kernlehrplan für den Grundkurs Kompetenzen gemäß KLP: Die Schülerinnen und Schüler erläutern die Bedeutung [ ] der charakteristischen
Versuch 20: Charakteristische Röntgenstrahlung 1. Einordung in den Kernlehrplan für den Grundkurs Kompetenzen gemäß KLP: Die Schülerinnen und Schüler erläutern die Bedeutung [ ] der charakteristischen
Röntgenstrahlung (RÖN)
 Röntgenstrahlung (RÖN) Manuel Staebel 2236632 / Michael Wack 2234088 1 Einleitung In diesem Versuch wird das Röntgenspektrum einer Molybdänanode auf einem x y Schreiber aufgezeichnet. Dies gelingt durch
Röntgenstrahlung (RÖN) Manuel Staebel 2236632 / Michael Wack 2234088 1 Einleitung In diesem Versuch wird das Röntgenspektrum einer Molybdänanode auf einem x y Schreiber aufgezeichnet. Dies gelingt durch
Hallwachs-Experiment. Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe
 Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
14. Atomphysik Physik für E-Techniker. 14. Atomphysik
 14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Analyse von Röntgenspektren bei unterschiedlicher Anodenspannung
 1 Abiturprüfung 2003 Vorschlag 2 Analyse von Röntgenspektren bei unterschiedlicher Anodenspannung 1. Skizziere und beschreibe den Aufbau einer Röntgenröhre. Beschreibe kurz, wie Röntgenstrahlung entsteht.
1 Abiturprüfung 2003 Vorschlag 2 Analyse von Röntgenspektren bei unterschiedlicher Anodenspannung 1. Skizziere und beschreibe den Aufbau einer Röntgenröhre. Beschreibe kurz, wie Röntgenstrahlung entsteht.
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Aufgabe 1: Kristallstrukturuntersuchungen
 Aufgabe 1: Kristallstrukturuntersuchungen Röntgenstrahlung entsteht in unserem Gerät durch das Auftreffen hochenergetischer Elektronen auf eine Molybdän-Anode (Abbildung 1). Im Spektrum der Strahlung (Abbildung
Aufgabe 1: Kristallstrukturuntersuchungen Röntgenstrahlung entsteht in unserem Gerät durch das Auftreffen hochenergetischer Elektronen auf eine Molybdän-Anode (Abbildung 1). Im Spektrum der Strahlung (Abbildung
14. Atomphysik. Inhalt. 14. Atomphysik
 Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Versuch O
 1 Grundlagen Plancksches Wirkungsquantum Das Plancksche Wirkungsquantum gibt den Zusammenhang zwischen Energie und Frequenz wieder und verknüpft damit die Welleneigenschaft mit der Teilcheneigenschaft.
1 Grundlagen Plancksches Wirkungsquantum Das Plancksche Wirkungsquantum gibt den Zusammenhang zwischen Energie und Frequenz wieder und verknüpft damit die Welleneigenschaft mit der Teilcheneigenschaft.
12.8 Eigenschaften von elektronischen Übergängen. Übergangsfrequenz
 phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
Das Periodensystem der Elemente
 Q34 LK Physik 17. November 2015 Aufbau Die ermittelten Zusammenhänge der Elektronenzustände in der Atomhülle sollen dazu dienen, den der Elemente zu verstehen. Dem liegen folgende Prinzipien zugrunde:
Q34 LK Physik 17. November 2015 Aufbau Die ermittelten Zusammenhänge der Elektronenzustände in der Atomhülle sollen dazu dienen, den der Elemente zu verstehen. Dem liegen folgende Prinzipien zugrunde:
Lösungen der Abituraufgaben Physik. Harald Hoiß 26. Januar 2019
 Lösungen der Abituraufgaben Physik Harald Hoiß 26. Januar 2019 Inhaltsverzeichnis 1. Wasserstoffatom 1 1.1. Spektren.............................................. 1 2. Anwendungen zum quantenmechanischen
Lösungen der Abituraufgaben Physik Harald Hoiß 26. Januar 2019 Inhaltsverzeichnis 1. Wasserstoffatom 1 1.1. Spektren.............................................. 1 2. Anwendungen zum quantenmechanischen
14. Atomphysik Aufbau der Materie
 14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Radiologie Modul I. Teil 1 Grundlagen Röntgen
 Radiologie Modul I Teil 1 Grundlagen Röntgen Teil 1 Inhalt Physikalische Grundlagen Röntgen Strahlenbiologie Technische Grundlagen Röntgen ROENTGENTECHNIK STRAHLENPHYSIK GRUNDLAGEN RADIOLOGIE STRAHLENBIOLOGIE
Radiologie Modul I Teil 1 Grundlagen Röntgen Teil 1 Inhalt Physikalische Grundlagen Röntgen Strahlenbiologie Technische Grundlagen Röntgen ROENTGENTECHNIK STRAHLENPHYSIK GRUNDLAGEN RADIOLOGIE STRAHLENBIOLOGIE
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Atommodell führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen.
 Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Das Bohr sche Atommodell: Strahlenabsorption, -emission, Elektromagentische Strahlung, Wellen, Wellenlänge, Frequenz, Wellenzahl. Postulate: * Elektronen bewegen
Wiederholung der letzten Vorlesungsstunde: Das Bohr sche Atommodell: Strahlenabsorption, -emission, Elektromagentische Strahlung, Wellen, Wellenlänge, Frequenz, Wellenzahl. Postulate: * Elektronen bewegen
Das Rutherfordsche Atommodelle
 Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
Das Wasserstoffatom Energiestufen im Atom
 11. 3. Das Wasserstoffatom 11.3.1 Energiestufen im Atom Vorwissen: Hg und Na-Dampflampe liefern ein charakteristisches Spektrum, das entweder mit einem Gitter- oder einem Prismenspektralapparat betrachtet
11. 3. Das Wasserstoffatom 11.3.1 Energiestufen im Atom Vorwissen: Hg und Na-Dampflampe liefern ein charakteristisches Spektrum, das entweder mit einem Gitter- oder einem Prismenspektralapparat betrachtet
Röntgenbeugung. 1. Grundlagen, Messmethode
 Röntgenbeugung 1. Grundlagen, Messmethode Beim Aufprall schneller Elektronen auf ein metallisches Anodenmaterial (hier: Kupfer) entsteht Röntgenstrahlung. Diese wird nach der Drehkristallmethode spektral
Röntgenbeugung 1. Grundlagen, Messmethode Beim Aufprall schneller Elektronen auf ein metallisches Anodenmaterial (hier: Kupfer) entsteht Röntgenstrahlung. Diese wird nach der Drehkristallmethode spektral
Jetzt noch die Strahlung aus der Elektronenhülle. Hüllenstrahlung. Kein Radioaktiver Zerfall. Kapitel 4 1
 Hüllenstrahlung Inhalt des 4.Kapitels Charakteristische Photonen- und Röntgenstrahlung - Röntgenfluoreszenz Augerelektronen Fluoreszenz- und Augerelektronenausbeute Bremsstrahlung Erzeugung von Röntgenstrahlung
Hüllenstrahlung Inhalt des 4.Kapitels Charakteristische Photonen- und Röntgenstrahlung - Röntgenfluoreszenz Augerelektronen Fluoreszenz- und Augerelektronenausbeute Bremsstrahlung Erzeugung von Röntgenstrahlung
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Die Elektronenzustände eines Atoms Quantenzahl Symbol Erlaubte Werte Hat zu tun mit Hauptquantenzahl n 1,2,3,... Abstand vom
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Die Elektronenzustände eines Atoms Quantenzahl Symbol Erlaubte Werte Hat zu tun mit Hauptquantenzahl n 1,2,3,... Abstand vom
Aufgaben zu Röntgenstrahlen LK Physik 13/1 Sporenberg Roentgen_September_2011 Datum:
 Aufgaben zu Röntgenstrahlen LK Physik 13/1 Sporenberg Roentgen_September_2011 Datum: 08.09.2011 1.Aufgabe: In einem Röntgengerät fällt monochromatische Strahlung ( λ = 71 pm) auf die Oberfläche eines LiF-Kristalls.
Aufgaben zu Röntgenstrahlen LK Physik 13/1 Sporenberg Roentgen_September_2011 Datum: 08.09.2011 1.Aufgabe: In einem Röntgengerät fällt monochromatische Strahlung ( λ = 71 pm) auf die Oberfläche eines LiF-Kristalls.
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Verfahren Grundlagen 1.2 Röntgen. 1.2 Grundlagen. Reichow-Heymann-Menke Handbuch Röntgen mit Strahlenschutz Grundwerk 11/801
 Verfahren 1.2 Röntgen 1.2 Reichow-Heymann-Menke Handbuch Röntgen mit Strahlenschutz Grundwerk 11/801 Verfahren 1.2 Röntgen Inhaltsvrzeichnis 1.2 Prof. Dr. Christian Blendl 1.2.1 Erzeugung ionisierender
Verfahren 1.2 Röntgen 1.2 Reichow-Heymann-Menke Handbuch Röntgen mit Strahlenschutz Grundwerk 11/801 Verfahren 1.2 Röntgen Inhaltsvrzeichnis 1.2 Prof. Dr. Christian Blendl 1.2.1 Erzeugung ionisierender
27. Vorlesung EP V. STRAHLUNG, ATOME, KERNE
 27. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 28. Atomphysik, Röntgenstrahlung (Fortsetzung: Röntgenröhre, Röntgenabsorption) 29. Atomkerne, Radioaktivität (Nuklidkarte, α-, β-, γ-aktivität, Dosimetrie)
27. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 28. Atomphysik, Röntgenstrahlung (Fortsetzung: Röntgenröhre, Röntgenabsorption) 29. Atomkerne, Radioaktivität (Nuklidkarte, α-, β-, γ-aktivität, Dosimetrie)
29. Lektion. Atomaufbau. 39. Atomaufbau und Molekülbindung
 29. Lektion Atomaufbau 39. Atomaufbau und Molekülbindung Lernziele: Atomare Orbitale werden von Elektronen nach strengen Regeln der QM aufgefüllt. Ein Orbital darf von nicht mehr als zwei Elektronen besetzt
29. Lektion Atomaufbau 39. Atomaufbau und Molekülbindung Lernziele: Atomare Orbitale werden von Elektronen nach strengen Regeln der QM aufgefüllt. Ein Orbital darf von nicht mehr als zwei Elektronen besetzt
Atome und ihre Eigenschaften
 Atome und ihre Eigenschaften Vom Atomkern zum Atom - von der Kernphysik zur Chemie Die Chemie beginnt dort, wo die Temperaturen soweit gefallen sind, daß die positiv geladenen Atomkerne freie Elektronen
Atome und ihre Eigenschaften Vom Atomkern zum Atom - von der Kernphysik zur Chemie Die Chemie beginnt dort, wo die Temperaturen soweit gefallen sind, daß die positiv geladenen Atomkerne freie Elektronen
 Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Leistungskurs Physik (Bayern): Abiturprüfung 2000 Aufgabe III Atomphysik
 Leistungskurs Physik (Bayern): Abiturprüfung 000 Aufgabe III Atomphysik 1. Laserbremsung eines Atomstrahls In einem Atomofen befindet sich Cäsium-Gas der Temperatur T. Die mittlere m Geschwindigkeit der
Leistungskurs Physik (Bayern): Abiturprüfung 000 Aufgabe III Atomphysik 1. Laserbremsung eines Atomstrahls In einem Atomofen befindet sich Cäsium-Gas der Temperatur T. Die mittlere m Geschwindigkeit der
Abiturprüfung Physik, Grundkurs. Aufgabe 1: Das Fadenstrahlrohr ausgewählte Experimente und Überlegungen
 Seite 1 von 8 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe 1: Das Fadenstrahlrohr ausgewählte Experimente und Überlegungen 1. Im Fadenstrahlrohr (siehe Abbildung 1) wird mit Hilfe einer
Seite 1 von 8 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe 1: Das Fadenstrahlrohr ausgewählte Experimente und Überlegungen 1. Im Fadenstrahlrohr (siehe Abbildung 1) wird mit Hilfe einer
Gymnasium / Realschule. Atomphysik 2. Klasse / G8. Aufnahme und Abgabe von Energie (Licht)
 Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Übungen zur Physik des Lichts
 ) Monochromatisches Licht (λ = 500 nm) wird an einem optischen Gitter (000 Striche pro cm) gebeugt. a) Berechnen Sie die Beugungswinkel der Intensitätsmaxima bis zur 5. Ordnung. b) Jeder einzelne Gitterstrich
) Monochromatisches Licht (λ = 500 nm) wird an einem optischen Gitter (000 Striche pro cm) gebeugt. a) Berechnen Sie die Beugungswinkel der Intensitätsmaxima bis zur 5. Ordnung. b) Jeder einzelne Gitterstrich
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Stern-Gerlach-Versuch, Orbitalmodell, Heisenberg sche Unschärferelation, Schrödinger Gleichung, Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen
Wiederholung der letzten Vorlesungsstunde: Stern-Gerlach-Versuch, Orbitalmodell, Heisenberg sche Unschärferelation, Schrödinger Gleichung, Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen
VL 20 VL Mehrelektronensysteme VL Periodensystem VL Röntgenstrahlung
 VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
43. Strahlenschutz und Dosimetrie. 36. Lektion Wechselwirkung und Reichweite von Strahlung
 43. Strahlenschutz und Dosimetrie 36. Lektion Wechselwirkung und Reichweite von Strahlung Lernziel: Die Wechselwirkung von radioaktiver Strahlung (α,β,γ( α,β,γ) ) ist unterschiedlich. Nur im Fall von α-
43. Strahlenschutz und Dosimetrie 36. Lektion Wechselwirkung und Reichweite von Strahlung Lernziel: Die Wechselwirkung von radioaktiver Strahlung (α,β,γ( α,β,γ) ) ist unterschiedlich. Nur im Fall von α-
22. Wärmestrahlung. rmestrahlung, Quantenmechanik
 22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
Physik ea Klausur Nr Oktober 2013
 Name: BE: / 77 = % Note: P. 1. Aufgabe: Röntgenstrahlung a. Skizziere den Aufbau einer Vorrichtung zur Herstellung eines gebündelten Röntgenstrahls, beschrifte ihre Bauteile und erläutere die Prozesse,
Name: BE: / 77 = % Note: P. 1. Aufgabe: Röntgenstrahlung a. Skizziere den Aufbau einer Vorrichtung zur Herstellung eines gebündelten Röntgenstrahls, beschrifte ihre Bauteile und erläutere die Prozesse,
Übungen zur Physik der Materie 1 Lösungsvorschlag Blatt 11 - Atomphysik. Aufgabe 28: Kurzfragen zur Atomphysik Teil 2
 Übungen zur Physik der Materie 1 Lösungsvorschlag Blatt 11 - Atomphysik Sommersemester 018 Vorlesung: Boris Bergues ausgegeben am 1.06.018 Übung: Nils Haag (Nils.Haag@lmu.de) besprochen am 6.06.018 Aufgabe
Übungen zur Physik der Materie 1 Lösungsvorschlag Blatt 11 - Atomphysik Sommersemester 018 Vorlesung: Boris Bergues ausgegeben am 1.06.018 Übung: Nils Haag (Nils.Haag@lmu.de) besprochen am 6.06.018 Aufgabe
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #26 04/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Spektrum des H-Atoms Energieniveaus der erlaubten Quantenbahnen E n = " m # e4 8 # h 2 # $ 0 2
Physik für Mediziner im 1. Fachsemester #26 04/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Spektrum des H-Atoms Energieniveaus der erlaubten Quantenbahnen E n = " m # e4 8 # h 2 # $ 0 2
Physik für Mediziner und Zahnmediziner
 Physik für Mediziner und Zahnmediziner Vorlesung 19 Prof. F. Wörgötter (nach M. Seibt) -- Physik für Mediziner und Zahnmediziner 1 PET: Positronen-Emissions-Tomographie Kernphysik PET Atomphysik Röntgen
Physik für Mediziner und Zahnmediziner Vorlesung 19 Prof. F. Wörgötter (nach M. Seibt) -- Physik für Mediziner und Zahnmediziner 1 PET: Positronen-Emissions-Tomographie Kernphysik PET Atomphysik Röntgen
Thema heute: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Versuch A05: Bestimmung des Planck'schen Wirkungsquantums
 Versuch A05: Bestimmung des Planck'schen Wirkungsquantums 25. April 2016 I Lernziele Entstehung des Röntgen-Bremskontinuums und der charakteristischen Röntgenstrahlung Zusammenhang zwischen Energie, Frequenz
Versuch A05: Bestimmung des Planck'schen Wirkungsquantums 25. April 2016 I Lernziele Entstehung des Röntgen-Bremskontinuums und der charakteristischen Röntgenstrahlung Zusammenhang zwischen Energie, Frequenz
Röntgenstrahlen (RÖN)
 TUM Anfängerpraktikum für Physiker II Wintersemester 2006/2007 Röntgenstrahlen (RÖN) Inhaltsverzeichnis 07.11.2006 1.Einleitung...2 2.Photonenemission...2 2.1.Bremsstrahlung...2 2.2.Charakteristische Röntgenstrahlung...2
TUM Anfängerpraktikum für Physiker II Wintersemester 2006/2007 Röntgenstrahlen (RÖN) Inhaltsverzeichnis 07.11.2006 1.Einleitung...2 2.Photonenemission...2 2.1.Bremsstrahlung...2 2.2.Charakteristische Röntgenstrahlung...2
VI. Quantenphysik. VI.1 Ursprünge der Quantenphysik, Atomphysik. Physik für Mediziner 1
 VI. Quantenphysik VI.1 Ursprünge der Quantenphysik, Atomphysik Physik für Mediziner 1 Mikroskopische Welt Physik für Mediziner 2 Strahlung des Schwarzen Körpers Schwarzer Körper: eintretendes Licht im
VI. Quantenphysik VI.1 Ursprünge der Quantenphysik, Atomphysik Physik für Mediziner 1 Mikroskopische Welt Physik für Mediziner 2 Strahlung des Schwarzen Körpers Schwarzer Körper: eintretendes Licht im
In der Abbildung ist ein vereinfachtes Energieniveauschema eines Lasers dargestellt.
 Klausur Physik III, 7.3.2016 Aufg. 1/5 Aufgabe 1) In der Abbildung ist ein vereinfachtes Energieniveauschema eines Lasers dargestellt. 1. Nennen Sie die wesentlichen Prozesse, die bei der Erzeugung von
Klausur Physik III, 7.3.2016 Aufg. 1/5 Aufgabe 1) In der Abbildung ist ein vereinfachtes Energieniveauschema eines Lasers dargestellt. 1. Nennen Sie die wesentlichen Prozesse, die bei der Erzeugung von
1. Ermitteln Sie die Gitterkonstante eines LiF-Kristalls aus der Messung des -2 -Spektrums unter Verwendung einer Wolframkathode.
 Fakultät für Physik und Geowissenschaften Physikalisches Grundpraktikum O 21 Röntgenstrahlung Aufgaben 1. Ermitteln Sie die Gitterkonstante eines LiF-Kristalls aus der Messung des -2-Spektrums unter Verwendung
Fakultät für Physik und Geowissenschaften Physikalisches Grundpraktikum O 21 Röntgenstrahlung Aufgaben 1. Ermitteln Sie die Gitterkonstante eines LiF-Kristalls aus der Messung des -2-Spektrums unter Verwendung
1. Ermitteln Sie die Gitterkonstante eines LiF-Kristalls aus der Messung des -2 -Spektrums unter Verwendung einer Wolframkathode.
 Fakultät für Physik und Geowissenschaften Physikalisches Grundpraktikum O 21 a Röntgenstrahlung Aufgaben 1. Ermitteln Sie die Gitterkonstante eines LiF-Kristalls aus der Messung des -2-Spektrums unter
Fakultät für Physik und Geowissenschaften Physikalisches Grundpraktikum O 21 a Röntgenstrahlung Aufgaben 1. Ermitteln Sie die Gitterkonstante eines LiF-Kristalls aus der Messung des -2-Spektrums unter
Thema: Spektroskopische Untersuchung von Strahlung mit Gittern
 Thema: Spektroskopische Untersuchung von Strahlung mit Gittern Gegenstand der Aufgaben ist die spektroskopische Untersuchung von sichtbarem Licht, Mikrowellenund Röntgenstrahlung mithilfe geeigneter Gitter.
Thema: Spektroskopische Untersuchung von Strahlung mit Gittern Gegenstand der Aufgaben ist die spektroskopische Untersuchung von sichtbarem Licht, Mikrowellenund Röntgenstrahlung mithilfe geeigneter Gitter.
8.3 Die Quantenmechanik des Wasserstoffatoms
 Dieter Suter - 409 - Physik B3 8.3 Die Quantenmechanik des Wasserstoffatoms 8.3.1 Grundlagen, Hamiltonoperator Das Wasserstoffatom besteht aus einem Proton (Ladung +e) und einem Elektron (Ladung e). Der
Dieter Suter - 409 - Physik B3 8.3 Die Quantenmechanik des Wasserstoffatoms 8.3.1 Grundlagen, Hamiltonoperator Das Wasserstoffatom besteht aus einem Proton (Ladung +e) und einem Elektron (Ladung e). Der
Versuch B 10: Versuch mit Röntgenstrahlen
 - B10.1 - Versuch B 10: Versuch mit Röntgenstrahlen 1. Literatur: Harbeck, Physik Oberstufe Gerthsen, Kneser, Vogel, Physik Pohl III, Optik u. Atomphysik Finkelnburg, Atomphysik Glocker, Materialprüfung
- B10.1 - Versuch B 10: Versuch mit Röntgenstrahlen 1. Literatur: Harbeck, Physik Oberstufe Gerthsen, Kneser, Vogel, Physik Pohl III, Optik u. Atomphysik Finkelnburg, Atomphysik Glocker, Materialprüfung
Aufbau von Atomen. Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem
 Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
FK Ex 4 - Musterlösung 08/09/2015
 FK Ex 4 - Musterlösung 08/09/2015 1 Spektrallinien Die Natrium-D-Linien sind emittiertes Licht der Wellenlänge 589.5932 nm (D1) und 588.9965 nm (D2). Diese charakteristischen Spektrallinien entstehen beim
FK Ex 4 - Musterlösung 08/09/2015 1 Spektrallinien Die Natrium-D-Linien sind emittiertes Licht der Wellenlänge 589.5932 nm (D1) und 588.9965 nm (D2). Diese charakteristischen Spektrallinien entstehen beim
Übungsaufgaben zur Experimentalphysik IV. X. Angeregte Zustände
 WALTHER-MEISSNER-INSTITUT Bayerische Akademie der Wissenschaften LEHRSTUHL FÜR TECHNISCHE PHYSIK E3 Technische Universität München PD DR. LAMBERT ALFF DATUM 18. Juni 00 Übungsaufgaben zur Experimentalphysik
WALTHER-MEISSNER-INSTITUT Bayerische Akademie der Wissenschaften LEHRSTUHL FÜR TECHNISCHE PHYSIK E3 Technische Universität München PD DR. LAMBERT ALFF DATUM 18. Juni 00 Übungsaufgaben zur Experimentalphysik
MO-Theorie: Molekülorbitale, Bindungsordnung, Molekülorbitaldiagramme von F 2, O 2, N 2, H 2 O, Benzol, Wasserstoffbrückenbindungen
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen VI Molkülorbitaltheorie II MO-Theorie: Molekülorbitale, Bindungsordnung, Molekülorbitaldiagramme von F 2, O 2, N 2, H 2 O, Benzol,
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen VI Molkülorbitaltheorie II MO-Theorie: Molekülorbitale, Bindungsordnung, Molekülorbitaldiagramme von F 2, O 2, N 2, H 2 O, Benzol,
Thema: Spektroskopische Untersuchung von Strahlung mit Gittern
 Thema: Spektroskopische Untersuchung von Strahlung mit Gittern Gegenstand der Aufgabe ist die spektroskopische Untersuchung von sichtbarem Licht, Mikrowellenund Röntgenstrahlung mithilfe geeigneter Gitter.
Thema: Spektroskopische Untersuchung von Strahlung mit Gittern Gegenstand der Aufgabe ist die spektroskopische Untersuchung von sichtbarem Licht, Mikrowellenund Röntgenstrahlung mithilfe geeigneter Gitter.
VL 20 VL Mehrelektronensysteme VL Periodensystem VL Röntgenstrahlung
 VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
10. Das Wasserstoff-Atom Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
2.4. Atome mit mehreren Elektronen
 2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus
 26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
Vorlesung 19: Roter Faden: Röntgenstrahlung Laserprinzip. Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag
 Vorlesung 19: Roter Faden: Röntgenstrahlung Laserprinzip Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag Juni 21, 2005 Atomphysik
Vorlesung 19: Roter Faden: Röntgenstrahlung Laserprinzip Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: Demtröder, Experimentalphysik 3, Springerverlag Juni 21, 2005 Atomphysik
Zentralabitur 2012 Physik Schülermaterial Aufgabe I ga Bearbeitungszeit: 220 min
 Thema: Wellen und Quanten Interferenzphänomene werden an unterschiedlichen Strukturen untersucht. In Aufgabe 1 wird zuerst der Spurabstand einer CD bestimmt. Thema der Aufgabe 2 ist eine Strukturuntersuchung
Thema: Wellen und Quanten Interferenzphänomene werden an unterschiedlichen Strukturen untersucht. In Aufgabe 1 wird zuerst der Spurabstand einer CD bestimmt. Thema der Aufgabe 2 ist eine Strukturuntersuchung
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch
 Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
Für Geowissenschaftler. EP WS 2009/10 Dünnweber/Faessler
 Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Radioökologie und Strahlenschutz
 Radioökologie und Strahlenschutz Vorlesung FHH: SS 2017 Ulrich J. Schrewe Themen: Anwendung kernphysikalischer Messverfahren in der industriellen Messtechnik Eigenschaften ionisierender Strahlung Strahlungswirkung
Radioökologie und Strahlenschutz Vorlesung FHH: SS 2017 Ulrich J. Schrewe Themen: Anwendung kernphysikalischer Messverfahren in der industriellen Messtechnik Eigenschaften ionisierender Strahlung Strahlungswirkung
Elemente der Quantenmechanik III 9.1. Schrödingergleichung mit beliebigem Potential 9.2. Harmonischer Oszillator 9.3. Drehimpulsoperator
 VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
Abbildung 1. Abbildung 2. R.Goldstein 1
 Wasserstoffatom, Spektrallinien Zusammengestellt von Roman Goldstein A1. Vor 100 Jahren haben Johannes Rydberg und Walter Ritz die Serienformel des Wasserstoffatoms aufgestellt: mit n 2 > n 1 wobei R H
Wasserstoffatom, Spektrallinien Zusammengestellt von Roman Goldstein A1. Vor 100 Jahren haben Johannes Rydberg und Walter Ritz die Serienformel des Wasserstoffatoms aufgestellt: mit n 2 > n 1 wobei R H
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
Examensaufgaben QUANTENPHYSIK
 Examensaufgaben QUANTENPHYSIK Aufgabe 1 (Juni 2006) Bei einem Versuch wurden folgende Messwerte ermittelt : Wellenlänge des Lichtes (nm) Gegenspannung (V) 436 0,83 578 0,13 a) Berechne aus diesen Werten
Examensaufgaben QUANTENPHYSIK Aufgabe 1 (Juni 2006) Bei einem Versuch wurden folgende Messwerte ermittelt : Wellenlänge des Lichtes (nm) Gegenspannung (V) 436 0,83 578 0,13 a) Berechne aus diesen Werten
HOCHSCHULE HARZ Fachbereich Automatisierung und Informatik. Physik. Der Franck-Hertz-Versuch
 Gruppe: HOCHSCHULE HARZ Fachbereich Automatisierung und Informatik Physik Versuch-Nr.: Der Franck-Hertz-Versuch Gliederung: 1. Theoretische Grundlagen 2. Versuchsbeschreibung 3. Versuchsaufbau 4. Messungen
Gruppe: HOCHSCHULE HARZ Fachbereich Automatisierung und Informatik Physik Versuch-Nr.: Der Franck-Hertz-Versuch Gliederung: 1. Theoretische Grundlagen 2. Versuchsbeschreibung 3. Versuchsaufbau 4. Messungen
Atome mit mehreren Elektronen
 Atome mit mehreren Elektronen In diesem Kapitel wollen wir uns in die reale Welt stürzen und Atome mit mehr als einem Elektron untersuchen. Schließlich besteht sie Welt nicht nur aus Wasserstoff. Die wesentlichen
Atome mit mehreren Elektronen In diesem Kapitel wollen wir uns in die reale Welt stürzen und Atome mit mehr als einem Elektron untersuchen. Schließlich besteht sie Welt nicht nur aus Wasserstoff. Die wesentlichen
Charakteristische Röntgenstrahlung von Wolfram
 Charakteristische Röntgenstrahlung TEP Verwandte Begriffe Röntgenröhren, Bremsstrahlung, charakteristische Röntgenstrahlung, Energieniveaus, Kristallstrukturen, Gitterkonstante, Absorption von Röntgenstrahlung,
Charakteristische Röntgenstrahlung TEP Verwandte Begriffe Röntgenröhren, Bremsstrahlung, charakteristische Röntgenstrahlung, Energieniveaus, Kristallstrukturen, Gitterkonstante, Absorption von Röntgenstrahlung,
Röntgenstrahlung ist eine elektromagnetische Strahlung, wie z.b. Licht sie ist für Menschen nicht sichtbar Röntgenstrahlung besitzt
 Röntgenstrahlung ist eine elektromagnetische Strahlung, wie z.b. Licht sie ist für Menschen nicht sichtbar Röntgenstrahlung besitzt Welleneigenschaften, ionisiert Gase, regt manche Stoffe zum Leuchten
Röntgenstrahlung ist eine elektromagnetische Strahlung, wie z.b. Licht sie ist für Menschen nicht sichtbar Röntgenstrahlung besitzt Welleneigenschaften, ionisiert Gase, regt manche Stoffe zum Leuchten
Abiturprüfung Physik, Grundkurs
 Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
2.4. Atome mit mehreren Elektronen
 2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
Klausurinformation. Sie dürfen nicht verwenden: Handy, Palm, Laptop u.ae. Weisses Papier, Stifte etc. Proviant, aber keine heiße Suppe u.dgl.
 Klausurinformation Zeit: Mittwoch, 3.Februar, 12:00, Dauer :90 Minuten Ort: Veterinärmediziner: Großer Phys. Hörsaal ( = Hörsaal der Vorlesung) Geowissenschaftler u.a.: Raum A140, Hauptgebäude 1. Stock,
Klausurinformation Zeit: Mittwoch, 3.Februar, 12:00, Dauer :90 Minuten Ort: Veterinärmediziner: Großer Phys. Hörsaal ( = Hörsaal der Vorlesung) Geowissenschaftler u.a.: Raum A140, Hauptgebäude 1. Stock,
UNIVERSITÄT BIELEFELD
 UNIVERSITÄT BIELEFELD 6. Atom- und Molekülphysik 6.1 - GV Atom- und Molekülspektren Durchgeführt am 22.11.06 Dozent: Praktikanten (Gruppe 1): Dr. Udo Werner Marcus Boettiger Sarah Dirk Marius Schirmer
UNIVERSITÄT BIELEFELD 6. Atom- und Molekülphysik 6.1 - GV Atom- und Molekülspektren Durchgeführt am 22.11.06 Dozent: Praktikanten (Gruppe 1): Dr. Udo Werner Marcus Boettiger Sarah Dirk Marius Schirmer
Periodensystem. Physik und Chemie. Sprachkompendium und einfache Regeln
 Periodensystem Physik und Chemie Sprachkompendium und einfache Regeln 1 Begriffe Das (neutrale) Wasserstoffatom kann völlig durchgerechnet werden. Alle anderen Atome nicht; ein dermaßen komplexes System
Periodensystem Physik und Chemie Sprachkompendium und einfache Regeln 1 Begriffe Das (neutrale) Wasserstoffatom kann völlig durchgerechnet werden. Alle anderen Atome nicht; ein dermaßen komplexes System
TEP Bestimmung der Rydbergkonstanten, Moseleysches Gesetz und Abschirmkonstante
 Bestimmung der Rydbergkonstanten, TEP Verwandte Themen Charakteristische Röntgenstrahlung, Bohrsches Atommodell, Energieniveaus, Bindungsenergie, Moseley-Gesetz, Rydberg- Frequenz, Abschirmkonstante, Bragg-Streuung.
Bestimmung der Rydbergkonstanten, TEP Verwandte Themen Charakteristische Röntgenstrahlung, Bohrsches Atommodell, Energieniveaus, Bindungsenergie, Moseley-Gesetz, Rydberg- Frequenz, Abschirmkonstante, Bragg-Streuung.
Licht als Teilchenstrahlung
 Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Lk Physik in 13/1 2. Klausur aus der Physik Blatt 1 (von 2)
 Blatt 1 (von 2) 1. Leuchtelektronen-Modell des Na-Atoms 5 BE Berechne aus dem experimentellen Wert der Ionisierungsenergie von Natrium, 5, 12 ev, die effektive Kernladungszahl für das Leuchtelektron der
Blatt 1 (von 2) 1. Leuchtelektronen-Modell des Na-Atoms 5 BE Berechne aus dem experimentellen Wert der Ionisierungsenergie von Natrium, 5, 12 ev, die effektive Kernladungszahl für das Leuchtelektron der
Physik im Querschnitt (nicht vertieft) Übungsblatt Atom- und Molekülphysik
 Physik im Querschnitt (nicht vertieft) Übungsblatt Atom- und Molekülphysik WS2018/19 Pupeza/Nubbemeyer 7.12.2018 Aufgabe 25 Spektroskopie von Quantenniveaus a) Benennen Sie zwei Experimente, mit denen
Physik im Querschnitt (nicht vertieft) Übungsblatt Atom- und Molekülphysik WS2018/19 Pupeza/Nubbemeyer 7.12.2018 Aufgabe 25 Spektroskopie von Quantenniveaus a) Benennen Sie zwei Experimente, mit denen
Vorlesung 9: Roter Faden: Franck-Hertz Versuch. Emissions- und Absorptionsspektren der Atome. Spektren des Wasserstoffatoms. Bohrsche Atommodell
 Vorlesung 9: Roter Faden: Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 9: Roter Faden: Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
chemische Vorgänge spielen sich in erster Linie in der Atomhülle ab, sind also mit einer Änderung der Energiezustände der Elektronen verbunden.
 1 Atomhülle - Elektronen chemische Vorgänge spielen sich in erster Linie in der Atomhülle ab, sind also mit einer Änderung der Energiezustände der Elektronen verbunden. Energie der Elektronen Die Energie
1 Atomhülle - Elektronen chemische Vorgänge spielen sich in erster Linie in der Atomhülle ab, sind also mit einer Änderung der Energiezustände der Elektronen verbunden. Energie der Elektronen Die Energie
Laborversuche zur Experimentalfysik II. Versuch II-10: Versuche mit Röntgenstrahlen
 Laborversuche zur Experimentalfysik II Versuch II-10: Versuche mit Röntgenstrahlen Versuchsleiter: Andre Langer Autoren: Kai Dinges Michael Beer Gruppe: 12 (Di) Versuchsdatum: 16. Mai 2006 Inhaltsverzeichnis
Laborversuche zur Experimentalfysik II Versuch II-10: Versuche mit Röntgenstrahlen Versuchsleiter: Andre Langer Autoren: Kai Dinges Michael Beer Gruppe: 12 (Di) Versuchsdatum: 16. Mai 2006 Inhaltsverzeichnis
Folgendes Röntgenspektrum wurde an einer Röntgenröhre aufgenommen, die mit der Beschleunigungsspannung
 Seite Aufgabe : Röntgenspektrum Folgendes Röntgenspektrum wurde an einer Röntgenröhre aufgenommen, die mit der Beschleunigungsspannung U = 30 kv betrieben wurde.. Berechnen Sie aus dem dargestellten Versuchsergebnis
Seite Aufgabe : Röntgenspektrum Folgendes Röntgenspektrum wurde an einer Röntgenröhre aufgenommen, die mit der Beschleunigungsspannung U = 30 kv betrieben wurde.. Berechnen Sie aus dem dargestellten Versuchsergebnis
Abiturprüfung Physik, Leistungskurs
 Seite 1 von 8 Abiturprüfung 2010 Physik, Leistungskurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer
Seite 1 von 8 Abiturprüfung 2010 Physik, Leistungskurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer
Übungen Atom- und Molekülphysik für Physiklehrer (Teil 2)
 Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
