Aneliya Petrova 1, Günter Westphal 1, Rafael Valbuena 1 und Jochen Ringe 2
|
|
|
- Klaus Kramer
- vor 7 Jahren
- Abrufe
Transkript
1 LIFIS ONLINE [ ] ISSN Aneliya Petrova 1, Günter Westphal 1, Rafael Valbuena 1 und Jochen Ringe 2 Struktur und technofunktionelle Eigenschaften von Kollagenen tierischen Ursprungs Kollagenhaltiges Bindegewebe von Därmen wird traditionell zur Einhüllung von Wurstbrät genutzt. Seit etwa 20 Jahren findet man Kollagene in verschiedenen kosmetischen Formulierungen, dann in Form sog. pads zur Wundauflage bzw. als Zellträger für die regenerative Medizin. Dabei wird als Rohstoff häufig die Haut von Kälbern verwendet. Gemeinsam mit der Charité, der Gruppe Tissue Engineering, haben wir Einsatzmöglichkeiten für in größerer Menge anfallende Schweinehaut im Bereich der regenerativen Medizin eröffnet. Sowohl für die Kollagengewinnung als auch für die Anwendung dieses Proteins sind die Kenntnisse über intra- und intermolekulare Quervernetzungen cross linkings essentiell. So sind im Besonderen die technofunktionellen Eigenschaften und dabei die physiologischen Funktionen der Kollagene von spezifischen Quervernetzungen abhängig. In unseren experimentellen Arbeiten, über die wir in Kürze berichten werden, waren und sind die Strukturen der vernetzten Kollagene bedeutsam. Die Vorstufen von Kollagenen, sog. Prokollagenen, werden in ihrer unikaten Aminosäurezusammensetzung in Bindegewebszellen in Form von linkshändigen alpha-polypeptidketten synthetisiert. Danach erfolgt extrazellulär über die Abspaltung der terminalen Propeptide die Herausbildung von rechtshändigen tripelhelikalen Tropokollagenen. In der Literatur findet man jedoch auch Hinweise auf eine intrazelluläre Abspaltung der Propeptide. Tropokollagene weisen zudem N- bzw. C-terminale, nichthelikale Sequenzen Telopeptide genannt auf (Abbildung 1) 3. Werden die nichthelikalen Strukturanteile aus technologischen Gründen, z.b. enzymatisch, abgespalten, erhält man die Atelokollagene. Die Stabilität der Tropokollagene wird im Besonderen durch die große Anzahl von Wasserstoffbrückenbindungen, entropiegesteuert, hervorgerufen. In den C- bzw. N-terminalen Tripelhelix-Enden und in den entsprechenden Telopeptiden werden altersabhängig kovalente Bindungen (Quervernetzungen) unter Vernetzung der Peptidstränge eingebaut. [1], [2] Die skizzierten Strukturelemente in den Tropokollagenen finden sich schließlich, gewebetypisch, in den Fibrillen und Fasern, Netzwerken, fibrillen- bzw. membranassoziierten Kollagenen sowie in multiplen Tripelhelices wieder. Bisher wurde über 29 Vertreter solcher Kollagene berichtet. [3] Nach der Expression der Tropokollagenmoleküle und der Herausbildung ihrer Endform außerhalb der Zelle tritt spontan eine Selbstanordnung zu Mikrofibrillen ein, die dann mechanisch stabilere 1 Institut für Agrar- und Stadtökologische Projekte an der Humboldt-Universität zu Berlin 2 Tissue Engineering Lab & Berlin-Brandenburg Center for Regenerative Therapies, Dept. of Rheumatology and Clinical Immunology, Charité-Universitätsmedizin Berlin 3 Alle Abbildungen siehe im Block am Textende. 1
2 Fibrillen bilden. Während dieses Prozesses der Selbststrukturierung finden enzymatisch und nicht enzymatische ( Glykierung ) Quervernetzungen statt. Diese Quervernetzungen sind hauptsächlich intermolekular, aber auch intramolekulare Quervernetzungen (innerhalb der Tropokollagenmoleküle) sind bekannt. Die enzymatische Quervernetzung in fibrillären Kollagenen basiert auf der oxidativen Bildung von Aldehydgruppen. Lysin oder Hydroxylysin werden dabei mittels Lysyloxidase (ein durch Cu- Ionen aktiviertes Enzym) zu Allysin bzw. Hydroxyallysin oxidiert (Abbildung 2). Die entsprechende Quervernetzung findet in der tripelhelikalen Region in den Positionen 87 und 930 statt. Charakteristisch für diese Positionen sind die Aminosäurensequenzen Lys-Gly-His- Arg-Gly oder Hyl-Gly-His-Arg-Gly. In Position 9 der N-terminalen Telopeptide aus Lysin- oder Hydroxylysinresten entstandene Aldehygruppen reagieren mit Lysin oder Hydroxylysin in der o.g. Sequenz der Tripelhelix und bilden Schiff sche Basen [4], wie zum Beispiel Dehydro-hydroxylysino-norleucin (deh-hlnl) oder Dehydro-lysino-norleucin (deh-lnl), die auch als Aldimine bekannt sind. [5] Erstere wird zwischen Allysin aus der Telopeptid-Region und Hydroxylysin aus der tripelhelikalen Region gebildet. Die zweite ist das Produkt aus der Reaktion zwischen der Aldehydgruppe von Allysin in der Telopeptid-Region und Lysin in der tripelhelikalen Region (Abbildung 3). Diese beiden Quervernetzungen sind divalent und kommen am häufigsten vor, da sie thermodynamisch stabile Produkte darstellen. Sie sind charakteristisch für Bindegewebe wie die Haut oder die Sehnen und werden bei sauren ph-werten leicht aufgespalten. Aus diesem Grund ist die Kollagengewinnung mit sauren Lösungen einfach zu realisieren, wenn diese aus der Haut junger Tieren erfolgt. Dieser Rohstoff enthält nämlich nur divalente Quervernetzungen. Mit zunehmendem Alter treten tri- und tetravalente Quervernetzungen auf, die dann säurestabil sind. Die divalenten Schiff schen Basen können über eine milde Reduktion mit Borhydrid für Analysen stabilisiert werden. Dabei entsteht Hydroxylysinonorleucin (HLNL) bzw. Lysinonorleucin (LNL) (siehe Abbildung 3). [4] HLNL kommt reichlich in den meisten Kollagenen vor, während LNL sowohl in Kollagen als auch in Elastin zu finden ist. [6] Eine zweite Gruppe von divalenten Quervernetzungen stellen AMADORI-Produkte, also α Amino-Ketone, dar. Diese entstehen zunächst aus der Reaktion zwischen der Aldehydgruppe von Hydroxyallysin (siehe Abbildung 2) in einem Telopeptid und Hydroxylysin in der tripelhelikalen Region. [4] Die gebildete Schiff sche Base unterliegt einer AMADORI-Umlagerung zu Hydroxylysino-5-ketonorleucin (HLKNL). Dieses kann nachfolgend zu Dihydroxy-lysino-norleucin (DHLNL) reduziert werden (Abbildung 4). Letzteres kommt häufig in mineralisierten Geweben wie Knochen und Knorpel vor [6] und ist säure- und wärmestabil. Die entsprechenden Gewebe sind dann unlöslich. Beide Gruppen von divalenten Quervernetzungen können durch weitere Reaktionen noch stabilere trivalente Quervernetzungen bilden. Beispielweise reagiert Dehydro-hydroxylysino-norleucin (deh-hlnl) mit Histidin zu Histidino-hydroxylysino-norleucin (HHLNL) (Abbildung 5). [3] Andere häufig vorkommende trivalente Quervernetzungen (Abbildung 6), die vorwiegend in reifen Bindegeweben (außer in der Haut) zu finden sind, führen unter Beteiligung von drei Hydroxylysin-Resten zu Hydroxlysylpyridinolinen (HP) bzw. unter Einbeziehung von zwei Hydroxylysin-Resten und einem Lysin-Rest zu Lysyl pyridinolin (LP) [7]. 2
3 Quervernetzungen zwischen zwei Allysin-Resten, bekannt als Aldolkondensationprodukte (ACP), finden bei Kollagen nur in der Nähe des Endes des N-Terminus statt. Sie gehören zu den intramolekularen Quervernetzungen in Kollagen und Elastin. [6] Über nachfolgende Reaktionen bilden die ACP tri- und tetravalente Quervernetzungen. Die Wechselwirkung mit Histidin führt zu einem Aldol-Histidin-Produkt (AH), eine trivalente Quervernetzung, die nach Tanzer [6], in Rinderhaut vorhanden ist. Bei Wechselwirkung mit Histidin und Hydroxyllysin entsteht Histidinohydroxymerodesmosin (HHMD), eine tetravalente Quervernetzung (Abbildung 7). Die enzymatische Quervernetzung kann also, zusammengefasst, abhängig von den Lysin- und Hydroxylysinresten in den Telopeptiden, über zwei Wege verlaufen. Quervernetzungen unter Beteiligung von Lysin sind typisch für die Haut und die Kornea, und wenn sie divalent vorliegen, können sie mit sauren Lösungen für die Kollagengewinnung in diesen Geweben aufgespalten werden. Sind tri- und tetravalente Quervernetzungen vorherrschend, ein Hinweis für reifes und alterndes Kollagen, wird die Kollagenextraktion schwieriger und ist mit sauren Lösungen wegen der Kollagenunlöslichkeit nicht mehr möglich. Andererseits gehen die Quervernetzungen in mineralisierten Geweben wie Knochen und Knorpel von Hydroxylysin aus. In diesem Fall können selbst divalente Quervernetzungen wie Dihydroxy-lysino-norleucin (DHLNL) mit sauren Lösungen nicht aufgespalten werden, und die Gewinnung von löslichem Kollagen ist auf diesem Wege nicht realisierbar. Die folgende Zusammenstellung bietet einen Überblick über die Art und das Vorkommen der verschiedenen Quervernetzungen in den Geweben: Divalent HLNL und LNL hauptsächlich in der Haut und in der Kornea; Divalent DHLNL vorwiegend in mineralisierten Geweben wie Knochen und Knorpel; Trivalent HHLNL hauptsächlich in der Haut und in der Kornea; Trivalent LP und HP vorwiegend in reifen Bindegeweben (außer in der Haut); Tetravalent HHMD überwiegend in der Haut und in Knorpel. In Abbildung 8 werden noch einmal zusammenfassend die enzymatischen Quervernetzungen in Abhängigkeit von den bei ihrer Bildung beteiligten Aminosäurenresten, Lysin oder Hydroxylysin, dargestellt. Die zweite Art von Quervernetzungen, die nichtenzymatische, die auch als Glykierung bekannt ist, erfolgt unter Einbeziehung von Kohlenhydraten (vor allem Glucose und Galactose). Dabei werden Lysin- oder Hydroxylysin-Reste mit fortschreitendem Alter der Gewebe durch Kohlenhydrate glycosidiert, und die Glycoside folgen den üblichen nichtenzymatischen Bräunungsmechanismen, so z.b. der MAILLARD-Reaktion. Es bilden sich vor allem intramolekular, unter Einbeziehung der Tripelhelices, wenig lösliche, aber widerstandsfähige Kollagennetze. [4], [5] Über die Separierung der Kollagene in lösliche und wenig lösliche Fraktionen wird in einem weiteren Beitrag berichtet. Danksagung Die für diese Publikation notwendigen Recherchen und experimentellen Arbeiten wurden im Rahmen des Verbundprojekts Hochadhäsives lösliches Kollagen durchgeführt, das mit Mitteln des Landes Berlin und des Europäischen Fonds für regionale Entwicklung (EFRE) über die Investitionsbank Berlin gefördert wurde. 3
4 Abbildungen Abbildung 1: Schematische Darstellung der Kollagenbiosynthese 4
5 Abbildung 2: Oxidation von Lysin und Hydroxylysin mittels Lysyloxidase 5
6 Abbildung 3: Bildung der reduzierbaren Schiff'schen Basen Dehydro-hydroxylysino-norleucin (deh-hlnl) und Dehydro-lysino-norleucin (deh-lnl) 6
7 Abbildung 4: Bildung von divalenten Quervernetzungen in mineralisierten Geweben. Hydroxylysino-5-ketonorleucin (HLKNL) und seine reduzierte Form Dihydroxy-lysino-norleucin (DHLNL) 7
8 Abbildung 5: Bildung der trivalenten Quervernetzung Histidino-hydroxylysino-norleucin (HHLNL) 8
9 Abbildung 6: Trivalente Quervernetzungen Hydroxylysyl pyridinolin (HP) und Lysyl pyridinolin (LP) 9
10 Abbildung 7: Bildung von trivalentem Aldol - Histidine (AH) und tetravalentem Histidinohydroxymerodesmosine (HHMD) 10
11 Abbildung 8: Überblick über die enzymatischen Quervernetzungen 11
12 Literatur [1] Hulmes, D. J. S.: Collagen Diversity, Synthesis and Assembly; in Collagen Structure and Mechanics, Herausgeber Fratzl, P.; Springer Science+business Media, 2008 [2] Hulmes, D. J. S.: Building Collagen Molecules, Fibrils and Suprafibrillar Structures. Journal of Structural Biology, 137 (2002), 2-10 [3] Shoulders, D. M., und Raines, T. R.: Collagen structure and stability. Ann. Rev. Biochem., 78 (2009), [4] Bailey, A. J.; Paul, R. G.; Knott, L.: Mechanisms of maturation and ageing of collagen. Mechanisms of Ageing and Development, 106 (1998), 1-56 [5] Reiser, K.; Mccormick, R. J.; Rucker, R. B.: Enzymatic and nonenzymatic cross-linking of collagen and elastin. The FASEB Journal, 6 (1992), [6] Tanzer, M. L.: Cross-linking of collagen. The SCIENCE Journal, 180 (1973), [7] Eyre D. R.; Paz, M. A.; Gallop, P. M.: Cross-linking in Collagen and Elastin. Ann. Rev. Biochem., 53 (1984), [ ] Kontakt: Dr. Rafael Valbuena Institut für Agrar- und Stadtökologische Projekte an der Humboldt-Universität zu Berlin Philippstraße 13, Haus 16 D Berlin rafael.valbuena@agrar.hu-berlin.de Das Vorhaben "Hochadhäsives lösliches Kollagen" wurde von der Europäischen Union kofinanziert (Europäischer Fonds für regionale Entwicklung) Investition in ihre Zukunft 12
Unter der Kollagensynthese versteht man die intrazellulär und extrazellulär. stattfindende Synthese von Kollagen.
 KOLLAGENSYNTHESE!! Unter der Kollagensynthese versteht man die intrazellulär und extrazellulär stattfindende Synthese von Kollagen. Das Kollagen ist im menschlichen Körper Bestandteil aller Binde. - und
KOLLAGENSYNTHESE!! Unter der Kollagensynthese versteht man die intrazellulär und extrazellulär stattfindende Synthese von Kollagen. Das Kollagen ist im menschlichen Körper Bestandteil aller Binde. - und
Anatomie - Histologie. Bindegewebe
 Bindegewebe 1 Binde- und Stützgewebe Lockeres Bindegew., Fettgewebe, Knorpel, Knochen 2 Binde- und Stützgewebe Zusammengesetzt aus Bindegewebszellen und größerer Mengen geformter, bzw. ungeformter Interzellularsubstanzen
Bindegewebe 1 Binde- und Stützgewebe Lockeres Bindegew., Fettgewebe, Knorpel, Knochen 2 Binde- und Stützgewebe Zusammengesetzt aus Bindegewebszellen und größerer Mengen geformter, bzw. ungeformter Interzellularsubstanzen
Peptide Proteine. 1. Aminosäuren. Alle optisch aktiven proteinogenen Aminosäuren gehören der L-Reihe an: 1.1 Struktur der Aminosäuren
 1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
 Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
und Reinstruktur Die Sekundärstruktur ist die Anordnung der Aminosäurenkette, wobei man in zwei Arten unterscheidet: o Faltblatt- oder β- Struktur
 Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
Denaturierung von Proteinen
 Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
Gewinnung von löslichen Kollagenen aus Schweineschwarten und deren Verwendung in der regenerativen Medizin
 LIFIS ONLINE [09.11.11] ISSN 1864-6972 Aneliya Petrova 1, Günter Westphal 1, Rafael Valbuena 1, Tilo Dehne 2, Jochen Ringe 2 Gewinnung von löslichen Kollagenen aus Schweineschwarten und deren Verwendung
LIFIS ONLINE [09.11.11] ISSN 1864-6972 Aneliya Petrova 1, Günter Westphal 1, Rafael Valbuena 1, Tilo Dehne 2, Jochen Ringe 2 Gewinnung von löslichen Kollagenen aus Schweineschwarten und deren Verwendung
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
2.1.5 Mechanische Eigenschaften von Holz. Experimente an Druckholz (MFA = 46 ) ID01. MFA wird unter Zug kleiner!
 2.1.5 Mechanische Eigenschaften von Holz 113 Experimente an Druckholz (MFA = 46 ) ID01 MFA wird unter Zug kleiner! Mikroskopischer Klettverschluß in Holz? 114 50 MFA ( ) σ (MPa) 40 30 20 10 0 45 42 39
2.1.5 Mechanische Eigenschaften von Holz 113 Experimente an Druckholz (MFA = 46 ) ID01 MFA wird unter Zug kleiner! Mikroskopischer Klettverschluß in Holz? 114 50 MFA ( ) σ (MPa) 40 30 20 10 0 45 42 39
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
9. ZUSAMMENFASSUNG DER UNTERSUCHUNGEN ZU KOLLAGEN IV
 9. ZUSAMMENFASSUNG DER UNTERSUCHUNGEN ZU KOLLAGEN IV 9.1. Struktur und Faltung von Kollagen Kollagene sind Proteine eukaryontischer Organismen, die aus drei Polypeptidketten aufgebaut sind. Sie werden
9. ZUSAMMENFASSUNG DER UNTERSUCHUNGEN ZU KOLLAGEN IV 9.1. Struktur und Faltung von Kollagen Kollagene sind Proteine eukaryontischer Organismen, die aus drei Polypeptidketten aufgebaut sind. Sie werden
10 BIOGENE-AMINE 4 NICHT-PROTEINOGENE- AS. 20 PROTEINOGENE AS glucoplastisch/ketoplastisch 8 ESSENTIELLE AS
 Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie
 1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
Arzneistoff der Woche. Alkohole. Eliminierungen. Organische Chemie Agenda. Johann Wolfgang Goethe -Universität Frankfurt am Main
 Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Signaltransduktion durch Zell-Zell und Zell-Matrix Kontakte
 Signaltransduktion durch Zell-Zell und Zell-Matrix Kontakte - Integrine als zentrale Adhäsionsrezeptoren - - Focal Adhesion Kinase (FAK) als zentrales Signalmolekül - Regulation von Zellfunktionen durch
Signaltransduktion durch Zell-Zell und Zell-Matrix Kontakte - Integrine als zentrale Adhäsionsrezeptoren - - Focal Adhesion Kinase (FAK) als zentrales Signalmolekül - Regulation von Zellfunktionen durch
Lösungsblatt zu Aufbau von Aminosäuren
 Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 2. Faserproteine - lange Moleküle deren
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 2. Faserproteine - lange Moleküle deren
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
1 Einleitung. 1.1 Die extrazelluläre Matrix
 3 1 Einleitung 1.1 Die extrazelluläre Matrix Als extrazelluläre Matrix (EZM) bezeichnet man die Strukturen, die den Raum zwischen den Zellen der verschiedenen Gewebe ausfüllen und für deren Integrität
3 1 Einleitung 1.1 Die extrazelluläre Matrix Als extrazelluläre Matrix (EZM) bezeichnet man die Strukturen, die den Raum zwischen den Zellen der verschiedenen Gewebe ausfüllen und für deren Integrität
DIPLOMARBEIT HOCHSCHULE MITTWEIDA UNIVERSITY OF APPLIED SCIENCES
 Caroline Vogler Quantifizierung verschiedener Kollagentypen in Gewebeproben mittels elektrophoretischer und chromatographischer Methoden eingereicht als DIPLOMARBEIT an der HOCHSCHULE MITTWEIDA UNIVERSITY
Caroline Vogler Quantifizierung verschiedener Kollagentypen in Gewebeproben mittels elektrophoretischer und chromatographischer Methoden eingereicht als DIPLOMARBEIT an der HOCHSCHULE MITTWEIDA UNIVERSITY
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Rekombinante Wirkstoffe. Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt
 Rekombinante Wirkstoffe Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Das Problem mit dem N-Terminus von rekombinanten Proteinen
Rekombinante Wirkstoffe Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Das Problem mit dem N-Terminus von rekombinanten Proteinen
Aldehyde und Ketone Carbonylverbindungen
 Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Fettsäurebiosynthese
 Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Proteine - nutritive und funktionelle Eigenschaften
 Gesunde Ernährung Healthy Nutrition Proteine - nutritive und funktionelle Eigenschaften Bearbeitet von Günter Westphal, Gerhard Gerber, Bodo Lipke 1. Auflage 2003. Buch. XXII, 458 S. Hardcover ISBN 978
Gesunde Ernährung Healthy Nutrition Proteine - nutritive und funktionelle Eigenschaften Bearbeitet von Günter Westphal, Gerhard Gerber, Bodo Lipke 1. Auflage 2003. Buch. XXII, 458 S. Hardcover ISBN 978
Was ist denn NAD / NADP??
 Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Nehmen Sie ausreichend. Vitamin C. zu sich? Magenfreundlich. ph-neutral. Gratis Hotline: Für Ihr Immunsystem
 Nehmen Sie ausreichend Vitamin C zu sich? Magenfreundlich und ph-neutral Gratis Hotline: 0800 112 25 25 Für Ihr Immunsystem Warum benötigen wir Vitamin C? Eines der wichtigsten Vitamine für uns Menschen
Nehmen Sie ausreichend Vitamin C zu sich? Magenfreundlich und ph-neutral Gratis Hotline: 0800 112 25 25 Für Ihr Immunsystem Warum benötigen wir Vitamin C? Eines der wichtigsten Vitamine für uns Menschen
Studiengang - Medizintechnik Kompetenzfeld: Vitale Implantate
 Studiengang - Medizintechnik Kompetenzfeld: Vitale Implantate Prof. Dr. rer. nat. Katja Schenke-Layland Department für Frauengesundheit, Forschungsinstitut für Frauengesundheit, Medizinische Fakultät der
Studiengang - Medizintechnik Kompetenzfeld: Vitale Implantate Prof. Dr. rer. nat. Katja Schenke-Layland Department für Frauengesundheit, Forschungsinstitut für Frauengesundheit, Medizinische Fakultät der
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Rekombinante Wirkstoffe. Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt
 Rekombinante Wirkstoffe Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Rekombinante Wirkstoffe Auf den ersten Blick liegt es
Rekombinante Wirkstoffe Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Rekombinante Wirkstoffe Auf den ersten Blick liegt es
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alle(s) Zucker oder was?
 Alle(s) Zucker oder was? Ein gesundes Gehirn Alles eine Frage des Zuckers? Werner Reutter Institut für Biochemie und Molekularbiologie Charité - Universitätsmedizin Berlin Campus Benjamin Franklin Konstanz
Alle(s) Zucker oder was? Ein gesundes Gehirn Alles eine Frage des Zuckers? Werner Reutter Institut für Biochemie und Molekularbiologie Charité - Universitätsmedizin Berlin Campus Benjamin Franklin Konstanz
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Das Zytoskelett (Gastvorlesung R. Brandt, Neurobiologie)
 Das Zytoskelett (Gastvorlesung R. Brandt, Neurobiologie) Inhalt: 1. Struktur und Dynamik der zytoskeletalen Filamentsysteme 2. Regulation der zytoskeletalen Komponenten 3. Molekulare Motoren 4. Zytoskelett
Das Zytoskelett (Gastvorlesung R. Brandt, Neurobiologie) Inhalt: 1. Struktur und Dynamik der zytoskeletalen Filamentsysteme 2. Regulation der zytoskeletalen Komponenten 3. Molekulare Motoren 4. Zytoskelett
Pharmazeutische Biologie Grundlagen der Biochemie
 Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
Intelligente Polymere. Anne Oestreicher
 Intelligente Polymere Anne Oestreicher 09.12.2014 2 Intelligente Polymere 1. Einleitung 2. Stimuli-responsive Polymere 3. Thermoresponsive Polymere a. Kritische Entmischungstemperaturen b. Thermodynamik
Intelligente Polymere Anne Oestreicher 09.12.2014 2 Intelligente Polymere 1. Einleitung 2. Stimuli-responsive Polymere 3. Thermoresponsive Polymere a. Kritische Entmischungstemperaturen b. Thermodynamik
Die Potenziale der Milchproteine zur Gelbildung
 Die Potenziale der Milchproteine zur Gelbildung Seminarvortrag von Petra Westmeier 18.11.2004 Universität Hohenheim Institut für Lebensmittel tierischer Herkunft Leitung: Prof. Dr. Jörg Hinrichs Betreuer:
Die Potenziale der Milchproteine zur Gelbildung Seminarvortrag von Petra Westmeier 18.11.2004 Universität Hohenheim Institut für Lebensmittel tierischer Herkunft Leitung: Prof. Dr. Jörg Hinrichs Betreuer:
Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )
![Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 ) Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )](/thumbs/74/69784240.jpg) 1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Aspekte der Eisenresorption. PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse Binningen
 Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
COOH. Die Aminosäuren tragen laborübliche Abkürzungen, so stehen z. B. Gly für Glycin oder Phe für Phenylalanin.
 Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Membranen (3a) Membrane
 Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Gewebelehre Zellfortsätze, Binde- und Stützgewebe
 Gewebelehre Zellfortsätze, Binde- und Stützgewebe David P. Wolfer Institut für Bewegungswissenschaften und Sport, D-HEST, ETH Zürich Anatomisches Institut, Medizinische Fakultät, Universität Zürich 76-0-00
Gewebelehre Zellfortsätze, Binde- und Stützgewebe David P. Wolfer Institut für Bewegungswissenschaften und Sport, D-HEST, ETH Zürich Anatomisches Institut, Medizinische Fakultät, Universität Zürich 76-0-00
Allgemeine Pathologie. Störungen im Kupfer- Stoffwechsel
 Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Das große Gesundheits-und Sportevent 12. und 13. Juni Gewebe in der Rehabilitation
 Das große Gesundheits-und Sportevent 12. und 13. Juni 2010 GluckerKolleg und GluckerSchule Gewebe in der Rehabilitation Philipp Hausser FOMT: Team (www.fomt.info) Histologie: Epithelgewebe Muskelgewebe
Das große Gesundheits-und Sportevent 12. und 13. Juni 2010 GluckerKolleg und GluckerSchule Gewebe in der Rehabilitation Philipp Hausser FOMT: Team (www.fomt.info) Histologie: Epithelgewebe Muskelgewebe
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
D-(+)-Biotin (Vitamin H)
 D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
D-(+)-Biotin (Vitamin H) Benedikt Jacobi 28. Januar 2005 1 Inhaltsverzeichnis 1 Einleitung 1 1.1 Aufgabenstellung: Prüfung der Stabilität von Biotin (Vitamin H) unter alltäglichen Bedingungen (Kochen,
Vorname: Frage 1. Nennen Sie drei Metalle, die :für den Menschen essentiell sind und als Mengenelemente Körper vorkommen (3 P) Frage 2
 1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
Lernpaket 3: Monosaccharide
 Lernpaket 3: Monosaccharide Saccharide Bei der Photosynthese werden aus Wasser und Kohlendioxid unter Freisetzung von Sauerstoff Kohlenhydrate (Zucker, Saccharide 1 ) hergestellt. Sie enthalten Kohlenstoff,
Lernpaket 3: Monosaccharide Saccharide Bei der Photosynthese werden aus Wasser und Kohlendioxid unter Freisetzung von Sauerstoff Kohlenhydrate (Zucker, Saccharide 1 ) hergestellt. Sie enthalten Kohlenstoff,
...-Arg-Met-Phe-Ala-Asn-His-Lys-Ser-Val-Gly-...
 1. Im Enzym Xase, das aus einer Polypeptidkette aus 300 Aminosäuren besteht, findet sich in der Region der Aminosäuren 40-50 die folgende Aminosäurensequenz:...-Arg-Met-Phe-Ala-Asn-His-Lys-Ser-Val-Gly-...
1. Im Enzym Xase, das aus einer Polypeptidkette aus 300 Aminosäuren besteht, findet sich in der Region der Aminosäuren 40-50 die folgende Aminosäurensequenz:...-Arg-Met-Phe-Ala-Asn-His-Lys-Ser-Val-Gly-...
Zucker und Polysaccharide (Voet Kapitel 10)
 Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Oxidativer Stress Vitamine
 1 Oxidativer Stress Vitamine 2 Reaktive Sauerstoffspezies (ROS) Reaktive Sauerstoffspezies (ROS) Ein-Elektronenreduktion von Sauerstoff durch Strahlung oder Autooxidation von reduzierten Stoffwechselzwischenprodukten
1 Oxidativer Stress Vitamine 2 Reaktive Sauerstoffspezies (ROS) Reaktive Sauerstoffspezies (ROS) Ein-Elektronenreduktion von Sauerstoff durch Strahlung oder Autooxidation von reduzierten Stoffwechselzwischenprodukten
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Klausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach (SS2011)
 Klausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach (SS2011) Musterlösung 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Amylose und Amylopektin bestehen nur aus D-Glucose
Klausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach (SS2011) Musterlösung 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Amylose und Amylopektin bestehen nur aus D-Glucose
Tyrosinkinase- Rezeptoren
 Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Chemie des Haares HAARE. a-helix-struktur der Haarproteine. Protein-Helix. Wasserstoffbrücke. b-ketten- oder Faltblatt-Struktur der Haarproteine
 Chemie des Haares Das Haar besteht zu 90 % aus dicht aneinander gereihten Zellen, die Keratin ein Eiweiß enthalten. Keratin wiederum besteht aus Aminosäuren, die zu langen Ketten (= Polypeptidketten) aneinander
Chemie des Haares Das Haar besteht zu 90 % aus dicht aneinander gereihten Zellen, die Keratin ein Eiweiß enthalten. Keratin wiederum besteht aus Aminosäuren, die zu langen Ketten (= Polypeptidketten) aneinander
Chemie-Tutorien zur Vorbereitung auf das Praktikum
 Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Halogen-, Interhalogenund Edelgas-Verbindungen
 Halogen-, Interhalogenund Edelgas-Verbindungen Vorkommen und Darstellung von 2,Cl 2, 2,I 2 17 2 Cl 2 2 I 2 Vorkommen Ca 2 (lussspat) Na 3 Al 6 (Kryolith) Ca 5 (PO 4 ) 3 (luorapatit) Cl - : gelöst in Meerwasser
Halogen-, Interhalogenund Edelgas-Verbindungen Vorkommen und Darstellung von 2,Cl 2, 2,I 2 17 2 Cl 2 2 I 2 Vorkommen Ca 2 (lussspat) Na 3 Al 6 (Kryolith) Ca 5 (PO 4 ) 3 (luorapatit) Cl - : gelöst in Meerwasser
Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner Samstag, Uhr Allgemeine Chemie
 Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Seite 1 von 6 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie Tutorien zur Vorbereitung auf das Vorphysikum der Zahnmediziner 25.02. 04.03.2017 Samstag, 25.02.17 15.00 17.00 Uhr Allgemeine Chemie Mittwoch,
Identification and Characterization of Collagen Glycosyltransferases of Human and Viral Origin
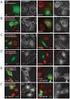 DISS. ETH NO. 17906 Identification and Characterization of Collagen Glycosyltransferases of Human and Viral Origin A dissertation submitted to ETH ZURICH for the degree of Doctor of Sciences presented
DISS. ETH NO. 17906 Identification and Characterization of Collagen Glycosyltransferases of Human and Viral Origin A dissertation submitted to ETH ZURICH for the degree of Doctor of Sciences presented
Bovine Spongiforme Enzephalopathie
 Bovine Spongiforme Enzephalopathie Biophysikalisches Seminar WS 06/07 von Bernhard Pfirrmann 1 Themen TSE allgemein BSE und nvcfk Die Suche nach dem BSE- Erreger PrP C und PrP Sc Folgen der Aggregation
Bovine Spongiforme Enzephalopathie Biophysikalisches Seminar WS 06/07 von Bernhard Pfirrmann 1 Themen TSE allgemein BSE und nvcfk Die Suche nach dem BSE- Erreger PrP C und PrP Sc Folgen der Aggregation
0.1 Eiweißstoffe (Proteine)
 1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
Übersicht: T-Zell-unabhängige und T-Zellabhängige. Humorales Gedächtnis
 Übersicht: T-Zell-unabhängige und T-Zellabhängige B-Zellaktivierung Humorales Gedächtnis Fachmodul Immunologie November 2010 Melanie Haars Übersicht I. Einleitung II. B-Zellaktivierung T-Zell-unabhängige
Übersicht: T-Zell-unabhängige und T-Zellabhängige B-Zellaktivierung Humorales Gedächtnis Fachmodul Immunologie November 2010 Melanie Haars Übersicht I. Einleitung II. B-Zellaktivierung T-Zell-unabhängige
ANTRAG AUF GENEHMIGUNG für Arzneimittel für neuartige Therapien
 ANTRAG AUF GENEHMIGUNG für Arzneimittel für neuartige Therapien nach 4 b Abs. 3 i.v.m. 21a Abs. 2-8 des Arzneimittelgesetzes (AMG) Modul 0 Einstufung des Arzneimittels als Arzneimittel für neuartige Therapien
ANTRAG AUF GENEHMIGUNG für Arzneimittel für neuartige Therapien nach 4 b Abs. 3 i.v.m. 21a Abs. 2-8 des Arzneimittelgesetzes (AMG) Modul 0 Einstufung des Arzneimittels als Arzneimittel für neuartige Therapien
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Kohlenhydrate und ihre Funktionen
 Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Chemie für Mediziner. Norbert Sträter
 Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
ATTO 565 und ATTO 590
 ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
Molekularbiologie 6c Proteinbiosynthese. Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird
 Molekularbiologie 6c Proteinbiosynthese Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird 1 Übersicht: Vom Gen zum Protein 1. 2. 3. 2 Das Dogma
Molekularbiologie 6c Proteinbiosynthese Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird 1 Übersicht: Vom Gen zum Protein 1. 2. 3. 2 Das Dogma
Stoffklasse: LIPIDE Funktionen in der Zelle
 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Einführung in die Biochemie Glykolyse
 Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Quantifizierung von Hydroxyprolin mittels ESI-MS
 Massenspektrometrie Prof. Dr. R. Hoffmann Quantifizierung von Hydroxyprolin mittels ESI-MS Julia Kuhlmann Henrik Teller 10.01.2008 Präsentierte Literatur 1) T. Langrock, P. Czihal, R. Hoffmann (2006) Amino
Massenspektrometrie Prof. Dr. R. Hoffmann Quantifizierung von Hydroxyprolin mittels ESI-MS Julia Kuhlmann Henrik Teller 10.01.2008 Präsentierte Literatur 1) T. Langrock, P. Czihal, R. Hoffmann (2006) Amino
Grundlagen der Medizinischen Chemie Sommersemester 2016
 Grundlagen der Medizinischen Chemie Sommersemester 2016 Prof. Dr. Franz Paintner Dienstag, 9 15-11 00 Uhr, Buchner-Hörsaal Mittwoch, 8 15-9 00 Uhr, Buchner-Hörsaal Aktuelle Informationen zur Vorlesung
Grundlagen der Medizinischen Chemie Sommersemester 2016 Prof. Dr. Franz Paintner Dienstag, 9 15-11 00 Uhr, Buchner-Hörsaal Mittwoch, 8 15-9 00 Uhr, Buchner-Hörsaal Aktuelle Informationen zur Vorlesung
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Herstellung des Benzoldiazoniumchlorids aus Anilin, Natriumnitrit und Salzsäure. Benzoldiazonium-Ion
 Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
 Bindegewebsphysiologie aus osteopathischer Sicht Karsten Fähle Heilpraktiker, Osteopath www. natural-medical-coach.decoach.de Osteopathie, Psycho-Neuro-Immunologie, Neuraltherapie, Labordiagnostik Literatur:
Bindegewebsphysiologie aus osteopathischer Sicht Karsten Fähle Heilpraktiker, Osteopath www. natural-medical-coach.decoach.de Osteopathie, Psycho-Neuro-Immunologie, Neuraltherapie, Labordiagnostik Literatur:
Stützgewebe 1/3. Knorpel
 Stützgewebe 1/3 Knorpel Knorpel Knorpelzellen Matrix Chondroblasten Chondrozyten Wasser (80%) Kollagen Typ II (Hauptanteil) Kollagen Typ IX (verbindet Typ II Fibrillen) Kollagen Typ X Kollagen Typ XI (Teil
Stützgewebe 1/3 Knorpel Knorpel Knorpelzellen Matrix Chondroblasten Chondrozyten Wasser (80%) Kollagen Typ II (Hauptanteil) Kollagen Typ IX (verbindet Typ II Fibrillen) Kollagen Typ X Kollagen Typ XI (Teil
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Aufgabe 5 (Supersekundärstruktur)
 Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Kl.10 LB2. Kl.10 LB2. Kl.10 LB2. Kl.10 LB2. Nenne 2 Vorkommen von Fetten.
 Nenne 2 Vorkommen von Fetten. Es gibt pflanzliche Fette (Kokosöl, livenöl) und tierische Fette (Schweinefett, Milchfett). Beschreibe die Löslichkeit der Fette. Fette sind nicht in Wasser aber in Benzin
Nenne 2 Vorkommen von Fetten. Es gibt pflanzliche Fette (Kokosöl, livenöl) und tierische Fette (Schweinefett, Milchfett). Beschreibe die Löslichkeit der Fette. Fette sind nicht in Wasser aber in Benzin
Biolaugung Mechanismus
 Biolaugung Mechanismus Von Wiebke Beysiegel und Greta Buschmann Was ist Biolaugung? Gewinnung von Metallen aus ihren Erzen mit Hilfe von Mikroorganismen durch Mo entstandene Metallkationen werden im Wasser
Biolaugung Mechanismus Von Wiebke Beysiegel und Greta Buschmann Was ist Biolaugung? Gewinnung von Metallen aus ihren Erzen mit Hilfe von Mikroorganismen durch Mo entstandene Metallkationen werden im Wasser
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Die Verknüpfung zweier kleinerer Bausteine zu einem größeren läuft in diesem Fall über eine sogenannte Aldoladdition.
 Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
2. Übung Grundlagen der Hauptgruppenchemie AC02
 Allgemeine und Anorganische Chemie 2. Übung Grundlagen der Hauptgruppenchemie AC02 Aufgabe 1: Vervollständigen und gleichen Sie die folgenden Gleichungen aus: a) CaO + H 2 O Ca(OH) 2 b) Al 2 O 3 + 6 H
Allgemeine und Anorganische Chemie 2. Übung Grundlagen der Hauptgruppenchemie AC02 Aufgabe 1: Vervollständigen und gleichen Sie die folgenden Gleichungen aus: a) CaO + H 2 O Ca(OH) 2 b) Al 2 O 3 + 6 H
Bestimmung von Plasma-Cholesterin und Triglycerid-Spiegel
 Plasma-Lipoproteine und -Fette Bestimmung von Plasma-Cholesterin und Triglycerid-Spiegel Charakteristisch für Lipide sind eine niedrige Polarität und eine begrenzte Wasserlöslichkeit. Ihre Plasmakonzentration
Plasma-Lipoproteine und -Fette Bestimmung von Plasma-Cholesterin und Triglycerid-Spiegel Charakteristisch für Lipide sind eine niedrige Polarität und eine begrenzte Wasserlöslichkeit. Ihre Plasmakonzentration
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
DER BÄNNJERRÜCKBOTE. Eine Zeitung von Bürgern für Bürger. Unabhängige Stadtteilzeitung Bännjerrück I Karl-Pfaff-Siedlung I Kaiserslautern
 Eine Zeitung von Bürgern für Bürger DER BÄNNJERRÜCKBOTE Unabhängige Stadtteilzeitung Bännjerrück I Karl-Pfaff-Siedlung I Kaiserslautern 4. Ausgabe, März 2009, ISSN 1867-1950 Dieses Projekt wird im Rahmen
Eine Zeitung von Bürgern für Bürger DER BÄNNJERRÜCKBOTE Unabhängige Stadtteilzeitung Bännjerrück I Karl-Pfaff-Siedlung I Kaiserslautern 4. Ausgabe, März 2009, ISSN 1867-1950 Dieses Projekt wird im Rahmen
