Multiple Sklerose. Modul 1: MS: Krankheitsaktivität und Schübe. 2. Klinisches Bild und Verlaufsformen. 1. Einleitung
|
|
|
- Emilia Bader
- vor 7 Jahren
- Abrufe
Transkript
1 Multiple Sklerose Modul 1: MS: Krankheitsaktivität und Schübe Prof. Dr. med. Tjalf Ziemssen, Neurologische Universitätsklinik Dresden VNR: Gültigkeitsdauer: Einleitung 2. Klinisches Bild und Verlaufsformen Die Multiple Sklerose (MS) ist in Deutschland die häufigste chronisch entzündliche Erkrankung des zentralen Nervensystems (ZNS) bei jungen Erwachsenen. Sie manifestiert sich meist zwischen dem 25. und 40. Lebensjahr mit einem schubförmig remittierenden Verlauf. Frauen sind etwa dreimal so häufig betroffen wie Männer [Koch-Hendriksen und Sorensen 2010]. Derzeit leben in Deutschland fast Patienten mit MS [Petersen et al. 2014]. Die Erkrankung führt bei vielen Betroffenen zu bleibender Behinderung und Frühverrentung [DGN / KKNMS 2014]. Bei MS handelt es sich um eine chronische entzündliche Auto immunerkrankung des ZNS, die mit einer Demy elinisierung der Nerven und Axonschädigungen verbunden ist [Compston und Coles 2008]. Da die MS das gesamte ZNS betrifft, ist das klinische Bild individuell sehr heterogen und verändert sich im Verlauf der Erkrankung. Häufige Symptome sind Sensibilitätsstörungen, Paresen, Visusbeeinträchtigung, Ataxie, Fatigue oder Blasen- / Darmstörungen. Zudem kann die MS mit kognitiven Einschränkungen oder psychiatrischen Auffälligkeiten verbunden sein [Wiendl und Kieseier 2010]. Die MS kann zwar nicht geheilt, aber immer besser behandelt werden. Zur Charakterisierung der individuellen MS und des Behandlungserfolgs werden die Schubrate, die Behinderungsprogression, MRT-Läsionen und die Hirnatrophie herangezogen. Bislang bestand das Behandlungsziel vor allem in der Reduzierung der Schubrate und der Verzögerung der Behinderungsprogression. Mit neuen Medikamenten wie Fingolimod oder Natalizumab wird jetzt das neue Ziel der bestmöglichen Krankheitskontrolle angestrebt ein Zustand ohne feststellbare Krankheitsaktivität (ohne Schübe, ohne Behinderungsprogression und ohne MS-Aktivität im MRT) [Bevan und Cree 2014, Fox und Rhoades 2014]. Um neurologische Schädigungen bereits im Frühstadium der MS zu vermeiden, wird eine frühzeitige Einstellung/Umstellung auf aktive Immuntherapeutika empfohlen [DGN / KKNMS 2014]. Dadurch kann das klinische Langzeitergebnis von MS-Patienten mit einiger Wahrscheinlichkeit deutlich verbessert werden [Fox und Rhoades 2014] Klassifizierung und Verlauf Die vorliegende Fortbildung, welche das erste Modul einer vierteiligen Fortbildungsreihe darstellt, informiert über die MS, die Bedeutung der Schubrate für den Verlauf der Erkrankung und über die leitliniengerechte Behandlung. Des Weiteren gibt sie einen Überblick zu allen derzeit zugelassenen Medikamenten für die verlaufsmodifizierende Behandlung der schubförmig remittierenden MS (RRMS). Die Multiple Sklerose kann in vier Stadien und Verlaufsformen klassifiziert werden: das klinisch isolierte Syndrom (KIS) die schubförmig remittierende MS (RRMS) die sekundär progrediente MS (SPMS) die primär progrediente MS (PPMS) Das KIS ist häufig das erste Anzeichen einer MS. Bei mehr als 80% der Patienten wird zu Beginn ein schubförmig remittierender Verlauf beobachtet, in dem sich akute neurologische Verschlechterungen mit einer vollständigen oder teilweisen Rückbildung der Symptome und stabilen gesundheitlichen Phasen abwechseln (Abbildung 1) [Wiendl und Kieseier 2010]. Ohne Behandlung treten anfangs jährlich etwa 1,8 Schübe auf, im weiteren Verlauf werden die Schübe dann seltener [Tremlett et al. 2008]. Bei mindestens 50 % der Patienten geht eine unbehandelte MS nach durchschnittlich 10 Jahren in die sekundäre Progredienz über. Nur bei 10 bis 15 % der Patienten wird eine PPMS beobachtet, bei der sich die neuro logischen Symptome von Beginn an ohne Schübe kontinuierlich verschlechtern [DGN / KKNMS 2014]. Bei der PPMS lässt sich im Vergleich zur RRMS relativ häufig kernspintomographisch eine Atrophie des Rückenmarks nachweisen [Bieniek et al. 2006]. Modul 1: MS: Krankheitsaktivität und Schübe 1
2 RRMS: schubförmig remittierend SPMS: sekundär progredient PPMS: primär progedient PPMS: mit aufgesetzten Schüben beispielsweise durch einen chirurgischen Eingriff oder Komorbiditäten, wie weitere immunologische Erkrankungen oder Diabetes mellitus sowie eine Entbindung und die postpartale Phase gehören zu den Triggerfaktoren für Exazerbationen [Djelilovic-Vranic et al. 2012]. Der Einfluss von Stress oder psychisch belastenden Lebensereignissen auf den Verlauf der MS wird kontrovers diskutiert [Nielsen et al. 2014] Krankheitsaktivität, Schub und Magnet resonanz- tomographie (MRT) Zur Evaluierung der MS können die Schubrate, die Behinderungsprogression, MRT-Läsionen und das Ausmaß der Hirnatrophie herangezogen werden. Im klinischen Alltag werden schwere Schübe mit nachfolgender Behinderung, aber auch Schübe mit geringer Symptomatik und rascher Rückbildung beobachtet [Hirst und Robertson 2012]. Eine Unterscheidung zwischen milden und schweren Schüben ist nach Ansicht vieler Experten jedoch nicht sinnvoll, da Schübe jeder Ausprägung auf eine anhaltende MS-Aktivität hinweisen [Hutchinson 2012]. Bei einem Schub handelt es sich um eine klinische Manifestation fokaler Läsionen. Oft repräsentiert er jedoch nur einen kleinen Ausschnitt der Gesamtereignisse, da die neurologischen Symptome eher mit dem Läsionsort im ZNS als mit der Entzündungs aktivität oder der Herdgröße zusammenhängen [Edan 2012]. Zur Beurteilung der MS-Aktivität wird die klinische Evaluierung deshalb durch die MRT ergänzt. Mit diesem Verfahren können sowohl aktive Entzündungsherde als auch klinisch stumme Läsionen bildlich dargestellt werden [DGN / KKNMS 2014] Definition des Schubs 3.4. Schubrate als Studienendpunkt Ein Schub wird als Auftreten neuer oder reaktivierter neurologischer Symptome definiert, die länger als 24 Stunden andauern und nach einem Zeitraum von mindestens 30 Tagen zum Beginn vorausgegangener Schübe auftreten. Zudem sind Schubsymptome nicht durch Änderungen der Körpertemperatur (Uhthoff-Phänomen) oder durch Infektionen erklärbar [DGN / KKNMS 2014]. Die Beachtung dieser Definition ist von großer Bedeutung. Die Anzahl der Schübe innerhalb eines bestimmten Zeitraums ist entscheidend für die Indikation einer verlaufsmodifizierenden Therapie und wird auch zur Beurteilung des Behandlungserfolgs herangezogen [DGN / KKNMS 2014]. Der Schub ist eng mit dem Krankheitsverlauf und der Prognose verknüpft. In Studien wurde beobachtet, dass sich der neurologische Zustand von MS-Patienten nach jedem Schub verschlechterte [Lublin et al. 2003, Weinshenker 1989] und dass neurologische Defizite nach einem ersten Schub mit der Geschwindigkeit der Behinderungsprogression korrelierten [Leray et al. 2010, Confavreux 2003]. In epidemiologischen Untersuchungen prädiktierten häufige Schübe und kurze Abstände zwischen den Schüben innerhalb der ersten 2 bis 5 Erkrankungsjahre eine kürzere Zeit bis zum Eintritt schwerer Behinderungen und bis zum Übergang in eine SPMS [Scalfari et al. 2010, Leray et al. 2010, Confavreux 2003, Lublin et al. 2003]. Mit einer Schubprävention kann die Behinderungsprogression maßgeblich verlangsamt werden. Die Reduzierung der Schubrate wird deshalb in den meisten klinischen Studien als primärer Endpunkt definiert [Fahrbach et al. 2013]. Als weiterer Endpunkt kann die Zeit bis zum nächsten Schub nach einem ersten neurologischen Ereignis dienen [Jacobs et al. 2000]. Abbildung 1: Verlaufsformen der Multiplen Sklerose [Wiendl und Kieseier 2010] 3. Schubrate 3.2. Ursachen / Auslöser Die MS wird durch komplexe Wechselwirkungen genetischer Dispositionen mit Umwelteinflüssen verursacht [ Compston und Coles 2008]. Die fluktuierende Krankheitsaktivität steht mit Veränderungen der Immunaktivität in Zusammen hang [Buljevac et al. 2002]. In Studien wird seit langem ein Zusammen hang zwischen Infektionen vor allem von Atemwegsinfektionen und dem Auftreten von Schüben beobachtet [Djelilovic-Vranic et al. 2012, Buljevac et al. 2002, Panitch 1994]. Aber auch größere körperliche Belastungen, 2
3 In der aktuellen Leitlinie der Deutschen Gesellschaft für Neurologie (DGN) und des Kompetenznetzes Multiple Sklerose (KKNMS) zur Diagnose und Therapie der MS von 2014 wird eine frühzeitige Behandlung mit Interferon-beta-Präparaten oder Glatirameracetat bei der Diagnose empfohlen. Bleibt die Krankheitsaktivität trotz einer Basistherapie bestehen, kann auf intensivere Therapien umgestellt werden. Versagt eine verlaufsmodifizierende Therapie bei milder / moderater Verlaufsform, werden die Patienten wie eine aktive MS behandelt. Bei aktiver und hochaktiver RRMS kann sofort mit wirksameren Medikamenten als First-Line-Therapie begonnen werden (Tabelle 1) [DGN / KKNMS 2014]. Ein aktiver Verlauf ist gekennzeichnet durch zwei funktionell relevante Schübe in den letzten zwei Jahren oder durch einen Schub mit schlechter Remission. Eine rasch fortschreitende hochaktive RRMS liegt vor, wenn im vorangegangenen Jahr mindestens2 Schübe mit Behinderungsprogression aufgetreten sind und im kraniellen MRT mindestens eine Gadolinium anreicherndeläsion oder eine signifikante Zunahme der T2-Läsionen im Vergleich zu einer 6 bis 12 Monate alten MRT nachweisbar sind [DGN / KKNMS 2014]. Im neu gestalteten Stufenschema der MS Therapie (Tabelle 1) wird zwischen milden / moderaten und aktiven oder hochaktiven Verlaufsformen der MS unterschieden. Dies trägt den regulatorischen Entscheidungen Rechnung, die schon früh- Tabelle 1: Stufenschema zur verlaufsmodifizierenden Behandlung der RRMS [modifiziert nach DGN/KKNMS 2014] Indikation Aktive und hochaktive Verlaufsform Die Behandlung der MS beinhaltet das Management der Symptome, die Behandlung des akuten Schubs und eine verlaufsmodifizierende Therapie. Zur Behandlung des akuten Schubs gelten Glukokortikosteroide (intravenös [i.v.] oder oral) als Therapiestandard. Bei funktionell beeinträchtigenden Schüben, die auf eine Hochdosis-Kortisonstoßtherapie nicht ansprechen, kommt die Plasmapherese zum Einsatz [DGN / KKNMS 2014]. Traditionell besteht das wichtigste Ziel der verlaufsmodifizierenden Behandlung in der möglichst langen Verzögerung von Behinderungs entwicklungen [Bergvall et al. 2014, Fahrbach et al. 2013]. Neue Medikamente ermöglichen jetzt jedoch eine wirksame frühzeitige und langfristige Kontrolle der MS-Aktivität, so dass nun immer öfter das Ziel der bestmöglichen Krankheitskontrolle angestrebt wird. In der angelsächsischen Literatur wird hierfür der Begriff No Evidence of Disease Activity (NEDA) benutzt, was übersetzt heißt keine feststellbare Krankheitsaktivität ohne Schübe, ohne Behinderungsprogression und ohne MS-Aktivität im MRT [Bevan und Cree, Fox und Rhoades 2014]. Als weiterer Parameter zur Beurteilung der NEDA wird die Reduzierung der Hirnatrophie in Zukunft sehr wahrscheinlich an Bedeutung gewinnen [De Stefano et al. 2014]. zeitig die Einstellung oder Umstellung von Basis therapien auf aktive Immuntherapeutika ermöglichen [DGN / KKNMS 2014]. Milde / moderate Verlaufsform 4. Behandlungsgrundsätze Therapien 1. Wahl Alemtuzumab Fingolimod Natalizumab 2. Wahl Mitoxantron 3. Wahl Experimentelle Verfahren Dimethylfumarat Glatirameracetat IFN-beta-1a (i.m.) IFN-beta-1a (s.c.) IFN-beta-1b (s.c.) PEG-IFN-beta-1a (s.c.) Teriflunomid i.m. = intramuskulär s.c. = subkutan IFN = Interferon PEG-IFN = pegyliertes Interferon 5. V erlaufsmodifizierende Therapie milde/moderate RRMS Interferon-beta-Präparate und Glatirameracetat haben sich seit mehr als 20 Jahren als wirksame und verträgliche Basis therapeutika erwiesen. Allerdings bleibt die MS unter diesen Substanzen bei bis zu 40 % der Patienten weiterhin aktiv [Tananescu et al. 2014]. Dimethylfumarat und Teriflunomid erweitern das therapeutische Spektrum als neue, oral applizier bare Substanzen mit vergleichbarer Wirksamkeit Glatirameracetat Glatirameracetat wird subkutan (s.c.) appliziert und ist zur Behandlung ambulanter Patienten mit RRMS zugelassen [DGN / KKNMS 2014]. Bei Glatirameracetat handelt es sich um ein synthetisches Polypeptid aus vier Aminosäuren (Glutamin, Lysin, Alanin und Tyrosin), das dem basischen Myelinprotein (BMP) ähnelt und der Demyelinisierung entgegenwirkt. Zu den wichtigsten immunmodulierenden Wirkungen gehört eine Verschiebung des Verhältnisses von proinflammatorischen Typ-1-T-Helferzellen zu antientzündlichen Typ-2-T-Helferzellen [Ziemssen und Schrempf 2007, Zhang et al. 2002]. In einer Zulassungsstudie der Phase-III mit 251 Patienten betrug die jährliche Schubrate 0,59 unter Glatirameracetat und 0,84 unter Plazebo. Somit ergab sich eine Reduzierung um 30 % im Vergleich zu Plazebo [Johnson et al. 1995]. Vergleichbare Ergebnisse wurden in einer Metaanalyse zu drei doppelblinden randomisierten plazebokontrollierten Studien mit 540 Patienten beobachtet. Hier lag die gepoolte Modul 1: MS: Krankheitsaktivität und Schübe 3
4 jährliche Schubrate bei 1,14 unter Plazebo und bei 0,82 unter Glatirameracetat (p = 0,004). Die Reduzierung betrug demnach 28 % [Martinelli Boneschi et al. 2003]. Seit 2015 steht in Deutschland zusätzlich eine neue Formulierung von Glatirameracetat zur Verfügung, die dreimal wöchentlich als 40 mg-dosis appliziert wird. Die verlässliche Wirksamkeit und Verträglichkeit bleiben bestehen, mit dem Vorteil einer niedrigeren Injektionsfrequenz. Glatirameracetat 40 mg reduziert im Vergleich mit Plazebo die jährliche Schubrate um 34% [Khan et al. 2013]. reduzierte sich die jährliche Schubrate entsprechend um 8 % im Vergleich zu Plazebo, und mit Interferon-beta-1b (8 Mio I.E.) um 34 % im Vergleich zu Plazebo. Somit zeigte sich in dieser Untersuchung ein dosisabhängiger Effekt (Abbildung 2) [IFNB 1993]. An der Phase-III-Zulassungsstudie für Peginterferon-beta1a (ADVANCE) nahmen MS-Patienten teil. Mit dem pegylierten Interferon-beta-1a wurde in einem Studienzeitraum von 48 Wochen eine jährliche Schubratenreduktion um 36 % im Vergleich zu Plazebo erreicht (jährliche Schubraten: 0,256 vs. 0,397) [Calabresi et al. 2014] Interferon-beta-1a / Interferon-beta-1b / Peginterferon-beta-1a In einer Phase-III-Zulassungsstudie mit 560 Patienten wurde nach ein und zwei Jahren unter Interferon-beta-1a (22 μg, s.c.) eine Schubrate von durchschnittlich 1,82 beobachtet. Bei höher dosiertem Interferon-beta-1a (44 μg, s.c.) betrug sie 1,73. Unter Plazebo war die Schubrate mit 2,56 signifikant höher (p < 0,005). Somit wurde mit Interferon-beta-1a eine Risikoreduzierung von 27 % bzw. 33 % im Vergleich zu Plazebo erzielt [PRISMS 1998]. Die Wirksamkeit von Interferon-beta-1b wurde in einer randomisierten doppelblinden Phase-III-Zulassungsstudie mit 372 MS-Patienten in zwei Dosierungen im Vergleich zu Plazebo geprüft. Nach zwei Jahren betrug die jährliche Schubrate unter Plazebo 1,27, unter Interferon-beta-1b (1,6 Mio I.E. [ Millionen internationale Einheiten]) 1,17 und unter Inter feron-beta-1b (8 Mio I.E.) 0,84 (Interferon-beta-1b 8 Mio I.E. vs. Plazebo: p = 0,0001; Interferon-beta-1b 1,6 Mio I.E. vs. Plazebo: p=0,0101; Interferon-beta-1b 8 Mio I.E. vs. Interferon-beta-1b 1,6 Mio I.E.: p = 0,0086). Mit Interferon-beta-1b (1,6 Mio I.E.) 4 p = 0,0001 2,0 p = 0,0101 Jährliche Schubrate Auch Interferon-beta-1b (s.c.), Interferon-beta-1a intramuskulär (i.m.) und Interferon-beta-1a (s.c.) sind zur Anwendung bei RRMS zugelassen. Als neue Option steht seit Juli 2014 auch Peginterferon-beta-1a (s.c.) zur Verfügung, das nur alle zwei Wochen appliziert werden muss [EMA 2014]. Bei den Interferon-Präparaten handelt es sich um gentechnisch hergestellte Varianten des körpereigenen Fibroblasteninterferons [DGN / KKNMS 2014]. Die Interferone binden an spezifische Zelloberflächenrezeptoren und lösen eine Signalwegkaskade aus, die eine Sekretion antiviraler, antiproliferativer und immun modulierender Substanzen bewirkt [Dhib-Jalbut 2002]. Da es sich bei den Interferonen um potentiell immunogene Substanzen handelt, kommt es zu einer individuell unterschiedlich ausgeprägten Bildung neutralisierender Antikörper (NAB). Anhaltend hohe NAB-Serumspiegel sind mit einem Wirkungsverlust der Interferonpräparate assoziiert [DGN / KKNMS 2014]. 1,5 1,43 1,27 1,12 1,0 p = 0,0086 1,33 1,17 1,03 0,97 0,84 0,72 0,5 0 Plazebo 1,6 Mio IE 8 Mio IE Abbildung 2: Jährliche Schubraten innerhalb der ersten beiden Behandlungsjahre [IFNB 1993] 5.3. Dimethylfumarat Dimethylfumarat wurde 2014 als Basistherapeutikum zur Be handlung der RRMS zugelassen [DGN / KKNMS 2014]. Der genaue Wirkmechanismus wird derzeit noch erforscht [Ruggieri et al. 2014]. Die Wirksamkeit von Dimethylfumarat zur Reduzierung der Schubrate wurde in den zwei Plazebokon t rollierten Phase-III-Zulassungsstudien DEFINE und CONFIRM nach gewiesen. In beiden Studien erhielten Patienten im Alter von 18 bis 55 Jahren zweimal täglich 240 mg D imethylfumarat (2 x 240 = 480 mg) oder dreimal täglich 240 mg Dimethyl fumarat (3 x 240 = 720 mg) versus Plazebo. In DEFINE war der Anteil der Patienten, die einen Schub erlitten hatten, in beiden Dimethylfumarat-Gruppen signifikant geringer (27 % unter 480 mg; 26 % unter 720 mg) als unter Plazebo (46 %), (p < 0,001 für beide Vergleiche). Die jährliche Schubrate betrug nach zwei Jahren 0,17 unter 480 mg und 0,19 unter 720 mg Dimethylfumarat, während unter Plazebo eine Schubrate von 0,36 beobachtet wurde. Dies entspricht einer relativen Reduzierung der jährlichen Schubrate um 53 % bzw. 48 % im Vergleich zu Plazebo (p < 0,001 für beide Vergleiche) [Gold et al. 2012].
5 In der Studie CONFIRM wurde zusätzlich Glatirameracetat als aktiver Vergleichsarm untersucht. Ein direkter Vergleich von Dimethylfumarat und Glatirameracetat war im Studiendesign jedoch nicht vorgesehen. In CONFIRM waren die jährlichen Schubraten nach zwei Jahren mit 0,22 unter Dimethylfumarat (480 mg), 0,20 unter Dimethylfumarat (720 mg) und 0,29 unter Glatirameracetat signifikant geringer im Vergleich zu Plazebo (0,40). Die relativen Reduzierungen der jährlichen Schubrate lagen bei 44 % unter Dimethylfumarat (480 mg) (p < 0,001), bei 51 % unter Dimethylfumarat (720 mg) (p < 0,001) und bei 29 % unter Glatirameracetat im Vergleich zu Plazebo (p = 0,01) [Fox et al. 2012] Teriflunomid Teriflunomid wurde 2013 zur Behandlung Erwachsener mit RRMS zugelassen. Diese Substanz inhibiert selektiv das Enzym Dihydroorotat-Dehydrogenase, was wiederum zu einer Hemmung der Proliferation aktivierter T- und B-Lymphozyten führt [Bar-Or et al. 2014]. Teriflunomid reduzierte in der dreiarmigen Phase-III-Studie TEMSO mit Patienten in Dosierungen von 7 mg / Tag und 14 mg / Tag in einem Studienzeitraum von 108 Wochen die jährliche Schubrate. Sie betrug 0,54 unter Plazebo und 0,37 unter Teriflunomid (7 oder 14 mg / Tag). Die relative Risikoreduzierung lag bei 31,2 % bzw. 31,5 % im Vergleich zu Plazebo (p < 0,001 für beide Vergleiche) [O Connor et al. 2011]. In die Phase-III-Studie TOWER wurden zwischen 2008 und 2011 insgesamt Patienten eingeschlossen. Die Behandlungsdauer mit Teriflunomid (7 mg / Tag oder 14 mg / Tag) oder Plazebo variierte und endete 48 Wochen nach Rekrutierung des letzten Patienten. Bei Studienende betrug die jährliche Schubrate unter Teriflunomid (14 mg / Tag) 0,32 (p = 0,0001 vs. Plazebo), unter Teriflunomid (7 mg / Tag) 0,39 (p = 0,0183 vs. Plazebo) und unter Plazebo 0,50. Die jährliche Schubrate verringerte sich somit unter Teriflunomid (14 mg / Tag) um 36 % und unter Teriflunomid (7 mg/ Tag) um 22 % im Vergleich zu Plazebo [Confavreux et al. 2014]. In der einfach verblindeten Phase-III-Studie TENERE mit 324 Patienten wurden unter Teriflunomid (14 mg / Tag) und Interferon-beta-1a vergleichbare jährliche Schubraten beobachtet [Vermersch et al. 2014]. 6. Verlaufsmodifizierende Behandlung Aktive und hochaktive RRMS Die folgenden Medikamente haben sich in Studien und im klinischen Alltag als signifikant wirksamer im Vergleich zu den Interferon-beta-Präparaten oder Glatirameracetat erwiesen und werden deshalb zur Therapie der aktiven und hochaktiven MS empfohlen Fingolimod Das oral applizierbare Fingolimod ist für zwei Patientengruppen zugelassen: Als Monotherapie für Patienten, bei denen trotz Behandlung mit mindestens einem Basismedikament eine hohe Krankheitsaktivität vorliegt. Dies sind Patienten, die unter einem Interferon-beta-Präparat, Glatirameracetat, Teri flunomid oder Dimethylfumarat im vorhergehenden Jahr mindestens einen Schub erlitten hatten und mindestens 9 T2-hyperintense Läsionen oder mindestens eine Gadolinium anreichernde Läsion im kraniellen MRT aufweisen. Als First-Line-Monotherapie für Patienten mit rasch fortschreitender hochaktiver RRMS. Bei Fingolimod handelt es sich um einen S phingosin-1phosphat-rezeptor-modulator, der die Freisetzung von Lympho z yten aus den Lymphknoten hemmt [Cohen et al. 2010]. Die Wirksamkeit zur Reduzierung der Schubrate wurde im Vergleich zur Plazebo und zur Standardmedikation mit Interferon-beta-1a (i.m.) nachgewiesen. In der 12-monatigen doppelblinden randomisierten PhaseIII-Studie FREEDOMS erhielten Patienten mit mindestens einem vorherigen Schub einmal täglich oral Fingolimod (0,5 mg), Fingolimod (1,25 mg; nicht zugelassene Dosis) oder Plazebo. Die jährlichen Schubraten betrugen 0,18 unter Fingolimod (0,5 mg), 0,16 unter Fingolimod (1,25 mg; nicht zugelassene Dosis) und 0,40 unter Plazebo (p < 0,001 für beide Dosierungen im Vergleich zu Plazebo). Unter der zugelassenen Dosierung von Fingolimod (0,5 mg) verringerte sich die jährliche Schubrate somit um 54 % im Vergleich zu Plazebo [Kappos et al. 2010]. In der 12-monatigen doppelblinden randomisierten PhaseIII-Studie TRANSFORMS erhielten Patienten mit mindestens einem vorherigen Schub einmal täglich oral Fingolimod (0,5 mg), Fingolimod (1,25 mg; nicht zugelassene Dosierung) oder einmal wöchentlich 30 μg Interferon-beta-1a (i.m.). In den beiden Fingolimod-Gruppen waren die jährlichen Schubraten mit 0,20 (95 %KI 0,16 0,26) unter Fingolimod (1,25 mg; nicht zugelassene Dosis) und 0,16 (95 % KI 0,12 0,21) unter Fingo Modul 1: MS: Krankheitsaktivität und Schübe 5
6 Adjustierte jährliche Schubrate 0,5 0,4 relative Reduzierung p < 0,001 0,3 00,3 0,33 52 % 0,2 0,16 0,1 0 Interferon-beta-1a n = 431 0,20 Fingolimod (0,5 mg) Fingolimod (1,25 mg)* n = 429 n = 420 Abbildung 3: Adjustierte jährliche Schubrate nach einem Behandlungsjahr [modifiziert nach Cohen et al. 2010]. *nicht zugelassene Dosis Mittlerweile liegen für die Wirksamkeit von Fingolimod auch Daten aus dem klinischen Alltag vor. In einer retrospektiven amerikanischen Real-World -Studie wurde der Unterschied der Schubraten nach einem Wechsel von Interferonen auf Fingolimod (132 Patienten) oder auf Glatirameracetat (132 Patienten) untersucht. Vor der Umstellung hatten 33,3 % der Patienten beider Gruppen mindestens einen Schub erlitten. Während der Post-Index-Periode war der Anteil von Patienten mit mindestens einem Schub in der Fingolimod-Gruppe (12,9 %) geringer als in der Glatirameracetat-Gruppe (25,0 %). Die jährliche Schubrate wurde unter Fingolimod (0,19) im Vergleich zu Glatirameracetat (0,51) um 62 % gesenkt [ Bergvall et al. 2014]. In der deutschen Registerstudie Post-Authorization Noninter ventional German safety study of GilEnyA in RRMS patients (PANGAEA) wird seit 2011 die Wirksamkeit und Sicherheit von Fingolimod im klinischen Alltag untersucht. Aus einer Analyse der Patientendaten nach 12 Monaten (n = 2.239) geht hervor, dass die jährliche Schubrate innerhalb eines Behandlungsjahres mit Fingolimod signifikant um 72 % reduziert werden konnte. Die jährliche Schubrate betrug zu Baseline 1,5 und nach einem Jahr 0,4 unabhängig von einer vorherigen Behandlung mit Interferon oder Glatirameracetat. Bei vorheriger Behandlung mit Natalizumab betrug die jährliche Schubrate 1,1 zu Baseline und nach 12 Monaten 0,4. [Ziemssen et al. 2014]. Diese Daten zeigen, dass mit Fingo limod eine wirksame Schubreduktion, unabhängig von einer 6 vorherigen Behandlung, erzielt werden kann Natalizumab Natalizumab wird i.v. appliziert und ist prinzipiell für die gleichen Patientengruppen zugelassen wie Fingolimod. Der humane monoklonale Antikörper Natalizumab hemmt die Migration von Lymphozyten durch die Blut-Hirnschranke über eine Blockierung des Oberflächenadhäsionsmoleküls Alpha4-Integrin [Hoepner et al. 2014]. Allerdings ist Natalizumab mit einem erhöhten Risiko für die Entwicklung einer progressiven multifokalen Leukoenzephalopathie (PML) verbunden. Daher muss vor und während der Behandlung der Serologie-Status des John-Cunningham-Virus (JCV), dem (opportunistischen) Erreger der PML, abgeklärt werden [DGN / KKNMS 2014]. Zudem kommt es im Zusammenhang mit Natalizumab zur Bildung von NAB, welches mit einem Nachlassen der Wirkung verbunden ist und auch mit allergischen Reaktionen einhergehen kann [KBV 2009]. In der Phase-III-Studie AFFIRM erhielten 627 Patienten alle 4 Wochen Natalizumab (300 mg, i.v.), und 315 Patienten erhielten Plazebo (i.v.). Der Studienzeitraum erstreckte sich über mehr als 2 Jahre. Nach einem Jahr hatte Natalizumab die Schubrate um 68 % im Vergleich zu Plazebo reduziert (p < 0,001) [Polman et al. 2006]. In der Phase-III-Studie SENTINEL erhielten Patienten, die zuvor trotz einer Behandlung mit Interferon-beta-1a mindestens einen Schub erlitten hatten, Interferon-beta-1a in Kombination mit Natalizumab (300 mg i.v., 589 Patienten) oder Interferon-beta-1a in Kombination mit Plazebo (i.v., 582 Patienten) alle vier Wochen über einen Zeitraum von bis zu 116 Wochen. Die Kombination war im Vergleich zu Interferon- beta-1a allein nach zwei Jahren mit einer um 55 % niedrigeren jährlichen Schubrate verbunden (jährliche Schubraten: 0,34 vs. 0,75; p < 0,001) (Abbildung 4). Unter Natalizumab kam es zu zwei PML-Fällen, von denen einer tödlich endete [Rudick et al 2006]. 1,0 0,8 Jährliche Schubrate limod (0,5 mg) signifikant niedriger als unter Interferon-beta-1a (Abbildung 3). Hier betrug die jährliche Schubrate 0,33 (95 % KI 0,26 0,42; p < 0,001 für beide Vergleiche). Die jährliche Schubrate konnte unter der zugelassenen Dosis Fingolimod (0,5 mg) im Vergleich zur aktiven Vergleichsmedikation Interferon-beta-1a um 52 % gesenkt werden [Cohen et al. 2010]. 0,75 relative Reduzierung p < 0,001 0,6 55 % 0,4 0,34 0,2 0 Interferon-beta-1a n = 582 Natalizumab n = 589 Abbildung 4: Reduzierung der jährlichen Schubrate nach 2 Jahren [erstellt nach Rudick et al. 2006]
7 Derzeit wird die Wirksamkeit und Sicherheit von Natalizumab im klinischen Alltag im Rahmen der offenen multizentrischen multinationalen Observationsstudie Tysabri observational program (TOP) bei einer Zielpopulation von MS-Patienten in Europa, Kanada und Australien untersucht. Mittlerweile liegen Zwischenergebnisse für 563 belgische Patienten aus dem Zeitraum von 2007 bis 2012 vor. Diese Patientenkohorte war im Vergleich zur Studienpopulation in AFFIRM bei Behandlungsbeginn älter, bereits länger an MS erkrankt, und wies eine höhere jährliche Schubrate auf. Die Wirksamkeit von Natalizumab war dennoch in beiden Studien vergleichbar. In der belgischen Kohorte wurden zwei PML-Fälle diagnostiziert [van Pesch et al. 2014] Alemtuzumab Alemtuzumab (i.v.) ist zur Behandlung der aktiven und hochaktiven RRMS zugelassen [Hersh und Cohen 2014]. Allerdings empfehlen die Leitlinienexperten der DGN / KKNMS, aufgrund der invasiven Wirkungsweise und des Nebenwirkungsprofils in klinischen MS-Studien, bis auf weiteres nur von einer Einsatzmöglichkeit in der erweiterten Eskalationsstufe zur Schubprophylaxe der RRMS auszugehen [DGN / KKNMS 2014]. Der humanisierte monoklonale Antikörper Alemtuzumab bindet an das Leukozyten-Antigen CD52 und induziert darüber eine rasche Depletion der im Blut zirkulierenden B- und T-Lymphozyten [Hersh und Cohen 2014]. In der Phase-III-Zulassungsstudie CARE MS I erhielten zuvor noch nicht behandelte MS-Patienten im Alter zwischen 18 und 50 Jahren über einen Zeitraum von zwei Jahren Alemtuzumab (12 mg / Tag; i.v.) oder Interferon-beta-1a (44 μg / Tag; s.c.). In die Primäranalyse wurden 187 Patienten aus der mit Interferon-beta-1a und 376 Patienten aus der mit Alemtuzumab behandelten Gruppe eingeschlossen. In dieser Studie konnte die jährliche Schubrate mit Alemtuzumab im Vergleich zu Interferon-beta-1a um 54 % gesenkt werden (jährliche Schubraten: 0,18 vs. 0,39), (Abbildung 5) [Cohen et al. 2012]. 0,4 relative Reduzierung Jährliche Schubrate 0,4 0,39 54 % 0,3 0,2 0,18 0,1 0 Interferon-beta-1a n = 187 In die Phase-III-Studie CARE MS II wurden Patienten im Alter zwischen 18 und 50 Jahren eingeschlossen, die zuvor unter Interferon-beta oder Glatirameracetat mindestens einen Schub erlitten hatten. In CARE MS II erhielten die Teilnehmer zwei Jahre lang im Verhältnis 1:2:2 Interferon-beta-1a (44 μg / Tag; s.c.) oder Alemtuzumab (12 mg / Tag; i.v.) oder Alemtuzumab (24 mg / Tag; i.v.; nicht zugelassene Dosis). Die Behandlung mit Alemtuzumab (24 mg / Tag) wurde während des Studienzeitraums abgebrochen. Der Abbruch erfolgte unabhängig von den Wirksamkeits- oder Sicherheitsdaten aufgrund einer Protokolländerung zur Beschleunigung der Patientenrekrutierung für die beiden anderen Gruppen. In die Primäranalyse wurden 202 (87 %) von 231 Patienten der Interferon-beta-1a-Gruppe sowie 426 (98 %) von 436 Patienten eingeschlossen, die Alemtuzumab (12 mg / Tag) erhalten hatten. Die jährlichen Schubraten betrugen 0,52 unter Interferon-beta-1a und 0,26 unter Alemtuzumab. Die Reduzierung der jährlichen Schubrate lag somit bei 50 % [Coles et al. 2012] Mitoxantron Mitoxantron (i.v.) ist seit 2002 zur Eskalationstherapie nicht an den Rollstuhl gebundener MS-Patienten mit progressiv schubförmiger Verlaufsform und anhaltender Krankheits aktivität nach Versagen oder Unverträglichkeit einer immunmodulatorischen Vorbehandlung zugelassen. In der kontrollierten doppelblinden randomisierten Zulassungsstudie erhielten 194 Patienten mit progredienter RRMS oder einer SPMS über 24 Monate alle 3 Monate rando misiert 5 mg / m2 oder 12 mg / m2 Mitoxantron oder Plazebo. Nach zwei Jahren konnten die Daten von 188 Patienten ausge wertet werden. Zu diesem Zeitpunkt wurde unter Mitoxantron (12 mg / m2) eine signifikante Reduzierung der Gesamtzahl behandelter Rückfälle im Vergleich zu Plazebo beobachtet (0,38 [0,18 0,59]; p = 0,0002) [Hartung et al. 2002]. Bei Anwendung von Mitoxantron besteht jedoch ein erhöhtes Risiko für schwere unerwünschte Ereignisse wie Kardiotoxizitäten oder der Entwicklung einer behandlungsbedingten akuten Leu kämie [Cocco und Marrosu 2014]. Die maximal über die Lebenszeit zulässige kumulative Gesamtdosis liegt bei 140 mg / m2 Körperoberfläche. Allerdings sollte eine Applikation über eine Gesamtdosis von 100 mg / m2 Körperoberfläche im Einzelfall unter strenger Nutzen- RisikoAbwägung in Rücksprache mit einem MS-Zentrum erfolgen [DGN / KKNMS 2014]. Alemtuzumab n = 376 Abbildung 5: Reduzierung der jährlichen Schubrate nach 2 Jahren [erstellt nach Cohen et al. 2012] Modul 1: MS: Krankheitsaktivität und Schübe 7
8 7. Fazit 8. Literatur Die MS ist die häufigste neurologische Erkrankung mit Beginn im jungen Erwachsenenalter. Als häufigste Verlaufsform wird die RRMS beobachtet. Häufige Schübe können vor allem in den ersten Erkrankungsjahren mit einer raschen Entwicklung bleibender Behinderungen verbunden sein. Eine frühzeitige verlaufsmodifizierende Behandlung verringert die Schubrate und verbessert die Prognose. Im neu gestalteten Stufenschema der MS-Therapie wird zwischen milden / moderaten und aktiven oder hochaktiven Verlaufsformen der MS unterschieden. Dies trägt den regulatorischen Entscheidungen Rechnung, die schon frühzeitig die Einstellung oder Umstellung von Basistherapien auf aktive Immuntherapeutika ermöglichen [DGN / KKNMS 2014]. Zur verlaufsmodifizierenden Behandlung der milden / moderaten RRMS stehen Interferon-beta-1a (i.m., s.c.), Interferon-beta-1b (s.c.) und Glatirameracetat (s.c.) als altbewährte Medikamente zur Verfügung. Das Spektrum der Interferon-beta-Präparate wurde durch Peginterferon-beta-1a (s.c.) erweitert, das nur alle zwei Wochen appliziert werden muss. Dimethylfumarat und Teriflunomid stehen als neue orale Medikamente für die verlaufsmodifizierende Behandlung der milden / moderaten RRMS zur Verfügung. Zur verlaufsmodifizierenden Behandlung der (trotz Vortherapie) aktiven RRMS haben sich orales Fingolimod und Natalizumab (i.v.) in klinischen Studien und im klinischen Alltag als wirksame und verträgliche Medikamente der ersten Wahl zur Reduzierung der Schubrate erwiesen. Alemtuzumab gehört ebenfalls zu den verlaufsmodifizierenden Medikamenten der ersten Wahl bei (hoch)aktiver RRMS, wird derzeit jedoch als Option in der erweiterten Eskalationsstufe zur Schubprophylaxe bei RRMS empfohlen. Als wichtigstes Behandlungsziel galt bis vor kurzem die Verzögerung der Behinderungsprogression. Mit neuen Medikamenten wie Fingolimod oder Natalizumab erreichte jedoch in Studien ein großer Anteil der Teilnehmer einen klinisch und radiologisch symptomfreien Zustand, so dass immer häufiger die vollständige Krankheitsfreiheit als neues Behandlungsziel und somit eine Verbesserung der Langzeitprognose von MS-Patienten angestrebt wird. In den folgenden CMEModulen wird näher auf die weiteren klinischen und radiologischen Parameter eingegangen. [1.] ar-or A, Pachner A, Menguy-Vacheron F et al. Teriflunomide and its mechanism of B action in multiple sclerosis. Drugs 2014;74: [2.] ergvall N, Makin C, Lahoz R et al. Relapse rates in patients with multiple sclerosis B switching from interferon to fingolimod or glatirameracetat: a US claims database study. PLoS ONE 2014;9(2):e88472 [3.] evan CJ und Cree BAC. Disease activity free status A new endpoint for a new era B in multiple sclerosis. JAMA Neurol 2014;71(3): [4.] B ieniek M, Altmann DR, Davies GR et al. Cord atrophy separates early primary progressive and relapsing remitting multiple sclerosis. J Neurol Neurosurg Psychiatry 2006;77: [5.] uljevac D, Flach HZ, Hop WC et al. Prospective study on the relationship between B infections and multiple sclerosis exacerbations. Brain 2002;125: [6.] alabresi PA, Kieseier BC, Arnold DL et al. Pegylated interferon beta-1a for relapc sing-remitting multiple sclerosis (ADVANCE): a randomised, phase3, double-blind study. Lancet Neurol 2014;13: [7.] occo E und Marrosu MG. The current role of mitoxantrone in the treatment of C multiple sclerosis. Expert Rev Neurother 2014;14(6): [8.] ohen JA, Barkhof F, Comi G et al. Oral fingolimod or intramuscular interferon for C relapsing multiple sclerosis. N Engl J Med 2010;362: [9.] ohen JA, Coles AJ, Arnold LD et al. Alemtuzumab versus interferon beta 1a as firstc line treatment for patients with relapsing-remitting multiple sclerosis: a randomized controlled phase 3 trial. Lancet 2012;380(9856): [10.] C oles AJ, Twyman CL, Arnold LD et al. Alemtuzumab for patients with relapsing multiple sclerosis after disease-modifying therapy: a randomized controlled phase 3 trial. Lancet 2012;380(9856): [11.] C ommittee for Medicinal Products for Human Use (CHMP). European Public Assessment Report (EPAR): Gilenya - Zusammenfassung der Merkmale des Arzneimittels. Fassung vom [12.] Compston A und Coles A. Multiple Sclerosis. Lancet 2008;372: [13.] C onfavreux C, O Connor P, Comi G et al. Oral Teriflunomid for patients with relapsing multiple sclerosis (TOWER): a randomized, double-blind, placebo-controlled, phase 3 trial. Lancet Neurol 2014;13(3): [14.] C onfavreux C, Vukusic S und Adeleine P. Early predictors and progression of irreversible disability in multiple sclerosis: An amnesic process. Brain 2003;126(4): [15.] D e Stefano N, Tomic D, Haering D et al. Proportion of patients with brain volume loss comparable to healthy adults in fingolimod phase 3 multiple sclerosis. Neurology 2014;82:Supplement S [16.] D eutsche Gesellschaft für Neurologie (DGN) und Kompetenznetz Multiple Sklerose (KKNMS). DGN / KKNMS Leitlinie zur Diagnose und Therapie der MS, Online-Version, Stand: [17.] D hib-jalbut Suhayl. Mechanisms of action of interferons and glatiramer acetate in multiple sclerosis. Neurology 2002;58(8 Suppl 4):S3 S9 [18.] D jelilovic-vranic J, Alajbegovic A, Tiric-Campara M et al. Stress as provoking factor for the first and repeated multiple sclerosis seizures. Mater Sociomed 2012;24(3): [19.] E dan G. There is no such thing as a mild MS relapse. The mild relapse is an Anglo-Saxon delusion Yes. Mult Scler 2012;18(7): [20.] E uropean Medicines Agency (EMA). EPAR Product Information, Plegridy -EMEA/H/ C/ IB/0002, Annex 1: Zusammenfassung der Merkmale des Arzneimittels, Fassung vom [21.] F ahrbach KF, Huelin R, Lartin AL et al. Relating relapse and T2 lesion changes to disability progression in multiple sclerosis: a systematic literature review and regression analysis. BMC Neurol 2013;13:180. doi: / [22.] F ox EJ und Rhoades RW. New treatments and treatment goals for patients with relapsing-remitting multiple sclerosis. Curr Opin Neurol 2012;Suppl:S11 9 [23.] F ox RJ, Miller DH, Hutchinson M et al. Placebo-controlled phase 3 study of oral BG-12 or glatiramer in multiple sclerosis. N Engl J Med 2012;367(12): [24.] G old R, Kappos L, Arnold DL et al. Placebo-controlled phase 3 study of oral BG-12 for relapsing multiple sclerosis. N Engl J Med 2012;367(12): [25.] H artung HP, Gonsette R, König N et al. Mitoxantrone in progressive multiple sclerosis: a placebo-controlled, double-blind, randomised, multicentre trial. Lancet 2002;360 (9350): [26.] H ersh CM und Cohen JA. Alemtuzumab for the treatment of relapsing-remitting multiple sclerosis. Immunotherapy 2014;6(3): [27.] H irst CL und Robertson NP. There is no such thing as a mild MS relapse. The mild relapse is an Anglo-Saxon delusion Commentary. Mult Scler 2012;18(7): [28.] H oepner R,Faissner S, Salmen A et al. Efficacy and side effects of natalizumab therapy in patients with multiple sclerosis. J Cent Nerv Sys Dis 2014;6:41 49 [29.] H utchinson M. There is no such thing as a mild MS relapse. The mild relapse is an Anglo-Saxon delusion Commentary. Mult Scler 2012;18(7): [30.] I FNB Multiple Sclerosis Study Group. Interferon beta-1b is effective in relapsing-remitting multiple sclerosis. I. Clinical results of a multicenter, randomized, double-blind, placebo-controlled trial. Neurol 1993;43(4):
9 [31.] J acobs DL, Beck RW, Simon JH et al. Intramuscular interferon beta-1a therapy initiated during a first demyelinating event in multiple sclerosis. N Engl J Med 2000;343: [32.] J ohnson KP, Brooks BR, Cohen JA et al. Copolymer 1 reduces relapse rate and improves disability in relapsing remitting multiple sclerosis: results of a phase III multicenter, double-blind placebo-controlled trial. Neurol 1995;45(7): [33.] K appos L, Radue EW, O Connor P et al. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis. N Engl J Med 2010;362: [34.] K assenärztliche Bundesvereinigung (KBV): Beschluss des gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie in Anlage 4: Therapiehinweis zu Natalizumab. Deutsches Ärzteblatt PP 2009;6: [35.] Khan O, Rieckmann P, Boyko A, et al. Three times weekly glatiramer acetate in relapsing-remitting multiple sclerosis. Ann Neurol 2013;73(6): [36.] K och-henriksen N und Sorensen PS. The changing demographic pattern of multiple sclerosis epidemiology. Lancet Neurol 2010;9: [37.] L eray E, Yaouanq J, Le Page E et al. Evidence for a two-stage diability progression in multiple sclerosis. Brain 2010;133(7): [38.] L ublin FD, Baier M und Cutter G. Effect of relapses on development of residual deficit in multiple sclerosis. Neurol 2003;61: [39.] M artinelli Boneschi F, Rovaris M, Johnson KP et al. Effects of glatiramer acetate on relapse rate and accumulated disability in multiple sclerosis: meta-analysis of three double-blind, randomized, placebo-controlled clinical trials. Multiple Sclerosis 2003;9: [40.] N ielsen NM, Bager P, Simonsen J et al. Major stressful life events in adulthood and risk of multiple sclerosis. J Neurol Neurosurg Psychiatry 2014;85(10): [41.] O Connor P, Wolinsky JS, Confavreux C et al. Randomized trial of oral teriflunomid for relapsing multiple sclerosis. N Engl J Med 2011;325: [42.] P anitch HS. Influence of infection on exacerbations of multiple sclerosis. Ann Neurol 1994;36:Suppl:S25 8 [43.] P etersen G, Wittmann R, Arndt V et al. Epidemiologie der Multiplen Sklerose in Deutschland. Regionale Unterschiede und Versorgungsstruktur in Abrechnungsdaten der gesetzlichen Krankenversicherung. Nervenarzt 2014;85: [44.] P olman CH, O Connor P, Havrdova E et al. A randomized, placebo-controlled trial of natalizumab for relapsing multiple sclerosis. N Engl J Med 2006;354: [45.] P RISMS Study Group. Randomised double blind placebo-controlled study of interferon beta-1a in relapsing/remitting multiple sclerosis. PRISM (Prevention of Relapses and Disability by Interferon beta-1a Subcutaneously in Multiple Sclerosis) study group. Lancet 1998;352: [46.] R udick RA, Stuart WH, Calabresi PA et al. Natalizumab plus interferon beta-1a for relapsing multiple sclerosis. N Engl J Med 2006;354: [47.] R uggieri S, Tortorelle C und Gasperini C. Pharmacology and clinical efficacy of dimethyl fumarate (BG-12) for treatment of relapsing-remitting multiple sclerosis. Ther Clin Risk Manag 2014;10: [48.] S calfari A, Neuhaus A, Degenhardt A et al. The natural history of multiple sclerosis, a geographically based study 10: Relapses and long-term disability. Brain 2010;133(7): [49.] T ananescu R, Ionete C, Chuo IJ et al. Advances in the treatment of relapsing-remitting multiple sclerosis. Biomed J 2014;37:41 49 [50.] T remlett H, Zhao Y, Joseph J et al. Relapses in multiple sclerosis are age and timedependent. J Neurol Neurosurg Psychiatry 2008;79: [51.] V an Pesch V, Bartholomé E, Bissay V et al. Safety and efficacy of natalizumab in belgian multiple sclerosis patients: subgroup analysis of the natalizumab observational program. Acta Neurol Belg 2014; 114(3): [52.] V ermersch P, Czlonkowska A, Grimaldi LM et al. Teriflunomide versus subcutaneous interferon beta-1a in patients with relapsing multiple sclerosis: a randomised, controlled phase 3 trial. Mult Scler 2014;20(6): [53.] W einshenker BG, Bass B, Rice GP et al. The natural history of multiple sclerosis: a geographically based study. 2. Predictive value of the early clinical course. Brain 1989;112: [54.] W iendl H und Kieseier BC. Multiple Sklerose Klinik, Diagnostik und Therapie. In: Brand TH, Hohlfeld R, Noth J, Reichmann H (Hrsg.). Klinische Neurologie, W. Kohlhammer Verlag, Stuttgart, 2010 [55.] Z hang J, Hutton G und Zang Y. A comparison of the mechanisms of action of interferon beta and glatiramer acetate in the treatment of multiple sclerosis. Clin Ther 2000;24(12): [56.] Z iemssen T, Diaz-Lorente M, Fuchs A et al. 24-month interim results of PANGAEA: a 5-year registry study evaluating long-term safety, efficacy and pharmaoeconomic data of german multiple sclerosis patients on fingolimod therapy. Annual Meeting, American Academy of Neurology (AAN) 2014;P3.152 [57.] Z iemssen T und Schrempf W. Glatiramer acetate: mechanism of action in multiple sclerosis. Int Rev Neurobiol 2007;79: Modul 1: MS: Krankheitsaktivität und Schübe 9
10 Lernkontrollfragen Bitte kreuzen Sie jeweils nur eine Antwort an. 1. Welche Aussage zur Epidemiologie der Multiplen Sklerose (MS) ist falsch? a) b) c) d) e) Die MS ist die häufigste chronisch entzündliche Erkrankung des ZNS bei jungen Erwachsenen. Sie manifestiert sich meist in einem Alter zwischen 25 und 40 Jahren. Männer sind etwa dreimal öfter betroffen als Frauen. Die MS verläuft meist schubförmig remittierend. Die Erkrankung führt bei vielen Patienten zu bleibender Behinderung und Frühverrentung. 2. Welche Aussage ist richtig? Die Anzahl der MS-Patienten beträgt in Deutschland derzeit etwa a) b) c) d) e) Welche Aussage zum klinischen Bild und zum Krankheitsverlauf ist falsch? a) Die MS ist mit einer Demyelinisierung der Nerven und mit Axonschädigungen verbunden. b) Da die Erkrankung das gesamte ZNS betrifft, ist das klinische Bild sehr einheitlich. c) Erstes Anzeichen der MS ist häufig ein klinisch isoliertes Syndrom (KIS). d) Bei mehr als 80% der Patienten wird zu Beginn ein schubförmig remittierender Verlauf beobachtet. e) Bei mindestens 50% der Patienten geht eine unbehandelte MS nach etwa 10 Jahren in die sekundäre Progredienz über. 4. Welche Aussage zur Definition oder den Ursachen des Schubs ist richtig? a) Der Schub wird definiert als Auftreten neuer oder reaktivierter neurologischer Symptome, die länger als 72 Stunden andauern. b) Neue oder reaktivierte neurologische Symptome müssen nach einem Zeitraum von mindestens 20 Tagen zum Beginn vorausgegangener Schübe auftreten. c) Die Schubsymptome sind durch Veränderungen der Körpertemperatur erklärbar. d) Die Anzahl der Schübe in einem bestimmten Zeitraum wird zur Beurteilung eines Behandlungserfolgs herangezogen. e) Die fluktuierende Krankheitsaktivität steht nicht mit der Immunaktivität in Zusammenhang. 5. Welche Aussage zur Krankheitsaktivität oder zur Schubrate ist falsch? a) In der Schubsymptomatik wird das neurologische Gesamtgeschehen deutlich. b) Der Schub ist eng mit dem Krankheitsverlauf und der Prognose verknüpft. c) Häufige Schübe und kurze Abstände zwischen zwei Schüben innerhalb der ersten 2 bis 5 Jahre prädiktieren einen frühzeitigen Eintritt schwerer Behinderungen. d) Mit der Schubprävention kann die Behinderungsprogression maßgeblich verlangsamt werden. e) Die Reduzierung der Schubrate wird in den meisten Studien als primärer Endpunkt definiert. 10
11 6. Welche Aussage zu den Behandlungsgrundsätzen ist falsch? a) Die Behandlung der MS beinhaltet das Management der Symptome, die Behandlung des akuten Schubs und eine verlaufsmodifizierende Therapie. b) Traditionell besteht das wichtigste Ziel der verlaufsmodifizierenden Behandlung in der möglichst langen Verzögerung der Behinderung. c) Als neues Behandlungsziel wird immer öfter ein Zustand ohne Schübe, ohne Behinderungsprogression und ohne MS-Aktivität im MRT angestrebt. d) Die Hirnatrophie spielt für die Beurteilung der Krankheitsaktivität keine Rolle. e) In der aktuellen Leitlinie der DGN/KKMNS wird eine frühzeitige Behandlung mit Interferon-beta-Präparaten oder Glatirameracetat bei der Diagnose empfohlen. 7. Welcher Wirkstoff gilt bei der aktiven und hochaktiven Verlaufsform der RRMS als Therapieoption der 1.Wahl? a) Interferon-beta-1a b) Interferon-beta 1b c) Mitoxantron d) Dimethylfumarat e) Fingolimod 8. Welche Aussage zur Therapie der milden / moderaten RRMS ist richtig? a) Unter Interferon-beta oder Glatirameracetat bleibt die MS bei bis zu 40% der Patienten weiterhin aktiv. b) Dimethylfumarat und Teriflunomid stehen als neue subkutan applizierbare Alternativen zur Behandlung der milden / moderaten RRMS zur Verfügung. c) Mit Glatirameracetat kann die Schubrate im Vergleich zu Plazebo um etwa 50% gesenkt werden. d) Das neue Peginterferon-beta-1a hat den Vorteil, dass es oral appliziert werden kann. e) In der Zulassungsstudie zu Interferon-beta-1b wurde eine dosisunabhängige Wirksamkeit im Hinblick auf die Reduzierung der Schubrate beobachtet. 9. Welche Aussage zu Fingolimod oder Natalizumab ist falsch? a) Fingolimod wird oral appliziert. b) Fingolimod und Natalizumab sind für Patienten zugelassen, bei denen trotz einer Basistherapie eine hohe Krankheitsaktivität vorliegt. c) Fingolimod und Natalizumab sind als First-Line-Monotherapie für Patienten mit rasch fortschreitender aktiver RRMS zugelassen. d) Natalizumab ist ein Sphingosin-1-Phosphat-Rezeptor-Modulator. e) Bei der Anwendung von Natalizumab besteht ein erhöhtes Risiko für die Entwicklung einer progressiven multifokalen Leukoenzephalopathie (PML). 10. Welche Aussage zu Alemtuzumab oder Mitoxantron ist richtig? a) Alemtuzumab wird subkutan verabreicht. b) Alemtuzumab induziert eine rasche Depletion der im Blut zirkulierenden B- und T-Lymphozyten. c) Mit Alemtuzumab konnte in Studien die Schubrate in vergleichbarer Größenordnung zu Interferon-beta-1a gesenkt werden. d) Mitoxantron ist mit einem günstigen Nebenwirkungsprofil verbunden. e) Die maximal über die Lebenszeit zulässige kumulative Gesamtdosis von Mitoxantron liegt bei 200 mg / m2 Körper fläche. Modul 1: MS: Krankheitsaktivität und Schübe 11
12 12
13 Auswertung der Lernerfolgskontrolle Modul 1: MS: Krankheitsaktivität und Schübe VNR: Gültigkeitsdauer: Vergabe eines Teilnahme-Zertifikates der Landesärztekammer Bayern: Ab 7 richtig beantworteten Fragen erhalten Sie 2 Fortbildungspunkte. Fax-Nr Außendienst-Stempel Bitte die Angaben zur Person leserlich ausfüllen: EFN bzw. Barcode Aufkleber EFN-Nummer eintragen oder Aufkleber aufkleben Frau: a b c d e Herr: 4 Titel, Vorname, Name 5 Straße, Hausnummer 6 7 PLZ, Ort Erklärung: Ich versichere, dass ich die Beantwortung der Fragen selbstständig und ohne fremde Hilfe durchgeführt habe. Der Zustellung der Teilnahmebescheinigung durch den Sponsor stimme ich zu Ort / Datum Unterschrift Zusätzliche Daten (Angabe ist freiwillig): niedergelassener Arzt angestellt - Klinik angestellt - sonstiger Arbeitgeber Fachgebiet: Arztstempel Datenschutz: Ihre Daten werden ausschließlich für die Auswertung der Antworten verwendet. Es erfolgt keine Speicherung der Ergebnisse über die für die Bearbeitung der Fortbildungseinheit notwendige Zeit hinaus. Namens- und Adressangaben dienen nur dem Versand der Teilnahmebescheinigungen. CME medipoint, Tel: / info@cme-medipoint.de
14 14
15 Evaluation der Fortbildung Modul 1: MS: Krankheitsaktivität und Schübe Diese Fortbildung wurde durch die bayrische Landesärztekammer für den Erwerb des Fortbildungszertifikates anerkannt. Bitte tragen Sie zur Qualitätssicherung der Fortbildung durch die Rückgabe des ausgefüllten Evaluationsbogens an den Veranstalter bei. Die Beantwortung der Evaluation ist freiwillig. Fax-Nr Bitte bewerten Sie nach dem Schulnoten-System (1 = ja, sehr, 6 = gar nicht) A) Meine Erwartungen hinsichtlich der Fortbildung haben sich erfüllt. B) Während des Durcharbeitens habe ich fachlich gelernt. C) Der Text hat Relevanz für meine praktische Tätigkeit. D) Die Didaktik, die Eingängigkeit und die Qualität des Textes sind sehr gut. E) Der Aufwand für die Bearbeitung hat sich (zeitlich und organisatorisch) gelohnt. F) In der Fortbildung wurde die Firmen- und Produktneutralität gewahrt. G) Diese Form der Fortbildung möchte ich auch zukünftig erhalten: H) Meine Fortbildungen verteilen sich prozentual wie folgt: ja nein % Präsenzveranstaltungen % digitale Fortbildung (Online, CD) % schriftliche Fortbildungen I) Wurden aus der Sicht Ihrer täglichen Praxis heraus wichtige Aspekte der Thematik nicht erwähnt? ja nein Wenn ja, welche? zu knapp abgehandelt? ja nein Wenn ja, welche? überbewertet? ja nein Wenn ja, welche? J) Welche Wünsche bleiben für künftige Fortbildungen offen? Vielen Dank für Ihre Mitarbeit! CME medipoint, Tel: / info@cme-medipoint.de
Multiple Sklerose. Modul 1: MS: Krankheitsaktivität und Schübe. 1. Einleitung. 2. Klinisches Bild und Verlaufsformen
 Multiple Sklerose Modul 1: MS: Krankheitsaktivität und Schübe Prof. Dr. med. Tjalf Ziemssen, Neurologische Universitätsklinik Dresden VNR: 2760909007178480012 Gültigkeitsdauer: 29.05.2017 29.05.2018 1.
Multiple Sklerose Modul 1: MS: Krankheitsaktivität und Schübe Prof. Dr. med. Tjalf Ziemssen, Neurologische Universitätsklinik Dresden VNR: 2760909007178480012 Gültigkeitsdauer: 29.05.2017 29.05.2018 1.
Sklerose verlangsamen
 Weniger Schübe, mehr Lebensqualität Frühe Basistherapie kann Krankheitsverlauf der Multiplen Sklerose verlangsamen Hamburg (12. September 2008) - Die Frühtherapie der Multiplen Sklerose war eines der relevanten
Weniger Schübe, mehr Lebensqualität Frühe Basistherapie kann Krankheitsverlauf der Multiplen Sklerose verlangsamen Hamburg (12. September 2008) - Die Frühtherapie der Multiplen Sklerose war eines der relevanten
Multiple Sklerose. Modul 1: MS: Krankheitsaktivität und Schübe. 2. Klinisches Bild und Verlaufsformen. 1. Einleitung
 Multiple Sklerose Modul 1: MS: Krankheitsaktivität und Schübe Prof. Dr. med. Tjalf Ziemssen, Neurologische Universitätsklinik Dresden VNR: 2760909005554650018 Gültigkeitsdauer: 01.02.2015 01.02.2016 1.
Multiple Sklerose Modul 1: MS: Krankheitsaktivität und Schübe Prof. Dr. med. Tjalf Ziemssen, Neurologische Universitätsklinik Dresden VNR: 2760909005554650018 Gültigkeitsdauer: 01.02.2015 01.02.2016 1.
Daten und Fakten: Therapie der Multiplen Sklerose mit Tysabri
 Hintergrundtext Fachmedien Daten und Fakten: Therapie der Multiplen Sklerose mit Tysabri Natalizumab Zulassung und Indikation Natalizumab (Tysabri ) ist der erste alpha-4-integrin-antagonist zur Behandlung
Hintergrundtext Fachmedien Daten und Fakten: Therapie der Multiplen Sklerose mit Tysabri Natalizumab Zulassung und Indikation Natalizumab (Tysabri ) ist der erste alpha-4-integrin-antagonist zur Behandlung
IMMUNTHERAPIE 2017 JETZT AUCH BEI CHRONISCHER MS? Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg
 IMMUNTHERAPIE JETZT AUCH BEI CHRONISCHER MS? Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg MS Therapie H. Houston Merritt The surest way to lose a reputation in neurology is
IMMUNTHERAPIE JETZT AUCH BEI CHRONISCHER MS? Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg MS Therapie H. Houston Merritt The surest way to lose a reputation in neurology is
Multiple Sklerose Modul 2: MS: Krankheitsaktivität und Behinderungsprogression
 Multiple Sklerose Modul 2: MS: Krankheitsaktivität und Behinderungsprogression Prof. Dr. Mathias Mäurer, Chefarzt der Klinik für Neurologie, Stiftung Juliusspital Würzburg VNR: 2760909006939360018 Gültigkeitsdauer:
Multiple Sklerose Modul 2: MS: Krankheitsaktivität und Behinderungsprogression Prof. Dr. Mathias Mäurer, Chefarzt der Klinik für Neurologie, Stiftung Juliusspital Würzburg VNR: 2760909006939360018 Gültigkeitsdauer:
Willkommen zum 4. Lüdenscheider Tag der MS
 Willkommen zum 4. Lüdenscheider Tag der MS Update 2012 Therapieoptionen bei MS Referent: Dr. med. Sebastian Schimrigk Lüdenscheid, den 11. Februar 2012 Was sind die Behandlungsziele? 1. Ordnung: Verhinderung
Willkommen zum 4. Lüdenscheider Tag der MS Update 2012 Therapieoptionen bei MS Referent: Dr. med. Sebastian Schimrigk Lüdenscheid, den 11. Februar 2012 Was sind die Behandlungsziele? 1. Ordnung: Verhinderung
remittierender Multipler Sklerose
 PLEGRIDY : Erstes pegyliertes Interferon alle 2 Wochen s.c. für erwachsene Patienten mit schubförmig r PLEGRIDY Erstes pegyliertes Interferon alle 2 Wochen s.c. für erwachsene Patienten mit schubförmig
PLEGRIDY : Erstes pegyliertes Interferon alle 2 Wochen s.c. für erwachsene Patienten mit schubförmig r PLEGRIDY Erstes pegyliertes Interferon alle 2 Wochen s.c. für erwachsene Patienten mit schubförmig
Wirksamkeit und Sicherheit
 Multiple Sklerose: Novartis Fingolimod (Gilenya ) zeigt in Registerstudien über fünf Jahre anhaltend hoh Multiple Sklerose Novartis Fingolimod (Gilenya ) zeigt in Registerstudien über fünf Jahre anhaltend
Multiple Sklerose: Novartis Fingolimod (Gilenya ) zeigt in Registerstudien über fünf Jahre anhaltend hoh Multiple Sklerose Novartis Fingolimod (Gilenya ) zeigt in Registerstudien über fünf Jahre anhaltend
Dr. med. Edeltraud Faßhauer, Deutsche Multiple Sklerose Gesellschaft Bundesverband e. V. Hannover
 Dr. med. Edeltraud Faßhauer, Deutsche Multiple Sklerose Gesellschaft Bundesverband e. V. Hannover Schnelligkeit oder Sicherheit: Was erwarten Patientinnen und Patienten von der Arzneimittelzulassung? 2
Dr. med. Edeltraud Faßhauer, Deutsche Multiple Sklerose Gesellschaft Bundesverband e. V. Hannover Schnelligkeit oder Sicherheit: Was erwarten Patientinnen und Patienten von der Arzneimittelzulassung? 2
Tecfidera bei schubförmig remittierender MS
 Kongress der Deutschen Gesellschaft für Neurologie (DGN): Neue Praxisdaten untermauern Stellenwert v Kongress der Deutschen Gesellschaft für Neurologie (DGN) Neue Praxisdaten untermauern Stellenwert von
Kongress der Deutschen Gesellschaft für Neurologie (DGN): Neue Praxisdaten untermauern Stellenwert v Kongress der Deutschen Gesellschaft für Neurologie (DGN) Neue Praxisdaten untermauern Stellenwert von
MS-Therapie mit Fingolimod (Gilenya ): Rechtzeitig wirksam behandeln und patientenbezogen optimieren
 MS-Therapie mit Fingolimod (Gilenya ) Rechtzeitig wirksam behandeln und patientenbezogen optimieren - Mild-moderater vs. (hoch)aktiver Verlauf: Entscheidend sind die langfristige Entwicklung der Krankheitsaktivität
MS-Therapie mit Fingolimod (Gilenya ) Rechtzeitig wirksam behandeln und patientenbezogen optimieren - Mild-moderater vs. (hoch)aktiver Verlauf: Entscheidend sind die langfristige Entwicklung der Krankheitsaktivität
Aktuelles zur Therapie der MS
 KLINIKEN LANDKREIS SIGMARINGEN GmbH AKADEMISCHES LEHRKRANKENHAUS DER UNIVERSITÄT TÜBINGEN Aktuelles zur Therapie der MS PD Dr. med. Oliver Neuhaus Chefarzt Abteilung Neurologie Was ist Multiple Sklerose?
KLINIKEN LANDKREIS SIGMARINGEN GmbH AKADEMISCHES LEHRKRANKENHAUS DER UNIVERSITÄT TÜBINGEN Aktuelles zur Therapie der MS PD Dr. med. Oliver Neuhaus Chefarzt Abteilung Neurologie Was ist Multiple Sklerose?
Neue Therapien in der MS
 Neue Therapien in der MS Prof. Dr. Heinz Wiendl Direktor Klinik für Allg. Neurologie Westfälische Wilhelms-Universität Münster Diese Veranstaltung wurde unterstützt von: -Biogen Idec -TEVA Pharma MS: Therapiesituationen
Neue Therapien in der MS Prof. Dr. Heinz Wiendl Direktor Klinik für Allg. Neurologie Westfälische Wilhelms-Universität Münster Diese Veranstaltung wurde unterstützt von: -Biogen Idec -TEVA Pharma MS: Therapiesituationen
Neue Medikamente bei der progredienten MS. Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg
 Neue Medikamente bei der progredienten MS Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg Progrediente MS Formen der progredienten MS SPMS PPMS sekundär chronisch >> primär chronisch
Neue Medikamente bei der progredienten MS Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg Progrediente MS Formen der progredienten MS SPMS PPMS sekundär chronisch >> primär chronisch
... was ist am Horizont?
 Neue Medikamente bei der Multiplen Sklerose... was ist am Horizont? Alexander Schwarz MS-Patiententag 2017 Agenda - B-Zelldepletion (Ocrelizumab / Ofatumumab) - Cladribin - Siponimod - Biotin (Vitamin
Neue Medikamente bei der Multiplen Sklerose... was ist am Horizont? Alexander Schwarz MS-Patiententag 2017 Agenda - B-Zelldepletion (Ocrelizumab / Ofatumumab) - Cladribin - Siponimod - Biotin (Vitamin
Multiple Sklerose. PD Dr. Ch. Kamm. Department of Neurology
 Multiple Sklerose PD Dr. Ch. Kamm Department of Neurology Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung Degeneration
Multiple Sklerose PD Dr. Ch. Kamm Department of Neurology Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung Degeneration
Daclizumab (Zinbryta ): Neues Wirkprinzip bei schubförmiger Multipler Sklerose (RMS)
 Presseinformation Daclizumab (Zinbryta ): Neues Wirkprinzip bei schubförmiger Multipler Sklerose (RMS) München/Ismaning, 8. September 2016 Mit der Zulassung von Daclizumab (Zinbryta ) steht eine neue,
Presseinformation Daclizumab (Zinbryta ): Neues Wirkprinzip bei schubförmiger Multipler Sklerose (RMS) München/Ismaning, 8. September 2016 Mit der Zulassung von Daclizumab (Zinbryta ) steht eine neue,
Fatigue, Gleichgewichtsstörungen und Kognitionsstörungen1. - Gilenya (Fingolimod) überzeugt in aktuellen Studien-Analysen
 Gilenya (Fingolimod) bei Multipler Sklerose (MS) Sichtbare Symptome kontrollieren unsichtbare Symptome adressieren - Aktuelle Umfrage: MS-Patienten am meisten belastet durch Fatigue, Gleichgewichtsstörungen
Gilenya (Fingolimod) bei Multipler Sklerose (MS) Sichtbare Symptome kontrollieren unsichtbare Symptome adressieren - Aktuelle Umfrage: MS-Patienten am meisten belastet durch Fatigue, Gleichgewichtsstörungen
Multiple Sklerose. PD Dr. med. Ch. Kamm
 Multiple Sklerose PD Dr. med. Ch. Kamm Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung Degeneration Krankheitsbeginn
Multiple Sklerose PD Dr. med. Ch. Kamm Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung Degeneration Krankheitsbeginn
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar?
 Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Themen: Übersicht der MS-Immuntherapeutika Off label Medikamente Welche Medikamtente bei welcher Patientensituation?
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Themen: Übersicht der MS-Immuntherapeutika Off label Medikamente Welche Medikamtente bei welcher Patientensituation?
Neue, orale Therapieoption zur Basistherapie der schubförmigen Multiplen Sklerose
 TECFIDERA (Dimethylfumarat) Neue, orale Therapieoption zur Basistherapie der schubförmigen Multiplen Sklerose München (28. Februar 2014) - Die Forschung zur Therapie der schubförmigremittierenden Multiplen
TECFIDERA (Dimethylfumarat) Neue, orale Therapieoption zur Basistherapie der schubförmigen Multiplen Sklerose München (28. Februar 2014) - Die Forschung zur Therapie der schubförmigremittierenden Multiplen
Zwei Studien bestätigen Wirksamkeit der Fumarsäure gegen MS
 Sichere Tablette in Aussicht Zwei Studien bestätigen Wirksamkeit der Fumarsäure gegen MS Berlin (20. September 2012) - Ein weiterer Meilenstein auf dem Weg zu einer Multiple-Sklerose-Tablette ohne gefährliche
Sichere Tablette in Aussicht Zwei Studien bestätigen Wirksamkeit der Fumarsäure gegen MS Berlin (20. September 2012) - Ein weiterer Meilenstein auf dem Weg zu einer Multiple-Sklerose-Tablette ohne gefährliche
Multiple Sklerose Modul 2: MS: Krankheitsaktivität und Behinderungsprogression
 Multiple Sklerose Modul 2: MS: Krankheitsaktivität und Behinderungsprogression Prof. Dr. Mathias Mäurer, Klinik für Neurologie, Caritas Krankenhaus Bad Mergentheim VNR: 2760909005947760011 Gültigkeitsdauer:
Multiple Sklerose Modul 2: MS: Krankheitsaktivität und Behinderungsprogression Prof. Dr. Mathias Mäurer, Klinik für Neurologie, Caritas Krankenhaus Bad Mergentheim VNR: 2760909005947760011 Gültigkeitsdauer:
Behandlung der Multiplen Sklerose durch Inhibition von Adhäsionsmolek. sionsmolekülen len. Dr. Martin Berghoff
 Behandlung der Multiplen Sklerose durch Inhibition von Adhäsionsmolek sionsmolekülen len Dr. Martin Berghoff Immunmodulierende Basistherapie (1) Interferon-β (IFN-β)1b (Betaferon) und 1a (Rebif / Avonex)
Behandlung der Multiplen Sklerose durch Inhibition von Adhäsionsmolek sionsmolekülen len Dr. Martin Berghoff Immunmodulierende Basistherapie (1) Interferon-β (IFN-β)1b (Betaferon) und 1a (Rebif / Avonex)
Medienmitteilung. Basel, den 20. Oktober Ocrelizumab wird in den laufenden Phase-III-Studien in zwei Formen von MS untersucht
 Medienmitteilung Basel, den 20. Oktober 2011 Phase-II-Studie mit ocrelizumab zeigt eine fast zwei Jahre anhaltende deutliche Reduktion der Krankheitsaktivität bei Patienten mit multipler Sklerose Ocrelizumab
Medienmitteilung Basel, den 20. Oktober 2011 Phase-II-Studie mit ocrelizumab zeigt eine fast zwei Jahre anhaltende deutliche Reduktion der Krankheitsaktivität bei Patienten mit multipler Sklerose Ocrelizumab
Zugelassene Medikamente bei der Multiplen Sklerose: Was gibt es Neues?
 Zugelassene Medikamente bei der Multiplen Sklerose: Was gibt es Neues? Prof. Dr. med. Ricarda Diem Neurologische Klinik Universitätsklinikum Heidelberg *NEDA = no evidence of disease activity Therapie
Zugelassene Medikamente bei der Multiplen Sklerose: Was gibt es Neues? Prof. Dr. med. Ricarda Diem Neurologische Klinik Universitätsklinikum Heidelberg *NEDA = no evidence of disease activity Therapie
Merck beantragt Zulassung in den USA für Cladribin-Tabletten als mögliche orale Kurzzeitbehandlung der Multiplen Sklerose
 Merck beantragt Zulassung in den USA für Cladribin-Tabletten als mögliche orale Kurzzeitbehandlung der Multiplen Sklerose Darmstadt (30. September 2009) - Die Merck KGaA hat heute bekannt gegeben, dass
Merck beantragt Zulassung in den USA für Cladribin-Tabletten als mögliche orale Kurzzeitbehandlung der Multiplen Sklerose Darmstadt (30. September 2009) - Die Merck KGaA hat heute bekannt gegeben, dass
Multiple Sklerose. PD Dr. med. Ch. Kamm. Department of Neurology
 Multiple Sklerose PD Dr. med. Ch. Kamm Department of Neurology Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung Degeneration
Multiple Sklerose PD Dr. med. Ch. Kamm Department of Neurology Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung Degeneration
Neue Daten zu Tysabri und Avonex belegen anhaltende Wirksamkeit
 Neue Daten zu Tysabri und Avonex belegen anhaltende Wirksamkeit Berlin (23. September 2008) Neue Daten belegen, dass Tysabri (Natalizumab) die Krankheitsaktivität der Multiplen Sklerose modulieren kann.
Neue Daten zu Tysabri und Avonex belegen anhaltende Wirksamkeit Berlin (23. September 2008) Neue Daten belegen, dass Tysabri (Natalizumab) die Krankheitsaktivität der Multiplen Sklerose modulieren kann.
Multiple Sklerose - Forschung
 Multiple Sklerose - Forschung Dr. Ch. Kamm Department of Neurology Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung
Multiple Sklerose - Forschung Dr. Ch. Kamm Department of Neurology Multiple Sklerose = Chronisch-entzündliche Erkrankung des Zentralen Nervensystems (=Autoimmunerkrankung) Entzündung / Demyelinisierung
Projekte: Erkrankungen des Nervensystems
 Literaturrecherchen für GKV-Preisverhandlungen in einer neurologischen Indikation Andere Literaturrecherchen für GKV-Preisverhandlungen Fallzahl: 0 Preparation of a study protocol in post-stroke arm spasticity
Literaturrecherchen für GKV-Preisverhandlungen in einer neurologischen Indikation Andere Literaturrecherchen für GKV-Preisverhandlungen Fallzahl: 0 Preparation of a study protocol in post-stroke arm spasticity
Multiple Sklerose Aktuelle Behandlungskonzepte. Matthias Bußmeyer Klinik für Neurologie und klinische Neurophysiologie 26.01.2013
 Multiple Sklerose Aktuelle Behandlungskonzepte Matthias Bußmeyer Klinik für Neurologie und klinische Neurophysiologie 26.01.2013 1 Säulen der MS-Therapie Therapie der Multiplen Sklerose Schubtherapie Krankheitsmodifizierende
Multiple Sklerose Aktuelle Behandlungskonzepte Matthias Bußmeyer Klinik für Neurologie und klinische Neurophysiologie 26.01.2013 1 Säulen der MS-Therapie Therapie der Multiplen Sklerose Schubtherapie Krankheitsmodifizierende
Orale MS Therapien. Ralf Gold Neurologische Klinik St. Josef Hospital, Klinikum der Ruhr-Universität Bochum
 rale MS Therapien Ralf Gold Neurologische Klinik St. Josef Hospital, Klinikum der Ruhr-Universität Bochum Was entwickelt sich in der Pipeline? Neue MS Therapie wird riskant..! rale Therapeutika: welche
rale MS Therapien Ralf Gold Neurologische Klinik St. Josef Hospital, Klinikum der Ruhr-Universität Bochum Was entwickelt sich in der Pipeline? Neue MS Therapie wird riskant..! rale Therapeutika: welche
Dossierbewertung A18-06 Version 1.0 Ocrelizumab (multiple Sklerose)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ocrelizumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ocrelizumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgt auf Basis eines
Behandlung der Multiplen Sklerose Betaferon (Interferon ß-1b) Tradition mit Zukunft
 Behandlung der Multiplen Sklerose Betaferon (Interferon ß-1b) Tradition mit Zukunft Nürnberg (24. September 2009) Bei der Diagnostik und Therapie der Multiplen Sklerose gibt es Fortschritte auf mehreren
Behandlung der Multiplen Sklerose Betaferon (Interferon ß-1b) Tradition mit Zukunft Nürnberg (24. September 2009) Bei der Diagnostik und Therapie der Multiplen Sklerose gibt es Fortschritte auf mehreren
Fampyra Verbesserung der Gehfähigkeit von Patienten mit Multipler Sklerose
 Fampyra Verbesserung der Gehfähigkeit von Patienten mit Multipler Sklerose Wiesbaden (29. September 2011) - Fampridin (Fampyra ) ist seit Juli dieses Jahres zur Behandlung von erwachsenen Patienten mit
Fampyra Verbesserung der Gehfähigkeit von Patienten mit Multipler Sklerose Wiesbaden (29. September 2011) - Fampridin (Fampyra ) ist seit Juli dieses Jahres zur Behandlung von erwachsenen Patienten mit
MS Basistherapie: Noch aktuell? Was sagen die Langzeitstudien über 20 Jahre? Ms katte Pat FB 2014 1
 MS Basistherapie: Noch aktuell? Was sagen die Langzeitstudien über 20 Jahre? Ms katte Pat FB 2014 1 Die MS-Therapie auf einen Blick Therapieswitsch Mitoxantron * Tysabri (Natalizumab) Gilenya (Fingolimod)
MS Basistherapie: Noch aktuell? Was sagen die Langzeitstudien über 20 Jahre? Ms katte Pat FB 2014 1 Die MS-Therapie auf einen Blick Therapieswitsch Mitoxantron * Tysabri (Natalizumab) Gilenya (Fingolimod)
Multiple Sklerose: Ocrelizumab bremst Krankheitsprogression zu jedem Zeitpunkt der Erkrankung
 DGN-Kongress 2017: Multiple Sklerose: Ocrelizumab bremst Krankheitsprogression zu jedem Zeitpunkt d DGN-Kongress 2017 Multiple Sklerose: Ocrelizumab bremst Krankheitsprogression zu jedem Zeitpunkt der
DGN-Kongress 2017: Multiple Sklerose: Ocrelizumab bremst Krankheitsprogression zu jedem Zeitpunkt d DGN-Kongress 2017 Multiple Sklerose: Ocrelizumab bremst Krankheitsprogression zu jedem Zeitpunkt der
Multiple Sklerose. Priv.-Doz. Dr. med. Zaza Katsarava Oberarzt Neurologische Universitätsklinik Essen
 Multiple Sklerose Priv.-Doz. Dr. med. Zaza Katsarava Oberarzt Neurologische Universitätsklinik Essen Multiple Sklerose Epidemiologie Prävalenz: 0,3-0,7 / 1000 Einwohner Alter: 20.-40. Lebensjahr; unter
Multiple Sklerose Priv.-Doz. Dr. med. Zaza Katsarava Oberarzt Neurologische Universitätsklinik Essen Multiple Sklerose Epidemiologie Prävalenz: 0,3-0,7 / 1000 Einwohner Alter: 20.-40. Lebensjahr; unter
Multiple Sklerose DIE KRANKHEIT MIT TAUSEND GESICHTERN
 Multiple Sklerose DIE KRANKHEIT MIT TAUSEND GESICHTERN DAMARIS WALLMEROTH JACQUELIN KASEMIR 25.07.2017 1 Inhaltsverzeichnis Myelinscheide Ionenkanäle am Axon Definition Multiple Sklerose (MS) Krankheitsbild
Multiple Sklerose DIE KRANKHEIT MIT TAUSEND GESICHTERN DAMARIS WALLMEROTH JACQUELIN KASEMIR 25.07.2017 1 Inhaltsverzeichnis Myelinscheide Ionenkanäle am Axon Definition Multiple Sklerose (MS) Krankheitsbild
Was die neuen MS-Therapien leisten können
 Multiple Sklerose Was die neuen MS-Therapien leisten können Durch die aktuellen medikamentösen Neuentwicklungen werden die therapeutischen Möglichkeiten der Multiplen Sklerose (MS) erheblich erweitert.
Multiple Sklerose Was die neuen MS-Therapien leisten können Durch die aktuellen medikamentösen Neuentwicklungen werden die therapeutischen Möglichkeiten der Multiplen Sklerose (MS) erheblich erweitert.
Cladribin (multiple Sklerose)
 IQWiG-Berichte Nr. 600 Cladribin (multiple Sklerose) Nutzenbewertung gemäß 35a SGB V Dossierbewertung Auftrag: A17-62 Version: 1.0 Stand: 27.02.2018 Impressum Herausgeber: Institut für Qualität und Wirtschaftlichkeit
IQWiG-Berichte Nr. 600 Cladribin (multiple Sklerose) Nutzenbewertung gemäß 35a SGB V Dossierbewertung Auftrag: A17-62 Version: 1.0 Stand: 27.02.2018 Impressum Herausgeber: Institut für Qualität und Wirtschaftlichkeit
zum Beschluss des Gemeinsamen Bundesausschusses zur Änderung der Arzneimittel-Richtlinie (AM-RL) Anlage IV: Therapiehinweis zu Alemtuzumab
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses zur Änderung der Arzneimittel-Richtlinie (AM-RL) Anlage IV: Therapiehinweis zu Vom 15. September 2016 Inhalt 1. Rechtsgrundlage... 2 2. Eckpunkte
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses zur Änderung der Arzneimittel-Richtlinie (AM-RL) Anlage IV: Therapiehinweis zu Vom 15. September 2016 Inhalt 1. Rechtsgrundlage... 2 2. Eckpunkte
Medienmitteilung. Basel, 26. April 2017
 Medienmitteilung Basel, 26. April 2017 Neue Daten auf der AAN-Tagung bestätigen den klinischen Nutzen von OCREVUS (Ocrelizumab) von Roche bei schubförmiger und primär progredienter multipler Sklerose Anzeichen
Medienmitteilung Basel, 26. April 2017 Neue Daten auf der AAN-Tagung bestätigen den klinischen Nutzen von OCREVUS (Ocrelizumab) von Roche bei schubförmiger und primär progredienter multipler Sklerose Anzeichen
Aktuelles therapeutisches Vorgehen bei Multipler Sklerose. Dr. J. Gößling Vortrag Bremen
 Aktuelles therapeutisches Vorgehen bei Multipler Sklerose Ebenen der Behandlung der MS Akute Behandlung der Schübe Dauerhafte Immunmodulation/ - suppression Basistherapie Eskalationstherapie Symptomatische
Aktuelles therapeutisches Vorgehen bei Multipler Sklerose Ebenen der Behandlung der MS Akute Behandlung der Schübe Dauerhafte Immunmodulation/ - suppression Basistherapie Eskalationstherapie Symptomatische
Vom 17. Januar I. Die Anlage 4 wird um den folgenden Therapiehinweis ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über die Einleitung eines Stellungnahmeverfahrens zur Änderung der Arzneimittel-Richtlinie in Anlage 4: Therapiehinweis zu Natalizumab Vom 17. Januar 2008 Der
Beschluss des Gemeinsamen Bundesausschusses über die Einleitung eines Stellungnahmeverfahrens zur Änderung der Arzneimittel-Richtlinie in Anlage 4: Therapiehinweis zu Natalizumab Vom 17. Januar 2008 Der
Neue Wege in der Therapie der Multiplen Sklerose. Diagnose MS: Grundprinzip. Klinische Diagnose. Unterstützung
 Neue Wege in der Therapie der Multiplen Sklerose Diagnose MS: Grundprinzip II. Herbsttagung Herz-Hirn-Stoffwechsel Schkopau, 05.11.2016 Prof. Dr. F. Then Bergh Multiple Sklerose, sofern keine andere Ursache
Neue Wege in der Therapie der Multiplen Sklerose Diagnose MS: Grundprinzip II. Herbsttagung Herz-Hirn-Stoffwechsel Schkopau, 05.11.2016 Prof. Dr. F. Then Bergh Multiple Sklerose, sofern keine andere Ursache
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar?
 Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Themen: Übersicht der MS-Immuntherapeutika Off label Medikamente Welche Medikamtente bei welcher Patientensituation?
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Themen: Übersicht der MS-Immuntherapeutika Off label Medikamente Welche Medikamtente bei welcher Patientensituation?
Rezidivprophylaxe bei schubförmig-remittierender Multipler Sklerose mit Cladribin oder Fingolimod
 AMB 2010, 44, 41 Rezidivprophylaxe bei schubförmig-remittierender Multipler Sklerose mit Cladribin oder Fingolimod Zusamenfassung: Die Bewertung von Nutzen und Risiken der lang erwarteten oralen Wirkstoffe
AMB 2010, 44, 41 Rezidivprophylaxe bei schubförmig-remittierender Multipler Sklerose mit Cladribin oder Fingolimod Zusamenfassung: Die Bewertung von Nutzen und Risiken der lang erwarteten oralen Wirkstoffe
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben?
 Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
Haben Sie externe Hilfestellungen in Anspruch genommen? Wenn ja, bitte geben Sie an, welche Hilfestellung Sie in Anspruch genommen haben? 1.1 Angefragte Untersuchungs- und Behandlungsmethode (Kurzbezeichnung
NEUE BEHANDLUNGSMÖGLICHKEITEN MONOKLONALE ANTIKÖRPER
 NEUE BEHANDLUNGSMÖGLICHKEITEN MONOKLONALE ANTIKÖRPER Was sind Antikörper? Antikörper patrouillieren wie Wächter im Blutkreislauf des Körpers und achten auf Krankheitserreger wie Bakterien, Viren und Parasiten
NEUE BEHANDLUNGSMÖGLICHKEITEN MONOKLONALE ANTIKÖRPER Was sind Antikörper? Antikörper patrouillieren wie Wächter im Blutkreislauf des Körpers und achten auf Krankheitserreger wie Bakterien, Viren und Parasiten
Projects: Nervous system disorders
 Literaturrecherchen für GKV-Preisverhandlungen in einer neurologischen Indikation Other Sample size: 0 Literature research for reimbursement negotiations with health insurances Preparation of a study protocol
Literaturrecherchen für GKV-Preisverhandlungen in einer neurologischen Indikation Other Sample size: 0 Literature research for reimbursement negotiations with health insurances Preparation of a study protocol
Pressemitteilung. 8. September 2017
 Ihr Ansprechpartner Erin-Marie Beals +49 151 1454 2694 8. September 2017 Mavenclad (Cladribin-Tabletten) erzielt bei oraler Verabreichung an maximal 20 Tagen eine bis zu vier Jahre anhaltende klinische
Ihr Ansprechpartner Erin-Marie Beals +49 151 1454 2694 8. September 2017 Mavenclad (Cladribin-Tabletten) erzielt bei oraler Verabreichung an maximal 20 Tagen eine bis zu vier Jahre anhaltende klinische
MS-Versorgung eine Herausforderung für die Pharmaindustrie? Birgit Fischer, 24. Juni 2014
 MS-Versorgung eine Herausforderung für die Pharmaindustrie? Birgit Fischer, 24. Juni 2014 Patientenwünsche Quelle: http://www.dmsg.de/wunschwand/ Seite 2 MS-Therapie, aktueller Stand ca. 120.000 Patientinnen
MS-Versorgung eine Herausforderung für die Pharmaindustrie? Birgit Fischer, 24. Juni 2014 Patientenwünsche Quelle: http://www.dmsg.de/wunschwand/ Seite 2 MS-Therapie, aktueller Stand ca. 120.000 Patientinnen
Was kann man erwarten?
 Neue Therapien der Multiplen Sklerose Was kann man erwarten? Prim. Univ.-Doz. Dr. Christian Eggers Neurologie mit Stroke Unit Krankenhaus der Barmherzigen Brüder Linz Derzeitige Medikamente in der Behandlung
Neue Therapien der Multiplen Sklerose Was kann man erwarten? Prim. Univ.-Doz. Dr. Christian Eggers Neurologie mit Stroke Unit Krankenhaus der Barmherzigen Brüder Linz Derzeitige Medikamente in der Behandlung
[_], [_] [_][_]. [_][_]. 20[_][_] (TT).(MM).JJJJ
![[_], [_] [_][_]. [_][_]. 20[_][_] (TT).(MM).JJJJ [_], [_] [_][_]. [_][_]. 20[_][_] (TT).(MM).JJJJ](/thumbs/68/58188402.jpg) Erfassungsdatum Dokumentierende Person Pseudonym Patienten Name Patienten Vorname Soziodemografische Daten Gab es Änderungen in den soziodemografischen Daten des Patienten? (Hochzeit, Schulabschluss, Ausbildung,
Erfassungsdatum Dokumentierende Person Pseudonym Patienten Name Patienten Vorname Soziodemografische Daten Gab es Änderungen in den soziodemografischen Daten des Patienten? (Hochzeit, Schulabschluss, Ausbildung,
Neue diagnostische Kriterien. Warum früh diagnostizieren? Wie sicher! - diagnostizieren?
 Neue diagnostische Kriterien Warum früh diagnostizieren? Wie sicher! - diagnostizieren? MS-Forum Buchholz 14.Juni 2008 Warum Früh? chronische Erkrankung bleibende Behinderungen Berufsunfähigkeit Psychische
Neue diagnostische Kriterien Warum früh diagnostizieren? Wie sicher! - diagnostizieren? MS-Forum Buchholz 14.Juni 2008 Warum Früh? chronische Erkrankung bleibende Behinderungen Berufsunfähigkeit Psychische
date Adjuvant Pegylated- Interferonalpha2b
 Organ/Bereich Krankheit Stadium Kurztitel Studie/ClinicalTrials.gov Identifier: Stand per: 11.05.2016 Hauttumore Melanom ulzeriertes primäres kutanes Melanom T(2-4)b N0 M0) Hauttumore Melanom nicht vorbehandeltes,
Organ/Bereich Krankheit Stadium Kurztitel Studie/ClinicalTrials.gov Identifier: Stand per: 11.05.2016 Hauttumore Melanom ulzeriertes primäres kutanes Melanom T(2-4)b N0 M0) Hauttumore Melanom nicht vorbehandeltes,
Fampyra : Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfüg
 Fampyra : Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfüg Fampyra Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfügbar
Fampyra : Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfüg Fampyra Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfügbar
Fampyra : Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfüg
 Fampyra : Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfüg Fampyra Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfügbar
Fampyra : Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfüg Fampyra Erstes Medikament zur Verbesserung der Gehfähigkeit bei Multipler Sklerose ab sofort verfügbar
Personalisierte Therapie von Multiple Sklerose entscheidet über Behandlungserfolg
 ENS 2013 Personalisierte Therapie von Multiple Sklerose entscheidet über Behandlungserfolg Barcelona, Spanien (10. Juni 2013) Trotz zahlreicher neuer Behandlungsoptionen lässt sich Multiple Sklerose immer
ENS 2013 Personalisierte Therapie von Multiple Sklerose entscheidet über Behandlungserfolg Barcelona, Spanien (10. Juni 2013) Trotz zahlreicher neuer Behandlungsoptionen lässt sich Multiple Sklerose immer
Multiple Sklerose ( Encephalomyelitis disseminata)
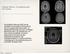 Multiple Sklerose ( Encephalomyelitis disseminata) Die Multiple Sklerose (MS) ist die häufigste neurologische Erkrankung, die im jungenerwachsenenalter zu bleibender Behinderung und vorzeitiger Berentung
Multiple Sklerose ( Encephalomyelitis disseminata) Die Multiple Sklerose (MS) ist die häufigste neurologische Erkrankung, die im jungenerwachsenenalter zu bleibender Behinderung und vorzeitiger Berentung
Therapie der Multiplen Sklerose
 Therapie der Multiplen Sklerose Teil 1: Update zu derzeit zugelassenen Präparaten Matthias Mehling, Urs Pohlman, Ludwig Kappos Neurologische Klinik und Poliklinik und Departement Biomedizin, Universitätsspital,
Therapie der Multiplen Sklerose Teil 1: Update zu derzeit zugelassenen Präparaten Matthias Mehling, Urs Pohlman, Ludwig Kappos Neurologische Klinik und Poliklinik und Departement Biomedizin, Universitätsspital,
Multiple Sklerose. Modul 3: MS: Krankheitsaktivität und Hirnatrophie
 Multiple Sklerose Modul 3: MS: Krankheitsaktivität und Hirnatrophie Prof. Dr. Sven Schippling, UniversitätsSpital Zürich* Dr. Roland Opfer, UniversitätsSpital Zürich und jung diagnostics GmbH Hamburg *wissenschaftlicher
Multiple Sklerose Modul 3: MS: Krankheitsaktivität und Hirnatrophie Prof. Dr. Sven Schippling, UniversitätsSpital Zürich* Dr. Roland Opfer, UniversitätsSpital Zürich und jung diagnostics GmbH Hamburg *wissenschaftlicher
FORMULAR FÜR DEN START DER BEHANDLUNG MIT TYSABRI
 Die europäischen Gesundheitsbehörden haben für die Markteinführung von TYSABRI Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information gehört - ist
Die europäischen Gesundheitsbehörden haben für die Markteinführung von TYSABRI Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information gehört - ist
Wie gut sind die Immuntherapiestudien bei Multipler Sklerose?
 Wie gut sind die Immuntherapiestudien bei Multipler Sklerose? C. Heesen MS-Tagesklinik, INIMS Universitätsklinikum Hamburg Eppendorf Vortrag DGN 21.9.2016 Die finnische FINGER-Studie: Zukunft der MS-Welt?
Wie gut sind die Immuntherapiestudien bei Multipler Sklerose? C. Heesen MS-Tagesklinik, INIMS Universitätsklinikum Hamburg Eppendorf Vortrag DGN 21.9.2016 Die finnische FINGER-Studie: Zukunft der MS-Welt?
Projekte: Erkrankungen der Haut und des Unterhautzellgewebes
 Monitoring services for one country for a multi-country registry in chronic urticaria Preparation of a CRF for a registry in chronic urticaria Development of a Clinical Study Protocol, Master PIC and CRF
Monitoring services for one country for a multi-country registry in chronic urticaria Preparation of a CRF for a registry in chronic urticaria Development of a Clinical Study Protocol, Master PIC and CRF
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome
 Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar?
 Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Dr. med. Jutta Scheiderbauer Seit den 1990er Jahren hat sich etabliert, die schubförmige Multiple Sklerose (MS) mit
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Dr. med. Jutta Scheiderbauer Seit den 1990er Jahren hat sich etabliert, die schubförmige Multiple Sklerose (MS) mit
Autoimmunerkrankung Erkrankung, bei der sich das Immunsystem gegen körpereigenes Gewebe richtet.
 Glossar Adhärenz Therapietreue: Konsequentes Einhalten der Therapie. Autoimmunerkrankung Erkrankung, bei der sich das Immunsystem gegen körpereigenes Gewebe richtet. Axon Fortsatz einer Nervenzelle, der
Glossar Adhärenz Therapietreue: Konsequentes Einhalten der Therapie. Autoimmunerkrankung Erkrankung, bei der sich das Immunsystem gegen körpereigenes Gewebe richtet. Axon Fortsatz einer Nervenzelle, der
Mitteilung an die Medien
 Mitteilung an die Medien Basel, 10. November 2017 OCREVUS (Ocrelizumab) von Roche erhält positives Gutachten des CHMP für schubförmige multiple Sklerose und primär progrediente multiple Sklerose Im Falle
Mitteilung an die Medien Basel, 10. November 2017 OCREVUS (Ocrelizumab) von Roche erhält positives Gutachten des CHMP für schubförmige multiple Sklerose und primär progrediente multiple Sklerose Im Falle
BAnz AT B7. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
PROBASE: Große deutsche Studie zum Prostatakrebs-Screening. PROBASE Große deutsche Studie zum Prostatakrebs-Screening
 PROBASE Große deutsche Studie zum Prostatakrebs-Screening Dresden (27. September 2013) Ziel der PROBASE-Studie (Risk-adapted prostate cancer early detection study based on a baseline PSA value in young
PROBASE Große deutsche Studie zum Prostatakrebs-Screening Dresden (27. September 2013) Ziel der PROBASE-Studie (Risk-adapted prostate cancer early detection study based on a baseline PSA value in young
Bedeutung von MAO-B-Hemmern
 DGN-Kongress 2014: Rasagilin verlässlicher Therapiepartner im Krankheitsverlauf Individuelle Konzepte in der Parkinson-Therapie: Bedeutung von MAO-B-Hemmern München (17. September 2014) - Wie kann der
DGN-Kongress 2014: Rasagilin verlässlicher Therapiepartner im Krankheitsverlauf Individuelle Konzepte in der Parkinson-Therapie: Bedeutung von MAO-B-Hemmern München (17. September 2014) - Wie kann der
Neues zur Therapie der Multiplen Sklerose
 Neues zur Therapie der Multiplen Sklerose Prof. Dr. Luisa Klotz Department für Neurologie Klinik für Allgemeine Neurologie Westfälische Wilhelms-Universität Münster Gliederung Substanzen für aktive Verlaufsformen
Neues zur Therapie der Multiplen Sklerose Prof. Dr. Luisa Klotz Department für Neurologie Klinik für Allgemeine Neurologie Westfälische Wilhelms-Universität Münster Gliederung Substanzen für aktive Verlaufsformen
Dimethylfumarat (Tecfidera) bei Multipler Sklerose
 verstehen abwägen entscheiden Dimethylfumarat (Tecfidera) bei Multipler Sklerose Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) Inhaltsverzeichnis Überblick Einleitung Anwendung
verstehen abwägen entscheiden Dimethylfumarat (Tecfidera) bei Multipler Sklerose Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) Inhaltsverzeichnis Überblick Einleitung Anwendung
Risiken der modernen MS Therapie wie müssen wir die Behandlung überwachen? PD Dr. Luisa Klotz
 Risiken der modernen MS Therapie wie müssen wir die Behandlung überwachen? PD Dr. Luisa Klotz Therapiealgorithmus Multiple Sklerose Schubtherapie CIS1 RRMS1 1. Wahl: - Alemtuzumab - Fingolimod - Natalizumab
Risiken der modernen MS Therapie wie müssen wir die Behandlung überwachen? PD Dr. Luisa Klotz Therapiealgorithmus Multiple Sklerose Schubtherapie CIS1 RRMS1 1. Wahl: - Alemtuzumab - Fingolimod - Natalizumab
DAUER DER STUDIE: Läuft seit Nov mindestens bis 2017.
 KLINISCHE STUDIE: Swiss Inflammatory Bowel Disease Cohort Study (SIBDCS) Multizentrische Beobachtungsstudie in der ganzen Schweiz (Basel, Bern, Genf, Lausanne, St-Gallen, Zürich) mit Patient die an einem
KLINISCHE STUDIE: Swiss Inflammatory Bowel Disease Cohort Study (SIBDCS) Multizentrische Beobachtungsstudie in der ganzen Schweiz (Basel, Bern, Genf, Lausanne, St-Gallen, Zürich) mit Patient die an einem
MS Therapie: Qual der Wahl?!
 MS Therapie: Qual der Wahl?! Prof. Dr. med. Mathias Mäurer Caritas Krankenhaus Bad Mergentheim Relapse therapy I mmunomodifying therapy Mild/ moderat disease course (Highly-) active course Therapieoptionen
MS Therapie: Qual der Wahl?! Prof. Dr. med. Mathias Mäurer Caritas Krankenhaus Bad Mergentheim Relapse therapy I mmunomodifying therapy Mild/ moderat disease course (Highly-) active course Therapieoptionen
Mitteilung an die Medien
 Mitteilung an die Medien Basel, 28. September 2017 OCREVUS (Ocrelizumab) von Roche in der Schweiz für primär progrediente und schubförmige multiple Sklerose zugelassen OCREVUS ist das erste und einzige
Mitteilung an die Medien Basel, 28. September 2017 OCREVUS (Ocrelizumab) von Roche in der Schweiz für primär progrediente und schubförmige multiple Sklerose zugelassen OCREVUS ist das erste und einzige
Schlaf 2015 Im Rahmen der MS Therapie
 Schlaf 2015 Im Rahmen der MS Therapie Schlafstörungen Vor und während der MS Behandlung Dr. med. Christoph Schenk Arzt für Neurologie und Psychiatrie Arzt für Psychotherapeutische Medizin Schlafmedizin,
Schlaf 2015 Im Rahmen der MS Therapie Schlafstörungen Vor und während der MS Behandlung Dr. med. Christoph Schenk Arzt für Neurologie und Psychiatrie Arzt für Psychotherapeutische Medizin Schlafmedizin,
Das 1 X 1 der MS Dr. H. Assar
 Das 1 X 1 der MS Dr. H. Assar 23.01.2018 1 Multiple Sklerose (MS) ist eine autoimmun mediierte, entzündliche, chronische Erkrankung, welche viele (multiple) Stellen im Zentralnervensystem befällt und zu
Das 1 X 1 der MS Dr. H. Assar 23.01.2018 1 Multiple Sklerose (MS) ist eine autoimmun mediierte, entzündliche, chronische Erkrankung, welche viele (multiple) Stellen im Zentralnervensystem befällt und zu
Journal: Journal of Clinical Oncology Publikationsjahr: 2012 Autoren: Paulo M. Hoff, Andreas Hochhaus, Bernhard C. Pestalozzi et al.
 Cediranib Plus FOLFOX/CAPOX Versus Placebo Plus FOLFOX/CAPOX in Patients With Previously Untreated Metastatic Colorectal Cancer: A Randomized, Double Blind, Phase III Study (HORIZON II) Journal: Journal
Cediranib Plus FOLFOX/CAPOX Versus Placebo Plus FOLFOX/CAPOX in Patients With Previously Untreated Metastatic Colorectal Cancer: A Randomized, Double Blind, Phase III Study (HORIZON II) Journal: Journal
Anlage III - Vorlage zur Abgabe einer schriftlichen Stellungnahme zur Nutzenbewertung nach 35a SGB V
 Anlage III - Vorlage zur Abgabe einer schriftlichen Stellungnahme zur Nutzenbewertung nach 35a SGB V Datum 23.01.2014 Stellungnahme zu Teriflunomid, Nr. 202, A13-38, Version 1.0, 20.12.2013 Stellungnahme
Anlage III - Vorlage zur Abgabe einer schriftlichen Stellungnahme zur Nutzenbewertung nach 35a SGB V Datum 23.01.2014 Stellungnahme zu Teriflunomid, Nr. 202, A13-38, Version 1.0, 20.12.2013 Stellungnahme
Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV
 Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV Von Dr. med. Markus Rupp, MSD SHARP & DOHME GMBH, Haar München (20. September 2008) Der World-Aids-Report
Integrase-Hemmung mit ISENTRESS : Eine neue Klasse antiretroviraler Wirkstoffe zur Behandlung von HIV Von Dr. med. Markus Rupp, MSD SHARP & DOHME GMBH, Haar München (20. September 2008) Der World-Aids-Report
Medienmitteilung. Basel 12. Januar 2018
 Medienmitteilung Basel 12. Januar 2018 OCREVUS (Ocrelizumab) von Roche erhält Zulassung in der Europäischen Union für schubförmige multiple Sklerose und primär progrediente multiple Sklerose Erstes und
Medienmitteilung Basel 12. Januar 2018 OCREVUS (Ocrelizumab) von Roche erhält Zulassung in der Europäischen Union für schubförmige multiple Sklerose und primär progrediente multiple Sklerose Erstes und
Antrag auf Aufhebung der Verschreibungspflicht ( 48 und 53 AMG) Racecadotril 30 mg Granulat zur sympt. Behandlung der akuten Diarrhoe bei Kindern ab
 Antrag auf Aufhebung der Verschreibungspflicht ( 48 und 53 AMG) Racecadotril 30 mg Granulat zur sympt. Behandlung der akuten Diarrhoe bei Kindern ab 5 Jahren und Jugendlichen Voraussetzungen für Selbstmedikation
Antrag auf Aufhebung der Verschreibungspflicht ( 48 und 53 AMG) Racecadotril 30 mg Granulat zur sympt. Behandlung der akuten Diarrhoe bei Kindern ab 5 Jahren und Jugendlichen Voraussetzungen für Selbstmedikation
ICLUSIG erweitert die Therapieoptionen der Chronischen Myeloischen Leukämie und der Philadelphia-C
 ICLUSIG erweitert die Therapieoptionen der Chronischen Myeloischen Leukämie und der Philadelphia-C ICLUSIG erweitert die Therapieoptionen der Chronischen Myeloischen Leukämie und der Philadelphia-Chromosom
ICLUSIG erweitert die Therapieoptionen der Chronischen Myeloischen Leukämie und der Philadelphia-C ICLUSIG erweitert die Therapieoptionen der Chronischen Myeloischen Leukämie und der Philadelphia-Chromosom
MS 10 Fragen und Antworten
 Hintergrundinformation MS 10 Fragen und Antworten Was ist MS? Multiple Sklerose (MS) ist eine chronische Erkrankung des Zentralen Nervensystems (ZNS), d.h. des Gehirns und des Rückenmarks. Bei der MS handelt
Hintergrundinformation MS 10 Fragen und Antworten Was ist MS? Multiple Sklerose (MS) ist eine chronische Erkrankung des Zentralen Nervensystems (ZNS), d.h. des Gehirns und des Rückenmarks. Bei der MS handelt
Fingolimod (neues Anwendungsgebiet)
 IQWiG-Berichte Nr. 245 Fingolimod (neues Anwendungsgebiet) Nutzenbewertung gemäß 35a SGB V Dossierbewertung Auftrag: A14-21 Version: 1.0 Stand: 26.09.2014 Impressum Herausgeber: Institut für Qualität und
IQWiG-Berichte Nr. 245 Fingolimod (neues Anwendungsgebiet) Nutzenbewertung gemäß 35a SGB V Dossierbewertung Auftrag: A14-21 Version: 1.0 Stand: 26.09.2014 Impressum Herausgeber: Institut für Qualität und
KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse
 Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
kolorektalen Karzinoms
 Signifikante Lebensverlängerung durch Angiogenese-Hemmung Avastin in der First-Line-Therapie des metastasierten kolorektalen Karzinoms Berlin (24. März 2006) - Erhalten Patienten mit metastasiertem kolorektalen
Signifikante Lebensverlängerung durch Angiogenese-Hemmung Avastin in der First-Line-Therapie des metastasierten kolorektalen Karzinoms Berlin (24. März 2006) - Erhalten Patienten mit metastasiertem kolorektalen
 Therapie der Multiplen Sklerose Neue Entwicklungen und Erkenntnisse Matthias Bußmeyer 15.10.2013 1 Medikamentöse Therapie der Multiplen Sklerose vor 3 Wochen 2 15.10.2013 Neu zugelassen: Aubagio (Teriflunomid)
Therapie der Multiplen Sklerose Neue Entwicklungen und Erkenntnisse Matthias Bußmeyer 15.10.2013 1 Medikamentöse Therapie der Multiplen Sklerose vor 3 Wochen 2 15.10.2013 Neu zugelassen: Aubagio (Teriflunomid)
Europäische Kommission erteilt Zulassung für Mavenclad (Cladribin-Tabletten)
 Ihre Ansprechpartner Friederike Segeberg 06151 72-6328 Investor Relations 06151 72-3321 25. August 2017 Europäische Kommission erteilt Zulassung für Mavenclad (Cladribin-Tabletten) Erste in Europa zugelassene
Ihre Ansprechpartner Friederike Segeberg 06151 72-6328 Investor Relations 06151 72-3321 25. August 2017 Europäische Kommission erteilt Zulassung für Mavenclad (Cladribin-Tabletten) Erste in Europa zugelassene
Früher Einsatz sichert protektive Wirkung von Tiotropium
 Früher Einsatz sichert protektive Wirkung von Tiotropium Mannheim (19. März 2009) Die chronisch obstruktive Lungenerkrankung (COPD) hat große Auswirkungen auf die Lebensqualität der betroffenen Patienten.
Früher Einsatz sichert protektive Wirkung von Tiotropium Mannheim (19. März 2009) Die chronisch obstruktive Lungenerkrankung (COPD) hat große Auswirkungen auf die Lebensqualität der betroffenen Patienten.
Zulassung für JANUMET (Sitagliptin/Metformin) zur Behandlung des Typ-2-Diabetes in der Europäischen Union
 Zulassung für JANUMET (Sitagliptin/Metformin) zur Behandlung des Typ-2-Diabetes in der Europäischen Union Haar (23. Juli 2008) JANUMET (Sitagliptin/Metformin, MSD) hat von der Europäischen Kommission die
Zulassung für JANUMET (Sitagliptin/Metformin) zur Behandlung des Typ-2-Diabetes in der Europäischen Union Haar (23. Juli 2008) JANUMET (Sitagliptin/Metformin, MSD) hat von der Europäischen Kommission die
