KAPITEL 7: LÖSUNGSMITTELEINFLUSS
|
|
|
- Walter Schubert
- vor 7 Jahren
- Abrufe
Transkript
1 7.1 Qualitative Aspekte des Lösungsmitteleinflusses 7.2 Kontinuum-Modelle 7.3 Explizite Beschreibung des Lösungsmittels KAPITEL 7: LÖSUNGSMITTELEINFLUSS
2 7.1 Lösungsmitteleffekte Lösungsmittel induziert nicht nur quantitative Änderungen der Dynamik (verglichen mit Reaktion in der Gasphase), sondern auch qualitative: In polaren Lösungsmitteln: Stabilisierung von Ionen (relative Energie v. Konfigurationen, z.b. α-helix vs. β-faltblatt von Proteinen, andere Reaktionspfade, ) Stöße des gelösten Moleküls mit Lösungsmittelmolekülen Käfig-Effekt: Lösungsmittel hülle verhindert Separation von Produkten/ Edukten
3 Lösungsmitteleffekte Lösungsmittel induziert nicht nur quantitative Änderungen der Dynamik (verglichen mit Reaktion in der Gasphase), sondern auch qualitative: In polaren Lösungsmitteln: Stabilisierung von Ionen Stöße des gelösten Moleküls mit Lösungsmittelmolekülen Käfig-Effekt: Lösungsmittel hülle verhindert Separation von Produkten/ Edukten Beispiel: S N 2 Reaktion X - + CH 3 X [XCH 3 X] - X - + CH 3 X Gasphase: starke Ion-Molekül-WW; Ion alleine energetisch ungünstiger stabiles Tal E solv E solv X - solv + CH 3 X IPC Friedrich-Schiller- Universität Jena [XCH 3 X] - solv E solv X - solv + CH 3 X 288 Flüssige Phase, polares LM: Ion von Solvathülle umgeben und stabilisiert energ. Absenkung (fast unabhängig vom Abstand), aber keine besondere Stabilisierung des TS
4 Lösungsmitteleffekte Lösungsmittel induziert nicht nur quantitative Änderungen der Dynamik (verglichen mit Reaktion in der Gasphase), sondern auch qualitative: Einfluss auf die Dynamik: Solvat und Lösungsmittel können nicht immer getrennt betrachtet werden. Zeitskala I: Ballistische Bewegung: auf sehr kurzen Zeitskalen: Lösungsmittel ist quasi gefroren und bewegt sich kaum. Reaktion ist schnell, aber Lösungsmittel benötigt Zeit, sich anzupassen ( zu antworten ). Diffusionskontrollierte Bewegung: System bewegt sich und reagiert langsam in Ort + Energie (Stöße) Zeitskala II: Die Schwingungsfrequenzen des Solvats können an das Lösungsmittel koppeln (Rotation + Translation sowieso) IPC Friedrich-Schiller- Universität Jena 289
5 Lösungsmittel: Solvatisierung Beiträge zur Solvatisierungsenergie: Entropie: für uni-molekulare Reaktionen wenig Unterschied zwischen Gasphase und flüssiger Phase; für bi-molekulare Reaktionen: Entropisch viel günstiger in Lösung (in Gasphase wird ein Translationsfreiheitsgrad bei Formen des TS verloren ). Beitrag zur Barriere in Lösung kleiner als in Gasphase (~exp( S vap /R) 100)* Enthalpie: Elektrostatischer Beitrag; Punktladung q im Zentrum einer Kugel mit Radius R befindet sich in einem klassischen Dielektrikum mit relativer Dielektrizitätskonstante ε r. G Solvatisierung = 2 q ε r 1 πε R 2ε r 4 0 * Anmerkung: in Wasser orientieren sich die Wassermoleküle um ein Ion; das kostet Entropie IPC Friedrich-Schiller- Universität Jena 290
6 Lösungsmittel: Solvatisierung; elektrostatisches Modell Elektrostatisches Modell Punktladung q im Zentrum einer Kugel mit Radius R befindet sich in einem klassischen Dielektrikum mit relativer Dielektrizitätskonstante ε r. Coulomb-Kraft F zwischen 2 Ladungen mit Abstand R: F q q 4π ε R 1 2 = ε 2 r = ε In Medium wird die relative Dielektrizitätskonstante verwendet. Die Coulomb-Kraft ist mit dem negativen des Gradienten des elektrischen Potentials verknüpft: q V = 4π ε rε 0 R Je polarer das Lösungsmittel, desto höher die Dielektrizitätskonstante und umso kleiner die Kraft, die eine Ladung auf eine andere Ladung in diesem Medium ausübt ε 0 IPC Friedrich-Schiller- Universität Jena 291
7 Lösungsmittel: Solvatisierung: Das Born sche Modell Elektrostatischer Beitrag: Punktladung q im Zentrum einer Kugel mit Radius R befindet sich in einem klassischen Dielektrikum mit relativer Dielektrizitätskonstante ε r. G Solvatisierung = 2 q ε r 1 πε R 2ε r 4 0 Herleitung: 4-Schritte: Geladen W Entladen Neutral 1.Entladen des Ions (Arbeit: W Entladung ) 2.Neutrales Teilchen ins LM (Arbeit: W Transfer ) 3.Laden des neutralen Teilchens (Arbeit: W Laden ) 4.Ion ins Vakuum (W Solvatisierung = - G Solvatisierung ) Geladen G Solvatisierung W Laden W Transfer Neutral Vakuum, ε r = 1 Lösungsmittel, ε r > 1 IPC Friedrich-Schiller- Universität Jena 292
8 Lösungsmittel: Solvatisierung: Das Born sche Modell Herleitung: 4-Schritte: 1.Entladen des Ions (Arbeit: W Entladung ) 2.Neutrales Teilchen ins LM (Arbeit: W Transfer ) 3.Laden des neutralen Teilchens (Arbeit: W Laden ) 4.Ion ins Vakuum (W Solvatisierung = - G Solvatisierung ) W Entladen + WTransfer + WLaden GSolvatisierung kleiner Beitrag = 0 Geladen W Entladen G Solvatisierung Neutral W Transfer Vakuum, ε r = 1 W Entladen + W Laden = G Solvatisierung Geladen W Laden Neutral Lösungsmittel, ε r > 1 IPC Friedrich-Schiller- Universität Jena 293
9 Lösungsmittel: Solvatisierung: Das Born sche Modell Herleitung: 4-Schritte: 1.Entladen des Ions (Arbeit: W Entladung ) 2.Neutrales Teilchen ins LM (Arbeit: W Transfer ) 3.Laden des neutralen Teilchens (Arbeit: W Laden ) 4.Ion ins Vakuum (W Solvatisierung = - G Solvatisierung ) W Entladen + W Laden = G Solvatisierung Evaluierung der Integrale für die Arbeit des Ladens bzw. Entladens: W W Laden = Entladen q 0 = V dq' = 0 q q V dq' = 2 q' q dq' = 4πε ε R 8πε ε R 0 r 0 0 q 2 q' q dq' = 4πε R 8πε R 0 r 0 0 Man erhält den Ausdruck für 1 Ion: G Solvatisierung = 2 2 q 1 q ε r 1 1 = πε 0 R ε r 4πε R 2ε r 4 0 IPC Friedrich-Schiller- Universität Jena 294
10 Lösungsmittel: Solvatisierung: Das Born sche Modell (Herleitung, Fortsetzung) Man erhält den Ausdruck für 1 Ion. Für 1 Mol Ionen wird mit der Avogadrozahl multipliziert: G Solvatisierung 2 q = 69.0 R ε 1 r ε r [ kcal / mol] (R in nm) Großer Beitrag der freien Energie zur Solvatisierung und ist daher wichtig bei Reaktionen von Ionen in Lösung. Vergleich des Born schen Modells mit dem Experiment? Direkter Vergleich schwierig; wieder Umweg über Enthalpie und Entropie S H Solvatisierung Solvatisierung G = T = N Solvatisierung A = N A 2 q 1 1 8πε 0R ε r 2 q 1 2 8πε R ε 0 T ε r r ε r T ε r T IPC Friedrich-Schiller- Universität Jena 295
11 Lösungsmittel: Solvatisierung: Das Born sche Modell Vergleich des Born schen Modells mit dem Experiment? Direkter Vergleich schwierig; wieder Umweg über Enthalpie und Entropie H Solvatisierung = N A 2 q 1 1 πε R ε r 8 0 T ε Was ist R? Der Radius des Hohlraums um das Ion, nicht der echte Ionenradius aus Kristalldaten. r ε r T Quelle: Levine, Molecular Reaction Dynamics IPC Friedrich-Schiller- Universität Jena 296
12 Lösungsmittel: Solvatisierung Veranschaulichung: NaCl: stabiles Molekül mit Bindungsenergie von 4.26 ev (= 411 kj/mol) für Dissoziation in neutrale Na und Cl Atome. Dissoziationsenergie für Na + und Cl - : Elektronentransfer: Na Na + (5.14 ev) Cl Cl - (-3.6 ev) Kosten: 1.5 ev (145 kj/mol) Zusammengerechnete Kosten: NaCl Na + + Cl - : 411 kj/mol kj/mol = 556 kj/mol In der Gasphase sehr endergonisch! In Wasser: Hydratisierungsenergien für die Ionen: kj/mol Hinreichend viel Energie für Bindungsbruch und Bildung von Ionenpaaren in wässriger Lösung. IPC Friedrich-Schiller- Universität Jena 297
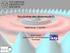
13 7.1 Lösungsmitteleffekte Im Wasser orientieren sich die H 2 O Moleküle in Richtung des Ions (gegensätzliche Ladungen). Struktur der Hydrathülle (auf Kosten der Entropie) Einfaches Bild eines kontinuierlichen Dielektrikums ist nicht ganz richtig. Lösungsmittelmoleküle ordnen sich in Schichten an. Ion Erste Hydratationsschale: rotationsgehinderte Wassermoleküle; Orientierung der Wassermoleküle um das Ion ( spezifische Lösungsmitteleffekte, kurzreichweitig) Zwischenlage Normales Wasser; Abschirmung der Ladung und Polarisation, (ε<1) (langreichweitig) Theoretische Beschreibung?
14 7.2 Kontinuumsmodelle Im Self-Consistent Reaction Field (SCRF) Modell wird das Lösungsmittel als uniformes, polarisierbares Medium mit Dielektrizitätskonstante ε r betrachtet, in dem das Solvat in ein Loch (ein Kavität) im Lösungsmittel platziert wird. Schritt 1: Erzeugen der Kavität. Dieser Schritt kostet Energie G cav, da Erniedrigung der Entropie und Reduktion der LM-LM Wechselwirkung
15 7.2 Kontinuumsmodelle Im Self-Consistent Reaction Field (SCRF) Modell wird das Lösungsmittel als uniformes, polarisierbares Medium mit Dielektrizitätskonstante ε r betrachtet, in dem das Solvat in ein Loch (ein Kavität) im Lösungsmittel platziert wird. Schritt 2: Platzieren des Solvats in der Kavität. Dieser Schritt ist energetisch günstig, da van-der-waals-wechselwirkung (Dispersion, G disp ) und elektrostatische Wechselwirkung (Polarisation, induzierte Ladung, G ele ) dazu kommt.
16 7.2 Kontinuumsmodelle Die freie Lösungsenthalpie G solv ist damit gegeben durch: G solv = G cav + G disp + G ele Die Reaktionsfeldmodelle unterscheiden sich u.a. in der Größe und Form der Kavität, Berechnung des Dispersionsanteils, Beschreibung des Lösungsmittels und des Solvats. Die einfachste Form der Kavität ist eine Kugel (oder ein Ellipsoid). Dann können die elektrostatischen WW zwischen Molekül und LM analytisch bestimmt werden.
17 7.2 Kontinuumsmodelle Verbesserte Modelle für die Kavität: Molekülform, erzeugt durch Kugeln um jedes Atom herum (typischerweise van-der-waals-radius 1.2) An diesen Bereich kommt das LM-Molekül nicht dran. Bessere Beschreibung: SAS (Solvent Assessable Surface)
18 7.2 Kontinuumsmodelle Annahme: Die Energie, die zum Erzeugen der Kavität aufgewandt wird + Stabilisierung durch van-der-waals ist proportional zur Oberfläche S (entweder eine Proportionalitätskonstante oder für jedes Atom extra): G cav + G disp = Atome i ξ S Anmerkung: Wird die Proportionalitätskonstante für die Atome an Experimente gefittet, sollten keine expliziten LM als Solvathülle zusätzlich verwendet werden. i i Modell funktioniert gut, falls elektrostatische Wechselwirkungen dominieren. Modell funktioniert schlecht, falls das gelöste Molekül mit dem LM wechselwirken kann (z.b. Wasserstoffbrückenbindungen mit dem Lösungsmittel).
19 7.2 Kontinuumsmodelle Was ist mit dem Beitrag der elektrostatischen Wechselwirkung, G ele? Ladungsdichte auf der Oberfläche der Kavität ist gegeben durch die Dielektrizitätskonstante ε r und das elektrische Feld F senkrecht zur Oberfläche. Für sphärische Kavitäten kann der Ausdruck analytisch bestimmt werden (Born Modell, 1920). Nur die Ladung q in einer kugelförmigen Kavität mit Radius a wird betrachtet a ε r q
20 Elektrostatisches Modell (Born-Näherung) Punktladung q im Zentrum einer Kugel mit Radius a befindet sich in einem klassischen Dielektrikum mit relativer Dielektrizitätskonstante ε r. Coulomb-Kraft F zwischen 2 Ladungen mit Abstand a: F q q 4π ε a 1 2 = ε 2 r 7.1 Lösungsmitteleffekte = ε In Medium wird die relative Dielektrizitätskonstante verwendet. Die Coulomb-Kraft ist mit dem negativen des Gradienten des elektrischen Potentials verknüpft: q V = 4π ε rε 0 a Je polarer das Lösungsmittel, desto höher die Dielektrizitätskonstante und umso kleiner die Kraft, die eine Ladung auf eine andere Ladung in diesem Medium ausübt ε 0
21 7.2 Kontinuumsmodelle Was ist mit dem Beitrag der elektrostatischen Wechselwirkung, G ele? Verbesserung des Born-Modells durch Onsager (Dipol) und Kirkwood (Multipol- Erweiterung) im Jahre Der molekulare Dipol µ erzeugt Ladung an der Oberfläche der Kavität, auf die das Lösungsmittel reagiert ( daher der Name Reaktionsfeld ) G ele 2 µ = 3 a ε r 1 2ε + 1 r a ε r µ
22 7.2 Kontinuumsmodelle Ein fester molekularer Dipol µ beschreibt kein SCRF, da Dipolmoment und Stabilisierung nicht selbst-konsistent berechnet werden. Rückpolarisation des Mediums ändert den molekularen Dipol (abhängig von der Polarisierbarkeit α des Moleküls) a ε r µ = a a G r r r r ele α ε ε ε ε µ
23 7.2 Kontinuumsmodelle Ein fester molekularer Dipol µ beschreibt kein SCRF, da Dipolmoment und Stabilisierung nicht selbst-konsistent berechnet werden. Rückpolarisation des Mediums ändert den molekularen Dipol (abhängig von der Polarisierbarkeit α des Moleküls. Induzierte Dipole im Medium bringen einen zusätzlichen Term VLM in den Hamilton- Operator ein: H = H0 + Vint V μ μ ˆ int = g E R g = 2( ε r 1) ( 2ε + 1) a μˆ = r + i r i α 3 Z α R α Das Reaktionsfeld E R wird in jedem Schritt aus dem (veränderten) Dipolmoment neu berechnet.
24 7.2 Kontinuumsmodelle Selbstkonsistente Lösung. Wie implementiert? 1. Berechnen der Wellenfunktion /Dichte ohne Lösungsmittel (im Vakuum), ψ (0), ρ (0) (r), H = H 0 2. Berechnen des Dipolmoments μ (0) (0) = ρ ( r) r dr + Z α αrα 3. Berechnen des Reaktionsfelds aus dem Dipolmoment 2( ε r 1) ER = ( 2ε r + 1) a 4. Bestimmen des Wechselwirkungsoperators V = μˆ E ˆint R 5. Neuberechnung der Wellenfunktion /Dichte im Lösungsmittel ψ (1), ρ (1) (r), H = H 0 + V int 3 μ ( 0) 6. Zurück zu (2) und Iterieren, bis sich µ, ρ, E R nicht mehr ändern.
25 7.2 Kontinuummodelle Polarizable Continuum Model (PCM): Ersetzen der kugelförmigen Kavität durch eine Form, die der Molekülform angepasst ist (Fläche über van-der-waals-radius definiert) Detaillierte Beschreibung des Elektrostatischen Potentials (nicht nur Punktladung bzw. Dipol) Parametrisierung der Kavität /Dispersion
26 7.2 Kontinuummodelle COnductor-like Screening MOdel (COSMO): Auch molekular-geformte Kavitäten Detaillierte Beschreibung des Elektrostatischen Potentials Unterschied zu PCM: Lösungsmittel wird als elektrischer Leiter (conductor, ε ) betrachtet; dann muss das elektrische Feld auf der Oberfläche der Kavität verschwinden. Bei bekannter Verteilung der Ladungen im Molekül lässt sich dann die Abschirm-Ladung an der Fläche bestimmen
27 7.3 Explizite Beschreibung des LM Explizite Beschreibung des Lösungsmittels: Hinzufügen einzelner / mehrerer Lösungsmittelmoleküle. Wann und warum wichtig? i.d.r. wenn Wasserstoffbrückenbindungen mit dem Lösungsmittel eine Rolle spielen.
28 7.3 Explizite Beschreibung des LM O OH Beispiel: Keto-Enol-Tautomerie CH 3 R CH 2 R Keto-Form Enol-Form Energie Übergangszustand Aktivierungsenergie E A E(Produkt) [Enol] E(Edukt) [Keto] G 0 Reaktionskoordinate
29 7.3 Explizite Beschreibung des LM O OH Keto-Enol-Tautomerie; σ-elektron-ziehende Substituenten R erhöhen die CH 3 R CH 2 R Reaktionsbarriere Keto-Form Enol-Form E A E(Produkt) E produkt -E edukt E A E(Edukt) E 0 Experiment: H = 20 kcal/mol Ref: N. González-Rivas, A. Cedillo, Comput. Theo. Chem. 994, (2012)
30 7.3 Explizite Beschreibung des LM O OH CH 3 R CH 2 R E A E(Produkt) +1 H 2 O Molekül E(Edukt) E 0 Ref: N. González-Rivas, A. Cedillo, Comput. Theo. Chem. 994, (2012) +2 H 2 O Moleküle
31 O 7.3 Explizite Beschreibung des LM OH CH 3 R CH 2 R +1 H 2 O Molekül E A E(Produkt) E(Edukt) E 0 Experiment: H = 20 kcal/mol +2 H 2 O Moleküle Ref: N. González-Rivas, A. Cedillo, Comput. Theo. Chem. 994, (2012)
32 7.3 Explizite Beschreibung des LM O OH CH 3 R CH 2 R E A E 0 Experiment: H = 20 kcal/mol Ref: N. González-Rivas, A. Cedillo, Comput. Theo. Chem. 994, (2012)
33 O 7.3 Explizite Beschreibung des LM OH CH 3 R CH 2 R Gasphase +1 H 2 O Molekül +2 H 2 O Moleküle N. González-Rivas, A. Cedillo, Comput. Theo. Chem. 994, (2012)
34 7.3 Explizite Beschreibung des LM
35 7.3 Explizite Beschreibung des LM
36 7.3 Kraftfeldmethode
37 7.3 Anwendungsbeispiele: Kraftfeld
38 Wiederholung: Kraftfeldmethoden: Prinzip Überlegung: Atome verhalten sich oft sehr ähnlich (z.b. C-H Schwingungen cm -1, Å). Weitere Diversifizierung: noch ähnlicher (Bsp: C(sp 3 )-H,...) Einteilung in Atom- Typen
39 Wiederholung: Kraftfelder
40 Wiederholung Kraftfeld: Streckung
41 Wiederholung Kraftfeld: Biegeschwingung
42 Wiederholung Kraftfeld: Torsion
43 Wiederholung: Nicht-bindende Wechselwirkung
44 Nicht-bindende Wechselwirkung van der Waals
45 Wiederholung: Implementierug
46 Wiederholung: Implementierung
47 7.3 Kraftfeldmethoden Für viele Systeme sind nicht-gleichgewicht Informationen wichtig. Beispiel: Transportphänomene, wie wandert ein Substrat zum Reaktionszentrum? Was passiert, wenn das Reaktionszentrum erreicht ist? Ändert sich die Form/Geometrie des Proteins / Enzyms? Des weiteren reicht es oft nicht zu wissen, was ein Molekül alleine macht, sondern was ein MOL an Molekülen macht ( statistische Thermodynamik). Es müssen die Bewegungen vieler Moleküle, die sich evtl. gegenseitig beeinflussen, simuliert werden. Hierzu muss die Bewegung der Moleküle simuliert werden ( Molecular Dynamics MD). Für statistische Informationen wird ein Mittelwert gebildet. Statistische Thermodynamik
48 7.3 QM/MM: Idee Für viele große Systeme ist eine genaue Beschreibung eines Teils des Gesamtsystem besonders wichtig. Beispiel: Enzyme. Die Beschreibung des sog. aktiven Zentrums des Enzyms (Reaktionszentrum) ist sehr wichtig; Rest ist nur eine Art Gerüst. Moleküle in Lösung. Die Beschreibung (chemische Reaktivität, Geometrie, angeregte Zustände) des Moleküls ist wichtig, Lösungsmittel ist nur Umgebung. Idee: Unterteilung des großen Systems in einen kleinen Teil, der quantenmechanisch beschrieben wird (DFT, HF, MP2, semiempirische Methoden, ), QM, und einen großen Rest, der mit Kraftfeldmethoden beschrieben wird, MM (molecular mechanics). Die beiden Rechnungen müssen dann noch irgendwie über einen Wechselwirkungsterm gekoppelt werden: QM/MM?
49 7.3 QM/MM Prinzip QM/MM: Verwendung von quantenmechanischen Methoden (QM) für den wichtigen / interessanten Teil des Systems Kraftfeld / Molecular Mechanics (MM) für den Rest des Systems MM Enzym Substrat QM Lösungsmittel/ Wasser MM
50 7.3 Anwendungsbeispiele: QM/MM
51 Halorhodopsin Chlorid-Pumpe Bild: J. Smith, Heidelberg 7.3 Anwendungsbeispiele: QM/MM
52 7.3 Anwendungsbeispiele: QM/MM Diels-Alder Reaktion katalysiert durch Enzym 1E9 (Antikörper-Katalysator)
53 7.3 QM/MM: MM Teil
54 7.3 QM/MM Hamiltonian Effektiver Hamilton-Operator für ein QM/MM System: ˆ ˆ ˆ + H eff = HQM + H MM HQM / MM ˆ QM: Hamilton-Operator des quantenmechanischen Systems (Vakuum), für MM wird die potentielle Energie genommen und QM/MM ist der Wechselwirkungsteil. Gesamtenergie des Systems: E ˆ ˆ Ψ + V = ΨQM HQM + HQM / MM QM MM Form des Wechselwirkungsteils?
55 Mechanisches Einbetten: 7.3 QM/MM Wechselwirkung E tot = E QM + E MM + E QM/MM E QM berechnet für das isolierte QM System. Wechselwirkung nur in der Energie Elektrostatisches Einbetten E tot = E QM + E MM + E QM/MM E QM berechnet für das eingebettete QM System. Polarisierbares Einbetten E tot = E QM + E MM + E QM/MM MM Ladungen werden durch das QM-System polarisiert
56 7.3 QM/MM Hamiltonian Effektiver Hamilton-Operator für ein QM/MM System: ˆ ˆ ˆ + H eff = HQM + H MM HQM / MM Form des Wechselwirkungsteils? (Einfachster) Ansatz: Mechanische Einbettung. Nur van-der-waals Wechselwirkung: i j MM QM Gibt hauptsächlich sterische Effekte (Vorteil): Effekte können auseinander gehalten werden ˆ ( r r ) vdw H = V, QM / MM ij i j
57 7.3 QM/MM Hamiltonian Effektiver Hamilton-Operator für ein QM/MM System: ˆ ˆ ˆ + H eff = HQM + H MM HQM / MM Form des Wechselwirkungsteils? Ansatz: Elektrostatische Einbettung, zusätzlich zu van-der-waals Wechselwirkung: H QM / MM = i j MM QM V vdw ij ( r, r ) i j + Es gibt viele verschiedene Einbettungsformen. Gut funktioniert es, Integrale über die QM Ladungsdichte und die diskreten MM Ladungen zu berechnen. ˆ i MM q i ρ QM ( r) r r i
58 7.3 QM/MM Hamiltonian Effektiver Hamilton-Operator für ein QM/MM System: ˆ ˆ ˆ + H eff = HQM + H MM HQM / MM Form des Wechselwirkungsteils? Ansatz: Elektrostatische Einbettung, zusätzlich zu van-der-waals Wechselwirkung: H QM / MM = i j MM QM V vdw ij ( r, r ) i j + Es gibt viele verschiedene Einbettungsformen. Gut funktioniert es, Integrale über die QM Ladungsdichte und die diskreten MM Ladungen zu berechnen. ˆ i MM q i ρ QM ( r) r r i
59 7.3 QM/MM Hamiltonian Form des Wechselwirkungsteils? Q = M α M H QM / MM + + i QM M MM ri, M α QM M MM Rα, M i = Summe über die QM Elektronen M= Summe über die MM Partialladungen α = Summe über die QM Kerne 1. Term: 1-Elektronen-Wechselwirkung zwischen QM Elektronendichte und MM Partialladungen 2. Term: Coulomb-WW zwischen QM Kernen und MM Ladungen Z Q V vdw (Nebenbemerkung: Woher bekommt man die Information über Atomladungen in QM? Populationsanalyse? ESP?
60 7.3 QM/MM Hamiltonian Was macht man, wenn (kovalente) Bindungen zwischen dem QM und dem MM Subsystem vorhanden sind? Information für Valenzelektronensituation in QM muss richtig sein Im MM System muss ein Partner-Atom vorhanden sein, damit die Geometrie kein loses Ende ist. Verknüpfungs-Atome: ein H-Atom (manchmal auch andere) wird ans lose Ende platziert. MM O HN QM NH 3 + MM O HN H C QM NH 3 + Schema nach Singh und Kollman (1986)
61 7.3 Lösungsmitteleffekte Lösungsmittel induziert nicht nur quantitative Änderungen der Dynamik (verglichen mit Reaktion in der Gasphase), sondern auch qualitative: In polaren Lösungsmitteln: Stabilisierung von Ionen (relative Energie v. Konfigurationen, andere Reaktionspfade, ) Stöße des gelösten Moleküls mit Lösungsmittelmolekülen Käfig-Effekt: Lösungsmittelhülle verhindert Separation von Produkten/ Edukten Self-Consistent Reaction Field (SCRF) Modell: Lösungsmittel ist uniformes, polarisierbares Medium mit Dielektrizitätskonstante ε r Explizite Beschreibung von Lösungsmittelmolekülen: mehrere Lösungsmittel werden den Rechnungen hinzugefügt (QM, QM/MM oder MM)
62 7.3 Lösungsmitteleffekte Self-Consistent Reaction Field (SCRF) Modell: Lösungsmittel ist uniformes, polarisierbares Medium mit Dielektrizitätskonstante ε r Modell funktioniert gut, falls elektrostatische Wechselwirkungen dominieren. Modell funktioniert schlecht, falls das gelöste Molekül mit dem LM wechselwirken kann (z.b. Wasserstoffbrückenbindungen mit dem Lösungsmittel). Explizite Beschreibung von Lösungsmittelmolekülen: mehrere Lösungsmittel werden den Rechnungen hinzugefügt (QM, QM/MM oder MM)
Selbstkonsistente Modelle/Solvatationsenergie. Generalized Born Solvation Model SM12
 Selbstkonsistente Modelle/Solvatationsenergie Generalized Born Solvation Model SM12 Marenich, A.; Cramer, C.; Truhlar, D.; J. Chem. Theroy Comput, 2013, 9, 609-620 Das Solventmodell SM12 We present a new
Selbstkonsistente Modelle/Solvatationsenergie Generalized Born Solvation Model SM12 Marenich, A.; Cramer, C.; Truhlar, D.; J. Chem. Theroy Comput, 2013, 9, 609-620 Das Solventmodell SM12 We present a new
Einführung in das Molecular Modelling
 Einführung in das Molecular Modelling Darstellung und Bearbeitung dreidimensionaler Molekülstrukturen Berechnung der physikochemischen Eigenschaften Ziel: Einsicht in die molekularen Mechanismen der Arzneistoffwirkung
Einführung in das Molecular Modelling Darstellung und Bearbeitung dreidimensionaler Molekülstrukturen Berechnung der physikochemischen Eigenschaften Ziel: Einsicht in die molekularen Mechanismen der Arzneistoffwirkung
6. Die Chemische Bindung
 6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
Kapitel 4. Die Grundlagen der Kinetik
 Kapitel 4. Die Grundlagen der Kinetik Monomolekulare Reaktion erster rdnung A Produkte; v = k [A] (S N 1) bimolekulare Reaktion zweiter rdnung (S N 2) A + B Produkte; v = k [A] [B] Einfluss der Aktivierungsbarrieren
Kapitel 4. Die Grundlagen der Kinetik Monomolekulare Reaktion erster rdnung A Produkte; v = k [A] (S N 1) bimolekulare Reaktion zweiter rdnung (S N 2) A + B Produkte; v = k [A] [B] Einfluss der Aktivierungsbarrieren
MM Kraftfelder. Michael Meyer. Vorlesung III. Kraftfelder
 MM 3.09.013 Kraftfelder Vorlesung III Kraftfelder Ziel Berechnung der potentiellen nergie eines bestimmten Moleküls als Funktion der Atomkoordinaten (potential energy surface). Beschreibung einer ganzen
MM 3.09.013 Kraftfelder Vorlesung III Kraftfelder Ziel Berechnung der potentiellen nergie eines bestimmten Moleküls als Funktion der Atomkoordinaten (potential energy surface). Beschreibung einer ganzen
Elektrolytlösungen, Leitfähigkeit, Ionentransport. Teil I
 Elektrolytlösungen, Leitfähigkeit, Ionentransport Teil I 1. Einführende Überlegungen 2. Solvatation, Hydratation 3. Ionenbeweglichkeiten und Leitfähigkeiten Literatur: Wedler 1.6.2-1.6.7 Teil II 4. Schwache
Elektrolytlösungen, Leitfähigkeit, Ionentransport Teil I 1. Einführende Überlegungen 2. Solvatation, Hydratation 3. Ionenbeweglichkeiten und Leitfähigkeiten Literatur: Wedler 1.6.2-1.6.7 Teil II 4. Schwache
22. Chemische Bindungen
 .05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
.05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
5.5 Elektrisches Zentralfeld, Coulombsches Gesetz
 5 Elektrizität und Magnetismus 5.5 Elektrisches Zentralfeld, Coulombsches Gesetz Elektrisches Zentralfeld Kugel mit Radius r um eine Punktladung = ǫ 0 Ed A = ǫ 0 E E d A Kugel da = ǫ 0 E(4πr 2 ) (5.26)
5 Elektrizität und Magnetismus 5.5 Elektrisches Zentralfeld, Coulombsches Gesetz Elektrisches Zentralfeld Kugel mit Radius r um eine Punktladung = ǫ 0 Ed A = ǫ 0 E E d A Kugel da = ǫ 0 E(4πr 2 ) (5.26)
Thermodynamik & Kinetik
 Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie,
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
Ferrofluide. Physikalische Grundlagen. http://en.wikipedia.org/wiki/file:ferrofluid_close.jpg
 Ferrofluide Physikalische Grundlagen http://en.wikipedia.org/wiki/file:ferrofluid_close.jpg Inhalt Definition Herstellung Maßnahmen zur Stabilisierung Abschätzung der Partikelgröße, Abstandsmechanismen
Ferrofluide Physikalische Grundlagen http://en.wikipedia.org/wiki/file:ferrofluid_close.jpg Inhalt Definition Herstellung Maßnahmen zur Stabilisierung Abschätzung der Partikelgröße, Abstandsmechanismen
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Die 3 Stoffklassen der Elemente
 Die Art der Bindung hängt davon ab, wie stark die Atome ihre Valenzelektronen anziehen. Elektronegativität (Abb. 17, S. 114) Qualitative Angabe, wie stark die Atomrümpfe die Elektronen in der Valenzschale
Die Art der Bindung hängt davon ab, wie stark die Atome ihre Valenzelektronen anziehen. Elektronegativität (Abb. 17, S. 114) Qualitative Angabe, wie stark die Atomrümpfe die Elektronen in der Valenzschale
Klausur zur Vorlesung Physikalische Chemie V Elektrochemie 6. bzw. 8. Fachsemester am , 10:00 bis 12:00 Uhr
 Universität Regensburg Institut für Physikalische und Theoretische Chemie Prof. Dr. G. Schmeer 18. Juli 27 Bitte füllen Sie zuerst dieses Deckblatt aus, das mit Ihren Lösungen abgegeben werden muss....
Universität Regensburg Institut für Physikalische und Theoretische Chemie Prof. Dr. G. Schmeer 18. Juli 27 Bitte füllen Sie zuerst dieses Deckblatt aus, das mit Ihren Lösungen abgegeben werden muss....
2 Grundgrößen und -gesetze der Elektrodynamik
 Grundgrößen und -gesetze der Elektrodynamik. Grundgrößen der Elektrodynamik.. Ladung und die dreidimensionale δ-distribution Ladung Q, q Ladungen treten in zwei Variationen auf: positiv und negativ Einheit:
Grundgrößen und -gesetze der Elektrodynamik. Grundgrößen der Elektrodynamik.. Ladung und die dreidimensionale δ-distribution Ladung Q, q Ladungen treten in zwei Variationen auf: positiv und negativ Einheit:
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Änderungen für nächste Woche Vorlesung
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Änderungen für nächste Woche Vorlesung
30. Lektion. Moleküle. Molekülbindung
 30. Lektion Moleküle Molekülbindung Lernziel: Moleküle entstehen aus Atomen falls ihre Wellenfunktionen sich derart überlappen, daß die Gesamtenergie abgesenkt wird. Begriffe Begriffe: Kovalente Bindung
30. Lektion Moleküle Molekülbindung Lernziel: Moleküle entstehen aus Atomen falls ihre Wellenfunktionen sich derart überlappen, daß die Gesamtenergie abgesenkt wird. Begriffe Begriffe: Kovalente Bindung
2 Das elektrostatische Feld
 Das elektrostatische Feld Das elektrostatische Feld wird durch ruhende elektrische Ladungen verursacht, d.h. es fließt kein Strom. Auf die ruhenden Ladungen wirken Coulomb-Kräfte, die über das Coulombsche
Das elektrostatische Feld Das elektrostatische Feld wird durch ruhende elektrische Ladungen verursacht, d.h. es fließt kein Strom. Auf die ruhenden Ladungen wirken Coulomb-Kräfte, die über das Coulombsche
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Lösung Sauerstoff: 1s 2 2s 2 2p 4, Bor: 1s 2 2s 2 2p 1, Chlor: 1s 2 2s 2 2p 6 3s 2 3p 5 Neon: 1s 2 2s 2 2p 6
 1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Grundlagen der Chemie Polare Bindungen
 Polare Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektronegativität Unter der Elektronegativität
Polare Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektronegativität Unter der Elektronegativität
Molecular Modelling. Molekulare Mechanik-Simulationen am Beispiel von DNA-Ligand-Komplexen
 Molecular Modelling Molekulare Mechanik-Simulationen am Beispiel von DNA-Ligand-Komplexen Florian Kamm, Dezember 2003 Halbkurs Algorithmen in der Bioinformatik Molecular Modelling Was ist das? Molecular
Molecular Modelling Molekulare Mechanik-Simulationen am Beispiel von DNA-Ligand-Komplexen Florian Kamm, Dezember 2003 Halbkurs Algorithmen in der Bioinformatik Molecular Modelling Was ist das? Molecular
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
(2.65 ev), da sich die beiden Elektronen gegenseitig abstossen.
 phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
Thema heute: Aufbau der Materie: Atommodelle 1
 Wiederholung der letzten Vorlesungsstunde: Naturwissenschaften, Unterteilung der Naturwissenschaften in einzelne Wissensgebiete, Modellvorstellungen, der "reine Stoff", thermische Eigenschaften, Siedepunkt,
Wiederholung der letzten Vorlesungsstunde: Naturwissenschaften, Unterteilung der Naturwissenschaften in einzelne Wissensgebiete, Modellvorstellungen, der "reine Stoff", thermische Eigenschaften, Siedepunkt,
Übungsblatt 3 - Lösungen
 Übungsblatt 3 - Lösungen zur Vorlesung EP2 (Prof. Grüner) im 2010 3. Juni 2011 Aufgabe 1: Plattenkondensator Ein Kondensator besteht aus parallelen Platten mit einer quadratischen Grundäche von 20cm Kantenlänge.
Übungsblatt 3 - Lösungen zur Vorlesung EP2 (Prof. Grüner) im 2010 3. Juni 2011 Aufgabe 1: Plattenkondensator Ein Kondensator besteht aus parallelen Platten mit einer quadratischen Grundäche von 20cm Kantenlänge.
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Wiederholung: Elektrisches Feld und Feldlinien I Feld zwischen zwei Punktladungen (pos. und neg.)
 Wiederholung: Elektrisches Feld und Feldlinien I Feld zwischen zwei Punktladungen (pos. und neg.) 1 Grieskörner schwimmen in Rhizinusöl. Weil sie kleine Dipole werden, richten sie sich entlang der Feldlinien
Wiederholung: Elektrisches Feld und Feldlinien I Feld zwischen zwei Punktladungen (pos. und neg.) 1 Grieskörner schwimmen in Rhizinusöl. Weil sie kleine Dipole werden, richten sie sich entlang der Feldlinien
PN 2 Einführung in die Experimentalphysik für Chemiker
 PN 2 Einführung in die Experimentalphysik für Chemiker 4. Vorlesung 9.5.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 2 Einführung in die Experimentalphysik für Chemiker 4. Vorlesung 9.5.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Elektromagnetische Felder und Wellen. Klausur Herbst Aufgabe 1 (5 Punkte) Aufgabe 2 (3 Punkte) Aufgabe 3 (5 Punkte) Aufgabe 4 (12 Punkte) Kern
 Elektromagnetische Felder und Wellen Klausur Herbst 2000 Aufgabe 1 (5 Punkte) Ein magnetischer Dipol hat das Moment m = m e z. Wie groß ist Feld B auf der z- Achse bei z = a, wenn sich der Dipol auf der
Elektromagnetische Felder und Wellen Klausur Herbst 2000 Aufgabe 1 (5 Punkte) Ein magnetischer Dipol hat das Moment m = m e z. Wie groß ist Feld B auf der z- Achse bei z = a, wenn sich der Dipol auf der
5 Elektrizität und Magnetismus
 5.1 Elektrische Ladung q Ursprung: Existenz von subatomaren Teilchen Proton: positive Ladung Elektron: negative Ladung besitzen jeweils eine Elementarladung e = 1.602 10 19 C (Coulomb) Ladung ist gequantelt
5.1 Elektrische Ladung q Ursprung: Existenz von subatomaren Teilchen Proton: positive Ladung Elektron: negative Ladung besitzen jeweils eine Elementarladung e = 1.602 10 19 C (Coulomb) Ladung ist gequantelt
Kolleg 1998/ Klausur aus der Physik Leistungskurs P 20 Blatt 1 (von 2) Kurshalbjahr 13/1
 Leistungskurs P 20 Blatt 1 (von 2) Kurshalbjahr 13/1 1. Rutherfordsches Atommodell Im Jahr 1904 entwickelte Thomson ein Atommodell, bei dem das Atom aus einer positiv geladenen Kugel mit homogener Massenverteilung
Leistungskurs P 20 Blatt 1 (von 2) Kurshalbjahr 13/1 1. Rutherfordsches Atommodell Im Jahr 1904 entwickelte Thomson ein Atommodell, bei dem das Atom aus einer positiv geladenen Kugel mit homogener Massenverteilung
Allgemeine Chemie 1. Skript Allgemeine und Anorganische Chemie
 Allgemeine Chemie 1 Skript Allgemeine und Anorganische Chemie Inhaltsverzeichnis: 1. Atome...3 A Elektronen...3 B Protonen...4 C Neutronen...5 D Aufbau von Atomen...5 E Isotope...6 F Radioaktivität...6
Allgemeine Chemie 1 Skript Allgemeine und Anorganische Chemie Inhaltsverzeichnis: 1. Atome...3 A Elektronen...3 B Protonen...4 C Neutronen...5 D Aufbau von Atomen...5 E Isotope...6 F Radioaktivität...6
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Quantenzahlen. Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale.
 Quantenzahlen Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale. l = 0, 1, 2, 3, (Orbital-)Symbol s, p, d, f, Zahl der Orbitale
Quantenzahlen Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale. l = 0, 1, 2, 3, (Orbital-)Symbol s, p, d, f, Zahl der Orbitale
Grundtypen der Bindung. Grundtypen chemischer Bindung. Oktettregel. A.8.1. Atombindung
 Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Chemische Bindung. Wie halten Atome zusammen? Welche Atome können sich verbinden? Febr 02
 Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Inhaltsverzeichnis Elektrostatik
 Inhaltsverzeichnis 1 Elektrostatik 1 1.1 Grundbegriffe...................................... 1 1.1.1 Elektrische Ladung, Coulomb-Gesetz..................... 1 1.1.2 Das elektrische Feld..............................
Inhaltsverzeichnis 1 Elektrostatik 1 1.1 Grundbegriffe...................................... 1 1.1.1 Elektrische Ladung, Coulomb-Gesetz..................... 1 1.1.2 Das elektrische Feld..............................
Das quantenmechanische Atommodell
 Ende 93 konzipierte de Broglie seine grundlegenden Ideen über die Dualität von Welle und Korpuskel. Albert Einstein hatte schon 905 von den korpuskularen Eigenschaften des Lichtes gesprochen; de Broglie
Ende 93 konzipierte de Broglie seine grundlegenden Ideen über die Dualität von Welle und Korpuskel. Albert Einstein hatte schon 905 von den korpuskularen Eigenschaften des Lichtes gesprochen; de Broglie
ν und λ ausgedrückt in Energie E und Impuls p
 phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #17 19/11/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Elektrizitätslehre Teil 2 Kondensator Kondensator Im einfachsten Fall besteht ein Kondensator aus
Physik für Mediziner im 1. Fachsemester #17 19/11/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Elektrizitätslehre Teil 2 Kondensator Kondensator Im einfachsten Fall besteht ein Kondensator aus
Kapitel 2: Die Born-Oppenheimer-Näherung
 Kapitel 2: Die Born-Oppenheimer-Näherung Übersicht: 2.1 Der molekulare Hamiltonoperator 2.2 Die Born-Oppenheimer-Näherung 2.3 Die Schrödingergleichung für die Kernbewegung 2.4 Die Born-Oppenheimer-Potentialfläche
Kapitel 2: Die Born-Oppenheimer-Näherung Übersicht: 2.1 Der molekulare Hamiltonoperator 2.2 Die Born-Oppenheimer-Näherung 2.3 Die Schrödingergleichung für die Kernbewegung 2.4 Die Born-Oppenheimer-Potentialfläche
Ionisierungsenergie und Elektronenaffinität. Bindigkeit Valenzstrichformel Molekülgeometrie
 Tendenzen im Periodensystem Ionisierungsenergie und Elektronenaffinität Atombindung (Elektronenpaarbindung) Bindigkeit Valenzstrichformel Molekülgeometrie Räumlicher Bau einfacher Moleküle Polare Atombindung
Tendenzen im Periodensystem Ionisierungsenergie und Elektronenaffinität Atombindung (Elektronenpaarbindung) Bindigkeit Valenzstrichformel Molekülgeometrie Räumlicher Bau einfacher Moleküle Polare Atombindung
UNIVERSITÄT GREIFSWALD. Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE. Arbeitskreis Biophysikalische Chemie
 UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Biophysikalische Chemie Prof. Dr. Walter Langel Modelle für elektronische Zustände Einfachstes klassisches
UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Biophysikalische Chemie Prof. Dr. Walter Langel Modelle für elektronische Zustände Einfachstes klassisches
Kerne und Teilchen. Aufbau der Kerne (1) Moderne Experimentalphysik III Vorlesung 17.
 Kerne und Teilchen Moderne Experimentalphysik III Vorlesung 17 MICHAEL FEINDT INSTITUT FÜR EXPERIMENTELLE KERNPHYSIK Aufbau der Kerne (1) KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Kerne und Teilchen Moderne Experimentalphysik III Vorlesung 17 MICHAEL FEINDT INSTITUT FÜR EXPERIMENTELLE KERNPHYSIK Aufbau der Kerne (1) KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
4.2) Mehrelektronenatome
 4.) Mehrelektronenatome Elektronen besetzen Zustände mit verschiedenen Kombinationen von n,l,m,s Reihenfolge der Füllung bestimmt durch Wechselwirkung zwischen V ( r) und dem Zentrifugalpotential l (l+1)/r
4.) Mehrelektronenatome Elektronen besetzen Zustände mit verschiedenen Kombinationen von n,l,m,s Reihenfolge der Füllung bestimmt durch Wechselwirkung zwischen V ( r) und dem Zentrifugalpotential l (l+1)/r
PHYSIK. Studienbrief Moleküle. AUTOR: Dr. Johannes Bernardi
 PHYSIK AUTOR: Dr. Johannes Bernardi Inhalt: 1 Einführung...3 2 Ionenbindung (heteropolare Bindung): A + B...4 3 Kovalente Bindung (chemische Bindung): AB...6 4 Van der Waals Bindung...7 5 Wasserstoffbindung...8
PHYSIK AUTOR: Dr. Johannes Bernardi Inhalt: 1 Einführung...3 2 Ionenbindung (heteropolare Bindung): A + B...4 3 Kovalente Bindung (chemische Bindung): AB...6 4 Van der Waals Bindung...7 5 Wasserstoffbindung...8
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Induktion, Polarisierung und Magnetisierung
 Übung 2 Abgabe: 11.03. bzw. 15.03.2016 Elektromagnetische Felder & Wellen Frühjahrssemester 2016 Photonics Laboratory, ETH Zürich www.photonics.ethz.ch Induktion, Polarisierung und Magnetisierung In dieser
Übung 2 Abgabe: 11.03. bzw. 15.03.2016 Elektromagnetische Felder & Wellen Frühjahrssemester 2016 Photonics Laboratory, ETH Zürich www.photonics.ethz.ch Induktion, Polarisierung und Magnetisierung In dieser
Modelle zur Beschreibung von Gasen und deren Eigenschaften
 Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Ferienkurs - Experimentalphysik 2 - Übungsblatt - Lösungen
 Technische Universität München Department of Physics Ferienkurs - Experimentalphysik 2 - Übungsblatt - Lösungen Montag Daniel Jost Datum 2/8/212 Aufgabe 1: (a) Betrachten Sie eine Ladung, die im Ursprung
Technische Universität München Department of Physics Ferienkurs - Experimentalphysik 2 - Übungsblatt - Lösungen Montag Daniel Jost Datum 2/8/212 Aufgabe 1: (a) Betrachten Sie eine Ladung, die im Ursprung
Feststellungsprüfung Chemie Lösungen. Wegen seiner hohen Reaktivität kommt Chlor in der Natur nicht elementar vor. = 26, ,957=35,45
 Thema I 1a 1b 1c 1d 1e 2a 2b Feststellungsprüfung Chemie Lösungen Wegen seiner hohen Reaktivität kommt Chlor in der Natur nicht elementar vor.,,,, = 26,496 8,957=35,45 Die relative Isotopenmasse ist die
Thema I 1a 1b 1c 1d 1e 2a 2b Feststellungsprüfung Chemie Lösungen Wegen seiner hohen Reaktivität kommt Chlor in der Natur nicht elementar vor.,,,, = 26,496 8,957=35,45 Die relative Isotopenmasse ist die
Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen.
 1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
Pfui Teufel, ein widerlicher Österreicherwitz! So etwas könnte sich tatsächlich zugetragen haben. Begründung: Antwort richtig nur mit Begründung!
 Musterprüfung: 1. Was ist ein Faradayscher Käfig? 2. Millikan fand auf einem Öltröpfchen eine Ladung Q von 8 10-19 C. Wie gross war die Ladung des Öltröpfchens wahrscheinlich auf vier signifikante Ziffern
Musterprüfung: 1. Was ist ein Faradayscher Käfig? 2. Millikan fand auf einem Öltröpfchen eine Ladung Q von 8 10-19 C. Wie gross war die Ladung des Öltröpfchens wahrscheinlich auf vier signifikante Ziffern
Misst man die Ladung in Abhängigkeit von der angelegten Spannung, so ergibt sich ein proportionaler Zusammenhang zwischen Ladung und Spannung:
 3.11 Der Kondensator In den vorangegangenen Kapiteln wurden die physikalischen Eigenschaften von elektrischen Ladungen und Feldern näher untersucht. In vielen Experimenten kamen dabei bereits Kondensatoren
3.11 Der Kondensator In den vorangegangenen Kapiteln wurden die physikalischen Eigenschaften von elektrischen Ladungen und Feldern näher untersucht. In vielen Experimenten kamen dabei bereits Kondensatoren
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik
 Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Unter Kapazität versteht man die Eigenschaft von Kondensatoren, Ladung oder elektrische Energie zu speichern.
 16. Kapazität Unter Kapazität versteht man die Eigenschaft von Kondensatoren, Ladung oder elektrische Energie zu speichern. 16.1 Plattenkondensator Das einfachste Beispiel für einen Kondensator ist der
16. Kapazität Unter Kapazität versteht man die Eigenschaft von Kondensatoren, Ladung oder elektrische Energie zu speichern. 16.1 Plattenkondensator Das einfachste Beispiel für einen Kondensator ist der
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Säuren und Basen Säure-Base-Konzepte Säure-Base-Gleichgewichte Säurestärke, Basenstärke ph-, poh-, pk-werte Pufferlösungen Titrationen 1 Säure-Base-Definition nach ARRHENIUS
Praktikumsrelevante Themen Säuren und Basen Säure-Base-Konzepte Säure-Base-Gleichgewichte Säurestärke, Basenstärke ph-, poh-, pk-werte Pufferlösungen Titrationen 1 Säure-Base-Definition nach ARRHENIUS
Enthalpie, Entropie und Temperatur des Phasenübergangs flüssig-gasförmig. eine Analyse von Elementen und chemischen Verbindungen
 Bayerisches Zentrum für Angewandte Energieforschung e.v. Enthalpie, Entropie und Temperatur des Phasenübergangs flüssiggasförmig eine Analyse von Elementen und chemischen Verbindungen Harald Mehling Berater
Bayerisches Zentrum für Angewandte Energieforschung e.v. Enthalpie, Entropie und Temperatur des Phasenübergangs flüssiggasförmig eine Analyse von Elementen und chemischen Verbindungen Harald Mehling Berater
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
IIE2. Modul Elektrizitätslehre II. Dielektrika
 IIE2 Modul Elektrizitätslehre II Dielektrika Ziel dieses Versuches ist, die Funktionsweise eines Kondensators mit Dielektrikum zu verstehen. Des weiteren soll die Kapazität des Kondensators und die relative
IIE2 Modul Elektrizitätslehre II Dielektrika Ziel dieses Versuches ist, die Funktionsweise eines Kondensators mit Dielektrikum zu verstehen. Des weiteren soll die Kapazität des Kondensators und die relative
Physikalische. Grundlagen. L. Kölling, Fw Minden
 Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
 www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid
 Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Organische Chemie 1 Teil 2 1. Vorlesung, Dienstag
 Inhalte der 1. Vorlesung: 1. Die Reaktivität organischer Moleküle 1.1 Warum geschehen Chemische Reaktionen 1.2 Gleichgewichtsreaktionen, Ungleichgewichtsreaktionen 1.2.1 Triebkraft chemischer Reaktionen
Inhalte der 1. Vorlesung: 1. Die Reaktivität organischer Moleküle 1.1 Warum geschehen Chemische Reaktionen 1.2 Gleichgewichtsreaktionen, Ungleichgewichtsreaktionen 1.2.1 Triebkraft chemischer Reaktionen
Relative Atommassen. Stefan Pudritzki Göttingen. 8. September 2007
 Relative Atommassen Stefan Pudritzki Göttingen 8. September 2007 Berechnung der relativen Atommassen Nach dem derzeitigen Kenntnisstand können die relativen Atommassen der chemischen Elemente mit einem
Relative Atommassen Stefan Pudritzki Göttingen 8. September 2007 Berechnung der relativen Atommassen Nach dem derzeitigen Kenntnisstand können die relativen Atommassen der chemischen Elemente mit einem
11. Polyelektrolyte. Schwache Polyelektrolyte = Ladungsdichte vom ph-wert der Lösung gegeben
 11. Polyelektrolyte 11.1 Definitionen Polyelektrolyte = Makromoleküle aus Monomeren mit ionisierbaren Gruppen, damit in polaren Lösungsmitteln erhebliche Anzahl an geladenen funktionellen Gruppen und Gegenionen
11. Polyelektrolyte 11.1 Definitionen Polyelektrolyte = Makromoleküle aus Monomeren mit ionisierbaren Gruppen, damit in polaren Lösungsmitteln erhebliche Anzahl an geladenen funktionellen Gruppen und Gegenionen
Theoretisch-chemische Übungen Quantenchemischer Teil
 Theoretisch-chemische Übungen Quantenchemischer Teil Gunther Zechmann Universität Wien Institut für Theoretische Chemie Sommersemester 2006 1 Berechnung der Rotationsbarriere von Ethan Auswahl der Rechenmethoden
Theoretisch-chemische Übungen Quantenchemischer Teil Gunther Zechmann Universität Wien Institut für Theoretische Chemie Sommersemester 2006 1 Berechnung der Rotationsbarriere von Ethan Auswahl der Rechenmethoden
Grundlagen der Chemie Ionenradien
 Ionenradien Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Ionenradien In einem Ionenkristall halten benachbarte
Ionenradien Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Ionenradien In einem Ionenkristall halten benachbarte
Bioorganische Chemie Enzymatische Katalyse 2011
 Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Gruppentheorie ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD. Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE
 ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
2. Klausur in K1 am
 Name: Punkte: Note: Ø: Physik Kursstufe Abzüge für Darstellung: Rundung:. Klausur in K am 7.. 00 Achte auf die Darstellung und vergiss nicht Geg., Ges., Formeln, Einheiten, Rundung...! Angaben: e =,60
Name: Punkte: Note: Ø: Physik Kursstufe Abzüge für Darstellung: Rundung:. Klausur in K am 7.. 00 Achte auf die Darstellung und vergiss nicht Geg., Ges., Formeln, Einheiten, Rundung...! Angaben: e =,60
Seminar zum Methodenkurs Christian Graßl
 Seminar zum Methodenkurs Christian Graßl Neue Typen von Wasserstoffbrückenbindungen in der Organometallchemie (Coord. Chem. Rev. 231 (2002) 165) http://upload.wikimedia.org/wikipedia/commons/d/dd/wasserstoffbr%c3%bcckenbindungen_des_wasser.png
Seminar zum Methodenkurs Christian Graßl Neue Typen von Wasserstoffbrückenbindungen in der Organometallchemie (Coord. Chem. Rev. 231 (2002) 165) http://upload.wikimedia.org/wikipedia/commons/d/dd/wasserstoffbr%c3%bcckenbindungen_des_wasser.png
Anorganische Chemie III
 Seminar zur Vorlesung Anorganische Chemie III Wintersemester 2015/16 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah # hexagonale Strukturtypen
Seminar zur Vorlesung Anorganische Chemie III Wintersemester 2015/16 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah # hexagonale Strukturtypen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Tropfenkonturanalyse
 Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden?
 41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
Temperature differentially affects encounter and docking thermodynamics of antibody-antigen association
 Temperature differentially affects encounter and docking thermodynamics of antibody-antigen association Journal of Molecular Recognition, 2002 Claudia A. Lipschultz, Anthony Yee, S. Mohan, Yili Li, Sandra
Temperature differentially affects encounter and docking thermodynamics of antibody-antigen association Journal of Molecular Recognition, 2002 Claudia A. Lipschultz, Anthony Yee, S. Mohan, Yili Li, Sandra
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Elektrizitätslehre 2.
 Elektrizitätslehre. Energieumwandlung (Arbeit) im elektrischen Feld Bewegung einer Ladung gegen die Feldstärke: E s Endposition s Anfangsposition g W F Hub s r F Hub r Fq FHub Eq W qes W ist unabhängig
Elektrizitätslehre. Energieumwandlung (Arbeit) im elektrischen Feld Bewegung einer Ladung gegen die Feldstärke: E s Endposition s Anfangsposition g W F Hub s r F Hub r Fq FHub Eq W qes W ist unabhängig
Der Ladungsbetrag Q, den jede Kondensatorplatten aufnimmt, ist dabei proportional zur angelegten. Q U = konst.
 I. Elektrostatik ==================================================================. Das elektrische Feld eines Plattenkondensators Ein Plattenkondensator besteht aus zwei sich parallel gegenüberliegenden
I. Elektrostatik ==================================================================. Das elektrische Feld eines Plattenkondensators Ein Plattenkondensator besteht aus zwei sich parallel gegenüberliegenden
Literatur. Supramolecular Chemistry, 2nd edition Jonathan W. Steed, Jerry L. Atwood Wiley
 A. Schiller Inhalt Einleitung Grundlagen Rezeptoren für Kationen Rezeptoren für Anionen Supramolekulare Koordinationschemie Rotaxane und Catenane Molekulare Maschinen Supramolekulare Katalyse FSU Jena
A. Schiller Inhalt Einleitung Grundlagen Rezeptoren für Kationen Rezeptoren für Anionen Supramolekulare Koordinationschemie Rotaxane und Catenane Molekulare Maschinen Supramolekulare Katalyse FSU Jena
Zwischenklausur Physik I für MWWT
 Prof. Martin H. Müser Lehrstuhl f. Materialsimulation Universität des Saarlandes 17. 12. 2011 Name: Zwischenklausur Physik I für MWWT Matrikelnummer: Die sechs besten Punktezahlen aus den acht reguären
Prof. Martin H. Müser Lehrstuhl f. Materialsimulation Universität des Saarlandes 17. 12. 2011 Name: Zwischenklausur Physik I für MWWT Matrikelnummer: Die sechs besten Punktezahlen aus den acht reguären
n = V Lsg m n l mol Grundwissen 9. Klasse Chemie (NTG) Analytische Chemie Stoffmenge n Molare Masse M Molares Volumen V M Stoffmengenkonzentration c
 Grundwissen 9. Klasse Chemie (NTG) 1. Analytische Chemie und Stöchiometrie Analytische Chemie Untersuchung von Reinstoffen und Stoffgemischen mit dem Ziel diese eindeutig zu identifizieren (= qualitativer
Grundwissen 9. Klasse Chemie (NTG) 1. Analytische Chemie und Stöchiometrie Analytische Chemie Untersuchung von Reinstoffen und Stoffgemischen mit dem Ziel diese eindeutig zu identifizieren (= qualitativer
12. Elektrodynamik Quellen von Magnetfeldern 12.2 Das Ampere sche Gesetz 12.3 Magnetische Induktion 12.4 Lenz sche Regel 12.5 Magnetische Kraft
 12. Elektrodynamik 12.1 Quellen von Magnetfeldern 12.2 Das Ampere sche Gesetz 12.3 Magnetische Induktion 12.4 Lenz sche Regel 12.5 Magnetische Kraft 12. Elektrodynamik Beobachtungen zeigen: - Kommt ein
12. Elektrodynamik 12.1 Quellen von Magnetfeldern 12.2 Das Ampere sche Gesetz 12.3 Magnetische Induktion 12.4 Lenz sche Regel 12.5 Magnetische Kraft 12. Elektrodynamik Beobachtungen zeigen: - Kommt ein
3.4 Magnetfelder. µ im Magnetfeld Æ B ein Drehmoment. M = Æ µ Æ B.
 - 151-3.4 Magnetfelder 3.4.1 Grundlagen Während die Wechselwirkungen zwischen statischen elektrischen Ladungen sich durch das Coulomb'sche Gesetz, resp. ein elektrisches Feld beschreiben lassen, treten
- 151-3.4 Magnetfelder 3.4.1 Grundlagen Während die Wechselwirkungen zwischen statischen elektrischen Ladungen sich durch das Coulomb'sche Gesetz, resp. ein elektrisches Feld beschreiben lassen, treten
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie. Allgemeine Chemie. Rückblick auf vorherige Übung
 Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
bestimmte mehratomige Anionen mit Sauerstoff werden mit dem lateinischen Namen benannt und enden auf at.
 DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
Dissoziation, ph-wert und Puffer
 Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Chemische Bindung. Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung
 Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
