SOPs, Arbeitsanweisungen & Co.
|
|
|
- Hansl Eberhardt
- vor 6 Jahren
- Abrufe
Transkript
1 SOPs, Arbeitsanweisungen & Co. Arbeitsabläufe richtig dokumentieren Jasmin Schäfer Bettina Merker-Pfister StuKo Treffen in Frankfurt,
2 Agendapunkt Agenda Block 1 SOPs, Arbeitsanweisungen & Co. Block 2 Praktische Gestaltung Typische Abläufe Block 3 Praktische Gestaltung Schnittstelle Apotheke Block 4 Praktische Gestaltung Individuelle Abläufe Details Grundsätzliches (Refresher) Regularien Schwache SOPs, Formale Anforderung an eine SOP Klassische und studienrelevante SOPs Gliederung einer SOP Flussdiagramm Welche Fehler treten in der Praxis am häufigsten auf? Erarbeitung des Prozesses Patienteneinschluss Ansicht von realen SOP Beispielen Erarbeitung des Prozesses Temperaturabweichung bei Medikationslagerung Erarbeitung des Prozesses Schnittstelle Apotheke Entwicklung einer SOP an einem Prozess Ihrer Wahl Erfahrungsaustausch Welche Abläufe sind lückenhaft, unklar, veraltet?
3 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Welche Regularien fordern SOPs? GXP (GCP, GLP, GVP, GMP, GDP ) ISO 9001:2008 und ISO 9001:2015 (Kap 4) EFQM AMG ( 63b) Europäische Richtlinien (2001/20/EG, 2005/28/EG) Chemikaliengesetz EU GMP Leitfaden Kap CFR part u (USA, Gesetze der FDA) u.a. 3
4 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Welche Schwächen von SOPs kennen Sie aus der Praxis? o Zu lang / zu ausführlich o Zu kurz / zu oberflächlich o Widersprüchlich / inkonsistent o Inhaltlich falsch oder veraltet o Verantwortlichkeiten unklar o Unvollständig o Unzureichendes Training von neuen oder komplexen SOPs o Sprachlich un- oder missverständlich o Schlechte Akzeptanz (Prozess wurde vor Freigabe mit Betroffenen nicht besprochen) 4
5 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Was sind die Konsequenzen von schwachen SOPs? o Fehler o Missverständnisse o Frustration o Ineffizientes Arbeiten und Mehrarbeit o Lücken im System o Beanstandungen in Audits und Inspektionen daran wollen wir arbeiten! 5
6 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Was sind formale Anforderungen an eine SOP? o Aktualität o Versionskontrolle o Schriftform o Anwendungsbereich und Zweck sollen klar werden o Vollständigkeit (Inhaltsverzeichnis oder Seitenzahlen) o Genauigkeit o Richtigkeit (4-Augen-Prinzip) o Genehmigung o Verfügbarkeit 6
7 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Warum brauchen wir SOPs bei unserer Arbeit? Damit wir gleichbleibende Qualität sicherstellen können Damit wir uns kontinuierlich verbessern können Damit wir uns leichter einarbeiten können Damit qualitätsrelevante Arbeiten von jedem (personenunabhängig) auf Anhieb richtig gemacht werden (reproduzierbar, nachvollziehbar, standardisiert und zulassungskonform) 7
8 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Welche klassischen SOPs sollte es in jedem QMS geben? o Risiko Management o Abweichungsmanagement (Deviation Management, CAPAs) o Fehlerursachenanalyse (Root Cause Analysis) o Änderungsmanagement (Change Control/Management) o Einarbeitung und Training o Prozessdokumentation o Kontinuierliche (Prozess-)Optimierung o Quality Control / Quality Management o Validierung von Computersystemen o Audit & Inspektionsmanagement o Krisen Management 8
9 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Welche studienrelevanten SOPs kennen Sie? o Patientenaufklärung o Screening und (ggfs.) Randomisierung o Studienmedikation (Buchführung, Aufbewahrung, Verabreichung) o AE/SAE Dokumentation und Meldung o Dokumentation und Dokumentenmanagement (Patientenakten, Prüfarztordner, Worksheets, CRF etc.) o Kalibrierung von Laborgeräten o Studienspezifische SOPs o Schnittstellenbeschreibung (Apotheke, Labor, Radiologie ) o Vertretungsregelung und Delegierung von Aufgaben 9
10 Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Wie sollte eine SOP gegliedert sein? Titel Namentliche Nennung der Autoren Freigabe durch wen und wann (inkl. Versionsnummer) Historie (Aufführung von Änderungen) Ziel/Zweck (Festlegung einer einheitlichen Vorgehensweise Geltungsbereich (für welche Abteilung/Personenkreis gültig) Glossar (Definition verwendeter Begrifflichkeiten/Abkürzungen) Verantwortlichkeiten/Prozess (konkrete Darstellung; wer macht was, wann und wie) 10
11 Pharmacy Study Nurse Investigator Grundsätzliches - SOPs, Arbeitsanweisungen & Co. Beispiel für Flussdiagramm END Patient enrolment Successful? NO Check & administer IP Create & send IP request YES Prepare infusion 11
12 Praktische Gestaltung 1: Typische Fehler Welche Fehler treten in der Praxis am häufigsten auf? Temperaturabweichung bei Medikationslagerung (Kühlschrank) Falsche Medikationsausgabe an Patienten (IxRS) Einschluss von nicht passenden Patienten ICF inkorrekte Version / kein Prüfer / inkomplett Verspätete SAE Meldung 12
13 Praktische Gestaltung 1: Patienteneinschluss Stellen Sie den Prozess Patienteneinschluss graphisch dar Beschreiben Sie die Arbeitsabläufe mit dem angemessenen Detailgrad Wer ist für was verantwortlich? Zeitliche Abfolge der Arbeitsschritte Welche Schritte sind zeitkritisch? Wo treten oft Fehler auf? Was wird wann, von wem und wo dokumentiert? Stellvertreterregelung? Wer ist aktiv/unterstützend involviert (Durchführung, Beteiligung) und wer muss nur informiert werden? 13
14 Ansicht von Beispiel SOPs Wir zeigen Ihnen jetzt 5 Beispiel SOPs was fällt Ihnen auf? 14
15 Praktische Gestaltung1: Temp.-Abweichung Stellen Sie den Prozess zu Temperaturabweichung bei Medikationslagerung graphisch dar 15
16 Praktische Gestaltung 2: Schnittstelle Apotheke Stellen Sie den Informationsfluss Klinik Apotheke graphisch dar Wer ist für was verantwortlich? Zeitliche Abfolge der Arbeitsschritte Welche Schritte sind zeitkritisch? Stellvertreterregelung? Wie sollte die Kommunikation idealerweise laufen? 16
17 Praktische Gestaltung 3: Individuelle Abläufe Erarbeiten Sie eine SOP zum Thema Ihrer Wahl Erfahrungsaustausch Welche Abläufe sind in ihrer Praxis lückenhaft oder unklar dargestellt? Welche Abläufe laufen unrund? 17
SOPs zur Studienabwicklung am Zentrum
 SOPs zur Studienabwicklung am Zentrum Studienkoordinatorentreffen 02. März 2016 Kathrin Seidel Roland Arndt Klinisches Monitoring & Auditing, GBG Forschungs GmbH Workshop Agenda Standardarbeitsanweisungen
SOPs zur Studienabwicklung am Zentrum Studienkoordinatorentreffen 02. März 2016 Kathrin Seidel Roland Arndt Klinisches Monitoring & Auditing, GBG Forschungs GmbH Workshop Agenda Standardarbeitsanweisungen
GCP-Routineinspektionen im Rahmen von klinischen Prüfungen - Ein Erfahrungsbericht -
 GCP-Routineinspektionen im Rahmen von klinischen Prüfungen - Ein Erfahrungsbericht - Katharina Thorn 11. DVMD-Fachtagung, Hannover Inspektionen / Audits GCP-Inspektionen im Rahmen von Zulassungsverfahren
GCP-Routineinspektionen im Rahmen von klinischen Prüfungen - Ein Erfahrungsbericht - Katharina Thorn 11. DVMD-Fachtagung, Hannover Inspektionen / Audits GCP-Inspektionen im Rahmen von Zulassungsverfahren
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v.
 Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Qualitätsmanagement in klinischen Prüfungen
 Qualitätsmanagement in klinischen Prüfungen Dr. Bärbel Witte und Medizinprodukte FG Klinische Prüfungen - GCP Inspektionen Themen Richtlinien, nach denen Qualitäts- Management in klinischen Prüfungen gefordert
Qualitätsmanagement in klinischen Prüfungen Dr. Bärbel Witte und Medizinprodukte FG Klinische Prüfungen - GCP Inspektionen Themen Richtlinien, nach denen Qualitäts- Management in klinischen Prüfungen gefordert
Patientenscreening und -einschluss
 Patientenscreening und -einschluss Version: 2.0.3 Gültig ab: 10. Februar 2015 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Julia Maurer Astrid Mattes, Klaus Ehrlich Klaus Ehrlich Klaus
Patientenscreening und -einschluss Version: 2.0.3 Gültig ab: 10. Februar 2015 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Julia Maurer Astrid Mattes, Klaus Ehrlich Klaus Ehrlich Klaus
Patientenscreening und -einschluss
 Patientenscreening und -einschluss Version: 2.0.4 Gültig ab: 22. November 2017 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: nicht festgelegt Silke Purschke, Julia Maurer Klaus Ehrlich
Patientenscreening und -einschluss Version: 2.0.4 Gültig ab: 22. November 2017 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: nicht festgelegt Silke Purschke, Julia Maurer Klaus Ehrlich
Qualitätsmanagement in klinischen Prüfungen
 Qualitätsmanagement in klinischen Prüfungen Dr. Katalina Mettke GCP Inspektorin FG GCP-Inspektionen 17. Januar 2017 Ringvorlesung QM K. Mettke 17.01.2017 Seite 1 Inhaltsverzeichnis 1. Was ist Qualitätsmanagement
Qualitätsmanagement in klinischen Prüfungen Dr. Katalina Mettke GCP Inspektorin FG GCP-Inspektionen 17. Januar 2017 Ringvorlesung QM K. Mettke 17.01.2017 Seite 1 Inhaltsverzeichnis 1. Was ist Qualitätsmanagement
Aktuelles aus dem GCP Bereich - Tätigkeitsbericht 2013 & Häufige Mängel
 Aktuelles aus dem GCP Bereich - Tätigkeitsbericht 2013 & Häufige Mängel DI(FH) Abteilung Klinische Prüfung Institut Überwachung AGES Gespräch Wien, 25. November 2014 www.ages.at Österreichische Agentur
Aktuelles aus dem GCP Bereich - Tätigkeitsbericht 2013 & Häufige Mängel DI(FH) Abteilung Klinische Prüfung Institut Überwachung AGES Gespräch Wien, 25. November 2014 www.ages.at Österreichische Agentur
Ressourcenplanung am Prüfzentrum Dorothee Arenz
 Ressourcenplanung am Prüfzentrum 11.03.2017 Dorothee Arenz Aufgaben des Prüfzentrums Sicherstellen des protokollgerechten Ablaufs der Studienbehandlung Externe Instanzen Ethikkommission Behörden Studienzentrale
Ressourcenplanung am Prüfzentrum 11.03.2017 Dorothee Arenz Aufgaben des Prüfzentrums Sicherstellen des protokollgerechten Ablaufs der Studienbehandlung Externe Instanzen Ethikkommission Behörden Studienzentrale
Grundlagen für die Durchführung klinischer Studien Nadine Röthling 05.11.2014, Praxistag Study Nurse
 SOPs für Prüfzentren Grundlagen für die Durchführung klinischer Studien Nadine Röthling 05.11.2014, Praxistag Study Nurse Standard Operating Procedures eilt nicht unbedingt der Ruf voraus, ein interessantes
SOPs für Prüfzentren Grundlagen für die Durchführung klinischer Studien Nadine Röthling 05.11.2014, Praxistag Study Nurse Standard Operating Procedures eilt nicht unbedingt der Ruf voraus, ein interessantes
Bearbeitung von Abweichungen - Checkliste
 Bearbeitung von Abweichungen - Checkliste Festlegen der Begriffe Definition des Begriffs Abweichung Festlegung der Bereiche/Abteilungen, für die dieses Abweichungsmanagement Anwendung findet Klassifizierung
Bearbeitung von Abweichungen - Checkliste Festlegen der Begriffe Definition des Begriffs Abweichung Festlegung der Bereiche/Abteilungen, für die dieses Abweichungsmanagement Anwendung findet Klassifizierung
Was ist anders bei Studien mit Medizinprodukten?
 Was ist anders bei Studien mit Medizinprodukten? CHRISTIAN WOLFLEHNER DR. ROBERT HEINZ & PARTNER GMBH CW RESEARCH & MANAGEMENT GMBH DACH SYMPOSIUM FREIBURG 07-MAR-2016 AMG versus MPG 2 Sehr viel Deckungsgleichheit
Was ist anders bei Studien mit Medizinprodukten? CHRISTIAN WOLFLEHNER DR. ROBERT HEINZ & PARTNER GMBH CW RESEARCH & MANAGEMENT GMBH DACH SYMPOSIUM FREIBURG 07-MAR-2016 AMG versus MPG 2 Sehr viel Deckungsgleichheit
Liste aller Anforderungen aus dem Bereich Studienzentren. Der Dokumentstatus wird nicht berücksichtigt.
 Liste aller Anforderungen aus dem Bereich Studienzentren. Der Dokumentstatus wird nicht berücksichtigt. 1. Studienzentren 1.1. Infrastruktur des Studienzentrums 1.1.1. Räumlichkeiten 1.1.1.1. Therapieeinrichtung
Liste aller Anforderungen aus dem Bereich Studienzentren. Der Dokumentstatus wird nicht berücksichtigt. 1. Studienzentren 1.1. Infrastruktur des Studienzentrums 1.1.1. Räumlichkeiten 1.1.1.1. Therapieeinrichtung
Hintergrund. Elektronische Archivierung von Patienten- und Forschungsunterlagen: Technik, Prozesse, Standards
 Elektronische Archivierung von Patienten- und Forschungsunterlagen: Technik, Prozesse, Standards Auditierung von digitalen Archiven nach GCP 18-Jan-2012 TMF e.v., Berlin, DE Rita Hattemer-Apostel CEO,
Elektronische Archivierung von Patienten- und Forschungsunterlagen: Technik, Prozesse, Standards Auditierung von digitalen Archiven nach GCP 18-Jan-2012 TMF e.v., Berlin, DE Rita Hattemer-Apostel CEO,
Systemvalidierung der Studiensoftware eresearch Network am Koordinierungszentrum für f r Klinische Studien DüsseldorfD. Dimitrios Venizeleas
 Systemvalidierung der Studiensoftware eresearch Network am Koordinierungszentrum für f r Klinische Studien DüsseldorfD Dimitrios Venizeleas AG Datenmanagement Koordinierungszentrum für Klinische Studien
Systemvalidierung der Studiensoftware eresearch Network am Koordinierungszentrum für f r Klinische Studien DüsseldorfD Dimitrios Venizeleas AG Datenmanagement Koordinierungszentrum für Klinische Studien
Qualitätssicherung am Prüfzentrum Sponsor Audits
 Qualitätssicherung am Prüfzentrum Sponsor Audits 8. März 2016, Nadja Pöhl-Koch DACH Symposium Freiburg Agenda Einleitung und Übersicht aktuelle Zahlen Audit Readiness- was ist zu beachten? Zusammenfassung
Qualitätssicherung am Prüfzentrum Sponsor Audits 8. März 2016, Nadja Pöhl-Koch DACH Symposium Freiburg Agenda Einleitung und Übersicht aktuelle Zahlen Audit Readiness- was ist zu beachten? Zusammenfassung
Übersicht über ISO 9001:2000
 Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
1.1 Historie von FitSM Der Aufbau von FitSM FitSM als leichtgewichtiger Ansatz... 6
 xv 1 Einführung 1 1.1 Historie von FitSM....................................... 2 1.2 Der Aufbau von FitSM.................................... 4 1.3 FitSM als leichtgewichtiger Ansatz...........................
xv 1 Einführung 1 1.1 Historie von FitSM....................................... 2 1.2 Der Aufbau von FitSM.................................... 4 1.3 FitSM als leichtgewichtiger Ansatz...........................
Praktische Erfahrungen der Überwachungsbehörden der Länder
 Praktische Erfahrungen der Überwachungsbehörden der Länder PMS-Workshop, 29.09.2005 Auswirkungen der 12. AMG-Novelle auf die klinische Forschung in Deutschland Dr. Sabine Paris Zentralstelle der Länder
Praktische Erfahrungen der Überwachungsbehörden der Länder PMS-Workshop, 29.09.2005 Auswirkungen der 12. AMG-Novelle auf die klinische Forschung in Deutschland Dr. Sabine Paris Zentralstelle der Länder
Aufklärung des Patienten und Einholen der Einwilligung
 Aufklärung des Patienten und Einholen der Einwilligung Version: 2.1.0 Gültig ab: 12. Februar 2015 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Julia Maurer Astrid Mattes, Klaus Ehrlich
Aufklärung des Patienten und Einholen der Einwilligung Version: 2.1.0 Gültig ab: 12. Februar 2015 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Julia Maurer Astrid Mattes, Klaus Ehrlich
Aufklärung des Patienten und Einholen der Einwilligung
 Aufklärung des Patienten und Einholen der Einwilligung Version: 2.0.1 Gültig ab: 01. Januar 2015 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Julia Maurer Astrid Mattes, Klaus Ehrlich
Aufklärung des Patienten und Einholen der Einwilligung Version: 2.0.1 Gültig ab: 01. Januar 2015 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Julia Maurer Astrid Mattes, Klaus Ehrlich
Translational Research Herausforderung für das Monitoring?
 Translational Research Herausforderung für das Monitoring? Karin Huber, M.Sc., Head of Monitoring CTC Nadine Bosbach, M.Sc., CRA Definition Translational Research Erste Zitate um 1993 Definitionen (T1,
Translational Research Herausforderung für das Monitoring? Karin Huber, M.Sc., Head of Monitoring CTC Nadine Bosbach, M.Sc., CRA Definition Translational Research Erste Zitate um 1993 Definitionen (T1,
BASISWISSEN PHARMAKOVIGILANZ I - VII
 BASISWISSEN PHARMAKOVIGILANZ I - VII 24. Februar 17. März 14. April 5. Mai 2. Juni 23. Juni 2015 Gesetzliche und regulatorische Grundlagen ( Wo steht das? ) Veränderungen und Konsequenzen ( Vom Stufenplanbeauftragten
BASISWISSEN PHARMAKOVIGILANZ I - VII 24. Februar 17. März 14. April 5. Mai 2. Juni 23. Juni 2015 Gesetzliche und regulatorische Grundlagen ( Wo steht das? ) Veränderungen und Konsequenzen ( Vom Stufenplanbeauftragten
Checkliste ISO/IEC 27001:2013 Dokumente und Aufzeichnungen
 Checkliste ISO/IEC 27001:2013 Dokumente und Aufzeichnungen Version: 1.1 Datum: 01.06.2016 Änderungsverfolgung Version Datum Geänderte Seiten / Kapitel Autor Bemerkungen 1.0 07.01.2016 Alle F. Thater Initiale
Checkliste ISO/IEC 27001:2013 Dokumente und Aufzeichnungen Version: 1.1 Datum: 01.06.2016 Änderungsverfolgung Version Datum Geänderte Seiten / Kapitel Autor Bemerkungen 1.0 07.01.2016 Alle F. Thater Initiale
PTS Training Service: Archivierung, Annex 11, Part 11. Annex 11. aus Sicht eines GMP Inspektors
 PTS Training Service: Archivierung, Annex 11, Part 11 Annex 11 aus Sicht eines GMP Inspektors Klaus Eichmüller c/o Regierung von Oberbayern ZAB Speyer, 1 Annex 11 Rechtsgrundlagen GS (GMP keine Beeinträchtigung
PTS Training Service: Archivierung, Annex 11, Part 11 Annex 11 aus Sicht eines GMP Inspektors Klaus Eichmüller c/o Regierung von Oberbayern ZAB Speyer, 1 Annex 11 Rechtsgrundlagen GS (GMP keine Beeinträchtigung
https://www.zlg.de/arzneimittel/qualitaetssystem/qualitaetssicherungshandbuch.html
 Anlage 1 PZ-QS01 1 Klinikkopf Checkliste Vor- und Nachbereitung Audits und Inspektionen Checkliste Vor- und Nachbereitung Audits und Inspektionen https://www.zlg.de/arzneimittel/qualitaetssystem/qualitaetssicherungshandbuch.html
Anlage 1 PZ-QS01 1 Klinikkopf Checkliste Vor- und Nachbereitung Audits und Inspektionen Checkliste Vor- und Nachbereitung Audits und Inspektionen https://www.zlg.de/arzneimittel/qualitaetssystem/qualitaetssicherungshandbuch.html
Studienkurztitel.: Monitoringbesuch Nr.: Prüfzentrums-Nr.: ggf. EudraCT Nr.: Besuchsdatum: On site von bis
 MO03-H-A1 1 Klinikkopf / KKS / Studienzentrale Bericht/Checkliste Besuch während der klinischen Prüfung Studienkurztitel.: Monitoringbesuch Nr.: Prüfzentrums-Nr.: ggf. EudraCT Nr.: Besuchsdatum: On site
MO03-H-A1 1 Klinikkopf / KKS / Studienzentrale Bericht/Checkliste Besuch während der klinischen Prüfung Studienkurztitel.: Monitoringbesuch Nr.: Prüfzentrums-Nr.: ggf. EudraCT Nr.: Besuchsdatum: On site
Das Kölner Sponsor Modell What s new?
 Das Kölner Sponsor Modell What s new? Dr. Christine Georgias Leitung Qualitätssicherung für klinische Prüfungen Forschungsdekanat der Medizinischen Fakultät Inhalt Neues: Formales Prozesse Bewährtes Zusammenfassung
Das Kölner Sponsor Modell What s new? Dr. Christine Georgias Leitung Qualitätssicherung für klinische Prüfungen Forschungsdekanat der Medizinischen Fakultät Inhalt Neues: Formales Prozesse Bewährtes Zusammenfassung
Stellenbeschreibung Fachtechnisch verantwortliche Person (FvP) Pharmalogistik
 Stellenbeschreibung (FvP) Pharmalogistik Funktionsbezeichnung: Vorgesetzte Stelle: Stellvertreter: Frau Monika Muster Herr Markus Muster Anforderungen an die Schweizer Gesetzgebung Die FvP respektiert
Stellenbeschreibung (FvP) Pharmalogistik Funktionsbezeichnung: Vorgesetzte Stelle: Stellvertreter: Frau Monika Muster Herr Markus Muster Anforderungen an die Schweizer Gesetzgebung Die FvP respektiert
Die QM-System. System- Dokumentaion
 Die QM-System System- Dokumentaion QM-Handbuch (QM-H) Allgemeiner Teil der QM-System Dokumentation, zu deren Gestaltung es keine verbindlichen Vorschriften gibt Im QM-H H sollte immer beschrieben und vorgestellt
Die QM-System System- Dokumentaion QM-Handbuch (QM-H) Allgemeiner Teil der QM-System Dokumentation, zu deren Gestaltung es keine verbindlichen Vorschriften gibt Im QM-H H sollte immer beschrieben und vorgestellt
Umsetzung der Rili-BÄK 2008 Erfahrungen der Überwachungsbehörde in Sachsen
 Umsetzung der Rili-BÄK 2008 Erfahrungen der Überwachungsbehörde in Sachsen 1 22. November 2011 Gabriele Schmidt Rechtliche Grundlagen In 4a MPBetreibV Verankerung der Richtlinie der Bundesärztekammer zur
Umsetzung der Rili-BÄK 2008 Erfahrungen der Überwachungsbehörde in Sachsen 1 22. November 2011 Gabriele Schmidt Rechtliche Grundlagen In 4a MPBetreibV Verankerung der Richtlinie der Bundesärztekammer zur
ISO 9001:2015 Delta Audits und Neuerungen der Norm. Claus Engler, Produktmanager für Risikomanagementsysteme, TÜV SÜD Management Service GmbH
 ISO 9001:2015 Delta Audits und Neuerungen der Norm Claus Engler, Produktmanager für Risikomanagementsysteme, TÜV SÜD Management Service GmbH Agenda Revision ISO 9001:2015 und Übergangsfrist Definition
ISO 9001:2015 Delta Audits und Neuerungen der Norm Claus Engler, Produktmanager für Risikomanagementsysteme, TÜV SÜD Management Service GmbH Agenda Revision ISO 9001:2015 und Übergangsfrist Definition
- Leseprobe - Auditfeststellungen und deren Bewertungen. Auditfeststellungen und deren Bewertungen. von Ralph Meß
 Auditfeststellungen und deren Bewertungen von Ralph Meß Der folgende Artikel beschreibt mögliche Feststellungen und Ergebnisse, die üblicherweise bei internen oder externen Audits dokumentiert werden können.
Auditfeststellungen und deren Bewertungen von Ralph Meß Der folgende Artikel beschreibt mögliche Feststellungen und Ergebnisse, die üblicherweise bei internen oder externen Audits dokumentiert werden können.
Vorgehensweise zur Einführung der ISO/IEC 27001: Sven Schulte
 - Sven Schulte Agenda Prozessüberblick Projektplanung / Projekteinführung Einführungsschulung Bestandsaufnahme Aktionsplan Projektumsetzung Aufgabenzuordnung Dokumentation Internes Audit Managementbewertung
- Sven Schulte Agenda Prozessüberblick Projektplanung / Projekteinführung Einführungsschulung Bestandsaufnahme Aktionsplan Projektumsetzung Aufgabenzuordnung Dokumentation Internes Audit Managementbewertung
Begriffe und Ziele von CAPA. Elemente des CAPA Systems. CAPA im Behördenfokus. Verbesserungsmanagement mit CAPA
 Medical Devices CAPA Pharmaceuticals Christiane Uhlig Hans-Georg Pfaff Health Care Überblick Begriffe und Ziele von CAPA Elemente des CAPA Systems CAPA im Behördenfokus Verbesserungsmanagement mit CAPA
Medical Devices CAPA Pharmaceuticals Christiane Uhlig Hans-Georg Pfaff Health Care Überblick Begriffe und Ziele von CAPA Elemente des CAPA Systems CAPA im Behördenfokus Verbesserungsmanagement mit CAPA
QualityRiskManagement
 QualityRiskManagement Workshop Bernd Bödecker GAA Hannover GMP-Gesprächskreis Niedersachsen Abbott Products GmbH, 8. November 2011 Ziele des Workshops (Vorschlag) o Gelegenheit zur allgemeinen Information
QualityRiskManagement Workshop Bernd Bödecker GAA Hannover GMP-Gesprächskreis Niedersachsen Abbott Products GmbH, 8. November 2011 Ziele des Workshops (Vorschlag) o Gelegenheit zur allgemeinen Information
Zentrale Arzneimittelüberwachung Bayern GCP- Fortbildungsveranstaltung am in München Qualität in klinischen Arzneimittelstudien am Menschen
 Zentrale Arzneimittelüberwachung Bayern GCP- Fortbildungsveranstaltung am 17.09.2009 in München Qualität in klinischen Arzneimittelstudien am Menschen Findings bei der Inspektion klinischer Prüfungen durch
Zentrale Arzneimittelüberwachung Bayern GCP- Fortbildungsveranstaltung am 17.09.2009 in München Qualität in klinischen Arzneimittelstudien am Menschen Findings bei der Inspektion klinischer Prüfungen durch
Was ist ein Lastenheft?
 Lastenheft Was ist ein Lastenheft? Wann wird ein Lastenheft erstellt? Wozu wird ein Lastenheft erstellt? Was beinhaltet ein Lastenheft? Wer erstellt ein Lastenheft? Wie wird ein Lastenheft erstellt? Was
Lastenheft Was ist ein Lastenheft? Wann wird ein Lastenheft erstellt? Wozu wird ein Lastenheft erstellt? Was beinhaltet ein Lastenheft? Wer erstellt ein Lastenheft? Wie wird ein Lastenheft erstellt? Was
PEFC SCHWEIZ NORMATIVES DOKUMENT ND 003. Anforderungen zur Zertifizierung auf Ebene eines Betriebes
 PEFC SCHWEIZ NORMATIVES DOKUMENT ND 003 Anforderungen zur Zertifizierung auf Ebene eines Betriebes verabschiedet durch das Lenkungsgremium am 3. April 2007 Inhaltsverzeichnis 4.1. ANTRAGSTELLER: EINZELBETRIEB
PEFC SCHWEIZ NORMATIVES DOKUMENT ND 003 Anforderungen zur Zertifizierung auf Ebene eines Betriebes verabschiedet durch das Lenkungsgremium am 3. April 2007 Inhaltsverzeichnis 4.1. ANTRAGSTELLER: EINZELBETRIEB
GCP-Workshop Adäquate Dokumentation SAE-Handling Handling von Study Drugs / IP. Bettina Merker-Pfister
 GCP-Workshop Adäquate Dokumentation SAE-Handling Handling von Study Drugs / IP Bettina Merker-Pfister Was ist GCP? GCP ist die Abkürzung für Good Clinical Practice = wissenschaftlich-ethischer Qualitätsstandard
GCP-Workshop Adäquate Dokumentation SAE-Handling Handling von Study Drugs / IP Bettina Merker-Pfister Was ist GCP? GCP ist die Abkürzung für Good Clinical Practice = wissenschaftlich-ethischer Qualitätsstandard
Einsparpotenziale bei der Validierung computergestützter Systeme
 Einsparpotenziale bei der Validierung computergestützter Systeme Die Stellschrauben zur Optimierung Kostenpotenziale GAMP 5 Risikobasiertes Vorgehen Lieferanten einbinden Standardisierung nutzen SOPs optimieren
Einsparpotenziale bei der Validierung computergestützter Systeme Die Stellschrauben zur Optimierung Kostenpotenziale GAMP 5 Risikobasiertes Vorgehen Lieferanten einbinden Standardisierung nutzen SOPs optimieren
Facility Management im GMP regulierten Umfeld ein Bericht aus der Praxis
 Facility Management im GMP regulierten Umfeld ein Bericht aus der Praxis Facility Management im GMP regulierten Umfeld ein Bericht aus der Praxis 1. GMP - Definition und Ziel 2. Gesetze, Verordnungen,
Facility Management im GMP regulierten Umfeld ein Bericht aus der Praxis Facility Management im GMP regulierten Umfeld ein Bericht aus der Praxis 1. GMP - Definition und Ziel 2. Gesetze, Verordnungen,
Normerfüllung in der Praxis am Beispiel "Tool Qualification" Dr. Anne Kramer, sepp.med gmbh
 Normerfüllung in der Praxis am Beispiel "Tool Qualification" Dr. Anne Kramer, sepp.med gmbh Über uns Mittelständischer IT-Service Provider 30 Jahre Industrieerfahrung Unsere Referenzen Medizintechnik Pharma
Normerfüllung in der Praxis am Beispiel "Tool Qualification" Dr. Anne Kramer, sepp.med gmbh Über uns Mittelständischer IT-Service Provider 30 Jahre Industrieerfahrung Unsere Referenzen Medizintechnik Pharma
Qualitätsmanagement kompakt, 13.09.2016 in Wiesbaden
 Qualitätsmanagement kompakt, 13.09.2016 in Wiesbaden Qualitätsmanagement für Nicht QS und Neu QS-Mitarbeiter Qualität leicht verständlich erklärt QS-, GMP- und GDP-Wissen für Fachabteilungen Aktuelle Regelwerke
Qualitätsmanagement kompakt, 13.09.2016 in Wiesbaden Qualitätsmanagement für Nicht QS und Neu QS-Mitarbeiter Qualität leicht verständlich erklärt QS-, GMP- und GDP-Wissen für Fachabteilungen Aktuelle Regelwerke
Studienregistrierung. Version: Gültig ab: 23. August Anmerkungen Das vorliegende Dokument ist eine Druckversion
 Studienregistrierung Version: 3.0.2 Gültig ab: 23. August 2016 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Astrid Mattes Emelie Müller, Julia Maurer Klaus Ehrlich Klaus Ehrlich Anmerkungen
Studienregistrierung Version: 3.0.2 Gültig ab: 23. August 2016 Erstellt durch: Review durch: Freigabe durch: Ansprechperson: Astrid Mattes Emelie Müller, Julia Maurer Klaus Ehrlich Klaus Ehrlich Anmerkungen
Die Kunst, Normen sinnvoll in einem Unternehmen umzusetzen. DI (FH) Susanne Keil
 Die Kunst, Normen sinnvoll in einem Unternehmen umzusetzen DI (FH) Susanne Keil Normen- 08/15? Das Militär entdeckt die Norm 1918: Die erste DIN war ein Waffenteil: DIN 1 Kegelstifte 1922: Einheitliche
Die Kunst, Normen sinnvoll in einem Unternehmen umzusetzen DI (FH) Susanne Keil Normen- 08/15? Das Militär entdeckt die Norm 1918: Die erste DIN war ein Waffenteil: DIN 1 Kegelstifte 1922: Einheitliche
Abweichungen. AG 7 Abweichungsmanagement 16. August 2010, Dr. Andrea Behrenswerth
 2010 Abweichungen DIN ISO 15378 Primärpackmittel für Arzneimittel Besondere Anforderungen für die Anwendung von ISO 9001:2000 entsprechend der Guten Herstellungspraxis (GMP) AG 7 Abweichungsmanagement
2010 Abweichungen DIN ISO 15378 Primärpackmittel für Arzneimittel Besondere Anforderungen für die Anwendung von ISO 9001:2000 entsprechend der Guten Herstellungspraxis (GMP) AG 7 Abweichungsmanagement
Nachvollziehbarkeit - sehr gut verständlich, klare innere Zusammenhänge zwischen den einzelnen Teilen der Planung
 Beurteilung DHD-Dossier Teil A (Dokument 1 + 2) Name, Vorname xx Dokument 1: Planung Thema der Planung xx Inhaltliche Aspekte Nachvollziehbarkeit - sehr gut verständlich, klare innere Zusammenhänge zwischen
Beurteilung DHD-Dossier Teil A (Dokument 1 + 2) Name, Vorname xx Dokument 1: Planung Thema der Planung xx Inhaltliche Aspekte Nachvollziehbarkeit - sehr gut verständlich, klare innere Zusammenhänge zwischen
Information Security Management System Informationssicherheitsrichtlinie
 Information Security Management System Informationssicherheitsrichtlinie I. Dokumentinformationen Version: 0.3 Datum der Version: 08.1.017 Erstellt durch: Kristin Barteis Genehmigt durch: Hannes Boekhoff,
Information Security Management System Informationssicherheitsrichtlinie I. Dokumentinformationen Version: 0.3 Datum der Version: 08.1.017 Erstellt durch: Kristin Barteis Genehmigt durch: Hannes Boekhoff,
PROGRAMM. 1. Schulungstag: Mittwoch, von 09:00-16:30 Uhr 2. Schulungstag: Mittwoch, von 09:00-16:30 Uhr
 PROGRAMM GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG mit Wissensprüfung* ) + Teilnahmezertifikat 1. Schulungstag: Mittwoch, 30.09.2015 von 09:00-16:30
PROGRAMM GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG mit Wissensprüfung* ) + Teilnahmezertifikat 1. Schulungstag: Mittwoch, 30.09.2015 von 09:00-16:30
Lenkung der QM-Dokumentation
 Datum des LAV-Beschlusses: 08.05.2007 Seite1 von 5 Inhalt 1 Zweck, Ziel... 1 2 Geltungsbereich... 1 3 Begriffe, Definitionen... 1 4 Beschreibung... 2 4.1 Struktur der QM-Dokumentation... 2 4.2 Aufbau der
Datum des LAV-Beschlusses: 08.05.2007 Seite1 von 5 Inhalt 1 Zweck, Ziel... 1 2 Geltungsbereich... 1 3 Begriffe, Definitionen... 1 4 Beschreibung... 2 4.1 Struktur der QM-Dokumentation... 2 4.2 Aufbau der
Kalibrierung. Dok.-Nr.: Seite 1 von 6
 Seite 1 von 6 Nummer Verfaßt von: Genehmigung durch Apothekenleitung: Seite 2 von 6 Inhaltsverzeichnis 1. Gegenstand... 3 2. Geltungsbereich... 3 3. Zuständigkeiten... 3 4. Durchführung... 3 4.1 Allgemeines...
Seite 1 von 6 Nummer Verfaßt von: Genehmigung durch Apothekenleitung: Seite 2 von 6 Inhaltsverzeichnis 1. Gegenstand... 3 2. Geltungsbereich... 3 3. Zuständigkeiten... 3 4. Durchführung... 3 4.1 Allgemeines...
Strukturen zur Übernahme der Sponsorfunktion- Gut schlafen trotz Sponsorverantwortung!
 Strukturen zur Übernahme der Sponsorfunktion- Gut schlafen trotz Sponsorverantwortung! Dr. Christine Georgias Qualitätssicherung für klinische Prüfungen Forschungsdekanat der Medizinischen Fakultät Sponsor
Strukturen zur Übernahme der Sponsorfunktion- Gut schlafen trotz Sponsorverantwortung! Dr. Christine Georgias Qualitätssicherung für klinische Prüfungen Forschungsdekanat der Medizinischen Fakultät Sponsor
QM-Handbuch. der. ReJo Personalberatung
 QM-Handbuch der ReJo Personalberatung Version 2.00 vom 30.11.2012 Das QM-System der ReJo Personalberatung hat folgenden Geltungsbereich: Beratung der Unternehmen bei der Gewinnung von Personal Vermittlung
QM-Handbuch der ReJo Personalberatung Version 2.00 vom 30.11.2012 Das QM-System der ReJo Personalberatung hat folgenden Geltungsbereich: Beratung der Unternehmen bei der Gewinnung von Personal Vermittlung
Online Kalender Reinraum und GxP 10_2015. Messen Fachtagungen Events 2015
 Messen - Fachtagungen Online Kalender Reinraum und GxP 10_2015 Messen Fachtagungen Events 2015 Hygieni-Con Veranstaltungsdatum: 19.-21. Oktober 2015 Veranstalter: Hygienic Design Weihenstephan Akademie
Messen - Fachtagungen Online Kalender Reinraum und GxP 10_2015 Messen Fachtagungen Events 2015 Hygieni-Con Veranstaltungsdatum: 19.-21. Oktober 2015 Veranstalter: Hygienic Design Weihenstephan Akademie
Was passiert, wenn der Inspektor vor der Tür steht? Katharina Thorn
 Was passiert, wenn der Inspektor vor der Tür steht? Katharina Thorn Regionales Monitoring DVMD-Tagung/Erlangen / März 2006 Wer kommt zur Inspektion? Audit = Überprüfung durch Sponsor Inspektion = Überprüfung
Was passiert, wenn der Inspektor vor der Tür steht? Katharina Thorn Regionales Monitoring DVMD-Tagung/Erlangen / März 2006 Wer kommt zur Inspektion? Audit = Überprüfung durch Sponsor Inspektion = Überprüfung
Gesamtleistungsrechnung der Vergütung bei der Durchführung einer klinischen Prüfung in einem Prüfzentrum
 Gemeinsame Empfehlungen zur Erstellung einer Gesamtleistungsrechnung der Vergütung bei der Durchführung einer klinischen Prüfung in einem Prüfzentrum (finale Fassung - Stand 12. Oktober 2017) Präambel
Gemeinsame Empfehlungen zur Erstellung einer Gesamtleistungsrechnung der Vergütung bei der Durchführung einer klinischen Prüfung in einem Prüfzentrum (finale Fassung - Stand 12. Oktober 2017) Präambel
Sicherheitskonzepte für Biobanken am Beispiel von GENOMatch
 Sicherheitskonzepte für Biobanken am Beispiel von GENOMatch Tembit Software GmbH 11. Dezember 2006 Sicherheitskonzepte in der vernetzten medizinischen Forschung, TMF-Workshop Tembit Software GmbH Sicherheitskonzepte
Sicherheitskonzepte für Biobanken am Beispiel von GENOMatch Tembit Software GmbH 11. Dezember 2006 Sicherheitskonzepte in der vernetzten medizinischen Forschung, TMF-Workshop Tembit Software GmbH Sicherheitskonzepte
Die erkannten Feststellungen werden bei der Vor-Ort-Prüfung dokumentiert. Dies
 1. Vorbereitung der Inspektion Einforderung von - WPK-Handbuch qualitätsrelevanten - Organigramm Unterlagen vom - Liste der mitgeltenden Dokumente Hersteller und Formblätter - Liste der dokumentierten
1. Vorbereitung der Inspektion Einforderung von - WPK-Handbuch qualitätsrelevanten - Organigramm Unterlagen vom - Liste der mitgeltenden Dokumente Hersteller und Formblätter - Liste der dokumentierten
Aufgabenstellung zur Prozesseinheit im 3. Lehrjahr (Private HS)
 Aufgabenstellung zur Prozesseinheit im 3. Lehrjahr (Private HS) 1. Prozess und Ausgangslage 1.1. Prozess Berufsbildnerin/Berufsbildner und Lernende/r bestimmen den zu erarbeitenden Prozess aufgrund des
Aufgabenstellung zur Prozesseinheit im 3. Lehrjahr (Private HS) 1. Prozess und Ausgangslage 1.1. Prozess Berufsbildnerin/Berufsbildner und Lernende/r bestimmen den zu erarbeitenden Prozess aufgrund des
Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis?
 D A CH Symposium für klinische Prüfungen 07. und 08. März 2016, Freiburg Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis? Alexander Mion, Leiter GCP/GVP Inspektorat - Abteilung Klinische Versuche,
D A CH Symposium für klinische Prüfungen 07. und 08. März 2016, Freiburg Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis? Alexander Mion, Leiter GCP/GVP Inspektorat - Abteilung Klinische Versuche,
INHALTSVERZEICHNIS. Kapitel 1 Einführung...15. Kapitel 2 Projektmanagement...27. Vorwort...11. Autoren...12
 Inhaltsverzeichnis INHALTSVERZEICHNIS Vorwort...11 Autoren...12 Kapitel 1 Einführung...15 1.1 GMP für die Arzneimittelsicherheit...16 1.1.1 Hintergrund...16 1.1.2 Zulassung von Arzneimitteln...17 1.1.3
Inhaltsverzeichnis INHALTSVERZEICHNIS Vorwort...11 Autoren...12 Kapitel 1 Einführung...15 1.1 GMP für die Arzneimittelsicherheit...16 1.1.1 Hintergrund...16 1.1.2 Zulassung von Arzneimitteln...17 1.1.3
GESCHÄFTSPROZESSOPTIMIERUNG (GPO)
 GESCHÄFTSPROZESSOPTIMIERUNG (GPO) fotolia.com Praxisbeispiel: Geschäftsprozessoptimierung (GPO) Topographie der Prozesslandschaft neu verstehen PROZESSE WERDEN ALS KOMPLIZIERT WAHRGENOMMEN DIE QUALITÄT
GESCHÄFTSPROZESSOPTIMIERUNG (GPO) fotolia.com Praxisbeispiel: Geschäftsprozessoptimierung (GPO) Topographie der Prozesslandschaft neu verstehen PROZESSE WERDEN ALS KOMPLIZIERT WAHRGENOMMEN DIE QUALITÄT
DGQ Regionalkreis Hamburg 21.05.2012 ISO 10007. Konfigurationsmanagement
 DGQ Regionalkreis Hamburg 21.05.2012 ISO 10007 Leitfaden zum Konfigurationsmanagement g Geschichte des Konfigurationsmanagements Mit stetig steigender Produktkomplexität entstanden zunehmend Probleme (z.b.
DGQ Regionalkreis Hamburg 21.05.2012 ISO 10007 Leitfaden zum Konfigurationsmanagement g Geschichte des Konfigurationsmanagements Mit stetig steigender Produktkomplexität entstanden zunehmend Probleme (z.b.
Integriertes Risikomanagement mit GAMP 5 Risiken effizient managen!
 Integriertes Risikomanagement mit GAMP 5 Risiken effizient managen! Autor: Thomas Halfmann Halfmann Goetsch Peither AG Mit GAMP 5 wurde im Jahr 2005 der risikobasierte Ansatz in die Validierung computergestützter
Integriertes Risikomanagement mit GAMP 5 Risiken effizient managen! Autor: Thomas Halfmann Halfmann Goetsch Peither AG Mit GAMP 5 wurde im Jahr 2005 der risikobasierte Ansatz in die Validierung computergestützter
Qualitätsmanagement in der klinischen Forschung. Dr. Marc Barthold Stabsstelle Qualitätsmanagement in der klinischen Forschung
 Qualitätsmanagement in der klinischen Forschung Dr. Marc Barthold Stabsstelle Qualitätsmanagement in der klinischen Forschung KERNAUFGABEN: Sicherstellung eines funktionalen Qualitätsmanagements des Sponsors
Qualitätsmanagement in der klinischen Forschung Dr. Marc Barthold Stabsstelle Qualitätsmanagement in der klinischen Forschung KERNAUFGABEN: Sicherstellung eines funktionalen Qualitätsmanagements des Sponsors
Einführung Systemvalidierung Schulung (Modul 0) Version: V03
 Einführung Systemvalidierung Schulung (Modul 0) Version: V03 Ronald Speer LIFE Leipzig Systemvalidierung - Schulung Modul 0 - Einführung Ronald Speer Seite 1 Einleitung Studiensoftware muss GCP-konform
Einführung Systemvalidierung Schulung (Modul 0) Version: V03 Ronald Speer LIFE Leipzig Systemvalidierung - Schulung Modul 0 - Einführung Ronald Speer Seite 1 Einleitung Studiensoftware muss GCP-konform
Westdeutsche Studiengruppe WSG GmbH Women s Healthcare Study Group
 Westdeutsche Studiengruppe WSG GmbH Women s Healthcare Study Group Fragebogen zur Planung neuer klinischer Studien der WSG Ansprechpartner Titel, Vor- u. Nachname: Klinik: Abteilung: Adresse Straße: PLZ:
Westdeutsche Studiengruppe WSG GmbH Women s Healthcare Study Group Fragebogen zur Planung neuer klinischer Studien der WSG Ansprechpartner Titel, Vor- u. Nachname: Klinik: Abteilung: Adresse Straße: PLZ:
Ansicht Anzeigen Haken bei Führungslinien setzten Start Folien Zurücksetzen Basiswissen GMP
 Basiswissen GMP Inhalt: Vorgaben Gesetzliche Grundlagen Vorschriften B-CH SRK Vereinbarungen mit Fraktionierern GMP Bedeutung/Definition Was ist GMP? Was regelt GMP? Was machen wir damit? Swiss Transfusion
Basiswissen GMP Inhalt: Vorgaben Gesetzliche Grundlagen Vorschriften B-CH SRK Vereinbarungen mit Fraktionierern GMP Bedeutung/Definition Was ist GMP? Was regelt GMP? Was machen wir damit? Swiss Transfusion
Quality Management as Key Factor for Economic Success in Biotechnology
 Quality Management as Key Factor for Economic Success in Biotechnology PHATOCON (Pharm/Tox Concept) Dr. Thomas W. Becker Am Klopferspitz 19 (im IZB) 82152 Planegg/Martinsried (Germany) BioM-Technica Service
Quality Management as Key Factor for Economic Success in Biotechnology PHATOCON (Pharm/Tox Concept) Dr. Thomas W. Becker Am Klopferspitz 19 (im IZB) 82152 Planegg/Martinsried (Germany) BioM-Technica Service
LF 5: Praktikum Arbeitsblatt HBF. Gliederung:
 LF 5: Praktikum Arbeitsblatt 10 11 HBF Gliederung: 1. Deckblatt 2. Inhaltsverzeichnis 3. Beschreibung des Praktikumsbetriebes 4. Tätigkeitsberichte 4.1 Tagesberichte 4.2 Wochenberichte 4.3 Ausführliche
LF 5: Praktikum Arbeitsblatt 10 11 HBF Gliederung: 1. Deckblatt 2. Inhaltsverzeichnis 3. Beschreibung des Praktikumsbetriebes 4. Tätigkeitsberichte 4.1 Tagesberichte 4.2 Wochenberichte 4.3 Ausführliche
Version: Datum Funktion Unterschrift Erstellt
 MO03-H 1 Klinikkopf / KKS / Studienzentrale ing-besuch während der klinischen Prüfung Inhaltsverzeichnis Seite 1 Ziel...2 2 Hintergrund...2 3 Prozesse...2 3.1 Festlegung des Besuchszeitpunktes...2 3.2
MO03-H 1 Klinikkopf / KKS / Studienzentrale ing-besuch während der klinischen Prüfung Inhaltsverzeichnis Seite 1 Ziel...2 2 Hintergrund...2 3 Prozesse...2 3.1 Festlegung des Besuchszeitpunktes...2 3.2
Technische Richtlinie
 Technische Richtlinie für Erzeugungseinheiten Teil 7: Instandhaltung von Kraftwerken für Erneuerbare Energien Rubrik D2: Zustands Ereignis Ursachen Schlüssel für Erzeugungseinheiten (ZEUS) Begriffe, Klassierung
Technische Richtlinie für Erzeugungseinheiten Teil 7: Instandhaltung von Kraftwerken für Erneuerbare Energien Rubrik D2: Zustands Ereignis Ursachen Schlüssel für Erzeugungseinheiten (ZEUS) Begriffe, Klassierung
ÄNDERUNGEN UND SCHWERPUNKTE
 REVISION ISO 9001:2015 ÄNDERUNGEN UND SCHWERPUNKTE FRANKFURT, 25. JULI 2014 Folie Agenda 1. High Level Structure nach Annex SL 2. QMS Structure 3. Schwerpunkte der Änderungen Revision Iso 9001:2015 06/14
REVISION ISO 9001:2015 ÄNDERUNGEN UND SCHWERPUNKTE FRANKFURT, 25. JULI 2014 Folie Agenda 1. High Level Structure nach Annex SL 2. QMS Structure 3. Schwerpunkte der Änderungen Revision Iso 9001:2015 06/14
PROJEKT MANAGEMENT IN DER TRILUX GROUP
 PROJEKTMANAGEMENT STRUKTUR FÜR TRILUX NUTZUNG EINES EINHEITLICHEN PROJEKT-TEMPLATES PROJEKT MANAGEMENT IN DER TRILUX GROUP 16.11.2017 / 1 WO STEHEN WIR HEUTE? Zentrales Projektmanagement für Produktentwicklung
PROJEKTMANAGEMENT STRUKTUR FÜR TRILUX NUTZUNG EINES EINHEITLICHEN PROJEKT-TEMPLATES PROJEKT MANAGEMENT IN DER TRILUX GROUP 16.11.2017 / 1 WO STEHEN WIR HEUTE? Zentrales Projektmanagement für Produktentwicklung
Eingesetzte Mittel Anlagen, Methoden, Fähigkeiten, Techniken, Geld, Kapital PROZESS. Bündel oder Folge von Aktivitäten
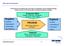 Was ist ein Prozess? Ein Prozess ist ein Bündel oder eine Folge von Aktivitäten, für die Vorgaben benötigt werden und die ein für den Kunden verwertbares Ergebnis erzeugen. Vorgaben Rohstoffe Halbfertigteile
Was ist ein Prozess? Ein Prozess ist ein Bündel oder eine Folge von Aktivitäten, für die Vorgaben benötigt werden und die ein für den Kunden verwertbares Ergebnis erzeugen. Vorgaben Rohstoffe Halbfertigteile
1 Formale Grundlagen -._,.'.,,/,.^'T.,^,'^/ '" ',,
 Vorwort 9 Zu den Verfasserinnen 11 Danksagungen 12 Einleitung 13 Abkürzungen 15 Glossar ^...... 17 ' '"' lh?--- - :;,'.' - v.$%&'';.-0 >.,;.; ; 1 Formale Grundlagen -._,.'.,,/,.^'T.,^,'^/ '" ',, 7.7 Arzneimittelgesetz
Vorwort 9 Zu den Verfasserinnen 11 Danksagungen 12 Einleitung 13 Abkürzungen 15 Glossar ^...... 17 ' '"' lh?--- - :;,'.' - v.$%&'';.-0 >.,;.; ; 1 Formale Grundlagen -._,.'.,,/,.^'T.,^,'^/ '" ',, 7.7 Arzneimittelgesetz
Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation. Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group
 Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Hämatologie im Wandel, Frankfurt 28. Februar 2015 2 Überblick Einführung
Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Hämatologie im Wandel, Frankfurt 28. Februar 2015 2 Überblick Einführung
AG 7 Abweichungsmanagement / Change Control
 2010 AG 7 Abweichungsmanagement / Change Control 3. GMP-Gesprächskreis Niedersachsen 01. Februar 2011 Vorstellung der Ergebnisse: Change Control Dr. Andrea Behrenswerth, Gerresheimer Bünde GmbH Vorbereitung:
2010 AG 7 Abweichungsmanagement / Change Control 3. GMP-Gesprächskreis Niedersachsen 01. Februar 2011 Vorstellung der Ergebnisse: Change Control Dr. Andrea Behrenswerth, Gerresheimer Bünde GmbH Vorbereitung:
Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung
 Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung Angestellten Forum des ZVK Stuttgart 04.03.2016 Birgit Reinecke ZentraleEinrichtungPhysiotherapieund
Was geht Qualitätsmanagement/ Qualitätsicherung die Physiotherapeutenan? Beispiel einer zertifizierten Abteilung Angestellten Forum des ZVK Stuttgart 04.03.2016 Birgit Reinecke ZentraleEinrichtungPhysiotherapieund
Klinische Studien in der onkologischen Praxis. Norbert Marschner Freiburg
 Klinische Studien in der onkologischen Praxis Norbert Marschner Freiburg Qualitätsmanagement Strukturqualität Personell Ausstattung Prozessqualität Ergebnisqualität Struktur Persönliche Kompetenz Ausgebildete
Klinische Studien in der onkologischen Praxis Norbert Marschner Freiburg Qualitätsmanagement Strukturqualität Personell Ausstattung Prozessqualität Ergebnisqualität Struktur Persönliche Kompetenz Ausgebildete
3. OFFIZIELLE GAMP 5 KONFERENZ
 3. OFFIZIELLE GAMP 5 KONFERENZ WORKSHOP W5: Validierung von computerisierten Systemen im GCP-Umfeld Ort: Neuss Datum: 7.12.2010 Workshopleiter: Dr. Christa Färber (Staatl. Gewerbeaufsichtsamt Hannover)
3. OFFIZIELLE GAMP 5 KONFERENZ WORKSHOP W5: Validierung von computerisierten Systemen im GCP-Umfeld Ort: Neuss Datum: 7.12.2010 Workshopleiter: Dr. Christa Färber (Staatl. Gewerbeaufsichtsamt Hannover)
Inspektion Computergestützter Systeme
 Werden computergestützte Systeme bei prä-/klinischen Studien (GLP, GCP), in der Herstellung (GMP) oder in der Verteilung (GDP) von Arzneimitteln eingesetzt, so müssen diese validiert sein. Aufgabe einer
Werden computergestützte Systeme bei prä-/klinischen Studien (GLP, GCP), in der Herstellung (GMP) oder in der Verteilung (GDP) von Arzneimitteln eingesetzt, so müssen diese validiert sein. Aufgabe einer
Das SOP-System der TMF zur Durchführung nicht-kommerzieller klinischer Studien
 Herzlich Willkommen! Bochum, 1. April 2009 Das SOP-System der TMF zur Durchführung nicht-kommerzieller klinischer Studien Dr. Ursula Paulus, Zentrum für Klinische Studien Köln TMF, Telematikplattform für
Herzlich Willkommen! Bochum, 1. April 2009 Das SOP-System der TMF zur Durchführung nicht-kommerzieller klinischer Studien Dr. Ursula Paulus, Zentrum für Klinische Studien Köln TMF, Telematikplattform für
Fachaudit Transfusionsmedizin und Patient Blood Management (PBM) in der gespag. Amtsärzte-Fortbildung 02.12.2013 (14:00 14:15) Ulrike Sandner
 Fachaudit Transfusionsmedizin und Patient Blood Management (PBM) in der gespag Amtsärzte-Fortbildung 02.12.2013 (14:00 14:15) Ulrike Sandner Agenda 1. Einleitung: Organisatorische Struktur 2. Qualitätsmanagementsystem
Fachaudit Transfusionsmedizin und Patient Blood Management (PBM) in der gespag Amtsärzte-Fortbildung 02.12.2013 (14:00 14:15) Ulrike Sandner Agenda 1. Einleitung: Organisatorische Struktur 2. Qualitätsmanagementsystem
Medizinische Dokumentare in der pharmazeutischen Produktion: GMP Good Manufacturing Practice und eine Ganze Menge Papier!
 Medizinische Dokumentare in der pharmazeutischen Produktion: GMP Good Manufacturing Practice und eine Ganze Menge Papier! Medizinisches Informationsmanagement 3.0 11. DVMD Fachtagung in Hannover 17. Februar
Medizinische Dokumentare in der pharmazeutischen Produktion: GMP Good Manufacturing Practice und eine Ganze Menge Papier! Medizinisches Informationsmanagement 3.0 11. DVMD Fachtagung in Hannover 17. Februar
Die wichtigsten Änderungen
 DIN ISO 9001:2015 Die wichtigsten Änderungen und was heißt das für die dequs? Neue Gliederungsstruktur der Anforderungen Neue Querverweismatrix der dequs Stärkere Bedeutung der strategischen Ausrichtung
DIN ISO 9001:2015 Die wichtigsten Änderungen und was heißt das für die dequs? Neue Gliederungsstruktur der Anforderungen Neue Querverweismatrix der dequs Stärkere Bedeutung der strategischen Ausrichtung
Qualifizierung von Studienpersonal an einer Medizinischen Fakultät
 Qualifizierung von Studienpersonal an einer Medizinischen Fakultät Dr. med. Steffen P. Luntz Leiter des KKS Heidelberg Vorstandsmitglied der TMF Gliederung Erwartungen an Forschungsstrukturen Motivation
Qualifizierung von Studienpersonal an einer Medizinischen Fakultät Dr. med. Steffen P. Luntz Leiter des KKS Heidelberg Vorstandsmitglied der TMF Gliederung Erwartungen an Forschungsstrukturen Motivation
Ausbildungslehrgang zum Qualitätsverifikator
 Ausbildungslehrgang zum Qualitätsverifikator Termin: Sa: 08.09.2007 = ÄK-Wien Weitere Termine folgen (drei Samstage) *********** Kursort: ÄK-Wien, Großer Sitzungsaal 1010 Wien, Weihburggasse 10-12 *************
Ausbildungslehrgang zum Qualitätsverifikator Termin: Sa: 08.09.2007 = ÄK-Wien Weitere Termine folgen (drei Samstage) *********** Kursort: ÄK-Wien, Großer Sitzungsaal 1010 Wien, Weihburggasse 10-12 *************
GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG
 GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG Kursleiter: Prof. Dr. Richard F. Schlenk Datum: 2. Schulungstag: 15.10.2014 Name Vorname Anleitung Tragen
GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG Kursleiter: Prof. Dr. Richard F. Schlenk Datum: 2. Schulungstag: 15.10.2014 Name Vorname Anleitung Tragen
Leitung der Herstellung und Produktionsabweichungen kompakt, in Köln
 Leitung der Herstellung und Produktionsabweichungen kompakt, 11.05.2016 in Köln Verantwortlichkeiten der Leitung der Herstellung Verantwortungsabgrenzungen Ablauf der Bearbeitung von Abweichungen, CAPAs
Leitung der Herstellung und Produktionsabweichungen kompakt, 11.05.2016 in Köln Verantwortlichkeiten der Leitung der Herstellung Verantwortungsabgrenzungen Ablauf der Bearbeitung von Abweichungen, CAPAs
Einsatz von OpenClinica in regulierten Umgebungen. Erfahrungen zu Validierung und Audit. Dr. med. Otmar Bayer, MPH
 Einsatz von OpenClinica in regulierten Umgebungen Erfahrungen zu Validierung und Audit Dr. med. Otmar Bayer, MPH Gliederung Kurzvorstellung IFB Allgemeines zum Audit-Prozeß Regulatorische Grundlagen CAPA,
Einsatz von OpenClinica in regulierten Umgebungen Erfahrungen zu Validierung und Audit Dr. med. Otmar Bayer, MPH Gliederung Kurzvorstellung IFB Allgemeines zum Audit-Prozeß Regulatorische Grundlagen CAPA,
Neuerungen in der ICH-GCP Guideline
 AGAH - Study Nurse Forum Neuerungen in der ICH-GCP Guideline Dr. med. Martin Coenen Studienzentrale Studienzentrum Bonn (SZB) Wo bin ich und warum? good clinical practice (GCP) ICH-GCP GCP-V Ethikkommission
AGAH - Study Nurse Forum Neuerungen in der ICH-GCP Guideline Dr. med. Martin Coenen Studienzentrale Studienzentrum Bonn (SZB) Wo bin ich und warum? good clinical practice (GCP) ICH-GCP GCP-V Ethikkommission
HERZLICH WILLKOMMEN. Regionalkreis Münsterland 14. März 2017
 HERZLICH WILLKOMMEN Regionalkreis Münsterland 14. März 2017 Prozess Darstellung mit Turtle- Diagramm Brigitte Recker QM-Systemberatung & Personalentwicklung www.brigitte-recker.de Prozessorientierter Ansatz
HERZLICH WILLKOMMEN Regionalkreis Münsterland 14. März 2017 Prozess Darstellung mit Turtle- Diagramm Brigitte Recker QM-Systemberatung & Personalentwicklung www.brigitte-recker.de Prozessorientierter Ansatz
