Biochemie. Freie Universität Berlin. Druckversion auf
|
|
|
- Sebastian Dresdner
- vor 8 Jahren
- Abrufe
Transkript
1 Freie Universität Berlin Druckversion auf
2 AMINOSÄUREN UND PROTEINE... 3 AMINOSÄUREN...3 PROTEINE... 3 ENZYME... 3 ENZYMHEMMUNG... 4 COENZYME... 4 COENZYM A... 5 ENZYMKINETIK...5 PRAKTIKUM - METHODEN... 5 PHOTOMETER... 5 PROTEIN-BESTIMMUNG NACH LOWRY... 6 EXTINKTIONSKOEFFIZIENT VON NADH... 6 TITRATIONSKURVE VON HISTIDIN... 6 KOHLENHYDRATE... 7 EINTEILUNG DER KOHLENHYDRATE... 7 HETEROGLYCANE... 7 GLUCOSE... 7 GALACTOSE... 8 FRUCTOSE... 8 GLYKOLYSE... 8 GLUCONEOGENESE... 9 PENTOSEPHOSPHAT-WEG... 9 REGULATION DES STOFFWECHSELS INSULIN GLUCAGON STEUERUNG DIABETES MELLITUS ENZYMATISCH-OPTISCHER TEST GÄRUNG VON SACCHARIDEN DURCH HEFE LIPIDE LIPIDE FETTSÄUREN FETTE PHOSPHOLIPIDE GLYCOLIPIDE ISOPRENOIDE STEROIDE CHOLESTEROL LIPOPROTEINE FETTSTOFFWECHSEL ABBAU VON FETTSÄUREN ß-OXIDATION BIOSYNTHESE VON FETTSÄUREN PRAKTIKUM ENERGIESTOFFWECHSEL ALLGEMEINES ATP - ADENOSINTRIPHOSPHAT PYRUVAT-DEHYDROGENASE CITRATCYCLUS ATMUNGSKETTE OXIDATIVE PHOSPHORYLIERUNG PRAKTIKUM Seite 2
3 Aminosäuren und Proteine Aminosäuren Aufbau: - überwiegend a-aminosäuren - 4 Substituenten: Carboxylat-Gruppe + Ammonium-Funktion + H-Atom + Rest - a-c-atom ist chirales Zentrum 2 verschiedene Enantiomere (L- + D-Aminosäuren) Einteilung: - alipathisch: - Glycin, Alanin, Valin, Leucin, Isoleucin - schwefelhaltig: - Cystein, Methionin - aromatisch: - Phenylalanin, Tyrosin, Tryptophan - neutral: - Serin, Threonin, Asparagin, Glutamin - sauer: - Aspartat, Glutamat - basisch: - Histidin, Lysin, Arginin - essentielle AS: - Threonin, Valin, Leucin, Isoleucin, Lysin, Methionin, Phenylalanin, Tryptophan - nicht-essentiell: - Glycin, Alanin, Serin, Arginin, Asparaginsäure, Asparagin, Glutaminsäure, Glutamin, Cystein, Tyrosin, Prolin, Histidin Funktion: - Bausteine von Peptiden und Proteinen - Bausteine anderer Naturstoffe (Coenzyme, Gallensalze, Antibiotika) - Signalstoffe (Neurotransmitter / Vorstufe: Neurotransmittern, Mediatoren, Hormonen) - Metabolite Proteine Struktur: Primärstruktur: - Sequenz der Aminosäuren - Positionierung von Cysteinen Sekundärstrukt: - periodische Wiederholung: - a-helix - ß-Faltblattstruktur - Kollagenhelix Tertiärstruktur: - Wechselwirkung weit voneinander entfernter AS (schwache Bindungen) Quartärstruktur: - Interaktion von Proteinen: - mit deutischen Allosterie - mit anderen Proteinen - mit Phospholipiden Funktion: - Enzyme und Enzymkatalyse - Transport und Speicherung (z.b. Hb, Myoglobin, Transfer, Calmodulin) - Koordinierte Bewegung (Aktin, Myosin, Tropomyosin) - Mechanische Stützfunktion - Immunabwehr (Antikörper, Interleukine) - Nervenleitung (Rezeptorproteine, GABA, Rhodopsien) - Wachstumskontrolle und Differenzierung Enzyme - Stoffwechselvorgänge nur in Anwesenheit von Enzymen möglich, von Enzymen umgesetzte Stoffe heißen Substrate - Coenzym + Apoenzym = Holoenzym Hauptklassen: 1. Oxidoreduktasen: Lactat-DH, Glutamat-DH, Succinat-DH, Pyruvat-DH 2. Transferasen: Hexokinase, Phosphorylase 3. Hydrolasen: Proteasen, Peptidasen, Esterasen, Glykosidasen 4. Lyasen: Aldolasen, Transketolasen 5. Isomerasen: Fumerase, Retinolisomerase Seite 3
4 6. Ligasen: Pyruvatcarboxylase, Thiokinase, Glutaminsynthetase Wirkungen: - substratspezifisch: Reaktion nur mit bestimmten Stoffwechsel-Intermediaten - stereospezifisch: Umsetzung nur eines von mehreren Enantiomeren (Schlüssel-Schloß) - wirkungsspezifisch: Katalyse nur einer von mehreren möglichen Reaktionen Eigenschaften: - jede enzymatische Reaktion beginnt mit reversibler Bindung des Substrates - keine Beeinflussung der Richtung einer Reaktion - Beschleunigung der Einstellung von Gleichgewichten - Enzyme gehen unverändert aus Reaktion hervor - Aktivität von Enzymen kann reguliert werden Struktur: - Enzyme sind meist globuläre Proteine - vielfach gefaltete Polypeptidkette bildet Gerüst zur Stabilisierung des aktiven Zentrums aktives Zentrum: Ort der Substratbindung - umfaßt nur Bruchteil d. gesamten Enzymstruktur, in Spalte der Enzymstruktur Enzymhemmung kompetitiv: unkompetitiv: - Inhibitior + Substrat konkurrieren um aktives Zentrum weniger Umsetzung - große Substrat-Konzentration kann Inhibitor vom Enzym verdrängen - Km-Wert steigt, Vmax gleich - Inhibitor besetzt Gruppe des Enzym-Substrat-Komplexes ( aktives Zentrum) - Affinität zum Substrat bleibt gleich, gehemmte Enzym-Substrat-Komplexes setzen nicht um - Km-Wert gleich, Vmax sinkt nicht-kompetitiv:- Inhibitior besetzt Gruppe des Enzyms + Enzym-Substrat-Komplexes - Affinität zum Substrat + Umsetzung von ES sinkt weniger Produkt - Km-Wert sinkt, Vmax sinkt Substrat- Überschuß: Produkt- Überschuß: allosterisch: - Substrat hemmt in extremen Konzentrationen das Enzym (überschüssiges Substrat wird unspezifisch gebunden Blockade des aktiven Zentrums) - abnehmende Reaktionsgeschwindigkeit Glockenform - kompetitiv: Produkt + Substrat konkurrieren um aktives Zentrum weniger Umsatz - allosterisch: Produkt bindet an allosterisches Zentrum Enzym-Inaktivierung - Inhibitor oder Aktivator bindet an allosterisches Zentrum Konformationsänderung des Enzyms Beeinflussung der Aktivität - K-Typ: Auswirkung auf die Affinität zum Substrat Änderung des Km-Wert - V-Typ: Auswirkung auf die Reaktionsgeschwindigkeit Änderung des Vmax Interkonversion: Übertragung von funktionellen Gruppen auf Enzym An-+ Abschaltung des Enzyms Coenzyme Coenzym: prosthetische Gruppe: - Nichtproteine, müssen bei einigen Enzymen da sein um Katalysefähigkeit zu ermöglichen - Funktion: Gruppenübertragung - häufig von Vitaminen abgleitet - nicht fest an Proteinanteil des Enzyms gebunden Abspaltung ist reversibel - wird bei der Reaktion verändert Regeneration durch anderes Enzym - Beispiel: NADH + NADPH - fest an Enzym gebunden Abspaltung führt zu irreversibler Enzym-Denaturierung - wird bei der Reaktion verändert Regeneration am gleichen Enzym - Beispiel: FAD Seite 4
5 Coenzym A - wichtige Rolle bei Aktivierung von Substanzen in vilen Stoffwechselwegen (ß-Oxidation der Fettsäuren, Pyruvatdehydrogenase, Fettsäure-Synthese - bildet einen Thioester mit der zu aktivierenden Substanz - wichtige Ester: Acetat + CoA Acetyl-CoA (aktivierte Essigsäure) Fettsäure + CoA Acetyl-CoA (aktivierte Fettsäure) Acetyl-CoA: Bedeutung: Acyl-CoA: Coenzym A: - entsteht beim Abbau von Glucose + Fetten + ketoplastischen Aminosäuren - Ausgangsstoff für: Synthese von Steroiden + Ketonkörpern + Fettsäurebildung - Abbau im Citratcyclus - Substrat für Citratcyclus (Abbau unter Bildung von Reduktionsäquivalenten) NADH, FADH2, Biosynthese von GTP + BIldung von CO2 (mitochondrial) - Ketogenese (mitochondrial, Leber) - de novo-biosynthese von Fettsäuren (Fettsäuresynthasekomplex: cytosolisch) - Acetylierung von Aminozuckern - Cholesterin + Steroidhormonsynthese - Verlängerung oder Verkürzung der Fettsäurekette, Bildung von ungesättigten Fettsäuren, Synthese von Sphingosin - Abbau zu Acetyl-CoA - enthält Vitamin Pantothensäure, ß-Alanin durch Säureamidbindung verknüpft - CoA wird mit SH-Gruppe als energiereicher Thioester an Substrat gebunden Enzymkinetik - E + S ES E + P - Initialgeschwindigkeit: zu Beginn liegt viel freies Enzym vor + wenig ES geringe Geschw. - Substratsättigung: Anstieg der Substratkonzentration bei konstanter Enzym-Menge Anstieg von ES bis v max weiterer Anstieg der Reaktionsgeschwindigkiet bei Substratsättigung nur durch Erhöhung der Enzymkonzentration Michaelis K.: - k m, Substrat-Konzentration bei halbmaximaler Geschwindigkeit (1/2 des Enzym mit Substrat gesättigt) unabhängig von der Enzymkonzentration - hohes k m : hohe Substrat-Konz. zur Halbsättigung des Enzyms notwendig kleine Affinität - kleines k m : geringe Substrat-Konzentration zur Halbsättigung notwendig große Affinität - Vorraussetzung: Substrat-Überschuß, Temperatur + ph konstant Gleichung: V = Vmax x ( S) Km + ( S) Praktikum - Methoden Pipetten: Glaspipetten: - 4 Pipettierhilfen: gelb (0,2µl), blau (2µl), grün (10µl), rot (25µl) - Vollpipette: Auslaufpipette - Meßpipette: Auslaufpipette - Enzympipette: Abgabe der Flüssigkeit bis Meniskus gewünschte Markierung erreicht Eppendorf-Pip.: - Kolbenhubpipette, genaueste Pipette - Typen: 200µl (1-200µl, gelbe Markierung + Pipettierhilfe), 1000µl ( µl, blaue) - Einstellen der Pipettiermenge am Rad der Volumenanzeige Photometer - Feststellung der Absorption und Extinktion gelöster Stoffe Seite 5
6 - mit Hilfe eines Filters wird Licht einer bestimmten Wellenlänge hergestellt (Lichtquelle: Quecksilberdampflampe) Lichstrahl durchdringt Küvette + trifft auf Photozelle (Sensor) - Extinktion: - Absorption E = -log Io I = ε c d - I = austretendes geschwächtes Licht - Io = einstrahlendes monochromatisches - Extinktion E ist proportional der Konzentration c des absorbierten Stoffes und der Schichtdicke - Absorptionskoeffizient ε ist abhängig von der Art der Substanz und der Wellenlänge Protein-Bestimmung nach Lowry - Reaktion von Peptidbindungen und Cu-II-Ionen zu einem blauen Komplex - Messung der Extinktion von Proteinlösungen unterschiedlicher Konzentration Auftragung von E gegen die Proteinmenge in einer Protein-Bezugskurve - Messung der Extinktion der Proteinlösung unbekannter Konz. Ablesen der Proteinmenge aus der Protein-Bezugskurve Umrechnen der Proteinmenge in die Proteinkonzentration Rechnung: - Werte: E = 0,66 Küvette = 1,5ml Probe = 25µl - Bezugskurve: bei E = 0,22 ist Protein-Menge = 0,1mg - 0,66 = x. 0,3mg in 25µl 0,3mg x = = 12g 0,22 0,1mg Extinktionskoeffizient von NADH Absorption: Versuch: Bestimmung des molaren Extinktionskoeffizienten bei 365nm (ε abhängig von Wellenlänge) - Absorptionsverhalten von NADH in Abhängigkeit von der Wellenlänge: 2 Maxima im UV- Bereich ( nm), NAD zeigt dagegen bei 340nm keine Absorption - Grund: im Pyrimidin-Ring des Nicotinamids ist die Mesomerie aufgehoben - Messung der Extinktion verschiedener NADH-Lös. bei 365nm Errechnen der NADH- Konzentration - Auftragen von Extinktion gegen NADH-Konzentration in einer Eichgerade - Steigung (E/c) der Geraden ist Extinktionskoeffizient ε - Lambert-Beersches-Gesetz ε = 3,34 cm²/µmol - m = E c = ε d Titrationskurve von Histidin - Bestimmung von ph-werten mit Glaselektroden H+-Ionen werden reversibel an Glasmembran aufgenommen Potentialdifferenz zur H+-Konz. im Glasinneren - AS können abhängig vom ph-wert als Säuren oder Basen auftreten (amphoter) - Histidin: einzige Aminosäure die durch Dissoziation oder Protonierung des Imino-Stickstoff im Imidazol-Ring eine Pufferwirkung im physiologischen ph-bereich zeigt - Titration: IP = 7,6 Seite 6
7 Kohlenhydrate Einteilung der Kohlenhydrate Monosaccharide: - Aldehyde + Ketone mehrwertiger Alkohole (Aldosen oder Ketosen) - Aldosen: Glycerinaldehyd (3), Erythrose (4), Ribose, 2-Desoxyribose, Xylose (5), Glucose, Mannose, Galactose (6) - Ketosen: Dihydroxyaceton (3), Erythrulose (4), Ribulose, Xylulose (5), Fructose (6), Sedoheptulose (7) - Gruppen: halbacetalische Hydroxylgruppe, primäre + sek. alkoholische Gruppen Reaktionen: glykosidische Bindung: - Bildung eines Halbacetals durch Reaktion der Aldehyd- bzw. Ketogruppe mit Hydroxylgruppe Ringform asymmetrisches Zentrum am halbacetalischen C - Oxidation der Aldehydgruppe Carbonsäuren - Reduktion der Aldehydgruppe Zuckeralkohole - Oxidation der CH 2 OH-Gruppe Uronsäure - Ersatz einer Hydroxylgruppe durch NH 2 Aminozucker - halbacetalische Hydroxylgruppe reagiert mit OH- oder NH2-Gruppe zum Vollacetal - sehr häufig: Nucleoside, Nucleotide, Polynucleotide, Di-, Oligo-, Polysaccharide Disaccharide: - Lactose: ß-1-4-Bindung aus Galactose + Glucose - Saccharose: a-1-2-bindung aus Glucose + Fructose - Maltose: a-1-4-bindung aus 2x Glucose Homoglycane: - Stärke und Glykogen - Polymere aus einem einzigen Monosaccharid Heteroglycane Glycoproteine: - Heteroglycane aus 2-10 Monosacchariden, enthalten Mannose + Galactose + Aminozucker - bilden integrale Membranproteine und extrazelluläre lösliche Proteine Proteoglykane: - Heteroglycane aus wiederhol. Disaccharideinheiten, die an Proteinskelette geknüpft sind - Kollagen, Elastin, Bestandteil der extrazellulären Matrix Peptidoglycane:- bestehen aus Peptiden aus 4-5 Aminosäuren und einem rezeptiven Disaccharid - bakerielle Zellwand Glycolipide: Oligosaccharide sind an Sphingosin oder Diacylglycerin oder Polyprenole gebunden Glucose Quantifizierung: - gekoppelter-enzymatisch-optischer Test - Glucose Hexokinase (ATP ADP) Glucose-6-P - Glucose-6-P Glucose-6-P-DH (NADP NADPH) 6-Phospho-gluconolacton - Messung der Extinktion (365nm) Errechnung der Konzentration (äquimolare Umsetzung) Hypoglykämie: - Verminderung der Glucose-Konzentration im Blut unter 2,8 mmol/l Ursachen: - Insulin-Überdosis / Überproduktion gesteigerte Glycolyse - Lebererkrankung verminderte Gluconeogenese - Fehlernährung verminderte Kohlenhydratzufuhr - Frühgeborene unreife Gluconeogenese - Alkoholabusus, Glykogenosen, Mangel an Insulinantagonisten, Fructose-Intoleranz, Nebennierenrindeninsuffizienz Folgen: Mangelversorgung des ZNS mit Glucose verminderte Glycolyse verminderte ATP- Produktion Bewußtlosigkeit Glykogenose I: Ursache: Mangel an Glucose-6-phosphatase Folgen: - verminderte Gluconeogenese Hypoglykämie verminderte Insulinsekretion gesteigerte Lipolyse Hyperlipidämie Seite 7
8 - verstärkte Glykogenspeicherung Hepatosplenomegalie - verstärkte Glykolyse Lactatacidose Galactose Stoffwechsel: - Nahrungsaufnahme: Lactose Lactase Galactose + Glucose - Verstoffwechselung zu Glucose in Leber und Niere - wird im Organismus in Sphingolipide und Glykoproteine eingebaut - Galactose Galactokinase Galactose-1-P - Galactose-1-P + UDP-Glucose Galactose-1-P-Uridyltransferase UDP-Galactose + Glucose-1-P 4 Epimerase UDP-Glucose + Glucose-1-P Quantifizierung: - gekoppelter enzymatisch-optischer Test - Galaktose wird enzymatisch oxidiert wobei NAD+ zu NADH reduziert wird - gemessene Extinktion des entstandenen NADH wird mit Hilfe des Lambert-Beer- Gesetzes in Konzentration der umgesetzten Galaktose umgerechnet - Umsetzung von NAD NADH ist äquimolar zur Galactose-Umsetzung Rechnung: - Werte: E = 0,34 Küvettenvolumen = 2,05 ml Probevolumen = 50 µl ε = 3,4 - Galactose-Menge in Probe: E x Küvettenvolumen = 0,205 µmol ε - Galactose-Konzentration: 0,205 µmol x = 4,1 mmol / l Galactosämie: - Ursache: Galaktokinase-Mangel, Galalctose-1-P-Uridyltransferase-Mangel - Wirkung: Anstieg des Galactose-1-P Hemmung der Glycolyse + Gluconeogenese - Folgen: Hypoglykämie, Galactosurie, Hepatomegalie, Nierenstörung, geistige Schäden Fructose Weg: Polyol-Weg: Weg: - Nahrungsaufnahme: Saccharose Saccharase Fructose + Glucose - Verstoffwechselung in Leber - Fructose Fructokinase Fructose-1-P Aldolase B Glyceral Aldehyd-Reduktase Glycerol Glyceron-3-P Glyceral-3-P (Umsetzung zu Glucose oder Abbau in Glycolyse) - extrahepatischer Abbau + Biosynthese der Fructose, Enzym-Testosteron-Kontrolle - stellt in der Samenblase notwendige Fructose bereit - Glucose Aldose-Reduktase (NADPH NADP) Sorbitol Sorbitol-DH (NAD NADH) Fructose Hyperfructosämie: > 1 mmol/l, Störung in Fructose-Metabolisierung (Frc-Kinase-Mangel, Frc-Intoleranz) Folgen: - Hypoglykämie, Fructosurie Fructose-Intoleranz: Ursache: Aldolase-B-Mangel Folgen: - Spaltung des Fructose-1-P Anhäufung im Stoffwechsel Hemmung der Glykogen- Phosphorylase + Frc-1,6-bis-Phosphatase Hypoglykämie Glykolyse Weg: - findet in jeder Zelle statt (außer Erys) - kataboler Stoffwechselweg (unabhängig ob aerobes oder anaerobes Leben) Glucose Hexokinase (ATP ADP) Glc-6-P Glc-6-P-Isomerase Frc-6-P Frc-6-P- Kinase (ATP ADP) Frc-1,6-bis-P Aldolase Glyceral-3-P + Glyceron-3-P Glyceral-3- P-Dehydrogenase (NAD NADH) 1,3-bis-P-Glycerat Phosphoglycerat-Kinase (2ADP 2ATP) 3-P-Glycerat Phosphoglycerat-Mutase 2-P-Glycerat Phosphopyruvat-Hydratase Phosphoenolpyruvat Pyruvat-Kinase (2ADP 2ATP) Pyruvat Seite 8
9 Gluconeogenese - Resynthese von Glucose - glucogene Aminosäuren: Muskulatur aus Nichtkohlenhydraten: - Lactat: Erys + O 2 -Mangel - Glycerol: Abbau von Fett - überwiegend in Leber + Niere (ca. 100%), im Mito + ER + Cytoplasma - Glucose für NS + Erys + Nierenmark einziges Substrat für Energiebedarfs - NS ist größter Glucose-Verbraucher (140g/24h), täglich Bildung von mehreren 100g Weg: Lactat oder Aminosäuren Pyruvat Pyruvat-Carboxylase (ATP ADP) Oxalacetat Malat-Dehydrogenase (NADH NAD) Malat Malat-Dehydrogenase (NAD NADH) Oxalacetat PEP-Carboxy-Kinase (GTP GDP) Phosphoenolpyruvat 2-P-Glycerat 3-P-Glycerat (ATP ADP) 1,3-bis-P-Glycerat (NADH NAD) Glyceral-3-P + Glyceron- 3-P Frc-1,6-bis-P Fructose-1,6-bisphosphatase Frc-6-P Glc-6-P Glucose-6- phosphatase Glucose Glykogen Synthese: Abbau: intrazellulär: - α α-1-6-glycosidisch verbundenen Glucose-Molekülen baumartige Struktur - Vorteile der Speicherung: osmotische Inaktivität, unlösliche Eigenschaft, verhältnismäßig kleine Größe (Kugel) durch baumartige Verzweigungen - Skelettmuskulatur (1g/100g), Leber (10g/100g) insgesamt 400g Glc-6-P Phosphatglucomutase Glc-1-P + UTP UDP-Glc-Phosphorylase UDP- Glc Glycogensynthase unverzw. Glycogen Amylo-1,4-1,6-Transglycosylase Glycogen - Glykogen Phosphorylase a spaltet 1-4-Bindungen Glucose-1-P - 4 Glc-Reste vor 1-6-Verzweigung Transglykosylase überträgt 3 Glc-Einheiten Hauptkette Amylo-1-6-Glycosidase spaltet verbleibenden 1-6-Glucoserestes - Glucose-1-P Phosphoglucomutase Glucose-6-P Glc-6-Phosphatase Glucose Intestinaltrakt: - a-amylase aus Speichel + Pankreassekret spaltet Polysaccharide in Oligosaccharide - Disaccharidasen + Oligosaccharidasen spalten in Monosaccharide Leber: - Glycogen-Phosphorylase spaltet vom nichtreduzierenden Ende Glucose-1-Phosphat - Transferisierung in Glucose-6-Phosphat Dephosphorylierung zu Glucose Reagenzglas: - partielle Spaltung: - Glycogen ß-Amylase Maltose + Grenzdextrin (nur Spaltung von a-1-4-bindungen kein Überspringen von Verzweigungen) - Maltose a-glucosidase Glucose (Spaltung 1-4-Bindungen) - vollständige Spaltung: - Glycogen Amyloglucosidase Glucose (Spaltung: ) Pentosephosphat-Weg Bedeutung: - liefert wichtige Vorstufen für anabole Prozesse - Bereitstellung von NADPH für Biosynthese (Fettsäure, Cholesterin, Steroidhormone) - Bereitstellung von NADPH (Erythrozyten) für Bildung von reduziertem Glutathion - Biosynthese von Pentosen (DNA, RNA) Seite 9
10 Weg: oxidativer: Glucose Hexokinase (ATP ADP) Glc-6-P Glucose-6-P-DH (NADP NADPH) 6- Phosphogluconolacton Gluconolacton-Hydrolase 6-Phosphogluconat 6-Phosphogluconat-DH (NADP NADPH) Ribulose-5-P Isomerase Ribose-5-P regenerativer: - Funktion: Anpassung der Netto-Produktion von NADPH + Pentosephosphaten - Reaktionen reversibel Umwandlung von Hexosephosphaten in Pentosephosphate - Xylulose-5-P Transketolase 2-C Ribose-5-P - Glyceral-3-P Transaldolase 3-C Sedoheptulose-7-P - Fructose-6-P Erythrose-4-P - Xylulose-5-P Transketolase 2-C Erythrose-4-P - Glyceral-3-P Fructose-6-P Bilanz: - 6 x Glucose-6-P 12 NADPH + 6 CO Glucose-6-P Regulation des Stoffwechsels Leber: Funktion: - Aufnahme der Nahrungs-KH durch Hepatozyten mittels carriervermittelter Diffusion - Aufnahme ist insulin-unabhängig - Glucostatfunktion: Konstanthaltung der Blutglucose - Abgabe von Glucose in V. hepatica (physiologische Glucose-Konzentration) - Speicherung überschüssiger Glucose als Glykogen - Biosynthese von Glucose (Gluconeogenese) aus Lactat + Pyruvat + AS + Glycerin - Umwandlung von Galactose und Fructose in Glucose Glc-Transport: - Plasmamembran für Glucose impermeabel Aufnahme mit Transportproteine - Enterozyten im Darm + Tubulusepithelien der Niere sekundär aktiver Na+-Symport - alle anderen Zellen Uniport - Glut 1 Glut 7 Insulin Biosynthese: - Peptidhormon der B-Zellen des Pankreas - Bildung einer Polypeptidkette (Translation an Ribosomen) Prä-pro-Insulin - Abspaltung der Signalsequenz, Bildung von Disulfidbrücken Pro-Insulin - Entfernung des C-Peptids durch eine Protease Insulin Wirkungsweise: - Bindung von Insulin an Rezeptor (2a+2ß-Untereinheiten, transmembranäres Protein) - ß-Untereinheit besitzt auf cytosolischer Seite eine Tyrosinkinase-Domäne - Aktivierung der Tyrosinkinase Insulin-Mangel: - fördert: - Glykogenabbau Glucose - Gluconeogenese von Aminosäuren Glucose - Proteolyse von Muskelproteinen Aminosäuren - Lipolyse von Fett Fettsäuren - hemmt: - Glykogensynthese - Glycolyse Pyruvat oder Fettsäuren - Umwandlung von Glucose Fett - Glucoseaufnahme in Muskulatur oder Fettgewebe - Merkmale: - Hyperglykämie, Hyperlipidämie, Acidose, Glucosurie, Ketonurie Seite 10
11 Glucagon Biosynthese: Wirkung: - Peptidhormon der a-zellen des Pankreas - Signal für Freisetzung von Glucagon: Abfall der Glc-Konzentration < 2,8mmol/l - Prä-pro-Glucagon Pro-Glucagon Glucagon - Insulinantagonist - Steigerung der hepatischen Glykogenolyse + Hemmung der Glykogensynthese Steuerung Glycolyse: - Hexokinase: Insulin, Glc-6-P - Frc-6-P-Kinase: Insulin + Frc-2,6-bis-P + AMP, ATP + Citrat - Pyruvat-Kinase: Insulin, Glucagon + camp + ATP + Acetyl-CoA Gluconeogenese: - Pyruvat-Carboxylase: Acetyl-CoA + Glucagon + Cortisol, Insulin - PEP-Carboxy-Kinase: Glucagon + Cortisol, Insulin - Frc-1,6-bis-Phosphatase: Glucagon + Cortisol, Insulin +Frc-2,6-bis-P - Glc-6-Phosphatase: Glucagon + Cortisol, Insulin Glycogenolyse: - Glycogen-Phosphorylase: Glucagon + Adrenalin + AMP Glycogen-Synth. Glycogen-Synthase: Insulin, Glucagon + Adrenalin Diabetes mellitus Biosynthese: - absoluter oder relativer Mangel - Typ I: insulinabhängiger Diabetes, insulinbildende Zellen werden in frühem Alter durch Autoimmunreaktion zerstört - Typ II: nicht-insulinabhängiger Diabetes, mildere Form im Alter, Ursache (Störung der Insulin-Sekretion + Rezeptorstörung) - Prä-pro-Insulin: Bildung einer Polypeptidkette (Translation an Ribosomen) - Pro-Insulin: Abspaltung der Signalsequenz, Bildung von Disulfidbrücken - Insulin: Entfernung des C-Peptids durch eine Protease Kohlenhydrate: - Glycolyse vermindert - Gluconeogenese gesteigert - Glucose-Fett-Umwandlung vermindert - Glucose-Aufnahme vermindert (Muskulatur + Fettgewebe) Hyperglykämie - Glykogen-Speicherung vermindert - Glykogen-Abbau verstärkt Lipide: Symptome: - Lipolyse gesteigert - Umwandlung der Fettsäuren in Lipoproteine Hyperlipidämie - ß-Oxidation der FS zu Acetyl-CoA Bildung von Ketonkörpern metab. Acidose - Hyperglykämie, Glucosurie, Hyperlipidämie, metabolische Acidosen, Ketonurie, Angiopathien, Nephropathien, Katarakt enzymatisch-optischer Test direkter: gekoppelter: - Konzentrations-Bestimmungen machen sich Reaktionen zu Nutze bei denen die Konzentration eines Edukts abnimmt oder eines Produkts zunimmt - meßbare Produkte: NADH bzw. NADPH, Farbstoffe - NADH absorbiert bei 365nm im Gegensatz zu NAD (Umsetzung von NAD NADH) - meßbare Verbindung entsteht im 1. Schritt (Galactose-Bestimmung) - meßbare Verbindung entsteht einige Schritte später (Glucose-Bestimmung) Seite 11
12 Gärung von Sacchariden durch Hefe Gärung: Pyr Lactat: Disaccharide Spaltung Monosaccharide Aufnahme in Zellen Monosaccharide Glycolyse Pyruvat Pyruvat-Decarboxylase Acetaldehyd Alkohol-DH Ethanol - findet nur unter anaeroben Bedingungen statt NADH / H+ wird zu NAD+ regeneriert - Pyruvat Lactat-Dehydrogenase (NADH NAD) Lactat Pyr Ethanol: - findet ausschließlich unter anaeroben Bedingungen statt - Pyruvat Pyruvat-Decarboxylase Ethanal Alkohol-DH Ethanol Seite 12
13 Lipide Lipide Bedeutung: Brennstoff: Baustoff: Isolator: Sonstiges: - gut löslich in organischen Lösungsmitteln (Methanol, Aceton, Chloroform, Benzol) - schlecht löslich in Wasser - hydrolisierbare: Komponenten durch Esterbindungen verknüpft enzymatisch oder chemisch spaltbar (Fette, Wachse, Sterolester, Phospholipide, Sphingolipide, Glycolipide) - nicht hydrolisierbar: Lipid-Alkohole, Fettsäuren - wichtiger Energieträger der Nahrung - bedeutende Energiereserve Lagerung der Fette in Lipidtröpfchen in der Zelle - Oxidation in Mitochondrien zu Wasser + CO 2 - Aufbau von Membranen - Membranlipide: Phospholipide, Glycolipide, Cholesterol - Fette liegen zur thermischen Isolierung in subkutannen Gewebe und um Organe - in Zellmembranen als mechanische + elektrische Zell-Isolierung gegenüber Umgebung - Aufbau eines elektrischen Membranpotentials - Signalfunktion (Steroide, Eicosanoide, Metabolite von Phospholipiden) - Hormone + Mediatoren + Second messenger - Cofaktoren von enzymatischen Reaktionen (Blutgerinnung) Fettsäuren ungesättigte: - Carbonsäuren mit langer Kohlenwasserstoffkette (ab 4-C) - Bausteine von Fetten + Membranlipiden (verestert mit Alkoholen), freie Fettsäure (unverestert) - ungesättigte Fettsäuren: eine oder mehrere Doppelbindungen (Ölsäure, Linolsäure) - müssen mit der Nahrung zugeführt werden - mehrfach ungesättigte Fettsäuren - Linolsäure, Linolensäure, Arachidonsäure Fette Bestimmung: Reaktionen: - Ester des dreiwertigen Alkohols Glycerol + 3 Fettsäuren (Triacylglycerol) - die 3 Fettsäuren eines Fettmoleküls können sich in Kettenlänge + Zahl der Doppelbindungen unterscheiden große Zahl an Kombinationsmöglichkeiten Quantitative Bestimmung von Triacylglyceriden (gekoppelt enzymatisch-optischer Test) - Triacylglyceride Lipasen + Esterasen + H 2 O Fettsäuren + Glycerin - Glycerin Glycerin-Kinase (ATP ADP) Glyceron-3-P... Phosphoenolpyruvat Pyruvat-Kinase (ADP ATP) Pyruvat Lactat-Dehydrogenase (NADH NAD+) Lactat - umgesetztes NADH wird im Photometer gemessen Rückschluß auf Triacylglycerid- Konzentration möglich, da beide äquimolar sind Rechnung: - Werte: E = 0,34 Küvettenvolumen = 1,6 ml Probevolumen = 50 µl ε = 3,4 - Fett-Menge in Probe: E x Küvettenvolumen = 0,16 µmol ε - Fett-Konzentration: 0,16 µmol x = 3,2 mmol / l Seite 13
14 Phospholipide - Hauptbestandteil der Membranen - Phosphorsäure-Rest ist mit Hydroxy-Gruppe an C-3 des Glycerols verestert Phospholipide tragen bei neutralem ph mindestens 1 negative Ladung Phophatidate: - einfachste Form der Phospholipide - Phosphatester des Diacylglycerols - wichtige Zwischenprodukte bei Biosynthesen von Fetten + Phospholipiden - können durch Phospholipasen aus Phospholipiden freigesetzt werden Sphingophospholipid: - kommen in Membranen von Nervenzellen vor - Sphingosin (Aminoalkohol mit Seitenkette) übernimmt Aufgaben des Glycerols + Acyl-Rest Phosphatid: Glycolipide Vertreter: - in allen Geweben Außenseite der Plasmamembran - Sphingosin + 1 FS + großer Oligosaccharid-Rest (Phosphat-Rest d. Phospholipide fehlt) Galactosyl-Ceramide, Glycosyl-Ceramide, Sulfatide, Ganglioside Isoprenoide Weg: Aufbau: - Acetyl-CoA Aufbau von Fetten, Phospholipiden, Glycolipiden, Fettsäure-Derivate - Acetyl-CoA Isopentenyl-diphosphat (aktives Isopren) Isoprenoide - alle Isoprenoide leiten sich von Isopren ab - Geraniol, Farnesol, Phytol, Dolichol, Squalen, Cholesterol Steroide Sterole: Gallensäure: - Steroid + Hydroxygruppe + Doppelbindungen - Bsp.: Cholesterol, Ergosterol, Stigmasterol - Bildung aus Cholesterol in der Leber - halten Cholesterol der Galle in Lösung, fördern Verdauung von Lipiden - Bsp.: Cholsäure, Lithocholsäure, Chenodesoxycholsäure Steroidhormone: - lipophile Signalstoffe, steuern Stoffwechsel + Wachstum + Reproduktion - Bsp.: Testosteron, Progesteron, Aldosteron, Cortisol, Estradiol, Calcitriol Cholesterol Funktion: Biosynthese: - Steranderivat mit 27 C-Atomen - Produktion in der Leber (1g pro Tag), Aufnahme aus Nahrung (0,3g pro Tag) - Baustein der Zellmembranen - Bestandteil von Lipoproteinen - Biosynthese von Gallensäuren + Steroidhormonen - Acetyl-CoA Mevalonat Isopentenyl-di-P Squalen Cholesterol 1. Acetyl-CoA Acetacetyl-CoA 3-HMG-CoA HMG-CoA-Reduktase Mevalonat 2. Mevalonat Mevalonat-di-P Isopentenyl-di-P 3. Isopentenyl-di-P + Dimethylallyl-di-P Geranyl-di-P Farnesyl-di-P Squalen 4. Squalen Lanosterol Cholesterol Konzentration: - LDL-Cholesterin: günstig: < 130 mg/dl (<3,3 mmol/l) Grenzbereich: mg/dl (3,3-4,1 mmol/l) Seite 14
15 Risikobereich: > 160 mg/dl (>4,1 mmol/l) - HDL-Cholesterin: günstig: > 55 mg/dl (>1,4 mmol/l) Risikobereich: < 35 mg/dl (<0,9 mmol/l) Quantitative Bestimmung von Gesamtcholesterol: Reaktionen: - Cholesterol-Ester + H 2 O Cholesterolesterase Cholesterol + Fettsäure - Cholesterol + O 2 Cholesteroloxidase 4 -Cholesten-3-on + H 2 O 2 - das entstehende H 2 O 2 reagiert mit Aminophenazon + Phenol zu chinoiden Farbstoff (rot) Extinktionsbestimmung bei 546 nm Hypercholesterämie: - Ursachen: überkalorische Ernährung und Rezeptordefekte (Mangel an LDL-Rezeptoren) - Folgen: Artheriosklerose - Konzentration von mg/dl (5,7-6,7 mmol/l) sind risikoverdächtig Lipoproteine - Lipoproteinkomplexe sind kugelförmige Aggregate - Kern: unpolare Lipide (Triacylglycerine + Cholesterol-Acylester) - Hülle: Apoproteine + amphipathische Lipide (Phospholipide + Cholesterol) Chylomikron: - Inhalt: TAG (94%), Cholesterin-Ester (3%), Phospholipide (3%), Apolipoproteine (2%) - Bildung in Darmmukosa Transport von Triacylglyceriden aus der Nahrung ins Blut (Lymphgefäße Ductus thoracicus Venenwinkel Blut) Abbau: VLDL: LDL: HDL: Pathologie: Hyperlipoproteinämie: - intravasal durch Lipoproteinlipase, Austausch v. Apolipoprotein zw. HDL + Chylomikronen % der Triacylglyceride werden abgebaut Restkörperchen werden rezeptorvermittelt von Leber aufgenommen und katabolisiert - prä-ß-lipoprotein - Inhalt: TAG (55%), Cholesterin-Ester (20%), Phospholipide (18%), Apolipoproteine (8%) - Bildung in Leber + Ausschleusung über Exozytose Transport von endogenen Lipiden intravasale Abgabe von Fettsäuren Übergang in IDL und LDL - ß-Lipoprotein - entsteht intravasal aus IDL + VLDL Transport von Cholesterin aus Leber in Peripherie - Zellaufnahme durch Endozytose (Bindung ApoB100+ApoE an LDL-Rezeptoren) - atherogene Wirkung - α-lipoprotein - entsteht intravasal Transport von überschüssigem Cholesterin (Peripherie zur Leber) - Erhöhung der Konzentration: hormonell (Estrogene bei Frauen), Sport, Rauchen, Wein - antiatherogene Wirkung - physiologisch nach einer fettreichen Nahrung - pathologisch bei mangelhafter Aktivität der Lipoproteinlipase (intravasal auf Endothelzellen und Adipozyten) Abbau der Chylomikronen und anderer Lipoproteine ist massiv gestört Seite 15
16 Fettstoffwechsel Dünndarm: Leber: Fettgewebe: Spaltung der Triacylglycerine in freie Fettsäuren + Monoacylglycerine Micellenbildung Resorption in Mucosa Bildung von Chylomikronen Abgabe ins Lymphsystem - Aufbau von Fettsäuren, Synthese von Fetten + Phospholipiden Abgabe ins Blut - Aufnahme von Fettsäuren aus Plasma Umwandlung in Ketonkörper - Aufbau von Cholesterol aus Acetat - Fettspeicher, wichtigste Energiereserve - Lipolyse (Spaltung in Fettsäuren + Glycerin) Abbau von Fettsäuren ß-Oxidation Aktivierung: ß-Oxidation: Transport: - Oxidation der durch Lipolyse entstandenen Fettsäuren zur Energiegewinnung - findet in der mitochondrialen Matrix statt - Aktivierung der Fettsäure zu aktivierter Fettsäure (Acyl-CoA) - Fettsäure + ATP Acyl-AMP Acyl-AMP + Coenzym A Acyl-Coa + AMP - Acyl-CoA Acyl-CoA-Dehydrogenase ²-trans-Enoyl-CoA Enoyl-CoA-Hydratase L-ß-Hydroxy-Acyl-CoA 3-Hydroxy-Acyl-CoA-Dehydrogenase (NAD NADH) ß-Ketoacyl- CoA Thiolase Acetyl-CoA + verkürzte Fettsäure neuer Zyklus entstehende Acetyl-Reste werden durch Citratcyclus zu CO 2 oxidiert ATP-Gewinnung - Abbau von ungradzahligen Fettsäuren: Propionyl-CoA entsteht einmalig als Produkt - Acyl-CoA wird durch die innere Mitochondrien-Membran als Carnitinester transportiert 1. Acyl-CoA + Carnitin Carnitin-Acyltransferase 1 Acylcarnitin + CoA 2. Transport von Acylcarnitin mit Carnitin-Acylcarnitin-Antiporter via innere Mito-Membran 3. Acylcarnitin + CoA Carnitin-Acyltransferase 2 Acyl-CoA + Carnitin Biosynthese von Fettsäuren Transfer: Synthese: - läuft im Cytoplasma ab (Leber, Fettgewebe, Niere, Lunge) - Glucose und Aminosäuren sind wichtigste Lieferanten der Kohlenstoff-Atome - Fettsäure-Synthase als Multienzymkomplex notwendig - Acetyl-Gruppen-Transfer (Mitochondrium Cytoplasma) - Acetyl-CoA + Oxalacetat Citrat (durchdringt Membran) ATP-Citrat-Lyase Acetyl- CoA + Oxalacetat (1 ATP pro transportiertes Acetyl-CoA) - Oxalacetat wird als Malat oder Pyruvat zurück ins Mitochondrium transportiert 1. Bildung des Substrates: Acetyl-CoA Biotin Malonyl-CoA 2. Anlagerung: Starter-Acetyl-Rest (periphere SH-Gruppe), Malonyl-Rest (zentrale Gruppe) 3. Verknüpfung: Malonyl-Rest + Acetyl-Rest 3-Oxoacyl-Synthase 3-Oxoacyl- (CO 2 ) 4. Reduktion: 3-Oxoacyl- 3-Oxoacyl-Reduktase Hydroxyacyl- (NADPH-abhängig) 5. Dehydratisierung: Hydroxyacyl- Hydroxyacyl-Hydratase trans-enoyl- 6. Reduktion: trans-enoyl- trans-enoyl-reduktase 4-C-Fettsäure (NADPH-abhängig) - neue Anlagerung eines Malonyl-Restes je Zyklus Verlänger. um 2 C-Atome Palmitat - Synthese ungradzahliger Fettsäuren: Propionyl-CoA statt Acetyl-CoA als Startermolekül FS-Synthase: - dimerer Komplex zweier multifunktioneller Proteine (2 identische Untereinheiten) - jede Untereinheit trägt sämtliche für Fettsäuresynthese benötigte Teilaktivitäten - jedes Monomer besitzt 2 essentielle SH-Gruppen (zentral + peripher) - Aktivitäten: Malonyl-Acetyl-Transferase, Keto-Acyl-Synthase, Ketoreduktase, Dehydratase, Enoylreduktase, Acyl-Carrier-Protein, Thioesterase Seite 16
17 Praktikum Dünnschicht-Chromatographie: - Trenntechnik beruht auf Wechselwirkungen von Stoffen zw. stationärer + mobiler Phase - stationäre Phase (Kieselgel, Schicht auf Trägermaterial), mobile Phase (Laufmittel) - Rf-Wert: Verhältnis von Substanzlaufstrecke / Laufmittelfront Ablauf: Substanzen werden an Startlinie auf Kieselgelplatte aufgetragen eintauchen in Laufmittel mobile Phase wandert durch Kapillarkräfte an stationärer Phase entlang je nach Löslichkeit im Laufmittel + Adsorption an stationärer Phase wandern Substanzen unterschiedlich weit Verdauung von Olivenöl: - Olivenöl ist Mischung aus verschiedenen Triacylglycerinen - Darm: Spaltung des Olivenöls durch Pankreaslipasen + Esterasen in Di- + Monoacylglycerine + Glycerin + Fettsäuren Resorption in Enterozyten Seite 17
18 Energiestoffwechsel Allgemeines Enzymaktivität: Units (U), Substratumsatz den ein Enzym in einer Minute katalysiert (1 µmol / min) katalyt. Konz: Enzymaktivität auf ein bestimmtes Volumen bezogen (U / Liter) spezif. Aktivität: Enzymaktivität auf eine bestimmte Protein- oder Gewebemenge bezogen (U / mg) ATP - Adenosintriphosphat Struktur: - Nucleotid-Coenzym - wichtigste Speicherform chemischer Energie in der Zelle - Spaltung von ATP ist stark exergon gewonnene chemische Energie wird genutzt um durch energetische Kopplung endergone Vorgänge anzutreiben - Kette von 3 Phosphat-Resten ist mit 5 OH-Gruppe von Adenosin verknüpft - Phosphorsäureester-Bindung: a-phosphat Ribose - Phosphorsäureanhydrid-Bindung: y ß a Phosphat, Instabilität durch Abstoßung neg.- geladener O 2 -Atome bei Hydrolyse von ATP entsteht freies Phosphat-Anion besser hydratisiert + mesomeriestabilisiert stark exergoner Charakter der ATP-Hydrolyse - Mg 2+ -Ion ist koordinativ an a+ß-phosphate gebunden ATP-Synthese: stark endergone ATP-Synthese muß mit stark exergonen Proz. gekoppelt werden 1. Weg: - oxidative Phosphorylierung (nur aerob) - die in elektrochemischen Gradienten gespeicherte Energie wird zur Bildung von ATP aus ADP + P genutzt - H+-transportierende ATP-Synthasen machen die im Gradienten gespeicherte Energie für ATP-Synthese nutzbar 2. Weg: - Übertragung von Phosphat-Resten auf ATP durch Metabolite mit hohem Phosphatübertragungspotential - auch unter anaeroben Bedingungen Kreatinphosphat Substratkettenphosphorylierung: - de novo-biosynthese von ATP (GTP) bei der von einem energiereichen Zwischenprodukt der energiereich-gebundene Phosphat-Rest auf ADP (GDP) übertragen wird - GTP-Synthese im Citrat-Cyclus, in der Glycolyse Pyruvat-Dehydrogenase Pyruvat Acetyl-CoA (vor Einschleusung in Citratcyclus, in Mitotochondrien) Cofaktoren: Thyaminpyrophosphat, Liponamid, CoA, FAD, NAD + Enzyme: - Pyruvatdecarboxylase - Dihydroliponamid-Acetyltransferase - Dihydroliponamid-Dehydrogenase Mechanismus: 1. Pyruvat-Decarboxylase: - Decarboxylierung des Pyruvats Übertragung des Hydroxyethyl-Rest auf TPP Oxidation des Hydroxyethyl-Rest zum Acetyl-Rest Übertragung des Acetyl-Rest auf Liponamid 2. Dihydroliponamid-Acetyltransferase: - Übertragung des Acetyl-Rest vom Liponamid auf Coenzym A 3. Dihydroliponamid-Dehydrogenase: - Oxidation von Dihydroliponamid zu Liponamid Bildung von NADH / H+ Seite 18
19 Citratcyclus Bedeutung: - in mitochondrialer Matrix lokalisiert - pro Cyclus: 2CO NADH + 1 FADH 2 Lieferung von 11 ATP in Atmungskette - Abbau von Acetyl-CoA zu CO 2 + Reduktionsäquivalenten Reoxidation der Reduktionsäquivalenten in Atmungskette liefert hohe Energiemengen als ATP - Lieferung von Ausgangsprodukten für: Gluconeogenese Fettsäurebiosynthese Hämbiosynthese Synthese -essentieller Aminosäuren Acetyl-CoA aus:- Pyruvat aus Glykolyse (Pyruvat-DH) - ß-Oxidation von Fettsäuren - Abbau von Aminosäuren Weg: Regulation: Acetyl-CoA + Oxalacetat Citrat-Synthase Citrat Aconitase Isocitrat Isocitrat-DH (NAD NADH) 2-Oxoglutarat 2-Oxoglutarat-DH (NAD NADH) Succinyl-CoA Succinat-CoA-Ligase (GDP GTP) Succinat Succinat-DH (FAD NADH 2 ) Fumarat Fumarase Malat Malat-DH (NAD NADH) Oxalacetat - Steigerung der Aktivität, wenn zellulärer Energiebedarf erhöht ist - NADH-Überschuß Hemmung von Pyruvat-DH, Citrat-Synthase, Isocitrat-DH, 2- Oxoglutarat-DH - Produkthemmung: Acetyl-CoA- + Succinyl-CoA hemmen ihre Enzyme Atmungskette - Teilprozess der oxidativen Phosphorylierung - katalysiert den Transport von Elektronen von NADH oder QH2 auf Sauerstoff - große Differenz der Redoxpotentiale von Donor + Akzeptor stark exergon - gewonnene Energie wird zum Aufbau eines Protonengradienten genutzt ATP-Synthase nutzt Gradienten zur ATP-Bildung Reoxidation: - in der mitochondrialen Innenmembran lokalisiert Redoxpotential: - NADH / NAD = -0,32 V + O 2 / O 2- = 0,82 V = 1,14V - abhängig von: ph-wert, Temperatur, Druck Komplexe: I: - NADH Ubichinon Oxidoreduktase - Oxidation von NADH Übertragung der H+ auf Ubichinon Ubichinol II: III: IV: - Succinat Ubichinon Reduktase - H+-Zufuhr: Succinat Fumarat, a-glycerophosp. DHAP, Acyl-CoA Enoyl-CoA - Oxidation von FADH 2 Übertragung der H+ auf Ubichinon Ubichinol - Ubichinon Cytochrom c Oxidoreduktase - Oxidation von Ubichinol Übertragung von Elektronen (Cytochrom b c a) - Cytochrom c Oxidase - Übertragung von Elektronen auf O 2 Bildung von H 2 O V: - ATP-Synthase Seite 19
20 Enzyme: Succinat-DH: Cytochrom: - Vorkommen in Citrat-Cyclus und Atmungskette (Komplex II) - katalysiert Reaktion Succinat Fumarat (FAD FADH 2 ), FAD prosthetische Gruppe - fest an innerer Mito-Membran (kompetitiv hemmbar durch Malonat + Oxalacetat) - Protein mit einer Häm-Struktur als prosthetische Gruppe - Häm: Protoporphyrinring mit zentralem Fe-Atom (Fe ist 6-bindig 4 Bindungen gehen zu 4 Ringen des Porphyrins + 2 Bind. zu anderen Stoffen, z.b. O 2 im Hämoglobin oder AS) - Cytochromoxidase: Aufbau aus 13 Untereinheiten (Häm a+häm a3+cu 2+ ), Aufgabe ist Übertragung von Elektronen auf O 2 und Protonen-Pumpe Atmungskontrolle: - Kopplung Substratoxidation + ATP-Bildung hohe ADP-Konzentration = hohe Atmungsgeschwindigkeit - ruhende Zellen: Überschuß (O 2 + Substrat), Mangel (ADP) - aktive Zellen: Überschuß (O 2 + ADP + Substrat) max. Atmungskettengeschw. oxidative Phosphorylierung ATP-Synthese: - gewonnene Energie der Atmungskette dient zum Aufbau eines Protonengradienten über innerer Mitochondrienmembran - ATP-Synthese an Protonen-Rückfluß vom Intermembranraum in Matrix gekoppelt ATP-Synthase: - H+-transportierende ATP-Synthase besteht aus 2 Teilen 1. in Membran integrierter Protonenkanal aus 13 Untereinheiten 2. in Matrix ragende katalytische Einheit, Kopf enthält 3 aktive Zentren katalyt. Zyklus: - jedes der 3 aktiven Zenten durchläuft nacheinander 3 Phasen Phasenwechsel wenn Protonen durch Kanalprotein in Matrix fließen 1. Bindung von ADP + P 2. Knüpfung der Anhydrid-Bindung 3. Abspaltung des Produktes Entkopplung: - Elektronentransport (NADH O 2 ) nicht mit ATP-Synthese verbunden - H+ umgehen Komplex V=F0F1 strömen durch permeablere innere Mito-Membran - Stoffe: Dinitrophenol (Praktikum), Dicumarol, Arsenat, Valiomycin - physiologisch: Thermogenin (im braunen Fettgewebe, bildet in innerer Mito-Membran einen Protonenkanal Zusammenbruch der protonenmotorischen Kraft Wärmebildung bei Neugeborenen) Praktikum energiereiche - besitzen ein hohes Gruppenübertragungspotential Spaltung der Bindung setzt Energie Bindung: frei exotherme Reaktion - Enol-Ester-Bindung (Phosphoenolpyruvat), Säureanhydrid-Bindung (ATP), Thioester- Bindung (Acetyl-CoA) katalytische Konzentration der Succinatdehydrogenase: Prinzip: - Succinat Succinat-Dehydrogenase (FAD FADH2) Fumarat - Teststoff nimmt H+ vom FADH2 auf und wird zu Farbstoff reduziert - Extraktion des Farbstoffs + Messung der Extinktion Berechnung des Substratumsatzes (äquimolare Umsetzung von Succinat + Teststoff) Berechnung der Enzymaktivität (Substratumsatz / Zeit) Berechnung der spez. Aktivität (Enzymaktivität/ Gewebemenge) Rechnung: - Werte: E=0,405 Homogenat=50 µl Ethylacetat=3 ml ε=13,5 Inkubations-Zeit=15 min - Substrat-Menge 0,405 x 3 = 0,09 (50µl Homogenat setzen in 15min 13,5 0,09µmol Substrat um) - katalytische Konzentration: 0,09 x = 120 U / l 15 Seite 20
AMINOSÄUREN UND PROTEINE...2
 1 AMINOSÄUREN UND PROTEINE...2 AMINOSÄUREN...2 PROTEINE...2 ENZYME...2 ENZYMHEMMUNG...3 COENZYME...3 COENZYM A...4 ENZYMKINETIK...4 PRAKTIKUM - METHODEN...4 PHOTOMETER...5 PROTEIN-BESTIMMUNG NACH LOWRY...5
1 AMINOSÄUREN UND PROTEINE...2 AMINOSÄUREN...2 PROTEINE...2 ENZYME...2 ENZYMHEMMUNG...3 COENZYME...3 COENZYM A...4 ENZYMKINETIK...4 PRAKTIKUM - METHODEN...4 PHOTOMETER...5 PROTEIN-BESTIMMUNG NACH LOWRY...5
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Parotis Pankreas. Dünndarm Bürstensaum. Amylose Amylopektin Glykogen. Maltose. Glucose. Isomaltose. Saccharose. Fructose. Lactose. Galaktose.
 Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Biochemie. Skript zur Vorklinik der Medizin und für das Physikum. Berlin, Juli Aminosäuren und Proteine. Kohlenhydrate.
 Biochemie Skript zur Vorklinik der Medizin und für das Physikum www.med-school.de mail@med-school.de Berlin, Juli 2000 Aminosäuren und Proteine Kohlenhydrate Lipide Energiestoffwechsel 1 Andreas Werner
Biochemie Skript zur Vorklinik der Medizin und für das Physikum www.med-school.de mail@med-school.de Berlin, Juli 2000 Aminosäuren und Proteine Kohlenhydrate Lipide Energiestoffwechsel 1 Andreas Werner
Foliensatz; Arbeitsblatt; Internet. Je nach chemischem Wissen können die Proteine noch detaillierter besprochen werden.
 03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
KOHLENHYDRATE PYRUVAT-DEHYDROGENASE
 PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
1. Biochemie-Klausur Zahnmediziner, WS 03/04
 1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat
 2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit
 Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit glukosespiegel: enge Regelung zum Schutz vor Unterund Überzuckerung (Hypo- bzw. Hyperglykämie) abhängig von Nahrungszufuhr und Stoffwechsel bei
Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit glukosespiegel: enge Regelung zum Schutz vor Unterund Überzuckerung (Hypo- bzw. Hyperglykämie) abhängig von Nahrungszufuhr und Stoffwechsel bei
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Nichtessentielle Aminosäuren. Stoffwechsel Nahrungskarenz
 Nichtessentielle Aminosäuren Stoffwechsel Nahrungskarenz Einleitung 11 nichtessentielle AS Können von Säugetierzellen selbstsynthetisiert werden. Im Vergleich zu essentiellen AS einfache Synthesewege Nichtessentiell
Nichtessentielle Aminosäuren Stoffwechsel Nahrungskarenz Einleitung 11 nichtessentielle AS Können von Säugetierzellen selbstsynthetisiert werden. Im Vergleich zu essentiellen AS einfache Synthesewege Nichtessentiell
Metabolisierung des Aminosäure-Kohlestoffgerüstes
 Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
Übungsfragen Biochemie 1. Erklären Sie die Begriffe
 Übungsfragen Biochemie 1 Erklären Sie die Begriffe Adsorption Diffusion Dialyse Enantiomere Diastereomere Verseifung Fett Lipid essentielle Fettsäure essentielle Aminosäure Kohlenhydrat Disaccharid Peptid
Übungsfragen Biochemie 1 Erklären Sie die Begriffe Adsorption Diffusion Dialyse Enantiomere Diastereomere Verseifung Fett Lipid essentielle Fettsäure essentielle Aminosäure Kohlenhydrat Disaccharid Peptid
Stoffwechsel - Energiebereitstellung - Biomoleküle
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Organische Chemie der biologischen Stoffwechselwege
 Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O O 2 6 CO H 2 O G kj
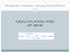 Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Pentosephosphatzyklus. Synonym: Hexosemonophosphatweg
 Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Autotrophe und heterotrophe Organismen
 Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
Mohammed Jaber KOHLENHYDRATE
 Mohammed Jaber KOHLENHYDRATE Wichtige Disaccharide: Maltose alpha-glc(1-4)glc entsteht als Zwischenprodukt beim Stärkeund Glykogenabbau Saccharose a-glc(1-6)ß-fru kann bei parenteraler Zufuhr nicht gespalten
Mohammed Jaber KOHLENHYDRATE Wichtige Disaccharide: Maltose alpha-glc(1-4)glc entsteht als Zwischenprodukt beim Stärkeund Glykogenabbau Saccharose a-glc(1-6)ß-fru kann bei parenteraler Zufuhr nicht gespalten
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Lösungsblatt zu Aufbau von Aminosäuren
 Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Fette und ihre Funktionen. Müssen Fette sein?
 Fette und ihre Funktionen Müssen Fette sein? Ja! Fette sind: Wichtiger Bestandteil unserer täglichen Nahrung Energieträger Nummer 1 Quelle für essentielle n Vehikel für die Aufnahme fettlöslicher Vitamine
Fette und ihre Funktionen Müssen Fette sein? Ja! Fette sind: Wichtiger Bestandteil unserer täglichen Nahrung Energieträger Nummer 1 Quelle für essentielle n Vehikel für die Aufnahme fettlöslicher Vitamine
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Auswahlverfahren Medizin Prüfungsgebiet Chemie. 6.Termin Organische Chemie Naturstoffe
 Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Biomembranen Transportmechanismen
 Transportmechanismen Barrierewirkung der Membran: freie Diffusion von Stoffen wird unterbunden durch Lipidbilayer selektiver Stofftransport über spezielle Membranproteine = Translokatoren Semipermeabilität
Transportmechanismen Barrierewirkung der Membran: freie Diffusion von Stoffen wird unterbunden durch Lipidbilayer selektiver Stofftransport über spezielle Membranproteine = Translokatoren Semipermeabilität
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Zellen verwandeln Zucker in Energie
 Zellen verwandeln Zucker in Energie Kohlenhydrate sind äusserst wichtige Brennstofflieferanten. Pflanzen können Zucker selber herstellen (vgl. autotrophe Organismen); Tiere hingegen müssen Zucker (und
Zellen verwandeln Zucker in Energie Kohlenhydrate sind äusserst wichtige Brennstofflieferanten. Pflanzen können Zucker selber herstellen (vgl. autotrophe Organismen); Tiere hingegen müssen Zucker (und
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Beispiele zur Multiple-Choice Prüfung in OC
 1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
Anaerobe NADH-Regeneration: Gärung
 Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Pentosephosphat. hosphatweg
 Pentosephosphat hosphatweg Wie aus dem Namen abzuleiten ist, werden C5-Zucker, einschließlich Ribose, aus Glucose synthetisiert. Das oxidierende Agens ist hierbei NADP + ; es wird zu NADP reduziert, das
Pentosephosphat hosphatweg Wie aus dem Namen abzuleiten ist, werden C5-Zucker, einschließlich Ribose, aus Glucose synthetisiert. Das oxidierende Agens ist hierbei NADP + ; es wird zu NADP reduziert, das
5. Biochemie- Seminar
 5. Biochemie- Seminar 5. Biochemie- Seminar Kohlenhydrate II und biologische Oxidation Verweise mit [L] beziehen sich auf Biochemie und Pathobiochemie von Löffler, Petrides, Heinrich; 8. Auflage. Glycogenbiosynthese
5. Biochemie- Seminar 5. Biochemie- Seminar Kohlenhydrate II und biologische Oxidation Verweise mit [L] beziehen sich auf Biochemie und Pathobiochemie von Löffler, Petrides, Heinrich; 8. Auflage. Glycogenbiosynthese
9. Abbau der Glukose zum Pyruvat
 9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte)
 Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Proteinbestimmung. Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der Proteinbestimmung mit den folgenden Lehrzielen:
 Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Fettsäurebiosynthese
 Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
P9 Kunststoffe Moleküle ohne Ende
 SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Stichpunkte zu den Vorlesungen von Prof. Dr. Peter Rehling
 Stichpunkte zu den Vorlesungen von Prof. Dr. Peter Rehling Kohlenhydratstoffwechsel, Citratzyklus, Oxidative Phosphorylierung, Transport von Metaboliten 1. Einführung zu Struktur und Funktion Beispiele
Stichpunkte zu den Vorlesungen von Prof. Dr. Peter Rehling Kohlenhydratstoffwechsel, Citratzyklus, Oxidative Phosphorylierung, Transport von Metaboliten 1. Einführung zu Struktur und Funktion Beispiele
Lipide. Prof. Dr. Albert Duschl
 Lipide Prof. Dr. Albert Duschl Funktionen der Lipide Definition: Lipide sind ölige oder fettige Derivate von Kohlenwasserstoffen. Biologische Lipide sind - Energiespeicher - Membrankomponenten - Pigmente
Lipide Prof. Dr. Albert Duschl Funktionen der Lipide Definition: Lipide sind ölige oder fettige Derivate von Kohlenwasserstoffen. Biologische Lipide sind - Energiespeicher - Membrankomponenten - Pigmente
Biologische Katalysatoren
 Biologische Katalysatoren Die Entdeckung der biologischen Katalysatoren (Enzyme) ist eng mit der Entstehungsgeschichte der Biochemie verknüpft: Ende 19. Jhdt: Speichel - Fleischverdauung durch Magensäfte
Biologische Katalysatoren Die Entdeckung der biologischen Katalysatoren (Enzyme) ist eng mit der Entstehungsgeschichte der Biochemie verknüpft: Ende 19. Jhdt: Speichel - Fleischverdauung durch Magensäfte
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Kohlenhydrate und ihre Funktionen
 Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Ueberblick des Zuckerabbaus: Pyruvat!
 Ueberblick des Zuckerabbaus: Pyruvat + 2 ATP Oxidativer Abbau Fermentation (Muskel) Alkohol-Gärung (Hefe) Alkoholische Gärung: In Hefe wird unter aneroben Bedingungen NAD + durch Umwandlung von Pyruvat
Ueberblick des Zuckerabbaus: Pyruvat + 2 ATP Oxidativer Abbau Fermentation (Muskel) Alkohol-Gärung (Hefe) Alkoholische Gärung: In Hefe wird unter aneroben Bedingungen NAD + durch Umwandlung von Pyruvat
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Biochemie. Kurzes Lehrbuch der. für Mediziner und Naturwissenschaftler. Von Peter Karlson. 12., völlig neubearbeitete Auflage
 Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Allgemeine Pathologie. Störungen im Kupfer- Stoffwechsel
 Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Kontrolle der Genexpression auf mrna-ebene. Abb. aus Stryer (5th Ed.)
 Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
Kontrolle der Genexpression auf mrna-ebene Abb. aus Stryer (5th Ed.) RNA interference (RNAi) sirna (small interfering RNA) mirna (micro RNA) Abb. aus Stryer (5th Ed.) Transcriptional silencing Inhibition
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
D) Die Verbindung enthält fünf sekundäre OH-Gruppen. E) Es handelt sich um einen zyklischen Ester (Lacton).
 1, Fragentyp D Welche der folgenden Aussagen ist (sind) richtig? 1. Nur die Zellwand grampositiver Bakterien besitzt als wesentliches Bauelement Peptidoglycan (Murein). 2. Murein besteht aus Heteropolysaccharidketten,
1, Fragentyp D Welche der folgenden Aussagen ist (sind) richtig? 1. Nur die Zellwand grampositiver Bakterien besitzt als wesentliches Bauelement Peptidoglycan (Murein). 2. Murein besteht aus Heteropolysaccharidketten,
Inhaltsverzeichnis. Organische Chemie und Biochemie 1. Proteine und Peptide 23. Enzyme 47. Coenzyme 71
 Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom
 Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
Lipidstoffwechsel. 5. Regulation des Fettsäurestoffwechsels. 1. Verdauung, Aufnahme und Transport von Fetten. 6. Cholesterinstoffwechsel
 Lipidstoffwechsel 1. Verdauung, Aufnahme und Transport von Fetten 2. Fettsäureoxidation 3. Ketonkörper 4. Biosynthese von Fettsäuren 5. Regulation des Fettsäurestoffwechsels 6. Cholesterinstoffwechsel
Lipidstoffwechsel 1. Verdauung, Aufnahme und Transport von Fetten 2. Fettsäureoxidation 3. Ketonkörper 4. Biosynthese von Fettsäuren 5. Regulation des Fettsäurestoffwechsels 6. Cholesterinstoffwechsel
Examensklausur Ernährungsphysiologie und angewandte Biochemie
 Examensklausur Ernährungsphysiologie und angewandte Biochemie Prüfungsnummer Bevor Sie beginnen + Teilen Sie sich Ihre Zeit gut ein! Die Arbeit umfasst 8 Aufgaben und sie haben 4 Stunden Zeit. Achten Sie
Examensklausur Ernährungsphysiologie und angewandte Biochemie Prüfungsnummer Bevor Sie beginnen + Teilen Sie sich Ihre Zeit gut ein! Die Arbeit umfasst 8 Aufgaben und sie haben 4 Stunden Zeit. Achten Sie
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
Kraftwerk Körper Energiegewinnung in unseren Zellen
 Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Asmaa Mebrad Caroline Mühlmann Gluconeogenese
 Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Die Wege des Kohlenstoffes
 Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Spektroskopie. im IR- und UV/VIS-Bereich. Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) http://www.analytik.ethz.
 Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
COOH. Die Aminosäuren tragen laborübliche Abkürzungen, so stehen z. B. Gly für Glycin oder Phe für Phenylalanin.
 Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
