European Germ Cell Cancer Consensus Group (EGCCCG) Urologische Universitätsklinik Essen Westdeutschen Tumorzentrum Essen e.v.
|
|
|
- Fritz Manfred Hartmann
- vor 7 Jahren
- Abrufe
Transkript
1 Klinik und Poliklinik für Urologie, Uroonkologie und Kinderurologie Direktor: Prof. Dr. med. Dr. h.c. H. Rübben Ansprechpartner: Dr. med. F. vom Dorp Hufelandstraße 55 5 Essen Tel Fax frankvomdorp@web.de European Germ Cell Cancer Consensus Group (EGCCCG) Urologische Universitätsklinik Essen Westdeutschen Tumorzentrum Essen e.v. (WTZE) in Kooperation mit Sektion Leitlinien des Arbeitskreises Uroonkologie Duisburg, Essen, Gelsenkirchen, Krefeld, Mönchengladbach, Mülheim, Neuss, Oberhausen, Troisdorf, Velbert Dr. med. Bröcheler Dr. med. Buck Prof. Dr. med. Fichtner Prof. Dr. med. Goepel Dr. med. Hautkappe Prof. Dr. med. Höfner Prof. Dr. med. Hutschenreiter Prof. Dr. med. Jacobi PD Dr. med. Krege Dr. med. Krüger PD Dr. med. Lümmen Prof. Dr. med. MeyerSchwickerath PD Dr. med. Miller Prof. Dr. med. Otto Dr. med. Rabs Prof. Dr. med. Dr. h.c. Rübben Prof. Dr. med. Schmid PD Dr. med. Sperling Dr. med. Stöblen Prof. Dr. med. Stuschke Prof. Dr. med. Wammack
2 . Einleitung Der testikuläre Keimzelltumor repräsentiert den häufigsten bösartigen Tumor in der Altersgruppe der 0 bis 0järigen Männer.Die Altersverteilung unterscheidet sich von den übrigen soliden Neoplasien dahingehend, dass ein erster Altersgipfel zwischen dem 5. und 35. Lebensjahr, ein zweiter geringerer Gipfel nach dem 80. Lebensjahr auftritt. Risikofaktoren Neben dem kontralateralen Hodentumor (EBM IIA: 5) sind auch Maldeszensus/ Kryptorchismus (EBM IIA: 68, EBM IIB: 9,0) und Hodentumoren bei erstgradigen Verwandten (EBM IIB: ) gesicherte Risikofaktoren. 3 Diagnostik Die Diagnostik beim gonadalen Primärtumor umfasst Palpation und Sonographie der Hoden (mindestens 7,5 MHzSchallkopf) (EBM IV: 5) sowie die Bestimmung der Tumormarker AFP, ßHCG, LDH und beim Seminom fakultativ PLAP (EBM IIA: 63). Besteht bei einem jungen Mann eine retroperitoneale und/oder mediastinale Raumforderung, ist auch an einen extragonadalen Keimzelltumor zu denken. Die Diagnose wird durch Erhöhung der genannten Tumormarker verifiziert. Bei einem Drittel der Fälle besteht gleichzeitig eine testikuläre intraepitheliale Neoplasie (TIN). Diese kann mittels Hodenbiopsie gesichert werden. In der Regel erfolgt jedoch zunächst eine systemische platinbasierte Chemotherapie aufgrund des extragonadalen Befundes. Die notwendige sekundäre Abklärung der Hoden sollte frühestens sechs Monate nach Abschluss der Chemotherapie durchgeführt werden (EBM IIA: 63, EBM VI: 5). Bei unauffälligen Tumormarkerwerten können eine Diagnosesicherung durch Biopsie aus dem Tumorprozess erfolgen oder unter der Verdachtsdiagnose eines extragonadalen Keimzelltumors das Ansprechen auf die Chemotherapie beobachtet und das weitere Vorgehen festgelegt werden. Behandlung des Primärtumors und kontralaterale Hodenbiopsie Orchiektomie Grundsätzlich wird zunächst der Primärtumor entfernt mit Ausnahme einer ausgedehnten, vital bedrohlichen Metastasierung, bei der primär mit der Chemotherapie begonnen wird und die Primärtumorentfernung nach deren Abschluss erfolgt (EBM IIB: 33,3). Die Semikastratio erfolgt über einen inguinalen Zugang (EBM IIA: 35, EBM IIB: 36,37). Der tumortragende Hoden wird mit Samenstrang in Höhe des inneren Leistenringes abgesetzt. Bei makroskopisch unklarer Dignität muss eine intraoperative Schnellschnittdiagnostik zur Klärung vorgenommen werden (EBM IIB: 380). Organerhaltende Operation Bei synchronen bilateralen Tumoren, metachronem kontralateralen Tumor oder Solitärhoden und präoperativ normalem Testosteronspiegel sollte die Möglichkeit eines organerhaltenden Vorgehens in Betracht gezogen werden (EBM IIB: 3). Die Operation sollte in kalter Ischämie erfolgen. Dabei müssen vom Tumorgrund und aus der Peripherie Biopsien entnommen werden. Zur Eradikation der immer vorliegenden testikulären intraepithelialen Neoplasie ist postoperativ eine Radiotherapie des Hodens mit 0 Gy erforderlich (EBM IIB: 5,).
3 3 Diagnose einer intraepithelialen Neoplasie Bei 5% der Patienten mit Hodentumoren liegt im kontralateralen Hoden eine TIN vor, die durch eine offene Biopsie in 99% der Fälle nachgewiesen werden kann. Bei Hodenvolumen < ml und Alter < 30 Jahre beträgt das Risiko für das Vorliegen einer TIN > 3% (EBM IIA: 5,,5). Zumindest bei diesen Konstellationen wird daher eine kontralaterale Hodenbiopsie empfohlen. Diese geschieht über einen Skrotalschnitt am ehesten im Rahmen der Ablatio testis (EBM IIA: 5,). Die Konservierung der kontralateralen Biopsie muss in Stieve oder BouinLösung erfolgen (nicht Formalin!) (EBM IIB: 6,7). 5 Pathologische Diagnostik Die Makropräparation des Hodens erfolgt vollständig, quer lamelliert. Mehrere Querschnitte werden durch den Samenstrang gelegt. Für die Beurteilung der Gewebeentnahmen ist es erforderlich, dass pro Zentimeter Tumor eine Scheibe (Block), jedoch mindestens drei insgesamt, sowie Blöcke aus der unmittelbaren Tumorumgebung und aus dem tumorfernen Hodengewebe histologisch untersucht werden. Weitere Entnahmen müssen aus dem Samenstrangabsetzungsrand und aus einem hodennahen ( cm Abstand) Querschnitt vom Samenstrang erfolgen. Die Tumoren werden entsprechend der WHOKlassifikation (8) klassifiziert. Die Definition eines anaplastischen Seminoms wurde gestrichen. Immunhistochemische Untersuchungen an Gewebe von Hodentumoren sind zur genaueren Charakterisierung der einzelnen Tumorkomponenten, zur Klärung differentialdiagnostischer Fragen und zur Erfassung einer Gefäßinvasion indiziert. Da die Gefäßinvasion die TKategorie beeinflußt, ist eine Endotheldarstellung obligat, wenn die Gefäßinvasion nicht sicher evident ist (was nur bei einem kleinen Teil der Fälle zutrifft). Weil die Therapie von einer zuverlässigen Unterscheidung zwischen seminomatös und nichtseminomatös abhängt, ist bei Seminomen eine Zytokeratin Darstellung ebenfalls obligat, da sonst kleine Herde eines embryonalen Karzinoms übersehen werden können. CD30, AFP, ßHCG und PlAP können fakultativ bei differentialdiagnostischen Schwierigkeiten in der Abgrenzung einzelner Tumorkomponenten benutzt werden (embryonales Karzinom, Dottersacktumor, Chorionkarzinom, TIN). Das histopathologische Gutachten, das nach den Richtlinien der Basisdokumentation für Tumorkranke (9) erstellt werden sollte, muss folgende Angaben enthalten: Tumorlokalisation (50) und größe, Seitenangabe, Hodendystopie, Tumorausbreitung (Rete testis, Tunica albuginea, Tunica vaginalis, Nebenhoden, Samenstrang, Skrotum), Blut und Lymphgefäßinvasion, ptkategorie nach der Klassifikation der UICC 997 (5), histologischer Typ (WHOICD0), intratubuläre Keimzellneoplasie (TIN). Bei pluriform strukturierten Tumoren sind fakultativ die nachgewiesenen Strukturen und ihr geschätzter prozentualer Anteil, bei Seminomen der Nachweis von Synzytiotrophoblasten, bei spermatozytischen Seminomen eine zusätzliche Sarkomkomponente anzugeben. Der morphologische Nachweis einer testikulären intraepithelialen Neoplasie erfolgt lichtmikroskopisch am HEPräparat mit immunhistologischem Nachweis der PLAP oder im Semidünnschnitt (bei entsprechender Erfahrung). Weitere Einzelheiten sind der vom Berufsverband Deutscher Pathologen herausgegebenen Anwendungsleitlinie
4 Pathologische Diagnostik von Hodentumoren zu entnehmen, die in Kürze publiziert wird. 6 Ausbreitungsdiagnostik Die nachfolgenden Angaben zur Wertigkeit der jeweiligen bildgebenden Diagnostikverfahren beruhen in der Regel nicht auf prospektiven Phase IIIStudien, sodass eine EBMGraduierung im Einzelnen nicht vorgenommen werden kann; allerdings ist die Validität der Angaben dem EBMGrad IIA (analog der Genauigkeit von Phase III Studien) gleichzusetzen, da das Ergebnis der Bildgebung in der Regel mit der histopathologischen Diagnose korreliert wird (5,53). Die Computertomographie (CT) von Thorax und Abdomen/Becken mit oralem und intravenös zu verabreichendem Röntgenkontrastmittel ist das Standardverfahren zur Festlegung der klinischen Stadienausbreitung (559). Unter Einhaltung der Richtlinien der Bundesärztekammer zum Geräte und Untersuchungsstandard (606) werden für das SpiralCT des Thorax und der Leber die Parameter 5/8/ mm (Kollimation/Tischvorschub/Inkrement), für die des übrigen Abdomen die Parameter 8/0/8 mm empfohlen. Für die Beurteilung der Lunge und des Mediastinum ist die Computertomographie sensitiver im Vergleich zur Röntgenuntersuchung des Thorax. Eine Röntgenuntersuchung der Thoraxorgane in zwei Ebenen kann in der Primärdiagnostik die CT Thoraxuntersuchung nicht ersetzen (58,59). Es muss allerdings beachtet werden, dass pulmonale/pleurale knotige Veränderungen < cm zu falsch positiven Bewertungen führen können (56,58,59,63,6). Auch mit einer Computertomographie des Abdomens/Beckens ist die Differenzierung der klinischen Stadien I und IIA nur begrenzt möglich aufgrund falsch positiver bzw. falsch negativer Befunde von bis zu 30% wegen schwieriger Differenzierung der Lymphknotendignität aufgrund morphologischer Größenbestimmung (5557,6567). Eine Sonograpie des Retroperitoneums ist für das Staging unzureichend; sie weist im Vergleich zum CT geringere Sensitivität und Treffsicherheit auf (55,68). Eine MRT des Abdomens/Beckens hingegen bringt keinen zusätzlichen diagnostischen Gewinn und ist daher nur bei Kontraindikation gegen die intravenöse Applikation von Röntgenkontrastmitteln (CTUntersuchung) einzusetzen (697). Die Positronen EmissionsTomographie (PET) führt zu falsch negativen Befunden bei differenzierten Teratomen, falsch positiven bei entzündlichen Reaktionen und kann Mikrometastasen nicht nachweisen; sie ist daher auf Studien beschränkt (780). Skelettszintigraphie und SchädelCT sind nur bei fortgeschrittener Erkrankung und Vorliegen von intermediate oder poor prognosis Charakteristika der International Germ Cell Cancer Collaborative Group (IGCCCG)(8,8) oder klinischer Symptomatik erforderlich (EBM IV: 8385). Für die Stadieneinteilung wird die TNMKlassifikation der UICC 997 (5) verwendet, in der auch die Tumormarker AFP, ßHCG und LDH berücksichtigt sind. Patienten mit fortgeschrittener Erkrankung sind darüber hinaus den Prognosegruppen nach den Kriterien der IGCCCG zuzuordnen: gute, intermediäre und schlechte Prognose (siehe Tabelle )(8,8). Die Prognoseklassifikation nach IGCCCG und die TNMKlassifikation sind kongruent und Grundlage für die Festlegung der individuellen Behandlungsstrategie. 7 Fertilität und therapiebedingte gonadale Toxizität
5 5 Im Rahmen der Primärdiagnostik sollten bei noch bestehendem Kinderwunsch Gesamttestosteron, LH und FSH bestimmt und ein Spermiogramm mit Hinweis auf die Möglichkeit einer Kryokonservierung des Ejakulates! durchgeführt werden (EBM IV: 8689). Liegen bilaterale Hodentumore oder ein Hodentumor mit kontralateraler testikulärer intraepithelialer Neoplasie vor, ist der Patient auf die Möglichkeit einer Kryokonservierung, bei Azoospermie auf die einer testikulären Spermienextraktion (TESE) hinzuweisen (EBM IV: 88,909). Eine Kontrazeption während der onkologischen Behandlung und ein Jahr danach wird empfohlen, obwohl es keinen Nachweis für eine Erhöhung des Risikos von Missbildungen bei nachfolgend geborenen Kindern gibt (EBM III: 95). Im Verlauf sind bei fortbestehendem Kinderwunsch frühestens ein Jahr nach abgeschlossener Therapie erneute Hormon und Ejakulatuntersuchungen, wie oben angeführt, sinnvoll. Umfang und Zeitpunkte weiterer Kontrollen orientieren sich an der durchgeführten Therapie. Bei Auftreten klinischer Symptome eines Androgenmangels sollten Hormonbestimmungen (Testosteron und LH) auch bei fehlendem Kinderwunsch durchgeführt werden. Nach bilateraler Orchiektomie muss eine TestosteronSubstitutionstherapie lebenslang erfolgen; nach einseitiger Ablatio testis oder Orchiektomie ohne oder mit kontralateraler Enukleation oder bei testikulärer intraepithelialer Neoplasie richtet sich die Substitutionstherapie nach den Testosteronwerten und klinischer Symptomatik (EBM I IV: 96,97). 8 Prognosefaktoren 8. Prognosefaktoren bei Frühstadien Seminom CS I: Signifikante, jedoch nicht prospektiv evaluierte unabhängige prognostische Parameter einer okkulten Metastasierung des Seminoms sind Tumorgröße (>/= cm) und Infiltration des Rete testis (EBM III: 98,99). Patientenalter (< 3 Jahre) und vorhandene vaskuläre Invasion sind von fraglicher prognostischer Relevanz (EBM IIA: 00,0, EBM III: 0,0). Nichtseminom CS I: Eine venöse und/oder lymphatische Infiltration von Tumorzellen (vaskuläre Invasion (VI)) im Primärtumor ist der entscheidende Prognosefaktor für eine okkulte Metastasierung (EBM IIA: 0307, EBM IIB: 08, EBM III: 63,,). 8% der Patienten mit VI gegenüber bis % ohne VI entwickeln Metastasen (EBM IIB: 0). Der Nachweis und Anteil von embryonalem Karzinom am Gesamttumor ist der nächst relevante Prognosefaktor, der zur Zeit jedoch klinisch keine Bedeutung hat (EBM IIB: 06,08,0, EBM III: 63,7). Nichtseminom PS IIA/B: Die Ausdehnung des retroperitonealen Befundes (< cm vs. bis 5 cm) (PS IIA vs. PS IIB) und die vaskuläre Invasion im Primärtumor sind prognostische Faktoren für das Auftreten eines Rezidivs, wenn keine adjuvante Chemotherapie durchgeführt wird (EBM III: 8,9). 8. Prognosefaktoren bei fortgeschrittenen Stadien
6 6 Patienten mit fortgeschrittenen Stadien werden nach IGCCCG in drei Prognosegruppen eingeteilt (EBM IAIII: 8,8) (Tabelle ): Tabelle : PrognoseKlassifikation der IGCCCG (8,8) Gute Prognose 5JahresÜberlebensrate ca. 90 % Nichtseminom Testis/primärer retroperitonealer Tumor und niedrige Marker und keine nicht pulmonalen viszeralen Metastasen "niedrige Marker": AFP <.000 ng/ml, ßHCG <.000 ng/ml (< IU/l) LDH <,5 x Normalwert Seminom jede Primärlokalisation, jede Markerhöhe und keine nicht pulmonalen viszeralen Metastasen Intermediäre Prognose 5JahresÜberlebensrate ca. 80 % Nichtseminom Testis/primärer retroperitonealer Tumor und "intermediäre Marker" und keine nicht pulmonalen viszeralen Metastasen "intermediäre Marker"*: AFP ng/ml ßHCG ng/ml ( IU/l) LDH,5 0 x Normalwert Seminom jede Primärlokalisation, jede Markerhöhe und nicht pulmonale viszerale Metastasen (Leber, ZNS, Skelett, Intestinum) Schlechte Prognose 5JahresÜberlebensrate ca. 50 % Nichtseminom primärer mediastinaler Keimzelltumor oder Testis/ retroperitonealer Tumor mit nicht pulmonalen viszeralen Metastasen (Leber, ZNS, Skelett, Instestinum) oder "hohem Marker" * mindestens LaborParameter muß die Bedingung erfüllen "hohe Marker"*: AFP > ng/ml, ßHCG > ng/ml ( U/l) LDH > 0 x Normalwert Der prognostische Wert eines vorübergehenden Tumormarkeranstiegs nach Therapiebeginn oder eines nicht zeitgerechten Markerabfalls ist nicht gesichert (EBM III: 0). Patienten mit Progress während oder innerhalb von vier Wochen nach cisplatinhaltiger Primärtherapie haben eine sehr schlechte Prognose (EBM IIB: ). Bei Vorliegen eines Rezidivs sind Lokalisation und Histologie des Primärtumors, Ansprechen auf die Primärtherapie, Dauer der vorangegangenen Remission und Höhe der Tumormarker AFP und ßHCG gesicherte Faktoren mit Einfluss auf das weitere Überleben (EBM IIB: ). 9 Therapie der testikulären intraepithelialen Neoplasie Bei Nachweis einer testikulären intraepithelialen Neoplasie (TIN) ist eine Therapie sinnvoll, da die kumulative Wahrscheinlichkeit für die Entwicklung eines Hodentumors nach sieben Jahren 70% beträgt (EBM IIB: ). Durch Orchiektomie oder Radiotherapie wird das residuelle Potential der Fertilität vernichtet, durch eine
7 7 Chemotherapie vorübergehend reduziert. Da die Tumorentwicklung aus der testikulären intraepithelialen Neoplasie zumeist verzögert abläuft, ist bei Patienten mit Kinderwunsch eine abwartende Strategie gerechtfertigt, vorausgesetzt, es bestehen eine (zur assistierten Konzeption ausreichende) Restspermiogenese und die Bereitschaft zu regelmäßigen Kontrolluntersuchungen. Die definitive Therapie hängt von der Gesamtsituation des Patienten ab (Übersicht: 3 (EBM IV)). Liegt eine testikuläre intraepitheliale Neoplasie im Einzelhoden vor (zum Beispiel kontralaterale testikuläre intraepitheliale Neoplasie bei Hodentumor), so ist eine Strahlentherapie mit 8 Gy das geeignete Vorgehen (EBM III: 9,,5). Die Dosis wird in neun Fraktionen von je Gy innerhalb von zwei Wochen eingestrahlt. Halbjährliche Kontrollen des Serumtestosterons sind notwendig. Eine Kontrollbiopsie ist nicht erforderlich. Eine Ablatio testis ist sinnvoll, wenn ein gesunder kontralateraler Hoden vorhanden ist und eine Bestrahlungsbehandlung der testikulären intraepithelialen Neoplasie den gesunden Hoden gefährdet (Streustrahlung) oder eventuell auch bei prätherapeutisch bereits stark atrophischem Hoden. Wenn primär eine Chemotherapie geplant ist, sollte die Radiotherapie der testikulären intraepithelialen Neoplasie zurückgestellt werden, da durch die Summation von Chemotherapie und Strahlentherapie zu starke Schäden an den LeydigZellen zu erwarten sind und etwa zwei Drittel der Fälle mit intraepithelialer Neoplasie allein durch eine Chemotherapie geheilt werden (EBM IIB: 5,6). Findet sich sechs Monate nach Chemotherapie in der Kontrollbiopsie eine Persistenz der intraepithelialen Neoplasie, sollte sekundär bestrahlt werden. 0 Therapie des Seminoms CS I Das Risiko einer okkulten Metastasierung in den lokoregionären Lymphknoten im Stadium I beträgt ca. 0% (EBM IIB: 00,79). Dennoch wird eine Heilungsrate von nahezu 00% erzielt. Sie kann mit zwei Strategien erreicht werden: adjuvante Strahlentherapie mit Verminderung des Rezidivrisikos auf 3 bis % (EBM IB: 30,3; EBM II A: 33) oder Surveillance mit definitiver Therapie nur bei Rezidiv (Radiotherapie oder Chemotherapie). Entsprechend einer Metaanalyse der publizierten waitandsee Studien besteht ein höheres Rezidivrisiko bei Patienten mit einer Primärtumorgröße von > cm oder bei einer Invasion des Rete testis (EBM III: 98,99,35). Diese Risikofaktoren sind jedoch bisher nicht prospektiv evaluiert worden, sodass ein risikoadaptiertes Vorgehen derzeit nicht gesichert ist. Das Zielvolumen bei adjuvanter Radiotherapie umfasst die infradiaphragmalen paraaortalen/parakavalen Lymphabflussgebiete (EBM IB: 30,3, EBM II A: 3,33). Die kraniale Feldgrenze entspricht der Oberkante des Brustwirbelkörpers (EBM IB: 30,3, EBM IIA: 3,33), die kaudale der Unterkante des Lendenwirbelkörpers 5. Die lateralen Feldgrenzen werden auf der Seite des Hodentumors durch den einzubeziehenden ipsilateralen Nierenhilus, contralateral durch die Enden der lumbalen Wirbelkörperquerfortsätze definiert (EBM IB: 30,3, EBM IIA: 3,33). Die Gesamtdosis der Bestrahlung wird in Einzeldosen von,0 Gy mit 5 Fraktionen pro Woche appliziert. In Abänderung der Empfehlung des aktualisierten Interdisziplinären Konsensus aus dem Jahr 000 (8) ist eine Gesamtdosis von 0 Gy ausreichend (bisher: 6 Gy). Diese aktuellen Änderungen bezüglich der erforderlichen Gesamtdosis, der ipsilateralen und der kaudalen Feldgrenzen begründen sich in den aktuell vorgelegten Ergebnissen der prospektiven randomisierten Studien TE8 und TE9 der
8 8 Testicular Tumour Working Party des Medical Research Council unter Einbeziehung von mehr als.000 Patienten. Hierbei wurden Gesamtdosen von 0 Gy oder 30 Gy appliziert und die Rezidivraten zwei Jahre nach Therapieabschluss verglichen. Es zeigten sich nach einer medianen Nachbeobachtungszeit von vier Jahren keine Unterschiede (EBM IB: 3) (die Empfehlung im UpdateKonsensus basierte auf nicht randomisierten Studien mit definierter Gesamtdosis von 6 Gy und im Vergleich zu den in den TE8 und TE9Studien knapperen Zielvolumina (EBM IIA: 3)). Die Bestrahlungen sollten an Linearbeschleunigern erfolgen. Eine Erweiterung des Bestrahlungsfeldes auf ipsilaterale iliakale, inguinale oder skrotale Bereiche bei anamnestischen Maldeszensus testis, inguinaler oder skrotaler Voroperation oder pt3/primärtumoren ist nicht erforderlich (EBM IIA: 35, EBM II B: 36, EBM III: 37,38). Es ist nicht gesichert, dass eine adjuvante Carboplatintherapie gleiche Ergebnisse wie eine Radiotherapie erreicht. Ähnliche Ergebnisse sind zu erwarten (EBM IIB: 39), allerdings ist die Anzahl notwendiger Therapiezyklen noch unklar (EBM IIB: 39,). Außerhalb aktueller Studien ist eine Carboplatintherapie nicht indiziert. Hinsichtlich der Bewertung, ob adjuvante Strahlenbehandlung und Surveillance als gleichwertig anzusehen sind, konnte kein Konsens erzielt werden, sodass keine Empfehlung ausgesprochen wird, welche der beiden Strategien als Standardvorgehen bevorzugt werden sollte. Stattdessen werden im Folgenden die Vor und Nachteile beider Optionen, adjuvante Radiotherapie und Surveillance, dargestellt: 0. Adjuvante Radiotherapie hvorteile: die möglichen Akutnebenwirkungen sind mild bis moderat (EBM IIA: 3), die Rezidivrate beträgt 3 bis %; Rezidive treten nur ausserhalb des Bestrahlungsvolumens auf (EBM IB: 30, EBM IIA: 3, EBM IIB: 3,) hnachteile: die Radiotherapie bedeutet für ca. 80% der Patienten eine Übertherapie, da diese auch ohne adjuvante Radiotherapie rezidivfrei bleiben, es besteht prinzipiell ein Risiko radiogener Induktion von Zweitmalignomen (EBM III: 57); allerdings liegen keine Daten über die Risikohöhe bei heutiger Radiotherapie mit reduzierten Dosen und Zielvolumina vor. 0. Surveillance hvorteil: ca. 80% der Patienten benötigen nach der Orchiektomie über die Nachsorge hinaus keine weitere Therapie. hnachteile: die Rezidivrate beträgt ca. 0% (97% retroperitoneal/hoch iliakal) (EBM IIB: 98,00,0,9,8,9); Rückfälle können spät auftreten (bis zu neun Jahren nach Diagnose des Primärtumors) (EBM IIB: 00,9, EBM III: 50), sodass eine verlängerte Nachsorge dieser Patienten notwendig ist,
9 9 bei diesen Patienten ist die nachfolgende Therapie intensiver (drei Viertel der Patienten benötigen eine höher dosierte und ausgedehntere Strahlentherapie, ein Viertel eine Chemotherapie) (EBM IIB: 9, EBM III: 8), aufgrund des höheren Rezidivrisikos besteht möglicherweise eine höhere psychische Belastung (EBM III: 5), innerhalb der ersten fünf Nachsorgejahre sind zusätzliche (sechs) CT Abdomenuntersuchungen notwendig. Therapie des Seminoms CS IIA/B Die Standardtherapie im klinischen Stadium IIA/B des Seminoms ist die Bestrahlung. Das Zielvolumen umfasst die retroperitonealen paraaortalen und ipsilateral iliakalen Lymphstationen. Die kraniale Feldgrenze entspricht der Oberkante des Brustwirbelkörpers, die kaudale Feldgrenze dem Oberrand des Acetabulums. Im Stadium IIA entsprechen die lateralen Feldgrenzen den Abschlüssen der Wirbelkörperquerfortsätze, im Stadium IIB werden sie individuell an die Ausdehnung der Lymphome angepasst. Es ist darauf zu achten, dass die Lymphome mit einem Sicherheitsabstand von bis,5 cm erfasst werden. Im klinischen Stadium IIA werden 30 Gy, im Stadium IIB 36 Gy homogen verabreicht; die Fraktionierung beträgt 5mal Gy pro Woche (EBM IIB: 5). Die Dosisspezifikation erfolgt auf die Mitte des Zentralstrahls (gemäß ICRUReport 50). Vier bis sechs Wochen nach Abschluss der Therapie erfolgt eine computertomographische Kontrolle zur Beurteilung des Ansprechens der Therapie (EBM IIB: 5, EBM III: 536). Eine Erweiterung des Bestrahlungsfeldes auf den kontralateralen iliakalen, inguinalen oder skrotalen Bereich bei anamnestischen Maldeszensus testis, inguinaler oder skrotaler Voroperation oder pt3/primärtumoren ist nicht erforderlich (EBM IIA: 35, EBM III: 37,6). Das rezidivfreie Überleben nach vier Jahren beträgt 9,5% im Stadium IIA/B (EBM IIB: 3). Wegen Rezidivraten in den Stadien IIA von knapp 5% bzw. IIB von % wird zur Zeit in Studien geprüft, ob eine Chemotherapie oder eine kombinierte Radio /Chemotherapie die mit alleiniger Bestrahlungsbehandlung erreichten Ergebnisse verbessern können (EBM IIB: 63). Therapie des Nichtseminoms CS I Die Heilungsrate beträgt unabhängig vom therapeutischen Vorgehen 99%. Dies kann mit zwei Therapiestrategien erreicht werden: der retroperitonealen Lymphadenektomie (RLA) oder einer risikoadaptierten Therapie mit Surveillance für Patienten mit niedrigem Risiko und adjuvanter Chemotherapie für die mit hohem Risiko (s.u.). Eine Radiotherapie wird nicht als adäquate Therapiealternative zur Surveillance angesehen (EBM IB: 6). Hinsichtlich der Bewertung, ob beide Strategien als gleichwertig anzusehen sind, konnte kein Konsens erzielt werden, sodass keine Empfehlung ausgesprochen wird, welche der beiden Strategien als Standardvorgehen bevorzugt werden sollte. Stattdessen werden im Folgenden die Vor und Nachteile beider Optionen dargestellt. Bei korrekt durchgeführtem klinischen Staging haben 7% (EBM III: 65) bis 30% (EBM III: 6,66) dieser Patienten okkulte retroperitoneale Metastasen; weitere 8% (EBM III: 67) werden Lungenmetastasen entwickeln.
10 0 Eine vaskuläre Invasion (VI) ist der einzige bisher in prospektiven klinischen Studien als signifikant identifizierte Risikofaktor für eine okkulte Metastasierung. 8% der Patienten mit VI (highriskgruppe) entwickeln Rezidive, die bei 6% retroperitoneal und bei 5% pulmonal auftreten (EBM IIB: 0). Bei Patienten ohne nachgewiesene VI (lowrisk Gruppe) tritt in bis % ein Rezidiv auf (EBM IIA: 0,06,5). Die Beurteilung einer vaskulären Invasion zeigt bei > 30% der Fälle Unterschiede zwischen lokaler und Referenzpathologie (EBM III: 9). Eine prospektive Evaluation der Risikofaktoren und der zur Verfügung stehenden Vorgehensweisen erfolgt zur Zeit in einer Studie der Arbeitsgruppe. Die Vor und Nachteile der beiden Vorgehensweisen werden im Folgenden beschrieben:. Primär operatives Vorgehen ohne Risikoadaptation hvorteile gegenüber dem risikoadaptierten Vorgehen (.): das Tumorstadium wird histopathologisch gesichert, das Risiko für die Entwicklung von retroperitonealen Metastasen wird auf 0 bis % gesenkt im Vergleich zur SurveillanceStrategie (EBM IIA: 68, EBM III: 66,69), 6 bis 75% dieser Patienten benötigen nachfolgend keine Chemotherapie, einfachere Nachsorge, da in erster Linie pulmonale Rezidive (8%) auftreten. hnachteile gegenüber dem risikoadaptierten Vorgehen (.): operatives Vorgehen bedeutet für 70 bis 83% der Patienten eine Übertherapie, da diese auch ohne Operation rezidivfrei bleiben, die akute operative Morbidität beträgt ca. 9% (EBM III: 70), nach Operation kann ein Ejakulationsverlust auftreten (% der Patienten in Zentren!) (EBM III: 66,69), bei 8 bis 0% der Patienten treten trotz Operation Lungenmetastasen und/oder retroperitoneale Rezidive bzw. eine ausschließliche Erhöhung der Tumormarker in den ersten beiden Jahren nach Operation auf (EBM III: 67).. Risikoadaptiertes Vorgehen mit Surveillance bei lowrisk und adjuvanter Chemotherapie bei highrisk.. Surveillance für lowrisk Gruppe (keine vaskuläre Invasion im Primärtumor; Risiko für retroperitoneale und/oder pulmonale Metastasierung: % (EBM IIA: 0,06,5)) hvorteil gegenüber primärem operativem Vorgehen (RLA) (.): 78 bis 86% der Patienten benötigen nach der Orchiektomie über die Nachsorge hinaus keine weitere Therapie. hnachteile gegenüber primärem operativem Vorgehen (RLA) (.): bis % der Patienten benötigen eine Chemotherapie beim Rezidiv (3 x PEB*) im Vergleich zu 8 bis 0% nach RLA, aufgrund des höheren Rezidivrisikos besteht möglicherweise eine höhere psychische Belastung (EBM III: 5),
11 innerhalb der ersten fünf Nachsorgejahre sind zusätzliche (sechs) CT Abdomenuntersuchungen notwendig... Adjuvante Chemotherapie ( x PEB*) für die highrisk Gruppe (Nachweis einer vaskulären Invasion im Primärtumor; Risiko für retroperitoneale und/oder pulmonale Metastasierung ohne adjuvante Chemotherapie 8%, mit adjuvanter Chemotherapie 3% (EBM IIB: 0)) hvorteile gegenüber primär operativem Vorgehen (.): über die Orchiektomie hinaus ist keine weitere Operation erforderlich, das Rezidivrisiko ist niedrig mit ca. 3% (EBM IIA: 7, EBM III: 7), die Nachsorge ist einfacher. hnachteile gegenüber primär operativem Vorgehen (.): adjuvante Chemotherapie bedeutet für 5% der Patienten eine Übertherapie, da diese auch ohne Chemotherapie rezidivfrei bleiben, es treten chemotherapieassoziierte Akuttoxizitäten durch zwei Zyklen Chemotherapie auf, es kommt zur vorübergehenden Beeinträchtigung der Fertilität für ca. 3 Jahre (EBM IIA: 7, EBM IIB: 73), es besteht prinzipiell ein Risiko der Induktion von Zweitmalignomen durch Zytostatika (EBM III: 57), allerdings liegen keine Daten über Risikohöhe bei Applikation von nur zwei Zyklen PEB vor (bisher kein Fall berichtet). * PEB: Cisplatin, Etoposid (VP 6), Bleomycin 3 Therapie des Nichtseminoms CS IIA/B Die Heilungsrate beim Nichtseminom CS IIA/B beträgt >/= 98%. Diese kann mit drei verschiedenen Strategien erreicht werden, die sich im Ausmaß der Therapie und den Morbiditäten unterscheiden: primäre nervschonende Lymphadenektomie und adjuvante Chemotherapie (xpeb)(option ), primäre nervschonende Lymphadenektomie ohne adjuvante Chemotherapie (Option ), primäre Chemotherapie +/ Residualtumorresektion (Option 3). Ein risikoadaptiertes Vorgehen ist nicht möglich, da die bekannten Faktoren nicht prospektiv evaluiert worden sind. Hinsichtlich der Bewertung, ob die drei Strategien als gleichwertig anzusehen sind, konnte kein Konsens erzielt werden, sodass keine Empfehlung ausgesprochen wird, welche dieser Strategien als Standardvorgehen bevorzugt werden sollte. Stattdessen werden im Folgenden die Vor und Nachteile beider Optionen dargestellt: 3. Primäre nervschonende Lymphadenektomie und adjuvante Chemotherapie (xpeb)(option )
12 hvorteil gegenüber primärer CTX +/ Residualtumorresektion (Option 3): bis 3% der Patienten wird eine Chemotherapie im Vergleich zur Option 3 erspart, da ein Stadium PS I (EBM IB:7, EBM IIA: 75) festgestellt wird, innerhalb der ersten fünf Nachsorgejahre sind drei CTAbdomenuntersuchungen weniger erforderlich als bei Option 3, hvorteil gegenüber RLA ohne CTX (Option ) und gegenüber primärer CTX +/ Residualtumorresektion (Option 3): die Rezidivrate beträgt 0 bis 7%; Rezidive treten im Vergleich zu Optionen und 3 fast ausschließlich außerhalb des Retroperitoneums auf (EBM IB: 7, EBM IIA: 75, EBM III: 76,77). hnachteil gegenüber RLA ohne CTX (Option ): es besteht prinzipiell ein Risiko der Induktion von Zweitmalignomen durch Zytostatika (EBM III: 57), allerdings liegen keine Daten über Risikohöhe bei Applikation von nur zwei Zyklen PEB vor (bisher kein Fall berichtet), hnachteil gegenüber primärer CTX +/ Residualtumorresektion (Option 3): die operative Morbidität ist relevant und beträgt an Zentren ca. 0% (EBM IIB: 78, EBM III: 70), nach Operation kann trotz nervschonender Intention ein Ejakulationsverlust auftreten (5 bis 5% der Patienten in Zentren, sonst in 3% im Vergleich zu 3% beim Vorgehen nach Option 3) (EBM IIA: 75, EBM III: 76,79), hnachteil gegenüber RLA ohne CTX (Option ) und gegenüber primärer CTX +/ Residualtumorresektion (Option 3): therapieassoziierte Toxizitäten erhöhen sich durch Operation plus Chemotherapie für alle Patienten (EBM IIA: 80, EBM III: 8). 3. Primäre nervschonende Lymphadenektomie ohne adjuvante Chemotherapie (Option ) hvorteil gegenüber RLA + adjuvanter CTX (Option ): die Behandlung wird auf eine Therapiemaßnahme begrenzt, hvorteil gegenüber primärer CTX +/ Residualtumorresektion (Option 3): ca. % der Patienten wird eine Chemotherapie im Vergleich zur Option 3 erspart, da ein Stadium PS I (EBM IB: 7, EBM IIA: 75) festgestellt wird, innerhalb der ersten fünf Nachsorgejahre sind drei CTAbdomenuntersuchungen weniger erforderlich als bei Option 3, hvorteil gegenüber RLA + adjuvanter CTX (Option ) und gegenüber primärer CTX +/ Residualtumorresektion (Option 3): die Chemotherapie wird im Vergleich zu den Optionen und 3 nur für 30% der Patienten im Stadium PS IIA bzw. für 50% im Stadium PS IIB notwendig. hnachteil gegenüber RLA + adjuvanter CTX (Option ): im Falle eines Progresses sind mindestens drei Zyklen Chemotherapie im Vergleich zu zwei Zyklen erforderlich, hnachteil gegenüber primärer CTX +/ Residualtumorresektion (Option 3):
13 3 die operative Morbidität ist relevant und beträgt an Zentren ca. 0% (EBM IIB: 78, EBM III: 70), nach Operation kann trotz nervschonender Intention ein Ejakulationsverlust auftreten (5 bis 5% der Patienten in Zentren, sonst in 3% im Vergleich zu 3% bei Option 3) (EBM IIA: 75, EBM III: 76,79), hnachteil gegenüber RLA + adjuvanter CTX (Option ) und gegenüber primärer CTX +/ Residualtumorresektion (Option 3): das Rezidivrisiko ist höher mit 30% im Stadium PS IIA und bis zu 50% im Stadium PS IIB (EBM IB: 7, EBM IIA: 8, EBM III: 76,77,83). 3.3 Primäre Chemotherapie +/ Residualtumorresektion (Option 3) hvorteil gegenüber RLA + adjuvanter CTX (Option ) und gegenüber RLA ohne CTX (Option ): wegen kompletter Remission (CR) nach Chemotherapie entfällt für die Mehrheit der Patienten eine Operation (CR im Stadium PS IIA: 83 bis 9%, im Stadium PS IIB: 6 bis 87%) (EBM IIA: 75, EBM IIB: 8, EBM III: 85,86), die Rezidivrate ist niedrig(er) (im Stadium PS IIA: bis 9%, im Stadium PS IIB: bis 5%) (EBM IIA: 75, EBM IIB: 8), ein Ejakulationsverlust tritt in 3% gegenüber 3% bei den Optionen und auf, da eine Residualtumorresektion nur bei 9 bis 7% der Patienten im Stadium CS IIA bzw. 3 bis 39% im Stadium IIB erforderlich wird (EBM IIA: 75). hnachteil gegenüber RLA + adjuvanter CTX (Option ) und gegenüber RLA ohne CTX (Option ): die Chemotherapie ist für bis 3% der Patienten unnötig, da bei ihnen ein Stadium PS I vorliegt (EBM IB*: 86, EBM IIA: 75, EBM III: 85,87,88), die operative Morbidität wird durch die Erfordernis einer Residualtumorresektion bei 9 bis 7% der Patienten im Stadium CS IIA bzw. bei 3 bis 39% im Stadium CS IIB erhöht (EBM IIA: 75, EBM III: 73,85,86,899), innerhalb der ersten fünf Nachsorgejahre sind drei CTAbdomenuntersuchungen mehr als bei primärer Operation erforderlich, die Chemotherapie ist bei dieser Option mit drei Zyklen gegenüber zwei Zyklen PEB bei der Kombination Operation + adjuvante Chemotherapie intensiver, hnachteil gegenüber RLA ohne CTX (Option ): es besteht prinzipiell ein Risiko der Induktion von Zweitmalignomen durch Zytostatika (EBM III: 57) *86: EBM IB bezogen auf erwähnte EORTCStudie in diesem Artikel Therapie der fortgeschrittenen Stadien Für Patienten mit good prognosis nach IGCCCG (8,8) besteht die Standardtherapie aus drei Zyklen PEB oder bei Kontraindikationen gegen Bleomycin in vier Zyklen PE (EBM IA: 8,8, EBM IB: 99). Die Effektivität des PEBRegimes, appliziert über 5 Tage mit Etoposid 00 mg/m² und Cisplatin 0mg/m² pro Tag ( amerikanisches Schema), ist gleichwertig zu dem PEBSchema mit Applikation von Etoposid 65 mg/m² an 3 Tagen und Cisplatin 50mg/m² an Tagen ( englisches Schema) (EBM IB: 9).
14 Allerdings ist die verkürzte Version mit einer höheren Langzeittoxizität (Ototoxizität, Nausea, Emesis, periphere Neurotoxizität, RaynaudPhänomen) belastet, wenn vier Zyklen gegeben werden, sodass das DreiTages gegenüber dem FünfTagesProtokoll nur äquitoxisch ist, wenn drei Zyklen verabreicht werden (EBM IB: 9,95). Bei Applikation von vier Zyklen (intermediate oder poorprognosisgruppen, s.u.) sollte das Originalprotokoll mit fünftägiger Therapie weiterhin alleiniger Standard sein. Die Therapie sollte ohne Dosisreduktion in tägigen Intervallen verabreicht werden; eine Verzögerung des nachfolgenden Chemotherapiezyklus ist nur bei Fieber mit Granulozytopenie oder Thrombopenie < / µl gerechtfertigt. Eine Indikation zur primären prophylaktischen Applikation von hämatopoetischen Wachstumsfaktoren, wie zum Beispiel GCSF, besteht nicht. Falls allerdings infektiöse Komplikationen unter der Chemotherapie aufgetreten sind, wird für die nachfolgenden Zyklen die prophylaktische Gabe von GCSF empfohlen (EBM IIA: 96,97). Mit der intermediate prognosis Gruppe in der IGCCCGKlassifikation wurde eine Gruppe von Patienten definiert, die eine FünfJahresÜberlebensrate von etwa 80% erreicht. Für diese Patienten gibt es keine abgeschlossenen prospektiven Studien. Die vorliegenden Daten unterstützen vier Zyklen PEB als Standardtherapie (EBM IA: 8,8, EBM IB: 98). Wegen der insgesamt ungünstigeren Prognose dieser Patientengruppe im Vergleich zu Patienten mit good prognosis sollte deren Therapie prinzipiell in prospektiven Studien erfolgen (EBM IV: 99). Bei Patienten mit poor prognosis besteht die Standardtherapie in vier Zyklen PEB; vier Zyklen PEI* sind gleich wirksam, aber myelotoxischer (EBM IB: 00). Das progressionsfreie Überleben nach fünf Jahren liegt zwischen 5 und 50% mit nachgewiesener Verbesserung der Überlebensraten in den letzten zwei Jahrzehnten (EBM III: 0). Es ist bisher nicht in prospektiven Studien nachgewiesen, dass eine Hochdosischemotherapie die Überlebensrate steigert. Da eine MatchedpairAnalyse eine bessere Überlebensrate ergeben hatte (EBM IIB: 0,03), sollten diese Patienten in prospektiven Studien behandelt werden, in denen der Wert einer Hochdosischemotherapie geprüft wird. Patienten, die poor prognosis Kriterien erfüllen, müssen daher an ein entsprechendes Zentrum überwiesen werden (EBM IV). Generelle Empfehlungen zu Therapiemodifikationen bei Patienten mit schlechtem Allgemeinzustand (Karnofsky < 50%), ausgedehnter Leberinfiltration (> 50%) und ausgedehnter pulmonaler Infiltration existieren nicht (EBM IV). *I: Ifosfamid 5 Therapie bei Hirnmetastasen Etwa 0% aller Patienten in fortgeschrittenen Erkrankungsstadien eines Hodentumors entwickeln eine zerebrale Metastasierung. Unter prognostischen Aspekten ist zwischen einer primären Hirnmetastasierung mit einer langfristigen Überlebenswahrscheinlichkeit von etwa 30 bis 0% (kurative Indikation) und einer unter Therapie oder im Rezidiv auftretenden Filialisierung mit einer FünfJahresÜberlebenswahrscheinlichkeit von etwa bis 5% zu unterscheiden. Die günstigste Prognosegruppe bilden Patienten mit unilokulärem Herd, der im Rahmen der Primärdiagnostik entdeckt wird (EBM IIA: 8, EBM III: 83). Der optimale Einsatz und die Sequenz der einzelnen Therapiemodalitäten (Chemotherapie, Radiotherapie, Operation) sind nicht abschließend geklärt. Das Vorliegen einer Hirnmetastasierung stellt keine Kontraindikation gegen die Durchführung einer intensivierten HochdosisChemotherapie (mit autologer Stammzell
15 5 Transplantation) dar. Entsprechend einer Analyse der GTCSG konnte durch diese Vorgehensweise bei poor prognosis Patienten mit Hirnmetastasierung eine Zwei JahresÜberlebensrate von 8% erreicht werden (EBM III: 0). Mit kurativer Zielsetzung in der Primärtherapie sollten Chemotherapie (vier Zyklen platinhaltige Standardkombinationen) und Strahlentherapie (Bestrahlung des gesamten Hirnes mit 050 Gy gegebenenfalls mit Aufsättigung der Metastasenregion auf hier resultierende Gesamtdosen von 550 Gy, appliziert in Einzeldosen von,8 bis Gy, 5mal pro Woche) vorzugsweise parallel, gegebenenfalls auch sequentiell (Chemotherapie gefolgt von Radiotherapie) eingesetzt werden (EBM IIA: 63, EBM III: 83; EBM IIB: 05). Ob grundsätzlich eine konsolidierende Bestrahlungsbehandlung des Hirnschädels nach chemotherapeutisch erreichter kompletter Remission erforderlich ist, ist ungeklärt. Die Indikation zur sekundären Resektion solitärer posttherapeutischer Residuen (MRT zwingend zur Abklärung von Mikrometastasen erforderlich) ist nicht gesichert; sie hängt vom Ausmaß der systemischen Erkrankung ab. Sie sollte nur in individuellen Fällen (Resektion sonstiger Herde im Körper möglich, teratomhaltige Primärhistologie, zystische Veränderung des Hirntumors in der Bildgebung und operationstechnisch günstige Lokalisation) erfolgen. 6 Therapiesteuerung Zunächst werden obligat zwei Zyklen der Chemotherapie gegeben; danach erfolgt die Reevaluation mit bildgebenden Verfahren und Bestimmung der Tumormarker. Bei Markerabfall und stabiler oder regredienter Tumormanifestation wird die Chemotherapie komplettiert (drei bzw. vier Zyklen je nach Ausgangsstadium) (EBM II A: 8,8,06,07). Bei Markerabfall, aber wachsenden Metastasen erfolgt eine Resektion nach Abschluss der Induktionstherapie, sofern keine Notfallsituation aufgrund des lokalen Tumorwachstums besteht (EBM IV). Nur bei dokumentiertem Markeranstieg nach Zyklen Chemotherapie ist ein frühzeitiger Wechsel der Therapie indiziert (am ehesten frühzeitige Hochdosistherapie; Wechsel auf andere, konventionell dosierte Therapieregime nicht effektiv) (EBM IIB: 03,08). Bei Patienten mit Markerplateau auf niedrigem Niveau nach Abschluss der Chemotherapie wird zunächst zugewartet, ob eine vollständige Normalisierung eintritt. Eine Salvagechemotherapie ist nur bei eindeutigem Markerprogress indiziert (EBM III: 09). 7 Residualtumorresektion Beim Seminom werden Residuen unabhängig von der Größe nicht reseziert, sondern zunächst bildgebend und mit Tumormarkerbestimmungen kontrolliert (EBM III: 06). Eine aktuelle retrospektive Analyse zum diagnostischen Wert der PET wies eine hohe Zuverlässigkeit bei der Bestimmung der Vitalität von Resttumoren nach Chemotherapie beim reinen Seminom nach. Falsch positive Befunde seien nicht zu erwarten, falsch negative Befunde traten bei Residuen >3cm nicht auf (EBM III: 7). Bei Progression wird eine Salvagechemotherapie durchgeführt, gegebenenfalls unter Einschluss von Resektion und Radiotherapie (EBM III: 8, EBM IV: 9,0). Nach primärer Radiotherapie sollte jedoch chemotherapiert werden aufgrund zu erwartender erhöhter operativer Morbidität. Beim Nichtseminom und kompletter Remission nach Chemotherapie ist eine sekundäre RLA nicht indiziert (EBM IIB:,, EBM III: 35, EBM IV: 8), wohingegen bei
16 6 residuellem Befund und Markernormalisierung der Restbefund reseziert wird (EBM IIA: 6,7, EBM IIB: 8,9, EBM III: 3033), EBM IV: 8). Weil gegenwärtig kein bildgebendes Diagnostikverfahren oder Prognosemodell eine histologische Differenzierung des Residualtumors vorhersagen kann, ist eine Residualtumorresektion obligat (EBM IIB:,,3, EBM III: 3,3537). Das operative Vorgehen hierbei ist beschrieben (6,9). Aufgrund diskordanter histologischer Befunde retroperitonealer und supradiaphragmaler Residuen (35 bis 50%) und nicht ausreichender prognostischer Modelle zur Vorhersage der Dignität der supradiaphragmalen Residuen (89% richtig positiv bei Nachweis von Nekrose im Retroperitoneum) kann bei supra und infradiaphragmalen zunächst auf eine Resektion der supradiaphragmalen verzichtet werden (EBM II B:,3,38,39, EBM III: 8,3,35). Eine Resektion retroperitonealer Residuen sollte daher der Entfernung supradiaphragmaler Reste unter Berücksichtigung der Dominanz der Tumorresiduen vorangehen (EBM IIB: 3, EBM III: 35). Die Indikation zur Resektion hämatogener Residualtumoren außerhalb der Lunge sollte individuell, gegebenenfalls nach Biopsie, gestellt werden (EBM III: 35,0,). 8 Konsolidierende Chemotherapie nach Resektion von vitalem Resttumor Nach Resektion von Nekrosen oder reifem Teratom ist keine weitere Therapie erforderlich. Bei Nachweis vitalen Karzinoms im Resektat ist die Erfordernis einer nachfolgenden (weiteren) Chemotherapie (z.b. zwei Zyklen konventionell dosierte cisplatinhaltige Chemotherapie (cave: kumulative Dosis von Bleomycin)) unklar. Eine aktuelle retrospektive Analyse ergab keine Verlängerung des Gesamtüberlebens nach Applikation einer konventionell dosierten cisplatinhaltigen Chemotherapie, sodass individuell alternativ auch eine abwartende Haltung gerechtfertigt scheint (EBM III: ). Prognostisch günstig und bei der Therapieentscheidung zu berücksichtigen sind komplette Resektion, good prognosis nach IGCCCGKlassifikation und ein Anteil von <0% vitaler Tumorzellen im Resektat. Die Prognose verschlechtert sich deutlich, wenn nach einer Second oder ThirdlineChemotherapie vitales Karzinom im Resektat nachgewiesen wird. Hier gibt es keinen Beleg dafür, dass eine postoperative Chemotherapie die Prognose verbessert (EBM IV: 3,36). 9 Systemische Salvagetherapie Seminom Patienten, die nach alleiniger Radiatio ein Rezidiv erleiden, haben in der Mehrzahl eine günstige Prognose mit Heilungsraten >90% und sollten eine cisplatinhaltige Chemotherapie analog den Therapiestrategien bei Seminomen fortgeschrittener Stadien erhalten (siehe Abschnitt ; EBM II A: 33). Patienten mit Rezidiv nach Chemotherapie können mit einer cisplatinhaltigen Salvagetherapie zu etwa 50% in eine erneute langfristige Remission gebracht werden (EBM IIB: 3). Für die Salvagebehandlung dieser Patienten bestehen folgende Optionen: vier Zyklen PEI/V*IP bzw. Vel**IP. Ob eine cisplatinhaltige Kombinationstherapie ausreicht oder eine frühzeitige Therapieintensivierung mit HochdosisChemotherapie erforderlich ist, kann derzeit nicht beurteilt werden (EBM IV: ). Aus diesem Grunde ist die Behandlung dieser Patienten an Zentren und innerhalb von Studien dringend erforderlich.
17 7 *V: VP6=Etoposid (Vepesid), ** Vel: Vinblastin (Velbe) Nichtseminom Patienten, die nach alleiniger Operation ein Rezidiv erleiden, haben in der Mehrzahl eine günstige Prognose mit Heilungsraten >90% und sollten eine cisplatinhaltige Chemotherapie analog den Therapiestrategien bei Nichtseminomen fortgeschrittener Stadien erhalten (siehe Abschnitt ). Bei Patienten mit Rezidiv nach Chemotherapie besteht die Standardtherapie für die Salvagebehandlung in der Gabe von vier Zyklen PEI/VIP bzw.veip. Eine konventionell dosierte Salvagetherapie erzielt, je nach Vorliegen von Risikofaktoren, langanhaltende Remissionen bei 5 bis 0% der Patienten (EBM IIB:,5). Eine Salvagetherapie mit VeIP ist wahrscheinlich anderen konventionell dosierten cisplatinhaltigen Therapiekombinationen nicht überlegen (EBM IIB:,5). Der Einsatz von konventionell dosierten Therapiekombinationen mit mehr als drei Substanzen scheint die Toxizität zu erhöhen, ohne jedoch die Ergebnisse zu verbessern (EBM IIB:,6). Abhängig von Prognosefaktoren sind die Behandlungsergebnisse im Rezidiv/Progress nach cisplatinhaltiger Therapie insgesamt ungünstig (EBM IIb: 0,). Phase II Studien deuten auf eine Verbesserung der Überlebensrate um 0% hin bei früher Intensivierung der Salvagebehandlung mit Hochdosischemotherapie (EBM III: 7). Daher sollten alle diese Patienten für laufende Studienprotokolle evaluiert und an Zentren überwiesen werden (EBM IV: ). 0 Operative Rezidiv/Salvagetherapie Residualtumoren nach Salvagechemotherapie sollten bei Markernormalisierung oder Bestätigung eines Markerplateaus nach vier bis sechs Wochen reseziert werden. Bei Markeranstieg und fehlenden weiteren chemotherapeutischen Optionen ist bei kompletter Resektabilität der Tumormanifestation eine Resektion anzustreben (in ca. 5% längerfristiges Überleben belegt) (EBM III:,50,9,3,37,39,856). Organisatorisches zur Durchführung der Lymphadenektomie und Chemotherapie Die Therapiemaßnahmen sollten grundsätzlich nur von Ärzten durchgeführt werden, die mit diesen Verfahren sowie mit der Erkennung und der Behandlung möglicher Komplikationen ausreichende Erfahrungen haben, da sich ansonsten die Prognose dieser Patienten signifikant verschlechtert (EBM III: 5759). Insbesondere bei Patienten mit Hodentumoren in fortgeschrittenen Stadien oder mit aus anderen Gründen schwieriger Konstellation sollte eine Kontaktaufnahme mit in der Behandlung von Hodentumoren ausgewiesenen Zentren erfolgen (Adressen über Internet: oder Evaluation des Therapieergebnisses Die Evaluation sollte individuell abhängig von Stadium und Therapie erfolgen. Ein CT des Abdomens einschließlich kranialer Beckenabschnitte bis in Höhe der Aufzweigung der Iliakalgefäße ist bei primärer Chemotherapie ab Stadium IIA notwendig, ein CT des Thorax lediglich bei supradiaphragmalem Befall (EBM IIB: 58,59,60) (Tabellen 3a und
18 8 3b). Die Tumormarker müssen unter Berücksichtigung der Halbwertzeiten (AFP 57 Tage, ßHCG 36 Stunden, LDH Stunden) nach Orchiektomie kontrolliert werden, wenn sie primär erhöht waren. Vor jeder weiteren Therapie und nach Abschluss der Gesamttherapie ist eine Markerkontrolle erforderlich. Ebenso muss vor jedem Chemotherapiezyklus eine Kontrolle der Marker erfolgen. Bei einem Markerplateau sollten zunächst eine engmaschige Kontrolle mittels Markerbestimmung und bildgebender Diagnostik und erst bei erneutem Markeranstieg eine Salvagetherapie durchgeführt werden. Tabelle 3: Einsatz der Computertomographie zur Evaluation des Therapieergebnisses beim Seminom und beim Nichtseminom nach Stadium und Behandlungsmodalität(en) Seminom Stadium I Stadien IIA/B Stadien IIC/III Therapiemodalität(en Radiati adj.ctx Radiat CTX CTX +/ OP ) o io Diagnostik CT Abdomen/Becken CTThorax bei supradiaphragmalem Befund Nichtseminom Stadium I Stadien IIA/B Stadien IIC/III Therapiemodalität(en RLA adj.ctx RLA CTX +/ CTX +/ OP ) OP Diagnostik CT + + Abdomen/Becken CTThorax bei supradiaphragmalem Befund Bei Feststellung von Tumorprogressionen/Rezidiven sollten Fehleranalysen bisheriger Diagnostik und Therapiemaßnahmen vorgenommen werden (EBM III: 5759). 3 Nachsorge Analysiert man die Literatur (überwiegend EBM III, s. Literaturangaben) hinsichtlich der Rezidivhäufigkeiten von Seminomen und Nichtseminomen unter Berücksichtigung von Stadium und Therapie, werden auch andere Nachsorgeintervalle und Häufigkeiten für den Einsatz der unterschiedlichen bildgebenden Diagnostikverfahren als nachfolgend aufgeführt (Tabellen ac) angegeben. Diese resultieren vielmehr aus durchgeführten Therapieverfahren mit jeweils definierten Nachsorgekonzepten und deren Ergebnissen. Inwieweit hierbei Unterschiede in den Ergebnissen erkennbar wären, wenn man die Nachsorge verändert, ist bisher nicht untersucht worden. In den aufgeführten Empfehlungen wurde jedoch zusätzlich auf die Praktikabilität Wert gelegt. Individuelle
19 9 Faktoren können ein von den vorliegenden Empfehlungen abweichendes Vorgehen notwendig machen, da nur der mindesterforderliche Rahmen dargestellt werden kann. Die Nachsorge besteht aus klinischer Untersuchung, Tumormarkerbestimmungen und bildgebender Diagnostik. Fakultativ können Testosteron und FSH bestimmt werden. Sonographische Kontrollen des kontralateralen Hodens sind notwendig, sofern nicht primär durch eine PE eine TIN ausgeschlossen oder eine nachgewiesene TIN bestrahlt wurden. Bei lediglich einer Angabe in der Literatur zur Frequenz sonographischer HodenUntersuchungen (EBM III: 6) ist eine jährliche Kontrolle vermutlich sinnvoll. Die Nachsorgeuntersuchungen sind mit Ausnahme der fortgeschrittenen Stadien mit intermediate oder poor prognosis Kriterien nach IGCCCG (8,8) weitgehend einheitlich für alle Stadien, Histologien und Therapiemodalitäten im ersten und zweiten Jahr alle drei Monate durchzuführen, nachfolgend in Abhängigkeit von der Tumorart und den erfolgten Therapiemodalitäten (Tabellen ac). Zur Beurteilung des Retroperitonealraumes ist eine Computertomographie, durchgeführt nach den Richtlinien der Bundesärztekammer zum Geräte und Untersuchungsstandard (606), einer Sonographie überlegen (EBM III: 55,6,68). Die CTUntersuchung muss die kranialen Beckenabschnitte einschließlich der Aufzweigung der Iliakalgefässe umfassen. Bei der Dauer der Nachsorge über das fünfte Jahr hinaus ist neben dem Risiko von Spätrezidiven auch zu beachten, dass nach Chemo und/oder Radiotherapie ein geringes Risiko (ca. zwei bis dreifach) für therapieinduzierte Zweitmalignome besteht (EBM III: 57). Ebenso ist bei 5% der Patienten, bei denen eine kontralaterale Hodenbiopsie nicht erfolgte, die Entwicklung eines testikulären Zweittumors zu erwarten (EBM IIB: ). In einigen Stadien wird auf Empfehlungen zu radiologischen Untersuchungen über das 5. Nachsorgejahr hinaus oder beim Nichtseminom im Stadium CS II A/B nach RLA und Chemotherapie verzichtet, weil keine Rezidive berichtet wurden und weil Zweittumoren durch BildgebungsDiagnostik nicht frühzeitig, sondern zumeist aufgrund klinischer Symptomatik erkannt werden. Bei diesen Patienten sollte individuell über die Relevanz und Frequenz der apparativen Nachsorge entschieden werden. Tabelle a: Nachsorgeintervall und einzusetzende Untersuchungsverfahren bei Patienten mit Seminom in Frühstadien ohne Resttumor nach Abschluß der Therapie differenziert nach primärem Tumorstadium und Therapiemodalität Stadiu m CS I Erfolgte Therapie Adjuv.Radiothe rapie Seminom Stadien I und II Klin. Untersuchung Und Prozedur LDH, AFP, ß HCG RöntgenThorax in E CT Abdomen/Becke n. Jahr Frequenz der jährlichen Nachsorgeuntersuchungen. Jahr 3. Jahr. Jahr 5. Jahr 5.0. Jahr
20 0 CS I Surveillance LDH, AFP, ß HCG RöntgenThorax in E CT Abdomen/Becke n CSII A/B Radiotherapie LDH, AFP, ß HCG RöntgenThorax in E CT Abdomen/Becke n Tabelle b: Nachsorgeintervall und einzusetzende Untersuchungsverfahren bei Patienten mit Nichtseminom in Frühstadien ohne Resttumor nach Abschluß der Therapie differenziert nach primärem Tumorstadium und Therapiemodalität(en) Stadiu m Erfolgte Therapie CS I Diagnost. RLA LDH, AFP, ß HCG RöntgenThorax in E CT Abdomen/Becke n CS I Surveillance LDH, AFP, ß HCG RöntgenThorax in E CT Abdomen/Becke CS I Adj. Chemotherapie Nichtseminom Stadien I und II Klin. Frequenz der jährlichen Untersuchung Nachsorgeuntersuchungen Und Prozedur n LDH, AFP, ß HCG RöntgenThorax in E CT Abdomen/Becke n Jahr Jahr Jahr Jahr Jahr Jahr
Hodentumoren: Diagnose und Therapie
 Hodentumoren: Diagnose und Therapie Dr. Axel Häcker Assistenzarzt, Urologische Universitätsklinik Mannheim Anamnese - Risikofaktoren Alter Gene 70%: 20-40 a -BrüderrR10 - Söhne rr 5.7 - Väter rr 2-4.3
Hodentumoren: Diagnose und Therapie Dr. Axel Häcker Assistenzarzt, Urologische Universitätsklinik Mannheim Anamnese - Risikofaktoren Alter Gene 70%: 20-40 a -BrüderrR10 - Söhne rr 5.7 - Väter rr 2-4.3
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN
 DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
1% aller soliden Malignome des Mannes. Häufigster bösartiger Tumor der jährigen Männer. Risikofaktoren: Titel. Folie 1
 Hodentumor-Epidemiologie 1% aller soliden Malignome des Mannes Häufigster bösartiger Tumor der 20-40 jährigen Männer Risikofaktoren: Maldeszensus testis: Erkrankungsrisiko bei Brüdern: Erkrankungsrisko
Hodentumor-Epidemiologie 1% aller soliden Malignome des Mannes Häufigster bösartiger Tumor der 20-40 jährigen Männer Risikofaktoren: Maldeszensus testis: Erkrankungsrisiko bei Brüdern: Erkrankungsrisko
Aktuelle Aspekte in der Diagnose und Therapie von Hodentumoren
 Aktuelle Aspekte in der Diagnose und Therapie von Hodentumoren PD Dr. Axel Häcker Urologische Universitätsklinik Mannheim EAU Guidelines 2005 Tumormarker Tumormarker AFP (HWZ 5-7 d) HCG (HWZ 24-36 h) LDH
Aktuelle Aspekte in der Diagnose und Therapie von Hodentumoren PD Dr. Axel Häcker Urologische Universitätsklinik Mannheim EAU Guidelines 2005 Tumormarker Tumormarker AFP (HWZ 5-7 d) HCG (HWZ 24-36 h) LDH
Therapie von fortgeschrittenen Hodenkarzinomen. Annette Dieing
 Therapie von fortgeschrittenen Hodenkarzinomen Annette Dieing 14.01.2014 Stadieneinteilung Fortgeschrittene Stadien Heilungsraten Anteil der Patienten Langzeit- Überleben Frühe Stadien 75% 99% Fortgeschrittene
Therapie von fortgeschrittenen Hodenkarzinomen Annette Dieing 14.01.2014 Stadieneinteilung Fortgeschrittene Stadien Heilungsraten Anteil der Patienten Langzeit- Überleben Frühe Stadien 75% 99% Fortgeschrittene
Therapie metastasierter Hodentumoren
 Therapie metastasierter Hodentumoren Prof. Dr. Jörg Beyer Vivantes Klinikum Am Urban Dieffenbachstrasse 1 joerg.beyer@vivantes.de Fall No 1: Patient 33 Jahre Hodentumor rechts Z.n. Orchidektomie reines
Therapie metastasierter Hodentumoren Prof. Dr. Jörg Beyer Vivantes Klinikum Am Urban Dieffenbachstrasse 1 joerg.beyer@vivantes.de Fall No 1: Patient 33 Jahre Hodentumor rechts Z.n. Orchidektomie reines
Diagnostik und Therapie germinaler Hodentumoren
 Diagnostik und Therapie germinaler Hodentumoren Stand November 2003 Diagnostik und Therapie germinaler Hodentumoren Weitere Informationen Tumor Zentrum Berlin e. V. Robert-Koch-Platz 7, 10115 Berlin Tel.
Diagnostik und Therapie germinaler Hodentumoren Stand November 2003 Diagnostik und Therapie germinaler Hodentumoren Weitere Informationen Tumor Zentrum Berlin e. V. Robert-Koch-Platz 7, 10115 Berlin Tel.
Interdisziplinäre Arbeitsgruppe Hodentumoren
 Interdisziplinäre Arbeitsgruppe Hodentumoren Vorschlag Nachsorgekonzept Hodentumoren Version 01 vom 30.03.2010 Ausarbeitung: Verabschiedet: Gültig bis: Richard Cathomas (Chur), Silke Gillessen (St. Gallen),
Interdisziplinäre Arbeitsgruppe Hodentumoren Vorschlag Nachsorgekonzept Hodentumoren Version 01 vom 30.03.2010 Ausarbeitung: Verabschiedet: Gültig bis: Richard Cathomas (Chur), Silke Gillessen (St. Gallen),
Welche Untersuchungen führt der Urologe bei Verdacht auf einen Hodentumor durch?
 Hodenkrebs Was ist ein Hodentumor, was ist Hodenkrebs? Ein Hodentumor ist ein in der Regel bösartiges Geschwulst (Tumor) im Hoden, der potentiell über den Blut oder Lymphweg Tochtergeschwulste (Metastasen)
Hodenkrebs Was ist ein Hodentumor, was ist Hodenkrebs? Ein Hodentumor ist ein in der Regel bösartiges Geschwulst (Tumor) im Hoden, der potentiell über den Blut oder Lymphweg Tochtergeschwulste (Metastasen)
Thema. Hodenkarzinom. Aufbaukurs Krebswissen WS 2015.16. Gero Kramer. Urologie. Autor, Einrichtung, Abteilung...
 Aufbaukurs Krebswissen WS 2015.16 Hodenkarzinom Gero Kramer Urologie 1 Hodenkarzinom Epidemiologie 1% aller bösartiger Neubildungen beim Mann 3-10 neue Fälle / 100 000 Männer / Jahr (Westen) Anstieg in
Aufbaukurs Krebswissen WS 2015.16 Hodenkarzinom Gero Kramer Urologie 1 Hodenkarzinom Epidemiologie 1% aller bösartiger Neubildungen beim Mann 3-10 neue Fälle / 100 000 Männer / Jahr (Westen) Anstieg in
Interdisziplinärer Konsensus zur Diagnostik und Therapie von Hodentumoren
 Strahlentherapie und Onkologie Urban & Vogel 2000 Aktuelles Forum Interdisziplinärer Konsensus zur Diagnostik und Therapie von Hodentumoren Ergebnisse einer Update-Konferenz auf Grundlage evidenzbasierter
Strahlentherapie und Onkologie Urban & Vogel 2000 Aktuelles Forum Interdisziplinärer Konsensus zur Diagnostik und Therapie von Hodentumoren Ergebnisse einer Update-Konferenz auf Grundlage evidenzbasierter
Hodentumoren. F2.3 Diagnostik. F2.1 Epidemiologie. Skrotaler Ultraschall. F2.2 Risikofaktoren und Prävention. Serumtumormarker. Brust/Weibl.
 F2 Hodentumoren 1 Brust/Weibl. Genitale Diese Leitlinie basiert auf einem interdisziplinären Konsens unter Zuhilfenahme der publizierten S2-Leitlinien zum Hodentumor (DKG) und den Konsensusempfehlungen
F2 Hodentumoren 1 Brust/Weibl. Genitale Diese Leitlinie basiert auf einem interdisziplinären Konsens unter Zuhilfenahme der publizierten S2-Leitlinien zum Hodentumor (DKG) und den Konsensusempfehlungen
Nachsorge und adjuvante Chemotherapie des Dickdarmkarzinoms. Sankt Marien-Hospital Buer
 Nachsorge und adjuvante Chemotherapie des Dickdarmkarzinoms Grundlagen und Ziele Nachsorgemethoden Wertigkeit der Nachsorgetests Stadienadaptierte Nachsorgepläne Adjuvante Chemotherapie Leitliniengemässe
Nachsorge und adjuvante Chemotherapie des Dickdarmkarzinoms Grundlagen und Ziele Nachsorgemethoden Wertigkeit der Nachsorgetests Stadienadaptierte Nachsorgepläne Adjuvante Chemotherapie Leitliniengemässe
Fehleranalyse der Diagnostik und Therapie testikulärer Keimzelltumoren
 Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. R. Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und Marburg
Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. R. Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und Marburg
Uterine Leiomyosarkome
 Uterine Leiomyosarkome U. A. Ulrich Martin-Luther-Krankenhaus, Berlin AGO State-of-the-Art München, 6. 8. April 2017 LMS: Epidemiologie 1,3 % der uterinen Malignome, 50 % der uterinen Sarkome medianes
Uterine Leiomyosarkome U. A. Ulrich Martin-Luther-Krankenhaus, Berlin AGO State-of-the-Art München, 6. 8. April 2017 LMS: Epidemiologie 1,3 % der uterinen Malignome, 50 % der uterinen Sarkome medianes
56 Hodentumoren. J.T. Hartmann und S. Krege Epidemiologie Pathologie und Stadieneinteilung Pathologie
 56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
56 Hodentumoren. J.T. Hartmann und S. Krege Epidemiologie Pathologie und Stadieneinteilung Pathologie
 56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
Therapie von Keimzelltumoren ein Überblick. 32. Zwickauer Onkologie-Symposium Neue Entwicklungen in der Onkologie 21. März 2015
 Therapie von Keimzelltumoren ein Überblick 32. Zwickauer Onkologie-Symposium Neue Entwicklungen in der Onkologie 21. März 2015 Anja Lorch Fachärztin für Innere Medizin, Hämatologie und Onkologie Leitung
Therapie von Keimzelltumoren ein Überblick 32. Zwickauer Onkologie-Symposium Neue Entwicklungen in der Onkologie 21. März 2015 Anja Lorch Fachärztin für Innere Medizin, Hämatologie und Onkologie Leitung
Behandlungspfade Interdisziplinäres Onkologisches Zentrum Klinikum Ernst von Bergmann Potsdam. Hodgkin- Lymphom. Stand Dezember 2017
 Hodgkin- Lymphom Stand Dezember 2017 Erstdiagnose Notwendige Diagnostik Risikofaktoren Hodgkin- Lymphom Referenzhistologie obligat Klinische Untersuchung Anamnese (Alkoholschmerz) B- Symptome Fieber Nachtschweiß
Hodgkin- Lymphom Stand Dezember 2017 Erstdiagnose Notwendige Diagnostik Risikofaktoren Hodgkin- Lymphom Referenzhistologie obligat Klinische Untersuchung Anamnese (Alkoholschmerz) B- Symptome Fieber Nachtschweiß
Untersuchung zur Bedeutung der. Positronen-Emissions-Tomographie zur Stadieneinteilung. und Therapiekontrolle bei Keimzelltumoren
 Aus der Medizinischen Klinik und Poliklinik II Abteilung für Onkologie, Hämatologie, Knochenmarktransplantation des Universitätsklinikums Hamburg Eppendorf Direktor: Prof. Dr. med. D.K. Hossfeld Untersuchung
Aus der Medizinischen Klinik und Poliklinik II Abteilung für Onkologie, Hämatologie, Knochenmarktransplantation des Universitätsklinikums Hamburg Eppendorf Direktor: Prof. Dr. med. D.K. Hossfeld Untersuchung
Therapiekonzepte Onkologie
 Therapiekonzepte Onkologie Bearbeitet von Siegfried Seeber, Hans-Joachim Schütte erweitert, überarbeitet 2007. Buch. lv, 1851 S. Hardcover ISBN 978 3 540 28588 5 Format (B x L): 12,7 x 20,3 cm Weitere
Therapiekonzepte Onkologie Bearbeitet von Siegfried Seeber, Hans-Joachim Schütte erweitert, überarbeitet 2007. Buch. lv, 1851 S. Hardcover ISBN 978 3 540 28588 5 Format (B x L): 12,7 x 20,3 cm Weitere
Keimzelltumoren. N. Meidenbauer Medizinische Klinik 5 Universitätsklinikum Erlangen
 Keimzelltumoren N. Meidenbauer Medizinische Klinik 5 Universitätsklinikum Erlangen Folien nur zur privaten Verwendung Folien teilweise übernommen www.esmo.org Jörg Beyer Andrea Necchi (E-learning) Robert
Keimzelltumoren N. Meidenbauer Medizinische Klinik 5 Universitätsklinikum Erlangen Folien nur zur privaten Verwendung Folien teilweise übernommen www.esmo.org Jörg Beyer Andrea Necchi (E-learning) Robert
Kleinzelliges Lungenkarzinom (SCLC)
 Kleinzelliges Lungenkarzinom (SCLC) Verantwortlich: Prof. Dr. Nestle, Dr. Rawluk, Prof. Waller, Dr. Wiesemann Freigabe: interdisziplinärer Qualitätszirkel Stand: 04/2016, gültig bis 10/2017 Version 3.2
Kleinzelliges Lungenkarzinom (SCLC) Verantwortlich: Prof. Dr. Nestle, Dr. Rawluk, Prof. Waller, Dr. Wiesemann Freigabe: interdisziplinärer Qualitätszirkel Stand: 04/2016, gültig bis 10/2017 Version 3.2
MALIGNE KEIMZELLTUMOREN DES OVARS. W. Schröder
 MALIGNE KEIMZELLTUMOREN DES OVARS W. Schröder INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren < 20 Jahren 3-10% aller
MALIGNE KEIMZELLTUMOREN DES OVARS W. Schröder INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren < 20 Jahren 3-10% aller
Leitlinie Bronchialkarzinom 2011 IOZ Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009
 Nr 27724 Version 1-0-0 Datum 29.08.11 Seite 1 von 5 Leitlinie Bronchialkarzinom 2011 Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009 Tab.1: Beschreibung der TNM-Parameter
Nr 27724 Version 1-0-0 Datum 29.08.11 Seite 1 von 5 Leitlinie Bronchialkarzinom 2011 Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009 Tab.1: Beschreibung der TNM-Parameter
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen Abteilung Nuklearmedizin
 Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Nachsorge in der Uroonkologie nach kurativer Therapie. Zusammenfassung aktueller Literatur.
 Zusammenfassung aktueller Literatur Nachsorge in der Uroonkologie nach kurativer Therapie Helios Klinikum Pirna Klinik für Urologie und Kinderurologie Priv.-Doz. Dr. med. Volker Janitzky 1. Auflage 2018
Zusammenfassung aktueller Literatur Nachsorge in der Uroonkologie nach kurativer Therapie Helios Klinikum Pirna Klinik für Urologie und Kinderurologie Priv.-Doz. Dr. med. Volker Janitzky 1. Auflage 2018
PATIENTENINFORMATION. der. Deutschen Gesellschaft für Urologie (DGU) und des. Berufsverbandes Deutscher Urologen (BDU) über.
 PATIENTENINFORMATION der Deutschen Gesellschaft für Urologie (DGU) und des Berufsverbandes Deutscher Urologen (BDU) über den Hodenkrebs Der Hodentumor Was Sie wissen sollten Hodenkrebs ist zwar sehr selten
PATIENTENINFORMATION der Deutschen Gesellschaft für Urologie (DGU) und des Berufsverbandes Deutscher Urologen (BDU) über den Hodenkrebs Der Hodentumor Was Sie wissen sollten Hodenkrebs ist zwar sehr selten
Postoperative Bestrahlung nach Mastektomie und brusterhaltender Operation: Vergleich prognostischer Faktoren und Bedeutung des Lokalrezidivs.
 Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. Jürgen Dunst) Postoperative Bestrahlung nach Mastektomie und brusterhaltender
Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. Jürgen Dunst) Postoperative Bestrahlung nach Mastektomie und brusterhaltender
Behandlung von Patienten mit metastasierten Hodentumoren
 Serie Behandlung von Patienten mit metastasierten Hodentumoren Carsten Bokemeyer 1, Jörg Beyer 2, Axel Heidenreich 3 Zusammenfassung Hodentumoren gehören zu den häufigsten Krebserkrankungen junger Männer.
Serie Behandlung von Patienten mit metastasierten Hodentumoren Carsten Bokemeyer 1, Jörg Beyer 2, Axel Heidenreich 3 Zusammenfassung Hodentumoren gehören zu den häufigsten Krebserkrankungen junger Männer.
Behandlungsergebnisse von Patienten mit nicht-seminomatösen Hodentumoren aus dem Universitätsklinikum des Saarlandes zwischen 1975 und 2005
 Aus der Klinik und Poliklinik für Urologie und Kinderurologie Universitätsklinikum des Saarlandes, Homburg/Saar - Direktor: Prof. Dr. med. M. Stöckle Behandlungsergebnisse von Patienten mit nicht-seminomatösen
Aus der Klinik und Poliklinik für Urologie und Kinderurologie Universitätsklinikum des Saarlandes, Homburg/Saar - Direktor: Prof. Dr. med. M. Stöckle Behandlungsergebnisse von Patienten mit nicht-seminomatösen
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung. Universitäts- Klinikum Jena
 Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
Aus der Klinik für Urologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION
 Aus der Klinik für Urologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION Analyse der Versorgungsqualität von Patienten mit Keimzelltumoren an der Charité Gegenüberstellung
Aus der Klinik für Urologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION Analyse der Versorgungsqualität von Patienten mit Keimzelltumoren an der Charité Gegenüberstellung
Uterine Sarkome. S2k Leitlinie AWMF-Nummer 015/074
 S2k Leitlinie AWMF-Nummer 015/074 Version 1 Gültig 08/15 07/18 Federführende Autoren: Dominik Denschlag Falk C. Thiel Matthias W. Beckmann Mitglieder der Arbeitsgruppe: Sven Ackermann Lars Christian Horn
S2k Leitlinie AWMF-Nummer 015/074 Version 1 Gültig 08/15 07/18 Federführende Autoren: Dominik Denschlag Falk C. Thiel Matthias W. Beckmann Mitglieder der Arbeitsgruppe: Sven Ackermann Lars Christian Horn
Hodenkrebs (1) D07.6 Carcinoma in situ: Sonstige und nicht näher bezeichnete männliche Genitalorgane
 Hodenkrebs (1) Epidemiologie: Hodenkrebs gehört zu den eher seltenen Malignomen. Das Robert-Koch-Institut in Berlin gibt für 2004 die rohe Rate der Neuerkrankungen pro 100 000 Männern mit 11,8 pro Jahr
Hodenkrebs (1) Epidemiologie: Hodenkrebs gehört zu den eher seltenen Malignomen. Das Robert-Koch-Institut in Berlin gibt für 2004 die rohe Rate der Neuerkrankungen pro 100 000 Männern mit 11,8 pro Jahr
Hodentumoren Highlights and Dark Zones
 Hodentumoren Highlights and Dark Zones Prof. Dr. Jörg Beyer Leitender Arzt Klinik für Onkologie Telefon 044 255 21 54 Fax 044 255 12 40 Mail: joerg.beyer@usz.ch Hotline 079 855 80 96 Themen: Aktuelle Diskussionen
Hodentumoren Highlights and Dark Zones Prof. Dr. Jörg Beyer Leitender Arzt Klinik für Onkologie Telefon 044 255 21 54 Fax 044 255 12 40 Mail: joerg.beyer@usz.ch Hotline 079 855 80 96 Themen: Aktuelle Diskussionen
TUMORMARKER "Serumbank"
 TUMORMARKER Tumormarker haben in den letzten Jahren die Differentialdiagnostik und insbesondere die Verlaufskontrolle der genannten Tumore wesentlich verbessert. Darüber hinaus konnten die Nachweisverfahren
TUMORMARKER Tumormarker haben in den letzten Jahren die Differentialdiagnostik und insbesondere die Verlaufskontrolle der genannten Tumore wesentlich verbessert. Darüber hinaus konnten die Nachweisverfahren
Nur in bestimmten Fällen werden Rezidive zuverlässiger erkannt als mit herkömmlichen Verfahren
 Nutzen von PET und PET/CT bei Eierstockkrebs ist nicht belegt Nur in bestimmten Fällen werden Rezidive zuverlässiger erkannt als mit herkömmlichen Verfahren Köln (23. Mai 2012) - Mangels Studien gibt es
Nutzen von PET und PET/CT bei Eierstockkrebs ist nicht belegt Nur in bestimmten Fällen werden Rezidive zuverlässiger erkannt als mit herkömmlichen Verfahren Köln (23. Mai 2012) - Mangels Studien gibt es
Gastrointestinale Stromatumoren (GIST) Dr. Dietmar Reichert, Westerstede
 1 Gastrointestinale Stromatumoren (GIST) Dr. Dietmar Reichert, Westerstede 2 ESMO: Klinische Empfehlungen 2009 Diagnose, Behandlung und Nachsorge 3 Diagnose GIST = 2 cm (wenn mgl.) endoskopische Biopsie
1 Gastrointestinale Stromatumoren (GIST) Dr. Dietmar Reichert, Westerstede 2 ESMO: Klinische Empfehlungen 2009 Diagnose, Behandlung und Nachsorge 3 Diagnose GIST = 2 cm (wenn mgl.) endoskopische Biopsie
Lungentumoren Frank Zimmermann Klinik für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel radioonkologiebasel.
 Lungentumoren Frank Zimmermann Klinik für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel radioonkologiebasel.ch Heutige Lernziele C IM 240 lung carcinoma 2 C SU 94 C RN 4 types of
Lungentumoren Frank Zimmermann Klinik für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel radioonkologiebasel.ch Heutige Lernziele C IM 240 lung carcinoma 2 C SU 94 C RN 4 types of
Pathologie, Typisierung, Ausbreitungsstadien
 1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
Offenlegung potentieller Interessenkonflikte für diese Sitzung
 Offenlegung potentieller Interessenkonflikte für diese Sitzung 1. Anstellungsverhältnis oder Führungsposition keine 2. Beratungstätigkeit Keine 3. Aktienbesitz keiner 4. Honorare Keine 5. Finanzierung
Offenlegung potentieller Interessenkonflikte für diese Sitzung 1. Anstellungsverhältnis oder Führungsposition keine 2. Beratungstätigkeit Keine 3. Aktienbesitz keiner 4. Honorare Keine 5. Finanzierung
20. Onkologische Konferenz Eisenach. Das Mammakarzinom der älteren und alten Frau
 20. Onkologische Konferenz Eisenach Das Mammakarzinom der älteren und alten Frau Anja Merte Altern ist ein individueller Prozeß, bestimmt durch biologische, soziologische und psychologische Aspekte 3.
20. Onkologische Konferenz Eisenach Das Mammakarzinom der älteren und alten Frau Anja Merte Altern ist ein individueller Prozeß, bestimmt durch biologische, soziologische und psychologische Aspekte 3.
Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom
 Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom Verantwortlich: M. Bossart, K.Henne Freigabe: interdisziplinärer Qualitätszirkel Stand: 06/16, gültig bis 07/18 Version 3.1
Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom Verantwortlich: M. Bossart, K.Henne Freigabe: interdisziplinärer Qualitätszirkel Stand: 06/16, gültig bis 07/18 Version 3.1
Therapie des Hodentumors
 Therapie des Hodentumors In unserer Klinik werden alle Therapieformen des Hodentumors von der Hodenentfernung über die organerhaltende Therapie, die systemische Chemotherapie in der Primär- als auch in
Therapie des Hodentumors In unserer Klinik werden alle Therapieformen des Hodentumors von der Hodenentfernung über die organerhaltende Therapie, die systemische Chemotherapie in der Primär- als auch in
Karzinome in der Urologie
 VIII. Onkologisches Fachtagung Berlin, 11.-13. 13. Juni 2005 Karzinome in der Urologie PD Dr. med. J. Roigas Klinik und Poliklinik für Urologie Campus Mitte Charité Universitätsmedizin Berlin wichtige
VIII. Onkologisches Fachtagung Berlin, 11.-13. 13. Juni 2005 Karzinome in der Urologie PD Dr. med. J. Roigas Klinik und Poliklinik für Urologie Campus Mitte Charité Universitätsmedizin Berlin wichtige
Was tun, wenn der Tumor wieder ausbricht
 Was tun, wenn der Tumor wieder ausbricht Sindelfingen 22.10.2016 Dr. Ulrich Haag, Urologie, Kliniken Nagold S3-Leitlinie Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie
Was tun, wenn der Tumor wieder ausbricht Sindelfingen 22.10.2016 Dr. Ulrich Haag, Urologie, Kliniken Nagold S3-Leitlinie Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie
Leitliniengerechte Therapie bei metastasiertem kolorektalem Karzinom
 Leitliniengerechte Therapie bei metastasiertem kolorektalem Karzinom Case Report NZW Dresden 2010 Stefan Schalbaba stefan.schalbaba@klinikum-memmingen.de Patientenidentität und Subjektive Daten Patient
Leitliniengerechte Therapie bei metastasiertem kolorektalem Karzinom Case Report NZW Dresden 2010 Stefan Schalbaba stefan.schalbaba@klinikum-memmingen.de Patientenidentität und Subjektive Daten Patient
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
STUDIEN PRO UND CONTRA
 V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
V) WEITERE THEMEN STUDIEN PRO UND CONTRA Die Erfahrung hat gezeigt, dass Behandlungsergebnisse an mehr oder weniger kleinen Patientenzahlen von Autor zu Autor auch bei Einsatz gleicher Zytostatika zu unterschiedlichen,
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
D i s s e r t a t i o n
 Aus der Universitätsklinik und Poliklinik für Urologie an der Martin- Luther- Universität Halle- Wittenberg (Direktor: Univ.- Prof. Dr. med. habil. P. Fornara) Diagnostik und Therapie beim testikulären
Aus der Universitätsklinik und Poliklinik für Urologie an der Martin- Luther- Universität Halle- Wittenberg (Direktor: Univ.- Prof. Dr. med. habil. P. Fornara) Diagnostik und Therapie beim testikulären
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom
 Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Chirurgische Kombinationstherapien: Nachbestrahlung von Resektionshöhlen
 Interdisziplinäres DGNC/DEGRO Update Symposium: Aktuelle Behandlung zerebraler Metastasen Chirurgische Kombinationstherapien: Nachbestrahlung von Resektionshöhlen 20. Oktober 2017, Frankfurt am Main Klinik
Interdisziplinäres DGNC/DEGRO Update Symposium: Aktuelle Behandlung zerebraler Metastasen Chirurgische Kombinationstherapien: Nachbestrahlung von Resektionshöhlen 20. Oktober 2017, Frankfurt am Main Klinik
Nicht-kleinzelliges Bronchialkarzinom
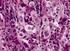 Rolle der Chemotherapie in der Behandlung des nicht-kleinzelligen Bronchialkarzinoms Was ist gesichert, was ist experimentell? Die Prognose der Gesamtheit der Patienten im Stadium III ist über die letzten
Rolle der Chemotherapie in der Behandlung des nicht-kleinzelligen Bronchialkarzinoms Was ist gesichert, was ist experimentell? Die Prognose der Gesamtheit der Patienten im Stadium III ist über die letzten
Was ist Strahlentherapie?
 Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Diagnostik und Therapie primärer und metastasierter Mammakarzinome
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Keimzelltumore. Keimzell- tumore. und. Nierenzell- karzinome. 18. Potsdamer Onkologisches Gespräch
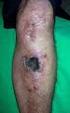 18. Potsdamer Onkologisches Gespräch Keimzell- tumore und Nierenzell- karzinome A. Dukat Klinik für Hämatologie, Onkologie u. Palliativmedizin Prof. Dr. G. Maschmeyer Keimzelltumore Keimzelltumore Epidemiologie
18. Potsdamer Onkologisches Gespräch Keimzell- tumore und Nierenzell- karzinome A. Dukat Klinik für Hämatologie, Onkologie u. Palliativmedizin Prof. Dr. G. Maschmeyer Keimzelltumore Keimzelltumore Epidemiologie
NACHSORGEPASS KLINIK FÜR THORAXCHIRURGIE. Patientenetikett
 NACHSORGEPASS KLINIK FÜR THORAXCHIRURGIE Patientenetikett Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen wurde eine Tumorerkrankung der Lunge in einem begrenzten Stadium festgestellt, so dass
NACHSORGEPASS KLINIK FÜR THORAXCHIRURGIE Patientenetikett Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen wurde eine Tumorerkrankung der Lunge in einem begrenzten Stadium festgestellt, so dass
Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation?
 Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation? H.-S. Hofmann Thoraxchirurgisches Zentrum Universitätsklinikum Regensburg Krankenhaus Barmherzige Brüder Regensburg Problem:
Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation? H.-S. Hofmann Thoraxchirurgisches Zentrum Universitätsklinikum Regensburg Krankenhaus Barmherzige Brüder Regensburg Problem:
1. Neoadjuvante Therapie. 2. Adjuvante Therapie. 3. Metastasiertes Mamma-Ca. 4. Mamma-Ca. in der Schwangerschaft. 5. Nicht-interventionelle Studien
 1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Adapt-Studie Katherine-Studie TREAT CTC-Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Adapt-Studie Katherine-Studie TREAT CTC-Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
O f f e n e S t u d i e n - August 2013 -
 Sehr geehrte Patientinnen und Angehörige, sehr geehrte Ärztinnen und Ärzte, Klinische Studien zur Behandlung des Ovarial-, Tuben-, Endometrium- und Peritonealkarzinoms: bevor antihormonelle, chemotherapeutische
Sehr geehrte Patientinnen und Angehörige, sehr geehrte Ärztinnen und Ärzte, Klinische Studien zur Behandlung des Ovarial-, Tuben-, Endometrium- und Peritonealkarzinoms: bevor antihormonelle, chemotherapeutische
Operative und systemische Therapie des Zervixkarzinoms
 Operative und systemische Therapie des Zervixkarzinoms J. Huober Workshop DESO St.Gallen 20./21. Februar 2015 Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen
Operative und systemische Therapie des Zervixkarzinoms J. Huober Workshop DESO St.Gallen 20./21. Februar 2015 Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen
IQWiG: Vorbericht zu PET und PET/CT bei Eierstockkrebs veröffentlicht
 IQWiG: Vorbericht zu PET und PET/CT bei Eierstockkrebs veröffentlicht Nutzen der Positronen-Emissions-Tomographie (PET) lässt sich mangels Studien derzeit nicht beurteilen Berlin (18. Juli 2011) - Der
IQWiG: Vorbericht zu PET und PET/CT bei Eierstockkrebs veröffentlicht Nutzen der Positronen-Emissions-Tomographie (PET) lässt sich mangels Studien derzeit nicht beurteilen Berlin (18. Juli 2011) - Der
Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Die stereotaktische Bestrahlung von Lungentumoren
 Hypofraktionierung Innovation oder Risiko? Die stereotaktische Bestrahlung von Lungentumoren Frank Zimmermann Institut für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch;
Hypofraktionierung Innovation oder Risiko? Die stereotaktische Bestrahlung von Lungentumoren Frank Zimmermann Institut für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch;
2 Jahren. Nachfolgende Chemo- und Strahlentherapie. Vor 10 Monaten Lokalrezidiv im Narbenbereich mit operativer
 378 Kapitel 7 Gynäkologie 7 7.5 Fallbeispiele 7.5.1 Patient 1 Mammakarzinom mit Lebermetastase Anamnese 45-jährige Patientin mit Zustand nach Mammakarzinom rechts mit brusterhaltender Therapie, Sentinellymphknotenentfernung
378 Kapitel 7 Gynäkologie 7 7.5 Fallbeispiele 7.5.1 Patient 1 Mammakarzinom mit Lebermetastase Anamnese 45-jährige Patientin mit Zustand nach Mammakarzinom rechts mit brusterhaltender Therapie, Sentinellymphknotenentfernung
Behandlungsassoziierte Spätfolgen nach Strahlentherapie maligner Erkrankungen im Kindesalter- und Jugendalter. Studienprotokoll
 Behandlungsassoziierte Spätfolgen nach Strahlentherapie maligner Erkrankungen im Kindesalter- und Jugendalter Studienprotokoll Studienleitung: Studienassistenz: Prof. Dr. N. Willich Prof. Dr. A. Schuck
Behandlungsassoziierte Spätfolgen nach Strahlentherapie maligner Erkrankungen im Kindesalter- und Jugendalter Studienprotokoll Studienleitung: Studienassistenz: Prof. Dr. N. Willich Prof. Dr. A. Schuck
Adjuvante und neoadjuvante Therapie beim KRK. PD Dr. med. Christian Pox Bremen
 10. addz - Jahrestagung Adjuvante und neoadjuvante Therapie beim KRK PD Dr. med. Christian Pox Bremen S3 Leitlinie Kolorektales Karzinom 2017 Update 2017 Themenkomplex I Themenkomplex II Themenkomplex
10. addz - Jahrestagung Adjuvante und neoadjuvante Therapie beim KRK PD Dr. med. Christian Pox Bremen S3 Leitlinie Kolorektales Karzinom 2017 Update 2017 Themenkomplex I Themenkomplex II Themenkomplex
Fakten zu Prostatakrebs
 Fakten zu Prostatakrebs Jetzt informieren: www.deine-manndeckung.de Prostatakrebs ist eine Krebsart, die mehr Menschen betrifft, als man denkt: Mit 57.400 Neuerkrankungen pro Jahr ist Prostatakrebs die
Fakten zu Prostatakrebs Jetzt informieren: www.deine-manndeckung.de Prostatakrebs ist eine Krebsart, die mehr Menschen betrifft, als man denkt: Mit 57.400 Neuerkrankungen pro Jahr ist Prostatakrebs die
Tumorerkrankungen im Kindesalter. - ein Überblick -
 Tumorerkrankungen im Kindesalter - ein Überblick - Elisabeth Holfeld 2. Brandenburger Krebskongress 25.02.2011 Hauptunterschiede zwischen Tumoren im Kindes- und Erwachsenenalter Häufigkeit der Tumoren
Tumorerkrankungen im Kindesalter - ein Überblick - Elisabeth Holfeld 2. Brandenburger Krebskongress 25.02.2011 Hauptunterschiede zwischen Tumoren im Kindes- und Erwachsenenalter Häufigkeit der Tumoren
Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Extragonadale Keimzelltumoren. Jörg Beyer, Bern
 Extragonadale Keimzelltumoren Jörg Beyer, Bern Lernziele Erkennen, Behandeln, Heilen Take home message Hodentumor ist die häufigste Krebserkrankung bei Männern zwischen 18 und 40 Jahren cave: ca. 3% der
Extragonadale Keimzelltumoren Jörg Beyer, Bern Lernziele Erkennen, Behandeln, Heilen Take home message Hodentumor ist die häufigste Krebserkrankung bei Männern zwischen 18 und 40 Jahren cave: ca. 3% der
Medizin im Vortrag. Herausgeber: Prof. Dr. med. Christoph Frank Dietrich. Kolorektales Karzinom
 Medizin im Vortrag Herausgeber: Prof. Dr. med. Christoph Frank Dietrich Kolorektales Karzinom Autoren: Dr. med. Stefan Krüger Dr. med. Edgar Hartung Kerstin Siehr Prof. Dr. med. Christoph Frank Dietrich
Medizin im Vortrag Herausgeber: Prof. Dr. med. Christoph Frank Dietrich Kolorektales Karzinom Autoren: Dr. med. Stefan Krüger Dr. med. Edgar Hartung Kerstin Siehr Prof. Dr. med. Christoph Frank Dietrich
Therapie: wenn ja, wann?
 Klinikum Stuttgart Medizin fürs Leben Neues zum Thema Prostatakrebs Universitätsklinikum Tübingen, 13. Juli 2008 Therapie: wenn ja, wann? Ulrich Humke, Urologische Klinik, Katharinenhospital Prof. Dr.
Klinikum Stuttgart Medizin fürs Leben Neues zum Thema Prostatakrebs Universitätsklinikum Tübingen, 13. Juli 2008 Therapie: wenn ja, wann? Ulrich Humke, Urologische Klinik, Katharinenhospital Prof. Dr.
Statistische Untersuchungen zur onkologischen Qualitätskontrolle anhand von Daten des Brandenburgischen Tumorzentrums
 Aus dem Institut für Pathologie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. S. Hauptmann) Statistische Untersuchungen zur onkologischen Qualitätskontrolle anhand von Daten
Aus dem Institut für Pathologie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. S. Hauptmann) Statistische Untersuchungen zur onkologischen Qualitätskontrolle anhand von Daten
6. Diskussion 6.1. Diskussion der Daten
 6. Diskussion 6.1. Diskussion der Daten Die 1995 im BJ publizierte Metaanalyse zeigte, dass für Patienten im Stadium III b und IV des Bronchialkarzinoms eine Chemotherapie einen Überlebensvorteil ergibt.
6. Diskussion 6.1. Diskussion der Daten Die 1995 im BJ publizierte Metaanalyse zeigte, dass für Patienten im Stadium III b und IV des Bronchialkarzinoms eine Chemotherapie einen Überlebensvorteil ergibt.
Hodgkin-Lymphom. Dr. med. Christoph Engel. Institut für Medizinische Informatik, Statistik und Epidemiologie (IMISE) Universität Leipzig
 Hodgkin-Lymphom Dr. med. Christoph Engel Institut für Medizinische Informatik, Statistik und Epidemiologie (IMISE) Universität Leipzig Hodgkin-Lymphom: Definition und klinische Symptomatik Definition:
Hodgkin-Lymphom Dr. med. Christoph Engel Institut für Medizinische Informatik, Statistik und Epidemiologie (IMISE) Universität Leipzig Hodgkin-Lymphom: Definition und klinische Symptomatik Definition:
Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie
 Neue Studie zu Iscador Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie Schwäbisch-Gmünd (2. Dezember 2009) - Eine prospektive randomisierte offene Pilotstudie ergab eine Verbesserung
Neue Studie zu Iscador Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie Schwäbisch-Gmünd (2. Dezember 2009) - Eine prospektive randomisierte offene Pilotstudie ergab eine Verbesserung
State of the Art Therapie bei Rezidiv und Metastasen. Peter Mallmann. Köln
 State of the Art 2017 Zervixkarzinom Therapie bei Rezidiv und Metastasen Peter Mallmann Köln Lokalrezidiv Die Lokalrezidivrate ist abhängig vom primären Tumorstadium Stadium Ib 10% Stadium IIa 17% Stadium
State of the Art 2017 Zervixkarzinom Therapie bei Rezidiv und Metastasen Peter Mallmann Köln Lokalrezidiv Die Lokalrezidivrate ist abhängig vom primären Tumorstadium Stadium Ib 10% Stadium IIa 17% Stadium
State of the art Gynäkologische Onkologie 2013 Berlin, 22. Juni 2013
 State of the art Gynäkologische Onkologie 2013 Berlin, 22. Juni 2013 INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren
State of the art Gynäkologische Onkologie 2013 Berlin, 22. Juni 2013 INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren
LYMPHOME. H. Jürgens. Vorlesung WS 2001/2002.
 LYMPHOME H. Jürgens Vorlesung WS 2001/2002 http://medweb.uni-muenster.de/institute/paedonco/lehre/index.html Differentialdiagnose (DD) - Lymphadenitis / Lymphom Lymphadenitis Lymphom Häufigkeit +++ (+)
LYMPHOME H. Jürgens Vorlesung WS 2001/2002 http://medweb.uni-muenster.de/institute/paedonco/lehre/index.html Differentialdiagnose (DD) - Lymphadenitis / Lymphom Lymphadenitis Lymphom Häufigkeit +++ (+)
Diagnostisches Vorgehen bei Leberraumforderungen. H. Diepolder
 Diagnostisches Vorgehen bei Leberraumforderungen H. Diepolder Bei 20% aller Routinesonographien fällt eine Leberraumforderung auf Problem Problem Bei 20% aller Routinesonographien fällt eine Leberraumforderung
Diagnostisches Vorgehen bei Leberraumforderungen H. Diepolder Bei 20% aller Routinesonographien fällt eine Leberraumforderung auf Problem Problem Bei 20% aller Routinesonographien fällt eine Leberraumforderung
Radiochemotherapie des nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT
 Radiochemotherapie des Nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT W. Huhnt Ruppiner Kliniken GmbH, Klinik für Strahlentherapie und Radioonkologie, Neuruppin GLIEDERUNG Einleitung: Überblick
Radiochemotherapie des Nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT W. Huhnt Ruppiner Kliniken GmbH, Klinik für Strahlentherapie und Radioonkologie, Neuruppin GLIEDERUNG Einleitung: Überblick
Lokal ablative Therapieverfahren bei oligometastasiertem Pankreaskarzinom:
 DEGRO AG_Frankfurt_2017 Lokal ablative Therapieverfahren bei oligometastasiertem Pankreaskarzinom: Non sense oder Konsens? Dr. med. S. Gerum Klinik und Poliklinik für Strahlentherapie und Radioonkologie
DEGRO AG_Frankfurt_2017 Lokal ablative Therapieverfahren bei oligometastasiertem Pankreaskarzinom: Non sense oder Konsens? Dr. med. S. Gerum Klinik und Poliklinik für Strahlentherapie und Radioonkologie
Radiotherapie im Frühstadium bei Morbus Dupuytren Langzeitergebnisse
 Radiotherapie im Frühstadium bei Morbus Dupuytren Langzeitergebnisse C. Schubert, M. Wielpütz, F. Guntrum, M.H. Seegenschmiedt Klinik für Radioonkologie & Strahlentherapie, Essen 13. Jahreskongress der
Radiotherapie im Frühstadium bei Morbus Dupuytren Langzeitergebnisse C. Schubert, M. Wielpütz, F. Guntrum, M.H. Seegenschmiedt Klinik für Radioonkologie & Strahlentherapie, Essen 13. Jahreskongress der
Benchmarking Brustzentren WBC
 Benchmarking Brustzentren WBC sauswertung 2010 Ergebnisbericht Städtische Kliniken Frankfurt-Höchst Klinik ID: 137 Anonymcode: 2969 Erstellungsdatum: 09.05.2011 Auswertezeitraum: 01.01.2010-31.12.2010
Benchmarking Brustzentren WBC sauswertung 2010 Ergebnisbericht Städtische Kliniken Frankfurt-Höchst Klinik ID: 137 Anonymcode: 2969 Erstellungsdatum: 09.05.2011 Auswertezeitraum: 01.01.2010-31.12.2010
Untersuchung der MDR1-Expression und ihrer klinischen Relevanz beim Keimzelltumor des Hodens
 Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. Rainer Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und
Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. Rainer Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und
Frauen mit Brustkrebs könnten von einer autologen Stammzelltransplantation profitieren
 Frauen mit Brustkrebs könnten von einer autologen Stammzelltransplantation profitieren IQWiG findet Belege für längeres ereignisfreies Überleben aber auch Hinweise auf schwerwiegende Komplikationen Berlin
Frauen mit Brustkrebs könnten von einer autologen Stammzelltransplantation profitieren IQWiG findet Belege für längeres ereignisfreies Überleben aber auch Hinweise auf schwerwiegende Komplikationen Berlin
Tumore der männlichen Genitalorgane
 Tumore der männlichen Genitalorgane Autoren: C. Bokemeyer, D. Hossfeld 1. Hodentumore Das hier empfohlene Vorgehen wurde interdisziplinär abgesprochen (AIO/AUO/ARO) (1). 1.1 Epidemiologie Inzidenz 8 9/100000
Tumore der männlichen Genitalorgane Autoren: C. Bokemeyer, D. Hossfeld 1. Hodentumore Das hier empfohlene Vorgehen wurde interdisziplinär abgesprochen (AIO/AUO/ARO) (1). 1.1 Epidemiologie Inzidenz 8 9/100000
Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION
 Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION Thema: Entscheidungskriterien vor radikaler Prostatektomie Eine retrospektive Untersuchung der Daten von 427 Patienten
Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION Thema: Entscheidungskriterien vor radikaler Prostatektomie Eine retrospektive Untersuchung der Daten von 427 Patienten
Ab durch die Mitte: Radiotherapie beim Pankreaskarzinom
 Ab durch die Mitte: Radiotherapie beim Pankreaskarzinom Alexandros Papachristofilou Pankreaskarzinom: Eine Herausforderung 0 1 Pankreaskarzinom: Eine Herausforderung 7.8/8.7 = 90% 10.1/10.7 = 94% 0 23.9/110.5
Ab durch die Mitte: Radiotherapie beim Pankreaskarzinom Alexandros Papachristofilou Pankreaskarzinom: Eine Herausforderung 0 1 Pankreaskarzinom: Eine Herausforderung 7.8/8.7 = 90% 10.1/10.7 = 94% 0 23.9/110.5
Bronchus - Karzinom. Bronchus - Karzinom. 2. Screening. Bronchus Karzinom - Allgemein. 1. Einleitung allgemeine Informationen. 3.
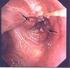 Bronchus - Karzinom J. Barandun LungenZentrum Hirslanden Zürich Screening Abklärung - Therapie Bronchus - Karzinom 1. Einleitung allgemeine Informationen 2. Screening 3. Abklärung 4. Therapie Bronchus
Bronchus - Karzinom J. Barandun LungenZentrum Hirslanden Zürich Screening Abklärung - Therapie Bronchus - Karzinom 1. Einleitung allgemeine Informationen 2. Screening 3. Abklärung 4. Therapie Bronchus
Universität zu Lübeck Institut für Krebsepidemiologie e.v.
 Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
