Bedeutung der Clinical Trial Regulation für die humanpharmakologische Forschung in Deutschland
|
|
|
- Sophie Richter
- vor 7 Jahren
- Abrufe
Transkript
1 Bedeutung der Clinical Trial Regulation für die humanpharmakologische Forschung in Deutschland Dr. rer. nat. Barbara Schug SocraTec R&D GmbH, Oberursel, Germany AGAH Workshop Bonn, 05. Dezember 2014
2 Wiege der Humanpharmakologie 1824 Philipp Friedrich Wilhelm Vogt (Gießen) Lehrbuch der Pharmakodynamik 1867 Rudolf Buchheim (Gießen / Dorpat) Begründer der experimentellen Pharmakologie 1873 Naunyn-Schmiedebergers (Leipzig) Zeitschrift für experimentelle Pathologie und Pharmakologie
3 Forschungsstandort Deutschland Vorteile für humanpharmakologische Forschung lange Tradition mit umfassendem methodischen Knowhow hohes berufsspezifisches Qualifikationsniveau des technischen Personals Study Nurses MTAs, PTAs, BTAs, CTAs Diätassistenten Laboranten hervorragende Infrastruktur im Vergleich zu anderen Ländern gute Patientenverfügbarkeit gute Probandenverfügbarkeit Der aufgeklärte Proband zur bewußten Teilnahme an Studien ohne therapeutischen Nutzen ist möglich!
4 Zauberwort Efficiency Regulation No. 536/2014 hat zum Ziel, die Bearbeitungszeiten und den Zulassungsaufwand insbesondere für multinationale Phase III Studien zu verringern: äußerst begrüßenswerter Ansatz Dr. Hartmut Krafft (PEI) BVMA-Symposium 2014 in München: circa 75 % aller in Europa durchgeführten Studien sind mononational (28.822/38.472) Das BfArM ist verlässlich, schnell, wissenschaftlich fundiert und Sachargumenten gegenüber kritisch-kompetent aufgeschlossen: sehr gute Bearbeitungszeiten bei der Zulassung klinischer Studien in Deutschland
5 Zauberwort Efficiency Bearbeitungszeiten bei der Genehmigung von Phase-I- Studien in Deutschland days Durchschnittliche Genehmigungsfristen nach Erhalt eines vollständigen Antrages bei m BfArM in den letzten Monaten (Quelle: BfArM) 0 Last months
6 Zauberwort Transparency Wem nutzt Transparenz? dem qualifiziert entscheidenden Arzt dem mündigen Patienten der kontrollierenden / zulassenden Behörde aber auch der Konkurrenz weltweit! Welche Transparenz für die eigentlichen Zielgruppen? efficacy safety (z. B. AE-Pattern, Interactions, Contraindication) laufende klinische Therapiestudien Wem schadet Transparenz? dem pharmazeutischen Unternehmer? dem CRO? Nein nicht wirklich! Aber: Transparenz zum falschen Zeitpunkt kann sehr schaden!
7 Das Wann ist die Gretchenfrage! Umfassender Informationszugang für Patienten und Fachkreise bei der Medikamentenauswahl: nach der Zulassung Gerade bei vital bedrohlichen oder irreversibel schädigenden Erkrankungen die Information für Patienten und Fachkreise, wo welche Studien stattfinden: bei Beginn der Phase III, in bestimmten Indikationen und bei bestimmten Designansätzen auch schon in der Phase II Welchen Nutzen für Patienten und Fachkreise hat die Transparenz in Phase I Studien ohne therapeutischen Nutzen? fördern wir damit nicht sogar eher zu frühe Hoffnung und Wundermittelglauben? Eher keinen!
8 Wovon sprechen wir? Total: 1418 Phase I Studien aus 4585, d.h. 30 % aller Studien (15 % bei PEI)
9 Regulation No. 536/ 2014: Early Phase Und was bedeutet die Clinical Trial Regulation für die humanpharmakologische Forschung in Deutschland? vermutlich zunächst komplizierte Prozesse (aber erfahrungsgemäß spielt sich so etwas ein) kurzfristiger Rückgang an Studien deutlich verlängerte Genehmigungszeiten zeitlich kritische Studien werden verlagert extrem frühe und sehr umfassende Offenlegung hochvertraulicher Firmendaten (sogar Investigator s Brochure?) alle Studien mit irgendwie vertraulich zu handhabenden Informationen werden verlagert Was bliebe dann noch übrig???
10 Was wäre sinnvoll für Early Phase? Zauberwort Efficiency : keine Verlängerung der Genehmigungszeiten Zauberwort Transparency : keine umfassende Informationstransparenz zum Zeitpunkt der Planung und Durchführung von klinischer Prüfungen der frühen Phasen ohne therapeutischen Nutzen oder positiv ausgedrückt: umfassende Transparenz dann, wenn für Fachkreise und Patienten relevant Auch Behörden und Gesetzgeber müssen sich der Frage nach dem Zusatznutzen ihrer Regularien stellen!
Informationsfluss in klinischen Studien Interaktion(en) zwischen den Verantwortlichen
 Arbeitsgemeinschaft für angewandte Humanpharmakologie e.v. Informationsfluss in klinischen Studien Interaktion(en) zwischen den Verantwortlichen Katharina Erb Zohar unter Mitwirkung von Thomas Fischer
Arbeitsgemeinschaft für angewandte Humanpharmakologie e.v. Informationsfluss in klinischen Studien Interaktion(en) zwischen den Verantwortlichen Katharina Erb Zohar unter Mitwirkung von Thomas Fischer
Neuerungen im Genehmigungsverfahren klinischer Prüfungen - EU Clinical Trials Regulation
 Study Nurse Forum Was gibt es Neues für die klinische Prüfung? Berlin, 17. Februar 2017 Neuerungen im Genehmigungsverfahren klinischer Prüfungen - EU Clinical Trials Regulation Dr. K. Breithaupt-Grögler
Study Nurse Forum Was gibt es Neues für die klinische Prüfung? Berlin, 17. Februar 2017 Neuerungen im Genehmigungsverfahren klinischer Prüfungen - EU Clinical Trials Regulation Dr. K. Breithaupt-Grögler
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v.
 Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Auswirkungen der 12. AMG-Novelle auf die klinische Forschung in Deutschland, Bilanz nach einem Jahr:
 Auswirkungen der 12. AMG-Novelle auf die klinische Forschung in Deutschland, Bilanz nach einem Jahr: Bilanz der Neuregelungen aus Sicht der forschenden Arzneimittelhersteller Dr. Dieter Götte 1 Erwartungen
Auswirkungen der 12. AMG-Novelle auf die klinische Forschung in Deutschland, Bilanz nach einem Jahr: Bilanz der Neuregelungen aus Sicht der forschenden Arzneimittelhersteller Dr. Dieter Götte 1 Erwartungen
Arzneimittelstudien. Eine Einführung in klinische Prüfungen für Ärzte, Studenten, medizinisches Assistenzpersonal und interessierte Laien
 Arzneimittelstudien Eine Einführung in klinische Prüfungen für Ärzte, Studenten, medizinisches Assistenzpersonal und interessierte Laien von Dr. Manfred Stapff, Isabella Stapff überarbeitet Arzneimittelstudien
Arzneimittelstudien Eine Einführung in klinische Prüfungen für Ärzte, Studenten, medizinisches Assistenzpersonal und interessierte Laien von Dr. Manfred Stapff, Isabella Stapff überarbeitet Arzneimittelstudien
Können Sie mir sagen, ob...? Arzneimittelinformation beim Krebsinformationsdienst, Deutsches Krebsforschungszentrum
 Anke Ernst 12.01.2013 Können Sie mir sagen, ob...? Arzneimittelinformation beim Krebsinformationsdienst, Deutsches Krebsforschungszentrum Dr. rer. nat. Anke Ernst Krebsinformationsdienst KID Deutsches
Anke Ernst 12.01.2013 Können Sie mir sagen, ob...? Arzneimittelinformation beim Krebsinformationsdienst, Deutsches Krebsforschungszentrum Dr. rer. nat. Anke Ernst Krebsinformationsdienst KID Deutsches
Praktische Erfahrungen eines Prüfers bei der Durchführung klinischer Studien Herausforderung und Chancen
 Praktische Erfahrungen eines Prüfers bei der Durchführung klinischer Studien Herausforderung und Chancen Prof. Dr. J. Bogner Klinikum der Universität München, Campus Innenstadt Pettenkoferstr. 8a 80336
Praktische Erfahrungen eines Prüfers bei der Durchführung klinischer Studien Herausforderung und Chancen Prof. Dr. J. Bogner Klinikum der Universität München, Campus Innenstadt Pettenkoferstr. 8a 80336
Berufliche Entwicklungschancen zertifizierter Study Nurses
 Berufliche Entwicklungschancen zertifizierter Study Nurses Ergebnisse einer nicht-repräsentativen Umfrage Burkhard Kerlin, AGAH Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v Study Nurse
Berufliche Entwicklungschancen zertifizierter Study Nurses Ergebnisse einer nicht-repräsentativen Umfrage Burkhard Kerlin, AGAH Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v Study Nurse
WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN
 CAMPUS INNENSTADT CAMPUS GROSSHADERN DIREKTOR: PROF. DR. MED. SVEN MAHNER WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN Informationsnachmittag - Leben mit Brustkrebs Was gibt es Neues? Was kann ich tun?
CAMPUS INNENSTADT CAMPUS GROSSHADERN DIREKTOR: PROF. DR. MED. SVEN MAHNER WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN Informationsnachmittag - Leben mit Brustkrebs Was gibt es Neues? Was kann ich tun?
Dr. Johannes Knollmeyer Direktor Gesundheitspolitik Sanofi-Aventis Deutschland GmbH
 Versorgungsforschungskongress 2015 Versorgungforschung und klinische Forschung: Synergien und Alleinstellungsmerkmale Perspektive der pharmazeutischen Industrie Dr. Johannes Knollmeyer Direktor Gesundheitspolitik
Versorgungsforschungskongress 2015 Versorgungforschung und klinische Forschung: Synergien und Alleinstellungsmerkmale Perspektive der pharmazeutischen Industrie Dr. Johannes Knollmeyer Direktor Gesundheitspolitik
Zweites Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften 16. AMG-Novelle. - PASS und PAES - Änderungen zur klinischen Prüfung
 Zweites Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften 16. AMG-Novelle - PASS und PAES - Änderungen zur klinischen Prüfung Rechtsanwalt Professor Burkhard Sträter Sträter Rechtsanwälte
Zweites Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften 16. AMG-Novelle - PASS und PAES - Änderungen zur klinischen Prüfung Rechtsanwalt Professor Burkhard Sträter Sträter Rechtsanwälte
Transparenz in der Zusammenarbeit mit Ärzten
 Transparenz in der Zusammenarbeit mit Ärzten Offenlegung von Zahlungen an Ärzte und andere Heilberufe Die Pharmaindustrie und Angehörige medizinischer Fachkreise arbeiten in vielen Bereichen zusammen:
Transparenz in der Zusammenarbeit mit Ärzten Offenlegung von Zahlungen an Ärzte und andere Heilberufe Die Pharmaindustrie und Angehörige medizinischer Fachkreise arbeiten in vielen Bereichen zusammen:
Statusseminar Klinische Studien. Herausforderungen und Probleme in der Studienvorbereitung Workshop 1
 Herausforderungen und Probleme in der Studienvorbereitung Workshop 1 Bericht der Arbeitsgruppe I Gründe für das Fortführen des Programms Herausforderungen bei Antragstellung und Begutachtung Herausforderungen
Herausforderungen und Probleme in der Studienvorbereitung Workshop 1 Bericht der Arbeitsgruppe I Gründe für das Fortführen des Programms Herausforderungen bei Antragstellung und Begutachtung Herausforderungen
Klinische Studien an der Charité. B. Wiedenmann Campus Virchow-Klinikum Charité Universitätsmedizin Berlin
 Klinische Studien an der Charité B. Wiedenmann Campus Virchow-Klinikum Charité Universitätsmedizin Berlin Ziele 1 Verbesserung der Qualität klinischer Studien Zulassungsstudien (company driven) Optimale
Klinische Studien an der Charité B. Wiedenmann Campus Virchow-Klinikum Charité Universitätsmedizin Berlin Ziele 1 Verbesserung der Qualität klinischer Studien Zulassungsstudien (company driven) Optimale
Zulassungsüberschreitende Anwendung von Arzneimitteln im Rahmen klinischer Studien ( 35c SGB V)
 Zulassungsüberschreitende Anwendung von Arzneimitteln im Rahmen klinischer Studien ( 35c SGB V) Berlin, 22. September 2009 Dr. Regina Skavron Abteilung Arzneimittel, Gemeinsamer Bundesausschuss Zulassungsüberschreitende
Zulassungsüberschreitende Anwendung von Arzneimitteln im Rahmen klinischer Studien ( 35c SGB V) Berlin, 22. September 2009 Dr. Regina Skavron Abteilung Arzneimittel, Gemeinsamer Bundesausschuss Zulassungsüberschreitende
Klinische Prüfung von Arzneimitteln: Öffentliche Informationen in PharmNet.Bund Clinical Trials (CT)
 Klinische Prüfung von Arzneimitteln: Öffentliche Informationen in PharmNet.Bund Clinical Trials (CT) Nutzertreffen, Köln 8. November 2011 Dr. Barbara Höfgen, Dr. Irina Bosman PharmNet.Bund-CT Gesetzliche
Klinische Prüfung von Arzneimitteln: Öffentliche Informationen in PharmNet.Bund Clinical Trials (CT) Nutzertreffen, Köln 8. November 2011 Dr. Barbara Höfgen, Dr. Irina Bosman PharmNet.Bund-CT Gesetzliche
Symposium Kommerzielle Klinische Forschung" Oktober 2007
 Symposium Kommerzielle Klinische Forschung" 08. 09. Oktober 2007 Klinische Studien: Suche nach der besten Therapie für den Patienten Dr. Bernd Eberwein BAH / Bonn 1 Zukunftsforschung ist Kratzen, bevor
Symposium Kommerzielle Klinische Forschung" 08. 09. Oktober 2007 Klinische Studien: Suche nach der besten Therapie für den Patienten Dr. Bernd Eberwein BAH / Bonn 1 Zukunftsforschung ist Kratzen, bevor
Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer
 Prüferbewertung und Eignung von Prüfstellen Worauf achtet die Ethikkommission? Prof. Dr. Joerg Hasford Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer Die nachfolgenden Ausführungen
Prüferbewertung und Eignung von Prüfstellen Worauf achtet die Ethikkommission? Prof. Dr. Joerg Hasford Vorsitzender der Ethikkommission der Bayerischen Landesärztekammer Die nachfolgenden Ausführungen
Pharmakologie und Toxikologie: Für Studium und Praxis. Mit einem Geleitwort von Eckart von Hirschhausen
 Pharmakologie und Toxikologie: Für Studium und Praxis. Mit einem Geleitwort von Eckart von Hirschhausen Click here if your download doesn"t start automatically Pharmakologie und Toxikologie: Für Studium
Pharmakologie und Toxikologie: Für Studium und Praxis. Mit einem Geleitwort von Eckart von Hirschhausen Click here if your download doesn"t start automatically Pharmakologie und Toxikologie: Für Studium
Orphan Drugs. Arzneimitteltherapie seltener Krankheiten
 Orphan Drugs Arzneimitteltherapie seltener Krankheiten Seltene Krankheiten 30 Millionen Europäer, davon etwa 4 Millionen Deutsche, leiden an seltenen Krankheiten. Als selten gilt hier eine Krankheit, wenn
Orphan Drugs Arzneimitteltherapie seltener Krankheiten Seltene Krankheiten 30 Millionen Europäer, davon etwa 4 Millionen Deutsche, leiden an seltenen Krankheiten. Als selten gilt hier eine Krankheit, wenn
- GSK-Forschungsstipendium für Studie zu möglichen Biomarkern bei COPD - Preis geht an Forscherin am Uniklinikum Hamburg-Eppendorf
 Deutsches Forschungsstipendium für Klinische Pneumologie: COPD: Neue Biomarker zur Prognose im V Deutsches Forschungsstipendium für Klinische Pneumologie COPD: Neue Biomarker zur Prognose im Visier - GSK-Forschungsstipendium
Deutsches Forschungsstipendium für Klinische Pneumologie: COPD: Neue Biomarker zur Prognose im V Deutsches Forschungsstipendium für Klinische Pneumologie COPD: Neue Biomarker zur Prognose im Visier - GSK-Forschungsstipendium
Kritische Gesichtspunkte zu Umbrella Protokollen und Adaptiven Designs aus der Sicht der Genehmigungsbehörde
 Kritische Gesichtspunkte zu Umbrella Protokollen und Adaptiven Designs aus der Sicht der Genehmigungsbehörde Heiko Preußer, BfArM Sachgebietsleiter Klinik Fachgebiet Klinische Prüfung Historischer Überblick
Kritische Gesichtspunkte zu Umbrella Protokollen und Adaptiven Designs aus der Sicht der Genehmigungsbehörde Heiko Preußer, BfArM Sachgebietsleiter Klinik Fachgebiet Klinische Prüfung Historischer Überblick
Neuerungen in der ICH-GCP Guideline
 AGAH - Study Nurse Forum Neuerungen in der ICH-GCP Guideline Dr. med. Martin Coenen Studienzentrale Studienzentrum Bonn (SZB) Wo bin ich und warum? good clinical practice (GCP) ICH-GCP GCP-V Ethikkommission
AGAH - Study Nurse Forum Neuerungen in der ICH-GCP Guideline Dr. med. Martin Coenen Studienzentrale Studienzentrum Bonn (SZB) Wo bin ich und warum? good clinical practice (GCP) ICH-GCP GCP-V Ethikkommission
Nutzenbewertung durch klinische Studien Wissenschaftliche Rationale oder Nomenklatura der Rationierung?
 Nutzenbewertung durch klinische Studien Wissenschaftliche Rationale oder Nomenklatura der Rationierung? Dr. med. Axel Meeßen Arbeiter- Symposium Kommerzielle Klinische Forschung, Motor des therapeutischen
Nutzenbewertung durch klinische Studien Wissenschaftliche Rationale oder Nomenklatura der Rationierung? Dr. med. Axel Meeßen Arbeiter- Symposium Kommerzielle Klinische Forschung, Motor des therapeutischen
IQWiG im Dialog 2016 Sind strengere Kriterien zur Evidenzbewertung notwendig? Zusammenfassung
 IQWiG im Dialog 2016 Sind strengere Kriterien zur Evidenzbewertung notwendig? Zusammenfassung Stefan Lange Stellvertretender Institutsleiter Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen
IQWiG im Dialog 2016 Sind strengere Kriterien zur Evidenzbewertung notwendig? Zusammenfassung Stefan Lange Stellvertretender Institutsleiter Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen
Studierende müssen mindestens 15 Credits aus dem gesamten Angebot Qualifikatonsprofil Prüfarzt nachweisen.
 Institut für Medizinische Statistik Direktor: Univ.-Prof. Dr. rer. nat. Ralf-Dieter Hilgers Qualifikationsprofil Prüfarzt Sehr geehrte Damen und Herren, das Institut für Medizinische Statistik bietet den
Institut für Medizinische Statistik Direktor: Univ.-Prof. Dr. rer. nat. Ralf-Dieter Hilgers Qualifikationsprofil Prüfarzt Sehr geehrte Damen und Herren, das Institut für Medizinische Statistik bietet den
SYMPOSIUM demenzerkrankungen - NEUE ansätze IN
 SYMPOSIUM demenzerkrankungen - NEUE ansätze IN GRUNDLAGENFORSCHUNG, DIAGNOSTIK, THERAPIE UND VERSORGUNG Wilhelm Klein-Strasse 27 CH-4012 Basel Tel. +41 61 325 51 11 Fax +41 61 325 55 12 info@upkbs.ch www.upkbs.ch
SYMPOSIUM demenzerkrankungen - NEUE ansätze IN GRUNDLAGENFORSCHUNG, DIAGNOSTIK, THERAPIE UND VERSORGUNG Wilhelm Klein-Strasse 27 CH-4012 Basel Tel. +41 61 325 51 11 Fax +41 61 325 55 12 info@upkbs.ch www.upkbs.ch
Anzahl klinischer Prüfungen und Studien
 Ergebnisse zur PHARMIG Umfrage Klinische Forschung in Österreich 201 ein Überblick zu den Leistungen der pharmazeutischen Industrie in Österreich Anzahl klinischer Prüfungen und Studien Anzahl der klinischen
Ergebnisse zur PHARMIG Umfrage Klinische Forschung in Österreich 201 ein Überblick zu den Leistungen der pharmazeutischen Industrie in Österreich Anzahl klinischer Prüfungen und Studien Anzahl der klinischen
Weltweit führend: Die deutsche Lymphomforschung. Vernetzung als Erfolgsmodell
 Weltweit führend: Die deutsche Lymphomforschung Vernetzung als Erfolgsmodell Michael Hallek Michael Hallek (Köln) 10 Jahre Kompetenznetze in der Medizin Festvortrag am 11. Juni 2009 Seite 1 Inzidenz und
Weltweit führend: Die deutsche Lymphomforschung Vernetzung als Erfolgsmodell Michael Hallek Michael Hallek (Köln) 10 Jahre Kompetenznetze in der Medizin Festvortrag am 11. Juni 2009 Seite 1 Inzidenz und
Phase: I. GKM Service Consulting, preparation of study synopses and protocols in the context of the early benefit assessment
 Statistical consulting Statistical consulting Beratung, Erstellung von Studiensynopsen und Prüfplänen zu Phase III Studien in verschiedenen Indikationen unter Berücksichtigung der möglichen Auswirkungen
Statistical consulting Statistical consulting Beratung, Erstellung von Studiensynopsen und Prüfplänen zu Phase III Studien in verschiedenen Indikationen unter Berücksichtigung der möglichen Auswirkungen
Pädiatrische Studien aus Sicht der Forschungsförderung
 Pädiatrische Studien aus Sicht der Forschungsförderung BfArM - Kinderarzneimittel-Symposium "More Medicines for Minors - Arzneimittelzulassung für Kinder und Jugendliche verbessern" Dr. Alexander Grundmann
Pädiatrische Studien aus Sicht der Forschungsförderung BfArM - Kinderarzneimittel-Symposium "More Medicines for Minors - Arzneimittelzulassung für Kinder und Jugendliche verbessern" Dr. Alexander Grundmann
IIT / AWB / NIS. Phasen klinischer Studien IIT = Investigator Initiated Trials
 IIT / AWB / NIS IIT = Investigator Initiated Trials AWB = Anwendungsbeobachtungen NIS = Nicht-interventionelle Studien Medical-Advisor-IIT-AWB-NIS Healthcare Marketing Dr. Umbach & Partner www.umbachpartner.com
IIT / AWB / NIS IIT = Investigator Initiated Trials AWB = Anwendungsbeobachtungen NIS = Nicht-interventionelle Studien Medical-Advisor-IIT-AWB-NIS Healthcare Marketing Dr. Umbach & Partner www.umbachpartner.com
Klinische Forschung ein Spannungsfeld zwischen Wissenschaft, Patientensicherheit und Sponsor-
 MEDIDATA GmbH Klinische Forschung ein Spannungsfeld zwischen Wissenschaft, Zulassungsanforderungen, Patientensicherheit und Sponsor- Interessen? Prof. Dr. med. Thomas D. Bethke, MBA, FFPM Medical Director,
MEDIDATA GmbH Klinische Forschung ein Spannungsfeld zwischen Wissenschaft, Zulassungsanforderungen, Patientensicherheit und Sponsor- Interessen? Prof. Dr. med. Thomas D. Bethke, MBA, FFPM Medical Director,
Regelungen des Rahmenvertrags. Aut-idem gemäß Rahmenvertrag: Austausch ohne Sachverstand? Wirkstoffgleichheit. Wirkstoffgleichheit
 Regelungen des Rahmenvertrags Aut-idem gemäß Rahmenvertrag: Austausch ohne Sachverstand? Prof. Dr. Henning Blume SocraTec R&D, Oberursel Concepts in Drug Research and Development www.socratec-pharma.de
Regelungen des Rahmenvertrags Aut-idem gemäß Rahmenvertrag: Austausch ohne Sachverstand? Prof. Dr. Henning Blume SocraTec R&D, Oberursel Concepts in Drug Research and Development www.socratec-pharma.de
Praktische Psychopharmakotherapie. Click here if your download doesn"t start automatically
 Praktische Psychopharmakotherapie Click here if your download doesn"t start automatically Praktische Psychopharmakotherapie Urban & Fischer Verlag/Elsevier GmbH Praktische Psychopharmakotherapie Urban
Praktische Psychopharmakotherapie Click here if your download doesn"t start automatically Praktische Psychopharmakotherapie Urban & Fischer Verlag/Elsevier GmbH Praktische Psychopharmakotherapie Urban
Actelion Pharmaceuticals Deutschland GmbH
 Methodologische Hinweise zur Umsetzung des FSA-Transparenzkodex für das Berichtsjahr 2015 Präambel Nach dem FSA-Transparenzkodex ist als Mitglied des FSA verpflichtet, sämtliche geldwerten Leistungen,
Methodologische Hinweise zur Umsetzung des FSA-Transparenzkodex für das Berichtsjahr 2015 Präambel Nach dem FSA-Transparenzkodex ist als Mitglied des FSA verpflichtet, sämtliche geldwerten Leistungen,
Programm Grundlagenkurs für Prüfer/Stellvertreter nach MPG und/oder AMG
 Programm Grundlagenkurs für Prüfer/Stellvertreter nach MPG und/oder AMG Termin: Freitag, 27.04.2018 & Samstag 28.4.2018 Ort: Osteosyntheseinstitut Ahrensburg Seminarraum 1. Stock Roggenweg 8, 22926 Ahrensburg
Programm Grundlagenkurs für Prüfer/Stellvertreter nach MPG und/oder AMG Termin: Freitag, 27.04.2018 & Samstag 28.4.2018 Ort: Osteosyntheseinstitut Ahrensburg Seminarraum 1. Stock Roggenweg 8, 22926 Ahrensburg
Die Ereignisse um Biotrial 2016
 Michael Wolzt michael.wolzt@meduniwien.ac.at Klinische Pharmakologie Medizinische Universität Wien Die Ereignisse um Biotrial 2016 Mar 2016 Disclaimer Diese Präsentation beruht auf öffentlich verfügbaren
Michael Wolzt michael.wolzt@meduniwien.ac.at Klinische Pharmakologie Medizinische Universität Wien Die Ereignisse um Biotrial 2016 Mar 2016 Disclaimer Diese Präsentation beruht auf öffentlich verfügbaren
Liebe Leserinnen und Leser,
 1 Liebe Leserinnen und Leser, viele von Ihnen tragen mit Ihrem Wissen und Ihrer Erfahrung zur Verbesserung von Arzneimitteln und zur Entwicklung neuer Therapien bei. Dass Sie dafür angemessenes Honorar
1 Liebe Leserinnen und Leser, viele von Ihnen tragen mit Ihrem Wissen und Ihrer Erfahrung zur Verbesserung von Arzneimitteln und zur Entwicklung neuer Therapien bei. Dass Sie dafür angemessenes Honorar
PATENT DE B4
 P A T E N T M E R K M A L E PATENT DE10 2007 048 094 B4 VERFAHREN UND PATENTGRUNDLAGE M.O.M HELENAA Das patentierte Verfahren M.O.M Helenaa beschreibt eine Technologie z.b. über Apps, als integrierte Lösung
P A T E N T M E R K M A L E PATENT DE10 2007 048 094 B4 VERFAHREN UND PATENTGRUNDLAGE M.O.M HELENAA Das patentierte Verfahren M.O.M Helenaa beschreibt eine Technologie z.b. über Apps, als integrierte Lösung
Was sind klinische Prüfungen Eine Einführung. Dr. Thorsten Ruppert Senior Referent Grundsatzfragen Forschung/Entwicklung/Innovation, vfa
 Was sind klinische Prüfungen Eine Einführung Dr. Thorsten Ruppert Senior Referent Grundsatzfragen Forschung/Entwicklung/Innovation, vfa Berlin, 28. Januar 2016 Klinische Studie vs. Klinische Prüfung Wie
Was sind klinische Prüfungen Eine Einführung Dr. Thorsten Ruppert Senior Referent Grundsatzfragen Forschung/Entwicklung/Innovation, vfa Berlin, 28. Januar 2016 Klinische Studie vs. Klinische Prüfung Wie
2016 brachte einen Rückgang der Klinischen Prüfungen in Österreich im Vergleich zu 2015, obwohl das Minimum von 2014 nicht erreicht wurde.
 Klinische Prüfungen: Statistik 216 Abteilung Klinische Prüfung (CLTR) Aktuelle Statistik der Klinischen Prüfung für Arzneimittel in Österreich 216 brachte einen Rückgang der Klinischen Prüfungen in Österreich
Klinische Prüfungen: Statistik 216 Abteilung Klinische Prüfung (CLTR) Aktuelle Statistik der Klinischen Prüfung für Arzneimittel in Österreich 216 brachte einen Rückgang der Klinischen Prüfungen in Österreich
Impfstoffsicherheit in Deutschland
 Impfstoffsicherheit in Deutschland Eine Standortbestimmung 1. Nationale Konferenz für differenziertes Impfen Wuppertal, 2. Oktober 2010 Dr. med Klaus Hartmann, Wiesbaden Arzneimittelsicherheit in Deutschland
Impfstoffsicherheit in Deutschland Eine Standortbestimmung 1. Nationale Konferenz für differenziertes Impfen Wuppertal, 2. Oktober 2010 Dr. med Klaus Hartmann, Wiesbaden Arzneimittelsicherheit in Deutschland
Diskrepanzen zwischen Zulassung und früher Nutzenbewertung Prof. Dr. Karl Broich
 Diskrepanzen zwischen Zulassung und früher Nutzenbewertung Prof. Dr. Karl Broich Gliederung Aufgaben der Zulassung Aktuelle und neue Zulassungswege Rolle des BfArM national/europäisch bei der Zusatznutzenbewertung
Diskrepanzen zwischen Zulassung und früher Nutzenbewertung Prof. Dr. Karl Broich Gliederung Aufgaben der Zulassung Aktuelle und neue Zulassungswege Rolle des BfArM national/europäisch bei der Zusatznutzenbewertung
Deutschland. Zum Firmenjubiläum der Gilead Sciences GmbH - 10 Jahre Fortschritt für HIV- und Hepatitis B-Patienten i
 Zum Firmenjubiläum der Gilead Sciences GmbH 10 Jahre Fortschritt für HIV und Hepatitis BPatienten i Zum Firmenjubiläum der Gilead Sciences GmbH 10 Jahre Fortschritt für HIV und Hepatitis BPatienten in
Zum Firmenjubiläum der Gilead Sciences GmbH 10 Jahre Fortschritt für HIV und Hepatitis BPatienten i Zum Firmenjubiläum der Gilead Sciences GmbH 10 Jahre Fortschritt für HIV und Hepatitis BPatienten in
KLINISCHE PRÜFUNG EINE EINFÜHRUNG. ATA Conference 2003 - Elke Vogt-Arendt
 KLINISCHE PRÜFUNG EINE EINFÜHRUNG ATA Conference 2003 - Elke Vogt-Arendt Was ist eine klinische Prüfung? Überprüfung von Wirkung, Nebenwirkung, Dosierung usw. eines neuen Arzneimittels vor Markteinführung.
KLINISCHE PRÜFUNG EINE EINFÜHRUNG ATA Conference 2003 - Elke Vogt-Arendt Was ist eine klinische Prüfung? Überprüfung von Wirkung, Nebenwirkung, Dosierung usw. eines neuen Arzneimittels vor Markteinführung.
Antrag zur Durchführung einer epidemiologischen Studie
 Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
Euros für Ärzte wie viel Transparenz verträgt die Medizin?
 MEZIS e.v.- Mein Essen zahl ich selbst Initiative unbestechlicher Ärztinnen und Ärzte Euros für Ärzte wie viel Transparenz verträgt die Medizin? www.mezis.de Bildquelle: privat MEZIS Mein Essen zahl ich
MEZIS e.v.- Mein Essen zahl ich selbst Initiative unbestechlicher Ärztinnen und Ärzte Euros für Ärzte wie viel Transparenz verträgt die Medizin? www.mezis.de Bildquelle: privat MEZIS Mein Essen zahl ich
Die Medizinische Überwachung von Klinischen Prüfungen in einem Auftragsforschungsinstitut
 Die Medizinische Überwachung von Klinischen Prüfungen in einem Auftragsforschungsinstitut 1 (CRO) Katharina Kotz Medical Monitoring Associate PRA International Themenübersicht Medizinische Schwerpunkte
Die Medizinische Überwachung von Klinischen Prüfungen in einem Auftragsforschungsinstitut 1 (CRO) Katharina Kotz Medical Monitoring Associate PRA International Themenübersicht Medizinische Schwerpunkte
Evidenzbasierte Chirurgie. Evidenzbasierte Chirurgie - Wirksame Strategien zur Umsetzung in die Praxis
 Evidenzbasierte Chirurgie - Wirksame Strategien zur Umsetzung in die Praxis C. M. Seiler 5. EBM-Symposium 12.-14.02.2004 in Lübeck IKT Konsortium Evidenzbasierte Chirurgie Integration der besten externen
Evidenzbasierte Chirurgie - Wirksame Strategien zur Umsetzung in die Praxis C. M. Seiler 5. EBM-Symposium 12.-14.02.2004 in Lübeck IKT Konsortium Evidenzbasierte Chirurgie Integration der besten externen
Das a s D eu e t u sc s h c e h e H äm ä o m p o h p i h liile i r e eg e i g s i t s er
 Das Deutsche Hämophilieregister Birgit Haschberger Deutsches Hämophilieregister mit Sitz am Paul-Ehrlich-Institut Paul-Ehrlich-Straße 51-59 D-63225 Langen +49 (0) 6103 77-1860 +49 (0) 6103 77-1276 E-Mail:
Das Deutsche Hämophilieregister Birgit Haschberger Deutsches Hämophilieregister mit Sitz am Paul-Ehrlich-Institut Paul-Ehrlich-Straße 51-59 D-63225 Langen +49 (0) 6103 77-1860 +49 (0) 6103 77-1276 E-Mail:
Wissen, worauf es ankommt
 Wissen, worauf es ankommt www.tuev-sued.de/akademie GmbH Westendstraße 160 80339 München Telefon: 089 5791 2389 E-Mail: akademie@tuev-sued.de Bleiben wir in Kontakt! AC46-Pharma-fly-210x297-w-15-07-03
Wissen, worauf es ankommt www.tuev-sued.de/akademie GmbH Westendstraße 160 80339 München Telefon: 089 5791 2389 E-Mail: akademie@tuev-sued.de Bleiben wir in Kontakt! AC46-Pharma-fly-210x297-w-15-07-03
Evaluierungsbogen zur pharmazeutischen Betreuung von klinischen Studien
 Studienbezeichnung/Name of Clinical Trial EudraCT-Nummer / EudraCT-Number Sponsor/VertreterIn des Sponsors / Sponsor or delegate of sponsor CRO / CRA Bewilligungen Votum der Ethikkommission Beschreibung
Studienbezeichnung/Name of Clinical Trial EudraCT-Nummer / EudraCT-Number Sponsor/VertreterIn des Sponsors / Sponsor or delegate of sponsor CRO / CRA Bewilligungen Votum der Ethikkommission Beschreibung
Praktische Durchführung von Phase I Studien in Patienten
 Praktische Durchführung von Phase I Studien in Patienten Was die Industrie will und was die Zentren bieten können Burkhard Kerlin, AGAH Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v
Praktische Durchführung von Phase I Studien in Patienten Was die Industrie will und was die Zentren bieten können Burkhard Kerlin, AGAH Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v
Patientenbeteiligung und EbM
 Patientenbeteiligung und EbM N. Skoetz CHMG Cochrane Haematological Malignancies Group (CHMG) Teilprojekt im Kompetenznetz Maligne Lymphome Seit Okt 2000 als Cochrane Review Group akkreditiert Cochrane
Patientenbeteiligung und EbM N. Skoetz CHMG Cochrane Haematological Malignancies Group (CHMG) Teilprojekt im Kompetenznetz Maligne Lymphome Seit Okt 2000 als Cochrane Review Group akkreditiert Cochrane
Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika
 Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika - Unterlagenschutz bei topisch angewendeten Produkten und Hilfsstoffen Markus Ambrosius ANWALTSKANZLEI STRÄTER Kronprinzenstraße
Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika - Unterlagenschutz bei topisch angewendeten Produkten und Hilfsstoffen Markus Ambrosius ANWALTSKANZLEI STRÄTER Kronprinzenstraße
EU Verordnung zu Klinischen Prüfungen Teil 1 des Genehmigungsverfahrens Begutachtung durch die Behörde BfArM Elke Stahl
 EU Verordnung zu Klinischen Prüfungen Teil 1 des Genehmigungsverfahrens Begutachtung durch die Behörde BfArM Elke Stahl Verordnung (EU) 536/2014 Europaweite Harmonisierung und Vereinfachung Verordnung
EU Verordnung zu Klinischen Prüfungen Teil 1 des Genehmigungsverfahrens Begutachtung durch die Behörde BfArM Elke Stahl Verordnung (EU) 536/2014 Europaweite Harmonisierung und Vereinfachung Verordnung
Klinische Prüfungen: Statistik 2017
 BASG / AGES Institut Überwachung/Abteilung Klinische Prüfung Traisengasse 5, 1200 Wien, Österreich Klinische Prüfungen: Statistik 2017 Aktuelle Statistik der Klinischen Prüfung für Arzneimittel in Österreich
BASG / AGES Institut Überwachung/Abteilung Klinische Prüfung Traisengasse 5, 1200 Wien, Österreich Klinische Prüfungen: Statistik 2017 Aktuelle Statistik der Klinischen Prüfung für Arzneimittel in Österreich
Methotrexat in der Therapie des Morbus Crohn wirksam, sicher, günstig
 Medac-Symposium auf dem DGVS-Kongress 2015 in Leipzig zur MTX-Therapie bei Morbus Crohn(1) Methotrexat in der Therapie des Morbus Crohn wirksam, sicher, günstig Leipzig / Wedel (17. September 2015) - Die
Medac-Symposium auf dem DGVS-Kongress 2015 in Leipzig zur MTX-Therapie bei Morbus Crohn(1) Methotrexat in der Therapie des Morbus Crohn wirksam, sicher, günstig Leipzig / Wedel (17. September 2015) - Die
Personalisierte Medizin der Patient als Nutznießer oder Opfer? Jahrestagung Deutscher Ethikrat
 Personalisierte Medizin der Patient als Nutznießer oder Opfer? Jahrestagung Deutscher Ethikrat Berlin 24. Mai 2012 10:00 bis 17:30 Uhr Berlin-Brandenburgische Akademie der Wissenschaften, Leibniz-Saal
Personalisierte Medizin der Patient als Nutznießer oder Opfer? Jahrestagung Deutscher Ethikrat Berlin 24. Mai 2012 10:00 bis 17:30 Uhr Berlin-Brandenburgische Akademie der Wissenschaften, Leibniz-Saal
Plazebo: Risiko in klinischen Prüfungen und ethisch bedenklich?
 Plazebo: Risiko in klinischen Prüfungen und ethisch bedenklich? Dr. Karl Broich Bundesinstitut für Arzneimittel Kurt-Georg-Kiesinger-Allee 38, D-53175 Bonn Schein-OP (Sham-Procedures) Ideales Arzneimittel
Plazebo: Risiko in klinischen Prüfungen und ethisch bedenklich? Dr. Karl Broich Bundesinstitut für Arzneimittel Kurt-Georg-Kiesinger-Allee 38, D-53175 Bonn Schein-OP (Sham-Procedures) Ideales Arzneimittel
Todesfälle bei klinischen Studien deutscher Pharmaunternehmen in Entwicklungs- und Schwellenländern
 Deutscher Bundestag Drucksache 17/10911 17. Wahlperiode 02. 10. 2012 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Niema Movassat, Annette Groth, Heike Hänsel, weiterer Abgeordneter
Deutscher Bundestag Drucksache 17/10911 17. Wahlperiode 02. 10. 2012 Antwort der Bundesregierung auf die Kleine Anfrage der Abgeordneten Niema Movassat, Annette Groth, Heike Hänsel, weiterer Abgeordneter
Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten
 Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten Arzneimittelmarktneuordnungsgesetz (AMNOG) 35a Bewertung des Nutzens von Arzneimitteln
Frühe Nutzenbewertungen nach AMNOG: Einblicke in die aktuellen Verfahren und mögliche Auswirkungen für Ärzte und Patienten Arzneimittelmarktneuordnungsgesetz (AMNOG) 35a Bewertung des Nutzens von Arzneimitteln
Newsletter. Sonderausgabe Juli 2013. Sonderausgabe. Editorial
 Sonderausgabe Juli 2013 Newsletter Sonderausgabe Editorial» Seite 2 Aktuelles aus dem FSA Transparenz schafft Vertrauen und bekämpft Misstrauen Pharma-Branche verabschiedet europäischen Transparenzkodex»
Sonderausgabe Juli 2013 Newsletter Sonderausgabe Editorial» Seite 2 Aktuelles aus dem FSA Transparenz schafft Vertrauen und bekämpft Misstrauen Pharma-Branche verabschiedet europäischen Transparenzkodex»
Endokrinologie- Assistent/in DGE
 Einladung zur Weiterbildung Endokrinologie- Assistent/in DGE Beginn: 15. Oktober 2018 Ende: 4. April 2019 Weiterbildung der Deutschen Gesellschaft für Endokrinologie Hotel am Schloßpark Zum Kurfürst, Oberschleißheim
Einladung zur Weiterbildung Endokrinologie- Assistent/in DGE Beginn: 15. Oktober 2018 Ende: 4. April 2019 Weiterbildung der Deutschen Gesellschaft für Endokrinologie Hotel am Schloßpark Zum Kurfürst, Oberschleißheim
Meine persönliche Checkliste
 Meine persönliche Checkliste Leitfaden für Ihr Gespräch mit dem Arzt und praktische Informationen rund um die Erkrankung und ihre Behandlung. Was Sie fragen sollten, was Sie wissen sollten Der Umgang mit
Meine persönliche Checkliste Leitfaden für Ihr Gespräch mit dem Arzt und praktische Informationen rund um die Erkrankung und ihre Behandlung. Was Sie fragen sollten, was Sie wissen sollten Der Umgang mit
Programmentwurf (vertrauliches Konzept, Referenten und Partner anzufragen) Rahmendaten
 Rahmendaten Veranstaltungstitel: Hochschule & Industrie Gemeinsam für die Pharmazie der Zukunft Termin: 7. und 8. April 2016 Ort: Otto-Stern-Zentrum, Campus Riedberg, Goethe-Universität, Frankfurt am Main
Rahmendaten Veranstaltungstitel: Hochschule & Industrie Gemeinsam für die Pharmazie der Zukunft Termin: 7. und 8. April 2016 Ort: Otto-Stern-Zentrum, Campus Riedberg, Goethe-Universität, Frankfurt am Main
Increasing value in clinical research Prof. Dr. med. Christiane Pauli-Magnus
 Increasing value in clinical research Prof. Dr. med. Christiane Pauli-Magnus Co-Leiterin Departement Klinische Forschung und Leiterin Clinical Trial Unit Universität und Universitätsspital Basel Die Forschungsqualität
Increasing value in clinical research Prof. Dr. med. Christiane Pauli-Magnus Co-Leiterin Departement Klinische Forschung und Leiterin Clinical Trial Unit Universität und Universitätsspital Basel Die Forschungsqualität
Prüfer und Prüfstelle
 Anforderung an Prüfer und Prüfeinrichtungen gemäß Empfehlungen der Bundesärztekammer Neues zu klinischen Prüfungen von Arzneimitteln und Medizinprodukten 19.-20. April 2010 Bonn Petra Knupfer Ethik-Kommission
Anforderung an Prüfer und Prüfeinrichtungen gemäß Empfehlungen der Bundesärztekammer Neues zu klinischen Prüfungen von Arzneimitteln und Medizinprodukten 19.-20. April 2010 Bonn Petra Knupfer Ethik-Kommission
Erfahrungen mit GCP Inspektionen von MPG Studien
 Erfahrungen mit GCP Inspektionen von MPG Studien Yvonne Borck, Universitätsklinik Bonn Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v Hintergrund Nach 26 MPG unterliegen Betriebe und
Erfahrungen mit GCP Inspektionen von MPG Studien Yvonne Borck, Universitätsklinik Bonn Arbeitsgemeinschaft für angewandte Humanpharmakologie (AGAH) e.v Hintergrund Nach 26 MPG unterliegen Betriebe und
Therapiefaktor Wohnort die Tücken der Versorgungslandschaft in der Onkologie
 Therapiefaktor Wohnort die Tücken der Versorgungslandschaft in der Onkologie Jochen Heymanns Berlin 20. April 2016 Potentielle Interessenkonflikte Heymanns Mitglied des Vorstandes des Berufsverbandes
Therapiefaktor Wohnort die Tücken der Versorgungslandschaft in der Onkologie Jochen Heymanns Berlin 20. April 2016 Potentielle Interessenkonflikte Heymanns Mitglied des Vorstandes des Berufsverbandes
Die Weiterbildung im Fach Hals-Nasen-Ohren-Heilkunde gliedert sich in die
 Empfehlungen für die Landesärztekammern der Bundesrepublik Deutschland zur Begutachtung von Anträgen auf Weiterbildungsbefugnis für das Fach Hals-Nasen-Ohren-Heilkunde Präambel: Die nachfolgenden Empfehlungen
Empfehlungen für die Landesärztekammern der Bundesrepublik Deutschland zur Begutachtung von Anträgen auf Weiterbildungsbefugnis für das Fach Hals-Nasen-Ohren-Heilkunde Präambel: Die nachfolgenden Empfehlungen
Auswertungsbericht Patientenbefragung 2018
 Auswertungsbericht Patientenbefragung 2018 Vergleich mit Ergebnis Vorberfragung, 2018 1. Vorbemerkung Grundgesamtheit Kunde Vergleich 2016 Befragungszeitraum 2018 2016 Ausgefüllte Fragebögen 99 99 Zeile
Auswertungsbericht Patientenbefragung 2018 Vergleich mit Ergebnis Vorberfragung, 2018 1. Vorbemerkung Grundgesamtheit Kunde Vergleich 2016 Befragungszeitraum 2018 2016 Ausgefüllte Fragebögen 99 99 Zeile
Arzt und Selbstmedikation. Ihr Kontakt: Dirk Balsmeier t +49 (0) f +49 (0) e
 Arzt und Selbstmedikation Ihr Kontakt: Dirk Balsmeier t +49 (0)521 9257-339 f +49 (0)521 9257-332 e dirk.balsmeier@tns-global.com 1 2 Inhalt Hintergrund und Zielsetzung Methode, Zielgruppe und Stichprobengröße
Arzt und Selbstmedikation Ihr Kontakt: Dirk Balsmeier t +49 (0)521 9257-339 f +49 (0)521 9257-332 e dirk.balsmeier@tns-global.com 1 2 Inhalt Hintergrund und Zielsetzung Methode, Zielgruppe und Stichprobengröße
WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN
 CAMPUS INNENSTADT KOMM. DIREKTOR: PROF. DR: C. DANNEKER STELLV. DIREKTOR: PD DR. T. WEISSENBACHER WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN Informationsnachmittag- Leben mit Brustkrebs Was gibt es Neues?
CAMPUS INNENSTADT KOMM. DIREKTOR: PROF. DR: C. DANNEKER STELLV. DIREKTOR: PD DR. T. WEISSENBACHER WAS BRINGEN KLINISCHE STUDIEN FÜR PATIENTEN Informationsnachmittag- Leben mit Brustkrebs Was gibt es Neues?
Off-Label Use in der Rheumatherapie
 Abseits der Wege: Off-Label Use in der Rheumatherapie Statement von Prof. Dr. med. Klaus Krüger Köln (23. September 2009) - Laut deutschem Sozialgesetzbuch ( 70) ist der behandelnde Arzt verpflichtet,
Abseits der Wege: Off-Label Use in der Rheumatherapie Statement von Prof. Dr. med. Klaus Krüger Köln (23. September 2009) - Laut deutschem Sozialgesetzbuch ( 70) ist der behandelnde Arzt verpflichtet,
Die Rolle von Patientenorganisationen bei Seltenen Erkrankungen
 Die Rolle von Patientenorganisationen bei Seltenen Erkrankungen Dr. Andreas L.G. Reimann, MBA Stellvertretender Vorsitzender, ACHSE e.v., Berlin Geschäftsführer, Mukoviszidose e.v., Bonn Was ist die ACHSE?
Die Rolle von Patientenorganisationen bei Seltenen Erkrankungen Dr. Andreas L.G. Reimann, MBA Stellvertretender Vorsitzender, ACHSE e.v., Berlin Geschäftsführer, Mukoviszidose e.v., Bonn Was ist die ACHSE?
COMMUNICATIONS TO SUCCESS. Marketing in der pharmazeutischen Industrie. Akademie
 Marketing in der pharmazeutischen Industrie Akademie 6.1. 2005 1 Ausgaben der GKV 2003 (in Millrd. Euro) 8,6 Krankenhauskosten 31,3 9,3 24,2 24,3 46,8 ärztliche Leistung Arzneimiitel Heil- und Hilfsmittel
Marketing in der pharmazeutischen Industrie Akademie 6.1. 2005 1 Ausgaben der GKV 2003 (in Millrd. Euro) 8,6 Krankenhauskosten 31,3 9,3 24,2 24,3 46,8 ärztliche Leistung Arzneimiitel Heil- und Hilfsmittel
 Vorhofflimmern hat viele Gesichter Vorhofflimmern ist die häufigste und klinisch wichtigste Herzrhythmusstörung 1% der erwachsenen Bevölkerung in Deutschland ist betroffen Die Häufigkeit des Vorhofflimmerns
Vorhofflimmern hat viele Gesichter Vorhofflimmern ist die häufigste und klinisch wichtigste Herzrhythmusstörung 1% der erwachsenen Bevölkerung in Deutschland ist betroffen Die Häufigkeit des Vorhofflimmerns
Kompetenznetz Parkinson Syndrome Erfolge
 Kompetenznetz Parkinson Syndrome 1999 2009 Erfolge Infrastruktur entwickelt vom KNP SecuTrial elektronisches Internet-basiertes Daten-Eingabe-System ecrf KNP SecuTrial Nationale Nutzung: KN Parkinson,
Kompetenznetz Parkinson Syndrome 1999 2009 Erfolge Infrastruktur entwickelt vom KNP SecuTrial elektronisches Internet-basiertes Daten-Eingabe-System ecrf KNP SecuTrial Nationale Nutzung: KN Parkinson,
Sicherheitsrelevante Hinweise für medizinische Fachkreise
 Sicherheitsrelevante Hinweise für medizinische Fachkreise für die Therapie des multiplen Myeloms mit Bortezomib in Abhängigkeit von den unterschiedlichen Indikationen im Rahmen der Indikationserweiterung
Sicherheitsrelevante Hinweise für medizinische Fachkreise für die Therapie des multiplen Myeloms mit Bortezomib in Abhängigkeit von den unterschiedlichen Indikationen im Rahmen der Indikationserweiterung
Frühe Nutzenbewertung im Gemeinsamen Bundesausschuss
 im Gemeinsamen Bundesausschuss Vortrag im Rahmen des 13. DGRA-Jahreskongresses in Bonn Referent: Dr. jur. Rainer Hess, G-BA Seite 1 3. Mai 2011 13. DGRA-Jahreskongress in Bonn 2011, Dr. jur. Rainer Hess
im Gemeinsamen Bundesausschuss Vortrag im Rahmen des 13. DGRA-Jahreskongresses in Bonn Referent: Dr. jur. Rainer Hess, G-BA Seite 1 3. Mai 2011 13. DGRA-Jahreskongress in Bonn 2011, Dr. jur. Rainer Hess
Anzeige einer klinischen Prüfung gemäß 67 Abs. 1 und 3 AMG und 12 Abs. 1-3 GCP-V bei der zuständigen Landesbehörde
 An (Name und Anschrift der zuständigen Behörde) Regierung von Oberbayern Zentrale Arzneimittelüberwachung Bayern (GMP/GCP) 80534 München Name (ggf. Firmenbezeichnung) und Anschrift des Anzeigenden Grund
An (Name und Anschrift der zuständigen Behörde) Regierung von Oberbayern Zentrale Arzneimittelüberwachung Bayern (GMP/GCP) 80534 München Name (ggf. Firmenbezeichnung) und Anschrift des Anzeigenden Grund
Das Arzneimittelmarktneuordnungsgesetz (AMNOG) - Welche Auswirkungen hat das Gesetz auf die Apotheken?
 Das Arzneimittelmarktneuordnungsgesetz (AMNOG) - Welche Auswirkungen hat das Gesetz auf die Apotheken? Dr. rer. nat. Holger Knoth, Leiter der Klinik-Apotheke Seite 1 Welche Tätigkeitsfelder in der Apotheke
Das Arzneimittelmarktneuordnungsgesetz (AMNOG) - Welche Auswirkungen hat das Gesetz auf die Apotheken? Dr. rer. nat. Holger Knoth, Leiter der Klinik-Apotheke Seite 1 Welche Tätigkeitsfelder in der Apotheke
V I N VerordnungsInfo Nordrhein
 V I N VerordnungsInfo Nordrhein Off-Label Verordnung von Arzneimitteln außerhalb ihrer Zulassung Für die Verordnung eines Arzneimittels zu Lasten der gesetzlichen Krankenkasse müssen die Präparate in der
V I N VerordnungsInfo Nordrhein Off-Label Verordnung von Arzneimitteln außerhalb ihrer Zulassung Für die Verordnung eines Arzneimittels zu Lasten der gesetzlichen Krankenkasse müssen die Präparate in der
Krebsinformation für Patienten, Angehörige und die Öffentlichkeit neue Kanäle und Medien
 Session: Gesundheitsforschung hat viele Zielgruppen das Format ist entscheidend Krebsinformation für Patienten, Angehörige und die Öffentlichkeit neue Kanäle und Medien Dr. med. Krebsinformationsdienst
Session: Gesundheitsforschung hat viele Zielgruppen das Format ist entscheidend Krebsinformation für Patienten, Angehörige und die Öffentlichkeit neue Kanäle und Medien Dr. med. Krebsinformationsdienst
Zulassung von Arzneimitteln. Klinische Untersuchungen. Katalin Müllner
 Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Zulassung von Arzneimitteln. Klinische Untersuchungen Katalin Müllner Arzneimittel In gesetzlicher Definition sind Arzneimittel Stoffe oder Zubereitungen aus Stoffen, die vom Hersteller, der sie in den
Umgang mit Transportverweigerung
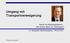 Umgang mit Transportverweigerung Recht im Rettungsdienst Mit einem Bein im Gefängnis? 13. Stuttgarter Intensivkongress 09.02.2017 Transportindikation und Patientenwille + - + RD hält Transport für indiziert
Umgang mit Transportverweigerung Recht im Rettungsdienst Mit einem Bein im Gefängnis? 13. Stuttgarter Intensivkongress 09.02.2017 Transportindikation und Patientenwille + - + RD hält Transport für indiziert
Das Krankheitsspektrum der Zukunft
 Pressekonferenz Das Krankheitsspektrum der Zukunft Expertenumfrage unter 100 führenden deutschen Forschern 10. August 2005 Berlin Das Krankheitsspektrum der Zukunft Herausforderung für die forschende Arzneimittelindustrie
Pressekonferenz Das Krankheitsspektrum der Zukunft Expertenumfrage unter 100 führenden deutschen Forschern 10. August 2005 Berlin Das Krankheitsspektrum der Zukunft Herausforderung für die forschende Arzneimittelindustrie
Studienzentrum des Universitätsklinikums Freiburg
 Studienzentrum des Universitätsklinikums Freiburg Zyklus der Generierung von Evidenz Zusammenarbeit von Fachgesellschaften, (deren) Studienzentren und Studienregistern Dr.med. Gabriele Dreier, Studienzentrum
Studienzentrum des Universitätsklinikums Freiburg Zyklus der Generierung von Evidenz Zusammenarbeit von Fachgesellschaften, (deren) Studienzentren und Studienregistern Dr.med. Gabriele Dreier, Studienzentrum
Die korrekte Ethikeinreichung. Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group
 Die korrekte Ethikeinreichung Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Einreichung bei EKs als Prüfzentrum als Sponsor 2 Prüfzentrum Unterlagen für Prüfer und Stellvertreter
Die korrekte Ethikeinreichung Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Einreichung bei EKs als Prüfzentrum als Sponsor 2 Prüfzentrum Unterlagen für Prüfer und Stellvertreter
Klinische Prüfung: Praktische Aspekte bei der Umsetzung der EU Regulation 536/2014. vfa VKliPha / Ruppert
 Klinische Prüfung: Praktische Aspekte bei der Umsetzung der EU Regulation 536/2014 -aus Sicht der pharmazeutischen h Industrie Anwendung der EU-CTR -noch unklar Seite 2 Anwendung der EU-CTR Auch die EMA
Klinische Prüfung: Praktische Aspekte bei der Umsetzung der EU Regulation 536/2014 -aus Sicht der pharmazeutischen h Industrie Anwendung der EU-CTR -noch unklar Seite 2 Anwendung der EU-CTR Auch die EMA
Major Achievements of Innovative Drug Therapy
 Nutzenbewertung durch klinische Studien - Wissenschaftliche Rationale oder Nomenklatura der Rationierung? Diskussionsbeitrag zum Symposium der Universität Bonn Kommerzielle Klinische Forschung. Motor des
Nutzenbewertung durch klinische Studien - Wissenschaftliche Rationale oder Nomenklatura der Rationierung? Diskussionsbeitrag zum Symposium der Universität Bonn Kommerzielle Klinische Forschung. Motor des
Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse -
 Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse - Franz Edler von Koch Klinikum Dritter Orden Klinik für Gynäkologie und Geburtshilfe Brustzentrum Gynäkologisches
Individuelle Therapieentscheidungen im Brustzentrum - zwischen Erfahrung und Laboranalyse - Franz Edler von Koch Klinikum Dritter Orden Klinik für Gynäkologie und Geburtshilfe Brustzentrum Gynäkologisches
Förderung Klinischer Studien durch die Deutsche Forschungsgemeinschaft
 Förderung Klinischer Studien durch die Deutsche Forschungsgemeinschaft Dr. Eckard Picht Deutsche Forschungsgemeinschaft Gruppe Medizin Übersicht des Vortrags Die Deutsche Forschungsgemeinschaft Förderung
Förderung Klinischer Studien durch die Deutsche Forschungsgemeinschaft Dr. Eckard Picht Deutsche Forschungsgemeinschaft Gruppe Medizin Übersicht des Vortrags Die Deutsche Forschungsgemeinschaft Förderung
Chancen und Risiken der digitalen Gesundheitsversorgung: Diagnose vor Therapie und Abwägung vor Versand
 Chancen und Risiken der digitalen Gesundheitsversorgung: Diagnose vor Therapie und Abwägung vor Versand Prof. Dr. Franz Porzsolt Versorgungsforschung an der Klinik für Allgemein-und Viszeralchirurgie,
Chancen und Risiken der digitalen Gesundheitsversorgung: Diagnose vor Therapie und Abwägung vor Versand Prof. Dr. Franz Porzsolt Versorgungsforschung an der Klinik für Allgemein-und Viszeralchirurgie,
Datentransparenz ein ethischer Imperativ
 Georg Marckmann Ludwig-Maximilians-Universität München Lehrstuhl für Geschichte, Theorie und Ethik der Medizin Datentransparenz ein ethischer Imperativ IQWiG Herbst-Symposium: Datentransparenz als Voraussetzung
Georg Marckmann Ludwig-Maximilians-Universität München Lehrstuhl für Geschichte, Theorie und Ethik der Medizin Datentransparenz ein ethischer Imperativ IQWiG Herbst-Symposium: Datentransparenz als Voraussetzung
