Diagnostik von Myopathien *
|
|
|
- Nicolas Hartmann
- vor 6 Jahren
- Abrufe
Transkript
1 Leitlinie 599 Diagnostik von Myopathien * Diagnosis of Myopathies Autoren M. Deschauer 1, **, C. R. Müller-Reible 2, K. M. Rösler 3, B. Schoser 4, J. Wanschitz 5, J. Weis 6, S. Zierz 7 Institute Die Institutsangaben sind am Ende des Beitrags gelistet. Schlüsselwörter " Leitlinie " Muskelerkrankung " Myopathie " Diagnostik Muskelbiopsie " Keywords " guideline " myopathy " muscular disorder " diagnosis muscle biopsy " Bibliografie DOI /s Akt Neurol 2016; 43: Georg Thieme Verlag KG Stuttgart New York ISSN Korrespondenzadresse Prof. Dr. med. Marcus Deschauer Klinik und Poliklinik für Neurologie, Klinikum rechts der Isar, Technische Universität München Ismaninger Str München marcus.deschauer@tum.de Zusammenfassung Hintergrund: Die Diagnosestellung von Myopathien im Erwachsenenalter ist aufgrund der klinischen und genetischen Heterogenität schwierig. Diese Leitlinie soll helfen, bei erwachsenen Patienten mit Muskelerkrankungen gezielt eine Diagnose zu stellen und so Patienten mit behandelbaren Myopathien einer Therapie zuführen zu können. Eine eindeutige Zuordnung hereditärer Myopathien ermöglicht eine bessere prognostische Einordnung und bildet die Grundlage für die genetische Familienberatung. Es ist von besonderer Bedeutung, die Indikation zur Muskelbiopsie korrekt zu stellen und aus dieser die maximale diagnostische Ausbeute zu erzielen. Methodik: Das Leitliniengremium bestand aus Neurologen mit myologischer Expertise aus Österreich, der Schweiz und aus Deutschland und Experten für Muskelerkrankungen aus der Neuropathologie und Humangenetik. Zusätzlich wurde ein Vertreter der Selbsthilfeorganisation Deutsche Gesellschaft für Muskelkranke e. V. einbezogen. Für die Überarbeitung der zuletzt 2012 erschienenen DGN-Leitlinie wurde die bis Anfang 2016 erschienene Literatur berücksichtigt und die Leitlinie auf S1-Niveau aktualisiert. Ergebnisse: Anhand der klinischen Symptomatik sollte zuerst eine syndromale Arbeitsdiagnose gestellt werden. Laborchemisch ist zu prüfen, ob eine persistierende Erhöhung der Kreatinkinase (CK) vorliegt, ergänzt durch weitere Laborwerte, die auf eine entzündliche oder endokrine Erkrankung hinweisen. Bei jedem Patienten mit Verdacht auf eine Myopathie sollte eine EMG-Untersuchung erfolgen, um neurogene von myopathischen Prozessen zu unterscheiden, und um eine * Den Leitlinientext zusammen mit der Interessenkonflikterklärung finden Sie auch auf sowie ** federführend Abstract Background: Diagnosis of myopathies can be difficult due to clinical and genetical heterogeneity. This guideline should enable a diagnostic workup in patients with myopathies to facilitate therapy in treatable disorders. A correct classification of hereditary forms is important for genetic counselling, estimation of the prognosis, and therapy. It is important to decipher indications for a muscle biopsy and to perform it in an appropriate way to reach maximal diagnostic yield. Methods: Members of the guideline committee were neurological experts for myopathies from Austria, Swiss and Germany but also a neuropathologist, a human geneticist, and a member of the German neuromuscular patient support group. For the update of the guideline, that was issued for the last time in 2012, the recent literature published until early 2016 was considered. The update was performed according to S1-level. Results: According to the clinical examination a syndrome diagnosis should be established. Laboratory testing should include creatine kinase (CK) supplemented by laboratory investigation for testing inflammatory and endocrine abnormalities. In all patients with suspected myopathy needle electromyography has to be performed to distinguish between neurogenic and myopathic weakness and to identify myotonia. For imaging of muscle magnetic resonance tomography is the most suitable method particularly to find the correct localization for the biopsy. Generally, a biopsy is indicated for the detection of inflammatory myopathies, although detection of specific antibodies can help to distinguish between different myositis forms. For the diagnosis of hereditary myopathies a biopsy is indicated if the phenotype is not specific and primary molecular genetic testing is difficult. The sample size of the biopsy must be sufficient and the specimen must be properly handled to enable histological
2 600 Leitlinie Myotonie zu identifizieren. Zur Bildgebung des Muskels ist das MRT am besten geeignet. Besonders hilfreich ist das MRT für die Auswahl des richtigen Biopsieorts. Zum Nachweis einer immunogen vermittelten Myopathie ist in der Regel eine Muskelbiopsie indiziert, auch wenn myositisspezifische Antikörperuntersuchungen bei der Zuordnung immer mehr hilfreich sind. Bei Patienten mit hereditären Myopathien ist eine Biopsie indiziert, wenn der klinische Phänotyp nicht eindeutig zugeordnet werden kann und eine primär molekulargenetische Diagnosestellung nicht möglich ist. Die Probe einer Muskelbiopsie muss ausreichend groß sein und sorgfältig aufbereitet werden, sodass nicht nur histologische, sondern auch immunhistologische Untersuchungen erfolgen können, und ggf. auch Westernblot-Analysen sowie enzymatische Messungen. Material sollte auch für die elektronenmikroskopische Untersuchungen und DNA-Analysen asserviert werden. Die Muskelprobe sollte an einem spezialisierten Zentrum untersucht werden. Bei einigen hereditären Myopathien sollte die Diagnosestellung primär über eine molekulargenetische Untersuchung ohne Muskelbiopsie angestrebt werden z. B. Dystrophinopathien, Myotone Dystrophie Typ 1 und 2, okulopharyngeale Muskeldystrophie und fazioskapulohumerale Muskeldystrophie Typ 1 und 2. Neue molekulargenetische Hochdurchsatzverfahren ( next generation sequencing, NGS) ermöglichen eine effiziente Untersuchung vieler Gene in einem Ansatz (Panel-Diagnostik) oder sogar aller Genabschnitte (Exom/Genom). Diese neuen Methoden sind bei in neuromuskulären Zentren ausgewählten Patienten mit gut definiertem Phänotyp sinnvoll, wenn der Phänotyp durch Mutationen in verschiedenen Genen bedingt sein kann, wie z. B. bei einer Muskeldystrophie vom Gliedergürteltyp. Seit sind kleine Gen-Panel-Untersuchungen (bis 25 Kilobasen) Regelleistung der Krankenkassen in Deutschland, umfangreichere NGS- Analysen bedürfen eines Antrags auf Kostenübernahme als Einzelfall. Was gibt es Neues? examinations including immunohistology, and Western blotting. Furthermore, additional specimen for enzyme measurements, electron microscopy and DNA extraction are needed. Analyses of the muscle biopsy should be performed in a specialized laboratory. In several hereditary myopathies diagnosis can be confirmed by molecular testing with dispensation of a biopsy, e. g. dystrophinopathies, myotonic dystrophy type 1 and 2, oculopharyngeal muscular dystrophy, facio-scapulo-humeral muscular dystrophy type 1 and 2. Next generation sequencing enables an efficient investigation of numerous genes in one assay (panel diagnosis) or even all parts of the genome (exome/genome). These novel methods should be used in selected patients examined in centers for neuromuscular disorders that show a defined phenotype that can be caused by mutations in different genes, e.g. limb girdle muscular dystrophy. Since the German insurance companies pay for small panels (maximum 25 kilo bases), cost coverage of more elaborate testing has to be applied for individually. Die Zahl der möglichen Gendefekte ist in den letzten Jahren weiter gestiegen, mittlerweile sind Defekte in über 100 Genen identifiziert worden, die zu Myopathien führen können [1]. Zum Beispiel wurde für die fazioskapulohumerale Muskeldystrophie (FSHD) ein zweiter Gendefekt (SMCHD1) identifiziert, der in Deutschland häufig ist [2]. Neue molekulargenetische Hochdurchsatzverfahren ( next generation sequencing ) ermöglichen die rasche und effiziente Untersuchung vieler Gene in einem Ansatz. Solche Untersuchungen sind bei Patienten mit gut definiertem Phänotyp, die in neuromuskulären Zentren ausgewählt wurden, eine sinnvolle Alternative zu invasiver Diagnostik und wirtschaftlicher als Einzelgensequenzierungen. Sie sollten dann zum Einsatz kommen, wenn der Phänotyp durch Defekte in verschiedenen Genen bedingt sein kann, wie z. B. bei einer Muskeldystrophie vom Gliedergürteltyp [3, 4]. Neue Autoantikörper wurden bei immunvermittelten Muskelerkrankungen identifiziert. Bei Patienten mit nekrotisierender Myopathie wurden Antikörper gegen die HMGCoA-Reduktase nachgewiesen, die teilweise durch eine Statineinnahme induziert werden [5, 6]. Auch bei der Einschlusskörpermyositis wurde 2013 erstmals ein Antikörper identifiziert: Ein Teil der Patienten weisen Antikörper gegen die zytoplasmische 5ʼ-Nukleotidase 1A (CN1A bzw. MUP44) auf. Schließlich wurden bei der Dermatomyositis neue Autoantikörper gefunden, die paraneoplastisch (TIF1 und NPX2) und nicht paraneoplastisch auftreten (SAE) [7]. Die wichtigsten Empfehlungen auf einen Blick Anhand der klinischen Symptomatik (insbesondere Verteilung der Paresen) sollte eine klinische Syndromdiagnose vorgenommen werden: Gliedergürtelsyndrom, distales myopathisches Syndrom, okulopharyngeales Syndrom oder fazioskapulohumeroperoneales Syndrom. Belastungsinduzierte Beschwerden und Myoglobinurie lassen eine metabolische Myopathie vermuten. Eine persistierende Erhöhung der Kreatinkinase (CK) nach körperlicher Schonung ist ein wichtiger Hinweis auf das Vorliegen einer Myopathie. Allerdings schließt ein normaler CK-Wert eine Myopathie nicht aus. Auch bei neurogener Muskelschwäche findet man vielfach eine mäßige CK-Erhöhung, die aber in der Regel nicht mehr als das 10-Fache ausmacht [8]. Bei jedem Patienten mit Verdacht auf eine Myopathie sollte eine EMG-Untersuchung erfolgen, um neurogene von myopathischen Prozessen zu unterscheiden, und um eine Myotonie zu identifizieren. Zur Bildgebung des Muskels ist das MRT am besten geeignet. Besonders hilfreich ist das MRT für die Auswahl des richtigen Biopsieorts.
3 Leitlinie 601 Zum Nachweis einer immunogen vermittelten Myositis ist in der Regel eine Muskelbiopsie indiziert. Bei Patienten mit hereditären Myopathien ist eine Biopsie indiziert, wenn der klinische Phänotyp nicht eindeutig zugeordnet werden kann und eine primär molekulargenetische Diagnosestellung nicht möglich ist. Die Probe einer Muskelbiopsie muss ausreichend groß sein und sorgfältig aufbereitet werden, sodass nicht nur histologische (ggf. auch immunhistologische) Untersuchungen erfolgen können, sondern auch Westernblot-Analysen, enzymatische Messungen, elektronenmikroskopische Untersuchungen und DNA-Analysen. Die Muskelprobe sollte an einem spezialisierten Zentrum untersucht werden. Bei folgenden Myopathien sollte die Diagnosestellung primär über eine molekulargenetische Untersuchung angestrebt werden: Dystrophinopathien, myotone Dystrophie Typ 1 und 2, fazioskapulohumerale Muskeldystrophie Typ 1 und 2, okulopharyngeale Muskeldystrophie, Hauptmann-Thannhauser-Muskeldystrophie und Ionenkanalmyopathien. Einführung Begründung der Notwendigkeit der Leitlinie Die Diagnosestellung von Myopathien ist aufgrund der klinischen und genetischen Heterogenität bei manchen Patienten schwierig. Die klinische Untersuchung alleine kann zwar vielfach eine Verdachtsdiagnose ermöglichen und die Richtung des weiteren diagnostischen Prozedere vorgeben, eine definitive diagnostische Einordnung gelingt meist aber erst nach Inanspruchnahme verschiedener spezieller Untersuchungsmethoden. Diese werden zum Teil nur in Speziallaboren vorgenommen. Dabei sind molekulargenetische Tests von großer Bedeutung. Eine molekulargenetische Diagnosestellung ist auch für die Familienberatung von Bedeutung. In der Praxis dauert es heute vielfach noch lange, bis die richtige Diagnose gestellt wird. Besonders wichtig ist es, Patienten mit behandelbaren Myopathien zu identifizieren. Eine klare Diagnosestellung ist aber auch hilfreich, um diagnostische Unsicherheit zu beenden und unwirksame nebenwirkungsreiche Therapien abzusetzen (z. B. Immunsuppression bei sekundär entzündlichen Veränderungen bei Muskeldystrophien). Allerdings können bei den erblichen Myopathien auch nach Ausschöpfung aller diagnostischen Möglichkeiten nicht alle Patienten exakt zugeordnet werden. Aufgrund der stetigen Verbesserung der Diagnostik ist bei unklarer Diagnose eine Re-Evaluation im Abstand einiger Jahre sinnvoll. Gerade solch diagnostisch schwierige Patienten sollten in Deutschland in einem der 26 neuromuskulären Zentren, die von der Deutschen Gesellschaft für Muskelkranke (DGM) zertifiziert werden, untersucht werden. Auch in Österreich und der Schweiz gibt es solch spezialisierte Zentren. Tab. 1 Hereditäre und erworbene Myopathien. hereditäre Myopathien progressive Muskeldystrophien kongenitale Myopathien mit Strukturbesonderheiten metabolische Myopathien: Glykogenosen Lipidmyopathien mitochondriale Myopathien Ionenkanalmyopathien Ziele der Leitlinie Die Leitlinie soll helfen, bei Patienten mit Muskelerkrankungen schneller die Diagnose zu stellen und die Zahl der ungeklärten Fälle zu reduzieren. Sie soll helfen, aus einer Muskelbiopsie die maximale diagnostische Ausbeute zu erzielen und unnötige Diagnostik zu vermeiden. Patienten mit behandelbaren Myopathien sollen so schneller einer Therapie zugeführt werden können. Eine klare Zuordnung hereditärer Myopathien ermöglicht eine bessere prognostische Einordnung und bildet die Grundlage für die genetische Familienberatung. Schließlich ist eine exakte Zuordnung von Myopathien auch für die Aufnahme in Patientenregister wichtig, die die Grundlage für zukünftige Therapiestudien sind. Patientenzielgruppe Die Leitlinie gilt primär für Erwachsene. Bei Kindern sind noch andere Aspekte zu berücksichtigen, die in der Leitlinie nicht enthalten sind. Bei Patienten mit Erstmanifestation im Kindesalter, die sich als Erwachsene zu Diagnostik vorstellen, ist die Leitlinie daher nicht umfassend. Versorgungsbereich Ambulante und stationäre Diagnostik. erworbene Myopathien Adressaten Neurologen und andere Ärzte, die in die Diagnostik von Muskelerkrankungen involviert sind. Schlüsselwörter Myopathien (ICD-10 G71, G72 und G73.4-7) Myositiden: immunogen (z. B. Polymyositis, Dermatomyositis, Einschlusskörpermyositis, Overlap-Syndrome) erregerbedingt (z.b. Coxsackie-, Influenza-, Echo-, Epstein-Barr-Viren) toxische Myopathien: medikamentös-toxisch (z.b. Statine, serotonerge Substanzen, Amiodaron) andere exogene Toxine (z. B. Alkohol, Heroin, Kokain) Critical-Illness-Myopathien endokrine Myopathien bei Schilddrüsenfunktionsstörungen (z. B. thyreotoxische Myopathie, hypothyreote Myopathie) bei Nebennierenrindenfunktionsstörungen (z. B. Steroidmyopathie) bei Hyperparathyreoidismus Definition Die Leitlinie gilt in der Diagnostik von hereditären und erworbenen Myopathien (vgl. " Tab. 1). Dies sind Erkrankungen, die primär die Muskulatur betreffen. Neurogene Muskelschwäche und Erkrankungen der neuromuskulären Übertragung (myasthene Erkrankungen) sind nicht eingeschlossen. Anamnese und klinische Untersuchung Eigenanamnese Die bei Muskelkrankheiten oft ganz im Vordergrund stehende Angabe der Muskelschwäche ist ein zunächst vieldeutiges Symptom, das nicht nur durch Myopathien bedingt sein kann, sondern
4 602 Leitlinie Clinical Pathway Diagnostik von Myopathien Basisdiagnostik Anamnese: Lokalisation Muskelschwäche Verlauf: Entstehung/Ausbreitung konkrete Bewegungsbehinderung Muskelschmerz inkl. Belastungsabhängigkeit Braunfärbung des Urins Medikamenteneinnahme (v. a. Statine) endokrine Störungen Familienanamnese körperliche Untersuchung, vor allem: Verteilungstyp Paresen Muskeltrophik Kontrakturen Skelettveränderungen myotone Zeichen Rippling des Muskels Labor: CK TSH ggf. Autoantikörper EMG Neurografie erweiterte Diagnostik (fakultativ) Bildgebung: MRT (CT, Sonografie) kardiale Diagnostik Lungenfunktion Ophthalmologie Endokrinologie Abb.1 Clinical Pathway. Gliedergürtelsyndrom distale Muskelschwäche auch von dissoziativen Störungen bis zu einer sog. Allgemeinsymptomatik bei internistischen Erkrankungen reichen kann. Hinsichtlich der Muskelschwäche sind genaue Angaben über deren Lokalisation, den zeitlichen Verlauf ihrer Entstehung und Ausbreitung (Symptombeginn, attackenartig oder langsam progredient, belastungsinduziert) ihr Ausmaß (praktische Beispiele für die konkrete Bewegungsbehinderung) der Grundstein für die richtige Diagnose. Dabei ist es auch wichtig, motorische Meilensteine in der kindlichen Entwicklung (z. B. das Alter, in dem das Gehen gelernt wurde) zu erfragen. Das Symptom Muskelschmerz bedarf einer eingehenden anamnestischen Eingrenzung. Nur der muskelkaterähnliche, tief im Inneren der großen Extremitätenmuskeln empfundene Schmerz kann als Charakteristikum einer Myopathie gelten. Schmerzhafte Muskelverspannungen mit sog. Triggerpoints beim myofaszialen Schmerzsyndrom sind abzugrenzen von Muskelschmerzen bei Myopathien (siehe auch Leitlinie Diagnostik und Differenzialdiagnose bei Myalgie ). Verlaufsbesonderheiten des Muskelschmerzes, vor allem die Frage seiner Abhängigkeit von Muskelarbeit, sind zu analysieren. Weiterhin ist nach Faszikulationen und nach Muskelkrämpfen zu fragen. Auch die Frage nach Braunverfärbung des Urins als Hinweis auf eine Myoglobinurie ist wichtig. Die Anamnese muss gezielte Fragen hinsichtlich der Möglichkeit von exogen-toxischen oder medikamentös (insbesondere Statine) bedingten Myopathien umfassen. Ebenso sind mögliche endokrine Störungen zu beachten ( " Abb.1). Myotonie (klinisch/emg) keine Myotonie (klinisch/emg) Myotonie (klinisch/emg) keine Myotonie (klinisch/emg) okulopharyngeales Syndrom/externe Ophthalmoplegie fazioskapulohumeroperoneales Syndrom Rhabdomyolyse-Attacken Myalgien/Krampi Myotonie/periodische Paralysen asymptomatische Hyper-CK-Ämie V. a. Gliedergürteldystrophie alle anderen Molekulargenetik myotone Dystrophie Typ 2 weiter s. LL Myotone Dystrophien, nicht dystrophe Myotonien und periodische Lähmungen Molekulargenetik: MLPA-Dystrophin-Gen ggf. Sequenzierung Dystrophin-Gen und LGMD-Gene kardiale Diagnostik kardiale Diagnostik bei Myositis weiter s. LL Myositiden Molekulargenetik myotone Dystrophie Typ 1 weiter s. LL Myotone Dystrophien, nicht dystrophe Myotonien und periodische Lähmungen Molekulargenetik OPMD Molekulargenetik FSHD Unterarmbelastungstest Acyl-Carnitin-Spektrum siehe LL Diagnostik und Differenzialdiagnose bei Myalgien Untersuchung Ionenkanalgene weiter s. LL Myotone Dystrophien, nicht dystrophe Myotonien und periodische Lähmungen MRT Muskeln oder Verlaufskontrolle einer Konsanguinität der Eltern wichtig. Da Muskelerkrankungen ein sehr variantenreiches Erscheinungsbild zeigen können, sollte man nach subtilen Symptomen fragen und ggf. erreichbare Familienangehörige selbst untersuchen und die CK bestimmen [9]. Klinische Untersuchung Muskelschwäche Die Lokalisation von Paresen hilft bei den differenzialdiagnostischen Überlegungen. Bei Myopathien sind an den Extremitäten in der Mehrzahl der Fälle die proximalen Muskeln deutlicher betroffen als die distalen Muskeln. Leichte Paresen lassen sich bei funktionellen Untersuchungen (z. B. Kniebeuge, auf einen Stuhl steigen, Hacken-/Zehengang) erkennen. Es können aber auch andere Muskel betroffen sein: mimische Muskulatur (Facies myopathica), extraokuläre Muskeln (Ptosis, Einschränkung der Bulbusmotilität) oropharyngeale Muskulatur (Dysphagie und Dysarthrie) axiale Muskulatur (Scapula alata, Hyperlordose und Skoliose) Atemmuskulatur (Hypoventilation) Abhängig von der Verteilung der Muskelschwäche lassen sich klinische Syndrome differenzieren, z. B. Gliedergürtelsyndrom, distales myopathisches Syndrom, okulopharyngeales Syndrom oder fazioskapulohumeroperoneales Syndrom (vgl. " Abb.1). Andere Manifestationen einer Myopathie können sein: Rhabdomyolyse- Attacken, belastungsinduzierte Myalgien, isolierte Myotonie oder periodische Paralysen. Manchmal fällt auch eine asymptomatische Hyper-CK-Ämie auf. Familienanamnese Eine große Zahl von Muskelerkrankungen ist hereditär, sodass der Familienanamnese besondere Bedeutung zukommt. Bei autosomal-rezessiv vererbten Erkrankungen ist die Frage nach Muskeltrophik Differenzialdiagnostische Bedeutung kommt der Frage zu, ob klinisch schwache Muskeln auch atrophisch sind. Hier muss allerdings einschränkend bedacht werden, dass subkutanes Fettge-
5 Leitlinie 603 chung einer Muskelbiopsie eine Myopathie. Andere muskelspezifische Serumparameter können ergänzend sinnvoll sein. TSH und ggf. Kortisol sowie die Elektrolyte (Natrium, Kalium, Kalzium und Phosphat) sollten zur Frage einer endokrinen Myopathie untersucht werden. Die Untersuchung von myositisspezifischen Autoantikörpern kann helfen, die Myositis näher zuzuordnen, was für das Management der Patienten wichtig ist. Organmanifestation, paraneoplastisches Auftreten und Therapieansprechen werden vom Antikörperstatus beeinflusst. Daher ist es insbesondere bei einer histologisch nachgewiesenen Myositis hilfreich zu wissen, welcher Antikörper vorliegt. Das Fehlen von Antikörpern schließt eine Myositis keineswegs aus. Als Suchtest bei unklarer Myopathie sind Antikörperbestimmungen nicht sinnvoll. Besonders ein allgemeines Screening auf antinukleäre Antikörper (ANA) liefert auch unspezifische Befunde und beweist keine Myositis. Nur wenn eine Differenzierung der ANA gelingt, hat es diagnostische Relevanz. Bei der Dermatomyositis können Antikörper gefunden werden, die nicht mit einer Tumorerkrankung einhergehen (Mi-2, SAE) während andere Antikörper häufig paraneoplastisch auftreten (TIF1, NXP2). Auch bei der Einschlusskörpermyositis wurde jetzt ein Antikörper identifiziert, gegen die zytoplasmische 5ʼ-Nukleotidase 1A (CN1A bzw. MUP44), der bei einem Teil der Patienten nachwiesen werden kann. Bei einer Myositis im Rahmen eines Overlap-Syndroms finden sich häufig Antikörper gegen Aminoacyl-tRNA-Synthetasen (insbesondere Jo-1-AK). Weitere myositisassoziierte Antikörper sind PM-Scl-AK und Ku-AK bei Sklerodermie oder U1/2/3-RNP-AK bei Mischkollagenose [7], vgl. auch Leitlinie Myositissyndrome. Bei Patienten mit akut aufgetretener Muskelschwäche und sehr deutlicher CK-Erhöhung sollten Antikörper gegen das Signal-Recognition-Particle (SRP) untersucht werden, die sich bei nekrookulobulbäres Syndrom Gliedergürtelsyndrom Abb.2 Klinische Syndrome der Myopathien (Quelle: [10]). webe sichtbare Atrophien kaschieren kann. Dabei kann aber eine Palpation helfen. Bei manchen Patienten wird auch eine Hypertrophie (Myotonien) oder eine Pseudohypertrophie (Muskeldystrophien) beobachtet. Andere klinische Zeichen Kontrakturen und Skelettveränderungen myotone Phänomene (Greif-, Augenschluss- oder Perkussionsmyotonie) Rippling des Muskels (Muskelwogen) distal myopathisches Syndrom fazioskapulohumeroperoneales Syndrom Zusatzdiagnostik Labordiagnostik Die Bestimmung der Kreatinkinase (CK) erlaubt einen einfachen und schnellen Überblick über das Ausmaß des Muskelfaseruntergangs, sie gibt aber keinen Hinweis auf den Grund des Zelluntergangs und damit auf die zugrunde liegende Erkrankung. Als Grundregel gilt: Die CK-Erhöhung sollte mindestens einmal bestätigt werden, wobei auf körperliche Schonung vor der Untersuchung geachtet werden muss. Im Allgemeinen gilt die Faustregel, dass eine mehr als 10-fache CK-Erhöhung stark auf eine primär myogene Ursache hindeutet und nicht neurogen bedingt ist [8]. Das Ausmaß der CK-Erhöhung ist bei den verschiedenen Myopathien sehr unterschiedlich ( " Tab.2a u. " Tab. 2b) und auch bei einer definierten Myopathie variabel. Wichtig ist, dass bei manchen Myopathien die CK normal sein kann. Eine falsch positive CK-Erhöhung misst man bei Vorliegen einer Makro-CK: dann ist in der Regel auch die CK-MB erhöht. Es gibt aber auch Patienten mit einer asymptomatischen Hyper-CK-Ämie, der eine (noch) nicht manifeste Myopathie zugrunde liegt. Je höher die CK und je jünger der Patient ist, desto häufiger findet sich bei Untersu-
6 604 Leitlinie Tab. 2a 1. Hilfen zur diagnostischen Zuordnung wichtiger Formen hereditärer und erworbener Myopathien. Fett gedruckt sind die wegweisenden Befunde, Teil Untersuchung Muskeldystrophie Muskelystrophie fazioskapulohume- myotone Dystro- okulopharyngeale distale Myopathie Typ Duchenne/ Gliedergürteltyp rale Muskeldystro- phie Typ 1/2 Muskeldystrophie Becker (LGMD) phie (FSHD) (OPDM) CK +++ (im späten Krankheitsstadium +möglich) andere Laboruntersuchungen Muskelbiopsie nur zur Differenzialdiagnose Molekulargenetik bei negativer MLPA- Genetik: Immunhistologie Western-Blot MLPA Dystrophin-Gen zum Nachweis von Deletionen/ Duplikationen Sequenzierung zum Nachweis von Punktmutationen ++/+++ + normal/+ + +/++/+++ Immunhistologie Western-Blot (v. a. Calpain 3) nur zur Differenzialdiagnose verkürzter Tandem-Repeat-Abschnitt D4Z4 auf Chromosom 4q Gamma GT Glukose nur zur Differenzialdiagnose Typ 1: CTG-Repeat- Expansion DMPG-Gen Typ 2: CCTG-Repeat- Expansion Zinkfinger-Gen 9 GCG/GCA-Repeat- Expansion PABPN1-Gen +=gering erhöht (1- bis 3-fach), ++=mäßig erhöht (3- bis 10-fach), +++=deutlich erhöht (mehr als 10-fach), CK=Kreatinkinase, IBM =Einschlusskörpermyositis Tab. 2b 2. Untersuchung Immunhistologie, Western-Blot Hilfen zur diagnostischen Zuordnung wichtiger Formen hereditärer und erworbener Myopathien. Fett gedruckt sind die wegweisenden Befunde, Teil metabolische Myopathien mitochondriale Myopathien kongenitale Myopathien mit Strukturbesonderheiten Ionenkanalmyopathien toxische/endokrine Myopathie immunogene Myositiden CK normal/+ normal/+ +/++ normal/+ normal/+/ (IBM: CK +/++) Muskelbiopsie Enzymhistologie Elektronenmikroskopie Kalium nur zur Differenzialdiagnose andere Laboruntersuchungen Unterarmbelastungstest Acylcarnitinspektrum im Serum Enzymaktivität im Blut Enzymhistologie Enzymmessung Enzymhistologie (einschl. COX/ SDH) Enzymmessung Molekulargenetik Chlorid-, Natrium-, Kalziumkanalgen (zum Teil nur aus Muskelgewebe möglich) TSH Cortisol Parathormon Fahrradbelastungstest Myositisautoantikörper Immunhistologie Elektronenmikroskopie bei IBM +=gering erhöht (1- bis 3-fach), ++=mäßig erhöht (3- bis 10-fach), +++=deutlich erhöht (mehr als 10-fach), CK =Kreatinkinase, IBM=Einschlusskörpermyositis tisierender Autoimmunmyopathie finden, die relativ schlecht auf Immunsuppression anspricht. Antikörper gegen die HMGCoA- Reduktase führen ebenfalls zu einer nekrotisierenden Myopathie, die teilweise statininduziert auftritt [6]. Nur wenige Enzyme, die im Muskelstoffwechsel eine Rolle spielen, können auch im Blut analysiert werden. Besondere Bedeutung hat die Messung der Alpha-Glukosidase bei Verdacht auf Morbus Pompe, die an Leukozyten, aber auch am Trockenblut vorgenommen werden kann. Die Bestimmung des Acyl-Carnitin-Spektrums im Serum kann bei einer Lipidmyopathie diagnostisch wertvoll sein. Die Untersuchung des Muskels unter Belastungsbedingungen erfolgt mithilfe des Unterarmbelastungstests zur Frage nach einer Glykogenose (fehlender Laktatanstieg bei normalem Ammoniakanstieg) oder eines Myoadenylatdeaminasemangel (fehlender Ammoniakanstieg bei normalem Laktatanstieg). Beim Ergometertest weist ein pathologisch hoher Laktatanstieg auf einen Defekt der mitochondrialen Atmungskette hin [11]. Elektromyografie Bei jedem Patienten mit Verdacht auf eine Myopathie sollte eine quantitative EMG-Untersuchung mit Nadelelektroden erfolgen,
7 Leitlinie 605 um neurogene von myopathischen Prozessen zu unterscheiden. Außerdem ist der Nachweis von myotonen Entladungen von großer Bedeutung. Es sollten mehrere Muskeln vorzugsweise an verschiedenen Extremitäten proximal und distal untersucht werden [12]. Aus einem mittels Nadel-EMG untersuchten Muskel sollte in den darauffolgenden Wochen keine Muskelbiopsie entnommen werden, da durch die EMG-Untersuchung auch Muskelfaseruntergänge mit zellulärer Abräumreaktion ausgelöst werden können und dann falsch positiv als Hinweis für eine Myopathie gewertet werden. Auch eine ergänzende Neurografie zur Frage einer Neuropathie ist bei jedem Patienten sinnvoll. Bildgebende Untersuchungen: MRT, CT, Sonografie Die Kernspintomografie ist das wichtigste bildgebende Verfahren bei Muskelkrankheiten. Muskelödem kann am besten in der fettunterdrückten STIR-Sequenz erkannt werden, es findet sich nicht nur bei Myositiden, sondern auch bei Muskeldystrophien. Bei chronischen Muskelerkrankungen kann in der T1-Wichtung der fettige Umbau erkannt werden. Eine Kontrastmittelgabe kann ergänzende Informationen liefern, sie findet sich insbesondere bei Myositiden, manchmal in geringem Ausmaß aber auch bei anderen Muskelerkrankungen. Das MRT ist besonders hilfreich, wenn klinisch die Auswahl des Biopsieortes schwierig ist. Die Biopsie sollte aus einem betroffenen Muskel erfolgen, bei dem aber noch kein vollständiger fettiger Umbau erfolgt ist. Weiterhin kann durch das MRT das Verteilungsmuster von Myopathien gut erfasst werden, was zur Eingrenzung mancher hereditärer Myopathien zusätzliche Informationen liefern kann. Eine CT kann Verkalkungen im Muskel nachweisen und bei Patienten mit Herzschrittmachern zum Einsatz kommen. Sonografisch kann man Muskelatrophien bzw. -hypertrophien erkennen. Durch Fetteinlagerung kann die Echogenität erhöht und durch Ödem vermindert sein [13]. Kardiale Diagnostik Zur Frage einer kardialen Mitbeteilung sollten EKG (Reizleitungsstörung), LZ-EKG (Rhythmusstörungen) und ein Herzecho (Kardiomyopathie) erfolgen. Optional ist eine MRT zum sensitiveren Nachweis einer Kardiomyopathie [14]. Pulmonale Untersuchungen Die Bestimmung der Vitalkapazität kann einen Hinweis auf eine Atemmuskelschwäche ergeben. Zur Frage einer Zwerchfellschwäche sollte sie nicht nur im Sitzen, sondern auch im Liegen gemessen werden. Bei Patienten mit Myositis ist zur Frage einer Lungenbeteiligung eine Schnittbilddiagnostik indiziert. Untersuchungen zur Frage Multisystembeteiligung Bei bestimmten Myopathien sind sinnvoll: ophthalmologische Untersuchung zur Frage Katarakt oder Retinopathie, endokrine Untersuchungen u. a. zur Frage Diabetes, Hypogonadismus, Hypothyreose, Schädel-MRT zur Frage zerebrale Mitbeteiligung. Muskelbiopsie Einige hereditäre Myopathien lassen sich primär molekulargenetisch diagnostizieren (vgl. S. 12), sodass in diesen Fällen auf eine Muskelbiopsie verzichtet werden kann. Bei den anderen Muskelerkrankungen nimmt die Biopsie eine zentrale Rolle in der Diagnostik ein. Sie ermöglicht breite differenzialdiagnostische Untersuchungen verschiedener Myopathien mit unterschiedlichen Methoden. Die Biopsie sollte möglichst nicht unter immunsuppressiver Medikation erfolgen. Nach einer Rhabdomyolyse sollte einige Wochen bis zur Muskelbiopsie gewartet werden. Zur Indikation der Muskelbiopsie bei Patienten, die keine Paresen aufweisen, sondern unter Myalgien leiden, wird auf die Leitlinie Diagnostik und Differenzialdiagnose bei Myalgien verwiesen. Als Biopsieort eignet sich prinzipiell ein moderat betroffener Muskel (Paresegrad 4/5). Die Biopsie muss ausreichend groß sein und wird daher in der Regel als offene Biopsie (bei Erwachsenen in der Regel in Lokalanästhesie) entnommen. Der Transport aus dem OP erfolgt in einer feuchten Kammer (auf einem mit Kochsalzlösung angefeuchteten Stück Gaze in einer verschlossenen Petri-Schale) [15]. Wenn der Transport mehrere Stunden dauert, sollte die Petrischale auf Eis transportiert werden (allerdings können dann biochemische Analysen verfälscht werden). Ein Anfrieren des Präparates muss unbedingt vermieden werden. Die Probe muss in Laboren, die eine Expertise zur Untersuchung von Muskelbiopsien aufweisen, sorgfältig aufbereitet werden, sodass nicht nur histologische Untersuchungen erfolgen können, sondern auch Westernblot-Analysen, enzymatische Messungen, elektronenmikroskopische Untersuchungen und DNA-Extraktion. Die Probe sollte langfristig asserviert werden, um eine spätere Re-Evaluierung zu ermöglichen. Die Probe wird in 3 Teile geteilt, die unterschiedlich behandelt werden: Aufblocken eines Gewebsstücks und Schockgefrieren in stickstoffgekühltem Isopentan für histologische Untersuchungen Tieffrieren eines unfixierten Muskelstückchens in flüssigem Stickstoff für biochemische Untersuchungen und DNA-Extraktion Fixation in Glutaraldehyd für Semidünnschnitte/Elektronenmikroskopie Das Risiko von Komplikationen (Nachblutungen, Wundinfektionen) ist bei einer Muskelbiopsie sehr niedrig. Myopathologische Untersuchung In einem ersten Schritt kann die histologische Beurteilung der Muskelbiopsie unterscheiden, ob ein myositisches, myopathisches oder neurogenes Gewebssyndrom vorliegt und ob es Hinweise auf eine metabolische Myopathie bzw. Myopathie mit charakteristischen Strukturveränderungen gibt. Bei Nachweis von Entzündungszellen sollten diese immunhistologisch differenziert werden. Besteht der Verdacht auf eine Muskeldystrophie, so sollte ein Defekt von Muskelproteinen immunhistologisch analysiert werden [16]. Elektronenmikroskopische Untersuchungen sind zum Nachweis tubulofilamentöser Einschlüsse bei der Einschlusskörpermyositis und zur Analyse von charakteristischen Strukturveränderungen u.a. bei kongenitalen Myopathien hilfreich [17]. Westernblot Mittels Westernblot lässt sich bei vielen Muskeldystrophien entweder ein fehlendes Protein oder ein im elektrophoretischen Laufverhalten verändertes Protein nachweisen. Dieses Verfahren ist besonders wichtig, wenn eine immunhistologische Untersuchung nicht möglich ist, wie z. B. bei Calpain-3 [16]. Biochemische Untersuchung Manche Enzymdefekte sind auf den Muskel beschränkt und daher auch nur im Muskel biochemisch nachweisbar. Dazu gehören Glykogenosen, aber auch mitochondriale Myopathien [11].
8 606 Leitlinie Molekulargenetische Untersuchung Einsendungen zur molekulargenetischen Diagnostik mit einem differenzialdiagnostisch weit gestreuten Suchauftrag sind nicht sinnvoll. Der Verdacht auf das Vorliegen einer definierten Entität muss gegeben sein. Die häufigste Ursache einer Muskeldystrophie vom Gliedergürteltyp ist eine Dystrophinopathie, der meist Deletionen oder Duplikationen im Dystrophin-Gen zugrunde liegen. Diese können mittels Multiplex-Ligation-Probe-Amplifikation (MLPA) auch bei Konduktorinnen sicher und relativ einfach nachgewiesen werden. Daher sollte eine MLPA-Analyse vor einer Biopsie erfolgen, wenn eine Dystrophinopathie differenzialdiagnostisch infrage kommt. Bei einigen anderen hereditären Myopathien kann aufgrund charakteristischer Phänotypen und einer positiven Familienanamnese bereits eine klinische Verdachtsdiagnose gestellt werden, die direkt durch eine molekulargenetische Analyse bestätigt werden kann. Die molekulargenetische Untersuchung ist dann Methode der ersten Wahl, zumal myohistologisch bei diesen Erkrankungen z.t. keine hochspezifischen Veränderungen zu finden sind. Dies gilt für die myotone Dystrophie Typ 1 und 2 sowie die FSHD Typ 1 und 2, die okulopharyngeale Muskeldystrophie und die Muskeldystrophie Hauptmann-Thannhauser (Lamin-A/C-Defekt), die alle autosomal-dominant vererbt werden [18]. Auch bei Muskelerkrankungen auf der Basis von Ionenkanaldefekten ist eine primäre molekulargenetische Diagnostik sinnvoll (vgl. Leitlininien Myotone Dystrophien, nichtdystrophe Myotonien und periodische Lähmungen ). Neue molekulargenetische Hochdurchsatzverfahren ( next generation sequencing ) ermöglichen die rasche und effiziente Untersuchung vieler Gene in einem Ansatz (Panel-Diagnostik). Es besteht auch die Möglichkeit der Untersuchung aller kodierenden Genabschnitte (Exom), derzeit aber nur im Rahmen wissenschaftlicher Untersuchungen. Manche Genveränderungen (z. B. Repeat-Erkrankungen wie die myotone Dystrophie Typ 1 und 2 sowie die Genexpansion D4Z4 der FSHD1) können aber methodisch bedingt nicht erkannt werden. Diese neuen Methoden sind bei in neuromuskulären Zentren ausgewählten Patienten mit gut definiertem Phänotyp eine sinnvolle Alternative zu invasiver Diagnostik und wirtschaftlicher als Einzelgensequenzierungen. Sie sollten dann zum Einsatz kommen, wenn der Phänotyp durch Defekte in verschiedenen Genen bedingt sein kann, wie z.b. bei einer Muskeldystrophie vom Gliedergürteltyp [3, 4]. Seit sind kleine Gen-Panel- Untersuchungen (bis 25 Kilobasen) Regelleistung der Krankenkassen in Deutschland, umfangreichere NGS-Analysen bedürfen eines Antrags auf Kostenübernahme als Einzelfall. Untersuchungsmaterial ist in der Regel EDTA-Blut, bei mitochondrialen Myopathien können Defekte der mitochondrialen DNA jedoch einer Blutuntersuchung entgehen, daher sollte bevorzugt Muskel-DNA analysiert werden (vgl. Leitlinie Mitochondriopathien). Versorgungskoordination Erste diagnostische Schritte (körperliche Untersuchung und CK- Bestimmung) können vom Hausarzt vorgenommen werden. Zur weiteren Diagnostik ist in der Regel eine Überweisung zum Neurologen notwendig. Besonders diagnostisch schwierige Patienten sollten in Neurologischen Kliniken an einem neuromuskulären Zentrum vorgestellt werden. Dort sollte die spezielle Diagnostik (einschließlich einer eventuell notwendigen Muskelbiopsie) erfolgen. Abhängig von der Komplexität der Diagnostik und bei akuten Fällen ist eine stationäre Untersuchung sinnvoll. Bei hereditären Muskelerkrankungen ist eine Vorstellung beim Facharzt für Humangenetik zu empfehlen. Um die Koordination der Beteiligten zu erleichtern, ist es sinnvoll, auch dem Patienten selbst die relevanten medizinischen Dokumente zur Verfügung zu stellen. Selbsthilfegruppe Deutsche Gesellschaft für Muskelkranke e.v. (DGM): Redaktionskomitee Prof. Dr. med. Marcus Deschauer, Klinik und Poliklinik für Neurologie, Technische Universität München Horst Ganter, Geschäftsführer der Deutschen Gesellschaft für Muskelkranke e.v. (DGM) als Patientenvertreter Prof. Dr. rer. nat. Clemens R. Müller-Reible, Institut für Humangenetik Universität Würzburg als Vertreter der Deutschen Gesellschaft für Humangenetik Prof. Dr. med. Kai M. Rösler, Neurologische Universitätsklinik, Inselspital Bern Prof. Dr. med. Benedikt Schoser, Friedrich-Baur-Institut, Neurologische Klinik und Poliklinik, Ludwig-Maximilians-Universität München Priv.-Doz. Dr. med. Julia Wanschitz, Neurologische Universitätsklinik Innsbruck Prof. Dr. med. Joachim Weis, Institut für Neuropathologie, Universitätsklinikum der RWTH Aachen als Vertreter der Deutschen Gesellschaft für Neuropathologie und Neuroanatomie (DGNN) und Leiter des Referenzzentrums für neuromuskuläre Erkrankungen Prof. Dr. med. Stephan Zierz, Klinik und Poliklinik für Neurologie, Martin-Luther-Universität Halle-Wittenberg Federführend: Prof. Dr. med. Marcus Deschauer, Klinik und Poliklinik für Neurologie, Klinikum rechts der Isar, Technische Universität München, Ismaninger Str. 22, München, marcus.deschauer@ tum.de Entwicklungsstufe der Leitlinie: S1 Finanzierung der Leitlinie Die Autoren haben die Leitlinie ehrenamtlich ohne Inanspruchnahme einer externen Finanzierung erstellt. Methodik der Leitlinienentwicklung Zusammensetzung der Leitliniengruppe, Beteiligung der Interessengruppen Einsetzung eines Autorengremiums durch die Kommission Leitlinien der DGN mit Neurologen, die auf dem Gebiet der Muskelerkrankungen eine besondere Expertise aufweisen (einschließlich je eines Vertreters der Österreichischen Gesellschaft für Neurologie und der Schweizerischen Neurologischen Gesellschaft)
9 Leitlinie 607 und mit einem Vertreter der Deutschen Gesellschaft für Neuropathologie und Neuroanatomie sowie der Deutschen Gesellschaft für Humangenetik. Außerdem wurde die Selbsthilfeorganisation Deutsche Gesellschaft für Muskelkranke e.v. beteiligt. Recherche und Auswahl wissenschaftlicher Belege Bezugnahme auf die bestehende Leitlinie und auf die Leitlinie der European Federation of Neurological Societies zum Thema Diagnosis and management of limb girdle muscular dystrophies [19] sowie systematische Literaturrecherche mittels des elektronischen Datenbanksystems PubMed. Verfahren zur Konsensfindung Diese Leitlinie ist von der Kommission Leitlinien der Deutschen Gesellschaft für Neurologie (DGN) sowie den am Konsensusprozess beteiligten Fachgesellschaften verabschiedet worden. Die Konsensusfindung erfolgte aufgrund einer Konsensuskonferenz am in München auf dem Kongress der Deutschen Gesellschaft für Neurologie sowie weiterer -Korrespondenz der Autoren. Vollständig überarbeitet: 15. März 2016 Online auf seit: 5. Juli 2016 Gültig bis: 14. März 2020 Kapitel: Erkrankungen der Muskulatur lt. Leitlinien für Diagnostik und Therapie in der Neurologie Zitierhinweis Deschauer M. et al. S1-Leitlinie Diagnostik von Myopathien In: Deutsche Gesellschaft für Neurologie, Hrsg. Leitlinien für Diagnostik und Therapie in der Neurologie. Online: (abgerufen am TT.MM.JJJJ) Anhang Wichtige Links Acknowledgement Frau Prof. Dr. med. Schara, leitende Ärztin Bereich Neuropädiatrie am Universitätsklinikum Essen, wird für hilfreiche Anmerkungen aus neuropadiätrischer Sicht gedankt. Abkürzungen ANA antinukleäre Antikörper CK Kreatinkinase CN zytoplasmische 5ʼ-Nukleotidase EDTA Ethylendiamintetraacetat FSHD fazioskapulohumerale Muskeldystrophie HMGCoA 3-Hydroxy-3-Methylglutaryl-Coenzym-A-Reduktase MLPA Multiplex-Ligation-Probe-Amplifikation NGS Next Generation Sequencing SRP Signal-Recognition-Particle STIR Short Tau Inversion Recovery Interessenkonflikt Siehe Interessenkonflikterklärung auf Institute 1 Klinik und Poliklinik für Neurologie, Technische Universität München 2 Institut für Humangenetik, Universität Würzburg 3 Neurologische Universitätsklinik, Inselspital Bern 4 Friedrich-Baur-Institut, Neurologische Klinik und Poliklinik, Ludwig-Maximilians-Universität München 5 Neurologische Universitätsklinik Innsbruck 6 Institut für Neuropathologie, Universitätsklinikum der RWTH Aachen 7 Klinik und Poliklinik für Neurologie, Martin-Luther-Universität Halle-Wittenberg Literatur 1 Kaplan JC, Hamroun D. The 2016 version of the gene table of monogenic neuromuscular disorders (nuclear genome). Neuromuscul Disord 2015; 25: Larsen M, Rost S, El Hajj N et al. Diagnostic approach for FSHD revisited: SMCHD1 mutations cause FSHD2 and act as modifiers of disease severity in FSHD1. Eur J Hum Genet 2015; 23: Ankala A, da Silva C, Gualandi F et al. A comprehensive genomic approach for neuromuscular diseases gives a high diagnostic yield. Ann Neurol 2015; 77: Kuhn M, Glaser D, Joshi PR et al. Utility of a next-generation sequencing-based gene panel investigation in German patients with genetically unclassified limb-girdle muscular dystrophy. J Neurol 2016; 263: Allenbach Y, Drouot L, Rigolet A et al. Anti-HMGCR autoantibodies in European patients with autoimmune necrotizing myopathies: inconstant exposure to statin. Medicine (Baltimore) 2014; 93: Mammen AL, Chung T, Christopher-Stine L et al. Autoantibodies against 3-hydroxy-3-methylglutaryl-coenzyme A reductase in patients with statin-associated autoimmune myopathy. Arthritis Rheum 2011; 63: Gunawardena H. The clinical features of myositis-associated autoantibodies: a review. Clin Rev Allergy Immunol 2015; DOI: / s Chahin N, Sorenson EJ. Serum creatine kinase levels in spinobulbar muscular atrophy and amyotrophic lateral sclerosis. Muscle Nerve 2009; 40: Zierz S. Muskelerkrankungen. Stuttgart: Thieme; Schoser B. Klinische Phänotypen hereditärer Myopathien und die Indikation zur Muskelbiopsie. Akt Neurol 2009; 36: Vorgerd M. Labordiagnostik von Myopathien. Akt Neurol 2009; 36: Reiners K. Elektromyografische Untersuchung bei Myopathien. Akt Neurol 2009; 36: Wessig C. Bildgebung bei Myopathien. Akt Neurol 2009; 36: Gaul C, Deschauer M, Tempelmann C et al. Cardiac involvement in limbgirdle muscular dystrophy 2I: conventional cardiac diagnostic and cardiovascular magnetic resonance. J Neurol 2006; 253: Bergmann M, Weis J, Probst-Cousin S. Muscle biopsy. Der Pathologe 2009; 30: Bushby K. Diagnosis and management of the limb girdle muscular dystrophies. Pract Neurol 2009; 9: Karpati G, Hilton-Jones D, Bushby K, Griggs RC, eds. Disorders of voluntary muscle. Cambridge: Cambridge University Press; Müller-Reible CR, Kress W, Meng C. Molekulargenetische Diagnostik der Myopathien. Akt Neurol 2009; 36: Norwood F, de Visser M, Eymard B et al. EFNS Guideline Task Force. EFNS guideline on diagnosis and management of limb girdle muscular dystrophies. Eur J Neurol 2007; 14:
Diagnostik von Myopathien
 AWMF-Registernummer: 030/115 Leitlinien für Diagnostik und Therapie in der Neurologie Diagnostik von Myopathien [ Deutschen Entwicklungsstufe: S1 Federführend: Prof. Dr. M. Deschauer Herausgegeben von
AWMF-Registernummer: 030/115 Leitlinien für Diagnostik und Therapie in der Neurologie Diagnostik von Myopathien [ Deutschen Entwicklungsstufe: S1 Federführend: Prof. Dr. M. Deschauer Herausgegeben von
Neuromuskuläre Erkrankungen
 Klinische Neurologie Neuromuskuläre Erkrankungen Bearbeitet von Jörn P Sieb, Bertold Schrank 1. Auflage 2009. Taschenbuch. 332 S. Paperback ISBN 978 3 17 018381 0 Format (B x L): 13,5 x 23,5 cm Gewicht:
Klinische Neurologie Neuromuskuläre Erkrankungen Bearbeitet von Jörn P Sieb, Bertold Schrank 1. Auflage 2009. Taschenbuch. 332 S. Paperback ISBN 978 3 17 018381 0 Format (B x L): 13,5 x 23,5 cm Gewicht:
Muskel- und Nervenerkrankungen
 WS 2016/17 Vorlesung Neuropathologie Muskel- und Nervenerkrankungen Tanja Kuhlmann Institut für Neuropathologie Klinische Symptomatik Muskelschwäche Muskelatrophie (Pseudo-)Muskelhypertrophie Schmerzen/Mißempfindungen
WS 2016/17 Vorlesung Neuropathologie Muskel- und Nervenerkrankungen Tanja Kuhlmann Institut für Neuropathologie Klinische Symptomatik Muskelschwäche Muskelatrophie (Pseudo-)Muskelhypertrophie Schmerzen/Mißempfindungen
Archiv - alte Auflage. Diagnostik von Myopathien. Was gibt es Neues? Die wichtigsten Empfehlungen auf einen Blick
 Diagnostik von Myopathien Was gibt es Neues? Die Möglichkeiten der molekularen Diagnostik zeigen, dass bisher phänotypisch scheinbar umschriebene Myopathien durchaus ein sehr viel breiteres klinisches
Diagnostik von Myopathien Was gibt es Neues? Die Möglichkeiten der molekularen Diagnostik zeigen, dass bisher phänotypisch scheinbar umschriebene Myopathien durchaus ein sehr viel breiteres klinisches
Pongratz Atlas der Muskelkrankheiten
 Pongratz Atlas der Muskelkrankheiten von D.E. Pongratz, CD. Reimers, D. Hahn, M. Nagele und W. Müller-Felber unter Mitarbeit von G. Hübner mit einem Vorwort von J. Lissner 411 Abbildungen und 20 Tabellen
Pongratz Atlas der Muskelkrankheiten von D.E. Pongratz, CD. Reimers, D. Hahn, M. Nagele und W. Müller-Felber unter Mitarbeit von G. Hübner mit einem Vorwort von J. Lissner 411 Abbildungen und 20 Tabellen
Klinische Neurologie. Herausgegeben von Thomas Brandt, Reinhard Hohlfeld, Johannes Noth und Heinz Reichmann
 Klinische Neurologie Herausgegeben von Thomas Brandt, Reinhard Hohlfeld, Johannes Noth und Heinz Reichmann Jörn P. Sieb Bertold Schrank Neuromuskuläre Erkrankungen Verlag W. Kohlhammer Dieses Werk einschließlich
Klinische Neurologie Herausgegeben von Thomas Brandt, Reinhard Hohlfeld, Johannes Noth und Heinz Reichmann Jörn P. Sieb Bertold Schrank Neuromuskuläre Erkrankungen Verlag W. Kohlhammer Dieses Werk einschließlich
Kongenitale Myopathien
 Kongenitale Myopathien Karin Jurkat-Rott, Herbert Schreiber, Hans H. Goebel, Frank Lehmann-Horn, 2005 Historie Seit der Einführung der Elektronenmikroskopie und Enzymhistochemie in die Diagnostik neuromuskulärer
Kongenitale Myopathien Karin Jurkat-Rott, Herbert Schreiber, Hans H. Goebel, Frank Lehmann-Horn, 2005 Historie Seit der Einführung der Elektronenmikroskopie und Enzymhistochemie in die Diagnostik neuromuskulärer
Diagnostik bei neuromuskulären Erkrankungen
 Diagnostik bei neuromuskulären Erkrankungen Neue Methoden der Genetik 7. DGM Fach- und Informationstag für Muskelkranke 2014 1. Juni 2014 Dr. Sabine Uhrig AGENDA 2 Menschliche Muskulatur 656 Muskeln 30-50%
Diagnostik bei neuromuskulären Erkrankungen Neue Methoden der Genetik 7. DGM Fach- und Informationstag für Muskelkranke 2014 1. Juni 2014 Dr. Sabine Uhrig AGENDA 2 Menschliche Muskulatur 656 Muskeln 30-50%
FAZIOSKAPULO- HUMERALE MUSKEL- DYSTROPHIE
 DGM INFO FAZIOSKAPULO- HUMERALE MUSKEL- DYSTROPHIE DGM Deutsche Gesellschaft für Muskelkranke e.v. 2 3 Die fazioskapulohumerale Muskeldystrophie (FSHD) Die fazioskapulohumerale Muskeldystrophie (FSHD)
DGM INFO FAZIOSKAPULO- HUMERALE MUSKEL- DYSTROPHIE DGM Deutsche Gesellschaft für Muskelkranke e.v. 2 3 Die fazioskapulohumerale Muskeldystrophie (FSHD) Die fazioskapulohumerale Muskeldystrophie (FSHD)
Neurologische Leitsymptome und diagnostische Entscheidungen
 Neurologische Leitsymptome und diagnostische Entscheidungen von Helmut Buchner 1. Auflage Thieme 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 97 3 13 1433 4 Zu Inhaltsverzeichnis schnell und portofrei
Neurologische Leitsymptome und diagnostische Entscheidungen von Helmut Buchner 1. Auflage Thieme 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 97 3 13 1433 4 Zu Inhaltsverzeichnis schnell und portofrei
Metabolische Myopathien
 Metabolische Myopathien Kurs Muskelerkrankungen: Leitpfade für Diagnostik und Therapie Marcus Deschauer Was sind metabolische Myopathien? Hereditäre Myopathien durch Defekte im Energiestoffwechsel des
Metabolische Myopathien Kurs Muskelerkrankungen: Leitpfade für Diagnostik und Therapie Marcus Deschauer Was sind metabolische Myopathien? Hereditäre Myopathien durch Defekte im Energiestoffwechsel des
Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale Erkrankungen (mitonet)
 Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale Erkrankungen (mitonet) Das wesentliche Ziel des mitonet ist der Aufbau eines deutschlandweiten Netzwerks aus Klinikern
Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale Erkrankungen (mitonet) Das wesentliche Ziel des mitonet ist der Aufbau eines deutschlandweiten Netzwerks aus Klinikern
Myopathie. Bianca Dräger
 Myopathie Bianca Dräger Klinik für Schlafmedizin und neuromuskuläre Erkrankungen Neuromuskuläres Zentrum Münster/Westfalen/Osnabrück Department für Neurologie Westfälische Wilhelms-Universität Münster
Myopathie Bianca Dräger Klinik für Schlafmedizin und neuromuskuläre Erkrankungen Neuromuskuläres Zentrum Münster/Westfalen/Osnabrück Department für Neurologie Westfälische Wilhelms-Universität Münster
Treffen der Kontaktgruppe Neurale Muskelatrophie der DGM e.v. Bad Sooden-Allendorf,
 CAMPUS INNENSTADT : Warum braucht man so was? Treffen der Kontaktgruppe Neurale Muskelatrophie der DGM e.v. Bad Sooden-Allendorf, Dr. med. Olivia Schreiber-Katz, Friedrich-Baur-Institut, München www.cmt-register.de
CAMPUS INNENSTADT : Warum braucht man so was? Treffen der Kontaktgruppe Neurale Muskelatrophie der DGM e.v. Bad Sooden-Allendorf, Dr. med. Olivia Schreiber-Katz, Friedrich-Baur-Institut, München www.cmt-register.de
Das Neuromuskuläre Zentrum Basel Organisation / Angebot
 Das Neuromuskuläre Zentrum Basel Organisation / Angebot Prof. Peter Fuhr Leiter Abt. klin. Neurophysiologie & NMZ Neurologische Klinik USB Epidemiologie Punkt-Prävalenz pro 100'000 Einwohner: Mononeuropathien
Das Neuromuskuläre Zentrum Basel Organisation / Angebot Prof. Peter Fuhr Leiter Abt. klin. Neurophysiologie & NMZ Neurologische Klinik USB Epidemiologie Punkt-Prävalenz pro 100'000 Einwohner: Mononeuropathien
Versorgung von Patienten mit Myalgien und Crampi
 Versorgung von Patienten mit Myalgien und Crampi Prof. Dr. Reinhard Kiefer Neurologische Klinik Neurologische Praxis im MVZ Diakoniekrankenhaus Rotenburg (Wümme) Patienten mit Myalgien - die Herausforderungen
Versorgung von Patienten mit Myalgien und Crampi Prof. Dr. Reinhard Kiefer Neurologische Klinik Neurologische Praxis im MVZ Diakoniekrankenhaus Rotenburg (Wümme) Patienten mit Myalgien - die Herausforderungen
Inhalt. Vorwort Diagnostik peripherer Nervenerkrankungen. 1 Der Patient mit neuropathischen Beschwerden... 15
 Inhalt Vorwort................................................ 11 A Diagnostik peripherer Nervenerkrankungen 1 Der Patient mit neuropathischen Beschwerden............. 15 2 Schlüsselinformationen aus Anamnese
Inhalt Vorwort................................................ 11 A Diagnostik peripherer Nervenerkrankungen 1 Der Patient mit neuropathischen Beschwerden............. 15 2 Schlüsselinformationen aus Anamnese
kontrolliert wurden. Es erfolgte zudem kein Ausschluss einer sekundären Genese der Eisenüberladung. Erhöhte Ferritinkonzentrationen wurden in dieser S
 5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
5.8 Zusammenfassung Auf der Grundlage der dargestellten Ergebnisse dieser Studie erscheint die laborchemische Bestimmung der Transferrinsättigung zur Abklärung einer unklaren Lebererkrankung und Verdacht
Die Myositis-Erkrankungen und ihre Therapie Stand der Forschung. J. Schmidt Göttingen
 Die Myositis-Erkrankungen und ihre Therapie Stand der Forschung J. Schmidt Göttingen Der Muskel Mechanismen der Entzündung: Übersicht Mechanismen der Entzündung: Beispiel Einteilung der Myositiden Dermatomyositis
Die Myositis-Erkrankungen und ihre Therapie Stand der Forschung J. Schmidt Göttingen Der Muskel Mechanismen der Entzündung: Übersicht Mechanismen der Entzündung: Beispiel Einteilung der Myositiden Dermatomyositis
Rationale Diagnostik ik von Autoimmunthyreopathien
 2. Mühldo orfer Schild ddrüs sensym mposium Rationale Diagnostik ik von Autoimmunthyreopathien Dr. Christos Koutsampelas Facharzt für Nuklearmedizin dia.log Diagnostische Radiologie Altötting Nuklearmedizinische
2. Mühldo orfer Schild ddrüs sensym mposium Rationale Diagnostik ik von Autoimmunthyreopathien Dr. Christos Koutsampelas Facharzt für Nuklearmedizin dia.log Diagnostische Radiologie Altötting Nuklearmedizinische
Vom unklaren Symptomkomplex zur ganzheitlichen Diagnose
 Morbus Fabry - Niereninsuffizienz Kardiomyopathie Neurologische Störungen - Vom unklaren Sympto Morbus Fabry Niereninsuffizienz Kardiomyopathie Neurologische Störungen Vom unklaren Symptomkomplex zur ganzheitlichen
Morbus Fabry - Niereninsuffizienz Kardiomyopathie Neurologische Störungen - Vom unklaren Sympto Morbus Fabry Niereninsuffizienz Kardiomyopathie Neurologische Störungen Vom unklaren Symptomkomplex zur ganzheitlichen
Deutsche Gesellschaft für Muskelkranke e.v.
 Deutsche Gesellschaft für Muskelkranke e.v. Herrn Prof. Dr. F.W.Schwartz Vorsitzender des Sachverständigenrates für die Konzertierte Aktion im Gesundheitswesen Bundesministerium für Gesundheit Am Probsthof
Deutsche Gesellschaft für Muskelkranke e.v. Herrn Prof. Dr. F.W.Schwartz Vorsitzender des Sachverständigenrates für die Konzertierte Aktion im Gesundheitswesen Bundesministerium für Gesundheit Am Probsthof
Rumpf- und Atemmuskelschwäche in der Muskelambulanz
 Rumpf- und Atemmuskelschwäche in der Muskelambulanz Deutsche Gesellschaft für Neurologie Mannheim 24.9.2010 Bertold Schrank Deutsche Klinik für Diagnostik Wiesbaden Atemmuskulatur Kehlkopf - Glottisschluss
Rumpf- und Atemmuskelschwäche in der Muskelambulanz Deutsche Gesellschaft für Neurologie Mannheim 24.9.2010 Bertold Schrank Deutsche Klinik für Diagnostik Wiesbaden Atemmuskulatur Kehlkopf - Glottisschluss
Autoantikörper bei idiopathischen Myositiden Karsten Conrad
 Autoantikörper bei idiopathischen Myositiden Karsten Conrad Medizinische Fakultät Carl Gustav Carus Idiopathische Myositiden Dermatomyositis (DM) AAK Polymyositis (PM) Myositis im Rahmen von Overlap-Syndromen
Autoantikörper bei idiopathischen Myositiden Karsten Conrad Medizinische Fakultät Carl Gustav Carus Idiopathische Myositiden Dermatomyositis (DM) AAK Polymyositis (PM) Myositis im Rahmen von Overlap-Syndromen
Klinische Symptomatik kongenitaler Myopathien
 Klinische Symptomatik kongenitaler Myopathien Folie 1 1 Heike Kölbel und Ulrike Schara Neuropädiatrie, Entwicklungsneurologie und Sozialpädiatrie Zentrum für Kinder- und Jugendheilkunde, Universitätsklinikum
Klinische Symptomatik kongenitaler Myopathien Folie 1 1 Heike Kölbel und Ulrike Schara Neuropädiatrie, Entwicklungsneurologie und Sozialpädiatrie Zentrum für Kinder- und Jugendheilkunde, Universitätsklinikum
Medizinische Genetik: Beispiele aus der Praxis
 Medizinische Genetik: Beispiele aus der Praxis SAGB/ASHM Jahrestagung Bern, 14.06.2012 Kontakt: Dr. Bernhard Steiner, Médecin Adjoint, Kinderspital Luzern bernhard.steiner@luks.ch Chinderarztpraxis, Ruopigenring
Medizinische Genetik: Beispiele aus der Praxis SAGB/ASHM Jahrestagung Bern, 14.06.2012 Kontakt: Dr. Bernhard Steiner, Médecin Adjoint, Kinderspital Luzern bernhard.steiner@luks.ch Chinderarztpraxis, Ruopigenring
Befall der Muskulatur beim Jo1- Syndrom: Symptome und diagnostische Wege
 Befall der Muskulatur beim Jo1- Syndrom: Symptome und diagnostische Wege Dr. F. Mühlhauser Facharzt für Neurologie ACURA MVZ Baden-Baden Aufgaben des Neurologen Muskel- oder Nervenerkrankung? Auskunft
Befall der Muskulatur beim Jo1- Syndrom: Symptome und diagnostische Wege Dr. F. Mühlhauser Facharzt für Neurologie ACURA MVZ Baden-Baden Aufgaben des Neurologen Muskel- oder Nervenerkrankung? Auskunft
2 Erkrankungen von Muskel und neuromuskulärer Synapse
 2 Erkrankungen von Muskel und neuromuskulärer Synapse... ÜBERSICHT Hereditäre degenerative Erkrankungen des Skelettmuskels durch molekulargenetisch definierte Gendefekte. Die Kenntnis der verantwortlichen
2 Erkrankungen von Muskel und neuromuskulärer Synapse... ÜBERSICHT Hereditäre degenerative Erkrankungen des Skelettmuskels durch molekulargenetisch definierte Gendefekte. Die Kenntnis der verantwortlichen
Autosomal-rezessiver Erbgang
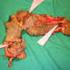 12 Autosomal-rezessiver Erbgang Bearbeitetes Informationsblatt herausgegeben vom Guy s and St. Thomas Hospital, London und dem London IDEAS Genetic Knowledge Park, entsprechend deren Qualitätsstandards.
12 Autosomal-rezessiver Erbgang Bearbeitetes Informationsblatt herausgegeben vom Guy s and St. Thomas Hospital, London und dem London IDEAS Genetic Knowledge Park, entsprechend deren Qualitätsstandards.
Biochemische Labor-Diagnostik der akuten und chronischen Porphyrien
 Biochemische Labor-Diagnostik der akuten und chronischen Porphyrien Dr. Harald Ertl, 5.6.2013 Biochemische Labor-Diagnostik der akuten und chronischen Porphyrien Einleitung Biochemische Parameter - Allgemeines
Biochemische Labor-Diagnostik der akuten und chronischen Porphyrien Dr. Harald Ertl, 5.6.2013 Biochemische Labor-Diagnostik der akuten und chronischen Porphyrien Einleitung Biochemische Parameter - Allgemeines
Wie können wir in Zukunft diese Fragen beantworten?
 Parkinson Krankheit: Diagnose kommt sie zu spät? Prof. Dr. med. Claudia Trenkwalder Mannheim (23. September 2010) - Die Frage, ob derzeit die Diagnosestellung einer Parkinson-Erkrankung zu spät kommt,
Parkinson Krankheit: Diagnose kommt sie zu spät? Prof. Dr. med. Claudia Trenkwalder Mannheim (23. September 2010) - Die Frage, ob derzeit die Diagnosestellung einer Parkinson-Erkrankung zu spät kommt,
Checkliste zur Kausalitätsattribuierung bei vermuteter toxischer Polyneuropathie
 Aus dem Fachbereich Medizin der Johann Wolfgang Goethe-Universität Frankfurt am Main Zentrum für Gesundheitswissenschaften Institut für Arbeitsmedizin, Sozialmedizin und Umweltmedizin Direktor: Prof. Dr.
Aus dem Fachbereich Medizin der Johann Wolfgang Goethe-Universität Frankfurt am Main Zentrum für Gesundheitswissenschaften Institut für Arbeitsmedizin, Sozialmedizin und Umweltmedizin Direktor: Prof. Dr.
Entwicklungsstörungen und Intelligenzdefekte im Licht neuer gendiagnostischer Verfahren
 Institut für Medizinische Genetik Entwicklungsstörungen und Intelligenzdefekte im Licht neuer gendiagnostischer Verfahren Prof. Dr. med. Anita Rauch Seite 1 Häufigkeit von Intelligenzminderung (ID) IQ
Institut für Medizinische Genetik Entwicklungsstörungen und Intelligenzdefekte im Licht neuer gendiagnostischer Verfahren Prof. Dr. med. Anita Rauch Seite 1 Häufigkeit von Intelligenzminderung (ID) IQ
Nicht-invasive molekulargenetische Pränataldiagnostik
 Nicht-invasive molekulargenetische Pränataldiagnostik Dr. rer. medic. Wera Hofmann Medical Director LifeCodexx AG Dr. Wera Hofmann, Medical Director Porto, ECA 2011 July 2, 2011 page 1 2011 LifeCodexx
Nicht-invasive molekulargenetische Pränataldiagnostik Dr. rer. medic. Wera Hofmann Medical Director LifeCodexx AG Dr. Wera Hofmann, Medical Director Porto, ECA 2011 July 2, 2011 page 1 2011 LifeCodexx
Periphere Nervenläsionen bei Sjögren-Syndrom Dr. A. Rosenbohm Neurologische Universitätsklinik Ulm
 Periphere Nervenläsionen bei Sjögren-Syndrom 22.09.2012 Dr. A. Rosenbohm Neurologische Universitätsklinik Ulm Diagnosestellung in der Neurologie Befragung (Anamneseerhebung) Körperliche Untersuchung (Befunderhebung)
Periphere Nervenläsionen bei Sjögren-Syndrom 22.09.2012 Dr. A. Rosenbohm Neurologische Universitätsklinik Ulm Diagnosestellung in der Neurologie Befragung (Anamneseerhebung) Körperliche Untersuchung (Befunderhebung)
SCLERODERMA LIGA e.v.
 SCLERODERMA LIGA e.v. Beilage zum Scleroderma INFOBRIEF Nr. 42 Dermatomyositis, Polymyositis, Einschlußkörpermyositis Klinik, Diagnostik und Therapie Dieter Pongratz Einleitung Die Dermatomyositis, Polymyositis
SCLERODERMA LIGA e.v. Beilage zum Scleroderma INFOBRIEF Nr. 42 Dermatomyositis, Polymyositis, Einschlußkörpermyositis Klinik, Diagnostik und Therapie Dieter Pongratz Einleitung Die Dermatomyositis, Polymyositis
Brustkrebs aktuell - OSP am Was ist eigentlich die Aufgabe des Pathologen in Diagnostik und Therapie des Mammakarzinoms?
 Brustkrebs aktuell - OSP am 21.10.2015 Was ist eigentlich die Aufgabe des Pathologen in Diagnostik und Therapie des Mammakarzinoms? Prof. Dr. German Ott, Institut für Pathologie Robert-Bosch-Krankenhaus
Brustkrebs aktuell - OSP am 21.10.2015 Was ist eigentlich die Aufgabe des Pathologen in Diagnostik und Therapie des Mammakarzinoms? Prof. Dr. German Ott, Institut für Pathologie Robert-Bosch-Krankenhaus
Genetik der Chorea Huntington
 Genetik der Chorea Huntington Prim. Univ. Doz. Dr. med. Hans-Christoph Duba Zentrum Medizinische Genetik Linz 17.10.2015 Genetik der Chorea Huntington 1 Chorea Huntington Chorea Huntington Häufigkeit =
Genetik der Chorea Huntington Prim. Univ. Doz. Dr. med. Hans-Christoph Duba Zentrum Medizinische Genetik Linz 17.10.2015 Genetik der Chorea Huntington 1 Chorea Huntington Chorea Huntington Häufigkeit =
ABKLÄRUNGS- UND BEHANDLUNGSSTRATEGIEN BEI NEUROMUSKULÄREN ERKRANKUNGEN. Warnzeichen bei hypotonen Säuglingen / floppy infants
 ABKLÄRUNGS- UND BEHANDLUNGSSTRATEGIEN BEI NEUROMUSKULÄREN ERKRANKUNGEN 22.03.16, Kinderspital Luzern, Petra Kolditz Warnzeichen bei hypotonen Säuglingen / floppy infants Respiratorische Insuffizienz Trinkschwäche
ABKLÄRUNGS- UND BEHANDLUNGSSTRATEGIEN BEI NEUROMUSKULÄREN ERKRANKUNGEN 22.03.16, Kinderspital Luzern, Petra Kolditz Warnzeichen bei hypotonen Säuglingen / floppy infants Respiratorische Insuffizienz Trinkschwäche
Leben mit chronischer Erschöpfung - CFS
 Leben mit chronischer Erschöpfung - CFS Ein Ratgeber für Patienten von J. Strienz überarbeitet Leben mit chronischer Erschöpfung - CFS Strienz schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG
Leben mit chronischer Erschöpfung - CFS Ein Ratgeber für Patienten von J. Strienz überarbeitet Leben mit chronischer Erschöpfung - CFS Strienz schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG
AKTUELLES ZUR DEMENZDIAGNOSTIK
 AKTUELLES ZUR DEMENZDIAGNOSTIK GHF am Medizinische Diagnostik 2 Biomarker Cerebrale Atrophien (MRT) Cerebraler Hypometabolismus (PET) Liquor Erhöhte Konzentration Abeta 42 (Amyloidprotein) Erhöhte Konzentraion
AKTUELLES ZUR DEMENZDIAGNOSTIK GHF am Medizinische Diagnostik 2 Biomarker Cerebrale Atrophien (MRT) Cerebraler Hypometabolismus (PET) Liquor Erhöhte Konzentration Abeta 42 (Amyloidprotein) Erhöhte Konzentraion
Muskeldystrophien und andere hereditäre Myopathien
 M.C. Walter, Th. Klopstock und andere hereditäre Myopathien ISBN 978-3-17-024555-6 Kapitel J9 aus T. Brandt, H.C. Diener, C. Gerloff (Hrsg.) Therapie und Verlauf neurologischer Erkrankungen 6., vollständig
M.C. Walter, Th. Klopstock und andere hereditäre Myopathien ISBN 978-3-17-024555-6 Kapitel J9 aus T. Brandt, H.C. Diener, C. Gerloff (Hrsg.) Therapie und Verlauf neurologischer Erkrankungen 6., vollständig
Fall einer hereditären Hämochromatose (HH) Dr. med. Carl M. Oneta Schaffhauserstrasse Winterthur
 Fall einer hereditären Hämochromatose (HH) Dr. med. Carl M. Oneta Schaffhauserstrasse 7 8400 Winterthur Fall (Klinik) 48 jähriger Patient, Wirtschaftsmanager, Vater von 3 Kindern, bisher immer bei guter
Fall einer hereditären Hämochromatose (HH) Dr. med. Carl M. Oneta Schaffhauserstrasse 7 8400 Winterthur Fall (Klinik) 48 jähriger Patient, Wirtschaftsmanager, Vater von 3 Kindern, bisher immer bei guter
Symptome und Diagnosestellung des Morbus Parkinson
 meine Hand zittert habe ich etwa Parkinson? Symptome und Diagnosestellung des Morbus Parkinson Dr. med. Sabine Skodda Oberärztin Neurologische Klinik Morbus Parkinson chronisch fortschreitende neurodegenerative
meine Hand zittert habe ich etwa Parkinson? Symptome und Diagnosestellung des Morbus Parkinson Dr. med. Sabine Skodda Oberärztin Neurologische Klinik Morbus Parkinson chronisch fortschreitende neurodegenerative
Leben mit chronischer Erschöpfung CFS
 Leben mit chronischer Erschöpfung CFS Ein Ratgeber für Patienten von Joachim Strienz überarbeitet W. Zuckschwerdt 2015 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 86371 169 6 Zu Leseprobe schnell
Leben mit chronischer Erschöpfung CFS Ein Ratgeber für Patienten von Joachim Strienz überarbeitet W. Zuckschwerdt 2015 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 86371 169 6 Zu Leseprobe schnell
Deutsches Netzwerk für mitochondriale Erkrankungen
 Deutsches Netzwerk für mitochondriale Erkrankungen mitonet Patientenregister DGM Deutsche Gesellschaft für Muskelkranke e. V. 3 Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale
Deutsches Netzwerk für mitochondriale Erkrankungen mitonet Patientenregister DGM Deutsche Gesellschaft für Muskelkranke e. V. 3 Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie
 Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Zyanose [35] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf Version 02.10.2013 Krankheitsbilder in Verbindung mit dem Behandlungsanlass
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Zyanose [35] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf Version 02.10.2013 Krankheitsbilder in Verbindung mit dem Behandlungsanlass
Pilzpneumonie. CT Diagnostik
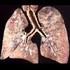 Pilzpneumonie CT Diagnostik Radiologie Prof. Dr. Claus-Peter Heussel Diagnostische und Interventionelle Radiologie Thoraxklinik Heidelberg Das CT Thorax ist eine sensitive Methode zum Nachweis pulmonaler
Pilzpneumonie CT Diagnostik Radiologie Prof. Dr. Claus-Peter Heussel Diagnostische und Interventionelle Radiologie Thoraxklinik Heidelberg Das CT Thorax ist eine sensitive Methode zum Nachweis pulmonaler
PD Dr. med. Andrea Klein Leitende Ärztin Neuropädiatrie Leiterin des pädiatrischen Teils des Neuromuskulären Zentrums Basel am UKBB
 PD Dr. med. Andrea Klein Leitende Ärztin Neuropädiatrie Leiterin des pädiatrischen Teils des Neuromuskulären Zentrums Basel am UKBB Andrea.klein@ukbb.ch T +61 704 29 38 Aus- und Weiterbildung Seit Dez
PD Dr. med. Andrea Klein Leitende Ärztin Neuropädiatrie Leiterin des pädiatrischen Teils des Neuromuskulären Zentrums Basel am UKBB Andrea.klein@ukbb.ch T +61 704 29 38 Aus- und Weiterbildung Seit Dez
Populationsrelevanz der Hämochromatose und klinische Konsequenzen
 Populationsrelevanz der Hämochromatose und klinische Konsequenzen 60. Tagung der DGVS Köln, 15.09.2005 Prof. Dr. med. Manfred Stuhrmann-Spangenberg Institut für Humangenetik Medizinische Hochschule Hannover
Populationsrelevanz der Hämochromatose und klinische Konsequenzen 60. Tagung der DGVS Köln, 15.09.2005 Prof. Dr. med. Manfred Stuhrmann-Spangenberg Institut für Humangenetik Medizinische Hochschule Hannover
handlungsfehler in der präklinischen Versorgung f. Dr. A. Ferbert.2008 10. Jahrestagung der ANB
 handlungsfehler in der präklinischen Versorgung f. Dr. A. Ferbert.2008 10. Jahrestagung der ANB Häufige Fehlerarten in der Prähospitalphase Schlaganfall bzw. TIA nicht diagnostiziert. SAB nicht diagnostiziert
handlungsfehler in der präklinischen Versorgung f. Dr. A. Ferbert.2008 10. Jahrestagung der ANB Häufige Fehlerarten in der Prähospitalphase Schlaganfall bzw. TIA nicht diagnostiziert. SAB nicht diagnostiziert
HOCM. Diagnostik, Risiko, Therapie. PD Dr. Marcel Halbach. Klinik III für Innere Medizin. Herzzentrum der Universität zu Köln
 HOCM Diagnostik, Risiko, Therapie PD Dr. Marcel Halbach Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Definition und Ätiologie der HCM Erhöhung der Wanddicke, die nicht allein durch
HOCM Diagnostik, Risiko, Therapie PD Dr. Marcel Halbach Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Definition und Ätiologie der HCM Erhöhung der Wanddicke, die nicht allein durch
Sehr geehrte Ratsuchende!
 Genetische Beratung Sehr geehrte Ratsuchende! Sie möchten sich über die Risiken einer erblichen Erkrankung informieren, die bei Ihnen selbst, Ihren Kindern oder Verwandten aufgetreten ist? Sie möchten
Genetische Beratung Sehr geehrte Ratsuchende! Sie möchten sich über die Risiken einer erblichen Erkrankung informieren, die bei Ihnen selbst, Ihren Kindern oder Verwandten aufgetreten ist? Sie möchten
Von Hüsteln, Schnupfen und ELVIS hereditäre Immundefekte im Erwachsenenalter
 Von Hüsteln, Schnupfen und ELVIS hereditäre Immundefekte im Erwachsenenalter PD Dr. Matthias Wahle Abteilung Rheumatologie, Medizinische Klinik II Klinikum der JW Goethe-Universität Frankfurt Frau Doktor/
Von Hüsteln, Schnupfen und ELVIS hereditäre Immundefekte im Erwachsenenalter PD Dr. Matthias Wahle Abteilung Rheumatologie, Medizinische Klinik II Klinikum der JW Goethe-Universität Frankfurt Frau Doktor/
Patienteninformation. Blutserum IR-Spektroskopie zur Diagnose der Hereditären Hämorrhagischen Teleangiektasie
 PD Dr. rer. nat. Andreas Lux Institut für Molekular- und Zellbiologie Hochschule Mannheim, Paul-Wittsackstr. 10, 68163 Mannheim fon 0621-2926537 fax 0621-2926420 mobil 0157-74233028 e-mail: A.Lux@hs-mannheim.de
PD Dr. rer. nat. Andreas Lux Institut für Molekular- und Zellbiologie Hochschule Mannheim, Paul-Wittsackstr. 10, 68163 Mannheim fon 0621-2926537 fax 0621-2926420 mobil 0157-74233028 e-mail: A.Lux@hs-mannheim.de
Programm Demenz-Prävention
 Programm Demenz-Prävention Mehr Lebensqualität durch individuelle Maßnahmen im Frühstadium der Erkrankung Ministère de la Santé Villa Louvigny/Allée Marconi L-2120 Luxembourg Tel. 00352/ 27861312 info@demence.lu/info@demenz.lu
Programm Demenz-Prävention Mehr Lebensqualität durch individuelle Maßnahmen im Frühstadium der Erkrankung Ministère de la Santé Villa Louvigny/Allée Marconi L-2120 Luxembourg Tel. 00352/ 27861312 info@demence.lu/info@demenz.lu
S2e-Niveau sichert Qualität bei Diagnose und Therapie der MS
 Multiple Sklerose (MS): Neue Leitlinie online verfügbar S2e-Niveau sichert Qualität bei Diagnose und Therapie der MS München/Berlin (18. April 2012) Die im Rahmen des 84. Kongresses der Deutschen Gesellschaft
Multiple Sklerose (MS): Neue Leitlinie online verfügbar S2e-Niveau sichert Qualität bei Diagnose und Therapie der MS München/Berlin (18. April 2012) Die im Rahmen des 84. Kongresses der Deutschen Gesellschaft
Verbesserung des Tuberkulose-Screenings bei Patienten mit rheumatischen Erkrankungen vor Beginn einer Therapie mit TNFα-Blockern
 Rheumatologie / Klinische Immunologie Prof. Dr. H.P. Tony (Leiter des Schwerpunktes) Prof. Dr. med. Ch. Kneitz Medizinische Poliklinik Klinikstr. 6-8 97070 Würzburg Abstract: 1 / 10 Verbesserung des Tuberkulose-Screenings
Rheumatologie / Klinische Immunologie Prof. Dr. H.P. Tony (Leiter des Schwerpunktes) Prof. Dr. med. Ch. Kneitz Medizinische Poliklinik Klinikstr. 6-8 97070 Würzburg Abstract: 1 / 10 Verbesserung des Tuberkulose-Screenings
Management of Neuromuscular Diseases
 Management of Neuromuscular Diseases Letter Nr. 37 Wertigkeit laborchemischer Untersuchungen bei neuromuskulären Erkrankungen Kathrin Traufeller und Stephan Zierz In der Diagnostik neuromuskulärer Erkrankungen
Management of Neuromuscular Diseases Letter Nr. 37 Wertigkeit laborchemischer Untersuchungen bei neuromuskulären Erkrankungen Kathrin Traufeller und Stephan Zierz In der Diagnostik neuromuskulärer Erkrankungen
Amyotrophe Lateralsklerose. Referat von Eva Montag
 Amyotrophe Lateralsklerose Referat von Eva Montag http://p5.focus.de/img/incoming/origs3195325/5738838139-w630-h412-o-q75-p5/wissen-hawking.jpg Inhalt 1. Definition Was genau ist ALS? 2. Verlauf und Symptomatik
Amyotrophe Lateralsklerose Referat von Eva Montag http://p5.focus.de/img/incoming/origs3195325/5738838139-w630-h412-o-q75-p5/wissen-hawking.jpg Inhalt 1. Definition Was genau ist ALS? 2. Verlauf und Symptomatik
Neue Diagnostik für akute myeloische Leukämie
 Neue Diagnostik für akute myeloische Leukämie Neuherberg (9. März 2011) - Wissenschaftler des Helmholtz Zentrums München und der Ludwig-Maximilians-Universität München haben eine Methode entwickelt, mit
Neue Diagnostik für akute myeloische Leukämie Neuherberg (9. März 2011) - Wissenschaftler des Helmholtz Zentrums München und der Ludwig-Maximilians-Universität München haben eine Methode entwickelt, mit
Wissenswertes zur Spinalen Muskelatrophie
 Wissenswertes zur Spinalen Muskelatrophie Rudolf Korinthenberg, Janbernd Kirschner Klinik für Neuropädiatrie und Muskelerkrankungen Zentrum für Kinderheilkunde und Jugendmedizin Universitätsklinikum Freiburg/Brsg.
Wissenswertes zur Spinalen Muskelatrophie Rudolf Korinthenberg, Janbernd Kirschner Klinik für Neuropädiatrie und Muskelerkrankungen Zentrum für Kinderheilkunde und Jugendmedizin Universitätsklinikum Freiburg/Brsg.
PraenaTest. Nicht-invasive Untersuchung auf Trisomien beim ungeborenen Kind. Qualität aus Deutschland JETZT NEU
 JETZT NEU PraenaTest express Ihr Ergebnis in 1 Woche PraenaTest Qualität aus Deutschland Nicht-invasive Untersuchung auf Trisomien beim ungeborenen Kind Information und Aufklärung für Schwangere Liebe
JETZT NEU PraenaTest express Ihr Ergebnis in 1 Woche PraenaTest Qualität aus Deutschland Nicht-invasive Untersuchung auf Trisomien beim ungeborenen Kind Information und Aufklärung für Schwangere Liebe
Manometrie des Ösophagus mit heliumperfundierten Kathetern im Kindesalter
 Aus der Universitätsklinik und Poliklinik für Kinderchirurgie an der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. habil. R. Finke Manometrie des Ösophagus mit heliumperfundierten
Aus der Universitätsklinik und Poliklinik für Kinderchirurgie an der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. habil. R. Finke Manometrie des Ösophagus mit heliumperfundierten
Definition. Entzündliche abakterielle Nierenerkrankungen mit Befall unterchiedlicher glomerulärer Strukturen
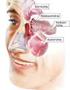 Glomerulonephritis Definition Entzündliche abakterielle Nierenerkrankungen mit Befall unterchiedlicher glomerulärer Strukturen Ursachen Insgesamt eher seltene Erkrankung Zweithäufigste Ursache einer chronischen
Glomerulonephritis Definition Entzündliche abakterielle Nierenerkrankungen mit Befall unterchiedlicher glomerulärer Strukturen Ursachen Insgesamt eher seltene Erkrankung Zweithäufigste Ursache einer chronischen
Auszug aus dem Strukturierten Qualitätsbericht
 Auszug aus dem Strukturierten Qualitätsbericht gemäß 137 Abs. 3 Satz 1 Nr. 4 SGB V für das Berichtsjahr 2010 Institut für Neuropathologie B-33 Institut für Neuropathologie B-33.1 Allgemeine Angaben : Institut
Auszug aus dem Strukturierten Qualitätsbericht gemäß 137 Abs. 3 Satz 1 Nr. 4 SGB V für das Berichtsjahr 2010 Institut für Neuropathologie B-33 Institut für Neuropathologie B-33.1 Allgemeine Angaben : Institut
Nodales Marginalzonen Lymphom Leitlinie
 Nodales Marginalzonen Lymphom Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie
Nodales Marginalzonen Lymphom Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie
Herzkrankheiten besser erkennen!
 Herzkrankheiten besser erkennen! Magnetresonanztomographie und andere neue diagnostische Methoden Dr. Wolfgang Pistner Medizinische Klinik I Klinikum Aschaffenburg Herzsportgruppe TuS Leider, AOK Aschaffenburg
Herzkrankheiten besser erkennen! Magnetresonanztomographie und andere neue diagnostische Methoden Dr. Wolfgang Pistner Medizinische Klinik I Klinikum Aschaffenburg Herzsportgruppe TuS Leider, AOK Aschaffenburg
Qualität t und Evidenz in der Ernährungsmedizin Sind Leitlinien eine Hilfe?
 Qualität t und Evidenz in der Ernährungsmedizin Sind Leitlinien eine Hilfe? H. Lochs Medizinische Klinik mit Schwerpunkt Gastroenterologie, Hepatologie und Endokrinologie h.lochs@charite.de Guidelines
Qualität t und Evidenz in der Ernährungsmedizin Sind Leitlinien eine Hilfe? H. Lochs Medizinische Klinik mit Schwerpunkt Gastroenterologie, Hepatologie und Endokrinologie h.lochs@charite.de Guidelines
Das Freiburger Zentrum für Seltene Erkrankungen
 Das Freiburger Zentrum für Seltene Erkrankungen Prof. Dr. med. Janbernd Kirschner Klinik Neuropädiatrie und Muskelerkrankungen 6. FORUM Patientennahe Klinische Forschung 26. November 2014 in Freiburg Seltene
Das Freiburger Zentrum für Seltene Erkrankungen Prof. Dr. med. Janbernd Kirschner Klinik Neuropädiatrie und Muskelerkrankungen 6. FORUM Patientennahe Klinische Forschung 26. November 2014 in Freiburg Seltene
Parkinson-Krankheit: Neue Leitlinie für Diagnostik und Therapie veröffentlicht
 Parkinson-Krankheit: Neue Leitlinie für Diagnostik und Therapie veröffentlicht Berlin (6. April 2016) Rechtzeitig vor dem Welt-Parkinson-Tag am 11. April veröffentlicht die Deutsche Gesellschaft für Neurologie
Parkinson-Krankheit: Neue Leitlinie für Diagnostik und Therapie veröffentlicht Berlin (6. April 2016) Rechtzeitig vor dem Welt-Parkinson-Tag am 11. April veröffentlicht die Deutsche Gesellschaft für Neurologie
Entwicklungsstörung. Abklären, erkennen, vorsorgen. Informationen für Eltern mit einem Sorgenkind
 Entwicklungsstörung Abklären, erkennen, vorsorgen Informationen für Eltern mit einem Sorgenkind Entwicklungsstörungen haben oft genetische Ursachen Was sind genetisch bedingte Störungen und Erkrankungen?
Entwicklungsstörung Abklären, erkennen, vorsorgen Informationen für Eltern mit einem Sorgenkind Entwicklungsstörungen haben oft genetische Ursachen Was sind genetisch bedingte Störungen und Erkrankungen?
Leistungsverzeichnis LV_SBGR. Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot)
 Seite 1 von 5 1. Klinische Indikation Analyt: Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot) V. a. und Differentialdiagnostik der progressiven Systemsklerose (), begrenzte (limitierte)
Seite 1 von 5 1. Klinische Indikation Analyt: Antikörper gegen Systemische Sklerose-assoziierte Antigene (Immunoblot) V. a. und Differentialdiagnostik der progressiven Systemsklerose (), begrenzte (limitierte)
Indolente Non Hodgkin- Lymphome (NHL) Leitlinie
 Indolente Non Hodgkin- Lymphome (NHL) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie
Indolente Non Hodgkin- Lymphome (NHL) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie
Mit Hirn, Hand und Hammer : erste diagnostische Schritte
 Mit Hirn, Hand und Hammer : erste diagnostische Schritte Prof. Dr. Reinhard Kiefer Neurologische Klinik Neurologische Praxis im MVZ Diakoniekrankenhaus Rotenburg (Wümme) Polyneuropathie warum ein einfaches
Mit Hirn, Hand und Hammer : erste diagnostische Schritte Prof. Dr. Reinhard Kiefer Neurologische Klinik Neurologische Praxis im MVZ Diakoniekrankenhaus Rotenburg (Wümme) Polyneuropathie warum ein einfaches
UNIVERSITÄTS-HAUTKLINIK Zertifiziert nach DIN EN ISO 9001:2000
 UNIVERSITÄTSKLINIKUM Universitäts-Hautklinik, Hauptstraße 7, D-79104 Freiburg UNIVERSITÄTS-HAUTKLINIK Zertifiziert nach DIN EN ISO 9001:2000 Ärztliche Direktorin Univ.-Prof. Dr. L. Bruckner-Tuderman Epidermolysis
UNIVERSITÄTSKLINIKUM Universitäts-Hautklinik, Hauptstraße 7, D-79104 Freiburg UNIVERSITÄTS-HAUTKLINIK Zertifiziert nach DIN EN ISO 9001:2000 Ärztliche Direktorin Univ.-Prof. Dr. L. Bruckner-Tuderman Epidermolysis
Vorzeichen von Multiple Sklerose früh erkennen
 Sehstörungen bei Kindern und Jugendlichen Vorzeichen von Multiple Sklerose früh erkennen München (29. August 2012) Multiple Sklerose (MS), eine chronisch-entzündliche Erkrankung von Gehirn und Rückenmark,
Sehstörungen bei Kindern und Jugendlichen Vorzeichen von Multiple Sklerose früh erkennen München (29. August 2012) Multiple Sklerose (MS), eine chronisch-entzündliche Erkrankung von Gehirn und Rückenmark,
Mathias Müller (FA Kinderheilkunde/ Neuropädiatrie) NEUROLOGISCHE ERKRANKUNGEN DES KINDESALTERS MIT BEATMUNGSNOTWENDIGKEIT
 Mathias Müller (FA Kinderheilkunde/ Neuropädiatrie) NEUROLOGISCHE ERKRANKUNGEN DES KINDESALTERS MIT BEATMUNGSNOTWENDIGKEIT Erkrankungen mit Heimbeatmungsnotwendigkeit Ursachen für chronische Ateminsuffizienz
Mathias Müller (FA Kinderheilkunde/ Neuropädiatrie) NEUROLOGISCHE ERKRANKUNGEN DES KINDESALTERS MIT BEATMUNGSNOTWENDIGKEIT Erkrankungen mit Heimbeatmungsnotwendigkeit Ursachen für chronische Ateminsuffizienz
Voruntersuchungen. Klinik für Anästhesiologie und Intensivmedizin
 Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
BLUTPROBEN FÜR DIE MOLEKULARGENETISCHE ANALYSE VON ERBKRANKHEITEN
 Klinik für Dermatologie & Venerologie Zertifiziert nach DIN EN ISO 9001 UNIVERSITÄTSKLINIKUM FREIBURG Klinik für Dermatologie und Venerologie. Hauptstr. 7. 79104 Freiburg Epidermolysis bullosa-zentrum
Klinik für Dermatologie & Venerologie Zertifiziert nach DIN EN ISO 9001 UNIVERSITÄTSKLINIKUM FREIBURG Klinik für Dermatologie und Venerologie. Hauptstr. 7. 79104 Freiburg Epidermolysis bullosa-zentrum
Indolente Non Hodgkin- Lymphome (NHL) Leitlinie
 Indolente Non Hodgkin- Lymphome (NHL) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie
Indolente Non Hodgkin- Lymphome (NHL) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie
Faktor-V-Leiden Mutation: Diagnose und Klinik
 INRswiss-Tag Solothurn, 21. November 2009 Faktor-V-Leiden Mutation: Diagnose und Klinik Dr. Giuseppe Colucci Universitätsklinik für Hämatologie und Hämatologisches Zentrallabor Inselspital Bern Faktor-V-Leiden
INRswiss-Tag Solothurn, 21. November 2009 Faktor-V-Leiden Mutation: Diagnose und Klinik Dr. Giuseppe Colucci Universitätsklinik für Hämatologie und Hämatologisches Zentrallabor Inselspital Bern Faktor-V-Leiden
Zur Situation betroffener Eltern. Karin Brosius, stellv. Sprecherin der Mito Diagnosegruppe in der Deutschen Gesellschaft für Muskelkranke e.v.
 Zur Situation betroffener Eltern Karin Brosius, stellv. Sprecherin der Mito Diagnosegruppe in der Deutschen Gesellschaft für Muskelkranke e.v. DGM L., 19 Jahre, mitochondriale Enzephalomyopathie (Leigh
Zur Situation betroffener Eltern Karin Brosius, stellv. Sprecherin der Mito Diagnosegruppe in der Deutschen Gesellschaft für Muskelkranke e.v. DGM L., 19 Jahre, mitochondriale Enzephalomyopathie (Leigh
Stufendiagnostik der KHK. Anamnese
 Risikofaktoren für KHK Westfälische Wilhelms- Universität Münster Diagnostik der KHK Anamnese Ischämie-Nachweis Hyperlipoproteinämie LDL-Cholesterin Lp(a) nicht modifizierbar Nikotinabusus Prof. Dr. med.
Risikofaktoren für KHK Westfälische Wilhelms- Universität Münster Diagnostik der KHK Anamnese Ischämie-Nachweis Hyperlipoproteinämie LDL-Cholesterin Lp(a) nicht modifizierbar Nikotinabusus Prof. Dr. med.
genomischen Mutation in bis zu 25 Kilobasen kodierender Sequenz 11445
 05315 Zuschlag zu den Gebührenordnungspositionen 31840, 31841, 36840 und 36841 11501 Zuschlag zu den Gebührenordnungspositionen 11502 und 11503 für die Anwendung eines Kulturverfahrens zur Anzucht von
05315 Zuschlag zu den Gebührenordnungspositionen 31840, 31841, 36840 und 36841 11501 Zuschlag zu den Gebührenordnungspositionen 11502 und 11503 für die Anwendung eines Kulturverfahrens zur Anzucht von
Woran muss man denken?
 Verstopfung, Durchfall- Woran muss man denken? Dr. med. Michael Steckstor 19.09.2013 1 Stuhlgang - So sieht's aus 1x Stuhlgang pro Tag normal? große individuelle Bandbreite: 3xTag bis 3xWoche, 100-200
Verstopfung, Durchfall- Woran muss man denken? Dr. med. Michael Steckstor 19.09.2013 1 Stuhlgang - So sieht's aus 1x Stuhlgang pro Tag normal? große individuelle Bandbreite: 3xTag bis 3xWoche, 100-200
Diabetische Polyneuropathie Diagnose nach Leitlinien
 AG-Fuß Rheinland-Pfalz/Saarland in der Arbeitsgemeinschaft Diabetologie und Endokrinologie (ADE) Rheinland-Pfalz e.v. Landesgruppe Rheinland-Pfalz der Deutschen Diabetes Gesellschaft Diabetische Polyneuropathie
AG-Fuß Rheinland-Pfalz/Saarland in der Arbeitsgemeinschaft Diabetologie und Endokrinologie (ADE) Rheinland-Pfalz e.v. Landesgruppe Rheinland-Pfalz der Deutschen Diabetes Gesellschaft Diabetische Polyneuropathie
Bad Pyrmonter Osteoporose Evaluationswoche
 Bad Pyrmonter Osteoporose Evaluationswoche Klinik DER FÜRSTENHOF Fachklinik für Orthopädie, Osteoporose, Stoffwechselerkrankungen des Knochens, Rheumatologie, Gynäkologie / gynäkologische Onkologie Christian
Bad Pyrmonter Osteoporose Evaluationswoche Klinik DER FÜRSTENHOF Fachklinik für Orthopädie, Osteoporose, Stoffwechselerkrankungen des Knochens, Rheumatologie, Gynäkologie / gynäkologische Onkologie Christian
Das EliA System. nn Protokolle, QC- und Rohdaten leicht zugänglich nn Optionaler Anschluss an die Laborsoftware nn Detailliertes QC-Management
 CCP Das EliA System Mehr Zeit für s Wesentliche nn Vollständig automatisiert (echter Walk-away-Modus, Übernachtläufe) nn Einfaches Management des Instruments mit maßgefertigter Software nn Barcode-Lesegerät
CCP Das EliA System Mehr Zeit für s Wesentliche nn Vollständig automatisiert (echter Walk-away-Modus, Übernachtläufe) nn Einfaches Management des Instruments mit maßgefertigter Software nn Barcode-Lesegerät
Der Rückenschmerz ist neuropathisch!
 Prof. Dr. Ralf Baron: Der Rückenschmerz nervt?! Debatte ohne Ende oder Ende der Debatte? Der Rücke Der Rückenschmerz nervt?! Debatte ohne Ende oder Ende der Debatte? Der Rückenschmerz ist neuropathisch!
Prof. Dr. Ralf Baron: Der Rückenschmerz nervt?! Debatte ohne Ende oder Ende der Debatte? Der Rücke Der Rückenschmerz nervt?! Debatte ohne Ende oder Ende der Debatte? Der Rückenschmerz ist neuropathisch!
Milenia Hybridetect. Detection of DNA and Protein
 Milenia Hybridetect Detection of DNA and Protein Firmenprofil und Produkte Milenia Biotec GmbH ist im Jahr 2000 gegründet worden. Die Firma entwickelt, produziert, vermarktet und verkauft diagnostische
Milenia Hybridetect Detection of DNA and Protein Firmenprofil und Produkte Milenia Biotec GmbH ist im Jahr 2000 gegründet worden. Die Firma entwickelt, produziert, vermarktet und verkauft diagnostische
Deutsches Netzwerk für mitochondriale Erkrankungen
 Deutsches Netzwerk für mitochondriale Erkrankungen mitonet Patientenregister DGM Deutsche Gesellschaft für Muskelkranke e. V. 3 Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale
Deutsches Netzwerk für mitochondriale Erkrankungen mitonet Patientenregister DGM Deutsche Gesellschaft für Muskelkranke e. V. 3 Information zum Patientenregister im Rahmen des Deutschen Netzwerks für mitochondriale
Gemeinsame genetische Risikofaktoren bei häufigen Epilepsiesyndromen entdeckt
 Epilepsie-Varianten Gemeinsame genetische Risikofaktoren bei häufigen Epilepsiesyndromen entdeckt Berlin (19. September 2014) - Epilepsien sind eine klinisch heterogene Gruppe neurologischer Erkrankungen.
Epilepsie-Varianten Gemeinsame genetische Risikofaktoren bei häufigen Epilepsiesyndromen entdeckt Berlin (19. September 2014) - Epilepsien sind eine klinisch heterogene Gruppe neurologischer Erkrankungen.
Neue Klassifikationssysteme in der Nierenpathologie
 Neue Klassifikationssysteme in der Nierenpathologie Kerstin Amann Abt. Nephropathologie Pathologisches Institut der Universität Erlangen-Nürnberg Krankenhausstr. 12 91054 Erlangen Histologische Klassifikationssysteme
Neue Klassifikationssysteme in der Nierenpathologie Kerstin Amann Abt. Nephropathologie Pathologisches Institut der Universität Erlangen-Nürnberg Krankenhausstr. 12 91054 Erlangen Histologische Klassifikationssysteme
Universität zu Lübeck Institut für Krebsepidemiologie e.v.
 Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Leukämie (CML) Was ist Chronische Myeloische Leukämie? Download. Published on Novartis Austria (https://www.novartis.at)
 Published on Novartis Austria (https://www.novartis.at) Home > Printer-friendly PDF > Leukämie (CML) Leukämie (CML) Was ist Chronische Myeloische Leukämie? Die chronische myeloische Leukämie (CML) ist
Published on Novartis Austria (https://www.novartis.at) Home > Printer-friendly PDF > Leukämie (CML) Leukämie (CML) Was ist Chronische Myeloische Leukämie? Die chronische myeloische Leukämie (CML) ist
Multiple Sklerose (MS)
 Bild: Kurzlehrbuch Neurologie, Thieme Multiple Sklerose 2 Multiple Sklerose (MS) Inhalt» Pathogenese» Symptome» Diagnostik» Therapie Multiple Sklerose 4 Multiple Sklerose 3 Klinischer Fall..\3) Sammlung\Klinischer
Bild: Kurzlehrbuch Neurologie, Thieme Multiple Sklerose 2 Multiple Sklerose (MS) Inhalt» Pathogenese» Symptome» Diagnostik» Therapie Multiple Sklerose 4 Multiple Sklerose 3 Klinischer Fall..\3) Sammlung\Klinischer
Diese Kombination von multiplen Geburtsfehlern ist relativ häufig (ca. 1/ 8500 Neugeborene). Selten zeigen Betroffene eine normale Intelligenz.
 Praxis für Humangenetik Heinrich-von-Stephan-Str. 5 D-79100 Freiburg Information CHARGE-Syndrom Molekulargenetische Untersuchung des Gens CHD7 Praxis für Humangenetik Prof. Dr. med. Jürgen Kohlhase Facharzt
Praxis für Humangenetik Heinrich-von-Stephan-Str. 5 D-79100 Freiburg Information CHARGE-Syndrom Molekulargenetische Untersuchung des Gens CHD7 Praxis für Humangenetik Prof. Dr. med. Jürgen Kohlhase Facharzt
Auswertung von Unterschieden der Androgene bei SBMA-Patienten
 Auswertung von Unterschieden der Androgene bei SBMA-Patienten Nicholas Di Prospero, MD, PhD National Institute of Neurological Disorders and Stroke NIH Von der Genetik zu einem Gen Spinale und Bulbäre
Auswertung von Unterschieden der Androgene bei SBMA-Patienten Nicholas Di Prospero, MD, PhD National Institute of Neurological Disorders and Stroke NIH Von der Genetik zu einem Gen Spinale und Bulbäre
Kompetenznetz Vorhofflimmern Atrial Fibrillation Network AFNET
 Kompetenznetz Vorhofflimmern Atrial Fibrillation Network AFNET ww.kompetenznetz-vorhofflimmern.de Vorstand: G. Breithardt (Münster) Sprecher Th. Meinertz (Hamburg) U. Ravens (Dresden) G. Steinbeck (München)
Kompetenznetz Vorhofflimmern Atrial Fibrillation Network AFNET ww.kompetenznetz-vorhofflimmern.de Vorstand: G. Breithardt (Münster) Sprecher Th. Meinertz (Hamburg) U. Ravens (Dresden) G. Steinbeck (München)
