Beschreibung von Biomolekülen
|
|
|
- Maya Meta Kerner
- vor 6 Jahren
- Abrufe
Transkript
1 Dr. Herbert Wank SS 2010 Beschreibung von Biomolekülen Physikalische Methoden zur Untersuchung struktureller und funktioneller Eigenschaften biologischer Moleküle Ein wesentliches Ziel biochemischer und biophysikalischer Arbeiten ist die Charakterisierung der Gestalt von Biomolekülen und die Bestimmung ihrer Molmasse. > In der Biochemie und Biophysik bestimmt man die Molmasse > von Makromolekülen im allg. nach folgenden Verfahren: > Osmometrie, Viskosimetrie, Sedimentationsgleichgewicht, > Licht-, Röntgen- und Neutronenstreuung und durch > chromatographische Verfahren.
2 Mittlere Molmasse in g/mol Fibrinogen Der Blutgerinnungsfaktor Fibrinogen ist ein Glykoprotein, das in der Leber gebildet wird. Fibrinogen wird bei der Blutgerinnung durch das Enzym Thrombin und Calcium in Fibrin umgewandelt, das für die Bildung des sekundären Thrombus verantwortlich ist. Die Plasma- und Gewebefaktoren (Integrin) wirken auf das Fibrinogen ein, so dass es Ketten bildet und die Wunde verschließt. An den Rändern setzen sich nun die Thrombozyten ab und verschließen die Wunde.
3 Insulin Maturation: Insulin ist ein für Menschen und alle Tiere lebenswichtiges Peptidhormon, das in den β- Zellen der Bauchspeicheldrüse gebildet wird. Diese spezialisierten Zellen befinden sich nur in den Langerhansschen Inseln. Wird aus dem Präproinsulin prozessiert. Es dient der Regulation der Konzentration von Traubenzucker (Glukose) im Blut. 1. Präproinsulin 2. Faltung 3. Ausbildung von Disulfidbrücken 4. Abspalten von Leader und C 5. Aktives Protein: 2 Peptidketten (21 bzw. 30 AA) Hämoglobin > Als Hämoglobin (Hb) bezeichnet man den eisenhaltigen roten Blutfarbstoff in den Erythrozyten der Wirbeltiere (und einiger Mollusken sowie weniger Crustaceen und Insekten) und seine Varianten. Es stellt wie auch das Myoglobin einen wichtigen Sauerstoff-Transporteur im Körper dar. Das Hämoglobin besteht aus vier Untereinheiten, wobei jede aus einem eisenhaltigen Protoporphyrin, dem Häm, als prosthetische Gruppe (Nichtproteinanteil) und einem Proteinanteil dem Globulin besteht. Die Häm-Gruppe ist außerdem für die rote Farbe des Hämoglobins verantwortlich.
4 Mittlere Molmasse in g/mol Idealisierte Formen: Stäbchen Ellipsoid Globulär Molmasse und Gestalt Ein wesentliches Ziel biochemischer und biophysikalischer Arbeiten ist die Charakterisierung der Gestalt von Biomolekülen und die Bestimmung ihrer Molmasse. Die Molmasse ist eine Stoffkonstante einer Substanz und keine Masse. Ein Mol eines Stoffes enthält N A = 6, Atome oder Moleküle. N A heißt Avogadro-Zahl Die Molare Masse (früher Molmasse, Atomgewicht, Molekulargewicht bzw. Molgewicht) (Formelzeichen M), ist der Quotient aus der Masse einer Substanz und der Stoffmenge dieser Substanz. Die Einheit ist Gramm pro Mol (Einheitenzeichen: g/mol) oder häufig auch Kilogramm pro Kilomol (Einheitenzeichen: kg/kmol). M = m n =N A. m M M: Molare Masse m: Masse n: Stoffmenge (Mol) m M : Molekülmasse (Summe der Atommassen bzw. Molekulargewicht) Berechnung der absoluten Molkülmasse von Wasser (H 2 O): M = 18,015 g mol -1 N A = 6, mol -1 M m = 18,015 g mol -1 / 6, mol -1 = 2, g
5 Mittlere Molare Masse (mittlere Molmasse) > Da sich biologische Makromoleküle meist nicht zu 100 % identisch oder rein sind, bezeichnet man die gemessene Molmasse auch als mittlere Molmasse, da Biomoleküle oft nicht molekular-gewichtseinheitlich sind und fast immer eine gewisse Verteilung (Streuung) in der Molmasse vorliegt. Auch intermolekulare Interaktionen machen die Bestimmung der Molaren Masse ungenauer. > Biopolymermoleküle sind polydispers d. h. die Molmasse besitzt eine gewisse Verteilung um einen zu definierenden Mittelwert ( Mstrich ). M n = i i n i M i n i M n : mittlere Molmasse M i : Molmasse eines Makromoleküls n i : Zahl der Makromoleküle gleicher Molmasse Die Molare Masse jeder niedermolekularen Verbindung lässt sich unter Verwendung stark verdünnter Lösungen durch Bestimmung - des osmotischen Drucks - des Dampfdruckes - des Gefrierpunktes - des Siedepunktes bestimmen, da diese sich durch Zugabe von kleinen Mengen eins gelösten Stoffes ändern. Kolligative Eigenschaften Unter kolligativen Eigenschaften versteht man Eigenschaften von Lösungen, die in erster Linie von der Menge des gelösten Stoffes beeinflusst werden und nicht von der Beschaffenheit der Stoffe. Zu diesen Eigenschaften zählen der Gefrierpunkt, der Siedepunkt, der Dampfdruck sowie der osmotische Druck. Der Gefrierpunkt einer Flüssigkeit wird durch die Anwesenheit von in der Flüssigkeit gelösten Stoffen gesenkt, der Siedepunkt hingegen wird erhöht. Diese beiden Phänomene eignen sich sehr gut zur Bestimmung der Molmasse von unbekannten Substanzen.
6 > Dazu wägt man eine bestimmte Masse desjenigen Stoffes, dessen Molmasse man bestimmen will, ein und löst sie in einem Lösungsmittel auf, dessen Gefrier- oder Siedepunkt bekannt ist. > Man misst nun den aktuellen Gefrier- oder Siedepunkt der Mischung und kann durch die festgestellte Differenz zwischen aktuellen Gefrier- oder Siedepunkt und den entsprechenden Daten des reinen Lösungsmittels die Stoffmenge, die in der eingewogenen Masse enthalten war, ermitteln. Auf dies Weise kann man die gesuchte Molmasse bestimmen. > Die Bestimmung der Molmasse mittels Messung der Gefrierpunktserniedrigung wird als Kryoskopie, die Bestimmung durch Messung der Siedepunktserhöhung als Ebullioskopie bezeichnet. Phasendiagramm KP (kritischer Punkt): Ist der kritische Punkt ein Zustand eines Stoffes, der sich durch Angleichen der Dichten von flüssiger- und Gasphase kennzeichnet. Die Unterschiede zwischen beiden Aggregatzuständen hören an diesem Punkt auf zu existieren. Im Phasendiagramm stellt der Punkt das obere Ende der Dampfdruckkurve dar. Wasser TP (Tripelpukt): Der Tripelpunkt des Wassers ist der einzige thermodynamische Zustand, in dem die drei Phasen Wasserdampf, Wasser und Eis im Gleichgewicht koexistieren.
7 Dampfdruckerniedrigung - Gefrierpunktserniedrigung - Siedepunktserhöhung s l g Messung der Gefrierpunktserniedrigung (Kryoskopie) Gefrierpunkt einer Lösung ist abhängig von der Zahl der im Lösungsmittel gelösten Moleküle und ist für jedes Lösungsmittel eine Konstante. Lösen von 1 Mol Substanz in 1000 g eines Lösungsmittels bewirkt die molare Gefrierpunktserniedrigung E g (wird auch als kryoskopische Konstante bezeichnet) Berechnung der Molmasse: M n = E g T. Masse gelöster Stoff Masse Lösungsmittel M n : Zahlenmittel der Molmasse E g : molare Gefrierpunktserniedrigung bzw. kryoskopische Konst. ΔT: Temperaturdifferenz Kryoskopische Konstante E g (Wasser) = 1,86 K kg mol-1.
8 Messung der Siedepunktserhöhung (Ebullioskopie) Analog zur Gefrierpunktserniedrigung bewirkt das Lösen einer Verbindung in einem Lösungsmittel auch eine molare Siedepunktserhöhung, die ebenfalls eine Molmassenbestimmung ermöglicht. Praktisches Beispiel: Gibt man Salz in kochendes Wasser, so endet der Kochvorgang zunächst, bevor das Wasser erneut zu sieden beginnt! Beide Methoden eignen sich zur Molmassenbestimmung für Mn bis ca g/mol, deshalb sind diese in der Molekularbiologie eher nicht gebräuchlich. Dampfdruckerniedrigung Löst man eine nichtflüchtige Substanz in einem flüchtigen Lösungsmittel, so sinkt der Dampfdruck. Dieser Vorgang wird als Dampfdruckerniedrigung bezeichnet: p = p1 x2 p = Dampfdruckerniedrigung p 1 = Dampfdruck des reinen Lösungsmittels X 2 = Stoffmengenanteil (Molenbruch) des Gelösten in der Lösung Physikalisch lässt sich dieser Effekt wie folgt vereinfacht erklären: Löst man z.b. Natriumchlorid in Wasser, so verteilt sich das gelöste Salz gleichmäßig darin. Dabei werden an der Oberfläche einige Wassermoleküle verdrängt und durch Salzmoleküle ersetzt. Bei gleicher Temperatur können nun weniger Wassermoleküle verdampfen. Die Kondensation bereits verdampfter Wassermoleküle hingegen wird nicht behindert. Konsequenz: Bei gleicher Temperatur stellt sicht ein niedrigerer Sättigungsdampfdruck ein.
9 > Stoffmengenanteil, ist ein Konzentrationsmaß, das den früher gebräuchlichen Molenbruch ersetzt. > Beispielsweise sind in einer Zweikomponentenmischung der Substanzen A und B deren Stoffmengenanteile xa und xb folgendermaßen definiert: xa = na/(na nb) bzw. xb = nb/(na nb). > Darin ist na bzw. nb die Anzahl der Mole der beiden Komponenten; das Mol ist die Einheit der Stoffmenge. > In Worten ausgedrückt: Der Stoffmengenanteil ist der Quotient aus der Stoffmenge (Molanzahl n) der betreffenden Komponente und der gesamten Stoffmenge (Gesamtzahl aller Mole) in der Mischung. Gemäß dieser Definition ist die Summe aller Stoffmengenanteile in einer Mischung oder Lösung stets gleich eins. Membrantransport Je kleiner die Moleküle sind, und noch wichtiger, je weniger Interaktionen diese mit H20 eingehen können, also weniger polar sind, desto leichter durchdringen diese einen Lipidbilayer. Die meisten Moleküle, welche als Nährstoffe von der Zelle benötigt werden sind zu groß bzw. zu polar!
10 Eigenschaften der Plasmamembran: Diffusionsbarriere > hydrophile Moleküle können nicht durch die Membran diffundieren > Konzentration einer Substanz im Zellinneren kann sich von ihrer Umgebungskonzentration unterscheiden > Konzentrationsgradient = chem. Gradient Ionen-Konzentrationen innerhalb und außerhalb einer Säugerzelle
11 Membranpotential Membran außen innen [K ] niedrig [K ] hoch kein Membranpotential K Ionenkanäle in der Plasmamembran sind für das Membranpotential verantwortlich K wandert durch leak channel nach außen K leak channel außen [K ] niedrig [K ] hoch innen Membranpotential
12 Elektrochemischer Gradient wichtig bei geladenen Stoffen, Ionen elektrochemischer Gradient kein Membranpotential elektrochem. Gradient = chem. Gradient Membranpotential elektrochem. Gradient = chem. Gradient Beispiele: - Protonengradient über die Mitochondrienmembran -K Gradient an der Membran von Nervenzellen Membrantransportproteine > Carrierproteine > Kanalproteine=Ionenkanäle» transportieren oft kleine org.» transportieren anorg. Ionen Moleküle (Zucker, AS, ect.) (Na, K, Ca 2, Cl-) oder Ionen» Transport des Moleküls mit Konformationsänderung des» Transport der Ionen nicht mit Carriers verbunden Konformationsänderung des Kanals verbunden» eher langsam (<10 3 Ionen/sec)» offen oder geschlossen» aktiv oder passiv» sehr schnell (10 6 Ionen/sec)» nur passiv
13 Carrierproteine Ionenkanäle Konformationsänderung Uniport, Symport, Antiport > Uniport: eine Substanz wird transportiert > Symport: zwei Substanzen werden in die gleiche Richtung transportiert > Antiport: zwei Substanzen werden in entgegengesetzter Richtung transportiert
14 passiver Transport aktiver Transport passiver Transport aktiver Transport > Transport entlang eines Konzentrationsgradienten ohne Energieaufwand > Transport gegen einen Konzentrationsgradienten mit Energieaufwand
15 Passiver Transport: Beispiel Glukosecarrier > in der Plasmamembran der meisten tier. Zellen > hat zumindest zwei Konformationen, Glukosebindungsstellen können entweder zum Zellinneren oder nach außen zeigen > der aktuelle Glukosegradient bestimmt die Transportrichtung > Beispiel Leberzellen:» nach einer Mahlzeit: viel Glukose im Blut --> Transport in die Leberzellen» bei Hunger: wenig Glukose im Blut, viel Glukose in der Zelle (durch Glykogenabbau) --> Transport ins Blut Passiver Glukosetransport durch Glukosecarrier
16 Aktiver Transport > entscheidend für Aufrechterhaltung des Stoffungleichgewichtes zw. Zellinnerem und Umgebung > Energie für aktiven Transport kommt aus» Konzentrationsgradient (gekoppelter Transport: Symport, Antiport)» ATP Hydrolyse» Membranpotential» Licht Diffusion Diffusion (v. lat.: diffundere ausgießen, verstreuen, ausbreiten ) ist ein physikalischer Prozess, der zu einer gleichmäßigen Verteilung von Teilchen und somit vollständigen Durchmischung zweier Stoffe führt. Diffusion beruht auf der thermischen Bewegung von Teilchen. Ein Molekül in Lösung erleidet in Folge thermischer Bewegungen und Schwingungen der Lösungsmoleküle von diesen je Sekunde etwa bis Stöße, die eine statistische Bewegung des Moleküls bewirken (Brownsche Bewegung). Bei ungleichmäßiger Verteilung bewegen sich statistisch mehr Teilchen aus Bereichen hoher in Bereiche geringer Konzentration bzw. Teilchendichte als umgekehrt.
17 Die Diffusionsrate ist abhängig von: > Konzentrationsgefälle an der Membran. > Molekülgröße > Fettlöslichkeit der Moleküle > Viskosität der wässrigen Phase > Dicke der hydrophoben Phase (Membran) Mittlere Verschiebungsquadrat Für die von einem diffundierenden Teilchen in der Zeit t zurückgelegte Strecke x lässt sich das mittlere Verschiebungsquadrat ausrechnen. x 2 = Ct x: mittlere zurückgelegte Strecke C: Konstante (beinhaltet den Diffusionskoeffizienten) t: Zeit Diffusionskoeffizient Grundlage: Einsteins Theorie der Brown schen Bewegung (1906) D enthält die speziellen strukturellen Eigenschaften der gelösten Moleküle, drückt im wesentlichen die Fähigkeit der Moleküle aus sich in einem Lösungsmittel bewegen zu können. D = kt 6 r k: Boltzmann Konstante T: absolute Temperatur : Viskosität der Lösung r: Radius des Moleküls D = 4.4 x 10-7 cm 2 /s für Myoglobin, Molekulargewicht D = 1.2 x 10-5 cm 2 /s für Sauerstoff, Molekulargewicht 32
18 Translationsdiffusion Stoffteilchen werden ohne Zufuhr von Energie zu einem anderen Ort transportiert (passiver Transport). Der Ausgleich von Konzentrationsunterschieden eines Stoffsystems wird durch die sog. Fick schen Gesetze beschrieben. Treibende Kraft der Translationsdiffusion ist ein Konzentrationsgefälle. Adolph Fick formulierte Gesetzmäßigkeiten, die die Zusammenhänge zwischen einer Partikel-Diffusionsstromdichte L und der Konzentrationsveränderung c auf einer Strecke x erfassen. Gelöste Teilchen bewegen sich aus einem Bereich hoher Konzentration solange in den Bereich niedriger Konzentration bis eine einheitliche Konzentration herrscht. Der Fluß der gelösten Teilchen ist proportional zum Konzentrationsgradienten (1. Fick sche Gesetz). Dieses Gesetz beschreibt die Diffusion aufgrund eines Konzentrationsgefälles, es kennt keine zeitliche Änderung, das Konzentrationsgefälle darf sich nicht ändern. Es beschreibt die Geschwindigkeit des Diffusionsvorganges. 1. Fick sche Gesetz J = n t = -D c x J: Partikel-Diffusionsstromdichte n: Teilchenzahl t: Zeit D: Diffusionskoeffizient c: Konzentration x: Weglänge c/ x: Konzentrationsgefälle n/ t: Teilchenstrom durch den Querschnitt A Der negative Wert bezeichnet die Bewegung der Teilchen weg von der konzentrierten Lösung zur weniger konzentrierten.
19 Das 2. Fick sche Gesetz Das 2. Fick sche Gesetz behandelt die zeitabhängige Diffusion. Die Konzentration variiert als Funktion von Ort und Zeit. c t x 2 c D 2 x t Messung des Diffusionskoeffizienten Die zu untersuchende Lösung wird mit reinem Lösungsmittel überschichtet. Extinktion (Abschwächung einer Strahlung) der absorbierenden Biomoleküle wird im Abstand x von der Überschichtungsgrenze gemessen. Messung der Diffusion von Teilchen in Lösung nach Herausnahme des Schiebers durch Zunahme der Extinktion mit der Zeit.
20 Osmometrie Die Osmose beschreibt die gerichtete Diffusion von Lösungsmittel durch eine selektiv permeable Membran. Triebkraft dieser Bewegung ist das Potentialgefälle (z.b. der Konzentrationsunterschied) zwischen beiden Seiten der Membran. Die resultierende Bewegung des Lösungsmittels vergrößert (bei konstant gehaltenem Volumen) den Druck auf einer Seite der Membran. Diesen Druckunterschied bezeichnet man als osmotischen Druck. In der biologischen Literatur wird Osmose, wegen ihrer Bedeutung für lebende Organismen, in vereinfachender Weise oft nur für wässerige Lösungen beschrieben. Sind 2 wässrige Lösungen verschiedener Konzentration durch eine semipermeable (halbdurchlässige) Membran getrennt, so versucht die konzentrierte Lösung sich durch Aufnahme von Wasser zu verdünnen. : reine Lösungsmittelphase : flüssige Mischphase (Lösung) enthält den Stoff S Zwischen und baut sich eine Druckdifferenz auf. steht dabei unter einem Zusatzdruck, dem osmotischen Druck. = p -p isotonisch: Der osmotische Druck auf beiden Seiten der Membran ist gleich. hypotonisch: Die Konzentration einer gelösten Substanz (z.b. in der Zelle) ist niedriger als in der Vergleichslösung (z.b. der Umgebung der Zelle) hypertonisch: Die Konzentration einer gelösten Substanz ist höher als in der Vergleichslösung. Wasser wandert so lange aus einer hypotonischen in eine hypertonische Lösung ein, bis beide isotonisch sind.
21 Osmose in biologischen Systemen Jede Zelle hat stets mit osmotischen Erscheinungen zu kämpfen. Zellwandlose Zellen in wässriger Lösung sind in der Regel hypertonisch, d.h., es erfolgt in sie ein kontinuierlicher Wassereinstrom, der seinerseits einen Druck von innen auf die Membran ausübt. Bei einigen Ciliaten (z.b. Paramecium) und Flagellaten (z.b. Euglena) wird es mittels pulsierender Vakuolen wieder herausgepumpt. Erythrozyten kommen normalerweise in einer isotonischen Umgebung (Blutplasma) vor. Verdünnt man Blut mit Wasser, platzen die Zellen, da die Membran dem osmotischen Druck des Zellinneren nicht standhält. Man kann das Platzen unterbinden, wenn man das Blut mit einer isotonischen Lösung (0,9 prozentige NaCl- Lösung = physiologische Kochsalzlösung) verdünnt. Pflanzenzellen Ist der osmotische Wert in der Zelle höher als im umgebenden Apoplasten, nimmt sie durch Osmose Wasser auf. Der in ihrem Inneren ansteigende Druck spannt die umgebende Zellwand. Aufgefangen wird der Turgor durch den elastischen Wanddruck, der ihm entgegenwirkt. Hat der Turgor seinen größtmöglichen Wert, so spricht man von voller Turgeszenz. Ist dagegen der osmotische Wert des umgebenden Milieus größer als im Zellsaft (hypertonisches Milieu), nimmt der Turgor ab und der Protoplast löst sich von der Zellwand (? Plasmolyse). Auf dem Zusammenspiel von Turgor und Wanddruck beruht die Festigkeit krautiger, nichtverholzter Pflanzen. Durch Änderungen des Turgor der Schließ- oder Nebenzellen kann die Pflanze den Öffnungszustand der Stomata (Spaltöffnungen) kontrollieren.
22 Ermittlung der Molmasse durch Messung des osmotischen Druckes Lösung und reines Lösungsmittel sind durch eine halbdurchlässige Membran getrennt Lösungsmittel diffundiert solange in die Lösung, bis sich ein Gleichgewicht eingestellt hat. Der osmotische Druck ist die Druckdifferenz, die sich zwischen Lösung und Lösungsmittel aufbaut. Mit Hilfe des van t Hoffschen Gesetzes kann man die molare Masse des gelösten Stoffes bestimmen. Der osmotische Druck kann bereits für kleine Konzentrationen bestimmt werden, wo die zunächst genannten Methoden (Kryoskopie und Ebullioskopie) versagen. Die Methode ist besonders geeignet zur Bestimmung der Molmasse von Polymeren bis ca g/mol. Van t Hoffsches Gesetz (Analog zur idealen Gasgleichung) Formel Anmerkung V Stoff R T Van t Hoffsches Gesetz Osmotischer Druck Stoff Anzahl der im Volumen V der Lösung befindlichen Mol des gelösten Stoffes V, R, T Volumen der Lösung, allgemeine Gaskonstante und Temperatur in K Aufgrund von Wechselwirkungen zwischen dem gelösten Stoff und den Lösungsmittelmolekülen, und zwischen den gelösten Molekülen untereinander, muss die Formel noch angepasst werden keine ideale Lösung.
23 Viskosimetrie Unter dem Begriff der Viskosimetrie (auch Viskometrie) werden alle Methoden zusammengefasst, mit denen Viskositäten (innere Reibung, Zähigkeit) von fluiden Medien (insbesondere von Flüssigkeiten) bestimmt werden. Makromoleküle erhöhen schon in geringer Konzentration die Viskosität beträchtlich. Die Viskositätserhöhung ist nicht nur vom Molekulargewicht sondern auch von der Konformation der Makromoleküle abhängig. Diese Konformation ist wiederrum abhängig vom Lösungsmittel und von der Meßtemperatur. Je verzweigter ein Molekül, desto viskoser ist die Flüssigkeit. Ursache viskosen Verhaltens Die Verschiebung einer gedachte Flüssigkeitsschicht ist gegenüber einer anderen Schicht nur unter Aufwendung einer Kraft möglich. Es tritt eine Reibungskraft zwischen den Schichten auf, die überwunden werden muss. F Reib = A ( ) dv dx Die Reibungskraft F Reib ist umso größer, je größer die zu bewegende Fläche A, die Geschwindigkeitsdifferenz dv und je kleiner der Abstand dx der Schichten ist. =Viskositätskoeffizient (dynamische Viskosität)
24 Das Ostwald-Viskosimeter ist ein Gerät zur Bestimmung der Viskosität von Flüssigkeiten in der physikalischen Chemie. Es wurde von Wolfgang Ostwald entwickelt. = K L t : Viskosität K : Gerätekonstante L : Dichte der Lösung t: Druchflußzeit Das Viskosimeter gehört zu den Kapillarviskosimetern, bei denen die Viskosität der Flüssigkeit durch Zeitmessung bestimmt wird. Man bestimmt die Zeit, die ein Meßvolumen benötigt um durch eine Kapillare zu strömen. Die Bestimmung von Viskositäten makromolekularer Lösungen erfolgt durch Vergleich mit dem reinen Lösungsmittel. Durch Messung von Viskositäten von verschieden konzentrierten Lösungen, kann die mittlere Molmasse der gelösten Substanz ermittelt werden. Sedimentation Durch das Gravitationsfeld werden Teilchen beschleunigt und wandern in Richtung des Gravitationszentrums. F schwer = mg F schwer = Schwerkraft m = Masse g = Erdbeschleunigung = 9,81 m/s 2 Wenn Teilchen in Lösung schwimmen, so verdrängen sie dabei Lösung der Masse m L. Dadurch wirkt auf die Teilchen neben der Schwerkraft F schwer noch eine Auftriebskraft F auf : F auf = m L g F auf = Auftriebskraft m L = Masse der verdrängten Lösung g = Erdbeschleunigung = 9,81 m/s 2
25 Effektiv treibenden Kraft im Schwerefeld: F treib = F schwer F auf = mg( 1 - L ) F treib : Treibende Kraft im Schwerefeld Auftriebsfaktor: 1-( L/ ) L : Dichte der Lösung : Effektive Dichte des Teilchens Die Geschwindigkeit der sinkenden Moleküle nimmt infolge der effektiven treibenden Kraft zunächst zu. Damit steigt jedoch die Reibungskraft F reib. F reib : Reibungskraft F reib = fv f: Reibungskoeffizient v: Geschwindigkeit Die Reibungskraft wächst proportional mit der Geschwindigkeit. Im Sedimentationsmedium erreichen die Teilchen schnell ihre Endgeschwindigkeit. Im Kräftegleichgewicht, also wenn F treib = F reib ist, gilt für kugelförmige Teilchen f=6 R s v. Daraus ergibt sich folgende Geschwindigkeit mit der die Teilchen sinken: ( 2R 1 - s2 g v = 9 L ) R s : Partikelradius : Viskosität
26 v = 2R s2 g(1 - L) 9 > Die Teilchen sinken mit einer Geschwindigkeit, die proportional Ihrem Radius, der effektiven Teilchendichte und dem Auftriebsfaktor ist. Sie sinken umso langsamer, je größer die Viskosität der Flüssigkeit ist. > Die Absenkungsgeschwindigkeit ist für große Teilchen größer als für Kleine: dadurch wird eine Bestimmung der Masse möglich. > Sedimentationsmessung: Absenkgeschwindigkeit sollte wesentlich größer sein, als die Diffusionsgeschwindigkeit, d. h. das ist nur bei relativ großen Teilchen der Fall (Blut- oder Hefezellen). Kleinere Teilchen (R s ca. 5 nm und kleiner) zeigen praktisch keine Sedimentation. > Mit Hilfe einer Ultrazentrifuge, in der sich eine über 105-fache Erdbeschleunigung erzielen lässt, kann die Absenkgeschwindigkeit drastisch erhöht werden, sodass auch für kleinere Teilchen die Molekülmasse ermittelt werden kann. Zentrifugation Trennung von Substanzen unterschiedlicher Masse durch Zentrifugalkraft. Prinzipiell handelt es sich um ein Sedimentationsverfahren, bei dem die durch die Gewichtskraft bewirkte Abtrennung von Teilchen unterschiedlicher Dichte mit Hilfe der Zentrifugalkraft beschleunigt wird.
27 Zentrifugentypen Tischzentrifugen Niedrigtourig, max rpm, gekühlt/ungekühlt, Normaldruck. Standzentrifugen Hochtourig, max rpm, idr. gekühlt, Vakuum.
28 Ultrazentrifugen Bis g, rpm, gekühlt, Hochvakuum Zentrifugen beinhalten durch ihre Hohen Zentrifugalkräfte ein großes Gefährdungspotential. Schutzmaßnahmen: Schutzgehäuse, Deckel mit Elektrischen Unterbrecherschalter, Automatische Unwuchtkontrolle d. H. kein Start bei Unwucht oder Ungenauer Rotorfixierung.
29 Zentrifugationstechniken > Differentielle Zentrifugation Ausnützen unterschiedlicher Sedimentationsgeschwindigkeiten im Festwinkelrotor. Stufenweise höheren Zentrifugalbeschleunigungen bei schrittweise verlängerten Zentrifugationszeiten. Trennung von Überstand und Pellet. Abb.2: Differentialzentrifugation von zwei Substanzen mit unterschiedlichen Sedimentationskoeffizienten. > Dichtegradientenzentrifugation Zentrifugation in einem Dichtegradienten (isopyknische Zentrifugation), (CsCl, Sucrose, Polysaccharide, Ficoll)» Fertiger Gradient: z. B. Zonenzentrifugation» Selbstbildender Gradient: z. B. Isopyknische Zentrifugation Abb.3: Zonenzentrifugation. Nach Bildung des Dichtegradienten wird die Probe aufgetragen. Im Zentrifugalfeld kommt es zur Trennung der Substanzen. Abb. 4: Isopyknische Zentrifugation im selbstbildenden Gradienten. Aus einer homogenen Lösung bildet sich unter dem Einfluß der Zentrifugalkraft ein Gradient aus, und die Substanzenbanden entsprechend ihrer Dichte.
30 Differentielle Zentrifugation Dichtegradientenzentrifugation
31 CsCl-Gradient Isolierung von DNA mittels Ultrazentrifugation Unter hohen zentrifugalen Kräften dissoziiert CsCl, und die schweren Cs -Atome werden gegen das untere Ende des Zentrifugenröhrchens gedrängt, sodass ein flacher Dichtegradient entsteht. In solch einem Gradienten wandern DNA Moleküle zu jenem Punkt, an dem die Dichte zwischen DNA und Gradient ident ist (isopyknische Zentrifugation). Der Gradient reicht aus, um DNA-Typen mit kleinen Differenzen in deren Dichte zu trennen (z. B. unterschiedlicher G-C Gehalt, lineare vs. Zirkuläre DNA) In dem Experiment links, konnten nach einer Zentrifugation für 10 Stunden bei rpm (450000g) zwei Banden unterschieden werden: eine für die lineare Kern-DNA und eine für die zirkuläre Mitochondrien-DNA. Aufreinigung von Plasmid DNA Abb.2 CsCl-Dichtegradienten-Zentrifugation zur Isolierung von Plasmid DNA. Gradientenmischer: Das Prinzip der Trennung von chromosomaler und Plasmid-DNA erfolgt während der Zentrifugation in Gegenwart von Ethidiumbromid. Ethidiumbromid interkaliert zwar auch in Doppelstrang-DNA wie die kovalent geschlossene ringförmige Form (supercoil) des Plasmids, jedoch lagern lineare DNA- Doppelstränge oder durch einen Einzelstrangbruch geöffnete Plasmide (nicked circled-dna) erheblich mehr Ethidiumbromid ein, das die Schwimmdichte dieser DNA-Formen erhöht. RNA-Ethidiumbromid- Komplexe weisen eine deutlich größere Dichte als die maximale Dichte des Gradienten auf und akkumulieren am Rand des Röhrchens. Die DNA-Bande kann nach der Zentrifugation unter UV-Licht mit Hilfe einer Kanüle aus dem CsCl- Gradienten abgezogen werden. Links oben in gelb befindet sich eine Lösung geringer Dichte. Rechts oben in blau befindet sich eine Lösung hoher Dichte. Der Behälter rechts oben wird gerührt, während von links die Lösung geringer Dichte zuläuft, und die Mischung der beiden Lösungen nach unten in den Gradienten-Behälter abläuft, wo sich die nachfolgenden Schichten geringerer Dichte über die vorher gehenden lagern. Auf diese Weise entstehen lineare Gradienten.
32 Meselson-Stahl Experiment Für ihr Experiment züchteten die Forscher zunächst Bakterien auf einem Nährmedium, welches ausschließlich ein Stickstoffisotop mit der Masse 15 enthielt. Dieses wurde dann von den Bakterien in ihre DNA integriert. Anschließend wurden Bakterien dieses Stammes auf ein Nährmedium aufgebracht, welches Stickstoff mit einer Masse von 14 enthielt. Nach einer Weile wurden dann Bakterien der F1- Generation entnommen und ihr Erbgut einer Dichtegradientenzentrifugation unterworfen. Es zeigte sich, dass die Sedimentationsebene der Bakterien-DNA genau zwischen den Referenzebenen von DNA, die ausschließlich 14 bzw. 15 Stickstoff enthielt, lag. Weiters wurde der Vorgang mit Individuen der F2-Generation wiederholt. Dabei ergab sich, dass das Erbgut der Bakterien zur Hälfte in der Ebene der F1- Generation und zur Hälfte in der 14-Referenzebene sedimentierte. Das Ergebnis entspricht genau den Vorhersagen der semikonservativen Theorie, d. H. Bei der Replikation der Erbinformation bleibt die Mutter- DNA in jedem Tochter-Molekül zur Hälfte erhalten. Die andere Hälfte wird neu ergänzt. Rotortypen
33 Nomogramm Zentrifugation Zur Bestimmung des RCF-Wertes bzw. des rpm-wertes > Die Erdbeschleunigung kann aus der Rotationsgeschwindigkeit und dem Rotordurchmesser für jeden Rotor berechnet werden. In einem Nomogramm kann dieser Wert graphisch abgelesen werden. Zentrifugation In der Zentrifuge wird statt der Schwerkraft die Zentrifugalkraft (oder Radialkraft) F z wirksam, die bei einer Kreisbewegung auftritt. Wird eine Masse m mit einer Geschwindig- Keit v im Abstand r um ein Drehzentrum bewegt, so ist die Zentrifugalkraft die auf diese Teilchen wirkt: F z = m 2 r Winkelgeschwindigkeit v/r v V: Umlauffrequenz (Drehzahl) des Motors=rpm/60 Die Zentrifugalkraft ist der Zentrifugalbeschleunigung (a= 2 r) proportional.
34 Korrektur für den Auftrieb: Auftriebsfaktor 1- L / r( F z = m 2 1- ) L RCF (relative centrifugal force) RCF = x r x rpm RCF ist die relative Zentrifugalbeschleunigung (Kraft) in Einheiten der Gravitationsbeschleunigung g auf der Erdoberfläche. Der Wert RCF wird in Publikationen angegeben (z. b x g), er berücksichtigt die wirksame Beschleunigung unabhängig vom Modell der im Labor verwendeten Zentrifuge (Umdrehungsgeschwindigkeit der Zentrifuge rpm und Größe des verwendeten Rotors r = Rotationsradius) Sedimentationskoeffiezient - Svedberg-Konstante Die Svedberg-Einheit S gibt an, mit welcher Geschwindigkeit sich große Moleküle oder kleine Teilchen im Einheitsbeschleunigungsfeld einer Ultrazentrifuge ablagern Mass für die Sedimentation. s = v 2 r Die Zentrifugalkraft beschleunigt das Teilchen radial nach außen. Mit zunehmender Geschwindigkeit des Teilchens steigt die Reibung zwischen dem sedimentierenden Teilchen und dem umgebenden Medium an. Die Sedimentation des Teilchens wird so lange beschleunigt, bis der Reibungswiderstand gleich der Zentrifugalkraft ist. Dividiert man diese Sedimentationsgeschwindigkeit v durch die Stärke des Zentrifugalfelds ω2 r, so erhält man eine Größe, die nur noch von der Beschaffenheit des Teilchens und seinem Reibungskoeffizienten in dem betreffenden Medium abhängig ist. Diese Größe wird als Sedimentationskoeffizient s bezeichnet. 1 S = s
35 > Die Sedimentationsgeschwindigkeit eines Teilchens ist seiner Masse proportional. > Ein dichtes Teilchen bewegt sich schneller als ein weniger dichtes, da die Auftriebskraft für ein dichtes Teilchen geringer ist. > Form eines Teilchens spielt eine Rolle: Reibungskoeffizient eines kugelförmigen Teilchens ist kleiner als eines ausgedehnten Teilchens gleicher Masse. > Molmasse ist nur näherungsweise bestimmbar. > Sedimentationsgeschwindigkeit hängt von der Dichte der Lösung ab. Teilchen sinken, wenn die effektive Dichte des Teilchens größer ist als die des LM, sie schwimmen wenn sie kleiner ist und sie schweben wenn sie gleich sind. Bestimmung des Sedimentationskoeffizienten Messen von Absenkgeschwindigkeit v, Umlauffrequenz des Rotors, Abstand der Teilchen zur Rotorachse r. s = v 2 r Zu Beginn der Zentrifugation ist die Lösung homogen. Die Grenzfläche der gelösten Teilchen bewegt sich bei der Sedimentation allmählich nach außen. Zentraler Schnitt durch die UZ-Zelle mit einem sektorenförmigen Ausschnitt, in dem sich die Lösung befindet. Die Zentrifugalkraft bewirkt die Sedimentation in Richtung auf den Unterteil der Zelle (aussen).
36 Bestimmung der Konzentration bzw. des Konzentrationsgradienten der Lösung an beliebiger Stelle der Flüssigkeitssäule während der Zentrifugation. a b c d Zu Beginn der Sedimentation sind die makromolekularen Partikel gleichförmig verteilt (a). Dann bildet sich ein Konzentrationsgradienten-Maximum (cd/cx) aus (b), das langsam in Richtung des Zellenbodens wandert (Verbreiterung durch Diffusion (c)) und schließlich den Bodensatz erreicht (d). Bestimmung der Molekülmasse aus dem Sedimentationskoeffizienten s = v 2 r = M (1-V ) N AV f s: Sedimentationskoeffiezient v: Sedimentationsgeschwindigkeit : Umlauffrequenz des Rotors r: Abstand zur Rotorachse M: Molekülmasse V: partielles spezifisches Volumen des Teilchens : Dichte der Lösung N AV : Avogadrosche Zahl f: Reibungskoeffizient des Moleküls
37 Dichteverteilung und Sedimentationskoeffizienten
Die Zelle. Membranen: Struktur und Funktion
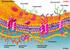 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Passive Transportvorgänge
 Passive Transportvorgänge Diffusion und Osmose sind passive Transportprozesse. Denn die Zelle muss keine Energie aufwenden, um den Transport der Stoffe zu ermöglichen. Diffusion Einzelsubstanzen sind bestrebt,
Passive Transportvorgänge Diffusion und Osmose sind passive Transportprozesse. Denn die Zelle muss keine Energie aufwenden, um den Transport der Stoffe zu ermöglichen. Diffusion Einzelsubstanzen sind bestrebt,
Sedimentation, Elektrophorese
 Sedimentation, Elektrophorese MEDIZINISCHE PHYSIK UND STATISTIK 2. Dr. Tamás Huber Institut für Biophysik 17. März 2016. Trennungsmethoden Trennverfahren in der Chemie oder Physik helfen dabei, zwei oder
Sedimentation, Elektrophorese MEDIZINISCHE PHYSIK UND STATISTIK 2. Dr. Tamás Huber Institut für Biophysik 17. März 2016. Trennungsmethoden Trennverfahren in der Chemie oder Physik helfen dabei, zwei oder
Diffusion. Prüfungsfrage
 Prüfungsfrage Diffusion Die Diffusion. Erstes Fick sches Gesetz. Der Diffusionskoeffizient. Die Stokes-Einstein Beziehung. Diffusion durch die Zellmembrane: passive, aktive und erleichterte Diffusion Lehrbuch
Prüfungsfrage Diffusion Die Diffusion. Erstes Fick sches Gesetz. Der Diffusionskoeffizient. Die Stokes-Einstein Beziehung. Diffusion durch die Zellmembrane: passive, aktive und erleichterte Diffusion Lehrbuch
2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg
![2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg 2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg](/thumbs/75/72774995.jpg) 2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
Zustandsbeschreibungen
 Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
Aggregatzustände fest Kristall, geordnet Modifikationen Fernordnung flüssig teilgeordnet Fluktuationen Nahordnung gasförmig regellose Bewegung Unabhängigkeit ngigkeit (ideales Gas) Zustandsbeschreibung
4 Theorie Zentrifugationstechniken zur Reinigung von Purpurmembranen und Kontrolle der Bakteriorhodopsinrekonstitution
 4 Theorie Zentrifugationstechniken zur Reinigung von Purpurmembranen und Kontrolle der Bakteriorhodopsinrekonstitution in Liposomen Unter dem Einfluss der Schwerkraft sedimentieren größere Teilchen in
4 Theorie Zentrifugationstechniken zur Reinigung von Purpurmembranen und Kontrolle der Bakteriorhodopsinrekonstitution in Liposomen Unter dem Einfluss der Schwerkraft sedimentieren größere Teilchen in
Diffusion und Osmose. Osmose 1
 Osmose 1 Diffusion und Osmose In flüssigen oder gasförmigen Medien sind die Moleküle in ständiger Bewegung. Sie bewegen sich gradlinig, bis sie auf ein anderes Molekül stossen. Diese Bewegung führt mit
Osmose 1 Diffusion und Osmose In flüssigen oder gasförmigen Medien sind die Moleküle in ständiger Bewegung. Sie bewegen sich gradlinig, bis sie auf ein anderes Molekül stossen. Diese Bewegung führt mit
Cholesterolmoleküle. Membranproteine können Zellen. miteinander verknüpfen. tragen Kohlenhydratketten. Manche Lipide (Glykolipide)
 Zellinnenraum Manche Lipide (Glykolipide) tragen Kohlenhydratketten. Membranproteine können Zellen miteinander verknüpfen. Manche Proteine (Glykoproteine) tragen Kohlenhydratketten. Cholesterolmoleküle
Zellinnenraum Manche Lipide (Glykolipide) tragen Kohlenhydratketten. Membranproteine können Zellen miteinander verknüpfen. Manche Proteine (Glykoproteine) tragen Kohlenhydratketten. Cholesterolmoleküle
Versuch 9: Siedepunktserhöhung und Gefrierpunktserniedrigung
 1 Versuch 9: Siedepunktserhöhung und Gefrierpunktserniedrigung 1. Theorie und Aufgabenstellung Theorie und Methode Lösungen bestehen aus einem Lösungsmittel und dem darin gelösten Stoff. Das Lösemittel
1 Versuch 9: Siedepunktserhöhung und Gefrierpunktserniedrigung 1. Theorie und Aufgabenstellung Theorie und Methode Lösungen bestehen aus einem Lösungsmittel und dem darin gelösten Stoff. Das Lösemittel
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Kinetische Gastheorie - Die Gauss sche Normalverteilung
 Kinetische Gastheorie - Die Gauss sche Normalverteilung Die Gauss sche Normalverteilung Die Geschwindigkeitskomponenten eines Moleküls im idealen Gas sind normalverteilt mit dem Mittelwert Null. Es ist
Kinetische Gastheorie - Die Gauss sche Normalverteilung Die Gauss sche Normalverteilung Die Geschwindigkeitskomponenten eines Moleküls im idealen Gas sind normalverteilt mit dem Mittelwert Null. Es ist
Abbildung 1: Diffusionsverbreiterung im zeitlichen Verlauf eines Sedimentationsgeschwindigkeitsexperiments
 Diffusion Einführung Zusätzlich zu den Sedimentations-, Auftriebs- und Reibungskräften unterliegt ein Partikel im Zentrifugalfeld der ungerichteten und der gerichteten (wechselseitigen) Diffusion. Dabei
Diffusion Einführung Zusätzlich zu den Sedimentations-, Auftriebs- und Reibungskräften unterliegt ein Partikel im Zentrifugalfeld der ungerichteten und der gerichteten (wechselseitigen) Diffusion. Dabei
Biologie der Zelle. Inhaltsverzeichnis 1... STOFFTRANSPORT DURCH MEMBRANEN 2
 Hochschule RheinMain University of Applied Sciences Biologie der Zelle Inhaltsverzeichnis Seite 1... STOFFTRANSPORT DURCH MEMBRANEN 2 1.1 Zelle als osmotisches System... 2 1.1.1 Plasmolyse... 2 1.1.2 Deplasmolyse...
Hochschule RheinMain University of Applied Sciences Biologie der Zelle Inhaltsverzeichnis Seite 1... STOFFTRANSPORT DURCH MEMBRANEN 2 1.1 Zelle als osmotisches System... 2 1.1.1 Plasmolyse... 2 1.1.2 Deplasmolyse...
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen!
 1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol
![Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol](/thumbs/50/26795947.jpg) 2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
dm A A = D --- (c 1 -c 2 ) = D --- δ c dt d d D: Diffusionskonstante, A: Betrachtete Fläche, d: Strecke c: Konzentration
 Diffusion ist die Bewegung von Teilchen aufgrund der brownschen Molekularbewegung in einem Lösungsmittel. Die Teilchen bewegen sich netto in Richtung der niedrigeren Konzentration. Ficksches Diffusionsgesetz:
Diffusion ist die Bewegung von Teilchen aufgrund der brownschen Molekularbewegung in einem Lösungsmittel. Die Teilchen bewegen sich netto in Richtung der niedrigeren Konzentration. Ficksches Diffusionsgesetz:
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 1. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 1: Übersicht 2 Zustandsgrößen 2.1 Thermische Zustandsgrößen 2.1.1 Masse und Molzahl 2.1.2 Spezifisches
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 1: Übersicht 2 Zustandsgrößen 2.1 Thermische Zustandsgrößen 2.1.1 Masse und Molzahl 2.1.2 Spezifisches
STOFFTRANSPORT DURCH BIOMEM- BRANEN
 DIE BIOMEMBRAN Vorkommen Plasmalemma Grenzt Cytoplasma nach außen ab Tonoplast Grenzt Vakuole vom Cytoplasma ab Zellkernmembran Mitochondrienmembran Plastidenmembran ER Kompartimente Durch Zellmembran
DIE BIOMEMBRAN Vorkommen Plasmalemma Grenzt Cytoplasma nach außen ab Tonoplast Grenzt Vakuole vom Cytoplasma ab Zellkernmembran Mitochondrienmembran Plastidenmembran ER Kompartimente Durch Zellmembran
 Sinkt ein Körper in einer zähen Flüssigkeit mit einer konstanten, gleichförmigen Geschwindigkeit, so (A) wirkt auf den Körper keine Gewichtskraft (B) ist der auf den Körper wirkende Schweredruck gleich
Sinkt ein Körper in einer zähen Flüssigkeit mit einer konstanten, gleichförmigen Geschwindigkeit, so (A) wirkt auf den Körper keine Gewichtskraft (B) ist der auf den Körper wirkende Schweredruck gleich
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Dissoziationsgrad und Gefrierpunkterniedrigung (DIS) Gruppe 8 Simone Lingitz, Sebastian Jakob
 Dissoziationsgrad und Gefrierpunkterniedrigung (DIS) Gruppe Simone Lingitz, Sebastian Jakob . Versuch. Versuchsaufbau Durch die Bestimmung der Gefrierpunktserniedrigung beim Lösen von KNO bzw. NaNO in
Dissoziationsgrad und Gefrierpunkterniedrigung (DIS) Gruppe Simone Lingitz, Sebastian Jakob . Versuch. Versuchsaufbau Durch die Bestimmung der Gefrierpunktserniedrigung beim Lösen von KNO bzw. NaNO in
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung
 Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Lösungen, Stoffmengen und Konzentrationen
 12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
Kinematik & Dynamik. Über Bewegungen und deren Ursache Die Newton schen Gesetze. Physik, Modul Mechanik, 2./3. OG
 Kinematik & Dynamik Über Bewegungen und deren Ursache Die Newton schen Gesetze Physik, Modul Mechanik, 2./3. OG Stiftsschule Engelberg, Schuljahr 2016/2017 1 Einleitung Die Mechanik ist der älteste Teil
Kinematik & Dynamik Über Bewegungen und deren Ursache Die Newton schen Gesetze Physik, Modul Mechanik, 2./3. OG Stiftsschule Engelberg, Schuljahr 2016/2017 1 Einleitung Die Mechanik ist der älteste Teil
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Physikalisches Anfaengerpraktikum. Dissoziationsgrad und Gefrierpunkterniedrigung
 Physikalisches Anfaengerpraktikum Dissoziationsgrad und Gefrierpunkterniedrigung Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe ) Montag, 1. Februar 00 1. Versuchsaufbau Um den Dissoziationsgrad
Physikalisches Anfaengerpraktikum Dissoziationsgrad und Gefrierpunkterniedrigung Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe ) Montag, 1. Februar 00 1. Versuchsaufbau Um den Dissoziationsgrad
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät
 Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät Grundlagen Lipid-Doppelschicht als Barriere für polare Moleküle! Abgrenzung für biochemische
Zellbiologie! Privatdozent Dr. T. Kähne! Institut für Experimentelle Innere Medizin! Medizinische Fakultät Grundlagen Lipid-Doppelschicht als Barriere für polare Moleküle! Abgrenzung für biochemische
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Dynamik. 4.Vorlesung EPI
 4.Vorlesung EPI I) Mechanik 1. Kinematik 2.Dynamik a) Newtons Axiome (Begriffe Masse und Kraft) b) Fundamentale Kräfte c) Schwerkraft (Gravitation) d) Federkraft e) Reibungskraft 1 Das 2. Newtonsche Prinzip
4.Vorlesung EPI I) Mechanik 1. Kinematik 2.Dynamik a) Newtons Axiome (Begriffe Masse und Kraft) b) Fundamentale Kräfte c) Schwerkraft (Gravitation) d) Federkraft e) Reibungskraft 1 Das 2. Newtonsche Prinzip
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #7 28/10/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Mechanik Teil 3 - Versuche M1 Dichte und Hydrodynamik: Bestimmung der Dichte eines zylindrischen
Physik für Mediziner im 1. Fachsemester #7 28/10/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Mechanik Teil 3 - Versuche M1 Dichte und Hydrodynamik: Bestimmung der Dichte eines zylindrischen
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11
 Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
Übungen zur Vorlesung Physikalische Chemie 1 (B. Sc.) Lösungsvorschlag zu Blatt 11 Prof. Dr. Norbert Hampp Jens Träger Sommersemester 2007 02. 07. 2007 Aufgabe 1 a) Die Dampfdrücke nach dem Raoult schen
MPA 1. Sem., Musterprüfung 1: Seite 1. Musterprüfung
 MPA 1. Sem., Musterprüfung 1: Seite 1 Musterprüfung Prüfungsdatum: 28. Okt. 2013 1. Modul: Diffusion und Osmose 1.1. Ein Körper besteht aus Molekülen. Diese Moleküle sind fortwährend in Bewegung. Wie wird
MPA 1. Sem., Musterprüfung 1: Seite 1 Musterprüfung Prüfungsdatum: 28. Okt. 2013 1. Modul: Diffusion und Osmose 1.1. Ein Körper besteht aus Molekülen. Diese Moleküle sind fortwährend in Bewegung. Wie wird
Übungen zur Vorlesung Physikalische Chemie I Lösungsvorschlag zu Blatt 7
 1. Aufgabe Die kyroskopische Konstante E k und die ebulloskopische Konstante E e werden wie folgt berechnet. E k Wasser = R T 2 schmelz M H schmelz = 8,31451 J 273,15 K 2 18,02 10 3 kg mol = 1,86 K kg
1. Aufgabe Die kyroskopische Konstante E k und die ebulloskopische Konstante E e werden wie folgt berechnet. E k Wasser = R T 2 schmelz M H schmelz = 8,31451 J 273,15 K 2 18,02 10 3 kg mol = 1,86 K kg
Grund- und Angleichungsvorlesung Fluidkinematik.
 1 Grund- und Angleichungsvorlesung Physik. Fluidkinematik. SS 18 2. Sem. B.Sc. LM-Wissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe
1 Grund- und Angleichungsvorlesung Physik. Fluidkinematik. SS 18 2. Sem. B.Sc. LM-Wissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe
Basiskenntnistest - Physik
 Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10
 Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Lars
Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Lars
Kolligative Eigenschaften
 Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Totipotent: Pluripotent:
 E BIO 1 KW 39 Totipotent: Pluripotent: Zellorganellen Stadtzeitung Lübeck (Ausgabe vom 13. Januar 2003) Salzstreuen verboten - Bereich warnt vor Umweltschäden Streusalz als Auftaumittel zu nehmen, ist
E BIO 1 KW 39 Totipotent: Pluripotent: Zellorganellen Stadtzeitung Lübeck (Ausgabe vom 13. Januar 2003) Salzstreuen verboten - Bereich warnt vor Umweltschäden Streusalz als Auftaumittel zu nehmen, ist
Masse, Kraft und Beschleunigung Masse:
 Masse, Kraft und Beschleunigung Masse: Seit 1889 ist die Einheit der Masse wie folgt festgelegt: Das Kilogramm ist die Einheit der Masse; es ist gleich der Masse des Internationalen Kilogrammprototyps.
Masse, Kraft und Beschleunigung Masse: Seit 1889 ist die Einheit der Masse wie folgt festgelegt: Das Kilogramm ist die Einheit der Masse; es ist gleich der Masse des Internationalen Kilogrammprototyps.
Lernziele: Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme,
 Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Modelle zur Beschreibung von Gasen und deren Eigenschaften
 Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
für jede Gasart x (analog für Flüssigkeiten, sogar Festkörper)...Dichte, z-richtung.. auf A
 6.5 Diffusion, Osmose und Dampfdruck: Z7/vo/mewae/Kap6_5DiffosmDampfdr_s3_040118 Diffusion: Eindringen eines Stoffes in einen anderen auf Grund der Wärmebewegung. Experiment: ruhende, verschieden gefärbte
6.5 Diffusion, Osmose und Dampfdruck: Z7/vo/mewae/Kap6_5DiffosmDampfdr_s3_040118 Diffusion: Eindringen eines Stoffes in einen anderen auf Grund der Wärmebewegung. Experiment: ruhende, verschieden gefärbte
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Kolligative Eigenschaften
 Prof. Dr. Norbert Hampp 1/8 11. Kolligative Eigenschaften Kolligative Eigenschaften Unter kolligativen Eigenschaften versteht man die Eigenschaften eines Systems die auf der Mischung unterschiedlicher
Prof. Dr. Norbert Hampp 1/8 11. Kolligative Eigenschaften Kolligative Eigenschaften Unter kolligativen Eigenschaften versteht man die Eigenschaften eines Systems die auf der Mischung unterschiedlicher
Experimentalphysik 2
 Repetitorium zu Experimentalphysik 2 Ferienkurs am Physik-Department der Technischen Universität München Gerd Meisl 5. August 2008 Inhaltsverzeichnis 1 Übungsaufgaben 2 1.1 Übungsaufgaben....................................
Repetitorium zu Experimentalphysik 2 Ferienkurs am Physik-Department der Technischen Universität München Gerd Meisl 5. August 2008 Inhaltsverzeichnis 1 Übungsaufgaben 2 1.1 Übungsaufgaben....................................
11. Wärmetransport. und Stoffmischung. Q t. b) Wärmeleitung (ohne Materietransport)
 11. Wärmetransport und Stoffmischung b) Wärmeleitung (ohne Materietransport) Wärme(energie) Q wird durch einen Wärmeleiter (Metall) der Querschnittsfläche A vom wärmeren zum kälteren transportiert, also
11. Wärmetransport und Stoffmischung b) Wärmeleitung (ohne Materietransport) Wärme(energie) Q wird durch einen Wärmeleiter (Metall) der Querschnittsfläche A vom wärmeren zum kälteren transportiert, also
Gefrierpunktserniedrigung
 Knoch, Anastasiya Datum der Durchführung: Petri, Guido 05.01.2016 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Gefrierpunktserniedrigung 1. Aufgabenstellung
Knoch, Anastasiya Datum der Durchführung: Petri, Guido 05.01.2016 (Gruppe 11) Datum der Korrektur: 02.02.2016 Praktikum Physikalische Chemie I. Thermodynamik Gefrierpunktserniedrigung 1. Aufgabenstellung
KAPITEL 1: Die Welt, in der wir uns bewegen
 KAPITEL 1: Die Welt, in der wir uns bewegen Kugel Kugel Tischplatte Zug beschleunigt Tischplatte Zug bremst Die Kugel möchte ihren Bewegungszustand beibehalten. Bestimmen der Masse mit einer Balkenwaage...
KAPITEL 1: Die Welt, in der wir uns bewegen Kugel Kugel Tischplatte Zug beschleunigt Tischplatte Zug bremst Die Kugel möchte ihren Bewegungszustand beibehalten. Bestimmen der Masse mit einer Balkenwaage...
Aufgabe: Es sind die kryoskopischen Konstante von Wasser und die Molmassen von darin löslichen Substanzen zu bestimmen.
 Versuchsanleitungen zum Praktikum Physikalische Chemie für nfänger 1 4 Kryoskopie ufgabe: Es sind die kryoskopischen Konstante von Wasser und die Molmassen von darin löslichen Substanzen zu bestimmen.
Versuchsanleitungen zum Praktikum Physikalische Chemie für nfänger 1 4 Kryoskopie ufgabe: Es sind die kryoskopischen Konstante von Wasser und die Molmassen von darin löslichen Substanzen zu bestimmen.
3. Diffusion und Brechungsindex
 3. Diffusion und Brechungsinde Die Diffusion in und aus einer Schicht ist die Grundlage vieler Sensoreffekte, wobei sich die einzelnen Sensoren dann nur noch in der Art der Übersetzung in ein meßbares
3. Diffusion und Brechungsinde Die Diffusion in und aus einer Schicht ist die Grundlage vieler Sensoreffekte, wobei sich die einzelnen Sensoren dann nur noch in der Art der Übersetzung in ein meßbares
Spezifische Wärme fester Körper
 1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Physikalische Chemie Praktikum. Mischphasenthermodynamik: Gefrierpunktserniedrigung Molmassenbestimmung
 Hochschule Emden / Leer Physikalische Chemie Praktikum Mischphasenthermodynamik: Gefrierpunktserniedrigung Molmassenbestimmung Vers.Nr. 17 Sept. 2015 Allgemeine Grundlagen a) Reine Stoffe Bei reinen Stoffen
Hochschule Emden / Leer Physikalische Chemie Praktikum Mischphasenthermodynamik: Gefrierpunktserniedrigung Molmassenbestimmung Vers.Nr. 17 Sept. 2015 Allgemeine Grundlagen a) Reine Stoffe Bei reinen Stoffen
Vakuum und Gastheorie
 Vakuum und Gastheorie Jan Krieger 9. März 2005 1 INHALTSVERZEICHNIS 0.1 Formelsammlung.................................... 2 0.1.1 mittlere freie Weglänge in idealen Gasen................... 3 0.1.2 Strömungsleitwerte
Vakuum und Gastheorie Jan Krieger 9. März 2005 1 INHALTSVERZEICHNIS 0.1 Formelsammlung.................................... 2 0.1.1 mittlere freie Weglänge in idealen Gasen................... 3 0.1.2 Strömungsleitwerte
A 2.6 Wie ist die Zusammensetzung der Flüssigkeit und des Dampfes eines Stickstoff-Sauerstoff-Gemischs
 A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
6.2 Temperatur und Boltzmann Verteilung
 222 KAPITEL 6. THERMODYNAMIK UND WÄRMELEHRE 6.2 Temperatur und Boltzmann Verteilung Im letzten Abschnitt haben wir gesehen, dass eine statistische Verteilung von Atomen eines idealen Gases in einem Volumen
222 KAPITEL 6. THERMODYNAMIK UND WÄRMELEHRE 6.2 Temperatur und Boltzmann Verteilung Im letzten Abschnitt haben wir gesehen, dass eine statistische Verteilung von Atomen eines idealen Gases in einem Volumen
Versuch Nr.53. Messung kalorischer Größen (Spezifische Wärmen)
 Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Physikalisch-Chemisches Grundpraktikum für Pharmazeuten. Physikalisch-Chemisches Grundpraktikum für Pharmazeuten
 Physikalisch-Chemisches Grundpraktikum für Pharmazeuten Seminar P3 Kolligative Eigenschaften: Kapitelübersicht Physikalisch-Chemisches Grundpraktikum für Pharmazeuten Seminar P3 Kolligative Eigenschaften
Physikalisch-Chemisches Grundpraktikum für Pharmazeuten Seminar P3 Kolligative Eigenschaften: Kapitelübersicht Physikalisch-Chemisches Grundpraktikum für Pharmazeuten Seminar P3 Kolligative Eigenschaften
2.4 Kinetische Gastheorie - Druck und Temperatur im Teilchenmodell
 2.4 Kinetische Gastheorie - Druck und Temperatur im Teilchenmodell Mit den drei Zustandsgrößen Druck, Temperatur und Volumen konnte der Zustand von Gasen makroskopisch beschrieben werden. So kann zum Beispiel
2.4 Kinetische Gastheorie - Druck und Temperatur im Teilchenmodell Mit den drei Zustandsgrößen Druck, Temperatur und Volumen konnte der Zustand von Gasen makroskopisch beschrieben werden. So kann zum Beispiel
Gefrierpunktserniedrigung
 Gefrierpunktserniedrigung Zur Darstellung der möglichen Phasen einer Substanz wird deren Verhalten bei verschiedenen Drücken und Temperaturen gemessen und in ein Druck-Temperatur- Diagramm eingetragen.
Gefrierpunktserniedrigung Zur Darstellung der möglichen Phasen einer Substanz wird deren Verhalten bei verschiedenen Drücken und Temperaturen gemessen und in ein Druck-Temperatur- Diagramm eingetragen.
Bestimmung der Molekularen Masse von Makromolekülen
 Bestimmung der Molekularen Masse von Makromolekülen Größenausschlußchromatographie Gelfiltration, SEC=size exclusion chromatography Größenausschlußchromatographie Gelfiltration, SEC=size exclusion chromatography
Bestimmung der Molekularen Masse von Makromolekülen Größenausschlußchromatographie Gelfiltration, SEC=size exclusion chromatography Größenausschlußchromatographie Gelfiltration, SEC=size exclusion chromatography
a) Stellen Sie das Diagramm Geschwindigkeits Zeit Diagramm für eine geeignete Kombination von Massen und dar.
 Atwood sche Fallmaschine Die kann zum Bestimmen der Erdbeschleunigung und zum Darstellen der Zusammenhänge zwischen Weg, Geschwindigkeit und Beschleunigung verwendet werden. 1) Aufgaben a) Stellen Sie
Atwood sche Fallmaschine Die kann zum Bestimmen der Erdbeschleunigung und zum Darstellen der Zusammenhänge zwischen Weg, Geschwindigkeit und Beschleunigung verwendet werden. 1) Aufgaben a) Stellen Sie
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Abbildung 1: Dichtegradient im Gleichgewicht (rechte Achse) und Hierbei sind neben einer Dichteverteilung auch die ungefähren Molmas-
 UZ-Dichtegradient Ziel des Experiments Häufig ist die Dichte eines sedimentierenden Partikels nicht bekannt oder sogar Hauptgegenstand der Untersuchung. Zur ausschließlichen Bestimmung der Teilchendichte
UZ-Dichtegradient Ziel des Experiments Häufig ist die Dichte eines sedimentierenden Partikels nicht bekannt oder sogar Hauptgegenstand der Untersuchung. Zur ausschließlichen Bestimmung der Teilchendichte
Thermodynamik. Wechselwirkung mit anderen Systemen Wärme, Arbeit, Teilchen
 18a Temperatur 1 Thermodynamik Thermodynamik ist eine phänomenologische Wissenschaft Sie beschreibt die Wechselwirkung von Systemen mit ihrer Umgebung Aus der Erfahrung und durch zahllose Beobachtungen
18a Temperatur 1 Thermodynamik Thermodynamik ist eine phänomenologische Wissenschaft Sie beschreibt die Wechselwirkung von Systemen mit ihrer Umgebung Aus der Erfahrung und durch zahllose Beobachtungen
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
Physikalisches Grundpraktikum
 Ernst-Moritz-Arndt-Universität Greifswald / Institut für Physik Physikalisches Grundpraktikum Praktikum für Mediziner M1 Viskose Strömung durch Kapillaren Name: Versuchsgruppe: Datum: Mitarbeiter der Versuchsgruppe:
Ernst-Moritz-Arndt-Universität Greifswald / Institut für Physik Physikalisches Grundpraktikum Praktikum für Mediziner M1 Viskose Strömung durch Kapillaren Name: Versuchsgruppe: Datum: Mitarbeiter der Versuchsgruppe:
Wie ist der Druck p allgemein definiert. Wie groß ist der Luftdruck unter Normalbedingungen ungefähr? Welche Einheit hat er?
 Wie ist der Druck p allgemein definiert? Welche Einheit hat er? Wie groß ist der Luftdruck unter Normalbedingungen ungefähr? Was kann man sich anschaulich unter dem Stempeldruck in einer Flüssigkeit vorstellen?
Wie ist der Druck p allgemein definiert? Welche Einheit hat er? Wie groß ist der Luftdruck unter Normalbedingungen ungefähr? Was kann man sich anschaulich unter dem Stempeldruck in einer Flüssigkeit vorstellen?
Physikalische Aspekte der Respiration
 Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuch 2. Physik für (Zahn-)Mediziner. c Claus Pegel 13. November 2007
 Versuch 2 Physik für (Zahn-)Mediziner c Claus Pegel 13. November 2007 1 Wärmemenge 1 Wärme oder Wärmemenge ist eine makroskopische Größe zur Beschreibung der ungeordneten Bewegung von Molekülen ( Schwingungen,
Versuch 2 Physik für (Zahn-)Mediziner c Claus Pegel 13. November 2007 1 Wärmemenge 1 Wärme oder Wärmemenge ist eine makroskopische Größe zur Beschreibung der ungeordneten Bewegung von Molekülen ( Schwingungen,
Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung)
 Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Abb.1 Zur Veranschaulichung: Scherung eines Fluids zwischen zwei Platten
 Viskosität Die innere Reibung von Fluiden wird durch ihre dynamische Viskosität η beschrieben. Die dynamische Viskosität η eines Fluids stellt dessen Widerstand gegen einen erzwungenen, irreversiblen Ortswechsel
Viskosität Die innere Reibung von Fluiden wird durch ihre dynamische Viskosität η beschrieben. Die dynamische Viskosität η eines Fluids stellt dessen Widerstand gegen einen erzwungenen, irreversiblen Ortswechsel
Physik I Mechanik und Thermodynamik
 Physik I Mechanik und Thermodynamik 1 Einführung: 1.1 Was ist Physik? 1.2 Experiment - Modell - Theorie 1.3 Geschichte der Physik 1.4 Physik und andere Wissenschaften 1.5 Maßsysteme 1.6 Messfehler und
Physik I Mechanik und Thermodynamik 1 Einführung: 1.1 Was ist Physik? 1.2 Experiment - Modell - Theorie 1.3 Geschichte der Physik 1.4 Physik und andere Wissenschaften 1.5 Maßsysteme 1.6 Messfehler und
Versuch 4 Messung der dynamischen Viskosität mit dem Rotationsviskosimeter (Grundlagen DIN 53018)
 Versuch 4 Messung der dynamischen Viskosität mit dem Rotationsviskosimeter (Grundlagen DIN 53018) Versuch 4 Messung der dynamischen Viskosität mit dem Rotationsviskosimeter (Grundlagen DIN 53018) 4.1 Begriff
Versuch 4 Messung der dynamischen Viskosität mit dem Rotationsviskosimeter (Grundlagen DIN 53018) Versuch 4 Messung der dynamischen Viskosität mit dem Rotationsviskosimeter (Grundlagen DIN 53018) 4.1 Begriff
Flüssigkeiten. einige wichtige Eigenschaften
 Flüssigkeiten einige wichtige Eigenschaften Die Oberflächenspannung einer Flüssigkeit ist die zur Vergröß ößerung der Oberfläche um den Einheitsbetrag erforderliche Energie (H 2 O bei 20 C: 7.29 10-2 J/m
Flüssigkeiten einige wichtige Eigenschaften Die Oberflächenspannung einer Flüssigkeit ist die zur Vergröß ößerung der Oberfläche um den Einheitsbetrag erforderliche Energie (H 2 O bei 20 C: 7.29 10-2 J/m
Physikalisches Praktikum I
 Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Grundpraktikum M6 innere Reibung
 Grundpraktikum M6 innere Reibung Julien Kluge 1. Juni 2015 Student: Julien Kluge (564513) Partner: Emily Albert (564536) Betreuer: Pascal Rustige Raum: 215 Messplatz: 2 INHALTSVERZEICHNIS 1 ABSTRACT Inhaltsverzeichnis
Grundpraktikum M6 innere Reibung Julien Kluge 1. Juni 2015 Student: Julien Kluge (564513) Partner: Emily Albert (564536) Betreuer: Pascal Rustige Raum: 215 Messplatz: 2 INHALTSVERZEICHNIS 1 ABSTRACT Inhaltsverzeichnis
Allgemeines Gasgesetz. PV = K o T
 Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H 2 O von
 Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Physik für Mediziner Flüssigkeiten II
 Modul Physikalische und physiologische Grundlagen der Medizin I Physik für Mediziner http://www.mh-hannover.de/physik.html Flüssigkeiten II Andre Zeug Institut für Neurophysiologie zeug.andre@mh-hannover.de
Modul Physikalische und physiologische Grundlagen der Medizin I Physik für Mediziner http://www.mh-hannover.de/physik.html Flüssigkeiten II Andre Zeug Institut für Neurophysiologie zeug.andre@mh-hannover.de
Physikalische Chemie 1
 Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
What is a Fourier transform? A function can be described by a summation of waves with different amplitudes and phases.
 What is a Fourier transform? A function can be described by a summation of waves with different amplitudes and phases. Fourier Synthese/Anaylse einer eckigen periodischen Funktion Fourier Interferomter
What is a Fourier transform? A function can be described by a summation of waves with different amplitudes and phases. Fourier Synthese/Anaylse einer eckigen periodischen Funktion Fourier Interferomter
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde VL # 14,
 Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde VL # 14, 20.05.2009 Vladimir Dyakonov Experimentelle Physik VI dyakonov@physik.uni-wuerzburg.de Professor Dr. Vladimir
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde VL # 14, 20.05.2009 Vladimir Dyakonov Experimentelle Physik VI dyakonov@physik.uni-wuerzburg.de Professor Dr. Vladimir
Versuch 6 Elektrophorese
 Versuch 6 Elektrophorese Till Biskup Matrikelnummer: 55567 2. Mai 2000 Einführung Ziel des Versuches ist es, die Zusammenhänge zwischen der elektristatischen Struktur auf Zelloberflächen und ihrem elektrokinetischen
Versuch 6 Elektrophorese Till Biskup Matrikelnummer: 55567 2. Mai 2000 Einführung Ziel des Versuches ist es, die Zusammenhänge zwischen der elektristatischen Struktur auf Zelloberflächen und ihrem elektrokinetischen
Tutorium Physik 2. Rotation
 1 Tutorium Physik 2. Rotation SS 16 2.Semester BSc. Oec. und BSc. CH 2 Themen 7. Fluide 8. Rotation 9. Schwingungen 10. Elektrizität 11. Optik 12. Radioaktivität 3 8. ROTATION 8.1 Rotation: Lösungen a
1 Tutorium Physik 2. Rotation SS 16 2.Semester BSc. Oec. und BSc. CH 2 Themen 7. Fluide 8. Rotation 9. Schwingungen 10. Elektrizität 11. Optik 12. Radioaktivität 3 8. ROTATION 8.1 Rotation: Lösungen a
Ideale Gase. Abb.1: Versuchsanordnung von Torricelli
 Ideale Gase 1 Empirische Gasgesetze, Einblick in die Geschichte der Naturwissenschaften. Wie hängt das Volumen eines Gases von Druck, Temperatur und Stoffmenge ab? Definition Volumen V: Das Volumen V ist
Ideale Gase 1 Empirische Gasgesetze, Einblick in die Geschichte der Naturwissenschaften. Wie hängt das Volumen eines Gases von Druck, Temperatur und Stoffmenge ab? Definition Volumen V: Das Volumen V ist
Grundpraktikum Physikalische Chemie V 18/19. Molekulargewichtsbestimmung. nach Rast, Dumas und durch. Gefrierpunktserniedrigung nach Beckmann
 Grundpraktikum Physikalische Chemie V 8/9 Molekulargewichtsbestimmung nach Rast, Dumas und durch Gefrierpunktserniedrigung nach Beckmann Kurzbeschreibung: Wird eine Substanz in einem bestimmten flüssigen
Grundpraktikum Physikalische Chemie V 8/9 Molekulargewichtsbestimmung nach Rast, Dumas und durch Gefrierpunktserniedrigung nach Beckmann Kurzbeschreibung: Wird eine Substanz in einem bestimmten flüssigen
Kurze Einführung in die Thermodynamik mit Begriffsklärungen
 Kurze Einführung in die Thermodynamik mit Begriffsklärungen Gliederung 1. Begriffsklärungen 2. Energieumwandlungen 3. Molare Volumenarbeit 4. Hauptsätze der Thermodynamik 5. Quellen 1. Begriffsklärungen
Kurze Einführung in die Thermodynamik mit Begriffsklärungen Gliederung 1. Begriffsklärungen 2. Energieumwandlungen 3. Molare Volumenarbeit 4. Hauptsätze der Thermodynamik 5. Quellen 1. Begriffsklärungen
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
