Rationaler Einsatz von Antibiotika
|
|
|
- Klaudia Geisler
- vor 5 Jahren
- Abrufe
Transkript
1 Rationaler Einsatz von Antibiotika Peter Walger 1 Einleitung Vor jeder Einleitung einer Therapie mit Antibiotika muss die Verdachtsdiagnose einer bakteriellen Infektion stehen. Zur Sicherung des Verdachtes dienen klinische Befunde (Fieber, Schmerzen, Tachypnoe, Bewusstseinsstörungen etc.), die Ergebnisse der körperlichen Untersuchung, laborchemische Parameter und Ergebnisse der Bildgebung sowie mikrobiologischer Untersuchungen. In Abhängigkeit vom Schweregrad der Erkrankung, dem vermuteten Sitz der Infektion, dem Alter und dem Risikoprofil des Patienten muss die Entscheidung zur antibiotischen Therapie zeitnah erfolgen. Bei den schwersten Verlaufsformen einer Infektion, der Sepsis oder dem septischen Schock, muss die erste Antibiotikagabe innerhalb von 1 Stunde nach Aufnahme ins Krankenhaus und nach Abnahme von mindestens 2 Blutkulturpärchen erfolgen. Bei weniger schweren Infektionen können Befunde der Bildgebung oder des Labors abgewartet werden, bevor die Therapie begonnen Dieses Kapitel basiert auf Walger P (2016) Rationaler Einsatz von Antibiotika. Der Internist, 06/2016, Springer- Verlag P. Walger (*) Internistische Intensivmedizin und Infektiologie, Johanniter-Krankenhaus, Johanniterkliniken Bonn, Bonn, Deutschland peter.walger@johanniter-kliniken.de wird, in der Regel innerhalb von 6 8 Stunden. Nur bei chronischen Infektionen von Knochen oder Gelenken sollten mikrobiologische Befunde abgewartet werden, um eine gezielte Therapie beginnen zu können. In der Regel ist der bakterielle Erreger nicht bekannt. Die Wahl des geeigneten Antibiotikums erfolgt empirisch-kalkuliert. Sitz der Infektion, Kenntnis der typischen Erreger, vorbekannte mikrobiologische Befunde, vorausgegangene antibiotische Therapien und die Kenntnisse der lokalen oder regionalen Resistenz- und Erregerprävalenzen sind die Voraussetzung für die Wahl des geeigneten Antibiotikums. Ist der Erreger identifiziert, erfolgt die weitere Therapie gezielt. Ein Wechsel des Antibiotikums zum Beispiel von einem Breit- auf ein Schmalspektrumantibiotikum oder Beendigung der Gabe eines Kombinationspartners können sinnvoll sein. Bei gutem Ansprechen der Therapie kann sequenziell von der parenteralen auf eine orale Applikation gewechselt werden. Die oft als Kollateralschäden bezeichneten negativen Auswirkungen und Komplikationen der Antibiotikatherapie sind ihre toxischen oder allergischen Nebenwirkungen, Risiken, die sich aus Interaktionen mit anderen Medikamenten oder Nahrungsbestandteilen ergeben, die Selektion pathogener Erreger und die Induktion oder Selektion von Resistenzen. # Springer-Verlag GmbH Deutschland 2016 H. Lehnert et al. (Hrsg.), DGIM Innere Medizin, Springer Reference Medizin, DOI / _
2 2 P. Walger 2 Indikationen für den Einsatz von Antibiotika Die Diagnose einer bakteriellen Infektion wird vermutet, wenn typische klinische Symptome in Verbindung mit körperlichen Untersuchungsbefunden und ggf. weiteren technischen und laborchemischen Untersuchungsergebnissen auf einen entzündlich-infektiologischen Organbefund hinweisen. In der Regel lässt sich eine bakterielle Infektion einem infizierten Organ oder einem Infektionsherd zuordnen. Infektionen ohne Herdbefund können sich als Fieber ohne Organzuordnung bzw. als Fieber unklarer Zuordnung (fever of unknown origin, FUO), als primäre Sepsis mit oder ohne Bakteriämie und mit oder ohne identifizierbare Eintrittspforte manifestieren. Die Abgrenzung zu einer Virusinfektion bei Nichtimmunsupprimierten stellt dabei eine Herausforderung bei respiratorischen Infektionen der tiefen Atemwege dar, während Infektionen der Harnwege oder der Haut- und Weichgewebe, der Knochen oder Gelenke, innerer Organe wie Gallenblase, Appendix, Intestinaltrakt in der Regel eindeutiger als bakteriell verursacht diagnostiziert werden können. Fehlende Klarheit in den Diagnosekriterien einer bakteriellen Infektion führt zu antibiotischen Therapien von Besiedlungen, von Virusinfektionen oder von Fieber nicht bakterieller Genese, d. h. zu Therapien ohne Indikation. Infektionen bei Immunsupprimierten und insbesondere bei neutropenen Patienten stellen eine besondere diagnostische Herausforderung dar, weil eine bakterielle Ursache nur ein Teil der infrage kommenden Ätiologien inflammatorisch febriler Zustände darstellt. Typische Befunde bei schweren bakteriellen Infektionen sind Fieber oder Hypothermie, Leukozytose oder Leukopenie, Erhöhung des C-reaktiven Proteins (CRP) und/oder des Procalcitonins (PCT), lokale Infektionszeichen mit Bezug auf das betroffene Organsystem und klinische Instabilität im Sinne systemischer Reaktionen auf die lokale Entzündung (Sepsis, septischer Schock). Diagnosekriterien und die Indikationen für eine antibiotische Therapie bei stationären Patienten sollten in hauseigenen Leitlinien schriftlich formuliert sein. Die Grundlagen sind in den Empfehlungen der Paul-Ehrlich-Gesellschaft (PEG) zur kalkulierten parenteralen Initialtherapie bakterieller Erkrankungen (Bodman et al. 2010) und zur oralen Therapie von Infektionen im Erwachsenenalter (Lode et al. 2006; Scholz et al. 1999) oder in den Leitlinien der wissenschaftlichen Fachgesellschaften unter anderem zur Sepsis (Reinhart et al. 2010; Dellinger et al. 2013), zur ambulant erworbenen Pneumonie (Ewig et al. 2016), zur nosokomialen Pneumonie (Dalhoff et al. 2012), zu den Harnwegsinfektionen (Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften 2016), zur Endokarditis (Habib et al. 2015), zu infektiösen Darmerkrankungen (Hagel et al. 2015) oder zur Therapie der Helicobacter-pylori- Infektion (Fischbach et al. 2016) festgelegt. Wichtige und häufige Infektionskrankheiten in der Allgemeinen und Inneren Medizin Zu den häufigeren bakteriellen Infektionskrankheiten bei ambulanten Patienten gehören die ambulant erworbene Pneumonie, die bakterielle Exazerbation der chronisch-obstruktiven Atemwegserkrankung (COPD), Harnwegsinfektionen, Hautund Weichgewebeinfektionen sowie infektiöse Darmerkrankungen und intraabdominelle Infektionen wie die Cholezystitis, Divertikulitis und die Helicobacter-assoziierte Gastritis. Die für die Therapie infrage kommenden Antibiotika sind in Tab. 1 aufgeführt. Fieber bei Neutropenie Eine besondere Herausforderung ist die adäquate antiinfektive Therapie bei Fieber in Neutropenie. Schwere Infektionen sind die führende Todesursache neutropener Patienten, die unmittelbare kausale antiinfektive Therapie ist lebensrettend. Das höchste Risiko für prolongierte Neutropenien als Therapiefolge haben Patienten mit hämatologischen Neoplasien, insbesondere einer Akuten myeloischen Leukämie (AML) sowie nach allogener Stammzelltransplantation. Ein hoher Anteil der Infektionen verläuft als Fieber ohne nachweisbaren Ursprung (fever of unknown origin, FUO), trotzdem ist eine komplette klinische und körperliche Untersuchung essenziell. Hierzu gehören die sorgfältige Untersuchung von
3 Rationaler Einsatz von Antibiotika 3 Tab. 1 Die wichtigsten ambulanten Infektionen und ihre leitliniengerechte Therapien Infektionen Antibiotika der 1. Wahl nach Leitlinie Alternativen Wichtigste Erreger und Anmerkungen Ambulant erworbene Pneumonie Einteilung nach Pneumonietriade: Ausschluss nosokomiale Pneumonie, Pneumonie bei Immunsuppression und Pneumonie bei (CAP) COPD Einteilung nach Schweregrad und Alter (CRB-65-Score), mit und ohne Komorbidität, Risikofaktoren Pflegeheim oder Bettlägerigkeit, Multiresistenzrisiko sehr gering (<1 %), individuelles Risiko abschätzen Leichte CAP, ambulant behandelbar CRB-65-Score = 0, ohne Komorbidität Leichte CAP, ambulant behandelbar CRB-65-Score = 0, mit Komorbidität Mittelschwere CAP, stationäre Behandlung erforderlich CRB-65-Score = 1 2 Schwere Pneumonie CRB-65-Score = 3 4 Amoxicillin (3 1 g oral) Moxifloxacin (1 400 mg oral) oder Levofloxacin (1 500 mg oral) Clarithromycin (2 500 mg oral) Doxycylin (2 100 mg Tag 1, dann mg) Amoxicillin/Clavulansäure (3 1 g oral [ mg]) Amoxicillin/Clavulansäure (3 4 2,2 g i.v.) Ampicillin/Sulbactam (3 4 3 g i.v.) Optional plus Makrolid für 3 Tage Piperacillin/Tazobactam (3 4 4,5 g) oder Ceftriaxon (1 2 g)oder Cefotaxim (3 2g) Obligat plus Makrolid für 3 Tage Akute Exazerbation einer COPD Je nach Schweregrad und Vortherapie: Amoxicillin/Clavulansäure Ampicillin/Sulbactam Piperacillin/Tazobactam Moxifloxacin oder Levofloxacin oral Pneumokokken In Deutschland keine relevante Penicillinresistenz, Non-Response von Amoxicillin bei atypischen Erregern, daher ambulante Responsekontrolle (second look) Orale Therapie mit Sultamicillin nicht empfohlen (keine Pneumoniedaten, keine ausreichende Bioverfügbarkeit bei Label-Use -Gabe) (2 tgl.) Moxifloxacin oder Levofloxacin In der Regel Sequenztherapie je nach Response nach 2 3 Tagen Bei schwerer CAP Sequenztherapie möglich, Bei Pneumokokken-Nachweis: gezielte Moxifloxacin oder Levofloxacin Therapie immer parenteral beginnen Therapie mit Penicillin G (4 5 Mega) Bei Legionellen-Nachweis: Levofloxacin (1 750 mg) Bei Staphylokokken-Nachweis (MSSA): Flucloxacillin (4 6 2g)oder Cefazolin (3 2g) Moxifloxacin oder Levofloxacin Pseudomonas-Risiko beachten, dann Carbapenem Gruppe 1 oder Kombination mit Ciprofloxacin erwägen Harnwegsinfektionen (HWI) Mit Ausnahme der Schwangerschaft bestehen keine Indikationen zur Therapie asymptomatischer Bakteriurien, Differenzierung einschließlich Niere und unkomplizierter und komplizierter HWI wichtig, bei Männern an Urethritis denken; Ausschluss einer sexuell übertragbaren Infektion Urogenitaltrakt (Neisseria gonorrhoeae, Chlamydia trachomatis, Ureoplasma urealyticum) Unkomplizierte HWI (Zystitis) Fosfomycin Trometamol ( mg, Einmalgabe) Nitrofurantoin ret. (2 100 mg für 3 5 Tage) Pivmecillinam (in Deutschland Ciprofloxacin Cotrimoxacol E. coli, Proteus mirabilis, Klebsiella pneumoniae Therapie möglichst nach Erregernachweis bzw. regionaler Resistenzlage, empirisch kalkuliert parenteral nur bei schweren (Fortsetzung)
4 4 P. Walger Tab. 1 (Fortsetzung) Infektionen Antibiotika der 1. Wahl nach Leitlinie Alternativen Wichtigste Erreger und Anmerkungen Komplizierte HWI, einschließlich Urosepsis Akute unkomplizierte Pyelonephritis einschließlich Urosepsis zugelassen seit 5/2016; mg für 3 Tage; auch gegen ESBL + E. coli wirksam) Ambulant erworben: Cephalosporine Gruppe 3a Fluorochinolone Carbapeneme Gruppe 2 (Ertapenem) Nosokomial erworben: Cephalosporine 3b oder 4 Fluorochinolone Piperacillin/Tazobactam Carbapenem Gruppe 1 (Imipenem, Meropenem) 3 5 Tage nach Entfieberung bzw. Fokuskontrolle Cephalosporin Gruppe 3a (Ceftriaxon oder Cefotaxim) oder Piperacillin/Tazobactam 5 7 Tage Bei Sepsis Kombination mit Aminoglykosid erwägen (Gentamycin 1 5 mg/kg KG) Prostatitis Therapieprinzipien wie unter Komplizierte HWI Dauer: 2 4 Wochen Akute Epididymitis, Epididymoorchitis Komplizierte Urogenitalinfektionen der Frau einschließlich Endometritis, Salpingitis, Tuboovarialabszess und Pelveoperitonitis Levofloxacin ( mg) bevorzugen, da neben den klassischen Uropathogenen auch Chlamydien adäquat abgedeckt sind Bei Gonorrhoe Ceftriaxon (1 g i.m.) plus Doxycyclin (1 200 mg p.o.) Dauer: 7 14 Tage Zusätzliche Therapie von Anaerobiern wichtig, daher Kombinationen mit Metronidazol wählen Individuelle Therapiekonzepte nach Schweregrad der Infektion und regionaler Der Stellenwert der neuen Kombination aus Ceftolozan/Tazobactam kann aktuell nicht ausreichend beurteilt werden Ciprofloxacin oder Levofloxacin Amoxicillin/Clavulansäure nur nach Resistenzlage Infektionen beginnen, ansonsten wenn möglich gezielte Therapie nach Erregernachweis Erregerspektrum erweitert um nosokomiale Keime wie Pseudomonas aeruginosa, Acinetobacter baumannii, andere Enterobacteriaceae, Enterokokken, Staphylokokken, multiresistente Erreger Therapie möglichst nach Erregernachweis durch Urinkultur, bei Urosepsis Therapiebeginn innerhalb der ersten Stunde nach Blutkulturentnahme, urologische Fokusdiagnostik Erregerspektrum wie bei unkomplizierter Zystitis Sequenztherapie nach Besserung, orale Therapiefortsetzung, meistens 7 Tage insgesamt ausreichend, bei Urosepsis siehe oben Anpassung nach Erregernachweis Siehe unter Komplizierte HWI Urethritis- und Urindiagnostik abwarten, Therapieanpassung nach den Ergebnissen Hohe Fluorochinolon-Resistenzen von E. coli beachten Erregerspektrum breit: Chlamydia trachomatis, Neisseria gonorrhoe, Prevotella spp., Bacteroides spp., Peptokokken, Peptostreptokokken Kombinationspartner bei
5 Rationaler Einsatz von Antibiotika 5 Resistenzlage Proben sollten laparoskopisch gewonnen werden Bakterielle Gastroenteritis Empirisch kalkuliert: Ciprofloxacin (2 500 mg p.o. oder mg i.v. für 3 5 Tage) oder Azithromycin (1 500 mg p.o. für 3 Tage) oder Ceftriaxon (1 2 g i.v. für 3 5 Tage) Anpassung der Therapie nach Erregernachweis und Resistenztestung: Salmonellen: Ciprofloxacin oder Ceftriaxon 5 7 Tage, bei Immunsuppression 14 Tage, bei fokalen Absiedlungen evtl. länger, bei prolongierter Ausscheidung >3 Monate Ciprofloxacin für 4 Wochen Shigellen: Azithromycin oder Ciprofloxacin Campylobacter: 1. Wahl: Azithromycin ( mg einmalig oder 500 mg für 3 Tage), Ciprofloxacin nur nach Resistenztestung Yersinien: Ciprofloxacin (für 5 7 Tage) oder Cotrimoxazol (1920 mg p.o. oder i.v. für 5 7 Tage) Bei Bakteriämie Ciprofloxacin oder Ceftriaxon für 7 14 Tage Clostridium-difficile-Kolitis Therapie nach Schweregrad: Leichte bis moderate Kolitis: Metronidazol (3 400 oder 500 mg oral oder i.v.) Schwere Kolitis: Vancomycin (4 125 mg oral) Divertikulitis Bei lokaler Peritonitis: Cefuroxim oder Cefotaxim oder Ceftriaxon oder Ciprofloxacin (jeweils zusammen mit Metronidazol) oder Ampicillin/ Antibiotische Therapie nur bei Fieber, systemischen Infektionszeichen, blutigen Diarrhoen, Immunsuppression Bei EHEC (enterohämorrhagischer E. coli) nur in Ausnahmefällen Therapie mit Carbapenem Das seit 5/2016 in Deutschland zur Therapie des unkomplizierten Harnwegsinfektes zugelassene Pivmecillinam ist auch wirksam gegen Salmonellen, Shigellen und Yersinien Kombination von Metronidazol und Vancomycin nicht durch Studien gesichert Bei schwerem Verlauf (diffuse Peritonitis): Piperacillin/Tazobactam oder Carbapenem 2 (Ertapenem) oder Tigecyclin oder Moxifloxacin Sequenztherapie: Doxycyclin, Clindamycin oder Metronidazol Campylobacter jejuni, C. coli, Salmonellen, Shigellen, Yersinien, obligat pathogene E. coli, Vibrio cholerae Erregerdiagnostik nur in begründeten Fällen (schweres Krankheitsbild, chronische Diarrhoe >4 Wochen, Immunsuppression, Hospitalisierung, Komorbiditäten, nosokomiale Diarrhoe, Ausbruchsgeschehen, arbeitsmedizinische Gründe, vor antibiotischer Therapie) Bei Rezidiven Vancomycin- Ausschleichschema oder Fidaxomycin (2 200 mg 10 Tage) Einzelfallbeschreibungen: Tigecyclin (2 50 mg i.v., höhere Dosierung [Off- Label-Anwendung] sinnvoll) In der Regel Mischinfektion durch Erreger der Darmflora (E. coli, Bacteroides fragilis, Enterokokken) Chirurgische Therapieoption abklären (Fortsetzung)
6 6 P. Walger Tab. 1 (Fortsetzung) Infektionen Antibiotika der 1. Wahl nach Leitlinie Alternativen Wichtigste Erreger und Anmerkungen Sulbactam oder Amoxicillin/ Clavulansäure i.v. Dauer: 4 5 Tage Cholezystitis Primär chirurgische Therapie innerhalb von 24 Stunden (Fokussanierung) Kurzzeittherapie (single shot) mit Piperacillin/Tazobactam, Cephalosporin Gruppe 3a oder 4 in Kombination mit Metronidazol Helicobacter-pylori-assoziierte Gastritis Eradikation mit Clarithromycin ( mg) plus Metronidazol ( mg) (italienisch) oder plus Amoxicillin ( mg) (französisch) für 7 14 Tage Jeweils plus Protonenpumpeninhibitor (PPI) Primäre Peritonitis Ceftriaxon (1 2 g) Cefotaxim (3 2g) Piperacillin/Tazobactam (3 4,5 g) Dauer: 7 Tage Bei CAPD-Patienten: Kombination mit Ciprofloxacin oder nach Erregernachweis anpassen Dauer: 7 10 Tage Nekrotisierende Pankreatitis mit infizierten Nekrosen Therapie nur nach Infektionsnachweis Fluorochinolone, Piperacillin/ Tazobactam, Carbapeneme, Tigecyclin Dauer: 7 10 Tage Bei Nachweis von Candida-Spezies 14 Tage Therapie mit einem Echinocandin oder bei moderater Klinik und C.-albicans-Nachweis Fluconazol Dauer: 5 Tage, bei nosokomialer Ätiologie 7 10 Tage Fluorochinolon oder Carbapenem nach Resistenzlage Zweitlinientherapie: Bismut-Kalium-Salz plus Tetracyclin (4 125 mg) plus Metronidazol (4 125 mg) (fixe Kombination) plus PPI Clarithromycin (2 500 mg) plus Amoxicillin ( mg) plus Metronidazol (2 500 mg) plus PPI Levofloxacin (2 500 mg) oder Moxifloxacin (2 400 mg) plus Amoxicillin ( mg) plus PPI Multiresistenzen wegen ambulanter Ätiologie selten Darmflora, am häufigsten E. coli und Klebsiella pneumoniae, nosokomiales Spektrum nach Interventionen Clarithromycin-Resistenzen aktuell steigend (>10 %), bei Herkunft aus Süd- Ost-Europa oder Clarithromycin- Vortherapie Tripletherapie ohne Makrolid wählen (französisch oder Bismut-haltige Vierfachtherapie [Quadrupel]) Patienten mit Aszites bei Leberzirrhose in 70 % Enterobacteriaceae (E. coli, Klebsiella pneumoniae), Staphylokokken (besonders bei kontinuierlicher ambulanter Peritonealdialyse [CAPD], Enterokokken, Streptokokken) Enterobacteriaceae, Enterokokken, Staphylokokken, Anaerobier, Candida spp. Multiresistente Erreger je nach individuellem Risiko
7 Rationaler Einsatz von Antibiotika 7 Akute bakterielle Haut- und Zu den primär konservativ zu behandelnden SSSI gehören Impetigo contagiosa, Furunkel, Karbunkel, Erysipel, begrenzte Phlegmone Weichgewebeinfektionen (acute und Erysipeloid bacterial skin and skin structure Indikationen für eine antibiotische Therapie sind die diffuse Ausbreitung der Infektion im Weichgewebe oder eine systemische infections, ABSSSI) Entzündungsreaktion mit Fieber, Leukozytose und CRP-Anstieg Impetigo/Ekthym Penicillin V (oral) Bei Non-Response nach 2 Tagen Wechsel β-hämolysierende Streptokokken A, B, C auf Cephalosporin 1 (Cefazolin) oder und G, Staphylococcus aureus 2 (Cefuroxim), bei oraler Gabe schlechte Lokale antiseptische Therapie zusätzlich Furunkel/Karbunkel Parenterale Gabe von Flucloxacillin oder Cefazolin bei Lokalisation im Gesichtsbereich (zentrofazial), ansonsten orale Therapie mit Flucloxacillin oder Clindamycin Erysipel Penicillin G (4 5 Mega für 7 14 Tage) Sequenztherapie nach 5 7 Tagen mit oralem Penicillin V (3 1,2 1,5 Mega) möglich Bei Penicillin-Allergie Clindamycin (3 600 mg) Begrenzte Phlegmone (Zellulitis) Parenterale Therapie bei kritischer Lokalisation (Gesicht, Sehnenbeugen) oder Tiefenausdehnung Cefazolin (3 2 g)oder Cefuroxim (3 1,5 g) oder Flucloxacillin (3 4 2g) Bei unkomplizierter Infektion orale Therapie möglich orale Bioverfügbarkeit beachten, dann eher Clindamycin In der Regel reicht die chirurgische Inzision, wenn keine systemischen Infektzeichen Bei MRSA-Nachweis Linezolid (2 600 mg oral) Bei Non-Response und schwieriger Abgrenzung zur Phlegmone Wechsel auf Cefazolin (3 2 g) oder Cefuroxim (3 1,5 g) (zusätzliche Staphylokokkenwirksamkeit) Clindamycin (3 600 mg i.v.) Bei chronischem Verlauf und antibiotischen Vortherapien sind zusätzlich gramnegative und anaerobe Erreger sowie Multiresistenzen zu berücksichtigen; Therapie mit Piperacillin/Tazobactam oder einem Carbapenem oder Tigecyclin erwägen Gezielte Therapie nach Erregernachweis anstreben Staphylococcus aureus (MSSA) An cmrsa oder MSSA mit Produktion von PVL (Panton-Valentine-Leukozidin) denken: übertragbare Furunkulose, Rezidivneigung, bei PVL-Nachweis von MSSA Hygienemanagement wie bei MRSA β-hämolysierende Streptokokken A, selten B-, C- oder G-Streptokokken Gelegentlich schwierige Abgrenzung zur begrenzten Phlegmone mit Haupterreger Staphylococcus aureus Bei chronisch-rezidivierendem Erysipel Langzeittherapie als Prophylaxe: Penicillin V (2 250 mg/tag bzw. 2 0,4 Mega für 12 Monate) Alternative bei Non-Compliance Benzathin-Penicillin (2,4 Mega i.m. alle 2 3 Wochen für zunächst 6 Monate) Bei Penicillinallergie Clarithromycin (2 250 mg oral) Staphylococcus aureus Infektion im Umfeld einer chronischen Wunde, Ulkus
8 8 P. Walger Haut und Schleimhäuten, Eintrittsstellen zentraler und peripherer Gefäßzugänge, Punktionsstellen, Atemwege, Urogenitaltrakt, Abdomen und Perianalregion. Diese erfolgt nach der initialen Entnahme von 2 2 Blutkulturen und der sofortigen empirisch kalkulierten parenteralen Gabe eines bakteriziden Breitspektrumantibiotikums in Form eines Carbapenems oder von Piperacillin-Tazobactam mit oder ohne Kombinationspartner in Abhängigkeit von der klinischen und mikrobiellen Risikokonstellation. Bei persistierendem Fieber oder klinischer Instabilität wird der Wechsel auf ein Carbapenem oder die Kombination mit einem Aminoglykosid oder einer anderen Substanz zum Schließen einer Wirkungslücke empfohlen. Bei Niedrigrisikopatienten ohne Zeichen einer schweren Infektion, ohne vorausgegangene Fluorochinolon-Prophylaxe und bei zu erwartender Neutropeniedauer von maximal 5 Tagen kann auch eine orale Antibiotikatherapie erfolgen. Eine besondere Herausforderung sind Lungeninfiltrate in der Neutropenie, die differenzialdiagnostisch als Manifestationen einer pulmonalen Pilzinfektion, in der Regel durch Aspergillus fumigatus, gewertet werden müssen. Eine Candida-Pneumonie ist eine Rarität. Bei intestinaler Mukositis kann es zu septischen Candida-Infektionen in der Regel in Form einer Candidämie ohne Organbeteiligung kommen. Wenn eine prolongierte Neutropenie von mehr als 10 Tagen erwartet wird, soll bei persistierendem Fieber eine empirisch kalkulierte antimykotische Therapie erwogen werden (Weissinger et al. 2012; Penack et al. 2014). 3 Grundprinzipien der antibiotischen Therapie 3.1 Die richtige Wahl des Antibiotikums Mit der Wahl des Antibiotikums nach Stellen der Diagnose oder Verdachtsdiagnose soll das für den Patienten relevante Erreger- und Resistenzspektrum erfasst sein. Dabei sind zeit- und ortsnahe Erreger- und Resistenznachweise im Patienten, in seiner unmittelbaren Umgebung, seiner Station oder Abteilung, seines Krankenhauses oder der Region relevant. Je schwerer der Patient erkrankt ist, desto sicherer sollen alle potenziellen Erreger im Spektrum des ausgewählten Antibiotikums liegen, desto sicherer soll es in einer adäquaten Konzentration an den Ort der Infektion gelangen und desto schneller soll es die verantwortlichen Erreger abtöten. Eine initial inadäquate antibiotische Therapie schwerer Infektionen korreliert mit erhöhter Morbidität und Mortalität. Für die empirisch kalkulierte Therapie schwerer Infektionen gelten daher folgende Regeln (Bodman et al. 2010; Reinhart et al. 2010; Dellinger et al. 2013): Wahl eines bakteriziden Antibiotikums mit breitem Spektrum Wirksamkeit gegen die wahrscheinlichsten Erreger und deren Resistenzen Parenterale Gabe Initial hohe Dosierung ohne Berücksichtigung einer eingeschränkten Elimination Einhaltung der korrekten Dosierungsintervalle Frühestmöglicher Beginn der Antibiotikagabe bei Sepsis oder septischem Schock innerhalb der 1. Stunde nach stationärer Aufnahme, bei sonstigen schweren Infektionen möglichst zeitnah nach Durchführung entsprechender Diagnostik innerhalb von 4 6 Stunden Zusätzliche Gabe eines weiteren Antibiotikums als Kombinationspartner in bestimmten Fällen Die wichtigsten bakteriziden Antibiotika sind die Beta-Laktam-Antibiotika mit den vier Untergruppen Penicilline, Cephalosporine, Carbapeneme und Monobactame und die Fluorochinolone. Eine Liste der wichtigsten bakteriziden Antibiotika mit den relevanten Indikationen und Zulassungen zeigt Tab. 2. Die relevanten bakteriostatischen Antibiotika werden in Tab. 3 zusammengefasst. Zu ihnen gehören die Makrolide (Erythromycin, Clarithromycin, Roxithromycin und Azithromycin), Tetracycline (einzige relevante Substanz Doxycyclin), Lincosamide (einzige
9 Rationaler Einsatz von Antibiotika 9 Tab. 2 Einteilung der wichtigsten bakteriziden Antibiotika nach Klassen und Gruppen mit Indikationen und Zulassungen (Bodman et al. 2010; Brodt 2013; Zugegriffen am ) Antibiotikaklasse Penicilline (Beta- Laktame) Gruppeneinteilung und relevante Substanzen Benzylpenicilline Penicillin G Penicillin V Isoxazolylpenicilline Flucloxacillin Flucloxacillin Aminopenicilline +/- Betalaktaminhibitor Ampicillin +/- Sulbactam Amoxicillin +/- Clavulansäure Amoxicillin Clavulansäure Sultamicillin Amidinopenicillin Mecillinam Pivmecillinam Acylaminopenicilline Piperacillin Beta-Laktam- Inhibitor Wichtige Eigenschaften Schmalspektrum, wirksam gegen Streptokokken, Pneumokokken, Meningokokken, Spirochäten, Clostridien, Actinomyces-Arten, Corynebakterien (Diphtherie), Borrelien, Leptospiren, Gonokokken Für eine kalkulierte-empirische Initialtherapie zu schmal Schmalspektrum gegen Methicillin-sensible Staphylococcus aureus, (MSSA) Für eine gezielte Therapie geeignet Wie Penicillin G, zusätzlich Enterococcus faecalis, Listerien, Haemophilus spp. Durch Kombination mit einem Betalaktamase-Inhibitor (BLI) Erweiterung des Spektrums auf Betalaktamase-bildende grampositive und gramnegative Erreger Für eine kalkulierte Therapie geeignet Nur im gramnegativen Bereich wirksam, besonders bei E. coli einschließlich ESBL-Bildnern, Klebsiellen, Proteus, Enterobacter, Serratia, auch gegen Salmonellen, Shigellen und Yersinien Breites Wirkungsspektrum einschließlich Pseudomonas aeruginosa und die meisten Enterobacteriaceae, durch Kombination mit dem Betalaktamaseinhibitor Tazobactam Erweiterung des Spektrums Für eine kalkulierte Therapie schwerer Infektionen geeignet Zulassung und Einschränkungen durch Resistenzen in Deutschland Breite Zulassung Keine relevanten Resistenzraten bei Pneumokokken, A-Streptokokken, Meningokokken Stärkste Wirkungsintensität bei Penicillin-sensiblem Erreger Gegen Staphylokokken unwirksam, da >80 % Penicillinasen bilden Infektionen durch Penicillinasebildende Staphylococcus aureus bei erhaltener Oxacillin- Sensibilität, keine Wirksamkeit bei Methicillin-resistenten Staphylococcus aureus (MRSA) Breite Zulassung Enterococcus faecalis nur in ca. 2 % resistent E. coli in >50 % resistent Standardtherapie BLI der ambulant erworbenen Pneumonie (CAP) Zulassung in Deutschland nur bei unkompliziertem Harnwegsinfekt, in Österreich auch bei Pyelonephritis, chronischen oder rezidivierenden HWI, symptomatische oder asymptomatische Bakteriurie in der Schwangerschaft; Salmonellosen, Shigellosen, Alternative bei Typhus abdominalis, Sanierung von Salmonellenausscheidern Geringe Resistenzentwicklungen in Ländern mit langjähriger Anwendung (u. a. Skandinavien) Breite Zulassung Resistenzraten von Enterobacteriaceae und Pseudomonas aeruginosa lokal variierend Bei Nachweis von extendedspectrum beta-lactamases (ESBL) oft noch wirksam Sehr langsame oder keine (Fortsetzung)
10 10 P. Walger Tab. 2 (Fortsetzung) Antibiotikaklasse Cephalosporine (Beta-Laktame) Gruppeneinteilung und relevante Substanzen Gruppe 1 Cefazolin Cefaclor Cefalexin Cefadroxil Gruppe 2 Cefuroxim Cefotiam Cefuroxim-Axetil Gruppe 3a Ceftriaxon Cefotaxim Cefixim Cefpodoxim-Proxetil Ceftibuten Gruppe 3b Ceftazidim Ceftazidim/ Avibactam Wichtige Eigenschaften Schmales Wirkspektrum gegen Streptokokken und Staphylokokken, unzureichend gegen E. coli, Klebsiella spp. Für eine gezielte Therapie von Staphylococcus-aureus- Infektionen und zur perioperativen Prophylaxe geeignet Wirksam gegen Streptokokken und Staphylokokken, erweitertes Spektrum im gramnegativen Bereich einschließlich Haemophilus influenzae Zur perioperativen Prophylaxe geeignet, wenn auch E. coli (Abdominalchirurgie) mit abgedeckt sein soll, Einschränkung der oralen Therapie wegen schlechter oraler Bioverfügbarkeit (ca. 40 %, bei alkalischem Magensaft z. B. unter PPI noch geringer) Gute Wirksamkeit gegen Pneumokokken und Streptokokken sowie gramnegative Erreger; zusätzlich Borrelien, Gonokokken, Meningokokken, gegen Staphylococcus aureus (MSSA) schwächer wirksam als Cephalosporine der Gruppe 1 oder 2, daher zur perioperativen Prophylaxe weniger gut geeignet Wirksamkeit gegen Pseudomonas aeruginosa, soweit keine Resistenzen; gegen Pneumokokken, Streptokokken und Staphylokokken (MSSA) unzureichend wirksam Durch Avibactam Erweiterung des Spektrums auf Carbapenem- Resistenzen Ambler-Klassen A und C, keine Wirkung gegenüber Metallobetalaktamasen (Ambler B) und der Mehrzahl der OXA- Serin-Betalaktamasen (Ambler D) Zulassung und Einschränkungen durch Resistenzen in Deutschland Resistenzentwicklung unter Therapie Breite Zulassung Keine Anaerobier-, Legionellenund Enterokokken-Wirksamkeit (natürliche Resistenz), keine Wirksamkeit bei MRSA Breite Zulassung Anaerobier-, Legionellen- und Enterokokken-Lücke, Inaktivierung durch ESBL Breite Zulassung Anaerobier-, Legionellen- und Enterokokken-Lücke, Inaktivierung durch ESBL, keine Pseudomonas-Wirksamkeit Breite Zulassung Steigende Pseudomonas- Resistenzen Anaerobier-, Legionellen- und Enterokokken-Lücke Inaktivierung durch ESBL Ceftazidim/Avibactam: FDA-Zulassung für komplizierte intraabdominelle Infektionen (ciai) und komplizierte HWI 2015, Zulassung in Europa 2016 für ciai, komplizierte Harnwegsinfektionen einschließlich Pyelonephritis (cuti), nosokomiale Pneumonie (HAP) einschließlich beatmungsassoziierte Pneumonie (VAP), Behandlung von aeroben (Fortsetzung)
11 Rationaler Einsatz von Antibiotika 11 Tab. 2 (Fortsetzung) Antibiotikaklasse Carbapeneme (Beta-Laktam) Gruppeneinteilung und relevante Substanzen Gruppe 4 Cefepim Gruppe 5 Ceftobiprol Ceftarolin Ceftolozan Gruppe 1 Meropenem Imipenem Wichtige Eigenschaften Gute Pseudomonas-aeruginosa- Wirksamkeit, auch gegen AmpC- Betalaktamasen-positive Enterobacteriaceae wie Enterobacter spp. und Citrobacter spp., nicht gegen ESBL wirksam Gegen Staphylococcus aureus wie Gruppe 3a und 3b unzureichend Ceftobiprol entspricht der Gruppe 4 plus MRSA- und Enterococcusfaecalis-Wirksamkeit Ceftarolin entspricht der Gruppe 3a plus MRSA- und Enterococcus-faecalis- Wirksamkeit Ceftolozan nur in fixer Kombination mit Tazobactam: Breites Wirkspektrum einschließlich multiresistenter Pseudomonas aeruginosa, entsprechend Gruppe 4 Aktuell noch geringe Anwendungserfahrungen Keine Wirksamkeit gegen MRSA, Enterokokken sowie einige ESBL Breitestes Wirkungsspektrum im grampositiven und gramnegativen Bereich einschließlich Pseudomonas aeruginosa, Acinetobacter baumannii, Anaerobier und Zulassung und Einschränkungen durch Resistenzen in Deutschland gramnegativen Infektionen bei erwachsenen Patienten, deren Behandlungsmöglichkeiten eingeschränkt sind Breite Zulassung Alle systemischen oder lokalen Infektionen durch sensible Erreger Anaerobier-, Legionellen- und Enterokokken-Lücke Inaktivierung durch ESBL Nur für ambulant erworbene Pneumonie (CAP) und hospitalacquired pneumonia (HAP) zugelassen, nicht jedoch für die Beatmungs-assoziierte Pneumonie (VAP) Wird durch ESBL inaktiviert Aktuell noch geringe Anwendungserfahrung MRSA-Indikation Off-Label- Anwendung Für CAP und acute bacterial skin and skin structure infection (ABSSSI) bzw. akute bakterielle Haut-Weichgewebeinfektionen (ABHWGI) (HWGI) zugelassen Wird durch ESBL inaktiviert Aktuell noch wenig Anwendungserfahrung MRSA-Indikation Off-Label- Anwendung Für komplizierte Harnwegsinfektionen einschließlich Pyelonephritis und komplizierte intraabdominelle Infektionen (ciai) durch gramnegative sensible Erreger, in den USA auch für nosokomiale Pneumonie (VAP) zugelassen Breite Zulassung Für Meningitis nur Meropenem zugelassen Inaktivierung durch Carbapenemasen oder Doppelresistenzen durch ESBL (Fortsetzung)
12 12 P. Walger Tab. 2 (Fortsetzung) Antibiotikaklasse Monobactame (Beta-Laktame) Gruppeneinteilung und relevante Substanzen Gruppe 2 Ertapenem Aztreonam (keine Zulassung in Deutschland) Inhalativ: Aztreonam inhalativ Fluorochinolone Gruppe 1 Nur oral: Norfloxacin Gruppe 2 Ciprofloxacin Ciprofloxacin Wichtige Eigenschaften ESBL-Bildner Keine Wirksamkeit gegen Stenotrophomonas maltophilia, MRSA und Enterococcus faecium Wie Gruppe 1, aber keine Wirksamkeit gegen Enterococcus faecalis, einige Enterobacteriaceae, Pseudomonas aeruginosa und Acinetobacter baumannii Ausschließlich gegen gramnegative Erreger wirksam außer Acinetobacter baumannii, Stenotrophomonas maltophilia und ESBL-Bildner, wirksam gegen Carbapenemase-Bildner vom MBL-Typ (Metallobetalaktamasen) Gramnegative Stäbchen, Pseudomonas aeruginosa Nur noch bei Harnwegsinfektionen oder zur Sekundärprophylaxe bei spontan bakterieller Peritonitis eingesetzt Gute Wirksamkeit gegen gramnegative Erreger einschließlich Pseudomonas aeruginosa und Haemophilus influenzae Unzureichend wirksam gegen Staphylococcus aureus (MSSA), Pneumokokken und Enterokokken Schwächer wirksam gegen Zulassung und Einschränkungen durch Resistenzen in Deutschland oder AmpC plus Porenverlust Resistenzen durch Carbapenemasen weltweit steigend, noch <1 %in Deutschland, aber Ausbrüche (!), auch polyklonale Ausbrüche durch Plasmidtransfer Breite Zulassung Nicht Meningitis! Inaktivierung durch Carbapenemasen (siehe oben) In Deutschland geringe Anwendungserfahrung In Zukunft bedeutsam in Kombination mit neuem Betalaktamase-Inhibitor Avibactam wegen Wirksamkeit gegen alle Carbapenemase- Bildner, einschließlich Metallobetalaktamasen (z. B. NDM-1), weil Aztreonam gegen MBL wirkt und Avibactam die Wirksamkeit auf Carbapenemasen vom Serin-Typ ausweitet Wegen hoher E.-coli-Resistenzen und fehlender systemischer Wirkung nur noch geringe Bedeutung Nach Risikobewertung durch die FDA (2016) wegen zum Teil schwerer irreversibler Nebenwirkungen am muskuloskelettalen System sowie am peripheren und zentralen Nervensystem Indikationseinschränkung nur noch für schwere Infektionen, bei denen es keine Alternativen gibt; eine Risikoneubewertung durch die EMA ist auch in Europa initiiert (2017) Breite Zulassung Nieren- und Harnwegsinfektionen, HNO, Atemwege (nicht bei Pneumokokken), Bauchraum, Genitalorgane, Knochen- und Gelenke, Haut- und Weichgewebe, Sepsis, Neutropenie Wegen steigender Resistenzen bei (Fortsetzung)
13 Rationaler Einsatz von Antibiotika 13 Tab. 2 (Fortsetzung) Antibiotikaklasse Aminoglykoside Gruppeneinteilung und relevante Substanzen Gruppe 3 Levofloxacin Levofloxacin Gruppe 4 Moxifloxacin Moxifloxacin Gentamicin Tobramycin Amikacin Streptomycin (TBC) Topisch: Neomycin (dermatologisch) Paramomycin (intestinal) Wichtige Eigenschaften atypische Pneumonieerreger Chlamydien, Legionellen und Mykoplasmen im Vergleich zu Fluorochinolonen der Gruppen 3 und 4 (siehe unten) Bessere Wirksamkeit gegen grampositive Erreger wie Staphylokokken (MSSA), Streptokokken, Pneumokokken sowie die Erreger atypischer Pneumonien Chlamydien, Legionellen und Mykoplasmen Gegen Pseudomonas aeruginosa schwächer als Ciprofloxacin (Gruppe 2) Wirkungsspektrum wie Gruppe 3, aber mit Pseudomonas-Lücke, deutlich höhere Wirksamkeit bei grampositiven Erregern und bessere Wirksamkeit bei den Erregern atypischer Pneumonien, zusätzlich gute Wirksamkeit gegenüber Anaerobiern, Stellenwert in der Tuberkulose- Therapie Gute Wirksamkeit im gramnegativen Bereich, aber in den letzten Jahren abnehmende Bedeutung wegen Oto- und Nephrotoxizität In der gezielten Therapie als Kombinationspartner bei Infektionen durch multiresistente Erreger und optional bei Endokarditis; wichtige Reserveantibiotika Keine Wirksamkeit im sauren und anaeroben Milieu Zulassung und Einschränkungen durch Resistenzen in Deutschland Enterobacteriaceae (besonders E. coli) sowie Selektion von MRSA und C. difficile Bedeutungsverlust in der kalkulierten Initialtherapie Einschränkung auf schwere Infektionen wegen Persistenz schwerer Nebenwirkungen (siehe oben) Breite Zulassung Ambulant erworbene Pneumonie (CAP), ABSSSI Wegen steigender Resistenzen bei Enterobacteriaceae (besonders E. coli) sowie Selektion von MRSA und C. difficile Bedeutungsverlust in der kalkulierten Initialtherapie schwerer Infektionen Einschränkung auf schwere Infektionen wegen Persistenz schwerer Nebenwirkungen (siehe oben) Breite Zulassung CAP, infektexazerbierte chronisch-obstruktive Lungenerkrankung (COPD), ABSSSI Wegen steigender Resistenzen bei Enterobacteriaceae (besonders E. coli) sowie Selektion von MRSA und C. difficile Bedeutungsverlust in der kalkulierten Initialtherapie Einschränkung auf schwere Infektionen wegen Persistenz schwerer Nebenwirkungen (siehe oben) Breite Zulassung Kombinationspartner bei schweren (nosokomialen) Infektionen durch gramnegative Erreger, Fieber in Neutropenie, Pseudomonas-Infektionen bei zystischer Fibrose und anderen strukturellen Lungenerkrankungen, Endokarditis Bei Therapie >3 Tage Therapeutisches Drug- Monitoring (TDM) indiziert (Fortsetzung)
14 14 P. Walger Tab. 2 (Fortsetzung) Antibiotikaklasse Glykopeptide Zyklische Lipopeptide Gruppeneinteilung und relevante Substanzen Vancomycin Teicoplanin Dalbavancin Oritavancin Vancomycin Teicoplanin Daptomycin Wichtige Eigenschaften Ausschließlich gegen grampositive Erreger wirksam, einschließlich MRSA und Enterococcus faecium Als orale Therapie ist Vancomycin bei C. difficile indiziert, Teicoplanin auch wirksam, aber keine Daten, keine Nennung in Leitlinien Ausschließlich gegen grampositive Erreger wirksam, einschließlich MRSA und VRE Polymyxine Colistin Ausschließlich gegen gramnegative Erreger wirksam, einschließlich multiresistente Enterobacteriaceae, Pseudomonas aeruginosa und Acinetobacter baumannii (ESBLund Carbapenemase-Bildner) Wichtiges Reserveantibiotikum mit steigender Bedeutung Zulassung und Einschränkungen durch Resistenzen in Deutschland Sepsis, Endokarditis, Knochenund Gelenksinfektionen, Haut- Weichgewebe-, Nieren- und Harnwegsinfektionen Wegen Nephrotoxizität TDM indiziert Keine relevante Resistenzen von MRSA, aber steigende induzierbare Resistenzen bei Enterococcus faecium (Vancomycin-resistente Enterokokken [VRE], VanA-Typ Vancomycin- und Teicoplaninresistent, VanB-Typ nur Vancomycin-resistent) Dalbavancin und Oritavancin: Zulassung für ABSSSI seit März 2016, lange Halbwertszeit, 1 oder 2 Applikationen im Abstand von 7 Tagen, aktuell noch keine ausreichenden Erfahrungen in der Anwendung Zugelassen zur Therapie der Rechtsherz- Endokarditis Bakteriämie durch MRSA, ABSSSI Sinnvoll bei VRE-Bakteriämie bzw. -Endokarditis Off-Label- Anwendung Kontraindiziert bei Pneumonie (Inaktivierung durch Surfactant) Aktuell noch keine relevanten Resistenzraten, aber sporadisch bei MRSA und VRE Wichtiges Reserveantibiotikum bei ABSSSI Wegen guter Gewebegängigkeit und Biofilmaktivität zunehmende Bedeutung bei Fremdkörperassoziierten Infektionen (Off-Label-Anwendung) Zulassung für Infektionen mit Colistin-empfindlichen Erregern, wenn die Behandlungsmöglichkeiten eingeschränkt sind Colistin soll möglichst mit einem anderen geeigneten Antibiotikum kombiniert werden; bei Monoeinsatz muss mit steigenden Resistenzen gerechnet werden Aktuell Beginn einer weltweiten Ausbreitung Colistin-resistenter E. coli nach Colistin-Einsatz in der Geflügelmast, Erstnachweis des übertragbaren Gens mcr-1 in China (Fortsetzung)
15 Rationaler Einsatz von Antibiotika 15 Tab. 2 (Fortsetzung) Antibiotikaklasse Epoxide Nitroimidazole Makrozykline Ansamycine Gruppeneinteilung und relevante Substanzen Fosfomycin Fosfomycin- Trometamol Metronidazol Metronidazol Fidaxomycin (nur oral verfügbar) Rifampicin Rifampicin Rifabutin (nur oral verfügbar) Rifaximin (nur oral verfügbar) Wichtige Eigenschaften Breites Wirkspektrum gegen gramnegative und grampositive Erreger einschließlich multiresistenter Erreger (ESBL- Bildner, MRSA, VRE) Nicht wirksam gegen Acinetobacter spp. und Anaerobier der Bacteroides- Spezies Wirksam gegen anaerobe grampositive und gramnegative Bakterien Nicht wirksam gegen Propionibakterien und Actinomyzeten Orales Schmalspektrumantibiotikum gegen Clostridium difficile Wichtiges Tuberkulostatikum in der Vierfachkombination Wirksamste Biofilm-aktive Substanz, Empirisch bei akuten Fremdkörper-assoziierten Infektionen und hoher Wahrscheinlichkeit von Staphylococcus aureus; ansonsten nur gezielt bei nachgewiesener Sensibilität von MRSA oder Koagulase-negativen Staphylokokken (KNS) Wirksamkeit gegen atypische Mykobakterien (Mycobacteriumavium-intracellulare-Komplex, MAI-Komplex) Wirksam gegen nichtinvasive bakterielle Erreger der Reisediarrhoe Keine ausreichende Wirksamkeit gegen Clostridium difficile Zulassung und Einschränkungen durch Resistenzen in Deutschland Breite Zulassung Wegen schneller sekundärer Resistenzentwicklung nur als Kombinationspartner einzusetzen Wichtiges Reserveantibiotikum bei multiresistenten Erregern, bei gramnegativen Erregern einschließlich Pseudomonas aeruginosa möglichst nur gezielt einsetzen (nach Resistogramm) Nephrotoxizität und Natriumbelastung beachten Breite Zulassung für Infektionen durch Anaerobier und zur perioperativen Prophylaxe In der Regel als Kombinationspartner bei Mischinfektionen; Monotherapie bei leichter bis mittelschwerer C.-difficile-Kolitis (oral und parenteral wirksam) Zusätzliche Indikationen bei Protozoen-Infektionen (Tab. 3) sowie bei Helicobacter-pyloriassoziierter Ulkus-/Gastritis- Krankheit als Teil der Tripletherapie Zulassung zur Therapie bei Rezidiven von C.-difficile-Kolitis Zulassung zur Therapie der Tuberkulose Bei Fremdkörper-assoziierten Infektionen durch Staphylococcus aureus und nachgewiesener Sensibilität in der Off-Label- Anwendung wichtigste Biofilmwirksame Substanz Bei Meningokokken-Meningitis und invasiven Haemophilusinfluenzae-Infektionen zur postexpositionellen Meningitis- Prophylaxe indiziert Prophylaxe und Therapie von Infektionen durch atypische Mykobakterien, besonders von MAI bei AIDS-Patienten Zugelassen zur Therapie der unkomplizierten Reisediarrhoe (zweifelhafte Indikation) sowie zur Rezidivprophylaxe der hepatischen Enzephalopathie Studienlage unzureichend (Fortsetzung)
16 16 P. Walger Tab. 2 (Fortsetzung) Antibiotikaklasse Nitrofurane Gruppeneinteilung und relevante Substanzen Nitrofurantoin (nur oral verfügbar) Wichtige Eigenschaften Wirksam gegen grampositive Erreger von Harnwegsinfektionen (HWI) (Staphylokokken, Streptokokken, Enterokokken, einschließlich E. faecium und VRE) sowie die wichtigsten gramnegativen Bakterien einschließlich ESBL-Bildner Keine Wirksamkeit gegen Pseudomonas aeruginosa, Acinetobacter spp. und Proteus spp. Zulassung und Einschränkungen durch Resistenzen in Deutschland Nach S3-Leitlinie zur Therapie des unkomplizierten HWI empfohlen (Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften AWMF Konsultationsfassung 2016) Trotz breiter Zulassung heute nur noch zur Therapie von unkomplizierten HWI verwendet Die Weiterverwendung dieses Chemotherapeutikums ist ein warnendes Beispiel für Perpetuierung historischer Irrtümer in der Medizin (Brodt 2013) BLI, Betalaktamase-Inhibitor; CAP, Ambulant erworbene Pneumonie (community-acquired pneumonia); COPD, chronisch-obstruktive Lungenerkrankung; ESBL, extended-spectrum beta-lactamases; FDA, Food and Drug Administration; HAP, hospital-acquired pneumonia, (chronic obstructive pulmonary diesease); Hp, Helicobacter pylori; ABHWGI, akute bakterielle Haut- und Weichgewebeinfektionen; HWI, Harnwegsinfektionen; KNS, Koagulase-negative Staphylokokken; MAI, Mycobacterium avium-intracellulare; MBL, Metallobetalaktamasen; MRSA, Methicillin-resistenter Staphylococcus aureus; MSSA, Methicillin-sensibler Staphylococcus aureus; ABSSSI acute bacterial skin and skin structure infection, skin and skin structure infection; TDM, Therapeutisches Drug-Monitoring; VAP, ventilator-associated pneumonia Substanz Clindamycin), Glycylcycline (einzige Substanz Tigecyclin), Cotrimoxazol und die Oxazolidinone Linezolid und Tedizolid. Bakteriostatische Antibiotika sind in der Regel bei Sepsis, schweren Infektionen mit Bakteriämie oder bei Infektionen in schlecht erreichbaren Organen bzw. Geweben in der empirisch kalkulierten Therapie nicht geeignet oder nur als Kombinationspartner zusammen mit einer bakteriziden Substanz einzusetzen (2, 13). Die häufigste Kombination betrifft das Schließen der Legionellenlücke aller Beta-Laktam-Antibiotika durch zusätzliche Gabe eines Makrolids bei der Initialtherapie der schweren ambulant erworbenen Pneumonie (community acquired pneumonia, CAP). Auch wenn Substanzen eingesetzt werden, die ausschließlich im grampositiven Erregerspektrum wirksam sind, wie zum Beispiel Daptomycin oder Linezolid bzw. Tedizolid, kann eine Kombination zur Erweiterung des Spektrums in den gramnegativen Bereich sinnvoll sein. Eine Mischätiologie kann zum Beispiel bei abdominellen oder komplizierten Haut- und Weichgewebeinfektionen oder bei einer Aspirationspneumonie vermutet werden. Relevante Wirkungslücken, die Anlass zu Kombinationstherapien sein können, sind die Enterokokken- und Anaerobierlücke der Cephalosporine bis zur 4. Generation oder die Pseudomonas-Lücke von Moxifloxacin, Ertapenem und Tigecyclin. Der unterschiedliche Zulassungsstatus der Antibiotika zeigt, dass im Gegensatz zu den älteren Substanzen mit sehr breitem Zulassungsspektrum die neueren Antibiotika in der Regel nur für wenige Indikationen zugelassen sind. Indikationen, die allein durch die Resistenzlage des Erregers erforderlich werden, weil sie ohne Alternative sind, liegen daher häufig im Off-Label- Bereich (Bodman et al. 2010; Brodt 2013; Karow und Lang-Roth 2016).
17 Rationaler Einsatz von Antibiotika Charakterisierung der Antibiotika Vgl. Tab. 3 und Richtige Anordnung der antibiotischen Therapie Zur richtigen Anordnung einer antibiotischen Therapie gehören folgende Festlegungen, die in Form einer schriftlichen Eintragung in der Patientenakte dokumentiert sein sollten: Indikationsdiagnose Nennung des Antibiotikums als Generikum (kein Produktname) Nennung von Dosis, Dosisintervall und Applikationsmodus Anordnung der Dauer (vorläufig, Änderung nach mikrobiologischen Befunden und Response) Anordnung der Response-Kontrollen nach 48 und/oder nach 72 Stunden In Abhängigkeit von mikrobiologischen Befunden, den Ergebnissen der Response- Kontrollen, von möglichen Nebenwirkungen und von pharmakokinetischen Aspekten (z. B. einer eingeschränkten Nierenfunktion) erfolgen Modifikationen der Dosis, des Dosisintervalls oder/und der Substanzwahl, oder es ist eine erweiterte Diagnostik oder zusätzliche Therapie erforderlich. Zeichen eines Response sind Besserung der klinischen Symptomatik, Rückbildung der klinischen Instabilität und Nachweis des Abfalls der inflammatorischen Parameter. Als definierte Zeichen der klinischen Stabilität können in Anlehnung an die S3-Leitlinie zur CAP folgende Parameter gewertet werden: Herzfrequenz <101/min Atemfrequenz <25/min Systolischer Blutdruck >89 mmhg Körpertemperatur <37,9 C Gesicherte Nahrungsaufnahme oral oder über sichere Zugänge Normaler Bewusstseinszustand oder status quo ante bei ZNS-Erkrankung Fehlen einer Hypoxämie, d. h. po 2 > 59 mmhg bzw. SaO 2 > 89 % unter Raumluft bzw. bei Patienten mit Sauerstoffpflichtigkeit unter Sauerstoffgabe 3.4 Richtige Dauer der antibiotischen Therapie In den letzten Jahren zeigte sich in zahlreichen Studien ein deutlicher Trend zu kürzeren Therapiezeiten (Tab. 5). Für viele Infektionen liegen aber keine gesicherten Daten aus kontrollierten Studien über die definitive Dauer der antibiotischen Therapie vor. In jedem Einzelfall ist daher die konkrete Entscheidung zur Beendigung der Therapie vom Nachweis eines Response abhängig. Bei schnellem Response innerhalb von 2 3 Tagen sind die kürzeren (leitliniengerechten) Therapiezeiten zu wählen. Aus den Leitlinien lassen sich die in Tab. 5 zusammengestellten Empfehlungen zur Therapiedauer geben. 3.5 Sequenztherapie Wechsel von parentaler auf orale Therapie Bei klinischem Ansprechen, Erzielen einer klinischen Stabilität und Rückgang der inflammatorischen Parameter kann frühzeitig von einer parenteralen auf eine orale Therapie umgestellt werden. Diese sequenzielle Therapie sollte frühestens ab dem 2. oder 3. Tag beginnen und nicht zu einer Verlängerung der gesamten Therapiedauer führen. Bei sehr gutem Ansprechen der Therapie bis Tag 2 und einer möglichen Therapiedauer von <5 Tagen kann auf die orale Umstellung verzichtet werden. Der Einsatz oraler Antibiotika sollte nur mit Substanzen erfolgen, die eine ausreichende orale Bioverfügbarkeit besitzen. Hierzu gehören (in der angegebenen ausreichend hohen Dosierung und unter Berücksichtigung zusätzlicher Empfehlun-
18 18 P. Walger Tab. 3 Einteilung der wichtigsten bakteriostatischen Antibiotika nach Klassen und Gruppen mit Indikationen und Zulassungen (Bodman et al. 2010; Brodt 2013; Zugegriffen am ) Antibiotikaklasse Oxazolidinone Glycylcycline Makrolide Lincosamide Folsäureantagonisten Relevante Substanzen Linezolid Tedizolid Linezolid Tedizolid Tigecyclin Erythromycin Clarithromycin Azithromycin Erythromycin Clarithromycin Azithromycin Roxithromycin Clindamycin Clindamycin Cotrimoxazol Cotrimoxazol Wichtige Eigenschaften Ausschließlich gegen grampositive Erreger wirksam, einschließlich MRSA und VRE Breites Wirkspektrum gegen gramnegative und grampositive Erreger, einschließlich ESBL- Bildner, MRSA, VRE, Anaerobier, Chlamydien, Legionellen, Mykoplasmen und Carbapenemresistente Enterobacteriaceae und Acinetobacter spp. Keine Wirksamkeit gegen Pseudomonas aeruginosa, Proteus spp. und Morganella morganii Gute Wirksamkeit gegen Mykoplasmen, Legionellen, Chlamydien, Streptokokken, einschließlich Pneumokokken und Bordetella pertussis sowie weitere atypische Infektionserreger wie Bartonella spp. (Katzenkratz- Krankheit), Campylobacter jejuni, Corynebacterium diphtheriae, Haemophilus ducreyi (weicher Schanker), atypische Mykobakterien (MAI) Unzureichend gegen Haemophilus influenzae, steigende Resistenzen bei Helicobacter pylori (Hp) Wirksam gegen Staphylokokken, Streptokokken, Anaerobier der Bacteroides-Spezies, Corynebakterien und Mycoplasma pneumoniae Hemmung der Toxinproduktion von Streptokokken und Staphylokokken bei Toxic-Shock- Syndromen Breites Wirkspektrum gegen grampositive und gramnegative Erreger, Nocardia spp. Zulassung und Einschränkungen durch Resistenzen in Deutschland Zugelassen zur Therapie von CAP, HAP und komplizierten ABSSSI Sporadisch Resistenzen von VRE und KNS, besonders bei hohem Selektionsdruck Keine Indikation bei Bakteriämie oder Sepsis Zugelassen zur Therapie komplizierter ABSSSI und komplizierter intraabdomineller Infektionen (ciai) Aktuell noch keine relevanten Resistenzen Keine Indikation bei Sepsis, Bakteriämie und nosokomialer Pneumonie Wichtiges Reserveantibiotikum bei Multiresistenz In der Standarddosierung (Label- Anwendung) eher unterdosiert Zulassung bei Atemwegsinfektionen, Keuchhusten, Diphtherie, Scharlach und Erysipel Wichtiger Kombinationspartner bei stationärer CAP (3 Tage), Clarithromycin ist Teil der Tripletherapie der Hp-Gastritis- Krankheit (cave: steigende Resistenzen) Es wird ein immunmodulatorischer Effekt angenommen (Amsden 2005) Resistenzen bei Pneumokokken fallend Wegen guter Gewebegängigkeit besonders bei Knochen- und Gelenksinfektionen, komplizierten ABSSSI und komplizierten Infektionen im HNO-, Zahn-, Mund- und Kieferbereich Breite Zulassung, aber sinkende Bedeutung als Harnwegsantibiotikum wegen hoher E.-coli-Resistenzen Mittel der Wahl in der Therapie der Pneumocystis-jiroveci-Pneumonie, Toxoplasmose-Enzephalitis (Tab. 4) und Nokardiose (Fortsetzung)
1 Infektion der Atemwege
 1 Infektion der Atemwege 1.1 Infektexazerbation bei COPD Ca. 50% der Exazerbationen einer COPD werden durch Infektionserreger ausgelöst, überwiegend durch respiratorische Viren. Die häufigsten bakteriellen
1 Infektion der Atemwege 1.1 Infektexazerbation bei COPD Ca. 50% der Exazerbationen einer COPD werden durch Infektionserreger ausgelöst, überwiegend durch respiratorische Viren. Die häufigsten bakteriellen
Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK.
 Antibiotika Dosierungen Stand:Januar 2017 Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK. Penicilline iv Standarddosierung Höhere Dosierung
Antibiotika Dosierungen Stand:Januar 2017 Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK. Penicilline iv Standarddosierung Höhere Dosierung
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST. Karlsruhe, im März Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege,
 EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im März 2019 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im März 2019 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST. Karlsruhe, im August Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege,
 EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im August 2018 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im August 2018 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
Empirische antibiotische Therapie bei schwerer Sepsis
 MEDIZINISCHE KLINIK TÜBINGEN Empirische antibiotische Therapie bei schwerer Sepsis Infektionsmedizin 2011 Reimer Riessen Internistische Intensivstation Bedeutung einer raschen Antibiotikatherapie Jede
MEDIZINISCHE KLINIK TÜBINGEN Empirische antibiotische Therapie bei schwerer Sepsis Infektionsmedizin 2011 Reimer Riessen Internistische Intensivstation Bedeutung einer raschen Antibiotikatherapie Jede
Antibiotikatherapie im Kassenärztlichen Notdienst. Dr. Bettina Tiemer Laborärztliche Gemeinschaftspraxis www. mrsaplus.
 Antibiotikatherapie im Kassenärztlichen Notdienst Dr. Bettina Tiemer Laborärztliche Gemeinschaftspraxis www.labor-luebeck.de www. mrsaplus.de MRSAplus 10. Fallkonferenz 16.09.2015 85-90% der Antibiotika-Verordnungen
Antibiotikatherapie im Kassenärztlichen Notdienst Dr. Bettina Tiemer Laborärztliche Gemeinschaftspraxis www.labor-luebeck.de www. mrsaplus.de MRSAplus 10. Fallkonferenz 16.09.2015 85-90% der Antibiotika-Verordnungen
Resistenzbericht Manfred Fille
 Resistenzbericht 216 Manfred Fille gefährli hste Erreger ( a h WHO, Februar 217) Kritische Priorität: Acinetobacter baumannii, resistent gegen Carbapeneme Pseudomonas aeruginosa, resistent gegen Carbapeneme
Resistenzbericht 216 Manfred Fille gefährli hste Erreger ( a h WHO, Februar 217) Kritische Priorität: Acinetobacter baumannii, resistent gegen Carbapeneme Pseudomonas aeruginosa, resistent gegen Carbapeneme
Ambulant erworbene Pneumonie
 Ambulant erworbene Pneumonie AWMF-Leitlinien-Register Nr. 82/001 Pneumologie. 2009 Oct;63(10):e1-68 Pneumologie. 2010 Mar;64(3):149-54 20, 21 Risikostratifizierung mit Hilfe des CRB- 65 Score C onfusion
Ambulant erworbene Pneumonie AWMF-Leitlinien-Register Nr. 82/001 Pneumologie. 2009 Oct;63(10):e1-68 Pneumologie. 2010 Mar;64(3):149-54 20, 21 Risikostratifizierung mit Hilfe des CRB- 65 Score C onfusion
Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang
 WWW.INFEKTIO.DE Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang Register 2016 Heft 1 Heft 2 Heft 3 Heft 4 Heft 5 Heft 6 Seiten 1-10 Seiten 11-20 Seiten 21-30 Seiten
WWW.INFEKTIO.DE Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang Register 2016 Heft 1 Heft 2 Heft 3 Heft 4 Heft 5 Heft 6 Seiten 1-10 Seiten 11-20 Seiten 21-30 Seiten
Erregerhäufigkeit bei akuter bakterieller Meningitis
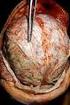 Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
Therapeutische Optionen bei Multiresistenten Erregern. OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel
 Therapeutische Optionen bei Multiresistenten Erregern OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel Themen Multiresistente Erreger MRSA MRGN VRE Therapeutische Optionen MRE-Netzwerk
Therapeutische Optionen bei Multiresistenten Erregern OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel Themen Multiresistente Erreger MRSA MRGN VRE Therapeutische Optionen MRE-Netzwerk
Trends und Resistenzeckdaten 2010
 Trends und Resistenzeckdaten 21 21 hat sich die Resistenzsituation weiter verschlechtert. Diese Tatsache ist vor allem auf den Anstieg von gramnegativen Darmbakterien zurückzuführen, die in der Lage sind,
Trends und Resistenzeckdaten 21 21 hat sich die Resistenzsituation weiter verschlechtert. Diese Tatsache ist vor allem auf den Anstieg von gramnegativen Darmbakterien zurückzuführen, die in der Lage sind,
Antibiotikatherapie - Grundlagen
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Antibiotikatherapie - Grundlagen B. Salzberger Hemmung der Zellwandsynthese: Penicilline, Cephalosporine, Glykopeptid-AB, Fosfomycin Proteinsynthese (Translation)
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Antibiotikatherapie - Grundlagen B. Salzberger Hemmung der Zellwandsynthese: Penicilline, Cephalosporine, Glykopeptid-AB, Fosfomycin Proteinsynthese (Translation)
UNIVERSALINSTRUMENT ANTIBIOTIKUM?
 CAMPUS GROSSHADERN CAMPUS INNENSTADT UNIVERSALINSTRUMENT ANTIBIOTIKUM? Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene 02.04.2014 B. Grabein DIE INSTRUMENTE Daptomycin Aminoglykoside
CAMPUS GROSSHADERN CAMPUS INNENSTADT UNIVERSALINSTRUMENT ANTIBIOTIKUM? Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene 02.04.2014 B. Grabein DIE INSTRUMENTE Daptomycin Aminoglykoside
ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH
 CAMPUS GROSSHADERN CAMPUS INNENSTADT ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene WANN KOMMT EIN IMPLANTATERHALTUNGSVERSUCH
CAMPUS GROSSHADERN CAMPUS INNENSTADT ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene WANN KOMMT EIN IMPLANTATERHALTUNGSVERSUCH
RESISTENZANALYSE Atemwegsinfekte
 RESISTENZANALYSE Atemwegsinfekte NEU - aktuelle Daten aus 2016 Die Daten geben einen Überblick der ausgebildeten Resistenzen bei den am häufigsten aufgetretenen Keimen Nur ambulante Patienten Antibiotika
RESISTENZANALYSE Atemwegsinfekte NEU - aktuelle Daten aus 2016 Die Daten geben einen Überblick der ausgebildeten Resistenzen bei den am häufigsten aufgetretenen Keimen Nur ambulante Patienten Antibiotika
Mikrobiologisches Labor Doz. Möst Erreger- und Resistenzstatistik Harnkulturen
 Harnkulturen Harnproben gesamt: 10869 Erregerspektrum Enterobakterien Escherichia coli 2967 davon ESBL bildend 245 (=8,2%) Klebsiella sp. 380 davon ESBL bildend 12 (=3,2%) Proteus mirabilis 221 Enterobacter
Harnkulturen Harnproben gesamt: 10869 Erregerspektrum Enterobakterien Escherichia coli 2967 davon ESBL bildend 245 (=8,2%) Klebsiella sp. 380 davon ESBL bildend 12 (=3,2%) Proteus mirabilis 221 Enterobacter
Dr. med. Stefan Schmitt MVZ Dr. Klein Dr. Schmitt & Kollegen, Kaiserslautern AGIL e.v. Grünstadt
 Passgenauigkeit in der Antibiotikatherapie Aktuelle regionale und bundesweite Daten zur Infektionslage bzw. Resistenzentwicklung als Grundlage einer rationellen Antibiotikatherapie Dr. med. Stefan Schmitt
Passgenauigkeit in der Antibiotikatherapie Aktuelle regionale und bundesweite Daten zur Infektionslage bzw. Resistenzentwicklung als Grundlage einer rationellen Antibiotikatherapie Dr. med. Stefan Schmitt
Antibiotikaverbrauch in der Arztpraxis in Hessen
 Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Antibiotikaresistenzen vermeiden Antibiotikaverbrauch in der Arztpraxis in Hessen 2008-2015 Dr. med. Harald Herholz, MPH Kassenärztliche Vereinigung
Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Antibiotikaresistenzen vermeiden Antibiotikaverbrauch in der Arztpraxis in Hessen 2008-2015 Dr. med. Harald Herholz, MPH Kassenärztliche Vereinigung
München. Zentrales Institut des Sanitätsdienstes der Bundeswehr. Rationale Antibiotikatherapie. OFA Bock. Text Stand: xx.xx.xxxx
 Zentrales Institut des Sanitätsdienstes der Bundeswehr München Rationale Antibiotikatherapie OFA Bock Einführung Schön wär`s gewesen wenn Einführung Bakterien sind schneller als die Menschen! Fragen für
Zentrales Institut des Sanitätsdienstes der Bundeswehr München Rationale Antibiotikatherapie OFA Bock Einführung Schön wär`s gewesen wenn Einführung Bakterien sind schneller als die Menschen! Fragen für
Mikrobiologisches Labor Doz. Möst Erreger- und Resistenzstatistik Harnkulturen. Erregerspektrum
 Harnkulturen Harnproben gesamt: 13117 Erregerspektrum Enterobakterien Escherichia coli 3718 davon ESBL bildend 281 (=8,1%) Klebsiella sp. 3 davon ESBL bildend 10 (=2,2%) Proteus mirabilis 290 Enterobacter
Harnkulturen Harnproben gesamt: 13117 Erregerspektrum Enterobakterien Escherichia coli 3718 davon ESBL bildend 281 (=8,1%) Klebsiella sp. 3 davon ESBL bildend 10 (=2,2%) Proteus mirabilis 290 Enterobacter
Übersicht Antibiotika
 Übersicht Antibiotika Seit Alexander Flemming 1928 das Penicillin erfand, sind im Laufe der Jahre immer mehr Antibiotika hinzugekommen. Um dennoch den Überblick zu bewahren findet ihr hier die indizierten
Übersicht Antibiotika Seit Alexander Flemming 1928 das Penicillin erfand, sind im Laufe der Jahre immer mehr Antibiotika hinzugekommen. Um dennoch den Überblick zu bewahren findet ihr hier die indizierten
Harnkulturen. Resistenzraten von E.coli in Harnkulturen (n=3797)
 Harnkulturen Harnproben gesamt: 439 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 3797 davon ESBL bildend 239 (=6,3%) Klebsiella sp. 42 davon ESBL bildend 9 (=4,6%) Proteus mirabilis
Harnkulturen Harnproben gesamt: 439 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 3797 davon ESBL bildend 239 (=6,3%) Klebsiella sp. 42 davon ESBL bildend 9 (=4,6%) Proteus mirabilis
Gramnegative multiresistente Erreger eine unterschätzte Gefahr
 Gramnegative multiresistente Erreger eine unterschätzte Gefahr Dr. Martin Kaase NRZ für gramnegative Krankenhauserreger Ruhr-Universität Bochum martin.kaase@rub.de E. coli Wildtyp Ampicillin Piperacillin
Gramnegative multiresistente Erreger eine unterschätzte Gefahr Dr. Martin Kaase NRZ für gramnegative Krankenhauserreger Ruhr-Universität Bochum martin.kaase@rub.de E. coli Wildtyp Ampicillin Piperacillin
Hier ist eine Zusammenstellung der vom RKI ermittelten Daten der Keime, bei denen jeweils mindestes 50 Proben auf Resistenzen getestet wurden.
 Keime und Resistenzen ARS 2011 oder Vorsicht, Antibiotika! Quelle: Robert Koch-Institut: ARS, https://ars.rki.de, Datenstand: 04.01.2012 Zusammenstellung und mehr zum Thema: www.krankenhhasser.de Die Datenbank
Keime und Resistenzen ARS 2011 oder Vorsicht, Antibiotika! Quelle: Robert Koch-Institut: ARS, https://ars.rki.de, Datenstand: 04.01.2012 Zusammenstellung und mehr zum Thema: www.krankenhhasser.de Die Datenbank
S3-Leitlinie. Kurzfassung. 1. Auflage. S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG.
 S3-Leitlinie Kurzfassung 1. Auflage S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Thieme 2005 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 133711 5 Inhaltsverzeichnis:
S3-Leitlinie Kurzfassung 1. Auflage S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Thieme 2005 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 133711 5 Inhaltsverzeichnis:
Häufige Infektionen im Erwachsenalter: Diagnostik & DD
 Häufige Infektionen im Erwachsenalter: Diagnostik & DD Dr. Boris Ehrenstein Infektiologie / Rheumatologie Klinik und Poliklinik für Innere Medizin I Häufige ambulant erworbene Infektionen Sinusitis, Otitis
Häufige Infektionen im Erwachsenalter: Diagnostik & DD Dr. Boris Ehrenstein Infektiologie / Rheumatologie Klinik und Poliklinik für Innere Medizin I Häufige ambulant erworbene Infektionen Sinusitis, Otitis
Antibiotikaresistenzen in der Humanmedizin
 BVL-Symposium Herausforderungen 24: Tierarzneimittel im Fokus Nutzen, Risiken, Resistenzen 5./6. November 23, Berlin Antibiotikaresistenzen in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
BVL-Symposium Herausforderungen 24: Tierarzneimittel im Fokus Nutzen, Risiken, Resistenzen 5./6. November 23, Berlin Antibiotikaresistenzen in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
Resistenzepidemiologie 2015
 Resistenzepidemiologie 215 Arne C. Rodloff Erreger Chirurgie Escherichia coli 386 Staphylococcus aureus 39 Enterococcus faecalis 31 Staphylococcus epidermidis 227 Proteus mirabilis 134 Pseudomonas aeruginosa
Resistenzepidemiologie 215 Arne C. Rodloff Erreger Chirurgie Escherichia coli 386 Staphylococcus aureus 39 Enterococcus faecalis 31 Staphylococcus epidermidis 227 Proteus mirabilis 134 Pseudomonas aeruginosa
Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 2016 für Urine
 Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 206 für Urine September 206 Sehr geehrte Kolleginnen und Kollegen, die klinische Leitlinie Unkomplizierte Harnwegsinfektionen
Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 206 für Urine September 206 Sehr geehrte Kolleginnen und Kollegen, die klinische Leitlinie Unkomplizierte Harnwegsinfektionen
Tabelle 1.2 Antiinfektiva-Dosierungen (Auswahl)* Gruppe Appl. Patient Dosis in 24 Std. ED max. 1. Penicilline
 Allgemeines. Antiinfektiva und Dosierungen Tabelle. Antiinfektiva-Dosierungen (Auswahl)*. Penicilline Penicillin G Mo. hoch Penicillin V Mo. 0, 0, Mio. IE/kg 0, 0, Mio. IE/kg Mio. IE 8 Mio. IE 0, Mio.
Allgemeines. Antiinfektiva und Dosierungen Tabelle. Antiinfektiva-Dosierungen (Auswahl)*. Penicilline Penicillin G Mo. hoch Penicillin V Mo. 0, 0, Mio. IE/kg 0, 0, Mio. IE/kg Mio. IE 8 Mio. IE 0, Mio.
Update antimikrobielle Therapie
 Update antimikrobielle Therapie Klinische Abteilung für Infektionen und Tropenmedizin Universitätsklinik für Innere Medizin 1 Bad Bugs No Drugs E Enterococcus faecium S Staphylococcus aureus C Clostridium
Update antimikrobielle Therapie Klinische Abteilung für Infektionen und Tropenmedizin Universitätsklinik für Innere Medizin 1 Bad Bugs No Drugs E Enterococcus faecium S Staphylococcus aureus C Clostridium
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER
 Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
Multiresistente Keime - Therapie
 Multiresistente Keime - Therapie Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Ted-Frage 1 Welche Erreger sind Ihrer Ansicht
Multiresistente Keime - Therapie Dr. med. Christian Lanckohr, EDIC ABS-Experte (DGI) Klinik für Anästhesiologie, operative Intensivmedizin und Schmerztherapie Ted-Frage 1 Welche Erreger sind Ihrer Ansicht
Bedeutung von Kreuzresistenz und Mehrfachresistenz bei bakteriellen Erregern für die Initialtherapie Michael Kresken. 21./22. März 2016, Königswinter
 Bad Honnef-Symposium 2016 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Empfehlungen zur kalkulierten Initialtherapie bakterieller Erkrankungen bei Erwachsenen 21./22. März 2016, Königswinter Bedeutung
Bad Honnef-Symposium 2016 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Empfehlungen zur kalkulierten Initialtherapie bakterieller Erkrankungen bei Erwachsenen 21./22. März 2016, Königswinter Bedeutung
Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I
 Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I Risikostratifizierung in der Praxis Definition individuelles Therapieziel Klinische Evaluation,
Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I Risikostratifizierung in der Praxis Definition individuelles Therapieziel Klinische Evaluation,
Antibiotika im ambulanten Bereich. Verordnungszahlen vor dem Hintergrund von Empfehlungen
 Symposium Antibiotikaresistenz mrsa Netzwerk Land Bremen, 12. September 2012 Antibiotika im ambulanten Bereich Verordnungszahlen vor dem Hintergrund von Empfehlungen Hans Wille Institut für Klinische Pharmakologie
Symposium Antibiotikaresistenz mrsa Netzwerk Land Bremen, 12. September 2012 Antibiotika im ambulanten Bereich Verordnungszahlen vor dem Hintergrund von Empfehlungen Hans Wille Institut für Klinische Pharmakologie
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2018 INHALT
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2018 INHALT
NEUE ANTIINFEKTIVA. Martin J. Hug Apotheke des Universitätsklinikums Freiburg
 NEUE ANTIINFEKTIVA Martin J. Hug Apotheke des Universitätsklinikums Freiburg Antiinfektivaentwicklung und Resistenzbildung PDR Acinetobacter u. Pseudomonas Ceftriaxon-R N. gonorrhoeae Ceftarolin-R Staphylococcus
NEUE ANTIINFEKTIVA Martin J. Hug Apotheke des Universitätsklinikums Freiburg Antiinfektivaentwicklung und Resistenzbildung PDR Acinetobacter u. Pseudomonas Ceftriaxon-R N. gonorrhoeae Ceftarolin-R Staphylococcus
Rationaler Einsatz von Antibiotika
 Rationaler Einsatz von Antibiotika P. Walger Organ des Berufsverbandes Deutscher InternistenOrgan der Deutschen Gesellschaft für Innere Medizin ISSN 0020-9554 Internist DOI 10.1007/s00108-016-0071-5 1
Rationaler Einsatz von Antibiotika P. Walger Organ des Berufsverbandes Deutscher InternistenOrgan der Deutschen Gesellschaft für Innere Medizin ISSN 0020-9554 Internist DOI 10.1007/s00108-016-0071-5 1
Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf
 Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf - Effekte eines intensivierten MRSA screenings- J.Mattes 14 November 2012 Mühldorf The Epidemic of Antibiotic-Resistant Infections: A Call
Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf - Effekte eines intensivierten MRSA screenings- J.Mattes 14 November 2012 Mühldorf The Epidemic of Antibiotic-Resistant Infections: A Call
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim
 MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
2.2. Empirische intravenöse Therapie gemäss vermutetem Fokus
 2.2. Empirische intravenöse Therapie gemäss vermutetem Fokus Abdominal nosokomial (> 48h Hospitalisation) Amoxicillin/Clavulansäure i.v. 2.2 g i.v. 3x/Tag oder Ceftriaxon 2 g i.v. + Metronidazol 500 mg
2.2. Empirische intravenöse Therapie gemäss vermutetem Fokus Abdominal nosokomial (> 48h Hospitalisation) Amoxicillin/Clavulansäure i.v. 2.2 g i.v. 3x/Tag oder Ceftriaxon 2 g i.v. + Metronidazol 500 mg
MRE-Netz Rhein-Main Prof. Dr. Ursel Heudorf Marlene Scherer
 EVA und WIM EVA: Einflussfaktoren auf die Verordnung von Antibiotika in der Praxis WIM: Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Daten und Erfahrungen aus Hessen MRE-Netz Rhein-Main Prof.
EVA und WIM EVA: Einflussfaktoren auf die Verordnung von Antibiotika in der Praxis WIM: Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Daten und Erfahrungen aus Hessen MRE-Netz Rhein-Main Prof.
SARI http://www.antibiotika-sari.de 1
 Daten zum Verbrauch der teilnehmenden Intensivstationen im Zeitverlauf Antibiotikaverbrauch: n=116 Antimykotikaverbrauch: n=94 Institut für Umweltmedizin und Krankenhaushygiene Breisacher Str. 115 b 7916
Daten zum Verbrauch der teilnehmenden Intensivstationen im Zeitverlauf Antibiotikaverbrauch: n=116 Antimykotikaverbrauch: n=94 Institut für Umweltmedizin und Krankenhaushygiene Breisacher Str. 115 b 7916
Dr. Müllner Katalin. Prinzipien der antibiotischen Therapie
 Dr. Müllner Katalin Prinzipien der antibiotischen Therapie Kalkulierte Therapie Bei klinischer Notwendigkeit des Therapiebeginns vor dem Vorliegen der Ergebnisse der Erregerdiagnostik oder des Antibiogramms,
Dr. Müllner Katalin Prinzipien der antibiotischen Therapie Kalkulierte Therapie Bei klinischer Notwendigkeit des Therapiebeginns vor dem Vorliegen der Ergebnisse der Erregerdiagnostik oder des Antibiogramms,
Neue Antiinfektiva Alexander Mischnik Infektiologie Universitätsklinikum Freiburg
 Neue Antiinfektiva 04.03.2016 Alexander Mischnik Infektiologie Universitätsklinikum Freiburg Wirkstoff Handelsname i.v./p.o. Markteinführung Tedizolid MSD Sivextro 1x 200mg i.v. + p.o. ABSSSI (cssti) 2015
Neue Antiinfektiva 04.03.2016 Alexander Mischnik Infektiologie Universitätsklinikum Freiburg Wirkstoff Handelsname i.v./p.o. Markteinführung Tedizolid MSD Sivextro 1x 200mg i.v. + p.o. ABSSSI (cssti) 2015
Harnkulturen. Resistenzraten von E.coli (n=5830)
 Harnkulturen Harnproben gesamt: 18950 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 5830 davon ESBL bildend 368 (=6,3%) Klebsiella sp. 828 davon ESBL bildend 46 (=5,6%) Proteus mirabilis
Harnkulturen Harnproben gesamt: 18950 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 5830 davon ESBL bildend 368 (=6,3%) Klebsiella sp. 828 davon ESBL bildend 46 (=5,6%) Proteus mirabilis
8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen
 8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Amoxicillin Amoxypen j Grampositive (nicht S. aureus) und gramnegative Keime (H. influenzae ca. 10 % Resistenz) * Erwachsene, Kinder 412 Jahre
8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Amoxicillin Amoxypen j Grampositive (nicht S. aureus) und gramnegative Keime (H. influenzae ca. 10 % Resistenz) * Erwachsene, Kinder 412 Jahre
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2017 INHALT
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2017 INHALT
Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika
 Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika Fortbildungsveranstaltung Netzwerk MRE Landkreis Stendal 14.06.2017 Gramnegative Bakterien Enterobakterien* Pseudomonas aeruginosa
Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika Fortbildungsveranstaltung Netzwerk MRE Landkreis Stendal 14.06.2017 Gramnegative Bakterien Enterobakterien* Pseudomonas aeruginosa
Harnwegsinfektionen von der Hausarztpraxis bis zur Intensivstation. Professor Christian Ruef Institut für Infektiologie und Spitalhygiene
 Harnwegsinfektionen von der Hausarztpraxis bis zur Intensivstation Professor Christian Ruef Institut für Infektiologie und Spitalhygiene 1 Themen Fallbeispiel Epidemiologie der Antibiotikaresistenz - International
Harnwegsinfektionen von der Hausarztpraxis bis zur Intensivstation Professor Christian Ruef Institut für Infektiologie und Spitalhygiene 1 Themen Fallbeispiel Epidemiologie der Antibiotikaresistenz - International
Klebsiella pneumoniae
 Enterobakterien E. coli Klebsiella spp., Klebsiella pneumoniae Enterobacter spp. (Serratia spp., Citrobacter spp., Proteus spp., Morganella morganii) Enterobakterien allgemein Natürliche Darmflora von
Enterobakterien E. coli Klebsiella spp., Klebsiella pneumoniae Enterobacter spp. (Serratia spp., Citrobacter spp., Proteus spp., Morganella morganii) Enterobakterien allgemein Natürliche Darmflora von
Evidenzbasierte Antibiotikatherapie
 Evidenzbasierte Antibiotikatherapie EbM-Guidelines für Allgemeinmedizin 2014 Artikel ID: ebd00023 (001.016) 2011 Duodecim Medical Publications Ltd Tonsillitis (Streptokokken) 1. Penicillin V (nicht verfügbar)
Evidenzbasierte Antibiotikatherapie EbM-Guidelines für Allgemeinmedizin 2014 Artikel ID: ebd00023 (001.016) 2011 Duodecim Medical Publications Ltd Tonsillitis (Streptokokken) 1. Penicillin V (nicht verfügbar)
Harnkulturen. Resistenzraten von E.coli (n=6252)
 Harnkulturen Harnproben gesamt: 20628 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 6252 davon ESBL bildend 422 (=6,7%) Klebsiella sp. 929 davon ESBL bildend 44 (=4,7%) Proteus mirabilis
Harnkulturen Harnproben gesamt: 20628 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 6252 davon ESBL bildend 422 (=6,7%) Klebsiella sp. 929 davon ESBL bildend 44 (=4,7%) Proteus mirabilis
Klassifizierung multiresistenter Keime. Dr. Ingrid Heller Sektion für Hygiene und Medizinische Mikrobiologie Hygieneteam LKI
 Klassifizierung multiresistenter Keime Dr. Ingrid Heller Sektion für Hygiene und Medizinische Mikrobiologie Hygieneteam LKI Definition Multiresistenz Mycobacteriumtuberculosis: MDR: Resistenz gegen INH
Klassifizierung multiresistenter Keime Dr. Ingrid Heller Sektion für Hygiene und Medizinische Mikrobiologie Hygieneteam LKI Definition Multiresistenz Mycobacteriumtuberculosis: MDR: Resistenz gegen INH
Aktuelles zum Thema Antibiotika
 Erreger der ESCAPE-Gruppe Die Ausbreitung von Infektionen durch multiresistente Erreger schreitet rasant voran. Aktuelles zum Thema Antibiotika Dr. Kathrin Marx E = Enterokokken, Vancomycin-resistent (VRE)
Erreger der ESCAPE-Gruppe Die Ausbreitung von Infektionen durch multiresistente Erreger schreitet rasant voran. Aktuelles zum Thema Antibiotika Dr. Kathrin Marx E = Enterokokken, Vancomycin-resistent (VRE)
ANTIBIOGRAMME - Interpretationshilfe -
 Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik ANTIBIOGRAMME - Interpretationshilfe - Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik
Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik ANTIBIOGRAMME - Interpretationshilfe - Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik
Zwischenbericht zur ESPED Studie. Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern
 Zwischenbericht zur ESPED Studie Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern Einleitung: Bei Routineabstrichen werden gelegentlich multiresistente bakterielle Infektionserreger
Zwischenbericht zur ESPED Studie Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern Einleitung: Bei Routineabstrichen werden gelegentlich multiresistente bakterielle Infektionserreger
Nationales Referenzzentrum für gramnegative Krankenhauserreger. MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke
 Nationales Referenzzentrum für gramnegative Krankenhauserreger MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke Was sind die Konsequenzen von Resistenz? Antibiotika gegen E. coli Ampicillin/Amoxicillin
Nationales Referenzzentrum für gramnegative Krankenhauserreger MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke Was sind die Konsequenzen von Resistenz? Antibiotika gegen E. coli Ampicillin/Amoxicillin
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger. Prof. Dr. C. Wendt
 ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
Bedeutung, Behandlung, Prophylaxe
 ESBL und andere mulitresistente gramnegative Keime Bedeutung, Behandlung, Prophylaxe Dr. Martin Kaase NRZ für gramnegative Krankenhauserreger Ruhr-Universität Bochum martin.kaase@rub.de E. coli Wildtyp
ESBL und andere mulitresistente gramnegative Keime Bedeutung, Behandlung, Prophylaxe Dr. Martin Kaase NRZ für gramnegative Krankenhauserreger Ruhr-Universität Bochum martin.kaase@rub.de E. coli Wildtyp
Prävention der Ausbreitung von multiresistenten gramnegativen
 Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Prävention der Ausbreitung von multiresistenten gramnegativen Erregern (MRGNE) Internetversion ohne Photos
Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Prävention der Ausbreitung von multiresistenten gramnegativen Erregern (MRGNE) Internetversion ohne Photos
Multiresistente Erreger. Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen?
 Hygiene in der Arztpraxis 3MRGN/4MRGN was ist das nun wieder?? 17.04.2013 Multiresistente Erreger Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen? Multiresistente Erreger Welche sollen
Hygiene in der Arztpraxis 3MRGN/4MRGN was ist das nun wieder?? 17.04.2013 Multiresistente Erreger Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen? Multiresistente Erreger Welche sollen
Antibiotikaresistenz und -einsatz in der Humanmedizin
 Europäischer Antibiotikatag Interdisziplinäres Symposium: Antibiotikaeinsatz - Wie wenig ist (noch) zu viel? 9. November 212, BVL, Berlin Antibiotikaresistenz und -einsatz in der Humanmedizin Michael Kresken
Europäischer Antibiotikatag Interdisziplinäres Symposium: Antibiotikaeinsatz - Wie wenig ist (noch) zu viel? 9. November 212, BVL, Berlin Antibiotikaresistenz und -einsatz in der Humanmedizin Michael Kresken
Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik
 Workshop Wundzentrum Hamburg 20. August 2010 Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik Dr. J. Ungeheuer Tel.: 040-76696-103 www.labor-froreich.de
Workshop Wundzentrum Hamburg 20. August 2010 Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik Dr. J. Ungeheuer Tel.: 040-76696-103 www.labor-froreich.de
Harnkulturen. Resistenzraten von E.coli (n=4543)
 Harnkulturen Harnproben gesamt: 17963 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 4543 davon ESBL bildend 283 (=6,2%) Klebsiella sp. 653 davon ESBL bildend 29 (=4,4%) Proteus mirabilis
Harnkulturen Harnproben gesamt: 17963 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 4543 davon ESBL bildend 283 (=6,2%) Klebsiella sp. 653 davon ESBL bildend 29 (=4,4%) Proteus mirabilis
Highlights der PEG- Resistenzstudie 2007
 Jahrestagung der PEG Sektion Grundlagen Bonn, 1. Oktober 28 Highlights der PEG- Resistenzstudie 27 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation,
Jahrestagung der PEG Sektion Grundlagen Bonn, 1. Oktober 28 Highlights der PEG- Resistenzstudie 27 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation,
Modul 3: Rationale Antibiotikatherapie bei Infektionen der unteren Atemwege
 Online-Fragebogen zur Fortbildung Modul 3: Rationale Antibiotikatherapie bei Infektionen der unteren Atemwege Bitte bearbeiten Sie die folgenden Multiple-Choice-Fragen. Beachten Sie, dass pro Frage nur
Online-Fragebogen zur Fortbildung Modul 3: Rationale Antibiotikatherapie bei Infektionen der unteren Atemwege Bitte bearbeiten Sie die folgenden Multiple-Choice-Fragen. Beachten Sie, dass pro Frage nur
Gute Antibiotikaregime
 Gute Antibiotikaregime 8. Hygiene Forum Bonn 08. September 2011 Peter Walger, Medizinische Klinik III, Universität Bonn International Study of the Prevalence and Outcomes of Infection in ICU's (EPIC II)
Gute Antibiotikaregime 8. Hygiene Forum Bonn 08. September 2011 Peter Walger, Medizinische Klinik III, Universität Bonn International Study of the Prevalence and Outcomes of Infection in ICU's (EPIC II)
Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de /
 Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de / mikro@labmed.de) seit April 2003 Akkreditierung (aktuell DIN EN ISO 15189; DACH) 1 1. Problematik multiresistenter
Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de / mikro@labmed.de) seit April 2003 Akkreditierung (aktuell DIN EN ISO 15189; DACH) 1 1. Problematik multiresistenter
Der Harnwegsinfekt - Therapie -
 Der Harnwegsinfekt - Therapie - Harnwegsinfektion Verhältnis Frauen/Männer Mindestens 50 % der Frauen entwickeln wenigstens einmal einen Harnwegsinfekt Seit 8 Monaten immer wieder Harnwegsinfekte 29 jährige
Der Harnwegsinfekt - Therapie - Harnwegsinfektion Verhältnis Frauen/Männer Mindestens 50 % der Frauen entwickeln wenigstens einmal einen Harnwegsinfekt Seit 8 Monaten immer wieder Harnwegsinfekte 29 jährige
Antibiotikaverbrauch im ambulanten Versorgungsbereich. Königswinter, / 1
 Antibiotikaverbrauch im ambulanten Versorgungsbereich Königswinter, 14.4.14 / 1 Verordnungsdichte im ambulanten Bereich, 2006-2011 (in DDD pro 1.000 Versicherte und Tag) Königswinter, 14.4.14 / 2 Antibiotika-Verordnungsdichten
Antibiotikaverbrauch im ambulanten Versorgungsbereich Königswinter, 14.4.14 / 1 Verordnungsdichte im ambulanten Bereich, 2006-2011 (in DDD pro 1.000 Versicherte und Tag) Königswinter, 14.4.14 / 2 Antibiotika-Verordnungsdichten
Antibiotika in der Praxis mit Hygieneratschlägen
 Antibiotika in der Praxis mit Hygieneratschlägen Bearbeitet von Uwe Frank, Franz Daschner 9., vollst. überarb. Aufl. 2010. Taschenbuch. XII, 201 S. Paperback ISBN 978 3 642 10459 6 Weitere Fachgebiete
Antibiotika in der Praxis mit Hygieneratschlägen Bearbeitet von Uwe Frank, Franz Daschner 9., vollst. überarb. Aufl. 2010. Taschenbuch. XII, 201 S. Paperback ISBN 978 3 642 10459 6 Weitere Fachgebiete
Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor. Dr. med. Arno Köster
 Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor Dr. med. Arno Köster Definition Multiresistenz (MRE) ICD-10-GM Version 2010 U81! Bakterien mit Multiresistenz gegen
Umgang mit multiresistenten Erregern (MRE) aus der Sicht des Mikrobiologischen Labor Dr. med. Arno Köster Definition Multiresistenz (MRE) ICD-10-GM Version 2010 U81! Bakterien mit Multiresistenz gegen
Zu unterscheiden ist zwischen Sepsis, schwerer Sepsis und septischem Schock.
 Sepsis in Deutschland Aktueller Stand und Perspektiven in Diagnose, Epidemiologie und Therapie der Sepsis Von Professor Dr. Michael Quintel München München (3. Mai 2007) - Der Verdacht auf eine Sepsis
Sepsis in Deutschland Aktueller Stand und Perspektiven in Diagnose, Epidemiologie und Therapie der Sepsis Von Professor Dr. Michael Quintel München München (3. Mai 2007) - Der Verdacht auf eine Sepsis
Kurstag 5. -Infektionen mit gramnegativen Erregern. -Therapie. -Auswertung der letzten Stunde. -Differenzierung gramnegativer Erreger
 Kurstag 5 -Infektionen mit gramnegativen Erregern -Therapie -Auswertung der letzten Stunde -Differenzierung gramnegativer Erreger Antibiotika-Seminar Freitag: Vorbesprechung Praktischer Teil Dienstag:
Kurstag 5 -Infektionen mit gramnegativen Erregern -Therapie -Auswertung der letzten Stunde -Differenzierung gramnegativer Erreger Antibiotika-Seminar Freitag: Vorbesprechung Praktischer Teil Dienstag:
Mathias W. Pletz Zentrum für Infektionsmedizin und Krankenhaushygiene
 Multiresistente Erreger Mathias W. Pletz Zentrum für Infektionsmedizin und Krankenhaushygiene Inhalte 1. Wo liegt das Problem? 2. MRSA 3. 3 und 4 MRGN Infektionsmedizin im 15. Jahrhundert im 21. Jahrhundert?
Multiresistente Erreger Mathias W. Pletz Zentrum für Infektionsmedizin und Krankenhaushygiene Inhalte 1. Wo liegt das Problem? 2. MRSA 3. 3 und 4 MRGN Infektionsmedizin im 15. Jahrhundert im 21. Jahrhundert?
Was sind MRGN? Mikrobiologie und Meldepflicht
 Was sind MRGN? Mikrobiologie und Meldepflicht Fortbildungsveranstaltung der LIgA, 29. Januar / 05. Februar 2014 Dr. med. Tilo Hackel Landesuntersuchungsanstalt Dresden, Fachgebiet Bakteriologie, Mykologie,
Was sind MRGN? Mikrobiologie und Meldepflicht Fortbildungsveranstaltung der LIgA, 29. Januar / 05. Februar 2014 Dr. med. Tilo Hackel Landesuntersuchungsanstalt Dresden, Fachgebiet Bakteriologie, Mykologie,
Inhalte 40 Std. 1 1 Antiinfektiva Grundlagen und Klassen IIK. 2 Antiinfektiva Pharmakokinetik und -dynamik IIK/ABS
 Curriculum Antibiotic Stewardship (ABS) Rationale Antiinfektivastrategien im Krankenhaus Modul 1 Grundkurs zum ABS-beauftragten Arzt Versionsdatum 16. Februar 2016 Inhalte 40 Std. 1 1 Antiinfektiva Grundlagen
Curriculum Antibiotic Stewardship (ABS) Rationale Antiinfektivastrategien im Krankenhaus Modul 1 Grundkurs zum ABS-beauftragten Arzt Versionsdatum 16. Februar 2016 Inhalte 40 Std. 1 1 Antiinfektiva Grundlagen
Resistenzsituation im Krankenhausbereich -
 2. estagung der PEG Antibiotikaverbrauch und Resistenz Wo steht Deutschland Resistenzsituation im Krankenhausbereich - Datenquellen, Entwicklung und aktuelle Situation Michael Kresken Antiinfectives Intelligence
2. estagung der PEG Antibiotikaverbrauch und Resistenz Wo steht Deutschland Resistenzsituation im Krankenhausbereich - Datenquellen, Entwicklung und aktuelle Situation Michael Kresken Antiinfectives Intelligence
LA GRANDE BOUFFE. Wie lange, soll was, womit behandelt werden? Katia Boggian Leitende Ärztin Infektiologie/Spitalhygiene
 LA GRANDE BOUFFE Wie lange, soll was, womit behandelt werden? Katia Boggian Leitende Ärztin Infektiologie/Spitalhygiene Das grosse Buffet: Was gibt s denn Gutes? Womit fangen wir an? Was kleckert mich
LA GRANDE BOUFFE Wie lange, soll was, womit behandelt werden? Katia Boggian Leitende Ärztin Infektiologie/Spitalhygiene Das grosse Buffet: Was gibt s denn Gutes? Womit fangen wir an? Was kleckert mich
ZEITSCHRIFT FÜR. Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 28. Jahrgang
 WWW.ZCT-BERLIN.DE ZEITSCHRIFT FÜR Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 28. Jahrgang Register 2007 A ACE-Hemmer Acinetobacter baumannii - Carbapenem-Resistenz 47 - Tigecyclin-Resistenz
WWW.ZCT-BERLIN.DE ZEITSCHRIFT FÜR Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 28. Jahrgang Register 2007 A ACE-Hemmer Acinetobacter baumannii - Carbapenem-Resistenz 47 - Tigecyclin-Resistenz
Thrombozytenaggregationshemmer. Allergie Antikoagulanzien, Gonokokken/Anaerobier
 08 Kapitel Infektiologie.3 Tabellarische Übersicht der wichtigsten in der Urologie verwendeten Antibiotika W. Vahlensieck Penicilline Benzylpenicilline Allergie Antikoagulanzien, Thrombozytenaggregationshemmer
08 Kapitel Infektiologie.3 Tabellarische Übersicht der wichtigsten in der Urologie verwendeten Antibiotika W. Vahlensieck Penicilline Benzylpenicilline Allergie Antikoagulanzien, Thrombozytenaggregationshemmer
Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie Außenstelle Großhadern. Béatrice Grabein
 Antibiotika als Tranquilizer und Antipyretika Der sinnvolle Einsatz von Antibiotika bei Knochen-, Gelenk- und Weichteilinfektionen Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und
Antibiotika als Tranquilizer und Antipyretika Der sinnvolle Einsatz von Antibiotika bei Knochen-, Gelenk- und Weichteilinfektionen Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und
Hygiene in der Arztpraxis
 Hygiene in der Arztpraxis 3MRGN/4MRGN Gefahr durch multiresistente Erreger? 22.04.2015 Multiresistente Erreger Welche sollen es denn diesmal sein? MRGN = Multiresistente Gramnegative Stäbchen Stäbchen?
Hygiene in der Arztpraxis 3MRGN/4MRGN Gefahr durch multiresistente Erreger? 22.04.2015 Multiresistente Erreger Welche sollen es denn diesmal sein? MRGN = Multiresistente Gramnegative Stäbchen Stäbchen?
Antibiotikaresistenz bei gramnegativen Bakterien
 Antibiotikaresistenz bei gramnegativen Bakterien - Fokus Carbapenemresistenz - Fachtagung multiresistente Erreger September 2012 Tilo Hackel LUA Dresden Antibiotikaresistenz ist die Folge von Antibiotikagebrauch.
Antibiotikaresistenz bei gramnegativen Bakterien - Fokus Carbapenemresistenz - Fachtagung multiresistente Erreger September 2012 Tilo Hackel LUA Dresden Antibiotikaresistenz ist die Folge von Antibiotikagebrauch.
Antibiotika: Wie bleibe ich am besten schlank?
 GESUNDHEIT Infekttag, 22. Februar 2018 Antibiotika: Wie bleibe ich am besten schlank? Ambulant-erworbene Pneumonie und unkomplizierte Harnwegsinfekte Philipp Kohler Parsimonitäts-Prinzip (Sparsamkeitsprinzip)
GESUNDHEIT Infekttag, 22. Februar 2018 Antibiotika: Wie bleibe ich am besten schlank? Ambulant-erworbene Pneumonie und unkomplizierte Harnwegsinfekte Philipp Kohler Parsimonitäts-Prinzip (Sparsamkeitsprinzip)
DIE NEUE PEG-LEITLINIE PARENTERALE ANTIBIOTIKA
 CAMPUS GROSSHADERN CAMPUS INNENSTADT DIE NEUE PEG-LEITLINIE PARENTERALE ANTIBIOTIKA Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene S2K-LEITLINIE KALKULIERTE PARENTERALE
CAMPUS GROSSHADERN CAMPUS INNENSTADT DIE NEUE PEG-LEITLINIE PARENTERALE ANTIBIOTIKA Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene S2K-LEITLINIE KALKULIERTE PARENTERALE
MVZ Dr. Eberhard & Partner Dortmund - 1
 Überblick MRSA-Netzwerktreffen Kreis Multiresistente Erreger und Antibiotika Dr. med. Arthur Pranada Facharzt für Mikrobiologie, Virologie und Infektionsepidemiologie Antibiotic Stewardship (ABS-)Experte
Überblick MRSA-Netzwerktreffen Kreis Multiresistente Erreger und Antibiotika Dr. med. Arthur Pranada Facharzt für Mikrobiologie, Virologie und Infektionsepidemiologie Antibiotic Stewardship (ABS-)Experte
Selektives Antibiogramm in Regensburg
 8. November 0 Selektives Antibiogramm in egensburg Dr. med. Verena Greifenberg Dr. med. Thomas Holzmann Institut für klinische Mikrobiologie und Hygiene egensburg Selektives Antibiogramm: was ist das?
8. November 0 Selektives Antibiogramm in egensburg Dr. med. Verena Greifenberg Dr. med. Thomas Holzmann Institut für klinische Mikrobiologie und Hygiene egensburg Selektives Antibiogramm: was ist das?
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA RESISTENZBERICHT 2016 INHALT Resistenzstatistik 2016....3 Einleitung....3
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA RESISTENZBERICHT 2016 INHALT Resistenzstatistik 2016....3 Einleitung....3
Orale Antibiotika in Klinik und Praxis
 Orale Antibiotika in Klinik und Praxis Praxisorientierte Empfehlungen zur Antibiotika-Therapie leichter bis mittelschwerer bakterieller Infektionen bei Erwachsenen im ambulanten und stationären Bereich
Orale Antibiotika in Klinik und Praxis Praxisorientierte Empfehlungen zur Antibiotika-Therapie leichter bis mittelschwerer bakterieller Infektionen bei Erwachsenen im ambulanten und stationären Bereich
3. Hygienetag Köln 31. Oktober 2012 Multiresistenzen bei Erregern im Krankenhaus und in Lebensmitteln
 3. Hygienetag Köln 31. Oktober 2012 Multiresistenzen bei Erregern im Krankenhaus und in Lebensmitteln Multiresistente Erreger (MRE) bei Kindern Michael Weiß, Reinhold Cremer, Frauke Mattner Klinik für
3. Hygienetag Köln 31. Oktober 2012 Multiresistenzen bei Erregern im Krankenhaus und in Lebensmitteln Multiresistente Erreger (MRE) bei Kindern Michael Weiß, Reinhold Cremer, Frauke Mattner Klinik für
Antibiotkatherapie in der Intensivmedizin.qxd :39 Sei
 V Vorwort Die Diagnostik und die Therapie von Infektionen in der Intensivmedizin stellen nach wie vor eine besondere Herausforderung dar. Die frühzeitige und adäquate Therapie ist für das Überleben kritisch
V Vorwort Die Diagnostik und die Therapie von Infektionen in der Intensivmedizin stellen nach wie vor eine besondere Herausforderung dar. Die frühzeitige und adäquate Therapie ist für das Überleben kritisch
ENDOKARDITIS-PROPHYLAXE FÜR ERWACHSENE
 ENDOKARDITIS-PROPHYLAXE FÜR ERWACHSENE Sie benötigen gemäss den geltenden Empfehlungen eine vorbeugende Behandlung gegen eine bakterielle Endokarditis. Vorname Name Geburtsdatum Herzfehler Penicillin-Allergie
ENDOKARDITIS-PROPHYLAXE FÜR ERWACHSENE Sie benötigen gemäss den geltenden Empfehlungen eine vorbeugende Behandlung gegen eine bakterielle Endokarditis. Vorname Name Geburtsdatum Herzfehler Penicillin-Allergie
Die neue PEG Leitlinie Update Wichtige Highlights
 Die neue PEG Leitlinie Update 2018 - Wichtige Highlights 15. Hygiene Forum Bonn Institut für Hygiene und Öffentliche Gesundheit des UKB in Zusammenarbeit mit dem VDH (NRW) 20. September 2018, 9:20 9:55
Die neue PEG Leitlinie Update 2018 - Wichtige Highlights 15. Hygiene Forum Bonn Institut für Hygiene und Öffentliche Gesundheit des UKB in Zusammenarbeit mit dem VDH (NRW) 20. September 2018, 9:20 9:55
Neue Wege zur Reduktion der Antibiotikaverordnung bei Atemwegsinfektionen.
 Neue Wege zur Reduktion der Antibiotikaverordnung bei Atemwegsinfektionen. Epidemiologie der antimikrobiellen Resistenzen in Deutschland und Europa Miriam Wiese-Posselt Institut für Hygiene und Umweltmedizin
Neue Wege zur Reduktion der Antibiotikaverordnung bei Atemwegsinfektionen. Epidemiologie der antimikrobiellen Resistenzen in Deutschland und Europa Miriam Wiese-Posselt Institut für Hygiene und Umweltmedizin
Antibiotikaresistenz Wie ernst ist die Lage?
 Antibiotikaresistenz Wie ernst ist die Lage? Dr med Olivier Dubuis, Viollier AG Antibiotikum Einführung Resistenzentwicklung Viollier AG 4123 Allschwil 09.08.2016 / 1 Staphylococcus aureus Trägerrate 20-40%
Antibiotikaresistenz Wie ernst ist die Lage? Dr med Olivier Dubuis, Viollier AG Antibiotikum Einführung Resistenzentwicklung Viollier AG 4123 Allschwil 09.08.2016 / 1 Staphylococcus aureus Trägerrate 20-40%
Universitätsklinikum Jena Zentrale Notfallaufnahme
 Seite 1 von 5 1. Fakten Zu Beginn: Sollte der Patient an die Urologie angebunden werden, bitte vor Antibiotikagabe wegen laufender Studien Kontakt mit der Urologie aufnehmen. Wenn dies medizinisch nicht
Seite 1 von 5 1. Fakten Zu Beginn: Sollte der Patient an die Urologie angebunden werden, bitte vor Antibiotikagabe wegen laufender Studien Kontakt mit der Urologie aufnehmen. Wenn dies medizinisch nicht
