Einsatz der IR-Spektroskopie bei der Prozessverfolgung von Hefe-Fermentationen sowie bei der Qualitätskontrolle von Getränken, Obst und Hefen
|
|
|
- Gerburg Katja Dressler
- vor 8 Jahren
- Abrufe
Transkript
1 Einsatz der IR-Spektroskopie bei der Prozessverfolgung von Hefe-Fermentationen sowie bei der Qualitätskontrolle von Getränken, Obst und Hefen von Master of Science (M.Sc.) Dominik Egly von der Fakultät III Prozesswissenschaften der Technischen Universität Berlin zur Erlangung des akademischen Grades Doktor der Ingenieurwissenschaften Dr.-Ing. genehmigte Dissertation Promotionsausschuss: Vorsitzender: Prof. Dr. Peter Neubauer (TU Berlin) Gutachter: Prof. Dr.-Ing. Frank-Jürgen Methner (TU Berlin) Gutachter: Prof. Dr. Thomas Beuermann (HS Mannheim) Tag der wissenschaftlichen Aussprache: 18. April 2012 Berlin 2012 D 83
2 Einsatz der IR-Spektroskopie bei der Prozessverfolgung von Hefe-Fermentationen sowie bei der Qualitätskontrolle von Getränken, Obst und Hefen von Master of Science (M.Sc.) Dominik Egly von der Fakultät III Prozesswissenschaften der Technischen Universität Berlin zur Erlangung des akademischen Grades Doktor der Ingenieurwissenschaften Dr.-Ing. genehmigte Dissertation Promotionsausschuss: Vorsitzender: Prof. Dr. Peter Neubauer (TU Berlin) Gutachter: Prof. Dr.-Ing. Frank-Jürgen Methner (TU Berlin) Gutachter: Prof. Dr. Thomas Beuermann (HS Mannheim) Tag der wissenschaftlichen Aussprache: 18. April 2012 Berlin 2012 D 83
3 Inhaltsübersicht I Inhaltsübersicht Inhaltsübersicht... I Vorwort und Danksagung... II Veröffentlichungen im Rahmen der Dissertation... III Abkürzungsverzeichnis... IV Inhaltsverzeichnis... VII 1 Zusammenfassung Einleitung und Ziele Stand des Wissens Material und Methoden Ergebnisse Diskussion Literatur- und Quellenverzeichnis Anhang
4 Vorwort und Danksagung II Vorwort und Danksagung Die Ergebnisse, welche in dieser Arbeit vorgestellt werden, sind in Kooperation mit der TU Berlin, Fachgebiet Brauwesen des Instituts für Biotechnologie der Fakultät Prozesswissenschaften und mit der Hochschule Mannheim, Institut für Prozessmesstechnik und innovative Energiesysteme im Rahmen eines von der Karl-Völker-Stiftung an der Hochschule Mannheim geförderten Forschungsprojektes (Projektleiter: Prof. Dr. Thomas Beuermann) erzielt worden. Allen, die mich während meiner Dissertation unterstützt haben, sei an dieser Stelle recht herzlich gedankt. Mein besonderer Dank gilt Herrn Prof. Dr. Thomas Beuermann und Herrn Prof. Dr.-Ing. Frank-Jürgen Methner für die hervorragende Betreuung und die Bereitstellung aller dafür benötigten Mittel. Als Ideengeber und durch deren kritische Anmerkungen haben beide maßgeblich zum Gelingen dieser Arbeit beigetragen. Weiterhin bedanken möchte ich mich bei Frau Kerris Isolde Klug, Herrn Daniel Geörg, Herrn Denis Kiawi und Frau Cyriane Meguo-Nwabo, meine unmittelbaren Arbeitskollegen, die mich mit vollem Engagement unterstützten haben. Vielen Dank auch an Herrn Christian Müller, Frau Claudia Lehmann, Frau Dayana Domingos und Herrn Solomon Kalu für deren tatkräftige Unterstützung. Ferner gilt mein Dank den Mitarbeitern des Instituts für Prozessmesstechnik und innovative Energiesysteme der Hochschule Mannheim für die gute Arbeitsatmosphäre und große Hilfsbereitschaft. Hervorheben möchte ich den Institutsleiter Herrn Prof. Dr. Matthias Rädle. Ihm danke ich für die zusätzliche Unterstützung und die Bereitstellung der für diese Arbeit notwendigen Materialen. Darüber hinaus danke ich den Mitarbeitern der Versuchsanstalt der Hefeindustrie, besonders Herrn Dr.-Ing. Michael Quantz und Herrn Claus Decker, für ihre freundliche Unterstützung und Beratung bei der Qualitätskontrolle von Hefen. Ebenfalls möchte ich mich bei den Mitarbeitern des Instituts für Mikrobiologie der Hochschule Mannheim für ihre wertvollen Ratschläge und großzügige Hilfsbereitschaft bedanken. Außerdem bedanke ich mich bei der Albert- und Anneliese- Konanz-Stiftung für das einjährige Stipendium, welches für mich finanziell eine große Hilfe darstellte. Abschließend gilt mein besonderer Dank meinen Freunden und meiner lieben Familie, insbesondere meiner Mutter, die mich sowohl mental als auch finanziell unterstützt hat. Wer kämpft, kann verlieren. Wer nicht kämpft, hat schon verloren. (Bertolt Brecht)
5 Veröffentlichungen im Rahmen der Dissertation III Veröffentlichungen im Rahmen der Dissertation Ergebnisse dieser Arbeit wurden in folgenden Tagungsbeiträgen und Journals veröffentlicht: 1. Klug K. I., Egly D., Geörg D. und Beuermann T. (2009). Poster: On-line Bioprocess Monitoring using Optical Sensors. 22. VH-Hefetagung, Berlin, April Egly D. und Beuermann T. (2010). MIR-ATR-Spectroscopy in combination with multivariate methods for fermentation control and determination of intracellular yeast constituents. 23. VH-Hefetagung, Wien, April Egly D., Geörg D., Klug K. I. und Beuermann T. (2010). Poster: On-line Carbon Balance Using Optical Sensors. 23. VH-Hefetagung, Wien, April Egly D. (2010). MIR-ATR-Spektroskopie für die Hefefermentationskontrolle und Getränkeanalyse. Bruker Optics GmbH, Anwendertreffen 2010, Ettlingen, November Beuermann T., Egly D., Geoerg D., Klug K. I., Storhas W., Methner F.-J. (2012). Online carbon balance of yeast fermentations using miniaturized optical sensors, Journal of Bioscience and Bioengineering 113 pp
6 Abkürzungsverzeichnis IV Abkürzungsverzeichnis ATR A BTM E Abgeschwächte-Totalreflexion Absorption Biotrockenmasse Energie C BTM Konzentration der Biotrockenmasse (g / L) C CO 2 CO 2 -Konzentration in der Gasphase (Vol.-%) C, Ethanolkonzentration in der Flüssigphase (g / L) EtOH f C, Ethanolkonzentration in der Gasphase (Vol.-%) EtOH g C Sac Saccharosekonzentration (g / L) C O 2 Sauerstoffkonzentration im Fermentationsabgas (Vol.-%) C-Quelle FT-IRS FT-MIR FT-MIR-ATR GC Gew.-% HPLC HTS IR λ LED M c Kohlenstoffquelle Fourier-Transformations-Infrarot-Spektroskopie Fouriertransformation-Mittel-Infrarot Fouriertransformation-Mittel-Infrarot-abgeschwächte-Totalreflexion Gaschromatographie Gewichtsprozent High Performance Liquid Chromatography Hefetrockensubstanz Infrarot Wellenlänge Leuchtdiode Molekulargewicht von Kohlenstoff (g / mol) M EtOH Molekulargewicht von Ethanol (g / mol) M Sac Molekulargewicht von Saccharose (g / mol) MIR c BTM Mittleres Infrarot n, Molzahl an Kohlenstoff in Form von produzierter Biotrockenmasse (mol) n c,co 2 Molzahl an Kohlenstoff in Form von produzierten CO 2 (mol) n c EtOH, f, Molzahl an Kohlenstoff in Form von produziertem Ethanol in der Flüssigphase (mol)
7 Abkürzungsverzeichnis V n c EtOH, g c Sac, Molzahl an Kohlenstoff in Form von produziertem Ethanol in der Gasphase (mol) n, Molzahl an Kohlenstoff in Form von ursprünglich eingesetzter Kohlenstoffquelle Saccharose (mol) n CO 2 Molzahl an CO 2 in der Gasphase (mol) n, Molzahl an Ethanol in der Flüssigphase (mol) EtOH f n, Molzahl an Ethanol in der Gasphase (mol) EtOH g n Sac Molzahl an Saccharose (mol) NIR NDIR p PCA PLS R R 2 RMSECV RMSEP rpm T T t UV Nahes Infrarot Nicht-dispersives Infrarot Atmosphärendruck (Pa) Principle Component Analysis Partial Least Squares Regression Ideale Gaskonstante (8,314 J / (mol K)) Bestimmtheitsmaß Root Mean Square Error of Cross Validation Root Mean Square Error of Prediction rounds per minute Temperatur des Fermentationsabgases (K) Transmission Zeit (h, min, sek) ultraviolett ν Frequenz (s -1 ) ν ~ Wellenzahl (cm -1 ) V & A V & B Abgasstrom (L / min) Begasungsrate (L / min) V CO 2 kumuliertes Volumen an produziertem CO 2 (L) V F V m VE-Wasser VIS vvm Vol.-% Fermentationsvolumen (L) Molvolumen (L / mol) vollentsalztes Wasser sichtbarer Bereich des Lichtes gas volume flow per unit of liquid volume per minute Volumenprozent
8 Abkürzungsverzeichnis VI x~ ij mittelwertzentrierte Variable der Datenmatrix X in der i-ten Spalte und c BTM j-ten Zeile x, Molarer Anteil an ursprünglich eingesetztem Kohlenstoff, welcher in Biotrockenmasse umgewandelt wurde (-) x c,co 2 Molarer Anteil an ursprünglich eingesetztem Kohlenstoff, welcher in x c EtOH, f Kohlendioxid umgewandelt wurde (-), Molarer Anteil an ursprünglich eingesetztem Kohlenstoff, welcher in x c EtOH, g Ethanol in der Flüssigphase umgewandelt wurde (-), Molarer Anteil an ursprünglich eingesetztem Kohlenstoff, welcher in Ethanol im Abgas umgewandelt wurde (-)
9 Inhaltsverzeichnis VII Inhaltsverzeichnis 1 Zusammenfassung Einleitung und Ziele Stand des Wissens IR-Spektroskopie Grundlagen IR-Spektrometer und Messaufbauten IR-Strahlungsquelle IR-Strahlungsempfänger (Detektor) Monochromator ATR-Messtechnik Kalibrationsmethoden in der optischen Spektroskopie Univariate und multivariate Kalibration PLS-Regression Mathematischer Hintergrund der PLS-Regression Bedeutung der PLS-Hauptkomponenten Spektrale Datenvorbereitung Subtraktion eines konstanten Offsets Subtraktion einer Geraden Vektornormierung (SNV) Minimum-Maximum-Normierung Multiplikative Streukorrektur (MSC) Erste und zweite Ableitung Validierungsmethoden Korrelationskoeffizient r und Bestimmtheitsmaß R Kreuzvalidierung Test-Set-Validierung Externe Validierung Prozessverfolgung von Hefefermentationen Stoffwechselvorgänge bei der Kultivierung von Hefen Sensorsysteme für die Bioprozessanalytik Temperatur und ph-wert Begasungsrate und Rührerdrehzahl Gelöst-Sauerstoff- und Gelöst-Kohlendioxidkonzentration Zelldichte und Biomasse Zusammensetzung der Fermentationsbrühe...35
10 Inhaltsverzeichnis VIII 3.4 Getränkeanalytik Chemische Zusammensetzung von Getränken Obst und Fruchtsäfte Softdrinks (Cola, Limonade etc.) Bier, Radler und Cola-Bier Analytische Verfahren Obst und Fruchtsäfte Bier und Bier-Mix-Getränke Hefeanalytik Chemische Zusammensetzung von Hefen Analyse von intrazellulären Hefebestandteilen Material und Methoden On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen Messtechnik am Bioreaktor Abgasanalytik Faseroptischer Rückstreumessaufbau Inokulum, Fermentationsbedingungen und Probennahme Referenzmethoden Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR-Spektroskopie MIR-ATR-Spektrometer-Aufbau Erstellung von Kalibrationsmethoden mit der OPUS Software Hintergrund- und Probenmessung Univariate Kalibrationsmodelle (Quant 1) Multivariate Kalibrationsmodelle (Quant 2) Quant 1 Analyse Quant 2 Analyse Referenzmethoden für die Analyse von Obst, Getränken und Hefen Verwendete Chemikalien Ergebnisse On-line Kohlenstoffbilanzierung von Backhefefermentationen In-line Verfolgung der Biomasse Bestimmung der Ethanolkonzentration in der flüssigen Phase On-line Verfolgung der Hefefermentation Kohlenstoffbilanzierung Analyse der Fermentationssuspension mittels MIR-ATR-Spektroskopie
11 Inhaltsverzeichnis IX Auswahl und Präparation der Kalibrationsproben Auswahl der gerätetechnischen Messparameter Sedimentation der Hefezellen während der MIR-ATR-Messungen MIR-ATR-Spektren der Fermentationsausträge und Analyten Optimale Parameter und Validierung der Kalibrationsmodelle At-line Verfolgung von Hefefermentationen Analyse von Bier, Cola-Bier, Obst und Fruchtsäften mittels MIR-ATR- Spektroskopie Auswahl der Kalibrationsproben MIR-Spektren von Fruchtsäften, Obst, Bier, Cola-Bier und deren Analyten Optimale Parameter und Validierung der Kalibrationsmodelle Analysen von Fruchtsäften, Obst, Bier und Cola-Bier Entwicklung eines photometrischen MIR-ATR-Sensors für die in-line Prozesskontrolle und Getränkeanalyse Univariate Kalibrationsmodelle basierend auf MIR-ATR-Spektren Temperaturabhängigkeit der univariaten Kalibrationsmodelle Getränkeanalyse mittels univariater Kalibrationsmodelle Technischer Entwurf des ATR-Sensors Bestimmung intrazellulärer Hefebestandteile mittels MIR-ATR-Spektroskopie Auswahl und Präparation der Kalibrationsproben MIR-ATR-Spektren von Hefen und den intrazellulären Komponenten Kalibrationsmodelle für die Analyse der intrazellulären Hefebestandteile Kalibrationsmodelle für die Bestimmung der Hefetrockensubstanz Modell mit Backhefen als Kalibrationsproben Modell mit Mischungen aus Trockenhefe und Wasser als Kalibrationsproben Diskussion On-line Kohlenstoffbilanz von Backhefe-Fermentationen Analyse der Fermentationssuspension mittels MIR-ATR-Spektroskopie MIR-ATR-Analysen von Getränken und Früchten Entwicklung eines photometrischen MIR-ATR-Sensors Intrazelluläre Hefeanalytik mittels MIR-ATR-Spektroskopie Literatur- und Quellenverzeichnis Anhang Abbildungsverzeichnis Tabellenverzeichnis
12 1 Zusammenfassung 1 1 Zusammenfassung Optische Sensoren und Spektrometer werden in den letzten Jahren für die Überwachung mikrobiologischer Prozesse immer häufiger eingesetzt, da mit diesen Techniken eine schnelle und nicht-invasive Messung von verschiedenen Analyten realisiert werden kann. Nahinfrarot- (NIR) und Mittelinfrarot- (MIR)-Spektrometer in Kombination mit multivariaten Kalibrationsmethoden wurden bereits erfolgreich für die simultane Bestimmung verschiedener Metaboliten in mikrobiologischen Prozessen verwendet. Darüber hinaus können photometrische Sensoren ebenfalls für die Überwachung von mikrobiologischen Vorgängen eingesetzt werden. Gegenüber Spektrometern besitzen photometrische Sensoren neben dem niedrigen Preis den Vorteil, dass diese kompakt und robust sind und so direkt am Bioreaktor installiert werden können. Mithilfe von zwei photometrischen IR-Gasanalysatoren wurden in dieser Arbeit der Ethanolund CO 2 -Gehalt im Abgas einer aeroben Backhefe-Fermentation sowie unter Verwendung eines faseroptischen Rückstreusensors die Hefetrockensubstanz in der Fermentationsbrühe on-line bestimmt. Der Ethanolgehalt der Fermentationsbrühe konnte durch die Messung der Ethanolkonzentration im Fermentationsabgas und die Anwendung eines Umrechnungsfaktors in Echtzeit verfolgt werden. Das Dampf- / Flüssigkeitsgleichgewicht und der damit verbundene Umrechnungsfaktor wird erheblich von dem Prozessparameter Temperatur jedoch nicht von der Begasungsrate und Rührerdrehzahl beeinflusst. Die Hefetrockensubstanz in der Fermentationssuspension konnte anhand des Rückstreusignals und der Verwendung einer linearen Kalibration in-line erfasst werden. Durch den Einsatz dieser drei optischen Sensoren war eine on-line Kohlenstoffbilanzierung mit einer Wiederfindungsrate von mehr als 90 % durchführbar. Ferner konnten mithilfe der MIR-ATR-Spektroskopie während aerober Backhefe- Fermentationen unmittelbar (innerhalb von ca. einer Minute) die Konzentrationen an Ethanol, Fructose, Glucose und Biomasse in den aus dem Bioreaktor entnommenen Fermentationsproben ermittelt werden. Es wurden sehr gute Übereinstimmungen zwischen den durch die MIR-ATR-Spektroskopie vorhergesagten Konzentrationen und der Referenzanalytik erreicht. Die mittleren Vorhersagefehler (RMSEP) und die Werte für das Bestimmtheitsmaß R 2 der externen Validierungen betrugen für Fructose 0,56 g / L (R 2 = 99,12 %), Glucose 0,42 g / L (R 2 = 99,39 %), Ethanol 0,24 g / L (R 2 = 99,42 %) und Biomasse 0,28 g / L (R 2 = 95,43 %). Die MIR-ATR-Spektroskopie in Kombination mit multivariaten Kalibrationsmethoden erwies
13 1 Zusammenfassung 2 sich als eine schnelle und einsatztaugliche Messmethode, welche für eine Prozessverfolgung von Hefe-Fermentationen geeignet ist. In dieser Arbeit wurde ebenfalls gezeigt, dass mithilfe der MIR-ATR-Spektroskopie und multivariater Analysenmethoden der Ethanol- und Dextringehalt von Bier sowie von Cola-Bier und die Zuckerkonzentrationen von Fruchtsäften, Cola und Cola-Bier bestimmt werden können. Anhand von ausgewählten mit der HPLC-Referenzmethode analysierten Bier-, Cola-Bier- und Fruchtsaftproben wurden die erstellten Kalibrationsmodelle überprüft. Die Analysenfehler der Kreuzvalidierungen lagen durchschnittlich unter 0,1 Gew.-%. Neben der spektroskopischen ist auch eine photometrische Kalibration für die quantitative Analyse von Ethanol, Dextrinen und Gesamtzucker in Getränken anhand ausgewählter MIR- Spektralbereiche möglich. Allerdings werden insbesondere die Vorhersagen der Ethanolkonzentration erheblich von der Probentemperatur beeinflusst. Neben einer Rohstoffkontrolle von flüssigen Produkten können mit der MIR-ATR-Spektroskopie auch Feststoffe wie biologisches Gewebe und Zellen analysiert werden. In dieser Arbeit wurde untersucht, ob sich die MIR-ATR-Spektroskopie dazu eignet, wichtige Zellinhaltsstoffe von Backhefen (Zucker, Proteine, Wasser) quantitativ zu bestimmen. Kalibrationsmodelle, welche anhand von wässrigen Proben mit eingewogenen Hauptbestandteilen der Hefezellen erstellt wurden, waren für die Analyse von Hefen ungeeignet. Allerdings wurde gezeigt, dass durch den Einsatz von Hefepräparaten ein Vorhersagemodell für den Wassergehalt bzw. die Hefetrockensubstanz entwickelt werden kann.
14 2 Einleitung und Ziele 3 2 Einleitung und Ziele Die Überwachung und Steuerung von Produktionsprozessen in der Biotechnologie und Lebensmittelindustrie stellen aufgrund der mikrobiologischen Komplexität eine besondere Herausforderung dar. Eine genaue und zeitnahe Prozessüberwachung ist Voraussetzung für die Produktivitätssteigerung sowie die Verbesserung von Ausbeute und Produktqualität [1]. Neben den bereits in der Biotechnologie etablierten Sensoren für die Erfassung der Prozessparameter Temperatur, ph-wert und Gelöst-Sauerstoff werden in den letzten Jahren immer häufiger optische Sensoren eingesetzt. Optische Messsysteme sind nicht-invasiv und besitzen den Vorteil, dass eine kontinuierliche Überwachung der Prozesse ohne aufwendige Probennahme durchgeführt werden kann [2, 3, 4, 5]. In biotechnologischen Prozessen werden verschiedene Zucker bzw. Zuckergemische (Glucose, Fructose, Saccharose, Maltose usw.) als C-Quellen eingesetzt, welche von den eingesetzten Mikroorganismen im Laufe der Zeit zu Biomasse, Kohlendioxid und weiteren Produkten abgebaut werden. Derzeit werden diese Parameter entweder relativ unspezifisch mittels Dichte- oder Brechungsindexmessung sowie mithilfe von selektiven enzymatischen oder anderen nasschemischen Methoden on-line verfolgt. Der bei Letzterem anfallende Verbrauch an Reagenzien ist erheblich und verursacht zusammen mit dem damit verbundenen Wartungs- bzw. Präparationsaufwand hohe Kosten. Ein weiterer Nachteil der enzymatischen Methoden ist, dass mit ihnen jeweils nur eine Zuckerspezies nachgewiesen werden kann und nicht gleichzeitig Zuckergemische analysiert werden können, wie sie bei Fermentationen und in der Getränkeindustrie vorkommen. Dagegen besitzt die in den letzten Jahren immer häufiger in den Betriebslabors und Produktionsprozessen der chemischen, pharmazeutischen und Lebensmittelindustrie eingesetzte IR-Spektroskopie das Potenzial, gleichzeitig mehrere Stoffe ohne größeren präparativen Aufwand quantitativ zu erfassen. Da eine große Bandbreite von organischen Komponenten charakteristische Absorptionsbanden im nahinfraroten und im mittelinfraroten Spektralbereich aufweisen, können mithilfe der IR-Spektroskopie gleichzeitig die Konzentrationen von mehreren verschiedenen Analyten bestimmt werden [6, 7, 8, 9, 10, 11, 12, 13]. Da die meisten Fermentationsmedien jedoch eine komplexe Zusammensetzung besitzen, zeigen die Absorptionsbanden der einzelnen Komponenten in der Fermentationsbrühe eine starke Überlappung, sodass die spektrale Interpretation sich als schwierig gestaltet. Durch den Einsatz von sogenannten multivariaten Auswertemethoden (Chemometrie) ist es nach einer auf die Problemstellung zugeschnittenen Kalibration möglich, komplexe Stoffgemische auch dann zu analysieren, wenn die IR-Absorptionsspektren der einzelnen Komponenten sich relativ unspezifisch überlagern [8],
15 2 Einleitung und Ziele 4 wie es z.b. bei den einzelnen Zuckern der Fall ist. Finn et al. konnte z.b. bei Hefefermentationen im Fed-Batch-Verfahren die Konzentrationen der Hauptkomponenten Biomasse, Ethanol, Glucose und Protein mittels NIR-Spektrometer in Kombination mit einer PLS-Regression bestimmen [14]. Im Vergleich zum MIR-Bereich, wo die optischen Lichtleiter auf wenige Meter beschränkt sind [17], besitzt die NIR-Spektroskopie den Vorteil, dass aufgrund der hohen Transmission der optischen Lichtleiter aus Quarzglas Distanzen von ca. 100 m überbrückt werden können. Hierdurch besteht die Möglichkeit, das Spektrometer und die Lichtquelle in einem geschützten Raum unterzubringen. In den letzten Jahren hat sich die NIR-Spektroskopie in Kombination mit multivariaten Kalibrationsmethoden zu einem wichtigen analytischen Verfahren in chemischen, pharmazeutischen, lebensmitteltechnischen sowie weiteren biotechnologischen Industriesparten entwickelt [15]. Dagegen hat der mittelinfrarote Spektralbereich gegenüber dem NIR den Vorteil, dass geringere Nachweisgrenzen und eine höhere Spezifität aufgrund der besser separierten Absorptionsbanden der chemischen Komponenten erreicht werden. Jedoch erfordert die hohe Absorption im MIR optische Schichtdicken von wenigen Mikrometern insbesondere bei wässrigen Proben. Im Gegensatz zu Transmissionsküvetten, bei denen es schwierig ist, solch geringe Schichtdicken zu realisieren, können mit der abgeschwächten Totalreflexion (ATR) Eindringtiefen von weniger als einer Wellenlänge erreicht werden. Mazarevica et al. verwendete z.b. ein FT-MIR-Spektrometer mit einer ATR- Messvorrichtung, um die Konzentrationen von Glucose und Ethanol während einer Backhefe-Fermentation zu verfolgen [10]. Die MIR-Spektren der Proben wurden kontinuierlich mithilfe eines automatischen Durchflusssystems (Durchfluss-ATR-Zelle) aufgenommen und mittels PLS-Regression analysiert. Dabros et al. verwendete ein FT-MIR-Spektrometer ausgestattet mit einer ATR-Diamant-Sonde für die in-line Messung der Metabolitkonzentrationen einer Hefe-Fermentation. Mit den vorhergesagten Analytkonzentrationen, der Zusammensetzung des Abgasstroms und der zugegebenen Menge an Lauge ist eine Massenbilanzierung durchgeführt worden [16]. In jener Forschungsarbeit wurde die ATR-Eintauchsonde mittels Spiegelarm mit dem FT-MIR-Spektrometer verbunden. In den letzten Jahren ist ein Trend weg von Spiegelarmen hin zu optischen MIR-Lichtleitern zu beobachten, da die Spiegelarm- Systeme einen relativ empfindlichen Aufbau besitzen [17]. MIR-Lichtleiter aus Schwermetallfluoriden, Chalkogeniden oder gemischte Silberhalide haben jedoch den Nachteil, dass sie mit der Zeit trübe werden und aufgrund der hohen Absorption dieser Materialen nur geringe Distanzen (weniger als 5 m) praktikabel sind. Aus diesem Grund muss das FT-MIR- Spektrometer nah an den Reaktor platziert und vor Spritzwasser oder anderen mechanischen Einwirkungen geschützt werden. Die Investitionskosten für ein on-line FT-MIR- Spektrometer ausgestattet mit einer ATR-Sonde liegen bei ca Euro. Aufgrund des
16 2 Einleitung und Ziele 5 großen Aufwands für die Implementierung von on-line FT-MIR-Spektrometern in einer Produktionsanlage ist der industrielle Einsatz dieser Geräte nicht weit verbreitet. Eine Alternative zu den teuren ATR-Sonden sind Durchfluss-ATR-Zellen, bei welchen mittels einer Pumpe und Schläuchen die Fermentationsbrühe aus dem Reaktor auf die ATR-Messvorrichtung gefördert wird. Neben dem günstigeren Preis bieten Durchfluss-ATR-Zellen gegenüber ATR- Sonden den Vorteil, dass längere Distanzen zwischen Gerät und Messort überbrückt werden können. Ein Nachteil insbesondere für die Mikrobiologie ist jedoch, dass durch die langen Wege vom Reaktor zur ATR-Zelle sich die Zusammensetzungen der biologischen Proben aufgrund von Stoffwechselvorgängen ändern können. Anstatt mikrobiologische Prozesse mit Spektrometern zu verfolgen, kann dies auch durch den Einsatz von photometrischen Sensoren erfolgen. Photometrische Sensoren besitzen optische Bandpassfilter in Spektralbereichen, die spezifisch für die jeweiligen zu analysierenden Komponenten sind. Vorteile von Photometern im Vergleich zu Spektrometern sind der niedrigere Preis (1.000 bis Euro je nach Sensor) sowie die Kompaktheit und der robuste Betrieb. Für eine on-line Überwachung von mikrobiologischen Prozessen können diese Sensoren ohne technische Schwierigkeiten an den Bioreaktoren angebracht werden. Ein Ziel dieser Promotion ist die Realisierung einer on-line Kohlenstoffbilanzierung von aeroben Backhefe-Fermentationen mithilfe von drei optischen Sensoren. Durch den Einsatz von zwei photometrischen IR-Sensoren werden die Konzentrationen von CO 2 und Ethanol im Fermentationsabgas on-line verfolgt. Über eine photometrische Rückstreumessung wird der Zuwachs an Biomasse während der Fermentation gemessen. Um von der in der Gasphase gemessenen Ethanolkonzentration auf den Ethanolgehalt in der Flüssigphase zu schließen, ist ein entsprechender Umrechnungsfaktor zu ermitteln. Für die Bestimmung des Biomassenzuwachses soll der an der Hochschule Mannheim (PI-Institut) entwickelte photometrische Rückstreusensor für die quantitative Analyse der Hefetrockensubstanz kalibriert werden. Weiterhin wird mithilfe der MIR-ATR-Spektroskopie eine direkte Bestimmung der Hauptbestandteile von Backhefe-Fermentationen wie Zucker (Saccharose, Fructose und Glucose) sowie Ethanol und Biomasse in der Flüssigphase realisiert. Hierfür sind robuste multivariate Kalibrationsmodelle mit hoher Vorhersagegenauigkeit auf Basis einer PLS-Regression zu entwickeln. Ein weiteres Ziel dieser Arbeit ist die Untersuchung der Einsatzmöglichkeit von MIR-ATR- Spektrometern bei der Qualitätskontrolle von Obst und Getränken wie Fruchtsäften, Softdrinks, Bier, Radler und Cola-Bier. Hierfür werden multivariate und univariate Kalibrationsmodelle entwickelt, mit welchen quantitative MIR-ATR-Analysen der einzelnen Zucker (Saccharose, Fructose und Glucose) in Obst, Fruchtsäften, Softdrinks (Cola, Limonade, etc.) so-
17 2 Einleitung und Ziele 6 wie in Cola-Bier-Mischungen durchgeführt werden können. Weiterhin sollen Modelle für die Bestimmung des Ethanol- und Dextringehalts in Bier und Cola-Bier ausgearbeitet werden. Anhand von Vergleichsmessungen mittels HPLC werden die Genauigkeiten der Analysenmodelle abgeschätzt. Ein Vorteil der MIR-ATR-Messungen in Kombination mit geeigneten Analysenmodellen im Vergleich zu den Standardverfahren wie z.b. HPLC oder enzymatische Methoden ist, dass innerhalb von ca. einer Minute simultan die Konzentrationen mehrerer Analyten mit einer relativ hohen Genauigkeit erfasst werden können. In Kooperation mit einem in der Getränkeindustrie tätigen Unternehmen soll auf Basis dieser Forschungsergebnisse ein photometrischer MIR-ATR-Sensor entwickelt werden, welcher eine in-line Bestimmung verschiedener Analyten wie Zucker, Ethanol, Gelöst-CO 2, usw. gestattet. Dazu werden univariate Kalibrationsmodelle für verschiedene Getränke wie Bier, Cola-Bier und Cola erstellt, mit welchen die theoretisch erzielbaren Genauigkeiten abgeschätzt werden können. Weiterhin ist der Aufbau des Prototyp-Sensors mit seinen optischen Komponenten (ATR- Kristall, Diamantplättchen, Detektor, Lichtquelle und Sensor) zu planen. Ferner soll im Rahmen dieser Forschungsarbeiten eine auf MIR-ATR-Spektroskopie in Kombination mit PLS-Regression basierende Messmethode für die intrazellulare Bestimmung der Hefebestandteile Trehalose-, Glykogen-, Protein-, Lipid- und den Wassergehalt ausgearbeitet werden. Durch Voruntersuchungen mit in VE-Wasser angesetzten Kalibrationsproben sowie mit geeigneten Hefezellpräparaten soll die theoretisch erreichbare Vorhersagegenauigkeit dieser intrazellulären Stoffe abgeschätzt werden. Die MIR-Analyse von intrazellulären Kohlenhydraten (Glykogen, Trehalose, etc.) in lebenden Organismen wie Hefe, die metabolischen Prozessen unterliegen, ist bisher nur qualitativ untersucht worden [18, 19, 80, 99]. Quantitative MIR-Resultate sind bis zu diesem Zeitpunkt nicht publiziert worden. Eine Herausforderung bei der Analyse von Zellsuspensionen stellt die Entwicklung geeigneter ATRbzw. Reflexions-Messvorrichtungen zur Realisierung definierter und repräsentativer Probenvolumina dar. Aufgrund der hohen Spezifität der MIR-Spektroskopie und den Vorteilen der ATR-Aufnahmetechnik bei wässrigen und Mehrphasensystemen sollten die besten Resultate bei der quantitativen Bestimmung verschiedener intrazellulärer Kohlenhydrate und anderer Zellbestandteile (Proteine, Lipide, Wasser, etc.) mittels ATR-MIR erzielt werden. Allerdings liegt hier die Eindringtiefe des Lichtstrahls in die Probe nur bei wenigen Mikrometern. Daher sollen die Messungen dahingehend optimiert werden, sodass ein repräsentatives Probenvolumina vermessen wird.
18 3 Stand des Wissens 3.1 IR-Spektroskopie 7 3 Stand des Wissens 3.1 IR-Spektroskopie Die IR-Spektroskopie ist eine Technik, welche auf die Anregung von Molekülschwingungen und -rotationen mit infrarotem Licht (Wellenlänge: 800 nm bis 1 mm) basiert [20]. Die Energie des infraroten Lichts wird dabei von den Molekülen in spektralen Bereichen absorbiert, welche spezifisch für die jeweiligen chemischen Verbindungen sind. Je höher die Konzentration der Moleküle in den Proben, desto mehr infrarotes Licht wird in diesen Bereichen absorbiert. Diese physikalische Eigenschaft, welche durch das Lambert-Beer-Gesetz beschrieben ist, wird u.a. genutzt, um die Inhaltsstoffe von biologischen oder chemischen Proben quantitativ zu analysieren Grundlagen Infrarotes Licht sind elektromagnetische Wellen wie auch ultraviolettes (UV) und visuelles (VIS) Licht, sowie Gammastrahlung, Radiowellen und Mikrowellen. Elektromagnetische Wellen können anhand der Wellenlänge λ, der Frequenz ν, der Wellenzahl ~ ν oder der Photonenenergie E unterschieden werden. Diese Größen lassen sich gemäß folgender Formeln ineinander umrechnen: ν = c / λ (3.1) E = h ν (3.2) ~ ν 1/ λ (3.3) Mit c = 2, m/s (Lichtgeschwindigkeit) und h = 6, Js (Planck sches Wirkungsquantum). Die Energie eines Lichtquants (Photon) E nimmt daher mit der Frequenz bzw. der Wellenzahl zu und mit der Wellenlänge ab. Die Strahlungsenergie E kann genutzt werden, um Moleküle in einen Energiezustand (Molekülschwingungen und -rotationen) anzuregen [21]. Für quantitative und qualitative Analysen ist das infrarote Licht im Wellenlängenbereich von 800 nm bis 25 µm interessant. Dabei unterscheidet man Nah-Infrarot- (NIR) und Mittelinfrarot- (MIR) Spektroskopie [22]: NIR: 0,8 2,5 µm MIR: 2,5 25 µm
19 3 Stand des Wissens 3.1 IR-Spektroskopie 8 Anstatt der Wellenlängenskala hat sich insbesondere in der MIR-Spektroskopie die Wellenzahl mit der Einheit cm -1 durchgesetzt. Für die Umrechnung der Wellenlänge in die Wellenzahl gilt: ~ ν / cm 1 = 4 10 λ / µ m Während im MIR-Spektralbereich im Wesentlichen innerhalb des elektronischen Grundzustandes S 0 Grundschwingungen von Molekülen angeregt werden, liegen im Nahinfrarotbereich die Kombinations- und Oberschwingungen (siehe Abbildung 3.1). Die Grundschwingungen im MIR bzw. die Absorptionsbanden einzelner Stoffe sind häufig besser separiert als die Oberschwingungen im NIR-Bereich [22, 24]. Insbesondere der Fingerprint -Bereich zwischen 1500 und 950 cm -1 eignet sich für eine Analyse von verschiedenen Molekülverbindungen, da hier keine Wasserabsorptionsbanden liegen. Im MIR-Spektralbereich ändert sich die Schwingungsquantenzahl v (vibronic number) von Null auf Eins. Die Energie bzw. Wellenzahl, bei welcher der Übergang v = 0 v = 1 stattfindet, hängt dabei von den jeweiligen Schwingungspartnern und der Art der Schwingung (Streckschwingung, Deformationsschwingung, etc.) ab. Im NIR ändert sich die Schwingungsquantenzahl v von Null auf 2, 3 usw., wobei mit zunehmender Quantenzahl v die Schwingungsniveaus bzw. Energieabstände immer geringer werden. E (3.4) Dissoziationsgrenze v = 3 v = 2 v = 1 MIR Atomabstand d NIR S 0 v = 0 (Grundzustand) Abbildung 3.1: Potentialdiagramm zur Veranschaulichung von Grundschwingungen (v = 0 v = 1) im MIR-Bereich und Oberschwingungen (v = 0 v = 2, 3, 4, ) in der Regel im NIR-Bereich Die benötigte Energie bzw. Wellenzahl zur Anregung einer Schwingung ist abhängig von der Bindungsstärke zwischen den jeweiligen Atomen und deren Masse sowie von der Schwin-
20 3 Stand des Wissens 3.1 IR-Spektroskopie 9 gungsform (Streckschwingung, Deformationsschwingung). Tendenziell gilt in Analogie zum klassischen Federpendel: a) Je leichter ein Schwingungspartner, desto höher die Frequenz bzw. Wellenzahl. b) Je stärker die Bindung (entspricht Kraftkonstante), desto höher die Wellenzahl. c) Deformationsschwingungen liegen bei kleineren Wellenzahlen als Streckschwingungen. Es können die Atome in funktionellen Gruppen gegeneinander schwingen oder sogar das gesamte Molekülgerüst bzw. Teile davon kollektiv schwingen. Es können allerdings nur solche Bindungen angeregt werden, bei denen sich durch die Schwingung das Dipolmoment ändert. Dies ist insbesondere bei polaren Bindungen wie bei den Carbonylen der Fall. Dagegen erfahren die beiden Hauptbestandteile der Luft, Stickstoff N 2 und Sauerstoff O 2, keine Dipolmomentänderung, wenn sich der Bindungsabstand ändert, sodass sie auch kein IR-Licht absorbieren. Für qualitative und quantitative Analysen von biologischen oder chemischen Proben wird die spektrale Absorption des Lichtes betrachtet, welche durch die Wechselwirkungen mit Molekülverbindungen verursacht wird. Die Absorption der Strahlungsenergie wird ermittelt, indem man die wellenlängenabhängige Intensitätsabnahme eines Lichtstrahls beim Durchgang durch die zu analysierende Probe vermisst. Dabei fällt das von der Lichtquelle emittierte Licht I 0 zunächst auf die Probe, wo es mehr oder weniger stark absorbiert wird. Die Basislinie I 0, auch Hintergrund oder engl. Background genannt, wird vor der Probenmessung häufig mithilfe einer Referenzmessung (sogenannter Nullbezug) festgelegt, indem z.b. im UV/VIS-Bereich bei flüssigen Proben zunächst eine Küvette mit reiner Matrix (Lösungsmittel ohne Analyt) im Probenraum vermessen wird. Bei der MIR-ATR-Technik wird häufig auch Luft als Hintergrund verwendet. Die von der Probe transmittierte Intensität I gelangt schließlich zum Nachweis auf den Detektor. Dabei ist zu beachten, dass sowohl I 0 als auch I aufgrund des Lampenspektrums, des Spektrometeraufbaus und der Probenbeschaffenheit von der Lichtwellenlänge λ abhängen. Das Verhältnis von transmittierter zu einfallender Lichtintensität wird als Transmission T bezeichnet: T = I / I 0 (3.5)
21 3 Stand des Wissens 3.1 IR-Spektroskopie 10 Die Absorption A, häufig auch Extinktion, Absorbanz oder optische Dichte genannt, ist der negative dekadische Logarithmus der Transmission: ( T ) = log ( I I ) A = log (3.6) / Für ein gutes Signal-Rausch-Verhältnis (S/N) bei quantitativen Analysen sollte man stets darauf achten, dass die Absorption A zwischen 0,1 und 2 liegt. 0 Im infraroten Spektralbereich ist Wasser ein starker Absorber. Getränke, Obst und Fermentationsproben bestehen zum größten Teil aus Wasser (85-99 %), sodass die IR- Absorptionsspektren der Proben hauptsächlich aus der Absorption des Wassers resultieren. In Abbildung 3.2 ist das MIR-Absorptionsspektrum von H 2 O in der Flüssigphase dargestellt. Bei ca cm -1 liegt die Streckschwingungsbande ~ ν ( O H ), deren Lage besonders von der Temperatur abhängt. Des Weiteren sorgen die H-Brücken für Schwingungen zwischen benachbarten Wassermolekülen, was sich in einer breiten Bande um ca. 500 cm -1 niederschlägt. Diese Schwingung kann wiederum mit der Deformationsschwingung ~ ν ( O H ) bei 1650 cm -1 koppeln, sodass eine spektral breit und flach verlaufende d Kombinationsschwingung bei der Summe dieser beiden Wellenzahlen (ca cm -1 ) entsteht. 0.4 S ṽ s (O-H) 3500 cm -1 ṽ(h-brücken) 500 cm Absorption [-] ṽ d (O-H) + ṽ(h-brücken) 2200 cm -1 ṽ d (O-H) 1650 cm Wellenzahl [cm -1 ] Abbildung 3.2: MIR-Absorptionsspektrum von H 2 O in der Flüssigphase. ṽ s = Streckschwingung; ṽ d = Deformationsschwingung
22 3 Stand des Wissens 3.1 IR-Spektroskopie IR-Spektrometer und Messaufbauten Ein dispersives Spektrometer ist prinzipiell mit einer Strahlungsquelle, einem Spektralapparat (Monochromator), einem Detektor und einer Messvorrichtung ausgestattet. Das Detektorsignal wird elektronisch verarbeitet und an einen Rechner übertragen. In Tabelle 3.1 sind die Lichtquellen, Detektoren sowie die Spektralapparate aufgelistet, welche üblicherweise in NIR- und MIR-Spektrometern eingesetzt werden. Tabelle 3.1: Lichtquellen, Detektoren und Spektralapparate für die NIR- und MIR-Spektroskopie Spektrometer Lichtquelle Detektor NIR Halogenlampe InGaAs, InAs, PbS, PbSe, Ge Spektralapparat (Monochromator) Gitter, FT MIR Globar, Nernst-Stift (D)TGS, MCT FT IR-Strahlungsquelle Als Strahlungsquellen werden sowohl in der NIR- als auch in der MIR-Spektroskopie Planck sche Strahler (Schwarzkörperstrahler) zur Probenanregung verwendet. Diese emittieren Licht mit einem spektralen Intensitätsverlauf, dessen maximale Lage temperaturabhängig ist und durch das plancksche Strahlungsgesetz beschrieben wird. Im NIR kommen ausschließlich Wolfram-Halogen-Lampen zum Einsatz, welche gegenüber den MIR-Lichtquellen höhere Betriebstemperaturen und somit höhere Intensitäten aufweisen. Die für den MIR- Spektralbereich am häufigsten eingesetzte Strahlungsquelle ist der Globar aus Siliciumcarbid (SiC). Dieser hat eine Brenntemperatur von ca C und wird in Form von Stäben oder Wendeln mit einer hohen mechanischen Festigkeit ausgeführt. Eine weitere MIR- Lichtquelle ist der Nernst-Stift bestehend aus Zirkoniumoxid (ZrO 2 ) mit Zusätzen von Yttriumoxid (Y 2 O 3 ) und anderen seltenen Metalloxiden. Die Betriebstemperatur liegt bei etwa 1900 C, sodass das Emissionsmaximum zwischen 1 und 2 µm auftritt. Aufgrund der mechanischen Empfindlichkeit von Nernst-Stiften muss das Spektrometer jedoch vor Erschütterungen geschützt werden [22]. Einige IR-Geräte verwenden als Lichtquelle Keramikstäbchen mit umwickelten Heizdrähten aus Platin bzw. Platinlegierungen, welche mit einer zusätzlich gesinterten Schicht z.b. aus Aluminiumoxid, Thoriumoxid oder Zirconiumsilikat umgeben sind. Der Vorteil dieser Lichtquellen liegt in deren mechanischen Stabilität, welche weitestgehend einen wartungsfreien Betrieb ermöglicht [21] IR-Strahlungsempfänger (Detektor) Als Strahlungsempfänger stehen im infraroten Spektralbereich verschiedene Detektorvarianten zur Verfügung. Es werden sowohl thermische, pyroelektrische als auch Quantendetektoren (Photodetektoren) verwendet, wobei die Auswahl nach dem gewünschten Spektralbe-
23 3 Stand des Wissens 3.1 IR-Spektroskopie 12 reich, Aufnahmegeschwindigkeit, Signal-Rausch-Verhältnis und deren Lebensdauer erfolgt. Ein thermischer Empfänger registriert die IR-Lichtstrahlung aufgrund von Temperaturänderungen des Detektormaterials. Unter den thermischen Empfängern ist das Thermoelement am meisten verbreitet. Dieses besteht aus zwei unterschiedlichen Metall- oder Halbleiterlegierungen, an deren Kontaktstellen eine temperaturabhängige Thermospannung entsteht. Die Thermospannung ist proportional zur einfallenden Strahlungsleistung und wird als Spannungssignal detektiert. Zur Realisierung eines Detektors werden mehrere Thermoelemente in Reihe geschaltet (Thermosäule), wodurch sich die Thermospannungen addieren. Die Thermosäule befindet sich meistens in einem evakuierten Gehäuse aus infrarotdurchlässigem Material (z.b. KBr, CaF 2 ) im Strahlungsein- und austritt. Vorteile dieser Detektoren gegenüber Quantendetektoren oder pyroelektrischen Sensoren sind der einfache und kostengünstige Aufbau sowie die von der Wellenlänge unabhängige Empfindlichkeit. Die Nachteile liegen in dem schlechten Signal-Rausch-Verhalten und in den langen Ansprechzeiten. Zur Aufnahme von schnell veränderlichen Signalen im Millisekundenbereich sind diese Detektoren ungeeignet. Weiterhin erlaubt die langsame Ansprechzeit des Detektors keine Kombination mit Interferometern [21]. Pyroelektrische Strahlungsempfänger bestehen aus ferroelektrischen Substanzen wie z.b. LiNbO 3, Triglycinsulfat (TGS) bzw. zur Empfindlichkeitssteigerung mit deuteriertes Triglycinsulfat (DTGS), welche auf einer Polarisationsänderung unterhalb des Curiepunktes beruhen. Aufgrund von rasanten Temperaturänderungen wird das Dipolmoment bzw. die Polarisation des Materials geändert, sodass eine messbare Spannung entsteht. Der Detektor wird hierzu als Dielektrikum in Form eines Kondensators verwendet. Vorteile des pyroelektrischen Empfängers sind der günstige Preis, der robuste Aufbau, die wellenlängenunabhängige Empfindlichkeit sowie die schnelle Ansprechzeit. Nichtgekühlte MIR-Spektrometer sind heute meistens mit DTGS-Detektoren ausgestattet. Photoelektrische Empfänger (Quantendetektoren) sind als Detektoren für IR-Strahlung ebenso weitverbreitet. Das Prinzip dieser Empfänger beruht auf die Veränderung der elektrischen Leitfähigkeit von Halbleitermaterialen aufgrund von Bestrahlung mit Licht. Die IR- Photonen setzen in der n-p-grenzschicht des Halbleiters Ladungsträger frei bzw. erzeugen Elektron-Loch-Paare, die eine der Strahlungsintensität proportionale, messbare Spannung erzeugen. Das Photosignal kann entweder als Spannungs- oder Stromflussänderung gemessen werden. Die Halbleiter PbS, PbSe, PbSnTe oder das quaternäre Halbleitersystem HgCdTe (in engl. MCT: Mercury Cadmium Telluride) besitzen im Vergleich zu den anderen Detektoren eine höhere Empfindlichkeit insbesondere im für die Analyse bedeutenden Fingerprint -Bereich und haben sich deshalb weitestgehend in den neuen FT-MIR- Spektrometern durchgesetzt. Allerdings ist die Detektivität von Halbleitern wellenlängenabhängig. NIR-Spektrometer verwenden als Detektoren Halbleitermaterialien z.b. aus InGaAs, InAs, PbS, PbSe, Ge oder Si, wobei diese sich in der wellenlängenabhängigen Empfindlich-
24 3 Stand des Wissens 3.1 IR-Spektroskopie 13 keit unterscheiden. Da bereits die Umgebungstemperatur Ladungsträger erzeugt und somit ein hohes Untergrundrauschen verursacht, ist für den Betrieb eine Kühlung der Photodetektoren unabdingbar. MCT-Detektoren für den MIR-Bereich müssen z.b. mit flüssigem N 2 gekühlt werden, wodurch der Betrieb in der Industrie erschwert wird Monochromator Für die spektrale Zerlegung des IR-Lichtes wird ein sogenannter Spektralapparat bzw. Monochromator eingesetzt. Nicht-dispersive IR-Geräte (NDIR), welche bei einer Wellenlänge bzw. in einem Wellenlängenbereich messen, werden IR-Photometer genannt. Die Einstellung der Wellenlänge erfolgt hier im Allgemeinen nicht durch Spektralapparate sondern mittels monochromatischer Lichtquellen (Laser, LEDs) oder optischer Bandpassfilter bei Verwendung einer breitbandigen Lichtquelle (siehe Abbildung 3.3). Das optische Bandpassfilter besitzt eine hohe Transmission, bei welchem der zu bestimmende Analyt absorbiert, und blockiert das restliche Spektrum. IR-Lichtquelle Optisches Filter Messvorrichtung IR-Detektor Probe Abbildung 3.3: Aufbau eines IR-Photometers: Der optische Filter kann sowohl vor als auch hinter der Probe (direkt vor dem Detektor) lokalisiert sein Bei einem Spektrometer mit einem Spektralapparat werden im Gegensatz zu einem Photometer Lichtintensitäten über das gesamte Lichtspektrum gemessen, wobei häufig - je nach Anwendung - in Transmissions-, Absorptions- oder Reflexionsspektrum umgerechnet wird. Gitterspektralapparate (Abbildung 3.4) werden ausschließlich bei NIR-Spektrometern eingesetzt. Bei dem sogenannten Diodenzeilen-Spektrometer (Diodenarray-Spektrometer) fällt zunächst das gesamte Lampenspektrum auf die Probe und wird erst anschließend mithilfe des fest montierten Reflexionsgitters in seine spektralen Anteile aufgespalten. Dabei interferiert Licht einer bestimmten Wellenlänge nur in eine bestimmte Richtung konstruktiv. Da sich auf einer Detektorzeile (Diodenzeile) 128, 256, 512 oder 1024 Photodetektoren (Pixel) nebeneinander befinden, fällt zeitgleich auf jedes dieser Pixel Licht einer bestimmten Wellenlänge bzw. eines engen Wellenlängenbereichs, wodurch gleichzeitig ein komplettes Intensitätsspektrum aufgenommen werden kann. Je mehr Pixel eine Diodenzeile bei gegebenem Wellenlängenbereich besitzt, desto besser ist das Auflösungsvermögen des Spektrometers. Jedoch ist eine größere Anzahl von Pixeln mit höheren Investitionskosten verbunden, und die Lichtintensität pro Pixel ist gleichzeitig geringer. Bedingt durch ihren kompakten und ro-
25 3 Stand des Wissens 3.1 IR-Spektroskopie 14 busten Aufbau können Diodenarray-Spektrometer nicht nur im Labor sondern auch unter Prozessbedingungen eingesetzt werden. IR-Lichtquelle Messvorrichtung D 1 D n Photodioden Probenraum mit Fenstern Beugungsgitter Abbildung 3.4: Aufbau eines NIR-Diodenarray-Spektrometers mit einer Diodenzeile aus InGaAs- Photodioden. Während man im NIR hauptsächlich Gitter- und Fourier-Transformations-Spektrometer (FT- Spektrometer) einsetzt, werden im MIR ausschließlich FT-Spektrometer verwendet, bei denen eine Aufspaltung des Lichts gemäß Wellenzahl ~ ν erfolgt. Aufgrund der sehr intensitätsschwachen MIR-Lichtquellen und der relativ lichtunempfindlichen MIR-Detektoren liefern die Gitterspektrometer im diesem Spektralbereich selbst bei langen Messzeiten Absorptionsspektren mit einem relativ schlechten Signal-Rausch-Verhältnis. Bei einem FT-Gerät gelangt sämtliches IR-Licht auf die Probe und entsprechend auf den Detektor, wodurch eine bessere Aussteuerung des Detektors erreicht wird. Dabei wird die auf den Detektor fallende Intensität bei jeder einzelnen Wellenlänge bzw. Wellenzahl anhand eines beweglichen Spiegels in einem Michelson-Interferometer unterschiedlich zeitlich moduliert. Da die Modulation bekannt ist, kann aus dem zeitlichen Detektorsignal mithilfe der mathematischen Fourier- Transformation ein Intensitätsspektrum und somit auch ein Absorptionsspektrum berechnet werden. IR-Lichtquelle fester Spiegel Bereich der Interferenz Strahlenteiler Kollimatorspiegel He-Ne- Laser IR-Detektor Probe Beweglicher Spiegel x Zentralposition ( x = 0) PC Abbildung 3.5: Aufbau eines Fourier-Transformations-Spektrometers
26 3 Stand des Wissens 3.1 IR-Spektroskopie 15 Die Spiegel und der Strahlteiler sind beim Fourier-Transform-Spektrometer gleichermaßen angeordnet wie bei einem Michelson-Interferometer. In dem rosa markierten Bereich des Strahlteilers (Abbildung 3.5) interferieren die vom festen Spiegel und die vom beweglichen Spiegel reflektierten Teilstrahlen je nach Gangunterschied. Der He-Ne-Laser dient als Wellenlängenstandard zur exakten Bestimmung der Position des beweglichen Spiegels. Als Messvorrichtung für die Probe können Küvetten, KBr-Presslinge oder ATR-Zellen verwendet werden. NIR-Spektrometer besitzen gegenüber MIR-Spektrometern den Vorteil, dass man Messsonden über Lichtleiterfasern, die mit dem Spektrometer verbunden sind, über eine große Entfernung (max. 100 m) direkt in den Prozess installieren kann, während das Spektrometer in einem geschützten Raum untergebracht ist. Je nach Anwendung kommen dabei Transmissions- oder Reflexionssonden zum Einsatz. Dabei gelangt das von der Lichtquelle emittierte Licht mithilfe der Sendefasern zur Sonde. Das an der Messstelle nicht absorbierte bzw. zurück reflektierte Licht gelangt schließlich mittels Empfangsfasern zum spektralen Nachweis ins Spektrometer. Bei einem MIR-Spektrometer können die Messvorrichtungen lediglich einige wenige Meter mit Eintauchsonden über einen Spiegelarm oder über MIR-Lichtleiter z.b. aus Silberhalogenid mit dem Spektrometer verbunden werden. Während der Spiegelarm einen relativ starren und justierempfindlichen Aufbau besitzt, haben die MIR-Lichtleiter aus Silberhalogenid den Nachteil, dass sie im Laufe der Zeit lichtundurchlässig werden und mit ihnen nur sehr kurze Distanzen von maximal zwei Metern überbrückt werden können. Dennoch ist in den letzten Jahren ein Trend weg von den Spiegelarmen hin zu den Lichtleitern zu verzeichnen aufgrund des Vorteils, dass mit ihnen eine direkte on-line Prozessverfolgung und Regelung möglich ist. Infolge des geringen Lichtdurchsatzes der Eintauchsonden ist jedoch ein lichtempfindlicher und teurer MCT-Detektor mit flüssiger N 2 -Kühlung in das MIR- Spektrometer einzubauen ATR-Messtechnik Bei stark absorbierenden Proben im MIR-Bereich, die nicht verdünnt werden können, ist es erforderlich, Schichtdicken im Mikrometerbereich zu realisieren, sodass die Absorption kleiner zwei wird (A < 2). Dies ist mit herkömmlichen Küvetten (Durchlicht- bzw. Transmissionsmessung) nur unter erheblichem Aufwand möglich. Dagegen werden bei der abgeschwächten Totalreflexions-Spektroskopie (ATR) Schichtdicken von weniger als einer Wellenlänge realisiert. Bei der ATR-Spektroskopie wird der mit dem Einfallswinkel β einfallende Lichtstrahl mit einem hoch brechenden Prisma z.b. aus Diamant, ZnSe oder Saphir auf die Grenzfläche ATR-Kristall / Probe abgelenkt (Abbildung 3.6). Bei der Totalreflexion wird der
27 3 Stand des Wissens 3.1 IR-Spektroskopie 16 Lichtstrahl allerdings nicht wie man in der geometrischen Optik lernt direkt an der Grenzfläche zurückreflektiert, sondern dringt beim Reflexionsvorgang noch etwas weniger als eine Lichtwellenlänge in das niedrig brechende Medium (Probe) ein und kann dabei teilweise absorbiert werden. Die Eindringtiefe des IR-Lichtes in die Probe kann durch folgende Formel berechnet werden: d p = 2 π n k λ 2 sin Mit n k = Brechungsindex des ATR-Kristalls und Werte sind n β n n k (Diamant) 2,4, n k (ZnSe) 2,4, n k (Saphir) 1,8, p k 2 (3.7) n P = Brechungsindex der Probe. Typische n P (H 2 O) 1,3, n P (Kohlenwasserstoffe) 1,4 1,5, n P (halogenierte Kohlenwasserstoffe) 1,45 1,6. Da der Lichtstrahl in die Probe hinein und wieder heraus gelangt, liegt die effektive Eindringtiefe bei d eff = 2 d, sodass eine ATR-Zelle mit n Reflexionen an der Grenzfläche Kristall / p Probe zu folgender vermessener Probenschichtdicke führt: d ATR n d n 2 d (3.8) eff p Da die Eindringtiefe proportional zur Wellenlänge ist, erscheinen im ATR-Spektrum langwellige Banden mit höheren Extinktionswerten als bei Absorptionsspektren, welche im Durchlicht (z.b. Küvette oder Pressling) aufgenommen wurden. Probe < λ β ATR-Zelle Interferometer IR-Detektor IR-Lichtquelle Abbildung 3.6: ATR-Messanordnung (drei Reflexionsstellen) in Kombination mit einem FT- Spektrometer für MIR-Anwendungen
28 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie Kalibrationsmethoden in der optischen Spektroskopie Die Aufgabe der Kalibration in der optischen Spektroskopie besteht darin, zwischen den Messgrößen z.b. der Absorption der IR-Strahlung und den Systemeigenschaften wie z.b. der Analytkonzentration einen Zusammenhang in Form einer empirischen Funktion herzustellen. Diese sogenannte Transferfunktion wird anschließend dazu verwendet, um eine unbekannte Konzentration aus unabhängigen, d.h. nicht im Kalibrationsdatensatz enthaltene Messdaten vorherzusagen. Bei der univariaten und multivariaten Kalibration werden zur Erstellung der Transferfunktion IR-Spektren von Proben mit bekannten Analytkonzentrationen (abhängige Variablen, Objekte) aufgenommen und mit den gemessenen Absorptionswerten bei einer bzw. mehreren Wellenlängen (unabhängige Variablen) gegenübergestellt. Grundlage für die Kalibration und die quantitative Analyse in der optischen Spektroskopie bildet das Lambert- Beer-Gesetz, mit dem ein linearer Zusammenhang zwischen einer Absorption bei einer bestimmten Wellenlänge λ des Spektrums und der Analytkonzentration beschrieben wird [27]. i ( λ) A i ( ) = ε ( λ) c d λ (3.9) A Absorption bzw. Extinktion des Analyten i bei der Wellenlänge λ i ε i ( λ) molarer dekadischer Extinktionskoeffizient des Analyten i bei der Wellenlänge λ in c i d λ [L/(mol cm)] Konzentration des Analyten i in [mol/l] optische Weglänge bzw. Schichtdicke in [cm] Wellenlänge = 1/ v ~ mit v ~ als Wellenzahl i Dieser lineare Zusammenhang ist allerdings nur für nicht streuende Lösungen sowie für Proben bei konstanter Temperatur und - je nach spektroskopischer Methode und verwendetem Spektrometer - in der Regel nur bei Absorptionen kleiner zwei gegeben. Zusätzlich bestehen die Proben häufig aus mehreren Komponenten, sodass sich das Absorptionsspektrum eines Gemisches A( λ ) Mischung im Idealfall aus einer linearen Superposition der Absorptionsspektren der Reinsubstanzen in der Mischung zusammensetzen. ( λ) ( ) Mischung = si Ai ( λ) m A λ (3.10) A Absorption des Spektrums der Reinsubstanz i (i = 1,,m) bei der Wellenlänge λ i i= 1 s i Anteil der Substanz i an der Mischung
29 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 18 Aufgrund spektroskopischer Überlappungen der Absorptionsspektren einzelner Komponenten sowie anderer Störphänomene wie z.b. intermolekulare Wechselwirkungen ist es schwierig, die Konzentration einer Komponente mithilfe des einfachen Lambert-Beer-Gesetzes aus Gleichung 3.9 eindeutig zu ermitteln. Nach einer auf die Problemstellung zugeschnittenen Kalibration ist es mittels sogenannter multivariater Auswertemethoden wie Partial Least Squares (PLS) oder Principal Component Regression (PCR) möglich, auch komplexe Stoffgemische zu analysieren. Im Gegensatz zu univariaten Kalibrationen, bei denen ein Extinktionswert bei einer Wellenlänge oder eine Bandenfläche in einem spektralen Bereich als Information für die Analytkonzentration dient, nutzen multivariate Methoden mithilfe einer Computer-Software und komplexen Rechenverfahren die gesamten spektralen Daten für die Kalibration. Durch die PCR- bzw. PLS-Methode erfolgt außerdem eine Separation und Gewichtung der spektralen Informationen. Die Anwendung von mathematischen und statistischen multivariaten Modellen auf experimentelle Analysendaten wird auch als Chemometrik oder Chemometrie bezeichnet [25] Univariate und multivariate Kalibration Bei der klassischen univariaten Kalibrationsmethode wird lediglich eine spektrale Information, wie der Absorptionswert bei einer bestimmten Wellenlänge oder eine Absorptionsbandenfläche in einem spektralen Bereich mit den Konzentrationen der Probe korreliert. Das Kalibrationsmodell wird hier durch eine lineare Gleichung beschrieben: y x a 1 a 0 y = a x + (3.11) 1 a 0 Konzentrationswert des Analyten in der Probe Absorptionswert bei einer bestimmten Wellenlänge bzw. Absorptionsbandenfläche in einem spektralen Bereich Regressionskoeffizient bzw. Steigung der Geraden Regressionskonstante bzw. Achsenabschnitt der Geraden Die für das Kalibrationsmodell zu ermittelten Parameter a 1 und a 0 werden nach der Methode der kleinsten Quadrate (engl. Least Squares Method) geschätzt [25]. Die Methode der kleinsten Fehlerquadrate ist das mathematische Standardverfahren in der Regressionsanalyse und wird nicht nur bei der univariaten linearen Regression, sondern auch bei nichtlinearen Polynomfunktionen, bei der multiplen linearen Regression (MLR) und Hauptkomponentenregression (PCR) sowie in erweiterter Form bei der Partial Least Squares Regression (PLS) angewendet [25].
30 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 19 Im Gegensatz zur multivariaten Kalibration sind bei univariaten Kalibrationen Extrapolarisationen erlaubt, sodass Konzentrationen über den Kalibrationsbereich hinaus bestimmt werden können. Ein weiterer Vorteil ist die direkte Bestimmung der Empfindlichkeit und Analytkonzentrationen aus der Modellgleichung. Die klassische univariate Bandenanalyse zur Konzentrationsbestimmung stößt jedoch bei Gemischen aus chemisch ähnlichen Substanzen oft an ihre Grenzen. Mithilfe sogenannter multivariater Auswertemethoden wie Partial Least Squares (PLS), Principal Component Regression (PCR), etc. ist es jedoch möglich, komplexe Stoffgemische auch dann zu analysieren, wenn die IR-Absorptionsspektren der einzelnen Analyten sich relativ unspezifisch überlagern, wie es z.b. bei Kohlenhydraten der Fall ist. Durch die multivariate Datenanalyse wird eine Regression von mehreren unabhängigen Variablen (mehrere Absorptionswerte eines Spektrums) und abhängigen Variablen (Analytkonzentrationen in den Kalibrationsproben) durchgeführt. Die Anzahl der vermessenen Proben mit unterschiedlichen Analytkonzentrationen werden durch den Index m markiert. Die Absorptionswerte bei den einzelnen Wellenlängen der Probenspektren werden durch den Index n gekennzeichnet. Für die Berechnungsalgorithmen der multivariaten Kalibration werden die spektroskopischen Messungen als spektrale Datenmatrix X mit m Zeilen und n Spalten zusammengefasst. In den Spalten der Datenmatrix X werden die einzelnen Absorptionswerte x mn eines Spektrums der Probe m aufgelistet. Analog dazu werden die Konzentrationswerte von mehreren Analyten p als Matrix Y zusammengefasst. X x11 x21 = M xm1 x x x M m2 L L O L x x x 1n 2n M mn (3.12) Y y y = M y m1 y y y M m1 K K O K y y y 1p 2 p M mp (3.13) x mn n-ter Absorptionswert im Spektrum der m-ten Probe y Konzentrationswert des p-ten Analyten in der m-ten Kalibrationsprobe mp Die Verknüpfung beider Matrizen erfolgt durch die Regressionsmatrix A: Y = X A + E (3.14) Y Matrix mit abhängigen Variablen (m bekannte Konzentrationsverhältnisse von p Analyten) mit der Ordnung m x p X Matrix mit unabhängigen Variablen (n Absorptionswerte für jede gemessene Probe) mit der Ordnung m x n A Matrix der Regressionsparameter mit der Ordnung n x p E Residuenmatrix (Residuen = Differenz zwischen den wahren und den mit dem Modell vorhergesagten y-werten mit der Ordnung m x p
31 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 20 Die unbekannte Regressionsmatrix A wird bis auf wenige Ausnahmen über die allgemeine Inverse durch die Methode der kleinsten Fehlerquadrate ermittelt, mit dem Ziel die Residuenmatrix E zu minimieren: A = T 1 T ( X X ) X Y (3.15) Das Vorhersagemodell zur Konzentrationsbestimmung der Analyten in einer unbekannten Probe lautet: Yˆ = X Aˆ (3.16) Yˆ Matrix mit vom Modell vorhergesagten Konzentrationen der p Analyten mit der Ordnung 1 x p X gemessenes Spektrum mit den unabhängigen Variablen (n Absorptionswerte) der unbekannten Probe (Matrix mit der Ordnung 1 x n) Â Regressionsmatrix des Modells mit der Ordnung n x p PLS-Regression Heutzutage wird für die IR-Kalibration fast ausschließlich die PLS-Regression (PLS: Partial Least Squares) verwendet. In der IR-Spektroskopie sind die Daten eines Spektrums oft multikollinear, d.h. die Variablen (Absorptionswerte) sind untereinander korreliert. Moleküle können z.b. mehrere IR-Absorptionsbanden besitzen, deren Intensitäten sich mit Zunahme der Konzentrationen ähnlich verhalten. Die Verwendung aller Absorptionswerte würde keine zusätzliche Information für das Kalibrationsmodell liefern. Es würde vielmehr die Gefahr bestehen, dass aufgrund der Korrelationen die Matrixinversion nach Gl fehlerbehaftet ist. Das IR-Spektrum, welches aus vielen korrelierten Absorptionswerten besteht, wird mithilfe der PLS in wenige unkorrelierte Variablen - sogenannte latente Variablen - transformiert, mit denen anschließend das Gleichungssystem 3.15 problemlos gelöst werden kann. Die PLS- Methode ist nah verwandt mit dem PCR-Algorithmus (Principle Component Regression), welcher aus einer Hauptkomponentenanalyse (engl. Principle Component Analysis, PCA) und einer anschließenden Regressionsanalyse nach der Methode der kleinsten Fehlerquadrate besteht. Mit der PCA werden die gemessenen Ausgangsdaten (spektrale Datenmatrix X) in neue sogenannte Faktoren bzw. Hauptkomponenten zerlegt, welche orthogonal (unkorreliert) zueinander sind. Diese Faktoren sind eine Linearkombination der ursprünglichen Variablen und werden als Summe der unterschiedlich gewichteten Varianzen (Streuung) der Originalvariablen berechnet [25], [29].
32 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 21 Der schematische Ablauf der Hauptkomponentenanalyse auf Basis der Kovarianzmatrix C ist in folgender Abbildung 3.7 zu sehen. Zuerst wird eine Mittelwertzentrierung der Datenmatrix X durchgeführt, indem von jedem Variablenwert xij in Zeile i = 1,,m und Spalte j = 1,,n der der j-te Spaltenmittelwert x j subtrahiert wird. ~ x ij = x ij x j (3.17) x~ ij mittelwertzentrierte Variable der Datenmatrix X in der i-ten Zeile und j-ten Spalte Der Spaltenmittelwert x j der Absorptionswerte (bei der Wellenzahl j) in den Proben m wird berechnet durch x 1 = m j x ij m i= 1 (3.18) x j x ij m Mittelwert der Absorptionswerte der Proben bei der Wellenzahl j Absorptionswert (Variable) der Probe i bei der Wellenzahl j (i = 1,,m; j = 1,...,n) Anzahl der gemessenen Kalibrationsproben (Objekte) Anschließend wird die mittelwertzentrierte Matrix transponiert und diese ( T X ~ ) mit der mittelwertzentrierten Datenmatrix X ~ multipliziert. Hierdurch erhält man die Kovarianzmatrix C, welche als Elemente alle möglichen Kombinationen der Kovarianzen und Varianzen der Variablen x ij enthält. Mithilfe des Eigenwertproblems der Kovarianzmatrix werden unkorrelierte Eigenvektoren bestimmt und diese spaltenweise in der Loading-Matrix P n zusammengefasst. Der Eigenvektor mit dem größten Eigenwert beschreibt die größte Varianz (Streuung) der spektralen Daten. Der Eigenvektor mit dem zweitgrößten Eigenwert ist orthogonal und somit linear unabhängig zu dem ersten Eigenvektor und beschreibt die nächst größere Veränderung in den Kalibrationsspektren [29]. Für die n x n Kovarianzmatrix C können maximal n Eigenwerte und n Eigenvektoren gefunden werden. Da sich in der Regel mit wenigen Hauptkomponenten bereits ein Großteil der Varianzen der Daten beschreiben lässt, müssen nicht alle n Hauptkomponenten für das Modell verwendet werden [25]. Für die Entscheidung über die Anzahl signifikanter Hauptkomponenten gibt es eine Vielzahl an statistischen Verfahren (siehe Kapitel 3.2.4). Nach Auswahl der für das Kalibrationsmodell signifikanten (normierten) Eigenvektoren k, werden diese in der Loading-Matrix P k zusammengefasst. Durch eine Hauptachsentransformation bzw. Multiplikation der Loading-Matrix P k mit der ursprünglichen Datenmatrix X erhält man die Score-Matrix T. Die erste Spalte dieser Matrix beschreibt die erste Hauptkomponente (1. Faktor). Die zweite Hauptkomponente (2. Faktor) wird durch die zweite Spalte der Score-Matrix erfasst usw. [25]. Für die PCA wird nun die Score-Matrix T anstelle der Datenmatrix X in Gl verwendet.
33 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 22 Rohdatenmatrix X Mittelwertzentrierte Datenmatrix X ~ ~ T ~ Kovarianzmatrix C = ( m 1) 1 X X Loading-Matrix P n Hauptkomponenten k Score-Matrix T = X P Mittelwertsubtraktion der n Variablen Transponierung der Datenmatrix X ~ und Multiplikation mit Eigenwertproblem: Berechnung der Eigenwerte λ und der Eigenvektoren p von C Auswahl der wichtigsten Varianzen (Eigenwerte) und zugehörigen Eigenvektoren Hauptachsentransformation = Multiplikation der Loading- Matrix P mit der ursprünglichen Datenmatrix X k X ~ T Abbildung 3.7: Schematischer Ablauf der PCA Mit der Partial Least Squares Regression (PLS) werden für die unabhängige spektrale Datenmatrix sowie für die abhängige Konzentrationsmatrix (Y) k Hauptkomponenten ermittelt, die sich in den jeweiligen Spalten der Score-Matrizen wiederfinden. Nach Ermittlung der Score-Matrizen wird auf Basis dieser eine Regressionsanalyse durchgeführt. Der Unterschied zur PCA ist, dass die Datenmatrix X nicht aufgrund ihrer maximalen Varianzen, sondern in Abhängigkeit von den Konzentrationen (maximale Kovarianz der Konzentrations- und der Datenmatrix) zerlegt wird [25], [28]. Die PLS beinhaltet also die Faktorisierung als einen Regressionsschritt, bei welchem die Zusatzinformation der Konzentrationswerte genutzt wird, um zwischen nützlicher und nicht nützlicher Information zu unterscheiden. Dies ist ein Vorteil der PLS-Regression gegenüber der PCA, da bereits bei der Zerlegung der Datenmatrix X in Hauptkomponenten eine Korrelation zu den Referenzwerten in der Matrix Y gesucht wird. Variablen, welche mit den vorgegebenen Konzentrationen hoch korrelieren, werden in der PLS besonders hoch gewichtet, weil mit diesen normalerweise bessere Vorhersagen über Konzentrationswerte unbekannter Proben erzielt werden können. Die Berechnungen der PLS-Methode basieren generell auf dem NIPALS (Nonlinear Iterative Partial Least Squares) Algorithmus, mit welchem auch nichtlineare Zusammenhänge erklärt werden können. Neben der Bruker Software OPUS Quant 2, welche speziell für die IR-Spektroskopie entwickelt wurde, können z.b. auch mit GRAMS, MATLAB, Unscrambler und SAS eine PCRoder PLS-Kalibration durchgeführt werden.
34 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie Mathematischer Hintergrund der PLS-Regression Die PLS-Regression berechnet Score-Vektoren für die spektrale Datenmatrix X sowie für die Konzentrationsmatrix Y und entwickelt auf Basis dieser Scores ein Regressionsmodell [30]: X T + = T P E (3.19) X Y T P und T Q T und U E und F m n k p T + Y = U Q F (3.20) spektrale Datenmatrix mit der Ordnung m x n Konzentrationsmatrix mit der Ordnung m x p Transponierte Loading-Matrizen mit der Ordnung k x n und k x p Score-Matrizen mit der Ordnung m x k Fehlermatrizen (Residuen) mit der Ordnung m x n und m x p Anzahl der Objekte (Kalibrationsproben) Anzahl der Variablen (Absorptionswerte bei bestimmten Wellenlängen) Anzahl der Hauptkomponenten Anzahl der Analyten Diese zwei Gleichungen werden als äußere Beziehungen bezeichnet. Die PLS versucht nun, die Fehlerterme E und F zu minimieren und im Gegensatz zur PCR gleichzeitig eine Korrelation zwischen den Originaldaten X und Y zu erhalten, indem die Matrizen T und U in Beziehung zueinander gesetzt werden: U = T D (3.21) mit D = Diagonalmatrix mit der Ordnung k x k Diese Gleichung wird innere Beziehung genannt. Dabei wird die Orthogonalmatrix T durch eine weitere Linearkombination der spektralen Datenmatrix X geschätzt: T = X W (3.22) W PLS-Gewichtungsmatrix mit der Ordnung n x k Das äußere und innere Gleichungssystem werden nun in Beziehung gebracht, mit dem Ziel den Fehlerterm E und F zu minimieren: Y T T = U Q = T D Q = X W D Q = X A T T A = W D Q (3.23) mit A als PLS-Regressionsmatrix mit der Ordnung n x p, welche für die Vorhersage unbekannter Analytkonzentrationen anhand eines gemessenen Spektrums in die Modellgleichung 3.16 eingesetzt wird.
35 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie Bedeutung der PLS-Hauptkomponenten Die ersten PLS-Hauptkomponenten (PLS-Faktoren) charakterisieren die für die spätere Auswertung wichtigsten Informationen des Kalibrationsmodells. Die höheren Faktoren beschreiben weniger bedeutende spektrale Änderungen u.a. das Rauschen. Um ein Modell zu entwickeln, das auf Hauptkomponenten basiert, muss man eine Grenze zwischen nützlicher Information und Rauschen festlegen. Wenn zu viele Faktoren eingeschlossen werden, resultiert dies in einer Überanpassung (Overfitting) des Modells, sodass auch Rauschen in die Modellbildung mit eingeht. Werden zu wenige Hauptkomponenten verwendet, hat dies eine schlechte Reproduktion der spektralen Daten zufolge (Underfitting). Hier kann das Modell die Änderungen in den spektralen Eigenschaften nicht ausreichend erkennen und es führt zu unbefriedigenden Analyseergebnissen. Overfitting des Modells ist wahrscheinlicher und kritischer zu bewerten als Underfitting, weil dabei die Güte des erstellten Kalibrationsmodells zu optimistisch eingeschätzt wird. Um die Auswahl der Faktorenzahl (Rang, Anzahl der Hauptkomponenten) und somit die Güte des Kalibrationsmodells realistisch einschätzen zu können, ist neben einer internen Validierung (Kreuzvalidierung) auch eine Test-Set-Validierung sowie eine externe Validierung notwendig. Der Unterschied und die Bedeutung dieser Validierungsmethoden werden im Kapitel genauer erläutert Spektrale Datenvorbereitung Die Datenvorbehandlung ist ein wichtiger Aspekt in der Auswertung von IR-Spektren. Ziel der Vorbehandlung ist es, irrelevante oder zufällige Variationsquellen (Rauschen) und systematische Fehlerquellen in den Spektren zu reduzieren. Dabei wird die spektrale Information verändert, was sich sowohl positiv als auch negativ auf das Kalibrationsmodell auswirken kann. Es stehen mehrere Vorbehandlungsmethoden zur Verfügung [26] Subtraktion eines konstanten Offsets Bei der Subtraktion eines konstanten Offsets wird von den Spektren ein konstanter Wert (Offset) linear in y-richtung abgezogen, bis der kleinste y-wert (Absorptionswert) bei Null liegt. Konstante lineare Basislinienverschiebungen werden so eliminiert Subtraktion einer Geraden Bei der Subtraktion einer Geraden wird in jedem selektierten Spektralbereich des Spektrums eine Gerade angepasst, welche nach der Methode der kleinsten Fehlerquadrate bestimmt wird. Diese Gerade wird dann von dem jeweiligen Spektrum subtrahiert. So können schräge bzw. gekippte Basislinienverschiebungen korrigiert werden. Die Methode Subtraktion eines konstanten Offsets oder Gerade empfiehlt sich insbesondere bei der Raman-Spektroskopie.
36 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie Vektornormierung (SNV) Bei der Vektornormierung wird zuerst das Spektrum mittelzentriert, indem der Mittelwert aller y-werte vom Spektrum subtrahiert wird. Anschließend wird die Summe der Quadrate aller y- Werte berechnet und das entsprechende Spektrum durch die Wurzel dieser Summe dividiert. Mithilfe dieser Datenvorbehandlung werden die Höhen der einzelnen Absorptionsbanden normiert, wobei die Struktur bzw. das Verhältnis der einzelnen Banden bestehen bleibt. Man verwendet Normierungen in der quantitativen Analytik, um Messungen bei unterschiedlichen Schichtdicken zu vergleichen. Die Schichtdicke hat einen Einfluss auf die Höhe der Absorptionsbanden jedoch nicht auf die Struktur des Spektrums. Bei diffuser Reflexion lassen sich so störende Einflüsse durch unterschiedliche Materialdichten oder Partikelorientierungen in der Probe minimieren. Normierungen können auf unterschiedliche Arten erfolgen. Häufig wird auf den Gesamtmittelwert eines Spektrums normiert. Außerdem ist es möglich, bei biologischen Proben auf den Mittelwert oder das Integral der C-H-Streckschwingungsbanden bei 2700 bis 3000 cm -1 zu normieren, da die Höhe der Absorptionsbande proportional zum gesamten organischen Material ist Minimum-Maximum-Normierung Die Minimum-Maximum-Normierung und deren Anwendung sind vergleichbar mit der Vektornormierung. Die Spektren werden linear so verschoben, dass der minimal auftretende y-wert gleich Null gesetzt wird. Dann werden die Spektren in y-richtung so expandiert, dass der maximal auftretende y-wert gleich Zwei ist. Für Absorptionsspektren entspricht dies zwei Absorptionseinheiten. In der Praxis kann die Minimum-Maximum Methode für Proben mit stark absorbierendem Lösungsmittel wie z.b. H 2 O von Vorteil sein, jedoch wird in solchen Fällen die SNV-Methode vorgezogen Multiplikative Streukorrektur (MSC) Bei der multiplikativen Streukorrektur wird zuerst aus allen Spektren des Datensatzes das Mittelwertspektrum gebildet. Dann wird jedes Spektrum linear transformiert, sodass der Unterschied des transformierten Spektrums zum Mittelwertspektrum möglichst klein ist. Diese Methode wird oftmals bei Messungen in diffuser Reflexion angewandt Erste und zweite Ableitung Eine der effektivsten Methoden der Datenvorbehandlung ist die Bildung von Ableitungen. Diese können die spektrale Auflösung verstärken. Allerdings wird dadurch auch das Signal- Rausch-Verhältnis verschlechtert, was den Effekt der besseren Auflösung wieder kompensieren kann. Durch die Bildung von Ableitungen verliert das Spektrum seine ursprüngliche Form, was nachfolgende Interpretationen erschwert. Trotzdem sind Ableitungen wegen ihrer
37 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 26 Einfachheit und Leistungsfähigkeit die beliebteste Methode, um Störeffekte aus Spektren zu entfernen. Durch die Bildung der Ableitung der jeweiligen Spektren gewinnen Signale mit steilem Anstieg eine höhere Bedeutung als solche mit flacheren, breiten Banden. Man verwendet die Ableitungen, wenn relativ kleine aber scharfbandige Signale von einem relativ hohen und breiten Untergrund überlagert werden. Mit der Ableitung bekommen die Strukturen eine steilere Form. Darüber hinaus eliminiert die erste Ableitung einen konstanten Offset und die zweite Ableitung eine schräge Basislinie. Nachteilig ist jedoch, dass das spektrale Rauschen an Einfluss gewinnt und die Auswertung stören kann. Insbesondere mit der zweiten Ableitung wird das spektrale Rauschen derart erhöht, dass diese Methode eher selten verwendet wird. Die Auswahl der optimalen Methode hängt vom jeweiligen System ab. Es kann keine generelle Empfehlung gegeben werden, welche Methode der Datenvorbehandlung verwendet werden soll. Die passende Methode der Datenvorbehandlung kann nur durch eine empirische Vorgehensweise herausgefunden werden. In vielen Fällen ist die Subtraktion einer Geraden, die Normierung der Spektren oder die Bildung der ersten Ableitung die beste Methode [26]. Manchmal erhält man auch mit der Kombination von zwei unterschiedlichen Datenvorbehandlungen ein besseres Kalibrationsmodell (z.b. erste Ableitung und Vektornormierung). Meistens werden aber für unterschiedliche Datenvorbehandlungen ähnlich gute Ergebnisse erhalten Validierungsmethoden Für die Beurteilung der Vorhersagegenauigkeit von Kalibrationsmodellen wird eine Validierung durchgeführt. Hierbei werden die Analytkonzentrationen von Referenzproben mithilfe des Kalibrationsmodells vorhergesagt. Ein Vergleich der resultierenden Analysenwerte mit den durch die Referenzanalytik bekannten (wahren) Werten zeigt, wie exakt das Modell arbeitet. Die Optimierung des Modells durch Auswahl der Anzahl an Hauptkomponenten, der relevanten spektralen Bereiche und der Datenvorbehandlung erfolgt durch derartige Validierungsvorgänge. Der Parametersatz, welcher zu den geringsten Vorhersagefehlern führt, kennzeichnet häufig die beste Methode. Dabei können auch Ausreißer in den Proben erkannt werden. Es wird zwischen interner Validierung (Kreuzvalidierung), Test-Set- und externer Validierung unterschieden (s.u.). Die Ergebnisse einer Validierung - r (Korrelationskoeffizient) bzw. R 2 (Bestimmtheitsmaß), RMSECV (Root Mean Squares Error of Cross Validation) und RMSEP (Root Mean Squares Error of Prediction) - erlauben die Leistungsfähigkeit einer multivariaten Kalibration abzuschätzen.
38 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 27 Bei einer großen Anzahl an vorhandenen Kalibrationsproben ist die Test-Set-Validierung von Vorteil, da sich der Rechenaufwand verringert und somit schnelle Ergebnisse erhalten werden. Im Gegensatz zur Kreuzvalidierung können mehrere unterschiedliche Test-Set- Validierungen durchgeführt werden, da die Probenzuordnung variabel ist. Stellt man fest, dass die Vorhersagefehler bei der Kreuzvalidierung deutlich besser als bei den Test-Set-Validierungen sind, so kann es durchaus sein, dass nicht genügend Proben vermessen wurden. Dies resultiert daher, dass bei der internen Kalibrierung ungefähr doppelt so viele Spektren im Kalibrierungsdatensatz enthalten sind als bei den Test-Set- Validierungen, wenn es sich um den gleichen Datensatz handelt. Letztendlich ist aber die externe Validierung entscheidend, da sich hier das Modell erstmals in der Praxis bewähren muss Korrelationskoeffizient r und Bestimmtheitsmaß R 2 Ein Maß für die Beurteilung des mittels Statistik gefundenen linearen Zusammenhangs zwischen den vorhergesagten Konzentrationen x 1 und den durch die Referenzanalytik bekannten (wahren) Werten x 2 ist der Korrelationskoeffizient. Er lässt sich anhand der Kovarianz sx 1 x 2 und den Varianzen s und s x2 von x 1 und x 2 durch folgende Gleichung abschätzen: x 1 r x1 x2 = s s x1 x1 x2 s x2 = 1 m 1 1 m 1 m ( ~ xi ) ( ~ 1 xi2 ) ( ~ 2 xi ) ( ~ 1 xi2 ) i= 1 m i= 1 1 m 1 m i= 1 2 (3.24) Die Varianz (Streuung) ist ein Maß dafür, wie die einzelnen Daten einer Variablen um den Mittelwert x j gestreut sind. Sie wird berechnet, indem die Summe der quadratischen Abweichungen vom Mittelwert durch die Anzahl der Proben m minus 1 dividiert wird. Die Quadratwurzel aus der Varianz wird als Standardabweichung bezeichnet. Die Varianz der Variable x j berechnet sich aus m 2 1 ( x ) = s = ( ~ x ) var j x ij (3.25) j m 1 Bei der Kovarianz werden die Streuung der zwei Variablen x 1 und x2 um deren Spaltenmittelwert gegenübergestellt, sodass diese bezüglich ihrer Varianzen miteinander vergleichbar 2 sind, wobei cov( x, x ) sx = ( x ) 1 = gilt. 1 1 var 1 i= 1 2 cov ( x, x ) s = ( ~ x ) ( ~ x ) 1 2 m 1 = x1 x2 i1 i2 m 1 i= 1 (3.26)
39 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 28 Der Korrelationskoeffizient r x 1 x 2 kann einen Wert zwischen -1 und 1 annehmen. Je näher der Wert an diese Grenzen stößt, desto größer ist der lineare Zusammenhang zwischen den Variablen. Ein Wert von Null impliziert keine Korrelation zwischen den Variablen, d.h. sie sind voneinander statistisch unabhängig. Das Bestimmtheitsmaß R 2 ist das Quadrat des Korrelationskoeffizienten und wird normalerweise in Prozent angegeben. ( ) 2 2 r x1 x2 R = (3.27) Die Werte von R 2 können zwischen 0 und 100 % liegen, wobei 100 % auf eine exakte Korrelation zwischen x 1 und x2 hinweist Kreuzvalidierung Für eine interne Validierung (Kreuzvalidierung, Cross Validation) werden aus dem vorhandenen m Spektren mit zugehörigen bekannten Konzentrationswerten m-1 Spektren zur Erstellung eines multivariaten Kalibrationsmodells herangezogen. Mit diesem Modell wird die aus dem Kalibrationsdatensatz entnommene Probe analysiert und die Abweichung Modell (Vorhersage) minus Wahr (Referenz) ermittelt. Im nächsten Schritt wird ein anderes Probenspektrum aus dem Datensatz entfernt und mit den nun verbliebenen m-1 Spektren erneut eine Kalibration erstellt, welche das nicht im Kalibrationsdatensatz enthaltene Spektrum auswertet. Dieser Vorgang wird so oft wiederholt, bis jedes Spektrum einmal separat analysiert wurde. Aus der Differenz zwischen den so ermittelten und den bekannten Konzentrationen jeder Probe wird für jeden Analyten ein RMSECV- Wert (RMSECV = Root Mean Square Error of Cross Validation bzw. Wurzel des mittleren Fehlerquadrates) berechnet: RMSECV = 1 m m i= 1 ( C Wahr C 2, i Modell, i ) (3.28) C Wahr unabhängig bestimmte Konzentration der Probe i (i = 1,..,m) (z.b. Standard bzw. Konzentrationswert durch externe Referenzanalyse) C Modell vom Modell vorhergesagter Konzentrationswert der Probe i m Anzahl der Proben Test-Set-Validierung Ist eine ausreichende Anzahl an Kalibrationsproben vorhanden, so kann auch eine Test-Set- Validierung durchgeführt werden. Bei der Test-Set-Validierung teilt man den vorhandenen Datensatz in zwei Probensätze - einen für die Methodenentwicklung (Kalibrationsdatensatz) und einen für die anschließende Methodenbewertung (Test-Set). Die Teilung sollte so erfolgen, dass beide Datensätze etwa gleich groß sind und den gleichen Konzentrationsbereich
40 3 Stand des Wissens 3.2 Kalibrationsmethoden in der optischen Spektroskopie 29 abdecken. In Analogie zum RMSECV wird hier ein RMSEP-Wert berechnet. Dabei steht die Abkürzung RMSEP für Root Mean Square Error of Prediction: RMSEP = 1 m m i= 1 ( C Wahr C 2, i Modell, i ) (3.29) Durch den Wert RMSECV bzw. RMSEP kann eine Aussage über den absoluten Vorhersagefehler gemacht werden. Je geringer diese Werte sind, desto besser ist normalerweise die Konzentrationsvorhersage. Beide Werte besitzen dieselbe Einheit, wie sie auch bei der Kalibration zugrunde gelegt wird. Häufig ist dies die Analytkonzentration Externe Validierung Der externen Validierung kommt die größte Bedeutung zu, da hier das Modell erstmals in der Praxis bzw. im realen Betrieb überprüft wird. Dazu werden unbekannte Proben zunächst spektroskopisch vermessen, anschließend Konzentrationsvorhersagen mit der erstellten Kalibrationsmethode durchgeführt und diese mit einer geeigneten Referenzanalytik verglichen. Die externe Validierung sollte über einen längeren Zeitraum wiederholt und ggf. angepasst werden, um die Stabilität und Genauigkeit des Kalibrationsmodells in der Praxis zu gewährleisten. Auch hier wird ein RMSEP berechnet.
41 3 Stand des Wissens 3.3 Prozessverfolgung von Hefefermentationen Prozessverfolgung von Hefefermentationen Ziel einer Prozessverfolgung von Hefefermentationen ist die Beobachtung der Messgrößen wie Fermentationstemperatur, ph-wert, Begasungsrate, Rührerdrehzahl sowie die Konzentrationen der Edukte und Produkte. Durch die Messung der einzelnen Parameter können der Verlauf, die Qualität und der aktuelle Zustand des Prozesses beurteilt werden, was, sofern nötig, ein gezieltes Eingreifen in den Prozess ermöglicht. Die Auswahl der Messausstattung hängt von der Art des Fermentationsverfahrens ab. Mikroorganismen wie Hefen können z.b. unter Sauerstoffausschluss (anaerob) oder O 2 -Aufnahme (aerob) im Batch-Verfahren (Satzverfahren), Fed-Batch-Verfahren (Zulaufverfahren) oder im kontinuierlichen Betrieb kultiviert werden. Beim Batch-Verfahren verläuft die Fermentation satzweise und diskontinuierlich, d.h. es findet weder ein Zulauf an Substrat noch ein Ablauf an Produkt während der Fermentation statt. In einer Brauerei werden die Propagation der Bierhefe aerob und die anschließende Gärung anaerob im Satzbetrieb durchgeführt. Die Fed-Batch-Kultivierung unterscheidet sich vom Batchverfahren durch eine Zugabe an Substrat(en) während der Fermentation. Ein Vorteil der Fed-Batch-Fahrweise ist, dass zu Beginn der Fermentation hohe Substratkonzentrationen vermieden werden können, welche die Produktion von Ethanol begünstigen jedoch das Hefewachstum hemmen. In der Backhefeindustrie wird das Fed-Batch-Verfahren eingesetzt, weil durch die gezielte Substratzufuhr höhere Ausbeuten an Biomasse (Hefezellen) erreicht werden. Bei einem kontinuierlichen Betrieb wird dem Reaktor fortlaufend frisches Kulturmedium zugespeist und ein gleich großer Volumenstrom an Zellsuspension aus dem Reaktor abgeführt. Zellen können so über einen längeren Zeitraum unter gleichen Bedingungen kultiviert werden. Kontinuierliche Verfahren werden vor allem im Labor für die Erforschung der Kinetik und des Verhaltens eines biologischen Systems eingesetzt. In der Industrie wird diese Fahrweise relativ selten verwendet, da mit einem (Fed-)Batch-Prozess eine hohe Produktkonzentration meist kostengünstiger realisiert werden kann. Zusätzlich besteht bei kontinuierlichen Verfahren über längere Zeiträume die Gefahr von Kontaminationen. Für die Ausarbeitung und Validierung der in dieser Arbeit entwickelten Messmethoden wurde der Batch-Betrieb verwendet, da hierbei mögliche Störeinflüsse durch den Substratzulauf (z.b. Kontaminationen) ausgeschlossen werden konnten. Im Fermentationsmedium ist eine hohe Zuckerkonzentration als C-Quelle vorgelegt worden, sodass aufgrund des Crabtree- Effektes während der Fermentationen neben Biomasse auch Ethanol produziert wurde.
42 3 Stand des Wissens 3.3 Prozessverfolgung von Hefefermentationen Stoffwechselvorgänge bei der Kultivierung von Hefen Die Stoffwechselvorgänge von Hefen sind von der Fahrweise der Fermentation abhängig. Unter anaeroben Bedingungen können Hefezellen nur bedingt Zellteilung durchführen, da sie zur Synthese von ungesättigten Fettsäuren und Steroiden Sauerstoff benötigen. Aus der C- Quelle Glucose werden hauptsächlich Ethanol und CO 2 gebildet. Der Großteil der C-Quelle dient der Energiegewinnung [32]. Unter aeroben Bedingungen (Atmung) kann eine vollständige Oxidation der C-Quelle zu CO 2 und Wasser erfolgen. In der Glykolyse (auch Fructose-diphosphat-Weg genannt) werden Hexosen zu Pyruvat abgebaut. Anschließend finden der Citratzyklus und die oxidative Phosphorylierung in der Atmungskette statt. Durch ein Überangebot an Glucose (Glucosekonzentrationen >100 mg / L) zu Beginn der Fermentation wird trotz des zugeführten Sauerstoffs zusätzlich Ethanol gebildet (Crabtree- Effekt). Die Ethanolbildung erfolgt ausgehend von dem in der Glykolyse hergestellten Pyruvat. Die Reaktion wird zunächst von der Pyruvat-Decarboxylase katalysiert, welche aus Pyruvat CO 2 und Acetaldehyd herstellt. Der Acetaldehyd wird anschließend mittels Alkohol- Dehydrogenase (ADH, Isoenzym I) zu Ethanol reduziert. Ist die Glucose verbraucht, nutzt die Hefe das Ethanol als C-Quelle (diauxisches Wachstum). Dazu wird Ethanol zunächst durch ADH (Isoenzym II) zu Acetaldehyd oxidiert. Anschließend wird der Acetaldehyd mittels Aldehyd-Dehydrogenase zu Acetat oxidiert. Das gebildete Acetat wird durch das Enzym Acetyl-CoA-Synthetase zu Acetyl-CoA aktiviert und als solches in den Citratzyklus transferiert. Während der Umstellung der Hefe von Glucoseabbau zu Ethanolabbau (Diauxic Shift) werden die zuvor transkribierten Gene für Glykolyse und Proteinbiosynthese abgeschaltet und im Gegenzug die Gene aktiviert, welche die Produkte für Atmung, Mitochondrienwachstum und Citratzyklus liefern [33, 34] Sensorsysteme für die Bioprozessanalytik Eine zeitnahe Prozessüberwachung ist von grundlegender Bedeutung für eine gute Prozessregelung. In den letzten Jahren ist eine rasante Entwicklung von neuen Sensoren zu beobachten, die in der Lage sind, Informationen in Echtzeit (in-situ) über den biotechnologischen Prozess zu liefern. Es handelt sich dabei um sogenannte in-line und on-line Messsysteme. In-line Sensoren werden direkt in den Prozess installiert, während bei einer on-line Messung die Sensoren in einem Bypass-Strom des Reaktors untergebracht sind. Bei off-line
43 3 Stand des Wissens 3.3 Prozessverfolgung von Hefefermentationen 32 Analysen werden Proben aus dem Fermenter gezogen. Falls die Probenmessung unmittelbar nach der Probennahme erfolgt, wird dies auch als at-line Analyse bezeichnet. Bei Bioprozessen werden neben Fermentationstemperatur, ph-wert, Begasungsrate, Rührerdrehzahl und Flüssigkeitsniveau häufig auch die Konzentrationen von O 2 und CO 2 in der Flüssigphase in-line verfolgt. Im Fall einer aeroben Fermentation werden in der Regel die Konzentrationen an O 2 und CO 2 in der Gasphase on-line gemessen, um aus diesen Werten z.b. den Respirationskoeffizienten bestimmen zu können. Für die oben genannten Kontrollvariablen sind bereits Sensoren auf dem Markt vorhanden, welche die erforderlichen Spezifikationen besitzen und sich daher in der Praxis bewährt haben. Bei den Messtechniken für die in-line und on-line Analyse der Zusammensetzung des Fermentationsmediums besteht weiterhin Entwicklungsbedarf, da die Instrumente nicht alle notwendigen Anforderungen wie Robustheit, Empfindlichkeit, Genauigkeit, Selektivität, Reproduzierbarkeit und kurzes Ansprechverhalten aufweisen Temperatur und ph-wert Eine der wichtigsten Prozessvariablen bei der Kultivierung von Mikroorganismen ist die Temperatur, welche für einen optimalen Fermentationsverlauf geregelt werden muss. Im Labor und in der Produktion werden vorwiegend Platin-Widerstandsthermometer Pt-100 (Widerstand 100 Ohm bei 0 C) mit einer Genauigkeit von ± 0,1 C für die Temperaturmessung in der Fermentationsbrühe eingesetzt [35]. Einen weiteren Einfluss auf das Wachstum und im Allgemeinen auch auf die metabolische Aktivität der Mikroorganismen hat der ph-wert des Mediums. Dieser muss für ein optimales Zellwachstum durch eine Säure- bzw. Alkalizugabe auf einem definierten Wert gehalten werden. Gemessen wird der ph-wert üblicherweise mit einer Silber-Silberchlorid-Elektrode, wobei das auf der Glasmembran gemessene Potential vom ph-wert der Probe abhängt. Weitere ph-meter sind die ph-optoden, bei denen der ph-wert über die Fluoreszenz eines mit UV-Licht angeregten ph-sensitiven Fluorophors oder Luminophors gemessen wird. ph-optoden besitzen jedoch in der Regel den Nachteil, dass sie nur für einen engen Betriebsbereich eingesetzt werden können und die Indikatoren beim Autoklavieren ihre Sensitivität verlieren [3, 31] Begasungsrate und Rührerdrehzahl Für aerobe Fermentationen ist die Begasungsrate eine wichtige Steuergröße zur Regelung des Gelöst-Sauerstoff-Eintrags. Der Volumenstrom der Gasströmung wird in der Biotechnologie mittels thermischer Durchflussmesser mit einer Genauigkeit von ± 2 % bestimmt [31]. Diese bestehen prinzipiell aus einem Rohr mit einer Heizspirale und zwei Temperatursensoren, mit denen die Temperatur des strömenden Gases vor und nach Aufheizen durch die
44 3 Stand des Wissens 3.3 Prozessverfolgung von Hefefermentationen 33 Heizspirale gemessen wird. Anhand des Temperaturunterschieds und bekannter Wärmekapazität sowie Dichte des Gases kann der Volumenstrom berechnet werden. Einen erheblichen Einfluss auf die Durchmischung sowie den Sauerstoff- und Wärmeeintrag in das Medium hat die Drehzahl des Rührers. Diese wird in der Industrie am häufigsten durch einen Wirbelstromdrehzahlmesser (Genauigkeit ± 1 %) kontrolliert. Die Überwachung des Flüssigkeitsniveaus im Reaktor ist vor allem bei einem Fed-Batch Betrieb sinnvoll, da so der Substratzulauf am Fermenter verfolgt und ein Überlaufen vermieden werden kann. Das Flüssigkeitsniveau und -gewicht kann bei Laboraufbauten z.b. mittels Differenzwägung (Genauigkeit ± 1%) bestimmt werden. Bei größeren Reaktoren muss der Füllstand mithilfe anderer Sensoren (Ultraschall, etc.) bestimmt werden Gelöst-Sauerstoff- und Gelöst-Kohlendioxidkonzentration Neben Temperatur und ph-wert beeinflussen die Gelöst-Sauerstoffkonzentration (po 2 ) sowie die Gelöst-Kohlendioxidkonzentration (pco 2 ) das Zellwachstum und die Produktbildung. Beide Parameter können in-situ verfolgt werden. Die Gelöst-Sauerstoffkonzentration wird meistens amperometrisch mit einer Clark-Elektrode gemessen, welche mit Edelmetall- Kathode und einer Anode in Elektrolytlösung sowie einer sauerstoffdurchlässigen Teflonmembran zur Trennung der flüssigen Probenlösungen ausgestattet ist. Der durch die Membran diffundierende Sauerstoff wird mittels externer Spannungsquelle an der Kathode reduziert, wobei OH - -Ionen entstehen. Dabei fließt ein Strom I, welcher dem Partialdruck po 2 des Sauerstoffs direkt proportional ist. Die Silber-Anode wird zu Silberionen oxidiert und bei Anwesenheit von Chlorid als unlösliche AgCl-Kruste an die Elektrode angelagert. Dies erfordert nach gewisser Betriebsdauer einen Ersatz der Anode. Bevor die Clark-Elektrode eingesetzt werden kann, muss die Elektrolytlösung für mehrere Stunden polarisiert werden. Aufgrund der zeitlichen Signaldrifts der Elektrode sind Kalibrierungen öfter notwendig [35]. Neuerdings werden auch optische Sensoren (Optoden) zur Messung der Konzentration des Gelöst- Sauerstoffes verwendet. Der optische po 2 -Sensor Visiferm DO von der Firma Hamilton besteht z.b. aus zwei Photodioden und aus einer blauen LED, welche auf einen Luminophor strahlt. Durch die Anregung mit blauem Licht werden Elektronen des Luminophors auf ein höheres Energieniveau gepumpt und fallen unter Abstrahlung roten Lichts (Fluoreszenz) wieder auf ihr Ursprungsniveau ab. Ist der Luminophor in Kontakt mit Sauerstoff, so absorbieren die O 2 -Moleküle die erhöhte Elektronenenergie, wodurch das rote Licht mit schwächerer Intensität abgestrahlt wird (Fluoreszenzlöschung). Eine Photodiode überwacht den Zustand der LED, die andere mit rotem Bandpassfilter misst das sauerstoffabhängige rote Fluoreszenzlicht. Vorteile der optischen po 2 -Sensoren gegenüber der Clark-Elektrode sind die schnelle Einsatzfähigkeit sowie die geringe Wartung. Jedoch ergänzen sich diese beiden Methoden sehr gut, da elektrochemische Sensoren die beste Leistung bei hohen Sauerstoff-
45 3 Stand des Wissens 3.3 Prozessverfolgung von Hefefermentationen 34 konzentrationen besitzen, während optische Sensoren optimal bei niedrigeren Konzentrationen (in der Regel 50 % der Sättigung) arbeiten. Ein weiterer Unterschied besteht darin, dass, im Gegensatz zu optischen Sensoren, elektrochemische Sensoren aktiv Sauerstoff verbrauchen [3]. Nachteil der optischen po 2 -Sensoren ist das Photobleichen des Luminophors, welches sich negativ auf die Langzeitstabilität auswirkt. Die Messung der Gelöst-CO 2 -Konzentration erfolgt über eine ph-elektrode, die in einer HCO - 3 -Lösung eingetaucht und vom Fermentationsmedium durch eine CO 2 -durchlässige Membran getrennt ist. CO 2 diffundiert durch die Membran in den inneren Elektrolyt, wo der ph-wert gemäß dem Gleichgewicht mit Hydrogenkarbonat verändert wird (Severinghaus- Prinzip). Die ph-wert-veränderung wird durch die einfach auszuwechselnde ph-elektrode gemessen. Da die Gleichgewichtseinstellungen zwischen Carbonatpuffer und Medium durch die Membran langsam ablaufen, liegen die Ansprechzeiten dieser Sensoren im Bereich von Minuten. Seit kurzer Zeit sind neue CO 2 -Sensoren auf dem Markt, die sowohl für Gas- als auch für Flüssigkeitsmessungen geeignet sind. Diese arbeiten wie die amperometrischen Sensoren nach dem Severinghaus-Prinzip, jedoch wird der ph-wert optisch über Fluoreszenzlöschung gemessen. Leider besitzen Sensoren für gelöstes Kohlendioxid nach dem Severinghaus-Prinzip den Nachteil, dass die Sterilisation der Elektrode und des Elektrolytpuffers die Sensitivität verringert [3]. Weiterhin müssen der Carbonatpuffer häufig aufgrund der Ionenstärkeabhängigkeit der optischen ph-messung ausgetauscht und die Sensoren oft rekalibriert werden [31, 36] Zelldichte und Biomasse Die Biomasse bzw. die Zelldichte gehört zu den bedeutenden Messgrößen einer Fermentation. Direkte Informationen über das Zellwachstum können entscheidend für die Kultivierung von Bakterien, Hefen und tierischen Zellkulturen sein. Im Fed-Batch-Betrieb ist die Messung der Zelldichte oft notwendig, um die Substratzufuhr für eine optimale Kultivierung zu regeln. Die klassischen off-line Referenzverfahren der Biomasse- bzw. Zellzahl-Bestimmung sind die Trocknung und anschließende Ermittlung des Zelltrockengewichtes durch Wägung sowie die Zählung unter dem Mikroskop in einer Neubauer- bzw. Thoma-Zählkammer. Beide Methoden sind aufgrund des präparativen Aufwands sehr zeitaufwendig, jedoch liefert insbesondere die Ermittlung des Zelltrockengewichtes durch Trocknung die zuverlässigsten Resultate. Die am häufigsten eingesetzten in-situ Sensoren für die on-line Bestimmung von Zelldichten basieren auf optischen Verfahren wie Nephelometrie, Turbidimetrie und/oder Rückstreumessungen. Die Vorwärtsstreuung (Nephelometrie) liefert die größte Empfindlichkeit (linearer Messbereich bei Hefezellen zwischen 10 2 bis 10 5 Hefezellen / ml), während im mittleren
46 3 Stand des Wissens 3.3 Prozessverfolgung von Hefefermentationen 35 Zelldichtebereich (10 5 bis 10 7 Hefezellen / ml) die Transmissionsmessung (Turbidimetrie) die Methode der Wahl ist. Die 180 -Rückstreumessung kann für quantitative Analysen im oberen Zelldichtebereich (10 7 bis Hefezellen / ml) herangezogen werden [37]. Aufgrund der Querempfindlichkeit gegenüber Luftblasen und Partikeln sowie der Problematik mit dem Sondenbewuchs ist der Einsatz von optischen Sensoren für die Biomassebestimmung in der Industrie limitiert. Neben optischen Sensoren werden elektro-chemische Verfahren, welche auf die Veränderung von Kapazität, Leitfähigkeit oder Dielektrizität des Fermentationsmediums durch das Zellwachstum beruhen, für die Biomassebestimmung eingesetzt. Mit der Messung des kapazitiven Widerstands lassen sich recht genaue Aussagen über die Biomassekonzentration machen [31]. Nachteilig sind jedoch die hohen Investitionskosten sowie die Querempfindlichkeit gegenüber der Mediumzusammensetzung. Dagegen erlauben die elektro-chemischen Sensoren im Gegensatz zu den optischen Verfahren, zwischen Zellen und suspendierten Feststoffteilchen zu unterscheiden. Besonders vielversprechend für die Überwachung von Zelldichten im Labor sind In-situ- Mikroskope [31, 38]. Durch die Auswertung der in-line aufgenommenen Bilder mit Bildverarbeitungsalgorithmen werden direkte und indirekte Zellparameter in Echtzeit ermittelt und stehen so einer Prozessregelung zur Verfügung. Aufgrund der fortlaufenden Entwicklung von leistungsfähigeren und günstigeren elektronischen Komponenten werden diese Geräte immer preiswerter. Leider ist bei den kommerziellen In-situ-Mikroskopen die Auflösung limitiert, sodass sich z.b. bakterielle Kulturen nur schwer analysieren lassen Zusammensetzung der Fermentationsbrühe In den letzten Jahren wird die Zusammensetzung des Fermentationsmediums immer häufiger nicht nur im Labor sondern auch in der Industrie mittels NIR- und FT-MIR-Spektrometern in-line oder on-line verfolgt. Die NIR- und MIR-Spektroskopie liefern eine große Bandbreite an Informationen über die Zusammensetzung des Mediums [5, 39, 40]. Zucker wie Saccharose, Glucose und Fructose sowie Ethanol, Di-Ammoniumsulfat, Glutamin, Glutamat, Prolin, Kohlendioxid und Phosphat können u.a. gemessen werden. Allerdings stehen die hohen Kosten und die komplexe Kalibrierung einer weiten Verbreitung dieser Methoden in der Industrie entgegen. Da die IR-Spektroskopie ein großes Potenzial für die Echtzeit- Überwachung einer Vielzahl von Bioprozessen bietet, wird sie insbesondere im Laboratorium für die Erforschung der Kinetik und des Verhaltens von biologischen Systemen eingesetzt. Anstatt mikrobiologische Prozesse mit Spektrometern zu verfolgen, kann dies auch durch den Einsatz von photometrischen Sensoren erfolgen. Photometrische Sensoren besitzen optische Bandpassfilter in Spektralbereichen, die spezifisch für die jeweiligen zu analysierenden Komponenten sind. Im Vergleich zu Spektrometern besitzen Photometer neben den
47 3 Stand des Wissens 3.3 Prozessverfolgung von Hefefermentationen 36 geringen Investitionskosten den Vorteil, dass sie aufgrund der Kompaktheit ohne technische Schwierigkeiten an den Bioreaktoren für eine on-line Überwachung von mikrobiologischen Prozessen angeschlossen werden können. Photometrische Sensoren werden in der Industrie u.a. für die Verfolgung der CO 2 -Konzentration im Fermentationsabgas eingesetzt. Die genaueste und empfindlichste Nachweismethode zur Bestimmung der Inhaltstoffe von Fermentationsbrühen wie Zucker und Ethanol ist die Chromatographie [42, 43]. Nachteile dieser Methode sind die hohen Kosten, die Notwendigkeit einer Probenvorbehandlung und die langen Messzeiten. Die Entwicklung eines on-line HPLC (High Perfomance Liquid Chromatography) Systems mit automatischer Probennahme, Filtration, Verdünnung sowie Probeninjektion für die Analyse von Glucose und Ethanol in der Fermentationsbrühe wird z.b. in [43] vorgestellt. Die langen Retentionszeiten der Chromatographie erlauben jedoch nur eine on-line Verfolgung in Messintervallen von 5 bis 20 Minuten. Schnellere Messungen, wenn auch etwas weniger präzise, werden durch die Verwendung von Biosensoren erreicht. Sie bestehen aus einer biologischen Komponente (Signalgeber z.b. ein Enzym, ein Antikörper oder ein Mikroorganismus), welche auf einem festen Träger immobilisiert ist und mit einem Analyten in der zu untersuchenden Probe direkt reagiert. Durch diese Reaktion kommt es in der Probe zur Veränderung einer physikalischen oder chemischen Größe (z.b. ph-wert, Leitfähigkeit, po 2 ), die mit einem Signalwandler (Transducer) wie z.b. einer Elektrode, einer Photodiode, einem Piezokristall oder einem Transistor registriert und in ein auswertbares Signal umgewandelt werden kann. Für die enzymatische Ethanol-Bestimmung wird u.a. das Enzym Alkohol-Oxidase verwendet, welches unter Sauerstoffverbrauch aus dem Ethanol Acetaldehyd und H 2 O 2 bildet. Der O 2 -Verbrauch oder die H 2 O 2 -Bildung wird gemessen und hieraus die Ethanolkonzentration bestimmt [44, 45]. Mit dem Enzym Alkohol-Dehydrogenase entsteht aus Ethanol Acetaldehyd und NADH. Anhand von NADH-Fluoreszenzmessungen kann ebenfalls auf den Ethanolgehalt geschlossen werden. Biosensoren besitzen eine hohe Spezifität und finden daher häufig Anwendung bei der Detektion spezieller Biomoleküle (z.b. Glucose, Fructose, Ethanol, Harnstoff und Lactat) sowie zur Erkennung spezifischer Proteine in komplexen biologischen Systemen. Als nachteilig erweist sich allerdings die geringe Stabilität der biologischen Komponenten bei längeren Messungen, sodass die Biosensoren ständig nachkalibiert werden müssen. Der Einsatz von In-situ Biosensoren ist dadurch limitiert, dass die biologische Komponente nicht autoklavierbar ist.
48 3 Stand des Wissens 3.4 Getränkeanalytik Getränkeanalytik Fruchtsäfte und Softdrinks (Cola, Limonade etc.) bestehen hauptsächlich aus Wasser und Zucker (Mischung aus Saccharose, Fructose und Glucose), wobei Bier und Bier-Mix- Getränke neben Zucker auch Ethanol und unvergorenen Restextrakt beinhalten. In den folgenden Abschnitten werden die chemischen Zusammensetzungen von Obst und Fruchtsäften, Softdrinks und Bier bzw. Bier-Mix-Getränke sowie die zugehörigen analytischen Verfahren vorgestellt. Aufgrund von gesetzlichen Vorgaben zur Qualitätsüberwachung von Lebensmitteln werden in der Getränke- und Brauindustrie die Produkte off-line im Labor und on-line im Betrieb analysiert. Da eine Vielzahl an verschiedenen Getränken auf dem Markt vorhanden ist, werden für jede Getränkeart unterschiedliche Messmethoden eingesetzt. Um z.b. Kontaminationen des Produktes festzustellen, werden mikrobiologische Untersuchungen angewendet [57]. Neben allgemeinen Parametern wie Dichte, ph-wert, Wassergehalt bzw. Trockensubstanzgehalt, Glührückstand, Rohfaser- oder Ballaststoffgehalt werden in den Lebensmitteln weiterhin die Inhaltsstoffe wie Fette, Proteine, Kohlenhydrate, Alkohole und Säuren analysiert. Bei der Referenzmethode für die Fettbestimmung in Lebensmitteln werden die homogenisierten Proben mit Salzsäure aufgeschlossen und das Fett durch Filtration abgetrennt (Soxhlet-Verfahren). Nach Waschung mit neutralem Wasser und anschließender Trocknung wird der Filterrückstand in einer Soxhlet-Apparatur extrahiert. Der getrocknete Extraktrückstand wird ausgewogen [56]. Zur analytischen Erfassung des Gesamtprotein- oder Rohprotein-Gehaltes wird in der Regel der Stickstoffanteil nach dem Aufschluss der Probe mit Schwefelsäure nach dem Kjeldahl- Verfahren bestimmt [56]. Die organischen Anteile der Probe werden dabei entfernt und der Stickstoff in Ammoniumsulfat umgewandelt. Die Zugabe einer starken Base setzt Ammoniak frei, das in Säure aufgefangen und durch Titration bestimmt wird. Mit folgenden nasschemischen Tests können spezielle Eiweißverbindungen in den Proben nachgewiesen werden: Biuret-Reaktion: Polypeptide reagieren mit verdünnter Kupfersulfat-Lösung in stark alkalischem Milieu und zeigen eine charakteristische Blaufärbung. Ninhydrin-Reaktion: α-aminosäuren (mit primären Aminogruppen) reagieren mit Ninhydrin unter Bildung eines Farbstoffes, der blauviolett bis rotbraun gefärbt ist. Xanthoprotein-Reaktion: Aus aromatischen Aminosäuren bilden sich bei Zusatz von konzentrierter Schwefelsäure gelb gefärbte Nitroderivate.
49 3 Stand des Wissens 3.4 Getränkeanalytik 38 Bleisulfid-Reaktion: Eine Schwarzfärbung zeigt sich bei Zusatz von Bleiacetat-Lösung und Anwesenheit von schwefelhaltigen Eiweißverbindungen im stark alkalischen Milieu. Für die Bestimmung von Kohlenhydraten in Lebensmitteln existiert eine Vielzahl an Messmethoden, deren Genauigkeiten u.a. von der Probenzusammensetzung abhängen und sehr unterschiedlich sein können. Die wichtigsten Verfahren sind: Chromatographie Polarimetrie Oxidation der Aldehyd-/Ketogruppe Enzymatische Verfahren Spektroskopische und photometrische Methoden Alkohole wie Methanol, Ethanol bis hin zu den Pentaolen werden vor der Analyse üblicherweise mit einem Destillationsverfahren aus dem Probenmaterial getrennt. Je nach Erfordernis werden anschließend der Gesamtalkohol oder Einzelkomponenten bestimmt. Zur Trennung der Komponenten werden Gas- und/oder Flüssigkeitschromatographie eingesetzt. Eine weitere Methode ist die enzymatische Alkoholbestimmung, mit der kürzere Messzeiten möglich sind [56]. Eine Alternative zu den herkömmlichen nasschemischen im Labor durchgeführten Analysenmethoden für die Beurteilung und die Kontrolle von Lebensmitteln wie Obst und Getränke ist die IR-Spektroskopie. In den letzten Jahren sind mehrere IR-spektroskopische Messverfahren entwickelt worden, welche u.a. in der Agrar- und Ernährungsindustrie eingesetzt werden können [48, 49, 50, 51, 52, 53, 54]. Diese Methoden bieten die Möglichkeit, in kurzer Zeit mehrere Eigenschaften der Probe oft zerstörungsfrei und mit minimaler Probenvorbereitung zu messen. Die Zuckerkonzentrationen in Apfel-, Trauben-, Aprikosen- und Mangosaft konnten mithilfe der FT-MIR-ATR-Spektroskopie und multivariater Analysen quantifiziert werden [48, 49, 50, 51]. Die Ethanolkonzentration, Gelöst-CO 2 und Kohlenhydratgehalte von unterschiedlichen Biersorten lassen sich per faseroptische Diamant-ATR-Sonde und einem FT-MIR-Spektrometer in-line in den Bierflaschen messen [54].
50 3 Stand des Wissens 3.4 Getränkeanalytik Chemische Zusammensetzung von Getränken Obst und Fruchtsäfte Als Obst werden Früchte bzw. Scheinfrüchte sowie Samen kultivierter und wildwachsender, mehrjähriger Pflanzen bezeichnet, die für die menschliche Ernährung geeignet sind und zum größten Teil roh verzehrt werden [46]. In der Praxis erfolgt eine Einteilung in Kernobst (z.b. Äpfel, Birnen), Steinobst (z.b. Pflaumen, Kirschen), Beerenobst (z.b. Weintrauben, Johannisbeeren), Südfrüchte (Zitrusfrüchte, Bananen), Wildfrüchte (z.b. Holunder, Hagebutte) und Schalenobst (Nüsse, Mandeln, Kastanien). Schalenobst weicht von den Inhaltsstoffen her stark von anderen Obstsorten ab. Die Hauptbestandteile in Obst sind Wasser, Zucker, Polysaccharide, organische Säuren sowie Rohfaser (Cellulose). Der Gehalt an Proteinen und Lipiden kann bis auf einige Ausnahmen (z.b. bei Schalenobst) vernachlässigt werden. In geringeren Konzentrationen kommen Pflanzenphenole sowie bestimmte Farbstoffe, Aromastoffe, Mineralien und Vitamine vor. Der Wassergehalt liegt je nach Art bei 75 bis 90 Gew.-% [47]. Bei Schalenobst liegt der Wassergehalt unter 10 %, der Gehalt an Stickstoffverbindungen um 20 % und der an Lipiden um 50 % [55]. Je nach Obstsorte, Lage, Witterung und Einlagerung kann die Zusammensetzung stark schwanken. Der Wassergehalt kann um ± 15 % variieren, und die Konzentrationen an Zucker das Drei- bis Siebenfache des niedrigsten Wertes erreichen [46]. Die folgenden Werte können deshalb nur zur Orientierung dienen. Eine Übersicht wichtiger Inhaltsstoffe in einigen ausgewählten Obstarten findet sich in der Tabelle 3.2. Tabelle 3.2: Inhaltstoffe von ausgewählten Obstarten in Gew.-% [46] in Gew.-% Kohlen Wasser -hydrate Eiweiß Fett Roh Mineral- Gesamt -faser stoffe -säure Apfel 85,3 11,9 0,3 0,4 2,3 0,3 0,7 Pflaume 83,7 11,9 0,6 0,2 1,7 0,5 1,4 Johannisbeeren, rot 84,7 7,9 1,1 0,2 3,5 0,6 2,4 Wallnüsse 4,4 12,1 14,4 62,5 4,6 2,0 x Orangen 85,7 9,5 1,0 0,2 2,2 0,5 x In unreifen Früchten findet man als Kohlenhydrate hauptsächlich Stärke, die mit zunehmendem Reifegrad zu Glucose, Fructose und Saccharose umgewandelt wird. Einige Früchte wie Weintraube und Brombeere enthalten Saccharose nur in geringen Mengen, wohingegen z.b. in Ananas und Pfirsich Saccharose den größeren Anteil an Zuckern ausmacht. Organische Säuren wie Zitronen-, Essig-, L-Apfelsäure und L-Lactat sind in den meisten Obstsorten vertreten. Im Durchschnitt liegt der Säuregehalt bei 1,0 Gew.-%. Höhere Konzentrationen an Säure besitzen Zitronen (4,9 Gew.-%), Johannisbeeren (2,5 Gew.-%)
51 3 Stand des Wissens 3.4 Getränkeanalytik 40 und Sauerkirschen (1,8 Gew.-%). In Tabelle 3.3 sind für ausgewählte Obstsorten die Anteile an Glucose, Fructose, Saccharose und organischen Säuren aufgelistet. Tabelle 3.3: Zuckerzusammensetzung und Säuregehalt in Gew.-% von ausgewählten Obstsorten [46, 47, 55] in Gew.-% Glucose Fructose Saccharose organische Säuren Ananas 2,3 2,4 7,9 x Apfel 2 5,7 2,5 0,46 Apfelsine 2,4 2,4 3,4 x Aprikose 1,7 0,9 5,1 1,4 Banane 3,5 3,4 10,3 x Birne 1,7 6,7 1,8 0,31 Brombeere 3 3,1 0,2 1,73 Erdbeere 2,2 2,3 1 1,05 Heidelbeere 2,5 3,3 0,2 1,37 Himbeere 1,8 2,1 1 2,12 Johannisbeere (rot) 2 2,5 0,3 2,37 Johannisbeere (schwarz) 2,3 3,1 0,7 2,63 Orange 2,3 2,5 3,5 x Pfirsich 1 1,2 5,7 0,57 Pflaume 3,4 2 3,4 1,25 Sauerkirsche 5,2 4,3 0,4 1,8 Süßkirsche 6,9 6,1 0,2 0,95 Weintraube 7,2 7,4 0,4 0,35 Zitrone 1,4 1,4 0,4 4,9 Fruchtsäfte sind flüssige Auszüge aus frischem Obst, welche durch mechanische Verfahren gewonnen werden. Um Transportkosten zu sparen, werden sie häufig mittels spezieller Verdampfer konzentriert, wobei die über Kolonnenkopf abdestillierten Aromastoffe kondensiert und dem Konzentrat wieder zugefügt werden. Vor allem Orangensäfte werden im Erzeugerland konzentriert und im Verbraucherland mit Wasser wieder auf die ursprüngliche Konzentration rückverdünnt. Geschmackskorrekturen mit Zucker sind gesetzlich geregelt. Vor oder bei Abfüllung werden die Säfte pasteurisiert. Der Gehalt an zugesetztem Zucker darf 20 Gew.-% des Gesamtgewichts nicht übersteigen. Säfte ohne Korrekturzuckerzusätze werden durch den Aufdruck Ohne Zuckerzusatz gekennzeichnet. Dieser Hinweis auf den Verpackungen ist freiwillig und bedeutet, dass wirklich nur Fruchtzucker und kein zusätzlicher Zucker im Saft enthalten ist Softdrinks (Cola, Limonade etc.) Diese Produkte werden aus Trinkwasser, Mineral-, Quell- oder Tafelwässern durch Zusatz von Fruchtsaft, Frucht- und Genusssäuren oder sonstigen Zusätzen hergestellt. Dazu werden die Ingredienzien als Sirup entweder in die Flasche vordosiert und mit kohlensäurehalti-
52 3 Stand des Wissens 3.4 Getränkeanalytik 41 gem Wasser aufgefüllt oder die beiden Anteile werden kontinuierlich vorgemischt (Intermix- Verfahren) und als fertiges Getränk in die Flasche gefüllt. Der Alkoholgehalt muss unter 0,5 Vol.-% liegen. Softdrinks bestehen zu ca. 99 Gew.-% aus Wasser und Zucker. Die restlichen ein Prozent sind Säuren wie Zitronen- bzw. Phosphorsäure (im Durchschnitt 0,05 Gew.-%), Kohlensäure, Aroma- und Farbstoffe, zudem Koffein jedoch nur in Softdrinks wie Cola. Die Gesamtzuckerkonzentration beträgt zwischen 10 und 11 Gew.-%, wobei der Zucker als Mischung aus Saccharose, Fructose und Glucose vorliegen kann. Die Zusammensetzung der Zucker kann je nach Hersteller und Produktionsland variieren. Rohrzucker wird meistens in Asien und Rübenzucker in Europa verwendet. Diese Sorten beinhalten hauptsächlich Saccharose. In den USA wird vorwiegend Maissirup, welcher ungefähr zur Hälfte aus Fructose und Glucose besteht, für das Zuckern von Softdrinks eingesetzt. Ein besonderes Produkt ist Coca Cola Zero, welches anstelle des Zuckers Süßstoffe enthält Bier, Radler und Cola-Bier Bier wird aus Hopfen, gemälztem Getreide, Hefe und Wasser hergestellt. Bezüglich der eingesetzten Hefesorte wird unterschieden zwischen untergärigen und obergärigen Biersorten. Beispiele für untergärige Biere sind Pils, Märzen, Helles, Lager, Export und Schwarzbier. Hier liegt die Hefe während des Brauprozess am Boden bei Fermentationstemperaturen von 5 bis 9 C. Obergärige Hefen werden bei höheren Temperaturen (15 bis 20 C) eingesetzt und bilden während der Fermentation Sprossverbände, sodass sie an der Oberfläche schwimmen. Beispiele für obergärige Biere sind Weizenbier (in Bayern auch als Weißbier bezeichnet), Kölsch, Alt, Stout und Berliner Weiße. Nach dem 1516 zuerst in Bayern erlassenen Reinheitsgebot, das von der deutschen Lebensmittelgesetzgebung übernommen wurde, dürfen untergärige Biere nur Gerstenmalz als Ausgangsmaterial für Alkohol enthalten. Neben Ethanol (ca. 4 Gew.-% je nach Biersorte) und gelöstem CO 2 (0,5 Gew.-% bei Pilsner Flaschenbier und bis zu 1,0 Gew.-% bei Weizenbier) beinhaltet Bier unvergorenen Restextrakt (ca. 3,5 Gew.-% je nach Biersorte), welcher den Gehalt der übrigen gelösten Stoffe im Bier darstellt. Der unvergorene Restextrakt von Bier besteht überwiegend aus Dextrinen. Diese sind aus mehreren Glucosemolekülen langkettig aufgebaut, wobei Dextrine eine Vielzahl von unterschiedlichen Kettenlängen besitzen können. Eine detaillierte Zusammensetzung von Bier ist im Anhang in Tabelle 8.1 und Tabelle 8.2 zu finden. In Deutschland richten sich die Bezeichnungen der Biere und die gesetzliche Biersteuer nach ihren Stammwürzegehalten (Stw). Sie betragen (Angaben in Gew.-%) für
53 3 Stand des Wissens 3.4 Getränkeanalytik 42 Einfachbiere 2 bis 5,5 % Vollbiere 11 bis 14 % Schankbiere 7 bis 8 % Starkbiere 16% und höher Die Stammwürze ist der Anteil an aus Malz und Hopfen gelösten Stoffen in der noch unvergorenen Würze, welche insbesondere aus Malzzucker, und in geringeren Mengen aus Eiweiß, Vitaminen, Mineralien und Aromastoffen besteht. Je höher der eingesetzte Stammwürzegehalt, desto größer ist die Ethanolkonzentration im Bier. Der Stammwürzegehalt wird im fertigen Bier nach den ASU-Methoden (Destillations- bzw. Refraktometer- Methode) durch Rückrechnung aus dem vorhandenen Alkohol- und dem unvergorenen Extraktgehalt nach der für ober- und untergärige Biere einheitlichen Balling-Formel ermittelt: Stw A E 100 Stw = 100 ( 2,0665 A + E) + ( 1,0665 A) in Gew.-% (3.30) der im nicht vergorenen Bier enthaltene ursprüngliche Stammwürzeextrakt in Gew.-% bzw. Grad-Plato oder Grad-Oechsle-Wert bei Bier-Mix-Getränken der im fertigen Bier enthaltene Ethanolgehalt in Gew.-% der im fertigen Bier enthaltene nicht vergorene Stammwürzeextrakt (Restextrakt) in Gew.-% Aus dem Restextrakt und ursprünglicher Stammwürze kann der Vergärungsgrad des Bieres berechnet werden [59]: ( Stw E) VG = in % (3.31) Stw Die Alkoholgehalte in Bier liegen für Vollbiere bei 3,5 bis 4,5 Gew.-% (4,5 bis 5,5 Vol.-%) und für Starkbiere bei 5 bis 5,5 Gew.-% (6 bis 6,5 Vol.-%). Alkoholfreie Biere dürfen nach deutschem und Schweizer Lebensmittelrecht maximal 0,5 Vol.-% Alkohol enthalten, jedoch sind die Konzentrationen meist geringer. Bier-Mix-Getränke wie Radler, Cola-Bier oder Alsterwasser sind Mischungen aus Bier und anderen Getränken. Meist werden Softdrinks wie Cola oder Limonade sowie Fruchtsäfte beigemischt. In der Regel bestehen sie zu mindestens 50 % aus Bier.
54 3 Stand des Wissens 3.4 Getränkeanalytik Analytische Verfahren Obst und Fruchtsäfte Zur Bestimmung einzelner wichtiger Inhaltsstoffe von Früchten und den verarbeiteten Obstprodukten stehen eine Reihe von Methoden aus der amtlichen Sammlung von Untersuchungsverfahren nach 64 LFGB (ASU) sowie die Analysenmethoden der Internationalen Fruchtsaftunion (IFU) zur Verfügung. In der Forschung werden Aromakomponenten hauptsächlich mittels Gaschromatographie (GC), Vitamine und sekundäre Pflanzeninhaltsstoffe meistens mittels Hochleistungsflüssigchromatographie (HPLC) untersucht [47, 56]. Weiterhin werden in Geräten wie dem CL-10 Plus der Firma BioControl Systems enzymatische Messmethoden für die Bestimmung der Zucker Saccharose, D-Glucose und D-Fructose sowie die Säuren Zitronensäure, Essigsäure, L-Apfelsäure und L-Lactat eingesetzt Bier und Bier-Mix-Getränke Die Qualitätskontrolle von Bier und Bier-Mix-Getränken hat verschiedene Ziele wie die Überwachung der Produktzusammensetzung (Stammwürze, Alkoholgehalt etc.), Haltbarkeitsprüfung, die Prüfung auf infektions- oder lagerbedingte Qualitätsminderung sowie Überprüfung auf Kontaminanten, die Bestimmung von Pestizidrückständen, Reinigungs- oder Desinfektionsmitteln bzw. technischen Hilfsstoffen. Weiterhin werden zur Kontrolle der Einhaltung des Reinheitsgebotes verwendete Roh- und Zusatzstoffe nachgewiesen. Nachfolgend sind nur einige bierspezifische Untersuchungsmethoden zusammengefasst. Für eine detaillierte Beschreibung wird auf die in Deutschland amtliche Sammlung von Untersuchungsverfahren hingewiesen [ASU-Methoden Nr. L bis L ]. Der Stammwürzegehalt wird im fertigen Bier nach den ASU-Methoden (Destillations- bzw. Refraktometer-Methode) durch Rückrechnung aus dem vorhandenen Alkohol- und dem unvergorenen Extraktgehalt nach der für ober- und untergärige Biere einheitlichen Balling- Formel ermittelt. Mit der Refraktometer-Methode wird über die Dichte des entgasten Bieres der "scheinbare" Restextraktgehalt bestimmt, welcher den Anteil des nicht zur Vergärung gelangten Extraktes im fertigen Bier inklusive des Alkohols beschreibt. Zur Feststellung des "wirklichen" Extrakts muss der Alkohol durch eine Destillation entfernt werden und mit Wasser auf das ursprüngliche Gewicht zurückgewogen werden. Beim Destillationsverfahren wird das entgaste Bier destilliert und die Menge sowie Dichte des Destillats (Alkohol-/H 2 O- Mischung) bestimmt. Hieraus berechnet sich der Alkoholgehalt. Der wirkliche Restextrakt wird ermittelt, indem der Destillatrückstand mit Wasser aufgefüllt und die Dichte mit einem Refraktometer bestimmt wird. Aus dem Alkoholgehalt und dem wirklichen Extrakt kann die wirkliche Stammwürze nach der Balling-Formel ermittelt werden. Im Falle einer nachträgli-
55 3 Stand des Wissens 3.5 Hefeanalytik 44 chen Alkoholverminderung ist die Balling-Formel nicht anwendbar. Es kann dann nur über bestimmte konzentrationsabhängige, aber nicht vergärbare Malzinhaltsstoffe (Kalium, Phosphat, Stickstoff, Prolin) näherungsweise auf den ursprünglichen Stammwürzegehalt zurückgerechnet werden (Methode Weber). Für die Bestimmung des Alkoholgehaltes alkoholfreier Biere und des Schwefeldioxidgehaltes der Biere werden enzymatische Methoden verwendet. Der Nachweis einer Rohfrucht -Verwendung (z.b. Mais, Reis, Hirse) gelingt mittels immunologischer Methoden (z.b. durch Geldiffusion nach Ouchterlony, Gegenstrom-Elektrophorese, Immun-Elektrophorese nach Grabar-Williams, ELISA). Siehe ASU-Methoden Nr. L , [47]. Die Bestimmung der Bitterstoffe (BE) erfolgt photometrisch nach den MEBAK-Methoden (Bd. 2, S. 318), wobei hauptsächlich Iso-α-Säuren (Humulone) erfasst werden. Eine differenzierte Bestimmung der α- und β-säuren gelingt mittels HPLC (MEBAK Bd. 2, S. 321). Die biologische Qualitätskontrolle konzentriert sich in der Regel nur auf obligat bierschädliche Mikroorganismen wie z.b. Laktobazillen, Pediokokken (Sarcina), Megasphaera, Pectinatus, wilde Hefen, Escherichia coli, Essigsäurebakterien und Schimmelpilze. Zum Nachweis verwendet man mikroskopische Techniken sowie kulturelle Anzucht- und Anreicherungsverfahren wie sie auch bei anderen Lebensmitteln üblich sind, jedoch mit entsprechenden würze- und bierspezifischen Nährmedien [47]. Im Anhang wird in der Tabelle 8.3 ein Überblick über wichtige Parameter und Messmethoden bei der Bieranalyse gegeben [60, 61]. 3.5 Hefeanalytik Hefen besitzen ein weites Spektrum an Anwendungen in der Lebensmittelindustrie. Sie werden u.a. im Bierbrauwesen, zur Wein- und Branntweinherstellung sowie zum Backen in der Bäckerei eingesetzt. Backhefen werden als Reinzucht obergäriger Stämme vorwiegend aerob in Nährlösungen hergestellt und kommen als Trockenhefe oder Presshefe in den Handel. Die Hefeanalytik ist ein Überbegriff für verschiedene analytische Verfahren, mit denen Hefezellen spezifiziert werden können. Es gibt ein Vielzahl an gesetzlich vorgeschriebenen Analysen, die für das Lebensmittel Hefe durchgeführt werden müssen. Die Versuchsanstalt der Hefeindustrie e.v. in Berlin (VH-Berlin) untersucht u.a. Inhaltsstoffe von unterschiedlichen Hefetypen (Backhefe, Bierhefe, Brennereihefe, Trockenhefe etc.) mit chemischphysikalischen Methoden und arbeitet hierfür sogenannte Standardverfahren (SOP: Standard operation procedure) aus. Weiterhin werden durch mikrobiologische Untersuchungen Hefestämme identifiziert sowie Hefe- und Fremdkeimgehalte bestimmt.
56 3 Stand des Wissens 3.5 Hefeanalytik 45 Mithilfe der Hefeanalytik, insbesondere der Analyse von Hefezellbestandteilen können außerdem Aussagen über die Vitalität, Leistungsfähigkeit sowie der Stoffwechseleigenschaft der Hefen gemacht werden [62]. Die Vitalität der Hefe ist aus Sicht der Backhefeindustrie entscheidend für die Triebkraft im Teig, dem Hauptleistungskriterium der Hefe, wohingegen im Brauprozess die Hefevitalität und ihre stoffwechselphysiologische Leistung die Zusammensetzung des Endproduktes Bier wesentlich beeinflusst [63, 64]. Jedoch führen die langen Analysenzeiten der etablierten nasschemischen Messmethoden dazu, dass frühestens nach einigen Stunden Fermentation ein Mangel der Reservestoffe erkannt wird und somit erst spät z.b. durch eine angepasste Fütterung der Hefe reagiert werden kann Chemische Zusammensetzung von Hefen Hefezellen (Saccharomyces cerevisiae) sind Ascomyceten, das heißt einzellige sporenbildende Pilze ohne Fruchtkörper und Hyphen, die sich in günstigen Nährmedien vegetativ durch Sprossung vermehren. Die Hefezellen sind ellipsoid mit Durchmessern von etwa 5 bis 10 µm auf der langen Seite und 1 bis 7 µm für die kurze Seite. Mit zunehmendem Alter werden die Zellen größer. Bierhefen sind generell größer als Backhefen [65]. Die Trockensubstanz von Backhefen besteht aus 45 bis 60 % Rohprotein, 15 bis 39 % Kohlenhydrate, 2 bis 12 % Rohfett und 6 bis 12 % Mineralien [66]. Das Rohprotein setzt sich aus Albumine, Globuline, Phosphorproteine, Nukleinsäuren, Nukleotide, Peptone, Polypeptide und Aminosäuren zusammen. Unter den Kohlenhydraten sind Glykogen, Trehalose, Mannan sowie Glucan vertreten. Gesamtfette, Neutralfette, Phosphatide, Lipoidsymplexe, Sterine und Cerebrine machen den Rohfettgehalt aus. Die oben aufgezählten Konzentrationen beziehen sich auf die Hefetrockensubstanz (HTS). Der HTS-Gehalt ist die Summe aus Proteinen, Kohlenhydraten, Fetten und Mineralien der Hefen. Frische Backpresshefen besitzen einen Wassergehalt von ca. 65 bis 75 %, wobei in intrazellulär gebundenem und extrazellulär vorliegendem Wasser unterschieden wird. Das extrazelluläre Wasser ist filmartig zwischen den Zellen verteilt. Die intrazelluläre und extrazelluläre Wasserverteilung in gepressten Hefen ist abhängig vom HTS-Gehalt, dem Hefestamm und der chemischen Zusammensetzung der Hefezellen (z.b. Rohproteingehalt). Zwischen dem HTS-Gehalt und der intrazellulären sowie extrazellulären Wasserverteilung existiert bei gleicher Hefe ein linearer Zusammenhang [66]. Bei einer gepressten Hefe mit einem HTS-Gehalt von 30 % sind 79 % des Wassers intrazellular und 21 % extrazellular gebunden. Bei derselben Hefe mit einem HTS von 35 % ist H 2 O nur noch in den Zellen vorhanden [66]. Im Zellplasma der Hefezellen liegen als Kohlenhydrat Glykogen (ca. 12 % der HTS bei Backhefen) und Trehalose (ca. 12 % der HTS bei Backhefen) vor. Brauereihefen besitzen
57 3 Stand des Wissens 3.5 Hefeanalytik 46 mehr Glykogen jedoch weniger Trehalose als Backhefen. Die Zellwand beinhaltet die zwei weiteren Kohlenhydrate Glucan (ca. 5 % der HTS bei Backhefen) und Mannan (ca. 10 % der HTS bei Backhefen). Aus vorliegenden Forschungen, sowohl in der Backhefe- als auch in der Brauereitechnologie, ist bekannt, dass die Konzentrationen der intrazellulären Kohlenhydrate Glykogen (Reservestoff) und Trehalose (Stressprotektor) spezifische Aussagen über die Vitalität der Hefen erlauben. Abhängig vom Status des Zellteilungszyklus, der Prozessführung und den äußeren Medienbedingungen können diese Stoffe intrazellulär auf- oder abgebaut werden [62, 63, 64, 67, 68, 69, 70]. Steigt der Glykogengehalt, sinkt der Rohproteingehalt und umgekehrt [66]. Ein hoher Glykogengehalt fördert die Haltbarkeit eines Flüssighefeansatzes oder einer Presshefe. Dagegen spielt Trehalose eine wichtige Rolle im Stressmetabolismus, insbesondere bezüglich der Thermotoleranz und der Trockenresistenz [71]. Bei Hitzestress akkumuliert die Hefe Trehalose [72] und schützt die Zelle dadurch, dass Proteine und Enzyme durch die Trehalose stabilisiert werden. Weiterhin wird so die Bildung von Proteinaggregaten bei Hitzeeinwirkung reduziert [70]. Das Disaccharid Trehalose wird als bester Stabilisator für Makromoleküle beschrieben [73] und hilft beispielsweise dem Protein Chaperon Hsp104 bei der Rückfaltung von hitzegeschädigten Proteinen [74]. Weiterhin wird Trehalose in Zellen akkumuliert, wenn Glucose im Medium erschöpft ist und die Zellen in einen akuten Energiemangelzustand kommen [75]. Die Trehalosekonzentration wird bei längeren Hungerperioden auch auf Kosten des Glykogenpools aufrechterhalten. Ein hoher Proteingehalt von Hefen fördert die intrazelluläre Speicherung von Wasser, sowie die Enzymbildung und Stoffwechselaktivität. Jedoch wird dadurch die Lagerfähigkeit verschlechtert, da solche Hefen schnell zur Autolyse neigen. In der Backindustrie wird für länger haltbare Presshefen ein Rohproteingehalt von rund 47 % und bei stoffwechselaktiven Hefen ein Rohproteingehalt von über 50 % angestrebt [66]. Das Reinprotein (überwiegend Enzymproteine) macht normalerweise 64 bis maximal 80 % des Rohproteins aus. Die Proteine befinden sich im Zytoplasma und der Zellwand der Hefen Analyse von intrazellulären Hefebestandteilen Die Trockensubstanz bzw. der Wassergehalt einer Hefe haben einen erheblichen Einfluss auf die Qualität der Backhefe, insbesondere auf ihre Haltbarkeit und Triebkraft [66]. Außerdem dient die Hefetrockensubstanz als Bezugsgröße für die Bestimmung der Zellkomponenten. Die Referenzanalyse hierfür ist die Trocknung der Proben mit anschließender Wiegung des Zelltrockengewichtes.
58 3 Stand des Wissens 3.5 Hefeanalytik 47 Die Bestimmung des Rohproteingehalts erfolgt normalweise mittels Kjeldahl-Analyse, welche nicht nur den Proteinstickstoff, sondern auch Aminosäuren, Nucleinsäuren, Nucleotide und andere stickstoffhaltige Substanzen der Hefe erfasst [56]. Die Polysaccharide Mannan und Glucan können nach fraktionierter Kohlenhydratextraktion aus einem Ansatz mit einer modifizierten Methode von Trevelyan & Harrison [76] ermittelt werden. Für die Quantifizierung der intrazellulären Kohlenhydrate Trehalose und Glykogen werden verschiedene Messverfahren wie Kolorimetrie [Anthron-Methode, 76] und HPLC [77] nach nasschemischer Extraktion, Fluoreszenzmarkierung und Durchflusszytometrie [67] herangezogen. Die am häufigsten verwendete kolorimetrische Methode, sowohl zum Nachweis von säurelöslichem, alkalilöslichem Glykogen als auch von Trehalose, nutzt die Anthron-Reaktion von Glucoseäquivalenten. Die Reaktion ist nicht spezifisch und die Genauigkeit ist abhängig von dem Gang der Extraktion. Dennoch können Vorhersagegenauigkeiten von ± 3 % für die einzelnen Zuckerfraktionen erzielt werden. Zur Durchführung von HPLC-Methoden sind zellfreie Hefeextraktfraktionen notwendig. Eine gute Korrelation von r = 0,995 und Wiederfindungsrate von 98 % für die Bestimmung von Trehalose in Hefezellen konnten durch den Einsatz von Standardsäulen und Acetonitril/Wasser-Elution erreicht werden [77]. Die Durchflusszytometrie ist in der Medizin eine Routinediagnostik, wo sie vorwiegend für die Untersuchung von malignen Zellen eingesetzt wird. In der Biotechnologie wurden mit dieser Methode bisher erfolgreich Mikroorganismen untersucht, indem spezifische Zellkomponenten mit Fluoreszenzfarbstoffen angefärbt und so detektiert werden konnten. Mit zytometrischen Messmethoden wurden in Bierhefen bereits erfolgreich der Zellzyklus und 3β-Hydroxygehalt [78], der Glykogen- und Neutrallipidgehalt [68, 69] sowie der Trehalosegehalt [67] bestimmt. Die Messung des intrazellulären ph-wertes mithilfe der Durchflusszytometrie konnte ebenfalls für die Vitalitätsbeurteilung von Bierhefen herangezogen werden [79]. Die zytometrischen Verfahren sind allerdings immer mit einem hohen zeitlichen Aufwand von mehreren Stunden, dem Einsatz von hochqualifiziertem und erfahrenem Personal, einem hohen Verbrauch an Reagenzien sowie z.t. hohen Investitionskosten verbunden. Sie sind deshalb für klein- und mittelständische Unternehmen nicht als Routineanalytik geeignet. Allerdings sind sie aufgrund ihrer vielfältigen Möglichkeiten, intrazelluläre Komponenten zu messen, eine wertvolle Referenzmethode. So können sehr gut intrazelluläre Matrixeffekte dargestellt werden, ohne die Hefe zu zerstören.
59 3 Stand des Wissens 3.5 Hefeanalytik 48 Ferner besitzt die in den letzten Jahren immer häufiger in den Betriebslabors und Produktionsprozessen der chemischen, pharmazeutischen und Lebensmittelindustrie eingesetzte IR- Spektroskopie das Potenzial, gleichzeitig mehrere Stoffe ohne größeren präparativen Aufwand quantitativ zu erfassen. In [80] wird am Beispiel von Hefen gezeigt, dass eine intrazelluläre Trehalose- und Glykogen-Bestimmung mittels NIR-Reflexionsspektroskopie möglich ist. Allerdings ist der Vorhersagefehler insbesondere bei Trockenhefen beträchtlich. Dies liegt u.a. daran, dass die in Reflexion gemessenen NIR-Spektren bzw. Streulichtintensitäten empfindlich von der Teilchengrößenverteilung im Pulver abhängen. Die MIR-Analyse von intrazellulären Kohlenhydraten (Glykogen, Trehalose, etc.) in lebenden Organismen (z.b. Hefe), die metabolischen Prozessen unterliegen, ist bislang nur qualitativ untersucht worden [18, 19, 80, 99]. Auf das Potenzial dieser Anwendung in Hinblick auf die Beurteilung der Hefe-Zell-Physiologie wurde erst kürzlich hingewiesen [19].
60 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen 49 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen Messtechnik am Bioreaktor Für die Hefekultivierung wurde ein Laborfermenter BIOSTAT E der Firma B. Braun (mittlerweile Sartorius BBI Systems GmbH) verwendet. Das Kulturgefäß hatte ein Volumen von 6 L und war mit einem Begasungsring sowie einem zweistufigen Scheibenrührer mit je sechs Rührblättern, einem Grundgerät und einem Mess- und Regelaufsatz ausgerüstet. Zur Überwachung und Steuerung der Fermentation war der Bioreaktor herstellerseitig mit einem Pt100-Temperaturmessfühler, Rührerdrehzahlmesser, Schwebekörper-Durchflussmesser (Rotameter) für die Bestimmung der Begasungsrate, einer ph-elektrode (405-DPAS-SC- K8S, Mettler Toledo, Schweiz) mit ph-regelung durch angeschlossenen Säure- und Alkali- Zulauf sowie einer Gelöstsauerstoff-Elektrode (Clark-Elektrode , Ingold, Schweiz) ausgestattet. Zusätzlich zu diesen Sensoren wurden zwei photometrische IR-Gasanalysatoren für die Bestimmung der CO 2 - und Ethanolkonzentration im Abgasstrom sowie die Eintauchsonde eines faseroptischen Rückstreumessaufbaus zur Bestimmung der Biomasse im Reaktor installiert. Alternativ wurde zur Bestimmung der CO 2 - und Ethanolkonzentration in Fermentationsabgas ein IR-Spektrometer eingesetzt. Die Geräte werden im Kapitel näher beschrieben. Weiterhin sind ein thermischer Massendurchflussmesser für die Bestimmung der Begasungsrate in der Zuluft sowie ein amperometrischer Sauerstoffsensor für die Messung des Sauerstoffgehalts im Abgasstrom eingesetzt worden. Die erhaltenen Messdaten wurden kontinuierlich mit der Software LabVIEW (Version 8.5, National Instruments) aufgezeichnet. Die dafür notwendige Bedieneroberfläche wurde vom Mitarbeiter Daniel Geörg des Institut für Prozessmesstechnik und innovative Energiesysteme der Hochschule Mannheim programmiert. Einen Überblick über die Messtechniken am Bioreaktor liefert Abbildung 4.1.
61 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen 50 Abgas Luftstrommessung Begasung Lab- VIEW Lauge Säure Abgaskühler Streulicht- Sonde O 2 -Sensor Drehzahl ph Elektrode NDIR-CO 2 -Sensor NDIR-Ethanol-Sensor po 2 Elektrode NIR-LED Si-Detektor Zelldichte Pt-100 Rührer Begasungsring Thermostatanschluss Abbildung 4.1: Messtechnik am Bioreaktor Abgasanalytik Das Fermentationsabgas wurde über einen temperierbaren Schlauch auf eine Temperatur von 25 C abgekühlt und zu den photometrischen IR-Gasanalysatoren, dem IR-Spektrometer und dem Sauerstoffsensor geleitet. Der Sauerstoffgehalt im Abgas wurde mittels des amperometrischen O 2 -Sensors (SO-D0-250-A087A, Unitronic, Düsseldorf) gemessen. Der Sauerstoffgehalt im Abgas gibt Auskunft über den Sauerstoffverbrauch der Zellen und somit über ihre Atmungsaktivität. Mit zwei nicht-dispersiven (photometrischen) IR-Gasanalysatoren (BlueSens Gas Sensor GmbH, Herten), welche im Abgasstrom montiert waren, wurde das von der Hefe gebildete Ethanol und CO 2 on-line erfasst. Aus der gemessenen Ethanolkonzentration in der Gasphase konnte durch einen Kalibrierungsfaktor direkt auf die Ethanolkonzentration in der Flüssigphase geschlossen werden (siehe Abschnitt 5.1.2). Das Funktionsprinzip der IR- Gasanalysatoren für CO 2 (Messbereich von 0 bis 10 Vol.-%, Genauigkeit ± 0,2 % vom Messbereichsendwert ± 3 % Anzeige, Drift pro Jahr <± 2 % Anzeige) und Ethanol (Messbe-
62 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen 51 reich von 0 bis 3,5 Vol.-%, Genauigkeit ± 0,2 % vom Messbereichsendwert ± 3 % Anzeige, Drift pro Jahr <± 2 % Anzeige) ist in Abbildung 4.2 dargestellt. Die Lichtquelle sendet infrarote Strahlung aus, welche beim Passieren der Gasküvette (optische Weglänge d = 1,4 cm) teilweise von den Gasmolekülen absorbiert wird. Für die spezifische Detektion der Analyten werden pyroelektrische Detektoren mit entsprechenden optischen Bandpassfiltern verwendet. Für die CO 2 - und Ethanol-Sensoren werden z.b. optische Bandpassfilter eingesetzt, welche eine hohe Transmission bei 4,26 ± 0,09 µm und bei 3,40 ± 0,08 µm besitzen und im restlichen IR-Spektralbereich das Licht blockieren. In beiden Gasanalysatoren ist darüber hinaus ein zweiter Detektor mit einem optischen Bandpassfilter im Referenzkanal für die Driftkompensation installiert. Aufgrund der langsamen Diffusion der Gasprobe durch einen Sterilfilter in das Innere der Sensoren liegt die charakteristische Totzeit der Gasanalysatoren zwischen 3 und 5 Minuten. IR-Lichtquelle Gasküvette f Probe f Referenz Optische Bandpassfilter d Probe d Referenz Pyroelektrische Detektoren Abbildung 4.2: Photometrische IR-Gasanalysatoren Um etwaige Querempfindlichkeiten der Gasanalysatoren auszuschließen, wurde zusätzlich die CO 2 -Konzentration im Abgas mit einem IR-Spektrometer (Equinox 55, Bruker Optics, Ettlingen) ermittelt. Nach Kalibration mit Prüfgasen für CO 2 kann über die Auswertung der IR- Extinktion im Absorptionsmaximum bei 2360 cm -1 bzw. der Fläche zwischen 2380 und 2310 cm -1 die CO 2 -Konzentration ermittelt werden. Alternativ konnte die Ethanolkonzentration im Abgas durch Auswertung der Fläche zwischen 3000 und 2860 cm -1 unter Verwendung des IR-Spektrometers bestimmt werden. Beide Auswertungen erfolgen mit der gerätezugehörigen Software OPUS Version 6.5.
63 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen Faseroptischer Rückstreumessaufbau Für die in-line Verfolgung der Biomasse (oder Zelldichte) wurde ein Rückstreusensor verwendet, da bei hohen Zelldichten die Rückstreumessung besser geeignet ist als eine Transmissionsmessung [81]. NIR-LED- Lichtquelle Photodetektor PC für Messdatenerfassung und -auswertung Sendefaser Empfangsfaser Stabsonde Streulicht Zelle Abbildung 4.3: Faseroptischer Rückstreusensor Der faseroptische Sensor ist ein hausinterner Aufbau und besteht aus einer NIR-LED (Emission bei 850 nm), einer autoklavierbaren faseroptischen Reflexionssonde für 0 / 180 Rückstreumessung sowie einer Silizium-Photodiode als Photodetektor (siehe Abbildung 4.3). Es handelt sich dabei um denselben Rückstreumessaufbau, welcher auch in Abbildung 4.1 dargestellt ist. Das NIR-Licht gelangt über die Sendefaser, die sich in der Tauchsonde befindet, in die Fermentationsbrühe. Dort vorhandene Zellen, z.b. Hefezellen, streuen einen Teil des einfallenden Lichts zurück in die Empfangsfasern. Die von der Si-Photodiode erfasste Streulichtintensität ist proportional zur Zellkonzentration bei den hier durchgeführten Hefe- Fermentationen (s.u.).
64 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen 53 Im Vergleich zu Halogen- oder Bogenlampen ist die Intensität der NIR-LED auch bei längerer Betriebsdauer relativ konstant, wodurch eine langfristige Stabilität der Kalibration von Biomasse gewährleistet wird. Ein weiterer Vorteil bei der Verwendung der LED ist, dass diese bei einer gewissen Frequenz (hier: 500 Hertz) moduliert und Licht mit unterschiedlicher Frequenz wie z.b. störendes Umgebungslicht durch eine elektronische Lock-In-Verstärkung des Detektorsignals herausgefiltert werden kann [82] Inokulum, Fermentationsbedingungen und Probennahme Als Inokulum für die Fermentationsprozesse wurden kommerziell erhältliche Backhefen (DHW VITAL-GOLD, Deutsche Hefewerke GmbH, Nürnberg sowie Wieninger, F.X. WIE- NINGER GmbH, Passau) der Spezies Saccharomyces cerevisiae eingesetzt. Die HTS- Gehalte, welche mittels Referenzverfahren (SOP H-01, Versuchsanstalt der Hefeindustrie e.v., Berlin) bestimmt wurden, betrugen für die Wieninger Hefe 32,1 Gew.-% und für die DHW Backhefe 29,7 Gew.-%. Das Kulturmedium wurde in entionisiertem Wasser hergestellt und enthält folgende Stoffe pro Liter: 16,0 g (NH 4 ) 2 SO 4 ; 1,15 g MgSO 4 x 7 H 2 O; 1,25 g NH 4 H 2 PO 4 ; 5,0 g KCl; 10,0 mg Calcium-D(+)-pantothenat; 105,0 mg myo-inositol; 1,0 mg D(+)-Biotin; 0,42 g CaCl 2 x 2 H 2 O; 15,0 mg FeCl 3 x 6 H 2 O; 9,0 mg ZnSO 4 x 7 H 2 O; 10,5 mg MnSO 4 x H 2 O; 2,4 mg CuSO 4 x 5 H 2 O; 30,0 g D(+)-Saccharose und 100,0 µl Antischaummittel (Aspumit AP, THOR GROUP LTD, Kent, UK). Alle Substanzen außer Saccharose wurden in 5 L VE-Wasser gelöst. Anschließend wurden 300 ml des Mediums entnommen und 50 g der kommerziellen Backhefe in diesem Aliquot suspendiert, sodass später im Fermenter eine Konzentration von 10 g / L vorlag. In dem restlichen Medium wurde die Saccharose gelöst. Nach Temperierung des Fermentationsmediums im Bioreaktor und Einstellen des ph-wertes wurde mit der Backhefesuspension angeimpft. Das Fermentationsvolumen betrug 5 L. Der Bioreaktor und die Messsonden wurden vor der Fermentation mit einer Lösung von 70 % Ethanol in Wasser sterilisiert. Während der Fermentation wurden die Temperatur auf 32 C, die Begasungsrate auf 1,0 vvm (gas volume flow per unit of liquid volume per minute) und die Rührerdrehzahl auf 700 rpm (rounds per minute) geregelt. Der ph-wert wurde durch automatische Zugabe von 5 M NaOH mit einer peristaltischen Pumpe konstant auf 5,2 gehalten. Das Fermentationsabgas wurde mittels Rückflusskühler auf eine Temperatur von 25 C abgekühlt und zu den photometrischen IR-Gasanalysatoren und einem Sauerstoffsensor geleitet.
65 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen 54 Im Verlauf der Fermentationsprozesse wurden 10,0 ml Probe in regelmäßigen Abständen alle 30 Minuten aus dem Reaktor entnommen und unmittelbar bei -18 C eingefroren. Im Anschluss wurden die Ethanol-, Zucker- und Biomasse-Konzentrationen der Proben durch die entsprechenden Referenzmethoden (HPLC bzw. Wägung) bestimmt Referenzmethoden Die Ethanol-, Saccharose-, Fructose- und Glucose-Konzentrationen in den Proben wurden mithilfe der High Performance Liquid Chromatographie (HPLC) und einem Differential- Refraktometer (Knauer GmbH, Hamburg) als Detektor analysiert. Die Ionenaustauschersäule (AT Polyspher OA HY, Merck KGaA, Darmstadt) wurde auf 30 C temperiert und 20 ul Probenvolumen aus der Probenschleife gepumpt (HPLC-Pumpe, 880-PU, Jasco GmbH, Deutschland). Als Laufmittel wurde Schwefelsäure (0,005 mol/l) mit einer Durchflussrate von 0,5 ml/min verwendet. Die Aufzeichnung der Chromatogramme erfolgte mit einem angeschlossenen Schreiber (HP 3394A Integrator, Hewlett Packard, USA). Zur Kalibrierung der HPLC wurden Standards von Saccharose, Glucose, Fructose und Ethanol hergestellt. Aus den daraus ermittelten Retentionszeiten und Flächen konnten die Konzentrationen dieser Substanzen während der Kultivierung bestimmt werden. Vor den Messungen wurde die Säule für 30 Minuten konditioniert, bis eine stabile Basislinie zu beobachten war. Für die off-line Analyse der Proben wurden die entnommenen 10 ml aufgetaut und in sterile Glasröhrchen gegeben, die zuvor für 2 h bei 100 C getrocknet wurden. Nach Zentrifugieren (Centrifuge 5415 R, Eppendorf, Hamburg) bei rpm und 4 C für 5 Minuten wurde der Überstand mit einen Sterilfilter (0,2 µm Celluloseacetat-Membran, VWR, Bruchsal) filtriert und vor der Injektion in die HPLC-Säule 1:10 verdünnt. Ein Chromatogramm der detektierten Substrate und Produkte während der Backhefekultivierungen ist der folgenden Abbildung 4.4 zu entnehmen. Die größte Retentionszeit von 17,45 Minuten besitzt Ethanol. Im Anhang in der Tabelle 8.4 sind die Kalibrationsproben sowie die Standardabweichungen für die HPLC- Analysen der Fermentationsproben aufgeführt.
66 4 Material und Methoden 4.1 On-line Kohlenstoffbilanzierung von Backhefe-Fermentationen 55 Saccharose Salze Glucose Fructose Glycerin Ethanol Abbildung 4.4: HPLC-Chromatogramm der Substrate und Produkte während der Backhefekultivierung (Angabe der Retentionszeiten in Minuten) Um die Hefetrockensubstanz (HTS) zu bestimmen, wurden die Pellets bei 100 C für 24 h im Umluftofen getrocknet. Nach der Trocknung ist Trockenmasse mittels analytischer Waage (Modell: ABT 120-DM, Kern & Sohn GmbH, Balingen-Frommern) bestimmt worden. Neben der Biomassenbestimmung mittels Trocknungsverfahren wurden die Zelldichten (Zellen / ml) direkt nach Probennahme (at-line) unter einem Mikroskop mit einer Neubauer-Zählkammer ermittelt. Die Tiefe der Zählkammer betrug 0,02 mm und die Fläche eines Kleinquadrates 0,0025 mm 2. Das Zählgitter bestand aus 4 x 4 Großquadraten, die ihrerseits wieder in 16 Kleinquadrate unterteilt waren. Da ein Großquadrat aus 16 Kleinquadraten aufgebaut war, betrug das Volumen eines Großquadrates ml. Für die Zellzählung wurden die Fermentationsproben 1:5 bzw. 1:10 mit einer Kochsalzlösung verdünnt. Um repräsentativ die Zellzahl mit geringen statistischen Fehlern zu ermitteln, wurden mindestens zehn Großquadrate in beiden Zählgitternetzen (je eines ober- und unterhalb des Steges) ausgezählt. Aus der mittleren Zellzahl x und dem Verdünnungsfaktor konnte die Zelldichte berechnet werden: x Zelldichte = Verdünnungsfaktor ml (4.1)
67 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR-Spektroskopie MIR-ATR-Spektrometer-Aufbau In Abbildung 4.5 ist das von der Firma Bruker Optics GmbH kommerziell erhältliche ALPHA FT-MIR-Spektrometer mit eingebautem Diamant-ATR-Modul zu sehen, welches in dieser Arbeit verwendet wurde. Ein Vorteil des FT-IR-Spektrometers ALPHA gegenüber anderen Geräten ist sein geringes Gewicht und sein kompakter Aufbau, wodurch es leicht transportabel ist und so universell an verschiedenen Orten im Labor eingesetzt werden kann. Abbildung 4.5: FT-MIR-Spektrometer ALPHA der Fa. Bruker Optics GmbH mit eingebautem ATR- Modul für flüssige Proben und Feststoffe Das Interferometer des ALPHA Spektrometers basiert auf das von Bruker Optics GmbH patentierte RockSolid TM -Verfahren. Hierbei sind die Spiegel nicht wie im einen herkömmlichen Interferometer eben, sondern in rechtwinkliger Geometrie aufgebaut (Cube Corner Technik). Vorteil dieser Konstruktion ist die Robustheit gegenüber Erschütterungen, da der Lichtstrahl unabhängig von der Spiegelneigung in gleicher Richtung zurückgestrahlt wird (siehe Abbildung 4.6).
68 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 57 Abbildung 4.6: Vorteil eines rechtwinkligen Interferometer-Spiegels (Cube Corner Technik) gegenüber einem flachen Spiegel [83] Folgende Spezifikationen besitzt das ALPHA Spektrometer: Gewicht: 7 kg Grundfläche: 22 x 30 cm (inklusive Probenmodul) Spektralbereich: cm -1 Spektral Auflösung besser als 2 cm -1 RockSolid TM Interferometer: Goldspiegel, 30 Einfallswinkel (maximaler Durchsatz minimale Polarisationseffekte), permanent justiert Automatische Instrumententests, integrierter Polystyrol Standard Detektor: DTGS Strahlungsquelle: SiC Globar IR-Fenster: ZnSe (nicht hygroskopisch, begrenzt jedoch Spektralbereich auf 6000 bis 500 cm -1 ) Je nachdem welche Art von Messung man durchführen möchte, kann das ALPHA Spektrometer durch das QuickSnap TM System mit einer Transmissions-, ATR- oder diffuser Reflexionsmessvorrichtung ausgestattet werden. Die QuickSnap TM -Probenmodule können ohne den Einsatz von Werkzeugen ausgetauscht werden. Nach automatischer Erkennung des Moduls und Perfomance-Test werden die entsprechenden Messparameter geladen. Bei dem verwendeten Diamant-ATR-Modul mit Einfach-Reflexion ist der ATR-Kristall (Fläche 2 mm 2 ) in eine Keramikplatte (Wolframcarbid) eingefasst, was eine chemisch inerte und mechanisch robuste Messoberfläche gewährleistet. Die Ein-Finger-Anpressvorrichtung mit 360 Schwenkmechanismus erlaubt einen ungehinderten Zugang zum Probenbereich.
69 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie Erstellung von Kalibrationsmethoden mit der OPUS Software In der Menüleiste Auswerten der Software OPUS befinden sich die Befehle Quant Methode erstellen für die Erstellung einer univariaten Kalibration und Quant 2 Methode erstellen für die Entwicklung einer multivariaten Kalibration. Die multivariate Methode basiert auf einer PLS1-Regression, mit welcher für jede Komponente ein eigenes Kalibrationsmodell entwickelt wird. Die prinzipielle Vorgehensweise bei der Erstellung von univariaten und multivariaten Kalibrationsmodellen mit OPUS Quant und Quant 2 wird am Beispiel der Zuckeranalytik von Fruchtsäften und Obst erläutert. Die beschriebene Modellentwicklung basiert auf gemessenen Absorptionsspektren von 50 Kalibrationsproben, welche aus unterschiedlichen in VE-Wasser eingewogenen Konzentrationen an Saccharose, Fructose und Glucose bestehen Hintergrund- und Probenmessung Für eine Absorptions- bzw. Transmissionsmessung wird ein entsprechendes Hintergrundspektrum benötigt, welches in gewissen Abständen aktualisiert werden sollte. Hintergrundmessungen in dieser Arbeit wurden immer mit der sauberen ATR-Zelle gegen Luft aufgenommen. Es empfiehlt sich, die Hintergrundmessung in gewissen Abständen, z.b. alle zwei Stunden, zu aktualisieren, da die Messbedingungen über einen längeren Zeitraum aufgrund von Temperaturänderungen, Schwankungen in der Zusammensetzung der Umgebungsluft und der Luftfeuchtigkeit nicht stabil sind. Eine Hintergrund- oder eine Probenmessung werden in der OPUS Software unter dem Menü Erweiterte Messungen (siehe Abbildung 4.7) durchgeführt. Im Fenster Grundeinstellungen können bereits gespeicherte Messparameter geladen werden. In der Karteikarte Erweitert (Abbildung 4.8) können neue Messparameter - wie spektrale Auflösung und die Anzahl von Scans pro Messung - definiert werden. Für die Messung der Kalibrationsproben müssen dabei dieselben Parameter eingestellt werden, die später auch beim Messen von unbekannten Proben verwendet werden. In dieser Arbeit wurden die Fermentationsproben mit einer Auflösung von 4 cm -1 und 32 Scans vermessen und für die Getränke- sowie Hefeanalytik eine Auflösung von 8 cm -1 mit 64 Scans gewählt. Für die Erstellung der Kalibrationsmodelle wurden ausschließlich Absorptionsspektren mit dem ATR-Modul aufgenommen. Hierzu wird unter Resultatspektrum auf Absorbance gestellt. Eine mögliche atmosphärische Kompensation, welche bei den Messungen den Einfluss von Wasserdampf und CO 2 in der Luft berücksichtigt, wurde in dieser Arbeit nicht verwendet.
70 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 59 Abbildung 4.7: Hintergrund- und Probenmessung mit der OPUS Software von Bruker Optics GmbH Abbildung 4.8: Einstellen der Messparameter mit der OPUS Software von Bruker Optics GmbH
71 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie Univariate Kalibrationsmodelle (Quant 1) Für die Erstellung von univariaten Modellen wird die Auswertesoftware Quant Methode erstellen geöffnet und die Schaltleiste weiter betätigt. Durch Klicken der Schaltfläche Komponente hinzufügen kann im folgenden Fenster (Abbildung 4.9) der Name der Komponente, für welche das Kalibrationsmodell erstellt werden soll, eingegeben werden. Im Fall der Zuckeranalytik von Obst und Fruchtsäften wird jeweils einer der Komponenten Saccharose, Fructose, Glucose oder Gesamtzucker mit entsprechender Einheit (alle in Gew.-%) für ein Modell hinzugefügt. Hierfür wird der Name und die Einheit geändert und übernehmen angewählt. Abbildung 4.9: Quant 1 Methode erstellen: Komponenten hinzufügen und Einheiten definieren Im weiteren Fenster (Abbildung 4.10) können die Spektren der Kalibrationsproben in die Methode geladen werden, indem die Schaltleiste Spektren hinzufügen betätigt und die im Ordner abgespeicherten Kalibrationsspektren im OPUS-Dateienformat ausgewählt werden.
72 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 61 Anschließend werden den einzelnen Spektren die entsprechenden Analytkonzentrationen zugewiesen. Diese können aus einer Excel-Tabelle in die Spalte kopiert werden. Abbildung 4.10: Quant 1 Methode erstellen: Spektren hinzufügen und Eingabe der Konzentrationswerte Im weiteren Fenster (Abbildung 4.11) werden die Integrationsbereiche für das univariate Modell festgelegt. Abbildung 4.11: Quant 1 Methode erstellen: Integrationsbereiche definieren
73 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 62 Die Methoden A bis I verwenden die Absorptionsbandenfläche und J bis R nutzen die Bandenhöhe (Extinktion) für die Kalibration. Es können hierbei verschiedene Grundlinienanpassungen gewählt werden. In dieser Arbeit werden ausschließlich die Methoden B, C, K oder L verwendet (siehe Abbildung 4.12). Mit der Methode B wird zwischen den Extinktionswerten an den beiden angegebenen Punkten eine Gerade gezogen. Die ausgefüllte Fläche darüber wird berechnet. Die Methode C verwendet zusätzlich eine Grundlinienkorrektur. Die Grundlinie wird durch den ersten und zweiten Grundlinienpunkt bestimmt. Der ausgefüllte Bereich innerhalb der Bande wird berechnet. Analog dazu erfolgt mit der K und L Methode die Bestimmung der maximalen Extinktionen zwischen zwei Grenzen ohne und mit Grundlinienkorrektur. Abbildung 4.12: Quant 1 Methode erstellen: Univariate Methoden B, C (Bandenfläche) und K, L (Extinktion) Die Auswahl des spektralen Bereichs ist entscheidend für die Vorhersagegenauigkeit des Kalibrationsmodells. Bei der univariaten Kalibration muss für jede Komponente im Idealfall eine isolierte Bande gefunden werden. Durch den Button interaktiv werden die Spektren der Kalibrationsproben angezeigt (Abbildung 4.13). Der spektrale Auswertebereich wird ausgewählt, indem die roten Linien an die gewünschte Stelle gezogen werden.
74 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 63 Abbildung 4.13: Quant 1 Methode erstellen: Interaktive spektrale Bereichswahl Nachdem die geeigneten Integrationsbereiche definiert sind, werden Kalibrationsmodelle durch Betätigen der Schaltleiste Kalibrieren berechnet (siehe Abbildung 4.14). Es können lineare, quadratische oder kubische Funktionen angepasst werden. In dieser Arbeit wird für die Erstellung von univariaten Modellen eine lineare Kalibration verwendet, da für Absorptionsspektren im Idealfall eine lineare Beziehung zwischen den Konzentrationen und den Intensitäten aufgrund des Lambert-Beer-Gesetzes zu erwarten ist. Anschließend kann die Methode in einem ausgewählten Ordner abgespeichert werden. Die Dateien der Quant 1 Methoden haben die Endung *.q1.
75 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 64 Abbildung 4.14: Quant 1 Methode erstellen: Methode berechnen und speichern Nach der Speicherung werden die Kalibrationsfunktion und der Korrelationskoeffizient r angegeben, mit denen die Modelle bewertet werden können (siehe Abbildung 4.15). In der Auswahlliste unten links können neben der hier gezeigten Auftragung Fit vs. Wahr (Anpassung gegen die wahren Konzentrationswerte) auch die Darstellungen der Differenz (C wahr minus C Modell ) gegen die wahren Werte Differenz vs. Wahr sowie eine Auftragung der wahren Werte gegen die Intensität (Extinktion) der Banden Wahr vs. X eingegeben werden. Im Kalibrationsreport werden die Kalibrationskurven in der Form Y = f(x) angegeben. Y steht für die Konzentrationswerte und X entspricht den Flächen bzw. Extinktionswerten, welche sich aus der Auswertung der Banden ergeben. Ein Maß für die Güte der Kalibration ist der Korrelationskoeffizient r (siehe auch Kapitel , Seite 27):
76 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 65 r = 1 m 1 1 m 1 m i= 1 m i= 1 ( C C ) ( C C ) m 2 1 ( C C ) ( C C ) wahr, i wahr, i wahr, M wahr, M m 1 Modell, i i= 1 Modell, i Modell, M Modell, M 2 (4.2) Mit C wahr als wahre und C Modell vom Modell vorhergesagten Konzentrationswerte. Der Index M steht für die jeweiligen Mittelwerte und m für die Anzahl der Kalibrationsproben. Abbildung 4.15: Quant 1 Methode erstellen: Ergebnis in Diagrammdarstellung Fit vs. Wahr (in der Kalibrationsgleichung entspricht Y den Konzentrationswerten und X den Flächen bzw. Extinktionswerten, welche sich aus der Auswertung der Banden ergeben) Für die Ermittlung des optimalen univariaten Modells werden die spektralen Bereiche, die Grundlinien und die Methoden B, C, K und L variiert, mit dem Ziel, einen maximalen Korrela-
77 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 66 tionskoeffizienten r zu erhalten und die Konzentrationen von unabhängigen Testproben mit einem geringen Fehler vorhersagen zu können Multivariate Kalibrationsmodelle (Quant 2) Die Erstellung von multivariaten Methoden ist ein iteratives Verfahren, bei dem mehrere Schritte notwendig sind. Zu Beginn ist eine ausreichend große Anzahl an Kalibrationsproben mit dem Spektrometer zu vermessen. Als Faustregel gilt, dass für eine Zweikomponentenmischung (z.b. Ethanol / Wasser) zwischen 10 und 20 Proben für die Kalibration verwendet werden sollten. Bei Mehrkomponentensystemen muss der Kalibrationsprobensatz entsprechend mehr Proben (ca. 10 bis 20 pro weitere Komponente) enthalten. Die Kalibrationsproben sollten einen größeren Konzentrationsbereich umfassen als die Proben, die später analysiert werden. Zu beachten ist, dass die Konzentrationswerte der einzelnen Komponenten möglichst gleichmäßig über den gesamten Konzentrationsbereich verteilt sind. Bei der Auswahl der Zusammensetzung der Kalibrierproben ist es wichtig, dass die Proben keine Kollinearitäten aufweisen. Dies bedeutet, dass im Probensatz die Konzentrationen mehrerer Analyten nicht im gleichen Maße zu- oder abnehmen sollten. Die Hauptkomponentenanalyse hat ansonsten Schwierigkeiten, Änderungen im spektralen Datensatz der richtigen Komponente zuzuordnen. Die Konzentrationen der einzelnen Komponenten können für Proben, welche mittels Einwaage im Labor erstellt werden, dementsprechend ausgewählt werden. Bei Kalibrationsproben, welche direkt aus einem Produktionsprozess entnommen und mittels Referenzmethode analysiert werden, sind die Konzentrationen durch den Prozess vorgeben. Hierbei lässt sich ein kollineares Verhalten häufig nicht vermeiden. Weiterhin sollte die Messgenauigkeit der Referenzanalytik bekannt sein, da diese die Präzision des Kalibrationsmodells im Wesentlichen beeinflusst. Auch spielen die gerätetechnischen spektroskopischen Messparameter wie Auflösung und Anzahl der Wiederholungsmessungen (Scans) eine bedeutende Rolle für die Kalibration. Nachdem die Kalibrationsspektren aufgenommen wurden, können diese durch unterschiedliche Datenvorbehandlungen modifiziert werden (siehe Kapitel 3.2.3, S. 24). Normalerweise ist die PLS-Regression eine sogenannte full spectrum Methode, d.h. je mehr spektrale Datenpunkte vorliegen, desto besser wird das chemometrische Modell. In vielen Fällen kann es jedoch hilfreich sein, den Wellenlängenbereich zu begrenzen, um spektrales Rauschen oder störende Nebenkomponenten von vornherein auszuschließen. Der ausgewählte Bereich sollte allerdings den gesamten Spektralbereich der jeweiligen funktionellen Gruppen (z.b. die C-O-Streckschwingung der Alkohole) berücksichtigen.
78 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 67 Der optimale Rang (Anzahl der Hauptkomponenten) für das Modell wird mithilfe einer Kreuzoder Test-Set-Validierung ermittelt, indem die Anzahl der Faktoren variiert und die zugehörigen Regressionen verglichen werden. Die Güte des Kalibrationsmodells kann über den RMSECV bzw. RMSEP sowie durch das Bestimmtheitsmaß R 2 (Quadrat des Korrelationskoeffizienten r) bewertet werden. Nachdem die PLS-Regression durchgeführt wurde, werden von der Quant 2 Software Ausreißer erkannt, welche sich u.a. durch einen überdurchschnittlich großen Vorhersagefehler bemerkbar machen. Handelt es sich um echte Ausreißer aufgrund falscher Einwaagen oder Referenzwerte, schlechte Probenvariation, Verunreinigungen, veraltete Hintergrundmessung und Inhomogenität der Proben, dann sollten die Spektren dieser Proben aus dem Kalibrationsdatensatz entfernt werden. Mit den übrigen Spektren wird anschließend eine neue PLS- Regression durchgeführt. Durch diese Vorgehensweise erhält man schließlich die optimale Methode, welche einen möglichst kleinen RMSE-Wert mit einer maximalen quadratischen Korrelation R 2 besitzt. Aussagekräftig werden diese beiden Parameter aber erst durch eine ausreichend hohe Anzahl von Proben mit unterschiedlicher Zusammensetzung sowie einer externen Validierung. Für die Erstellung von multivariaten Kalibrationsmodellen mit der OPUS Software wird in der Symbolleiste Auswerten der Menüpunkt Quant 2 Methode erstellen ausgewählt. Beim Klicken auf die Schaltfläche Methode laden kann eine bereits abgespeicherte Quant 2 Methode mit der Dateiendung *.q2 geladen werden. In dem Gruppenfeld Überblick sind statistische Informationen zu der geladenen Quant 2 Methodendatei aufgeführt wie Anzahl der Spektren (Kalibrations- und Testspektren), Anzahl der Komponenten, verwendete Spektralbereiche, Anzahl der verwendeten Datenpunkte sowie die Datenvorbehandlungsmethode. Eine neue Methode wird ebenfalls in diesem Fenster erstellt. Mit der Schaltfläche Komponenten hinzufügen werden die Komponenten für das neue Modell ausgewählt (Abbildung 4.17), und deren Namen sowie Konzentrationseinheiten definiert. Weiterhin besteht die Möglichkeit, die Nachkommastellen der Konzentrationen und Ergebnisse (RMSECV und RMSEP) auszuwählen. Als Standardeinstellung werden fünf Nachkommastellen angezeigt.
79 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 68 Abbildung 4.16: Quant 2 Methode erstellen: Neu Mit der Schaltfläche Komponenten hinzufügen werden die Komponenten für das neue Modell ausgewählt (Abbildung 4.17) und deren Namen sowie Konzentrationseinheiten definiert. Weiterhin besteht die Möglichkeit, die Nachkommastellen der Konzentrationen und Ergebnisse (RMSECV und RMSEP) auszuwählen. Als Standardeinstellung werden fünf Nachkommastellen der Konzentrationswerte angezeigt.
80 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 69 Abbildung 4.17: Quant 2 Methode erstellen: Komponenten hinzufügen Anschließend werden in der Menüleiste Spektren hinzufügen die gemessenen Kalibrationsspektren aus dem entsprechenden Ordner geladen und die Werte der verschiedenen Analytkonzentrationen für jede Probe eingegeben bzw. aus der Excel-Tabelle kopiert. Bei einer Änderung der Dateiennamen oder des Speicherortes der Kalibrationsspektren müssen unter Pfad ändern die Proben neu zugewiesen werden.
81 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 70 Abbildung 4.18: Quant 2 Methode erstellen: Spektren hinzufügen und Eingabe der Konzentrationswerte In der Spalte Datensatz können die Spektren in unterschiedliche Datensatztypen unterteilt werden. Mit Kalibration werden die Proben als Kalibrationsproben und mit Test als Testproben definiert sowie mit Nicht aktiv aus dem Probensatz ausgeschlossen. Wenn z.b. ein Spektrum nach der Validierung als Ausreißer erkannt wird, kann diese Probe auf nicht aktiv gestellt werden, ohne dass es von der Spektrenliste entfernt werden muss. Sind Proben als Test definiert, dann kann mit diesen eine Test-Set-Validierung durchgeführt werden (siehe Kapitel , S. 28). Die Proben können auch automatisch als Test-Proben über die Schaltleiste Datensatz definiert werden (Abbildung 4.19). Die Auswahl erfolgt simultan über alle Konzentrationswerte, sodass diese auf beide Datensätze gleichmäßig verteilt sind. Die Proben mit der niedrigsten und höchsten Konzentration kommen immer in den Kalibrationsdatensatz, die nächsten in den Testdatensatz und die dazwischen werden entsprechend verteilt. Für die Test-Set- Validierung werden gemäß Standardeinstellung 50 % der Proben als Test-Set gewählt und validiert.
82 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 71 Abbildung 4.19: Quant 2 Methode erstellen: Proben (Spektren) einem Datensatz zuordnen Die Kollinearität der Konzentrationen der einzelnen Analyten kann durch Betätigen der Schaltfläche Komp.-Korrelationen in Abbildung 4.18 überprüft werden. Ein Fenster (Abbildung 4.20) öffnet sich, in welchem die Konzentrationsverteilung jedes Komponentenpaars für die Proben anzeigt wird. Je geringer das Bestimmtheitsmaß R 2, desto weniger sind die Analytkonzentrationen kollinear zueinander. Bei einer nicht vermeidbaren hohen Korrelation der Analytkonzentrationen ist die Auswahl der spektralen Bereiche durch den Benutzer entscheidend für eine gute Modellentwicklung.
83 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 72 Abbildung 4.20: Quant 2 Methode erstellen: Korrelation der Komponenten Falls jede Kalibrationsprobe mehrmals gemessen wurde, muss den Proben die entsprechende Probennummer richtig zugeordnet werden. Es empfiehlt sich, die Spektren z.b. von Probe 1 als 1.0, 1.1, 1.2 usw. abzuspeichern, da unter Quant 2 die Probennummer automatisch den Dateinamen der Spektren zugewiesen werden kann. Hierzu wird mit der Schaltleiste Probennummern in Abbildung 4.18 das Fenster (Abbildung 4.21) geöffnet und dort der Haken Probennummern entsprechend den Dateinamen setzen aktiviert sowie der Button Setzen betätigt. Falls die Spektren unter einem anderen Namen abgespeichert jedoch von jeder Probe gleich viele Wiederholungsmessungen durchgeführt werden, kann die Anzahl der gemessenen Spektren pro Probe vom Benutzer festgelegt werden.
84 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 73 Abbildung 4.21: Quant 2 Methode erstellen: Probennummern setzen Im Fenster Parameter können unterschiedliche Datenvorbehandlungen und spektrale Datenbereiche (Wellenzahlbereiche) durch den Anwender ausgewählt werden (Abbildung 4.22). Die Verwendung des gesamten Spektrums für die Kalibration ist in den meisten Fällen nicht sinnvoll, da es Bereiche gibt, in denen starkes Rauschen auftritt oder Absorptionsbanden von nicht einkalibrierten Nebenkomponenten liegen. Bereiche wie spektrales Rauschen am Anfang und Ende des Spektrums sowie Bereiche mit Totalabsorptionen (Extinktion > 2) sollten vermieden werden. Unter Bereiche interaktiv wählen werden die Wellenzahlbereiche ausgewählt bzw. können mit rechter Maustaste hinzugefügt oder gelöscht werden. Eine Verbesserung des Kalibrationsmodells ist eventuell auch durch eine Datenvorbehandlung der Spektren möglich. Wenn das Kontrollkästchen Datenzentrierung im Fenster Parameter aktiviert ist, werden die spektralen Daten und die Konzentrationswerte vor der PLS-Regression mittelwertzentriert (siehe Kapitel 3.2.2, Seite 20). Diese Skalierung ist in den meisten Fällen vorteilhaft für die Modellentwicklung und wird auch in dieser Arbeit verwendet.
85 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 74 Abbildung 4.22: Quant 2 Methode erstellen: Parameter Im Fall einer Wiederholungsmessung einzelner Proben kann unter Probenstatistik die spektrale statistische Abweichung einer Probenmessung geprüft und die Spektren von potentiellen Ausreißern im Vorfeld der Validierung in der Spektrenliste auf Nicht aktiv gesetzt werden. Die Probenstatistik basiert dabei auf den ausgewählten Wellenzahlbereichen und den vorbehandelten Spektren. In dem Diagramm (Abbildung 4.23) wird der Unterschied zwischen jedem Spektrum einer Probe und dem entsprechenden berechneten Mittelwertspektrum im Verhältnis zur Probennummer graphisch dargestellt. Wenn die Differenz zwischen Spektrum und mittlerem Probenspektrum groß ist, dann deutet dies auf eine schlechte Reproduzierbarkeit der Wiederholungsmessungen hin. Gründe dafür können verschmutzte Messvorrichtungen (z.b. Oberfläche des ATR-Kristalls), veraltete Hintergrundmessungen aber auch eine Überanpassung des Modells durch eine zu hohe Anzahl an verwendeten Faktoren (Hauptkomponenten) sein.
86 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 75 Abbildung 4.23: Quant 2 Methode erstellen: Probenstatistik der Wiederholungsmessungen Im Fenster Validieren wird die Kreuz- oder Test-Set-Validierung der Kalibrationsmethoden durchgeführt (Abbildung 4.24). Mit der Schaltleiste Validieren wird die Validierung der PLS- Methode gestartet. Validiert werden jedoch nur die Methoden der Komponenten, deren Kontrollkästchen als Aktiv markiert sind. Der Fortschritt der Berechnungen wird im Statusbalken angezeigt. Sobald die Berechnungen abgeschlossen sind, wechselt das Programm automatisch auf die Seite Grafik, in der die Validierungsergebnisse in Diagrammform angezeigt werden. In der Spalte Max. Rang kann der Benutzer festlegen, bis zu welchem Rang (Anzahl der Hauptkomponenten) die Validierungen durchgeführt werden sollen. OPUS wählt automatisch als maximalen Rang einen Wert von 10. Es kann jedoch von Vorteil sein, den Rang auf einen geringeren Wert einzuschränken, um z.b. kürzere Berechnungszeiten zu erreichen oder von vornherein unbedeutende Varianzen auszuschließen. Ein zu hoher Rang kann unter Umständen zu komplexen instabilen Modellen führen. Die Anzahl der leave-out Proben bei der Kreuzvalidierung, die pro Berechnungszyklus ausgelassen werden soll, richtet sich nach der Anzahl der Proben im Kalibrationsdatensatz. Ein zu hoher Wert führt zu schlechteren Ergebnissen, da zu viele Proben temporär ausgelassen werden. Niedrige Werte können lange Rechenzeiten verursachen. Als Faustregel gilt, dass die Anzahl der Kalibrationsproben geteilt durch 30 die Anzahl der leave-out Proben sein sollte.
87 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 76 Abbildung 4.24: Quant 2 Methode validieren Mithilfe der Validierung werden wichtige Kenngrößen berechnet wie das Bestimmtheitsmaß R 2 (in %) und der Vorhersagefehler RMSECV bzw. RMSEP (in den Einheiten der Komponenten - hier Gew.-%) sowie RPD und der Bias. Mit diesen Werten können verschiedene Methoden verglichen und beurteilt werden. Gute Werte für R 2 sind größer 90 % für Feststoffund größer 99 % für Flüssigkeitsmessungen [26]. Um den Vorhersagefehler RMSECV bzw. RMSEP unter Berücksichtigung des Konzentrationsbereichs der Kalibrationsproben zu bewerten, kann der RPD-Wert herangezogen werden, welcher das Verhältnis der Standardabweichung der Konzentrationen zum RMSECV- bzw. RMSEP-Wert angibt. Gute Vorhersagemodelle besitzen im Allgemeinen einen RPD-Wert, der größer als 10 ist. Mithilfe der Validierung können ebenfalls Ausreißer erkannt werden, die sich beispielsweise durch überdurchschnittliche Vorhersagefehler auszeichnen. Falls es sich um echte Messfehler bzw. Präparationsfehler handelt, sollten diese Ausreißer aus dem Datensatz entfernt werden. Die Ausreißer sind in den Grafiken Vorhersage vs. Wahr und Differenz vs. Wahr rot gekennzeichnet und können als nicht aktiv definiert werden. In Abbildung 4.25 Vorhersage vs. Wahr werden die vom Modell vorhergesagten Konzentrationen mit den wahren
88 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 77 Konzentrationen (durch Benutzereingabe) gegenübergestellt. Die grüne Linie im Diagramm ist nicht die Ausgleichsgerade sondern die Winkelhalbierende, die dem Idealfall einer 100 %- igen Korrelation zwischen vorhergesagten und durch Einwaage oder Referenzanalytik bekannten Konzentrationen entspricht. Abbildung 4.25: Quant 2 Methode validieren: Grafik Vorhersage vs. Wahr In dem Differenz vs. Wahr Diagramm (Abbildung 4.26) wird die Differenz zwischen den wahren Komponentenwerten C wahr (vom Benutzer eingegeben) und den vorhergesagten Werten C Modell angezeigt. Auf der Y-Achse werden die Abweichungen (C wahr - C Modell ) dargestellt. Auf der X-Achse sind die wahren Konzentrationen C wahr aufgetragen. Im optimalen Fall wären die Differenzen gleich Null, sodass alle Punkte auf der roten Linie (Nulllinie) liegen würden. Jedoch ist dies in der Praxis nicht möglich, da jede Messung und auch die Referenzmessung mit statistischen Fehlern verbunden sind. Die blaue Linie unterhalb der roten Nulllinie in Abbildung 4.26 stellt den Bias dar, dessen Wert auch links im Fenster angegeben wird. Der Bias wird berechnet, indem alle positiven und negativen Abweichungen summiert werden. Falls die Konzentrationswerte in negative und positive Richtung gleichmäßig gestreut sind, ist der Bias Null. Weichen die Werte jedoch systematisch in eine Richtung ab,
89 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 78 dann besitzt der Bias einen entsprechend hohen Wert, was häufig auf einen systematischen Fehler hinweist. Abbildung 4.26: Quant 2 Methode validieren: Grafik Differenz vs. Wahr In Abbildung 4.27 wird der RMSECV gegen den Rang dargestellt. Mithilfe dieses Diagramms kann der optimale Rang ermittelt werden, welcher sich in unmittelbarer Nähe des Minimums der Kurve befindet. Der von der OPUS Software als optimal angesehene Rang wird blau markiert. Allerdings ist es in den meisten Fällen von Vorteil, einen geringeren Rang zu wählen, da das Modell bei einer hohen Anzahl an Faktoren zu optimistisch angepasst werden kann. Außerdem lassen sich bei niedrigen Faktoren besser echte Ausreißer erkennen.
90 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 79 Abbildung 4.27: Quant 2 Methode validieren: Grafik RMSECV vs. Rang Eine weitere Überprüfung des Modells bzw. der Mehrfachmessung der Proben kann durch Abbildung 4.28 erfolgen. Hier wird die Differenz zwischen jedem vorhergesagten Konzentrationswert einer Probe und dem Durchschnittswert der vorhergesagten Werte der entsprechenden Probe in Abhängigkeit der Probennummer dargestellt (grüne Dreiecke im Diagramm). Außerdem wird in der Abbildung 4.28 für jede Mehrfachmessung die Standardabweichung in Form eines blauen Kreuzes angezeigt. Falls für jede Wiederholungsmessung der gleiche Konzentrationswert vorhergesagt wird, dann liegen alle blauen Punkte auf der roten Nulllinie. Manchmal kann ein Modell einen relativ guten RMSECV-Wert besitzen, jedoch werden bei den Wiederholungsmessungen zum großen Teil unterschiedliche Werte ermittelt. Dies ist häufig ein Hinweis auf ein instabiles Modell bzw. eine zu hohe Anzahl an verwendeten Faktoren.
91 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 80 Abbildung 4.28: Quant 2 Methode validieren: Grafik Mehrfachmessung Folgende Abbildung 4.29 kann ebenfalls verwendet werden, um spektrale Ausreißer zu erkennen. In diesem Fenster wird die Mahalanobisdistanz in Abhängigkeit des spektralen Residuums dargestellt. Die Mahalanobisdistanz ist definiert als der euklidische Abstand zwischen dem tatsächlich gemessenen Spektrum (Originalspektrum) der zu analysierenden (Kalibrations-)Probe und dem Mittelwert aller Spektren des Kalibrationsdatensatzes, welcher bei einer Rekonstruktion der spektralen Datenmatrix für die betrachtete Faktorenzahl (Rang) gemäß Gl resultiert. Das spektrale Residuum (SpecRes) ist allgemein die Differenz (euklidische Distanz) zwischen dem Originalspektrum und dem Spektrum der Probe, welches im Rahmen der Faktorzerlegung erwartet wird. Je besser die Rekonstruktion eines faktorzerlegten Spektrums ist, desto kleiner ist das spektrale Residuum. Spektren, die deutlich rechts oben in der Abbildung 4.29 liegen, sind potentielle spektrale Ausreißer, es sei denn die Proben weisen extreme Analytkonzentrationen (Minimum und Maximum des Kalibrationsbereichs) auf. Die Grenze der Mahalanobisdistanz für die Ausreißererkennung liegt bei 0,6 bis 0,8. Höhere Werte weisen auf einen spektralen Ausreißer hin, der eventuell auch von einem zu hoch gewählten Rang herrühren könnte. Die PLS-Regression kann solche spektralen Ausreißer oft verarbeiten. Schwierigkeiten bereiten Ausreißer dann, wenn sie auf
92 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 81 falscher Einwaage bzw. Referenzanalytik basieren, da mit der PLS-Regression diese möglicherweise angepasst und so nicht erkannt werden. Abbildung 4.29: Quant 2 Methode validieren: Grafik Mahalanobisdistanz vs. spektrales Residuum Unter der Grafik Score Koeffizienten (Abbildung 4.30) können die Score-Diagramme angezeigt werden. In dieser Grafik sind auf der x-achse die Score-Werte der ersten Hauptkomponente und auf der y-achse die Scores der zweiten Hauptkomponente gegeneinander aufgetragen. Die Scores beschreiben die Lage (Koordinaten) der Proben im sogenannten Faktorraum. Diese Darstellung wird häufig in der qualitativen Analytik ( Ident-Methode ) angewendet. Liegen die Proben nah beieinander oder bilden sie einzelne Gruppen in diesem Koordinatensystem, so besitzen diese Proben ähnliche Spektren. Liegt ein Messpunkt in x- oder y- Richtung weit entfernt von den anderen, könnte es sich um einen markanten Ausreißer handeln.
93 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 82 Abbildung 4.30: Quant 2 Methode validieren: Score Koeffizienten Der Vektor des Regressionskoeffizienten (Regressionsmatrix A der Ordnung nx1 bei PLS1- Algorithmus) und die PLS-Vektoren (Hauptkomponenten) für das Vorhersagemodell der zu bestimmenden Komponente können durch die Schaltfläche Loadings angesehen werden (Abbildung 4.31). Diese Darstellung ist hilfreich, um den Rang (Anzahl der Hauptkomponenten bzw. der PLS-Vektoren) festzulegen. Im oberen Teil des Fensters sind der Vektor des Regressionskoeffizienten rot und die PLS-Vektoren der verschiedenen Faktoren in anderen Farben dargestellt. Der Vektor des Regressionskoeffizienten ist eine grafische Darstellung der Kalibrationsfunktion A, welcher die Gewichtungen der einzelnen Wellenzahlen im Modell für die Umrechnung in Konzentrationseinheiten anzeigt. Bei der Zuckeranalytik sind die größten Varianzen des Regressionskoeffizienten aufgrund von Konzentrationsänderungen im Bereich der C-H- und C-O-Streckschwingungen zu erwarten.
94 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 83 Abbildung 4.31: Quant 2 Methode validieren: PLS-Regressionskoeffizient (rot) und Hauptkomponenten (PLS-Loadings) vs. Wellenzahl Die PLS-Vektoren (auch PLS-Loadings genannt) beschreiben die Gewichtung der einzelnen Absorptionswerte in Bezug auf ihren Beitrag zur Varianz. In Abbildung 4.32 wird als Beispiel der erste PLS-Vektor (blaue Kurve) mit dem PLS-Vektor des 9. Rangs (rote Kurve) verglichen. Zu erkennen ist, dass der erste Faktor eine große Ähnlichkeit mit dem MIR-Spektrum von Saccharose aufweist, während die Hauptkomponente mit Faktorenzahl bzw. Rang 9 nur noch Varianzen aufgrund von Rauschen beinhaltet und sich durch unspezifische hochfrequente Schwingungen auszeichnet.
95 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 84 Abbildung 4.32: Quant 2 Methode validieren: Loadings vs. Wellenzahl Durch die Menüleiste Report wird ein Reportfenster geöffnet, indem die Informationen der Validierung angezeigt werden (Abbildung 4.33). Es werden die vorhergesagten und wahren Konzentrationswerte der einzelnen Komponenten, die Differenz und die Komponentenwertdichte aufgelistet. Die Komponentenwertdichte gibt Auskunft über die Anzahl der Kalibrationsspektren, die sich in der Nähe des vorhergesagten Konzentrationswertes befinden. Ein hoher Wert der Komponentenwertdichte steht für einen Konzentrationsbereich, in welchem viele Kalibrationsspektren vertreten sind.
96 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 85 Abbildung 4.33: Quant 2 Methode validieren: Reportansicht Die Standardabweichungen der vorhergesagten Konzentrationswerte der Wiederholungsmessungen werden unter Report und Mehrfachmessungen angezeigt (siehe Abbildung 4.34).
97 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 86 Abbildung 4.34: Quant 2 Methode validieren: Reportansicht Standardabweichungen der vorhergesagten Konzentrationswerte bei den Mehrfachmessungen Nach der Optimierung wird die PLS-Methode mit Methode speichern in einem Ordner gespeichert.
98 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 87 Abbildung 4.35: Quant 2 Methode speichern Die Quant 2 Software bietet ein Optimierungsverfahren (Fenster Optimieren, Abbildung 4.36) an, bei welchem das Programm verschiedene Kombinationen von spektralen Bereichen und Datenvorbehandlungen für die Kalibration testet. Für jeden Durchlauf wird die Rangordnung bzw. Faktorisierung mit den geringsten RMSECV-Werten berechnet und aufgelistet.
99 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 88 Abbildung 4.36: Quant 2 Methode automatisch optimieren Wählt man für die Optimierung die Methode Allgemein A, dann wird der gesamte Wellenzahlbereich zunächst in 10 gleich große Teilbereiche unterteilt. Um aus diesen zehn Bereichen die optimale Auswahl treffen zu können, beginnt die Berechnung mit allen zehn Teilbereichen gleichzeitig und schließt sukzessiv einen Teilbereich aus. Dies wird solange fortgeführt, bis der RMSECV- bzw. der RMSEP-Wert sich nicht weiter verbessern. Bei der Einstellung auf Allgemein B wird der komplette Wellenzahlbereich wie bei Methode A in 10 gleich große Teilbereiche unterteilt. Um die optimale Kombination zu ermitteln, beginnt die Berechnung im Gegensatz zur Methode Allgemein A mit einem Spektralbereich und fügt nacheinander weitere Bereiche hinzu. Mit der Optimierungsart NIR werden fünf Wellenlängenbzw. Wellenzahlbereiche verwendet, die für NIR-Applikationen typisch sind. Diese fünf Bereiche werden sowohl einzeln als auch in allen möglichen Kombinationen getestet. Nach der Optimierung werden die Spektralbereiche und Datenvorbehandlungen sowie der optimale Rang aufgelistet. Die Ergebnisse werden mit steigendem RMSECV-Wert dargestellt. Anschließend können die vorgeschlagenen Modelle durch Anklicken Parameter verwenden ausgewählt und die Validierungsergebnisse angesehen werden. Ferner besteht die
100 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 89 Möglichkeit, die Datenvorbehandlungsmethoden und die spektralen Bereiche manuell für die Optimierung unter Einstellungen auszuwählen. Ein erfahrener Analytiker verwendet in Abhängigkeit der Probenbeschaffenheit und Aufnahmetechnik von vornherein nur die geeigneten Datenvorbehandlungsmethoden und grenzt auch den spektralen Bereich entsprechend ein Quant 1 Analyse Mit dem Befehl Quant Analyse in der Menüleiste Auswerten wird eine univariate Analyse mit der Quant 1 Methode durchgeführt. Unter Quant Methode laden in Abbildung 4.37 können einzeln die Methoden für Saccharose, Fructose, Glucose und Gesamtzucker ausgewählt werden. Die Spektren der zu analysierenden Proben werden in das Auswahlfeld Datei(en) für die Quant Analyse eingefügt. Mit der Schaltfläche Analysieren werden die Analytkonzentrationen der Proben vorhergesagt. Abbildung 4.37: Quant 1 Analyse
101 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 90 Das Ergebnis wird in einem Report zusammen mit den analysierten Spektren gespeichert (Abbildung 4.38). In der Kopfzeile des Auswertefensters werden der Name der Analysenmethode und das Erstellungsdatum der Methode angegeben. In der Spalte Komponente sind die Namen der Analyten aufgelistet, die in der Methode spezifiziert werden. Weiterhin wird die vorhergesagte Konzentration, der Vertrauensbereich Sigma, die Maßeinheit (hier in Gew.-%) und die ermittelte Absorptionsfläche oder Extinktion als Integrationswert angezeigt. Abbildung 4.38: Quant 1 Analyse: Ergebnisfenster Der Fehler, der bei der Analyse unbekannter Proben für die Vorhersage der Konzentrationswerte zu erwarten ist, wird durch den Vertrauensbereich der Kalibration σ abgeschätzt: m f i= 1 i ( C Wahr, i CModell, i ) 1 2 σ = (4.3) mit m Anzahl der Kalibrationsspektren und f Zahl der Freiheitsgrade (linear 2, quadratisch 3, kubisch 4) Unter Verwendung des 1-Sigma-Niveaus bezogen auf die Normalverteilung liegt der vorhergesagte Konzentrationswert C ± σ [84]. Modell C Modell mit einer Wahrscheinlichkeit von 68,27 % im Intervall Quant 2 Analyse Mit dem OPUS Fenster Quant 2 Analyse / Dateiliste in der Menüleiste Auswerten werden neue unbekannte Proben mittels der erstellten PLS-Methoden analysiert (siehe Abbildung 4.39). Durch Aktivierung der Schaltfläche Methoden hinzufügen können die Quant 2 Methoden ausgewählt werden. Hierbei wird für jede Komponente der geladenen Quant 2 Methode eine Zeile in der Spektrenliste hinzugefügt.
102 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 91 Abbildung 4.39: Quant 2 Analyse Methode hinzufügen Anschließend werden in der Menüleiste Spektren die zu analysierenden Spektren in OPUS geladen (Abbildung 4.40). Sind die Konzentrationswerte der Proben z.b. durch ein anderes analytisches Verfahren (Referenzmethode) bekannt, können wie im Beispiel die wahren Komponentenwerte in die Komponentenspalte(n) eingegeben werden. OPUS berechnet dann statistische Parameter, mit denen z.b. eine externe Validierung bewertet werden kann. Mit der externen Validierung wird das Kalibrationsmodell in der Praxis getestet.
103 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 92 Abbildung 4.40: Quant 2 Analyse Spektren hinzufügen Mit der Menüleiste Analyse-Ergebnisse und der Schaltfläche Analysieren wird für jedes hinzugefügtes Probenspektrum mit den gewählten Methoden eine Analyse durchgeführt. Die Ergebnisse, wie in Abbildung 4.41 gezeigt, werden dann automatisch dargestellt. In der aufgeführten Ergebnistabelle werden der Datei- und der Probenname, die verwendete Methode, die zu analysierende Komponente sowie wahrer und vorhergesagter Konzentrationswert der einzelnen Komponenten mit zugehöriger Maßeinheit dargestellt. Außerdem werden in dem Fenster die Mahalanobisdistanz (Mah. Dist.) und deren Grenzwert (Grenze) für die Ausreißererkennung, die Ausreißer (in rot dargestellt) und die Dichte der Konzentrationswerte für jede Komponente angegeben. Bei der PLS-Regression werden die Mahalanobisdistanzen aller vorhandenen Kalibrationsspektren berechnet. Aus diesen Werten wird dann der maximal zulässige Grenzwert (Grenze) der Mahalanobisdistanz abgeleitet. Spektren von unbekannten Proben, deren Mahalanobisdistanzen unterhalb dieses Schwellenwerts liegen, werden nicht als Ausreißer markiert. Wenn das Kontrollkästchen Spektrale Residuen aktiviert wird, werden zusätzlich das spektrale Residuum und der F-Wert sowie der FProb-Wert in der Tabelle aufgeführt. Die F-Werte
104 4 Material und Methoden 4.2 Verfolgung der Hefefermentation sowie Obst-, Getränke- und Hefeanalyse mittels MIR-ATR- Spektroskopie 93 können zur Erkennung möglicher Ausreißer herangezogen werden. Je größer diese Werte sind, umso größer ist die Wahrscheinlichkeit, dass es sich bei der Probe um einen Ausreißer handelt. Der F-Wert wird berechnet, indem das Quadrat eines spektralen Residuums (SpecRes) durch den mittleren Wert der anderen Residuen geteilt wird: F-Wert i = ( m 1) ( SpecRes ) m ( SpecRes j ) j i 2 i 2 (4.4) Aus dem F-Wert und der Anzahl der Freiheitsgrade wird der sogenannte FProb-Wert berechnet. Dieser gibt die auf die gesamte Verteilung der F-Werte bezogene Wahrscheinlichkeit für einen spektralen Ausreißer an. Ein FProb-Wert von Null bedeutet, dass die Probe mit einer Wahrscheinlichkeit von 100 % kein Ausreißer ist. Der Grenzwert für die automatische Ausreißererkennung liegt bei 99 %. Abbildung 4.41: Quant 2 Analyse - Ergebnisse Falls die durch eine Referenzmethode bekannten Konzentrationswerte der unabhängigen Proben zuvor in die Komponentenspalte(n) (siehe Abbildung 4.40) eingegeben wurden, dann werden im Fenster Statistik (Abbildung 4.42) für alle geladenen Quant 2 Methoden der je-
Olten (CH) Online Ueberwachung von Bioprozessen mit ATR-IR oder NIR: Vor und Nachteile. [Dr. Florian Eigenmann]
![Olten (CH) Online Ueberwachung von Bioprozessen mit ATR-IR oder NIR: Vor und Nachteile. [Dr. Florian Eigenmann] Olten (CH) Online Ueberwachung von Bioprozessen mit ATR-IR oder NIR: Vor und Nachteile. [Dr. Florian Eigenmann]](/thumbs/75/71489579.jpg) 17.6.2009 Olten (CH) Online Ueberwachung von Bioprozessen mit ATR-IR oder NIR: Vor und Nachteile [Dr. Florian Eigenmann] Agenda Einleitung MIR-NIR, Nachweisgrenzen, Interpretation,... Realisierte Fermentationsreaktionen:
17.6.2009 Olten (CH) Online Ueberwachung von Bioprozessen mit ATR-IR oder NIR: Vor und Nachteile [Dr. Florian Eigenmann] Agenda Einleitung MIR-NIR, Nachweisgrenzen, Interpretation,... Realisierte Fermentationsreaktionen:
Spektroskopie. im IR- und UV/VIS-Bereich. Spektrometer. http://www.analytik.ethz.ch
 Spektroskopie im IR- und UV/VIS-Bereich Spektrometer Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers Lichtintensität d I 0 Probe I
Spektroskopie im IR- und UV/VIS-Bereich Spektrometer Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers Lichtintensität d I 0 Probe I
Einblick in die Technik und das System FTIR
 Einblick in die Technik und das System FTIR Dr. Martin Geßner Fachzentrum Analytik oenologische und pflanzliche Analytik Fouriertransformationsinfrarotspektrometer FTIR Folie 2 FTIR-Vom Zauberwort zur
Einblick in die Technik und das System FTIR Dr. Martin Geßner Fachzentrum Analytik oenologische und pflanzliche Analytik Fouriertransformationsinfrarotspektrometer FTIR Folie 2 FTIR-Vom Zauberwort zur
Sensorlabor II. Versuch: FFT-IR Spektroskopie. Gruppe 1: Oliver Knaus Rodrigo Kuhfs
 Sensorlabor II Versuch: FFT-IR Spektroskopie Gruppe : Oliver Knaus Inhaltsverzeichnis Inhaltsverzeichnis... 2 2 Aufbau und Meßprinzip eines FFT IR Spektrometers... 3 2. Nachweisbare Stoffe... 4 2.2 Verwendete
Sensorlabor II Versuch: FFT-IR Spektroskopie Gruppe : Oliver Knaus Inhaltsverzeichnis Inhaltsverzeichnis... 2 2 Aufbau und Meßprinzip eines FFT IR Spektrometers... 3 2. Nachweisbare Stoffe... 4 2.2 Verwendete
Teil 1 Schwingungsspektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Spektroskopie. im IR- und UV/VIS-Bereich. Proben, Probengefässe, Probenvorbereitung.
 Spektroskopie im IR- und UV/VIS-Bereich Proben, Probengefässe, Probenvorbereitung Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers d
Spektroskopie im IR- und UV/VIS-Bereich Proben, Probengefässe, Probenvorbereitung Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers d
Flüssigkeitschromatographie
 Flüssigkeitschromatographie Flüssigkeitschromatographie Einteilung nach Druck: LC MPLC: HPLC: Liquid chromatography Flüssigkeitschromatographie Medium performance (pressure) LC Mittelleistungs (druck)
Flüssigkeitschromatographie Flüssigkeitschromatographie Einteilung nach Druck: LC MPLC: HPLC: Liquid chromatography Flüssigkeitschromatographie Medium performance (pressure) LC Mittelleistungs (druck)
IR-Spektroskopie. Helmut Günzler Hans-Ulrjch Gremiich. Eine Einfuhrung. Vierte, vollständig überarbeitete und aktualisierte Auflage
 Helmut Günzler Hans-Ulrjch Gremiich IR-Spektroskopie Eine Einfuhrung Vierte, vollständig überarbeitete und aktualisierte Auflage WILEY- VCH WILEY-VCH GmbH & Co. KGaA Inhaltsverzeichnis 1 Einführung 1 1.1
Helmut Günzler Hans-Ulrjch Gremiich IR-Spektroskopie Eine Einfuhrung Vierte, vollständig überarbeitete und aktualisierte Auflage WILEY- VCH WILEY-VCH GmbH & Co. KGaA Inhaltsverzeichnis 1 Einführung 1 1.1
Seminar zum Praktikumsversuch: Optische Spektroskopie. Tilman Zscheckel Otto-Schott-Institut
 Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
 Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Physik 3 exp. Teil. 30. Optische Reflexion, Brechung und Polarisation
 Physik 3 exp. Teil. 30. Optische Reflexion, Brechung und Polarisation Es gibt zwei Möglichkeiten, ein Objekt zu sehen: (1) Wir sehen das vom Objekt emittierte Licht direkt (eine Glühlampe, eine Flamme,
Physik 3 exp. Teil. 30. Optische Reflexion, Brechung und Polarisation Es gibt zwei Möglichkeiten, ein Objekt zu sehen: (1) Wir sehen das vom Objekt emittierte Licht direkt (eine Glühlampe, eine Flamme,
Spektroskopische Methoden
 Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
FTIR-Absorptionsspektroskopie
 Institut für Physik Physikalisches Praktikum für Fortgeschrittene 2000 M 1 FTIR-Absorptionsspektroskopie 1. Versuchsziel Aus den Infrarotspektren erhält man Informationen über das Rotationsund Schwingungsverhalten
Institut für Physik Physikalisches Praktikum für Fortgeschrittene 2000 M 1 FTIR-Absorptionsspektroskopie 1. Versuchsziel Aus den Infrarotspektren erhält man Informationen über das Rotationsund Schwingungsverhalten
Systemtheorie Statischer Fourier-Spektrometer - Modellierung und Implementierung
 Lehrstuhl für Elektrische Messtechnik Technische Universität München Systemtheorie Statischer Fourier-Spektrometer - Modellierung und Implementierung Frank Palme Vollständiger Abdruck der von der Fakultät
Lehrstuhl für Elektrische Messtechnik Technische Universität München Systemtheorie Statischer Fourier-Spektrometer - Modellierung und Implementierung Frank Palme Vollständiger Abdruck der von der Fakultät
FT-IR-Spektroskopie. Jean-Pierre Lindner Thies Nolte
 FT-IR-Spektroskopie Jean-Pierre Lindner Thies Nolte Übersicht - Aufbau und Funktionsweise eines FT-IR- Spektrometers - Beispiele verschiedener Anwendungen - Apparativer Versuch Aufbau eines FT-IR-Spektrometers
FT-IR-Spektroskopie Jean-Pierre Lindner Thies Nolte Übersicht - Aufbau und Funktionsweise eines FT-IR- Spektrometers - Beispiele verschiedener Anwendungen - Apparativer Versuch Aufbau eines FT-IR-Spektrometers
Übungen zur Experimentalphysik 3
 Übungen zur Experimentalphysik 3 Prof. Dr. L. Oberauer Wintersemester 2010/2011 10. Übungsblatt - 10. Januar 2011 Musterlösung Franziska Konitzer (franziska.konitzer@tum.de) Aufgabe 1 ( ) (6 Punkte) a)
Übungen zur Experimentalphysik 3 Prof. Dr. L. Oberauer Wintersemester 2010/2011 10. Übungsblatt - 10. Januar 2011 Musterlösung Franziska Konitzer (franziska.konitzer@tum.de) Aufgabe 1 ( ) (6 Punkte) a)
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Laborpraktikum Sensorik. Versuch. Optische Konzentrations- bestimmung MS 2
 Otto-von-Guericke-Universität Magdeburg Fakultät für Elektrotechnik und Informationstechnik Institut für Mikro- und Sensorsysteme (IMOS) Laborpraktikum Sensorik Versuch Optische Konzentrations- bestimmung
Otto-von-Guericke-Universität Magdeburg Fakultät für Elektrotechnik und Informationstechnik Institut für Mikro- und Sensorsysteme (IMOS) Laborpraktikum Sensorik Versuch Optische Konzentrations- bestimmung
SCHWEIZER JUGEND FORSCHT. Chemie und Materialwissenschaften
 SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Wie Heavy Metal ist der Boden?
 Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Club Apollo 13, 14. Wettbewerb Aufgabe 1.
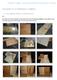 Club Apollo 13, 14. Wettbewerb Aufgabe 1. (1) a) Grundlagenteil: Basteln und Experimentieren Wir haben den Versuchsaufbau entsprechend der Versuchsanleitung aufgebaut. Den Aufbau sowie die Phase des Bauens
Club Apollo 13, 14. Wettbewerb Aufgabe 1. (1) a) Grundlagenteil: Basteln und Experimentieren Wir haben den Versuchsaufbau entsprechend der Versuchsanleitung aufgebaut. Den Aufbau sowie die Phase des Bauens
. Nur wenn ε m (λ 1 ) = ε m (λ 2 ), dann ist E = ε m c d.
 Das Lambert-Beersche Gesetz gilt nur für monochromatisches Licht: Wird eine Substanz mit dem molaren Extinktionskoeffizienten ε m (λ) bei der Wellenlänge λ 1 mit der Intensität I 1 und bei der Wellenlänge
Das Lambert-Beersche Gesetz gilt nur für monochromatisches Licht: Wird eine Substanz mit dem molaren Extinktionskoeffizienten ε m (λ) bei der Wellenlänge λ 1 mit der Intensität I 1 und bei der Wellenlänge
(nunj UNIVERSITÄT K=/ DRESDEN. Alkenylbernsteinsäureanhydrid (ASA) STS TECHNISCHE. Untersuchungen zur Papierleimung mit. Doktor-Ingenieur (Dr.-Ing.
 STS TECHNISCHE (nunj UNIVERSITÄT K=/ DRESDEN MuhBt Font-, Gbo- und Hydrawlsienschaftin Untersuchungen zur Papierleimung mit Alkenylbernsteinsäureanhydrid (ASA) Dissertation zur Erlangung des akademischen
STS TECHNISCHE (nunj UNIVERSITÄT K=/ DRESDEN MuhBt Font-, Gbo- und Hydrawlsienschaftin Untersuchungen zur Papierleimung mit Alkenylbernsteinsäureanhydrid (ASA) Dissertation zur Erlangung des akademischen
Infrarot-Spektroskopie
 SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
Bestimmung der spektralen Strahlungsverteilung eines Infrarot- Strahlers des Typs Trans lucent VWS 500 Q der Firma Inframagic
 Bestimmung der spektralen Strahlungsverteilung eines Infrarot- Strahlers des Typs Trans lucent VWS 500 Q der Firma Inframagic Prüfobjekt: Der zu vermessende Infrarot-Strahler bestehet aus einem Strahlerstab
Bestimmung der spektralen Strahlungsverteilung eines Infrarot- Strahlers des Typs Trans lucent VWS 500 Q der Firma Inframagic Prüfobjekt: Der zu vermessende Infrarot-Strahler bestehet aus einem Strahlerstab
Gutachter: Prof. Dr. Gert Fricker Prof. Dr. Jürgen Reichling.
 Echtzeit NIR Spektroskopie und At-Iine NIR Chemical Imaging als PAT Tools zur Bestimmung der Homogenität von Pulvermischungen in der frühen pharmazeutischen Entwicklung Gutachter: Prof. Dr. Gert Fricker
Echtzeit NIR Spektroskopie und At-Iine NIR Chemical Imaging als PAT Tools zur Bestimmung der Homogenität von Pulvermischungen in der frühen pharmazeutischen Entwicklung Gutachter: Prof. Dr. Gert Fricker
Bayerische Landesanstalt für Landwirtschaft Abteilung Qualitätssicherung und Untersuchungswesen
 Bayerische Landesanstalt für Landwirtschaft Abteilung Qualitätssicherung und Untersuchungswesen 20.02.2014 Weiterentwicklung spektroskopischer Schnellverfahren zum Nachweis von Kleberproteinen bei Weizenkorn
Bayerische Landesanstalt für Landwirtschaft Abteilung Qualitätssicherung und Untersuchungswesen 20.02.2014 Weiterentwicklung spektroskopischer Schnellverfahren zum Nachweis von Kleberproteinen bei Weizenkorn
Übungsaufgaben zur HPLC für Biolaboranten
 Übungsaufgaben zur HPLC für Biolaboranten 1.1 Trennung von Paracetamol und HPLC Im LTC-Praktikum wurde in einer Kalibrierlösung Paracetamol und Coffein über eine HPLC getrennt. Bedingungen: β(cof) = 12,5
Übungsaufgaben zur HPLC für Biolaboranten 1.1 Trennung von Paracetamol und HPLC Im LTC-Praktikum wurde in einer Kalibrierlösung Paracetamol und Coffein über eine HPLC getrennt. Bedingungen: β(cof) = 12,5
 Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Schwingungsspektroskopie
 In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
Optische Eigenschaften fester Stoffe. Licht im neuen Licht Dez 2015
 Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Eigenschaften von Halbleitern mit der Fourier-Transform-Infrarot-Spektroskopie
 D Eigenschaften von Halbleitern mit der Fourier-Transform-Infrarot-Spektroskopie Wissenschaftliche Arbeit im Fach Physik Eingereicht von Carsten Bundesmann Universität Leipzig Fakultät für Physik und Geowissenschaften
D Eigenschaften von Halbleitern mit der Fourier-Transform-Infrarot-Spektroskopie Wissenschaftliche Arbeit im Fach Physik Eingereicht von Carsten Bundesmann Universität Leipzig Fakultät für Physik und Geowissenschaften
TIVITA Tissue System. » High Performance Hyperspectral Imaging Kontinuierliche Echtzeit VIS/NIR Hyperspektrale Kamera.
 TIVITA Tissue System» High Performance Hyperspectral Imaging Kontinuierliche Echtzeit VIS/NIR Hyperspektrale Kamera» Datenblatt www.diaspective-vision.com 1 NICHTINVASIVE ERFASSUNG VON GEWEBEOXYGENIERUNG,
TIVITA Tissue System» High Performance Hyperspectral Imaging Kontinuierliche Echtzeit VIS/NIR Hyperspektrale Kamera» Datenblatt www.diaspective-vision.com 1 NICHTINVASIVE ERFASSUNG VON GEWEBEOXYGENIERUNG,
HANDOUT. Vorlesung: Glasanwendungen. Überblick optische Eigenschaften
 Materialwissenschaft und Werkstofftechnik an der Universität des Saarlandes HANDOUT Vorlesung: Glasanwendungen Überblick optische Eigenschaften Leitsatz: 21.04.2016 Die Ausbreitung von Licht durch ein
Materialwissenschaft und Werkstofftechnik an der Universität des Saarlandes HANDOUT Vorlesung: Glasanwendungen Überblick optische Eigenschaften Leitsatz: 21.04.2016 Die Ausbreitung von Licht durch ein
Atomabsorptionsspektrometrie (AAS)
 Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Spektroskopie-Seminar SS Infrarot-Spektroskopie. Infrarot-Spektroskopie
 Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Spektroskopie-Seminar WS 17/18 3 Infrarot-Spektroskopie. Infrarot-Spektroskopie
 WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002
 Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Fernerkundung mittels Infrarotspektrometrie: Anwendungen. Grundlagen Fernerkundungssystem SIGIS Abbildendes Fourier-Spektrometer Gaskamera
 Fernerkundung mittels Infrarotspektrometrie: Anwendungen Grundlagen Fernerkundungssystem SIGIS Abbildendes Fourier-Spektrometer Gaskamera Fernerkundung von Gefahrstoffen mittels Infrarotspektrometrie Spektrometer
Fernerkundung mittels Infrarotspektrometrie: Anwendungen Grundlagen Fernerkundungssystem SIGIS Abbildendes Fourier-Spektrometer Gaskamera Fernerkundung von Gefahrstoffen mittels Infrarotspektrometrie Spektrometer
Wie das unsichtbare Infrarotweltall seine Geheimnisse Preis gibt Cecilia Scorza
 Wie das unsichtbare Infrarotweltall seine Geheimnisse Preis gibt Cecilia Scorza Einen großen Teil ihrer Information über die kosmischen Objekte erhalten die Astronomen im Infrarotbereich, einem Bereich
Wie das unsichtbare Infrarotweltall seine Geheimnisse Preis gibt Cecilia Scorza Einen großen Teil ihrer Information über die kosmischen Objekte erhalten die Astronomen im Infrarotbereich, einem Bereich
Photom etrieren Photometrie Fraunhofer sche Linien
 17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
Optik. Lichtstrahlen -Wellen - Photonen. Wolfgang Zinth Ursula Zinth. von. 4., aktualisierte Auflage. OldenbourgVerlag München
 Optik Lichtstrahlen -Wellen - Photonen von Wolfgang Zinth Ursula Zinth 4., aktualisierte Auflage OldenbourgVerlag München Inhaltsverzeichnis Vorwort 1 Einführung und historischer Überblick v 1 Licht als
Optik Lichtstrahlen -Wellen - Photonen von Wolfgang Zinth Ursula Zinth 4., aktualisierte Auflage OldenbourgVerlag München Inhaltsverzeichnis Vorwort 1 Einführung und historischer Überblick v 1 Licht als
Technische Raytracer
 University of Applied Sciences 05. Oktober 2016 Technische Raytracer 2 s 2 (1 (n u) 2 ) 3 u 0 = n 1 n 2 u n 4 n 1 n 2 n u 1 n1 n 2 5 Licht und Spektrum 19.23 MM Double Gauss - U.S. Patent 2,532,751 Scale:
University of Applied Sciences 05. Oktober 2016 Technische Raytracer 2 s 2 (1 (n u) 2 ) 3 u 0 = n 1 n 2 u n 4 n 1 n 2 n u 1 n1 n 2 5 Licht und Spektrum 19.23 MM Double Gauss - U.S. Patent 2,532,751 Scale:
Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU
 Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU 1 Agilent engagiert sich für Ausbildung und Lehre und möchte den Zugang zu firmeneigenem Material ermöglichen. Diese
Die Grundlagen der Spektroskopie: Theorie FÜR EINE BESSERE WISSENSCHAFT AGILENT AND YOU 1 Agilent engagiert sich für Ausbildung und Lehre und möchte den Zugang zu firmeneigenem Material ermöglichen. Diese
Max Planck: Das plancksche Wirkungsquantum
 Max Planck: Das plancksche Wirkungsquantum Überblick Person Max Planck Prinzip schwarzer Strahler Klassische Strahlungsgesetze Planck sches Strahlungsgesetz Beispiele kosmische Hintergrundstrahlung Sternspektren
Max Planck: Das plancksche Wirkungsquantum Überblick Person Max Planck Prinzip schwarzer Strahler Klassische Strahlungsgesetze Planck sches Strahlungsgesetz Beispiele kosmische Hintergrundstrahlung Sternspektren
Anwendungsbeispiele für die FT-IR-Spektroskopie
 Institut für Prozessmesstechnik und innovative Energiesysteme (PI) Institut für Chemische Verfahrenstechnik Anwendungsbeispiele für die FT-IR-Spektroskopie Bruker Optik Anwendertreffen 2016 M.Sc. Tobias
Institut für Prozessmesstechnik und innovative Energiesysteme (PI) Institut für Chemische Verfahrenstechnik Anwendungsbeispiele für die FT-IR-Spektroskopie Bruker Optik Anwendertreffen 2016 M.Sc. Tobias
TIVITA Tissue. » High Performance Hyperspectral Imaging Kontinuierliche Echtzeit VIS/NIR Hyperspektrale Kamera. » Datenblatt
 » High Performance Hyperspectral Imaging Kontinuierliche Echtzeit VIS/NIR Hyperspektrale Kamera» Datenblatt www.diaspective-vision.com 1 NICHTINVASIVE ERFASSUNG VON GEWEBEOXYGENIERUNG, NIR-PERFUSION, GEWEBE-
» High Performance Hyperspectral Imaging Kontinuierliche Echtzeit VIS/NIR Hyperspektrale Kamera» Datenblatt www.diaspective-vision.com 1 NICHTINVASIVE ERFASSUNG VON GEWEBEOXYGENIERUNG, NIR-PERFUSION, GEWEBE-
Physik und Sensorik. Photodetektoren. Chemnitz 8. Oktober 2017 Prof. Dr. Uli Schwarz
 Photodetektoren Optische Sensoren Z.B. Transmission durch Gewebe Lichtquelle Gewebe Photodetektor Verstärker Bildquelle: http://www2.hs-esslingen.de/~johiller/pulsoximetrie/pics/po06.jpg 2 Photodetektoren
Photodetektoren Optische Sensoren Z.B. Transmission durch Gewebe Lichtquelle Gewebe Photodetektor Verstärker Bildquelle: http://www2.hs-esslingen.de/~johiller/pulsoximetrie/pics/po06.jpg 2 Photodetektoren
18.Elektromagnetische Wellen 19.Geometrische Optik. Spektrum elektromagnetischer Wellen Licht. EPI WS 2006/7 Dünnweber/Faessler
 Spektrum elektromagnetischer Wellen Licht Ausbreitung von Licht Verschiedene Beschreibungen je nach Größe des leuchtenden (oder beleuchteten) Objekts relativ zur Wellenlänge a) Geometrische Optik: Querdimension
Spektrum elektromagnetischer Wellen Licht Ausbreitung von Licht Verschiedene Beschreibungen je nach Größe des leuchtenden (oder beleuchteten) Objekts relativ zur Wellenlänge a) Geometrische Optik: Querdimension
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
Standard Optics Information
 SUPRASIL 1, 2 (Grade A & B) und SUPRASIL Standard 1. ALLGEMEINE PRODUKTBESCHREIBUNG SUPRASIL 1, 2 (Grade A & B) und SUPRASIL Standard sind hochreine synthetische Quarzglassorten, die durch die Flammenhydrolyse
SUPRASIL 1, 2 (Grade A & B) und SUPRASIL Standard 1. ALLGEMEINE PRODUKTBESCHREIBUNG SUPRASIL 1, 2 (Grade A & B) und SUPRASIL Standard sind hochreine synthetische Quarzglassorten, die durch die Flammenhydrolyse
Physikalische Grundlagen zur Wärmegewinnung aus Sonnenenergie
 7 Physikalische Grundlagen zur Wärmegewinnung aus Sonnenenergie Umwandlung von Licht in Wärme Absorptions- und Emissionsvermögen 7.1 Umwandlung von Licht in Wärme Zur Umwandlung von Solarenergie in Wärme
7 Physikalische Grundlagen zur Wärmegewinnung aus Sonnenenergie Umwandlung von Licht in Wärme Absorptions- und Emissionsvermögen 7.1 Umwandlung von Licht in Wärme Zur Umwandlung von Solarenergie in Wärme
Inkohärente Lichtquellen NIR-Strahlungsquellen
 Inkohärente Lichtquellen NIR-Strahlungsquellen Marc Scheffer Physikalische Technik 30.04.2014 Inhalt 1. Historischer Hintergrund der IR-Strahlung 2. Einteilung der Infrarotstrahlung 3. Arten von NIR-Strahlungsquellen
Inkohärente Lichtquellen NIR-Strahlungsquellen Marc Scheffer Physikalische Technik 30.04.2014 Inhalt 1. Historischer Hintergrund der IR-Strahlung 2. Einteilung der Infrarotstrahlung 3. Arten von NIR-Strahlungsquellen
Komponenten, Aufbau und Funktionsweise einer. Glasfaserdatenübertragung
 Komponenten, Aufbau und Funktionsweise einer Folie 1 Folie Optische Kommunikation (1) 1880 Photophon (Graham Bell) Sonnenlicht Spiegel Halbleiter Lautsprecher Änderung der Lichtstärke Übertragung von der
Komponenten, Aufbau und Funktionsweise einer Folie 1 Folie Optische Kommunikation (1) 1880 Photophon (Graham Bell) Sonnenlicht Spiegel Halbleiter Lautsprecher Änderung der Lichtstärke Übertragung von der
Wärmestrahlung. Einfallende Strahlung = absorbierte Strahlung + reflektierte Strahlung
 Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
V. Optik in Halbleiterbauelementen
 V.1: Einführung V. Optik in Halbleiterbauelementen 1. Kontakt 1. 3.. 1. Kontakt Abb. VI.1: Spontane Emission an einem pn-übergang Rekombination in der LED: - statistisch auftretender Prozess - Energie
V.1: Einführung V. Optik in Halbleiterbauelementen 1. Kontakt 1. 3.. 1. Kontakt Abb. VI.1: Spontane Emission an einem pn-übergang Rekombination in der LED: - statistisch auftretender Prozess - Energie
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
= 6,63 10 J s 8. (die Plancksche Konstante):
 35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
NIR-Spektroskopie & Chemmetrie
 NIR-Spektroskopie & Chemmetrie www.hiperscan.com, 28-Feb-16, Folie 1 NIR-Spektroskopie Eignung der Methode NIR-Spektroskopie Methode für verschiedene pharmazeutische Analysen, insbesondere auch für die
NIR-Spektroskopie & Chemmetrie www.hiperscan.com, 28-Feb-16, Folie 1 NIR-Spektroskopie Eignung der Methode NIR-Spektroskopie Methode für verschiedene pharmazeutische Analysen, insbesondere auch für die
Ungefilterte Detektoren für LED-Photometrie PhotoLED
 Ungefilterte Detektoren für LED-Photometrie PhotoLED Schneider, P., Sperling, A. Fachbereich 4.1 Photometrie und angewandte Radiometrie Physikalisch-Technische Bundesanstalt (PTB), Braunschweig, Germany
Ungefilterte Detektoren für LED-Photometrie PhotoLED Schneider, P., Sperling, A. Fachbereich 4.1 Photometrie und angewandte Radiometrie Physikalisch-Technische Bundesanstalt (PTB), Braunschweig, Germany
Festkorperspektroskopie
 Hans Kuzmany Festkorperspektroskopie Eine Einführung Mit 222 Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris Tokyo Hong Kong 1. Einleitung 1 2. Grundlagen der Festkörperphysik 4 2.1
Hans Kuzmany Festkorperspektroskopie Eine Einführung Mit 222 Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris Tokyo Hong Kong 1. Einleitung 1 2. Grundlagen der Festkörperphysik 4 2.1
Ist die Chromatographie in der Weinanalytik noch zeitgemäß?
 Ist die Chromatographie in der Weinanalytik noch zeitgemäß? Ein Methodenvergleich und Fallstudien sowie die tägliche Herausforderung in der Analytik Dr. G. Barka Die häufigsten Bestimmungen in einem Weinlabor
Ist die Chromatographie in der Weinanalytik noch zeitgemäß? Ein Methodenvergleich und Fallstudien sowie die tägliche Herausforderung in der Analytik Dr. G. Barka Die häufigsten Bestimmungen in einem Weinlabor
Wellenlänge, Wellenzahl, Lichtgeschwindigkeit
 Das -Feld Wellenlänge, Wellenzahl, Lichtgeschwindigkeit Harmonische Welle: macht harmonische Schwingung sin[ωt + φ( r)] an jedem Punkt im Raum; variiert bei festem t sinusförmig entlang z Wellenfronten
Das -Feld Wellenlänge, Wellenzahl, Lichtgeschwindigkeit Harmonische Welle: macht harmonische Schwingung sin[ωt + φ( r)] an jedem Punkt im Raum; variiert bei festem t sinusförmig entlang z Wellenfronten
Versuchsprotokoll. Mathematisch-Naturwissenschaftliche Fakultät I Institut für Physik. Versuch O8: Fraunhofersche Beugung Arbeitsplatz Nr.
 Mathematisch-Naturwissenschaftliche Fakultät I Institut für Physik Physikalisches Grundpraktikum I Versuchsprotokoll Versuch O8: Fraunhofersche Beugung Arbeitsplatz Nr. 1 0. Inhaltsverzeichnis 1. Einleitung.
Mathematisch-Naturwissenschaftliche Fakultät I Institut für Physik Physikalisches Grundpraktikum I Versuchsprotokoll Versuch O8: Fraunhofersche Beugung Arbeitsplatz Nr. 1 0. Inhaltsverzeichnis 1. Einleitung.
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
NG Brechzahl von Glas
 NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
NG Brechzahl von Glas Blockpraktikum Frühjahr 2007 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Geometrische Optik und Wellenoptik.......... 2 2.2 Linear polarisiertes
Medizinische Biophysik 6
 Eigenschaften des Lichtes Medizinische Biophysik 6 Geradlinige Ausbreitung Energietransport Licht in der Medizin. 1 Geometrische Optik Wellennatur Teilchennatur III. Teilchencharakter des Lichtes a) Lichtelektrischer
Eigenschaften des Lichtes Medizinische Biophysik 6 Geradlinige Ausbreitung Energietransport Licht in der Medizin. 1 Geometrische Optik Wellennatur Teilchennatur III. Teilchencharakter des Lichtes a) Lichtelektrischer
Protokoll: Infrarotspektroskopie
 Protokoll: Infrarotspektroskopie Durchführung und Beobachtung 1. Backgroundmessung im leeren Gerät Man erkennt, dass das Gerät ausreichend mit getrockneter Luft gespült wurde. Durch die Backgroundmessung
Protokoll: Infrarotspektroskopie Durchführung und Beobachtung 1. Backgroundmessung im leeren Gerät Man erkennt, dass das Gerät ausreichend mit getrockneter Luft gespült wurde. Durch die Backgroundmessung
Physikalische Analytik
 Labor im Lehrfach Physikalische Analytik Studiengang Applied Life Sciences Versuch IR-Spektroskopie Standort Zweibrücken Gruppe: Teilnehmer: Verfasser: Semester: Versuchsdatum: Bemerkungen: Inhalt 1. Einführung
Labor im Lehrfach Physikalische Analytik Studiengang Applied Life Sciences Versuch IR-Spektroskopie Standort Zweibrücken Gruppe: Teilnehmer: Verfasser: Semester: Versuchsdatum: Bemerkungen: Inhalt 1. Einführung
Physik, grundlegendes Anforderungsniveau
 Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Das Versagen der klassischen Physik Die Entwicklung der Quantenphysik. Quantenmechanische Lösung
 Das Versagen der klassischen Physik Die Entwicklung der Quantenphysik Problem Thermisches Strahlungsspektrum Photoelektrischer Effekt, Compton Effekt Quantenmechanische Lösung Planck sche Strahlungsformel:
Das Versagen der klassischen Physik Die Entwicklung der Quantenphysik Problem Thermisches Strahlungsspektrum Photoelektrischer Effekt, Compton Effekt Quantenmechanische Lösung Planck sche Strahlungsformel:
Vortrag 2: Kohärenz VON JANIK UND JONAS
 Vortrag 2: Kohärenz VON JANIK UND JONAS Vortrag 2: Kohärenz Inhalt: Kohärenz im Allgemeinen Kohärenzlänge Kohärenzbedingungen Zeitliche Kohärenz Räumliche Kohärenz MICHELSON Interferometer zum Nachweis
Vortrag 2: Kohärenz VON JANIK UND JONAS Vortrag 2: Kohärenz Inhalt: Kohärenz im Allgemeinen Kohärenzlänge Kohärenzbedingungen Zeitliche Kohärenz Räumliche Kohärenz MICHELSON Interferometer zum Nachweis
Ferienkurs Experimentalphysik 3
 Ferienkurs Experimentalphysik 3 Musterlösung Montag 14. März 2011 1 Maxwell Wir bilden die Rotation der Magnetischen Wirbelbleichung mit j = 0: ( B) = +µµ 0 ɛɛ 0 ( E) t und verwenden wieder die Vektoridenditäet
Ferienkurs Experimentalphysik 3 Musterlösung Montag 14. März 2011 1 Maxwell Wir bilden die Rotation der Magnetischen Wirbelbleichung mit j = 0: ( B) = +µµ 0 ɛɛ 0 ( E) t und verwenden wieder die Vektoridenditäet
Anfängerpraktikum D11 - Röntgenstrahlung
 Anfängerpraktikum D11 - Röntgenstrahlung Vitali Müller, Kais Abdelkhalek Sommersemester 2009 1 Messung des ersten Spektrums 1.1 Versuchsaufbau und Hintergrund Es sollte das Spektrum eines Röntgenapparates
Anfängerpraktikum D11 - Röntgenstrahlung Vitali Müller, Kais Abdelkhalek Sommersemester 2009 1 Messung des ersten Spektrums 1.1 Versuchsaufbau und Hintergrund Es sollte das Spektrum eines Röntgenapparates
Physik für Naturwissenschaften. Dr. Andreas Reichert
 Physik für Naturwissenschaften Dr. Andreas Reichert Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Termine Klausur: 5. Februar?, 12-14 Uhr,
Physik für Naturwissenschaften Dr. Andreas Reichert Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Modulhandbuch Termine Klausur: 5. Februar?, 12-14 Uhr,
Flavonoide in Zitronensaft. Stabilität und antioxidative Wirkung
 Medizin Vanessa Schuh Flavonoide in Zitronensaft. Stabilität und antioxidative Wirkung Masterarbeit UNTERSUCHUNGEN ZUR STABILITÄT UND ANTIOXIDATIVEN WIRKUNG VON FLAVONOIDEN IM ZITRONENSAFT Masterarbeit
Medizin Vanessa Schuh Flavonoide in Zitronensaft. Stabilität und antioxidative Wirkung Masterarbeit UNTERSUCHUNGEN ZUR STABILITÄT UND ANTIOXIDATIVEN WIRKUNG VON FLAVONOIDEN IM ZITRONENSAFT Masterarbeit
TANGO-T und NIR-Messungen an Flüssigkeiten. Dr. Andreas Niemöller
 TANGO-T und NIR-Messungen an Flüssigkeiten Dr. Andreas Niemöller Die TANGO-Geschichte geht weiter Das TANGO-T für Transmissionsmessungen Das TANGO für Transmissionsmessungen Ein Messkanal InGaAs-Detektor,
TANGO-T und NIR-Messungen an Flüssigkeiten Dr. Andreas Niemöller Die TANGO-Geschichte geht weiter Das TANGO-T für Transmissionsmessungen Das TANGO für Transmissionsmessungen Ein Messkanal InGaAs-Detektor,
ÜBER DIE TYPISCHE MINDESTSPANNUNG AN MONOCHROMATISCHEN LEUCHTDIODEN
 ÜBER DIE TYPISCHE MINDESTSPANNUNG AN MONOCHROMATISCHEN LEUCHTDIODEN Eugen Grycko, Werner Kirsch, Tobias Mühlenbruch Fakultät für Mathematik und Informatik FernUniversität Universitätsstrasse 1 D-58084
ÜBER DIE TYPISCHE MINDESTSPANNUNG AN MONOCHROMATISCHEN LEUCHTDIODEN Eugen Grycko, Werner Kirsch, Tobias Mühlenbruch Fakultät für Mathematik und Informatik FernUniversität Universitätsstrasse 1 D-58084
(21. Vorlesung: III) Elektrizität und Magnetismus 21. Wechselstrom 22. Elektromagnetische Wellen )
 . Vorlesung EP (. Vorlesung: III) Elektrizität und Magnetismus. Wechselstrom. Elektromagnetische Wellen ) IV) Optik = Lehre vom Licht. Licht = sichtbare elektromagnetische Wellen 3. Geometrische Optik
. Vorlesung EP (. Vorlesung: III) Elektrizität und Magnetismus. Wechselstrom. Elektromagnetische Wellen ) IV) Optik = Lehre vom Licht. Licht = sichtbare elektromagnetische Wellen 3. Geometrische Optik
Metamaterialien mit negativem Brechungsindexeffekt. Vortrag im Rahmen des Hauptseminars SS2008 Von Vera Eikel
 Metamaterialien mit negativem Brechungsindexeffekt Vortrag im Rahmen des Hauptseminars SS8 Von Vera Eikel Brechungsindex n 1 n Quelle: http://www.pi.uni-stuttgart.de Snellius sches Brechungsgesetz: sin
Metamaterialien mit negativem Brechungsindexeffekt Vortrag im Rahmen des Hauptseminars SS8 Von Vera Eikel Brechungsindex n 1 n Quelle: http://www.pi.uni-stuttgart.de Snellius sches Brechungsgesetz: sin
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
EP 2 264 414 A1 (19) (11) EP 2 264 414 A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: 22.12.2010 Patentblatt 2010/51
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 264 414 A1 (43) Veröffentlichungstag: 22.12.2010 Patentblatt 2010/51 (51) Int Cl.: G01J 1/04 (2006.01) G01J 1/42 (2006.01) (21) Anmeldenummer: 09007968.2
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 264 414 A1 (43) Veröffentlichungstag: 22.12.2010 Patentblatt 2010/51 (51) Int Cl.: G01J 1/04 (2006.01) G01J 1/42 (2006.01) (21) Anmeldenummer: 09007968.2
6 Elektromagnetische Schwingungen und Wellen. E y. E(z=0) Polarisation Richtung des E-Vektors gibt die Polarisation an.
 6 Elektromagnetische Schwingungen und Wellen E y E(z=0) E 0 z E y E 0 t Abbildung 6.10: (a) E(z, t = t 1 ): Momentaufnahme für t = t 1. (b) E(z = z 1, t): Zeitabhängigkeit an festem Ort z = z 1. Polarisation
6 Elektromagnetische Schwingungen und Wellen E y E(z=0) E 0 z E y E 0 t Abbildung 6.10: (a) E(z, t = t 1 ): Momentaufnahme für t = t 1. (b) E(z = z 1, t): Zeitabhängigkeit an festem Ort z = z 1. Polarisation
Observatoriumspraktikum WS 2006/07. Teil 1 CCD-Kamera Dunkelstrombestimmung
 Observatoriumspraktikum WS 2006/07 Teil 1 CCD-Kamera Dunkelstrombestimmung Matr. Nr.: 04000944 Christoph Saulder Theorie Eine CCD (Charge-coupled Device) ist ein Photodetektor, welcher ein Signal, welches
Observatoriumspraktikum WS 2006/07 Teil 1 CCD-Kamera Dunkelstrombestimmung Matr. Nr.: 04000944 Christoph Saulder Theorie Eine CCD (Charge-coupled Device) ist ein Photodetektor, welcher ein Signal, welches
Vorlesung Physik für Pharmazeuten PPh - 10a. Optik
 Vorlesung Physik für Pharmazeuten PPh - 10a Optik 15.01.2007 1 Licht als elektromagnetische Welle 2 E B Licht ist eine elektromagnetische Welle 3 Spektrum elektromagnetischer Wellen: 4 Polarisation Ein
Vorlesung Physik für Pharmazeuten PPh - 10a Optik 15.01.2007 1 Licht als elektromagnetische Welle 2 E B Licht ist eine elektromagnetische Welle 3 Spektrum elektromagnetischer Wellen: 4 Polarisation Ein
Neuartiges optisches Messverfahren für Schall. Applikationsbeispiel: Ermüdungsprüfung
 21. Kolloquium Schallemission Vortrag 10 More info about this article: http://www.ndt.net/?id=21576 Neuartiges optisches Messverfahren für Schall. Applikationsbeispiel: Ermüdungsprüfung Kurzfassung Thomas
21. Kolloquium Schallemission Vortrag 10 More info about this article: http://www.ndt.net/?id=21576 Neuartiges optisches Messverfahren für Schall. Applikationsbeispiel: Ermüdungsprüfung Kurzfassung Thomas
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
Applikationsfeld / Industriezweig:
 Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Optik. Lichtstra h len - Wellen - Photonen. Wolfgang Zinth Ursula Zinth. Oldenbourg Verlag München. 3-, verbesserte Auflage. von
 Optik Lichtstra h len - Wellen - Photonen von Wolfgang Zinth Ursula Zinth 3-, verbesserte Auflage Oldenbourg Verlag München Inhaltsverzeichnis Vorwort V 1 Einführung und historischer Überblick 1 2 Licht
Optik Lichtstra h len - Wellen - Photonen von Wolfgang Zinth Ursula Zinth 3-, verbesserte Auflage Oldenbourg Verlag München Inhaltsverzeichnis Vorwort V 1 Einführung und historischer Überblick 1 2 Licht
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
