4. Bohr, Stern, Gerlach, Pauli, Goudsmit, Uhlenbeck der Spin des Elektrons und die 'Fermistatistik'
|
|
|
- Cornelius Neumann
- vor 7 Jahren
- Abrufe
Transkript
1 4. Bohr, Stern, Gerlach, Pauli, Goudsmit, Uhlenbeck der Spin des Elektrons und die 'Fermistatistik' Gegen Ende des 19. Jahrhunderts stand die Frage nach Ursprung und Gesetzmäßigkeit der vielfältigen im optischen Bereich beobachteten Spektrallinien im Fokus der Atomphysik. Im Jahr 1885 veröffentlichte der Basler Zeichenlehrer Jakob Balmer eine empirisch gefundene Formel, die 'Balmerformel', mit der sich die im optischen Bereich beobachteten Wasserstofflinien verblüffend gut wiedergeben ließen: 1/λ = ν/c = RH (1/2 2-1/n 2 ) (4.1) mit der 'Rydbergkonstanten' R H = cm -1 (R H x hc = 1/2 m e c 2 α 2 = 13,6 ev) und n = 3, 4,... Für n = 3 ergibt sich z.b. 1/λ = 15241,25 cm -1, also λ = 6,56 x 10-5 cm = 656 nm, eine der stärksten sichtbaren Emissionslinien des Wasserstoffs. Später entdeckte T. Lyman Linien im UV, die sich alle gemäß 1/λ = RH (1/1 2-1/n 2 ) (4.1a) beschreiben ließen, mit n = 2, 3... ('Lymanserie'). Offenbar steckte eine einfache aber noch völlig unbekannte Gesetzmäßigkeit hinter allen diesen Linien. Niels Bohr, der als einer der wenigen Plancks Wirkungsquantum und die Einsteinsche Deutung des Photoeffekts 'ernst' genommen hatte, veröffentlichte daraufhin 1912 das 'Bohrsche Atommodell'; in dem sich die Elektronen auf diskreten Bahnen um den Kern bewegen, und dann gelegentlich in tiefere Bahnen 'springen', unter Emission von Photonen, deren Wellenlängen exakt durch Gl. (4.1, 41a), bzw. deren Analoga R H (1/3 2-1/n 2 ), n = 4,5...; R H (1/4 2-1/n 2 ), n = 5,6...; usw. beschrieben werden. Der (Bahn)-Drehimpuls L dieser Elektronen ist dabei quantisiert, L = nh, mit der 'Hauptquantenzahl n', deren wahre Bedeutung den Physikern erst nach der Formulierung der Quantenmechanik durch Heisenberg und Schrödinger, der Entdeckung des Eigendrehimpulses (Spin) S = 1/2 h des Elektrons (s. Kap. 5) und der Einführung des 'Pauliprinzips' ganz bewusst wurde. Die (negative) Bindungsenergie E n eines Elektrons im Wasserstoff auf der n-ten Bohrschen Bahn (mit Bahndrehimpuls L = n h) ist dann (α = e 2 /(hc) 1/137): En = - 1/2 x 1/n 2 me 2 c 2 α 2 = -1/2 x 1/n 2 x 27,2 ev und die 'Übergangsenergie' eines Photons vom Zustand 'm' in den Zustand 'n' : Em - En = hνnm= 13,6 ev (1/n 2-1/m 2 ) (4.2) 27
2 Zur 50. Wiederkehr der von Niels Bohr ( ) im Jahr 1913 aufgestellten 'Quantenbedingungen' für die Photonenenergien hν im Atom Otto Stern Walther Gerlach
3 Obwohl dieses Modell sehr erfolgreich war, blieben einige wesentliche Fragen offen, insbesondere die Dublettaufspaltung der Linien und die zusätzliche Linienaufspaltung im Magnetfeld (Zeemaneffekt). Der Durchbruch zur 'richtigen' Beschreibung des Wasserstoffatoms kam dann durch die Kombination von vier 'Essenzen': 1. Dualismus von Welle und Teilchen (de Broglie 1924). 2. Quantenmechanik in den Formen der 'Matrizenmechanik' Heisenbergs (1925) und der äquivalenten Wellenmechanik Schrödingers ( ). 3. Entdeckung der Richtungsquantelung durch Stern und Gerlach (1922) und deren Deutung als Widerspiegelung des halbzahligen Elektronenspins durch Goudsmit und Uhlenbeck (1925). 4. Paulis Ausschließungsprinzip für Fermionen (Pauliprinzip 1925). Wir verzichten hier auf eine Diskussion der Schrödingergleichung des Wasserstoffatoms und befassen uns 'nur' mit dem epochemachenden Experiment von Otto Stern und Walther Gerlach und dessen weitestreichenden Konsequenzen. Stellt man sich im Bohrschen Atommodell -das später von Arnold Sommerfeld zu 'der' vorquantenmechanischen Theorie ausgebaut wurde- dann ein Elektron mit dem Bahndrehimpuls L = nh vor, so kann die Projektion m = L z von L auf die 'Quantisierungsachse z' nur die diskreten Werte hn, h(n-1),...h(-n +1), h(-n) annehmen. Für ganzzahliges L muss es also immer eine endliche, ungerade Anzahl solcher Projektionszustände L z geben (1 für n = 0, 3 für n = 1, 5 für n =2,...). In der klassischen Theorie hingegen kann L z bzw. das L z zugeordnete 'magnetische Bahnmoment in z-richtung' des Elektrons auf einer Kreisbahn in der x/y -Ebene mit Radius r und Geschwindigkeit v, µ z = (Strom)x(Fläche) = (ev/2πr)x(π r 2 ) = e/2m L z jeden beliebigen Wert zwischen + L und - L annehmen. 'Magnetisches Bahnmoment µ' = Strom x Fläche n (n = Flächennormale): µ = ev/(2π r) x (π r 2 ) n = e/2m L (4.3) 29
4 Otto Stern und Walther Gerlach überlegten sich nun ein 'experimentum crucis', das entscheiden sollte, ob die klassische Theorie oder die 'neue' Vorstellung der quantisierten, diskreten L z -Werte richtig ist. Ihre Überlegung war folgende: In einem Magnetfeld B = B z z in z-richtung ist die 'magnetische Energie' eines Elektrons E = - µ B = - µ z B z = - e/2m L z B z. Ist B z inhomogen ( / z B z 0), dann wirkt auf ein Elektron mit L z eine Kraft F z - L z / z (B z ). Sind die L z - Werte diskret, dann führt dies -bei entsprechend großem Gradienten des Magnetfelds und entsprechend großer Flugstrecke des Elektrons durch das inhomogene Feld- zu einer räumlichen Aufspaltung der Flugbahnen und anschließenden diskreten Spuren auf einem geeigneten Schirm, deren Zahl n = 2 L + 1 sein muss. Im 'klassischen' Fall dagegen, mit kontinuierlichen L z -Werten, sollte sich ein einziger homogener Fleck ergeben. Stern und Gerlach überlegten sich im Jahr 1922, dass ein Magnetfeld mit einem Gradienten von ca. 1T/cm und einer Länge von einigen 10 cm ausreichen sollte, die 'Flecken' zu trennen, falls der Bahndrehimpuls wirklich quantisiert sein sollte. Sie benutzten einen Silber-Atomstrahl mit der Annahme -gemäß der damaligen Theoriedass dort 46 der insgesamt 47 Elektronen ihre Bahndrehimpulse zu L = 0 koppeln (abgeschlossene Schalen) und ein 'Leuchtelektron' mit L = 1 übrig bleibt. Sie erwarteten daher drei getrennte Flecken, falls die Theorie des gequantelten Drehimpulses richtig sein sollte. Sie sahen aber zwei diskrete Spuren!! Erwartung von drei Flecken für den Fall L = 1 des Silberatoms. 30
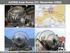
5 Abb. 1: Stern-Gerlach-Experiment. Ein Silberatomstrahl aus einem Ofen wird in einem inhomogenen Magnetfeld abgelenkt und in zwei Teilstrahlen aufgespalten Abb. 2: Beobachtete Intensität des Silberatomstrahls als Funktion des Abstandes von der Strahlachse mit (gestrichelte Linie) und ohne (durchgezogenen Linie) Magnetfeld 31
6 Abb. 2: Original-Ergebnis des Stern-Gerlach Experiments mit einem Silber-Atomstrahl. Die durchgezogene Spur (Mitte) ergab sich für B z = 0 ; die beiden deutlich getrennten Linien (Abstand der Maxima ca. 0,5 mm) ergaben sich für ein Magnetfeld mit einem Gradienten d/dz (B z ) von etwa 1 T/cm und einer Länge von ca. 60 cm. Stern und Gerlach fanden also als Ergebnis nicht die von der klassischen Theorie vorhergesagte kontinuierliche Verteilung der Silberatome, sondern in spektakulärer Weise eine Richtungsquantelung -aber nicht die von der Theorie vorhergesagte ungerade Zahl von Linien! Was war falsch?? Aus heutiger Sicht weiß man, dass die Annahme L = 1 für das Leuchtelektron im Silberatom falsch war; das siebenundvierzigste Elektron besetzt die 5s -Schale und hat daher L = 0. Dann hätte man aber einen Fleck erwarten müssen und nicht zwei! Die Lösung des Rätsels kam im Jahr 1925 durch Goudsmit, Uhlenbeck und Pauli, der sein 'Ausschließungsprinzip' für das Elektron in folgender Form formulierte: 1. es muss eine vierte 'Quantenzahl' für das Elektron geben außer seiner Energie (Hauptquantenzahl 'n' für ein im Atom gebundenes Elektron), seinem (Bahn)- Drehimpuls L und dessen Projektion L z. 2. kein Elektron darf dieselben Quantenzahlen wie ein anderes haben. Goudsmit und Uhlenbeck studierten in Leyden unter Paul Ehrenfest die 'Anomalien' der Feinstrukturspektren von Alkaliatomen. Paulis Hypothese einer 'vierten Quantenzahl' interpretierten sie als einen zusätzlichen Freiheitsgrad des Elektrons, nämlich als dessen quantisierte, halbzahlige 'Eigenrotation' (Spin S) mit den Eigenwerten S 2 = 3/4 h 2 und S z = +/- 1/2 h. Diesem zugeordnet ist dann ein magnetisches 'Spinmoment' µ s des Elektrons mit µ s = g e/(2m e ) S ('g-faktor' = 2 in der 'klassischen' quantenmechanischen Theorie). Sie stellten diese Hypothese ohne jede Erwähnung des Experiments von Stern und Gerlach auf -obwohl sich damit deren Ergebnis ganz 'einfach' erklären ließ. r B r µ S r S 32
7 Wolfgang Pauli Samuel Goudsmit
8 George Uhlenbeck Paulis Ausschließungsprinzip gilt für alle Fermionen -Teilchen mit halbzahligem Spin-, aber nicht für Bosonen. Dieses Theorem (das später in theoretischen Arbeiten über 'Spin und Statistik' halbwegs 'bewiesen' wurde) ist wahrscheinlich das wichtigste Postulat der Physik des 20. Jahrhunderts, da es erklärt, warum Atome so sind wie sie sind, und warum so etwas wie 'Chemie' überhaupt erst möglich wird und warum Photonen (Bosonen) im Laserstrahl sich so völlig anders verhalten wie Elektronen (Fermionen) im Atom. In mathematischem Gewand führt das Pauliprinzip in Verbindung mit dem Prinzip der Ununterscheidbarkeit der Teilchen zur 'Antisymmetrisierung' der Wellenfunktion von Fermionen bzw. zur 'Symmetrisierung für Bosonen: Beispiel: Zwei Elektronen (1,2) im niedrigsten Energiezustand eines Atoms (n = 1, L = 0, L z = 0); wenn sie die gleichen Quantenzahlen (n, L, L z ) haben, dann müssen sie sich in der vierten Quantenzahl (S z ) unterscheiden. Radialfunktion R n für beide Elektronen : R 1 (1), bzw. R 1 (2) Winkelfunktion Y LLz für beide Elektronen: Y 00 (1), bzw. Y 00 (2) Spineigenfunktionen s 1 bzw. s 2 = α > (s z = + 1/2 h), bzw. = β> (s z = - 1/2 h) Wenn die vierte Quantenzahl (s z ) nicht identisch sein darf, muss gelten: Wenn Elektron 1 im Zustand α> ist, muss Elektron 2 in β> sein und umgekehrt. 34
9 Der Spin S des Gesamtsystems der Elektronen muss dann die Form haben: S z = s z (1) + s z (2) = 0; ferner muss gelten: S = s 1 + s 2 = 0. Ansatz für die Gesamtwellenfunktion ψ: ψ = R 1 (1) R 1 (2) Y 00 (1) Y 00 (2) α(1) β(2) + R 1 (2)R 1 (1)Y 00 (2)Y 00 (1)α(2)β(1) = R 1 (1)R 1 (2)Y 00 (1)Y 00 (2) [ 1/ 2 {α(1)β(2) + α(2)β(1)}] die Funktion S s = 1/ 2 {α(1)β(2) + α(2)β(1)} ist Eigenfunktion zu S z = 0, aber S = 1! Sa = 1/ 2 { α(1) β(2) - α(2) β(1)} ist zu nehmen (S z = 0, S = 0) (S a, das Spinsingulett, ist antisymmetrisch bezüglich der Vertauschung 1 2) Die 'richtige' Gesamtwellenfunktion ist dann: ψ(1,2) = R1(1) R1(2) Y00(1) Y00(2) 1/ 2 {α(1) β(2) - α(2) β(1)} (4.4) Vertauscht man hier die Teilchen (1,2) dann geht ψ(1,2) - ψ(2,1) Ein drittes, viertes... Elektron in dieser Energieschale ist nicht 'erlaubt', da es mit einem der beiden Elektronen in allen vier Quantenzahlen (Freiheitsgraden) übereinstimmen würde, was aber für Teilchen mit halbzahligem Spin 'verboten' ist. Als man nach Aufstellung der Schrödingergleichung (1926) noch die Bedeutung der Hauptquantenzahl n (diskrete Energieniveaus E n mit n = 1, 2... ) und die Einschränkung für den Bahndrehimpuls L ( L max = (n - 1) h) erkannt und die 'Feinstruktur' (Kopplung von L und S zum Gesamtdrehimpuls J) entdeckt hatte, ergab sich -unter Berücksichtigung des Pauliprinzips- das Bauprinzip aller Atome, die 'Schalenstruktur': n L (h) L z (h) S z (1/2 h) Zahl Gesamtzahl in n , , , +1, -1 +1, , , +1, -1 +1, , +- 1, , usw. 35
10 Diese Schalenstruktur des Atomaufbaus zeigt sich am deutlichsten, wenn man das erste Ionisationspotential (Energie, um das erste Elektron aus einem neutralen Atom zu entfernen) gegen die Elementnummer (Kernladungszahl Z) aufträgt. Gleichzeitig werden die chemischen Analogien der Elemente deutlich und die im Aufbau der Elektronenschalen liegenden Unterschiede von elektrischen Leitern (Metallen) und Nichtleitern. Was Meyer und Mendelejev in ihrem 'Periodensystem der Elemente' noch intuitiv erahnt hatten, erhielt jetzt seine mikroskopische Begründung. Eine quantitative Beschreibung aller Elektronenzustände ergab sich dann unmittelbar später aus der Schrödingerschen 'Wellengleichung', die ihrerseits auf den neuen Ideen von Max Born und Werner Heisenberg beruhte. Max Born , um
11 Erwin Schrödinger , um 1922 Werner Heisenberg , um
12 Elektronen in Leitern, Halbleitern, Isolatoren oder Sternplasmen bezeichnet man als 'Fermigas'. Diese Zustandsform ist wichtig für alle 'Fermionen', d.h. Teilchen mit halbzahligem Spin, und sie weist dramatische Unterschiede gegenüber der Zustandsform 'herkömmlicher' Materie auf. Das Fermigas spielt eine große Rolle in vielen Bereichen der Physik z.b. in der Kernphysik (Nukleonen im Atomkern), der Festkörper- und Halbleiterphysik (Leitungsband, Valenzband, Energielücke, Supraleitung der Elektronen...), der Astrophysik ('entartete' Elektronen in Weißen Zwergen, 'entartete' Neutronen in Neutronensternen...). Quantenmechanisch verteilen sich n Elementarteilchen, die man in ein Volumen V = d 3 'einsperrt' (anschaulich: unendlich hohe Potentialwand am Rande) auf diskrete Energieniveaus, deren Abstand mit abnehmender Länge d -und das heißt mit zunehmender Teilchendichte ρ- zunimmt. Jetzt gibt es einen fundamentalen Unterschied zwischen Bosonen, Teilchen mit ganzzahligem Spin, und Fermionen, Teilchen mit halbzahligem Spin, auf der anderen Seite: Während beliebig viele Bosonen in einen Energiezustand gehen können, sind es für Fermionen wegen des Pauliprinzips nur exakt 2S +1 (S = Spin; für S = 1/2 also 2, für S = 3/2 = 4...) Verteilung von Bosonen bzw. Fermionen auf die diskreten Energieniveaus im Potential eines harmonischen Oszillators (ohne Spinmultiplizität) Dies bedeutet aber, dass bei gleicher Teilchenzahl n und gleichem Volumen V, also bei gleicher Teilchenzahldichte, die mittlere Energie von Fermionen (erheblich) größer als die von Bosonen ist. 38
13 Für ein Fermion, das sich mit dem Impuls p = (p x, p y, p z ) im Volumen V = d 3 bewegt, gilt nach der Unschärferelation: p x d h; p y d h; p z d h p 2 pf 2 = px 2 + py 2 + pz 2 3 h 2 /d 2 pf = 3 h/d (pf = 'Fermi-Impuls') (4.5) Dies lässt sich mit einem qualitativ gleichen Ergebnis anschaulich auch so formulieren: p 3 d 3 = p 3 V h 3 (4.6) das heißt: der 'Phasenraum' p 3 V eines Fermions muss immer h 3 sein, oder, andersherum: in der Phasenraum-Einheitszelle h 3 darf sich höchstens ein Fermion aufhalten (mit Berücksichtigung des Spins S dürfen es 2S +1 sein, also z.b. für S = 1/2 = 2). Führt man die Teilchendichte ρ n = 1/d 3 = Zahl der Fermionen/cm 3 ein, folgt aus Gl.4.5: p 3 /ρn h 3, bzw. ρn < p 3 /h 3 (4.7) bei gegebenem Impuls p (d.h. kinetischer Energie) kann die Dichte eines Fermionensystems nicht beliebig groß werden Diese Bedingung führt zur 'Fermistatistik', der Wahrscheinlichkeitsverteilung f(e,t) der Energien E eines Fermionensystems (man vergleiche dies mit der Statistik für Bosonen (Photonen), Gl. 2.1!) bei der Temperatur T: f(e,t) {exp[(e - EF)/kT] + 1} -1 (4.8) mit der 'Fermienergie' E F : EF pf 2 /2m = 3h 2 /(2md 2 ) = 3h 2 /2m ρn 2/3 (E F << mc 2, nichtrelativistisch) EF pf c = 3 hc/d = 3 hc ρn 1/3 (E F >> mc 2, relativistisch) EF ergibt sich auch aus der Bedingung f(ef,t) = 1/2 39
14 Fermiverteilung f(e,t) Die Folge ist nun die: Wird E F > kt (bzw. > 3/2 kt, die mittlere thermische Energie) dann verhält sich ein Gas nicht mehr gemäß der idealen Gasgleichung pv = R T bzw. p = ρ/( <µ> mh) kt (4.9) mit ρ = Dichte [g/cm 3 ] <µ> m H = mittlere Atommasse in [g] (z.b. für ein Proton- Elektron-Plasma = 0,5 x 1,6 x g), k = Boltzmann-Konstante = 1,38 x [(gcm 2 )/(s 2 K)] vielmehr muss man in der Gasgleichung die 'thermische Energie' kt durch die Fermienergie E F ersetzen. Man nennt das Gas dann 'entartet'. Dies hat dramatische Konsequenzen: Die ideale Gasgleichung garantiert nämlich eine wunderbare 'Selbstregulierung' von Druck, Temperatur und Dichte z.b. im Innern eines Sterns: wird die Temperatur T größer (z.b. durch eine plötzlich ansteigende Fusionsrate), nimmt der Gasdruck p zu, das Gas expandiert, kühlt sich dabei ab, wird wieder komprimiert unter Temperaturzunahme...Dieser Vorgang schwingt solange hin und her, bis sich ein neues stabiles Gleichgewicht eingestellt hat. Ein entartetes Gas hingegen reagiert nicht mehr 'selbstregulierend' auf eine Änderung der Temperatur oder des Drucks, da Druck und Temperatur nicht mehr durch die ideale Gasgleichung verknüpft sind! Dies führt zu dramatischen Effekten in 'Weißen Zwergen' (entartete Elektronen) bzw. 'Neutronensternen' (entartete Nukleonen). 40
15 Beispiel: Ist das Elektronengas im Zentrum der Sonne entartet? Ist also E F (e - ) > 3/2 kt? 1. T(r=0) = 1,5 x 10 7 K 3/2 kt = 3/2 x 1,38 x [erg/k] x 1,5 x 10 7 K = 3,1 x 10-9 erg = 1,94 kev Dichte (r=0) = 150 g/cm 3 Protonenzahl/cm 3 = Elektronenzahl/cm 3 = ρ n (0): ρn (0) = 150 x 6, 02 x = 9 x cm -3 d = ρn -1/3 = 2,2 x 10-9 cm = 2,2 x10 4 fm 2. EF(e -, nichtrelativ.)= p F2 /2m e = 3h 2 /(2m e d 2 ) = 3h 2 c 2 /(2m e c 2 d 2 ) = 0,236 kev EF (e - ) 0,1 x 3/2 kt Elektronen sind nicht entartet (Entartung würde eintreten ab d 0,77 x 10 4 fm) ρ n (Ent.,e - ) 23 x ρ n (0) = 2 x10 27 cm 3 Dies entspräche bei gleicher Protonen- und Elektronenzahl einer Massendichte des Wasserstoffs im Zentrum der Sonne von 3,45 kg/cm 3 Fermiverteilung von Elektronen in einem (Halb) Leiter 41
Der Stern-Gerlach-Versuch
 Der Stern-Gerlach-Versuch Lukas Mazur Physik Fakultät Universität Bielefeld Physikalisches Proseminar, 08.05.2013 1 Einleitung 2 Wichtige Personen 3 Motivation 4 Das Stern-Gerlach-Experiment 5 Pauli-Prinzip
Der Stern-Gerlach-Versuch Lukas Mazur Physik Fakultät Universität Bielefeld Physikalisches Proseminar, 08.05.2013 1 Einleitung 2 Wichtige Personen 3 Motivation 4 Das Stern-Gerlach-Experiment 5 Pauli-Prinzip
14. Atomphysik Physik für E-Techniker. 14. Atomphysik
 14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik. Inhalt. 14. Atomphysik
 Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Atommodell führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen.
 Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten
 Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Das Bohr sche Atommodell: Strahlenabsorption, -emission, Elektromagentische Strahlung, Wellen, Wellenlänge, Frequenz, Wellenzahl. Postulate: * Elektronen bewegen
Wiederholung der letzten Vorlesungsstunde: Das Bohr sche Atommodell: Strahlenabsorption, -emission, Elektromagentische Strahlung, Wellen, Wellenlänge, Frequenz, Wellenzahl. Postulate: * Elektronen bewegen
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
14. Atomphysik Aufbau der Materie
 14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
10 Teilchen und Wellen. 10.1 Strahlung schwarzer Körper
 10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
SS 2015 Supplement to Experimental Physics 2 (LB-Technik) Prof. E. Resconi
 Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
3. Feinstruktur von Alkalispektren: Die gelbe D-Linie des Na ist ein Dublett, sollte aber nur eine Linie sein.
 13. Der Spin Experimentelle Fakten: 2. Normaler Zeeman-Effekt ist die Ausnahme: Meist sieht man den anormalen Zeeman-Effekt (Aufspaltung beobachtet, für die es keine normale Erklärung gab wegen Spin).
13. Der Spin Experimentelle Fakten: 2. Normaler Zeeman-Effekt ist die Ausnahme: Meist sieht man den anormalen Zeeman-Effekt (Aufspaltung beobachtet, für die es keine normale Erklärung gab wegen Spin).
Atome und ihre Eigenschaften
 Atome und ihre Eigenschaften Vom Atomkern zum Atom - von der Kernphysik zur Chemie Die Chemie beginnt dort, wo die Temperaturen soweit gefallen sind, daß die positiv geladenen Atomkerne freie Elektronen
Atome und ihre Eigenschaften Vom Atomkern zum Atom - von der Kernphysik zur Chemie Die Chemie beginnt dort, wo die Temperaturen soweit gefallen sind, daß die positiv geladenen Atomkerne freie Elektronen
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
Atommodell. Atommodell nach Bohr und Sommerfeld Für sein neues Atommodell stellte Bohr folgende Postulate auf:
 Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Aufbau von Atomen. Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem
 Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
10. Das Wasserstoff-Atom Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Elemente der Quantenmechanik III 9.1. Schrödingergleichung mit beliebigem Potential 9.2. Harmonischer Oszillator 9.3. Drehimpulsoperator
 VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
Das Bohrsche Atommodell
 Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
10.7 Moderne Atommodelle
 10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
Teil II: Quantenmechanik
 Teil II: Quantenmechanik Historisches [Weinberg 1] Den ersten Hinweis auf die Unmöglichkeit der klassischen Physik fand man in der Thermodynamik des elektromagnetischen Feldes: Das klassische Strahulungsfeld
Teil II: Quantenmechanik Historisches [Weinberg 1] Den ersten Hinweis auf die Unmöglichkeit der klassischen Physik fand man in der Thermodynamik des elektromagnetischen Feldes: Das klassische Strahulungsfeld
Atomkerne und Kernmaterie
 Atomkerne und Kernmaterie Atomkerne 1000 m 10 cm 1 cm < 0.01 mm Kernmaterie ρ = 4 10 17 kg/m³ Struktur von Atomkernen Atomkerne sind eine Agglomeration von Nukleonen (Protonen und Neutronen), die durch
Atomkerne und Kernmaterie Atomkerne 1000 m 10 cm 1 cm < 0.01 mm Kernmaterie ρ = 4 10 17 kg/m³ Struktur von Atomkernen Atomkerne sind eine Agglomeration von Nukleonen (Protonen und Neutronen), die durch
8 Das Bohrsche Atommodell. 8. Das Bohrsche Atommodell
 1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse, Isotopie 4. Atomkern und Hülle:
1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse, Isotopie 4. Atomkern und Hülle:
Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen Mechanik).
 phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
Übungen zur Physik der Materie 1 Blatt 10 - Atomphysik
 Übungen zur Physik der Materie 1 Blatt 10 - Atomphysik Sommersemester 018 Vorlesung: Boris Bergues ausgegeben am 14.06.018 Übung: Nils Haag (Nils.Haag@lmu.de) besprochen am 0.06.018 Hinweis: Dieses Übungsblatt
Übungen zur Physik der Materie 1 Blatt 10 - Atomphysik Sommersemester 018 Vorlesung: Boris Bergues ausgegeben am 14.06.018 Übung: Nils Haag (Nils.Haag@lmu.de) besprochen am 0.06.018 Hinweis: Dieses Übungsblatt
Proseminar: Theoretische Physik. und Astroteilchenphysik. Fermi- und Bose Gase. Thermodynamisches Gleichgewicht
 Proseminar: Theoretische Physik und Astroteilchenphysik Thermodynamisches Gleichgewicht Fermi- und Bose Gase Inhalt 1. Entropie 2. 2ter Hauptsatz der Thermodynamik 3. Verteilungsfunktion 1. Bosonen und
Proseminar: Theoretische Physik und Astroteilchenphysik Thermodynamisches Gleichgewicht Fermi- und Bose Gase Inhalt 1. Entropie 2. 2ter Hauptsatz der Thermodynamik 3. Verteilungsfunktion 1. Bosonen und
8.3 Die Quantenmechanik des Wasserstoffatoms
 Dieter Suter - 409 - Physik B3 8.3 Die Quantenmechanik des Wasserstoffatoms 8.3.1 Grundlagen, Hamiltonoperator Das Wasserstoffatom besteht aus einem Proton (Ladung +e) und einem Elektron (Ladung e). Der
Dieter Suter - 409 - Physik B3 8.3 Die Quantenmechanik des Wasserstoffatoms 8.3.1 Grundlagen, Hamiltonoperator Das Wasserstoffatom besteht aus einem Proton (Ladung +e) und einem Elektron (Ladung e). Der
15. Vom Atom zum Festkörper
 15. Vom Atom zum Festkörper 15.1 Das Bohr sche Atommodell 15.2 Quantenmechanische Atommodell 15.2.1 Die Hauptquantenzahl n 15.2.2 Die Nebenquantenzahl l 15.2.3 Die Magnetquantenzahl m l 15.2.4 Die Spinquantenzahl
15. Vom Atom zum Festkörper 15.1 Das Bohr sche Atommodell 15.2 Quantenmechanische Atommodell 15.2.1 Die Hauptquantenzahl n 15.2.2 Die Nebenquantenzahl l 15.2.3 Die Magnetquantenzahl m l 15.2.4 Die Spinquantenzahl
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2016 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 2. Vorlesung, 17. 3. 2016 Wasserstoffspektren, Zeemaneffekt, Spin, Feinstruktur,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2016 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 2. Vorlesung, 17. 3. 2016 Wasserstoffspektren, Zeemaneffekt, Spin, Feinstruktur,
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
29. Lektion. Atomaufbau. 39. Atomaufbau und Molekülbindung
 29. Lektion Atomaufbau 39. Atomaufbau und Molekülbindung Lernziele: Atomare Orbitale werden von Elektronen nach strengen Regeln der QM aufgefüllt. Ein Orbital darf von nicht mehr als zwei Elektronen besetzt
29. Lektion Atomaufbau 39. Atomaufbau und Molekülbindung Lernziele: Atomare Orbitale werden von Elektronen nach strengen Regeln der QM aufgefüllt. Ein Orbital darf von nicht mehr als zwei Elektronen besetzt
Moderne Physik. von Paul A. Tipler und Ralph A. LIewellyn. Oldenbourg Verlag München Wien
 Moderne Physik von Paul A. Tipler und Ralph A. LIewellyn Oldenbourg Verlag München Wien Inhaltsverzeichnis I Relativitätstheorie und Quantenmechanik: Die Grundlagen der modernen Physik 1 1 Relativitätstheorie
Moderne Physik von Paul A. Tipler und Ralph A. LIewellyn Oldenbourg Verlag München Wien Inhaltsverzeichnis I Relativitätstheorie und Quantenmechanik: Die Grundlagen der modernen Physik 1 1 Relativitätstheorie
Ferienkurs Experimentalphysik Lösung zur Übung 2
 Ferienkurs Experimentalphysik 4 01 Lösung zur Übung 1. Ermitteln Sie für l = 1 a) den Betrag des Drehimpulses L b) die möglichen Werte von m l c) Zeichnen Sie ein maßstabsgerechtes Vektordiagramm, aus
Ferienkurs Experimentalphysik 4 01 Lösung zur Übung 1. Ermitteln Sie für l = 1 a) den Betrag des Drehimpulses L b) die möglichen Werte von m l c) Zeichnen Sie ein maßstabsgerechtes Vektordiagramm, aus
Welche Prinzipien bestimmen die quantenmechanischen Zustände, beschrieben durch ihre Quantenzahlen, die die Elektronen eines Atoms einnehmen?
 phys4.021 Page 1 12. Mehrelektronenatome Fragestellung: Betrachte Atome mit mehreren Elektronen. Welche Prinzipien bestimmen die quantenmechanischen Zustände, beschrieben durch ihre Quantenzahlen, die
phys4.021 Page 1 12. Mehrelektronenatome Fragestellung: Betrachte Atome mit mehreren Elektronen. Welche Prinzipien bestimmen die quantenmechanischen Zustände, beschrieben durch ihre Quantenzahlen, die
Das Wasserstoffatom Energiestufen im Atom
 11. 3. Das Wasserstoffatom 11.3.1 Energiestufen im Atom Vorwissen: Hg und Na-Dampflampe liefern ein charakteristisches Spektrum, das entweder mit einem Gitter- oder einem Prismenspektralapparat betrachtet
11. 3. Das Wasserstoffatom 11.3.1 Energiestufen im Atom Vorwissen: Hg und Na-Dampflampe liefern ein charakteristisches Spektrum, das entweder mit einem Gitter- oder einem Prismenspektralapparat betrachtet
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
(a) Warum spielen die Welleneigenschaften bei einem fahrenden PKW (m = 1t, v = 100km/h) keine Rolle?
 FK Ex 4-07/09/2015 1 Quickies (a) Warum spielen die Welleneigenschaften bei einem fahrenden PKW (m = 1t, v = 100km/h) keine Rolle? (b) Wie groß ist die Energie von Lichtquanten mit einer Wellenlänge von
FK Ex 4-07/09/2015 1 Quickies (a) Warum spielen die Welleneigenschaften bei einem fahrenden PKW (m = 1t, v = 100km/h) keine Rolle? (b) Wie groß ist die Energie von Lichtquanten mit einer Wellenlänge von
Die Schrödingergleichung II - Das Wasserstoffatom
 Die Schrödingergleichung II - Das Wasserstoffatom Das Wasserstoffatom im Bohr-Sommerfeld-Atommodell Entstehung des Emissionslinienspektrums von Wasserstoff Das Bohr-Sommerfeld sche Atommodell erlaubt für
Die Schrödingergleichung II - Das Wasserstoffatom Das Wasserstoffatom im Bohr-Sommerfeld-Atommodell Entstehung des Emissionslinienspektrums von Wasserstoff Das Bohr-Sommerfeld sche Atommodell erlaubt für
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
LEHRBUCH DER THEORETISCHEN PHYSIK
 LEHRBUCH DER THEORETISCHEN PHYSIK VON DR.PHIL. DR.H.C. SIEGFRIED FLÜGGE ORDENTLICHER PROFESSOR AN DER UNIVERSITÄT FREIBURG/BREISGAU IN FÜNF BÄNDEN BAND IV QUANTENTHEORIE I SPRINGER-VERLAG BERLIN GÖTTINGEN
LEHRBUCH DER THEORETISCHEN PHYSIK VON DR.PHIL. DR.H.C. SIEGFRIED FLÜGGE ORDENTLICHER PROFESSOR AN DER UNIVERSITÄT FREIBURG/BREISGAU IN FÜNF BÄNDEN BAND IV QUANTENTHEORIE I SPRINGER-VERLAG BERLIN GÖTTINGEN
2. Max Planck und das Wirkungsquantum h
 2. Max Planck und das Wirkungsquantum h Frequenzverteilung eines schwarzen Strahlers Am 6. Dezember 1900, dem 'Geburtsdatum' der modernen Physik, hatte Max Planck endlich die Antwort auf eine Frage gefunden,
2. Max Planck und das Wirkungsquantum h Frequenzverteilung eines schwarzen Strahlers Am 6. Dezember 1900, dem 'Geburtsdatum' der modernen Physik, hatte Max Planck endlich die Antwort auf eine Frage gefunden,
Das Rutherfordsche Atommodelle
 Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
Das quantenmechanische Atommodell
 Ende 93 konzipierte de Broglie seine grundlegenden Ideen über die Dualität von Welle und Korpuskel. Albert Einstein hatte schon 905 von den korpuskularen Eigenschaften des Lichtes gesprochen; de Broglie
Ende 93 konzipierte de Broglie seine grundlegenden Ideen über die Dualität von Welle und Korpuskel. Albert Einstein hatte schon 905 von den korpuskularen Eigenschaften des Lichtes gesprochen; de Broglie
Abb.15: Experiment zum Rutherford-Modell
 6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
VL 12. VL11. Das Wasserstofatom in der QM II Energiezustände des Wasserstoffatoms Radiale Abhängigkeit (Laguerre-Polynome)
 VL 12 VL11. Das Wasserstofatom in der QM II 11.1. Energiezustände des Wasserstoffatoms 11.2. Radiale Abhängigkeit (Laguerre-Polynome) VL12. Spin-Bahn-Kopplung (I) 12.1 Bahnmagnetismus (Zeeman-Effekt) 12.2
VL 12 VL11. Das Wasserstofatom in der QM II 11.1. Energiezustände des Wasserstoffatoms 11.2. Radiale Abhängigkeit (Laguerre-Polynome) VL12. Spin-Bahn-Kopplung (I) 12.1 Bahnmagnetismus (Zeeman-Effekt) 12.2
4. Aufbau der Elektronenhülle 4.1. Grundlagen 4.2. Bohrsches Atommodell 4.3. Grundlagen der Quantenmechanik 4.4. Quantenzahlen 4.5.
 4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches Atommodell 4.3. Grundlagen der Quantenmechanik 4.4. Quantenzahlen 4.5. Atomorbitale 4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches
4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches Atommodell 4.3. Grundlagen der Quantenmechanik 4.4. Quantenzahlen 4.5. Atomorbitale 4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches
8.2 Aufbau der Atome. auch bei der Entdeckung der Kathodenstrahlen schienen die Ladungsträger aus den Atomen herauszukommen.
 Dieter Suter - 404 - Physik B3 8.2 Aufbau der Atome 8.2.1 Grundlagen Wenn man Atome als Bausteine der Materie i- dentifiziert hat stellt sich sofort die Frage, woraus denn die Atome bestehen. Dabei besteht
Dieter Suter - 404 - Physik B3 8.2 Aufbau der Atome 8.2.1 Grundlagen Wenn man Atome als Bausteine der Materie i- dentifiziert hat stellt sich sofort die Frage, woraus denn die Atome bestehen. Dabei besteht
Bohrsches Atommodell / Linienspektren. Experimentalphysik für Biologen und Chemiker, O. Benson & A. Peters, Humboldt-Universität zu Berlin
 Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
2.4. Atome mit mehreren Elektronen
 2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
Übungen Quantenphysik
 Ue QP 1 Übungen Quantenphysik Kernphysik Historische Entwicklung der Atommodelle Klassische Wellengleichung 5 Schrödinger Gleichung 6 Kastenpotential (Teilchen in einer Box) 8 Teilchen im Potentialtopf
Ue QP 1 Übungen Quantenphysik Kernphysik Historische Entwicklung der Atommodelle Klassische Wellengleichung 5 Schrödinger Gleichung 6 Kastenpotential (Teilchen in einer Box) 8 Teilchen im Potentialtopf
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale
 Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
UniversitätQ Osnabrück Fachbereich Physik Dr. W. Bodenberger
 UniversitätQ Osnabrück Fachbereich Physik Dr. W. Bodenberger Statistik der Elektronen und Löcher in Halbleitern Die klassische Theorie der Leitungselektronen in Metallen ist nicht anwendbar auf die Elektronen
UniversitätQ Osnabrück Fachbereich Physik Dr. W. Bodenberger Statistik der Elektronen und Löcher in Halbleitern Die klassische Theorie der Leitungselektronen in Metallen ist nicht anwendbar auf die Elektronen
Kerne und Teilchen. Aufbau der Kerne (1) Moderne Experimentalphysik III Vorlesung 17.
 Kerne und Teilchen Moderne Experimentalphysik III Vorlesung 17 MICHAEL FEINDT INSTITUT FÜR EXPERIMENTELLE KERNPHYSIK Aufbau der Kerne (1) KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Kerne und Teilchen Moderne Experimentalphysik III Vorlesung 17 MICHAEL FEINDT INSTITUT FÜR EXPERIMENTELLE KERNPHYSIK Aufbau der Kerne (1) KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum
Quantentheorie für Nanoingenieure Klausur Lösung
 07. April 011 PD Dr. H. Kohler Quantentheorie für Nanoingenieure Klausur Lösung K1. Ja Nein Fragen (8P) Jede richtige Antwort liefert einen Punkt, jede falsche Antwort liefert einen Minuspunkt. Eine nicht
07. April 011 PD Dr. H. Kohler Quantentheorie für Nanoingenieure Klausur Lösung K1. Ja Nein Fragen (8P) Jede richtige Antwort liefert einen Punkt, jede falsche Antwort liefert einen Minuspunkt. Eine nicht
Theoretical Biophysics - Quantum Theory and Molecular Dynamics. 10. Vorlesung. Pawel Romanczuk WS 2016/17
 Theoretical Biophysics - Quantum Theory and Molecular Dynamics 10. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Der Spin Grundlegende Eigenschaften Spin
Theoretical Biophysics - Quantum Theory and Molecular Dynamics 10. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Der Spin Grundlegende Eigenschaften Spin
Der Spin des Elektrons
 Kapitel 13 Der Spin des Elektrons Wie in Abbschnitt 12.4 angedeutet, ist in der Realität die Aufspaltung der Spektrallinien im homogenen externen Magnetfeld nicht alleine durch den normalen Zeeman-Effekt
Kapitel 13 Der Spin des Elektrons Wie in Abbschnitt 12.4 angedeutet, ist in der Realität die Aufspaltung der Spektrallinien im homogenen externen Magnetfeld nicht alleine durch den normalen Zeeman-Effekt
Die Macht und Ohnmacht der Quantenwelt
 Die Macht und Ohnmacht der Quantenwelt Prof. Dr. Sebastian Eggert Tag der Physik, TU Kaiserslautern, 5. Dezember 2015 Quantenmechanik heute Quanteninformatik Ultrakalte Quantengase Supraleitung und Vielteilchenphysik
Die Macht und Ohnmacht der Quantenwelt Prof. Dr. Sebastian Eggert Tag der Physik, TU Kaiserslautern, 5. Dezember 2015 Quantenmechanik heute Quanteninformatik Ultrakalte Quantengase Supraleitung und Vielteilchenphysik
Die Welt der Quanten Murmeln oder Wellen? Max Camenzind Senioren Uni WS2013
 Die Welt der Quanten Murmeln oder Wellen? Max Camenzind Senioren Uni Würzburg @ WS2013 Die Krise des mechanischen Weltbildes und die Gründerväter der modernen Physik. Elektromagnetische Strahlung Maxwell,
Die Welt der Quanten Murmeln oder Wellen? Max Camenzind Senioren Uni Würzburg @ WS2013 Die Krise des mechanischen Weltbildes und die Gründerväter der modernen Physik. Elektromagnetische Strahlung Maxwell,
Für Geowissenschaftler. EP WS 2009/10 Dünnweber/Faessler
 Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Festkörperelektronik 4. Übung
 Festkörperelektronik 4. Übung Felix Glöckler 23. Juni 2006 1 Übersicht Themen heute: Feedback Spin Drehimpuls Wasserstoffatom, Bohr vs. Schrödinger Wasserstoffmolekülion, kovalente Bindung Elektronen in
Festkörperelektronik 4. Übung Felix Glöckler 23. Juni 2006 1 Übersicht Themen heute: Feedback Spin Drehimpuls Wasserstoffatom, Bohr vs. Schrödinger Wasserstoffmolekülion, kovalente Bindung Elektronen in
27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus
 26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
2.4. Atome mit mehreren Elektronen
 2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
2.4. Atome mit mehreren Elektronen 2.4.1. Das Heliumatom Wellenfunktion für das Heliumatom Nach dem Wasserstoffatom ist das Heliumatom das nächst einfachere Atom. Das Heliumatom besitzt einen Kern der
22. Wärmestrahlung. rmestrahlung, Quantenmechanik
 22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
1 Physikalische Hintergrunde: Teilchen oder Welle?
 Skript zur 1. Vorlesung Quantenmechanik, Montag den 11. April, 2011. 1 Physikalische Hintergrunde: Teilchen oder Welle? 1.1 Geschichtliches: Warum Quantenmechanik? Bis 1900: klassische Physik Newtonsche
Skript zur 1. Vorlesung Quantenmechanik, Montag den 11. April, 2011. 1 Physikalische Hintergrunde: Teilchen oder Welle? 1.1 Geschichtliches: Warum Quantenmechanik? Bis 1900: klassische Physik Newtonsche
H LS = W ( r) L s, (2)
 Vorlesung 5 Feinstruktur der Atomspektren Wir betrachten ein Wasserstoffatom. Die Energieeigenwerte des diskreten Spektrums lauten E n = mα c n, (1 wobei α 1/137 die Feinstrukturkonstante, m die Elektronmasse
Vorlesung 5 Feinstruktur der Atomspektren Wir betrachten ein Wasserstoffatom. Die Energieeigenwerte des diskreten Spektrums lauten E n = mα c n, (1 wobei α 1/137 die Feinstrukturkonstante, m die Elektronmasse
A. Erhaltungsgrößen (17 Punkte) Name: Vorname: Matr. Nr.: Studiengang: ET Diplom ET Bachelor TI WI. Platz Nr.: Tutor:
 Prof. Dr. O. Dopfer Prof. Dr. A. Hese Priv. Doz. Dr. S. Kröger Cand.-Phys. A. Kochan Technische Universität Berlin A. Erhaltungsgrößen (17 Punkte) 1. Unter welcher Bedingung bleiben a) der Impuls b) der
Prof. Dr. O. Dopfer Prof. Dr. A. Hese Priv. Doz. Dr. S. Kröger Cand.-Phys. A. Kochan Technische Universität Berlin A. Erhaltungsgrößen (17 Punkte) 1. Unter welcher Bedingung bleiben a) der Impuls b) der
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
1. Zusammenfassung: Masse in der klassischen Mechanik. 2. Energie des klassischen elektromagnetischen Feldes
 2. Vorlesung 1. Zusammenfassung: Masse in der klassischen Mechanik + 1. Übungsaufgabe 2. Energie des klassischen elektromagnetischen Feldes Literatur: beliebiges Lehrbuch klassische Elektrodynamik z.b.
2. Vorlesung 1. Zusammenfassung: Masse in der klassischen Mechanik + 1. Übungsaufgabe 2. Energie des klassischen elektromagnetischen Feldes Literatur: beliebiges Lehrbuch klassische Elektrodynamik z.b.
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwörter von der letten Vorlesung können Sie sich noch erinnern? Elektronmikroskopie Die Energie eines Elektrons in einer Elektronenfalle En π = ml n Photonenabsorption & Photonenemission
An welche Stichwörter von der letten Vorlesung können Sie sich noch erinnern? Elektronmikroskopie Die Energie eines Elektrons in einer Elektronenfalle En π = ml n Photonenabsorption & Photonenemission
4. Quantenmechanik. Offene Fragen am Ende des 19. Jahrhunderts:
 4. Quantenmechanik Offene Fragen am Ende des 19. Jahrhunderts: - Strahlungsspektrum schwarzer Körper (z.b. der Sonne) - Merkwürdigkeiten beim lichtelektrische Effekt (Photoeffekt) - Aufbau der Atome -
4. Quantenmechanik Offene Fragen am Ende des 19. Jahrhunderts: - Strahlungsspektrum schwarzer Körper (z.b. der Sonne) - Merkwürdigkeiten beim lichtelektrische Effekt (Photoeffekt) - Aufbau der Atome -
5. Atome mit 1 und 2 Leucht-Elektronen 5.1 Alkali-Atome 5.2 He-Atom
 5. Atome mit 1 und 2 Leucht- 5.1 Alkali-Atome 5.2 He-Atom 5.1 5.1 Alkali Atome ein "Leuchtelektron" Alkali Erdalkali 5.2 Tauchbahnen grosser Bahndrehimpuls l: geringes Eintauchen kleiner Bahndrehimpuls
5. Atome mit 1 und 2 Leucht- 5.1 Alkali-Atome 5.2 He-Atom 5.1 5.1 Alkali Atome ein "Leuchtelektron" Alkali Erdalkali 5.2 Tauchbahnen grosser Bahndrehimpuls l: geringes Eintauchen kleiner Bahndrehimpuls
[ H, L 2 ]=[ H, L z. ]=[ L 2, L z. U r = Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2. r 1 2. y 2 2. z 2 = 2. r 2 2 r
![[ H, L 2 ]=[ H, L z. ]=[ L 2, L z. U r = Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2. r 1 2. y 2 2. z 2 = 2. r 2 2 r [ H, L 2 ]=[ H, L z. ]=[ L 2, L z. U r = Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2. r 1 2. y 2 2. z 2 = 2. r 2 2 r](/thumbs/71/65107015.jpg) Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2 y 2 2 z 2 = 2 r 2 2 r r 1 2 L r 2 ħ 2 11. Das Wasserstoffatom H = p2 2 U r μ = Masse (statt m, da m später als Quantenzahl verwendet wird) U r = e2
Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2 y 2 2 z 2 = 2 r 2 2 r r 1 2 L r 2 ħ 2 11. Das Wasserstoffatom H = p2 2 U r μ = Masse (statt m, da m später als Quantenzahl verwendet wird) U r = e2
Gesamtdrehimpuls Spin-Bahn-Kopplung
 Gesamtdrehimpuls Spin-Bahn-Kopplung > 0 Elektron besitzt Bahndrehimpuls L und S koppeln über die resultierenden Magnetfelder (Spin-Bahn-Kopplung) Vektoraddition zum Gesamtdrehimpuls J = L + S Für J gelten
Gesamtdrehimpuls Spin-Bahn-Kopplung > 0 Elektron besitzt Bahndrehimpuls L und S koppeln über die resultierenden Magnetfelder (Spin-Bahn-Kopplung) Vektoraddition zum Gesamtdrehimpuls J = L + S Für J gelten
TC1 Grundlagen der Theoretischen Chemie
 TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Topic: Helium-Atom Vorlesung: Mo 10h-12h, Do9h-10h Übungen: Do 8h-9h Web site: http://www.theochem.uni-frankfurt.de/tc1
TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Topic: Helium-Atom Vorlesung: Mo 10h-12h, Do9h-10h Übungen: Do 8h-9h Web site: http://www.theochem.uni-frankfurt.de/tc1
Fachschule für f. r Technik. Dipl.FL. D.Strache FST UH
 . FST UH Ein Atommodell ist eine Vorstellung von den kleinsten Teilen der Stoffe. Lange Zeit gab es keine experimentellen Hinweise für die Existenz kleinster Teilchen, sondern lediglich die intuitive Ablehnung
. FST UH Ein Atommodell ist eine Vorstellung von den kleinsten Teilen der Stoffe. Lange Zeit gab es keine experimentellen Hinweise für die Existenz kleinster Teilchen, sondern lediglich die intuitive Ablehnung
Atomphysik NWA Klasse 9
 Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
n r 2.2. Der Spin Magnetische Momente In einem klassischen Atommodell umkreist das Elektron den Kern Drehimpuls
 2.2. Der Spin 2.2.1. Magnetische Momente In einem klassischen Atommodell umkreist das Elektron den Kern Drehimpuls Dies entspricht einem Kreisstrom. n r r I e Es existiert ein entsprechendes magnetisches
2.2. Der Spin 2.2.1. Magnetische Momente In einem klassischen Atommodell umkreist das Elektron den Kern Drehimpuls Dies entspricht einem Kreisstrom. n r r I e Es existiert ein entsprechendes magnetisches
9. Das Wasserstoff-Atom. 9.1 Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 09. Wasserstoff-Atom Page 1 9. Das Wasserstoff-Atom 9.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
09. Wasserstoff-Atom Page 1 9. Das Wasserstoff-Atom 9.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Vorlesung 21. Identische Teilchen und das Pauli-Prinzip
 Vorlesung 1 Identische Teilchen und das Pauli-Prinzip Identische Teilchen: Jede Art von Teilchen in der Natur definieren wir durch ihre Eigenschaften, z.b. Massen, Spins, Ladungen usw. Das bedeutet, dass
Vorlesung 1 Identische Teilchen und das Pauli-Prinzip Identische Teilchen: Jede Art von Teilchen in der Natur definieren wir durch ihre Eigenschaften, z.b. Massen, Spins, Ladungen usw. Das bedeutet, dass
3. Geben Sie ein Bespiel, wie man Bra und Ket Notation nützen kann.
 Fragen zur Vorlesung Einführung in die Physik 3 1. Was ist ein quantenmechanischer Zustand? 2. Wenn die Messung eines quantenmechanischen Systems N unterscheidbare Ereignisse liefern kann, wie viele Parameter
Fragen zur Vorlesung Einführung in die Physik 3 1. Was ist ein quantenmechanischer Zustand? 2. Wenn die Messung eines quantenmechanischen Systems N unterscheidbare Ereignisse liefern kann, wie viele Parameter
VI. Quantenphysik. VI.1 Ursprünge der Quantenphysik, Atomphysik. Physik für Mediziner 1
 VI. Quantenphysik VI.1 Ursprünge der Quantenphysik, Atomphysik Physik für Mediziner 1 Mikroskopische Welt Physik für Mediziner 2 Strahlung des Schwarzen Körpers Schwarzer Körper: eintretendes Licht im
VI. Quantenphysik VI.1 Ursprünge der Quantenphysik, Atomphysik Physik für Mediziner 1 Mikroskopische Welt Physik für Mediziner 2 Strahlung des Schwarzen Körpers Schwarzer Körper: eintretendes Licht im
lichen auf sehr engem Raum konzentriert ist und die positive Ladung trägt
 lichen auf sehr engem Raum konzentriert ist und die positive Ladung trägt Kanalstrahlexperimente hatten schwere, positiv geladene Teilchen beim Wasserstoff nachgewiesen Aufgrund von Streuexperimenten postulierte
lichen auf sehr engem Raum konzentriert ist und die positive Ladung trägt Kanalstrahlexperimente hatten schwere, positiv geladene Teilchen beim Wasserstoff nachgewiesen Aufgrund von Streuexperimenten postulierte
Entwicklung der Atommodelle
 Entwicklung der Atommodelle Entwicklung der Atommodelle Demokrit 460 v Chr. Nur scheinbar hat ein Ding eine Farbe, nur scheinbar ist es süß oder bitter; in Wirklichkeit gibt es nur Atome im leeren Raum.
Entwicklung der Atommodelle Entwicklung der Atommodelle Demokrit 460 v Chr. Nur scheinbar hat ein Ding eine Farbe, nur scheinbar ist es süß oder bitter; in Wirklichkeit gibt es nur Atome im leeren Raum.
Ein schwarzer Körper und seine Strahlung
 Quantenphysik 1. Hohlraumstrahlung und Lichtquanten 2. Max Planck Leben und Persönlichkeit 3. Das Bohrsche Atommodell 4. Niels Bohr Leben und Persönlichkeit 5. Wellenmechanik 6. Doppelspaltexperiment mit
Quantenphysik 1. Hohlraumstrahlung und Lichtquanten 2. Max Planck Leben und Persönlichkeit 3. Das Bohrsche Atommodell 4. Niels Bohr Leben und Persönlichkeit 5. Wellenmechanik 6. Doppelspaltexperiment mit
Musterlösung 02/09/2014
 Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
Vorlesungsteil II - Atombau und Periodensystem
 Chemie Zusammenfassung Vorlesungsteil II - Atombau und Periodensystem Zwei wichtige Formeln dazu: Coulombkraft: Schrödinger Gleichung: beschreibt die Kraft zwischen zwei kugelsymmetrisch verteilten elektrischen
Chemie Zusammenfassung Vorlesungsteil II - Atombau und Periodensystem Zwei wichtige Formeln dazu: Coulombkraft: Schrödinger Gleichung: beschreibt die Kraft zwischen zwei kugelsymmetrisch verteilten elektrischen
Thema heute: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Übungsblatt 06. PHYS4100 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, oder 3. 6.
 Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
PN 2 Einführung in die Experimentalphysik für Chemiker
 PN 2 Einführung in die Experimentalphysik für Chemiker 13. Vorlesung 11.7.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 2 Einführung in die Experimentalphysik für Chemiker 13. Vorlesung 11.7.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
6. Viel-Elektronen Atome
 6. Viel-Elektronen 6.1 Periodensystem der Elemente 6.2 Schwerere 6.3 L S und j j Kopplung 6.1 6.1 Periodensystem der Elemente 6.2 Auffüllen der Elektronen-Orbitale Pauliprinzip: je 1 Elektron je Zustand
6. Viel-Elektronen 6.1 Periodensystem der Elemente 6.2 Schwerere 6.3 L S und j j Kopplung 6.1 6.1 Periodensystem der Elemente 6.2 Auffüllen der Elektronen-Orbitale Pauliprinzip: je 1 Elektron je Zustand
VL Landé-Faktor (Einstein-deHaas Effekt) Berechnung des Landé-Faktors Anomaler Zeeman-Effekt
 VL 14 VL13. Spin-Bahn-Kopplung (II) 13.1. Landé-Faktor (Einstein-deHaas Effekt) 13.2. Berechnung des Landé-Faktors 13.3. Anomaler Zeeman-Effekt VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2.
VL 14 VL13. Spin-Bahn-Kopplung (II) 13.1. Landé-Faktor (Einstein-deHaas Effekt) 13.2. Berechnung des Landé-Faktors 13.3. Anomaler Zeeman-Effekt VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2.
Physikalisches Praktikum A 5 Balmer-Spektrum
 Physikalisches Praktikum A 5 Balmer-Spektrum Versuchsziel Es wird das Balmer-Spektrum des Wasserstoffatoms vermessen und die Rydberg- Konstante bestimmt. Für He und Hg werden die Wellenlängen des sichtbaren
Physikalisches Praktikum A 5 Balmer-Spektrum Versuchsziel Es wird das Balmer-Spektrum des Wasserstoffatoms vermessen und die Rydberg- Konstante bestimmt. Für He und Hg werden die Wellenlängen des sichtbaren
Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4)
 Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4) Gesetzmäßigkeiten in der Anordnung der Spektrallinien eines Stoffes? Wasserstoff Johann Jacob Balmer 1825-1898 A=364.4 nm n ganzzahlig > 2 Eine
Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4) Gesetzmäßigkeiten in der Anordnung der Spektrallinien eines Stoffes? Wasserstoff Johann Jacob Balmer 1825-1898 A=364.4 nm n ganzzahlig > 2 Eine
