In vitro Evaluation des DLR BVADs: Entwicklung eines neuen implantierbaren, pulsatilen und biventrikulären Herzunterstützungssystems
|
|
|
- Hansl Wagner
- vor 7 Jahren
- Abrufe
Transkript
1 In vitro Evaluation des DLR BVADs: Entwicklung eines neuen implantierbaren, pulsatilen und biventrikulären Herzunterstützungssystems Inaugural-Dissertation zur Erlangung des Doktorgrades der Hohen Medizinischen Fakultät der Rheinischen Friedrich-Wilhelms-Universität Bonn Tim-Oliver Robert Trotzke aus Bonn 14
2 Angefertigt mit Genehmigung der Medizinischen Fakultät der Universität Bonn 1. Gutachter: Prof. Dr. med. Armin Welz 2. Gutachter: PD Dr. med. Ulf Günther Tag der Mündlichen Prüfung: Aus der Klinik und Poliklinik für Herzchirurgie Direktor: Prof. Dr. med. Armin Welz
3 Gewidmet meiner Familie für jahrelange Unterstützung und viel Geduld
4
5 5 Inhaltsverzeichnis Abkürzungsverzeichnis 6 1. Einleitung Epidemiologie der Herzinsuffizienz Aktuelle Therapie der chronischen Herzinsuffizienz Einteilung der ventrikulären Herzunterstützungssysteme Entwicklung und aktuelle Situation Komplikationen und Rechtsherzversagen unter LVAD Therapie Ziele der vorliegenden Dissertation Methoden Das DLR BVAD Versuchsanordnung und Teststand Auswertung 2.4 Bestimmung der Kennlinien Bestimmung der VAD-Funktionskurven Temperaturmessung Berechnung des Wirkungsgrads Ergebnisse Kennlinien Interventrikuläre Differenz VAD-Funktionskurven Temperatur Stromverbrauch Wirkungsgrad Diskussion Zusammenfassung Anhang Abbildungsverzeichnis Tabellenverzeichnis Referenzen Danksagung Lebenslauf 81
6 6 Abkürzungsverzeichnis ACC ACE AHA ARB bpm BTR BTT BVAD CFD CL LV CL RV CRT CVA DLR DT ESC FDA ICD INTERMACS IP ISHLT l/min LV American College of Cardiology Angiotensin Converting Enzyme American Heart Association Angiotensin Rezeptor Blocker Beats per minute (Schläge pro Minute) Bridge To Recovery (VAD-Therapie bis zur Heilung) Bridge To Transplant (VAD-Therapie bis zur Transplantation) Biventricular Assist Device (Biventrikuläres Herzunterstützungssystem) Computational Fluid Dynamics (Numerische Strömungsmechanik) Linksventrikuläre Kennlinie Rechtsventrikuläre Kennlinie Cardiac Resynchronization Therapy (Kardiale Resynchronisationstherapie) Cerebro-Vascular Accident (Cerebrovaskuläres Ereignis) Deutsches Zentrum für Luft- und Raumfahrt Destination Therapy (VAD-Therapie als Endlösung) European Society of Cardiology US Food and Drug Administration Implantable Cardioverter Defibrillator (Implantierbarer Kardioverter-Defibrillator) The Interagency Registry for Mechanically Assisted Circulatory Support Inflow Pressure (Vorlast am Einflusskonduit) International Society for Heart and Lung Transplantation Liter pro Minute Linker Ventrikel
7 7 LVAD NYHA OMT PAP RHF RV RVAD SAP sys VAD VFC Leftventricular Assist Device (Linksventrikuläres Herzunterstützungssystem) New York Heart Association Only Medical Treatment (ausschließlich medikamentöse Therapie) Pulmonalarterieller Druck Right Heart Failure (Rechtsherzversagen) Rechter Ventrikel Rightventricular Assist Device (Rechtsventrikuläres Herzunterstützungssystem) Systemischer arterieller Druck Systolisch Ventricular Assist Device (Ventrikuläres Herzunterstützungssystem) VAD-Funktionskurve
8 8 1. Einleitung 1.1 Epidemiologie der Herzinsuffizienz In Deutschland leiden 1-2 % der Bevölkerung an chronischer Herzinsuffizienz (Meyer und Struber, 09). Mit etwa neuen Fällen pro Jahr und einer durchschnittlichen 5-Jahres Mortalität von 78,5 % ist die chronische Herzinsuffizienz als klinisches Endstadium verschiedener Krankheitsprozesse, wie zum Beispiel arterieller Hypertonie, ischämischer oder dilatativer Kardiomyopathie sowie Klappenvitien, eine der häufigsten Ursachen für eine stationären Behandlung (Cowie et al., 1997; Goldberg et al., 07; Massie et al., 1997). Die European Society of Cardiology (ESC) definiert Herzinsuffizienz als eine funktionelle oder strukturelle Herzstörung, die zur Unfähigkeit des Herzens führt, das benötigte Sauerstoffangebot für den Körper bei physiologischen Füllungsdrücken zur Verfügung zu stellen. Klinisch wird die Herzinsuffizienz als ein Syndrom mit verschiedenen typischen Symptomen definiert. Typische Symptome sind zum Beispiel Dyspnoe, Unterschenkelödeme und reduzierte körperliche Leistungsfähigkeit. Klinische Zeichen sind zum Beispiel gestaute Halsvenen und Herzgeräusche (siehe Tabelle 1). Die Diagnose Herzinsuffizienz wird definitionsgemäß beim Vorliegen eines oder mehrerer typischer Symptome und klinischer Zeichen, in Verbindung mit einer reduzierten linksventrikulären Pumpfunktion, einer relevanten strukturellen Herzerkrankung oder einer diastolischen Dysfunktion gestellt. Traditionell wird die Herzinsuffizienz klinisch gemäß der Klassifikation der New York Heart Association (NYHA) in Grad I-IV eingeteilt. Die neuere ACC/AHA-Klassifikation des American College of Cardiology (ACC) und der American Heart Association (AHA) teilt die chronische Herzinsuffizienz in vier Stadien gemäß der pathophysiologischen Progression ein (McMurray et al., 12; Muth et al., 06).
9 9 Symptome Typisch Dyspnoe Orthopnoe Paroxysmale nächtliche Dyspnoe Müdigkeit, verlängerte Erholungszeit Unterschenkelödeme Zeichen Sehr spezifisch Gestaute Halsvenen Hepatojugulärer Reflux Dritter Herzton (Galopprhythmus) Hebender Herzspitzenstoß Irreguläre Herzgeräusche Weniger typisch Nächtlicher Husten Verstärkte Atemgeräusche Gewichtszunahme > 2 kg/woche Gewichtsverlust im fortgeschrittenen Stadium Meteorismusgefühl Appetitverlust Verwirrtheit Depression Palpitationen Synkope Weniger spezifisch Periphere Ödeme Knisterende Atemgeräusche Abgeschwächte Lungenperkussion Tachykardie Pulsveränderungen Tachypnoe > 16/min Hepatomegalie Aszites Kachexie Tab. 1: Symptome und klinische Zeichen der Herzinsuffizienz (McMurray et al., 12). Das klinische Bild der terminalen Herzinsuffizienz wird in den aktuellen internationalen Leitlinien definiert als Herzinsuffizienz, die der leitliniengerechten Standardtherapie (siehe Abbildung 1) nicht mehr zugänglich ist und im Verlauf die Indikation für eine Herztransplantation oder eine mechanische Herzunterstützung gestellt werden muss. In der NYHA-Klassifikation wird die terminale Herzinsuffizienz dem Stadium IV zugeordnet und entspricht dem Stadium D der ACC/AHAKlassifikation. Dem klinischen Alltag entsprechend wurde eine genauere Einteilung der terminalen Herzinsuffizienz auf Basis der INTERMACS-Datenbank (The Interagency Registry for Mechanically Assisted Circulatory Support) INTERMACS-Klassifikation eingeführt (siehe Tabelle 2) (Raake et al., 12). die
10 10 INTERMACS NYHA ACC/AHA Klinischer Zustand 1 IV D Kritischer kardiogener Schock 2 IV D Steigender Katecholaminbedarf 3 IV D Stabil unter Gabe von Inotropika 4 IV D Häufige Dekompensation 5 IV C Ruhebeschwerden/nicht belastbar 6 IV C Ruhebeschwerden/kaum belastbar 7 IIIb C Kaum belastbar Tab. 2: Die INTERMACS-Einteilung der terminalen Herzinsuffizienz im Vergleich zu den gängigen klinischen Einteilung der chronischen Herzinsuffizienz nach NYHA und ACC/AHA. Im Vergleich zu den gängigen Klassifikationen erlaubt die INTERMACSEinteilung eine genauere Einteilung der Patienten, die sich am Ende der leitliniengerechten Standardtherapie befinden (Raake et al., 12). 1.2 Aktuelle Therapie der chronischen Herzinsuffizienz Weinbrenner et al. (12) schreiben in der aktuellen Nationalen Versorgungsleitlinie Chronische Herzinsuffizienz: "Bei jedem Patienten mit chronischer Herzinsuffizienz soll unter Berücksichtigung der Gesamtsituation des Patienten zunächst die Ursache der Herzinsuffizienz behandelt werden, da die Heilung oder Linderung der Grunderkrankung unter Umständen zu einer kompletten Remission der Herzinsuffizienz führen kann." Unabhängig von der kausalen Therapie hat sich bei der chronischen systolischen Herzinsuffizienz ein standardisierter, evidenzbasierter Behandlungsalgorithmus etabliert, der sowohl Mortalität und Hospitalisierung, als auch Symptomreduktion berücksichtigt.
11 11 Im Vordergrund steht - neben der kausalen Therapie und Reduktion von Risikofaktoren - in allen Stadien zunächst die Pharmakotherapie wie in Abbildung 1 gezeigt. Bei Versagen der Pharmakotherapie sind beim Vorliegen spezieller Voraussetzungen weiterführende apparative Therapien, wie zum Beispiel die kardiale Resynchronisationstherapie, indiziert. Die Ultima Ratio und gleichzeitig der Goldstandard für die Behandlung der terminalen Herzinsuffizienz stellt die orthotope Herztransplantation dar. Diese bringt für Patienten mit terminaler Herzinsuffizienz eine signifikante Verbesserung der Lebensqualität; die 1-Jahres-Überlebensrate wird mit 88,3 % angegeben (Weinbrenner et al., 12; Muth et al., 06; Riedmayr et al 1998). Die International Society for Heart and Lung Transplantation (ISHLT) gibt für die orthotope Herztransplantation zwischen dem 1. Oktober 08 und. September 12 in Europa eine 3-Jahres-Überlebensrate von 73 % bei insgesamt 429 Überlebenden an. Nach Evaluation der spezifischen Indikations- und Kontraindikationskriterien werden geeignete Patienten auf einer Warteliste der europäischen, multinationalen Eurotransplant Organisation gelistet. Im Jahre 12 warteten insgesamt 1235 Patienten auf ein Spenderherz. Die durchschnittliche Wartezeit auf eine Herztransplantation betrug etwa 15 Monate, wobei die Mortalität der gelisteten Patienten im Jahr 12 bei 18,3 % lag. Tatsächlich wurden in der EurotransplantZone im Jahr 12 lediglich 607 Herztransplantationen durchgeführt und damit wurde nur etwa jeder zweite Patient, der gelistet war, operiert (Rahmel, 14).
12 12 Abb. 1: Leitliniengerechte Therapie der chronischen Herzinsuffizienz (McMurry et al., 12). Erst nach Ausschöpfen der medikamentösen Therapie ergibt sich bei fortbestehenden klinischen Zeichen der Herzinsuffizienz die Indikation zur operativen Therapie mittels CRT (kardiale Resynchronisationstherapie) oder ICD (Implantierbarer Kardioverter-Defibrillator). Im Endstadium der Erkrankung können die orthotope Herztransplantation oder die Implantation eines Herzunterstützungssystems erwogen werden.
13 13 Dieses Missverhältnis zwischen Angebot und Nachfrage und die Anzahl an Patienten, die aufgrund der strengen Indikationskriterien gar nicht erst gelistet werden können, hat zu einer steten Entwicklung von Alternativen geführt. Maschinelle Herzunterstützungssysteme - sogenannte VADs (Ventricular Assist Devices) - haben sich daher neben der medikamentösen und der kardialen Resynchronisations-Therapie als ein fester Bestandteil der chirurgischen Therapie der chronischen Herzinsuffizienz etabliert (siehe Abbildung 1). Slaughter et al. (11) ziehen aufgrund der erhöhten Mortalität nach Implantation eines ventrikulären Herzunterstützungssystems im INTERMACS-Stadium 1 insbesondere Patienten in den Stadien 2 bis 5 für eine VAD-Implantation mit dem Ziel einer dauerhaften Therapie (DT) in Betracht (siehe Tabelle 2). Abb. 2: Durchschnittliche Wartezeit von der Aufnahme auf die Warteliste bis zur Transplantation in Monaten (Rahmel, 14). Durch Stagnation der Organspenderzahlen und Zunahme des Transplantatbedarfs kam es innerhalb der letzten 10 Jahre zu einer stetigen Zunahme der Wartezeit. Die hellblaue Linie zeigt die Verdopplung der Wartezeit auf eine Herztransplantation auf etwa 15 Monate im Jahr 12.
14 Einteilung der ventrikulären Herzunterstützungssysteme Herzunterstützungssysteme sind mechanische oder hydraulische Pumpen, die über ein Einflusskonduit Blut aus dem linken oder rechten Ventrikel des erkrankten Herzen ansaugen und über ein, an der Aorta thoracalis oder der Arteria pulmonalis angeschlossenes, Ausflusskonduit dem systemischen oder pulmonalen Kreislauf wieder zuführen. In der aktuellen Literatur ist die Einteilung der ventrikulären Herzunterstützungssysteme in drei Generationen üblich. Bei der ersten Generation von VADs handelt es sich um große, parakorporal gelegene Verdrängerpumpen, die einen pulsatilen Fluss erzeugen, indem sie Pumpkammern verschiedener Größen entweder hydraulisch oder mechanisch komprimieren. Beispiele hierfür sind das Thoratec PVAD (Thoratec Corp., Pleasanton, California, USA) und das ABIOMED BVS 5000 (ABIOMED Inc., Danvers, Massachusett, USA). VADs der zweiten Generation sind weitgehend implantierbar und erzeugen den pulsatilen Fluss meist über eine Druckplatte: Thoratec Heartmate I, World Heart Novacor (World Heart Corp., Salt Lake City, Utah, USA), Arrow LionHeart (Arrow International, Teleflex Medical Inc., Research Triangle Park, North Carolina, USA) sind Beispiele hierfür. VADs der dritten Generation sind in der Regel Axialpumpen, die nach dem archimedischen Schraubenprinzip einen nicht-pulsatilen Fluss erzeugen. Sie sind wesentlich kleiner und leichter als alle vorherigen VADs. Beispiele hierfür sind das Heartmate II der Firma Thoratec, der Jarvik 00 FlowMaker von Jarvik Heart (Jarvik Heart Inc., New York City, New York, USA), das Incor von Berlin Heart (Berlin Heart GmbH, Berlin) und das Heart Assist 5 /DeBakey VAD von MicroMed (MicroMed Cardiovascular Inc., Houston, Texas, USA). Das einzige pulsatile VAD dieser Gruppe ist das IVAD von Thoratec. Dies ist ein implantierbares BVAD auf Basis des parakorporalen Thoratec PVADs. Ein Weiteres VAD der dritten Generation ist das HeartWare HVAD (HeartWare Inc., Framingham, Massachusetts, USA) (siehe Abbildung 3), welches nach dem Prinzip der
15 15 Zentrifugalpumpen arbeitet (Christiansen et al., 13; Hetzer et al., 10; Krabatsch et al., 11; Mitter und Sheinberg, 10; Reichenbach et al., 01; Slaughter et al., 07; Strueber et al. 10; Timms, 11). Tabelle 3 zeigt eine Liste der aktuell in den USA von der FDA (Food and Drug Administration) für verschiedene Indikationen zugelassenen ventrikulären Herzunterstützungssysteme. Parallel zur Entwicklung der VADs wurden Systeme für den kompletten Herzersatz (Total Artificial Hearts oder TAH) entwickelt, wie zum Beispiel das CardioWest Total Artificial Heart (SynCardia Systems Inc., Tucson, Arizona, USA) und das AbioCor Implantable Replacement Heart von ABIOMED. Im Gegensatz zum VAD System wird bei TAHs ein großer Teil des erkrankten Herzens entfernt und im Sinne einer orthotopen Implantation ersetzt (Morris, 08). Typ Dauerhafter Einsatz Nicht pulsatil Pulsatil extrakorporal Pulsatil intrakorporal Totaler Herzersatz (TAH) Temporärer Einsatz Modell Thoratec HeartMate II Heartware HVAD MicroMed DeBakey Child VAD Thoratec PVAD Heart Excor HeartMate IP HeartMate VE HeartMate XVE Thoratec IVAD NovaCor PC NovaCor PCq SynCardia CardioWest AbioCor IRH Abiomed AB5000 Abiomed BVS 5000 Levitronix Centrimag Biomedicus Tandem Heart Tab. 3: Aufstellung der im Jahre 13 in den USA von der FDA zugelassenen Herzunterstützungssysteme (Kirklin et al., 13).
16 16 Abb. 3: CT-Topogramm eines Patienten mit implantiertem LVAD der dritten Generation (HeartWare HVAD ). Gut erkennbar sind die intrathorakale Lage des LVADs (rote Markierung) sowie ein zusätzlich implantierter DreikammerSchrittmacher/ICD (grüne Markierung) zur kardialen Resynchronisationstherapie (CRT). (Klinik und Poliklinik für Herzchirurgie der Universitätsklinik Bonn)
17 Entwicklung und aktuelle Situation Die ersten ventrikulären Herzunterstützungssysteme wurden in den 1970er Jahren für den Kurzzeiteinsatz zur postoperativen Herz-Lungen-Maschinen-Entwöhnung entwickelt. Nach der Einführung des Immunsuppressivums Ciclosporin A (ein Calcineurin-Inhibitor) gewann die Herztransplantation zur Therapie der terminalen Herzinsuffizienz in den 1980er Jahren an Bedeutung, so dass 1986 das erste linksventrikuläre Unterstützungssystem (LVAD) zur Überbrückung bis zur Transplantation (Bridge To Transplant - BTT) erfolgreich implantiert wurde (Frazier et al., 1992; Frazier, 10). Aktuell werden 70 % aller VAD-Implantationen als BTT durchgeführt und weisen eine perioperative Mortalität von 10-25% auf (Hammer et al., 1997). Dass herztransplantierte Patienten trotz vorheriger Therapie mittels eines VADs vergleichbare 1- und 5-Jahres-Überlebensraten zu herztransplantierten Patienten ohne vorherige VAD-Implantation besitzen, hat zu der regelhaften Anwendung dieser Systeme als Bridge To Transplant in der heutigen Zeit geführt (Hetzer et al., 10). Aufgrund sinkender Spenderzahlen und strenger Indikationskriterien für eine Herztransplantation hat sich für die VAD-Implantation auch die Indikation einer sogenannten Destination Therapy (DT) ergeben. Dies bedeutet, dass das VAD permanent implantiert bleibt und keine anschließende Herztransplantation durchgeführt wird. Die im Jahre 02 veröffentlichte REMATCH Studie verglich Patienten mit terminaler Herzinsuffizienz und vorliegenden Kontraindikationen für eine Herztransplantation. Verglichen wurde die rein medikamentöse Therapie mit der VAD-Implantation. Es zeigte sich eine Mortalitätsreduktion der VAD-Gruppe um fast 50 % im Vergleich zur Gruppe mit rein medikamentöser Therapie (OMT). Die 2Jahres-Überlebensrate der VAD-Gruppe betrug 23 % verglichen mit 8 % der OMTGruppe. Dieses Ergebnis führte zu der Zulassung des HeartMate VE LVAD zur DT durch die US Food and Drug Administration (FDA) (Rose et al., 01). Eine weitere prospektive Studie zur Untersuchung der VAD-Implantation als DT wurde im Jahr 07 veröffentlicht. Es handelt sich dabei um die INTrEPID Studie, in der das Novacor LVAD der rein medikamentösen Therapie gegenübergestellt
18 18 wurde. In der VAD-Gruppe betrug die 1-Jahres-Überlebensrate 27 % im Vergleich zu 11 % in der OMT-Gruppe (Christiansen et al., 08; Rogers et al., 07). Die dritte Indikation zur VAD-Implantation stellt die sogenannte Bridge To Recovery (BTR) dar. Insbesondere bei einer akuten Herzinsuffizienz nach Kardiotomie, im Rahmen einer fulminanten Myokarditis oder nach Myokardinfarkt ist die Erholung der Ventrikelfunktion nach initialer Kreislaufstabilisierung und kardialer Entlastung durch ein VAD beschrieben (Kumpati et al., 01; Young, 01). Seit 06 erhebt die Interagency Registry for Mechanically Assisted Circulatory Support (INTERMACS) Daten aller FDA-zugelassenen, implantierten VADs aus 145 kooperierenden Krankenhäusern. In dem Zeitraum vom Juni 06 bis zum Juni 12 wurden insgesamt 6561 VAD Implantationen erfasst (Kirklin et al., 13). Abb. 4: Überleben in Abhängigkeit der primären Implantationsstrategie (Kirklin et al., 13). Unabhängig vom Typ des implantierten VADs zeigt die blaue Kurve eine erhöhte Mortalität bei der primären Implantationsstrategie DT (Destination Therapy). Die rote Kurve BTT (Bridge To Transplant) zeigte eine Mortalität innerhalb von 12 Monaten von 19,1 % im Vergleich zu 23,9 % bei der blauen Kurve (DT).
19 Komplikationen und Rechtsherzversagen unter LVAD Therapie Die REMATCH- (01) und später die INTrEPID-Studie (07) konnten zwar einen deutlichen Überlebensvorteil der VAD-Gruppen im Vergleich zu den jeweiligen Kontrollgruppen nachweisen, verdeutlichen aber auch die Probleme der damaligen Systeme. Die REMATCH-Studie beschreibt eine Infektion des VADs mit konsekutiver Sepsis bei 28 % der operierten Patienten innerhalb von 6 Monaten nach Implantation. In 42 % der Fälle traten relevante, insbesondere zerebrale Blutungen (CVA) auf. Innerhalb von 24 Monaten nach Implantation kam es in 35 % der Fälle zu technischen Fehlern des VADs. Abbildung 5 zeigt die Ergebnisse der INTrEPIDStudie (Rogers et al., 07; Rose et al., 01). Der fünfte Jahresreport der INTERMACS (13) verdeutlicht das Fortbestehen der Hauptkomplikationen Infektionen und zerebrale Blutungen nach LVAD-Implantation, obwohl durch den Fortschritt der VAD-Entwicklung bei den nicht-pulsatilen VADs der dritten Generation ein deutlicher Rückgang dieser Komplikationen im Vergleich zu den pulsatilen Systemen der zweiten Generation zu verzeichnen ist (Kirklin et al., 13). Ein weiteres Problem der mechanischen, linksventrikulären Herzunterstützung stellt die Rechtsherz-Insuffizienz dar. Aktuelle Studien beziffern das Auftreten eines Rechtsherzversagens (RHF) mit konsekutiver Notwendigkeit einer RVAD Implantation unter LVAD Therapie mit 11 % bis 44 % (Drakos et al., 10; Fitzpatrick 3rd et al., 08; Matthews et al., 08; Romano et al., 10; Takeda et al., 14). Zudem benötigen % der Patienten mit terminaler Herzinsuffizienz eine primär biventrikuläre mechanische Unterstützung, so dass erste Versuche mit zwei getrennt arbeitenden VADs - eines zur Rechts- und eines zur Linksherzunterstützung durchgeführt worden sind (Kirklin et al., 10; Krabatsch et al., 11). Neben den oben genannten Komplikationen der LVAD-Therapie ist das Rechtsherzversagen ein ernstzunehmendes Risiko mit deutlich erhöhter Mortalität (siehe Tabelle 4 und Abbildungen 5 und 6).
20 Abb. 5: Die Abbildung zeigt das Auftreten relevanter klinischer Ereignisse und Risiken innerhalb der beiden Vergleichsgruppen der INTrEPID-Studie (Rogers et al., 07). Die blauen Balken stellen die relative Häufigkeit der Ereignisse der OMT-Gruppe (ausschließlich medikamentöse Therapie) denen der LVAD-Gruppe (Therapie mittels mechanischer linksventrikulärer Herzunterstützung) (rote Balken) gegenüber. In der LVAD-Gruppe zeigt sich eine signifikante Minderung der kardiovaskulären Ereignisse und eine signifikante Minderung der renalen Ereignisse bei erhöhtem Blutungs- und Infektionsrisiko sowie einer erhöhte Rate an cerebrovaskulären Ereignissen (CVA).
21 21 Ereignisse VAD-Defekt Blutung RHF Myokardinfarkt Arrhythmie Perikardtamponade Periphere Embolie Thrombose Hämolyse Infektion Neurologische Komplikation Renale Dysfunktion Hepatische Dysfunktion. Pulmonale Komplikation Wundkomplikation Psychische Auffälligkeiten Total Pulsatil (n=594) Absolut Relativ 119 3, , ,47 2 0, , , , , , , ,81 Nicht-pulsatil (n=5358) Absolut Relativ 660 1, , ,79 0, , , , , , , ,83 Pulsatil/Nichtpulsatil Relativ p-wert 2,04 <0,0001 1,83 <0,0001 1,38 0,001 0,75 0,47 1,5 <0,0001 2,88 <0,0001 2,14 0,001 2,31 <0,0001 0,87 0,69 2,85 <0,0001 2,08 <0, ,96 1, ,41 0,6 2,1 2,2 <0,0001 <0, , ,52 2,42 <0, ,49 2, ,18 1,03 2,75 2,31 <0,0001 <0, , ,22 2,13 <0,0001 Tab. 4: Häufigste Komplikationen innerhalb von 12 Monaten nach LVAD Implantation gemäß der INTERMACS Datenbank (Kirklin et al., 13). Insgesamt zeigt sich eine deutlich höhere Komplikationsrate bei den pulsatilen LVADs der zweiten Generation im Vergleich zu den nicht pulsatilen Systemen der dritten Generation. Deutlich wird jedoch auch der Bauart bedingte Vorteil der geringeren Hämolyse der pulsatilen Systeme.
22 22 Abb. 6: Überleben in Abhängigkeit von der Rechtsherzfunktion nach Implantation eines LVADs oder BVADs. Es wurden Patienten 36 Monate postoperativ betrachtet, die ein VAD als Destination Therapie oder Bridge To Transplantation erhielten. Die grüne Kurve zeigt das relative Überleben bei schwerem Rechtsherzversagen (RHF) mit Indikation zur Implantation eines biventrikulären Herzunterstützungssystems. Die rote Kurve (moderates RHF) und die blaue Kurve (leichtes RHF) zeigen deutlich bessere Überlebenswahrscheinlichkeiten (Kirklin et al., 13). 1.6 Ziele der vorliegenden Dissertation Unter Berücksichtung der Probleme und Komplikationen der vorangegangen VADGenerationen wurde ein vollimplantierbares, biventrikuläres und pulsatiles VAD entwickelt. Das DLR BVAD ist eine eigenständige Entwicklung, hervorgegangen aus einer Kooperation des Deutschen Zentrums für Luft- und Raumfahrt (DLR) und der Klinik und Poliklinik für Herzchirurgie der Universitätsklinik Bonn. In der vorliegenden Dissertation werden die Ergebnisse einer experimentellen Studie, welche die hämodynamische Leistungsfähigkeit des DLR BVAD in einem eigens entwickelten, artifiziellen Testkreislauf geprüft hat, präsentiert und die Ergebnisse im Hinblick auf die klinische Anwendbarkeit diskutiert.
23 23 2. Methoden 2.1 Das DLR BVAD Das DLR BVAD wurde vor dem Hintergrund entwickelt, dass ein physiologisches Blutflußprofil im Ventrikel die entstehenden Scherspannungen minimiert und somit Hämolyse und die Aktivierung von Thrombozyten sowie der plasmatischen Gerinnung reduziert. Das DLR BVAD ist als vollimplantierbares, biventrikuläres und pulsatiles VAD konzipiert, welches den VAD-Fluss mittels zweier artifizieller Ventrikel generiert, die durch eine Kompressionsplatte wechselseitig komprimiert werden. Die Kompressionsplatte ist mit den Ventrikeln nicht fest verbunden. Sobald ein Ventrikel komprimiert wird, entsteht im abgeschlossenen BVAD-Gehäuse ein Unterdruck, der die Füllung des anderen Ventrikels zur Folge hat. Die Kompressionsplatte wird über ein Gleitkeilgetriebe durch einen bürstenlosen Elektromotor angetrieben. Diese komprimiert wechselseitig die aus medizinischem Polyurethan gefertigten artifiziellen Ventrikel. Für die Geometrie der artifiziellen Ventrikel wurden MRT-Datensätze humaner Herzventrikel ausgewertet und in Datensätze für rechnergestütztes Konstruieren (CAD) umgewandelt und für die Anwendung in einem VAD mit Hilfe numerischer Strömungsmechanik (CFD) optimiert. Da der systemische Widerstand im Normalfall größer ist als der pulmonalarterielle Widerstand, wurde das DLR BVAD mit zwei unterschiedlich großen artifiziellen Ventrikeln ausgestattet. Den unterschiedlichen Anforderungen des klinischen Alltags entsprechend wurden zwei Versionen des DLR BVADs konstruiert. Die in der vorliegenden Dissertation beschriebene und getestete Version entspricht der kleinen Version, welche für eine Patienten-Körperoberfläche von bis zu 1,7 m² konstruiert wurde. Dies entspricht etwa einem Menschen mit einer Größe von 165 cm und einem Gewicht von 65 kg. Der linke Ventrikel (LV) besitzt ein Füllvolumen von 65 ml und der rechte Ventrikel (RV) von 45 ml, was circa 70 % des Linken entspricht.
24 24 Abb. 7: Konstruktionszeichnung des DLR BVADs in Pro/ENGINEER (Parametric Technology Corp., Needham, Massachusetts, USA). Zu sehen sind rot eingefärbt die artifiziellen Ventrikel und grau eingefärbt der Elektromotor sowie die Kraftübertragung auf die Druckplatte. Abb. 8: Illustration der Entwicklung der artifiziellen Ventrikel: Von der Simulation zum Polyurethan Prototypen.
25 25 Das Gehäuse des DLR BVADs besteht aus zwei Polyamid Mantelschalen mit einem Gesamtvolumen von 3 cm³ bei einem Gesamtleergewicht von 390 g. Es ist mit vier Konduits mit einem Durchmesser von 24 mm aus Polytetrafluorethylen (PTFE) der Firma Gore-Tex (W. L. Gore & Associates Inc., Newark, Delaware, USA) an den humanen Kreislauf angeschlossen. und in Gerichtet diesen wird der Fall an den Blutstrom artifiziellen durch vier Testkreislauf perikardiale Aortenklappenprothesen (Carpentier-Edwards PERIMOUNT, Edwards Lifesciences Corp., Irvine, California, USA). Abb. 9: Fotoaufnahme des verwendeten DLR BVADs. Im Gegensatz zu dem sonst baugleichen in vivo Modell besitzt das hier verwendete Modell aus Wartungs- und Evaluationsgründen eine durchsichtige Mantelschale.
26 Versuchsanordnung und Teststand Die im Folgenden dargestellten Versuche wurden in den Laboren des Instituts für Robotik und Mechatronik des Deutschen Zentrums für Luft- und Raumfahrt in Oberpfaffenhofen durchgeführt. Um die hämodynamische Effektivität des DLR BVADs zu bestimmen, wurde ein artifizieller Testkreislauf entwickelt, der die charakteristischen Eigenschaften des humanen Kreislaufs simuliert und gleichzeitig eine genaue Erfassung verschiedener Parameter erlaubt. Um eine möglichst störungsarme und genaue Datenaufnahme zu gewährleisten, haben wir uns bei der Entwicklung des Teststands für zwei separate Kreisläufe entschieden, das heißt einen Kreislauf je Ventrikel ohne eine physiologisch vorhandene Verknüpfung von Körper- und Lungenstrombahn. Dies erlaubt die interferenzfreie und korrekte Einstellung verschiedener physiologischer und pathologischer Parameter für den rechten und linken Ventrikel. Die Verbindung des VADs an den Rohrkreislauf des Teststands mit einem Innendurchmesser von 21 mm erfolgt, wie oben bereits beschrieben, über vier PTFEKonduits mit einem Durchmesser von je 24 mm. Es existieren zwei identisch aufgebaute Kreisläufe mit jeweils drei Zylindern. Der erste Zylinder in Blutstromrichtung nach dem linken Ventrikel des VADs simuliert den Windkesseleffekt der humanen Aorta. Der Zweite bildet ein Reservoir und repräsentiert die kapillare Strombahn. Die Füllhöhe des dritten Zylinders reguliert die Vorlast. Analog hierzu simuliert der Kreislauf für den rechten Ventrikel des VADs den Lungenkreislauf. Als Modellfluid wurde aufgrund der langen Haltbarkeit und der guten Klappenverträglichkeit in dieser Versuchsreihe stets isotone (0,9 prozentige) Kochsalzlösung verwendet.
27 27 Abb. 10: Fotoaufnahme des verwendeten, eigens entwickelten Teststands. Zu sehen sind unter anderem das getestete DLR BVAD, die vier Druckabnehmer (blaue Markierung) sowie eine Ultraschallsonde zur Flussmessung (rote Markierung). Jeder Ventrikel wird durch einen separaten Testkreislauf mit jeweils drei Zylindern, welche die Windkesselfunktion, die kapillare Strombahn, als auch die Vorlast simulieren, evaluiert.
28 28 Abb. 11: Schemazeichnung des Teststands. Zur besseren Übersicht ist lediglich einer der beiden identischen Kreisläufe abgebildet. Der Blutfluss wird über jeweils zwei biologische Aortenklappen pro Ventrikel gerichtet. Über zwei Drucksensoren kann die Vor- und Nachlast ermittelt werden. Der Fluss des verwendeten Fluids (isotone Kochsalzlösung) wird ultraschallgestützt im Bereich des Ausfluss-Konduits gemessen. Über zwei Drosseln wird der systemische Widerstand geregelt; die abgebildeten Zylinder simulieren unter anderem die Windkesselfunktion der Aorta.
29 29 Der periphere Widerstand wurde über zwei serielle Drosseln reguliert. Die erste Drossel ist in Blutstromrichtung vor dem ersten Zylinder positioniert und ist in erster Linie für die gemessene Blutdruckamplitude verantwortlich. Die zweite Drossel ist zwischen den ersten und zweiten Zylinder geschaltet und beeinflusst in erster Linie den gemessenen Mitteldruck. Der Blutfluss des VADs wird für den rechten und linken Ventrikel individuell bestimmt, dabei wurde das ultraschallbasierte Flussmeter (HT311 Flow QC, Transonic Systems Inc., Ithaca, New York, USA) direkt hinter dem Ausflusskonduit positioniert. Die Drucksensoren sind zum einen hinter dem Ausflusskonduit - zur Bestimmung der Nachlast - und zum anderen vor dem Einflusskonduit - zur Bestimmung der Vorlast positioniert. Bei den verwenden Drucksensoren der Firma Huba Control handelt es sich um das Modell TYP (0-0.3 bar) für die Nachlast und TYP ( bar) für die Vorlast (Huba Control AG, Wuerenlos, Schweiz). Die Schemazeichnung des Testkreislaufs in Abbildung 11 zeigt die oben beschriebene Messanordnung für den linken Ventrikel. Neben hämodynamischen Parametern wurden zur Beurteilung des Wirkungsgrads und Anwendbarkeit die Leistungsaufnahme und die Temperatur im Innengehäuse gemessen sowie die Positionsparameter der Druckplatte erfasst.
30 2.3 Auswertung Die erhobenen Daten wurden mittels einer speziell programmierten Makrosoftware basierend auf NI LabVIEW 8.2 (National Instruments Corp., Austin, Texas, USA) erfasst und in Microsoft Excel (Microsoft Corporation, Redmond, Washington, USA) exportiert. Die folgenden Parameter wurden für die im Folgenden beschriebenen Experimente als physiologisch definiert: Der am Ausflusskonduit gemessene Druck repräsentiert im linksventrikulären Kreislauf den Aortendruck (SAP); als physiologisch wurde ein Druck von 1/80 mmhg angenommen. Der im Bereich des rechtsventrikulären Ausflusstrakts gemessene Druck entspricht dem pulmonalarteriellen Druck (PAP). Dieser wurde zur besseren Durchführbarkeit auf /5 mmhg festgesetzt. Die Vorlast der beiden artifiziellen Ventrikel wird in vivo durch den Druck innerhalb der Ventrikel des erkrankten Herzens bestimmt. Im Versuchsstand wird die Vorlast durch den dritten Zylinder erzeugt und am Einflusskonduit gemessen. Für die Versuchsreihe werden für die Vorlast (Inflow Pressure - IP) folgende Werte als physiologische definiert: Die Vorlast des linken Ventrikels (IP LV) wird auf 10 mmhg und die Vorlast des rechten Ventrikels (IP RV) auf 5 mmhg festgesetzt. Alle Messungen am Testkreislauf wurden nach Einstellung eines über mindestens 10 Minuten stabilen Zustandes und unabhängig voneinander dreimal durchgeführt. Die in den Ergebnissen präsentierten Daten sind auf zwei Nachkommastellen gerundet und stellen das arithmetische Mittel der jeweils durchgeführten Messungen dar. Auf eine Darstellung der Standardabweichung wird zugunsten der Übersichtlichkeit in den folgenden Abbildungen verzichtet: 14b, 17b, Die in den Abbildungen präsentierten Messdaten und arithmetischen Mittelwerte sind im Anhang tabellarisch mit Standardabweichung aufgeführt.
31 31 Abb. 12a: Bildschirmausschnitt der verwendeten, speziell angepassten Software auf Basis von NI LabVIEW 8.2 (National Instruments Corp., Austin, Texas, USA).
32 32 Abb. 12b: Bildschirmausschnitt der graphischen Darstellung der linksventrikulären Druckkurve. Gut erkennbar: Das nahezu physiologische Druckprofil mit Inzisur (siehe Markierung) bei Schluss der Aortenklappe.
33 Bestimmung der ventrikulären Kennlinien Um die hämodynamische Leistungsfähigkeit des DLR BVADs zu beschreiben, sollten Kennlinien erstellt werden. Kennlinien sind spezifisch für jeden Ventrikel des VADs und beschreiben die Abhängigkeit des erzeugten Flusses von der Nachlast. Sie wurden für jeden Ventrikel einzeln bestimmt, indem bei konstanter Frequenz eine diskrete Steigerung der Nachlast vorgenommen und der resultierende Fluss gemessen wurde. Während dieser Messungen wurde der Testkreislauf des jeweils anderen Ventrikels auf physiologische - entsprechend der oben genannten Definition - Werte festgesetzt. Zur Bestimmung der linksventrikulären Kennlinie (CL LV) wurde die linksventrikuläre Vorlast (IP LV) auf 10 mmhg, die rechtsventrikuläre Nachlast (PAP) auf /5mmHg und die rechtsventrikuläre Vorlast (IP RV) auf 5 mmhg gesetzt. Als Frequenzspanne wurden 60 bis 1 Schläge pro Minute (bpm) festgelegt. Die Widerstände des linksventrikulären Testkreislaufs wurde jeweils so eingestellt, dass die gemessenen systemischen arteriellen Drücke (SAP) von /60 mmhg bis 0/160 mmhg reichten. Die genauen Einstellungen der einzelnen Messungen können der Tabelle 5 entnommen werden. Die rechtsventrikuläre Kennlinie (CL RV) wurde in analoger Weise - mit an den pulmonalen Kreislauf angepassten Parametern - ermittelt. Die Widerstände wurden so eingestellt, dass pulmonalarterielle Drücke (PAP) von /5 mmhg bis /80 mmhg erreicht wurden. Die Vorlast (IP RV) wurde auf 5 mmhg und die Widerstände des linken Ventrikels entsprechend der oben definierten physiologischen Parameter festgesetzt. Tabelle 6 zeigt die gewählten Einstellungen der rechtsventrikulären Kennlinie. Bewusst wurden bei Ermittlung der Kennlinien auch unphysiologisch hohe Nachlasten gewählt, um das VAD im hämodynamischen Grenzbereich zu testen und die Auswirkungen beschreiben. auf Leistungsaufnahme und Temperaturentwicklung zu
34 34 Linksventrikuläre Kennlinie (CL LV) Frequenzen: 60, 70, 80, und 1 bpm Nachlast LV (SAP) Vorlast LV (IP LV) Nachlast RV (PAP) Vorlast RV (IP RV) /60 mmhg 10 mmhg /5 mmhg 5 mmhg 1/80 mmhg 10 mmhg /5 mmhg 5 mmhg 1/ mmhg 10 mmhg /5 mmhg 5 mmhg 160/1 mmhg 10 mmhg /5 mmhg 5 mmhg 180/1 mmhg 10 mmhg /5 mmhg 5 mmhg 0/160 mmhg 10 mmhg /5 mmhg 5 mmhg Tab. 5: Aufstellung der Kreislaufparameter zur Erstellung der linksventrikulären Kennlinie. Bei stabiler Vorlast (IP LV) wurden bei Frequenzen von 60 bis 1 bpm die dargestellten Druckverhältnisse eingestellt und der resultierende VAD-Fluss gemessen. Die Messungen wurden nach 10 Minuten stabiler Druck- und Flussverhältnisse dreimal unabhängig voneinander durchgeführt. Rechtsventrikuläre Kennlinie (CL RV) Frequenzen: 60, 70, 80, und 1 bpm Nachlast LV (SAP) Vorlast LV (IP LV) Nachlast RV (PAP) Vorlast RV (IP RV) 1/80 mmhg 10 mmhg /5 mmhg 5 mmhg 1/80 mmhg 10 mmhg /10 mmhg 5 mmhg 1/80 mmhg 10 mmhg / mmhg 5 mmhg 1/80 mmhg 10 mmhg 60/ mmhg 5 mmhg 1/80 mmhg 10 mmhg 80/60 mmhg 5 mmhg 1/80 mmhg 10 mmhg /80 mmhg 5 mmhg Tab. 6: Einstellung der Kreislaufparameter zur Ermittlung der rechtsventrikulären Kennlinie.
35 Bestimmung der VAD-Funktionskurven Um die hämodynamische Leistungsfähigkeit des neuen BVADs zu beschreiben, wurde zusätzlich zu den oben beschriebenen Kennlinien die Abhängigkeit des VADFlusses von der Vorlast bei konstanter Nachlast getestet. Die resultierenden Kurven entsprechen den sogenannten Cardiac Function Curves des menschlichen Herzens und werden im folgenden als VAD-Funktionskurven bezeichnet. Hierfür wurde bei konstanter Nachlast und Frequenz die Vorlast in diskreten Schritten variiert und der resultierende VAD-Fluss gemessen. Wie bei den oben beschriebenen Kennlinien wurden Frequenzen von 60 bis 1 bpm gewählt. Zur Bestimmung der linksventrikulären VAD-Funktionskurven (VFC LV) wurden, bei jeweils konstantem systemischen arteriellen Druck (SAP), diskrete Vorlasten (IP LV) von - 10 bis mmhg gewählt. Die Messungen der VFC LV wurden bei einem SAP von 1/80, 1/ und 160/1 mmhg durchgeführt. Als Frequenzen wurden 60, 80, und 1 bpm gewählt; die Parameter des rechtsventrikulären Kreislaufs wurden auf physiologische Werte eingestellt (siehe Tabelle 7). Zur Bestimmung der rechtsventrikulären VAD-Funktionskurve (VFC RV) wurde die Nachlast des rechten Kreislaufs (PAP) auf /5 mmhg festgesetzt und die Parameter des linken Kreislaufs auf physiologische Parameter eingestellt (siehe Tabelle 8). 2.6 Temperaturmessung Die Temperaturmessung wurde im Rahmen der Bestimmung der links- und rechtventrikulären Kennlinien, nach 10 minütigem, stabilen Zustand nach der Hämodynamikmessung durchgeführt. Die Temperatursonde war innen am Gehäuse, zwischen Elektromotor und Ventrikel positioniert, das Gehäuse luftdicht verschlossen und die Umgebungstemperatur weitgehend konstant auf 25 C gehalten.
36 36 Linksventrikuläre VAD-Funktionskurve (VFC LV) Frequenzen: 60, 80, und 1 bpm Nachlast LV (SAP) Vorlast LV (IP LV) Nachlast RV (PAP) Vorlast RV (IP RV) 1/80 mmhg - 10 mmhg /5 mmhg 5 mmhg 1/80 mmhg 0 mmhg /5 mmhg 5 mmhg 1/80 mmhg 10 mmhg /5 mmhg 5 mmhg 1/80 mmhg mmhg /5 mmhg 5 mmhg 1/80 mmhg mmhg /5 mmhg 5 mmhg 1/80 mmhg mmhg /5 mmhg 5 mmhg 1/ mmhg - 10 mmhg /5 mmhg 5 mmhg 1/ mmhg 0 mmhg /5 mmhg 5 mmhg 1/ mmhg 10 mmhg /5 mmhg 5 mmhg 1/ mmhg mmhg /5 mmhg 5 mmhg 1/ mmhg mmhg /5 mmhg 5 mmhg 1/ mmhg mmhg /5 mmhg 5 mmhg 160/1 mmhg - 10 mmhg /5 mmhg 5 mmhg 160/1 mmhg 0 mmhg /5 mmhg 5 mmhg 160/1 mmhg 10 mmhg /5 mmhg 5 mmhg 160/1 mmhg mmhg /5 mmhg 5 mmhg 160/1 mmhg mmhg /5 mmhg 5 mmhg 160/1 mmhg mmhg /5 mmhg 5 mmhg Tab. 7: Die Aufstellungen zeigen die Einstellungen des Testkreislaufs zur Ermittlung der linksventrikulären VAD-Funktionskurven. Bei den abgebildeten systemischen Nachlastniveaus (1/60, 1/ und 160/1 mmhg) wurden fünf verschiedene Vorlasten (- 10 bis mmhg) eingestellt und so der Einfluss der Vorlast bei gleicher Nachlast und VAD-Frequenz auf den VAD-Fluss bestimmt.
37 37 Rechtsventrikuläre VAD-Funktionskurve (VFC RV) Frequenzen: 60, 80, und 1 bpm Nachlast LV (SAP) Vorlast LV (IP LV) Nachlast RV (PAP) Vorlast RV (IP RV) 1/80 mmhg 10 mmhg /5 mmhg - 10 mmhg 1/80 mmhg 10 mmhg /5 mmhg 0 mmhg 1/80 mmhg 10 mmhg /5 mmhg 10 mmhg 1/80 mmhg 10 mmhg /5 mmhg mmhg 1/80 mmhg 10 mmhg /5 mmhg mmhg 1/80 mmhg 10 mmhg /5 mmhg mmhg Tab. 8: Die Aufstellung zeigt die Einstellungen des Testkreislaufs zur Ermittlung der rechtsvenrikulären VAD-Funktionskurven.
38 Berechnung des Wirkungsgrads Der Wirkungsgrad (η) eines VADs ist definiert als Quotient aus der hydraulischen und der elektrischen Leistung. Die elektrische Leistung (Pel) bei Gleichstrom ist definiert als das Produkt aus elektrischer Spannung (U) und elektrischer Stromstärke (I): [ ]= [ ] [ ] Zur Berechnung wird die in den Experimenten gemessene Stromstärke (I) mit der internen Betriebsspannung (U) multipliziert. Die hydraulische Leistung (Ph) ist definiert als Produkt von Druckdifferenz (Δp) und Volumenstrom (Q): [ ]= [ ] Zur Berechnung muss stets die hydraulische Leistung des rechten und linken Ventrikels berücksichtigt werden, demnach gilt: [ ]= [ ] [ + ] Somit gilt für den Wirkungsgrad (η) des DLR BVADs folgender Zusammenhang: [%] = [ ] [ ] [ ] [ ]
39 39 3. Ergebnisse 3.1 Kennlinien Die linksventrikulären Kennlinien werden in den Abbildungen 14 a und b gezeigt und stellen die wichtigsten hämodynamischen Eckpunkte des DLR BVADs graphisch dar. Der größte VAD-Fluss wird bei der geringsten Nachlast (/60 mmhg) und der größten Frequenz (1 bpm) dieser Versuchsreihe erreicht und beträgt 4,2 (±0,3) Liter pro Minute (l/min). Wie bei einer Verdrängerpumpe zu erwarten, zeigt sich ein weitgehend linearer Zusammenhang zwischen VAD-Frequenz und Fluss. Bei physiologischen Kreislaufparametern (siehe Methoden), das heißt einer konstanten Nachlast von 1/80 mmhg für den linken Ventrikel und /5 mmhg für den Rechten, zeigt sich für den linken Ventrikel ein Abfall von 4,13 (±0,15) l/min bei 1 bpm auf 3,43 (±0,21) l/min bei bpm, auf 2,6 (±0,2) l/min bei 80 bpm, auf 2,13 (±0,25) l/min bei 70 bpm und auf 1,87 (±0,06) l/min bei 60 bpm. Für den rechten Ventrikel kann eine ähnliche Beziehung, bedingt durch die unterschiedlichen Ventrikelgrößen, auf niedrigerem Niveau gezeigt werden: 3,43 (±0,55) l/min bei 1 bpm auf 2,87 (±0,49) l/min bei bpm, auf 2,23 (±0,31) l/min bei 80 bpm, auf 1,77 (±0,32) l/min bei 70 bpm und auf 1,3 (±0,2) l/min bei 60 bpm (siehe Abbildung 13).
40 4,5 Fluss [l/min] 4,0 3,5 3,0 2,5 Fluss LV 2,0 1,5 1, Frequenz [bpm] 4,5 Fluss [l/min] 4,0 3,5 3,0 2,5 Fluss RV 2,0 1,5 1, Frequenz [bpm] 4,5 4,0 Fluss [l/min] 3,5 3,0 Fluss LV 2,5 Fluss RV 2,0 1,5 1, Frequenz [bpm] Abb. 13: Die Graphen zeigen den VAD-Fluss [l/min] des linken (LV) und rechten (RV) Ventrikels in Abhängigkeit von der Frequenz [bpm] bei konstanter Nachlast (LV: 1/80 mmhg; RV: /5 mmhg) und konstanter Vorlast (IP LV = 5 mmhg; IP RV = 10 mmhg).
41 41 Trägt man bei konstanter Frequenz [bpm] den linksventrikulären VAD-Fluss [l/min] in Abhängigkeit von der Nachlast (systemischer arterieller Druck (SAP) [mmhg]) auf, erhält man die Kennlinie des linken Ventrikels (siehe Abbildungen 14 a und b). In dem für den praktischen Einsatz relevanten Nachlastspektrum kann ein weitgehend linearer Zusammenhang zwischen VAD-Fluss und Nachlast beschrieben werden. Der maximale VAD-Fluss von 4,2 (±0,3) l/min wird bei einer Frequenz 1 bpm und einer Nachlast von /60 mmhg bereitgestellt und fällt bei 1/80 mmhg auf 4,13 (±0,15) l/min, bei 1/ mmhg auf 3,87 (±0,42) l/min, bei 160/1 mmhg auf 3,67 (±0,23) l/min, bei 180/1 mmhg auf 3,43 (±0,06) l/min und bei 0/160 mmhg auf minimal 3,13 (±0,15) l/min. Der kleinste gemessene linksventrikuläre VAD-Fluss beträgt 1,6 (±0,1) l/min bei einer Frequenz von 60 bpm und einer Nachlast von 0/160 mmhg. Senkt man die Nachlast von 0/160 auf /60 mmhg werden bei gleicher Frequenz (60 bpm) 1,82 (±0,06) l/min bereitgestellt. Setzt man die Kennlinien zueinander in Beziehung, erhält man das VAD-spezifische Kennfeld. In diesem ist erkennbar, dass das DLR BVAD bei hohen Frequenzen sensitiver auf Nachlaständerungen reagiert als bei niedrigen Frequenzen (Abbildung 15). Entsprechend ist dies auch in Abbildung 14b zu sehen: Die Steilheit des Abfalls der Flusskurve ist mit zunehmender Nachlast bei hohen Frequenzen größer als bei niedrigen Frequenzen.
42 Fluss [l/min] 42 2,0 1,8 1,6 60 bpm 1, Fluss [l/min] SAP sys [mmhg] 2,4 2,2 2,0 1,8 1,6 70 bpm Fluss [l/min] SAP sys [mmhg] 3,1 2,6 2,1 80 bpm 1, Fluss [l/min] SAP sys [mmhg] 3,8 3,4 3,0 2,6 2,2 1,8 bpm Fluss [l/min] SAP sys [mmhg] 4,3 3,8 3,3 1 bpm 2, SAP sys [mmhg] Abb. 14a: Linksventrikuläre Kennlinien. Dargestellt ist die weitgehend lineare Abhängigkeit des linksventrikulären VADFlusses [l/min] von der Nachlast (SAP sys [mmhg]) bei jeweils konstanter Frequenz [bpm]. (PAP = /5 mmhg; IP RV = 10 mmhg)
43 43 4,5 4,0 Fluss [l/min] 3,5 1 bpm 3,0 bpm 2,5 80 bpm 70 bpm 2,0 60 bpm 1,5 1, SAP sys [mmhg] Abb. 14b: Linksventrikuläre Kennlinien. In der Übersicht aller Frequenzen zeigt sich für die Frequenzen und 1 bpm ein größerer Einfluss der Nachlast (SAP sys [mmhg]) auf den gemessenen VAD-Fluss [l/min] als bei den niedrigeren Frequenzen. (PAP = /5 mmhg; IP RV = 10 mmhg) 4,5 Fluss [l/min] 4,0 3,5 3,0 4,0-4,5 2,5 3,5-4,0 2,0 3,0-3,5 1,5 2,5-3,0 1,0 2,0-2,5 1,5-2,0 1,0-1,5 SAP sys [mmhg] Frequenz [bpm] Abb. 15: Kennfeld des linken Ventrikels. Weitgehend lineare Beziehungen von VAD-Fluss [l/min] und Frequenz [bpm], sowie VAD-Fluss [l/min] und Nachlast (SAP sys [mmhg]).
44 44 Analog zu dem linken Ventrikel wurden, mit an die Anforderungen des Lungenkreislaufes angepassten Parametern (siehe Methoden), Kennlinien des rechten Ventrikels erstellt. Aufgrund des ml kleineren Ventrikels ist das resultierende effektive Schlagvolumen des rechten Ventrikels bei physiologischen Kreislaufparametern mit 27,54 (±3,11) ml um 4,67 ml kleiner als das Schlagvolumen des linken Ventrikels (32,21 (±1,77) ml), dies entspricht einer Differenz von 14,5 % (siehe Abbildung 16). Für den linken Ventrikel ergibt sich somit eine Auswurffraktion von 50 % und für den Rechten eine Auswurffraktion von 61 % bezogen auf das maximale Füllvolumen des jeweiligen Ventrikels. Der maximale VAD-Fluss des rechten Ventrikels ist bei 1 bpm und /5 mmhg mit 3,63 (±0,25) l/min um etwa 0,6 l/min geringer verglichen mit dem des linken Ventrikels (4,2 (±0,3) l/min). Bei 1 bpm fällt mit zunehmender Nachlast der VADFluss von 3,47 (±0,12) l/min bei einem pulmonalarteriellen Druck (PAP) von / mmhg auf 3,23 (±0,4) l/min bei 60/ mmhg und auf 2,63 (±0,21) l/min bei /80 mmhg. Auch die Kennlinien des rechten Ventrikel zeigen eine weitgehend lineare Abhängigkeit von VAD-Fluss und Nachlast. Vergleicht man die frequenzspezifischen Kennlinien untereinander ist auffällig, dass die beim linken Ventrikel ausgeprägte Nachlastsensitivität bei hohen Frequenzen auf den rechten Ventrikel, aufgrund des insgesamt niedrigeren Nachlastniveaus des Lungenkreislaufs, so nicht zutrifft (siehe Abbildungen 17 a und b).
45 45 Schlagvolumen [ml] Linker Ventrikel (LV) Rechter Ventrikel (RV) Abb. 16: Arithmetisches Mittel der errechneten Schlagvolumina des linken und rechten Ventrikels bei physiologischen Testbedingungen und Frequenzen von 60 bis 1 bpm. Das Schlagvolumen (SV) des linken Ventrikels ist mit 32,21 (±1,77) ml um etwa 14,5 % größer als das rechtsventrikuläre SV mit 27,54 (±3,11) ml.
46 Fluss [l/min] 46 1,8 1,6 1,4 1,2 1,0 60 bpm Fluss [l/min] PAP sys [mmhg] 2,4 2,2 2,0 1,8 1,6 1,4 1,2 70 bpm Fluss [l/min] PAP sys [mmhg] 2,8 2,6 2,4 2,2 2,0 1,8 80 bpm Fluss [l/min] PAP sys [mmhg] 3,5 3,0 2,5 bpm 2, Fluss [l/min] PAP sys [mmhg] 4,0 3,5 3,0 2,5 2,0 1 bpm PAP sys [mmhg] Abb. 17a: Rechtsventrikuläre Kennlinien. Dargestellt ist, analog zu den linksventrikulären Kennlinien, die weitgehend lineare Abhängigkeit des rechtsventrikulären VAD-Flusses [l/min] von der Nachlast (PAP sys [mmhg]) bei konstanter Frequenz [bpm]. (SAP = 1/80 mmhg; IP LV = 5 mmhg)
47 47 4,0 Fluss [l/min] 3,5 3,0 1 bpm bpm 2,5 80 bpm 2,0 70 bpm 60 bpm 1,5 1, PAP sys [mmhg] Abb. 17b: Rechtsventrikuläre Kennlinien. An den weitgehend parallelen Ausgleichsgeraden kann man, verglichen mit den linksventrikulären Kennlinien, eine geringere Nachlastsensitivität bei hohen Frequenzen erkennen. 4,0 Fluss [l/min] 3,5 3,0 2,5 3,5-4,0 2,0 3,0-3,5 1,5 2,5-3,0 2,0-2,5 1,0 1,5-2,0 1,0-1,5 PAP sys [mmhg] Frequenz [bpm] Abb. 18: Kennfeld des rechten Ventrikels. Ähnlich dem linken Ventrikel besteht eine weitgehend lineare Beziehung von VADFluss [l/min] und Frequenz [bpm], sowie VAD-Fluss [l/min] und Nachlast (PAP sys [mmhg]).
48 Interventrikuläre Differenz Zur Evaluation eines möglichen Lungenödems während des klinischen Einsatzes des DLR BVADs wurde die Flussdifferenz des linken und rechten Ventrikels bei singulärer und diskreter Steigerung der Nachlast des linken Ventrikels, wie es im Rahmen einer hypertonen Krise vorkommen könnte, gemessen. Wie oben dargestellt, besteht bei physiologischen Testbedingungen eine Flussdifferenz von maximal 0,6 l/min. Mit steigender Nachlast des linken Ventrikels sinkt der gemessene VAD-Fluss, was zu einer geringeren Differenz (ΔFluss) führt. Bei 60 und 70 bpm besteht bei allen Nachlasten stets ein positives ΔFluss (grün markierter Bereich in Abbildung 19). Bei 80 bpm führt lediglich eine Nachlast von 0/160 mmhg zu einem ΔFluss von -0,05 l/min (gelb markierter Bereich Abbildung 19). Bei höheren Frequenzen kommt es bereits ab einer Nachlast von 160/1 mmhg zu einem negativen ΔFluss. Bei einer Frequenz von bpm und einer Nachlast von 0/160 mmhg ist ΔFluss mit -0,55 l/min minimal (rot markierter Bereich in Abbildung 19). Dies bedeutet, dass im klinischen Einsatz bei hypertonen Phasen mit Blutdrücken über 0/160 mmhg die Gefahr eines Lungenödems besteht, da der linke Ventrikel das anfallende Volumen nicht vollständig in den Körperkreislauf befördern kann. 3.3 VAD-Funktionskurven Die folgenden VAD-Funktionskurven (VFC) zeigen den Zusammenhang von Vorlast und VAD-Fluss bei konstanter Nachlast (siehe Abbildungen und 21). Grundsätzlich besteht bei allen ermittelten VFC ein nicht linearer Zusammenhang zwischen Vorlast und VAD-Fluss. Weiterhin kann man bei allen ermittelten Kurven ein Flussplateau bei etwa bis mmhg erkennen. Ein nicht linearer Zusammenhang mit Ausbildung eines Flussplateaus ist charakteristisch für Verdrängerpumpen. Repräsentativ ist die linksventrikuläre Kurve bei einer Frequenz
49 49 von bpm und einer Nachlast von 1/80 mmhg: Bei einer Vorlast von 0 mmhg kann ein VAD-Fluss von 2,23 (±0,15) l/min gemessen werden und bei 10 mmhg 3,47 (±0,15) l/min. Der maximale VAD-Fluss dieser Kurve wird bei einer Vorlast von mmhg mit 4,23 (±0,06) l/min erreicht. Bei mmhg beträgt der gemessene VADFluss 3,93 (±0,06) l/min und bei mmhg 4,0 (±0,17) l/min. 0,6 ΔFluss [l/min] 0,4 0,2 60 bpm 70 bpm -1E , bpm bpm 1 bpm -0,4-0,6 SAP sys [mmhg] Abb. 19: Differenz des links- und rechtsventrikulären VAD-Flusses (ΔFluss [l/min]) bei steigender linksventrikulärer Nachlast (SAP). Dies entspricht dem klinischen Szenario einer hypertonen Krise. Bei physiologischen Testbedingungen ist der linksventrikuläre VAD-Fluss größer als der Rechtsventrikuläre, das heißt ΔFluss ist positiv (grüner Bereich). Der gelbe Bereich markiert ein grenzwertig kleines ΔFluss bei mittleren Nachlasten, der rotmarkierte Bereich zeigt die Testbedingung mit einem stark negativen ΔFluss bei Nachlasten von 0/160 mmhg, bei welchem es bei der klinischen Anwendung zur Gefahr eines Lungenödems kommen kann. (PAP = /5 mmhg; IP LV = 5 mmhg; IP RV = 10 mmhg)
50 Fluss [l/min] 4 1 bpm 3 bpm 2 80 bpm 1 60 bpm IP LV [mmhg] 50 SAP = 1/80 mmhg 6 5 Fluss [l/min] 4 1 bpm 3 bpm 2 80 bpm 1 60 bpm IP LV [mmhg] 50 SAP = 1/ mmhg 6 5 Fluss [l/min] 4 1 bpm 3 bpm 2 80 bpm 1 60 bpm IP LV [mmhg] 50 SAP = 160/1 mmhg Abb. : Linksventrikuläre VAD-Funktionskurven bei Nachlasten (SAP) von 1/80, 1/ und 160/1 mmhg. Die Graphen zeigen die Abhängigkeit des VAD-Flusses [l/min] von der Vorlast (IP LV [mmhg]) bei stabilen Nachlasten, analog der humanen kardialen Funktionskurven. (PAP = /5 mmhg; IP RV = 10 mmhg)
51 Fluss [l/min] 4 1 bpm 3 bpm 2 80 bpm 1 60 bpm IP RV [mmhg] Abb. 21: Rechtsventrikuläre VAD-Funktionskurven bei einer Nachlast von /5 mmhg. Analog zu dem linken Ventrikel wird die Abhängigkeit des VAD-Flusses [l/min] von der Vorlast (IP RV [mmhg]), in diesem Fall klinisch dem Druck im rechten Ventrikel des erkrankten Herzens entsprechend, bei stabiler Nachlast aufgezeigt. (SAP = 1/80 mmhg; IP LV = 5 mmhg) 3.4 Temperatur Als wichtiger Parameter für die spätere Patientenverträglichkeit wurde während der gesamten Experimente die Innengehäusetemperatur gemessen, wobei die PolyamidHalbschalen eine geringe Wärmeleitfähigkeit besitzen. Die Abbildung 22 zeigt den Temperaturverlauf bei der Messung der links- und rechtsventrikulären Kennlinien. Bei Messung der linksventrikulären Kennlinie wird bei einer linksventrikulären Nachlast von 0/160 mmhg und einer Frequenz von 1 bpm und sonst physiologischen Einstellungen mit 38,4 C die höchste Temperatur gemessen. Das arithmetische Mittel beträgt bei diesen Parametern 38,0 (±0,53) C. Bei Bestimmung der rechtsventrikulären Kennlinie beträgt bei einer Nachlast von /80 mmhg und einer Frequenz von 1 bpm und sonst physiologischen Parametern das arithmetische Mittel 37,6 (±1,46) C.
52 52 Insgesamt ist die Temperaturentwicklung insbesondere bei Frequenzen oberhalb von 70 bpm deutlich stärker von den gewählten Frequenzen als von der Nachlast abhängig. Temperatur [ C] bpm 34 bpm bpm 70 bpm 60 bpm SAP sys [mmhg] Temperatur [ C] bpm 34 bpm bpm 70 bpm 60 bpm PAP sys [mmhg] Abb. 22: Innengehäusetemperatur bei Ermittlung der links- (oben) und rechtventrikulären (unten) Kennlinien. Bei Frequenzen oberhalb 70 bpm ist die Temperatur stärker von der Frequenz als von der Nachlast abhängig. (IP LV = 5mmHg; IP RV = 10 mmhg; Oben: PAP = /5 mmhg; Unten: SAP 1/80 mmhg)
53 Stromverbrauch Ein niedriger Stromverbrauch trägt maßgeblich zu einer längeren Akkulaufzeit und somit entscheidend zur Patientenmobilität und Patientenzufriedenheit bei. Die Abbildung 23 zeigt die Leistungsaufnahme des DLR BVADs - als Maß für den Stromverbrauch in einer Stunde - bei Bestimmung der links- und rechtsventrikulären Kennlinien. Bedingt durch das höhere Nachlastniveau des linken Ventrikels besteht hier neben der Frequenzabhängigkeit eine deutliche Abhängigkeit der Leistungsaufnahme von der Nachlast. Bei einer Nachlast von /60 mmhg und einer Frequenz von 60 bpm beträgt die Leistungsaufnahme des Gesamtsystems 5,54 (±0,28) W. Die größte Leistungsaufnahme tritt bei einer Nachlast von 180/1 mmhg und einer Frequenz von 1 bpm auf und beträgt 9,7 (±0,8) W. Aufgrund des niedrigeren Nachlastniveaus hängt die Leistungsaufnahme bei Bestimmung der rechtventrikulären Kennlinien maßgeblich von der gewählten Frequenz ab. Das arithmetische Mittel der VAD-Leistungsaufnahme bei 60 bpm beträgt 5,02 (±0.06) W, bei 80 bpm 6.01 (±0.15) W und bei 1 bpm 7,84 (±0.16) W. 3.6 Wirkungsgrad Mithilfe der gemessenen Kennlinien (Abbildungen 14 a und b, 15, 17 a und b sowie 18) und der gemessenen Leistungsaufnahme (Abbildung 23) kann der Wirkungsgrad in Abhängigkeit von Frequenz und Nachlast berechnet werden (siehe Methoden). Die in Abbildung 24 dargestellten Kurven zeigen für den linken und den rechten Ventrikel ein ähnliches Verhalten. Unerwarteterweise zeigt sich der Wirkungsgrad proportional zur Nachlast und Frequenz. Bei der linksventrikulären Kennlinie wird der höchste Wirkungsgrad von etwa 14 % bei einer Nachlast von 0/160 mmhg und einer Frequenz von 1 bpm erreicht. Der rechte Ventrikel erreicht 15,8 % bei /80 mmhg und bpm.
54 54 10,0 9,5 El. Leistung [W] 9,0 8,5 8,0 1 bpm 7,5 bpm 7,0 80 bpm 6,5 70 bpm 6,0 60 bpm 5,5 5, SAP sys [mmhg] 9,0 8,5 El. Leistung [W] 8,0 7,5 7,0 1 bpm 6,5 bpm 6,0 80 bpm 5,5 70 bpm 5,0 60 bpm 4,5 4, PAP sys [mmhg] Abb. 23: Leistungsaufnahme bei Ermittlung der links- (oben) und rechtventrikulären (unten) Kennlinien. Im Vergleich der links- und rechts ventrikulären Graphen ist die ausgeprägte Korrelation der Leistungsaufnahme [W] zur Nachlast bei Ermittlung der linksventrikulären Kennlinien auffällig. Der untere Graph zeigt eine im Wesentlichen frequenzabhängige Leistungsaufnahme bei den Messungen mit variabler RVNachlast. (IP LV = 5; IP RV = 10 mmhg; Oben: PAP = /5 mmhg; Unten: SAP 1/80 mmhg)
Linksventrikuläre Assist Devices: auch langfristig bei schwererer Herzinsuffizienz?
 KARDIOLOGIE UPDATE 2012 München 16.Dezember Linksventrikuläre Assist Devices: auch langfristig bei schwererer Herzinsuffizienz? Bernhard Voss Deutsches Herzzentrum München Klinik für Herz- und Gefäßchirurgie
KARDIOLOGIE UPDATE 2012 München 16.Dezember Linksventrikuläre Assist Devices: auch langfristig bei schwererer Herzinsuffizienz? Bernhard Voss Deutsches Herzzentrum München Klinik für Herz- und Gefäßchirurgie
Herzunterstützungssysteme: In Zukunft Ersatz für die Herztransplantation?
 Herzunterstützungssysteme: In Zukunft Ersatz für die Herztransplantation? Markus J. Wilhelm Klinik für Herz- und Gefässchirurgie Universitätsspital Zürich 0 Anzahl Herztransplantationen weltweit Number
Herzunterstützungssysteme: In Zukunft Ersatz für die Herztransplantation? Markus J. Wilhelm Klinik für Herz- und Gefässchirurgie Universitätsspital Zürich 0 Anzahl Herztransplantationen weltweit Number
Kunstherz statt Herztransplantation -Aktueller Stand -
 Kunstherz statt Herztransplantation -Aktueller Stand - Christian M. Hagl Herzchirurgische Klinik und Poliklinik Großhadern Herzklinik im Augustinum Aktuelle Situation der Transplantation Evolution der
Kunstherz statt Herztransplantation -Aktueller Stand - Christian M. Hagl Herzchirurgische Klinik und Poliklinik Großhadern Herzklinik im Augustinum Aktuelle Situation der Transplantation Evolution der
Qualitätssicherung für Herzunterstützungssysteme
 Qualitätssicherung für Herzunterstützungssysteme und Kunstherzen Weiterentwicklung des Leistungsbereichs Herztransplantation Göttingen, 14. Mai 2014 Thaddäus Tönnies AQUA Institut für angewandte Qualitätsförderung
Qualitätssicherung für Herzunterstützungssysteme und Kunstherzen Weiterentwicklung des Leistungsbereichs Herztransplantation Göttingen, 14. Mai 2014 Thaddäus Tönnies AQUA Institut für angewandte Qualitätsförderung
Herz-Unterstützungs-Systeme Kunstherz
 Herz-Unterstützungs-Systeme Kunstherz PD Dr. A. Rastan HKZ Rotenburg Jahrestagung des Bundesverbandes Defibrillator (ICD) Deutschland e.v. 08.03.2014 Unser Herz Minute 60 Stunde 3600 Tag 86,400 Monat 2,592,000
Herz-Unterstützungs-Systeme Kunstherz PD Dr. A. Rastan HKZ Rotenburg Jahrestagung des Bundesverbandes Defibrillator (ICD) Deutschland e.v. 08.03.2014 Unser Herz Minute 60 Stunde 3600 Tag 86,400 Monat 2,592,000
Tabelle 1. Prä- und intraoperative Daten in beiden Gruppen.
 6. Ergebnisse 6.1 Patientendaten Es gab keine wesentlichen Unterschiede zwischen beiden Gruppen bei den prä- und intraoperativen Parametern. Der Kreatininwert war präoperativ signifikant höher und der
6. Ergebnisse 6.1 Patientendaten Es gab keine wesentlichen Unterschiede zwischen beiden Gruppen bei den prä- und intraoperativen Parametern. Der Kreatininwert war präoperativ signifikant höher und der
Ventrikuläre Dysfunktion und der Blick auf den kleinen Kreislauf
 60. kardiologisches Expertengespräch Ventrikuläre Dysfunktion und der Blick auf den kleinen Kreislauf Samstag, 24. September 2016 Loisium, Langenlois Faculty Prim. Univ.-Prof. Dr. Herbert Frank Universitätsklinik
60. kardiologisches Expertengespräch Ventrikuläre Dysfunktion und der Blick auf den kleinen Kreislauf Samstag, 24. September 2016 Loisium, Langenlois Faculty Prim. Univ.-Prof. Dr. Herbert Frank Universitätsklinik
Echokardiographie. Definition: Verschiedene Verfahren: Lernhilfen zur Blockpraktikum Kardiologie WS 2015/2016 Mahabadi/Schmidt/Baars
 Definition: Def.: Echokardiographie : Echokardiographie Sonographisches Verfahren zur Beurteilung von Herz und Perikard Liefert detaillierte Informationen über Struktur und Funktion der Herzwände und klappen,
Definition: Def.: Echokardiographie : Echokardiographie Sonographisches Verfahren zur Beurteilung von Herz und Perikard Liefert detaillierte Informationen über Struktur und Funktion der Herzwände und klappen,
Mechanische Herz-Kreislauf- Unterstützung
 Udo Boeken Alexander Assmann Frank Born Christof Schmid (Hrsg.) Mechanische Herz-Kreislauf- Unterstützung Indikationen, Systeme, Implantationstechniken Mit 133 Abbildungen und 28Tabellen Springer IX Inhaltsverzeichnis
Udo Boeken Alexander Assmann Frank Born Christof Schmid (Hrsg.) Mechanische Herz-Kreislauf- Unterstützung Indikationen, Systeme, Implantationstechniken Mit 133 Abbildungen und 28Tabellen Springer IX Inhaltsverzeichnis
Herzinsuffizienz als Syndrom
 Herzinsuffizienz Elektrische Erregung und Kontraktion Westfälische Wilhelms- Universität Münster Herzinsuffizienz als Syndrom Prof. Dr. med. Paulus Kirchhof Medizinische Klinik und Poliklinik C Universitätsklinikum
Herzinsuffizienz Elektrische Erregung und Kontraktion Westfälische Wilhelms- Universität Münster Herzinsuffizienz als Syndrom Prof. Dr. med. Paulus Kirchhof Medizinische Klinik und Poliklinik C Universitätsklinikum
Eine der häufigsten internistischen Folgeerkrankungen
 Herzinsuffizienz Epidemiologie Eine der häufigsten internistischen Folgeerkrankungen Steigende Prävalenz hohe Morbidität und Mortalität 2% der Gesamtbevölkerung altersabhängige Prävalenz Epidemiologie
Herzinsuffizienz Epidemiologie Eine der häufigsten internistischen Folgeerkrankungen Steigende Prävalenz hohe Morbidität und Mortalität 2% der Gesamtbevölkerung altersabhängige Prävalenz Epidemiologie
Herzinsuffizienz wie kann das Pumpversagen vermieden (und behandelt) werden?
 Nottwil, 13. April 2013 Herzinsuffizienz wie kann das Pumpversagen vermieden (und behandelt) werden? René Lerch, Genève Spätkomplikationen des Herzinfarkts Erneuter Infarkt Plötzlicher Herztod 10 30 %
Nottwil, 13. April 2013 Herzinsuffizienz wie kann das Pumpversagen vermieden (und behandelt) werden? René Lerch, Genève Spätkomplikationen des Herzinfarkts Erneuter Infarkt Plötzlicher Herztod 10 30 %
EINSATZ DER IABP IN DER HERZCHIRURGIE
 FRAGEBOGEN ZUR ERSTELLUNG EINER LEITLINIE ZUM EINSATZ DER IABP IN DER HERZCHIRURGIE UNTER FEDERFÜHRUNG DER DEUTSCHEN GESELLSCHAFT FÜR THORAX-, HERZ - UND GEFÄßCHIRURGIE (DGTHG) Frage 1: Wieviele Operationen
FRAGEBOGEN ZUR ERSTELLUNG EINER LEITLINIE ZUM EINSATZ DER IABP IN DER HERZCHIRURGIE UNTER FEDERFÜHRUNG DER DEUTSCHEN GESELLSCHAFT FÜR THORAX-, HERZ - UND GEFÄßCHIRURGIE (DGTHG) Frage 1: Wieviele Operationen
Herztransplantation Interdisz. Vorlesung Prof. Albert Schütz, Deutsches Herzzentrum München
 Herztransplantation Interdisz. Vorlesung 11.05.2005 Prof. Albert Schütz, Deutsches Herzzentrum München Anfänge der Herztransplanation 3.12.1967 Capetown Überleben 18 d 6.12.1967 New York Überleben 6 d
Herztransplantation Interdisz. Vorlesung 11.05.2005 Prof. Albert Schütz, Deutsches Herzzentrum München Anfänge der Herztransplanation 3.12.1967 Capetown Überleben 18 d 6.12.1967 New York Überleben 6 d
Mechanische Herz-Kreislauf-Unterstützung
 Mechanische Herz-Kreislauf-Unterstützung Indikationen, Systeme, Implantationstechniken Bearbeitet von Udo Boeken, Alexander Assmann, Frank Born, Christof Schmid 1. Auflage 2012. Taschenbuch. xxii, 370
Mechanische Herz-Kreislauf-Unterstützung Indikationen, Systeme, Implantationstechniken Bearbeitet von Udo Boeken, Alexander Assmann, Frank Born, Christof Schmid 1. Auflage 2012. Taschenbuch. xxii, 370
KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse
 Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Neue Ergebnisse aus der BEAUTIfUL-Studie KHK mit Angina pectoris: Ivabradin reduziert kardiale Ereignisse Barcelona, Spanien, 31. August 2009 Aktuelle Daten einer auf dem Kongress der European Society
Mechanische Herzunterstützung bei terminaler Niereninsuffizienz. Heiko Mahrholdt Robert Bosch Krankenhaus Stuttgart
 Mechanische Herzunterstützung bei terminaler Niereninsuffizienz Heiko Mahrholdt Robert Bosch Krankenhaus Stuttgart Enhanced survival in other cardiovascular diseases, as well as the aging population, has
Mechanische Herzunterstützung bei terminaler Niereninsuffizienz Heiko Mahrholdt Robert Bosch Krankenhaus Stuttgart Enhanced survival in other cardiovascular diseases, as well as the aging population, has
Telemonitoring von Patienten mit chronischer Herzinsuffizienz - Stellenwert nicht-invasiv ermittelter Vitalparameter
 Aus dem Städtischen Klinikum Brandenburg Brandenburg an der Havel Klinik für Kardiologie, Pulmologie, Angiologie Abteilungsleiter: Prof. Dr. med. Oeff Telemonitoring von Patienten mit chronischer Herzinsuffizienz
Aus dem Städtischen Klinikum Brandenburg Brandenburg an der Havel Klinik für Kardiologie, Pulmologie, Angiologie Abteilungsleiter: Prof. Dr. med. Oeff Telemonitoring von Patienten mit chronischer Herzinsuffizienz
Auf schnellem Weg zur Diagnose
 HERZINSUFFIZIENZ BEI DIABETIKERN Auf schnellem Weg zur Diagnose Denken Sie bei Ihren Diabetes- Patienten an Symptome und Anzeichen einer Herzinsuffizienz. Wir lieben das Leben. Welche Ihrer Diabetes-Patienten
HERZINSUFFIZIENZ BEI DIABETIKERN Auf schnellem Weg zur Diagnose Denken Sie bei Ihren Diabetes- Patienten an Symptome und Anzeichen einer Herzinsuffizienz. Wir lieben das Leben. Welche Ihrer Diabetes-Patienten
NEUE WEGE BEI DER BEHANDLUNG VON HERZINSUFFIZIENZ. VAD-Therapie
 NEUE WEGE BEI DER BEHANDLUNG VON HERZINSUFFIZIENZ VAD-Therapie WELTWEIT ENTWICKELT SICH DIE VAD-THERAPIE ZU EINEM WESENTLICHEN BESTANDTEIL IN DER BEHANDLUNG VON HERZINSUFFIZIENZ. Bei Patienten mit fortgeschrittener
NEUE WEGE BEI DER BEHANDLUNG VON HERZINSUFFIZIENZ VAD-Therapie WELTWEIT ENTWICKELT SICH DIE VAD-THERAPIE ZU EINEM WESENTLICHEN BESTANDTEIL IN DER BEHANDLUNG VON HERZINSUFFIZIENZ. Bei Patienten mit fortgeschrittener
13.04.2015. Mechanische Herzunterstützung AKH Wien. Das Wichtigste für den betreuenden Arzt Herzunterstützungssysteme technisch
 Das Wichtigste für den betreuenden Arzt Herzunterstützungssysteme technisch Thomas Schlöglhofer, BSc. Zentrum für Medizinische Physik und Biomedizinische Technik, Medizinische Universität Wien; Abteilung
Das Wichtigste für den betreuenden Arzt Herzunterstützungssysteme technisch Thomas Schlöglhofer, BSc. Zentrum für Medizinische Physik und Biomedizinische Technik, Medizinische Universität Wien; Abteilung
Obstruktive Schlafapnoe: Risikofaktoren, Therapie und kardiovaskuläre Konsequenzen
 Obstruktive Schlafapnoe: Risikofaktoren, Therapie und kardiovaskuläre Konsequenzen Bernd Sanner Agaplesion Bethesda Krankenhaus Wuppertal Schlafapnoe - Epidemiologie 2-4% der erwachsenen Bevölkerung sind
Obstruktive Schlafapnoe: Risikofaktoren, Therapie und kardiovaskuläre Konsequenzen Bernd Sanner Agaplesion Bethesda Krankenhaus Wuppertal Schlafapnoe - Epidemiologie 2-4% der erwachsenen Bevölkerung sind
Assist-Device Jede Menge Technik im Patienten
 3. internistischer Notfallmedizinkongress Heidelberg 09.12.2017 Assist-Device Jede Menge Technik im Patienten Jan Beckendorf Abt. Innere Medizin III Kardiologie, Angiologie und Pneumologie Warum brauchen
3. internistischer Notfallmedizinkongress Heidelberg 09.12.2017 Assist-Device Jede Menge Technik im Patienten Jan Beckendorf Abt. Innere Medizin III Kardiologie, Angiologie und Pneumologie Warum brauchen
Mitralklappen-Clipping bei Hochrisikopatienten mit degenerativer oder funktioneller Mitralklappeninsuffizienz
 Deutsche Gesellschaft für Kardiologie Herz- und Kreislaufforschung e.v. (DGK) Achenbachstr. 43, 40237 Düsseldorf Geschäftsstelle: Tel: 0211 / 600 692-0 Fax: 0211 / 600 692-10 E-Mail: info@dgk.org Pressestelle:
Deutsche Gesellschaft für Kardiologie Herz- und Kreislaufforschung e.v. (DGK) Achenbachstr. 43, 40237 Düsseldorf Geschäftsstelle: Tel: 0211 / 600 692-0 Fax: 0211 / 600 692-10 E-Mail: info@dgk.org Pressestelle:
Kardiomyopathien. Kardiomyopathien -I- Dilatative, hypertrophe, restriktive und andere. Prof. Dr. med. Matthias Paul
 Kardiomyopathien Kardiomyopathien -I- -I- Dilatative, hypertrophe, restriktive und andere Dilatative, hypertrophe, restriktive und andere Prof. Dr. med. Matthias Paul Department für Kardiologie und Angiologie
Kardiomyopathien Kardiomyopathien -I- -I- Dilatative, hypertrophe, restriktive und andere Dilatative, hypertrophe, restriktive und andere Prof. Dr. med. Matthias Paul Department für Kardiologie und Angiologie
6 Nebenwirkungen der Beatmung
 344 6 Nebenwirkungen der Beatmung Neben den positiven Effekten der maschinellen Beatmung, nämlich der Verbesserung des Gasaustausches mit gesteigerter O 2 -Transportkapazität und der Reduzierung der Atemarbeit,
344 6 Nebenwirkungen der Beatmung Neben den positiven Effekten der maschinellen Beatmung, nämlich der Verbesserung des Gasaustausches mit gesteigerter O 2 -Transportkapazität und der Reduzierung der Atemarbeit,
Die Thrombin-Therapie beim Aneurysma spurium nach arterieller Punktion
 Aus der Universitätsklinik und Poliklinik für Innere Medizin III der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. K. Werdan) und dem Herzzentrum Coswig Klinik für Kardiologie und
Aus der Universitätsklinik und Poliklinik für Innere Medizin III der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. K. Werdan) und dem Herzzentrum Coswig Klinik für Kardiologie und
Harald, trägt seit 2014 das HeartMate 3 DAS LEBEN GENIESSEN. mit jedem neuen Tag. Astrid, trägt seit 2014 das HeartMate 3
 Harald, trägt seit 2014 das HeartMate 3 DAS LEBEN GENIESSEN mit jedem neuen Tag Astrid, trägt seit 2014 das HeartMate 3 Fortgeschrittene Herzinsuffizienz verstehen Wenn Ihr Herz gut funktioniert, bemerken
Harald, trägt seit 2014 das HeartMate 3 DAS LEBEN GENIESSEN mit jedem neuen Tag Astrid, trägt seit 2014 das HeartMate 3 Fortgeschrittene Herzinsuffizienz verstehen Wenn Ihr Herz gut funktioniert, bemerken
II. ERKRANKUNGEN DES PERIKARDS KARDIOMYOPATHIEN MYOKARDHYPERTROPHIE HERZINSUFFIZIENZ
 Herz, Kreislauf, Gefässe II. ERKRANKUNGEN DES PERIKARDS KARDIOMYOPATHIEN MYOKARDHYPERTROPHIE HERZINSUFFIZIENZ PERIKARD Aufbau Viszerales Blatt (=Epikard) Parietales Blatt (=Perikard) Funktion Schutzfunktion
Herz, Kreislauf, Gefässe II. ERKRANKUNGEN DES PERIKARDS KARDIOMYOPATHIEN MYOKARDHYPERTROPHIE HERZINSUFFIZIENZ PERIKARD Aufbau Viszerales Blatt (=Epikard) Parietales Blatt (=Perikard) Funktion Schutzfunktion
Die mechanische Kreislaufunterstützung (MKU) wird heute bei verschiedenen Indikationen. Überschneidungen und Änderungen der Therapieziele.
 10 Kapitel 2 Indikationen zur mechanischen Kreislaufunterstützung 2.1 Therapieziele (BTB, BTT, BTR, DT) 2 Die mechanische Kreislaufunterstützung (MKU) wird heute bei verschiedenen Indikationen eingesetzt:»bridge
10 Kapitel 2 Indikationen zur mechanischen Kreislaufunterstützung 2.1 Therapieziele (BTB, BTT, BTR, DT) 2 Die mechanische Kreislaufunterstützung (MKU) wird heute bei verschiedenen Indikationen eingesetzt:»bridge
Möglichkeiten und sinnvolle Grenzen der präoperativen Diagnostik des multimorbiden Dialysepatienten aus internistisch-kardiologischer Sicht
 Möglichkeiten und sinnvolle Grenzen der präoperativen Diagnostik des multimorbiden Dialysepatienten aus internistisch-kardiologischer Sicht Dr. med. Michael Liebetrau 1 Kardiovaskuläre Risikofaktoren 2
Möglichkeiten und sinnvolle Grenzen der präoperativen Diagnostik des multimorbiden Dialysepatienten aus internistisch-kardiologischer Sicht Dr. med. Michael Liebetrau 1 Kardiovaskuläre Risikofaktoren 2
Monate Präop Tabelle 20: Verteilung der NYHA-Klassen in Gruppe 1 (alle Patienten)
 Parameter zur Beschreibung der Leistungsfähigkeit Klassifikation der New-York-Heart-Association (NYHA) Gruppe 1 (alle Patienten): Die Eingruppierung der Patienten in NYHA-Klassen als Abbild der Schwere
Parameter zur Beschreibung der Leistungsfähigkeit Klassifikation der New-York-Heart-Association (NYHA) Gruppe 1 (alle Patienten): Die Eingruppierung der Patienten in NYHA-Klassen als Abbild der Schwere
Herzinsuffizienz-Chirurgie Terminale Herzinsuffizienz
 Herzinsuffizienz-Chirurgie Terminale Herzinsuffizienz Dr. Mehmet Oezkur Bereichsleiter Herzinsuffizienz Mitteldeutsches Herzzentrum Universitätsmedizin Halle (Saale) 2 Epidemie Herzinsuffizienz Entwicklung
Herzinsuffizienz-Chirurgie Terminale Herzinsuffizienz Dr. Mehmet Oezkur Bereichsleiter Herzinsuffizienz Mitteldeutsches Herzzentrum Universitätsmedizin Halle (Saale) 2 Epidemie Herzinsuffizienz Entwicklung
Medikation und apparative Therapie der Herz-/ Niereninsuffizienz. Prof. Dr. med. Michael Koch
 Medikation und apparative Therapie der Herz-/ Niereninsuffizienz Prof. Dr. med. Michael Koch Agenda Epidemiologie der Herzinsuffizienz Pathophysiologie der Herzinsuffizienz Pathophysiologie der Rechtsherzinsuffizienz
Medikation und apparative Therapie der Herz-/ Niereninsuffizienz Prof. Dr. med. Michael Koch Agenda Epidemiologie der Herzinsuffizienz Pathophysiologie der Herzinsuffizienz Pathophysiologie der Rechtsherzinsuffizienz
Rehabilitation von Patienten mit Herzinsuffizienz , Uhr 4. Gesundheitssymposium Mainfranken DZHI Würzburg P. Deeg
 Rehabilitation von Patienten mit Herzinsuffizienz 23.03.2017, 17.40 Uhr 4. Gesundheitssymposium Mainfranken DZHI Würzburg P. Deeg Häufigkeit der Herzinsuffizienz in Deutschland 2015 Herzinsuffizienz Verstorben
Rehabilitation von Patienten mit Herzinsuffizienz 23.03.2017, 17.40 Uhr 4. Gesundheitssymposium Mainfranken DZHI Würzburg P. Deeg Häufigkeit der Herzinsuffizienz in Deutschland 2015 Herzinsuffizienz Verstorben
Experimentelle und klinische Dosimetrie. bei der Doppelkontrastuntersuchung des Dünndarms. (Enteroklysma nach Sellink / Herlinger)
 Aus der Klinik für Radiologie und Nuklearmedizin des Universitätsklinikums Benjamin Franklin der Freien Universität Berlin Geschäftsführender Direktor: Prof. Dr. K.-J. Wolf Experimentelle und klinische
Aus der Klinik für Radiologie und Nuklearmedizin des Universitätsklinikums Benjamin Franklin der Freien Universität Berlin Geschäftsführender Direktor: Prof. Dr. K.-J. Wolf Experimentelle und klinische
Herzinsuffizienz-Wachstation oder Advanced Heart Failure Unit (AHFU)
 Fakten im Überblick Herzinsuffizienz-Wachstation oder Advanced Heart Failure Unit (AHFU) - Die Heidelberger Herzinsuffizienz-Wachstation Advanced Heart Failure Unit (AHFU) hat deutschlandweit Modellcharakter;
Fakten im Überblick Herzinsuffizienz-Wachstation oder Advanced Heart Failure Unit (AHFU) - Die Heidelberger Herzinsuffizienz-Wachstation Advanced Heart Failure Unit (AHFU) hat deutschlandweit Modellcharakter;
DEUTSCHE GESELLSCHAFT FÜR KARDIOLOGIE HERZ- UND KREISLAUFFORSCHUNG e.v. German Cardiac Society
 Vergleich zwischen Flächen- und Perimeter-basierter Bestimmung der effektiven Anulusgröße mit der direkten intraoperativen Messung Dr. Won-Keun Kim, Bad Nauheim Einleitung: Die präzise Messung des Aortenanulus
Vergleich zwischen Flächen- und Perimeter-basierter Bestimmung der effektiven Anulusgröße mit der direkten intraoperativen Messung Dr. Won-Keun Kim, Bad Nauheim Einleitung: Die präzise Messung des Aortenanulus
Herztransplantation und Herzersatzsysteme
 Herztransplantation und Herzersatzsysteme Dr. med. N. Pizanis Klinik für Thorax- und Kardiovaskuläre Chirurgie nikolaus.pizanis@uk-essen.de www.whze.de Do Fr Mo Di Fr 22.10.09 23.10.09 26.10.09 27.10.09
Herztransplantation und Herzersatzsysteme Dr. med. N. Pizanis Klinik für Thorax- und Kardiovaskuläre Chirurgie nikolaus.pizanis@uk-essen.de www.whze.de Do Fr Mo Di Fr 22.10.09 23.10.09 26.10.09 27.10.09
Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H.
 Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H. Dralle Gastric-banding als Operationsmethode bei morbider Adipositas
Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H. Dralle Gastric-banding als Operationsmethode bei morbider Adipositas
Leitfaden Herztransplantation
 Leitfaden Herztransplantation Interdisziplinäre Betreuung vor, während und nach Herztransplantation Bearbeitet von Christof Schmid, Stephan Hirt, Hans Heinrich Scheld 3. Aufl. 2009. Taschenbuch. xi, 208
Leitfaden Herztransplantation Interdisziplinäre Betreuung vor, während und nach Herztransplantation Bearbeitet von Christof Schmid, Stephan Hirt, Hans Heinrich Scheld 3. Aufl. 2009. Taschenbuch. xi, 208
Herzinsuffizienz und Vorhofflimmern
 und Vorhofflimmern Herzinsuffizienz - braucht jeder einen ICD? Hans-Joachim Trappe Med. Univ.-Klinik II II (Kardiologie/Angiologie) Ruhr-Universität Bochum 23. 23. Bielefelder Seminar über über aktuelle
und Vorhofflimmern Herzinsuffizienz - braucht jeder einen ICD? Hans-Joachim Trappe Med. Univ.-Klinik II II (Kardiologie/Angiologie) Ruhr-Universität Bochum 23. 23. Bielefelder Seminar über über aktuelle
Unverändert höheres Risikoprofil von Frauen in der Sekundärprävention der KHK Sechs-Jahres-Verlauf an Patienten
 Deutsche Gesellschaft für Kardiologie Herz- und Kreislaufforschung e.v. (DGK) Achenbachstr. 43, 40237 Düsseldorf Geschäftsstelle: Tel: 0211 6006920 Fax: 0211 60069267 mail : info@dgk.org Pressestelle:
Deutsche Gesellschaft für Kardiologie Herz- und Kreislaufforschung e.v. (DGK) Achenbachstr. 43, 40237 Düsseldorf Geschäftsstelle: Tel: 0211 6006920 Fax: 0211 60069267 mail : info@dgk.org Pressestelle:
Akute und langfristige hämodynamische Auswirkungen einer MitraClip-Implantation auf eine vorbestehende sekundäre Rechtsherzinsuffizienz
 Akute und langfristige hämodynamische Auswirkungen einer MitraClip-Implantation auf eine vorbestehende sekundäre Rechtsherzinsuffizienz Dr. Mark Hünlich, Göttingen Die Mitralklappeninsuffizienz ist nach
Akute und langfristige hämodynamische Auswirkungen einer MitraClip-Implantation auf eine vorbestehende sekundäre Rechtsherzinsuffizienz Dr. Mark Hünlich, Göttingen Die Mitralklappeninsuffizienz ist nach
Behandlung der arteriellen Hypertonie - Wie lautet der Zielwert 2016?
 Behandlung der arteriellen Hypertonie - Wie lautet der Zielwert 2016? Hannes Reuter Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Patient 1 Risikofaktoren: Blutdruck 167/96 mmhg Typ
Behandlung der arteriellen Hypertonie - Wie lautet der Zielwert 2016? Hannes Reuter Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Patient 1 Risikofaktoren: Blutdruck 167/96 mmhg Typ
Ist der Ersatz der Porzellanaorta bei Aortenstenose ein Hochrisikoeingriff?
 Aus der Klinik für Thorax- Herz-Gefäßchirurgie Universitätsklinikum des Saarlandes, Homburg / Saar Ist der Ersatz der Porzellanaorta bei Aortenstenose ein Hochrisikoeingriff? Dissertation zur Erlangung
Aus der Klinik für Thorax- Herz-Gefäßchirurgie Universitätsklinikum des Saarlandes, Homburg / Saar Ist der Ersatz der Porzellanaorta bei Aortenstenose ein Hochrisikoeingriff? Dissertation zur Erlangung
3.1 Dauerhafter Hochdruck versus temporärer. 3.1 Dauerhafter Hochdruck versus temporärer Hochdruck
 3.1 Dauerhafter Hochdruck versus temporärer 9 3.1 Dauerhafter Hochdruck versus temporärer Hochdruck A Grundsätzlich muss zwischen den dauerhaften und den temporären Blutdrucksteigerungen unterschieden
3.1 Dauerhafter Hochdruck versus temporärer 9 3.1 Dauerhafter Hochdruck versus temporärer Hochdruck A Grundsätzlich muss zwischen den dauerhaften und den temporären Blutdrucksteigerungen unterschieden
Die Bedeutung des Shuntvolumens bei linksventrikulärer Funktionseinschränkung
 Die Bedeutung des Shuntvolumens bei linksventrikulärer Funktionseinschränkung Dr. med. Michael Liebetrau Gliederung Definition Herzinsuffizienz Shuntfluß und Cardiac Output Beziehung zwischen Herzinsuffizienz
Die Bedeutung des Shuntvolumens bei linksventrikulärer Funktionseinschränkung Dr. med. Michael Liebetrau Gliederung Definition Herzinsuffizienz Shuntfluß und Cardiac Output Beziehung zwischen Herzinsuffizienz
6. Qualitätssicherungskonferenz
 6. Qualitätssicherungskonferenz Externe stationäre Qualitätssicherung Herz- und Lungentransplantation Berlin, 23.09.2014 Prof. Dr. Martin Strüber Universität Leipzig, Herzzentrum 2014 AQUA-Institut GmbH
6. Qualitätssicherungskonferenz Externe stationäre Qualitätssicherung Herz- und Lungentransplantation Berlin, 23.09.2014 Prof. Dr. Martin Strüber Universität Leipzig, Herzzentrum 2014 AQUA-Institut GmbH
Herzinsuffizienz Sehen, worauf es ankommt
 Herzinsuffizienz Sehen, worauf es ankommt NEUE LEITLINIEN DER E U R O P E A N S O C I E T Y I O L O G Y O F C A R D NT-proBNP für eine frühere Diagnose und bessere Therapieüberwachung Könnte es vom Herzen
Herzinsuffizienz Sehen, worauf es ankommt NEUE LEITLINIEN DER E U R O P E A N S O C I E T Y I O L O G Y O F C A R D NT-proBNP für eine frühere Diagnose und bessere Therapieüberwachung Könnte es vom Herzen
Betreuung des Patienten mit einem VAD
 Betreuung des Patienten mit einem VAD Jacqueline Zuber Zibung & Beate Hugi-Mayr VAD-Koordinatorin/Pflegefachfrau VAD-Koordinatorin/Kardiotechnikerin Universitätsklinik für Kardiologie Definition VAD (Ventricular
Betreuung des Patienten mit einem VAD Jacqueline Zuber Zibung & Beate Hugi-Mayr VAD-Koordinatorin/Pflegefachfrau VAD-Koordinatorin/Kardiotechnikerin Universitätsklinik für Kardiologie Definition VAD (Ventricular
Möglichkeiten der Devicetherapie bei Herzinsuffizienz Was für wen?
 MHHas Rhythm 02.12.2017 Möglichkeiten der Devicetherapie bei Herzinsuffizienz Was für wen? CRT Baroreflexaktivierung Linksschenkelblock Vorhofflimmern erhöhter Sympathikotonus Herzinsuffizienz (HFrEF)
MHHas Rhythm 02.12.2017 Möglichkeiten der Devicetherapie bei Herzinsuffizienz Was für wen? CRT Baroreflexaktivierung Linksschenkelblock Vorhofflimmern erhöhter Sympathikotonus Herzinsuffizienz (HFrEF)
am Was ist neu in der Kardiologie? H.Reuter
 am 22.5.2007 Seite 1 Körperliche Belastung bei Herzerkrankungen: Ist Sport wirklich Mord? Hannes Reuter Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Körperliche Belastung bei Herzerkrankungen:
am 22.5.2007 Seite 1 Körperliche Belastung bei Herzerkrankungen: Ist Sport wirklich Mord? Hannes Reuter Klinik III für Innere Medizin Herzzentrum der Universität zu Köln Körperliche Belastung bei Herzerkrankungen:
Bundesauswertung zum Erfassungsjahr Herzunterstützungssysteme/Kunstherzen. Qualitätsindikatoren
 Bundesauswertung zum Erfassungsjahr 2015 Herzunterstützungssysteme/Kunstherzen Qualitätsindikatoren Erstellt am: 25.05.2016 Impressum Impressum Herausgeber: IQTIG Institut für Qualitätssicherung und Transparenz
Bundesauswertung zum Erfassungsjahr 2015 Herzunterstützungssysteme/Kunstherzen Qualitätsindikatoren Erstellt am: 25.05.2016 Impressum Impressum Herausgeber: IQTIG Institut für Qualitätssicherung und Transparenz
standardisierten Fragebogen, dokumentiert. Ebenso wurde bei den 14 Patienten mit CSA spiroergometrisch eine Verbesserung der ventilatorischen
 4 DISKUSSION Anhand der Ergebnisse dieser Studie ergaben sich keine signifikanten Änderungen bei den nächtlich untersuchten kardiorespiratorischen Polygraphieparametern im Akutversuch einer kardialen Resynchronisation
4 DISKUSSION Anhand der Ergebnisse dieser Studie ergaben sich keine signifikanten Änderungen bei den nächtlich untersuchten kardiorespiratorischen Polygraphieparametern im Akutversuch einer kardialen Resynchronisation
Datenfelder mit Leitlinienbezug im Leistungsbereich Implantierbare Defibrillatoren Implantation (09/4) Erfassungsjahr 2019
 Datenfelder mit Leitlinienbezug im Leistungsbereich Implantierbare Defibrillatoren Implantation (09/4) Erfassungsjahr 2019 Erstellt im Auftrag des Gemeinsamen Bundesausschusses Stand: 31. Juli 2018 Impressum
Datenfelder mit Leitlinienbezug im Leistungsbereich Implantierbare Defibrillatoren Implantation (09/4) Erfassungsjahr 2019 Erstellt im Auftrag des Gemeinsamen Bundesausschusses Stand: 31. Juli 2018 Impressum
Kardiogener Schock. Interventionelle und kreislaufunterstützende Therapie
 Kardiogener Schock Interventionelle und kreislaufunterstützende Therapie Ralf Westenfeld Klinik für Kardiologie, Pneumologie und Angiologie Heinrich-Heine-Universität Düsseldorf 2010_Kardiogener_Schock.ppt
Kardiogener Schock Interventionelle und kreislaufunterstützende Therapie Ralf Westenfeld Klinik für Kardiologie, Pneumologie und Angiologie Heinrich-Heine-Universität Düsseldorf 2010_Kardiogener_Schock.ppt
Ventrikuläre Extrasystolen - wann und wie behandeln?
 BIK Bayerischer Internisten Kongress München, 21.10.2017 Ventrikuläre Extrasystolen - wann und wie behandeln? Christopher Reithmann Medizinische Klinik I Kardiologie und Internistische Intensivmedizin
BIK Bayerischer Internisten Kongress München, 21.10.2017 Ventrikuläre Extrasystolen - wann und wie behandeln? Christopher Reithmann Medizinische Klinik I Kardiologie und Internistische Intensivmedizin
MEDOS VAD III -System. mobiles Herzunterstützungssystem für Erwachsene, Kinder und Säuglinge
 MEDOS VAD III -System mobiles Herzunterstützungssystem für Erwachsene, Kinder und Säuglinge MEDOS VAD III -System mobiles Herzunterstützungssystem für Erwachsene, Kinder und Säuglinge Das MEDOS VAD III
MEDOS VAD III -System mobiles Herzunterstützungssystem für Erwachsene, Kinder und Säuglinge MEDOS VAD III -System mobiles Herzunterstützungssystem für Erwachsene, Kinder und Säuglinge Das MEDOS VAD III
Mitralklappeninsuffizienz
 Mitralklappeninsuffizienz Definition: Mitralklappeninsuffizienz Schlussunfähigkeit der Mitralklappe mit systolischem Blutreflux in den linken Vorhof Zweithäufigstes operiertes Klappenvitium Jährliche Inzidenz:
Mitralklappeninsuffizienz Definition: Mitralklappeninsuffizienz Schlussunfähigkeit der Mitralklappe mit systolischem Blutreflux in den linken Vorhof Zweithäufigstes operiertes Klappenvitium Jährliche Inzidenz:
Voruntersuchungen. Klinik für Anästhesiologie und Intensivmedizin
 Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Inhalt. 1 Lage, Größe und Form des Herzens Diagnostische Möglichkeiten 15
 Inhalt 1 Lage, Größe und Form des Herzens 13 2 Diagnostische Möglichkeiten 15 2.1 Inspektion 15 2.2 Palpation 16 2.3 EKG 16 2.3.1 Belastungs-EKG 17 2.3.2 Langzeit-EKG 18 2.4 Herzkatheter 19 2.4.1 Diagnostische
Inhalt 1 Lage, Größe und Form des Herzens 13 2 Diagnostische Möglichkeiten 15 2.1 Inspektion 15 2.2 Palpation 16 2.3 EKG 16 2.3.1 Belastungs-EKG 17 2.3.2 Langzeit-EKG 18 2.4 Herzkatheter 19 2.4.1 Diagnostische
Leben mit künstlicher Herzunterstützung (VAD) Info-Broschüre für Patientinnen, Patienten und ihre Angehörigen
 Leben mit künstlicher Herzunterstützung (VAD) Info-Broschüre für Patientinnen, Patienten und ihre Angehörigen Herz- und Diabeteszentrum NRW Bad Oeynhausen Liebe Patientin, lieber Patient, Wer weiß schon,
Leben mit künstlicher Herzunterstützung (VAD) Info-Broschüre für Patientinnen, Patienten und ihre Angehörigen Herz- und Diabeteszentrum NRW Bad Oeynhausen Liebe Patientin, lieber Patient, Wer weiß schon,
Bedeutung der Bestimmung der Vitamin D 3 - Konzentration im Serum bei dialysepflichtiger terminaler Niereninsuffizienz
 Aus der Universitätsklinik und Poliklinik für Innere Medizin II an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. B. Osten) Bedeutung der Bestimmung der Vitamin D 3 - Konzentration
Aus der Universitätsklinik und Poliklinik für Innere Medizin II an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. B. Osten) Bedeutung der Bestimmung der Vitamin D 3 - Konzentration
Prädisponierende Faktoren für kardiale Ereignisse bei Patienten mit langem QT-Syndrom der Unterform 2 (LQT2)
 Prädisponierende Faktoren für kardiale Ereignisse bei Patienten mit langem QT-Syndrom der Unterform 2 (LQT2) Dr. Sven Zumhagen, Münster Hintergrund: Das angeborene, lange QT-Syndrom (LQTS) ist charakterisiert
Prädisponierende Faktoren für kardiale Ereignisse bei Patienten mit langem QT-Syndrom der Unterform 2 (LQT2) Dr. Sven Zumhagen, Münster Hintergrund: Das angeborene, lange QT-Syndrom (LQTS) ist charakterisiert
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie
 Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Schwindel [75] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf unter Mitarbeit von Dr. med. V.T. Schulze Version 02.10.2013
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Schwindel [75] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf unter Mitarbeit von Dr. med. V.T. Schulze Version 02.10.2013
Kardiale Unterstützungssysteme
 T. Pier, St. Seiler, St. Klotz, Ch. Schmid, Ch. D. Etz, H. H. Scheld Klinik und Poliklinik für Thorax-, Herz- und Gefäßchirurgie Westfälische Wilhelms-Universität Münster (Direktor: Prof. Dr. H. H. Scheld)
T. Pier, St. Seiler, St. Klotz, Ch. Schmid, Ch. D. Etz, H. H. Scheld Klinik und Poliklinik für Thorax-, Herz- und Gefäßchirurgie Westfälische Wilhelms-Universität Münster (Direktor: Prof. Dr. H. H. Scheld)
Krankheitsbild und Epidemiologie des akuten Koronarsyndroms
 Krankheitsbild und Epidemiologie des akuten Koronarsyndroms Uwe Zeymer Herzzentrum Ludwigshafen Institut für Herzinfarktforschung Ludwigshafen Forum Herz: Versorgung bei Akutem Koronarsyndrom Berlin, 26.11.2015
Krankheitsbild und Epidemiologie des akuten Koronarsyndroms Uwe Zeymer Herzzentrum Ludwigshafen Institut für Herzinfarktforschung Ludwigshafen Forum Herz: Versorgung bei Akutem Koronarsyndrom Berlin, 26.11.2015
Max. Sauerstoffaufnahme im Altersgang
 Max. Sauerstoffaufnahme im Altersgang Motorische Hauptbeanspruchungsformen im Alter Anteil chronischer Erkrankungen an den Gesamtkosten in Abhängigkeit vom Alter AOK Bundesverband, Bonn, 2002 Prävalenz
Max. Sauerstoffaufnahme im Altersgang Motorische Hauptbeanspruchungsformen im Alter Anteil chronischer Erkrankungen an den Gesamtkosten in Abhängigkeit vom Alter AOK Bundesverband, Bonn, 2002 Prävalenz
ESC München Schrittmacher, ICD, kardiale Resynchronisation ( CRT ) Dr. Dorothee Meyer zu Vilsendorf
 ESC München 2008 Schrittmacher, ICD, kardiale Resynchronisation ( CRT ) Dr. Dorothee Meyer zu Vilsendorf Klinik für Kardiologie und Internistische Intensivmedizin, Städtische Kliniken Bielefeld ESC München
ESC München 2008 Schrittmacher, ICD, kardiale Resynchronisation ( CRT ) Dr. Dorothee Meyer zu Vilsendorf Klinik für Kardiologie und Internistische Intensivmedizin, Städtische Kliniken Bielefeld ESC München
Dissertation. zur Erlangung des akademischen Grades Doktor der Medizin (Dr. med.)
 Aus der Universitätsklinik und Poliklinik für Innere Medizin III an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. K. Werdan) Arrhythmien und eingeschränkte Herzfrequenzvariabilität
Aus der Universitätsklinik und Poliklinik für Innere Medizin III an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. K. Werdan) Arrhythmien und eingeschränkte Herzfrequenzvariabilität
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie
 Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Patient mit Schock/Kreislaufversagen [45] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf unter Mitarbeit von Dr. med. S.
Study Guide Klinik für Kardiologie, Pneumologie und Angiologie Task: Patient mit Schock/Kreislaufversagen [45] Autoren: Dr. med. S. Keymel/Univ.-Prof. Dr. med. T. Rassaf unter Mitarbeit von Dr. med. S.
Implementation eines präoperativen Risikoscores zur Abschätzung der Sterblichkeit nach Implantation eines ventrikulären mechanischen Assist-Systems
 Aus dem Universitätsklinikum Münster Klinik und Poliklinik für Thorax-, Herz- und Gefäßchirurgie Direktor: Univ.-Prof. Dr. med. Hans H. Scheld Implementation eines präoperativen Risikoscores zur Abschätzung
Aus dem Universitätsklinikum Münster Klinik und Poliklinik für Thorax-, Herz- und Gefäßchirurgie Direktor: Univ.-Prof. Dr. med. Hans H. Scheld Implementation eines präoperativen Risikoscores zur Abschätzung
3.2 Auswertung der 12-Kanal-Langzeit-EKGs über 24 Stunden
 16 3 Ergebnisse 3.1 Patientenkollektiv In unserer Studie wurden insgesamt 55 Patientinnen und Patienten untersucht. Darunter fanden sich 18 Gesunde, das sogenannte Kontrollkollektiv, 12 Patienten mit koronarer
16 3 Ergebnisse 3.1 Patientenkollektiv In unserer Studie wurden insgesamt 55 Patientinnen und Patienten untersucht. Darunter fanden sich 18 Gesunde, das sogenannte Kontrollkollektiv, 12 Patienten mit koronarer
Komplikationen der Transplantat-Nephrektomie
 Komplikationen der Transplantat-Nephrektomie Stefan Hauser Klinik und Poliklinik für Urologie und Kinderurologie AK Nierentransplantation am 22.11-23.11.13 Ergebnisse Nierentransplantation Verlust der
Komplikationen der Transplantat-Nephrektomie Stefan Hauser Klinik und Poliklinik für Urologie und Kinderurologie AK Nierentransplantation am 22.11-23.11.13 Ergebnisse Nierentransplantation Verlust der
Kardiale apparative Diagnostik Echokardiographie. Echokardiographie. Einführung in die Echokardiographie Standardschnitte
 Kardiale apparative Diagnostik Echokardiographie Medizinische Klinik und Poliklinik I Direktor: Prof. Dr. Stefan Frantz Echokardiographie Nicht invasiv Bildgebung Diameter Wandstärken Klappen Einführung
Kardiale apparative Diagnostik Echokardiographie Medizinische Klinik und Poliklinik I Direktor: Prof. Dr. Stefan Frantz Echokardiographie Nicht invasiv Bildgebung Diameter Wandstärken Klappen Einführung
Echokardiographie: Das Flaggschiff der Bildgebung in der Herzinsuffizienz
 Echokardiographie: Das Flaggschiff der Bildgebung in der Herzinsuffizienz Caroline Morbach Academic Core Lab Ultrasound-based Cardiovascular Imaging Deutschen Zentrum für Herzinsuffizienz und Medizinische
Echokardiographie: Das Flaggschiff der Bildgebung in der Herzinsuffizienz Caroline Morbach Academic Core Lab Ultrasound-based Cardiovascular Imaging Deutschen Zentrum für Herzinsuffizienz und Medizinische
4.1 AV-Zeitverlängerung nach atrialer Stimulation
 41 4 ERGEBNISSE 4.1 AV-Zeitverlängerung nach atrialer Stimulation Nach Ausschluss von Hinweisen auf eine höhergradige atrioventrikuläre Leitungsstörung wurde die AV-Zeit nach atrialer Stimulation im DDIR-Modus
41 4 ERGEBNISSE 4.1 AV-Zeitverlängerung nach atrialer Stimulation Nach Ausschluss von Hinweisen auf eine höhergradige atrioventrikuläre Leitungsstörung wurde die AV-Zeit nach atrialer Stimulation im DDIR-Modus
Neues aus der Intensivmedizin: Kardiogener Schock
 Klinische Präsentation der akuten Herzinsuffizienz Medizinische Klinik und Poliklinik I Direktor: Prof. Dr. G. Ertl Einteilung nach ESC-Leitlinien Neues aus der Intensivmedizin: Kardiogener Schock Stefan
Klinische Präsentation der akuten Herzinsuffizienz Medizinische Klinik und Poliklinik I Direktor: Prof. Dr. G. Ertl Einteilung nach ESC-Leitlinien Neues aus der Intensivmedizin: Kardiogener Schock Stefan
Weiterentwicklung des Leistungsbereiches Herztransplantation
 Sektorenübergreifende Qualitätssicherung im Gesundheitswesen nach 137a SGB V Weiterentwicklung des Leistungsbereiches Herztransplantation Indikatorenset 1.0 Stand: 15. März 2014 AQUA Institut für angewandte
Sektorenübergreifende Qualitätssicherung im Gesundheitswesen nach 137a SGB V Weiterentwicklung des Leistungsbereiches Herztransplantation Indikatorenset 1.0 Stand: 15. März 2014 AQUA Institut für angewandte
HumanLib - Modellbildung des menschlichen Herz-Kreislauf-Systems
 HumanLib - Modellbildung des menschlichen Herz-Kreislauf-Systems Dymola & Modelica Informationstag 15. November 2007 Anja Brunberg IRT, RWTH Aachen Gliederung 1 Hintergrund Herz-Kreislauf-System Problemstellung
HumanLib - Modellbildung des menschlichen Herz-Kreislauf-Systems Dymola & Modelica Informationstag 15. November 2007 Anja Brunberg IRT, RWTH Aachen Gliederung 1 Hintergrund Herz-Kreislauf-System Problemstellung
Atriale und ventrikuläre Arrhythmie Wann an Ablation denken?
 Bayerischer Internisten Kongress 20.-21.Oktober 2018, München Atriale und ventrikuläre Arrhythmie Wann an Ablation denken? Christopher Reithmann Medizinische Klinik I Kardiologie und Intern. Intensivmedizin
Bayerischer Internisten Kongress 20.-21.Oktober 2018, München Atriale und ventrikuläre Arrhythmie Wann an Ablation denken? Christopher Reithmann Medizinische Klinik I Kardiologie und Intern. Intensivmedizin
Bei näherer Betrachtung des Diagramms Nr. 3 fällt folgendes auf:
 18 3 Ergebnisse In diesem Kapitel werden nun zunächst die Ergebnisse der Korrelationen dargelegt und anschließend die Bedingungen der Gruppenbildung sowie die Ergebnisse der weiteren Analysen. 3.1 Ergebnisse
18 3 Ergebnisse In diesem Kapitel werden nun zunächst die Ergebnisse der Korrelationen dargelegt und anschließend die Bedingungen der Gruppenbildung sowie die Ergebnisse der weiteren Analysen. 3.1 Ergebnisse
Die Lungenembolie in der Notfallaufnahme. Oana-Maria Driga
 Die Lungenembolie in der Notfallaufnahme Oana-Maria Driga Definition: partieller oder vollständiger Verschluss eines Lungenarterienastes durch einen verschleppten (Thromb)embolus in ca. 90% sind Becken-Bein-
Die Lungenembolie in der Notfallaufnahme Oana-Maria Driga Definition: partieller oder vollständiger Verschluss eines Lungenarterienastes durch einen verschleppten (Thromb)embolus in ca. 90% sind Becken-Bein-
Therapie der Herzinsuffizienz S. Achenbach, Medizinische Klinik 2, Universitätsklinikum Erlangen
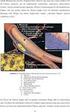 Therapie der Herzinsuffizienz 2013 S. Achenbach, Medizinische Klinik 2, Universitätsklinikum Erlangen Häufigkeit der Herzinsuffizienz 10-20% der 70-80 jährigen 15 Millionen Patienten in der EU Überleben
Therapie der Herzinsuffizienz 2013 S. Achenbach, Medizinische Klinik 2, Universitätsklinikum Erlangen Häufigkeit der Herzinsuffizienz 10-20% der 70-80 jährigen 15 Millionen Patienten in der EU Überleben
Diagnostik und Therapie Schlafbezogener Atmungsstörungen
 Diagnostik und Therapie Schlafbezogener Atmungsstörungen Cheyne-Stokes-Atmung und Herzinsuffizienz Ulrich Heidland Preventicum The Fat Boy in The Pickwick Papers (Charles Dickens, London, 1837) 1 Erstbeschreibung
Diagnostik und Therapie Schlafbezogener Atmungsstörungen Cheyne-Stokes-Atmung und Herzinsuffizienz Ulrich Heidland Preventicum The Fat Boy in The Pickwick Papers (Charles Dickens, London, 1837) 1 Erstbeschreibung
Herzklappe in Mitral- und Aortenposition
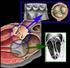 Minimalinvasive Behandlung: Edwards erhält Europäische Zulassung für Valve-in-Valve -Implantationen mit Sapien XT Herzklappe in Mitral- und Aortenposition IRVINE, CA, USA (5. Februar 2014) Edwards Lifesciences
Minimalinvasive Behandlung: Edwards erhält Europäische Zulassung für Valve-in-Valve -Implantationen mit Sapien XT Herzklappe in Mitral- und Aortenposition IRVINE, CA, USA (5. Februar 2014) Edwards Lifesciences
Jahresauswertung 2011 Implantierbare Defibrillatoren-Implantation 09/4. Sachsen Gesamt
 09/4 Sachsen Teilnehmende Krankenhäuser (Sachsen): 42 Anzahl Datensätze : 1.632 Datensatzversion: 09/4 2011 14.0 Datenbankstand: 29. Februar 2012 2011 - D11668-L76947-P36360 Eine Auswertung des BQS-Instituts
09/4 Sachsen Teilnehmende Krankenhäuser (Sachsen): 42 Anzahl Datensätze : 1.632 Datensatzversion: 09/4 2011 14.0 Datenbankstand: 29. Februar 2012 2011 - D11668-L76947-P36360 Eine Auswertung des BQS-Instituts
Tabelle 1: Altersverteilung der Patienten (n = 42) in Jahren
 3. Ergebnisse Die 42 Patienten (w= 16, m= 26) hatten ein Durchschnittsalter von 53,5 Jahren mit einem Minimum von und einem Maximum von 79 Jahren. Die 3 Patientengruppen zeigten hinsichtlich Alters- und
3. Ergebnisse Die 42 Patienten (w= 16, m= 26) hatten ein Durchschnittsalter von 53,5 Jahren mit einem Minimum von und einem Maximum von 79 Jahren. Die 3 Patientengruppen zeigten hinsichtlich Alters- und
Wie stelle ich eine Herzinsuffizienz fest. Ein Diagnostikvortrag
 Herzinsuffizienz fest Ein Diagnostikvortrag Die Vortragsordnung Definition Klinik Elektrokardiogramm Bildgebung Labor Invasive Funktionsuntersuchungen Definition Eine Herzinsuffizienz ist Folge einer verringerten
Herzinsuffizienz fest Ein Diagnostikvortrag Die Vortragsordnung Definition Klinik Elektrokardiogramm Bildgebung Labor Invasive Funktionsuntersuchungen Definition Eine Herzinsuffizienz ist Folge einer verringerten
Nosokomiale Infektionen bei neuen Verfahren in der Intensivmedizin. Teodor Bachleda Markus Plimon
 Nosokomiale Infektionen bei neuen Verfahren in der Intensivmedizin Teodor Bachleda Markus Plimon ECMO - extrakorporale Membranoxygenierung Veno-venöse ECMO (vv-ecmo) respiratorische Unterstützung (akutes
Nosokomiale Infektionen bei neuen Verfahren in der Intensivmedizin Teodor Bachleda Markus Plimon ECMO - extrakorporale Membranoxygenierung Veno-venöse ECMO (vv-ecmo) respiratorische Unterstützung (akutes
Aktuelles aus der Herztransplantation. Prof. Dr. med. Christof Schmid Herz, Thorax- u. herznahe Gefäßchirurgie Universitätsklinikum Regensburg
 Aktuelles aus der Herztransplantation Prof. Dr. med. Christof Schmid Herz, Thorax- u. herznahe Gefäßchirurgie Universitätsklinikum Regensburg Als Indikation für eine Herztransplantation wird das terminale
Aktuelles aus der Herztransplantation Prof. Dr. med. Christof Schmid Herz, Thorax- u. herznahe Gefäßchirurgie Universitätsklinikum Regensburg Als Indikation für eine Herztransplantation wird das terminale
Perioperative Hypertonie Was ist zu beachten?
 Perioperative Hypertonie Was ist zu beachten? FORTGESCHRITTENENKURS SAALFELDEN 2017 PD. OÄ. DR. SABINE PERL UNIVERSITÄTSKLINIK FÜR INNERE MEDIZIN GRAZ, ABTEILUNG FÜR KARDIOLOGIE Intraoperative Veränderungen
Perioperative Hypertonie Was ist zu beachten? FORTGESCHRITTENENKURS SAALFELDEN 2017 PD. OÄ. DR. SABINE PERL UNIVERSITÄTSKLINIK FÜR INNERE MEDIZIN GRAZ, ABTEILUNG FÜR KARDIOLOGIE Intraoperative Veränderungen
Dissertation Zur Erlangung des akademischen Grades Doktor der Medizin (Dr. med.)
 Aus dem Institut für Pharmakologie und Toxikologie an der Martin-Luther-Universität Halle-Wittenberg (kommissarischer Direktor: Prof. Dr. P. Presek) Einfluß einer β 1 -Blockade auf die Barorezeptorsensitivität
Aus dem Institut für Pharmakologie und Toxikologie an der Martin-Luther-Universität Halle-Wittenberg (kommissarischer Direktor: Prof. Dr. P. Presek) Einfluß einer β 1 -Blockade auf die Barorezeptorsensitivität
Dissertation zur Erlangung des akademischen Grades Doktor der Medizin (Dr. med.)
 Aus der Universitätsklinik und Poliklinik für Innere Medizin I an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. W. E. Fleig) und der Klinik für Innere Medizin der Kreiskrankenhaus
Aus der Universitätsklinik und Poliklinik für Innere Medizin I an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. W. E. Fleig) und der Klinik für Innere Medizin der Kreiskrankenhaus
Renale Anämie und kardiale Morbidität bei Niereninsuffizienz
 Renale Anämie und kardiale Morbidität bei Niereninsuffizienz Roland E. Winkler Rostock C 1 Diabetische Nephropathie und Mortalität Diabetiker mit Proteinurie haben eine 40fach höhere Mortalität als Patienten
Renale Anämie und kardiale Morbidität bei Niereninsuffizienz Roland E. Winkler Rostock C 1 Diabetische Nephropathie und Mortalität Diabetiker mit Proteinurie haben eine 40fach höhere Mortalität als Patienten
THERAPIE DER HERZINSUFFIZIENZ MICHAEL M. HIRSCHL LANDESKLINIKUM ZWETTL ABTEILUNG FÜR INNERE MEDIZIN
 THERAPIE DER HERZINSUFFIZIENZ MICHAEL M. HIRSCHL LANDESKLINIKUM ZWETTL ABTEILUNG FÜR INNERE MEDIZIN THERAPIE DER HERZINSUFFIZIENZ MEDIKAMENTÖSE THERAPIE ACE-HEMMER/ANGIOTENSIN-REZEPTOR-BLOCKER (I) BETABLOCKER
THERAPIE DER HERZINSUFFIZIENZ MICHAEL M. HIRSCHL LANDESKLINIKUM ZWETTL ABTEILUNG FÜR INNERE MEDIZIN THERAPIE DER HERZINSUFFIZIENZ MEDIKAMENTÖSE THERAPIE ACE-HEMMER/ANGIOTENSIN-REZEPTOR-BLOCKER (I) BETABLOCKER
Baden 04/2012 PD Dr. med. J-P Schmid 2
 Neue Erkenntnisse zum Ausdauertraining beim Herzpatienten PD Dr. med. Jean-Paul Schmid Bestimmung der Belastungsintensität Negatives Remodeling (Zunahme des Durch- messers des linken Ventrikels) Arrhythmien
Neue Erkenntnisse zum Ausdauertraining beim Herzpatienten PD Dr. med. Jean-Paul Schmid Bestimmung der Belastungsintensität Negatives Remodeling (Zunahme des Durch- messers des linken Ventrikels) Arrhythmien
Ich habe Vorhofflimmern! Was nun?
 Ich habe Vorhofflimmern! T. Meinertz Universitäres Herzzentrum Hamburg Klinik und Poliklinik für allgemeine und interventionelle Kardiologie Überblick I. Was ist Vorhofflimmern? II. Welche Prävalenz hat
Ich habe Vorhofflimmern! T. Meinertz Universitäres Herzzentrum Hamburg Klinik und Poliklinik für allgemeine und interventionelle Kardiologie Überblick I. Was ist Vorhofflimmern? II. Welche Prävalenz hat
