Versuch Nr. 9 Magnetische Suszeptibilität
|
|
|
- Philipp Althaus
- vor 6 Jahren
- Abrufe
Transkript
1 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: Ziel des Versuches Versuch Nr. Magnetische Suszeptibilität Bei diesem Versuch soll die Suszeptibilität von verschiedenen Komplexsalzen bestimmt werden. Durch Messungen an AgO/Ag O soll das Mischungsverhältnis von diesem bestimmt werden. Zusätzlich wird mittels der Suszeptibilität die Reinheit in Y O -Proben bestimmt werden.. Theorie.1 Suszeptibilität Wenn ein Körper in ein Magnetfeld eingebracht wird, welches die Flussdichte B hat, so können sich die Feldlinien im inneren des Körpers verdichten oder auseinander gedrängt werden. Das verdichten der Feldlinie im Körper nennt man Paramagnetismus,das auseinander drängen Diamagnetismus. Die Magnetisierung M ist proportional zur magnetischen Feldstärke H. Die Suszeptibilität χ m ist der Proportionalitätsfaktor. M = χ H m Da die magnetische Suszeptibilität χ m zwei verschiedene mathematische Vorzeichen haben kann, wird auch der Magnetismus in zwei verschiedene Arten unterteilt. 1. M ist H entgegengerichtet. Daraus folgt das χ m negativ ist und man spricht von Diamagnetismus.. M hat die gleiche Richtung wie H. Hier ist χ m positiv und man spricht von Paramagnetismus. Zusätzlich gibt es noch eine Gruppe von Stoffen die sich durch besonders große positive Werte der Suszeptibilität auszeichnet. Dies nennt man Ferromagnetismus.
2 µ = µ Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: In Analogie zur magnetischen Suszeptibilität kann man auch über die Proportionalität zwischen der magnetischen Flussdichte und der magnetischen Feldstärke auf das Verhalten von Stoffen im magnetischen Feld schließen. B = µ r H = µ H µ µ ist die magnetische Permeabilität und µ r die relative Permeabilität eines Stoffes. Bei diamagnetischen Stoffen ist µ r < 1 und χ m <. Bei paramagnetischen Stoffen ist µ r > 1 und χ m >. B = µ = µ ( M + H ) = µ ( H + χ H ) H ( 1+ χ ) = µ H m µ 1 7 = 4 π m kg s A ( χ m ) µ µ r µ = µ 1+. Diamagnetismus Magnetische Momente werden bei Stoffen durch Spin- und Bahndrehmomente der einzelnen Elektronen verursacht. Bei Diamagnetismus kompensieren sich die magnetischen Momente der Spins und der Drehimpulse. Wird ein so ein Stoff in ein magnetisches Feld gebracht, so kommt es zu einem induzierten Strom, an den ein Magnetfeld gekoppelt ist. Aufgrund der Lenz schen Regel ist dessen magnetisches Moment dem verursachenden Feld entgegengerichtet. Daraus folgt das diamagnetische Substanzen von Magnetfeldern abgestoßen werden. Da die mittleren Elektronenabstände von der Temperatur unabhängig sind, ist auch die diamagnetische Suszeptibilität temperaturunabhängig. Der Diamagnetismus ist um mehrere Größenordnungen schwächer als der Paramagnetismus. Diamagnetismus tritt bei allen Stoffen auf. χ = χ dia + χ para Diamagnetisch sind solche Stoffe, welche über eine gerade Anzahl von Elektronen verfügen. Diese sind jeweils mit antiparallelem Spin in den Orbitalen gepaart. Diamagnetische Stoffe werden von dem Magnetfeld der Gouy-Waage abgestoßen, wodurch sie leichter erscheinen.. Paramagnetismus Paramagnetismus tritt immer dann auf, wenn ungepaarte Elektronen vorhanden sind und sich die magnetischen Momente deshalb nicht aufheben. Er kann aber auch bei Stoffen mit einer geraden Anzahl an Elektronen aufgrund der Ligandenfeldaufspaltung auftreten. Hierbei wird zwischen low-spin und high-spin Komplexen unterschieden. Sind kein Anteile des Bahndrehimpulses am gesamten magnetischen Moment vorhanden, so ist die Größe des magnetischen Momentes gegeben durch die Spin-only-Formel. ( n + ) B m = n µ
3 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: e h µ 4π m n = Anzahl der ungepaarten Spins µ B = Bohrsche Magneton e = Elementarladung h = Plancksches Wirkungsquantum m e = Masse eines Elektrons 4 1 B = =,748 1 J T e Paramagnetismus nimmt mit T 1 ab, da die gleichmäßige Ausrichtung der Elektronen durch die Temperaturerhöhung erschwert wird. Die Temperaturabhängigkeit der paramagnetischen Suszeptibilität kann mit Curie-Gesetz C beschrieben χ para =. Da diese Temperaturabhängigkeit nur für Gase gilt, wo die Moleküle T weit genug voneinander entfernt sind, um miteinander in Wechselwirkung zu treten, muß die Gleichung ein kleinwenig geändert werden und man gelangt so zum Curie-Weiss-Gesetz. C χ para = T Θ µ N A C = µ m k µ = magnetische Feldkonstante N A = Avogadro-Konstante k = Boltzmann-Konstante Θ ist die Weisssche Konstante und ist für jeden Stoffcharakteristisch. Paramagnetische Stoffe werden bei der Gouy-Waage in das Magnetfeld hinein gezogen, wodurch sie schwerer erscheinen..4 Ligandenfeldtheorie Die Theorie der Ligandenfeldaufspaltung dient der Beschreibung der Wechselwirkungen in Komplexen. Bei Übergangsmetall-Ionen besitzen in isolierter Form alle fünf d-orbitale die gleiche Energie, sie sind entartet. Wenn man nun ein Übergangsmetall-Ion in einem Komplex mit sechs oktaedrisch angeordneten Liganden betrachtet, sind die Orbitale die in d x-y und d z liegen energetisch höher gelegen, da deren Elektronenwolken einer stärkeren Abstoßung unterliegen. Die d xy, d xz und d yz Orbitale unterliegen einer geringeren Abstoßung und sind energetisch günstiger. Das höhere Energieniveau wird als e g -Orbital bezeichnet und das tiefere Energieniveau bezeichnet man als t g -Orbital. Die Größe der Aufspaltung wird mit 1 Dq bezeichnet, wobei das tiefere Energieniveau um 4 Dq vom Grundzustand erniedrigt ist und das höhere Energieniveau um 6 Dq vom Grundzustand aus erhöht ist. Bei 1- Elektronen wird das t g -Orbital entsprechend der Hund schen Regel aufgefüllt. Bei dem vierten bis siebten Elektron wird beim auffüllen geschaut ob das höhere Orbital oder die Spinpaarungsenergie günstiger ist. Falls die Spinpaarungsenergie günstiger ist entsteht ein low-spin-komplex. Wenn es energetisch günstiger ist das höhere Orbital zu besetzen entsteht ein high-spin-komplex. Bei dem 8-1ten Elektron ist wieder nur noch eine Möglichkeit zur Besetzung der Orbitale möglich.
4 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: Funktionsweise der Gouy-Waage Bei diesem Versuch wurde eine Gouy-Waage benutzt, deren Prinzip leicht abgewandelt ist. Hier wird nicht die Kraft gemessen die ein Magnetfeld auf eine Probe ausübt, sondern die Kraft welche die Probe auf einen Magneten ausübt. Um diese Kraft zu messen ist der Magnet an einem Torisionsdraht aufgehängt. Die Auslenkung des Magneten wird mittels einer Magnetspule ausgeglichen. Der dafür benutzte Strom ist proportional zu der von der Probe ausgeübten Kraft und somit auch zu deren ausgeübten magnetischen Volumensuszeptibilität χ V. Zur Bestimmung der Massensuszeptibilität gilt: χ g l Luft ( C ( R R ) + 1 χ * A) = 1 m C = Kalibrierkonstante R = Messwert des Probenröhrchens mit Probe [cm -1 ] R = Messwert des leeren Röhrchens [cm -1 ] l = Füllhöhe des Röhrchens [cm] m = Probenmasse A = Innenquerschnitt des Probenröhrchens [cm ] χ V Luft = Volumensuszeptibilitat der verdrängten Luft V Luft Für pulverförmige Proben kann der Korrekturterm 1 χ V A in der Regel vernachlässigt werden. Laut der Versuchsvorschrift beträgt R = -6, cm -1 ± 1,1 cm -1.
5 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: Auswertung.1 Bestimmung der Kalibrierkonstanten C R 1 17 R 16 R 1 Mittelwert 17, Füllhöhe[cm],7±,1 Masse[g],46 Der Fehler der Masse wird mit angegeben, da wird den Werten welche auf den Schildchen stehen vertrauen müssen. Die Standardabweichung des Mittelwertes wird nach folgender formel berechnet: ( R Rmittel ) i σrmittel = n ( n 1) Daraus ergibt sich für den Mittelwert R = 17, cm -1 ±,88 cm -1 Die Suszeptibilität wird nach der Gleichung l ( C ( R R )) χ g = berechnet, wobei man die Kalibrierkonstante weg lässt, da sie ja erst 1 m ermittelt wird. Hier heraus ergibt sich für χ g = 14,5*1-6 g -1 ±,5*1-1 g -1 Der Fehler der Suszeptibilität ergibt sich nach der Gaußschen Fehlerfortpflanzung durch die Formel: ( R R ) l l χ = R R + + l 1 m 1 m 1 m Mit den hier ermittelten Werten, ergibt sich für die Kalibrierkonstante C = 1,1 ± 1,76*1 - C = 16,44 1 χ 6 1 g χ
6 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: Auswertung der Suszeptibilitäten verschiedener Salze Die gemessenen Suszeptibilitäten und die anderen Werte werden zur Vereinfachung in eine Tabelle eingetragen, und die Formeln zu deren Berechnung und der Berechnung deren Fehler werden im nachhinein aufgeführt. Salz R 1 [cm -1 ] R [cm -1 ] R [cm -1 ] Ni(NH ) 6 Cl 46 ± 1 46 ± 1 46 ± 1 K Cr O 7-6 ± 1-6 ± 1-6 ± 1 K Co(CN) 6-85 ± 1-85 ± 1-86 ± 1 NiCl 6H O 144 ± 148 ± 15 ± K 4 Fe(CN) 6 H O -88 ± 1-87 ± 1-87 ± 1 KMnO 4-4 ± 1-44 ± 1-44 ± 1 (NH 4 ) Fe(SO 4 ) 6H O 1571 ± 1576 ± 1575 ± K Fe(CN) 6 46 ± 1 46 ± 1 47 ± 1 Cu(Oac) H O 14 ± 1 14 ± 1 14 ± 1 Salz m[g] l[cm] R mittel [cm -1 ] χ[g -1 ] Ni(NH ) 6 Cl,56,7 ±,1 461, ±,666 1,677*1-5 ±,84 * 1-1 K Cr O 7,18, ±,1-6 ± 5,71*1-8 ± 7,86 * 1-16 K Co(CN) 6,1761,7 ±,1-85, ±, -5,11*1-7 ± 1,718 * 1-15 NiCl 6H O,151 1,8 ±,1 147 ± 1,764 1,86*1-5 ± 1, * 1-1 K 4 Fe(CN) 6 H O,167,6 ±,1-87, ±, -4,177*1-7 ± 1,85 * 1-15 KMnO 4,48, ±,1-4,6 ±,,5*1-7 ± 7,15 * 1-16 (NH 4 ) Fe(SO 4 ) 6H O,156,7 ±, ± 1,58 4,55*1-5 ± 1,54 * 1-1 K Fe(CN) 6,186,7 ±,1 46, ±, 6,8*1-6 ± 6,54 * 1-14 Cu(Oac) H O,1751, ±,1 14,6 ±, 4,64*1-6 ± 1,85 * 1-14 Die Standardabweichung der Mittelwerte wird nach der gleichen Formel aus 4.1 berechnet. Die Suszeptibilität wird ebenfalls nach der Formel aus 4.1 berechnet. Die Fehler der Suszeptibilität berechnet man durch Gaußsche Fehlerfortpflanzung durch die Gleichung: χ = l C 1 m R l C + 1 m R + ( R R ) l C ( R R ) 1 m C + 1 m l
7 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: In die nachfolgende Tabelle werden die gefundenen Literaturwerte, die molaren Massen und die in Grammsuszeptibilität umgerechneten Literaturwerte eingetragen. Dies lässt sich einfach umrechnen indem man einfach die Molsuszeptibilität durch die molare Masse teilt. Salz Literaturwert für χ in mol -1 Molare Masse in g * mol -1 Literaturwert umgerechnet in g -1 Ni(NH ) 6 Cl, ,4,44*1-5 K Cr O 7,4 1,78 1,68*1-7 K Co(CN) 6 -,1 7,61-5,61*1-7 NiCl 6H O,44,4 1,76*1-5 K 4 Fe(CN) 6 H O -,17 1,65-8,6*1-7 KMnO 4, 4,185 6,78*1-8 (NH 4 ) Fe(SO 4 ) 6H O,14 476,44,6*1-5 K Fe(CN) 6,,44 6,55*1-6 Cu(Oac) H O,87,1,1*1-6 Negative Suszeptibilitäten, und damit ein Diamagnetischer Stoff ist zum einen K Co(CN) 6 und zu anderen K 4 Fe(CN) 6 * H O. Dies stimmt genau mit der Ligandenfeldtheorie überein. Denn Cyanid als Ligand bewirkt eine große Aufspaltung des hier oktaedrischen Ligandenfelds und somit ist die Spinpaarung in den niedrig liegenden t g Orbitalen bevorzugt. Aufgrund der Elektronenkonfiguration im Eisen(II) und Cobalt(III) mit jeweils d 6 - Elektronen kommt es, dass die drei t g - Orbitale mit sechs Elektronen komplett gefühlt sind und der Stoff diamagnetisch ist. Wenn man das K Fe(CN) 6 betrachtet, ist auch hier von einem oktaedrischen low-spin Komplex auszugehen. Doch da dem Eisen(III) nur fünf Elektronen zur Verfügung stehen kann der t g - Zustand nicht komplett gefüllt werden und man bekommt ein ungepaartes Elektron. Der Stoff ist paramagnetisch. Eisen(II) und Eisen(III) kommen überwiegend als oktaedrische high-spin Komplexe vor außer, wie schon gesehen, bei Liganden mit großer Ligandenfeldaufspaltung. Deshalb gilt für das (NH 4 ) Fe(SO 4 ) * 6H O, dass wegen der kleinen Aufspaltung der Liganden die Elektronen nach der Hundt schen Regel auf die Orbitale des t g - und des e g - Zustands gleichmäßig verteilt werden. Dies hat zur folge, dass vier von sechs Elektronen ungepaart sind und so ein starker Paramagnetismus hevorgerufen wird. Ähnliches gilt für die beiden Nickel(II)- Verbindungen Ni(NH ) 6 Cl und NiCl * 6H O, bei denen das Nickel in einer d 8 - Konfiguration vorliegt. Die Elektronen werden auf alle Orbitale gleichmäßig verteilt und man bekommt zwei ungepaarte Elektronen, die das paramagnetische Moment hervorrufen. Entgegen der Erwartung liegen bei K Cr O 7 und KMnO 4, trotz der höchsten Oxidationsstufe kein Diamagnetismus vor. Beide weisen ein schwaches paramagnetisches Moment auf. Erklärbar ist dieses Verhalten, wenn man sich vor Augen führt, dass der gebundene Sauerstoff eine große Elektronendichte, und das Metall leere Orbitale besitzt. Es kommt zur Verschiebung der Elektronendichte vom Liganden zum Komplexzentrum. Diesen Vorgang nennt man charge-transfer und er bewirkt eine intensive Färbung. Beim Cu(OAc) * H O wurde ebenfalls ein Paramagnetismus gemessen, der aber hier aus der Elektronenzahl des Kupfers ergibt. Kupfer besitzt mit seiner 4s 1 d 1 elf Elektronen. Hier liegt Kupfer(II) vor. Folglich verfügt das Kupfer nur noch über neun Elektronen und ist somit zwangsweise paramagnetisch.
8 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: Bestimmung des Mischungsverhältnisses einer AgO/Ag O Mischung Es wurde das Suszeptibilität der im Praktikum ausliegenden Probe gemessen, und daraus das Mischungsverhältnis der Probe bestimmt. Die Suszeptibilität und die Fehler wurden genauso wie im vorherigen Versuchsteil berechnet. Salz R 1 [cm -1 ] R [cm -1 ] R [cm -1 ] AgO/Ag O -84 ± 1-85 ± 1-85 ± 1 Salz m[g] l[cm] R mittel [cm -1 ] χ[g -1 ] AgO/Ag O,5,7 ±,1-84,7 ±, -,5*1-7 ± 6,48 * 1-16 Die Literaturwerte und in Grammsuszeptibilität umgerechneten Literaturwerte betragen: Salz Suszeptibilität in mol -1 Molare Masse in g * mol -1 Suszeptibilität in g -1 Ag O -14*1-6 1,76-5,78*1-7 AgO -1,6*1-6 18,868-1,544*1-7 Bei der Berechnung der Suszeptibilität muß man einfach ein Gleichungssystem lösen. m χ = m( Ag O) * χ( Ag O) + m( AgO) χ( AgO) m = Masse der Probe m(ag O) = Masse an Ag O m(ago) = Masse an AgO χ = gemessene Suszeptibilität χ(ag O) = Literaturwert für Ag O χ(ago) = Literaturwert für AgO Dieses Gleichungssystem hat im Prinzip zwei Unbekannte, und zwar die Massen an Ag O und AgO. Da aber die beiden Massen addiert die Masse der Probe ergeben müssen kann man die eine Massen durch die Gesamtmasse subtrahiert der anderen Masse ersetzen. m( Ag O) = m m( AgO) wenn man diese Gleichung oben einsetzt und nach der Masse von AgO umstellt erhält man die Masse von AgO. ( χ χ( Ag O) ) m( AgO) = m ( χ( AgO) χ( Ag O) ) wenn man alle Werte einsetzt erhält man für die Masse an AgO: m(ago) =,157 g ±,6*1-1 g dadurch kann man auch die Masse an Ag O ausrechnen. m(ag O) =,8 g ±,6*1-1 g Der Fehler wurde wieder durch Gaußsche Fehlerfortpflanzung berechnet. Da nur χ mit einem Fehler behaftet ist ergibt sich die für den Fehler der Masse von AgO die einfache Formel: m m( AgO) = χ χ( AgO) χ( Ag O) Da man die Masse von Ag O durch Subtraktion von der Gesamtmasse erhält hat sie natürlich den selben Fehler. Dadurch ergibt sich ein Mischungsverhältnis von: m(ago) = 65,6%
9 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: m(ago) = 4,7% Man kann noch über die Molaren Massen eine Stoffmenge ausrechnen. n(ago) = 1,*1 - mol ±,8*1-1 g n(ag O) =,55*1-4 mol ± 1,56*1-1 g Die Fehler der Stoffmenge berechnen sich nach der Gleichung: m n = M n Fehler der Stoffmenge m Fehler der Masse Die Probenzusammensetzung ist also durch das Mischungsverhältnis n(ago):n(ag O) =,44 : 1 gegeben.
10 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: Bestimmung der Reinheit von Y O -Proben Die gemessenen Werte werden wieder zur besseren Übersicht in einer Tabelle eingetragen, und die Erklärungen später gegeben. Die einzelnen Messwerte werden diesmal weggelassen, und direkt die gemittelten Werte eingetragen. Die einzelnen Werte können bei Bedarf dem Messprotokoll entnommen werden. Probe Y O Masse [g] l[cm] R mittel [cm -1 ] χ[g -1 ] hochrein,15, ±,1-75 ± -1,76*1-6 ± 1,64*1-15 technisch,56, ±,1-7,67 ±, -7,1*1-7 ±,1*1-16 P,18,5 ±,1 -,67 ±, -5,*1-7 ± 1,1*1-16 P,145,4 ±,1-1, ±, -,45*1-7 ±,75*1-16 P4,6,8 ±,1-6 ±,577 -,44*1-7 ± 7,85*1-16 P5,15,7 ±,1,67 ±, 4,1*1-7 ±,8*1-16 P6,161,6 ±,1-56,67 ±, -8,5*1-7 ± 6,1*1-16 Die Berechnung der Mittelwerte, Standardabweichungen der Mittelwerte, Suszeptibilitäten und Fehler der Suszeptibilitäten erfolgt analog den anderen Aufgaben. In der Praktikumsvorschrift ist die magnetische Suszeptibilität des Präsodymiumsulfat mit -476 cm³ * mol -1 angegeben, dies kann nicht stimmen, da Präsodymiumsulfat paramagnetisch sein soll. Deshalb wird bei diesem Wert ein positives Vorzeichen genommen. Die Verunreinigung an Präsodymiumsulfat kann analog wie im vorangegangenen Aufgabenteil erledigt werden. m( Pr obe) χ( Pr obe) = m( YO ) χ( YO ) + m( Pr ( SO4 ) ) χ( Pr ( SO4 ) ) wenn man die Masse des Y O durch die Gesamtmasse minus der Masse von Präsodymiumsulfat ersetzt, und die Gleichung umstellt, erhält man direkt die Masse des Präsodymiumsulfat mit dem die Probe verunreinigt ist. ( ( ) ) ( ) ( χ( Pr obe) χ( YO )) m Pr SO4 = m Pr obe ( χ( Pr ( SO4 ) ) χ( YO )) Der Fehler der Masse an Präsodymiumsulfat berechnet sich nach der Gaußschen Fehlerfortpflanzung: m(pr ( SO ) ) = 4 ( χ( Pr ( SO ) ) χ( Y O )) ( χ( Pr ( SO ) ) χ( Y O )) ( χ( Pr ( SO ) ) χ( Y O )) m(pr obe) 4 χ (Pr obe) + m(pr obe) 4 + m(pr obe) ( χ (Pr obe) χ( Y O )) Die Ergebnisse werden in die Tabelle eingetragen, und die Verunreinigung an ( 4 ) Massenprozent der Gesamtmasse wiedergegeben. Verunreinigung[g] Fehler [g] Verunreinigung[%] Fehler [%] technisch 5,78E-6,171485,556 5, P,7655E-5,11761, ,64664 P,784E-5,1647, ,64415 P4,857E-5,11788, ,47587 P5 7,685E-5,14118,4155 6,45 P6 1,5614E-5,15414,7841 5, Die prozentuale Verunreinigung wurde errechnet durch die Gleichung: Pr SO /m(probe)*1 Verunreinigung = m ( 4 ) Für den Fehler der prozentualen Verunreinigung wurde statt der Masse an ( 4 ) Fehler der Masse Pr ( SO 4 ) eingesetzt. 4 Pr SO in Pr SO der χ ( Y O )
11 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: Messung der Suszeptibilität von KCl Für die Messung von KCl wurde erst mal eine neue Kalibrierkonstante bestimmt, da diesmal andere Rörchen benutzt wurden. Dazu war ein Röhrchen der selben Art mit einer Standardlösung gefüllt. Der Messwert ist so eingestellt das gilt R Standard R O = 1 Bei der Kalibrierung wurden erhalten für R:17, 145,15 Der Mittelwert beträgt hierbei R mittel = 15, ±,88 Die Standardabweichung des Mittelwertes wurde dabei wie in.1 bestimmt. Als Kalibrierkonstante erhält man: C = 1/[15,-(-)] C =,45 ±,1888 Nun haben wir ein leeres Probenröhrchen gemessen, und erhielten dabei einen R -Wert von 6,5 cm -1 ± 1 Danach wurde das Probenröhrchen gefüllt, die Füllhöhe bestimmt und die Masse der Probe gewogen. Die Probenmasse beträgt: m =,166g ±,g Die Füllhöhe betrug l =,1 cm ±,1 cm Für R erhielten wir:, 7, 6, 7 Den Fehler von R ist 1. Nun kann man die Suszeptibilität des Salzes berechnen: ( R R ) l C χ = 1 m χ = 1,18*1-6 Der Literaturwert beträgt 8,8*1-6 mol -1 also 5,4*1-7 g -1 Fehlerbetrachtung Fehler sind im Versuch dadurch zustande gekommen, das die Waage sehr stoßempfindlich ist, und der Versuch nebenan eine dauernd laufende Vakuumpumpe benötigt die gestört haben könnte. Zusätzlich können auch die Bewegungen der anderen Praktikumsteilnehmer störend auf den Versuch eingewirkt haben da jede Bewegung eine Schwankung auf der Waage verursacht hat. Weiterhin können Fehle durch die Füllhöhenmessung, zustande kommen, falls das Röhrchen nicht homogen gefüllt ist. Weitere Fehler sind z.b. wenn das Salz mit Luftsauerstoff, der ja eigentlich nicht vorhanden sein dürfte, da sie ja im Vakuum eingeschweißt sind, reagiert, wie es im Fall der Oxidation von KMnO 4 zu Braunstein anzutreffen ist, oder bei Versuchsteil 5 Fehler beim wiegen der Masse, oder unreines KCl.
Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment
 1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
Fortgeschrittenenpraktikum. Physikalische Chemie. Versuch B3. Magnetische Suszeptibilität
 Fortgeschrittenenpraktikum Physikalische Chemie Wintersemester 1998/99 Versuch B3 Magnetische Suszeptibilität Durchgeführt von: Assistent: 1. Abgabe: 23.04.1999 2. Abgabe: 10.05.1999 3. Abgabe: 18.05.1999
Fortgeschrittenenpraktikum Physikalische Chemie Wintersemester 1998/99 Versuch B3 Magnetische Suszeptibilität Durchgeführt von: Assistent: 1. Abgabe: 23.04.1999 2. Abgabe: 10.05.1999 3. Abgabe: 18.05.1999
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Materie im Magnetfeld
 . Stromschleifen - Permanentmagnet Materie im Magnetfeld EX-II SS007 = > µmag = I S ˆn S = a b µ bahn = e m L µ spin = e m S Stromschleife im Magnetfeld Magnetisierung inhomogenes Magnetfeld = D = µmag
. Stromschleifen - Permanentmagnet Materie im Magnetfeld EX-II SS007 = > µmag = I S ˆn S = a b µ bahn = e m L µ spin = e m S Stromschleife im Magnetfeld Magnetisierung inhomogenes Magnetfeld = D = µmag
Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4]
![Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4]](/thumbs/72/67239082.jpg) Versuch M3: Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] Es sollen 3 g Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] (wasserfrei) nach beiliegender Vorschrift dargestellt
Versuch M3: Darstellung von Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] Es sollen 3 g Kobalt(II)-tetrathiocyanatomercurat(II) Co[Hg(SCN)4] (wasserfrei) nach beiliegender Vorschrift dargestellt
Anorganische Chemie II
 Anorganische Chemie II Magnetismus Skript zur Vorlesung Magnetismus Mai 2007 Dieses Skript soll einen kurzen Überblick über Magnetismus und magnetische Phänome geben. Es ist als Ergänzung zum Skript zur
Anorganische Chemie II Magnetismus Skript zur Vorlesung Magnetismus Mai 2007 Dieses Skript soll einen kurzen Überblick über Magnetismus und magnetische Phänome geben. Es ist als Ergänzung zum Skript zur
Magnetismus der Materie. Bernd Fercher David Schweiger
 Magnetismus der Materie Bernd Fercher David Schweiger Einleitung Erste Beobachtunge in China und Kleinasien Um 1100 Navigation von Schiffen Magnetismus wird durch Magnetfeld beschrieben dieses wird durch
Magnetismus der Materie Bernd Fercher David Schweiger Einleitung Erste Beobachtunge in China und Kleinasien Um 1100 Navigation von Schiffen Magnetismus wird durch Magnetfeld beschrieben dieses wird durch
Magnetochemie. Lehrbücher:H. Lueken, Magnetochemie, Teubner Studienbücher, R. L. Carlin, Magnetochemistry, Springer-Verlag, 1986.
 Magnetochemie Lehrbücher:H. Lueken, Magnetochemie, Teubner Studienbücher, 2000 R. L. Carlin, Magnetochemistry, Springer-Verlag, 1986. Grundbegriffe des Magnetismus Magnetische Flußdichte Magnetisierung
Magnetochemie Lehrbücher:H. Lueken, Magnetochemie, Teubner Studienbücher, 2000 R. L. Carlin, Magnetochemistry, Springer-Verlag, 1986. Grundbegriffe des Magnetismus Magnetische Flußdichte Magnetisierung
Praktikum Instrumentelle Analytik
 Praktikum Instrumentelle Analytik Sommersemester 2004 Protokoll zum Teil Magnetochemie Gruppe 1 Jasmin Fischer 1 1.1 Kurze Zusammenfassung der theoretischen Grundlagen für den Versuch Grundlage dieser
Praktikum Instrumentelle Analytik Sommersemester 2004 Protokoll zum Teil Magnetochemie Gruppe 1 Jasmin Fischer 1 1.1 Kurze Zusammenfassung der theoretischen Grundlagen für den Versuch Grundlage dieser
Darstellung von Cobaltammoniumphosphat Monohydrat (CoNH 4 PO 4 H 2 O)
 Versuch M4: Darstellung von Cobaltammoniumphosphat Monohydrat (CoNH 4 PO 4 H 2 O) Cobaltammoniumphosphat Monohydrat soll nach folgender Vorschrift dargestellt werden. Die Phasenreinheit des Präparats wird
Versuch M4: Darstellung von Cobaltammoniumphosphat Monohydrat (CoNH 4 PO 4 H 2 O) Cobaltammoniumphosphat Monohydrat soll nach folgender Vorschrift dargestellt werden. Die Phasenreinheit des Präparats wird
Suszeptibilitätsmessungen mit der Gouy-Waage 1. Theorie 2. Versuchsdurchführung:
 Protokoll zum Versuch Suszeptibilitätsmessungen mit der Gouy-Waage Betreuerin: Kirsten Feddern 1. Theorie Materie, die einem magnetischen Feld ausgesetzt ist, zeigt verschiedene Effekte. Einige davon sind
Protokoll zum Versuch Suszeptibilitätsmessungen mit der Gouy-Waage Betreuerin: Kirsten Feddern 1. Theorie Materie, die einem magnetischen Feld ausgesetzt ist, zeigt verschiedene Effekte. Einige davon sind
Magnetismus. Prof. DI Michael Steiner
 Magnetismus Prof. DI Michael Steiner www.htl1-klagenfurt.at Magnetismus Natürlicher Künstlicher Magneteisenstein Magnetit Permanentmagnete Stabmagnet Ringmagnet Hufeisenmagnet Magnetnadel Temporäre Magnete
Magnetismus Prof. DI Michael Steiner www.htl1-klagenfurt.at Magnetismus Natürlicher Künstlicher Magneteisenstein Magnetit Permanentmagnete Stabmagnet Ringmagnet Hufeisenmagnet Magnetnadel Temporäre Magnete
PD Para- und Diamagnetismus
 PD Para- und Diamagnetismus Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Magnetfeld in Materie............................ 2 1.2 Arten von Magnetismus...........................
PD Para- und Diamagnetismus Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Magnetfeld in Materie............................ 2 1.2 Arten von Magnetismus...........................
PN 2 Einführung in die Experimentalphysik für Chemiker
 PN 2 Einführung in die Experimentalphysik für Chemiker 4. Vorlesung 9.5.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 2 Einführung in die Experimentalphysik für Chemiker 4. Vorlesung 9.5.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
15.Magnetostatik, 16. Induktionsgesetz
 Ablenkung von Teilchenstrahlen im Magnetfeld (Zyklotron u.a.): -> im Magnetfeld B werden geladene Teilchen auf einer Kreisbahn abgelenkt, wenn B senkrecht zu Geschwindigkeit v Kräftegleichgewicht: 2 v
Ablenkung von Teilchenstrahlen im Magnetfeld (Zyklotron u.a.): -> im Magnetfeld B werden geladene Teilchen auf einer Kreisbahn abgelenkt, wenn B senkrecht zu Geschwindigkeit v Kräftegleichgewicht: 2 v
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel )
 EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
Komplexchemie des Nickels Ligandenaustauschreaktionen
 Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
Theta (deg.)
 NaCl, MoKα, λ = 0.7107 Å Intensity (a.u.) 40000 31400 22800 14200 5600-3000 10 20 30 40 50 60 70 80 2 Theta (deg.) Atomare und molekulare Bewegung in Kristallen Temperaturbewegung erniedrigt die Auflösung
NaCl, MoKα, λ = 0.7107 Å Intensity (a.u.) 40000 31400 22800 14200 5600-3000 10 20 30 40 50 60 70 80 2 Theta (deg.) Atomare und molekulare Bewegung in Kristallen Temperaturbewegung erniedrigt die Auflösung
Heute: Magnetismus. Mathematisch-Naturwissenschaftliche Fakultät. Abteilung Anorganische Festkörperchemie. Prof. Dr. Martin Köckerling.
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Festkörperchemie Vorlesung Anorganische Chemie VI Materialdesign Heute: Magnetismus 1 Gliederung Magnetismus Elektromagnetismus
Mathematisch-Naturwissenschaftliche Fakultät Institut für Chemie Abteilung Anorganische Festkörperchemie Vorlesung Anorganische Chemie VI Materialdesign Heute: Magnetismus 1 Gliederung Magnetismus Elektromagnetismus
Elektrizitätslehre und Magnetismus
 Elektrizitätslehre und Magnetismus Othmar Marti 30. 06. 2008 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Klassische und Relativistische Mechanik 30. 06.
Elektrizitätslehre und Magnetismus Othmar Marti 30. 06. 2008 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Physik Klassische und Relativistische Mechanik 30. 06.
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 07. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 07. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
3.5. Materie im Magnetfeld. Exp. 36: Dipol im Magnetfeld. Exp. 25b Magnetisierung eines Stahldrahtes Magnetisches Moment
 - 205-3.5. Materie im Magnetfeld 3.5.1. Magnetisches Moment Wie wir bei der Diskussion der stromdurchflossenen Leiterschleife gesehen hatten erzeugen elektrische Kreisströme magnetische Dipolmomente Exp.
- 205-3.5. Materie im Magnetfeld 3.5.1. Magnetisches Moment Wie wir bei der Diskussion der stromdurchflossenen Leiterschleife gesehen hatten erzeugen elektrische Kreisströme magnetische Dipolmomente Exp.
Das magnetische Feld
 Das Magnetfeld wird durch Objekte erzeugt und wirkt gleichzeitig auf Objekte repräsentiert die Kraftwirkung aufgrund des physikalischen Phänomens Magnetismus ist gerichtet und wirkt vom Nordpol zum Südpol
Das Magnetfeld wird durch Objekte erzeugt und wirkt gleichzeitig auf Objekte repräsentiert die Kraftwirkung aufgrund des physikalischen Phänomens Magnetismus ist gerichtet und wirkt vom Nordpol zum Südpol
Versuch E11 - Hysterese Aufnahme einer Neukurve. Abgabedatum: 24. April 2007
 Versuch E11 - Hysterese Aufnahme einer Neukurve Sven E Tobias F Abgabedatum: 24. April 2007 Inhaltsverzeichnis 1 Ziel des Versuchs 3 2 Physikalischer Zusammenhang 3 2.1 Magnetisches Feld..........................
Versuch E11 - Hysterese Aufnahme einer Neukurve Sven E Tobias F Abgabedatum: 24. April 2007 Inhaltsverzeichnis 1 Ziel des Versuchs 3 2 Physikalischer Zusammenhang 3 2.1 Magnetisches Feld..........................
Ligandenfeldtheorie Magnetismus von Komplexen
 Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
Magnetisierung der Materie
 Magnetisierung der Materie Das magnetische Verhalten unterschiedlicher Materialien kann auf mikroskopische Eigenschaften zurückgeführt werden. Magnetisches Dipolmoment hängt von Symmetrie der Atome und
Magnetisierung der Materie Das magnetische Verhalten unterschiedlicher Materialien kann auf mikroskopische Eigenschaften zurückgeführt werden. Magnetisches Dipolmoment hängt von Symmetrie der Atome und
AC II Praktikum SoSe 04
 AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
Versuch 15 Dia- und Paramagnetismus
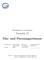 Physikalisches A-Praktikum Versuch 15 Dia- und Paramagnetismus Praktikanten: Gruppe: Julius Strake Niklas Bölter B006 Betreuer: Johannes Schmidt Durchgeführt: 07.09.2012 Unterschrift: E-Mail: niklas.boelter@stud.uni-goettingen.de
Physikalisches A-Praktikum Versuch 15 Dia- und Paramagnetismus Praktikanten: Gruppe: Julius Strake Niklas Bölter B006 Betreuer: Johannes Schmidt Durchgeführt: 07.09.2012 Unterschrift: E-Mail: niklas.boelter@stud.uni-goettingen.de
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Punkte. Bitte eintragen: Matrikelnummer: Bitte ankreuzen: Biotechnologie Pharmazie
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Demonstration der "Elektronenreibung" in Metallen
 Stromdurchflossene Leiter im Magnetfeld Barlowsches Rad: Demonstration der "Elektronenreibung" in Metallen Anlegen einer Spannung zwischen Achse und Quecksilberwanne führt zu einem Strom durch die Scheibe
Stromdurchflossene Leiter im Magnetfeld Barlowsches Rad: Demonstration der "Elektronenreibung" in Metallen Anlegen einer Spannung zwischen Achse und Quecksilberwanne führt zu einem Strom durch die Scheibe
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 24. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie II B. Sc. Chemieingenieurwesen 24. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
erzeugen elektrische Kreisströme magnetische Dipolmomente
 Prof. Dieter Suter Physik A3 WS 02 / 03 3.6 Materie im Magnetfeld 3.6.1 Magnetisches Moment Wie wir bei der Diskussion der stromdurchflossenen Leiterschleife gesehen hatten erzeugen elektrische Kreisströme
Prof. Dieter Suter Physik A3 WS 02 / 03 3.6 Materie im Magnetfeld 3.6.1 Magnetisches Moment Wie wir bei der Diskussion der stromdurchflossenen Leiterschleife gesehen hatten erzeugen elektrische Kreisströme
Physik 4 Praktikum Auswertung Hall-Effekt
 Physik 4 Praktikum Auswertung Hall-Effekt Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Elektrischer Strom in Halbleitern..... 2 2.2. Hall-Effekt......... 3 3. Durchführung.........
Physik 4 Praktikum Auswertung Hall-Effekt Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Elektrischer Strom in Halbleitern..... 2 2.2. Hall-Effekt......... 3 3. Durchführung.........
E19 Magnetische Suszeptibilität
 Aufgabenstellung: 1. Untersuchen Sie die räumliche Verteilung des Magnetfeldes eines Elektromagneten und dessen Abhängigkeit vom Spulenstrom. 2. Bestimmen Sie die magnetische Suszeptibilität vorgegebener
Aufgabenstellung: 1. Untersuchen Sie die räumliche Verteilung des Magnetfeldes eines Elektromagneten und dessen Abhängigkeit vom Spulenstrom. 2. Bestimmen Sie die magnetische Suszeptibilität vorgegebener
Elektrische und magnetische Materialeigenschaften
 Die elektrischen Eigenschaften von Dielektrika und Paraelektrika sind keine speziellen Eigenschaften fester oder kristalliner Substanzen. So sind diese Eigenschaften z.b. auch in Molekülen und Flüssigkeiten
Die elektrischen Eigenschaften von Dielektrika und Paraelektrika sind keine speziellen Eigenschaften fester oder kristalliner Substanzen. So sind diese Eigenschaften z.b. auch in Molekülen und Flüssigkeiten
Magnetische Suszeptibilität: Magnetismusarten
 agnetische Suszeptibilität, agnetismusarten agnetische Suszeptibilität: Im allgemeinen ist H: = χ m H χ m = magnetische Suszeptibilität [χ m ] = 1 Damit wird: at = µ 0 ( H + ) = µ 0 (1 + χ m ) }{{} =µ
agnetische Suszeptibilität, agnetismusarten agnetische Suszeptibilität: Im allgemeinen ist H: = χ m H χ m = magnetische Suszeptibilität [χ m ] = 1 Damit wird: at = µ 0 ( H + ) = µ 0 (1 + χ m ) }{{} =µ
Magnetisches Feld. Grunderscheinungen Magnetismus - Dauermagnete
 Magnetisches Feld Grunderscheinungen Magnetismus - Dauermagnete jeder drehbar gelagerte Magnet richtet sich in Nord-Süd-Richtung aus; Pol nach Norden heißt Nordpol jeder Magnet hat Nord- und Südpol; untrennbar
Magnetisches Feld Grunderscheinungen Magnetismus - Dauermagnete jeder drehbar gelagerte Magnet richtet sich in Nord-Süd-Richtung aus; Pol nach Norden heißt Nordpol jeder Magnet hat Nord- und Südpol; untrennbar
Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO 2-4 PO 3-4 +H + -H+ +H + Stefan Wuttke # 1
 Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO - 4 HPO 2-4 PO 3-4 +H + -H+ +H + -H+ +H + Stefan Wuttke # 1 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner + AgNO 3 AgCl +
Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO - 4 HPO 2-4 PO 3-4 +H + -H+ +H + -H+ +H + Stefan Wuttke # 1 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner + AgNO 3 AgCl +
LK Lorentzkraft. Inhaltsverzeichnis. Moritz Stoll, Marcel Schmittfull (Gruppe 2) 25. April Einführung 2
 LK Lorentzkraft Blockpraktikum Frühjahr 2007 (Gruppe 2) 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Magnetfeld dünner Leiter und Spulen......... 2 2.2 Lorentzkraft........................
LK Lorentzkraft Blockpraktikum Frühjahr 2007 (Gruppe 2) 25. April 2007 Inhaltsverzeichnis 1 Einführung 2 2 Theoretische Grundlagen 2 2.1 Magnetfeld dünner Leiter und Spulen......... 2 2.2 Lorentzkraft........................
F-Praktikum Physik: Widerstand bei tiefen Temperaturen
 F-Praktikum Physik: Widerstand bei tiefen Temperaturen David Riemenschneider & Felix Spanier 11. Januar 2001 1 Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Grüneisen-Theorie...............................
F-Praktikum Physik: Widerstand bei tiefen Temperaturen David Riemenschneider & Felix Spanier 11. Januar 2001 1 Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Grüneisen-Theorie...............................
Spezifische Wärme fester Körper
 1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
Magnetische Momente (Gouysche Waage)
 Stand: 7/3 III.5.1 Magnetische Momente (Gouysche Waage) Ziel des Versuches Der Versuch dient dem ennenlernen der Grundbegriffe des magnetischen Feldes (Feldstärke, magnetische Induktion, Suszeptibilität,
Stand: 7/3 III.5.1 Magnetische Momente (Gouysche Waage) Ziel des Versuches Der Versuch dient dem ennenlernen der Grundbegriffe des magnetischen Feldes (Feldstärke, magnetische Induktion, Suszeptibilität,
Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Sommer 2014 Vorlesung 4 Thema: Elektromagnetische Schwingungen, elektromagnetische Wellen und Spezielle Relativitätstheorie Technische Universität München 1 Fakultät für
Ferienkurs Experimentalphysik 2 Sommer 2014 Vorlesung 4 Thema: Elektromagnetische Schwingungen, elektromagnetische Wellen und Spezielle Relativitätstheorie Technische Universität München 1 Fakultät für
FT-Seminar der CSG e.v.
 F-Seminar der CSG e.v. Magnetische Messungen am SQUID-Magnetometer Peter homa 4.4.2 Stephan Schlamp F-Seminar der CSG e.v. Gerätevorstellung und Probenpräparation Peter homa 4.4.2 Schematische Gegenüberstellung
F-Seminar der CSG e.v. Magnetische Messungen am SQUID-Magnetometer Peter homa 4.4.2 Stephan Schlamp F-Seminar der CSG e.v. Gerätevorstellung und Probenpräparation Peter homa 4.4.2 Schematische Gegenüberstellung
4.7 Magnetfelder von Strömen Magnetfeld eines geraden Leiters
 4.7 Magnetfelder von Strömen Aus den vorherigen Kapiteln ist bekannt, dass auf stromdurchflossene Leiter im Magnetfeld eine Kraft wirkt. Die betrachteten magnetischen Felder waren bisher homogene Felder
4.7 Magnetfelder von Strömen Aus den vorherigen Kapiteln ist bekannt, dass auf stromdurchflossene Leiter im Magnetfeld eine Kraft wirkt. Die betrachteten magnetischen Felder waren bisher homogene Felder
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Magnetische Eigenschaften von Materie
 Magnetische Eigenschaften von Materie Abb. 1: Magnetisches Fluid im Feld eines starken, kugelförmigen Magneten zieht sich zu symmetrischen Mustern zusammen Geräteliste: Gasverflüssiger, Sauerstoff, Dewar
Magnetische Eigenschaften von Materie Abb. 1: Magnetisches Fluid im Feld eines starken, kugelförmigen Magneten zieht sich zu symmetrischen Mustern zusammen Geräteliste: Gasverflüssiger, Sauerstoff, Dewar
Magnetische Pigmente. Jonas Berg & Michael Luksin
 Magnetische Pigmente Jonas Berg & Michael Luksin Inhaltsverzeichnis Pigmente Magnetismus Was für Magnetismen gibt es? Welche Bedingungen müssen magnetische Pigmente erfüllen? Magnetische Pigmente Magnetit
Magnetische Pigmente Jonas Berg & Michael Luksin Inhaltsverzeichnis Pigmente Magnetismus Was für Magnetismen gibt es? Welche Bedingungen müssen magnetische Pigmente erfüllen? Magnetische Pigmente Magnetit
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen
 Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Magnetochemie. Eine Einführung in Theorie und Anwendung. Von Prof. Dr. rer. nat. Heiko Lueken Rheinisch-Westfälische Technische Hochschule Aachen
 Magnetochemie Eine Einführung in Theorie und Anwendung Von Prof. Dr. rer. nat. Heiko Lueken Rheinisch-Westfälische Technische Hochschule Aachen B. G.Teubner Stuttgart Leipzig 1999 Inhalt s Verzeichnis
Magnetochemie Eine Einführung in Theorie und Anwendung Von Prof. Dr. rer. nat. Heiko Lueken Rheinisch-Westfälische Technische Hochschule Aachen B. G.Teubner Stuttgart Leipzig 1999 Inhalt s Verzeichnis
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 11. Vorlesung, 4.7. 2013 Para-, Dia- und Ferromagnetismus Isingmodell, Curietemperatur,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 11. Vorlesung, 4.7. 2013 Para-, Dia- und Ferromagnetismus Isingmodell, Curietemperatur,
3.7 Das magnetische Feld in Materie
 15 KAPITEL 3. MAGNETOSTATIK 3.7 Das magnetische Feld in Materie Wie wir in den vorangegangenen Kapiteln bereits gesehen haben, wird die magnetische Induktionsdichte B durch ein Vektorpotenzial A charakterisiert,
15 KAPITEL 3. MAGNETOSTATIK 3.7 Das magnetische Feld in Materie Wie wir in den vorangegangenen Kapiteln bereits gesehen haben, wird die magnetische Induktionsdichte B durch ein Vektorpotenzial A charakterisiert,
316 - Magnetfeldmessungen
 316 - Magnetfeldmessungen 1. Aufgaben 1.1 Die magnetische Induktion B eines Elektromagneten auf der Polschuhachse ist mit einer Hall- Sonde in Abhängigkeit vom Magnetisierungsstrom für unterschiedliche
316 - Magnetfeldmessungen 1. Aufgaben 1.1 Die magnetische Induktion B eines Elektromagneten auf der Polschuhachse ist mit einer Hall- Sonde in Abhängigkeit vom Magnetisierungsstrom für unterschiedliche
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Musterlösung. Bitte eintragen: Matrikelnummer: 0815 Name: Musterstudi.
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen?
 Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen? Michael Kalcher 7AM In h a l t Eisen - Eigenschaften 2 Wertigkeit und Oxidationszahl 2 Üb e r g a n g s m e ta l l e 3
Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen? Michael Kalcher 7AM In h a l t Eisen - Eigenschaften 2 Wertigkeit und Oxidationszahl 2 Üb e r g a n g s m e ta l l e 3
2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment
 Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Ferromagnetismus: Heisenberg-Modell
 Ferromagnetismus: Heisenberg-Modell magnetische Elektronen nehmen nicht an der chemischen Bindung teil lokalisierte Beschreibung (4f und 5f Systeme seltene Erden) 4f-Ferromagnete nahe am atomaren Wert!
Ferromagnetismus: Heisenberg-Modell magnetische Elektronen nehmen nicht an der chemischen Bindung teil lokalisierte Beschreibung (4f und 5f Systeme seltene Erden) 4f-Ferromagnete nahe am atomaren Wert!
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
2 Elektrostatik. 2.1 Coulomb-Kraft und elektrische Ladung. 2.1 Coulomb-Kraft und elektrische Ladung
 2.1 Coulomb-Kraft und elektrische Ladung 2 Elektrostatik 2.1 Coulomb-Kraft und elektrische Ladung Abb. 2.1 Durch Reiben verschiedener Stoffe aneinander verbleiben Elektronen der Atomhüllen überwiegend
2.1 Coulomb-Kraft und elektrische Ladung 2 Elektrostatik 2.1 Coulomb-Kraft und elektrische Ladung Abb. 2.1 Durch Reiben verschiedener Stoffe aneinander verbleiben Elektronen der Atomhüllen überwiegend
Systematisierung Felder und Bewegung von Ladungsträgern in Feldern
 Systematisierung Felder und Bewegung von Ladungsträgern in Feldern Systematisierung Feld Unterschiede: Beschreibung Ursache Kräfte auf elektrisches Feld Das elektrische Feld ist der besondere Zustand des
Systematisierung Felder und Bewegung von Ladungsträgern in Feldern Systematisierung Feld Unterschiede: Beschreibung Ursache Kräfte auf elektrisches Feld Das elektrische Feld ist der besondere Zustand des
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ
 Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Anorganische Chemie II Veröffentlichung vom 26. Juni Valende Bond Theorie Grundlagen Mängel des Modells...
 Anorganische Chemie II Veröffentlichung vom 26. Juni 2005 Inhaltsverzeichnis 1 Valende Bond Theorie 2 1.1 Grundlagen............................................. 2 1.2 Mängel des Modells.........................................
Anorganische Chemie II Veröffentlichung vom 26. Juni 2005 Inhaltsverzeichnis 1 Valende Bond Theorie 2 1.1 Grundlagen............................................. 2 1.2 Mängel des Modells.........................................
Physikalische Chemie Praktikum. Elektrolyte: Dissoziationskonstante von Essigsäure λ von NaCl ist zu ermitteln
 Hochschule Emden/Leer Physikalische Chemie Praktikum Vers. Nr. 16 April 2017 Elektrolyte: Dissoziationskonstante von Essigsäure λ von NaCl ist zu ermitteln In diesem Versuch soll die Dissoziationskonstante
Hochschule Emden/Leer Physikalische Chemie Praktikum Vers. Nr. 16 April 2017 Elektrolyte: Dissoziationskonstante von Essigsäure λ von NaCl ist zu ermitteln In diesem Versuch soll die Dissoziationskonstante
Physikalische Übungen für Pharmazeuten
 Helmholtz-Institut für Strahlen- und Kernphysik Seminar Physikalische Übungen für Pharmazeuten Ch. Wendel Max Becker Karsten Koop Dr. Christoph Wendel Übersicht Inhalt des Seminars Praktikum - Vorbereitung
Helmholtz-Institut für Strahlen- und Kernphysik Seminar Physikalische Übungen für Pharmazeuten Ch. Wendel Max Becker Karsten Koop Dr. Christoph Wendel Übersicht Inhalt des Seminars Praktikum - Vorbereitung
Messung der Hystereseschleife (HYS)
 Messung der Hystereseschleife (HYS) Seite 1 Messung der Hystereseschleife (HYS) 1. Stichworte Magnetfeld und magnetische Flußdichte Dia-, Para- und Ferromagnetismus Hysterese, Remanenz und Koerzitivkraft
Messung der Hystereseschleife (HYS) Seite 1 Messung der Hystereseschleife (HYS) 1. Stichworte Magnetfeld und magnetische Flußdichte Dia-, Para- und Ferromagnetismus Hysterese, Remanenz und Koerzitivkraft
Magnetismus. Referat zu Theoretische Physik für das Lehramt 2, WS 2013/2014
 Magnetismus Andreas Wiederin David Gröbner Referat zu Theoretische Physik für das Lehramt 2, WS 2013/2014 Vorbemerkungen Ein grundlegendes (klassisches) Verständnis des Magnetismus, wie in den Lehrveranstaltungen
Magnetismus Andreas Wiederin David Gröbner Referat zu Theoretische Physik für das Lehramt 2, WS 2013/2014 Vorbemerkungen Ein grundlegendes (klassisches) Verständnis des Magnetismus, wie in den Lehrveranstaltungen
Praktikum I PP Physikalisches Pendel
 Praktikum I PP Physikalisches Pendel Hanno Rein Betreuer: Heiko Eitel 16. November 2003 1 Ziel der Versuchsreihe In der Physik lassen sich viele Vorgänge mit Hilfe von Schwingungen beschreiben. Die klassische
Praktikum I PP Physikalisches Pendel Hanno Rein Betreuer: Heiko Eitel 16. November 2003 1 Ziel der Versuchsreihe In der Physik lassen sich viele Vorgänge mit Hilfe von Schwingungen beschreiben. Die klassische
Übungsaufgaben zur Koordinationschemie
 Übungsaufgaben zur Koordinationschemie 1. Wie entstehen Komplexe und wie sind sie zusammengesetzt? Warum bilden die Nebengruppenelemente besonders stabile Koordinationsverbindungen? 2. Formulieren Sie
Übungsaufgaben zur Koordinationschemie 1. Wie entstehen Komplexe und wie sind sie zusammengesetzt? Warum bilden die Nebengruppenelemente besonders stabile Koordinationsverbindungen? 2. Formulieren Sie
Versuch 17: Kennlinie der Vakuum-Diode
 Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
Versuch 17: Kennlinie der Vakuum-Diode Inhaltsverzeichnis 1 Einleitung 3 2 Theorie 3 2.1 Prinzip der Vakuumdiode.......................... 3 2.2 Anlaufstrom.................................. 3 2.3 Raumladungsgebiet..............................
Experimentelle Bestimmung der magnetischen Flussdichte
 Experimentelle Bestimmung der magnetischen Flussdichte Vorversuch: Um die magnetische Flussdichte zu bestimmen führen wir einen Vorversuch durch um die Kräftewirkung im magnetischen Feld zu testen. B F
Experimentelle Bestimmung der magnetischen Flussdichte Vorversuch: Um die magnetische Flussdichte zu bestimmen führen wir einen Vorversuch durch um die Kräftewirkung im magnetischen Feld zu testen. B F
An welche Stichwörter von der letzten Vorlesung
 An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Der magnetische Fluss durch eine Schleife: da Φ = Das faradaysche Induktionsgesetz: Die Induktivität: l A L = NF i Die Spannung
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Der magnetische Fluss durch eine Schleife: da Φ = Das faradaysche Induktionsgesetz: Die Induktivität: l A L = NF i Die Spannung
Elektronenspinresonanz-Spektroskopie
 Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
Versuch 17. Ferromagnetismus. Wintersemester 2005 / Daniel Scholz.
 Physikalisches Praktikum für das Hauptfach Physik Versuch 17 Ferromagnetismus Wintersemester 2005 / 2006 Name: Mitarbeiter: EMail: Gruppe: Daniel Scholz Hauke Rohmeyer physik@mehr-davon.de B9 Assistent:
Physikalisches Praktikum für das Hauptfach Physik Versuch 17 Ferromagnetismus Wintersemester 2005 / 2006 Name: Mitarbeiter: EMail: Gruppe: Daniel Scholz Hauke Rohmeyer physik@mehr-davon.de B9 Assistent:
Versuchsvorbereitung P1-80: Magnetfeldmessung
 Versuchsvorbereitung P1-80: Magnetfeldmessung Kathrin Ender Gruppe 10 5. Januar 2008 Inhaltsverzeichnis 1 Induktivität einer Spule 2 1.1 Entmagnetisieren des Kerns............................ 2 1.2 Induktiver
Versuchsvorbereitung P1-80: Magnetfeldmessung Kathrin Ender Gruppe 10 5. Januar 2008 Inhaltsverzeichnis 1 Induktivität einer Spule 2 1.1 Entmagnetisieren des Kerns............................ 2 1.2 Induktiver
Magnetismus. Prinzip: Kein Monopol nur Dipole. Kräfte:
 Elektromagnetismus Magnetismus Prinzip: Kein Monopol nur Dipole Kräfte: S N Richtung des Magnetischen Feldes I B Kraft auf Ladungen im B-Feld + Proportionalitätskonstante B FM = q v B Durch Messung: LORENTZ
Elektromagnetismus Magnetismus Prinzip: Kein Monopol nur Dipole Kräfte: S N Richtung des Magnetischen Feldes I B Kraft auf Ladungen im B-Feld + Proportionalitätskonstante B FM = q v B Durch Messung: LORENTZ
Versuch Nr.53. Messung kalorischer Größen (Spezifische Wärmen)
 Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Die Bindung in Übergangsmetallkomplexenn. Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth
 Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
III Elektrizität und Magnetismus
 20. Vorlesung EP III Elektrizität und Magnetismus 19. Magnetische Felder 20. Induktion Versuche: Diamagnetismus, Supraleiter Induktion Leiterschleife, bewegter Magnet Induktion mit Änderung der Fläche
20. Vorlesung EP III Elektrizität und Magnetismus 19. Magnetische Felder 20. Induktion Versuche: Diamagnetismus, Supraleiter Induktion Leiterschleife, bewegter Magnet Induktion mit Änderung der Fläche
Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung.
 Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung. Prinzip In einer langen Spule wird ein Magnetfeld mit variabler Frequenz
Verwandte Begriffe Maxwell-Gleichungen, elektrisches Wirbelfeld, Magnetfeld von Spulen, magnetischer Fluss, induzierte Spannung. Prinzip In einer langen Spule wird ein Magnetfeld mit variabler Frequenz
3. Magnetostatik 3.1. Grundbegriffe
 3. Magnetostatik 3.1. Grundbegriffe In der Natur existieren magnetische Felder. Es gibt allerdings keine Quellen des magnetischen Feldes, d. h. es wurden noch nie magnetischen Ladungen (magnetische Monopole)
3. Magnetostatik 3.1. Grundbegriffe In der Natur existieren magnetische Felder. Es gibt allerdings keine Quellen des magnetischen Feldes, d. h. es wurden noch nie magnetischen Ladungen (magnetische Monopole)
Physikalisches Fortgeschrittenenpraktikum Spezifische Wärme. Vorbereitung. 1 Thermodynamische Grundlagen. 1.1 Die spezifische Wärme eines Festkörpers
 Physikalisches Fortgeschrittenenpraktikum Spezifische Wärme Vorbereitung Armin Burgmeier Robert Schittny In diesem Versuch wollen wir die spezifische Wärme eines Festkörpers, in unserem Fall Dysprosium,
Physikalisches Fortgeschrittenenpraktikum Spezifische Wärme Vorbereitung Armin Burgmeier Robert Schittny In diesem Versuch wollen wir die spezifische Wärme eines Festkörpers, in unserem Fall Dysprosium,
O. Sternal, V. Hankele. 4. Magnetismus
 4. Magnetismus Magnetfelder N S Rotationsachse Eigenschaften von Magneten und Magnetfeldern Ein Magnet hat Nord- und Südpol Ungleichnamige Pole ziehen sich an, gleichnamige Pole stoßen sich ab. Es gibt
4. Magnetismus Magnetfelder N S Rotationsachse Eigenschaften von Magneten und Magnetfeldern Ein Magnet hat Nord- und Südpol Ungleichnamige Pole ziehen sich an, gleichnamige Pole stoßen sich ab. Es gibt
Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld
 Simon Lewis Lanz 2015 simonlanzart.de Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld Zeeman-Effekt, Paschen-Back-Effekt, Fein- und Hyperfeinstrukturaufspaltung Fließt elektrischer Strom
Simon Lewis Lanz 2015 simonlanzart.de Aufspaltung der Energieniveaus von Atomen im homogenen Magnetfeld Zeeman-Effekt, Paschen-Back-Effekt, Fein- und Hyperfeinstrukturaufspaltung Fließt elektrischer Strom
Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 (MOL)
 Seite 1 Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 1 Literatur W. Walcher, Praktikum der Physik, Teubner Themengebiet: Thermodynamik Bundesanstalt für Arbeitsschutz und
Seite 1 Bestimmung der Molaren Masse von Dichlormethan mit der Methode nach Dumas 1 1 Literatur W. Walcher, Praktikum der Physik, Teubner Themengebiet: Thermodynamik Bundesanstalt für Arbeitsschutz und
Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O
![Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O](/thumbs/78/78095730.jpg) Matthias Hinrichs 22.11.1999 Praktikum Anorganische Chemie II Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O 1. Theorie: Die rklärung zur Art und Struktur von Komplexen, werden am besten durch die Kristallfeldtheorie
Matthias Hinrichs 22.11.1999 Praktikum Anorganische Chemie II Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O 1. Theorie: Die rklärung zur Art und Struktur von Komplexen, werden am besten durch die Kristallfeldtheorie
Klausur 12/1 Physik LK Elsenbruch Di (4h) Thema: elektrische und magnetische Felder Hilfsmittel: Taschenrechner, Formelsammlung
 Klausur 12/1 Physik LK Elsenbruch Di 18.01.05 (4h) Thema: elektrische und magnetische Felder Hilfsmittel: Taschenrechner, Formelsammlung 1) Ein Kondensator besteht aus zwei horizontal angeordneten, quadratischen
Klausur 12/1 Physik LK Elsenbruch Di 18.01.05 (4h) Thema: elektrische und magnetische Felder Hilfsmittel: Taschenrechner, Formelsammlung 1) Ein Kondensator besteht aus zwei horizontal angeordneten, quadratischen
Ferienkurs Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Vorlesung 4 Magnetostatik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 16.09.2010 1 Allgemeines In der Magnetostatik gibt es viele Analogien zur Elektrostatik. Ein
Ferienkurs Experimentalphysik 2 Vorlesung 4 Magnetostatik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 16.09.2010 1 Allgemeines In der Magnetostatik gibt es viele Analogien zur Elektrostatik. Ein
Quadratische Gleichungen
 Quadratische Gleichungen Alle aufgezeigten Lösungswege gelten für Gleichungen, die schon vereinfacht und zusammengefasst wurden. Es darf nur noch + vorhanden sein!!! (Also nicht + und auch nicht 3 ; bitte
Quadratische Gleichungen Alle aufgezeigten Lösungswege gelten für Gleichungen, die schon vereinfacht und zusammengefasst wurden. Es darf nur noch + vorhanden sein!!! (Also nicht + und auch nicht 3 ; bitte
Repetitionen Magnetismus
 TECHNOLOGISCHE GRUNDLAGEN MAGNETISMUS Kapitel Repetitionen Magnetismus Θ = Θ l m = H I I N H µ µ = 0 r N B B = Φ A M agn. Fluss Φ Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
TECHNOLOGISCHE GRUNDLAGEN MAGNETISMUS Kapitel Repetitionen Magnetismus Θ = Θ l m = H I I N H µ µ = 0 r N B B = Φ A M agn. Fluss Φ Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Probeklausur zur anorganischen Chemie II
 Probeklausur zur anorganischen Chemie II Prof. Dr. K. Heinze Johannes Gutenberg-Universität Mainz Institut für Anorganische und Analytische Chemie xx. xxxx xxx xx - xx Uhr, C01 Beantworten Sie die Fragen
Probeklausur zur anorganischen Chemie II Prof. Dr. K. Heinze Johannes Gutenberg-Universität Mainz Institut für Anorganische und Analytische Chemie xx. xxxx xxx xx - xx Uhr, C01 Beantworten Sie die Fragen
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
Physik. Abiturwiederholung. Das Elektrische Feld
 Das Elektrische Feld Strom Strom ist bewegte Ladung, die Stromstärke ergibt sich also als Veränderung der Ladung nach der Zeit, also durch die Ableitung. Somit kann man die Ladung als Fläche betrachten,
Das Elektrische Feld Strom Strom ist bewegte Ladung, die Stromstärke ergibt sich also als Veränderung der Ladung nach der Zeit, also durch die Ableitung. Somit kann man die Ladung als Fläche betrachten,
Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel
 Naturwissenschaft Martina Meincken Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel Diplomarbeit Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel
Naturwissenschaft Martina Meincken Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel Diplomarbeit Magnetische Eigenschaften von periodisch angeordneten Nanopartikeln aus Nickel
Kinematik & Dynamik. Über Bewegungen und deren Ursache Die Newton schen Gesetze. Physik, Modul Mechanik, 2./3. OG
 Kinematik & Dynamik Über Bewegungen und deren Ursache Die Newton schen Gesetze Physik, Modul Mechanik, 2./3. OG Stiftsschule Engelberg, Schuljahr 2016/2017 1 Einleitung Die Mechanik ist der älteste Teil
Kinematik & Dynamik Über Bewegungen und deren Ursache Die Newton schen Gesetze Physik, Modul Mechanik, 2./3. OG Stiftsschule Engelberg, Schuljahr 2016/2017 1 Einleitung Die Mechanik ist der älteste Teil
