Parenterale Antibiotika bei Kindern und Jugendlichen
|
|
|
- David Möller
- vor 7 Jahren
- Abrufe
Transkript
1 PEG-Empfehlungen Parenterale Antibiotika bei Kindern und n Empfehlungen einer Expertenkommission der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Horst Scholz unter Mitarbeit von Marianne Abele-Horn, Dieter Adam, Bernd H. Belohradsky, Werner Handrick, Ulrich Heininger, Horst Luckhaupt, Rainer Noack, Reinhard Roos und Michael Weiß Nach der Publikation der Empfehlungen zum rationalen Einsatz oraler Antibiotika bei Kindern und n [15] erschien es sinnvoll, auch Empfehlungen zum Einsatz parenteraler Antibiotika für die Pädiatrie zu veröffentlichen. Die folgenden Empfehlungen der Paul- Ehrlich-Gesellschaft (PEG) sind als Ergänzung der 200 in 4. Auflage erschienenen Empfehlungen der Deutschen Gesellschaft für Pädiatrische nfektiologie (DGP) zur Antibiotika-Therapie von nfektionskrankheiten gedacht [6]. Die Empfehlungen der DGP wurden 2002 in Arbeitsgruppen unter Leitung eines Koordinators erarbeitet (Literaturrecherche, Auswertung klinischer Studien und praktizierter therapeutischer Konzepte). Ausgehend von dieser Basis erfolgte von der PEG-Arbeitsgruppe eine Aktualisierung. Das Ergebnis sind die in einem mehrmaligen Umlauf abgestimmten vorliegenden Empfehlungen zur nitialtherapie bei Kindern und n. n den Empfehlungen werden alle gebräuchlichen Antibiotika abgehandelt. Für die wichtigsten ndikationen werden unter Berücksichtigung des wahrscheinlichen Erregerspektrums (kalkulierte Therapie), des Wandels im Erregerspektrum, der Veränderungen im Resistenzverhalten, der eingeschränkten Zulassung moderner Antibiotika für Kinder und, der Ergebnisse aktueller Therapiestudien und der Kosten Antibiotika ausgewählt, die den Anforderungen im stationären (und ambulanten) Bereich bestmöglichst entsprechen. Zum besseren Verständnis werden vereinzelt auch orale Antibiotika angegeben, und wenn es sinnvoll erschien, wird die Antibiotika-Therapie um andere wichtige therapeutische Maßnahmen ergänzt. Wo immer möglich, liegen den Empfehlungen Evidenz-basierte Daten zugrunde, die angelehnt an das Leitlinien-Manual der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) und der Ärztlichen Zentralstelle für Qualitätssicherung äzq bewertet werden. Die Evidenz-Kriterien (siehe Kasten) werden im Einzelnen in den Tabellen angegeben. Die teilweise geringe Evidenz der Therapie im Kindesalter ist meist Folge der ethischen Bedenken, randomisierte Studien im Kindesalter unter Einschluss von n und Kleinkindern durchzuführen. Bei Fehlen Evidenz-basierter Daten stellen die Empfehlungen einen Kompromiss dar, auch wenn in den meisten Aussagen eine Übereinstimmung der Experten erzielt worden ist. Diese Empfehlungen sollen helfen, die initiale antimikrobielle Therapie nach rationalen und rationellen Gesichtspunkten zu gestalten. Daher werden in der Regel mehrere Therapieoptionen genannt, die in ihrem Wirkungsspektrum nicht immer gleichwertig sind. Sie erlauben dem behandelnden Arzt, seine Entscheidung dem Risikoprofil und der Krankheitssituation des einzelnen Patienten anzupassen, die lokale Erregerepidemiologie zu berücksichtigen, Antibiotika-Unverträglichkeiten zu verringern und nteraktionen mit anderen Medikamenten zu umgehen. Evidenz-Grade Evidenz : Metaanalysen randomisierter Studien oder mindestens eine randomisierte, kontrollierte Studie Evidenz : Mindestens eine gut angelegte, nicht randomisierte, kontrollierte Studie bzw. quasi experimentelle Studie Evidenz : Deskriptive Studien wie Vergleichstudien, Korrelationsstudien und Fall-Kontrollstudien Evidenz : Expertenmeinung, Konsensuskonferenzen, Erfahrung anerkannter Autoritäten Fehlende Zulassungen im Kindesalter Bei der Auswahl der Antibiotika darf nicht übersehen werden, dass viele Antibiotika wegen fehlender Studien auch viele Jahre nach Ausbietung nicht für Kinder oder nur ab einem bestimmten Alter zugelassen sind. Zahlreiche Antibiotika werden in Deutschland außerhalb der in der Zulassung festgelegten Bedingungen ( Off-Label ) oder als nicht zugelassene ( unlicensed ) Medikamente verordnet. Dieser Missstand führt dazu, dass Kinder nicht im selben Maße am medizinischen Fortschritt teilhaben wie Erwachsene, dass Kinder bei Anwendung nicht zugelassener Antiinfektiva einem höheren Nebenwirkungsrisiko ausgesetzt werden als bei Verordnungen, die der Zulassung entsprechen, dass der Kinderarzt bei Anwendung von nicht zugelassenen Antiinfektiva mit einem deutlich höheren Zeitaufwand belastet wird, weil der Einsatz von nicht zugelassenen Antiinfektiva eine Aufklärung wie unter Studienbedingungen erfordert, und dass dennoch der Kinderarzt bei Anwendung derartiger Antiinfektiva einem erhöhten juristischen Risiko ausgesetzt ist. Es ist zu verstehen, dass die Pharmaindustrie ökonomisch am kleinen pädiatrischen Markt nur sekundär interessiert ist. Schwer verständlich ist aber, dass zum Beispiel bestimmte Beta-Lactam-Antibiotika, die seit über 10 Jahren bei Erwachsenen erfolgreich angewen- Chemother J 2004;1:115-. Für die Verfasser: Doz. Dr. Horst Scholz, Straße 6, Nr. 2, 1125 Berlin 1. Jahrgang Heft /
2 det werden, für Kinder unter 12 Jahren nur für einen sehr eingeschränkten ndikationsbereich und/oder nicht für alle Altersgruppen zugelassen sind. Es sind daher staatliche Maßnahmen erforderlich, die ndustrie und zuständige Behörden motivieren, das Kind als vollwertigen Patienten zu akzeptieren. Wie das erreicht werden kann, zeigen erste Regelungen in den USA. Pharmakoökonomie Bei der adäquaten Antibiotika-Behandlung bakterieller nfektionskrankheiten handelt es sich im Gegensatz zu vielen anderen Krankheiten um eine kausale Therapie, bei der die klinische Wirksamkeit das entscheidende Kriterium für die Wahl des Antibiotikums darstellt. Rechtzeitig eingesetzte potente Antibiotika haben eine hohe medizinische Effektivität und führen zu einem raschen Therapieerfolg. Dadurch werden trotz manchmal höherer Tageskosten die Gesamtkosten, die für die Berechnung der Nutzen-Kosten-Relation einer Krankheit entscheidend sind, gesenkt. nadäquate Antibiotika oder eine zu niedrige Dosierung führen häufig zu längerer Therapiedauer oder zum Therapieversagen und bedingen dadurch Folgekosten. Diese ergeben sich aus zusätzlichen diagnostischen und therapeutischen Maßnahmen, verlängerten Krankenhausaufenthalten oder im ungünstigsten Fall aus Dauerschäden, die auf Grund der hohen Lebenserwartung der Kinder mit hohem finanziellen Aufwand verbunden sein können. Folglich muss eine Behandlung mit teureren Antibiotika nicht zwangsweise mit höheren Kosten verbunden sein. Sie kann die Gesamtkosten der Krankheit sogar reduzieren und damit die Solidargemeinschaft entlasten. Unter pharmakoökonomischen Gesichtspunkten sollte also nicht primär eine Verringerung der Antibiotika-Kosten angestrebt werden, sondern es sollten Antibiotika gewählt werden, die hohe medizinische Effektivität garantieren und Therapieversagerrate, Therapiedauer, Monitoring- und Applikationskosten, Umweltbelastungen, etc. minimieren. Eine Möglichkeit, dieses Konzept umzusetzen, ist die Sequenztherapie, worunter eine initiale parenterale Therapie mit oraler Folgetherapie verstanden wird. Das per os verabfolgte Antibiotikum muss dabei nicht mit dem parenteralen Antibiotikum identisch sein, es sollte aber ein ähnliches Wirkungsspektrum besitzen und sich durch hohe Bioverfügbarkeit auszeichnen. Von Nachfolgepräparaten (Generika) müssen wissenschaftlich gesicherte und garantierte Daten mindestens über die Bioverfügbarkeit und über die Konstanz der Qualität vorliegen. Eine Sequenztherapie ist u. a. sinnvoll bei nfektionskrankheiten der Atem- und Harnwege, der Haut und Weichteile und bei anderen Krankheiten, die schnell auf eine initiale parenterale Therapie ansprechen. Die Sequenztherapie verbietet sich dagegen bei schweren bakteriellen nfektionskrankheiten wie Sepsis, Meningitis, Endokarditis, nosokomialen nfektionen mit resistenten Erregern und nfektionen immundefizienter Patienten. Bei diesen Krankheiten muss unverzüglich eine kalkulierte nitialtherapie eingeleitet werden, die alle mutmaßlichen Erreger erfasst. Ein Warten auf mikrobiologische Ergebnisse verbietet sich. So können am ehesten die Letalität verringert, Komplikationen vermieden und Kosten reduziert werden. Ambulante parenterale Therapie Zunehmend werden auch im ambulanten Bereich parenterale Antibiotika eingesetzt. Das belastet zwar das Budget des niedergelassenen Arztes, verringert aber die Gesamtkosten. Außerdem wird diese organisatorisch aufwendige Therapie von vielen Patienten gut akzeptiert. Mögliche ndikationen im Kindesalter sind unter anderem Mukoviszidose, Lyme-Borreliose, Osteomyelitis (nach stationärem Therapiebeginn), Exazerbation einer chronischen Otitis media und Fieber bei onkologischen Patienten mit nfektionsverdacht mit niedrigem Risiko. Wichtige Voraussetzungen für eine ambulante parenterale Therapie sind stabiler klinischer Status, gesicherte fachgerechte Pflege und Verfügbarkeit einmal täglich applizierbarer Antibiotika wie z. B. Ceftriaxon, Teicoplanin und Aminoglykoside. Mikrobiologie, Pharmakodynamik Für die kalkulierte Antibiotika-Therapie ist die Kenntnis des Erregerspektrums und der lokalen Resistenzsituation wichtig. Für einzelne Stationen (z. B. ntensivstationen, onkologische Stationen) ist außerdem die Kenntnis der stationsinternen Resistenzsituation zu fordern. Die überregionale Resistenzlage wichtiger Bakterienspezies wird in regelmäßigen Abständen von der PEG in ausgewählten Laboratorien Deutschlands, Österreichs und der Schweiz mit Hilfe einheitlicher, standardisierter Methoden untersucht ( Diese langfristigen Untersuchungen haben gezeigt, dass beispielsweise die Resistenzrate von E. coli gegenüber Ampicillin von 1998 bis 2001 von 41 % auf 49 % zugenommen hat und dass bei Klebsiella pneumoniae der Anteil von Stämmen mit Extendedspectrum-Beta-Lactamasen (ESBL), die auch Cephalosporine der Gruppe inaktivieren können, von 4,7 % auf 8,2 % gestiegen ist. Bei Pseudomonas spp. war die Zunahme der Resistenz gegenüber Ceftazidim und Piperacillin um 8 bis 9 % auffällig. Bei Staphylokokken stieg der Anteil Methicillin-resistenter S.-aureus-solate (MRSA) und Methicillin-resistenter S.-epidermidis-Stämme (MRSE) von 15 % auf 21 % bzw. von 59 % auf 69 %. Für eine gezielte effiziente und wirtschaftliche Antibiotika-Therapie ist eine mikrobiologische Diagnostik erforderlich. Die Referenzmethode für die Bestimmung der antimikrobiellen Aktivität eines Antibiotikums ist die Messung der minimalen Hemmkonzentration (MHK). Der vielerorts angewandte Blättchentest kann eine Fehlerquote von bis zu 15 % haben. Bei schweren, lebensbedrohlichen und seltenen nfektionskrankheiten sollte daher vom Mikrobiologen die Bestimmung des MHK- Werts angefordert werden. Bei Anwendung von Beta-Lactam-Antibiotika und Makroliden ist die Zeit, in der die Konzentration des Antibiotikums im Plasma größer als der MHK-Wert ist, bedeutungsvoll; t > MHK sollte mindestens 40 % des Dosierungsintervalls betragen (zeitabhängige Bakterizidie). Bei Aminoglykosiden und Fluorchinolonen korreliert der Quotient aus AUC-Werten (area under the curve) oder Spitzenspiegel, der in der Praxis leichter zu ermitteln ist, und MHK-Wert mit dem Therapieerfolg (konzentrationsabhängige Bakterizidie). Angestrebt wird ein Plasmaspitzenspiegel, der 5- bis 10fach höher als der MHK-Wert ist. Darüber hinaus sollten von den verwendeten Antibiotika die wichtigsten phar Jahrgang Heft /2004
3 makokinetischen Eigenschaften (Halbwertszeit, Elimination, Gewebegängigkeit, Verteilung im Gewebe) und toxikologischen Wirkungen (Nebenwirkungen, nteraktionen) bekannt sein. Charakterisierung der Antibiotika aus pädiatrischer Sicht Penicilline Penicilline sind bewährte Antibiotika mit einer großen therapeutischen Breite. Für die Anwendung müssen jedoch wegen steigender Resistenzraten mancher Bakterien die regionalen Besonderheiten beachtet werden. Die pharmakokinetischen Daten der Penicilline zeigen keine große Variabilität. Penicilline verteilen sich vornehmlich extrazellulär. Die Halbwertszeiten nierengesunder Patienten werden mit etwa 1 h gemessen. Die Elimination erfolgt meist unverändert renal. Penicillin G (Benzylpenicillin) (1. E. Penicillin G = 0,6 µg; 1 µg = 1,67. E.) gilt nach wie vor als Mittel der Wahl bei Krankheiten durch Streptokokken, Pneumokokken (in Deutschland), Meningokokken und Spirochäten. Es gibt weltweit keine Penicillin-resistenten Streptokokken der Gruppe A. Penicillinresistente Pneumokokken sind derzeit in Deutschland mit < 1 % noch selten, die Prävalenz intermediär-resistenter Stämme liegt jedoch bereits bei 5 bis 15 %. Bei Patienten, die aus endemischen Ländern (z. B. Frankreich, Spanien, Ungarn, ehemaliges Jugoslawien, USA) einreisen, muss dagegen mit einer wesentlich höheren Penicillin-Resistenzrate gerechnet werden. Penicillin-resistente Stämme zeigen eine verminderte Empfindlichkeit gegenüber Cephalosporinen und sind häufig resistent gegenüber Makroliden. 5 bis 10 % der oralen Streptokokken (S. milleri u. a.) sind gegenüber Penicillin resistent. Etwa 80 % der Staphylokokken bilden Penicillinase und gelten als resistent gegen alle Penicillinase-labilen Penicilline. Mit Depot-Penicillinen (Tab. 12) werden nur niedrige Plasmakonzentrationen erzielt. hr Einsatz beschränkt sich daher auf Patienten mit schlechter Compliance und die Rezidivprophylaxe des akuten rheumatischen Fiebers. Die Aminopenicilline (Ampicillin: Binotal u. a.) haben ein breiteres Spektrum. Neben Streptokokken erfassen sie Enterococcus faecalis (etwa 2 % der Stämme sind Ampicillin-resistent, bei E. faecium sind es etwa 75 %), Haemophilus influenzae, H. parainfluenzae und Listerien. Die Wirkung gegenüber gramnegativen Bakterien, vor allem Enterobacteriaceae, Moraxella catarrhalis und Bacteroides fragilis, ist wegen zunehmender Resistenz der Erreger durch Bildung von Beta-Lactamasen eingeschränkt. Durch Kombination mit einem Beta-Lactamase-nhibitor (BL) kann das Wirkungsspektrum um Beta-Lactamase-bildende Erreger, z. B. Staphylococcus aureus, M. catarrhalis, H. influenzae (in Deutschland etwa 5 % Beta-Lactamase-positive Stämme), E. coli und Bacteroides-Spezies, erweitert werden. Als fixe Kombinationen werden Amoxicillin-Clavulansäure in einem Mischungsverhältnis von 5 : 1 und 10 : 1 (Augmentan ) und Ampicillin- Sulbactam in einem Mischungsverhältnis von 2 : 1 (Unacid ) angeboten. Bei bis zu 10 % der mit einem Aminopenicillin behandelten Kinder kann, gewöhnlich in der zweiten Woche, ein makulöses Exanthem auftreten. Die Ursache ist unbekannt, es handelt sich dabei nicht um eine Allergie. Die Exanthemrate ist besonders hoch bei Kindern mit infektiöser Mononukleose und Leukämie, weshalb diese Patienten nicht mit Aminopenicillinen behandelt werden sollten. Beide Aminopenicillin-BL- Kombinationen sind bei parenteraler Anwendung gut verträglich. Bei der Kombination mit Clavulansäure kommt es sehr selten zu hepatotoxischen Reaktionen. Das breiteste Wirkungsspektrum der Penicilline besitzen die Acylaminopenicilline Mezlocillin (Baypen ) und Piperacillin (Pipril ). Sie zeichnen sich durch eine gute Wirkung gegen Enterobakterien und Pseudomonaden (nur Piperacillin) aus. Da auch Acylaminopenicilline durch Beta-Lactamasen hydrolysiert werden, kann ihr Wirkungsspektrum durch Kombination mit einem BL gegen Beta-Lactamase-bildende Bakterien wie Staphylokokken, Bacteroides und einige Enterobakterien erweitert werden. Zur Wahl stehen freie Kombinationen mit Sulbactam (Combactam ) und eine fixe Kombination aus Piperacillin und Tazobactam (Tazobac ), die allerdings nur für die Behandlung von intraabdominalen nfektionen für Kinder ab 2 Jahren zugelassen ist. Die soxazolylpenicilline Oxacillin (nfectostaph ) und Flucloxacillin (Staphylex ) sind Penicillinase-feste Penicilline, deren Einsatz auf Krankheiten durch S. aureus begrenzt ist. Die Wirkung der soxazolylpenicilline gegen Streptokokken ist schwächer als die des Benzylpenicillins. Gegen MRSA sind soxazolylpenicilline unwirksam. Cephalosporine Die parenteralen Cephalosporine können nach dem Wirkungsspektrum in fünf Gruppen eingeteilt werden (Tab. 1). Die Cephalosporine zeigen bei den pharmakokinetischen Eigenschaften teilweise erhebliche Unterschiede. Die meisten Cephalosporine werden überwiegend unverändert renal ausgeschieden. Die durchschnittlichen Halbwertszeiten nierengesunder Patienten betragen 1 bis 2 h, bei dem über die Galle ausgeschiedenen Ceftriaxon jedoch 6,5 bis 8 h. Cephalosporine verteilen sich wie die Penicilline extrazellulär. Von den Penicillinen unterscheiden sich die Cephalosporine durch ihre zwar unterschiedliche, aber generell bessere Beta-Lactamase-Stabilität. Hervorzuheben ist die gute Aktivität der Cephalosporine der Gruppen 1 und 2 (Basis-Cephalosporine) gegenüber S. aureus. Gegen MRSA sind alle Cephalosporine unwirksam. Die Empfindlichkeit gramnegativer Erreger ist sehr variabel. Alle Cephalosporine sind inaktiv gegen Enterokokken, Listerien, Bordetellen, Chlamydien, Mykoplasmen und Legionellen. Grampositive Anaerobier werden von den Cephalosporinen mehr oder weniger gut erfasst, gramnegative Anaerobier sind meist resistent. Die Cephalosporine der Gruppe 1 wirken vorwiegend gegenüber Streptokokken und Staphylokokken. Die Wirkung gegen gramnegative Bakterien ist vergleichsweise gering. Gegenüber Haemophilus spp. sind Cephalosporine der Gruppe 1 unwirksam. Die Cephalosporine der Gruppe 2 sind weitgehend Beta-Lactamase-stabil. Sie sind gegen gramnegative Stäbchen wesentlich wirksamer als die Cephalosporine der Gruppe 1. Cefotiam und Cefuroxim haben eine gute Aktivität gegen Streptokokken, Staphylokokken (außer MRSA und MRSE), H. influenzae, M. catarrhalis, E. coli und Klebsiellen und erfassen damit die häufigsten im Kindesalter vorkommenden Erreger. Bei Enterobacter und Proteus muss mit einer hohen Resistenzrate gerechnet werden. Cefamandol wird wegen der möglichen Blutungsgefahr und anderer 1. Jahrgang Heft /
4 Tab. 1. Gruppeneinteilung der parenteralen Cephalosporine Gruppe NN Handelsname (Auswahl) 1 Cefazolin Elzogram 2 Cefuroxim Cefotiam a b Cefotaxim Ceftriaxon Ceftizoxim Ceftazidim 4 Cefepim Cefpirom 1 Zinacef Spizef Claforan Rocephin Ceftix Fortum Maxipime Cefrom 5 Cefoxitin Mefoxitin Mittel der Wahl: Cefuroxim, Cefotiam, Cefotaxim, Ceftazidim und Cefepim, eingeschränkt Ceftriaxon 1 n Österreich ab 12 Jahre zugelassen Nebenwirkungen für Kinder nicht mehr empfohlen. Die Cephalosporine der Gruppe zeichnen sich durch ein breiteres Wirkungsspektrum und eine starke antibakterielle Aktivität gegenüber gramnegativen Bakterien aus. Die Resistenzsituation ist nach wie vor günstig. Cefotaxim, Ceftriaxon und Ceftazidim sind gut liquorgängig und haben wesentlich dazu beigetragen, die Letalität der bakteriellen Meningitis, Sepsis und anderer schwerer nfektionskrankheiten bei Kindern zu senken. Die Cephalosporine der Gruppe a unterscheiden sich in ihren pharmakokinetischen Eigenschaften. Ceftriaxon braucht aufgrund der langen Halbwertszeit nur einmal täglich verabfolgt zu werden und ist damit auch für die ambulante Therapie gut geeignet. Nachteilig sind die durch die hohe biliäre Ausscheidung (etwa 40 %) bedingten Nebenwirkungen (Selektionsdruck, reversible Bildung von Gallengrieß ) und die hohe Plasmaeiweißbindung (> 90 %), die zur Verdrängung von Bilirubin aus der Albuminbindung führen kann. Ceftriaxon ist daher bei Früh- und Neugeborenen, vor allem bei Hyperbilirubinämie, kontraindiziert. Die Cephalosporine der Gruppe b (Ceftazidim) und 4 (Cefepim) erfassen zusätzlich Pseudomonas aeruginosa. Cefepim hat im Vergleich zu Ceftazidim eine höhere Aktivität gegenüber S. aureus, Penicillin- und Makrolid-resistenten Pneumokokken sowie S. viridans, wirkt gegen Enterobacter spp. und verfügt über eine höhere Stabilität gegenüber Extended-spectrum-Beta-Lactamasen (ESBL) und Typ-1-Beta-Lactamasen. Cefoxitin gehört zu den Cephalosporinen der Gruppe 5. Es besitzt das Wirkungsspektrum der Cephalosporine der Gruppe 2, verfügt aber über eine besonders hohe Beta-Lactamase-Stabilität und eine zusätzliche Wirkung gegen Bacteroides fragilis und andere gramnegative Anaerobier. Cephalosporine werden im Allgemeinen gut vertragen. Zu den wichtigsten Nebenwirkungen der parenteralen Cephalosporine gehören Überempfindlichkeitsreaktionen, vor allem Exantheme. Kreuzreaktionen zu den Penicillinen sind selten. Bei Ceftriaxon ist die Diarrhö-Rate erhöht. Carbapeneme Carbapeneme sind weiterentwickelte Beta-Lactam-Antibiotika. Die Verteilung der Carbapeneme erfolgt extrazellulär. Sie werden teilweise metabolisiert und vorzugsweise renal eliminiert. Die Halbwertszeit nierengesunder Patienten liegt bei einer Stunde, bei Ertapenem bei etwa 4 h. Carbapeneme sind weitestgehend Beta-Lactamase-stabil. Sie haben im Vergleich zu Penicillinen und Cephalosporinen ein erweitertes Wirkungsspektrum. Carbapeneme wirken gegen grampositive Bakterien einschließlich Erysipelothrix, Aktinomyzeten und Nocardien mit Ausnahme von MRSA und MRSE (resistent), Enterokokken (mäßige Wirkung) und Corynebacterium spp., insbesondere Corynebacterium jeikeium (resistent). m gramnegativen Wirkungsspektrum der Carbapeneme liegen nahezu alle Enterobacteriaceae. Unzureichend ist die Aktivität gegenüber Stenotrophomonas, Burkholderia cepacia, Acinetobacter, Legionellen und Brucellen. Von den Anaerobiern werden grampositive Kokken und gramnegative Erreger einschließlich Bacteroides fragilis gut erfasst, dagegen ist die Wirksamkeit gegenüber Clostridien nicht optimal. mipenem/cilastatin (Zienam ) wurde als erster Vertreter dieser Gruppe eingeführt. Es sollte nur zur Behandlung schwerer nfektionskrankheiten eingesetzt werden. Überdosierungen (> 60 mg/kg KG/Tag) und zu rasche Applikation können Krampfanfälle auslösen. Zur Therapie der Meningitis ist mipenem daher nicht geeignet. Meropenem (Meronem ) ist ein weiterer Vertreter dieser Gruppe mit einem ähnlichen Wirkungsspektrum. Es zeigt gegenüber grampositiven Erregern (Enterokokken) eine etwas geringere, gegenüber Pseudomonas aeruginosa eine etwas höhere Aktivität. Meropenem benötigt keinen Nierenschutzstoff. Es ist bei entzündeten Meningen gut liquorgängig und für die Therapie der Meningitis zugelassen. Ertapenem (nvanz ) wird in verschiedenen Studien klinisch geprüft, ist für Kinder und aber noch nicht zugelassen. Es braucht auf Grund der langen Halbwertszeit nur einmal täglich verabfolgt zu werden und ist für die empirische Behandlung schwerer ambulant erworbener nfektionen (z. B. intraabdominale und gynäkologische nfektionen, Atemwegsinfektionen) geeignet. Aztreonam Das Monobactam zeigt ein den Penicillinen ähnliches pharmakokinetisches und pharmakodynamisches Verhalten. Aztreoanam kann bei nfektionen durch P. aeruginosa und andere gramnegative Stäbchenbakterien indiziert sein, wenn diese gegenüber anderen Antibiotika resistent sind und die Gabe eines Aminoglykosids kontraindiziert ist. Gegenüber grampositiven Bakterien ist Aztreonam unwirksam. Aminoglykoside Aminoglykoside (Tab. 2 ) sind bewährte bakterizide Antibiotika mit einer ausgeprägten, schnell einsetzenden, konzentrationsabhängigen Bakterizidie. Der postantibiotische Effekt kann in Abhängigkeit von Plasmaspiegel, Kombinationspartner und mmunstatus des Patienten mehrere Stunden andauern. Aminoglykoside verteilen sich extrazellulär. Sie werden unverändert renal eliminiert. Die Liquorpenetration ist gering. Die Halbwertszeiten nierengesunder Patienten betragen 1,5 bis 2 h, bei eingeschränkter Nierenfunktion können deutlich längere Werte erreicht werden. Aminoglykoside werden vor allem für die Kombinationstherapie schwerer nfektionskrankheiten verwendet. Das antimikrobielle Spektrum umfasst weitgehend alle Enterobacteriaceae, P. aeruginosa (hier insbesondere Tobramycin) und Staphylokokken. Gegenüber Streptokokken, Enterokokken, H. influenzae und Legionellen sind Aminoglykoside nur mäßig aktiv. Pneumokokken, Stenotrophomonas maltophilia, Burkholderia cepacia, Acinetobacter-Spezies und Anaerobier sind gegenüber Aminoglykosiden resistent. n Kombination mit Penicillinen wirken Aminoglykoside syner Jahrgang Heft /2004
5 Tab. 2. Aminoglykoside NN Handelsname Streptomycin Strepto-Fatol, -Hefa Gentamicin Refobacin, Gencin u. a. Tobramycin Netilmicin Amikacin Gernebcin, Brulamycin Certomycin Biklin gistisch auf Enterokokken, Streptokokken der Gruppe A und B, auch wenn eine Niedrigresistenz gegen Gentamicin nachgewiesen ist, und auf Listerien. n Kombination mit Cephalosporinen besteht ein Synergismus gegenüber gramnegativen Bakterien wie zum Beispiel Klebsiellen und Pseudomonas spp. Das Wirkungsspektrum der verschiedenen Aminoglykoside ist weitgehend ähnlich. Tobramycin zeigt gegenüber Pseudomonaden eine bessere n-vitro- Aktivität. Die Resistenzraten sind für Gentamicin, Tobramycin und Netilmicin annähernd gleich, für Amikacin dagegen bei vielen Enterobacteriaceae günstiger. Amikacin erfasst zusätzlich Mycobacterium tuberculosis, einige atypische Mykobakterien und Nocardien. Streptomycin zählt zu den älteren Aminoglykosiden und wird heute nur noch zur Behandlung der Tuberkulose eingesetzt. m sauren Milieu (Abszess) sind Aminoglykoside inaktiv. Alle Aminoglykoside sind potenziell nephro- und ototoxisch. Außerdem können sie die neuromuskuläre Übertragung stören und sind deshalb bei Myasthenia gravis kontraindiziert. Aminoglykoside kumulieren im nnenohr (Vestibularis- und Cochleaschäden) und in der Nierenrinde. Das Risiko für toxische Schäden steigt besonders bei einer Nierenfunktionsstörung, bei einer Therapiedauer länger als sieben bis zehn Tage, wenn der Patient innerhalb von sechs Wochen vor Beginn der Therapie schon einmal mit einem Aminoglykosid behandelt worden ist und bei gleichzeitiger Gabe anderer nephro- oder ototoxischer Medikamente. Ob die Toxizität durch tägliche Einmalgaben als Kurzinfusion über 0 min verringert werden kann, ist vielfach untersucht worden. n zehn Metaanalysen, mehreren neueren kontrollierten Studien und einigen Doppelblindstudien an Erwachsenen konnte gezeigt werden, dass die Einmalgabe von Aminoglykosiden effektiv und sicher ist. Studien mit Aminoglykosiden bei Kindern wurden in einer neuen Übersicht ausgewertet [9]. Etwa 700 Kinder älter als einen Monat wurden mit Aminoglykosiden mit erweitertem Dosierungsintervall behandelt, neun Studien (etwa 450 Patienten) untersuchten die klinische und/oder bakteriologische Wirksamkeit der Einmalgabe, elf Studien werteten die Nephrotoxizität aus und acht Studien analysierten die Ototoxizität. Eine geringe Nephrotoxizität wurde in den analysierten Studien bei 4 von 50 Kindern mit der Einmalgabe und bei keinem Kind mit traditioneller Aminoglykosid-Therapie festgestellt. Dieses Ergebnis, obwohl gleichwertig, besagt, dass bei Kindern die theoretisch durch die tägliche Einmalgabe erwartete niedrigere Nephrotoxizität infolge länger anhaltender niedrigerer Talspiegel nicht substanziell ist (vermutlich wegen der höheren Aminoglykosid-Clearance und besseren Verträglichkeit bei Kindern). Eine Ototoxizität wurde bei 4,1 % der Patienten mit der Einmalgabe gegenüber 2,4 % der Patienten mit der traditionellen Mehrmalgabe gefunden. Die klinische und bakteriologische Wirksamkeit der Einmalgabe war bei Kindern mit Harnwegsinfektion [] und vermuteter nfektion durch gramnegative Bakterien nicht schlechter als bei der Mehrmalgabe. Die Versagerquote war bei neutropenischen Patienten mit Fieber zwischen beiden Therapieformen ähnlich [10]. Diese Aussagen gelten jedoch nur für die Kombinationstherapie (und nicht für die Monotherapie mit einem Aminoglykosid). Demnach scheint die tägliche Einmalgabe von Gentamicin, Tobramycin, Netilmicin und Amikacin zusammen mit einem Beta-Lactam-Antibiotikum oder einem gegen Pseudomonas wirksamen Antibiotikum im Kindesalter geeignet zu sein bei schweren nfektionen einschließlich Sepsis durch gramnegative Bakterien sowie bei Kindern mit Neutropenie und Fieber. Nicht zu empfehlen ist die tägliche Einmalgabe bei Patienten mit Verbrennungen oder Nierenfunktionsstörungen. Die tägliche Einmalgabe von Aminoglykosiden reduziert das Risiko für subtherapeutische Konzentrationen. Die Nephro- und Ototoxizität scheinen bei täglicher Einmalgabe nicht größer als mit der Mehrmalgabe zu sein. Bei Vorliegen von Risikofaktoren (Nierenfunktionsstörung, Früh- und Neugeborene usw., siehe oben) ist ein Drug- Monitoring anzuraten. Bei traditioneller Gabe der Aminoglykoside und normaler Nierenfunktion ist eine kontinuierliche Kontrolle der Serumspiegel nicht notwendig. Wegen der individuell unterschiedlichen Serumkonzentrationen sollte aber gegebenenfalls, z. B. bei Neu- und Frühgeborenen, der Spitzenspiegel bestimmt werden, um subtherapeutischen Serumkonzentrationen entgegensteuern zu können. Hierfür wird Serum 0 bis 60 Minuten nach Ende der. Gabe entnommen. Bei Einmalgabe der Aminoglykoside sollte vor allem der Talspiegel vor Gabe der (2. oder). Dosis geprüft werden. Als therapeutische Zielbereiche innerhalb eines 24- h-dosierungsintervalls werden Talspiegel unter 1,0 mg/l (Gentamicin, Tobramycin, Netilmicin) oder unter 5 mg/l (Amikacin) und Spitzenspiegel von 15 bis 20 mg/l (Gentamicin, Tobramycin), mindestens 20 mg/l (Netilmicin) und etwa 60 mg/l (Amikacin) angestrebt. Lokal sollten Aminoglykoside wegen des Risikos der Resistenzentwicklung möglichst nicht verabfolgt werden, ausgenommen sind ophthalmologische nfektionen und die nhalation bei Patienten mit Mukoviszidose. Makrolide Die Makrolide haben sich in der Pädiatrie seit über 40 Jahren bewährt. Sie werden vorwiegend per os angewendet. ntravenös stehen Erythromycinlactobionat (Erythrocin ) und für Kinder ab zwölf Jahre Clarithromycin (Klacid ) zur Verfügung. Makrolide verteilen sich intra- und extrazellulär. Die Halbwertszeiten betragen für Erythromycinlactobionat etwa 2,5 h und für Clarithromycin 2 bis 5 h. Beide Makrolide werden in der Leber metabolisiert und vorzugsweise biliär ausgeschieden. Makrolide sind wirksam gegenüber den wichtigsten Erregern von Atemwegsinfektionen einschließlich Mycoplasma pneumoniae, Legionella-Arten und Chlamydia pneumoniae. Darüber hinaus sind sie aktiv gegen Chlamydia trachomatis, Bordetellen, Borrelien, Helicobacter pylori, Corynebacterium diphtheriae, Erysipelothrix rhusiopathiae, atypische Mykobakterien und Ureaplasma urealyticum. Weniger gut bis mäßig empfindlich sind Streptokokken der Viridans-Gruppe, Haemophilus influenzae, Campylobacter jejuni, Treponema pallidum und Rickettsien. Die Wirkungsunterschiede zwischen Erythromycinlactobionat und Clarithromycin sind marginal. 1. Jahrgang Heft /
6 Wie in anderen Ländern nimmt auch in Deutschland die Resistenz der A-Streptokokken sowie der Pneumokokken gegenüber Makroliden zu und beträgt gegenwärtig etwa 10 % bzw. 15 bis 25 % (regional sogar um 0 %). Das ist vor allem für die Behandlung von Kindern von Nachteil, weil als Alternativpräparate die neuen Fluorchinolone und die Ketolide nicht bzw. noch nicht zur Verfügung stehen. Die Verträglichkeit der Makrolide bei Kindern ist gut. Zu beachten sind jedoch die vielfältigen nteraktionen mit anderen Pharmaka (u. a. Theophyllin, Carbamazepin, Terfenadin, Triazolam, Midazolam, Astemizol). Die Behandlung von Neugeborenen mit Erythromycin ist mit einem gehäuften Vorkommen der hypertrophischen Pylorusstenose assoziiert. Die intravenöse Gabe von Erythromycin führt oft zur Venenreizung oder Phlebitis. Daher sollte die intravenöse Gabe von Erythromycin als nfusion über eine Stunde erfolgen, bei längerer intravenöser Therapie ist die Anlage eines zentral-venösen Zuganges zu erwägen. Auch kardiotoxische Wirkungen können auftreten: QT-Verlängerung und Herzrhythmusstörungen (Frühgeborene). Bei Erwachsenen sind nach intravenöser Gabe hoher Dosen von Erythromycin reversible Hörstörungen beschrieben. Lincosamide Clindamycin (Sobelin, Turimycin ) verteilt sich extra- und intrazellulär. Es wird zu mehr als 80 % metabolisiert. Die Halbwertszeit beträgt 2,5 h. Clindamycin penetriert nicht in den Liquor cerebrospinalis. Clindamycin zeigt eine bakteriostatische, zeitabhängige Wirkung gegen grampositive Bakterien (Streptokokken, Pneumokokken, Staphylokokken, Korynebakterien), Anaerobier, Toxoplasmen und Plasmodien. Die Resistenz gegenüber Streptokokken der Gruppe B nimmt zu. MRSA sind nur zu etwa 50 % sensibel. Enterokokken, Ureaplasmen, Haemophilus und andere gramnegative Bakterien sind gegenüber Clindamycin resistent. Hauptindikationen von Clindamycin sind Haut- und Weichteilinfektionen, odontogene nfektionen, Knochenund Gelenkinfektionen und nfektionskrankheiten durch anaerobe Bakterien. Die bei Erwachsenen als Nebenwirkung gefürchtete pseudomembranöse Enterokolitis ist bei Kindern selten. Oxazolidinone Als erster Vertreter dieser Gruppe mit völlig neuer Struktur und neuem Wirkungsmechanismus (daher keine Kreuzresistenz mit anderen Antibiotika) wurde Linezolid (Zyvoxid ) zugelassen, bisher in Deutschland jedoch noch nicht für Kinder und. Es kann parenteral und per os verabfolgt werden. Linezolid wird in der Leber metabolisiert und hauptsächlich renal ausgeschieden. Die Halbwertszeit beträgt 5 bis 7 h. Das Wirkungsspektrum umfasst zahlreiche grampositive Erreger einschließlich MRSA, MRSE, Penicillin-resistenter Pneumokokken und Vancomycin-resistenter Enterokokken (VRE), Corynebacterium spp., Listeria monocytogenes, Clostridien und Bacillus spp. Streptogramine Streptogramine sind zyklische Peptidantibiotika. Für Erwachsene ist Quinupristin/Dalfopristin (Synercid ) zugelassen, eine Kombination aus einem Streptogramin der Gruppe A und B. Beide Substanzen werden metabolisiert und vorzugsweise biliär ausgeschieden. Die Halbwertszeit beträgt etwa eine Stunde. Die Kombination wirkt bakterizid und besitzt einen lang anhaltenden postantibiotischen Effekt. Das Wirkungsspektrum umfasst Staphylokokken einschließlich MRSA/MRSE, Streptokokken einschließlich Penicillin- und Makrolid-resistenter Pneumokokken, E. faecium inklusive Vancomycin-resistenter Stämme und einige andere Bakterien. E. faecalis ist resistent. Quinupristin/Dalfopristin ist ein Reserve-Antibiotikum. Nebenwirkungen: schlechte Venenverträglichkeit, gastrointestinale Beschwerden, zahlreiche nteraktionen. Glykopeptide Glykopeptide wirken zeitabhängig. Sie verteilen sich extrazellulär. Die Halbwertszeit nierengesunder Patienten beträgt für Vancomycin (Vancomycin Lilly u. a.) 6 h und für Teicoplanin (Targocid ) 0 bis 80 h. Teicoplanin kann einmal täglich gegeben werden, eine i. m. Gabe ist möglich. Damit ist Teicoplanin auch für die ambulante Therapie geeignet. Beide Glykopeptide werden hauptsächlich unverändert renal ausgeschieden. Die Liquorpenetration ist sehr gering, bei Vancomycin können aber durch eine höhere Dosierung therapeutisch wirksame Spiegel erreicht werden. Vancomycin und Teicoplanin wirken ausschließlich gegen grampositive Bakterien: Staphylokokken inklusive MRSA und MRSE, Enterokokken einschließlich E. faecium, Streptokokken, Pneumokokken inklusive Penicillin-resistenter Stämme, Clostridium difficile, Korynebakterien (auch Corynebacterium jeikeium), Listerien und grampositive Anaerobier. Teicoplanin ist im Vergleich zu Vancomycin weniger aktiv gegen Staphylokokken (S. haemolyticus), aber etwas wirksamer gegen Enterokokken. Bei MRSA, MRSE und Enterokokken wurden weltweit vereinzelt resistente Stämme isoliert. Um der Resistenzentwicklung und der Selektion resistenter Stämme vorzubeugen, sollten Glykopeptide sehr restriktiv verordnet werden. Glykopeptide sind Reserve-Antibiotika. n Deutschland sind Vancomycin-intermediäre MRSA (VSA, GSA) und Vancomycin-resistente Enterokokken (VRE) noch äußerst selten. Die Resistenz der Enterokokken gegen Vancomycin (zumeist vana und vanb) und gegen Teicoplanin (vana) lässt sich am sichersten mit dem Screening-Test nachweisen. Diese Methode eignet sich auch zum Nachweis Vancomycin-intermediärer Staphylokokken. Das Ergebnis des Tests gilt ebenfalls für Teicoplanin. Glykopeptide können durch Kumulation nephro- und ototoxische Wirkungen haben. Teicoplanin ist weniger nephrotoxisch als Vancomycin. Nach rascher Gabe von Vancomycin kann ein generalisiertes Erythem ( Red-Man -Syndrom) beobachtet werden. Bei Patienten mit Niereninsuffizienz und Vorliegen anderer Risikofaktoren ist ein Drug-Monitoring anzuraten. Für Vancomycin sollten Spitzenspiegel (eine Stunde nach nfusionsende) von 15 bis 40 mg/l und Talspiegel < 10 mg/l angestrebt werden. Der therapeutische Bereich für Teicoplanin liegt zwischen 10 und 20 mg/l. Tetracycline (Doxycyclin) Doxycyclin reichert sich intrazellulär an und ist gut gewebegängig. Es wird teilweise metabolisiert und biliär und renal eliminiert. Die durchschnittliche Halbwertszeit beträgt etwa 15 h. Doxycyclin wirkt bakteriostatisch. Sein Wirkungsbereich erstreckt sich u. a. auf Mykoplasmen, Chlamydien, Brucellen, Rickettsien, Campylobacter, Vibrio cholerae, Yersinien, Borrelien (B. burgdor Jahrgang Heft /2004
7 feri), Spirochäten, Leptospiren, Francisella tularensis, Burkholderia mallei und B. pseudomallei. Zu beachten sind die örtlich unterschiedlichen Resistenzraten. Staphylokokken, A-Streptokokken und Pneumokokken werden nur unsicher erfasst. Tetracyclin-Calcium- Komplexe werden irreversibel im Knochen und in den Zähnen abgelagert, so dass die Applikation bei Kindern unter neun Jahren und bei Schwangeren vermieden werden sollte. Chloramphenicol Chloramphenicol zeichnet sich durch gute Gewebegängigkeit einschließlich Liquor und Hirngewebe aus. Es wird vorwiegend renal ausgeschieden. Die Halbwertszeit beträgt 1,5 bis h. Die orale Bioverfügbarkeit beträgt 90 %. Chloramphenicol erfasst eine Vielzahl grampositiver und gramnegativer Bakterien. Es bestehen allerdings teilweise hohe Resistenzraten. Der Einsatz von Chloramphenicol ist wegen der Nebenwirkungen, vor allem wegen der seltenen irreversiblen, dosisunabhängigen aplastischen Anämie, und der zumeist bestehenden Alternativen sehr begrenzt. Es wird noch als Alternative zur Behandlung von bakterieller Meningitis (Allergie gegen Beta- Lactam-Antibiotika) und Hirnabszessen genannt. Sonstige antibakterielle Chemotherapeutika Fosfomycin (nfectofos ) ist chemisch mit keinem anderen Antibiotikum verwandt. Daher sind auch keine Kreuzallergien zu erwarten. Fosfomycin verteilt sich ausschließlich im extrazellulären Raum. Es wirkt gegen Staphylokokken sowie einige weitere grampositive und gramnegative Bakterien. Fosfomycin penetriert gut in Knochen und Gelenke sowie in das ZNS, auch bei kaum gestörter Blut-Liquor-Schranke. Fosfomycin ist besonders zur Behandlung von nfektionen durch Staphylokokken einschließlich MRSA und MRSE geeignet. Aufgrund rascher Resistenzentwicklung unter Monotherapie sollte es immer mit einem Breitspektrumpenicillin oder Cephalosporin kombiniert werden. Zu beachten ist, dass mit 1 g Fosfomycin 14,5 mmol Na + zugeführt werden. Metronidazol (Clont u. a.) wirkt auf anaerobe Bakterien einschließlich C. difficile und B. fragilis (und auf Parasiten). Es zeigt eine konzentrationsabhängige Bakterizidie. Gute Gewebegängigkeit einschließlich Liquor und Gehirn. Metronidazol wird metabolisiert und hauptsächlich renal ausgeschieden. Die Halbwertszeit beträgt etwa 7 h. Metronidazol wird meist in Kombination mit anderen Antibiotika eingesetzt. Unerwünschte Wirkungen sind metallischer Geschmack, dunkel verfärbter Urin, Exantheme, Schwindel und Ataxien. Rifampicin (Eremfat, Rifa ) ist gut gewebegängig. Es reichert sich intrazellulär an. Rifampicin wird biliär und renal ausgeschieden. Die Halbwertszeit ist von der Therapiedauer abhängig. Rifampicin wirkt gegen Mycobacterium tuberculosis, M. leprae, atypische Mykobakterien, Staphylokokken, Streptokokken, Enterokokken, Meningokokken, H. influenzae, Chlamydien und Legionellen. Da es bei Rifampicin zu einer schnellen Resistenzentwicklung der Erreger unter der Therapie kommen kann, sollte es nur in Kombination mit anderen antibakteriell wirksamen Medikamenten eingesetzt werden. Zu beachten sind nteraktionen mit anderen hepatisch metabolisierten Pharmaka. So kann es durch Enzyminduktion zu einem raschen Abbau oraler Kontrazeptiva kommen. Rifampicin ist in der Schwangerschaft kontraindiziert; es verfärbt Urin und Kontaktlinsen orange. Fluorchinolone Alle Fluorchinolone verteilen sich extra- und intrazellulär und zeigen eine gute Gewebegängigkeit. Ciprofloxacin wird renal, hepatisch und intestinal ausgeschieden, Levofloxacin wird ausschließlich renal eliminiert. Die Halbwertszeit von Ciprofloxacin beträgt bis 4 h, die von Levofloxacin wird mit 7 bis 8 h angegeben. Die Fluorchinolone weisen eine konzentrationsabhängige Bakterizidie auf. Das Wirkungsspektrum der Fluorchinolone der Gruppe 2 (Ciprofloxacin, Ofloxacin) umfasst in erster Linie gramnegative Bakterien: Enterobacteriaceae, Pseudomonas aeruginosa, H. influenzae, M. catarrhalis und Neisserien. Darüber hinaus sind die Fluorchinolone der Gruppe 2 gut wirksam gegenüber M. pneumoniae, M. hominis, C. pneumoniae, C. trachomatis, Legionellen und U. urealyticum. Streptokokken, Pneumokokken und Enterokokken werden in vitro unzureichend gehemmt. Die Fluorchinolone der Gruppen und 4 zeigen eine verbesserte Aktivität gegen grampositive Kokken, insbesondere Pneumokokken inklusive Penicillin-resistenter Stämme (sog. Atemwegschinolone) und gegen Anaerobier. Zu den häufigsten Nebenwirkungen gehören gastrointestinale Beschwerden, zentralnervöse Störungen, Phototoxizität und Ruptur der Achillessehne. Wegen der bei jungen Hunden unter Belastung beobachteten irreversiblen Knorpelschäden ist in Deutschland außer Ciprofloxacin (für Kinder ab fünf Jahren mit einer Pseudomonas-nfektion bei zystischer Fibrose) kein Chinolon für Kinder und zugelassen. Die irreversiblen Schädigungen der Gelenkknorpel sind jedoch bislang bei Kindern und n bei über Anwendungen, vorwiegend mit Ciprofloxacin mit einer durchschnittlichen Dosierung von 20 bis 0 mg/kg KG/Tag per os und einer durchschnittlichen Dauer von 20 bis 25 Tagen, und mit Pefloxacin, nicht beobachtet worden. Darüber hinaus haben Untersuchungen mit der Magnetresonanz-Tomographie und Sektionsbefunde keine destruktiven Knorpelschädigungen beim Menschen gezeigt. Weiterhin gibt es einige randomisierte Studien mit Ciprofloxacin bei Mukoviszidose, die ebenfalls keinen Hinweis auf irreversible Knorpelschäden ergeben haben. Als Nebenwirkungen sind zwar Arthralgien beobachtet worden, diese waren aber fast immer nach Absetzen der Therapie reversibel, traten nicht häufiger als in der Kontrollgruppe auf und ähnelten nicht den in den Tierversuchen beschriebenen Knorpelschäden. Daher können in Übereinstimmung mit medizinischen Fachgesellschaften Fluorchinolone auch bei Kindern und n im Einzelfall angewendet werden, wenn es für die indizierte Therapie keine Alternative gibt und wenn die Aufklärung wie unter den Bedingungen der klinischen Prüfung geschieht. Von den Fluorchinolonen sollte Ciprofloxacin (Ciprobay ) bevorzugt werden, weil es für Kinder am besten dokumentiert ist und seit einigen Jahren eine Saftzubereitung zur Verfügung steht. ndikationen für die Anwendung von Fluorchinolonen im Kindes- und Jugendalter sind nfektionskrankheiten durch Pseudomonas aeruginosa oder multiresistente gramnegative Bakterien, so vor allem pulmonale Exazerbation bei zystischer Fibrose, komplizierte Harnwegsinfektion (in den USA hierfür zugelassen), schwere akute Exazerbation der chronischen Otitis media, Shunt- nfektionen, Shigellose, Osteomyelitis 1. Jahrgang Heft /
8 Tab.. Empfehlungen zur parenteralen Therapie von nfektionskrankheiten der Atemwege für Kinder und (BL = Beta-Lactamase-nhibitor) Diagnose Häufigste Erreger Mittel der Wahl Alternativen Evidenz Akute Otitis media Akute Sinusitis Mastoiditis S. pneumoniae, H. influenzae, S. aureus, seltener M. catarrhalis, S. pyogenes dentische Erreger, selten P. aeruginosa und schwere Formen von Milzbrand (z. B. Lungenmilzbrand) sowie in Entwicklungsländern auch Salmonellose, Typhus und Prophylaxe der Meningokokken-Meningitis. Kombinationen von Sulfonamiden und Trimethoprim (Co-trimoxazol) Parenterale Sulfonamide haben heute nur noch eine geringe Bedeutung. Der wichtigste Vertreter dieser Gruppe ist Co-trimoxazol, eine Kombination aus Sulfamethoxazol und Trimethoprim. Beide Substanzen verteilen sich extraund intrazellulär, werden teilweise metabolisiert und renal ausgeschieden. Die Halbwertszeiten für Sulfamethoxazol und Trimethoprim betragen 10 bzw. 12 h. Aminopenicillin ± BL, Cefuroximaxetil, Loracarbef, Cefpodoximproxetil, jeweils oral Cefuroxim oder Cefotiam, Operation Co-trimoxazol (Cotrim, Eusaprim ) wirkt gegen verschiedene grampositive und gramnegative Bakterien insbesondere grampositive Kokken (außer A-Streptokokken), Enterobacteriaceae einschließlich Salmonellen und Shigellen, V. cholerae, H. influenzae, M. catarrhalis, B. pertussis, Listerien, Brucellen und Nocardia spp. Die Resistenzzunahme ist jedoch beachtlich waren z. B. in Deutschland 1,7 % der E.-coli-Stämme gegen Co-trimoxazol resistent. Gegen Enterokokken, Mykoplasmen, Chlamydien und Legionellen ist die Kombination unwirksam. Von Bedeutung ist vor allem die Aktivität gegenüber Pneumocystis jiroveci (früher: P. carinii), Stenotrophomonas maltophilia und Burkholderia spp. Co-trimoxazol kann auch einmal eine Alternative in der Ceftriaxon Aminopenicillin-BL, Operation Bemerkungen: Die akute Otitis media und die akute Sinusitis haben eine hohe Selbstheilungsrate. Eine Antibiotika-Therapie ist indiziert bei Kindern in den ersten zwei Lebensjahren, schweren Formen, Komplikationen und Koexistenz einer schweren Grundkrankheit. Amoxicillin ist ggf. hoch zu dosieren (90 mg/kg KG/Tag). Bei Therapieversagen oder schlechter Compliance kann auch im ambulanten Bereich eine Therapie mit Ceftriaxon, einmal 50 mg/kg/tag als Kurzinfusion (oder i. m. ), für Tage versucht werden. Chronische Otitis media Otitis externa diffusa Orbitalphlegmone P. aeruginosa, seltener S. aureus, Proteus spp. P. aeruginosa, seltener Proteus spp., Streptokokken, Staphylokokken S. aureus, S. pneumoniae, H. influenzae, P. aeruginosa, Anaerobier HNO-Arzt! Operation, ggf. Versuch mit Ceftazidim + Tobramycin Lokale antientzündliche Therapie Ceftazidim (+ Clindamycin) oder Cefepim oder Aminopenicillin-BL, ggf. Operation Cefepim + Tobramycin Ceftazidim oder Cefepim + Tobramycin Piperacillin + BL, Carbapenem Bemerkungen: Bei Nachweis von S. aureus Cephalosporin Gruppe 2 oder Aminopenicillin-BL, bei Nachweis von P. aeruginosa Ceftazidim oder Cefepim (+ Tobramycin) Stirnbeinosteomyelitis S. aureus, S. pneumoniae, H. influenzae, P. aeruginosa Ceftazidim (+ Clindamycin), Cefepim, Aminopenicillin-BL, Operation Piperacillin + BL, Carbapenem Bemerkungen: Bei Nachweis von S. aureus Cephalosporin Gruppe 2 oder Aminopenicillin-BL, bei Nachweis von P. aeruginosa Ceftazidim oder Cefepim (+ Tobramycin) Mundbodenphlegmone, schwere Formen der Lymphadenitis colli Epiglottitis Anaerobier, Streptokokken, S. aureus Streptokokken, Staphylokokken, Haemophilus spp.; H. influenzae Typ B (früher am häufigsten) Aminopenicillin-BL Cefuroxim oder Cefotiam + Metronidazol Cefotaxim oder Ceftriaxon Aminopenicillin-BL Behandlung von Keuchhusten, Listeriose und unter Beachtung der lokalen Resistenzraten auch von Shigellose, Typhus und Paratyphus sein. Von den Nebenwirkungen sind vor allem gastrointestinale Beschwerden, toxische epidermale Nekrolyse, Kristallurie, Nephritis, Hepatitis und Blutbildveränderungen zu nennen. ndikationen für eine parenterale Antibiotika- Therapie Die parenterale Gabe von Antibiotika ist im Kindesalter bei mittelschweren bis schweren nfektionskrankheiten und bei fehlender Möglichkeit zu einer oralen Therapie indiziert Jahrgang Heft /2004
9 Tab.. Fortsetzung Diagnose Häufigste Erreger Mittel der Wahl Alternativen Evidenz Pneumonie, ambulant erworbene (stationäre Therapie) Nosokomiale Pneumonie Abszedierende Pneumonie, Pleuropneumonie Aspirationspneumonie ambulant erworbene nosokomiale S. pneumoniae, H. influenzae, M. pneumoniae, Chlamydia spp., selten S. aureus; Viren Die Tabellen bis 10 geben einen Überblick über die Antibiotika-Auswahl zur initialen Therapie der häufigsten bakteriellen nfektionskrankheiten. Die Tabellen sind als orientierende Hilfe für den Arzt gedacht, der nach dem vermuteten Erreger und der lokalen Resistenzsituation entscheiden muss, welches Antibiotikum oder welche Antibiotika- Kombination am besten geeignet ist. nfektionskrankheiten der Atemwege K. pneumoniae u. a. Enterobacteriaceae, S. aureus, P. aeruginosa, seltener S. pneumoniae, H. influenzae, L. pneumophila; Staphylokokken, seltener H. influenzae und P. aeruginosa Aerob wie ambulant erworbene Pneumonie, Peptostreptokokken, Peptokokken, Fusobakterien Aerob wie nosokomiale Pneumonie, Prevotella spp., Bacteroides, Peptostreptokokken, Fusobakterien Staphylokokkenwirksames Cephalosporin oder Aminopenicillin-BL + Makrolid. Sequenztherapie mit Cefuroximaxetil oder Cefpodoximproxetil + Makrolid s. Text Bemerkungen: An Fremdkörperaspiration (Erdnuss, Plastikspielzeug) denken. Pneumonie bei mmundefizienz S. aureus, P. aeruginosa u. a. Pneumonie-Erreger, Opportunisten einschließlich Parasiten, Viren und Pilze Cephalosporin Gruppe 2 oder + Aminoglykosid, Cefepim Makrolid (+ Rifampicin) Cefotiam oder Cefuroxim (+ Aminoglykosid) Aminopenicillin + BL, Cephalosporin Gruppe 2 + Metronidazol Cephalosporin Gruppe oder Cefepim + Metronidazol oder Clindamycin Ceftazidim oder Cefepim + Aminoglykosid (+ Antimykotikum), Co-trimoxazol bei PcP-Verdacht Pneumonie [6] Die Mehrzahl der Kinder mit einer ambulant erworbenen Pneumonie kann heute ambulant behandelt werden. in den ersten sechs Lebensmonaten, schwerkranke Kinder und Kinder mit unzureichender häuslicher Pflege oder fehlender Bereitschaft zur oralen Therapie sind frühzeitig stationär einzuweisen. Bei Patienten mit Abwehrschwäche sollte man, auch wenn das im Kindesalter schwierig ist, einen Erregernachweis anstreben, um gezielt behandeln zu können. Für die initiale Antibiotika-Behandlung der ambulant erworbene Pneumonie haben sich in den letzten Jahrzehnten im Wesentlichen zwei orale Therapieformen bewährt: Entweder beginnt man mit einem Aminopenicillin mit oder ohne Beta-Lactamase-Hemmer oder mit einem Staphylokokken-wirksamen Oralcephalosporin und setzt bei Unwirksamkeit auf ein Makrolid um bzw. kombiniert mit diesem oder man beginnt mit einem Makrolid und setzt die Therapie bei Unwirksamkeit auf eines der zuvor genannten Antibiotika um bzw. kombiniert mit diesem. Wegen der zunehmenden Pneumokokken-Resistenz gegenüber Makroliden muss heutzutage die empirische Monotherapie mit Makroliden in Frage gestellt werden. Darüber hinaus ist an Penicillin-resistente Pneumokokken zu denken, insbesondere nach Aufenthalt im endemischen Ausland. Bei entsprechender ndikation (s. o.) werden die Antibiotika initial parenteral Meropenem oder mipenem, Doxycyclin (ab neun Jahre bei Mykoplasmen- oder Chlamydien-Pneumonie) Carbapenem, Piperacillin + Cephalosporin Gruppe a Doxycyclin (s. Text) Cephalosporin Gruppe oder Cefepim + Clindamycin, Glykopeptid, Meropenem Carbapenem, Piperacillin-Tazobactam (ab 12 Jahre) Carbapenem Ceftazidim oder Cefepim oder Carbapenem + Vancomycin oder Teicoplanin + Antimykotikum; Makrolid, Ciprofloxacin (s. Text) verabfolgt und sobald wie möglich auf eine orale Gabe umgesetzt. Meist ist eine Kombination von Beta-Lactam-Antibiotikum und Makrolid sinnvoll. Die nosokomiale Pneumonie manifestiert sich nach > 48 Stunden Krankenhausaufenthalt oder innerhalb von sieben Tagen nach der Entlassung. Das Erregerspektrum ähnelt in den ersten fünf Tagen des stationären Aufenthalts dem der ambulant erworbenen Pneumonie. Danach sind die in der Tabelle genannten Erreger am häufigsten. Die Behandlung muss sich nach den in der jeweiligen nstitution vorkommenden Erregern und deren Resistenz richten. Kinder mit einer abszedierenden Pneumonie mit und ohne Pleuritis müssen stationär behandelt werden. Die ausgewählten Antibiotika sollten immer gegen Staphylokokken und H. influenzae wirksam sein und bei begründetem Verdacht auch P. aeruginosa einschließen. Die Dauer der Antibiotika-Behandlung ist unterschiedlich. Die Antibiotika sollten so früh wie möglich auf eine orale 1. Jahrgang Heft /
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST. Karlsruhe, im März Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege,
 EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im März 2019 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im März 2019 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
Erregerhäufigkeit bei akuter bakterieller Meningitis
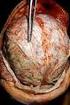 Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST. Karlsruhe, im August Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege,
 EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im August 2018 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
EINSENDERINFORMATION ANTIBIOTIKA-DOSIERUNGEN NACH EUCAST Sehr verehrte Frau Kollegin, sehr geehrter Herr Kollege, Karlsruhe, im August 2018 in den nachfolgenden Tabellen möchten wir Sie über die Antibiotika-Dosierungen
Empirische antibiotische Therapie bei schwerer Sepsis
 MEDIZINISCHE KLINIK TÜBINGEN Empirische antibiotische Therapie bei schwerer Sepsis Infektionsmedizin 2011 Reimer Riessen Internistische Intensivstation Bedeutung einer raschen Antibiotikatherapie Jede
MEDIZINISCHE KLINIK TÜBINGEN Empirische antibiotische Therapie bei schwerer Sepsis Infektionsmedizin 2011 Reimer Riessen Internistische Intensivstation Bedeutung einer raschen Antibiotikatherapie Jede
Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK.
 Antibiotika Dosierungen Stand:Januar 2017 Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK. Penicilline iv Standarddosierung Höhere Dosierung
Antibiotika Dosierungen Stand:Januar 2017 Die folgende Tabelle (empfohlene Antibiotika und Dosierungen; intravenös und oral) richtet sich nach EUCAST und NAK. Penicilline iv Standarddosierung Höhere Dosierung
1 Infektion der Atemwege
 1 Infektion der Atemwege 1.1 Infektexazerbation bei COPD Ca. 50% der Exazerbationen einer COPD werden durch Infektionserreger ausgelöst, überwiegend durch respiratorische Viren. Die häufigsten bakteriellen
1 Infektion der Atemwege 1.1 Infektexazerbation bei COPD Ca. 50% der Exazerbationen einer COPD werden durch Infektionserreger ausgelöst, überwiegend durch respiratorische Viren. Die häufigsten bakteriellen
UNIVERSALINSTRUMENT ANTIBIOTIKUM?
 CAMPUS GROSSHADERN CAMPUS INNENSTADT UNIVERSALINSTRUMENT ANTIBIOTIKUM? Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene 02.04.2014 B. Grabein DIE INSTRUMENTE Daptomycin Aminoglykoside
CAMPUS GROSSHADERN CAMPUS INNENSTADT UNIVERSALINSTRUMENT ANTIBIOTIKUM? Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene 02.04.2014 B. Grabein DIE INSTRUMENTE Daptomycin Aminoglykoside
Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 2016 für Urine
 Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 206 für Urine September 206 Sehr geehrte Kolleginnen und Kollegen, die klinische Leitlinie Unkomplizierte Harnwegsinfektionen
Fachinformation Harnwegsinfektionen Regionale Erreger- und Resistenzstatistik 206 für Urine September 206 Sehr geehrte Kolleginnen und Kollegen, die klinische Leitlinie Unkomplizierte Harnwegsinfektionen
Antibiotikatherapie - Grundlagen
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Antibiotikatherapie - Grundlagen B. Salzberger Hemmung der Zellwandsynthese: Penicilline, Cephalosporine, Glykopeptid-AB, Fosfomycin Proteinsynthese (Translation)
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Antibiotikatherapie - Grundlagen B. Salzberger Hemmung der Zellwandsynthese: Penicilline, Cephalosporine, Glykopeptid-AB, Fosfomycin Proteinsynthese (Translation)
8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen
 8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Amoxicillin Amoxypen j Grampositive (nicht S. aureus) und gramnegative Keime (H. influenzae ca. 10 % Resistenz) * Erwachsene, Kinder 412 Jahre
8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Amoxicillin Amoxypen j Grampositive (nicht S. aureus) und gramnegative Keime (H. influenzae ca. 10 % Resistenz) * Erwachsene, Kinder 412 Jahre
ANTIBIOGRAMME - Interpretationshilfe -
 Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik ANTIBIOGRAMME - Interpretationshilfe - Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik
Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik ANTIBIOGRAMME - Interpretationshilfe - Institut für Medizinische Mikrobiologie und Hygiene Abteilung: Klinische Diagnostik
München. Zentrales Institut des Sanitätsdienstes der Bundeswehr. Rationale Antibiotikatherapie. OFA Bock. Text Stand: xx.xx.xxxx
 Zentrales Institut des Sanitätsdienstes der Bundeswehr München Rationale Antibiotikatherapie OFA Bock Einführung Schön wär`s gewesen wenn Einführung Bakterien sind schneller als die Menschen! Fragen für
Zentrales Institut des Sanitätsdienstes der Bundeswehr München Rationale Antibiotikatherapie OFA Bock Einführung Schön wär`s gewesen wenn Einführung Bakterien sind schneller als die Menschen! Fragen für
Übersicht der getesteten Antibiotika
 Übersicht der getesteten Antibiotika Penicilline (bakteriozid) Schmalspektrum-Penicilline Orale Penicilline (Penicillin V und Propicillin) sind bei Infektionen mit Keimen des "klassischen Penicillin-G-
Übersicht der getesteten Antibiotika Penicilline (bakteriozid) Schmalspektrum-Penicilline Orale Penicilline (Penicillin V und Propicillin) sind bei Infektionen mit Keimen des "klassischen Penicillin-G-
Mikrobiologisches Labor Doz. Möst Erreger- und Resistenzstatistik Harnkulturen
 Harnkulturen Harnproben gesamt: 10869 Erregerspektrum Enterobakterien Escherichia coli 2967 davon ESBL bildend 245 (=8,2%) Klebsiella sp. 380 davon ESBL bildend 12 (=3,2%) Proteus mirabilis 221 Enterobacter
Harnkulturen Harnproben gesamt: 10869 Erregerspektrum Enterobakterien Escherichia coli 2967 davon ESBL bildend 245 (=8,2%) Klebsiella sp. 380 davon ESBL bildend 12 (=3,2%) Proteus mirabilis 221 Enterobacter
Resistenzbericht Manfred Fille
 Resistenzbericht 216 Manfred Fille gefährli hste Erreger ( a h WHO, Februar 217) Kritische Priorität: Acinetobacter baumannii, resistent gegen Carbapeneme Pseudomonas aeruginosa, resistent gegen Carbapeneme
Resistenzbericht 216 Manfred Fille gefährli hste Erreger ( a h WHO, Februar 217) Kritische Priorität: Acinetobacter baumannii, resistent gegen Carbapeneme Pseudomonas aeruginosa, resistent gegen Carbapeneme
Trends und Resistenzeckdaten 2010
 Trends und Resistenzeckdaten 21 21 hat sich die Resistenzsituation weiter verschlechtert. Diese Tatsache ist vor allem auf den Anstieg von gramnegativen Darmbakterien zurückzuführen, die in der Lage sind,
Trends und Resistenzeckdaten 21 21 hat sich die Resistenzsituation weiter verschlechtert. Diese Tatsache ist vor allem auf den Anstieg von gramnegativen Darmbakterien zurückzuführen, die in der Lage sind,
Antibiotikaresistenz und -einsatz in der Humanmedizin
 Europäischer Antibiotikatag Interdisziplinäres Symposium: Antibiotikaeinsatz - Wie wenig ist (noch) zu viel? 9. November 212, BVL, Berlin Antibiotikaresistenz und -einsatz in der Humanmedizin Michael Kresken
Europäischer Antibiotikatag Interdisziplinäres Symposium: Antibiotikaeinsatz - Wie wenig ist (noch) zu viel? 9. November 212, BVL, Berlin Antibiotikaresistenz und -einsatz in der Humanmedizin Michael Kresken
Resistenzsituation im Krankenhausbereich -
 2. estagung der PEG Antibiotikaverbrauch und Resistenz Wo steht Deutschland Resistenzsituation im Krankenhausbereich - Datenquellen, Entwicklung und aktuelle Situation Michael Kresken Antiinfectives Intelligence
2. estagung der PEG Antibiotikaverbrauch und Resistenz Wo steht Deutschland Resistenzsituation im Krankenhausbereich - Datenquellen, Entwicklung und aktuelle Situation Michael Kresken Antiinfectives Intelligence
Bakterielle Entzündung des ZNS Antibiotikawahl nach Erreger bei der akuten eitrigen Meningitis
 Bakterielle Entzündung des ZNS Antibiotikawahl nach Erreger bei der akuten eitrigen Meningitis Meningokokken - Penicillin G - Cefotaxim oder Ceftriaxon Pneumokokken - Penicillin G - Cefotaxim oder Ceftriaxon
Bakterielle Entzündung des ZNS Antibiotikawahl nach Erreger bei der akuten eitrigen Meningitis Meningokokken - Penicillin G - Cefotaxim oder Ceftriaxon Pneumokokken - Penicillin G - Cefotaxim oder Ceftriaxon
ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH
 CAMPUS GROSSHADERN CAMPUS INNENSTADT ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene WANN KOMMT EIN IMPLANTATERHALTUNGSVERSUCH
CAMPUS GROSSHADERN CAMPUS INNENSTADT ANTIBIOTIKATHERAPIE BEI IMPLANTATERHALTUNGSVERSUCH Dr. Béatrice Grabein Stabsstelle Klinische Mikrobiologie und Krankenhaushygiene WANN KOMMT EIN IMPLANTATERHALTUNGSVERSUCH
Antibiotika in der Praxis mit Hygieneratschlägen
 Antibiotika in der Praxis mit Hygieneratschlägen Bearbeitet von Uwe Frank, Franz Daschner 9., vollst. überarb. Aufl. 2010. Taschenbuch. XII, 201 S. Paperback ISBN 978 3 642 10459 6 Weitere Fachgebiete
Antibiotika in der Praxis mit Hygieneratschlägen Bearbeitet von Uwe Frank, Franz Daschner 9., vollst. überarb. Aufl. 2010. Taschenbuch. XII, 201 S. Paperback ISBN 978 3 642 10459 6 Weitere Fachgebiete
Antibiotikaresistenzen in der Humanmedizin
 BVL-Symposium Herausforderungen 24: Tierarzneimittel im Fokus Nutzen, Risiken, Resistenzen 5./6. November 23, Berlin Antibiotikaresistenzen in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
BVL-Symposium Herausforderungen 24: Tierarzneimittel im Fokus Nutzen, Risiken, Resistenzen 5./6. November 23, Berlin Antibiotikaresistenzen in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
9 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Kosten
 9 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Kosten 9 Amikacin Amikacin j Grampositive (Staphylokokken, nicht: Pneumokokken, Streptokokken, Enterokokken), gramnegative Keime, insbesondere
9 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Kosten 9 Amikacin Amikacin j Grampositive (Staphylokokken, nicht: Pneumokokken, Streptokokken, Enterokokken), gramnegative Keime, insbesondere
Tabelle 1.2 Antiinfektiva-Dosierungen (Auswahl)* Gruppe Appl. Patient Dosis in 24 Std. ED max. 1. Penicilline
 Allgemeines. Antiinfektiva und Dosierungen Tabelle. Antiinfektiva-Dosierungen (Auswahl)*. Penicilline Penicillin G Mo. hoch Penicillin V Mo. 0, 0, Mio. IE/kg 0, 0, Mio. IE/kg Mio. IE 8 Mio. IE 0, Mio.
Allgemeines. Antiinfektiva und Dosierungen Tabelle. Antiinfektiva-Dosierungen (Auswahl)*. Penicilline Penicillin G Mo. hoch Penicillin V Mo. 0, 0, Mio. IE/kg 0, 0, Mio. IE/kg Mio. IE 8 Mio. IE 0, Mio.
Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang
 WWW.INFEKTIO.DE Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang Register 2016 Heft 1 Heft 2 Heft 3 Heft 4 Heft 5 Heft 6 Seiten 1-10 Seiten 11-20 Seiten 21-30 Seiten
WWW.INFEKTIO.DE Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 37. Jahrgang Register 2016 Heft 1 Heft 2 Heft 3 Heft 4 Heft 5 Heft 6 Seiten 1-10 Seiten 11-20 Seiten 21-30 Seiten
Mikrobiologisches Labor Doz. Möst Erreger- und Resistenzstatistik Harnkulturen. Erregerspektrum
 Harnkulturen Harnproben gesamt: 13117 Erregerspektrum Enterobakterien Escherichia coli 3718 davon ESBL bildend 281 (=8,1%) Klebsiella sp. 3 davon ESBL bildend 10 (=2,2%) Proteus mirabilis 290 Enterobacter
Harnkulturen Harnproben gesamt: 13117 Erregerspektrum Enterobakterien Escherichia coli 3718 davon ESBL bildend 281 (=8,1%) Klebsiella sp. 3 davon ESBL bildend 10 (=2,2%) Proteus mirabilis 290 Enterobacter
Therapeutische Optionen bei Multiresistenten Erregern. OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel
 Therapeutische Optionen bei Multiresistenten Erregern OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel Themen Multiresistente Erreger MRSA MRGN VRE Therapeutische Optionen MRE-Netzwerk
Therapeutische Optionen bei Multiresistenten Erregern OA Dr. Michael Siemann Zentrallabor Städtisches Krankenhaus Kiel Themen Multiresistente Erreger MRSA MRGN VRE Therapeutische Optionen MRE-Netzwerk
Häufige Infektionen im Erwachsenalter: Diagnostik & DD
 Häufige Infektionen im Erwachsenalter: Diagnostik & DD Dr. Boris Ehrenstein Infektiologie / Rheumatologie Klinik und Poliklinik für Innere Medizin I Häufige ambulant erworbene Infektionen Sinusitis, Otitis
Häufige Infektionen im Erwachsenalter: Diagnostik & DD Dr. Boris Ehrenstein Infektiologie / Rheumatologie Klinik und Poliklinik für Innere Medizin I Häufige ambulant erworbene Infektionen Sinusitis, Otitis
Bedeutung von Kreuzresistenz und Mehrfachresistenz bei bakteriellen Erregern für die Initialtherapie Michael Kresken. 21./22. März 2016, Königswinter
 Bad Honnef-Symposium 2016 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Empfehlungen zur kalkulierten Initialtherapie bakterieller Erkrankungen bei Erwachsenen 21./22. März 2016, Königswinter Bedeutung
Bad Honnef-Symposium 2016 Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Empfehlungen zur kalkulierten Initialtherapie bakterieller Erkrankungen bei Erwachsenen 21./22. März 2016, Königswinter Bedeutung
RESISTENZANALYSE Atemwegsinfekte
 RESISTENZANALYSE Atemwegsinfekte NEU - aktuelle Daten aus 2016 Die Daten geben einen Überblick der ausgebildeten Resistenzen bei den am häufigsten aufgetretenen Keimen Nur ambulante Patienten Antibiotika
RESISTENZANALYSE Atemwegsinfekte NEU - aktuelle Daten aus 2016 Die Daten geben einen Überblick der ausgebildeten Resistenzen bei den am häufigsten aufgetretenen Keimen Nur ambulante Patienten Antibiotika
Harnkulturen. Resistenzraten von E.coli in Harnkulturen (n=3797)
 Harnkulturen Harnproben gesamt: 439 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 3797 davon ESBL bildend 239 (=6,3%) Klebsiella sp. 42 davon ESBL bildend 9 (=4,6%) Proteus mirabilis
Harnkulturen Harnproben gesamt: 439 Erregerspektrum (nur Erstisolate) Enterobakterien Escherichia coli 3797 davon ESBL bildend 239 (=6,3%) Klebsiella sp. 42 davon ESBL bildend 9 (=4,6%) Proteus mirabilis
Therapie von Infektionen beim alten Menschen
 Bad Honnef-Symposium 2011 Therapie von Infektionen beim alten Menschen 18./19. April 2011, Königswinter Resistenzsituation bei Harnwegsisolaten von älteren Patienten Ergebnisse aus der Resistenzstudie
Bad Honnef-Symposium 2011 Therapie von Infektionen beim alten Menschen 18./19. April 2011, Königswinter Resistenzsituation bei Harnwegsisolaten von älteren Patienten Ergebnisse aus der Resistenzstudie
Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion?
 Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion? Katja de With Medizinische Universitätsklinik Freiburg Entwicklung antibiotikaresistenter
Dosierung parenteraler ß-Laktame: Welche klinischen Vorteile bieten höhere Dosen und die kontinuierliche Infusion? Katja de With Medizinische Universitätsklinik Freiburg Entwicklung antibiotikaresistenter
Highlights der PEG- Resistenzstudie 2007
 Jahrestagung der PEG Sektion Grundlagen Bonn, 1. Oktober 28 Highlights der PEG- Resistenzstudie 27 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation,
Jahrestagung der PEG Sektion Grundlagen Bonn, 1. Oktober 28 Highlights der PEG- Resistenzstudie 27 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation,
Thrombozytenaggregationshemmer. Allergie Antikoagulanzien, Gonokokken/Anaerobier
 08 Kapitel Infektiologie.3 Tabellarische Übersicht der wichtigsten in der Urologie verwendeten Antibiotika W. Vahlensieck Penicilline Benzylpenicilline Allergie Antikoagulanzien, Thrombozytenaggregationshemmer
08 Kapitel Infektiologie.3 Tabellarische Übersicht der wichtigsten in der Urologie verwendeten Antibiotika W. Vahlensieck Penicilline Benzylpenicilline Allergie Antikoagulanzien, Thrombozytenaggregationshemmer
Multiresistente Erreger. Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen?
 Hygiene in der Arztpraxis 3MRGN/4MRGN was ist das nun wieder?? 17.04.2013 Multiresistente Erreger Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen? Multiresistente Erreger Welche sollen
Hygiene in der Arztpraxis 3MRGN/4MRGN was ist das nun wieder?? 17.04.2013 Multiresistente Erreger Welche sollen es denn diesmal sein? Stäbchen? Kokken? Spiralen? Multiresistente Erreger Welche sollen
Dr. med. Stefan Schmitt MVZ Dr. Klein Dr. Schmitt & Kollegen, Kaiserslautern AGIL e.v. Grünstadt
 Passgenauigkeit in der Antibiotikatherapie Aktuelle regionale und bundesweite Daten zur Infektionslage bzw. Resistenzentwicklung als Grundlage einer rationellen Antibiotikatherapie Dr. med. Stefan Schmitt
Passgenauigkeit in der Antibiotikatherapie Aktuelle regionale und bundesweite Daten zur Infektionslage bzw. Resistenzentwicklung als Grundlage einer rationellen Antibiotikatherapie Dr. med. Stefan Schmitt
Geld oder Leben? Antibiotikatherapie im Spannungsfeld zwischen Ökonomie und Resistenz
 Geld oder Leben? Antibiotikatherapie im Spannungsfeld zwischen Ökonomie und Resistenz Wiesbaden (15. April 2007 ) In Deutschland ist laut Prof. Dieter Adam aus München seit 1985 ein deutlicher Anstieg
Geld oder Leben? Antibiotikatherapie im Spannungsfeld zwischen Ökonomie und Resistenz Wiesbaden (15. April 2007 ) In Deutschland ist laut Prof. Dieter Adam aus München seit 1985 ein deutlicher Anstieg
Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika
 Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika Fortbildungsveranstaltung Netzwerk MRE Landkreis Stendal 14.06.2017 Gramnegative Bakterien Enterobakterien* Pseudomonas aeruginosa
Mirkobiologische Diagnostik und Befundung bei MRGN Dr. med. Martin Chwoika Fortbildungsveranstaltung Netzwerk MRE Landkreis Stendal 14.06.2017 Gramnegative Bakterien Enterobakterien* Pseudomonas aeruginosa
Hier ist eine Zusammenstellung der vom RKI ermittelten Daten der Keime, bei denen jeweils mindestes 50 Proben auf Resistenzen getestet wurden.
 Keime und Resistenzen ARS 2011 oder Vorsicht, Antibiotika! Quelle: Robert Koch-Institut: ARS, https://ars.rki.de, Datenstand: 04.01.2012 Zusammenstellung und mehr zum Thema: www.krankenhhasser.de Die Datenbank
Keime und Resistenzen ARS 2011 oder Vorsicht, Antibiotika! Quelle: Robert Koch-Institut: ARS, https://ars.rki.de, Datenstand: 04.01.2012 Zusammenstellung und mehr zum Thema: www.krankenhhasser.de Die Datenbank
Die glorreichen Sieben
 1 von 7 09.02.2012 19:51 Druckansicht: Die glorreichen Sieben Ordnung im Antibiotika-Dschungel bei ambulant erworbenen Infektionen PD Dr. med. Dieter Hassler Was haben der Filmklassiker The Magnificent
1 von 7 09.02.2012 19:51 Druckansicht: Die glorreichen Sieben Ordnung im Antibiotika-Dschungel bei ambulant erworbenen Infektionen PD Dr. med. Dieter Hassler Was haben der Filmklassiker The Magnificent
Resistenzepidemiologie 2015
 Resistenzepidemiologie 215 Arne C. Rodloff Erreger Chirurgie Escherichia coli 386 Staphylococcus aureus 39 Enterococcus faecalis 31 Staphylococcus epidermidis 227 Proteus mirabilis 134 Pseudomonas aeruginosa
Resistenzepidemiologie 215 Arne C. Rodloff Erreger Chirurgie Escherichia coli 386 Staphylococcus aureus 39 Enterococcus faecalis 31 Staphylococcus epidermidis 227 Proteus mirabilis 134 Pseudomonas aeruginosa
3. Hygienetag Köln 31. Oktober 2012 Multiresistenzen bei Erregern im Krankenhaus und in Lebensmitteln
 3. Hygienetag Köln 31. Oktober 2012 Multiresistenzen bei Erregern im Krankenhaus und in Lebensmitteln Multiresistente Erreger (MRE) bei Kindern Michael Weiß, Reinhold Cremer, Frauke Mattner Klinik für
3. Hygienetag Köln 31. Oktober 2012 Multiresistenzen bei Erregern im Krankenhaus und in Lebensmitteln Multiresistente Erreger (MRE) bei Kindern Michael Weiß, Reinhold Cremer, Frauke Mattner Klinik für
Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I
 Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I Risikostratifizierung in der Praxis Definition individuelles Therapieziel Klinische Evaluation,
Was gibt es neues in der Therapie der Pneumonie? M. Kolditz Universitätsklinikum Dresden Medizinische Klinik I Risikostratifizierung in der Praxis Definition individuelles Therapieziel Klinische Evaluation,
Situation im Antibiotikaverbrauch und Erregerresistenz in der Humanmedizin
 Interdisziplinäres Symposium Antibiotikaresistenz Vom Wissen zum Handeln 19. / 20. September 2012 - Erlangen Situation im Antibiotikaverbrauch und Erregerresistenz in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
Interdisziplinäres Symposium Antibiotikaresistenz Vom Wissen zum Handeln 19. / 20. September 2012 - Erlangen Situation im Antibiotikaverbrauch und Erregerresistenz in der Humanmedizin Michael Kresken Paul-Ehrlich-Gesellschaft
Kurstag 5. -Infektionen mit gramnegativen Erregern. -Therapie. -Auswertung der letzten Stunde. -Differenzierung gramnegativer Erreger
 Kurstag 5 -Infektionen mit gramnegativen Erregern -Therapie -Auswertung der letzten Stunde -Differenzierung gramnegativer Erreger Antibiotika-Seminar Freitag: Vorbesprechung Praktischer Teil Dienstag:
Kurstag 5 -Infektionen mit gramnegativen Erregern -Therapie -Auswertung der letzten Stunde -Differenzierung gramnegativer Erreger Antibiotika-Seminar Freitag: Vorbesprechung Praktischer Teil Dienstag:
Übersicht Antibiotika
 Übersicht Antibiotika Seit Alexander Flemming 1928 das Penicillin erfand, sind im Laufe der Jahre immer mehr Antibiotika hinzugekommen. Um dennoch den Überblick zu bewahren findet ihr hier die indizierten
Übersicht Antibiotika Seit Alexander Flemming 1928 das Penicillin erfand, sind im Laufe der Jahre immer mehr Antibiotika hinzugekommen. Um dennoch den Überblick zu bewahren findet ihr hier die indizierten
Antibiotikatherapie im Kassenärztlichen Notdienst. Dr. Bettina Tiemer Laborärztliche Gemeinschaftspraxis www. mrsaplus.
 Antibiotikatherapie im Kassenärztlichen Notdienst Dr. Bettina Tiemer Laborärztliche Gemeinschaftspraxis www.labor-luebeck.de www. mrsaplus.de MRSAplus 10. Fallkonferenz 16.09.2015 85-90% der Antibiotika-Verordnungen
Antibiotikatherapie im Kassenärztlichen Notdienst Dr. Bettina Tiemer Laborärztliche Gemeinschaftspraxis www.labor-luebeck.de www. mrsaplus.de MRSAplus 10. Fallkonferenz 16.09.2015 85-90% der Antibiotika-Verordnungen
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER
 Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
Einführung in die Mikrobiologie DR. KAREN-ANJA MODER Inhalt Allgemeines Übertragung Resistenzen MRE Allgemeines Allgemeine Bakteriologie Bakterien Formen Aufbau Bakterien Prokaryonten Keinen echten, mit
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2018 INHALT
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2018 INHALT
Antibiotika im Krankenhaus
 APOTHEKE ARZNEIMITTELINFORMATION Antibiotika im Krankenhaus Dr. Alexandra Weber, Apotheke Apotheke Klinikum der Universität München Wechselbeziehungen PATIENT ERREGER Resistenz Wirkung ANTIBIOTIKUM 2 1
APOTHEKE ARZNEIMITTELINFORMATION Antibiotika im Krankenhaus Dr. Alexandra Weber, Apotheke Apotheke Klinikum der Universität München Wechselbeziehungen PATIENT ERREGER Resistenz Wirkung ANTIBIOTIKUM 2 1
Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de /
 Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de / mikro@labmed.de) seit April 2003 Akkreditierung (aktuell DIN EN ISO 15189; DACH) 1 1. Problematik multiresistenter
Laboratoriumsmedizin Dortmund Dr.med.Eberhard und Partner Abteilung MIKROBIOLOGIE (www.labmed.de / mikro@labmed.de) seit April 2003 Akkreditierung (aktuell DIN EN ISO 15189; DACH) 1 1. Problematik multiresistenter
LA GRANDE BOUFFE. Wie lange, soll was, womit behandelt werden? Katia Boggian Leitende Ärztin Infektiologie/Spitalhygiene
 LA GRANDE BOUFFE Wie lange, soll was, womit behandelt werden? Katia Boggian Leitende Ärztin Infektiologie/Spitalhygiene Das grosse Buffet: Was gibt s denn Gutes? Womit fangen wir an? Was kleckert mich
LA GRANDE BOUFFE Wie lange, soll was, womit behandelt werden? Katia Boggian Leitende Ärztin Infektiologie/Spitalhygiene Das grosse Buffet: Was gibt s denn Gutes? Womit fangen wir an? Was kleckert mich
SARI http://www.antibiotika-sari.de 1
 Daten zum Verbrauch der teilnehmenden Intensivstationen im Zeitverlauf Antibiotikaverbrauch: n=116 Antimykotikaverbrauch: n=94 Institut für Umweltmedizin und Krankenhaushygiene Breisacher Str. 115 b 7916
Daten zum Verbrauch der teilnehmenden Intensivstationen im Zeitverlauf Antibiotikaverbrauch: n=116 Antimykotikaverbrauch: n=94 Institut für Umweltmedizin und Krankenhaushygiene Breisacher Str. 115 b 7916
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim
 MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
MRSA, ESBL und mehr ProblemKeime (und Niere) J.Mattes 5.Mai 2012 Rosenheim The Epidemic of Antibiotic-Resistant Infections: A Call to Action for the Medical Community from the Infectious Diseases Society
Inhaltsverzeichnis VII
 Inhaltsverzeichnis 1 Infektion... 3 1.1 Ablauf einer Infektion: Übertragung, Pathogenese...3 1.1.1 Übertragung...5 1.1.2 Kolonisation...7 1.1.3 Invasion...7 1.1.4 Etablierung... 9 1.1.5 Schädigung...11
Inhaltsverzeichnis 1 Infektion... 3 1.1 Ablauf einer Infektion: Übertragung, Pathogenese...3 1.1.1 Übertragung...5 1.1.2 Kolonisation...7 1.1.3 Invasion...7 1.1.4 Etablierung... 9 1.1.5 Schädigung...11
Antibiotkatherapie in der Intensivmedizin.qxd :39 Sei
 V Vorwort Die Diagnostik und die Therapie von Infektionen in der Intensivmedizin stellen nach wie vor eine besondere Herausforderung dar. Die frühzeitige und adäquate Therapie ist für das Überleben kritisch
V Vorwort Die Diagnostik und die Therapie von Infektionen in der Intensivmedizin stellen nach wie vor eine besondere Herausforderung dar. Die frühzeitige und adäquate Therapie ist für das Überleben kritisch
Antibiotikaverbrauch in der Arztpraxis in Hessen
 Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Antibiotikaresistenzen vermeiden Antibiotikaverbrauch in der Arztpraxis in Hessen 2008-2015 Dr. med. Harald Herholz, MPH Kassenärztliche Vereinigung
Weniger ist mehr Antibiotika verantwortungsvoll einsetzen Antibiotikaresistenzen vermeiden Antibiotikaverbrauch in der Arztpraxis in Hessen 2008-2015 Dr. med. Harald Herholz, MPH Kassenärztliche Vereinigung
Antibiotikaverbrauch im ambulanten Versorgungsbereich. Königswinter, / 1
 Antibiotikaverbrauch im ambulanten Versorgungsbereich Königswinter, 14.4.14 / 1 Verordnungsdichte im ambulanten Bereich, 2006-2011 (in DDD pro 1.000 Versicherte und Tag) Königswinter, 14.4.14 / 2 Antibiotika-Verordnungsdichten
Antibiotikaverbrauch im ambulanten Versorgungsbereich Königswinter, 14.4.14 / 1 Verordnungsdichte im ambulanten Bereich, 2006-2011 (in DDD pro 1.000 Versicherte und Tag) Königswinter, 14.4.14 / 2 Antibiotika-Verordnungsdichten
Modul 3: Rationale Antibiotikatherapie bei Infektionen der unteren Atemwege
 Online-Fragebogen zur Fortbildung Modul 3: Rationale Antibiotikatherapie bei Infektionen der unteren Atemwege Bitte bearbeiten Sie die folgenden Multiple-Choice-Fragen. Beachten Sie, dass pro Frage nur
Online-Fragebogen zur Fortbildung Modul 3: Rationale Antibiotikatherapie bei Infektionen der unteren Atemwege Bitte bearbeiten Sie die folgenden Multiple-Choice-Fragen. Beachten Sie, dass pro Frage nur
Situation AB-Verbrauch & Erreger- Resistenz in der Humanmedizin
 Symposium I: Antibiotikaverbrauch und -resistenz Symposium der Initiative GERMAP Situation AB-Verbrauch & Erreger- Resistenz in der Humanmedizin Michael Kresken Antiinfectives Intelligence GmbH Campus
Symposium I: Antibiotikaverbrauch und -resistenz Symposium der Initiative GERMAP Situation AB-Verbrauch & Erreger- Resistenz in der Humanmedizin Michael Kresken Antiinfectives Intelligence GmbH Campus
S3-Leitlinie. Kurzfassung. 1. Auflage. S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG.
 S3-Leitlinie Kurzfassung 1. Auflage S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Thieme 2005 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 133711 5 Inhaltsverzeichnis:
S3-Leitlinie Kurzfassung 1. Auflage S3-Leitlinie schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Thieme 2005 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 133711 5 Inhaltsverzeichnis:
Evidenzbasierte Antibiotikatherapie
 Evidenzbasierte Antibiotikatherapie EbM-Guidelines für Allgemeinmedizin 2014 Artikel ID: ebd00023 (001.016) 2011 Duodecim Medical Publications Ltd Tonsillitis (Streptokokken) 1. Penicillin V (nicht verfügbar)
Evidenzbasierte Antibiotikatherapie EbM-Guidelines für Allgemeinmedizin 2014 Artikel ID: ebd00023 (001.016) 2011 Duodecim Medical Publications Ltd Tonsillitis (Streptokokken) 1. Penicillin V (nicht verfügbar)
Antibiotikaverbrauch und Resistenzsituation in der ambulanten Versorgung
 Infektiologie Update 2012 23. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Symposium V: Infektionen in der Primärversorgung 13. Oktober 2012, Dresden Antibiotikaverbrauch und Resistenzsituation
Infektiologie Update 2012 23. Jahrestagung der Paul-Ehrlich-Gesellschaft für Chemotherapie e. V. Symposium V: Infektionen in der Primärversorgung 13. Oktober 2012, Dresden Antibiotikaverbrauch und Resistenzsituation
Multiresistenz Erfahrungen aus der PEG-Studie
 Multiresistenz Erfahrungen aus der PEG-Studie Bad Honnef- Symposium 2001 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation, Bonn Bad Honnef
Multiresistenz Erfahrungen aus der PEG-Studie Bad Honnef- Symposium 2001 Michael Kresken Antiinfectives Intelligence Gesellschaft für klinisch-mikrobiologische Forschung und Kommunikation, Bonn Bad Honnef
Nationales Referenzzentrum für gramnegative Krankenhauserreger. MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke
 Nationales Referenzzentrum für gramnegative Krankenhauserreger MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke Was sind die Konsequenzen von Resistenz? Antibiotika gegen E. coli Ampicillin/Amoxicillin
Nationales Referenzzentrum für gramnegative Krankenhauserreger MRGN-Klassifikation und Meldepflicht: Hinweise und Fallstricke Was sind die Konsequenzen von Resistenz? Antibiotika gegen E. coli Ampicillin/Amoxicillin
Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie Außenstelle Großhadern. Béatrice Grabein
 Antibiotika als Tranquilizer und Antipyretika Der sinnvolle Einsatz von Antibiotika bei Knochen-, Gelenk- und Weichteilinfektionen Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und
Antibiotika als Tranquilizer und Antipyretika Der sinnvolle Einsatz von Antibiotika bei Knochen-, Gelenk- und Weichteilinfektionen Dr. med. Béatrice Grabein Max von Pettenkofer-Institut für Hygiene und
Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf
 Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf - Effekte eines intensivierten MRSA screenings- J.Mattes 14 November 2012 Mühldorf The Epidemic of Antibiotic-Resistant Infections: A Call
Regionale Resistenzsituation am Beispiel der Kreisklinik Mühldorf - Effekte eines intensivierten MRSA screenings- J.Mattes 14 November 2012 Mühldorf The Epidemic of Antibiotic-Resistant Infections: A Call
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger. Prof. Dr. C. Wendt
 ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
ESBL heißt jetzt MRGN Neues über multiresistente gramnegative Erreger Prof. Dr. C. Wendt Weitere Co-Resistenzen E. coli ESBL+ / Chin-S E. coli ESBL+ / Chin-R Klebsiella spp. ESBL+ / Chin-S Klebsiella spp.
Umsetzung vorgezogene Regelung /5
 Hinweise zur Umsetzung der auf 2019 vorgezogenen Regelung zur Mitteilung des S nur gültig bei hoher Dosis als I, sensibel bei erhöhter Exposition NAK, 14.12.2018 Die Stellungnahme des NAK vom 26.10.2018
Hinweise zur Umsetzung der auf 2019 vorgezogenen Regelung zur Mitteilung des S nur gültig bei hoher Dosis als I, sensibel bei erhöhter Exposition NAK, 14.12.2018 Die Stellungnahme des NAK vom 26.10.2018
Update antimikrobielle Therapie
 Update antimikrobielle Therapie Klinische Abteilung für Infektionen und Tropenmedizin Universitätsklinik für Innere Medizin 1 Bad Bugs No Drugs E Enterococcus faecium S Staphylococcus aureus C Clostridium
Update antimikrobielle Therapie Klinische Abteilung für Infektionen und Tropenmedizin Universitätsklinik für Innere Medizin 1 Bad Bugs No Drugs E Enterococcus faecium S Staphylococcus aureus C Clostridium
Der Weg von CLSI zu EUCAST
 Der Weg von CLSI zu EUCAST Michael Lefmann, 25.03.2013 Von CLSI zu EUCAST Resistenztestung Entscheidung für EUCAST Implementierung Resistenzstatistik 1 Der wahre Breakpoint??? Kahlmeter et al. JAC2003(52):145-8
Der Weg von CLSI zu EUCAST Michael Lefmann, 25.03.2013 Von CLSI zu EUCAST Resistenztestung Entscheidung für EUCAST Implementierung Resistenzstatistik 1 Der wahre Breakpoint??? Kahlmeter et al. JAC2003(52):145-8
10 Antibiotikatherapie der wichtigsten Infektionen bei Kindern und Erwachsenen
 10 Antibiotikatherapie der wichtigsten Infektionen bei Kindern und Erwachsenen Im Folgenden werden Antibiotikadosierungen nur angegeben, wenn sie von den Dosierungsempfehlungen in Kap. 9 abweichen. 10
10 Antibiotikatherapie der wichtigsten Infektionen bei Kindern und Erwachsenen Im Folgenden werden Antibiotikadosierungen nur angegeben, wenn sie von den Dosierungsempfehlungen in Kap. 9 abweichen. 10
F. Daschner U. Frank Antibiotika am Krankenbett. Unter Mitarbeit von W. Ebner
 F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner 13., vollständig überarbeitete Auflage Professor
F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner 13., vollständig überarbeitete Auflage Professor
Hygiene in der Arztpraxis
 Hygiene in der Arztpraxis 3MRGN/4MRGN Gefahr durch multiresistente Erreger? 22.04.2015 Multiresistente Erreger Welche sollen es denn diesmal sein? MRGN = Multiresistente Gramnegative Stäbchen Stäbchen?
Hygiene in der Arztpraxis 3MRGN/4MRGN Gefahr durch multiresistente Erreger? 22.04.2015 Multiresistente Erreger Welche sollen es denn diesmal sein? MRGN = Multiresistente Gramnegative Stäbchen Stäbchen?
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2017 INHALT
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA-EMPFINDLICHKEIT HÄUFIGER BAKTERIELLER ERREGER JAHRESBERICHT 2017 INHALT
Prävention der Ausbreitung von multiresistenten gramnegativen
 Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Prävention der Ausbreitung von multiresistenten gramnegativen Erregern (MRGNE) Internetversion ohne Photos
Landesamt für Gesundheit und Soziales Abteilung Gesundheit Krankenhaushygiene, Allgemeine Hygiene Prävention der Ausbreitung von multiresistenten gramnegativen Erregern (MRGNE) Internetversion ohne Photos
Verzeichnis der Abbildungen und Tabellen
 Verzeichnis der Abbildungen und Tabellen Abbildungen Seite 1 Infektionswege..................... 2 Infektionen und Erreger in Abhangigkeit von der Beatmungsdauer................ 3 Wirkungsspektrum von
Verzeichnis der Abbildungen und Tabellen Abbildungen Seite 1 Infektionswege..................... 2 Infektionen und Erreger in Abhangigkeit von der Beatmungsdauer................ 3 Wirkungsspektrum von
NEUE ANTIINFEKTIVA. Martin J. Hug Apotheke des Universitätsklinikums Freiburg
 NEUE ANTIINFEKTIVA Martin J. Hug Apotheke des Universitätsklinikums Freiburg Antiinfektivaentwicklung und Resistenzbildung PDR Acinetobacter u. Pseudomonas Ceftriaxon-R N. gonorrhoeae Ceftarolin-R Staphylococcus
NEUE ANTIINFEKTIVA Martin J. Hug Apotheke des Universitätsklinikums Freiburg Antiinfektivaentwicklung und Resistenzbildung PDR Acinetobacter u. Pseudomonas Ceftriaxon-R N. gonorrhoeae Ceftarolin-R Staphylococcus
Zwischenbericht zur ESPED Studie. Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern
 Zwischenbericht zur ESPED Studie Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern Einleitung: Bei Routineabstrichen werden gelegentlich multiresistente bakterielle Infektionserreger
Zwischenbericht zur ESPED Studie Invasive Infektionen durch multiresistente Erreger (MRE) bei Kindern Einleitung: Bei Routineabstrichen werden gelegentlich multiresistente bakterielle Infektionserreger
F. Daschner U. Frank Antibiotika am Krankenbett. Unter Mitarbeit von W. Ebner
 F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner 13., vollständig überarbeitete Auflage Professor
F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner F. Daschner U. Frank Antibiotika am Krankenbett Unter Mitarbeit von W. Ebner 13., vollständig überarbeitete Auflage Professor
Inhaltsverzeichnis. Antibiotika inklusive Antituberkulotika und Antimykotika
 VII Inhaltsverzeichnis Vorwort zur 4. Auflage... Vorwort zur 3. Auflage... Autorenverzeichnis... Abkürzungsverzeichnis... V VI XV XVI TEIL A Grundlagen 1 Definitionen... 3 2 Pharmakokinetik... 8 2.1 Resorption...
VII Inhaltsverzeichnis Vorwort zur 4. Auflage... Vorwort zur 3. Auflage... Autorenverzeichnis... Abkürzungsverzeichnis... V VI XV XVI TEIL A Grundlagen 1 Definitionen... 3 2 Pharmakokinetik... 8 2.1 Resorption...
Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik
 Workshop Wundzentrum Hamburg 20. August 2010 Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik Dr. J. Ungeheuer Tel.: 040-76696-103 www.labor-froreich.de
Workshop Wundzentrum Hamburg 20. August 2010 Antibiotikatherapie bei Wundinfektionen in der ambulanten Medizin - Probeentnahme/Abstrichtechnik Dr. J. Ungeheuer Tel.: 040-76696-103 www.labor-froreich.de
Antibiotika-Verbrauch und Antibiotika- Resistenzsituation in der Humanmedizin
 Europäischer Antibiotikatag, 18. November 2011 Paul Ehrlich gratuliert Gerhard Domagk 75 Jahre antibakterielle Therapie quo vadis Antibiotika? Brennpunkt Resistente Escherichia coli Antibiotika-Verbrauch
Europäischer Antibiotikatag, 18. November 2011 Paul Ehrlich gratuliert Gerhard Domagk 75 Jahre antibakterielle Therapie quo vadis Antibiotika? Brennpunkt Resistente Escherichia coli Antibiotika-Verbrauch
ZEITSCHRIFT FÜR. Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 28. Jahrgang
 WWW.ZCT-BERLIN.DE ZEITSCHRIFT FÜR Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 28. Jahrgang Register 2007 A ACE-Hemmer Acinetobacter baumannii - Carbapenem-Resistenz 47 - Tigecyclin-Resistenz
WWW.ZCT-BERLIN.DE ZEITSCHRIFT FÜR Informationen für Ärzte und Apotheker zur rationalen Infektionstherapie 28. Jahrgang Register 2007 A ACE-Hemmer Acinetobacter baumannii - Carbapenem-Resistenz 47 - Tigecyclin-Resistenz
GERMAP-Ergebnisse: Antibiotikaverbrauch und Resistenzsituation im Humanbereich. Michael Kresken
 GERMAP-Ergebnisse: Antibiotikaverbrauch und Resistenzsituation im Humanbereich Michael Kresken Antiinfectives Intelligence GmbH Campus FH Bonn-Rhein-Sieg, Rheinbach GERMAP Humanbereich / 1 Verbrauch Antibiotikaverbrauch
GERMAP-Ergebnisse: Antibiotikaverbrauch und Resistenzsituation im Humanbereich Michael Kresken Antiinfectives Intelligence GmbH Campus FH Bonn-Rhein-Sieg, Rheinbach GERMAP Humanbereich / 1 Verbrauch Antibiotikaverbrauch
Rationale und rationelle Antibiotika-Therapie
 Rationale und rationelle Antibiotika-Therapie C. Berg Med. Klinik Abt. I = vernünftige nftige und zweckmäß äßige / wirtschaftliche Antibiotika-Therapie Vancomycin Zyvoxid Sobelin Penicilin G Staphylex
Rationale und rationelle Antibiotika-Therapie C. Berg Med. Klinik Abt. I = vernünftige nftige und zweckmäß äßige / wirtschaftliche Antibiotika-Therapie Vancomycin Zyvoxid Sobelin Penicilin G Staphylex
Tabelle 4-01: Absolute und relative Verteilung der Patienten nach Altersklassen
 Die in den XLS-Dateien vorhandene ATB-Streifen-Bezeichnungen sowie die Köpfe der einzelnen Spalten werden, da in der Access-Tabelle nicht gebraucht, verworfen. Um zu gewährleisten, daß keine neuen Streifen,
Die in den XLS-Dateien vorhandene ATB-Streifen-Bezeichnungen sowie die Köpfe der einzelnen Spalten werden, da in der Access-Tabelle nicht gebraucht, verworfen. Um zu gewährleisten, daß keine neuen Streifen,
Antibiotika und Antimykotika
 Antibiotika und Antimykotika.1 Bakteriologie 222.2 Antibiotika 223.3 Antimykotika 248 M. Fresenius, M. Heck, Repetitorium Intensivmedizin, DOI 10.1007/978-3-642-16879-6_, Springer-Verlag Berlin Heidelberg
Antibiotika und Antimykotika.1 Bakteriologie 222.2 Antibiotika 223.3 Antimykotika 248 M. Fresenius, M. Heck, Repetitorium Intensivmedizin, DOI 10.1007/978-3-642-16879-6_, Springer-Verlag Berlin Heidelberg
Dr. Müllner Katalin. Prinzipien der antibiotischen Therapie
 Dr. Müllner Katalin Prinzipien der antibiotischen Therapie Kalkulierte Therapie Bei klinischer Notwendigkeit des Therapiebeginns vor dem Vorliegen der Ergebnisse der Erregerdiagnostik oder des Antibiogramms,
Dr. Müllner Katalin Prinzipien der antibiotischen Therapie Kalkulierte Therapie Bei klinischer Notwendigkeit des Therapiebeginns vor dem Vorliegen der Ergebnisse der Erregerdiagnostik oder des Antibiogramms,
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001
 _Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA RESISTENZBERICHT 2016 INHALT Resistenzstatistik 2016....3 Einleitung....3
_Alle Laboruntersuchungen _Mikrobiologie, Genanalysen _Alle Kassen und Privat _Zertifiziert nach ISO 9001 & ISO 14001 ANTIBIOTIKA RESISTENZBERICHT 2016 INHALT Resistenzstatistik 2016....3 Einleitung....3
2 Arzneimittelgruppen und ihre Wirkungen
 2 Arzneimittelgruppen ihre Wirkungen 21 2.1 Adstringenzien Adstringenzien (Gerbstoffe) fällen Eiweiße aus oder fixieren diese bilden dadurch eine feste oberflächliche Proteinmembran. Sie wirken abdichtend,
2 Arzneimittelgruppen ihre Wirkungen 21 2.1 Adstringenzien Adstringenzien (Gerbstoffe) fällen Eiweiße aus oder fixieren diese bilden dadurch eine feste oberflächliche Proteinmembran. Sie wirken abdichtend,
ESBL und VRE berühmt und berüchtigt. Carola Schönborn Fachkrankenschwester für f r Hygiene, Charité
 ESBL und VRE berühmt und berüchtigt Carola Schönborn Fachkrankenschwester für f r Hygiene, Charité Walk of Fame der MRE ESBL VRE Was ist ESBL? Extended Spectrum ß-Lactamasen Betrifft nur gramnegative Bakterien,
ESBL und VRE berühmt und berüchtigt Carola Schönborn Fachkrankenschwester für f r Hygiene, Charité Walk of Fame der MRE ESBL VRE Was ist ESBL? Extended Spectrum ß-Lactamasen Betrifft nur gramnegative Bakterien,
Antibiotika im perioperativen Setting
 Antibiotika im perioperativen Setting Referent: Dr. Michael Sturm Mikrobiologe, Prüfstellenleiter und allg. beeideter gerichtlich beeideter SV für Hygiene und Mikrobiologie Hygienezentrum Dr. Sturm GmbH
Antibiotika im perioperativen Setting Referent: Dr. Michael Sturm Mikrobiologe, Prüfstellenleiter und allg. beeideter gerichtlich beeideter SV für Hygiene und Mikrobiologie Hygienezentrum Dr. Sturm GmbH
Institut für Qualität im Gesundheitswesen Nordrhein Fortbildungsveranstaltung, Düsseldorf, 13. Mai 2009
 Institut für Qualität im Gesundheitswesen Nordrhein Fortbildungsveranstaltung, Düsseldorf, 13. Mai 2009 Verordnungssicherheit Teil 6: Das Kind ein kleiner Erwachsener? Herausforderung bei der Verschreibung
Institut für Qualität im Gesundheitswesen Nordrhein Fortbildungsveranstaltung, Düsseldorf, 13. Mai 2009 Verordnungssicherheit Teil 6: Das Kind ein kleiner Erwachsener? Herausforderung bei der Verschreibung
Resistenzbericht Dorothea Orth-Höller Sektion für Hygiene und Medizinische Mikrobiologie Medizinische Universität Innsbruck
 Resistenzbericht 2017 Dorothea Orth-Höller Sektion für Hygiene und Medizinische Mikrobiologie Medizinische Universität Innsbruck Inhalt Überblick über Vorkommen von Multiresistenten Keimen in Tirol in
Resistenzbericht 2017 Dorothea Orth-Höller Sektion für Hygiene und Medizinische Mikrobiologie Medizinische Universität Innsbruck Inhalt Überblick über Vorkommen von Multiresistenten Keimen in Tirol in
The Bacteria strike back
 Wintersemester 2008/2009 Spezielle Pharmakologie/Pharmakotherapie Antimikrobielle Chemotherapie Therapie multiresistenter Erreger Barbara Kahl Peter Boknik Eingangsstatement Ständige Zunahme multiresistenter
Wintersemester 2008/2009 Spezielle Pharmakologie/Pharmakotherapie Antimikrobielle Chemotherapie Therapie multiresistenter Erreger Barbara Kahl Peter Boknik Eingangsstatement Ständige Zunahme multiresistenter
Antibiotika im ambulanten Bereich. Verordnungszahlen vor dem Hintergrund von Empfehlungen
 Symposium Antibiotikaresistenz mrsa Netzwerk Land Bremen, 12. September 2012 Antibiotika im ambulanten Bereich Verordnungszahlen vor dem Hintergrund von Empfehlungen Hans Wille Institut für Klinische Pharmakologie
Symposium Antibiotikaresistenz mrsa Netzwerk Land Bremen, 12. September 2012 Antibiotika im ambulanten Bereich Verordnungszahlen vor dem Hintergrund von Empfehlungen Hans Wille Institut für Klinische Pharmakologie
Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie
 Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie Ein Konsensuspapier der Deutschen Gesellschaft für Pneumologie DGP) und der Paul-Ehrlich-Gesellschaft für Chemotherapie PEG) unter Mitarbeit von
Nosokomiale Pneumonie: Prävention, Diagnostik und Therapie Ein Konsensuspapier der Deutschen Gesellschaft für Pneumologie DGP) und der Paul-Ehrlich-Gesellschaft für Chemotherapie PEG) unter Mitarbeit von
Initialtherapie bei HNO-Infektionen
 Initialtherapie bei HNO-Infektionen PD Dr. Bernhard Olzowy Weitere Mitglieder der Arbeitsgruppe: HNO: Prof. Dr. Rainer Müller (Dresden), Dr. Miriam Havel (München) MKG: Prof. Dr. Dr. Bilal Al-Nawas, Dr.
Initialtherapie bei HNO-Infektionen PD Dr. Bernhard Olzowy Weitere Mitglieder der Arbeitsgruppe: HNO: Prof. Dr. Rainer Müller (Dresden), Dr. Miriam Havel (München) MKG: Prof. Dr. Dr. Bilal Al-Nawas, Dr.
