Bilanzierung und Modellierung des BTEX-Austrags aus dem Grundwasser eines Gaswerksgeländes
|
|
|
- Helene Thomas
- vor 7 Jahren
- Abrufe
Transkript
1 Bilanzierung und Modellierung des BTEX-Austrags aus dem Grundwasser eines Gaswerksgeländes Zur Erlangung des akademischen Grades eines Doktors der Naturwissenschaften an der Fakultät für Bio- und Geowissenschaften der Universität Karlsruhe genehmigte DISSERTATION von Dipl.-Chem. Karolin Christiane Weber aus Bochum Karlsruhe 2002 Tag der mündlichen Prüfung: Referent: Prof. Dr. H. Hötzl Korreferenten: Prof. Dr. B. Reichert
2
3 KURZFASSUNG Für die Abschätzung des von einer Untergrundkontamination langfristig ausgehenden Gefährdungspotentials sind neben den schadstoffspezifischen Eigenschaften alle maßgeblichen Transport- und Transformationsprozesse zu berücksichtigen. Während das Verhalten vieler anorganischer und organischer Schadstoffe innerhalb der gesättigten und ungesättigten Zone weitestgehend geklärt ist, sind die naturwissenschaftlichen Grundlagen für den gasförmigen Übergang leichtflüchtiger Substanzen vom Grundwasser über den Kapillarsaum in die ungesättigte Zone noch unvollständig erfaßt. An einem sich selbst überlassenen Altlastenstandort mit gaswerksspezifischen Untergrundkontaminationen wurde anhand der Konzentrationsverteilung von Benzol, Toluol, Ethylbenzol und Xylol (BTEX) im Grundwasser der Hauptschadensherd lokalisiert und die ausgedehnte Kontaminationsfahne räumlich eingegrenzt. Trotz der relativ hohen Volatilität von BTEX und eines angenommenen Mindestalters der Kontamination von 50 Jahren wurden in der Bodenluft im Vergleich zum Grundwasser nur um den Faktor 10 6 geringe Schadstoffkonzentrationen gemessen. Zur Ergründung der Ursache für die im Gelände beobachtete, geringe Volatilisationsrate wurden zunächst Massentransferversuche unter kontrollierten Bedingungen im Labor durchgeführt. Die Experimente ermöglichten eine Charakterisierung der einzelnen Phasenübergänge im System Boden/Bodenluft/Haft-/Grundwasser inklusive ihrer kausalen Abhängigkeiten von unterschiedlichsten Steuerparametern. Ferner zeigte sich, daß, abgesehen von den Transporteigenschaften der betrachteten volatilen Substanz, der luftgefüllte Porenraum, der Wassergehalt sowie die vertikale Wassergehaltsverteilung des Untergrunds den Prozess der Volatilisation am stärksten beeinflussen. Um das im Labor gewonnene Verständnis der maßgeblichen Einzelprozesse auf den Altlastenstandort übertragen zu können, wurde das bereits bestehende, im Rahmen dieser Arbeit weiterentwickelte Computer-Modell YACPIM verwendet. Die Validierung des weiterentwickelten Computer-Modells erfolgte mit Hilfe der im Rahmen der Massentransferversuche gewonnenen Labordaten. Das Computer-Modell eignet sich zur Simulation des durch Advektion und molekularer Diffusion verursachten, horizontalen und vertikalen Transports leichtflüchtiger Substanzen in einem aus beliebig vielen, sich in ihren Transporteigenschaften unterscheidenden horizontalen Schichten aufgebauten Untergrund. Besondere Berücksichtigung gilt dabei dem Stoffübergang von der gesättigten zur ungesättigten Zone. I
4 Die Simulation des Schadstofftransports im Untergrund des Altlastenstandorts ergab, daß der Beitrag der Volatilisation an der Schadstoffabnahme in der sich selbst überlassenen Kontaminationsfahne auf einer Strecke von 50 m unter quasistationären Verhältnissen nur 0,01 % beträgt. Die geringe Volatilisationsrate steht im Einklang mit den in der Bodenluft des Altlastenstandorts gemessenen, niedrigen Schadstoffkonzentrationen und ist dem Modell zufolge auf die geologische Struktur und der daraus resultierenden Wassergehaltsverteilung des Untergrundes zurückzuführen. Im Bereich des Altlastenstandorts schließt sich im Hangenden des Grundwasserleiters eine bis zu 5,7 m mächtige, sandig-schluffige Auelehmschicht an, wodurch es zur Ausbildung eines teilweise über 2 m mächtigen Kapillarsaums kommt. Der mächtige Kapillarsaum erschwert den diffusiven Stofftransport und verringert somit den Stoffaustrag in die Atmosphärenluft. Der Prozess der Volatilisation ist allerdings bei der Betrachtung des Stofftransports im Untergrund nicht in jedem Fall vernachlässigbar. Besonders für sandig/kiesige, durch leichtflüchtige Schadstoffe verunreinigte Untergrunde stellt die Volatilisation einen nicht zu unterschätzenden Dekontaminationspfad da. Simulationen mit dem Computer-Modell YACPIM zeigten, daß der Beitrag der Volatilisation auf einer Strecke von nur m unter quasistationären Verhältnissen je nach Untergrundaufbau für o-xylol, einem semivolatilen Schadstoff, deutlich über 1 % liegen kann. II
5 VORWORT Die vorliegende Dissertation entstand am Lehrstuhl für Angewandte Geologie der Universität Karlsruhe im Rahmen des von der Deutschen Forschungsgemeinschaft geförderten Schwerpunktprogramms Geochemische Prozesse mit Langzeitfolgen im anthropogen beeinflußten Sickerwasser und Grundwasser mit dem Teilschwerpunkt Phasenübergänge beim Transport und Abbau leichtflüchtiger organischer Substanzen. Ohne die Hilfe und Unterstützung meiner Arbeitskollegen, der Projektpartner und zahlreicher Freunde hätte diese Arbeit nie erfolgreich abgeschlossen werden können. Ich möchte mich deshalb an dieser Stelle bei allen für das mir entgegengebrachte Wohlwollen und Vertrauen herzlich bedanken. Meinem Doktorvater Prof. Dr. Heinz Hötzl danke ich für die Vergabe dieser Arbeit, die zahlreichen wertvollen Diskussionen und Anregungen sowie die mir gewährte Freiheit bei der wissenschaftlichen Bearbeitung und Terminierung. Frau Prof. Dr. Barbara Reichert, Geologisches Institut der Universität Bonn, gilt mein besonderer Dank für ihre stete Diskussionsbereitschaft, die fachliche Unterstützung während der Bearbeitung des Themas und die Bereitschaft das Korreferat zu übernehmen. Viele der durchgeführten Untersuchungen fanden in enger Kooperation mit befreundeten Instituten statt. In diesem Zusammenhang möchte ich mich bedanken bei Herrn Dipl.-Phys. Kai Daumiller (Institut für Kernphysik, Forschungszentrum Karlsruhe Technik und Umwelt), Frau Dr. Kathleen McCarthy (U.S. Geological Survey, Portland, OR), Frau Dipl.-Ing. Meike Bücker (Institut für Hydromechanik, Universität Karlsruhe), Herrn Dr. Ulf Mohrlok (Institut für Hydromechanik, Universität Karlsruhe), Herrn Dipl.-Math. Stefan Schläger (Institut für Boden- und Felsmechanik, Universität Karlsruhe), Herrn Dr. Christoph Hübner (Institut für Meterologie und Klimaforschung, Forschungszentrum Karlsruhe Technik und Umwelt), Herrn Dr. Martin Blumenstock (Institut für Ökologische Chemie und Umweltanalytik, Universität München), Herrn Dr. Martin Herfort (Institut für Geowissenschaften, Universität Jena) und Herrn Dr. Wolfgang Schröder (Institut für Elektrotechnik, Technische Universität Hamburg Harburg) Allen Kolleginnen und Kollegen am Lehrstuhl für Angewandte Geologie gebührt ein herzlicher Dank für die jahrelange Unterstützung und das stets sehr gute Arbeitsklima. Hervorheben möchte ich hierbei Frau Daniela Meyer, die im Laufe der hervorragenden Zusammenarbeit zu einer guten Freundin III
6 geworden ist und Herrn Dr. Matthias Eiswirth, der mir zahlreiche Impulse und Denkanstöße gegeben hat. Zur Klärung von Detailfragen wurden im Rahmen der hier vorgestellten Untersuchungen Diplomarbeiten vergeben. Für die zum größten Teil sehr guten Ergebnisse möchte ich mich bedanken bei Herrn Dipl. Geol. Thomas Schneider, Frau Dipl. Geol. Gudrun Jahnel, Herrn Dipl. Geol. Björn Schäfle, Herrn Dipl. Geol. Norbert Brandsch und Herrn Dipl. Geol. Claus Heske. Bedanken möchte ich mich auch bei Frau Gabiele Gregolec und Herrn Dipl. Geol. Claus Heske für die kritische Durchsicht des Manuskriptes. Allen studentischen Hilfskräften, die bei der Durchführung der Gelände- und Laboruntersuchungen mithalfen, sei herzlich gedankt. Ohne den Rückhalt und die Unterstützung meiner Eltern Christel und Helmut Weber sowie meines Freundes Jürgen Schefcsik hätte ich es wohl nicht geschafft, diese Arbeit fertigzustellen. Deshalb gebührt ihnen an dieser Stelle mein ganz besonderer Dank. IV
7 INHALTSVERZEICHNIS KURZFASSUNG...I VORWORT... III INHALTSVERZEICHNIS... V ABBILDUNGSVERZEICHNIS...VII TABELLENVERZEICHNIS...XI SYMBOL- UND ABKÜRZUNGSVERZEICHNIS...XII 1 EINFÜHRUNG UND PROBLEMSTELLUNG Einleitung Zielsetzung THEORETISCHE GRUNDLAGEN DER TRANSPORT- UND ABBAUPROZESSE VON BTEX Transportmechanismen Molekulare Diffusion Advektion Dispersion Phasenübergänge Biotische Umwandlungen STANDORTBESCHREIBUNG Geographische Lage und historischer Überblick Geologie Hydrogeologie METHODIK Geländeuntersuchungen Grundwasser Bodenluft Bodentemperatur Bodenfeuchte Laboruntersuchungen Versuchsrinne Aufbau der Rinnenversuche Rinnenversuch mit Mittelsand Rinnenversuch mit Mittelsand und Lößlehmauflage Numerische Modellierung Modellbeschreibung Modellrechnungen ERGEBNISSE UND DISKUSSION Geländeuntersuchungen V
8 5.1.1 Grundwasser Bodenluft Bodentemperatur Bodenfeuchte Laboruntersuchungen Rinnenversuch mit Mittelsand Rinnenversuch mit Mittelsand und Lößlehmauflage Numerische Modellierung Simulation des Stofftransports im Mittelsand Simulation des Stofftransports im Mittelsand mit Lößlehmauflage Simulation des Stofftransports im Untersuchungsgebiet ZUSAMMENFASSUNG LITERATUR VI
9 ABBILDUNGSVERZEICHNIS Abb. 2.1: Übersicht über die für die BTEX-Ausbreitung im Untergrund relevanten Prozesse Abb. 2.2: Vergleich zwischen gemessenen und berechneten effektiven Diffusionskoeffizienten (JIN & JURY, 1996)... 8 Abb. 2.3: Einfluß der Abstandsgeschwindigkeit auf den dominierenden Transportprozess (PERKINS & JOHNSON 1963) Abb. 2.4: Sequenz der durch Mikroorganismen katalysierten Redoxprozesse in aquatischen Systemen bei ph 7 wobei {CH 2 O} die abbaubare organische Verbindung symbolisiert. Der Pfeilanfang gibt den Bereich des Redoxpotentials an, ab dem die Reaktion auftritt, die Pfeillänge ist ein Maß für die bei der jeweiligen Reaktion freigesetzte Energie (nach STUMM & MORGAN 1981) Abb. 2.5: Idealisierte Verteilung der terminalen Elektronenakzeptor- Prozesse in geringmächtigen, mit organischen Schadstoffen kontaminierten Grundwasserleitern (nach LOVLEY et al. Abb. 2.6: 1994b) Schematische Übersicht des aeroben Abbaus verschiedener Aromaten (AKW, PAK, Phenol) zu Kohlendioxid und Biomasse (nach SCHLEGEL 1985, GOTTSCHALK 1986) Abb. 3.1: Skizze des Untersuchungsgebietes mit Meßstellennetz Abb. 3.2: Geologisches Profil im nördlichen Bereich des Untersuchungsgebietes (HESKE 1998), zur Lage der einzelnen Bohrungen vgl. Abb Abb. 3.3: Grundwassergleichenplan des Neckarkies- Grundwasserleiters, September 1997 (modifiziert nach SCHÄFLE 1997) Abb. 4.1: Schematische Zeichnung der Bodenluft-Probenahme mit dem mobilen Gaschromatographen (HESKE 1998) Abb. 4.2: Schematische Zeichnung des Rinnenversuchsaufbaus Abb. 4.3: Abb. 4.4: Abb. 4.5: Schematische Zeichnung der mit Mittelsand gefüllten Versuchsrinne Fotografische Ansicht des Rinnenversuchsstandes mit TDR- Meßeinrichtung Körnungslinie des Auelehms aus dem Untersuchungsgebiet und des in die Rinne eingebauten Lößlehms aus dem Pfinztal VII
10 Abb. 4.6: Schematische Zeichnung der Versuchsrinne mit Mittelsand und Lößlehmauflage...61 Abb. 4.7: Simulierter Bereich mit den verwendeten Bezeichnungen (Tab. 4.3.) Abb. 4.8: Anpassung der resultierenden Wassergehaltsverteilung nach Van Genuchten an die TDR-Meßwerte zur Ermittlung der Parameter n r, α und n Abb. 4.9: Anpassung der nach Van Genuchten berechneten Wassergehaltsverteilung an die gravimetrisch bestimmten Wassergehalte zur Ermittlung der Van Genuchten Parameter...78 Abb. 4.10: Vergleich der in der Simulation verwendeten und der bei B50 am gemessenen Wassergehaltsverteilung Abb. 5.1: BTEX Konzentrationen und Redoxpotentiale des Grundwassers im Untersuchungsgebiet, Stichtagsmessung August 1997 (REICHERT et al. 1998)...84 Abb. 5.2: Konzentration an gelöstem Eisen und Sulfat im Grundwasser des Untersuchungsgebietes, Stichtagsmessung August 1997 (REICHERT et al. 1998)...85 Abb. 5.3: Konzentrationsverteilung ausgewählter Grundwasserinhaltsstoffe entlang der Transekte B50-B41, Stichtagsmessung August Abb. 5.4: Zonierung des Grundwassers entlang der Transekte B50 B41 1 m unterhalb des Wasserspiegels, Stichtagsmessung August Abb. 5.5: Kornsummenverteilung des Grundwasserleiters im Bereich der Grundwassermeßstelle B56 (nach unveröffentl. Datenmaterial von HERFORT) Abb. 5.6: Stabilitätsfeld der festen und gelösten Eisenspezies als eine Funktion von E H und ph (WEBER et al. 2000). Die eingezeichneten Bereichsgrenzen wurden mit PHREEQE (PARKHURST et al. 1990) auf Basis der Grundwasserzusammensetzung im Zustrom des Abb. 5.7: Schadensherdes (B58) berechnet...90 CO 2 - und O 2 - Konzentrationen in der Bodenluft des Untersuchungsgebietes 1 m unterhalb der Geländeoberkante (Stichtagsmessung August 1997) Abb. 5.8: Konzentrationsverteilung von Benzol, Ethylbenzol, o-, m- und p-xylol entlang der Transekte B50-B53 (Stichtagsbeprobung September 1999)...93 VIII
11 Abb. 5.9: Tiefenabhängiger Konzentrationsverlauf von Benzol, Ethylbenzol, o-, m- und p-xylol in der Bodenluft bzw. im Grundwasser der Meßstelle B59 (Stichtagsbeprobung September 1999) Abb. 5.10: Saisonale Variation der tiefenabhängigen Temperaturverteilung in der ungesättigten Zone der Meßstelle B50 (nach HESKE 1998) Abb. 5.11: Tiefenabhängige Bodenfeuchteverteilungverteilung in der ungesättigten Zone der Meßstelle B50 (nach HESKE 1998) Abb. 5.12: Vergleich der gravimetrisch und mittels TDR-Band bestimmten Wassergehaltsverteilung in der mit Mittelsand gefüllten Versuchsrinne (modifiziert nach SCHLAGER 2001, SCHLAGER et al. 2001) Abb. 5.13: Verteilung der Gesamtkonzentration von o-xylol in der mit Mittelsand gefüllten Rinne am 68. Tag nach Versuchsbeginn Abb. 5.14: Einfluß der täglichen Beregung auf die Wassergehaltsverteilung in der Versuchsrinne Abb. 5.15: Einstellung einer quasistationären Wassergehaltsverteilung in der Versuchsrinne nach zweiwöchiger Beregnung Abb. 5.16: Einfluß der stündlichen Beregung auf die Wassergehaltsverteilung in der Versuchsrinne Abb. 5.17: Batchversuch mit Lößlehm Abb. 5.18: Verteilung der Gesamtkonzentration von o-xylol in der mit Mittelsand und Lößlehm gefüllten Rinne am 70. Tag nach Versuchsbeginn Abb. 5.19: Vergleich zwischen der simulierten und der meßtechnisch bestimmten, vertikalen Schadstoffverteilung am 68. Tag nach Beginn der o-xylol-einleitung Abb. 5.20: Einfluß des Van Genuchten Parameters α auf den sigmoidalen Verlauf des Wassergehaltes Abb. 5.21: Abhängigkeit des effektiven Diffusionskoeffizienten vom Van Genuchten Parameter α Abb. 5.22: Einfluß der Wassergehaltsverteilung auf die stationäre vertikale Verteilung der normierten Simulationsergebnisse Abb. 5.23: Einfluß des K d -Wertes auf die vertikale Verteilung der normierten Simulationsergebnisse am 68. Tag nach Beginn der o-xylol-einleitung Abb. 5.24: Vergleich zwischen der simulierten und der meßtechnisch bestimmten, vertikalen Schadstoffverteilung am 70. Tag nach Beginn der o-xylol-einleitung (WEBER et al. 1999) IX
12 Abb. 5.25: Bilanzierung des Gasaustrags entlang der betrachteten Transekte im Untersuchungsgebiet 275 Jahre nach Beginn der Kontamination X
13 TABELLENVERZEICHNIS Tab. 2.1: Berechnete, freie Diffusionskoeffizienten von BTEX bei 20 C (Gleichung 2.3 bzw. Gleichung 2.4)... 6 Tab. 2.2: Wasserlöslichkeit (S w ) und Octanol/Wasser-Verteilungskoeffizient (K ow ) von BTEX bei 20 C Tab. 2.3: Organischer Kohlenstoff/Wasser-Verteilungskoeffizient (K oc ) von o-xylol bei 20 C für unterschiedliche Untergrundkompartimente im Untersuchungsgebiet (in Anlehnung an HOWARD 1990 und KOPINKE et al. 1995) Tab. 2.4: Für BTEX berechnete Henry-Koeffizienten (H) sowie analytisch bestimmte Dampfdrücke (p o ) bei 20 C Tab. 4.1: Sedimentologische und mineralogische Charakteristik des Einbaumaterials Tab. 4.2: Sedimentologische Charakteristik des Lößlehms und des Auelehms Tab. 4.3: Liste der in der Eingabedatei berücksichtigten Parameter Tab. 4.4: Eingabeparameter für die Simulation des Rinnenversuchs mit Mittelsand (S1-1) Tab. 4.5: Variationen von Eingabedateien zur numerische Modellierung des Stofftransports in einem homogenen System Tab. 4.6: Tab. 4.7: Tab. 5.1: Tab. 5.2: Eingabeparameter für die Simulation des Rinenversuchs mit Mittelsand und Lößlehmauflage (S2) Eingabeparameter für die Simulation des Stofftransportes im Untersuchungsgebiet O-Xylol Verteilung in der mit Mittelsand gefüllten Rinne bei stationärer Wassergehaltsverteilung Trockendichte ρ, totale Porosität n t sowie wasser- und luftgefüllte Porosität n w bzw. n g des in die Rinne eingebauten Mittelsandes Tab. 5.3: O-Xylol Verteilung in der mit Mittelsand gefüllten Rinne bei instationärer Wassergehaltsverteilung Tab. 5.4: O-Xylol Verteilung in der mit Mittelsand und Lößlehm gefüllten Rinne Tab. 5.5: Trockendichte ρ, totale Porosität n t sowie wasser- und luftgefüllte Porosität n w bzw. n g des in die Rinne eingebauten Lößlehms bzw. Mittelsandes Tab. 5.6: Mineralbestand des Lößlehms XI
14 SYMBOL- UND ABKÜRZUNGSVERZEICHNIS a schadstoffspezifische Konstante (> 0) [m 6 mol -1 kg -1 ] α Van Genuchten Parameter zur Beschreibung des sigmoidalen Verlaufs der Wassergehaltsverteilung [m -1 ] α L dynamische Dispersivität in Fließrichtung [m] α T transversale dynamische Dispersivität [m] b schadstoffspezifische Konstante ( 0) [-] C Stoffkonzentration [kg m -3 ] c schadstoffspezifische Konstante (> 0) [m 3 kg -1 ]. dc/dx Konzentrationsgradient [kg m -4 ] C g Konzentration in der Gasphase [kg m -3 ] C ges Gesamtkonzentration [kg m -3 ] C i Sättigungskonzentration der i-ten Komponente im Wasser bei Anwesenheit strukturell ähnlicher Organika [mol l -1 ] C ol Konzentration einer Substanz in n-octanol [kg m -3 ] C s Konzentration in der Bodenmatrix [kg kg -1 ] C sal Salzgehalt des Wassers [mol m -3 ] C t Gesamtkonzentration [kg m -3 ] C w Konzentration in der wäßrigen Phase [kg m -3 ] C sat w Sättigungskonzentration in reinem Wasser [mol m -3 ] C sat w,co Sättigungskonzentration bei Anwesenheit eines Kosolventen [mol l -1 ] C sat w,sal Sättigungskonzentration in mineralisiertem Wasser [mol m -3 ] d mittlerer Korndurchmesser [m] δ Konstriktivität [-] D * effektiver Diffusionskoeffizient [m 2 s -1 ] D * g effektiver Diffusionskoeffizient in der Bodenluft [m 2 s -1 ] D * w effektiver Diffusionskoeffizient in der wäßrigen Phase [m 2 s -1 ] D f freier Diffusionskoeffizient [m 2 s -1 ] D f g freier Diffusionskoeffizient in Luft [m 2 s -1 ] D f w freier aquatischer Diffusionskoeffizient [m 2 s -1 ] D m-l Koeffizient für longitudinale mechanische Dispersion [m 2 s -1 ] D L longitudinaler hydrodynamischer Dispersionskoeffizient [m 2 s -1 ] D T transversaler hydrodynamischer Dispersionskoeffizient [m 2 s -1 ] E H Redox-Spannung [V] ε d diffusionswirksame Porosität [-] F Massenfluß pro Einheitsfläche und Zeiteinheit [kg m -2 s -1 ] f co volumetrischer Anteil des Kosolventen im Wasser [m 3 m -3 ] XII
15 f oc organisch gebundener Kohlenstoffgehalt bezogen auf das Gesamtgewicht der Feststoffmasse [kg kg -1 ] h Höhe über dem freien Wasserspiegel, h > 0 [m] H Henry-Koeffizient [-] H Henry-Konstante [N m -2 ] H s e Exzess-Lösungsenthalpie [kg m 2 s -2 mol -1 ] H T Henry-Koeffizient bei Temperatur T [-] H verd,m molare Verdampfungsenthalpie [kg m 2 s -2 mol -1 ] η w dynamische Viskosität des Wassers [kg m -1 s -1 ] K d Verteilungskoeffizient Boden/Wasser [m 3 kg -1 ] K oc organischer Kohlenstoff/Wasser-Verteilungskoeffizient [m 3 kg -1 ] K sal oc organischer Kohlenstoff/Wasser-Verteilungskoeffizient in salzhaltigem Wasser [m 3 kg -1 ] K ow Octanol/Wasser-Verteilungskoeffizient [-] K s salting-out - bzw. Setschenow-Konstante [m 3 mol -1 ] K sg Verteilungskoeffizient Boden/Gasphase [m 3 kg -1 ] L lineare Fließstrecke [m] M Molmasse [kg mol -1 ] m Van Genuchten Parameter zur Beschreibung der sigmoidalen Wassergehalt - Kapillarspannungskurve [-] M g Molekulargewicht der Luft ( 28, kg mol -1 ) M m Molekulargewicht der diffundierenden Substzanz [kg mol -1 ] n Van Genuchten Parameter zur Beschreibung des sigmoidalen Verlaufs der Wassergehaltsverteilung [-] n e effektive Porosität [-] n g luftgefüllte Porosität [-] n r residualer wassergefüllter Porenanteil [-] n t totale Porosität [-] n w wassergefüllte Porosität [-] p Druck [N m -2 ] Pe Pecletzahl [-] p i Partialdampfdruck der iten Komponente der flüssigen Mischphase [N m -2 ] p o Sättigungsdampfdruck [N m -2 ] p o,t1 Sättigungsdampfdruck bei der Temperatur T1 [N m -2 ] p o,t2 Sättigungsdampfdruck bei der Temperatur T2 [N m -2 ] R allgemeine Gaskonstante [= 8,317 kg m 2 s -2 K -1 mol -1 ] R t Retardierungsfaktor [-] S * relative Erhöhung der Wasserlöslichkeit einer Substanz durch Anwesenheit eines Kosolventen [-] XIII
16 S i Wasserlöslichkeit der i-ten Komponente in ihrer puren Form [mol l -1 ] S w Wasserlöslichkeit [kg m -3 ] S w,t Wasserlöslichkeit bei Temperatur T [kg m -3 ] T Temperatur [K] ρ Trockendichte des Feststoffs [kg m -3 ] dt Zeit [s] T1, T2 Temperatur [K] σ Solubilisierungskonstante [-] v Abstandgeschwindigkeit [m s -1 ] V g Molvolumen der Luft ( 20, m 3 mol -1 ) V m Molvolumen der gelösten diffundierenden Substanz [m 3 mol -1 ] τ Tortuosität [-] dx horizontaler Abstand [m] x i Molenbruch der iten Komponente der flüssigen Mischphase [-] (x i ) org Molenbruch der iten Komponente in der organischen Phase [-] x sat w Sättigungsmolenbruch einer flüssigen organischen Verbindung in der wäßrigen Phase [-] ω Formationsfaktor [-] γ i Aktivitätskoeffizient der iten Komponente innerhalb der flüssigen Mischphase [-] (γ i ) aq Aktivitätskoeffizient der iten Komponente in der wäßrigen Phase in Anwesenheit hydrophilerer organischer Substanzen [-] (γ p i ) aq Aktivitätskoeffizient der iten Komponente in der wäßrigen Phase ohne Anwesenheit weiterer Substanzen [-] (γ i ) org Aktivitätskoeffizient der iten Komponente in der organischen Phase in Anwesenheit hydrophilerer organischer Substanzen [-] z vertikaler Abstand [m] XIV
17 1 Einführung und Problemstellung 1 EINFÜHRUNG UND PROBLEMSTELLUNG 1.1 Einleitung In der Bundesrepublik Deutschland gibt es derzeit rund erfaßte Altlastenverdachtsflächen (BEHLING 2001). Hierzu zählen allein in Baden- Württemberg über 100 ehemalige Gaswerksstandorte (LFU 1990). In diesen ehemaligen Gaswerken wurde hauptsächlich durch Entgasung von Steinkohle Stadtgas gewonnen. Die dabei anfallenden Nebenprodukte Gaswerksteer, verbrauchte Gasreinigermasse, Ammoniakwasser, Kondensate und Waschflüssigkeiten wurden häufig unsachgemäß gelagert und entsorgt, wodurch es zu Kontaminationen des Untergrundes kam. Das Schadstoffspektrum der Kontaminationen umfaßt dabei sowohl anorganische als auch organische umweltrelevante Substanzen. Zu ersteren zählen Schwefel, Sulfide, Thiocyanate, Cyanide, Schwermetalle und Ammoniak. Unter den organischen Verbindungen stellen die leichtflüchtigen aromatischen Kohlenwasserstoffe Benzol, Toluol, Ethylbenzol und Xylol (BTEX) die größte Fraktion dar. In deutlich geringeren Konzentrationen treten polycyclische aromatische Kohlenwasserstoffe (PAK), Phenole und heterocyclische aromatische Kohlenwasserstoffe auf. BTEX zeichnen sich bedingt durch ihre relativ hohe Wasserlöslichkeit gekoppelt mit ihrem verhältnismäßig hohen Dampfdruck durch eine große Mobilität im Untergrund aus. Aufgrund ihrer Mobilität und des mit zwei der Substanzen verbundenen, bekannten Gesundheitsrisikos - Benzol ist ein bewiesenes Cancerogen und Toluol besitzt eine neurotoxische Wirkung (SITTIG 1985) geht von in den Untergrund eingetragenen BTEX ein erhebliches Gefährdungspotential für die Umwelt und den Menschen aus. Diesem erheblichen Gefährdungspotential trägt auch das Bundes-Bodenschutzgesetz (BBodSchG) Rechnung. Nach BBodSchG Anhang 2 Abs. 3 beträgt der Prüfwert zur Beurteilung des Wirkungspfades Boden-Grundwasser für die Summe leichtflüchtiger aromatischer Kohlenwasserstoffe (Benzol, Toluol, Xylole, Ethylbenzol, Styrol, Cumol) 20 µg l -1, für die Einzelsubstanz Benzol wurde der Prüfwert auf 1 µg l -1 festgelegt. Werden diese Prüfwerte im Sickerwasser überschritten, ist nach 8 Abs.1 Satz 2 Nr.1 des Bundes-Bodenschutzgesetzes unter Berücksichtigung der Bodennutzung eine einzelfallbezogene Prüfung durchzuführen und festzustellen ob eine schädliche Bodenveränderung oder Altlast vorliegt. In diesem Regelwerk sind allerdings für leichtflüchtige aromatische Kohlenwasserstoffe bzw. für deren Einzelsubstanzen keine expliziten Konzentrationsangaben enthalten, bei deren Überschreitung entsprechende Maßnahmen ergriffen werden müssen. 1
18 1.2 Zielsetzung 1.2 Zielsetzung Vor dem Hintergrund des von Untergrundkontaminationen potentiell für die Umwelt und den Menschen ausgehenden Gefährdungspotentials und dem großen Defizit in dem für Langzeitprognosen erforderlichem Verständnis der entscheidenden Transport- und Transformationsprozesse wurde 1995 von der Deutschen Forschungsgemeinschaft ein Schwerpunktprogramm Geochemische Prozesse mit Langzeitfolgen im anthropogen beeinflußten Sicker- und Grundwasser ausgeschrieben. Ziel des von der Deutschen Forschungsgemeinschaft von 1996 bis 1999 geförderten Teilschwerpunktes Phasenübergänge beim Transport und Abbau leichtflüchtiger organischer Substanzen war es, die naturwissenschaftlichen Grundlagen für das Verhalten leichtflüchtiger organischer Schadstoffe im Untergrund weiter zu vervollständigen. Im Vordergrund des Interesses stand die Charakterisierung der dominierenden vertikalen Transportmechanismen des Schadstoffübergangs vom Grundwasser über den Kapillarsaum in die ungesättigte Zone und die Umsetzung dieses Prozessverständnisses in ein Computer-Modell. Zur Verfolgung dieser Zielsetzung sollten Untersuchungen sowohl im Gelände als auch im Labor durchgeführt werden. Als Untersuchungsgebiet wurde gemeinsam mit anderen Antragstellern ein ehemaliger Gaswerksstandort in Stuttgart mit einer ausgedehnten BTEX-Abstromfahne gewählt. Die Geländeuntersuchungen sollten Auskunft über die konkrete Belastungssituation geben und der quantitativen Bestimmung der für den BTEX-Transport in und zwischen den Kompartimenten Boden, Bodenluft, Haft- und Grundwasser entscheidenden Parameter dienen. Parallel zu den Geländeuntersuchungen sollten Massentransferversuche unter kontrollierten Randbedingungen im Labor realisiert werden. Ziel der Laborversuche war es, ein umfassendes Verständnis der einzelnen Transportprozesse im System Boden/Bodenluft/Haft-/Grundwasser inklusive ihrer kausalen Abhängigkeiten von unterschiedlichsten Steuerparametern zu gewinnen. Auf dem Verständnis der Einzelprozesse aufbauend sollte eine Modellvorstellung für das Gesamtsystem entwickelt und in ein Computer-Modell umgesetzt werden. Schließlich sollte mit Hilfe des entwickelten Computer-Modells die zeitliche und räumliche Entwicklung der sich selbst überlassenen BTEX-Abstromfahne im Untersuchungsgebiet simuliert und der durch Volatilisation bedingte Schadstoffaustrag entlang der Fahne quantifiziert werden. 2
19 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX 2 THEORETISCHE GRUNDLAGEN DER TRANSPORT- UND ABBAUPROZESSE VON BTEX 2.1 Transportmechanismen Unterschiedlichste physikochemische Prozesse sind für den Transport von BTEX im Untergrund verantwortlich (Abb. 2.1). Die einzelnen Prozesse werden nachfolgend erläutert. Atmosphäre advektivdispersiver Sickerwassertransport Luftdruckschwankungen Infiltration von Niederschlag Diffusion zur Atmosphäre Sorption und Desorption an Bodenmatrix BTEX Grundwasserfließrichtung Lösung im Sickerwasser Lösung im Bodenwasser advektiv-dispersiver Transport Kontaminationsquellen Ausgasung aus dem Bodenwasser Lösung im Grundwasser Sorption und Desorption am Aquifermaterial Ungesättigte Zone Kapillarsaum molekulare Diffusion in Bodenluft und Bodenwasser Volatilisation in die ungesättigte Zone Gesättigte Zone diffusiver Transport im Grundwasser Abb. 2.1: Übersicht über die für die BTEX-Ausbreitung im Untergrund relevanten Prozesse. 3
20 2.1 Transportmechanismen Molekulare Diffusion Die molekulare Diffusion beschreibt den Massentransport durch thermische Eigenbewegung der Atome oder Moleküle (BROWN sche Molekularbewegung) und führt zu einem Konzentrationsausgleich innerhalb eines Fluids. Mathematisch wird der diffusive Massenfluß durch das erste FICK sche Gesetz beschrieben. Die eindimensionale Variante des ersten FICK schen Gesetzes zur Beschreibung von Diffusionsprozessen in Einphasen-Systemen lautet (FICK 1855): ( dc / dx) f F = D (2.1) mit F Massenfluß pro Einheitsfläche und Zeiteinheit [kg m -2 s -1 ], D f freier Diffusionskoeffizient [m 2 s -1 ], C Stoffkonzentration [kg m -3 ], dc/dx Konzentrationsgradient [kg m -4 ]. Für Systeme mit instationärer Konzentrationsverteilung gilt das zweite FICK sche Gesetz. In seiner eindimensionalen Form stellt es sich wie folgt dar (FICK 1855): mit t Zeit [s]. f 2 2 C / t = D C / x (2.2) Der freie Diffusionskoeffizient D f, hängt von den physikochemischen Eigenschaften der diffundierenden Substanz (z.b. Molekulargewicht, Molvolumen) sowie des Mediums in dem die Diffusion stattfindet (z.b. dynamische Viskosität) ab. Der Wert des Diffusionskoeffizienten steigt mit sinkendem Druck, sinkender Dichte und zunehmender Temperatur des betrachteten Systems. So verdoppelt er sich etwa durch eine Temperaturerhöhung von 5 C auf 25 C (ROBINSON & STOKES 1965). Es gibt verschiedenste empirische Methoden zur Ermittlung der freien Diffusionskoeffizienten (LYMAN et al. 1990). Im weiteren Verlauf dieser Arbeit wird für die Berechnung des freien aquatischen Diffusionskoeffizienten D f w, die empirische Gleichung nach HAYDUK & LAUDIE (1974) verwendet: 4
21 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX D f w = 13,26 3 1,14 6 0,589 9 ( η 10 ) ( V 10 ) 10 w mit D f w freier aquatischer Diffusionskoeffizient [m 2 s -1 ], V m Molvolumen der gelösten diffundierenden Substanz [m 3 mol -1 ], η w dynamische Viskosität des Wassers [kg m -1 s -1 ]. m (2.3) Besonders geeignet für die Berechnung des freien Diffusionskoeffizienten von Aromaten in Luft D f g, ist die empirische Gleichung nach FULLER et al. (1966): ( M + M ) 5 1,75 m g 3 1, T 10 M m M f g D = (2.4) g p 100 V m Vg mit D f g freier Diffusionskoeffizient in Luft [m 2 s -1 ], T Temperatur [K], M m Molekulargewicht der diffundierenden Substanz [kg mol -1 ], M g Molekulargewicht der Luft ( 28, kg mol -1 ), p Druck [N m -2 ], V m Molvolumen der diffundierenden Substzanz [m 3 mol -1 ], V g Molvolumen der Luft ( 20, m 3 mol -1 ). In Tab. 2.1 sind die für BTEX nach den oben erläuterten Verfahren berechneten, freien Diffusionskoeffizienten in Wasser und in Luft bei 20 C und unter Atmosphärendruck aufgeführt. Da die beiden Abschätzmethoden nicht isomerenspezifisch sind, gilt der für Xylol angegebene Wert für alle drei Isomere. Wie anhand der Tab. 2.1 ersichtlich wird, ist der freie Diffusionskoeffizient in Luft um den Faktor höher als der im Wasser. 5
22 2.1 Transportmechanismen Tab. 2.1: Berechnete, freie Diffusionskoeffizienten von BTEX bei 20 C (Gleichung 2.3 bzw. Gleichung 2.4). Substanz D f w [m 2 s -1 ] D f g [m 2 s -1 ] Benzol 8, , Toluol 7, , Ethylbenzol 7, , Xylol 7, , In natürlichen porösen Mehrphasen-Systemen wird der Diffusionsprozeß darüberhinaus durch die Geometrieeigenschaften des Porenraums beeinflußt. Aus diesem Grund muß zur Berechnung des diffusiven Stofftransports in porösen Mehrphasen-Systemen der freier Diffusionskoeffizient in Gleichung (2.1) und (2.2) durch den effektiven Diffusionskoeffizienten ersetzt werden. Der effektive Diffusionskoeffizient entspricht dem Produkt aus Formationsfaktor und freiem Diffusionskoeffizienten (BEAR 1972, FRICK 1993): D D * w * g = D = D f w f g ω = D bzw. ω = D f w f g δ ε d 2 τ δ ε d 2 τ mit D * w effektiver Diffusionskoeffizient in der wäßrigen Phase [m 2 s -1 ], D f w freier aquatischer Diffusionskoeffizient [m 2 s -1 ], D * g effektiver Diffusionskoeffizient in der Bodenluft [m 2 s -1 ], D f g freier Diffusionskoeffizient in Luft [m 2 s -1 ], ω Formationsfaktor [-], δ Konstriktivität [-], τ Tortuosität [-], ε d diffusionswirksame Porosität [-]. (2.5) Der Formationsfaktor ist immer kleiner als eins und hängt von der Struktur des porösen Mediums ab. Über die Konstriktivität und Tortuosität berücksichtigt er die Porengeometrie, über die diffusionswirksame Porosität trägt er den dead-end-poren (LEVER et al. 1985) Rechnung. In Dreiphasensystemen wie der ungesättigten Zone wird die durchflußwirksame Porosität durch das Vorhandensein einer zweiten fluiden Phase beeinflußt. Aus diesem Grund muß sie für beide fluiden Phasen getrennt betrachtet werden. 6
23 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX Da Konstriktivität, Tortuosität und diffusionswirksame Porosität als Einzelparameter nicht direkt zu bestimmen sind, werden sie zum dimensionslosen Formationsfaktor zusammengefaßt. Für die Berechnung des Formationsfaktors wurden verschiedene empirische Gleichungen aufgestellt (Abb. 2.2). Die Formel von MILLINGTON & QUIRK (1960) für den Formationsfaktor in der Gasphase lautet: mit ω Formationsfaktor [-], n g luftgefüllte Porosität [-], n t totale Porosität [-] g 2 nt n ω = (2.6) Unter Verwendung dieser Formel wird der effektive Diffusionskoeffizient in der Bodenluft, D * g, allerdings meist unterschätzt (Abb. 2.2). Im Gegensatz hierzu liefert die Gleichung nach PENMAN (1940) (Gleichung (2.7)) in einem weiten Porositätsbereich zu hohe Werte für D g * (Abb. 2.2): ω = 0, 66. (2.7) n g Nach JIN & JURY (1996) ergibt die ebenfalls von MILLINGTON & QUIRK (1960) entwickelte, zweite Gleichung (Gleichung (2.8)) für den Formationsfaktor die beste Übereinstimmung zwischen den gemessenen und berechneten effektiven Diffusionskoeffizienten (Abb. 2.2): n ω =. (2.8) n 2 g 2 3 t Der Formationsfaktor für die wäßrige Phase berechnet sich analog (COLLIN & RASMUSON 1988). Unter Verwendung der zweiten Gleichung von MILLINGTON & QUIRK (1960) gilt für den effektiven Diffusionskoeffizienten in der wäßrigen Phase: 7
24 2.1 Transportmechanismen D * w f n = Dw. (2.9) n mit D * w effektiver Diffusionskoeffizient in der wäßrigen Phase [m 2 s -1 ], D f w freier aquatischer Diffusionskoeffizient [m 2 s -1 ], n w wassergefüllte Porosität [-]. 2 w 2 3 t 0,5 0,4 JIN et al. (1994) PETERSEN et al. (1994) TAYLOR (1949) Gleichung (2.6) Gleichung (2.8) Gleichung (2.7) D * g / D f g 0,3 0,2 SHEARER et al. (1972) XU et al. (1992) KARIMI et al. (1987) 0,1 0,0 0,0 0,1 0,2 0,3 0,4 0,5 Abb. 2.2: Vergleich zwischen gemessenen und berechneten effektiven Diffusionskoeffizienten (JIN & JURY, 1996). Die wassergefüllte Porosität homogener Böden läßt sich nach VAN GENUCHTEN (1980) in Abhängigkeit von der Höhe über dem freien Wasserspiegel berechnen: mit n w = n r + n g n n t r [ 1 + ( α h) ] n m ( ) (2.10) m = 1 1 (2.11) n 8
25 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX mit n w wassergefüllte Porosität [-], n r residualer wassergefüllter Porenanteil [-], n t totale Porosität [-], α Van Genuchten Parameter zur Beschreibung der sigmoidalen Wassergehalt - Kapillarspannungskurve [m -1 ], h Höhe über dem freien Wasserspiegel, h > 0 [m], n Van Genuchten Parameter zur Beschreibung der sigmoidalen Wassergehalt - Kapillarspannungskurve [-], m Van Genuchten Parameter zur Beschreibung der sigmoidalen Wassergehalt - Kapillarspannungskurve [-]. Die luftgefüllte Porosität ergibt sich aus der Differenz zwischen der totalen und der wassergefüllten Porosität. Der diffusive Transportprozess in der ungesättigten Zone setzt sich aus der Diffusion in der Bodenluft und der im Bodenwasser zusammen. Die eindimensionale Transportgleichung für die molekulare Diffusion in der ungesättigten Zone lautet: C t = D z C z + D ges * w * w g C z mit C ges Gesamtkonzentration [kg m -3 ], t Zeit [s], z vertikaler Abstand [m], D * w effektiver Diffusionskoeffizient in der wäßrigen Phase [m 2 s -1 ], C w Konzentration in der wäßrigen Phase [kg m -3 ], D * g effektiver Diffusionskoeffizient in der Bodenluft [m 2 s -1 ], C g Konzentration in der Gasphase [kg m -3 ]. g (2.12) Advektion Advektion beschreibt die Verlagerung von Stoffen mit einem strömenden Fluid. Konvektion wird häufig als Synonym für Advektion verwendet, wobei Konvektion wärmegesteuerte Fluidbewegungen mit einbezieht. Advektiv werden die Stoffe mit der Abstandsgeschwindigkeit des Fluids in Richtung des Strömungsvektors transportiert. Die Strömung resultiert aus dem Ausgleich von Druck-, Dichte- sowie Temperaturunterschieden und umfaßt u.a. Bodenluftströmung aufgrund atmosphärischer Luftdruckschwankungen, gra- 9
26 2.1 Transportmechanismen vimetrisch bedingten Sickerwassertransport sowie Grundwaserströmung aufgrund von Potentialunterschieden. Der eindimensionale advektive Massenfluß läßt sich wie folgt berechnen (FETTER 1999): F = v n C (2.13) mit F Massenfluß pro Einheitsfläche und Zeiteinheit [kg m -2 s -1 ], v Abstandgeschwindigkeit [m s -1 ], n e effektive Porosität [-], C Konzentration [kg m -3 ]. e Für die zeitliche eindimensionale Änderung der Stoffkonzentration aufgrund von Advektion gilt (FETTER 1999): C C = v (2.14) t x mit t dx Zeit [s], horizontaler Abstand (Abstand in Fließrichtung) [m] Dispersion Im Gegensatz zur Diffusion findet die Dispersion nur bei einer Fluidbewegung (Advektion) statt. Anders als bei der Betrachtung der Advektion fließt das Fluid nicht auf geraden Bahnen mit einer bestimmten Abstandsgeschwindigkeit, sondern umströmt auf seinem Weg die Körner des porösen Mediums. Es kommt zu einer Aufweitung des Strömungsprofils, da einige Fluidpartikel für die gleiche Distanz längere Pfade zurück legen als andere. Hinzukommt, daß die Strömungsgeschwindigkeit in der Mitte des Porenkanals am größten ist und zur Kornoberfläche hin bis auf Null abnimmt. Außerdem variiert die Strömungsgeschwindigkeit in Abhängigkeit von der Geometrie der Poren (BEAR 1972). Die aus der unterschiedlichen Geschwindigkeit und Richtung des Fluidstroms resultierende Vermischung wird als mechanische Dispersion bezeichnet. Tritt sie in Fließrichtung auf, wird sie longitudinale Dispersion genannt, senkrecht zur Fließrichtung handelt es sich um die transversale Dispersion. 10
27 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX Analog dem ersten FICK schen Gesetz läßt sich der longitudinale mechanischdispersive Massenfluß in einem homogenen porösen Medium wie folgt berechnen (KLOTZ 1973, BERTSCH 1978): F = Dm L ne ( dc / dx) und Dm L = α L v (2.15) mit D m-l Koeffizient für longitudinale mechanische Dispersion [m 2 s -1 ], α L dynamische longitudinale Dispersivität [m]. Die dynamische Dispersivität oder einfach Dispersivität ist eine Materialeigenschaft des porösen Mediums. Sie hängt von dessen Korngröße, Porösität und Struktur ab. Der Prozeß der molekularen Diffusion und mechanischen Dispersion wird zumeist gemeinsam unter dem Begriff der hydrodynamischen Dispersion betrachtet. Für den longitudinalen bzw. transversalen hydrodynamischen Dispersionskoeffizient gilt: DL = α L v + D = α v T T + mit D L longitudinaler hydrodynamischer Dispersionskoeffizient [m 2 s -1 ], D T transversaler hydrodynamischer Dispersionskoeffizient [m 2 s -1 ], α T transversale dynamische Dispersivität [m], v Abstandgeschwindigkeit [m s -1 ], D * effektiver Diffusionskoeffizient [m 2 s -1 ]. * D * D (2.16) Die mittlere Abstandsgeschwindigkeit sowie der mittlere Korndurchmesser des porösen Mediums bzw. die lineare Fließstrecke bestimmen den Beitrag der einzelnen Transportprozesse zur resultierenden Stoffverfrachtung innerhalb des Systems. Zur zahlenmäßigen Erfassung dieses Sachverhaltes wurde die dimensionslose Pecletzahl eingeführt. Sie berechnet sich wie folgt (FETTER 1999): 11
28 2.1 Transportmechanismen v d Pe = bzw. f D mit Pe Pecletzahl [-], d mittlerer Korndurchmesser [m], D f freier Diffusionskoeffizient [m 2 s -1 ], L lineare Fließstrecke [m]. v L Pe = (2.17) Der dimensionslose Dispersionskoeffizient, der Quotient aus D L und D f bzw. D T und D f, kann als Maß für den jeweiligen Anteil der Advektion, mechanischen Dispersion sowie molekularen Diffusion am gesamten Transportprozess verwendet werden. Der funktionelle Zusammenhang zwischen der Pecletzahl und dem dimensionslosen Dispersionskoeffizienten wurde von PERKINS & JOHNSON (1963) untersucht. Deren Tracerversuche im gesättigten, gleichförmigen Sand ergaben für sehr kleine mittlere Abstandsgeschwindigkeiten von der Pecletzahl unabhängige dimensionslose Dispersionskoeffizienten von 0,7 (Abb. 2.3). Dieser Wert entspricht dem Formationsfaktor ω von gesättigtem, gleichförmigem Sand (McCarthy & Johnson 1995). Der Beitrag der mechanischen Dispersion am resultierendem Stofftransport ist demnach bei sehr kleinen mittleren Abstandsgeschwindigkeiten vernachlässigbar gering (Gleichung 2.16 bzw. 1.5) während der Prozess der molekularen Diffusion dominiert. Die Dominanz der molekularen Diffusion herrscht bei der Betrachtung der longitudinalen hydrodynamischen Dispersion bei Pecletzahlen kleiner 0,02. Gegenüber der transversalen hydrodynamischen Dispersion dominiert die molekulare Diffusion bis Pecletzahlen von 1. In gleichförmigem gesättigtem Sand sind bei Pecletzahlen zwischen 0,4 und 6 die Prozesse der molekularen Diffusion und der longitudinalen mechanischen Dispersion mehr oder weniger gleichwertig. Für die transversale mechanische Dispersion und molekulare Diffusion gilt dies bei Pecletzahlen zwischen 6 und 100. Für jeweils höhere Pecletzahlen kann die molekulare Diffusion vernachlässigt werden, Advektion und Dispersion sind die transportrelevanten Prozesse (Abb. 2.3). D L 12
29 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX D L : longitudinaler hydrodynamischer Dispersionskoeffizient [m 2 /s] D f : freier Diffusionskoeffizient [m 2 /s] v : mittlere Abstandsgeschwindigkeit [m/s] d : mittlerer Korndurchmesser [m] D L D f 1 Diffusion Advektion Dispersion 0,1 0,001 0,01 0, v d D f D T : transversaler hydrodynamischer Dispersionskoeffizient [m 2 /s] D f : freier Diffusionskoeffizient [m 2 /s] v : mittlere Abstandsgeschwindigkeit [m/s] d : mittlerer Korndurchmesser [m] D T D f 1 Diffusion Advektion Dispersion 0,1 0, v d Abb. 2.3: D f Einfluß der Abstandsgeschwindigkeit auf den dominierenden Transportprozess (PERKINS & JOHNSON 1963). 13
30 2.1 Transportmechanismen Phasenübergänge Im Untergrund befindliche BTEX können sowohl als flüssige Phase vorliegen als auch an der Feststoffmatrix sorbiert, im Boden- bzw. Grundwasser gelöst oder gasförmig in der Bodenluft verteilt sein (vgl. Abb. 2.1). Ein Wechsel des Schadstoffs von einer Phase in eine andere wird als Phasenübergang bezeichnet. Die wichtigsten Prozesse, die zu einem Phasenübergang von BTEX im Untergrund führen und somit das Transportverhalten dieser Schadstoffe entscheidend beeinflussen, werden nachfolgend näher erläutert Lösung Die Sättigungskonzentration unpolarer organischer Verbindungen in reinem Wasser ist eine Funktion des Grades zu dem sie von polaren Wassermolekülen angezogen werden (FETTER 1999), wobei die Anziehung mit zunehmender Polarität bzw. abnehmender Lipophilie des organischen Moleküls steigt. Die Lipophilie einer Substanz läßt sich über ihren Octanol/Wasser- Verteilungskoeffizienten (K ow ) quantifizieren: C ol K ow = (2.18) Cw mit K ow Octanol/Wasser-Verteilungskoeffizient [-], C ol Konzentration einer Substanz in n-octanol [kg m -3 ], C w Konzentration in der wäßrigen Phase [kg m -3 ]. Benzol, Toluol, Ethylbenzol und Xylol gehören als nichtionische, organische Schadstoffe zu den unpolaren, nur mäßig wasserlöslichen Verbindungen. Die Wasserlöslichkeit sowie der Octanol/Wasser-Verteilungskoeffizient von BTEX bei 20 C sind in Tab. 2.2 aufgeführt. Die Wasserlöslichkeit organischer Moleküle nimmt mit ihrer Molekülgröße ab, da mit zunehmender unpolarer Oberfläche des zu lösenden Moleküls die Exzess-Lösungsenthalpie, H s e zu- und die Exzess-Lösungsentropie S s e abnimmt (SCHWARZENBACH et al. 1993). 14
31 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX Tab. 2.2: Wasserlöslichkeit (S w ) und Octanol/Wasser-Verteilungskoeffizient (K ow ) von BTEX bei 20 C. Organische Verbinung S w [kg m -3 ] K ow [-] Benzol 1,76 a 135 b Toluol 0,55 a 490 c Ethylbenzol 0,19 d 1413 c o-xylol 0,175 c 1445 e m-xylol 0,16 b 1585 b p-xylol 0,20 c 1413 c a KEELEY et al. (1988), b ABDUL et al. (1987), c VERSCHUEREN (1997), d OWENS et al. (1986), e HODSON & WILLIAMS (1988). Darüberhinaus ist die Wasserlöslichkeit temperaturabhängig (SCHWARZEN- BACH et al. 1993): d ln x dt sat w e H s = (2.19) 2 R T mit xw sat Sättigungsmolenbruch einer flüssigen organischen Verbindung in der wäßrigen Phase [-], T Temperatur [K], H s e Exzess-Lösungsenthalpie [kg m 2 s -2 mol -1 ], R allgemeine Gaskonstante (8,317 kg m 2 s -2 mol -1 K -1 ). Die Stärke und Tendenz des Temperatureffektes ist substanzspezifisch und variiert vielfach mit dem betrachteten Temperaturbereich. So steigt die Wasserlöslichkeit von Benzol oberhalb 20 C mit zunehmender Temperatur, nimmt jedoch unterhalb von 15 C mit steigender Temperatur ab, da sich auch die Exzess-Lösungsenthalpie mit der Temperatur ändert. Zumeist sind neben der betrachteten organischen Verbindung weitere organische und anorganische Substanzen im Wasser enthalten und wirken sich je nach Art und Konzentration unterschiedlich auf die Wasserlöslichkeit des Schadstoffs aus. Das Löslichkeitsverhalten von Mischungen strukturell ähnlicher organischer Substanzen in wäßrigen Lösungen ist näherungsweise als ideal zu bezeichnen (BANERJEE 1984): 15
32 2.1 Transportmechanismen C i = (2.20) S i ( x i ) org mit C i Sättigungskonzentration der i-ten Komponente im Wasser bei Anwesenheit strukturell ähnlicher Organika [mol l -1 ], S i Wasserlöslichkeit der i-ten Komponente in ihrer puren Form [mol l -1 ], (x i ) org Molenbruch der i-ten Komponente in der organischen Phase [-]. Die maximale Konzentration einer organischen Substanz in einer wäßrigen, mit strukturell ähnlichen organischen Stoffen gesättigten Lösung ist somit geringer als in reinem Wasser und abhängig von ihrem Anteil in der organischen Phase. Bei der Berechnung des Löslichkeitsverhaltens von Mischungen unterschiedlich polarer organischer Substanzen in wäßrigen Lösungen sind die Aktivitätskoeffizienten in der organischen und wäßrigen Phase vielfach nicht mehr vernachlässigbar (BANERJEE 1984): C S p ( x ) ( γ ) ( γ ) i i org i org i = aq (2.21) i ( γ i ) aq mit C i Sättigungskonzentration der i-ten Komponente im Wasser bei Anwesenheit strukturell ähnlicher Organika [mol l -1 ], S i Wasserlöslichkeit der i-ten Komponente in ihrer puren Form [mol l -1 ], (x i ) org Molenbruch der i-ten Komponente in der organischen Phase [-], (γ i ) org Aktivitätskoeffizient der i-ten Komponente in der organischen Phase in Anwesenheit hydrophilerer organischer Substanzen [-], (γ p i ) aq Aktivitätskoeffizient der i-ten Komponente in der wäßrigen Phase ohne Anwesenheit weiterer Substanzen [-], (γ i ) aq Aktivitätskoeffizient der i-ten Komponente in der wäßrigen Phase in Anwesenheit hydrophilerer organischer Substanzen [-]. Durch die Anwesenheit hydrophilerer Organika steigt der Wassergehalt in der organischen Phase, was wiederum einen Anstieg des Aktivitätskoeffizienten in der organischen Phase, (γ i ) org zur Folge hat. Dieser Effekt wirkt sich auf die hydrophobste organische Komponente in der Mischung am stärksten aus 16
33 2 Theoretische Grundlagen der Transport- und Abbauprozesse von BTEX (BANERJEE 1984). Desweiteren führen vermehrte intermolekulare Wechselwirkungen in der wäßrigen Phase in Gegenwart hydrophilerer organischer Substanzen zu einer Absenkung des Aktivitätskoeffizienten in der wäßrigen Phase ((γ i ) aq < (γ i p ) aq ). Diese Absenkung ist um so größer je unpolarer die hydrophilere organische Substanz ist. Ein Anstieg von (γ i ) org bzw. Abfall von (γ i ) aq führt zu einer erhöhten Wasserlöslichkeit der entsprechenden organischen Komponente. Man spricht hier von einem Kosolvent-Effekt, die hydrophilere organische Substanz wird als Kosolvent bezeichnet. Die relative Erhöhung der Wasserlöslichkeit durch Anwesenheit eines Kosolventen, S * läßt sich nach YALKOWSKY & ROSEMAN (1981) berechnen: S * sat Cw, co = = exp σ S i ( f ) co (2.22) mit S * relative Erhöhung der Wasserlöslichkeit einer Substanz durch Anwesenheit eines Kosolventen [-], Cw,co sat Sättigungskonzentration bei Anwesenheit eines Kosolventen [mol l -1 ], S i Wasserlöslichkeit der i-ten Komponente in ihrer puren Form [mol l -1 ], f co volumetrischer Anteil des Kosolventen im Wasser [m 3 m -3 ], σ Solubilisierungskonstante [-]. S * steigt mit zunehmendem Volumenanteil des Kosolventen im Wasser, wobei für manche Kosolventen oberhalb eines f co -Wertes von 0,5 Abweichungen vom exponentiellen Verhalten aufgrund verstärkter gegenseitiger Lösungserscheinungen beobachtet worden sind (PINAL et al. 1990). Im Wasser gelöste anorganische Salze erhöhen den Aktivitätskoeffizienten unpolarer organischer Verbindungen in der wäßrigen Phase, (γ i ) aq und setzen somit ihre Sättigungskonzentration im Wasser herab. Dieser Effekt wird als Aussalzen bezeichnet und läßt sich mit Hilfe der von SETSCHENOW (1889) entwickelten empirischen Formel quantifizieren: 17
34 2.1 Transportmechanismen mit C sat C sat 18 C sat w s log = K C sat sal (2.23) Cw, sal w Sättigungskonzentration in reinem Wasser [mol m -3 ], w,sal Sättigungskonzentration in mineralisiertem Wasser [mol m -3 ], K s salting-out - bzw. Setschenow-Konstante [m 3 mol -1 ], C sal Salzgehalt des Wassers [mol m -3 ]. Die Setschenow-Konstante, K s ist ein Maß für die Effektivität eines bestimmten Salzes oder einer Kombination von Salzen eine gegebene organische Substanz auszusalzen und nimmt Werte zwischen und m 3 mol -1 (MCDEVIT & LONG 1952) an. Sowohl das Sorptions- als auch das Ausgasungsverhalten einer organischen Substanz ist abhängig von ihrer Wasserlöslichkeit. Somit stellt die Wasserlöslichkeit einen entscheidenden Parameter für das Transportverhalten organischer Schadstoffe im Untergrund dar Sorption Unter dem Begriff der Sorption werden Festlegungsprozesse von Stoffen an Feststoffpartikeln zusammengefaßt. Prinzipiell kann zwischen zwei Arten von Sorptionsprozessen differenziert werden: der Adsorption und der Absorption. Die Adsorption beschränkt sich auf Wechselwirkungen zwischen dem adsorbierten Teilchen und der Feststoffoberfläche, während die Absorption Prozesse beschreibt, bei denen das Sorptiv das Sorbens intrapartikulär diffundiert (KARICKHOFF 1984) und an der inneren Oberfläche des Sorbens sorptiv festgelegt wird (WOOD et al. 1990). Aufgrund des komplexen Aufbaus des Untergrundes können dort beide Sorptionsprozesse gleichermaßen nebeneinander ablaufen. Da die Adsorption und Absorption im Untergrund experimentell nicht getrennt voneinander quantifizierbar sind, werden sie im weiteren Verlauf dieser Arbeit unter dem Oberbegriff der Sorption gemeinsam betrachtet. Generell können physikalische, chemische und elektrostatische Wechselwirkungen zur Sorption von organischen Schadstoffen im Untergrund führen (GRATHWOHL 1989). Benzol, Toluol, Ethylbenzol und Xylol gehören zu den unpolaren organischen Schadstoffen und verfügen zudem über keine chemisch aktive funktionelle Gruppe. Aus diesem Grunde spielen für BTEX chemische und starke elektrostatische Kräfte, wie sie beim Ionenaustausch, der Chelatbildung sowie der Wasserstoffbrückenbildung auftreten, keine Rolle. Hier sind hauptsächlich schwache physikalische Bindungskräfte für die
Grundwasser: chemische Vorgänge bei der Infiltration. Redoxprozesse im Grundwasser Transport reaktiver Spezies
 Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
3. Diffusion und Brechungsindex
 3. Diffusion und Brechungsinde Die Diffusion in und aus einer Schicht ist die Grundlage vieler Sensoreffekte, wobei sich die einzelnen Sensoren dann nur noch in der Art der Übersetzung in ein meßbares
3. Diffusion und Brechungsinde Die Diffusion in und aus einer Schicht ist die Grundlage vieler Sensoreffekte, wobei sich die einzelnen Sensoren dann nur noch in der Art der Übersetzung in ein meßbares
Diffusion. Prüfungsfrage
 Prüfungsfrage Diffusion Die Diffusion. Erstes Fick sches Gesetz. Der Diffusionskoeffizient. Die Stokes-Einstein Beziehung. Diffusion durch die Zellmembrane: passive, aktive und erleichterte Diffusion Lehrbuch
Prüfungsfrage Diffusion Die Diffusion. Erstes Fick sches Gesetz. Der Diffusionskoeffizient. Die Stokes-Einstein Beziehung. Diffusion durch die Zellmembrane: passive, aktive und erleichterte Diffusion Lehrbuch
11 Stofftransport in Böden Grundlagen
 wichtige Prozesse für das Verhalten von gelösten Stoffen in Böden Extended multistep outflow method for the accurate determination of soil hydraulic properties close to water saturation 11 Stofftransport
wichtige Prozesse für das Verhalten von gelösten Stoffen in Böden Extended multistep outflow method for the accurate determination of soil hydraulic properties close to water saturation 11 Stofftransport
Inhaltsverzeichnis 1 Theorie...1
 Inhaltsverzeichnis 1 Theorie...1 1.1 Gleichgewichtsreaktionen...1 1.1.1 Einführung...1 1.1.2 Thermodynamische Grundlagen...5 1.1.2.1 Massenwirkungsgesetz...5 1.1.2.2 Gibbs sche freie Energie...7 1.1.2.3
Inhaltsverzeichnis 1 Theorie...1 1.1 Gleichgewichtsreaktionen...1 1.1.1 Einführung...1 1.1.2 Thermodynamische Grundlagen...5 1.1.2.1 Massenwirkungsgesetz...5 1.1.2.2 Gibbs sche freie Energie...7 1.1.2.3
Verteilungskoeffizienten
 VL Limnochemie Verteilungskoeffizienten Sorption I Inhalt Verteilungskoeffizienten K H,K d, K OW, K OC, Rd Sorption I Begriffe und Definitionen Grundlagen Sorptive Sorbentien 1 VERTEILUNGS- KOEFFIZIENTEN
VL Limnochemie Verteilungskoeffizienten Sorption I Inhalt Verteilungskoeffizienten K H,K d, K OW, K OC, Rd Sorption I Begriffe und Definitionen Grundlagen Sorptive Sorbentien 1 VERTEILUNGS- KOEFFIZIENTEN
12 Stofftransport in Böden Mathematische Beschreibung
 Extended multistep outflow method for the aurate determination of soil hydrauli properties lose to water saturation 1.1 Massenerhaltung 1 Stofftransport in Böden Mathematishe Beshreibung W. Durner: Wasser-
Extended multistep outflow method for the aurate determination of soil hydrauli properties lose to water saturation 1.1 Massenerhaltung 1 Stofftransport in Böden Mathematishe Beshreibung W. Durner: Wasser-
Diplomarbeit: Modellierung des Austausches zwischen Oberflächenwasser und Grundwasser mit Hilfe des Umwelttracers Temperatur
 Diplomarbeit: Modellierung des Austausches zwischen Oberflächenwasser und Grundwasser mit Hilfe des Umwelttracers Temperatur Von Johannes Ahrns Betreuer Prof. Dr.-Ing. Thomas Grischek Dipl.-Ing. Kerstin
Diplomarbeit: Modellierung des Austausches zwischen Oberflächenwasser und Grundwasser mit Hilfe des Umwelttracers Temperatur Von Johannes Ahrns Betreuer Prof. Dr.-Ing. Thomas Grischek Dipl.-Ing. Kerstin
Aspekte der Angewandten Geologie
 Aspekte der Angewandten Geologie Geohydromodellierung Institut für Geowissenschaften Christian-Albrechts-Universität zu Kiel 2-1 Wo ist das Grundwasser? 2-2 Hier 2-3 d 2-4 Das unterirdische Wasser befindet
Aspekte der Angewandten Geologie Geohydromodellierung Institut für Geowissenschaften Christian-Albrechts-Universität zu Kiel 2-1 Wo ist das Grundwasser? 2-2 Hier 2-3 d 2-4 Das unterirdische Wasser befindet
Transport im Grundwasser
 Transport im Grundwasser Matthias Willmann, Joaquin Jimenez-Martinez, Wolfgang Kinzelbach HS 2016 Grundwasser I / Transport im Grundwasser 1 Motivation Mit Grundwasser werden auch gelöste Stoffe transportiert
Transport im Grundwasser Matthias Willmann, Joaquin Jimenez-Martinez, Wolfgang Kinzelbach HS 2016 Grundwasser I / Transport im Grundwasser 1 Motivation Mit Grundwasser werden auch gelöste Stoffe transportiert
Stofftransport durch pharmazeutisch relevante Membranen
 Stofftransport durch pharmazeutisch relevante Membranen Inaugural-Dissertation zur Erlangung, der Doktorwürde der Fakultät für Chemie und Pharmazie der Albert-Ludwigs-Universität zu Freiburg i. Br. vorgelegt
Stofftransport durch pharmazeutisch relevante Membranen Inaugural-Dissertation zur Erlangung, der Doktorwürde der Fakultät für Chemie und Pharmazie der Albert-Ludwigs-Universität zu Freiburg i. Br. vorgelegt
Untersuchungen zum Einsatz alternativer
 Prozesswissenschaften Untersuchungen zum Einsatz alternativer Waschmedien für die Rückgewinnung aromatischer Kohlenwasserstoffe aus Kokereigasen vorgelegt von Diplom Ingenieur Diethmar Richter aus Bremen
Prozesswissenschaften Untersuchungen zum Einsatz alternativer Waschmedien für die Rückgewinnung aromatischer Kohlenwasserstoffe aus Kokereigasen vorgelegt von Diplom Ingenieur Diethmar Richter aus Bremen
Berechnung des thermischen Verhaltens von Kies-Wasser-Speichern
 Berechnung des thermischen Verhaltens von Kies-Wasser-Speichern Von der Fakultät für Maschinenbau der Technischen Universität Chemnitz genehmigte Dissertation zur Erlangung des akademischen Grades Doktoringenieur
Berechnung des thermischen Verhaltens von Kies-Wasser-Speichern Von der Fakultät für Maschinenbau der Technischen Universität Chemnitz genehmigte Dissertation zur Erlangung des akademischen Grades Doktoringenieur
Versuch 41: Viskosität durchgeführt am
 Physikalisch-chemisches Grundpraktikum Gruppe 6 Philipp von den Hoff Andreas J. Wagner Versuch 4: Viskosität durchgeführt am 26.05.2004 Zielsetzung: Ziel des Versuches ist es, die Viskosität von n-butan-2-ol
Physikalisch-chemisches Grundpraktikum Gruppe 6 Philipp von den Hoff Andreas J. Wagner Versuch 4: Viskosität durchgeführt am 26.05.2004 Zielsetzung: Ziel des Versuches ist es, die Viskosität von n-butan-2-ol
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan
 Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung)
 Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
D i p l o m a r b e i t
 D i p l o m a r b e i t Auswirkung von Tiefbauwerken auf die Grundwassertemperatur in Dresden Inhalt 1 Einleitung 2 Methodik 3 Auswertung 4 Zusammenfassung/ Schlussfolgerungen Von Linda Wübken Betreuer:
D i p l o m a r b e i t Auswirkung von Tiefbauwerken auf die Grundwassertemperatur in Dresden Inhalt 1 Einleitung 2 Methodik 3 Auswertung 4 Zusammenfassung/ Schlussfolgerungen Von Linda Wübken Betreuer:
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie
 1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
Lösungen, Stoffmengen und Konzentrationen
 12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Ein Berechnungsinstrument für Sickerwasserprognosen
 ALTEX 1D Ein Berechnungsinstrument für Sickerwasserprognosen Volker Zeisberger HLUG-Altlastenseminar 12./13.6.2013 in Limburg Sickerwasserprognose nach BBodSchV Die Sickerwasserprognose ist die Abschätzung
ALTEX 1D Ein Berechnungsinstrument für Sickerwasserprognosen Volker Zeisberger HLUG-Altlastenseminar 12./13.6.2013 in Limburg Sickerwasserprognose nach BBodSchV Die Sickerwasserprognose ist die Abschätzung
Rührkesselmodell in Deutschland Konsequenzen für Untersuchungsstrategien
 Rührkesselmodell in Deutschland Konsequenzen für Untersuchungsstrategien Jochen Stark Referat Boden und Altlasten, Grundwasserschutz und Wasserversorgung Workshop der MAGPlan - Begleitgruppe 28./29. Juni
Rührkesselmodell in Deutschland Konsequenzen für Untersuchungsstrategien Jochen Stark Referat Boden und Altlasten, Grundwasserschutz und Wasserversorgung Workshop der MAGPlan - Begleitgruppe 28./29. Juni
ALLGEMEINE CHEMIE - GRUNDLAGEN
 ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
Chemische Thermodynamik ENTROPIE LÖSUNGEN
 L-Üb29: Die Standardentropie der Edelgase steigt in regelmässiger Weise mit der molaren Masse. Diese schöne Regelmässigkeit kommt daher, dass die Edelgase nur Translationsenergie besitzen und keine Schwingungsenergie
L-Üb29: Die Standardentropie der Edelgase steigt in regelmässiger Weise mit der molaren Masse. Diese schöne Regelmässigkeit kommt daher, dass die Edelgase nur Translationsenergie besitzen und keine Schwingungsenergie
! " # # # $%&!& && % ' ( ) *++,-*++.
 ! " # # # $%&!& && % ' ( ) *++,-*++. /0 0. Literatur 1. Einführung 1.1 Aufgaben und Ziele der Geohydrologie 1.2 Anwendungsgebiete und Fragestellungen der Geohydraulik 1.3 Grundwasser und seine Bedeutung
! " # # # $%&!& && % ' ( ) *++,-*++. /0 0. Literatur 1. Einführung 1.1 Aufgaben und Ziele der Geohydrologie 1.2 Anwendungsgebiete und Fragestellungen der Geohydraulik 1.3 Grundwasser und seine Bedeutung
Physikalische Grundlagen der Klimaarchive Eis und Grundwasser
 Inhalt der heutigen Vorlesung Physikalische Grundlagen der Klimaarchive Eis und Grundwasser 6. Grundwasser: Dynamik, Transport von Spurenstoffen, Eignung als Archiv 1) Dynamik von Grundwasser Grundlagen
Inhalt der heutigen Vorlesung Physikalische Grundlagen der Klimaarchive Eis und Grundwasser 6. Grundwasser: Dynamik, Transport von Spurenstoffen, Eignung als Archiv 1) Dynamik von Grundwasser Grundlagen
DAMPF-FLÜSSIG-GLEICHGEWICHTE WÄSSRIGER ELEKTROLYT- MISCHUNGEN MIT FLÜCHTIGEN KOMPONENTEN
 DAMPF-FLÜSSIG-GLEICHGEWICHTE WÄSSRIGER ELEKTROLYT- MISCHUNGEN MIT FLÜCHTIGEN KOMPONENTEN Zur Erlangung des akademischen Grades eines DOKTORS DER INGENIEURWISSENSCHAFTEN (Dr.-Ing.) von der Fakultät für
DAMPF-FLÜSSIG-GLEICHGEWICHTE WÄSSRIGER ELEKTROLYT- MISCHUNGEN MIT FLÜCHTIGEN KOMPONENTEN Zur Erlangung des akademischen Grades eines DOKTORS DER INGENIEURWISSENSCHAFTEN (Dr.-Ing.) von der Fakultät für
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14,
 ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
Rolf Mull Hartmut Holländer. Grundwasserhydraulik. und -hydrologie. Eine Einführung. Mit 157 Abbildungen und 20 Tabellen. Springer
 Rolf Mull Hartmut Holländer Grundwasserhydraulik und -hydrologie Eine Einführung Mit 157 Abbildungen und 20 Tabellen Springer VI 1 Bedeutung des Grundwassers 1 2 Strukturen der Grundwassersysteme 4 2.1
Rolf Mull Hartmut Holländer Grundwasserhydraulik und -hydrologie Eine Einführung Mit 157 Abbildungen und 20 Tabellen Springer VI 1 Bedeutung des Grundwassers 1 2 Strukturen der Grundwassersysteme 4 2.1
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
Tabelle 7.1 Typische Werte von ausgewählten Inhaltsstoffen ungereinigter Rauchgase [48]
![Tabelle 7.1 Typische Werte von ausgewählten Inhaltsstoffen ungereinigter Rauchgase [48] Tabelle 7.1 Typische Werte von ausgewählten Inhaltsstoffen ungereinigter Rauchgase [48]](/thumbs/69/60047537.jpg) Einfluß der Abgaszusammensetzung 43 7 Einfluß der Abgaszusammensetzung Reale Abgase bestehen in den meisten Fällen aus komplexen Stoffsystemen. Die Menge und die Art der im Prozeß verwendeten Stoffe, sowie
Einfluß der Abgaszusammensetzung 43 7 Einfluß der Abgaszusammensetzung Reale Abgase bestehen in den meisten Fällen aus komplexen Stoffsystemen. Die Menge und die Art der im Prozeß verwendeten Stoffe, sowie
Kapitel 10 - Gase. Kapitel 10 - Gase. Gase bestehen aus räumlich weit voneinander getrennten Atome/Moleküle in schneller Bewegung
 Kapitel 0 - Gase Gase bestehen aus räumlich weit voneinander getrennten Atome/Moleküle in schneller ewegung Druck Kraft pro Fläche in Pa(scal) oder bar Normdruck = 760mm = 0,35 KPa =,035 bar = atm Messung
Kapitel 0 - Gase Gase bestehen aus räumlich weit voneinander getrennten Atome/Moleküle in schneller ewegung Druck Kraft pro Fläche in Pa(scal) oder bar Normdruck = 760mm = 0,35 KPa =,035 bar = atm Messung
Physikalisches Praktikum
 Physikalisches Praktikum Viskosität von Flüssigkeiten Laborbericht Korrigierte Version 9.Juni 2002 Andreas Hettler Inhalt Kapitel I Begriffserklärungen 5 Viskosität 5 Stokes sches
Physikalisches Praktikum Viskosität von Flüssigkeiten Laborbericht Korrigierte Version 9.Juni 2002 Andreas Hettler Inhalt Kapitel I Begriffserklärungen 5 Viskosität 5 Stokes sches
Basiskenntnistest - Physik
 Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
Lehrbuch Chemische Technologie
 C. Herbert Vogel Lehrbuch Chemische Technologie Grundlagen Verfahrenstechnischer Anlagen WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA IX Inhaltsverzeichnis 1 Einführung 1 1.1 Das Ziel industrieller Forschung
C. Herbert Vogel Lehrbuch Chemische Technologie Grundlagen Verfahrenstechnischer Anlagen WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA IX Inhaltsverzeichnis 1 Einführung 1 1.1 Das Ziel industrieller Forschung
ETH-Aufnahmeprüfung Herbst Physik U 1. Aufgabe 1 [4 pt + 4 pt]: zwei unabhängige Teilaufgaben
![ETH-Aufnahmeprüfung Herbst Physik U 1. Aufgabe 1 [4 pt + 4 pt]: zwei unabhängige Teilaufgaben ETH-Aufnahmeprüfung Herbst Physik U 1. Aufgabe 1 [4 pt + 4 pt]: zwei unabhängige Teilaufgaben](/thumbs/64/51931310.jpg) ETH-Aufnahmeprüfung Herbst 2015 Physik Aufgabe 1 [4 pt + 4 pt]: zwei unabhängige Teilaufgaben U 1 V a) Betrachten Sie den angegebenen Stromkreis: berechnen Sie die Werte, die von den Messgeräten (Ampere-
ETH-Aufnahmeprüfung Herbst 2015 Physik Aufgabe 1 [4 pt + 4 pt]: zwei unabhängige Teilaufgaben U 1 V a) Betrachten Sie den angegebenen Stromkreis: berechnen Sie die Werte, die von den Messgeräten (Ampere-
Tracer in der aquatischen Umwelt. Tracertests Auswertung von Durchbruchskurven. Sebastian Bauer
 Tracer in der aquatischen Umwelt Tracertests Auswertung von Durchbruchskurven Geohydromodellierung Institut für Geowissenschaften Christian-Albrechts-Universität zu Kiel 8-1 Tracerversuche Tracerversuche
Tracer in der aquatischen Umwelt Tracertests Auswertung von Durchbruchskurven Geohydromodellierung Institut für Geowissenschaften Christian-Albrechts-Universität zu Kiel 8-1 Tracerversuche Tracerversuche
Übungen zur Vorlesung Physikalische Chemie I Lösungsvorschlag zu Blatt 7
 1. Aufgabe Die kyroskopische Konstante E k und die ebulloskopische Konstante E e werden wie folgt berechnet. E k Wasser = R T 2 schmelz M H schmelz = 8,31451 J 273,15 K 2 18,02 10 3 kg mol = 1,86 K kg
1. Aufgabe Die kyroskopische Konstante E k und die ebulloskopische Konstante E e werden wie folgt berechnet. E k Wasser = R T 2 schmelz M H schmelz = 8,31451 J 273,15 K 2 18,02 10 3 kg mol = 1,86 K kg
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Transportkoeffizienten von Alkoholen und Wasser: Molekulare Simulation und Messungen mit der Taylor-Dispersions Methode
 ProcessNet Jahrestagung, 8 - September 9, Mannheim Transportkoeffizienten von Alkoholen und Wasser: Molekulare Simulation und Messungen mit der Taylor-Dispersions Methode Gabriela Guevara-Carrión, Jadran
ProcessNet Jahrestagung, 8 - September 9, Mannheim Transportkoeffizienten von Alkoholen und Wasser: Molekulare Simulation und Messungen mit der Taylor-Dispersions Methode Gabriela Guevara-Carrión, Jadran
Der Deal Flow von Business Angels - Eine empirische Analyse
 Der Deal Flow von Business Angels - Eine empirische Analyse Von der Fakultät für Wirtschaftswissenschaften der Rheinisch-Westfälischen Technischen Hochschule Aachen zur Erlangung des akademischen Grades
Der Deal Flow von Business Angels - Eine empirische Analyse Von der Fakultät für Wirtschaftswissenschaften der Rheinisch-Westfälischen Technischen Hochschule Aachen zur Erlangung des akademischen Grades
= n + + Thermodynamik von Elektrolytlösungen. Wdhlg: Chemisches Potential einer Teilchenart: Für Elektrolytlösungen gilt: wobei : und
 Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Elektrolyte Teil III Solvatation, elektrische Leitfähigkeit, starke und schwache Elektrolyte, Ionenstärke, Debye Hückeltheorie, Migration, Diffusion, Festelektrolyte Thermodynamik von Elektrolytlösungen
Kolligative Eigenschaften
 Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
Kolligative Eigenschaften Kolligative (lat. colligare, sammeln) Eigenschaften (in verdünnter Lösung): f(nzahl der eilchen des gelösten Stoffs) f(rt der eilchen des gelösten Stoffs) eispiel: Gefrierpunkt,
Fachgespräche Arbeitshilfe zur Sanierung von Grundwasserverunreinigungen - Einführung, Anlass, Rechtsgrundlagen
 Fachgespräche Arbeitshilfe zur Sanierung von Grundwasserverunreinigungen - Einführung, Anlass, Rechtsgrundlagen Holger Strömmer Hess. Ministerium für Umwelt, ländlichen Raum und Verbraucherschutz - Referat
Fachgespräche Arbeitshilfe zur Sanierung von Grundwasserverunreinigungen - Einführung, Anlass, Rechtsgrundlagen Holger Strömmer Hess. Ministerium für Umwelt, ländlichen Raum und Verbraucherschutz - Referat
Physikalische Aspekte der Respiration
 Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
Oberflächenspannung. Abstract. 1 Theoretische Grundlagen. Phasen und Grenzflächen
 Phasen und Grenzflächen Oberflächenspannung Abstract Die Oberflächenspannung verschiedener Flüssigkeit soll mit Hilfe der Kapillarmethode gemessen werden. Es sollen die mittlere Abstand der einzelnen Moleküle
Phasen und Grenzflächen Oberflächenspannung Abstract Die Oberflächenspannung verschiedener Flüssigkeit soll mit Hilfe der Kapillarmethode gemessen werden. Es sollen die mittlere Abstand der einzelnen Moleküle
! #!! % & ( )! ! +, +,# # !.. +, ) + + /) # %
 ! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
Bei der Wärmeübertragung kann man drei Transportvorgänge voneinander unterscheiden:
 6 ärmeübertragung Bei der ärmeübertragung kann man drei Transportvorgänge voneinander unterscheiden: ärmeleitung ärmeübergang / onvektion ärmestrahlung Der ärmetransport durch Leitung oder onvektion benötigt
6 ärmeübertragung Bei der ärmeübertragung kann man drei Transportvorgänge voneinander unterscheiden: ärmeleitung ärmeübergang / onvektion ärmestrahlung Der ärmetransport durch Leitung oder onvektion benötigt
Simulationstechnik V
 Simulationstechnik V Vorlesung/Praktikum an der RWTH Aachen Numerische Simulation von Strömungsvorgängen B. Binninger Institut für Technische Verbrennung Templergraben 64 4. Teil Finite-Volumen-Methode
Simulationstechnik V Vorlesung/Praktikum an der RWTH Aachen Numerische Simulation von Strömungsvorgängen B. Binninger Institut für Technische Verbrennung Templergraben 64 4. Teil Finite-Volumen-Methode
Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H 2 O von
 Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Aufgabe 1: Berechnen Sie die Wärmemenge in kj, die erforderlich ist, um 750g H O von 0 C bis zum Siedepunkt (100 C) zu erwärmen. Die spezifische Wärmekapazität von Wasser c = 4.18 J K - 1 g -1. Lösung
Foto: Fritsch. Übung 3: Bestimmung der gesättigten hydraulischen Leitfähigkeit (k f -Wert) - Ermittlung aus der Kornverteilungskurve -
 Übung 3 Hydrogeologie I: Bestimmung der gesättigten hydraulischen Leitfähigkeit Dipl.-Geoökol. M. Schipek TU Bergakademie Freiberg, Institut für Geologie Lehrstuhl für Hydrogeologie Foto: Fritsch Kenngrößen
Übung 3 Hydrogeologie I: Bestimmung der gesättigten hydraulischen Leitfähigkeit Dipl.-Geoökol. M. Schipek TU Bergakademie Freiberg, Institut für Geologie Lehrstuhl für Hydrogeologie Foto: Fritsch Kenngrößen
Entwicklung einer universellen Gruppenbeitragszustandsgleichung
 Entwicklung einer universellen Gruppenbeitragszustandsgleichung Vom Fachbereich Chemie der Carl von Ossietzky Universität Oldenburg zur Erlangung des Grades eines Doktors der Naturwissenschaften angenommene
Entwicklung einer universellen Gruppenbeitragszustandsgleichung Vom Fachbereich Chemie der Carl von Ossietzky Universität Oldenburg zur Erlangung des Grades eines Doktors der Naturwissenschaften angenommene
2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg
![2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg 2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg](/thumbs/75/72774995.jpg) 2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
Einführung in die Chromatographie
 Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/32 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/32 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ Zusammenfassung
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst HCI D323 Martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/ Zusammenfassung
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Viskositätsmessung mit dem Rotationsviskosimeter
 Versuch: 1 Versuchsziel und Anwendung Viskositätsmessung mit dem Rotationsviskosimeter Die Aufgabe besteht darin, ein Schmieröl auf sein Viskositätsverhalten in Abhängigkeit von der Temperatur zu untersuchen.
Versuch: 1 Versuchsziel und Anwendung Viskositätsmessung mit dem Rotationsviskosimeter Die Aufgabe besteht darin, ein Schmieröl auf sein Viskositätsverhalten in Abhängigkeit von der Temperatur zu untersuchen.
Semi-volatile Organic Compound (SVOC) Aerosols. Verhalten von mittelflüchtigen Stoffen
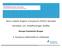 Semi-volatile Organic Compound (SVOC) Aerosols Verhalten von mittelflüchtigen Stoffen George-Constantin Dragan 4. Symposium Gefahrstoffe am Arbeitsplatz Überblick Einleitung Aerosole Dispersionen aus festen
Semi-volatile Organic Compound (SVOC) Aerosols Verhalten von mittelflüchtigen Stoffen George-Constantin Dragan 4. Symposium Gefahrstoffe am Arbeitsplatz Überblick Einleitung Aerosole Dispersionen aus festen
Prognose des deutschen Verkehrsunfallgeschehens unter Berücksichtigung der Fahrzeugsicherheitssysteme
 Prognose des deutschen Verkehrsunfallgeschehens unter Berücksichtigung der Fahrzeugsicherheitssysteme Von der Fakultät für Maschinenbau, Verfahrens- und Energietechnik der Technischen Universität Bergakademie
Prognose des deutschen Verkehrsunfallgeschehens unter Berücksichtigung der Fahrzeugsicherheitssysteme Von der Fakultät für Maschinenbau, Verfahrens- und Energietechnik der Technischen Universität Bergakademie
Landau-Theorie der Phasenumwandlung von Membranen
 Landau-Theorie der Phasenumwandlung von Membranen Vorbemerkung Vorbemerkung: Um Einblick in die thermodynamischen aber auch strukturellen Eigenschaften von Lipidschichten zu erhalten, ist die klassische
Landau-Theorie der Phasenumwandlung von Membranen Vorbemerkung Vorbemerkung: Um Einblick in die thermodynamischen aber auch strukturellen Eigenschaften von Lipidschichten zu erhalten, ist die klassische
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
4.3 Reaktionsgeschwindigkeit und Katalysator
 4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 2: Übersicht 2 Zustandsgrößen 2.3 Bestimmung von Zustandsgrößen 2.3.1 Bestimmung der Phase 2.3.2 Der Sättigungszustand
Thermodynamik (Wärmelehre) III kinetische Gastheorie
 Physik A VL6 (07.1.01) Thermodynamik (Wärmelehre) III kinetische Gastheorie Thermische Bewegung Die kinetische Gastheorie Mikroskopische Betrachtung des Druckes Mawell sche Geschwindigkeitserteilung gdes
Physik A VL6 (07.1.01) Thermodynamik (Wärmelehre) III kinetische Gastheorie Thermische Bewegung Die kinetische Gastheorie Mikroskopische Betrachtung des Druckes Mawell sche Geschwindigkeitserteilung gdes
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 2. Das reale Gas. Das reale Gas
 Prof. Dr. Norbert Hampp 1/9 2. Das reale Gas Das reale Gas Für die Beschreibung des realen Gases werden die Gasteilchen betrachtet als - massebehaftet - kugelförmig mit Durchmesser d - Wechselwirkungen
Prof. Dr. Norbert Hampp 1/9 2. Das reale Gas Das reale Gas Für die Beschreibung des realen Gases werden die Gasteilchen betrachtet als - massebehaftet - kugelförmig mit Durchmesser d - Wechselwirkungen
Die chemische Zusammensetzung natiirlicher Gewasser
 Inhaltsverzeichnis Vorwort XI KAPITEL 1 KAPITEL 2 Die chemische Zusammensetzung natiirlicher Gewasser 1.1 Einleitung 1.2 Verwitterungsprozesse 1.3 Wechselwirkungen zwischen Organismen und Wasser 1.4 Das
Inhaltsverzeichnis Vorwort XI KAPITEL 1 KAPITEL 2 Die chemische Zusammensetzung natiirlicher Gewasser 1.1 Einleitung 1.2 Verwitterungsprozesse 1.3 Wechselwirkungen zwischen Organismen und Wasser 1.4 Das
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Poröse Materialien. Porösität - Porentypen. a) geschlossene Poren. b-f) offene Poren
 Inhalt: Allgemeines Porösität - Porentypen a) geschlossene Poren b-f) offene Poren b) blind ink-bottle-shaped c) open cylindrical pores d) slit-shaped e) through pores f) blind cylindrical pores Inhalt:
Inhalt: Allgemeines Porösität - Porentypen a) geschlossene Poren b-f) offene Poren b) blind ink-bottle-shaped c) open cylindrical pores d) slit-shaped e) through pores f) blind cylindrical pores Inhalt:
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Klausur Technische Chemie SS 2007 Prof. M. Schönhoff // PD Dr. C. Cramer-Kellers Klausur zur Vorlesung
 Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 9.7.2007 9:00 Uhr bis 11.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit Worten
Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 9.7.2007 9:00 Uhr bis 11.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit Worten
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid
 Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Energie- und Ökoeffizienz von Wohngebäuden
 Energie- und Ökoeffizienz von Wohngebäuden Entwicklung eines Verfahrens zur lebenszyklusorientierten Bewertung der Umweltwirkungen unter besonderer Berücksichtigung der Nutzungsphase Vom Fachbereich Bauingenieurwesen
Energie- und Ökoeffizienz von Wohngebäuden Entwicklung eines Verfahrens zur lebenszyklusorientierten Bewertung der Umweltwirkungen unter besonderer Berücksichtigung der Nutzungsphase Vom Fachbereich Bauingenieurwesen
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
Phasengleichgewicht und Phasenübergänge. Gasförmig
 Phasengleichgewicht und Phasenübergänge Siedetemperatur Flüssig Gasförmig Sublimationstemperatur Schmelztemperatur Fest Aus unserer Erfahrung mit Wasser wissen wir, dass Substanzen ihre Eigenschaften bei
Phasengleichgewicht und Phasenübergänge Siedetemperatur Flüssig Gasförmig Sublimationstemperatur Schmelztemperatur Fest Aus unserer Erfahrung mit Wasser wissen wir, dass Substanzen ihre Eigenschaften bei
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 1. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 1: Übersicht 2 Zustandsgrößen 2.1 Thermische Zustandsgrößen 2.1.1 Masse und Molzahl 2.1.2 Spezifisches
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 1: Übersicht 2 Zustandsgrößen 2.1 Thermische Zustandsgrößen 2.1.1 Masse und Molzahl 2.1.2 Spezifisches
(1) und ist bei unserem Versuch eine Funktion der Temperatur, nicht aber der Konzentration.
 Praktikum Teil A und B 15. AUFLÖSUNGSGESCHWINDIGKEIT Stand 11/4/1 AUFLÖSUNGSGESCHWINDIGKEIT EINES SALZES 1. ersuchsplatz Komponenten: - Thermostat - Reaktionsgefäß mit Rührer - Leitfähigkeitsmessgerät
Praktikum Teil A und B 15. AUFLÖSUNGSGESCHWINDIGKEIT Stand 11/4/1 AUFLÖSUNGSGESCHWINDIGKEIT EINES SALZES 1. ersuchsplatz Komponenten: - Thermostat - Reaktionsgefäß mit Rührer - Leitfähigkeitsmessgerät
Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol
![Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol](/thumbs/50/26795947.jpg) 2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
Physikalisches Anfaengerpraktikum. Zustandsgleichung idealer Gase und kritischer Punkt
 Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Modellierung der Schwebstoffaggregation in Verbindung mit persistenten Schadstoffen
 Modellierung der Schwebstoffaggregation in Verbindung mit persistenten Schadstoffen Dr.-Ing. Gudrun Hillebrand, BfG Dipl.-Ing. Irina Klassen, KIT (i-1) i (i+1) Übersicht Grundfragestellung Flockungsmodellierung
Modellierung der Schwebstoffaggregation in Verbindung mit persistenten Schadstoffen Dr.-Ing. Gudrun Hillebrand, BfG Dipl.-Ing. Irina Klassen, KIT (i-1) i (i+1) Übersicht Grundfragestellung Flockungsmodellierung
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Physikalische Chemie Praktikum. Mischphasenthermodynamik: Gefrierpunktserniedrigung Molmassenbestimmung
 Hochschule Emden / Leer Physikalische Chemie Praktikum Mischphasenthermodynamik: Gefrierpunktserniedrigung Molmassenbestimmung Vers.Nr. 17 Sept. 2015 Allgemeine Grundlagen a) Reine Stoffe Bei reinen Stoffen
Hochschule Emden / Leer Physikalische Chemie Praktikum Mischphasenthermodynamik: Gefrierpunktserniedrigung Molmassenbestimmung Vers.Nr. 17 Sept. 2015 Allgemeine Grundlagen a) Reine Stoffe Bei reinen Stoffen
Tropfenkonturanalyse
 Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
ALLGEMEINE CHEMIE - GRUNDLAGEN
 ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung der allgemeinen chemischen Grundlagen und Aspekte, die für alle Bereiche der Chemie notwendig sind; Modellvorstellungen Inhaltsübersicht:
ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung der allgemeinen chemischen Grundlagen und Aspekte, die für alle Bereiche der Chemie notwendig sind; Modellvorstellungen Inhaltsübersicht:
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Die Modellierung einer Lithium-Batterie Zwischenpräsentation zum Praktikum Nichtlineare Modellierung in den Naturwissenschaften
 MÜNSTER Die Modellierung einer Lithium-Batterie Zwischenpräsentation zum Praktikum Nichtlineare Modellierung in den Naturwissenschaften Christoph Fricke, Natascha von Aspern, Carla Tameling 12.06.2012
MÜNSTER Die Modellierung einer Lithium-Batterie Zwischenpräsentation zum Praktikum Nichtlineare Modellierung in den Naturwissenschaften Christoph Fricke, Natascha von Aspern, Carla Tameling 12.06.2012
Dissertation zur Erlangung des akademischen Grades Doktor der Naturwissenschaften (Dr. rer. nat.) Der Fakultät Chemie der Universität Duisburg-Essen
 Untersuchungen zur Gasphasen-Photolyse atmosphärenrelevanter Carbonylverbindungen (Acetaldehyd, Diacetyl, Acetylcyanid, Essigsäure, Propionaldehyd, Butyraldehyd) im Wellenlängenbereich 193-355 nm Dissertation
Untersuchungen zur Gasphasen-Photolyse atmosphärenrelevanter Carbonylverbindungen (Acetaldehyd, Diacetyl, Acetylcyanid, Essigsäure, Propionaldehyd, Butyraldehyd) im Wellenlängenbereich 193-355 nm Dissertation
Abschlussbericht zu Kennziffer 2472: Experimentelle Bestimmung von Grenzaktivitätskoeffizienten in ternären und höheren Elektrolytsystemen
 Abschlussbericht zu Kennziffer 2472: Experimentelle Bestimmung von Grenzaktivitätskoeffizienten in ternären und höheren Elektrolytsystemen Während es bei Nichtelektrolytsystemen möglich ist, mit Hilfe
Abschlussbericht zu Kennziffer 2472: Experimentelle Bestimmung von Grenzaktivitätskoeffizienten in ternären und höheren Elektrolytsystemen Während es bei Nichtelektrolytsystemen möglich ist, mit Hilfe
