Monoklonale Gammopathie unklarer Signifikanz (MGUS) und Multiples Myelom
|
|
|
- Heidi Kaiser
- vor 7 Jahren
- Abrufe
Transkript
1 Zurich Open Repository and Archive University of Zurich Main Library Strickhofstrasse 39 CH-8057 Zurich Year: 2012 Monoklonale Gammopathie unklarer Signifikanz (MGUS) und Multiples Myelom Schleiffenbaum, Boris Abstract: Unspecified DOI: / /a Posted at the Zurich Open Repository and Archive, University of Zurich ZORA URL: Accepted Version Originally published at: Schleiffenbaum, Boris (2012). Monoklonale Gammopathie unklarer Signifikanz (MGUS) und Multiples Myelom. Praxis, 101: DOI: / /a001137
2 DOI / /a ((PX 24_Rubrik CME)) Monoklonale Gammopathie unklarer Signifikanz (MGUS) und Multiples Myelom MGUS und Multiples Myelom sind klonale Plasmazelldyskrasien.Sie stellen die beiden Enden im Kontinuum einer malignen Plasmazell-Infiltration des Knochenmarks dar, wobei das MGUS durch eine geringe Plasmazellinfiltration (<10%) und fehlende klinische Komplikation definiert ist und im Gegensatz dazu das Multiple Myelom durch eine hohe Plasmazellinfiltration (>10%), bzw. durch den Nachweis einer Sekundärfolge der Plasmazelldyskrasie. Die ein Multiples Myelom definierenden Sekundärkomplikation kann man sich mit Hilfe des Wortes «CRAB» merken: Erhöhte Kalziumwerte (hypercalcemia, Ca>0,25 mmol/l oberhalb der Normgrenze oder >2,75 mmol/l), Niereninsufffizienz (renal insufficiency; Kreatinin >173 µmol/l), Anämie (Hb-Abfall >20 g/l unter die Normgrenze oder Hb<100 g/l), Knochenfrakturen bzw. Osteolysen (bone fractures, radiologisch). Zudem besteht vor allem in den späteren Phasen der Myelom-Erkrankung eine erhöhte Infektneigung (>2 bakterielle Infekte in 12 Monaten). Hyperviskositätssyndrom, Polyneuropathie und AL-Amyloidose sind Komplikationen der Paraproteinämie die sowohl beim MGUS als auch beim Multiplen Myelom auftreten können und damit unabhängig von der Plasmazellinfiltration. Sowohl MGUS wie auch dem Multiplen Myelom liegt eine klonale Proliferation von Plasmazellen zugrunde. Diese terminal differenzierten Effektorzellen der B-Lymphoyzten-Reihe produzieren physiologischerweise Antikörper (Immunglobuline) als Antwort auf den Antigen-Kontakt im Rahmen vor allem von Infektionen und sind somit der zelluläre Eckstein der plasmatischen Immunabwehr. Das initiale molekulare Ereignis in der Entstehung des malignen Klons ist nicht bekannt. Wohl aber weiss man, dass die Erkrankung gehäuft auftritt nach Strahlen- oder Benzen-Exposition. Die bei den Plasmazelldyskrasien nachweisbaren zytogenetischen Aberrationen spielen sicher in der Progression der Erkrankung eine Rolle, der genaue Mechanimus ist jedoch auch hier unbekannt. Das bunte klinische Bild, das von vollkommener Beschwerdefreiheit bis hin zu schwersten invalidisierenden Schmerzen reicht, ergibt sich einerseits aus dieser unterschiedlichen Progression, andererseits aus dem Isotyp und der Menge des sezernierten, nicht-funktionellen Immunglobulins (Paraprotein) und der so aufgrund von negativen Feedback- Mechanismen ausgelösten Hypogammaglobulinämie. Diese ist Ursache der Infektanfälligkeit der Myelom-Patienten. An dieser Stelle sollte angemerkt werden, dass Paraproteinämien auch im Rahmen von Non-Hodgkin-Lymphomen gefunden werden können, eine Paraproteinämie damit nicht gleichbedeutend ist mit der Diagnose Plasmazelldyskrasie (dies gilt insbesodere für den Isotyp IgM: Lymphoplasmozytisches Lymphom/M. Waldenström). Das Paraprotein kann, muss aber nicht, über den tubulären Ausfall und die Toxizität der nierengängigen Leichtketten zur Niereninsuffizienz führen, ebenso wie zur Polyneuropathie, oder kann als Amyloid im Gewebe abgelagert werden. Auch die Interaktion der malignen Plasmazellen mit ihrem Mikroenvironment im Knochenmark ist ganz unterschiedlich: Es kann, muss aber nicht, über eine Interaktion mit den ortsständigen Osteoklasten zum Knochenabbbau und damit zur Hyperkalziämie, zu Osteolysen und im Extremfall zu pathologischen Frakturen kommen. Die von Patient zu Patient unterschiedliche Interaktion mit der Erythropoiese (Hepcidin) wiederum bestimmt das Ausmass der die Plasmazelldyskrasie begleitenden Anämie. Erst im Endstadium der Erkrankung hat die Knochenmarksinfiltration direkte pathophysiologische Auswirkungen und es kommt zur Knochenmarksverdrängung und ineffizienz (Neutropenie, Thrombopenie, verstärkte Anämie). Die Erkrankung tritt im mittleren und höheren Alter auf (nur 35% <65 Jahre!) und betrifft Frauen etwas häufiger als Männer (M:F=1,4:1).
3 Die Prognose des MGUS ist im Grunde gut, die des Multiplen Myeloms eher schlecht. Eine MGUS-Phase geht bei so gut wie allen Patienten der Diagnose eines Multiplen Myeloms voraus. Nicht ein jedes MGUS geht jedoch in ein Multiples Myelom über (durchschnittlich 1%/Jahr, siehe auch Tab. 1). Für das MGUS und das Multiple Myelom gibt es inzwischen relativ gut definierte Subgruppen, die sehr unterschiedlich rasch voranschreiten und im Falle des Multiplen Myeloms ganz unterschiedlich auf die Therapie ansprechen (siehe unten). ((hier etwa Tab. 1)) Im Artikel verwendete Abkürzungen: FISH Fluoreszenz-in-situ-Hybridisierung Hb Hämoglobin MGUS Monoklonale Gammopathie unklarer Signifikanz MRD Minimal residual disease NHL Non-Hodgkin-Lymphom OS Gesamtüberleben (overall survial) PFS Progression free survival PR Partial response scr Stringent complete remission sflc Serum-Freie-Leichtketten (serum free light chains) TTP Time to progression, in diesem Fall zum symptomatischen Multiplen Myelom VGPR Very good partial response Klinik und Komplikationen ((Ü1)) Klinik ((Ü2)) Sowohl MGUS als auch ein Multiples Myelom kann sich mit den Symptomen und Zeichen einer Polyneuropathie (meist sensorisch distal betont, Hyp- und Parästhesie, Ausfall der Muskeleigenreflexe) oder einer Amyloidose (Herz- oder Niereninsuffizienz, Polyneuopathie, gastrointestinale Symptomatik) präsentieren. Die Klinik des MGUS ist sonst defintionsgemäss stumm, während sich das Multiple Myelom vor allem das Beschwerdebild seiner Komplikationen zeigt (siehe unten). Fortgeschrittene Stadien eines Multiplen Myeloms, mit rezidivierenden Infekten als Zeichen der Immundefizienz oder gar Allgemeinsymptomen (Schwäche, Müdigkeit, Fieber, Gewichtsverlust, Nachtschweiss) oder Folgen einer Zytopenie (wiederum Infekte bei Neutropenie, bzw. hämorrhagische Diathese in Folge einer Thrombopathie bzw. Thrombasthenie) sieht man heute bei Erstdiagnose selten. Komplikationen ((Ü2)) Abgesehen von Polyneuropathie und Amyloidose (siehe oben) zeigt das MGUS keine Komplikationen. Spontanfrakturen der langen Röhrenknochen, der Rippen vor allem aber des Achsenskeletts (Rückenschmerzen! Höhenminderung), die gerne im Rahmen einer generaliserten Osteoporose gedeutet werden, müssen immer auch an ein Multiples Myelom denken lassen. Seltener präsentiert sich ein Multiples Myelom heutzutage mit dem Beschwerdebild eines manifesten Nierenversagens (Müdigkeit, Pruritus, Foetor), einer schweren Anämie (Müdigkeit, Dyspnoe und sogar Angina pectoris und Synkopen) 2
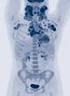
4 oder einer Hyperkalziämie (psychiatrische oder zentralnervöse Symptomatik; Diabetes insipidus; Erbrechen, Obstipation). Im Rahmen der Abklärung einer Niereninsuffizienz bzw. einer Anämie, die bei asymptomatischen oder interkurrent anderweitig erkrankten Patienten als Zufallsbefunde diagnostiziert wurden, sollte der Arzt jedoch relativ bald auch an die Diagnose eines Multiplen Myeloms denken und entsprechende Abklärungsschritte einleiten (siehe unten). Abklärungsstrategie ((Ü1)) In der Anamnese sollte nach Knochenschmerzen, einer Verminderung der Körpergrösse, rezidivierende Infekte und Müdigkeit als Ausdruck einer Niereninsuffizienz oder auch einer Anämie gefragt werden. Dyspnoe, Angina pectoris oder Synkopen können auf eine schwere Anämie hinweisen, während die Atemnot auch Ausdruck einer Kardiomyopathie im Rahmen einer Amyloidose sein kann, die sich im übrigen auch mit gastrointestinalen Symptomen (Schluckbeschwerden, Obstipation/Diarrhoe) oder wie die Leichtketten-Erkrankung oder die Paraprotein-assoziierte tubuläre Nephritis mit den Zeichen einer Niereninsuffzienz bzw. eines nephrotischen Syndroms (Ödeme) präsentieren kann. Zentralnervöse Störungen oder Persöhnlichkeitsveränderungen hingegen können auf eine Hyperkalziämie hinweisen. In der körperlichen Untersuchung sind pathologische Frakturen der langen Röhrenknochen zum Teil sehr einfach zu diagnostizeren. Rippenfrakturen aber können z.b. sehr lange unentdeckt bleiben, während Einbruchfrakturen der Wirbelkörper klinisch oft nicht bemerkt werden (Gibbus; lokale Klopfdolenz). Die klinischen Zeichen der Anämie und der Niereninsuffizienz sind relativ unspezifisch. Trotzdem sollte der internistische Status ebenso wie die persönliche und die Systemanamnese unbedingt vollständig sein, um einerseits einen Infekt, und andererseits Begleiterkrankungen zu erfassen, die in der Altersgruppe der Myelom-Patienten häufig sind. Eine erste Blutuntersuchung sollte ein grosses Blutbild mit morphologischer Differenzierung (Anämie; Hinweise auf die Genese der Anämie; Rouleaux-Formation und Proteinfilm als Hinweise auf eine Paraproteinämie; sehr selten bei Diagnose: Plasmazell-Leukämie), das Kreatinin (Niereninsuffizienz), ein CRP (Infekt), das Kalzium (Hyperkalzämie) und einen Urinstatus (nephrotisches Syndrom; cave: die Stix-Untersuchung erfasst eine Bence-Jones-Proteinurie nicht!) umfassen. Dreh- und Angelpunkt in der Diagnostik des MGUS und des Multiplen Myeloms ist für den Hausarzt und Praktiker die Serumeiweisselektrophorese, ob sie nun im Rahmen einer allgemeinen Abklärung oder auch spezifisch mit dem Verdacht auf eine Plasmazelldyskrsasie durchgeführt wurde: Zeigt sich hier ein M-Gradient, so muss die klonale Genese dieses «peaks» in der Elektrophorese mit Hilfe der Immunfixation bewiesen und der Isotyp des Paraproteins klassifiziert werden. Die Immunfixation hat bei der Diagnostik unter dem Verdacht auf ein Multiples Myelom eine besondere Bedeutung, weist sie doch eine etwa 10fache Sensitivität verglichen mit der Serumeiweisselektropherese auf. Im Hinblick auf die Formen des Multiplen Myeloms, die vornehmlich Leichtketten sezernieren (20 25%! «Leichtkettenerkrankung») ist die Bestimmung der «freien Leichtketten» im Serum ein Muss bei klinischem Verdacht auf ein Multiples Myelom (alternativ: Bence-Jones-Proteine im Urin). Bei Vorliegen einer Paraproteinämie (inkl. klonal vermehrter freier Leichtketten im Serum) kann bzw. sollte in Abhängigkeit von der Höhe des Paraproteins und der Klinik (Tab. 1) eine Knochenmarkspunktion erfolgen: Das Knochenmarkaspirat (EDTA/Ausstrichpräparate; eine relativ schnelle Diagnostik) ermöglicht dabei die morphologische Beurteilung (Plasmoblastom?), die Immunphänotypisierung (wichtig in morphologisch schwierigen Grenzfällen in der Abgrenzung zum Immunblastom und zum Plasmazell-reichen Lymphomplasmozyoidem NHL) und die Karyotypisierung, 3
5 inkl. FISH (sehr wichtig in der Prognostik, siehe unten), während die Biopsie (inkl. Immunhistologie) oft erst die definitive Diagnose, insbesondere aber die Beurteilung des Infiltrationsgrades des Knochenmarks erlaubt. Bei klinischem Verdacht auf ein Multiples Myelom ist eine Knochenmarkspunktion immer indiziert, auch bei fehlender Paraproteinämie oder fehlender Erhöhung der sflc («nicht-sezernierendes» Multiples Myelom, 2 3%). Abbildung 1 zeigt die typische Infiltration des Knochenmarks durch asynchrone, grössenpolymorphe, Plasmazellen, die z.t. auch zwei- und mehrkernig sein können und deren Klonalität in der Immunhistologie bewiesen werden kann (Abb. 2). Unabhängig von Röntgenaufnahmen bei Frakturverdacht sollte mit Hilfe von Radiographien des Schädels, der langen Röhrenknochen, der Rippen und des Achsenskelettes nach Osteolysen gesucht werden und Multiples Myelom ausgeschlossen werden. Heutztage ist hier die Computertomographie im Knochenfenster eine valable Alternative. ((hier etwa Abb. 1und 2)) Diagnosekriterien und Differenzialdiagnose ((Ü1)) Diagnosekriterien ((Ü2)) Ein MGUS diagnostiziert man, wenn eine Paraproteinämie/erhöhte sflc vorliegen und ein Multiples Myelom bzw. eine andersartige B-Zellproliferation/NHL (siehe oben) ausgeschlossen werden konnte (siehe unten, Tab. 1). Somit kann diese Diagnose letztendlich mit Sicherheit nur nach erfolgter Knochenmarkspunktion gestellt werden. Ein Multiples Myelom wird diagnostiziert, wenn >10% klonale Plasmazellen im Knochenmark nachgewiesen werden können, bzw. wenn Komplikationen im Sinne der CRAB-Kriterien vorliegen (siehe oben; Tab. 1). Schlussendlich wird noch zwischen einem «smouldering myeloma» mit erhöhtem Anteil klonaler Plasmazellen im Knochenmark und einem klinisch manifesten, und damit therapiebedürftigem Multiplen Myelom mit CRAB-Komplikationen unterschieden (cave: aufgrund einer Polyneuropathie oder einer Amyloidose kann auch einmal ein «smouldering myeloma» oder selbst ein MGUS therapiebedürftig sein). Um als Kriterium für ein therapiebedürftiges Myelom zu gelten, muss die Nierensuffizienz nicht nur ein bestimmtes Ausmass erreicht haben (Kreatinin >173 mmol/l) ((Autor: oben warens 173 µmol/l, was stimmt?)), es müssen auch andere Ursachen ausgeschlossen worden bzw. unwahrscheinlich sein (arterielle Hypertonie, Diabetes mellitus, Stauungsnieren, Glomerulonephritis und andere). Ähnliches gilt natürlich auch für die anderen Kriterien, insbesondere die Anämie (Hb<100 g/l). Zusätzlich zu Kreatinin (renale Anämie) und CRP («anemia of chronic disease»), sollten hier Ferritin/GPT (Eisenmangel), Vitamin B12, Folat und TSH (Hypothrese) bestimmt werden. Auch die sensorische, distal betonte Polyneuropathie hat andere, viel häufigere Ursachen als eine Paraproteinämie, bzw. ein Multiples Myelom (vor allem Alkohol, Diabetes mellitus). Differenzialdiagnose ((Ü2)) Neben der Plasmazelldyskrasie kann auch eine klonale B-Zell Proliferation/NHL Ursache einer Paraproteinämie sein. Dies gilt insbesondere für den IgM Subtyp, der meist im Rahmen eines lymphoplasmozytoiden NHL gesehen wird. Die Unterscheidung ist von grösster Wichtigkeit, da die und Therapie dieses NHL ganz anders ist als die von MGUS und Multiplem Myelom. Auch andere Malignome treten mit zunehmendem Alter gehäuft auf und das MGUS ist im Alter fast schon endemisch (>70 Jahre: ca. 10%). Somit sollte bei Osteolysen trotz Vorliegen einer Paraproteinämie und Nachweis klonaler 4
6 Plasmazellen im Knochenmark immer auch die Möglichkeit eines Zweittumors erwogen werden. Bei hohem Verdacht (bekanntes Mamma- oder Prostata-Karzinom) ist hier u.u. sogar die direkte Punktion des osteolytischen Herdes selbst eine diagnostische Möglichkeit. Prognose und Therapie ((Ü1)) Prognose ((Ü2)) Die Prognose des MGUS wird bestimmt durch den Isotyp des Paraproteins, die Höhe des Paraproteins und der sflc (Tab. 1). Das Intervall der Kontrolluntersuchung und die Notwendigkeit einer Knochenmarksuntersuchung wird somit auch durch die Risikogruppe bestimmt, in die der jeweilige Patient fällt (durchschnittliche Progression MGUS zu einem Multiples Myelom 1%/Jahr; Tab. 1). Es empfiehlt sich im Allgemeinen ein Kontrollintervall von 1 Jahr, für Patienten mit hohem Risiko von sechs Monaten, um so den Übergang in ein Multiples Myelom frühzeitig zu diagnostizieren und schwerwiegende Komplikationen zu verhindern. Ein steiler Anstieg der κ/λ-ratio scheint am Ende der MGUS-Phase dem klinisch manifesten Mylom vorauszugehen (Leichtketten-MGUS vor Leichtketten-Myelom!). Als wichtigstes Kriterium in der Prognostik des Multiplen Myeloms hat sich ein den letzten Jahren der Karyotyp der malignen Plasmazellen etabliert. Eine Hochrisikogruppe wird dabei durch Patienten mit 17p Deletionen und t14;16 und t14;20 Translokalisationen definiert, ein mittleres Risiko haben die Patienten mit hypoploidem Chromosomensatz und Translokalisation t4;14 sowie Deletion 13 q, während alle Patienten mit einem normalen Karyotyp oder einer Hyperploidie zur Niedrig-Risko-Gruppe gezählt werden können. Als Zusatzkriterien für die Prognose des Multiplen Myeloms und damit auch die Wahl einer spezifischen Therapie gelten Alter, «Performance-Status», Komorbiditäten (Niereninsuffizienz! Polyneuropathie), das β2-mikroglobulin und die Höhe des Albuminspiegels bzw. der LDH sowie der ISS-Score (I: β2-mikroglobulin <3,5 mg/l, Albumin >3,5 mg/l; II: nicht I oder III; III: β2-mikroglobulin >5,5 mg/l). Auch das Ansprechen auf die Therapie («minimal residual disease» MRD) ist von Bedeutung für die Prognose der Erkrankung. Therapie ((Ü2)) Die Notwendikeit zur Therapie ergibt sich aus dem Nachweis, z.t. auch der Schwere von Komplikationen (s.o.). Die Therapie selbst gehört in die Hand des spezialisierten Hämatologen oder Onkologen. Nach erfolgter Induktions-, Transplantations- und Konsoldationstherapie können die Verlaufskontrollen aber durchaus in Zusammenarbeit von Spezialist und Hausarzt erfolgen, wobei sich die Kontrollintervalle nach dem individuellen Patienten richten sollten (Klinik; Serumeiweisselektropherese, Immunfixation, sflc; Ca, Kreatinin; Blutbild; Urinstatus). Die Art und die Strategie der Therapie werden durch das Alter des Patienten, selten auch durch die Prognose bei Diagnosestellung und immer auch durch die Art der zu erwartenden Nebenwirkungen einer geplanten Chemotherapie bestimmt. Als Standardtherapiestrategie für jüngere Patienten (<65 Jahre als arbiträre Grenze der Studienprotokolle; je nach Gesundheitszustand ist die Tranplantation jedoch sicher und durchführbar auch für Patienten im Alter Jahre) gilt heute ein Schema, das eine Induktionsphase mit anschliessender autologer Stammzelltransplantation (Single oder Tandem-Transplantation; Tandem-Transplantation am ehesten für Hoch-Risiko Patienten bzw. bei ungenügendem Ansprechen), eine daran anschliessende Konsolidationsphase und/oder eine Maintenance-Phase umfasst. Die allogene Transplantation ist in der Therapie des Multiplen Mymeloms weiterhin sehr umstritten. Je nach Prognose und Verlauf des individuellen Falles und der Verfügbarkeit eines Familien- oder Fremdspenders wird man aber unter Umständen 5
7 auch eine allogene Transplantation in Erwägung ziehen (zytogenetische Hoch-Risiko-Gruppe, siehe unten; schlechtes Ansprechen auf die Induktionstherapie). Bei älteren Patienten (>65 Jahre, bzw. >75 Jahre, s. o.), für die eine Stammzelltransplantation nicht mehr in Frage kommt, schliesst sich die Konsolidationsphase direkt an die Induktionsphase an. Als Standardtherapie, vor allem für niereninsuffiziente und Hoch-Risiko-Patienten, in der Induktionsphase gilt heute das VMP-Schema (Velcade /Bortezomib 1,3 mg/m 2, d1,4,8,11, Alkeran /Melphalan 9 mg/m 2, d1-4, jeden 2. Zyklus, Prednison 60 mg/m 2, jeden 2. Zyklus, d1-4; Zyklus 21d, 8 Zyklen). Dieses Therapie ist der konventionellen Behandlung mit Alkylantien und Steroiden nicht nur in der Remissionrate und der Tiefe der Remission, sondern auch im PFS und Gesamtüberleben (OS) überlegen. Unter dem Schema kann es zu Zytopenien kommen, Prednison hat die für Kortikosteroide typischen Nebenwirkungen (verschlechterte Glukosetoleranz, erhöhter Blutdruck, Infektneigung), eigentliche cushingoide Bilder sind aber eher selten, und Velcade kann relativ schwere, schmerzhafte Polyneuropathien auslösen oder auch einen Herpes zoster reaktivieren. Alternativ stehen heute zudem die Immunmodulatoren Thalidomid (NW: Müdigkeit, Polyneuropathie, Thrombembolien) und Revlimid /Levalidomid (NW: Zytopenien; geringe Polyneuropathie, Thrombembolien, mit Aspirin beherrscht; unter Umständen vermehrt Sekundärkarzinome; schlechter geeignet in der Niereninsuffizienz) zur Verfügung. Neue Proteasom-Inhibitoren (Typ Velcade /Bortezomib) bzw. Immunmodulatoren wie Carfilzomib (36 mg/m 2 iv, d1, 2, 8, 9, 16; 28d Zyklus) und Pomalidomide (4 mg/d po, d1-21, 28 d Zyklus) sowie Myelom-spezische Antikörper (anticsi, Elotuzumab, 10/20 mg/kgkg iv, d1, 8, 15, 21; 28d Zyklus; anti-cd56, Lorovotuzumab, 75 mg/m 2, d1, 8, 15; 28d Zyklus) sind in der klinischen Erprobungsphase. In manchen Therapie-Schemata wird statt Alkeran /Melphalan ein anderes Alkylans (Cyclophosphamide, liposomales Doxorubicin, Bendamustin) verwendet. Prednison wird in manchen Schemata durch Dexamethason ersetzt. In der Konsolidationsphase finden wiederum Velcade /Bortezumib, Alkeran /Melphalan und Prednison bzw. Dexamethason bzw. alternativ Thalidomid /Revlimid Verwendung. Ziel ist die Vertiefung des therapeutischen Erfolges, so z.b. von einem partial response (PR) zu einem very good partial response (VGPR), bis hin zur stringent complete remission, (scr). Die Wertigkeit der Maintenance-Therapie mit Velcade /Bortezomib (1,3mg/m 2, d1, 4, 8,11 alle drei Monate) oder Thalidomid (50 mg/d p.o., Dauertherapie; nicht bei Hochrisiko-Patienten) bzw. Revlimid (10 mg/d 21/28d; nicht bei Hochrisiko-Patienten) wirkt wahrscheinlich vor allem günstig bei Patienten mit relativ guter Prognose (Thalidomid, Revlimid ). Sie ist auch heute noch umstritten, insbesondere, da bei einem Rezidiv die Salvage-Therapie zum Teil mit den gleichen schon in der Induktions- und Konsolidationsphase verwendeten Medikamenten erfolgreich ist. Für Revlimid wurde zudem eine Vermehrung der Sekundärkarzinome diskutiert. Ältere Patienten (>70 Jahre) können und sollen prinzipiell genauso behandelt werden wie jüngere Patienten, bei denen eine Stammzelltranplantation nicht mehr infrage kommt. Der zu erwartende therapeutische Vorteil muss aber noch sorgfältiger gegen die zu erwartenden, im Alter oft schwereren Nebenwirkungen der Therapie (Polyneuropathie) abgewogen werden, insbesondere wenn schwerwiegendere Begleiterkrankungen bekannt sind. Leider muss abschliessend gesagt werden dass trotz grossen in den letzten Jahren erzielten Fortschritten in der Therapie des Multiplen Myeloms und einer damit deutlich verbesserten Morbidität und Mortalität der Erkrankung auch heute eine Heilung des Multiplen Myeloms selten, wenn überhaupt, zu erwarten und möglich ist. 6
8 7
9 Fallbericht zu MGUS und Multiples Myelom Kommentar ((Ü1)) Anamnese des Patienten ((Ü1)) Anlässlich einer Routine-Untersuchung wird bei dem damals 75-jährigen Patienten eine Panzytopenie festgestellt. Der Patient ist beschwerdefrei, insbesondere bestehen keine Allgemeinsymptome wie Müdigkeit, Gewichtsverlust, Nachtschweiss oder Fieber. Er ist in regelmässiger hausärztlicher Kontrolle wegen eines Typ-2-Diabetes mellitus und einer arteriellen Hypertonie bei Adipositas und metabolischem Syndrom. Es liegt jedoch schon eine hypertensive Kardiomyopathie vor. Wegen eines intermittierendem Vorhofflimmerfns wurde er zweimal elektroablatiert. Zudem ist eine leichte Niereninsuffizienz bekannt. Die Zuweisung erfolgt zur weiteren Abklärung der Panzytopenie. Der Hausarzt äussert den Verdacht auf ein myelodysplastisches Syndrom. Angesichts einer relativ flächendeckend engen ärztlichen Überwachung wird heute eine Anämie häufig erfasst bevor sie symptomatisch ist. Die leichte Niereninsuffizienz, die man in der Folge der arteriellen Hypertonie und des Diabetes interpretierte, hätte wohl eine geringgradige Anämie erklären können, nicht aber eine Panzytopenie. Die gleichzeitige Verminderung des Hb, der Thrombozyten und der Neutrophilen Granulozyten hatten den Hausarzt den Verdacht auf eine genuine Knochenmarkserkrankung äussern lassen. Kommentar ((Ü1)) Befunde des Patienten ((Ü1)) Status ((Ü2)) Afebril, 35,5 C, guter AZ, leichte Stamm- Adipositas (BMI 25,0). Puls 60/min, unregelmässig, >10 ES/min; es fehlt der Puls der linken A. dorsalis pedis; Blutdruck 165/100 mmhg, kardiopulmonal kompensiert. Auch der abdominelle Befund ist unauffällig, insbesondere keine Organomegalie. Unauffälliger Neurostatus. Aktuelle Therapie ((Ü2)) Meto-Zerok 1x25 mg, Lisinopril 1x5 mg, Marcoumar n. V. Der erhöhte Blutdruck ist u.u. durch die Situation einer Erstuntersuchung erklärt. Der unregelmässige Puls hingegen weist wohl auf eine rhythmologische Instabilität auch nach den zwei stattgehabten Elektroablationen. Ein unauffälliger Untersuchungsbefund, insbesondere bei vermehrtem Bauchfett, schliesst eine Splenomegalie nicht aus, die in Zusammenhang mit einer Thrombopenie bzw. Neutropenie, wie sie bei diesem Patienten besteht, immer gesucht bzw. ausgeschlossen werden muss. Kommentar ((Ü1)) Es besteht eine antihypertensive Therapie und eine Prophylaxe bei intermittierendem Vorhofflimmern. Der Diabetes mellitus wird diätetisch kontrolliert. 8
10 RoutineLabor ((Ü2)) Hb 98 g/l, MCV 103 fl, MCHC 334 g/l, Reti 63 G/l/17 promille, Thrombozyten 172 G/l, Leukozyten 1,8 G/l, Neutrophile 0,8 G/l. CRP 7,7 mg/l, Kreatinin 123 µmol/l, GFR 50 ml/min, GPT 41 IU/l. Methylmalonsäure 322 nmol/l, Folat (Ec) 900 nmol/l Weitere Befunde ((Ü2)) Die Sonographie zeigt eine Splenomegalie (16 cm) und eine Lebersteatose, aber keine Zeichen eines zirrhotischen Umbaus bzw. einer portalen Hypertension. Erweitertes Labor ((Ü2)) Ferritin 295 mg/l, TSH 1,37 mu/l; Die Elektrophorese zeit einen M-Gradienten von 7,5 g/l, Paraprotein IgG kappa 12,83 g/l (6,64 14,94); IgA 0,68 g/l (0,57 3,24), IgM 0,21 g/l (0,39 1,57); sflc kappa 20,90 mg/l (3,30 19,40), lambda 3,78 mg/l (5,70 26,30), κ/λ 5,53 (0,26 1,65) Aspirat und Biopsie zeigen eine Infiltration des Knochenmarks durch asynchrone, klonale Plasmazellen (kappa; 30 40%); die Kongorot- Färbung ist negativ Kalzium 2,23 mmol/l; Erythropietin 68,8 IU/l Ein Ganzkörper-CT im Knochenfenster zeigt keine Osteolysen Die leichte Niereinsuffizienz reicht nicht, um das Ausmass der makrozytären, normochromen hyporegenerativen Anämie zu erklären. Ein Vitaminmangel besteht nicht (cave: Niereninsuffzien = leicht erhöhte Methylmalonsäurewerte). Mit einem Hypersplenismus könnte man nun die Neutropenie und die Thrombopenie gut erklären, wobei die Werte typischerweise, wie in diesem Falle, schwanken. Damit ändert sich die diagnostische Herausforderung nun gänzlich: Wir suchen nicht mehr nach einer Ursache für eine Panzytopenie, sondern nach einer Ursache für die Splenomegalie und nach einer Ursache für die Anämie, wobei es natürlich ein und dieselbe Ursache sein kann. Ein Eisenmangel oder eine Hypothyreose (als Ursache einer makrozytären Anämie) liegen nicht vor. Die Paraproteinämie wie auch der pathologische Quotient der freien Leichtketten beweisen die Plasmazelldyskrasie. Die grenzwertig tiefen Werte des IgAs und des IgMs weisen darauf hin, dass trotz der relativ niedrigen Spiegel des Paraproteins und der kappa-leichtkette im Serum die Krankheit schon fortgeschritten sein könnte (Suppression der normalen Plasmazellen durch den malignen Klon). Damit ist die Diagnose eines Multiplen Myeloms gestellt. Eine Amyloidose liegt nicht vor. Es besteht keine Hyperkalziämie und es finden sich keine Hinweise auf Osteolysen. 9
11 Die leichte Niereninsuffizienz ist vorbekannt und wahrscheinlich nicht Folge der Paraproteinämie bzw. vermehrten Leichtketten im Serum. Die Anämie hingegen kann nicht als renal interpretiert werden, was auf Grund der GFR schon vermutet werden konnte und durch die deutlich erhöhten Erythropoetinwerte nochmals bestätigt wird. Das Ausmass der Anämie wie auch der Abfall des Hb (Vorwerte>140 g/l) weisen auf den Zusammenhang mit dem Multiplen Myelom hin und lassen die Indikation zur Therapie stellen. Eine Amyloidose bestand nicht, die die Splenomegalie erklärt hätte. Eine Ursache für die Milzvergrösserung konnte bis heute nicht gefunden werden: kein HIV/HBV/HCV/EBV/CMV-Infekt; kein Hinweis auf eine Sphärozytose oder eine zweite lymphoproliferative oder myeloproliferative Erkrankung. Es wurde beschlossen, diesbezüglich ein expektatives Verhalten einzunehmen. Therapie Trotz des erhöhten Risikos für eine Polyneuropathie (Diabetes mellitus), entschlossen wir uns zu einer Therapie mit Bortezomib (Velcade ), Melphalan (Alkeran ) und Prednison. Nach anfänglichem Erfolg (Anstieg des Hb; der niedrige Paraprotein-Spiegel bzw. sflc kappa-spiegel konnten nicht als Verlaufsparameter dienen) zeigte sich aber eine Resistenz und die Therapie musste nach nur vier Zyklen abgesetzt werden. Der Patient befindet sich jetzt unter einer Therapie mit Lenalidomid (Revlimid ) und Dexamethason. Er ist wohlauf mit Hb-Werten um g/l. Es besteht eine leichtgradige Polyneuropathie. 10
12 Autor PD Dr. med. Boris Eugen Schleiffenbaum, Hirslanden Klinik Im Park, Bellariastrasse 38, 8038 Zürich Bibliographie ((Autor: Ref. bitte im Text mit eckigen Klammern [..] erwähnen)) 1. International Myeloma Working Group: Criteria for the classification of monoclonal gammopathies, multiple myeloma and related disorders: a report of the International Myeloma Working Group. Br J Haematol 2003; 121: Ludwig H, Durie BG, McCarthy P, Palumbo A, San Miguel J, Barlogie B, et al.: IMWG consensus on maintenance therapy in multiple myeloma. Blood 2012; 119: Weiss BM, Abadie J, Verma P, Howard RS, Kuehl WM: A monoclonal gammopathy precedes multiple myeloma in most patients. Blood 2009; 113: Cavo M, Rajkumar SV, Palumbo A, Moreau P, Orlowski R, Bladé J, et al.: IMWG consensus approach to the treatment of multiple myeloma patients who are candidates for autologous stem cell transplantation. Blood 2011; 117: Kumar S, Giralt S, Stadtmauer EA, Harousseau JL, Palumbo A, Bensinger W, et al.: Mobilization in myeloma revisited: IMWG consensus perspectives on stem cell collection following initial therapy with thalidomide-, lenalidomide-, or bortezomib-containing regimens. Blood 2009, 114: Armeson KE, Hill EG, Costa LJ: Tandem autologous vs autologous plus reduced intensity allogeneic transplantation in the upfront management of multiple myeloma: meta-analysis of trials with biological assignment. Bone Marrow Transplant 2012 sep 10; [Epub ahead of print]. 11
13 Fragen zu MGUS und Multiples Myelom Frage 1 Eine 57-jährige Patientin mit bekannter Osteoporose präsentiert sich mit akuter Lumbago. Ein Röntgenbild zeigt eine frische LWK2-Fraktur. Die BSR ist nicht erhöht, Hb und Kreatinin wie auch die Transaminasen sind normal. Die Elektrophorese zeigt keinen M-Gradienten. Welche der folgenen Aussagen ist korrekt? (Einfachauswahl, 1 richtige Antwort) a) Die vorbekannte Osteoporose erklärt das Bild ausreichend. Weitere Abklärung sind daher nicht indiziert. b) Die normale Elektrophorese schliesst die Diagnose eines Multiplen Myeloms aus. c) Als ergänzende Untersuchung sollte man hier noch eine Bence-Jones-Proteinurie mit dem Uro-Stix suchen. d) Bei begründetem klinischen Verdacht kann nur eine Knochenmarksuntersuchung ein Multiples Myelom beweisen oder ausschliessen. Frage 2 Bei einem 67-jährigen Patienten wurde ein M-Gradient von 37 g/l festgestellt. Welche der folgenen Aussagen ist korrekt? (Einfachauswahl, 1 richtige Antwort) a) Bei der Knochenmarkspunktion sollte neben Material für die morphologische Untersuchungen (Zytologie/Histologie) auch Material für molekulargenetische Analysen (PCR) entnommen werden, da nur aufgrund dieser Untersuchungen bei einem Multiplen Myelom die Risikostratifikation und damit die Planung der richtigen Thrapie erfolgen kann. b) Der Paraproteinspiegel ist so hoch, dass damit die Diagnose eines Multiplen Myeloms als gesichert gelten darf. c) Wenn keine konkomitierenden Krankheiten bestehen, sollte die Therapieplanung dieses Patienten nach einer Induktionsphase die autologe Stammzelltransplantation vorsehen. d) Angesichts der Höhe der Paraproteinämie und des damit weit fortgeschrittenen Stadiums der Erkrankung, wird die Behandlung des Multiplen Myeloms dieses Patienten eine allogene Stammzelltransplantation einschliessen müssen. Frage 3 Welche der folgenden Aussagen zur modernen Therapie des Multiplen Myeloms ist korrekt? (Einfachauswahl, 1 richtige Antwort) a) Moderne Therapeutika wie Velcade (Bortezomib) und Revlimid (Lenalidomid) sind zwar deutlich besser verträglich als die bisherige Therapie mit Alkylanzien und Kortikosteroiden, haben aber bisher das Gesamtüberleben der Patienten nicht verlängern können. b) Unter den neuen Therapeutika, wie z.b. Revlimid (Lenalidomid), treten keine schwerwiegenden hämatologischen Komplikationen (wie z.b. eine Neutropenie) mehr auf. c) Patienten unter Revlimid (Lenalidomid) und Thalidomid müssen wegen des Thromboembolie-Risikos oral antikoaguliert werden. d) Trotz des Risikos einer schmerzhaften Polyeuropathie gilt die Kombination Velcade (Bortezomib), Alkeran (Melphalan), Prednison heute als Standard-Induktionstherapie des Multiplen Myeloms. Frage 4 Bei einem 78-jährigen, bisher gesunden Patienten, der sich wegen Rückenschmerzen beim Hausarzt gemeldet hatte, wurde die Diagnose eines Multiplen Myeloms gestellt (Knochenmarksinfiltrationsgrad 70%). Welche der folgenden Aussagen ist korrekt? (Einfachauswahl, 1 richtige Antwort) a) Angesichts des Alters des Patienten verbietet sich eine Therapie mit Revlimid (Lenalidomid). 12
14 b) Die Therapie mit Velcade (Bortezomib), Alkeran (Melphalan) und Prednison kann ambulant erfolgen. Der Patient sollte aber engmaschig ärztlich überwacht werden, um mögliche Komplikationen frühzeitig erkennen und behandeln zu können. c) Sonst gesunde, ältere Patienten vertragen die Therapie mit Velcade (Bortezomib), Alkeran (Melphalan) und Prednison nicht und sollten daher konventionell induziert werden. d) Die autologe Stammzelltransplantation ist die Methode der Wahl, da sie durch die Anwendung der neuen Therapeutika wie Velcade (Bortezomib) und Revlimid (Lenalidomid) auch für ältere Patienten gut verträglich geworden ist. Frage 5 Welche der folgenen Aussagen zurm MGUS ist nicht korrekt? (Einfachauswahl, 1 richtige Antwort) a) Das MGUS ist prinzipiell nicht behandlungsbedürftig. b) Das MGUS ist prinzipiell nicht behandlungsbedürftig. Eine Polyneuropathie kann aber eine Indikation zur Therapie darstellen. c) Patienten mit einem MGUS sollten jährlich ärztlich nachkontrolliert werden (Klinik, Blutbild, Elektrophorese, Immunfixation, sflc; Kalzium). d) Das MGUS geht so gut wie immer einem Multiplen Myelom voraus (durchschnittliche Rate 10%/Jahr). 13
15 DOI / /a ((PX 25_Rubrik CME-Antworten)) Fragen zu MGUS und Multiples Myelom aus PRAXIS Nr. 24 Frage 1 Antwort d) ist richtig. Die vorbekannte Osteoporose könnte die Fraktur zwar auch erklären. Eine Osteoporose schliesst ein Multiples Myelom aber nicht aus, ebensowenig wie eine normale Elektrophorese, da in einem Teil der Fälle das Paraprotein nur durch die sensitivere Methode der Immunfixation erkannt wird, bzw. wenn ein Leichtketten-Myelom oder ein nicht-sezernierendes Myelom vorliegt. Der Nachweis von Bence-Jones Proteinen im Urin dient zwar der Diagnose des Leichtketten-Myeloms, der Uro-stix ist methodisch hierfür aber nicht geeignet. Nur die Knochenmarkspunktion kann ein Multiples Myelom beweisen oder ausschliessen. Frage 2 Antwort c) ist richtig. Die Diagnose eines Multiplen Myeloms muss immer zytologisch, besser noch histologisch erfolgen. PCR-Methoden spielen heute in der Diagnostik und Prognostik des Multiplen Meloms (im Gegensatz zur Zytogenetik) noch keine Rolle. Bei einem einem sonst gesunden Patenten kann auch im Alter von 67 Jahren noch eine autologe Stammzelltransplantation Teil der Therapie des Patienten mit Multiplem Myelom sein, da so mit der höchsten Wahrscheinlichkeit die tiefsten Remissionen erzielt werden können. Die allogene Stammzelltransplantation bietet wahrscheinlich auch beim jüngeren Patienten im Allgemeinen keine Vorteile gegenüber der autologen Transplantation und sollte beim älteren Patienten nicht durchgeführt werden. Frage 3 Antwort d) ist richtig. Auch das Gesamtüberleben der Patienten einem Multiplen Myelom wird durch die neuen Therapeutika wie Velcade (Bortezomib) und Revlimid (Lenalidomid) verlängert. Die Standard-Therapie des Multiplen Myeloms ist heute deswegen Velcade in der Kombination mit Alkeran (Melphalan) und Prednison. Aber auch die modernen Therapeutika, obwohl insgesamt sicher sehr gut verträglich, haben Nebenwirkungen: So kann es unter Revlimid durchaus zu schweren Neutropenien kommen, und sowohl Thalidomid wie auch Revlimid erhöhen das Thrombembolie-Risiko. Als Gegenmassnahme genügt hier jedoch die Gabe von Aspirin (1x100 mg/d), eine orale Antikoagulation ist nicht notwendig. Frage 4 Antwort b) ist richtig. Auch für ältere Patienten ist die Therapie mit Velcade (Bortezomib), Alkeran (Melphalan) und Prednison geeignet. Sie hat aber etwas mehr Komplikationen zu Folge als bei jüngeren Patienten, und muss daher ärztlich gut überwacht werden, kann aber ambulant erfolgen. Revlimid (Lenalidomid) und Velcade werden auch im Alter relativ gut vertragen und sind daher auch geeignet für die Therapie dieser Patientengruppe. Eine autologe Stammzelltransplantation verbietet sich aber in der Alterskategorie dieses Patienten weiterhin. Frage 5 Antwort d) ist richtig. 14
16 Das MGUS ist zwar prinzipiell nicht behandlungsbedürftig. Dies kann sich aber ändern, wenn eine Polyneutropathie auftritt, die mit Wahrscheinlichkeit auf das Paraprotein zurückgeführt werden muss. Patienten mit einem MGUS müssen jährlich ärztlich nachkontrolliert werden, um den Übergang in ein Multiples Mmyelom rechtzeitig zu erkennen und damit schwerwiegende Komplikationen zu verhindern. Auch wenn fast jedem Multiplen Myelom ein MGUS vorausgeht, so entwickelt sich bei weitem nicht aus jedem MGUS ein Multiples Myelom. Die Rate ist durchschnittlich nur 1% pro Jahr (und nicht 10%/Jahr); nur in der Hoch-Risiko Gruppe werden mehr als die Hälfte der Patienten in zehn Jahren ein Multiples Myelom entwickeln. 15
Workshop. Aktuelles zu Anämieabklärung, Eiweisselektrophorese, Gerinnung & Co. 42. Aerztekongress Arosa
 Workshop Aktuelles zu Anämieabklärung, Eiweisselektrophorese, Gerinnung & Co 42. Aerztekongress Arosa 29.3.2019 bernhard.gerber@eoc.ch Anämieabklärung JA Andere Auffälligkeiten im Blutbild? (Leukozyten,
Workshop Aktuelles zu Anämieabklärung, Eiweisselektrophorese, Gerinnung & Co 42. Aerztekongress Arosa 29.3.2019 bernhard.gerber@eoc.ch Anämieabklärung JA Andere Auffälligkeiten im Blutbild? (Leukozyten,
Multiples Myelomeine chronische Erkrankung?
 Multiples Myelomeine chronische Erkrankung? Dr. med. Gabriela Totok Medizinische Klinik und Poliklinik III Klinikum der Universität München - Großhadern 08.11.2009 Monoklonale Gammopathien Osteolysen B
Multiples Myelomeine chronische Erkrankung? Dr. med. Gabriela Totok Medizinische Klinik und Poliklinik III Klinikum der Universität München - Großhadern 08.11.2009 Monoklonale Gammopathien Osteolysen B
Kleine Laborkunde. Prof. Dr. Bernhard Wörmann. Plasmozytom / Multiples Myelom NRW Schwelm, 6. April 2019
 Kleine Laborkunde Prof. Dr. Bernhard Wörmann Plasmozytom / Multiples Myelom NRW Schwelm, 6. April 2019 Kleine Laborkunde Plasmazellen - Immunglobuline Produktion von Immunglobulinen Röteln Jede Plasmazelle
Kleine Laborkunde Prof. Dr. Bernhard Wörmann Plasmozytom / Multiples Myelom NRW Schwelm, 6. April 2019 Kleine Laborkunde Plasmazellen - Immunglobuline Produktion von Immunglobulinen Röteln Jede Plasmazelle
5. Entlebucher Hausärztetage. Von der EW-Elektrophorese zum Multiplen Myelom. 42. jährige Frau. Elektrophorese-Anwendung
 5. Entlebucher Hausärztetage Elektrophorese-Anwendung Von der EW-Elektrophorese zum Multiplen Myelom Prof. Dr. Dr. med. Walter A. Wuillemin Chefarzt Abteilung Hämatologie und Hämatologisches Zentrallabor
5. Entlebucher Hausärztetage Elektrophorese-Anwendung Von der EW-Elektrophorese zum Multiplen Myelom Prof. Dr. Dr. med. Walter A. Wuillemin Chefarzt Abteilung Hämatologie und Hämatologisches Zentrallabor
GERIATRIE. ÜBERRASCHEND VIELFÄLTIG.
 GERIATRIE. ÜBERRASCHEND VIELFÄLTIG. KASUISTIK Rückenschmerzen unklarer Genese bei einem 71-jährigen Mann Ein Fall von Dr. med. Gabriele Röhrig, Oberärztin Lehrstuhl für Geriatrie an der Universität zu
GERIATRIE. ÜBERRASCHEND VIELFÄLTIG. KASUISTIK Rückenschmerzen unklarer Genese bei einem 71-jährigen Mann Ein Fall von Dr. med. Gabriele Röhrig, Oberärztin Lehrstuhl für Geriatrie an der Universität zu
Diagnostische Abklärung des multiplen Myeloms
 Diagnostische Abklärung des multiplen Myeloms Heinz Gisslinger Univ. Klinik für Innere Medizin I Medizinische Universität Wien Abt. f. Hämatologie u. Hämostaseologie Wichtigste Herausforderung Differentialdiagnose
Diagnostische Abklärung des multiplen Myeloms Heinz Gisslinger Univ. Klinik für Innere Medizin I Medizinische Universität Wien Abt. f. Hämatologie u. Hämostaseologie Wichtigste Herausforderung Differentialdiagnose
Free light chain und Heavylight chain Tests zur Krankheitsbeurteilung beim multiplem Myelom
 Free light chain und Heavylight chain Tests zur Krankheitsbeurteilung beim multiplem Myelom H. Ludwig I. Medizinische Abteilung, Zentrum für Onkologie, Hämatologie und Palliativmedizin Wilhelminenspital,
Free light chain und Heavylight chain Tests zur Krankheitsbeurteilung beim multiplem Myelom H. Ludwig I. Medizinische Abteilung, Zentrum für Onkologie, Hämatologie und Palliativmedizin Wilhelminenspital,
(C) Hypercalcämie. (R) Niereninsuffizienz. (A) Unklare Anämie (meist normochrom, normozytär) (B) Knochenschmerzen (Osteopenie, pathologische
 Steckbrief Paraprotein 2. Pilatus-Symposium 9. November 2017 Diagnostik von Paraproteinämien Dr. Kornelius Arn, Oberarzt m.b.f. Abteilung Hämatologie und Hämatologisches Zentrallabor, Luzern Abnormes Immunglobulin
Steckbrief Paraprotein 2. Pilatus-Symposium 9. November 2017 Diagnostik von Paraproteinämien Dr. Kornelius Arn, Oberarzt m.b.f. Abteilung Hämatologie und Hämatologisches Zentrallabor, Luzern Abnormes Immunglobulin
Aktueller Stand zur Therapie des MM
 KEM. Kompetenz. Exzellenz. Menschlichkeit. Patiententag Multiples Myelom Aktueller Stand zur Therapie des MM Prof. Dr. med. Peter Reimer Direktor der Klinik für Hämatologie, Intern. Onkologie und Stammzelltransplantation
KEM. Kompetenz. Exzellenz. Menschlichkeit. Patiententag Multiples Myelom Aktueller Stand zur Therapie des MM Prof. Dr. med. Peter Reimer Direktor der Klinik für Hämatologie, Intern. Onkologie und Stammzelltransplantation
Kontrolluntersuchungen Welche und wie oft?
 Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Dr. med. Christian Taverna Kantonsspital Münsterlingen Kontrolluntersuchungen
Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Dr. med. Christian Taverna Kantonsspital Münsterlingen Kontrolluntersuchungen
Diagnostik und Prognose des multiplen Myeloms
 Diagnostik und Prognose des multiplen Myeloms Priv.-Doz. Dr. med. Christian Straka Chefarzt Abteilung Hämatologie H und Onkologie Argirov Klinik Starnberger See Multiples Myelom: Epidemiologie Inzidenz
Diagnostik und Prognose des multiplen Myeloms Priv.-Doz. Dr. med. Christian Straka Chefarzt Abteilung Hämatologie H und Onkologie Argirov Klinik Starnberger See Multiples Myelom: Epidemiologie Inzidenz
Patient Blood Management in der Orthopädie. 9. Juni Uniklinik Balgrist. Diagnose und Behandlung. der prä-operativen Anämie
 Diagnose und Behandlung der prä-operativen Anämie PD Dr. med. Boris Schleiffenbaum Ursachen für Morbidität und Mortalität nach Knie- und Hüftgelenksoperationen 1. Blutungen 2. Thrombembolien 3. Wundinfekte
Diagnose und Behandlung der prä-operativen Anämie PD Dr. med. Boris Schleiffenbaum Ursachen für Morbidität und Mortalität nach Knie- und Hüftgelenksoperationen 1. Blutungen 2. Thrombembolien 3. Wundinfekte
KliChi. Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Monoklonale Gammopathie. Dr. med. Bernhard Schlüter. Sommersemester
 Sommersemester 2009 Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Monoklonale Gammopathie Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium
Sommersemester 2009 Sommersemester 2012-1 - Klinische Chemie & Laboratoriumsdiagnostik Vorlesung: Monoklonale Gammopathie Dr. med. Bernhard Schlüter Centrum für Laboratoriumsmedizin Zentrallaboratorium
MULTIPLES MYELOM UND ANDERE PARAPROTEINAEMIEN. Dr. med. Peter Reismann Zweite Medizinische Klinik Semmelweis Universitaet
 MULTIPLES MYELOM UND ANDERE PARAPROTEINAEMIEN Dr. med. Peter Reismann Zweite Medizinische Klinik Semmelweis Universitaet PLASMAZELLEN Zentrale Zellen der humorale Immunabwehrsystem B-Zellen Ursprung Spezielle
MULTIPLES MYELOM UND ANDERE PARAPROTEINAEMIEN Dr. med. Peter Reismann Zweite Medizinische Klinik Semmelweis Universitaet PLASMAZELLEN Zentrale Zellen der humorale Immunabwehrsystem B-Zellen Ursprung Spezielle
Behandlungspfade Interdisziplinäres Onkologisches Zentrum Klinikum Ernst von Bergmann Potsdam. Multiples Myelom Stand Dezember 2017
 Multiples Myelom Stand Dezember 2017 Multiples Myelom: Diagnosesicherung Klinische Untersuchung Geriatrisches Assessment bei 70 J. Verdachtsdiagnose Myelom Labor-Untersuchung (Blut): Blutbild mit Differentialblutbild
Multiples Myelom Stand Dezember 2017 Multiples Myelom: Diagnosesicherung Klinische Untersuchung Geriatrisches Assessment bei 70 J. Verdachtsdiagnose Myelom Labor-Untersuchung (Blut): Blutbild mit Differentialblutbild
Diagnostik bei multiplem Myelom
 Diagnostik bei multiplem Myelom OÄ Dr.Daniela Voskova, PhD Klinik für Interne 3 Schwerpunkt Hämatologie und Onkologie 31.1.2017 20.01.2017 Hier können Sie unter dem Reiter "Einfügen" bei "Kopf- und Fußzeile"
Diagnostik bei multiplem Myelom OÄ Dr.Daniela Voskova, PhD Klinik für Interne 3 Schwerpunkt Hämatologie und Onkologie 31.1.2017 20.01.2017 Hier können Sie unter dem Reiter "Einfügen" bei "Kopf- und Fußzeile"
Multiples Myelom. Therapie älterer, nichttransplantierbarer Patienten. Christoph Renner
 Multiples Myelom Therapie älterer, nichttransplantierbarer Patienten Christoph Renner Altersdefinition beim Myelom? 1. Wann ist man alt? 1. Wann ist man nicht mehr transplantierbar? Altersdefinition beim
Multiples Myelom Therapie älterer, nichttransplantierbarer Patienten Christoph Renner Altersdefinition beim Myelom? 1. Wann ist man alt? 1. Wann ist man nicht mehr transplantierbar? Altersdefinition beim
Monoklonale Gammopathien: Paraproteindiagnos5k. Dr. Janina Hintze Frankfurt am Main, 16.09.2014 Janina.Hintze@bindingsite.de
 Monoklonale Gammopathien: Paraproteindiagnos5k Dr. Janina Hintze Frankfurt am Main, 16.09.2014 Janina.Hintze@bindingsite.de Übersicht ProdukAon der Immunglobuline (Ig) Nachweis monoklonaler Ig und Freier
Monoklonale Gammopathien: Paraproteindiagnos5k Dr. Janina Hintze Frankfurt am Main, 16.09.2014 Janina.Hintze@bindingsite.de Übersicht ProdukAon der Immunglobuline (Ig) Nachweis monoklonaler Ig und Freier
Anämie im Alter. Behandeln oder nicht behandeln, ist das eine Frage? Christian Kalberer
 Anämie im Alter Behandeln oder nicht behandeln, ist das eine Frage? Christian Kalberer Inhalt das normale Blutbild Definition, Häufigkeit der Anämie im Alter Beschreibung der Anämie Anämieabklärung nach
Anämie im Alter Behandeln oder nicht behandeln, ist das eine Frage? Christian Kalberer Inhalt das normale Blutbild Definition, Häufigkeit der Anämie im Alter Beschreibung der Anämie Anämieabklärung nach
Grundlagen und Therapieoptionen bei Non-Hodgkin Lymphomen
 Grundlagen und Therapieoptionen bei Non-Hodgkin Lymphomen Univ. Prof. Dr. Johannes Drach AKH Wien Univ. Klinik für Innere Medizin I Klinische Abteilung für Onkologie NHL: Grundlagen der Behandlungsmöglichkeiten
Grundlagen und Therapieoptionen bei Non-Hodgkin Lymphomen Univ. Prof. Dr. Johannes Drach AKH Wien Univ. Klinik für Innere Medizin I Klinische Abteilung für Onkologie NHL: Grundlagen der Behandlungsmöglichkeiten
Responsbeurteilung beim Myelom
 Responsbeurteilung beim Myelom Dr. Niklas Zojer 1.Medizinische Abteilung Zentrum für Onkologie und Hämatologie Wilhelminenspital Wien Myelom- und Lymphom-Symposium 26. Juni 2009 Monoklonales Paraprotein
Responsbeurteilung beim Myelom Dr. Niklas Zojer 1.Medizinische Abteilung Zentrum für Onkologie und Hämatologie Wilhelminenspital Wien Myelom- und Lymphom-Symposium 26. Juni 2009 Monoklonales Paraprotein
Monoklonale Gammopathie Unklarer Signifikanz (MGUS) Leitlinie
 Monoklonale Gammopathie Unklarer Signifikanz (MGUS) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Monoklonale Gammopathie Unklarer Signifikanz (MGUS) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Multiples Myelom: Diagnose und Therapie Fortschritte in den letzten 15 Jahren Aussicht auf die Zukunft Personalisierte Therapie Immuntherapie
 Multiples Myelom: Diagnose und Therapie Fortschritte in den letzten 15 Jahren Aussicht auf die Zukunft Personalisierte Therapie Immuntherapie Dr. med. Christian Taverna Leitender Arzt Onkologie Kantonsspital
Multiples Myelom: Diagnose und Therapie Fortschritte in den letzten 15 Jahren Aussicht auf die Zukunft Personalisierte Therapie Immuntherapie Dr. med. Christian Taverna Leitender Arzt Onkologie Kantonsspital
Multiples Myelom aktuelle Therapiestudien
 Multiples Myelom aktuelle Therapiestudien Martin Schreder 1.Med. Abteilung Zentrum für Onkologie und Hämatologie, Wilhelminenspital Wien Wien, 16.Oktober 2010 Klinische Studien Ablauf kontrollierte Behandlung
Multiples Myelom aktuelle Therapiestudien Martin Schreder 1.Med. Abteilung Zentrum für Onkologie und Hämatologie, Wilhelminenspital Wien Wien, 16.Oktober 2010 Klinische Studien Ablauf kontrollierte Behandlung
Johann Perné. Monoklonale Gammopathien MGUS Smoldering Myelom Multiples Myelom
 Monoklonale Gammopathien Smoldering Myelom Multiples Myelom Das Vorhandensein eines M-Gradienten in der Serum-Elektrophorese wird als monoklonale Gammopathie bezeichnet. Die Ursache ist eine maligne Proliferation
Monoklonale Gammopathien Smoldering Myelom Multiples Myelom Das Vorhandensein eines M-Gradienten in der Serum-Elektrophorese wird als monoklonale Gammopathie bezeichnet. Die Ursache ist eine maligne Proliferation
Monoklonale Gammopathie Unklarer Signifikanz (MGUS)
 Monoklonale Gammopathie Unklarer Signifikanz (MGUS) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Monoklonale Gammopathie Unklarer Signifikanz (MGUS) Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Das multiple Myelom Allgemeine Grundlagen. Dr. med. Christian Taverna Leitender Arzt Onkologie
 Das multiple Myelom Allgemeine Grundlagen Dr. med. Christian Taverna Leitender Arzt Onkologie Inhalt Was ist ein multiples Myelom? Welches sind mögliche Symptome? Welche Untersuchungen sind notwendig?
Das multiple Myelom Allgemeine Grundlagen Dr. med. Christian Taverna Leitender Arzt Onkologie Inhalt Was ist ein multiples Myelom? Welches sind mögliche Symptome? Welche Untersuchungen sind notwendig?
Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil
 CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
Das Multiple Myelom (Plasmozytom)
 Das Multiple Myelom (Plasmozytom) Diagnose und Therapie UNI-MED Verlag AG Bremen - London - Boston Inhaltsverzeichnis Inhaltsverzeichnis ^J Terminologie und Historie 12 1.1. Terminologie 12 1.2. Historie
Das Multiple Myelom (Plasmozytom) Diagnose und Therapie UNI-MED Verlag AG Bremen - London - Boston Inhaltsverzeichnis Inhaltsverzeichnis ^J Terminologie und Historie 12 1.1. Terminologie 12 1.2. Historie
Neue Substanzen beim Multiplen Myelom
 Neue Substanzen beim Multiplen Myelom A. Weltermann Abteilung für Innere Medizin I Zentrum für Hämatologie und Stammzelltransplantation, Hämostaseologie und medizinische Onkologie Krankenhaus der Elisabethinen
Neue Substanzen beim Multiplen Myelom A. Weltermann Abteilung für Innere Medizin I Zentrum für Hämatologie und Stammzelltransplantation, Hämostaseologie und medizinische Onkologie Krankenhaus der Elisabethinen
Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid
 10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
Multiples Myelom. Neues zu Diagnostik und Therapie. MKgS/Luzern PD Dr. med. Andreas Himmelmann. Zentrum Zug & OnkoZentrum Luzern
 Multiples Myelom Neues zu Diagnostik und Therapie MKgS/Luzern 22.10.2009 PD Dr. med. Andreas Himmelmann OHZ Onko-Hämatologisches Zentrum Zug & OnkoZentrum Luzern Übersicht: Allgemeine Einführung Neues
Multiples Myelom Neues zu Diagnostik und Therapie MKgS/Luzern 22.10.2009 PD Dr. med. Andreas Himmelmann OHZ Onko-Hämatologisches Zentrum Zug & OnkoZentrum Luzern Übersicht: Allgemeine Einführung Neues
Multiples Myelom. Dr. med. Matthias Grube. Klinik und Poliklinik für Innere Medizin III Klinikum der Universität Regensburg
 Multiples Myelom Dr. med. Matthias Grube Klinik und Poliklinik für Innere Medizin III Klinikum der Universität Regensburg Allgemeines Multiples Myelom (MM, Plasmozytom, Morbus Kahler) in Mitteleuropa ca.
Multiples Myelom Dr. med. Matthias Grube Klinik und Poliklinik für Innere Medizin III Klinikum der Universität Regensburg Allgemeines Multiples Myelom (MM, Plasmozytom, Morbus Kahler) in Mitteleuropa ca.
GFR / Kreatinin Clearance < 60 ml/min/ 1,73m 2. Δ Serum Kreatinin Anstieg > 50% Niereninsuffizienz ja oder nein? Wie heisst der Referent?
 Quelle: youtube.com Wie heisst der Referent? Niereninsuffizienz ja oder nein? GFR / Kreatinin Clearance < 60 ml/min/ 1,73m 2 Soll man die Kreatinin Clearance messen oder berechnen?? Δ Serum Kreatinin Anstieg
Quelle: youtube.com Wie heisst der Referent? Niereninsuffizienz ja oder nein? GFR / Kreatinin Clearance < 60 ml/min/ 1,73m 2 Soll man die Kreatinin Clearance messen oder berechnen?? Δ Serum Kreatinin Anstieg
CME-Labor 47: Monoklonale Gammopathien
 Zurich Open Repository and Archive University of Zurich Main Library Strickhofstrasse 39 CH-8057 Zurich www.zora.uzh.ch Year: 2016 CME-Labor 47: Monoklonale Gammopathien Annema, Wijtske; von Eckardstein,
Zurich Open Repository and Archive University of Zurich Main Library Strickhofstrasse 39 CH-8057 Zurich www.zora.uzh.ch Year: 2016 CME-Labor 47: Monoklonale Gammopathien Annema, Wijtske; von Eckardstein,
Aktuelle und künftige Therapieoptionen beim Multiplen Myelom Therapieeinleitung ja oder nein?
 Aktuelle und künftige Therapieoptionen beim Multiplen Myelom Vortrag vom Prof. Dr. med. Hermann Einsele, Direktor der Med. Klinik und Poliklinik II der Universität Würzburg, der AMM-Online zur Verfügung
Aktuelle und künftige Therapieoptionen beim Multiplen Myelom Vortrag vom Prof. Dr. med. Hermann Einsele, Direktor der Med. Klinik und Poliklinik II der Universität Würzburg, der AMM-Online zur Verfügung
Linzer Hämato-Onkologische Tage 8./9. Nov Ein Unglück kommt selten alleine. Karl Moyses LK Mostviertel Scheibbs Interne Abteilung
 Linzer Hämato-Onkologische Tage 8./9. Nov. 2013 Ein Unglück kommt selten alleine Karl Moyses LK Mostviertel Scheibbs Interne Abteilung Kasuistik Blutbild Leukozyten G/l 3,0-50a, - arterielle Hypteronie
Linzer Hämato-Onkologische Tage 8./9. Nov. 2013 Ein Unglück kommt selten alleine Karl Moyses LK Mostviertel Scheibbs Interne Abteilung Kasuistik Blutbild Leukozyten G/l 3,0-50a, - arterielle Hypteronie
Wann ist der richtige Zeitpunkt für den Beginn der Myelomtherapie?
 Wann ist der richtige Zeitpunkt für den Beginn der Myelomtherapie? Erklärungen und Zusammenfassung der Fragen und Antworten von Herrn DI Dr. Busch (Myelompatient), korrigiert und überarbeitet von Prof.
Wann ist der richtige Zeitpunkt für den Beginn der Myelomtherapie? Erklärungen und Zusammenfassung der Fragen und Antworten von Herrn DI Dr. Busch (Myelompatient), korrigiert und überarbeitet von Prof.
Auswirkungen der Neuen WHO- Klassifikation auf die histologische Knochenmarksdiagnostik
 46. Symposion der Deutschen Abteilung der IAP e. V. vom 26. 28. Februar 2010 in Bonn Histologisches Schnittseminar: Auswirkungen der Neuen WHO- Klassifikation auf die histologische Knochenmarksdiagnostik
46. Symposion der Deutschen Abteilung der IAP e. V. vom 26. 28. Februar 2010 in Bonn Histologisches Schnittseminar: Auswirkungen der Neuen WHO- Klassifikation auf die histologische Knochenmarksdiagnostik
Das Multiple Myelom Einführung in die Erkrankung und ihre Behandlung
 Prof. Dr. med. Peter Reimer Das Multiple Myelom Einführung in die Erkrankung und ihre Behandlung 32. Patienten - und Angehörigenseminar Essen, 9. November 2013 Multiples Myelom - Definition Maligne (bösartige)
Prof. Dr. med. Peter Reimer Das Multiple Myelom Einführung in die Erkrankung und ihre Behandlung 32. Patienten - und Angehörigenseminar Essen, 9. November 2013 Multiples Myelom - Definition Maligne (bösartige)
Multiples Myelom
 Multiples Myelom - 2013 Rudolf Weide Praxisklinik für Hämatologie und Onkologie Neversstrasse 5 56068 Koblenz Stammbaum der Blutbildung Myelomzelle Kaushansky K. N Engl J Med 2006;354:2034-2045 1 Entstehung
Multiples Myelom - 2013 Rudolf Weide Praxisklinik für Hämatologie und Onkologie Neversstrasse 5 56068 Koblenz Stammbaum der Blutbildung Myelomzelle Kaushansky K. N Engl J Med 2006;354:2034-2045 1 Entstehung
Praxisrelevante Fortschritte bei MM PatientInnen, die für eine Transplantation in Frage kommen. Braille Haus 18. Februar 2016
 Praxisrelevante Fortschritte bei MM PatientInnen, die für eine Transplantation in Frage kommen OA Priv. Doz. Dr. Niklas Zojer 1.Medizinische Abteilung Zentrum für Onkologie und Hämatologie & Palliativmedizin
Praxisrelevante Fortschritte bei MM PatientInnen, die für eine Transplantation in Frage kommen OA Priv. Doz. Dr. Niklas Zojer 1.Medizinische Abteilung Zentrum für Onkologie und Hämatologie & Palliativmedizin
Monoklonale Gammopathie unklarer Signifikanz. was tun?
 Monoklonale Gammopathie unklarer Signifikanz was tun? eberhard.gunsilius@i-med.ac.at Immunglobuline benefiziell vs. Autoaggression. Einfachster Test: Serumelektrophorese Indikation zur Serumelektrophorese
Monoklonale Gammopathie unklarer Signifikanz was tun? eberhard.gunsilius@i-med.ac.at Immunglobuline benefiziell vs. Autoaggression. Einfachster Test: Serumelektrophorese Indikation zur Serumelektrophorese
Neues bei Multiplem Myelom und Nierenbeteiligung
 Neues bei Multiplem Myelom und Nierenbeteiligung 9. Oberbayrische Nephrologietagung 15. Juni 2013 Dr. T. Unterweger Nomenklatur Multiples Myelom - Akkumulation eines Plasmazellklons (meist im KM) mit Bildung
Neues bei Multiplem Myelom und Nierenbeteiligung 9. Oberbayrische Nephrologietagung 15. Juni 2013 Dr. T. Unterweger Nomenklatur Multiples Myelom - Akkumulation eines Plasmazellklons (meist im KM) mit Bildung
Behandlungspfade Interdisziplinäres Onkologisches Zentrum Klinikum Ernst von Bergmann Potsdam. Hodgkin- Lymphom. Stand Dezember 2017
 Hodgkin- Lymphom Stand Dezember 2017 Erstdiagnose Notwendige Diagnostik Risikofaktoren Hodgkin- Lymphom Referenzhistologie obligat Klinische Untersuchung Anamnese (Alkoholschmerz) B- Symptome Fieber Nachtschweiß
Hodgkin- Lymphom Stand Dezember 2017 Erstdiagnose Notwendige Diagnostik Risikofaktoren Hodgkin- Lymphom Referenzhistologie obligat Klinische Untersuchung Anamnese (Alkoholschmerz) B- Symptome Fieber Nachtschweiß
Dr. med. Jeroen Goede FMH Innere Medizin, Medizinische Onkologie, Hämatologie FAMH Hämatologie Chefarzt Hämatologie Kantonsspital Winterthur
 Dr. med. Jeroen Goede FMH Innere Medizin, Medizinische Onkologie, Hämatologie FAMH Hämatologie Chefarzt Hämatologie Kantonsspital Winterthur Überblick Diagnostik Therapie 2 3 Hämatologische Neoplasien
Dr. med. Jeroen Goede FMH Innere Medizin, Medizinische Onkologie, Hämatologie FAMH Hämatologie Chefarzt Hämatologie Kantonsspital Winterthur Überblick Diagnostik Therapie 2 3 Hämatologische Neoplasien
Abklärung Niereninsuffizienz
 1. Frage Abklärung Niereninsuffizienz Niereninsuffizienz ja oder nein? Soll man die Kreatinin Clearance messen oder berechnen?? Definition Niereninsuffizienz GFR / Kreatinin Clearance < 60 ml/min/ 1,73m
1. Frage Abklärung Niereninsuffizienz Niereninsuffizienz ja oder nein? Soll man die Kreatinin Clearance messen oder berechnen?? Definition Niereninsuffizienz GFR / Kreatinin Clearance < 60 ml/min/ 1,73m
Akutes Nierenversagen unter ART. Silvia Ernst Spitalzentrum Biel
 Akutes Nierenversagen unter ART Silvia Ernst Spitalzentrum Biel 1 Herr X.Y. 46 jährig HIV-Infektion CDC Stadium A3 ED 1/22 Transmission heterosexuell Katatone Schizophrenie mit akustischen Halluzinationen
Akutes Nierenversagen unter ART Silvia Ernst Spitalzentrum Biel 1 Herr X.Y. 46 jährig HIV-Infektion CDC Stadium A3 ED 1/22 Transmission heterosexuell Katatone Schizophrenie mit akustischen Halluzinationen
XXIV. Intensivkurs Innere Medizin
 XXIV. Intensivkurs Innere Medizin Dr. med. Christian Bogner (MM) und Chronisch Lymphatische Leukämie (CLL) Dr. med. Christian Bogner XXIV. Intensivkurs Innere Medizin Pathophysiologie Fallbeispiel Patient
XXIV. Intensivkurs Innere Medizin Dr. med. Christian Bogner (MM) und Chronisch Lymphatische Leukämie (CLL) Dr. med. Christian Bogner XXIV. Intensivkurs Innere Medizin Pathophysiologie Fallbeispiel Patient
Publikumsvortrag an der AndreasKlinik Cham Zug vom 30. Mai 2006 Leukämien bei älteren Patienten: Neue diagnostische und therapeutische Möglichkeiten
 Publikumsvortrag an der AndreasKlinik Cham Zug vom 30. Mai 2006 Leukämien bei älteren Patienten: Neue diagnostische und therapeutische Möglichkeiten PD Dr.med. Andreas Himmelmann PD Dr.med. Andreas Himmelmann
Publikumsvortrag an der AndreasKlinik Cham Zug vom 30. Mai 2006 Leukämien bei älteren Patienten: Neue diagnostische und therapeutische Möglichkeiten PD Dr.med. Andreas Himmelmann PD Dr.med. Andreas Himmelmann
MULTIPLES MYELOM Partizipier in Genesung
 MULTIPLES MYELOM Partizipier in Genesung Lerne mehr und Spende Marlies Van Hoef, MD, PhD, MBA Multiples Myelom Krankheit von Kahler wurde zuerst diagnostiziert in 1848 Bösartige Abnormalität des Plasmazellen;
MULTIPLES MYELOM Partizipier in Genesung Lerne mehr und Spende Marlies Van Hoef, MD, PhD, MBA Multiples Myelom Krankheit von Kahler wurde zuerst diagnostiziert in 1848 Bösartige Abnormalität des Plasmazellen;
Aktuelle Therapiestrategien bei Patienten mit multiplem Myelom
 Aktuelle strategien bei Patienten mit multiplem Myelom Univ. Prof. Dr. Heinz Ludwig I. Medizinische Abteilung Zentrum für Onkologie und Hämatologie Wilhelminenspital Wer benötigt eine Behandlung? Patienten
Aktuelle strategien bei Patienten mit multiplem Myelom Univ. Prof. Dr. Heinz Ludwig I. Medizinische Abteilung Zentrum für Onkologie und Hämatologie Wilhelminenspital Wer benötigt eine Behandlung? Patienten
Nierenerkrankungen Teil 2
 Nierenerkrankungen Teil 2 Chronische Nierenerkrankungen Gemeinschaftspraxis Drs. Gäckler/ Jäkel/ Fricke/ Reinsch Nephrologische und diabetologische Schwerpunktpraxis Bürkle-de-la-Camp-Platz 2, 44789 Bochum
Nierenerkrankungen Teil 2 Chronische Nierenerkrankungen Gemeinschaftspraxis Drs. Gäckler/ Jäkel/ Fricke/ Reinsch Nephrologische und diabetologische Schwerpunktpraxis Bürkle-de-la-Camp-Platz 2, 44789 Bochum
Multiples Myelom: Behandlungsmöglichkeiten im Rezidiv. Univ.-Doz. Dr. Eberhard Gunsilius Hämatologie & Onkologie Universitätsklinik Innsbruck
 Multiples Myelom: Behandlungsmöglichkeiten im Rezidiv Univ.-Doz. Dr. Eberhard Gunsilius Hämatologie & Onkologie Universitätsklinik Innsbruck Myelom: Therapeutisches Arsenal Verbesserung der Prognose Interferon,
Multiples Myelom: Behandlungsmöglichkeiten im Rezidiv Univ.-Doz. Dr. Eberhard Gunsilius Hämatologie & Onkologie Universitätsklinik Innsbruck Myelom: Therapeutisches Arsenal Verbesserung der Prognose Interferon,
Immunhämatologische Resultate in der Hausarztpraxis
 Immunhämatologische Resultate in der Hausarztpraxis Interpretation, Konsequenzen Dr. med. T. Braschler, OAmbF Hämatologie 08.03.2018 Inhalt Der Immunhämatologische Befund Type and Screen Untersuchung Bedeutung
Immunhämatologische Resultate in der Hausarztpraxis Interpretation, Konsequenzen Dr. med. T. Braschler, OAmbF Hämatologie 08.03.2018 Inhalt Der Immunhämatologische Befund Type and Screen Untersuchung Bedeutung
Update hämatologische Milzerkrankungen
 Update hämatologische Milzerkrankungen Axel Rüfer Abteilung Hämatologie und Hämatologisches Zentrallabor 1. Hospitalisation in auswärtigem Spital Hämoglobin 58 g/l Transfusion von drei Erythrozytenkonzentraten
Update hämatologische Milzerkrankungen Axel Rüfer Abteilung Hämatologie und Hämatologisches Zentrallabor 1. Hospitalisation in auswärtigem Spital Hämoglobin 58 g/l Transfusion von drei Erythrozytenkonzentraten
Definition modifiziert nach IMWG; Br J Haematol ; 2003
 Definition modifiziert nach IMWG; Br J Haematol; 2003 MGUS/SMM das Muttermal der Hämatologie? Myelomagenesis - Genetischer Hintergrund Foundermutationen bereits im F MGUS Stadium detektierbar Morgan et
Definition modifiziert nach IMWG; Br J Haematol; 2003 MGUS/SMM das Muttermal der Hämatologie? Myelomagenesis - Genetischer Hintergrund Foundermutationen bereits im F MGUS Stadium detektierbar Morgan et
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien. Ein Vortrag von Univ. Prof. Dr. Heinz Ludwig Wilhelminenspital Wien
 Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Heinz Ludwig Wilhelminenspital Wien Multiples Myelom I. Medizinische Abteilung, Zentrum für
Welt Lymphom Tag Seminar für Patienten und Angehörige 15. September 2007 Wien Ein Vortrag von Univ. Prof. Dr. Heinz Ludwig Wilhelminenspital Wien Multiples Myelom I. Medizinische Abteilung, Zentrum für
Wichtige Laborparameter beim Myelom
 Wichtige Laborparameter beim Myelom OA Dr. Adalbert Weißmann 1. Medizinische Abteilung mit Onkologie Zentrum für Onkologie und Hämatologie Wilhelminenspital Wien exposed surface hidden surface Kappa exposed
Wichtige Laborparameter beim Myelom OA Dr. Adalbert Weißmann 1. Medizinische Abteilung mit Onkologie Zentrum für Onkologie und Hämatologie Wilhelminenspital Wien exposed surface hidden surface Kappa exposed
Autoren: PD Dr. Kai Neben, Dr. med. Marc-S. Raab, Dr. med. Jens Hillengass
 Kongressbericht vom ASH 2009 aus New Orleans Autoren: PD Dr. Kai Neben, Dr. med. Marc-S. Raab, Dr. med. Jens Hillengass Dieses Jahr stand der Kongress ganz im Fokus des Multiplen Myeloms. Zeitweise fanden
Kongressbericht vom ASH 2009 aus New Orleans Autoren: PD Dr. Kai Neben, Dr. med. Marc-S. Raab, Dr. med. Jens Hillengass Dieses Jahr stand der Kongress ganz im Fokus des Multiplen Myeloms. Zeitweise fanden
Monoklonale Gammopathien: Diagnostik und Verlaufskontrolle
 Monoklonale Gammopathien: Diagnostik und Verlaufskontrolle Dr. Nicolas Graf Hämatologie-Onkologie, Schwerpunkt Multiples Myelom Schön-Klinik Starnberger See, Berg Übersicht Einleitung Nachweis monoklonaler
Monoklonale Gammopathien: Diagnostik und Verlaufskontrolle Dr. Nicolas Graf Hämatologie-Onkologie, Schwerpunkt Multiples Myelom Schön-Klinik Starnberger See, Berg Übersicht Einleitung Nachweis monoklonaler
Textskript Monoklonale Gammopathie Dr. med. Bernhard Schlüter
 Textskript Monoklonale Gammopathie Dr. med. Bernhard Schlüter Definition Der Begriff Monoklonale Gammopathie beschreibt die Vermehrung eines durch Entartung eines B- Zell-Klones gebildeten monoklonalen
Textskript Monoklonale Gammopathie Dr. med. Bernhard Schlüter Definition Der Begriff Monoklonale Gammopathie beschreibt die Vermehrung eines durch Entartung eines B- Zell-Klones gebildeten monoklonalen
Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms
 AMB 2006, 40, 89 Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms Mit Thalidomid, Lenalidomid und Bortezomib (Velcade ) stehen inzwischen neue Wirkstoffe für die
AMB 2006, 40, 89 Wirksamkeit und Sicherheit von Thalidomid in der primären Therapie des multiplen Myeloms Mit Thalidomid, Lenalidomid und Bortezomib (Velcade ) stehen inzwischen neue Wirkstoffe für die
Definition. Entzündliche abakterielle Nierenerkrankungen mit Befall unterchiedlicher glomerulärer Strukturen
 Glomerulonephritis Definition Entzündliche abakterielle Nierenerkrankungen mit Befall unterchiedlicher glomerulärer Strukturen Ursachen Insgesamt eher seltene Erkrankung Zweithäufigste Ursache einer chronischen
Glomerulonephritis Definition Entzündliche abakterielle Nierenerkrankungen mit Befall unterchiedlicher glomerulärer Strukturen Ursachen Insgesamt eher seltene Erkrankung Zweithäufigste Ursache einer chronischen
2 State of the art lectures
 Plasma-Zell Myelom Prof Jakob R Passweg Normale B-Lymphozyten Ausreifung und Entsprechungen der B-Zell Neoplasien Plasma-Zell Myelom Neoplasie der terminal differenzierten Zelle MGUS Smoldering Myelom
Plasma-Zell Myelom Prof Jakob R Passweg Normale B-Lymphozyten Ausreifung und Entsprechungen der B-Zell Neoplasien Plasma-Zell Myelom Neoplasie der terminal differenzierten Zelle MGUS Smoldering Myelom
Laborhandbuch. Monoklonale Gammopathien. Einführung
 Laborhandbuch Monoklonale Gammopathien Einführung Monoklonale Gammopathien sind charakterisiert durch eine übermässige Produktion von monoklonalem Immunglobulin, das in derartigem Überschuss gebildet wird,
Laborhandbuch Monoklonale Gammopathien Einführung Monoklonale Gammopathien sind charakterisiert durch eine übermässige Produktion von monoklonalem Immunglobulin, das in derartigem Überschuss gebildet wird,
Vorwort der Autoren. Geschätzte Leserin, geschätzter Leser
 Das Multiple Myelom Vorwort der Autoren Geschätzte Leserin, geschätzter Leser Aus zahlreichen Gesprächen wissen wir, dass es für Betroffene und Angehörige oft sehr schwierig ist, sich ein klares Bild über
Das Multiple Myelom Vorwort der Autoren Geschätzte Leserin, geschätzter Leser Aus zahlreichen Gesprächen wissen wir, dass es für Betroffene und Angehörige oft sehr schwierig ist, sich ein klares Bild über
Plasma-Zell Myelom. Prof Jakob R Passweg
 Plasma-Zell Myelom Prof Jakob R Passweg Normale B-Lymphozyten Ausreifung und Entsprechungen der B-Zell Neoplasien Plasma-Zell Myelom Neoplasie der terminal differenzierten Zelle Klonale Evolution MGUS
Plasma-Zell Myelom Prof Jakob R Passweg Normale B-Lymphozyten Ausreifung und Entsprechungen der B-Zell Neoplasien Plasma-Zell Myelom Neoplasie der terminal differenzierten Zelle Klonale Evolution MGUS
Morbus Waldenström. Diagnostische Empfehlung. Methode Antikoagulans Empfehlung. Zytomorphologie EDTA obligat
 1/7 Morbus Waldenström Diagnostische Empfehlung Methode Antikoagulans Empfehlung Zytomorphologie EDTA obligat Immunphänotypisierung EDTA oder Heparin obligat Chromosomenanalyse Heparin fakultativ FISH
1/7 Morbus Waldenström Diagnostische Empfehlung Methode Antikoagulans Empfehlung Zytomorphologie EDTA obligat Immunphänotypisierung EDTA oder Heparin obligat Chromosomenanalyse Heparin fakultativ FISH
Düsseldorfer Ergebnisse zur Hochdosis-Chemotherapie mit autologer Blutstammzelltransplantation bei Patienten mit Multiplem Myelom.
 Aus der Klinik für Hämatologie, Onkologie und Klinische Immunologie Direktor: Univ.-Prof. Dr. med. Rainer Haas Düsseldorfer Ergebnisse zur Hochdosis-Chemotherapie mit autologer Blutstammzelltransplantation
Aus der Klinik für Hämatologie, Onkologie und Klinische Immunologie Direktor: Univ.-Prof. Dr. med. Rainer Haas Düsseldorfer Ergebnisse zur Hochdosis-Chemotherapie mit autologer Blutstammzelltransplantation
Ergänzende Stichpunkte vom 29. Deutschen Krebskongress der Deutschen Krebsgesellschaft ( Februar 2010 in Berlin)
 Verfasserin: Dr. med. Sabine Schock, PMM Mittelhessen Ergänzende Stichpunkte vom 29. Deutschen Krebskongress der Deutschen Krebsgesellschaft (24. 27. Februar 2010 in Berlin) Erstlinientherapie junger Patient
Verfasserin: Dr. med. Sabine Schock, PMM Mittelhessen Ergänzende Stichpunkte vom 29. Deutschen Krebskongress der Deutschen Krebsgesellschaft (24. 27. Februar 2010 in Berlin) Erstlinientherapie junger Patient
CME-Sonographie 47: Ungewöhnliches Steal-Phänomen
 Zurich Open Repository and Archive University of Zurich Main Library Strickhofstrasse 39 CH-8057 Zurich www.zora.uzh.ch Year: 2012 CME-Sonographie 47: Ungewöhnliches Steal-Phänomen Thalhammer, C Abstract:
Zurich Open Repository and Archive University of Zurich Main Library Strickhofstrasse 39 CH-8057 Zurich www.zora.uzh.ch Year: 2012 CME-Sonographie 47: Ungewöhnliches Steal-Phänomen Thalhammer, C Abstract:
Systemische Leichtketten-Amyloidose 03.03.14
 Systemische Leichtketten-Amyloidose 03.03.14 Amyloidosen Proteinfehlfaltungs- und Ablagerungskrankheiten Lokale systemische Erkrankung Gutartig tödlicher Verlauf Erblich erworben Assoziiert mit dem Altern
Systemische Leichtketten-Amyloidose 03.03.14 Amyloidosen Proteinfehlfaltungs- und Ablagerungskrankheiten Lokale systemische Erkrankung Gutartig tödlicher Verlauf Erblich erworben Assoziiert mit dem Altern
Fallvorstellung 8. Mai 2007
 Fallvorstellung 8. Mai 2007 67jährige Patientin mit CLL und Fieber 5 Süd Anamnese Aktuelle Anamnese: Aufnahme 13.3.2007 bei Fieber bis 38.8 C, Müdigkeit, Nachtschweiß Bisherige Anamnese: CLL ED 1997 Z.n.
Fallvorstellung 8. Mai 2007 67jährige Patientin mit CLL und Fieber 5 Süd Anamnese Aktuelle Anamnese: Aufnahme 13.3.2007 bei Fieber bis 38.8 C, Müdigkeit, Nachtschweiß Bisherige Anamnese: CLL ED 1997 Z.n.
Multiples Myelom für Anfänger
 Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Univ. Prof. Dr. Heinz Ludwig Wilhelminenspital Wien Multiples Myelom für
Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Univ. Prof. Dr. Heinz Ludwig Wilhelminenspital Wien Multiples Myelom für
Behandlung des Rezidives
 Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Univ. Prof. Dr. Heinz Ludwig Wilhelminenspital Wien Behandlung des Rezidives
Internationales Multiples Myelom Symposium für PatientInnen und Angehörige 5.Mai 2007 Kardinal König Haus in Wien Ein Vortrag von Univ. Prof. Dr. Heinz Ludwig Wilhelminenspital Wien Behandlung des Rezidives
Im Fokus: Maligne Lymphome und multiples Myelom ERIKA LERCH ONKOLOGIE 4/
 Das multiple Myelom Therapieoptionen: Entwicklungen seit 1962 In den letzten 10 Jahren hat die Behandlung des multiplen Myeloms sehr grosse Fortschritte erfahren. Die seit einigen Jahren eingesetzten neuen
Das multiple Myelom Therapieoptionen: Entwicklungen seit 1962 In den letzten 10 Jahren hat die Behandlung des multiplen Myeloms sehr grosse Fortschritte erfahren. Die seit einigen Jahren eingesetzten neuen
Sportmedizin in der Hausarztpraxis
 Sportmedizin in der Hausarztpraxis Sportärztliche Untersuchung: Fokus Herz Asthma und Leistungssport: Vorgehen bei der Medikamentenwahl Sportlabor Welchen Patienten empfehlen wir Sport Herzkreislauferkrankungen
Sportmedizin in der Hausarztpraxis Sportärztliche Untersuchung: Fokus Herz Asthma und Leistungssport: Vorgehen bei der Medikamentenwahl Sportlabor Welchen Patienten empfehlen wir Sport Herzkreislauferkrankungen
Sicherheitsrelevante Hinweise für medizinische Fachkreise
 Sicherheitsrelevante Hinweise für medizinische Fachkreise für die Therapie des multiplen Myeloms mit Bortezomib in Abhängigkeit von den unterschiedlichen Indikationen im Rahmen der Indikationserweiterung
Sicherheitsrelevante Hinweise für medizinische Fachkreise für die Therapie des multiplen Myeloms mit Bortezomib in Abhängigkeit von den unterschiedlichen Indikationen im Rahmen der Indikationserweiterung
Paclitaxel Gemcitabin
 135 16 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2.1 Paclitaxel Gemcitabin Paclitaxel Gemcitabin Fortgeschrittenes Urothelkarzinom
135 16 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2.1 Paclitaxel Gemcitabin Paclitaxel Gemcitabin Fortgeschrittenes Urothelkarzinom
UNIVERSITÄTSKLINIKUM HAMBURG- EPPENDORF
 UNIVERSITÄTSKLINIKUM HAMBURG- EPPENDORF Interdisziplinäre Klinik und Poliklinik für Stammzelltransplantation Onkologisches Zentrum Direktor: Prof. Dr. Nicolaus Kröger Polyklonale Erhöhung der freien Leichtketten
UNIVERSITÄTSKLINIKUM HAMBURG- EPPENDORF Interdisziplinäre Klinik und Poliklinik für Stammzelltransplantation Onkologisches Zentrum Direktor: Prof. Dr. Nicolaus Kröger Polyklonale Erhöhung der freien Leichtketten
Kurzprotokoll. GMMG-HD4 / HOVON-65 Studie
 Kurzprotokoll GMMG-HD4 / HOVON-65 Studie 2.1 Titel Hochdosistherapie und autologe Stammzelltransplantation gefolgt von einer Thalidomid-Erhaltungstherapie vs. Bortezomib plus Hochdosistherapie und autologe
Kurzprotokoll GMMG-HD4 / HOVON-65 Studie 2.1 Titel Hochdosistherapie und autologe Stammzelltransplantation gefolgt von einer Thalidomid-Erhaltungstherapie vs. Bortezomib plus Hochdosistherapie und autologe
der Beitrag der Labordiagnostik im modernen Umfeld der Krebstherapie
 der Beitrag der Labordiagnostik im modernen Umfeld der Krebstherapie Was können die Labors heute leisten? Prof. Dr. med. Wolfgang Korte Chefarzt und CEO Zentrum für Labormedizin St. Gallen Der klinische
der Beitrag der Labordiagnostik im modernen Umfeld der Krebstherapie Was können die Labors heute leisten? Prof. Dr. med. Wolfgang Korte Chefarzt und CEO Zentrum für Labormedizin St. Gallen Der klinische
Leukämie (CML) Was ist Chronische Myeloische Leukämie? Download. Published on Novartis Austria (https://www.novartis.at)
 Published on Novartis Austria (https://www.novartis.at) Home > Printer-friendly PDF > Leukämie (CML) Leukämie (CML) Was ist Chronische Myeloische Leukämie? Die chronische myeloische Leukämie (CML) ist
Published on Novartis Austria (https://www.novartis.at) Home > Printer-friendly PDF > Leukämie (CML) Leukämie (CML) Was ist Chronische Myeloische Leukämie? Die chronische myeloische Leukämie (CML) ist
Diagnostisches Vorgehen bei Leberraumforderungen. H. Diepolder
 Diagnostisches Vorgehen bei Leberraumforderungen H. Diepolder Bei 20% aller Routinesonographien fällt eine Leberraumforderung auf Problem Problem Bei 20% aller Routinesonographien fällt eine Leberraumforderung
Diagnostisches Vorgehen bei Leberraumforderungen H. Diepolder Bei 20% aller Routinesonographien fällt eine Leberraumforderung auf Problem Problem Bei 20% aller Routinesonographien fällt eine Leberraumforderung
Morbus Waldenström. PD Dr. Manfred Hensel Medizinische Klinik und Poliklinik V Universität Heidelberg
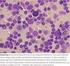 Morbus Waldenström PD Dr. Manfred Hensel Medizinische Klinik und Poliklinik V Universität Heidelberg Jan Gösta Waldenström 1906-1996 Biographie: Jan Gösta Waldenström war der Sohn von Johann Henning Waldenström
Morbus Waldenström PD Dr. Manfred Hensel Medizinische Klinik und Poliklinik V Universität Heidelberg Jan Gösta Waldenström 1906-1996 Biographie: Jan Gösta Waldenström war der Sohn von Johann Henning Waldenström
Wirken, Handeln, Begegnen, von Mensch zu Mensch, Gemeinsam in christlicher Gesinnung.
 NEBENWIRKUNGSMANAGEMENT BEI DER THERAPIE DES MULTIPLEN MYELOMS Mathias Nietzke Leiter Zytostatika-Abteilung Zentral-Apotheke St.-Johannes-Hospital Dortmund Wirken, Handeln, Begegnen, von Mensch zu Mensch,
NEBENWIRKUNGSMANAGEMENT BEI DER THERAPIE DES MULTIPLEN MYELOMS Mathias Nietzke Leiter Zytostatika-Abteilung Zentral-Apotheke St.-Johannes-Hospital Dortmund Wirken, Handeln, Begegnen, von Mensch zu Mensch,
Morbus Waldenström Leitlinie
 Morbus Waldenström Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie und Medizinische
Morbus Waldenström Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft für Hämatologie und Medizinische
Möglichkeiten und sinnvolle Grenzen der präoperativen Diagnostik des multimorbiden Dialysepatienten aus internistisch-kardiologischer Sicht
 Möglichkeiten und sinnvolle Grenzen der präoperativen Diagnostik des multimorbiden Dialysepatienten aus internistisch-kardiologischer Sicht Dr. med. Michael Liebetrau 1 Kardiovaskuläre Risikofaktoren 2
Möglichkeiten und sinnvolle Grenzen der präoperativen Diagnostik des multimorbiden Dialysepatienten aus internistisch-kardiologischer Sicht Dr. med. Michael Liebetrau 1 Kardiovaskuläre Risikofaktoren 2
Wie (un-)sicher ist die Computertomographie (Cardio-CT)? Dr. med. D. Enayat
 Wie (un-)sicher ist die Computertomographie (Cardio-CT)? Dr. med. D. Enayat Cardio-CT - Welche Untersuchungen sind möglich? Kalk-Score (Agatston-Score) = Gesamtlast der Kalkeinlagerung Koronarangiographie
Wie (un-)sicher ist die Computertomographie (Cardio-CT)? Dr. med. D. Enayat Cardio-CT - Welche Untersuchungen sind möglich? Kalk-Score (Agatston-Score) = Gesamtlast der Kalkeinlagerung Koronarangiographie
Onkologische Therapieoptionen bei Niereninsuffizienz. Stellenwert der High Cut Off Dialyse beim multiplen Myelom
 Onkologische Therapieoptionen bei Niereninsuffizienz Stellenwert der High Cut Off Dialyse beim multiplen Myelom 3. Brandenburger Nephrologie Kolleg 6. 7. Juni 2013 Dr. med. Annegret Kunitz Innere Medizin
Onkologische Therapieoptionen bei Niereninsuffizienz Stellenwert der High Cut Off Dialyse beim multiplen Myelom 3. Brandenburger Nephrologie Kolleg 6. 7. Juni 2013 Dr. med. Annegret Kunitz Innere Medizin
Anämie. André Tichelli
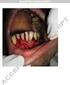 Anämie André Tichelli Anämie ist die häufigste Blutbildveränderung Alters- und Geschlechtsverteilung im Laufe des Lebens - Wachstum - Physiologischer Verlust bei der Frau: Menstruationen Schwangerschaft
Anämie André Tichelli Anämie ist die häufigste Blutbildveränderung Alters- und Geschlechtsverteilung im Laufe des Lebens - Wachstum - Physiologischer Verlust bei der Frau: Menstruationen Schwangerschaft
Aktuelle klinische Studien in Österreich
 Aktuelle klinische Studien in Österreich Dr. E. Müldür Wilhelminenspital,Zentrum für Hämatologie- u. Onkologie Vorstand: Univ.Prof.Dr.H.Ludwig Aktuelle klinische Studien in Österreich -LD-STUDIE -BBD-STUDIE
Aktuelle klinische Studien in Österreich Dr. E. Müldür Wilhelminenspital,Zentrum für Hämatologie- u. Onkologie Vorstand: Univ.Prof.Dr.H.Ludwig Aktuelle klinische Studien in Österreich -LD-STUDIE -BBD-STUDIE
HD6 Studie der GMMG-Studiengruppe (German-Speaking Myeloma Multicenter Group) in Heidelberg rekrutiert seit Juni 2015
 HD6 Studie der GMMG-Studiengruppe (German-Speaking Myeloma Multicenter Group) in Heidelberg rekrutiert seit Juni 2015 - ein Beitrag von Dr. Annemarie Angerer, Dr. Uta Bertsch, Dr. Jana Schlenzka, Dr. Barbara
HD6 Studie der GMMG-Studiengruppe (German-Speaking Myeloma Multicenter Group) in Heidelberg rekrutiert seit Juni 2015 - ein Beitrag von Dr. Annemarie Angerer, Dr. Uta Bertsch, Dr. Jana Schlenzka, Dr. Barbara
Pathophysiologie: Fallbeispiele Hämatologie
 Fall 8 Pathophysiologie: Fallbeispiele Hämatologie Eine Frau mittleren Alters fühlt sich seit zwei Wochen schwach und zunehmend müde. Ihr Familienarzt hat eine Laboruntersuchung durchgeführt und hat sie
Fall 8 Pathophysiologie: Fallbeispiele Hämatologie Eine Frau mittleren Alters fühlt sich seit zwei Wochen schwach und zunehmend müde. Ihr Familienarzt hat eine Laboruntersuchung durchgeführt und hat sie
