AMINOSÄUREN UND PROTEINE
|
|
|
- Stanislaus Martin
- vor 7 Jahren
- Abrufe
Transkript
1 10 AMINOSÄUREN UND PROTEINE Zwanzig verschiedene Aminosäuren sind die üblichen Bausteine der Proteine. Die Dreibuchstaben- Abkürzungen und Strukturformeln der Aminosäuren sind auf der umstehenden Tabelle wiedergegeben. Man unterscheidet saure, neutrale und basische Aminosäuren oder apolare (aliphatische, aromatische) und polare Aminosäuren. In den Proteinen sind die Aminosäuren durch Peptidbindungen miteinander verknüpft. Die Aminosäurensequenz (Primärstruktur) bestimmt die dreidimensionale Anordnung der Peptidkette im Raum (Sekundär- und Tertiärstruktur). Häufig sind zwei und mehr Peptidketten mit ausgebildeter Sekundär- und Tertiärstruktur zu stabilen oligomeren Molekülen zusammengelagert (Quartär-struktur). Für die ausführliche Behandlung von Struktur und Konformation der Proteine sei auf Vorlesung und Lehrbücher verwiesen. Primäre Aminogruppen von Aminosäuren und Proteinen werden mit der Ninhydrin-Reaktion nachgewiesen. Ninhydrin reagiert mit Ammoniak und primären Aminogruppen zu einem blauen Farbstoff. α-aminosäuren werden durch Ninhydrin oxidativ desaminiert und decarboxyliert. Auf analoge Weise reagiert auch die ε-nh 2 -Gruppe der Lysin-Seitenkette. Deshalb geben auch Proteine eine positive
2 11
3 Ninhydrinreaktion. Zur quantitativen Bestimmung von Aminosäuren wird die blaue Ninhydrin-Farbe photometrisch gemessen. Die Trennung verschiedener Aminosäuren mittels Ionenaustauscher- Chromatographie (Chromatographie S. 27 und Exp. 2.4) und anschliessende photometrische Konzentrationsbestimmung mit Ninhydrin wird im sog. Aminosäurenanalysator vollautomatisch durchgeführt (Fig. 6 S. 30). 12 Biuret-Test: Peptidbindungen bilden blau-violette Cu 2+ -Komplexe. In stark alkalischer Lösung entstehen aus Proteinen und Kupfersulfat Koordinationskomplexe zwischen Cu 2+ -Ionen und benachbarten Amid- Stickstoff-Atomen von Peptidbindungen. Biuret (H 2 N-CO-NH-CO-NH 2 ) ist die einfachste Verbindung, welche einen derartigen blauvioletten Kupferkomplex bildet. Der Biuret-Test dient zur quantitativen photometrischen Proteinbestimmung (Exp. 4.1). Die Farbe des Komplexes ist in der Regel unabhängig von der Art des Proteins, so dass eine für Serumalbumin bestimmte photometrische Eichkurve auch für viele andere Proteine benutzt werden kann (Exp. 4.1 und Photometrie S. 31). Tryptophan und Tyrosin geben den Proteinen ein charakteristisches UV-Spektrum mit Absorptionsmaximum bei 280 nm. Wie die Spektren in Figur 1 zeigen, trägt Tryptophan am meisten und Phenylalanin kaum zur Absorption der Proteine im nahen UV-Bereich bei. ε mm Fig. 1 Absorptionsspektren der aromatischen Aminosäuren In Figur 1 bedeutet ε mm "millimolarer Extinktionskoeffizient". Der millimolare Extinktions-
4 koeffizient ist die Absorption einer millimolaren Lösung der entsprechenden Aminosäure (Photometrie S. 31). Je nach dem Gehalt an aromatischen Aminosäuren ändert die UV-Absorption von Proteinen. In Figur 2 sind die UV-Spektren von Lösungen gleicher Massenkonzentration (mg/ml) von Lysozym, γ-globulin und Ribonuclease dargestellt. Alle Peptide und Proteine absorbieren sehr stark bei 220 nm aufgrund ihrer Peptidbindungen. Die drei Proteine enthalten unterschiedlich viel Tyrosin und Tryptophan. Zur Konzentrationsbestimmung kann die UV-Absorption bei 280 nm benutzt werden, wegen des variablen Gehalts an aromatischen Aminosäuren gilt jedoch eine Eichkurve nur für ein bestimmtes Protein. Manche Proteine absorbieren sichtbares Licht. Für das sichtbare Absorptionsspektrum sind prosthetische Gruppen verantwortlich (Häm, Flavin, etc.). 13 Fig. 2 Absorptionsspektren von Proteinen mit verschiedenem Gehalt an aromatischen Aminosäuren. Die Spektren wurden mit Proteinlösungen gleicher Konzentration (1 mg/ml) aufgenommen. Tryptophan- und Tyrosingehalt in g Aminosäure pro 100 g Protein: Lysozym (Hühnereiweiss) 8.6 Trp 4.0 Tyr Ovalbumin (Hühnereiweiss) 1.3 Trp 3.8 Tyr Ribonuclease (Rind) Tyr
5 Grossmolekulare Proteine werden von kleinen Molekülen durch Dialyse oder Gelchromatographie abgetrennt. Gewisse Cellophanmembranen sind für grosse Moleküle undurchlässig, für Wasser und andere kleine Moleküle durchlässig. Wird eine Protein-Salzlösung in einem Cellophanschlauch für längere Zeit (Stunden) in Wasser eingetaucht, so stellt sich für die frei passierbaren Moleküle durch Diffusion ein Konzentrations-Gleichgewicht über das gesamte Flüssigkeitsvolumen ein. Die grossen Proteinmoleküle werden im Schlauch zurückgehalten. Der Vorgang wird Dialyse genannt. Durch Dialyse können Proteinlösungen entsalzt werden (Exp. 3.10, Exp. 5.1), oder ein Protein in einem Puffer A kann durch Dialyse in einen neuen Puffer B gebracht werden. Die Hämodialyse (künstliche Niere) arbeitet nach demselben Prinzip. Mit der Gelchromatographie ist eine feinere Trennung von Molekülen unterschiedlicher Grösse möglich als mit der Dialyse (Exp. 5.1 und 5.4). Molekularmasse von Proteinen: Die meisten Proteine haben eine Molekularmasse (M r ) im Bereich 10'000 bis 100'000. Beispiele: Glucagon 4'500 (ein Peptid), Ribonuclease 13'700, Myoglobin 17'000, Chymotrypsin 25'000, Hämoglobin 64'500, Serumalbumin 69'000, Aldolase 160'000, Phosphorylase a 390'000. Gebräuchliche Methoden zur Molekularmassebestimmung von Proteinen sind Gelchromatographie, SDS-Gelelektrophorese und Sedimentationsanalyse in der Ultrazentrifuge. Molekularmassebestimmung mit Gelchromatographie wird im Kapitel "Chromatographie" näher beschrieben (S. 30). Die heute gebräuchlichste Methode ist die SDS-Gelelektrophorese. Bei dieser speziellen Elektrophoresemethode ist die Wanderungsgeschwindigkeit im elektrischen Feld fast ausschliesslich eine Funktion der Molekülgrösse. Proteine mit niedriger Molekularmasse wandern schneller als solche mit hoher Molekularmasse (SDS siehe S. 17). Die SDS-Gelelektrophorese ist nicht zu verwechseln mit der üblichen Proteinelektrophorese, bei der native Proteine aufgrund ihrer Ladung getrennt werden (Elektrophorese S. 27 und Elektrophorese von Serumproteinen in Exp. 4.2). Die Molekularmassebestimmung in der Ultrazentrifuge ist aufwendig. Sie gibt aber zusätzlich Information über die Form und den Aggregationszustand von Proteinmolekülen. Im künstlichen Schwerefeld der Ultrazentrifuge ist die Sedimentationsgeschwindigkeit v s einer Partikel von ihrer Grösse abhängig gemäss v s = S@Γ. Die Zentrifugalfeldstärke Γ wird bestimmt durch den Radius der Zentrifuge und die Tourenzahl. S ist die für die untersuchte Partikel charakteristische Sedimentationskonstante, welche experimentell gemäss der obigen Gleichung bestimmt werden kann. S ist unter anderem eine Funktion der Molekülmasse, und daher kann letzteres aus dem experimentell bestimmten S berechnet werden. Die Beziehung lautet 14 S = M@D (1 - ρ m /ρ p ) RT M = Molekularmasse, D = Diffusionskonstante, ρ m und ρ p = Dichte von Medium und Partikel, RT = Gaskonstante und absolute Temperatur. Die Sedimentationskonstanten werden in Svedberg-Einheiten (S) (1 Svedberg = sec) ausgedrückt und auf ρ m von Wasser und 20EC normalisiert (S 20,w ). Typische Werte sind 2 S für Myoglobin, 40 S und 60 S für Ribosomen-Untereinheiten, etwa 200 S für Viren und über 1000 S für ganze Zellen.
6 15 Denaturierung von Proteinen: Die native Struktur von Proteinen wird unter dem Einfluss verschiedenster Faktoren zerstört, dazu gehören Wärme, Schaumbildung, Zusatz von organischen Lösungsmitteln, Säuren, Basen, Schwermetallionen oder hohe Konzentration von Harnstoff. Die für die Sekundär-, Tertiär- und Quartärstruktur verantwortlichen, nicht-kovalenten Bindungen werden teilweise oder ganz gelöst, während die für die Primärstruktur verantwortlichen kovalenten Bindungen erhalten bleiben. Man bezeichnet diesen Prozess der partiellen oder vollständigen Entfaltung der Peptidkette als Denaturierung. Ein denaturiertes Protein hat die gleiche Primärstruktur wie das native, hat aber keine einheitliche räumliche Struktur und andere physikalisch-chemische Eigenschaften (Beispiel: Hartwerden von Eiern beim Kochen). Bei der Denaturierung geht die biologische Aktivität verloren. (Beispiele: Hitze-Inaktivierung von Enzymen und Proteinhormonen). Denaturierung kann, muss aber nicht reversibel sein. Denaturierung verringert in der Regel die Löslichkeit der Proteine. Denaturierte Proteine werden von Proteasen leichter gespalten als native: gekochtes Fleisch ist leichter verdaulich. Proteine sind an ihrem isoelektrischen Punkt am wenigsten löslich. Die Löslichkeit der Proteine variiert stark. Globuläre Proteine wie Serumalbumin und Globuline sind im allgemeinen gut, Faserproteine (Kollagen, Keratin) sehr schlecht löslich. Proteine sind Polyelektrolyte (Platz 2: Aminosäuren und Proteine). Elektrostatische Kräfte zwischen Proteinmolekülen einerseits und zwischen Proteinmolekülen und Wasserdipolen andererseits beeinflussen die Löslichkeit. Proteine mit vielen geladenen Gruppen sind häufig gut wasserlöslich. Die Löslichkeit eines Proteins ist am geringsten, wenn seine Gesamtladung gleich Null ist. Dies ist der Fall, wenn das Molekül gleich viele positive wie negative Ladungen trägt. Man bezeichnet den ph-wert der wässrigen Lösung, bei dem dies zutrifft, als isoelektrischen Punkt (IEP) des Proteins. Manche Proteine fallen am IEP aus (= werden unlöslich). Bei ph-werten über und unter dem IEP bewirken negative bzw. positive Überschussladungen gegenseitige Abstossung der Proteinmoleküle und damit bessere Löslichkeit. Fig. 3 Löslichkeit von β-lactoglobulin (IEP 5.2) in Abhängigkeit vom ph-wert bei 25 0 C. Die Löslichkeit ist bei ph 6 mehr als 40mal grösser als bei ph 5.2. Proteine werden aus wässrigen Lösungen durch Zugabe von Salz, organischen Lösungsmitteln oder bestimmten Säuren ausgefällt. Zur Isolierung und Reinigung werden Proteine häufig ausgefällt. Solche Fällungen müssen reversibel sein, soll das Protein seine biologische Aktivität behalten: Ein
7 isoliertes Enzym muss nach der Fällung wieder gelöst werden können und unverminderte Aktivität besitzen. Bei manchen Analysemethoden stören anwesende Proteine; sie werden deshalb irreversibel ausgefällt und durch Zentrifugation abgetrennt. Eine solche "Deproteinisierung" ist z.b. nötig bei der Bestimmung von Glucose im Serum (Exp. 5.6). Die meisten Fällungen beruhen auf der Änderung der elektrostatischen Wechselwirkungen zwischen Proteinmolekülen. So werden Proteine aus wässrigen Lösungen durch Zugabe von organischen Lösungsmitteln ausgefällt (Exp. 3.9), weil in organischen Lösungsmitteln die gegenseitige Anziehung der geladenen Proteinmoleküle grösser wird (Proteine haben ein unregelmässiges Muster von positiven und negativen Ladungen auf ihrer Oberfläche). Gemäss dem Coulombschen Gesetz über die Anziehung entgegengesetzt geladener Teilchen nimmt die elektrostatische Anziehung mit abnehmender Dielektrizitätskonstante des Mediums zu. Organische Lösungsmittel haben eine niedrigere Dielektrizitätskonstante als Wasser. Industriell bedeutungsvoll ist die Fällung von Blutplasmaproteinen mit Alkohol und Aceton (Cohn-Fraktionierung). Die Fällung geschieht bei tiefen Temperaturen, damit die Plasmaproteine nicht irreversibel denaturiert werden. Zusatz eines Salzes in hoher Konzentration zu einer Proteinlösung bewirkt die Erniedrigung der effektiven Konzentration (Aktivität) des Wassers und dadurch eine Herabsetzung der für die Lösung des Proteins verfügbaren Wassermenge. Das Protein wird ausgefällt. Man bezeichnet die durch Salzzugabe bewirkte Ausfällung als Aussalzung. Sie ist meist reversibel und deshalb zur Isolierung von Enzymen geeignet. Gewöhnlich wird für die Aussalzung Ammoniumsulfat verwendet, weil es besonders gut löslich ist. Zur Ausfällung von verschiedenen Proteinen werden unterschiedliche Konzentrationen von Ammoniumsulfat benötigt. Ein Proteingemisch kann deshalb aufgetrennt werden durch schrittweises Zufügen von Ammoniumsulfat (Exp. 3.8). 16 LIPIDE Die Lipide sind eine heterogene Stoffklasse. Ein hoher Gehalt an hydrophoben Gruppen ist ihnen gemeinsam. Lipide sind daher in organischen Lösungsmitteln gut, in Wasser schlecht löslich. Die Lipide können unterteilt werden in einfache Lipide, komplexe Lipide und Isoprenoidlipide. Zu den einfachen Lipiden gehören die Neutralfette oder Triacylglycerine. Es sind häufige Nahrungsbestandteile und Energiespeicher der Zelle. Zu den komplexen Lipiden werden z.b. die Membranbestandteile Lecithin, Cerebroside und Cardiolipin gezählt. Die Isoprenoidlipide sind Abkömmlinge des Isoprens und umfassen Verbindungen wie Cholesterin, Vitamin A, Steroidhormone und Gallensäuren. Cholesterin ist ein universeller Membranbestandteil, aber auch Ausgangsprodukt für die Biosynthese von Gallensäuren, Steroidhormonen und Vitamin D. Die physikalischen Eigenschaften der Neutralfette werden durch die Struktur der Fettsäuren bestimmt. Die Fette und Öle der Nahrung sind Gemische verschiedener Triacylglycerine. Triacylglycerine sind Verbindungen, die aus einem Molekül Glycerin, verestert mit drei Molekülen Fettsäure, bestehen. Sie tragen im Gegensatz zu den komplexen Lipiden keine ionisierbaren Gruppen, daher auch der Name Neutralfette. Die physikalischen und chemischen Eigenschaften der Neutralfette sind je nach Fettsäuren-Zusammensetzung verschieden. So ist der Schmelzpunkt von Fetten um so niedriger, je kürzer die Fettsäuren und je grösser die Zahl der ungesättigten Bindungen. Öle enthalten vorwiegend Triacylglycerine mit ungesättigten Fettsäuren. Tierische Fette haben einen Schmelzpunkt, der etwas unter der physiologischen Gewebstemperatur liegt. Fett aus dem Unterhautfettgewebe hat einen niedrigeren Schmelzpunkt als Fett aus dem Innern des Körpers.
0.1 Eiweißstoffe (Proteine)
 1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
THEORETISCHER TEIL GEBRÄUCHLICHE EINHEITEN FÜR SUBSTANZQUANTITÄT, VOLUMEN UND KONZENTRATION
 5 THEORETISCHER TEIL GEBRÄUCHLICHE EINHEITEN FÜR SUBSTANZQUANTITÄT, VOLUMEN UND KONZENTRATION Substanzquantität wird als Masse oder als Stoffmenge angegeben. Masse: Basiseinheit ist das Kilogramm. Gebräuchliche
5 THEORETISCHER TEIL GEBRÄUCHLICHE EINHEITEN FÜR SUBSTANZQUANTITÄT, VOLUMEN UND KONZENTRATION Substanzquantität wird als Masse oder als Stoffmenge angegeben. Masse: Basiseinheit ist das Kilogramm. Gebräuchliche
Polyacrylamid-Gelelektrophorese Vereinfachte quantitative Behandlung der Wanderungsgeschwindigkeit qeladener Teilchen im elektrischen Feld.
 Das Auflösungsvermögen der Polyacrylamid-Gelelektrophorese ist besonders hoch, weil im Gel Moleküle aufgrund ihrer Ladung und ihrer Grösse aufgetrennt werden. Während auf Agarose die Serumproteine nur
Das Auflösungsvermögen der Polyacrylamid-Gelelektrophorese ist besonders hoch, weil im Gel Moleküle aufgrund ihrer Ladung und ihrer Grösse aufgetrennt werden. Während auf Agarose die Serumproteine nur
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
PRAKTIKUMSTEIL BIOCHEMIE (1. Studienjahr)
 60 PRAKTIKUMSTEIL BIOHEMIE (1. Studienjahr) PLATZ 4: AMINOSÄUREN UND PROTEINE Die physikalisch-chemischen Eigenschaften von Aminosäuren und Proteinen sind eng mit ihrer Fähigkeit verknüpft, Protonen abzugeben
60 PRAKTIKUMSTEIL BIOHEMIE (1. Studienjahr) PLATZ 4: AMINOSÄUREN UND PROTEINE Die physikalisch-chemischen Eigenschaften von Aminosäuren und Proteinen sind eng mit ihrer Fähigkeit verknüpft, Protonen abzugeben
Proteindenaturierung:
 Proteindenaturierung: Inhalt Was passiert bei einer Denaturierung? Eigenschaften der Proteine Möglichkeiten zur Fällung/Denaturierung Gründe für Fällungen Beispiele Was passiert bei einer Denaturierung?
Proteindenaturierung: Inhalt Was passiert bei einer Denaturierung? Eigenschaften der Proteine Möglichkeiten zur Fällung/Denaturierung Gründe für Fällungen Beispiele Was passiert bei einer Denaturierung?
Versuch 1. Aminosäure- und Proteinbestimmungen
 Versuch 1 Aminosäure- und Proteinbestimmungen Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de Chemie X X Prof. Dr. Schäfer Aminosäure und Proteinbestimmungen
Versuch 1 Aminosäure- und Proteinbestimmungen Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de Chemie X X Prof. Dr. Schäfer Aminosäure und Proteinbestimmungen
und Reinstruktur Die Sekundärstruktur ist die Anordnung der Aminosäurenkette, wobei man in zwei Arten unterscheidet: o Faltblatt- oder β- Struktur
 Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Kl.10 LB2. Kl.10 LB2. Kl.10 LB2. Kl.10 LB2. Nenne 2 Vorkommen von Fetten.
 Nenne 2 Vorkommen von Fetten. Es gibt pflanzliche Fette (Kokosöl, livenöl) und tierische Fette (Schweinefett, Milchfett). Beschreibe die Löslichkeit der Fette. Fette sind nicht in Wasser aber in Benzin
Nenne 2 Vorkommen von Fetten. Es gibt pflanzliche Fette (Kokosöl, livenöl) und tierische Fette (Schweinefett, Milchfett). Beschreibe die Löslichkeit der Fette. Fette sind nicht in Wasser aber in Benzin
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH
 B I O C H E M I S C H E S P R A K T I K U M F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH 2003 INHALTSVERZEICHNIS *) Zum Biochemischen Praktikum steht Ihnen
B I O C H E M I S C H E S P R A K T I K U M F Ü R S T U D I E R E N D E D E R M E D I Z I N BIOCHEMISCHES INSTITUT DER UNIVERSITÄT ZÜRICH 2003 INHALTSVERZEICHNIS *) Zum Biochemischen Praktikum steht Ihnen
Intensivkurs Biologie
 Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Fragen zum Versuch 1. Kohlenhydrate. Fragen zum Versuch 2. Aminosäuren. Fragen zum Versuch 3. Lipide
 Fragen zum Versuch 1 Kohlenhydrate 1) Worin unterscheiden sich chemisch die folgenden Kohlenhydrate? a) Glucose und Fructose b) Laktose und Saccharose c) Stärke, Glykogen und Dextrin d) Was ist Agar-Agar,
Fragen zum Versuch 1 Kohlenhydrate 1) Worin unterscheiden sich chemisch die folgenden Kohlenhydrate? a) Glucose und Fructose b) Laktose und Saccharose c) Stärke, Glykogen und Dextrin d) Was ist Agar-Agar,
Denaturierung von Proteinen
 Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
U. Helmich, Intensivkurs "Proteine" Seite 1
 U. Helmich, Intensivkurs "Proteine" Seite 1 Crashkurs "Proteine" Proteine bestehen aus Aminosäuren, von denen es rund 20 verschiedene gibt. Die meisten Proteine bestehen mehreren hundert oder sogar mehreren
U. Helmich, Intensivkurs "Proteine" Seite 1 Crashkurs "Proteine" Proteine bestehen aus Aminosäuren, von denen es rund 20 verschiedene gibt. Die meisten Proteine bestehen mehreren hundert oder sogar mehreren
ATTO 565 und ATTO 590
 ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
ATTO 565 und ATTO 590 Allgemeine Informationen ATTO 565 und ATTO 590 sind Fluoreszenzmarker aus der Familie der Rhodamin-Farbstoffe. Diese Farbstoffe besitzen als gemeinsames Strukturelement einen Carboxyphenyl-
Versuchsprotokoll: Chromatographie. Gelchromatographische Trennung eines Proteingemischs
 Versuchsprotokoll: Chromatographie Gelchromatographische Trennung eines Proteingemischs 1.1. Einleitung Das Ziel der Gelchromatographie ist es ein vorhandenes Proteingemisch in die einzelnen Proteine zu
Versuchsprotokoll: Chromatographie Gelchromatographische Trennung eines Proteingemischs 1.1. Einleitung Das Ziel der Gelchromatographie ist es ein vorhandenes Proteingemisch in die einzelnen Proteine zu
Peptide Proteine. 1. Aminosäuren. Alle optisch aktiven proteinogenen Aminosäuren gehören der L-Reihe an: 1.1 Struktur der Aminosäuren
 1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
8. Tutorium AMB/OBOE
 8. Tutorium AMB/OBOE 15.12.05 4.13 Welches Begriffspaar vervollständigt folgenden Satz über funktionelle Gruppen in der organischen Chemie. Carboxyl verhält sich zu wie zu Base. a) Säure... Carboxyl b)
8. Tutorium AMB/OBOE 15.12.05 4.13 Welches Begriffspaar vervollständigt folgenden Satz über funktionelle Gruppen in der organischen Chemie. Carboxyl verhält sich zu wie zu Base. a) Säure... Carboxyl b)
Name:... EHA-code:... Gruppe:...
 D-2008/09. I. 1. KLAUSUR 29. 09. 08. Name:... EHA-code:... Gruppe:... 1 Studieren Sie die Abbildung und beantworten Sie die Fragen! Einfache Antwortmöglichkeit (Bei diesem Fragentyp handelt es sich um
D-2008/09. I. 1. KLAUSUR 29. 09. 08. Name:... EHA-code:... Gruppe:... 1 Studieren Sie die Abbildung und beantworten Sie die Fragen! Einfache Antwortmöglichkeit (Bei diesem Fragentyp handelt es sich um
Versuch 3. Elektrophorese
 Versuch 3 Elektrophorese Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Prof. Dr. Schäfer Wird benotet?: 1. Einleitung Ziel des ersten Versuches
Versuch 3 Elektrophorese Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Prof. Dr. Schäfer Wird benotet?: 1. Einleitung Ziel des ersten Versuches
Aufgabengruppe BMS Chemie
 Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
Aufgabengruppe BMS Chemie Zeitvorgabe: Bitte lösen Sie die folgenden 24 Aufgaben innerhalb von 18 Minuten! 1) Welche Aussagen treffen auf Proteine zu? I. Die Primärstruktur gibt die Aminosäurenabfolge
1 Eigenschaften der Lipide
 1 Eigenschaften der "" ist eine Sammelbezeichnung für viele verschiedene Stoffgruppen, die ähnliche Eigenschaften haben. sind: hydrophob, d.h. in polaren Lösungsmitteln wie Wasser unlöslich 2 Eigenschaften
1 Eigenschaften der "" ist eine Sammelbezeichnung für viele verschiedene Stoffgruppen, die ähnliche Eigenschaften haben. sind: hydrophob, d.h. in polaren Lösungsmitteln wie Wasser unlöslich 2 Eigenschaften
Sedimentation, Elektrophorese
 Sedimentation, Elektrophorese MEDIZINISCHE PHYSIK UND STATISTIK 2. Dr. Tamás Huber Institut für Biophysik 17. März 2016. Trennungsmethoden Trennverfahren in der Chemie oder Physik helfen dabei, zwei oder
Sedimentation, Elektrophorese MEDIZINISCHE PHYSIK UND STATISTIK 2. Dr. Tamás Huber Institut für Biophysik 17. März 2016. Trennungsmethoden Trennverfahren in der Chemie oder Physik helfen dabei, zwei oder
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine
 Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
PROTEINBESTIMMUNG. Vergleich Bradford und BCA
 PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
PROTEINBESTIMMUNG Vergleich Bradford und BCA ÜBERSICHT Einleitung Theorie Durchführung Resultate und Diskussion Fragen EINLEITUNG Aufgabenstellung: Vergleich der Methoden zur quantitativen Proteinbestimmung
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Übungsaufgaben zu Aminosäuren, Peptiden und Proteinen
 Übungsaufgaben zu Aminosäuren, Peptiden und Proteinen T ilfsmittel: Blatt mit den Strukturformeln aller proteinogenen AS (außer bei den Aufgaben, bei denen die Strukturformel einer AS anhand des Trivialnamens
Übungsaufgaben zu Aminosäuren, Peptiden und Proteinen T ilfsmittel: Blatt mit den Strukturformeln aller proteinogenen AS (außer bei den Aufgaben, bei denen die Strukturformel einer AS anhand des Trivialnamens
Versuchsprotokoll: Aminosäure- und Proteinbestimmung
 Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
Versuchsprotokoll: Aminosäure- und Proteinbestimmung a) Proteinbestimmung mit Biuret-Reagenz 1.1. Einleitung Das Ziel des Versuchs ist es nach Aufstellen einer Eichgerade mit gegeben Konzentrationen, die
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Chemie für Mediziner. Norbert Sträter
 Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
Chemie für Mediziner Norbert Sträter Verlag Wissenschaftliche Scripten 2012 Inhaltsverzeichnis Allgemeine und Anorganische Chemie... 1 1 Atombau... 1 1.1 Fundamentale Begriffe... 1 1.2 Atome und Elemente...
VERDAUUNG. Der lange Weg durch den Verdauungstrakt
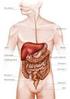 VERDAUUNG Der lange Weg durch den Verdauungstrakt Sonja Zankl SS 2002 DEFINITION Abbau der Nahrungsstoffe im Verdauungstrakt in resorptionsfähige Bestandteile & Aufnahme in Blut bzw. Lymphe Wozu Verdauung?
VERDAUUNG Der lange Weg durch den Verdauungstrakt Sonja Zankl SS 2002 DEFINITION Abbau der Nahrungsstoffe im Verdauungstrakt in resorptionsfähige Bestandteile & Aufnahme in Blut bzw. Lymphe Wozu Verdauung?
V1: Methoden der Proteinbestimmung
 V1: Methoden der Proteinbestimmung Methodik: Proteinkonzentrationsbestimmung mittels Bradford sowie der Korrekturverfahren nach Warburg & Christian sowie Kalb & Bernlohr UV-Spektren von Protein- und Nukleinsäurelösungen
V1: Methoden der Proteinbestimmung Methodik: Proteinkonzentrationsbestimmung mittels Bradford sowie der Korrekturverfahren nach Warburg & Christian sowie Kalb & Bernlohr UV-Spektren von Protein- und Nukleinsäurelösungen
Aminosäuren und Proteine
 Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Chemiepraktikum für Biologen. Versuchsprotokoll. Dünnschichtchromatographie (von Farbstoffen, Aminosäuren und Monosacchariden)
 Johannes Gutenberg Universität Fachbereich Biologie Chemiepraktikum für Biologen SS 2002 Versuchsprotokoll zum Thema Dünnschichtchromatographie (von Farbstoffen, Aminosäuren und Monosacchariden) von 1)
Johannes Gutenberg Universität Fachbereich Biologie Chemiepraktikum für Biologen SS 2002 Versuchsprotokoll zum Thema Dünnschichtchromatographie (von Farbstoffen, Aminosäuren und Monosacchariden) von 1)
Versuch: Enzyme (LDH)
 Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
2.2. Peptide. Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure
 2.2. Peptide Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure Peptid: bis zu ~30 linear über Peptidbindung verknüpfte Aminosäuren
2.2. Peptide Peptide entstehen durch Kondensation der a-carboxylgruppe einer Aminosäure mit der a-aminogruppe einer anderen Aminosäure Peptid: bis zu ~30 linear über Peptidbindung verknüpfte Aminosäuren
4.3. Fragen zu Proteinen
 4.3. Fragen zu Proteinen Funktionelle Gruppen im Vergleich Gib für die folgenden Stoffklassen für jede typische Reaktion ein Beispiel an. Formuliere je eine Reaktionsgleichung mit den Strukturformeln und
4.3. Fragen zu Proteinen Funktionelle Gruppen im Vergleich Gib für die folgenden Stoffklassen für jede typische Reaktion ein Beispiel an. Formuliere je eine Reaktionsgleichung mit den Strukturformeln und
Klausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach (SS2011)
 Klausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach (SS2011) Musterlösung 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Amylose und Amylopektin bestehen nur aus D-Glucose
Klausur zum chemischen Praktikum für Studierende mit Chemie als Nebenfach (SS2011) Musterlösung 1. (10P) Was ist richtig (mehrere Richtige sind möglich)? a) Amylose und Amylopektin bestehen nur aus D-Glucose
Orbital. Atombindung, Bindung. Elektronegativität. Dipol
 GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
1.1 Was versteht man unter sauren bzw. basischen Aminosäureresten? Die Aminosäuren unterscheiden sich in ihren Seitenketten.
 Fragenkatalog Proteinchemie Vorlesung 1-12 SS 2011 1.1 Was versteht man unter sauren bzw. basischen Aminosäureresten? Die Aminosäuren unterscheiden sich in ihren Seitenketten. 1.2 Zeichnen Sie die Strukturen
Fragenkatalog Proteinchemie Vorlesung 1-12 SS 2011 1.1 Was versteht man unter sauren bzw. basischen Aminosäureresten? Die Aminosäuren unterscheiden sich in ihren Seitenketten. 1.2 Zeichnen Sie die Strukturen
Aromatische Diazoniumionen
 Aromatische Diazoniumionen Wichtige Reaktive Zwischenstufe Aromatische Diazoniumionen Aromatische Diazoniumionen Azofarbstoffe Organische Chemie für MST 7 Lienkamp/ Prucker/ Rühe 7 Inhalt Amine Nomenklatur,
Aromatische Diazoniumionen Wichtige Reaktive Zwischenstufe Aromatische Diazoniumionen Aromatische Diazoniumionen Azofarbstoffe Organische Chemie für MST 7 Lienkamp/ Prucker/ Rühe 7 Inhalt Amine Nomenklatur,
Membranen (3a) Membrane
 Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Proteine I. Fällung Konzentrationsbestimmung. Dr. Richard Weiss
 Proteine I Fällung Konzentrationsbestimmung Dr. Richard Weiss Praktikumsaufbau Tag 1: Konzentrieren Denaturierende und native Fällung Protein Konzentrationsbestimmung Tag 2: Entsalzen Gelchromatographie
Proteine I Fällung Konzentrationsbestimmung Dr. Richard Weiss Praktikumsaufbau Tag 1: Konzentrieren Denaturierende und native Fällung Protein Konzentrationsbestimmung Tag 2: Entsalzen Gelchromatographie
Biochemische Übungen
 Dr. Arnulf Hartl Biochemische Übungen Proteine Tag 1: Tag 2: Tag 3: Konzentrieren Denaturierende und native Fällungen Protein Konzentrationsbestimmung Entsalzen Gelchromatographie Dialyse Elektrophorese
Dr. Arnulf Hartl Biochemische Übungen Proteine Tag 1: Tag 2: Tag 3: Konzentrieren Denaturierende und native Fällungen Protein Konzentrationsbestimmung Entsalzen Gelchromatographie Dialyse Elektrophorese
Gase sind in Wasser löslich Solche Lösungen können auch gesättigt sein
 4. TRENNEN UND MISCHEN ARBEITSBLATT 4.1 DIE LÖSLICHKEIT VON GASEN IN FLÜSSIGKEITEN Können sich Gase wie Festkörper in Flüssigkeiten lösen? Was lässt sich über die Löslichkeit von Kohlendioxid in Wasser
4. TRENNEN UND MISCHEN ARBEITSBLATT 4.1 DIE LÖSLICHKEIT VON GASEN IN FLÜSSIGKEITEN Können sich Gase wie Festkörper in Flüssigkeiten lösen? Was lässt sich über die Löslichkeit von Kohlendioxid in Wasser
Vorlesung 47. Aminosäuren, Peptide und Proteine
 Vorlesung 47. Aminosäuren, Peptide und Proteine Bedeutung der Proteine in der atur: Vollhardt, 3. Aufl., S. 1285/1286, 4. Aufl., S. 1371; art S. 608-609; Buddrus, S. 753. Etwa 18% des menschlichen Körpers
Vorlesung 47. Aminosäuren, Peptide und Proteine Bedeutung der Proteine in der atur: Vollhardt, 3. Aufl., S. 1285/1286, 4. Aufl., S. 1371; art S. 608-609; Buddrus, S. 753. Etwa 18% des menschlichen Körpers
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Physikalische Chemie
 Physikalische Chemie Prüfungstag 03.02.2017 Bitte beachten Sie Erlaubt sind 4 Seiten Zusammenfassung plus ein Periodensystem. Erlaubt ist ein Taschenrechner. Alle Hilfsmittel, die nicht explizit erlaubt
Physikalische Chemie Prüfungstag 03.02.2017 Bitte beachten Sie Erlaubt sind 4 Seiten Zusammenfassung plus ein Periodensystem. Erlaubt ist ein Taschenrechner. Alle Hilfsmittel, die nicht explizit erlaubt
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Zusammensetzung und Struktur der Proteine. Stryer (6. Auflage) Kapitel 2
 Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Biochemische Übungen I: Proteine I Fällung und Konzentrationsbestimmung
 Biochemische Übungen I: Proteine I Fällung und Konzentrationsbestimmung Lerninhalt: Allgemeine Proteineigenschaften (Löslichkeit, Ladung, Hydrophobizität). Native Fällung: Aussalzen mit Ammoniumsalz. Denaturierende
Biochemische Übungen I: Proteine I Fällung und Konzentrationsbestimmung Lerninhalt: Allgemeine Proteineigenschaften (Löslichkeit, Ladung, Hydrophobizität). Native Fällung: Aussalzen mit Ammoniumsalz. Denaturierende
Circulardichroismus (CD) und Fluoreszenz - Anwendungen in der Proteinchemie -
 Circulardichroismus (CD) und Fluoreszenz - Anwendungen in der Proteinchemie - Circulardichroismus (CD) - Einführung Circulardichroismus (CD) - Prinzip Circulardichroismus (CD) - Formel Meßsignal beruht
Circulardichroismus (CD) und Fluoreszenz - Anwendungen in der Proteinchemie - Circulardichroismus (CD) - Einführung Circulardichroismus (CD) - Prinzip Circulardichroismus (CD) - Formel Meßsignal beruht
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 03.02.2016 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 03.02.2016 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Name: Matrikelnummer: Geburtsdatum: Hilfsmittel: Formelsammlung (beigefügt), Periodensystem (beigefügt), Taschenrechner
 Chemie für Physiker B. Sc. Physikalische Technik XXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXX Prof. Dr. Thomas Jüstel / Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Chemie für Physiker B. Sc. Physikalische Technik XXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXXX Prof. Dr. Thomas Jüstel / Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
1 Biomoleküle. und ihre Wechselwirkungen. 1.1 Die Entstehung des Lebens. Die Entstehung des Lebens
 1 Biomoleküle und ihre Wechselwirkungen Das Leben ist im Wasser entstanden, und Wasser ist der quantitativ wichtigste Bestandteil aller Lebewesen. Wasser ist das Lösungsmittel, in welchem die chemischen
1 Biomoleküle und ihre Wechselwirkungen Das Leben ist im Wasser entstanden, und Wasser ist der quantitativ wichtigste Bestandteil aller Lebewesen. Wasser ist das Lösungsmittel, in welchem die chemischen
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Einführung in die praktische Biochemie
 H.Aebi BOTAN. INSTITUT Medizinisch-chemisches Institut der Universität Bern lechn. HOCM^rur ir r- 6100 - ' ochul^ Einführung in die praktische Biochemie für Studierende der Medizin, Veterinärmedizin, Pharmazie
H.Aebi BOTAN. INSTITUT Medizinisch-chemisches Institut der Universität Bern lechn. HOCM^rur ir r- 6100 - ' ochul^ Einführung in die praktische Biochemie für Studierende der Medizin, Veterinärmedizin, Pharmazie
Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen
 Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen Einleitung Um die Anfangssequenz aus drei Aminosäuren eines Proteins zu bestimmen, benutzen wir eine Methode, bei der schrittweise vom N-terminalen
Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen Einleitung Um die Anfangssequenz aus drei Aminosäuren eines Proteins zu bestimmen, benutzen wir eine Methode, bei der schrittweise vom N-terminalen
Organische Experimentalchemie
 PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 rganische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und Biologie
PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 rganische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und Biologie
Biochemie-Praktikum Wintersemester 05/06 1. Klausur
 Biochemie-Praktikum Wintersemester 05/06 1. Klausur 01. Welches Verfahren eignet sich am wenigsten zur Trennung von Proteinmolekülen? Ionenaustauschchromatographie Ausschlusschromatographie Papierchromatographie
Biochemie-Praktikum Wintersemester 05/06 1. Klausur 01. Welches Verfahren eignet sich am wenigsten zur Trennung von Proteinmolekülen? Ionenaustauschchromatographie Ausschlusschromatographie Papierchromatographie
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Biostatistik, Winter 2018/19
 1/32 Biostatistik, Winter 2018/19 Folgen, Summen,, Lambert-Beer Prof. Dr. Achim Klenke http://www.aklenke.de 2. Vorlesung: 26.10.2018 2/32 Inhalt 1 Folgen Begriffsbildung Grenzwerte 2 Summen und Produkte
1/32 Biostatistik, Winter 2018/19 Folgen, Summen,, Lambert-Beer Prof. Dr. Achim Klenke http://www.aklenke.de 2. Vorlesung: 26.10.2018 2/32 Inhalt 1 Folgen Begriffsbildung Grenzwerte 2 Summen und Produkte
Wiederholung fürs Abitur: wichtigste Reaktionen in Chemie
 1) elektrophile Addition mit einem Alken z. B. Ethen und Brom heterolytische Spaltung Nachweisreaktion für Doppelbindung Mechanismus 2) nukleophile Addition (H + ) Alkanal + Alkohol z. B. Aldehydgruppe
1) elektrophile Addition mit einem Alken z. B. Ethen und Brom heterolytische Spaltung Nachweisreaktion für Doppelbindung Mechanismus 2) nukleophile Addition (H + ) Alkanal + Alkohol z. B. Aldehydgruppe
Die Zelle. Membranen: Struktur und Funktion
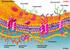 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Rund um das Hühnerei - die Chemie der Proteine
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Rund um das Hühnerei - die Chemie der Proteine Das komplette Material finden Sie hier: School-Scout.de VII/B Organische Verbindungen
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Rund um das Hühnerei - die Chemie der Proteine Das komplette Material finden Sie hier: School-Scout.de VII/B Organische Verbindungen
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Welcher Indikator ist für die Titration von Essigsäure (pks =4.76) mit Natronlauge am besten geeignet?
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Kohlenwasserstoffe. Homologe Reihe. Alkane. Alkene. HGA-Grundwissen Chemie-10. Klasse NTG
 GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
plasmatischen Seite. Einige der neutralen Glykolipide sind für die Blutgruppenspezifität von roten Blutzellen verantwortlich.
 plasmatischen Seite. Einige der neutralen Glykolipide sind für die Blutgruppenspezifität von roten Blutzellen verantwortlich. 20 NUCLEINSÄUREN Zur Reinigung und Trennung grossmolekularer Nucleinsäuren,
plasmatischen Seite. Einige der neutralen Glykolipide sind für die Blutgruppenspezifität von roten Blutzellen verantwortlich. 20 NUCLEINSÄUREN Zur Reinigung und Trennung grossmolekularer Nucleinsäuren,
V-Modul 427. Methoden der Zellfraktionierung und Proteomanalyse bis
 V-Modul 427 Methoden der Zellfraktionierung und Proteomanalyse 05.12.2016 bis 16.12.2016 Institut für Molekulare Evolution Heinrich-Heine-Universität Düsseldorf Methodik der Proteomanalyse Schritt 1: Isolierung
V-Modul 427 Methoden der Zellfraktionierung und Proteomanalyse 05.12.2016 bis 16.12.2016 Institut für Molekulare Evolution Heinrich-Heine-Universität Düsseldorf Methodik der Proteomanalyse Schritt 1: Isolierung
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
Lösungen, Stoffmengen und Konzentrationen
 12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Thematische Aufgliederung der Prüfungsfragen
 Seite 1 Thematische Aufgliederung der Prüfungsfragen (gemäss Abschlussprüfungen im Fach Chemie der Eidgenössischen Berufsmaturitätsprüfung Technischer Richtung) 1. Heterogene Mischungen; Trennmethoden
Seite 1 Thematische Aufgliederung der Prüfungsfragen (gemäss Abschlussprüfungen im Fach Chemie der Eidgenössischen Berufsmaturitätsprüfung Technischer Richtung) 1. Heterogene Mischungen; Trennmethoden
Lipide. Dr. med. Tamás Pándics. Biochemie I. SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie
 Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
GEBRAUCHSANLEITUNG. Lowry Assay Kit. Kit für die Proteinkonzentrationsbestimmung. (Kat.-Nr )
 GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
GEBRAUCHSANLEITUNG Lowry Assay Kit Kit für die Proteinkonzentrationsbestimmung (Kat.-Nr. 39236) SERVA Electrophoresis GmbH Carl-Benz-Str. 7 D-69115 Heidelberg Phone +49-6221-138400, Fax +49-6221-1384010
Komplexbildung. CoCl 3 5 NH 3. CoCl 3 6 NH 3. CoCl 3 4 NH 3 Alfred Werner The Nobel Prize in Chemistry 1913
 Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
Inhalt SEMINAR 1: mit zu bringen ist: 1. DC von Aminosäuren. 2. Pipettierübung (Präzisionskontrolle) 3. Gelfiltration
 SEMINAR 1: mit zu bringen ist: Arbeitsmantel Skriptum Rechner, Bleistift, Lineal... Protokollheft Und darin eingeklebt das Anwesenheitsblatt 1 Inhalt 1. DC von Aminosäuren 2. Pipettierübung (Präzisionskontrolle)
SEMINAR 1: mit zu bringen ist: Arbeitsmantel Skriptum Rechner, Bleistift, Lineal... Protokollheft Und darin eingeklebt das Anwesenheitsblatt 1 Inhalt 1. DC von Aminosäuren 2. Pipettierübung (Präzisionskontrolle)
Ungefähre Zusammensetzung des Blutes und des Blutplasmas. Die häufigsten Bestandteile des Blutplasmas (Mittelwerte)
 Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Puffer /Zusammensetzung des Blutes 1 Zusammensetzung des Blutes Das Blut der Wirbeltiere besteht zu 55% aus flüssigem Blutplasma und zu 45% aus darin schwimmenden festen Bestandteilen, den Blutkörperchen.
Aufbau und Konformation von Polypeptiden
 1 Aufbau und Konformation von Polypeptiden Peter Güntert, Sommersemester 2009 Hierarchie von Proteinstrukturen Primärstruktur: Aminosäuresequenz Sekundärstruktur: Helices, Faltblätter, Turns, Loops Tertiärstruktur:
1 Aufbau und Konformation von Polypeptiden Peter Güntert, Sommersemester 2009 Hierarchie von Proteinstrukturen Primärstruktur: Aminosäuresequenz Sekundärstruktur: Helices, Faltblätter, Turns, Loops Tertiärstruktur:
Angelika Stöcklinger. Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate
 Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Nach Terpenen und Kohlenhydraten nun eine weitere große Klasse an Naturstoffen
 260 17. Aminosäuren, Peptide ach Terpenen und Kohlenhydraten nun eine weitere große Klasse an aturstoffen 17.1 Übersicht Analog zu ydroxycarbonsäuren α-, β-, γ- Aminocarbonsäuren möglich: 2 3 2 2 α-amino-essigsäure
260 17. Aminosäuren, Peptide ach Terpenen und Kohlenhydraten nun eine weitere große Klasse an aturstoffen 17.1 Übersicht Analog zu ydroxycarbonsäuren α-, β-, γ- Aminocarbonsäuren möglich: 2 3 2 2 α-amino-essigsäure
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Kapitel II Elemente, kleine Moleküle, Makromoleküle Wiederholung
 Kapitel II Elemente, kleine Moleküle, Makromoleküle Wiederholung Biologie für Physikerinnen und Physiker Kapitel II Elemente, Moleküle, Makromoleküle 1 Anteil der Elemente die im menschlichen Körper und
Kapitel II Elemente, kleine Moleküle, Makromoleküle Wiederholung Biologie für Physikerinnen und Physiker Kapitel II Elemente, Moleküle, Makromoleküle 1 Anteil der Elemente die im menschlichen Körper und
