LK Physik 13 Quantenphysik. Richard Reindl
|
|
|
- Heidi Kurzmann
- vor 9 Jahren
- Abrufe
Transkript
1 LK Physik 13 Quantenphysik Richard Reindl 4
2 Die aktuellste Version des Skriptes findet man unter Das Werk steht unter einer Creative Commons - Namensnennung - Nicht-kommerziell - Weitergabe unter gleichen Bedingungen 3. Unported Lizenz 8. Oktober 13
3 1 Materiewellen 1.1 Elektronenbeugung 197 untersuchten Davisson und Germer sowie unabhängig davon P.G. Thomson das Verhalten von Elektronen, die auf ein Kristallgitter treffen. Thomson wandte dabei das Debye- Scherrer-Verfahren an, wie wir in unserem Versuch: Elektronen durchlaufen eine Beschleunigungsspannung U und treten dann durch eine polykristalline Grafitfolie. Die an der Folie gestreuten Elektronen treffen auf einen kugelförmigen Leuchtschirm (Radius: a = 14,cm), dessen Mittelpunkt in der Grafitfolie liegt. Auf dem Schirm beobachtet man zwei Beugungskreise, die zu den Netzebenenabständen d 1 = 1,3Å und d =,13Å ge- + U _ ϕ 6V a Grafitfolie Abb Versuch: Elektronenbeugung r hören. Die Radien dieser Kreise, auf dem kugelförmigen Schirm gemessen (Bogenlängen), seien r 1 und r. Erstes Versuchsergebnis: Elektronen zeigen Interferenzerscheinungen!! Aus der Bragg schen Beziehung n λ = d sinϕ (1.1.1) folgt mit ϕ = r a (wir beobachten in erster Ordnung, d.h. n = 1) λ = d sin r a (1.1.) Bei konstantem λ gehört zum größeren r das kleinere d, d.h. r 1 > r. Wir vergleichen die gemessenen λ-werte mit der kinetischen Energie W k und dem Impuls p der Elektronen: Das qualitative Versuchsergebnis W k = m v = e U = p = m v = emu (1.1.3) größeres U = kleineres r = kleineres λ legt die Vermutung nahe, dass λ entweder zu W k oder zu p proportional ist. In der Tabelle auf der folgenden Seite sind die Messergebnisse für verschiedene Beschleunigungsspannungen zusammengestellt. Die λ-werte für die beiden Radien r 1 und r sollten gleich sein, wir wählen den Mittelwert λ = λ 1 +λ. Der letzten Zeile der Tabelle entnimmt man, dass λ p = h = konst. (1.1.4) ist. Für die Konstante erhält man h = 6,7+6,63+6,63+6, Js = 6, Js (1.1.5) 3
4 1 Materiewellen U in V r 1 in m,18,145,15,115 r in m,3,6,5, λ 1 in 1 11 m,738,6 1,9 1,749 λ in 1 11 m,86,8 1,974 1,756 λ in 1 11 m,77,43 1,938 1,753 W k in 1 16 J 3, 4,8 6,4 8, p in 1 3 kgm s,416,959 3,416 3,8 W k λ in 1 6 kgm3 s,886 1,8 1,4 1,4 p λ in 1 34 kgm s 6,7 6,63 6,63 6,69 Der genaue Wert für das Plancksche Wirkungsquantum oder die Planckkonstante ist Weitere Versuche zeigen: h = 6, Js = 4, MeVs (1.1.6) Jeder Körper mit dem Impuls p zeigt Interferenzerscheinungen wie eine Welle mit der Wellenlänge λ = h (1.1.7) p. Diese 197 experimentell gefundene Tatsache wurde von Louis de Broglie schon 194 theoretisch vorausgesagt. Mit der Abkürzung und der Wellenzahl folgt aus (1.1.4) oder endgültig = h π = 1, Js = 6,581 1 MeVs (1.1.8) k = π λ p = h λ = πk π (1.1.9) = k (1.1.1) p = h λ = k (1.1.11) (de Broglie-Relation) Mit der Gesamtenergie E lautet die Energie-Impuls-Relation für ein Teilchen der Masse m E = p c +m c 4 = p c +E (1.1.1) oder p = 1 ( E c E ) 1 = c (E E ) (E +E ) = 1 c E k (E +E k ) (1.1.13) p = 1 c Ek (E +E k ) (1.1.14) Für langsame Teilchen kann man E k in der Summe gegen E vernachlässigen und es gilt E k m v ; damit geht (1.1.14) in die klassische Formel über: p 1 c Ek E 1 c mv mc = mv (1.1.15) Für die Wellenlänge eines Teilchens der kinetischen Energie E k gilt dann λ = hc Ek (E +E k ) (1.1.16) 4
5 1 Materiewellen 1. Die Wellenfunktion und ihre physikalische Bedeutung Ein Doppelspaltversuch mit Elektronen bereitet wegen der Kleinheit der Wellenlängen ungeheuere technische Schwierigkeiten. Gelöst wurden diese Schwierigkeiten 1961 von C. Jönsson an der Universität Tübingen, was eine weitere Bestätigung des Wellencharakters der Elektronen erbrachte. Durch das Auszählen der schwarzen Punkte auf dem Film kann die Zählrate S = Zahl der e Zeit (1..1) v v v 1 s z Film s in Abhängigkeit vom Ort bestimmt werden. Die experimentell gefundene Zählrate entspricht genau der Intensitätsverteilung einer Film Abb.1..1 Doppelspalt mit e klassischen Welle (z.b. Licht) mit der Wellenlänge λ = h p = h mv (1..) Das Interferenzverhalten der Elektronen versucht man durch eine den Elektronen zugeordnete Wellenfunktion ψ(x,t) zu beschreiben. Da Elektronen im Allgemeinen lokalisierbar sind, muss ψ(x, t) räumlich begrenzt sein. Dazu wird die Gleichung einer nach rechts fortschreitenden Welle (y = sin(k x ω t)) mit einer ortsabhängigen Amplitudenfunktion ϕ(x, t) multipliziert: ψ(x,t) = ϕ(x,t) sin(kx ωt) (1..3) (1..3) beschreibt ein sogenanntes Wellenpaket (siehe Abb. 1..). Wenn das Beugungsbild beim Doppelspaltversuch durch Interferenz der Wellenpakete verschiedener Elektronen entstehen würde, dann müssten alle während der Kohärenzzeit τ = x v durch die Spalte tretenden Elektronen gleichphasig sein, da es sonst keine konstruktive Interferenz geben würde. Die Annahme der Gleichphasigkeit der Wellenfunktionen verschiedener Elektronen ist aber durch nichts zu begründen. Es läßt sich also folgende Hypothese aufstellen: ψ ψ x Abb.1.. Wellenpaket ϕ v x Das Wellenpaket eines Elektrons teilt sich in zwei Teilpakete auf, die miteinander interferieren. (1..4) Die Hypothese (1..4) lässt sich folgendermaßen überprüfen: Ein sehr intensitätsarmer Elektronenstrahl wird durch den Doppelspalt geschickt. Die Intensität sei so gering, dass praktisch nie mehrere Elektronen gleichzeitig durch die Spalte treten. Mit S 1 bzw. S bezeichnen wir die Zählraten, wenn nur Spalt 1 bzw. nur Spalt geöffnet ist, S 1 sei die Zählrate, wenn beide Spalte gleichzeitig geöffnet sind. Wenn unsere Hypothese (1..4) 5
6 1 Materiewellen falsch wäre, d.h. wenn das ganze Wellenpaket eines Elektrons nur durch einen Spalt treten würde, dann könnte es bei unserem intensitätsarmen Strahl keine Interferenzen geben, da dann jedes einzeln durch einen Spalt gehende Elektron weder mit anderen Elektronen noch mit sich selbst interferieren könnte. Damit würden sich die Beugungsbilder der Einzelspalte überlagern zu S 1 = S 1 +S (siehe Abb. 1..3). Das Experiment liefert aber auch bei einer sehr geringen Intensität des einfallenden Elektronenstrahls das gleiche Interferenzbild wie bei einer starken Intensität (siehe Abb. 1..4). Damit scheint unsere Hypothese (1..4) experimentell abgesichert zu sein. Zur Kontrolle wird noch folgender Versuch ausgeführt: S S 1 S 1 S S 1 = S 1 +S Abb.1..3 Nur jeweils ein Spalt offen S S 1 S 1 S S 1 S 1 +S Abb.1..4 Beide Spalte offen z z Direkt hinter den Einzelspalten werden Zähler angebracht, die einzelne Elektronen registrieren können. Entgegen unserer Hypothese (1..4) wird ein Elektron beim Durchgang durch den Doppelspalt immer nur von einem Zähler registriert! Die volle Energie eines Elektrons geht nur durch einen Spalt! (1..5) Um die einander widersprechenden, aber doch experimentell abgesicherten Tatsachen (1..4) und (1..5) miteinander in Einklang zu bringen, wurden die höchsten philosophischen Purzelbäume geschlagen. Der populärste dieser Purzelbäume, der auch heute noch durch viele Physikbücher geistert, ist der sogenannte Dualismus Welle-Teilchen. Dieser Dualismus besagt Folgendes: v v v 1 Zähler 1 Zähler Abb.1..5 Beide Spalte offen Elektronen und andere Mikroobjekte sind Gebilde, die in manchen Versuchen Teilchen- und in anderen Versuchen Wellencharakter zeigen (Wellen-Teilchen-Dualismus). (1..6) Um diesen logisch unbefriedigenden Dualismus aus der Welt zu schaffen, müssen wir uns überlegen, welche Aufgabe einer physikalischen Theorie überhaupt zukommt: Eine physikalische Theorie hat die Aufgabe, bei einer gegebenen Versuchsanordnung die experimentell messbaren physikalischen Größen vorherzusagen. (1..7) Betrachten wir unseren Doppelspaltversuch: Messbar sind nur die Auftrefforte der Elektronen in der Beobachtungsebene und diese Auftrefforte sind sogar statistisch verteilt. Wirklich messbar ist also nur die Auftreffwahrscheinlichkeit eines Elektrons an einem bestimmten Ort. Die Theorie hat die Aufgabe, diese Auftreffwahrscheinlichkeit zu berechnen, nichts sonst! 6
7 1 Materiewellen Ausssagen wie Das Elektron ist ein Teilchen, Das Elektron ist eine Welle oder Das Elektron ist würfelförmig gehören in das Reich der Spekulationen, solange sie nicht direkt experimentell zugänglich sind. Experimentell zugänglich sind aber nur die Wirkungen der Elektronen auf geeignete Messapparaturen und nur diese Wirkungen können durch eine sinnvolle physikalische Theorie beschrieben werden. Literatur: The Feynman Lectures on Physics, Bd. 3 Berkeley Physics Course, Bd. 4 Kommen wir jetzt zu der Frage, wie man die Wahrscheinlichkeit, ein Elektron an einem bestimmten Ort zu finden, berechnen kann. Die Wahrscheinlichkeit dp, das Elektron im Intervall [x, x + dx] anzutreffen, ist sicher proportional zu dx, d.h. dp = w(x,t)dx (1..8) mit der Wahrscheinlichkeitsdichte w(x, t). Die zentrale Frage ist jetzt, wie w(x, t) mit der Wellenfunktion ψ(x,t) = ϕ(x,t) sin(kx ωt) zusammenhängt. Da w(x,t) gilt und ψ(x,t) oszilliert und somit auch negative Werte annimmt, kann ψ nicht gleich w sein. Diese Schwierigkeit wird überwunden, wenn man den Betrag w w = ψ ϕ w(x,t) = ψ = ϕ sin(kx ωt) (1..9) v oder das Quadrat x w(x,t) = ψ = ϕ sin (kx ωt) (1..1) Abb.1..6 w(x,t) = ψ(x,t) der Wellenfunktion als Wahrscheinlichkeitsdichte interpretiert. (1..9) hat den Nachteil, dass viele nichtdifferenzierbare Stellen (Spitzen) vorhanden sind. Auch(1..1) hat noch einen Nachteil: Innerhalb des Wellenpakets der Breite x hat w(x,t) noch viele Nullstellen, was den experimentellen Tatsachen widerspricht (ein Elektron ist nicht zerhackt ). Die ideale Form von w w = ψ Abb.1..7 w(x,t) = ψ(x,t) ϕ v x w(x, t) wäre die von Abb Die Wellenfunktion ψ(x, t) selbst muss aber den oszillierenden Term sin(kx ωt) enthalten, um die experimentell beobachteten Interferenzen richtig zu beschreiben. Diese Schwierigkeit wird elegant überwunden, wenn man statt sin(kx ωt) den komplexen Term w w Abb.1..8 Das ideale w(x, t) v x e i(kx ωt) = cos(kx ωt)+i sin(kx ωt) (1..11) verwendet und die Wahrscheinlichkeitsdichte als das Quadrat des Betrages von ψ(x, t) definiert (Max Born, 196): w(x,t) = ψ(x,t) = ψ(x,t) ψ (x,t) (1..1) mit ψ(x,t) = ϕ(x,t) e i(kx ωt) (1..13) 7
8 1 Materiewellen Wegen e iα = 1 gilt w(x,t) = ψ(x,t) = ϕ(x,t) (1..14) Die Betragsstriche bei ϕ lassen wir stehen, damit im Bedarfsfall ϕ auch komplex gewählt werden kann. Die Wahrscheinlichkeit, das Elektron zur Zeit t im Intervall [a, b] anzutreffen, ist P(a,b) = b a w(x,t)dx = Da sich das Teilchen irgendwo zwischen und + befinden muss, ist Es gilt also die Normierungsbedingung + b a ψ(x,t) dx (1..15) P(,+ ) = 1 (1..16) w(x,t)dx = + ψ(x,t) dx = 1 (1..17) Für räumliche Probleme muss x in obigen Gleichungen durch den Ortsvektor r und dx durch das Volumenelement dv ersetzt werden: P(V) = w( r,t)dv = ψ( r,t) dv (1..18) V ist somit die Wahrscheinlichkeit, das Teilchen im Raumbereich V anzutreffen. Die Normierungsbedingung lautet dann ganzer Raum w( r,t)dv = V ganzer Raum ψ( r,t) dv = 1 (1..19) Damit die Wellenfunktion zur Beschreibung von Interferenzen geeignet ist, muss das Superpositionsprinzip gelten: Sind die ψ ν gültige Wellenfunktionen eines physikalischen Systems, dann ist auch n ψ = a ν ψ ν ν=1 eine Wellenfunktion des Systems. Die a ν müssen dabei so gewählt werden, dass ψ wieder normiert ist. (1..) Wellenfunktionen können also, mit geeigneten Gewichtungsfaktoren a ν, zu neuen Wellenfunktionen addiert werden, nicht aber die Wahrscheinlichkeitsdichten: w = ψ n = a ν ψ ν ν=1 n a ν ψ ν = ν=1 n a ν w ν (1..1) ν=1 8
9 1 Materiewellen 1.3 Wellenpakete als Überlagerung ebener Wellen Das Ziel der Quantenmechanik (QM) ist es, eine möglichst einfache Differentialgleichung F(ψ, ψ, ψ,..., ψ, ψ,...) = (1.3.1) für die Wellenfunktion ψ zu finden, die das Verhalten der Mikroobjekte richtig beschreibt. Wegen des Superpositionsprinzips (siehe (1..)) muss die Summe zweier Lösungen von (1.3.1) wieder eine Lösung ergeben. Das ist nur möglich, wenn (1.3.1) eine lineare Differentialgleichung ist, d.h. wenn ψ und die Ableitungen von ψ nur linear in die Gleichung eingehen: F(ψ, ψ,...) = aψ +b 1 ψ +b ψ c1 ψ +c ψ +... = (1.3.) Als weitere Forderung stellen wir an (1.3.1), dass die einfachste Wellenfunktion, nämlich die einer ebenen Welle ψ(x,t) = A e i(kx ωt) (1.3.3) eine Lösung ist. Wegen der Linearität von (1.3.1) ist damit jede Überlagerung ebener Wellen ψ(x,t) = n A ν e i(kνx ωνt) (1.3.4) ν=1 ebenfalls eine Lösung von (1.3.1). Es lässt sich exakt zeigen, dass auch die Überlagerung unendlich vieler ebener Wellen, deren Wellenzahlen k kontinuierlich verteilt sind, eine Lösung von (1.3.1) ist. Aus den diskreten Amplitudenwerten A ν in (1.3.4) wird dann die Funktion A(k) und das Summenzeichen geht in ein Integral über: wobei ω eine Funktion von k ist: ψ(x,t) = A(k) e i(kx ωt) dk (1.3.5) ω = ω(k) (1.3.6) In der sogenannten Dispersionsrelation (1.3.6) steckt die konkrete Physik der betrachteten Welle. Für elektromagnetische Wellen im Vakuum mit der Wellenlänge λ und der Frequenz f gilt z.b. λ f = π k ω π Bei Gültigkeit von (1.3.7) sagt man, es herrscht keine Dispersion. Alle Teilwellen eines Wellenpakets breiten sich mit der gleichen Geschwindigkeit aus, die Form des Wellenpakets bleibt also erhalten: = c = ω = ω(k) = c k mit konstantem c (1.3.7) w(x,t) = w(x ct,) (1.3.8) w w(x,) c t Abb Keine Dispersion w(x,t) = w(x ct,) c x 9
10 1 Materiewellen Leite zur Übung (1.3.8) aus (1.3.5) und (1.3.7) her! In Materie ist die Lichtgeschwindigkeit von der Wellenlänge bzw. der Frequenz abhängig, d.h. die Teilwellen eines Wellenpakets (1.3.4) oder (1.3.5) laufen mit verschiedenen Geschwindigkeiten. Damit ändert sich die Form eines Wellenpakets mit der Zeit, das Wellenpaket zerfließt, es herrscht Dispersion. w w(x,) c t Abb.1.3. Mit Dispersion w(x,t) w(x ct,) c x Die Dispersionsrelation und das Zerfließen von Materiewellen behandeln wir im nächsten Kapitel. Die Dirac sche Deltafunktion ist durch folgende Eigenschaften definiert: δ(x) = für x δ(x x ) f(x)dx = f(x ) (1.3.9) Mit der Deltafunktion kann die Überlagerung endlich vieler Wellen (1.3.4) auch als Integral (1.3.5) geschrieben werden, wenn man folgendes A(k) wählt und ω ν = ω(k ν ) beachtet: A(k) = n A ν δ(k k ν ) (1.3.1) Eine Grenzwertdarstellung der Deltafunktion behandeln wir in den Aufgaben. ν=1 Als einfachstes Beispiel betrachten wir zunächst die Überlagerung von zwei ebenen Wellen mit den Amplituden A 1 = A = 1: ψ(x,t) = e i(k 1x ω 1 t) +e i(k x ω t) (1.3.11) In den Aufgaben zu unseren mathematischen Hilfsmitteln haben wir die Formel bewiesen. Damit folgt e ia +e ib = cos a b e i a+b (1.3.1) mit ψ(x,t) = cos k x ω t k = k k 1, ω = ω ω 1, k = k 1 +k In Abb sind die Grafen des Realteils des Imaginärteils Re(ψ(x,t) = cos Im(ψ(x,t) = cos k x ω t k x ω t 1 e i(k x ω t) und ω = ω 1 +ω (1.3.13) (1.3.14) cos(k x ω t) (1.3.15) sin(k x ω t) (1.3.16)
11 1 Materiewellen und der Einhüllenden ±ϕ(x, t) mit ϕ(x,t) = cos k x ω t (1.3.17) für k 1 = 3, k = 4 und t = dargestellt, der rechte Teil der Abbildung zeigt die (in diesem Fall nicht normierbare) Wahrscheinlichkeitsdichte k x ω t w(x,t) = 4 cos (1.3.18) ebenfalls zur Zeit Null. Die Breite x einer Schwebungsgruppe ist die halbe Wellenlänge der Einhüllenden, d.h. oder Die Wellenlänge der eigentlichen Welle ist x = 1 π k = π k (1.3.19) x k = π (1.3.) λ = π k (1.3.1) und damit ist die Zahl n von Wellenzügen innerhalb einer Schwebungsgruppe n = x λ = k k (1.3.) Je kleiner k ist, umso ausgeprägter ist die Schwebung, d.h. umso mehr Wellenzüge sind in einer Schwebungsgruppe. Die Welle selbst breitet sich mit der Phasengeschwindigkeit v p = ω k (1.3.3) aus, die Geschwindigkeit einer Schwebungsgruppe oder auch von w(x, t) ist die Gruppengeschwindigkeit v g = ω (1.3.4) k Für eine ordentliche Schwebung (viele Wellenzüge pro Gruppe) ist k klein, d.h. ω(k) kann im Intervall [k 1, k ] linear angenähert werden. Weil k wegen (1.3.14) der Mittelpunkt dieses Intervalls ist, gilt v g dω dk (1.3.5) k=k 11
12 1 Materiewellen ψ(x) = e 3ix +e 4ix w(x) = cosx Abb ψ(x) = e 3ix +e 3,5ix +e 4ix w(x) = 4cos x +cosx Abb ψ(x) = e 4ix +e 4.5ix +e 5ix +e 5.5ix +e 6ix w(x) = ψ(x) Abb ψ(x) = e 4ix +e 4.5ix +e 5ix +e 5.5ix +e 6ix w(x) = ψ(x) Abb ψ(x) = e 4ix +e 4,1ix +3e 4,ix +4e 4,3ix +4e 4,4ix + 3e 4,5x +e 4,6x +e 4,7x w(x) = ψ(x) Abb
13 1 Materiewellen Den Abbildungen Abb bis Abb (mit MAPLE erstellt) entnimmt man, dass immer mehr kleine Schwebungsgruppen zwischen zwei großen Gruppen auftreten, wenn die Zahl der überlagerten Wellen zunimmt oder anders ausgedrückt: Je mehr Wellen überlagert werden, umso weiter rücken die Hauptschwebungsgruppen auseinander. Wir wollen jetzt untersuchen, wie die Überlagerung von unendlich vielen Wellen gleicher Amplitude A mit Wellenzahlen aus dem Intervall [k 1, k ] aussieht, wobei wir uns auf die Zeit Null beschränken. Mit der Wellenzahlverteilung { A für k 1 k k A(k) = (1.3.6) sonst folgt aus (1.3.5) k ψ(x,) = A e ikx dk = k 1 Mit der Formel e ia e ib = i sin a b (Aufgaben zu den mathematischen Hilfsmitteln) folgt A ( ) ix e ikx e ik 1x (1.3.7) e i a+b (1.3.8) mit ψ(x,) = A x sin k x e ik x k = k k 1 und k = k 1 +k Die Wahrscheinlichkeitsdichte zur Zeit Null ist dann (1.3.9) (1.3.3) w(x,) = 4A x sin k x (1.3.31) Als Breite x des Paketes definieren wir den Abstand der beiden Nullstellen des Hauptpaketes: woraus x = π k (1.3.3) x k = 4π (1.3.33) folgt. Beispiele für die Grafen von Re(ψ(x,)), Im(ψ(x,)) und w(x,) findet man in Abb und Abb w(x,) ist nicht normiert, da es uns nur um die Form des Wellenpaketes geht. Wir kommen der idealen Form eines Wellenpaketes schon näher, aber es stört noch das Auftreten der immer kleiner werdenden Nebengruppen. Diese verdanken ihr Vorhandensein den scharfen Kanten in der Wellenzahlverteilung. Daher betrachten wir als nächstes Beispiel eine Gauß sche Wellenzahlverteilung ohne Ecken und Kanten: Die Überlagerung aller Teilwellen ergibt dann die Wellenfunktion ψ(x,t) = A A(k) = A e (k k ) a (1.3.34) e (k k ) a e i(kx ω(k)t) dk (1.3.35) 13
14 1 Materiewellen 1 A(k) Re(ψ) und Im(ψ) w(x) = 1 cosx π x Abb A(k) Re(ψ) und Im(ψ).4 w(x) = 1+3cosx 4cos3 x π x Abb A(k) = e (k 4) Re(ψ) und Im(ψ) w(x) = e x 4π Abb A(k) = e 4(k 4) Re(ψ) und Im(ψ).1 w(x) = e x 8 16π Für t = erhält man Ein Integral der Form ψ(x,) = A Abb F(x) = 1 π e (k k ) a e ikx dk (1.3.36) A(u) e iux du (1.3.37) nennt man die inverse Fouriertransformierte von A(u). In einer mathematischen Formelsammlung (allerdings nicht in unserer Schulformelsammlung) findet man unter dem Kapitel Fouriertransformation A(u) = e u a = F(x) = a π e a 4 x (1.3.38) 14
15 1 Materiewellen Damit folgt aus (1.3.36) mit der Substitution u = k k (du = dk) ψ(x,) = A = A e ik x e u a e iux+ik x dk = e u a e iux dk = = A a π e a 4 x e ik x (1.3.39) Die Wahrscheinlichkeitsdichte unseres Wellenpaketes ist dann w(x,) = ψ(x,) = A a π e a x (1.3.4) d.h. wenn A(k) eine Gauß sche Funktion ist, dann ist es auch w(x). Als Breite einer Gaußfunktion definiert man üblicherweise die Breite in der 1 e-fachen Höhe des Maximums: A(k) = A() e w(x) = w() e Für das Produkt der Breiten erhalten wir = k = k ± a (1.3.41) = x = a (1.3.4) k = a und x = a (1.3.43) k x = 4 (1.3.44) Das Integral (1.3.35) kann für t nur ausgewertet werden, wenn die Funktion ω(k) bekannt ist. Wenn k klein ist, dann kann ω(k) in dem Bereich, in dem A(k) wesentlich von Null verschieden ist, linear angenähert werden: ω(k) = ω +v g (k k ) (1.3.45) ω(k ) A(k) ω(k) mit ω = ω() und v g = ω (k ) = dω dk (1.3.46) k=k Damit berechnet sich die Wellenfunktion (1.3.35) zu k 1 k k Abb Lineare Näherung k ψ(x,t) = A = A = A e i(k v g ω )t e (k k ) a e i(kx ωt) dk = e (k k ) a e i(kx ω t v gkt+v gk t) dk = e (k k ) a e ik(x vgt) dk (1.3.47) 15
16 1 Materiewellen Mit der Substitution u = k k gilt du = dk und somit ψ(x,t) = A e i(k v g ω )t = A e i(k v g ω )t e ik (x v gt) = A e i(k x ω t) e u a e i(u+k )(x v gt) du = e u a e iu(x vgt) du e u a e iu(x vgt) du = (1.3.48) Mit (1.3.37) und (1.3.38) folgt dann ψ(x,t) = π A e i(k x ω t) a π e a 4 (x vgt) (1.3.49) oder endgültig mit der Wahrscheinlichkeitsdichte ψ(x,t) = A a π e a 4 (x vgt) e i(k x ω t) (1.3.5) w(x,t) = A a π e a (x vgt) (1.3.51) (1.3.5) und (1.3.51) sind noch nicht normiert. Mit der Integralformel e b x dx = π b (1.3.5) folgt aus (1.3.51) N := = A a π w(x,)dx = A a π π a = A a π 3 Division von w durch N und von ψ durch N liefert endgültig e a x dx = a ψ(x,t) = e a 4 (x vgt) e i(k x ω t) π (1.3.53) (1.3.54) und w(x,t) = a π e a (x vgt) = w(x v g t,) (1.3.55) Die Einhüllende von ψ und die Wahrscheinlichkeitsdichte w behalten also ihre Form und bewegen sich mit der Gruppengeschwindigkeit v g in Richtung der positiven x-achse. Wenn wir statt der linearen die quadratische Näherung für ω(k) verwendet hätten, würde auch die Formänderung des Wellenpakets (Zerfließen) richtig beschrieben. 16
17 1.4 Teilchen als Wellenpakete 1 Materiewellen In diesem Kapitel wollen wir versuchen, die Bewegung eines wechselwirkungsfreien materiellen Teilchens (z.b. eines Elektrons) quantenmechanisch richtig zu beschreiben. Das Teilchen habe den klassischen (d.h. nicht quantenmechanischen) Impuls p und die Masse m. Unsere bisherige Modellvorstellung sieht folgendermaßen aus: Dem Teilchen ist eine Wellenfunktion ψ(x,t) zugeordnet, die als Überlagerung ebener Wellen geschrieben werden kann (Wellenpaket): ψ(x,t) = A(k) e i(kx ω(k)t) dk (1.4.1) Die Aufenthaltswahrscheinlichkeit des Teilchens im Intervall [x 1,x ] ist P(x 1,x ) = x x 1 w(x,t)dx mit w(x,t) = ψ(x,t) (1.4.) DieKreisfrequenzω derwellenfunktion ist einefunktionderwellenzahl k,d.h. ω = ω(k) (Dispersionsrelation). Die klassische Geschwindigkeit v des Teilchens ist gleich der Gruppengeschwindigkeit des Wellenpakets; v = p m = v g = ω (k ) = dω dk (1.4.3) k=k k entspricht dabei dem Maximum der Wellenzahlverteilung A(k). Es gilt die de Broglie-Relation p = k = h λ (1.4.4) Was wir noch nicht kennen, ist die Gleichung der Funktion ω(k). Zu ihrer Berechnung verwenden wir (1.4.3) und (1.4.4): v = ω (k ) = p m = m k (1.4.5) Da diese Beziehung für jedes k gelten muss, folgt ω (k) = k (1.4.6) m und damit ω(k) = k m Die kinetische Energie des Teilchens ist W = m v = p m = k m +C (1.4.7) (1.4.7) = ω(k ) C (1.4.8) Da ω gilt, ist die Wertemenge von W nach (1.4.8) gleich [ C, + ]. Da die tatsächliche Wertemenge von W [, + ] ist, muss C = sein. Die Dispersionsrelation für ein wechselwirkungsfreies, nichtrelativistisches Teilchen lautet also ω(k) = k m (1.4.9) 17
18 Aus (1.4.8) folgt dann die Planck-Relation 1 Materiewellen W = ω(k ) = ω = hf (1.4.1) Für ein relativistisches Teilchen beginnen wir mit der Energie-Impuls-Relation, wobei E die relativistische Gesamtenergie des Teilchens bezeichnet: E = p c +m c 4 = k c +m c 4 (1.4.11) Differenzieren nach ω ergibt mit und E = γmc, p = γmv, γ = 1 1 β dk dω = 1 dω dk = 1 v unter Verwendung der Kettenregel (1.4.1) Setzt man (1.4.16) in (1.4.11) ein, dann erhält man E de dω = c k dk dω = c k 1 v (1.4.13) γmc de dω = c k 1 v (1.4.14) de dω = k γmv = p = p (1.4.15) E = ω +C (1.4.16) ( ω + C ) = k c + m c 4 (1.4.17) Zur Probe differenzieren wir (1.4.17) nach k: ( ω + C ) dω dk = kc (1.4.18) dω dk = kc ω + C = kc ω +C = pc E = γmvc γmc = v (1.4.19) Die Beziehung v = dω dk gilt also unabhängig von der Wahl der Konstanten C. Wir wählen natürlich den einfachsten Wert C =. Damit gilt auch im relativistischen Fall die Planck- Relation E = ω (1.4.) und die Dispersionsrelation (1.4.17) lautet für ein relativistisches Teilchen ω = k c + m c 4 (1.4.1) Es sei hier noch einmal mit aller Deutlichkeit darauf hingewiesen, dass nichts mit der Frequenz f = ω π schwingt und ω somit nicht gemessen werden kann. ω ist eine reine Rechengröße, die zur Berechnung der messbaren Aufenthaltswahrscheinlichkeiten verwendet wird. So ist es auch kein Dilemma, dass sich das klassische und das relativistische ω auch für kleine Geschwindigkeiten beträchtlich voneinander unterscheiden (siehe Aufgaben). Im vorhergehenden Kapitel haben wir Wellenpakete aus ebenen Wellen aufgebaut, ohne einen konkreten physikalischen Hintergrund dafür zu haben. Jetzt kennen wir die Dispersionsrelation eines freien Teilchens und können uns, mit kräftiger Unterstützung eines Computeralgebrasystems (MAPLE), an die Konstruktion der Wellenfunktion eines (nichtrelativistischen) Teilchens 18
19 1 Materiewellen mit der Masse m undder Geschwindigkeit v = v g heranmachen. Wir gehen von einer Gauß schen Wellenzahlverteilung A(k) = A e (k k ) a (1.4.) aus. Mit (1.4.1) und (1.4.9) erhalten wir ψ(x,t) = A e (k k ) a e i(kx k m t) dk (1.4.3) Nach einigem guten Zureden (siehe MAPLE-Worksheet) erhalten wir vom CAS folgende Ergebnisse: ψ(x,t) = ϕ(x,t) e i(k x ω t) (1.4.4) mit und die normierte Wahrscheinlichkeitsdichte (x vt) 4(bt i) ϕ(x,t) = konst. eia (1.4.5) 1+ibt (x vt) w(x,t) = a e a (1+b t ) (1.4.6) π 1+b t mit ω = W = mv und b = a m (1.4.7) ϕ(x, t) ist nicht reell, d.h. ψ(x, t) ist keine ebene Welle mit ortsabhängiger Amplitude. Vielmehr hängt sogar die Wellenlänge des Paketes vom Ort ab. Das hat aber alles keine Bedeutung, da nur w(x, t) gemessen werden kann. Zur grafischen Darstellung der Wellenfunktion kann man noch folgende Schreibweise wählen: ψ(x,t) = w(x,t) ξ(x,t) (1.4.8) Da ψ = w gilt, ist ξ(x,t) = 1, d.h. ξ(x,t) ist eine Welle mit der Amplitude 1 und w(x,t) ist die Einhüllende. In Abb sind die Realteile von ψ und ξ zu zwei verschiedenen Zeiten gezeichnet. t = 4s 1 1 t = 4s 1 1 Abb ψ(x,t) und ξ(x,t) 19
20 1 Materiewellen t = s t =,5,5 5 5,5,5 t = s t = 4s,5,5 5 5,5,5 t = 6s t = 8s,5,5 5 5,5,5 Abb.1.4. Re(ψ), Im(ψ) und die Einhüllenden ± w Abb.1.4. zeigt die zeitliche Entwicklung eines Wellnpaketes für a = 1, b = 1 und v = 4. Mit MAPLE kann man viele dieser Bilder berechnen und dann mit dem Befehl animate als eindrucksvollen Film ablaufen lassen. Es ist deutlich das Zerfließen des Wellenpaketes zu erkennen! Aber aufgepasst: Nicht das Teilchen selbst wird immer breiter, sondern nur unsere Kenntnis vom Aufenthaltsort des Teilchens! Man beachte die zeitliche Symmetrie der Bilder zum Zeitnullpunkt! Man muss das ganze Geschehen wie folgt interpretieren: Zur Zeit Null wird der Aufenthaltsort des Teilchens gemessen. Das Ergebnis der Messung ist die Funktion w(x, ), deren Breite die Genauigkeit der Ortsmessung wiederspiegelt. Da w(x,t) für t breiter ist als w(x,), kann die Geschwindigkeit des Teilchens zum Zeitpunkt der Ortsmessung nicht genau bekannt sein. Genaueres hierzu in den Aufgaben und im nächsten Kapitel. 1.5 Die Unbestimmtheitsrelationen Die Bewegung eines Teilchens der Masse m mit der Geschwindigkeit v wird beschrieben durch die Wahrscheinlichkeitsdichte (1.4.6) a (x v w(x,t) = a e t) (1+b t ) (1.5.1) π 1+b t mit der Wellenzahlverteilung der Gruppengeschwindigkeit A(k) = A e (k k ) a (1.5.) v = p m = k m (1.5.3)
21 und der Konstanten 1 Materiewellen b = a v = a k m (1.5.4) Wir wählen eine Zeit t, zu der die Breite x des Wellenpaketes (beim 1 e-fachen des Maximalwertes) groß ist gegen seine Breite x zur Zeit Null. Aus (Nachweis!) folgt x = (1+b t ) a x x t 1 b (1.5.5) (1.5.6) Wenn das Teilchen exakt die Geschwindigkeit v hätte, wäre es zur Zeit t am Ort x = v t (bis auf eine Ungenauigkeit in der Größenordnung der Anfangsbreite, die wir vernachlässigen). Ist die Geschwindigkeit des Teilchens aber v = v + v, dann befindet es sich zur Zeit t am Ort x = v t = x + v t. Die Wahrscheinlichkeit W p dafür, dass das Teilchen zur Zeit Null einen Impuls aus dem Intervall [p, p + δp] hat ist gleich der Wahrscheinlichkeit, dass seine Geschwindigkeit aus w v t δx x x v t Abb Bewegung eines Wellenpakets x dem Intervall [v, v + δv] mit δv = δp m ist. Diese Wahrscheinlichkeit ist aber gleich der Wahrscheinlichkeit W x, das Teilchen zur Zeit t im Ortsintervall [x, x+δx] mit δx = (v +δv) t v t = δv t = δp zu finden. Bezeichnen wir mit w p die Wahrscheinlichkeitsdichte für den Impuls, dann gilt Wegen (1.5.6) gilt t m W p = w p (p) δp = W x = w(x,t) δx = w(x,t) δp t m (1.5.7) (1.5.8) 1+b t b t (1.5.9) Mit guter Näherung folgt dann aus (1.5.8) und (1.5.1) unter Berücksichtigung von x v t = x + v t x = v t (1.5.1) w p (p) = w(x,t) t m = a p b m = a e a π bm v t b t e a π bt (1.5.4) = t m = a e p π a (1.5.11) w p (p) = a e (p p) π a (1.5.1) Die Wahrscheinlichkeit, dass die Wellenzahl aus dem Intervall [k, k + δk] stammt, ist W k = w k (k) δk = w p (p) δp = w p ( k) δk (1.5.13) 1
22 1 Materiewellen Damit folgt w k (k) = a e (k k) a π (1.5.14) Ein Vergleich mit (1.5.) zeigt, dass w k (k) = A(k) (1.5.15) gilt, wenn A geeignet gewählt wird. Die Betragsstriche schreiben wir vorsichtshalber, weil A(k) auch komplex sein könnte. (1.5.1) zeigt, dass nicht nur der Ort des Teilchens, sondern auch sein Impuls eine Größe ist, die durch eine Wahrscheinlichkeitsdichte beschrieben wird. Die 1 e -Breite der Impulsverteilung ist p = a (1.5.16) Für die Breite der Ortsverteilung folgt für t 1 b aus (1.5.5) und (1.5.16) x(t) = a m t = p m t = v t (1.5.17) v ist somit die Geschwindigkeit, mit der das Wellenpaket immer breiter wird. Abb.1.4. bzw. Gleichung (1.5.5) entnimmt man, dass das Wellenpaket zur Zeit Null die geringste Breite hat. Diese Tatsache muss man so interpretieren: Zur Zeit t = wird der Ort und der Impuls des Teilchens gemessen. Die Unbestimmtheiten der Messung sind x und p. Zu allen anderen Zeiten (sowohl t > als auch t < ) ist die Unbestimmtheit des Aufenthaltsortes wegen der Unbestimmtheit des Impulses größer als zur Zeit Null. (1.5.5) entnimmt man die Ortsunschärfe zur Zeit Null: x = x() = a (1.5.18) Aus (1.5.16) und (1.5.18) folgt für die Unschärfen zur Zeit der Messung x p = 4 (1.5.19) (für 1 e -Breiten) (1.5.19) ist unsere erste Fassung der berühmten Unschärferelation für Ort und Impuls, die Werner Heisenberg im Jahre 197 als erster entdeckte. Heisenberg verwendete aber nicht die 1 e-breiten der Wahrscheinlichkeitsdichten, sondern die Standardabweichungen von den Mittelwerten von Ort und Impuls (Überprüfe die folgenden Gleichungen!): σ x = σ p = x = p = (x x ) = (p p ) = w(x,) xdx = (1.5.) w p (p) pdp = p (1.5.1) w(x,) x dx = 1 a (1.5.) w p (p) (p p ) dx = 1 4 a (1.5.3)
23 Damit lautet die Unschärferelation 1 Materiewellen σ x σ p = (für Standardabweichungen) (1.5.4) (1.5.19) und (1.5.4) haben wir für ein Gauß sches Wellenpaket abgeleitet. Heisenberg zeigte, dass allgemein σ x σ p (1.5.5) gilt. Das Gleichheitszeichen gilt nur für ein Gauß sches Paket. Im dreidimensionalen Fall gilt: σ x σ px σ y σ py σ z σ pz (1.5.6) Diese Gleichungen müssen wie folgt interpretiert werden: Misst man bei einer Vielzahl von identisch präparierten Teilchen gleichzeitig den Ort und den Impuls, dann gelten für die Standardabweichungen der Messwerte die Ungleichungen (1.5.6). Abb.1.5. zeigt den Zusammenhang zwischen der Standardabweichung σ p und einer möglichen Definition der Breite p der Wahrscheinlichkeitsdichte w p (p) (Analoges gilt für σ x und x). Für ein Gauß sches Wellenpaket findet man das Teilchen mit den folgenden Wahrscheinlichkeiten in den entsprechenden Intervallen (die gleichen Wahrscheinlichkeiten gelten für die entsprechenden x- Intervalle): w p p p 1 p p Abb.1.5. Breite und Standardabweichung σ p σ p p P[p σ p, p +σ p ] = 68,3% P[p σ p, p +σ p ] = 95,4% P[p 3σ p, p +3σ p ] = 99,7% (1.5.7) x = σ x p = σ p = x p,3h (68,3%) x = 4σ x p = 4σ p = x p 8 1,7h (95,4%) x = 6σ x p = 6σ p = x p 18,86h (99,7%) (1.5.8) Wenn es nur auf Größenordnungen ankommt, schreibt man (1.5.8) meist in der einfachen Form x p h (1.5.9) Neben der Unschärferelation für Ort und Impuls gibt es eine analoge Beziehung für die Unschärfen von Energie und Zeit. Da die exakte Herleitung dieser Beziehung über die Wahrscheinlichkeitsverteilungen der Größen Energie und Zeit nicht ganz einfach ist, beschränken wir uns auf eine Plausibilitätsbetrachtung. Als sinnvolle Breite der Energieverteilung eines Gauß schen Wellenpaketes bietet sich (siehe Abb.1.5.) E = σ E = E E 1 = p m p 1 m (1.5.3) 3
24 1 Materiewellen an. Mit p 1 = p σ p und p = p +σ p folgt daraus σ E = (p +σ p ) (p σ p ) 4m = p σ p m (1.5.31) Die Wahrscheinlichkeit, das Teilchen im Zeitintervall [t, t + dt] am Ort x = zu finden, ist w t (t) dt. Das Wellenpaket bewegt sich mit der Gruppengeschwindigkeit v = p m über den Beobachter am Ort x = hinweg. Als Breite der Zeitverteilung bietet sich daher t = σ t = x v = σ x v (1.5.3) an. Damit gilt oder zusammengefasst σ E σ t = p σ p m σx v = σ x σ p σ E σ t (1.5.33) (1.5.34) Analog zu (1.5.9) erhält man E t h (1.5.35) Diese Gleichung muss folgendermaßen interpretiert werden: Werden bei einer Vielzahl von identisch präparierten physikalischen Zuständen Energiemessungen der mittleren Zeitdauer t ausgeführt und bezeichnet E die Unschärfe der Messwerte, dann gilt (1.5.35). Eine Energiemessung der Dauer t ist also notwendigerweise mit dem Fehler E h t (1.5.36) behaftet. Mit der gleichen Energieunschärfe ist ein physikalischer Zustand behaftet, der nur für eine gewisse Zeit t ( Lebensdauer ) existiert. Wir werden in einem späteren Kapitel mit (1.5.36) die Frequenzbreite von Spektrallinien berechnen, die eng mit der Energieunschärfe von atomaren Zuständen zusammenhängt. Die Unschärfebeziehung (1.5.36) zwingt uns auch dazu, den Energiesatz neu zu überdenken: Verletzungen des Energiesatzes um δe sind für Zeitdauern t mit einer gewissen Wahrscheinlichkeit möglich, wenn δe kleiner oder ungefähr gleich der quantenmechanischen Energieunschärfe E ist: (1.5.37) δe E h t So können z.b. aus dem Nichts für kurze Zeiten t Teilchen der Gesamtenergie mc h t entstehen (virtuelle Teilchen). Mit einer entsprechend geringeren Wahrscheinlichkeit können auch Teilchen mit einer größeren Energie entstehen. Das Vakuum ist also kein strukturloses Gebilde, sondern von virtuellen Teilchen durchsetzt (Vakuumfluktuationen), die mit real existierenden Teilchen in Wechselwirkung treten. Die Einflüsse dieser Wechselwirkungen sind durchaus messbar und müssen berücksichtigt werden, wenn Energiewerte von quantenmechanischen Zuständen mit hoher Genauigkeit berechnet werden. Es sei noch bemerkt, dass die virtuellen Teilchen nicht wirklich existieren, sondern nur dem Versuch entspringen, sich gewisse Terme in den Gleichungen der Quantenfeldtheorie vorzustellen! 4
25 1 Materiewellen Bei der Entstehung virtueller Teilchen müssen gewisse Regeln (Erhaltungssätze) eingehalten werden. So können wegen der Ladungserhaltung z.b. keine isolierten geladenen Teilchen wie Elektronen oder Protonen entstehen. Geladene Teilchen entstehen nur mit dem entsprechenden Antiteilchen, das genau die negative Ladung des Teilchens trägt. So kann z.b. ein Proton- Antiproton-Paar für die Zeitdauer entstehen. t h δe = h mc 1 4 s Der Drehimpuls L eines Teilchens mit dem Impuls p und der Masse m bezüglich eines Punktes O ist definiert durch L = r p = m r v (1.5.38) m α p Für den Betrag des Drehimpulses erhält man L = L = mvr sinα (1.5.39) Der Drehimpuls ist deshalb eine wichtige Größe in der Physik, weil für ihn wie für den Impuls und die Energie ein Erhaltungssatz gilt. r α O Abb Drehimpulsdefinition Der Drehimpuls eines Teilchens, das mit der Geschwindigkeit v eine Kreisbahn mit Radius r beschreibt, ist wegen sinα = 1 ( v r) L = mvr = pr (1.5.4) Da es in der Quantenmechanik wegen der Unschärferelationen keine exakt definierte Teilchenbahn gibt, ist das Folgende nur eine Plausibilitätsbetrachtung. Ist ϕ die Änderung des Mittelpunktswinkels, dann gehört dazu die Bogenlänge O r v ϕ m x x = r ϕ auf der Kreisbahn. Aus (1.5.9) folgt dann Abb Kreisbewegung x p = ϕ r p = ϕ L h (1.5.41) oder ϕ L h (1.5.4) Die größtmögliche Winkelunschärfe auf der Kreisbahn ist ϕ = π, woraus die kleinstmögliche Drehimpulsunschärfe L min h = (1.5.43) π folgt. verwendet man deshalb als Drehimpulseinheit in der Quantenmechanik. Viele Elementarteilchen haben neben dem Bahndrehimpuls L = r p noch einen Eigendrehimpuls oder Spin bezüglich ihres Schwerpunktes (wie ein um seine Achse rotierender Ball). Die Spins der Elementarteilchen sind ganzzahlige Vielfache von. Ein Spin-1 -Teilchen (wie z.b. das Elektron) hat den Eigendrehimpuls. Es sei bemerkt, dass die exakte Behandlung des Drehimpulses in der Quantenmechanik eine komplizierte Sache ist, die unsere Möglichkeiten weit übersteigt. 5
26 Stationäre Zustände.1 Die Schrödingergleichung In Kapitel 1 haben wir die Bewegung von freien Teilchen behandelt. Auf ein freies Teilchen wirkt keine Kraft, d.h. seine potentielle Energie ist konstant; das freie Teilchen bewegt sich in einem konstanten Potential. Damit man auch Teilchen in einem nicht-konstanten Potential beschreiben kann, muss die schon in (1.3.1) und (1.3.) angekündigte Grundgleichung der Quantenmechanik gefunden werden. Für ein freies Teilchen muss nach (1.3.3) eine ebene Welle ψ(x,t) = A e i(kx ωt) (.1.1) eine Lösung der gesuchten Gleichung sein. Differenzieren von (.1.1) nach x und t liefert ψ(x,t) = iωae i(kx ωt) = iωψ(x,t) (.1.) ψ (x,t) = ikae i(kx ωt) = ikψ(x,t) (.1.3) ψ (x,t) = k Ae i(kx ωt) = k ψ(x,t) (.1.4) Mit der Planck-Relation folgt aus (.1.) oder nach Multiplikation mit i W = ω (.1.5) ψ(x,t) = i W ψ(x,t) (.1.6) i ψ(x,t) = W ψ(x,t) (.1.7) Die Gleichungen (.1.4), (.1.5) und (.1.7) gelten für ein freies Teilchen. Erwin Schrödinger ( , Nobelpreis 1933 gemeinsam mit Dirac) forderte, dass diese Gleichungen auch bei Anwesenheit eines beliebigen Potentials erfüllt sein sollen. Aus (.1.5) wird dann mit der potentiellen Energie V(x) ω = W = m v +V(x) = p m +V(x) = k +V(x) (.1.8) m (.1.8) ist die nichtrelativistische Dispersionsrelation bei Anwesenheit eines Potentials. Einsetzen von (.1.8) in (.1.7) liefert i ψ(x,t) = m k ψ(x,t)+v(x) ψ(x,t) (.1.9) Mit (.1.4) folgt schließlich die zeitabhängige, eindimensionale Schrödingergleichung (196) i ψ(x,t) = m ψ (x,t)+v(x) ψ(x,t) (.1.1) 6
27 Stationäre Zustände Mit (.1.1) haben wir eine Gleichung konstruiert, die für V(x) = die ebene Welle (.1.1) als Lösung besitzt. Da (.1.1) linear ist, ist auch jede Überlagerung ebener Wellen und somit jedes Wellenpaket ψ(x,t) = eine Lösung der Schrödingergleichung mit V(x) =. A(k)e i(kx ωt) dk (.1.11) Unser Weg von (.1.1) zu (.1.1) ist keinesfalls zwingend! Es können sogar unendlich viele lineare Differentialgleichungen aufgestellt werden, die (.1.1) als Lösung besitzen (siehe Aufgaben). Ihre Rechtfertigung erhält die Schrödingergleichung nur dadurch, dass sie im nichtrelativistischen Fall alle bekannten Versuchsergebnisse richtig beschreibt! Die Beschreibung zeitabhängiger quantenmechanischer Erscheinungen ist, außer beim freien Teilchen, recht kompliziert und wird meist numerisch in Angriff genommen. Wir wenden uns jetzt dem Studium der sogenannten stationären Zustände zu: Definition: Ein physikalischer Zustand, dessen Wellenfunktion nur über den Faktor e iωt von der Zeit abhängt, heisst stationärer Zustand. Für einen stationären Zustand gilt also ψ(x,t) = ϕ(x) e iωt (.1.1) mit einer nur vom Ort (und nicht von der Zeit) abhängigen Funktion ϕ(x). Wegen w(x,t) = ψ(x,t) = ϕ(x) e iωt = ϕ(x) (.1.13) ist die Wahrscheinlichkeitsdichte eines stationären Zustands von der Zeit unabhängig! Zur Ableitung einer Differentialgleichung für die zeitunabhängige Funktion ϕ(x) setzt man (.1.1) in (.1.1) ein: i ( iω)ϕ(x) e iωt = m ϕ (x) e iωt +V(x) ϕ(x) e iωt ωϕ(x) = m ϕ (x)+v(x) ϕ(x) (.1.14) MitderGesamtenergie W = ω desbetrachteten Zustandesundderortsabhängigen potentiellen Energie V(x) lautet die zeitunabhängige Schrödingergleichung m ϕ (x)+v(x) ϕ(x) = W ϕ(x) (.1.15) Die dreidimensionale Verallgemeinerung von (.1.15) lautet ( ) m ϕ x + ϕ y + ϕ z +V( r) ϕ( r) = W ϕ( r) (.1.16) Die Lösung von (.1.16) für eine konstante potentielle Energie V(x) = V lautet ϕ(x) = A e αx +B e αx mit α = 1 m(v W), (.1.17) wie man leicht durch Einsetzen nachweist. Für W < V ist α reell und ϕ(x) ist die Summe von zwei reellen Exponentialfunktionen. Dieser Fall ist in der klassischen Mechanik nicht möglich, weil die Gesamtenergie als Summe aus potentieller und kinetischer Energie mindestens so groß 7
28 Stationäre Zustände wie die potentielle Energie sein muss. Nach der Quantenmechanik kann sich das Teilchen mit einer gewissen Wahrscheinlichkeit also an Orten aufhalten, an denen es nach der klassischen Mechanik nie sein kann. Wir werden diesen Fall an konkreten Beispielen noch genau studieren. Für W > V ist die kinetische Energie des Teilchens positiv und es gilt Aus (.1.17) folgt W k = m v = W V (.1.18) α = 1 m(w V ) = i m v = i p = ik (.1.19) ϕ(x) = A e ikx +B e ikx mit k = p für W > V (.1.) (.1.) beschreibt die Überlagerung einer nach rechts laufenden mit einer nach links laufenden Welle, denn für stationäre Zustände gilt ψ(x,t) = ϕ(x) e iωt und damit ψ(x,t) = ϕ(x) e iωt = A e i(kx ωt) +B e i( kx ωt) (.1.1) Da in (.1.15) die zweite Ableitung von ϕ(x) nach x steht, muss ϕ(x) mindestens zweimal differenzierbar sein. Notwendig dafür ist folgende Stetigkeitsforderung: ϕ(x) und ϕ (x) sind stetig für alle x (.1.) Mit Hilfe dieser Stetigkeitsforderung (die auch an Unstetigkeitsstellen von V(x) gelten muss) und der Normierungsbedingung ϕ(x) dx = 1 (.1.3) werden die Konstanten in ϕ(x) berechnet. Die Konstanten A und B in (.1.17) und (.1.) sind i.a. komplex, d.h. es gilt A = a 1 +a i und B = b 1 +b i (.1.4) mit reellen Zahlen a 1, a, b 1 und b. Im Fall W > V erhält man aus (.1.) die Wahrscheinlichkeitsdichte (siehe Aufgaben) w(x) = A [1+ D +d 1 coskx+d sinkx ] mit = A [1+ D + D sin(kx+σ) ] (.1.5) D = B A = d 1 +d i und tanσ = d 1 d (.1.6) Für den Mittelwert von w(x) erhält man durch Integration über eine Wellenlänge w = k π π k w(x)dx = A (1+ D ) = A + B (.1.7) 8
29 Stationäre Zustände Zusammenfassung: Die zeitunabhängige Schrödingergleichung für ein Teilchen der Gesamtenergie W und der potentiellen Energie V(x) m ϕ (x)+v(x) ϕ(x) = W ϕ(x) hat für V(x) = V = konst. die Lösung W < V ϕ(x) = A e αx +B e αx mit α = 1 m(v W) W > V ϕ(x) = A e ikx +B e ikx mit k = 1 m(w V ) w(x) = A [1+ D + D sin(kx+σ) ] mit D = B A und tanσ = Re(D) Im(D) Die Konstanten in ϕ berechnet man nach folgenden Regeln: Auch an Unstetigkeitsstellen von V(x) müssen ϕ(x) und ϕ (x) stetig sein. Normierung von ϕ(x) mit ϕ(x) dx = 1. Potentialbarrieren In der klassischen Mechanik wird eine Potentialbarriere der Höhe V von einem Teilchen mit der Gesamtenergie W > V sicher überwunden. Ein Teilchen mit W < V kehrt am Ort x mit V(x ) = W seine Bewegungsrichtung um. Quantenmechanisch könnte man dasproblem Teilchen gegen Potentialbarriere folgendermaßen angehen: Man sucht eine Lösung der zeitabhängigen Schrödingergleichung (.1.1) mit dem zur Zeit Null V V W x Abb...1 Potentialbarriere x bekannten Wellenpaket ψ(x, ). Diese Methode ist, zumindest numerisch, immer durchführbar, aber recht aufwendig. An den wesentlichen Ergebnissen ändert sich nichts, wenn man ein Teilchen mit scharf definiertem Impuls verwendet, dessen Wellenfunktion durch ψ(x,t) = C e i(kx ωt) = C e ikx e iωt (..1) gegebenist( p =, x = ).Wegen (.1.1) handeltessichhierumeinenstationären Zustand mit ϕ(x) = C e ikx und das Problem wird durch die zeitunabhängige Schrödingergleichung (.1.15) beschrieben. (..1) kann auch als Wellenfunktion eines Stromes von vielen identischen Teilchen gleicher Geschwindigkeit betrachtet werden. Die Größe dp = ψ dx = w(x)dx (..) 9
30 Stationäre Zustände ist dann proportional zur mittleren Zahl dn der Teilchen im Intervall [x, x+ dx]: Da der Impuls p das gleiche Vorzeichen hat wie k, gilt: Im Folgenden betrachten wir Beispiele, in denen ein von links einfallender Teilchenstrom auf eine Potentialbarriere trifft. Für x < und für x > d sei die potentielle Energie konstant (siehe Abb...). Ist die Teilchenenergie W kleiner als die maximale potentielle Energie V, dann muss das Teilchen, klassisch gesehen, umkehren, d.h. es wird nie in den Bereich x > d vordringen. Die Lösung der Schrödingergleichung für unser Problem zeigt auch für den Bereich x > d eine von Null verschiedene Aufenthaltswahrscheinlichkeit (Tunneleffekt). dn = konst. w(x) dx (..3) Teilchenstrom nach rechts : ϕ(x) = A e ikx Teilchenstrom nach links : ϕ(x) = B e ikx (..4) w max w L W V W 1 W V 1 V w L w w min Abb... Potentialbarriere Die Lösung der Schrödingergleichung in den Bereichen mit konstanter potentieller Energie ist für W > max(v 1,V ) nach (.1.) d d w T x x { A e ik 1 ϕ(x) = x +B e ik 1x für x < Ee ik x für x > d (..5) mit k 1 = p 1 = 1 m(w V 1 ) (..6) k = p = 1 m(w V ) (..7) Dem einfallenden Strahl entspricht die Wellenfunktion A e ik1x, der Summand B e ik1x muss als Wellenfunktion eines reflektierten Strahls interpretiert werden. Im durchgehenden Strahl, also für x > d, gibt es keine reflektierten Teilchen (kein Summand mit e ikx ). Nach (.1.5) gilt für die Wahrscheinlichkeitsdichte { A w(x) = + B + A B sin(k 1 x+σ) für x < E für x > d (..8) Der Mittelwert der Wahrscheinlichkeitsdichte im Bereich links der Barriere ist nach (.1.7) w L = A + B (..9) 3
31 Stationäre Zustände Dabei ist A die Wahrscheinlichkeitsdichte für den einfallenden und B für den reflektierten Teil des Teilchenstroms. In einem Zeitintervall t fallen N Teilchen ein, N R Teilchen werden reflektiert und N T Teilchen durchdringen die Barriere. Die Teilchenzahlen sind proportional zu den Wahrscheinlichkeiten, die Teilchen in Ortsintervallen der Breiten v 1 t bzw. v t zu finden: N R N v 1 t Abb...3 Teilchenzahlen N = ε A v 1 t = ε A v 1 N R = ε B v 1 t = ε B v 1 N T = ε E v t = ε E v N T v t x (..1) Der Reflexionskoeffizient R und der Transmissionsskoeffizient T sind die Wahrscheinlichkeiten für Reflexion bzw. für das Durchdringen der Barriere: R = N R N = B A, T = N T N = E v A v 1 (..11) Wir betrachten nur Vorgänge, bei denen keine Teilchen erzeugt oder vernichtet werden, d.h. es gilt N R +N T = N bzw. R+T = 1 (..1) Da w(x) nach dem Durchdringen einer Potentialbarriere konstant ist, beginnt man die numerische Lösung der Schrödingergleichung für Probleme dieser Art im Bereich nach der Barriere und rechnet dann rückwärts. Da im Bereich nach der Barriere ϕ(x) = E e ik x gilt und ϕ (x) = E e ik (x x ) diegleiche Wahrscheinlichkeitsdichte wieϕergibt, kannman diekonstante x beliebig wählen. Mit einem beliebigen x nach der Barriere lauten dann die Anfangsbedingungen für die numerische Lösung ϕ(x ) = E, ϕ (x ) = ike (..13) Aus den numerisch gewonnenen Funktionswerten von w im Bereich vor der Barriere berechnet man mit einer geeigneten Interpolation (Parabel durch drei Funktionswerte) das Maximum und das Minimum von w(x). Dazu wählt man aus einer möglichst feinen Wertetabelle den maximalen Wert und seine beiden Nachbarn (siehe Abb...4). Durch Einsetzen der drei Wertepaare in die Parabelgleichung w w 1 w w max w 3 x 1 x x 3 Abb...4 Maximumsberechnung x g(x) = ax +bx+c (..14) erhält man drei Gleichungen zur Berechnung der Koeffizienten a, b und c. Der Scheitelwert der so erhaltenen Parabel ist eine gute Näherung für das wahre Maximum von w(x). Analog berechnet man das Minimum und erhält so (siehe Abb...) w L = 1 (w min +w max ) (..15) 31
32 Stationäre Zustände Da bei der numerischen Rechnung E bekannt ist (Anfangswerte!), kann man jetzt den Transmissionskoeffizienten T berechnen. Aus folgt Auflösen nach A und Einsetzen in (..11) ergibt T = N +N R = N N T (..16) w L v 1 = A v 1 E v (..17) E v w L v 1 + E v = E k w L k 1 + E k (..18) Da in den messbaren Wahrscheinlichkeiten T und R nur Verhältnisse der Beträge der Konstanten A, B und E vorkommen, kann eine der Konstanten noch frei gewählt werden. Zweckmäßigerweise wählt man E = 1 in den Anfangsbedingungen und erhält dann mit (..15) T = 4k (w min +w max ) k 1 +k (..19) Als erstes Beispiel betrachten wir eine Potentialschwelle { für x < V(x) = (..) V für x mit einer Teilchenenergie W < V. Die Lösungder Schrödingergleichung ist (L steht für links, d.h. x < und R für rechts, d.h. x >, wir wählen A = 1) wegen (.1.17) und (.1.): V V Abb...5 Potentialschwelle x ϕ L (x) = e ikx +B e ikx (..1) ϕ R (x) = C e αx +D e αx (..) mit k = 1 1 mw und α = m(v W) (..3) Wegen der Normierbarkeit muss D = gewählt werden. Die Stetigkeitsforderungen bei x = lauten Die Lösung dieses Gleichungssystems ist mit ϕ L () = ϕ R () = 1+B = C (..4) ϕ R() = ϕ R() = ik ikb = αc (..5) B = 1 β βi 1+β und C = βi 1+β (..6) β = α k = V W 1 (..7) Für die Wahrscheinlichkeitsdichte erhält man mit (..8) 1+ B + B sin(kx+σ) für x < w(x) = C e αx für x > (..8) 3
33 Stationäre Zustände Abb...6 zeigt w(x) für ein Elektron mit V = 1eVundW =,5eV. Beachtenswert ist das Eindringen des Elektrons in den klassisch verbotenen Bereich x >. Für x < liegt eine typische stehende Welle vor, die durch Überlagerung der Wellenfunktionen der einfallenden und reflektierten Teilchen entsteht. w(x) Å 1Å 1Å Abb...6 w(x) bei der Potentialschwelle Als nächstes Beispiel betrachten wir eine Rechtecksbarriere der Breite d: V { Be ikx V V für x d V(x) = (..9) e sonst ikx mit W < V. Aus (.1.17) und (.1.) folgt für die Wellenfunktion (A = 1 wurde gewählt) e ikx +B e ikx für x < d ϕ(x) = Ce αx +De αx für x d Ee ikx für x > d und aus (.1.5) für die Wahrscheinlichkeitsdichte 1+ B + B sin(kx+σ) für x < w(x) = E für x > d Ee ikx d x Abb...7 Rechtecksbarriere (..3) (..31) Mit einem Computeralgebrasystem berechnet man aus den Stetigkeitsforderungen für ϕ und ϕ an den Stellen x = und x = d die Konstanten B, C, D und E und erhält dann aus (..11) mit A = 1 und v 1 = v für den Transmissionskoeffizienten T := E = γ e αd +e αd +γ mit γ = 16 W ) (1 WV V (..3) Å x 1Å d Abb...8 w(x) bei der Rechtecksbarriere Abb...9 Transmissionskoeffizient Abb...8 zeigt w(x) für ein Elektron mit V = 1eV, W =,9eV und d = 1Å. In Abb...9 ist die Funktion T(d) dargestellt, die wegen der Exponentialfunktion im Nenner mit wachsendem d sehr schnell gegen Null geht. 33
34 Stationäre Zustände Eine schöne Bestätigung des Tunneleffekts war die theoretische Erklärung des radioaktiven α-zerfalls durch Gamow (siehe Abb...1). Das Potential des α-teilchens ( 4 He-Kern) ist eine Überlagerung des Coulombpotentials und des Potentials der starken Wechselwirkung..3 Gebundene Zustände Abb...1 α-zerfall Wir betrachten ein Teilchen der Masse m im Potential { für x a V(x) = (.3.1) + sonst V n = 3 Die Schrödingergleichung m ϕ (x)+v(x)ϕ(x) = W ϕ(x) (.3.) hat in den Bereichen x < und x > a für ein endliches W die Lösung ϕ(x) =. n = n = 1 a x Abb..3.1 Unendlich tiefer Potentialtopf Im Intervall x a lautet die Lösung nach (.1.) Die Stetigkeit von ϕ(x) bei x = ergibt d.h. ϕ(x) = A Aus der Stetigkeit von ϕ(x) bei x = a folgt d.h. und ϕ(x) = Ae ikx +Be ikx (.3.3) ϕ() = A+B = = B = A (.3.4) ( e ikx e ikx) = A(coskx+isinkx coskx+isinkx) (.3.5) ϕ(x) = Ai sinkx (.3.6) sinka = = k = n π a ϕ n (x) = w n (x) = ϕ n (x) = { Ai sin ( nπ a x) für x a sonst Die Normierung von ϕ dient zur Berechnung von A: mit n N (.3.7) { 4A sin ( nπ a x) für x a sonst a (.3.8) (.3.9) w n (x) dx = 4A sin ( nπ ) a x dx = [ x = a ( nπ )] a 4nπ sin a x = 4A a = 1 (.3.1) 34
35 Damit gilt A = 1 a Stationäre Zustände und die normierte Wahrscheinlichkeitsdichte lautet w n (x) = { a sin( nπ a x) für x a sonst (.3.11) Die wesentliche Erkenntnis aus unseren Rechnungen ist, dass die Schrödingergleichung für das eingesperrte Teilchen nur für ganz bestimmte Teilchenenergien W n eine Lösung hat. Aus (.3.7) folgt W n = p n m = kn m = π ma n = h 8ma n (.3.1) Für n = ist w(x) =, d.h. es ist überhaupt kein Teilchen vorhanden. Die niedrigste Teilchenenergie ist also W 1, d.h. es gibt kein eingesperrtes, ruhendes Teilchen!! Allgemein gilt: V Kontinuum V W 3 W 4 metastabil Kontinuum W W 1 x diskret x Abb..3. Energiespektrum Abb..3.3 Metastabile diskrete Zustände neben einem Kontinuum am Beispiel eines α-teilchens im Potential des Restkerns Zu jedem streng gebundenen Zustand (Teilchen in einer Potentialmulde mit unendlich breiten Wänden) gibt es nur diskrete Energiewerte W n mit ganzen Quantenzahlen n. Ausserhalb des Bereichs der streng gebundenen Zustände sind alle Energiewerte möglich (freies Teilchen, Kontinuum, siehe Abb..3.). Aus einem Potentialtopf mit endlich breiten Wänden verschwindet das Teilchen nach einer gewissen Zeit (Tunneleffekt). Es existieren quasistationäre (metastabile) Zustände neben einem Kontinuum. In einem Leiter oder Halbleiter bewegen sich die Elektronen im periodischen Potential der Atomrümpfe. Dadurch verbreitern sich die diskreten Energiewerte zu Energiebändern. Im Valenzband (unterstes Band in Abb..3.4) sind die Elektronen an die Atomrümpfe gebunden, im Leitungsband sind sie, innerhalb des Metalls, frei beweglich. Die Zahl N der Elektronen im Leitungsband ist eine Funktion der Temperatur: V Kontinuum Austrittsarbeit Leitungsband Abb..3.4 Energiezustände in einem Leiter x N(T) = A e B T mit Konstanten A und B. (.3.13) 35
36 Stationäre Zustände EW = 1,95 ev EW = 1,96 ev 5 5 EW = 1,951 ev EW = 1,9519 ev 1 EW = 1,95 ev 1 EW = 1, ev Abb..3.5 Schrittweises Annähern an die richtige Wellenfunktion für V(x) = x Zur numerischen Lösung bringt man die Schrödingergleichung d ψ(x) dx in eine einheitenfreie Form. Für ein Elektron erhält man mit = 6,581 1 MeVs, m =, MeV c X = xå, ψ(x) = ϕ(x) die einheitenfreie Gleichung (Aufgabe!) = m [U(X) W] ψ(x) (.3.14), c = m s 1 Å, U(X) = V(x)eV, W = EW ev d ϕ(x) dx = B [V(x) EW] ϕ(x) mit B =, (.3.15) Für einen zu x = achsensymmetrischen Potentialtopf muss auch die Wahrscheinlichkeitsdichte w(x) zu x = achsensymmetrisch sein. Die Wellenfunktion ϕ(x) ist dann entweder zu x = achsensymmetrisch (gerade Funktion) oder zum Ursprung punktsymmetrisch (ungerade Funktion). Als Anfangsbedingung wählt man für gerade Funktionen ϕ() = 1 und ϕ () =, für ungerade Funktionen ϕ() = und ϕ () = 1 (ϕ ist damit noch nicht normiert). Um die Normierbarkeit von ϕ zu gewährleisten, muss lim ϕ(x) = gelten. Durch Probieren findet x man die richtigen Energiewerte EW (Eigenwerte), für die ϕ im Unendlichen verschwindet. Dieses Verfahren ist aber recht zeitaufwendig, da für jeden Versuch die Schrödingergleichung numerisch gelöst werden muss (siehe Abb..3.5). Schneller geht es mit dem Newtonverfahren: Für ein genügend großes x berechnet man g(ew) = ϕ(x ) und sucht die Lösung von g(ew) =. ϕ x g(ew) Abb..3.6 Newtonverfahren zur EW- Bestimmung x 36
37 .4 Der Franck-Hertz-Versuch Stationäre Zustände Franck und Hertz führten 1914 folgenden Versuch durch (siehe Abb..4.1): Eine evakuierte Elektronenröhre mit einem Quechsilbertropfen im Inneren wird in einem Ofen erhitzt, um eine Hg-Atmosphäre zu schaffen. Die Spannung U wird von Null bis ca. 3V hochgeregelt und dabei der Strom I(U) mit einem Messverstärker gemessen. Der Verlauf der Funktion I(U) ist in Abb..4. dargestellt. K 6,3V Hg-Dampf U R = 1kΩ 3V + Abb..4.1 Franck-Hertz-Versuch G A + U B I Die Maxima von I misst man bei Der Mittelwert von U ist U in V 6,8 11,5 16, 1,6 6,5 U in V 4,7 4,7 5,3 4,9 U = 4,9V (.4.1) Das Versuchsergebnis kann wie folgt erklärt werden: Die Hg-Atome befinden sich im Grundzustand mit der Energie W, ihr erster angeregter Zustand hat die Energie W 1 = W +4,9eV. Elektronen mit einer kinetischen Energie W < 4,9eV stoßen nur elastisch mit den Hg-Atomen zusammen und verlieren wegen m e m Hg fast keine Energie. Bei U = 4,9V reicht die ki- netische Energie der Elektronen aus, um die Hg-Atome in den ersten angeregten Zustand zu versetzen. Dabei verlieren die Elektronen ihre gesamte kinetische Energie und können nicht mehr gegen die Bremsspannung U B zwischen Gitter und Anode anlaufen, d.h. I wird kleiner. Wird U weiter vergrößert, dann wandert die Zone der unelastischen Stöße vom Gitter weg nach links. Zwischen dieser Zone und dem Gitter nimmt die kinetische Energie der Elektronen wieder zu und der ganze Vorgang wiederholt sich. Der offensichtlich falsche Spannungswert des ersten Maximums ergibt sich aus einer Verschiebung der ganzen UI-Kurve. Gemessen wird nämlich die Spannung U zwischen Punkten im Inneren I na 1 U V 3 Abb..4. I(U) beim Franck-Hertz-Versuch G U = 4,9V G 4,9V < U < 9,8V G U = 9,8V Abb..4.3 Zonen der unelastischen Stöße von Kathode und Gitter. Das Feld zwischen Kathode und Gitter hängt aber von der Spannung U zwischen den Oberflächen der Leiter ab. Da Kathode und Gitter i.a. aus verschiedenen 37
38 Stationäre Zustände Materialien bestehen (warum?), unterscheidet sich die tatsächliche Beschleunigungsspannung U um die Differenz der Austrittsarbeiten der verwendeten Materialien von der gemessenen Spannung U : und damit U +A 1 = U +A (.4.) U = U +A 1 A (.4.3) Die genaue Form der UI-Kurve ergibt sich aus der Röhrenkennline ohne Hg-Dampf (siehe Abb..4.5) und der Maxwellschen Geschwindigkeitsverteilung der aus der Kathode austretenden Glühelektronen. A 1 U U A Abb..4.4 Die wahre Beschleunigungsspannung U I I ohne Hg-Dampf U Abb..4.5 Röhrenkennlinie 38
39 3 Wechselwirkung von elektromagnetischer Strahlung mit Materie 3.1 Der Übergang zwischen stationären Zuständen - Spektrallinien Wechselt ein Teilchen von einem stationären Zustand in einen anderen stationären Zustand ψ m = ϕ m (x) e iωmt mit W m = ω m = h f m (3.1.1) ψ n = ϕ n (x) e iωnt mit W n = ω n = h f n, (3.1.) dann geschieht dieser Wechsel nicht plötzlich, sondern für kurze Zeit sind beide Zustände gleichzeitig vorhanden. Für den Überlagerungszustand gilt ψ = ψ m +ψ n = ϕ m (x) e iωmt +ϕ n (x) e iωnt (3.1.3) und die Wahrscheinlichkeitsdichte des Überlagerungszustandes ist damit w(x,t) = ψ = ψ ψ = = ( ϕ m e iωmt +ϕ n e iωnt) (ϕ m eiωmt +ϕ n eiωnt) = = ϕ m + ϕ n +ϕ m ϕ n e i(ωm ωn)t +ϕ mϕ n e i(ωm ωn)t (3.1.4) Die Wahrscheinlichkeitsdichte oszilliert also im Übergangszustand mit der Frequenz f mn = ω mn π = 1 π ω m ω n = f m f n (3.1.5) Bei einem geladenen Teilchen ist die Ladungsdichte ρ zur Wahrscheinlichkeitsdichte w proportional. Beim Übergang ψ m ψ n mit W m > W n (f m > f n ) schwingt also die Ladungsverteilung mit der Frequenz f mn, d.h. es wirdeine elektromagnetische Welle der Frequenz f mn ausgestrahlt. Die Gesamtenergie der bei einem Übergang ausgestrahlten Welle ist nach dem Energiesatz W mn = W m W n = h(f m f n ) = h f mn (3.1.6) Fällt umgekehrt eine elektromagnetische Welle der Frequenz f auf ein geladenes Teilchen im Zustand ψ n (z.b. auf ein Elektron in einem Atom) und ist f gleich einer der Resonanzfrequenzen f mn, dann wird der Mischzustand ψ m + ψ n angeregt und das Teilchen geht mit der Übergangswahrscheinlichkeit P mn in den Zustand ψ m über. Dabei wird der Welle die Energie W mn = h f mn entzogen. Die Berechnung von P mn erfolgt mit der quantenmechanischen Störungsrechnung, würde hier aber zu weit führen. W m f mn W n Abb Übergang mit Strahlung 39
40 3 Wechselwirkung von elektrom. Strahlung mit Materie Es folgt eine Zusammenfassung der bisherigen Ergebnisse: Ein Atom (oder ein anderer quantenmechanischer Zustand) mit den Energieeigenwerten W ν, ν N, kann nur Licht absorbieren oder aussenden, dessen Frequenz gleich einer der Resonanzfrequenzen ist. f mn = 1 h (W m W n ) Ein Atom (oder ein anderer quantenmechanischer Zustand) kann aus einem elektromagnetischen Wellenfeld der Frequenz f nur den Energiebetrag aufnehmen. W = hf Die Energie eines von Atomen ausgesandten elektromagnetischen Wellenfeldes der Frequenz f ist ein ganzzahliges Vielfaches von hf = ω (3.1.7) (3.1.8) (3.1.9) Mit der Wellenlänge der ausgesandten bzw. absorbierten Strahlung gilt λ mn = c f mn (3.1.1) W m W n = h f mn = hc λ mn (3.1.11) (Bohr sche Frequenzbedingung) Die Wellenlängen λ mn können mit Prismen- oder Gitterspektrometern sehr genau gemessen werden. Die optische Untersuchung von Spektren ist also mit Hilfe von (3.1.11) der experimentelle Weg zur Bestimmung der Energiedifferenzen W m W n. Tritt Licht, das von leuchtenden Gasen (also von wechselwirkungsfreien Atomen) ausgesandt wird, durch ein Gitter, dann beobachtet man einzelne, scharf begrenzte Spektrallinien. Jeder Spektrallinie ist eindeutig eine Wellenlänge zugeordnet. Wegen (3.1.11) sind somit die Linienspektren eine direkte experimentelle Bestätigung für die Existenz diskreter Energiewerte von Atomen. Wir betrachten jetzt den Mechanismus der Lichtentstehung etwas genauer: Einem Atom im Grundzustand (W ) wird die Energie W m zugeführt, das Atom hat dann die Energie W m. Die Energiezufuhr geschieht durch Stöße mit anderen Atomen (Wärmebewegung, Glühlampe), durch Stöße mit Elektronen (Leuchtstoffröhre, Bildschirm) oder durch Licht (Resonanzfluoreszenz). Die angeregten Zustände eines Atoms haben meistens eine sehr kurze Lebensdauer τ in der Größenordnung von 1 8 s. Nach dieser kurzen Zeit gibt das Atom seine Anregungsenergie in einem ein- oder mehrstufigen Prozess in Form von elektromagnetischer Strahlung wieder ab. 4
41 3 Wechselwirkung von elektrom. Strahlung mit Materie Einen Überblick über alle möglichen Frequenzen, die ein quantenmechanisches System ausstrahlen oder absorbieren kann, erhält man mit einem sogenannten Termschema (siehe Abb. 3.1.). Mit Hilfe der Spektralanalyse können die Bestandteile sehr kleiner Proben eines Stoffes ermittelt werden. In einer elektrischen Funkenstrecke z.b. kann die Probe in ein leuchtendes Gas verwandelt und sein Spektrum untersucht werden. f 1 f 1 Abb.3.1. Termschema W 3 W W 1 W Ein Versuch zur Resonanzabsorption: Das Licht einer Natriumdampflampe wird von einem Spektrometer in seine Bestandteile zerlegt. Man beobachtet eine intensive gelbe Linie bei λ = 589nm. Anschließend ersetzt man die Natriumdampflampe durch eine Kohlenbogenlampe, die weißes Licht ausstrahlt. Bringt man Natriumdampf in den Strahlengang, dann fehlt im kontinuierlichen Spektrum der Bogenlampe genau die gelbe Natriumlinie bei λ = 589nm, Lampe Na Spalt Linse Gitter Schirm Abb Spektrometer Statt des Gitters kann auch ein Geradsichtprisma verwendet werden d.h. an dieser Stelle ist eine schwarze Linie zu erkennen (Umkehrung der Natriumlinie). Das Licht mit λ = 589nm regt die Na-Atome an, die es dann isotrop wieder abstrahlen, d.h. am Ort des Spalts ist diese Wellenlänge nur mit geringer Intensität vertreten (Resonanzstreuung). Das ist ein direkter Beweis für die Resonanzabsorption. Als Absorptionsspektrum bezeichnet man ein Spektrum weißen Lichtes mit schwarzen Absorptinslinien. Die Absoptionslinien im Sonnenspektrum werden nach ihrem Entdecker Fraunhoferlinien genannt (J. Fraunhofer, 1814, Straubing). Die Fraunhoferlinien geben Aufschluss über die Elemente, die in der Sonnenatmosphäre vorkommen. Als weiteres Beispiel unserer Theorie der Lichtentstehung betrachten wir die prinzipielle Funktionsweise eines Lasers (Light Amplifier by Stimulated Emission of Radiation): Ein Atom befinde sich im Energiezustand W n. Die Wahrscheinlichkeit für den spontanen ÜbergangindenGrundzustandistP n.wirddasatomimzustandw n voneinerelektromagnetischen Welle der Frequenz f n = Wn W h getroffen, dann ist die Übergangswahrscheinlichkeit S n in den Grundzustand viel größer als P n (stimulierte Emission). Man verwendet eine Atomsorte, für die P mn P n (3.1.1) ist und die eine nicht zu kleine Wahrscheinlichkeit P mn für den Übergang von W m W n haben. Werden die Atome mit Licht der Frequenz W m W n f n f m = W m W h (3.1.13) bestrahlt, dann gehen die Atome zunächst in den Zustand W m über. Wegen (3.1.1) gibt es mit der Zeit W Abb Prinzip des Lasers immer mehr Atome im Zustand W n (optisches Pumpen). Jetzt werden die angeregten Atome 41
42 mit Licht der Frequenz 3 Wechselwirkung von elektrom. Strahlung mit Materie f n = W n W h (3.1.14) bestrahlt. Schlagartig nimmt die Wahrscheinlichkeit für den Übergang nach W zu (aus P n wird S n )undalleatomestrahlenfastgleichzeitig einewellederfrequenzf n ab(zündendeslasers). Wir betrachten den Zündvorgang des Lasers etwas genauer: Die einfallende Welle trifft zur Zeit t 1 auf das Atom A 1 und zur Zeit t = t 1 + x c (3.1.15) x A 1 A t 1 1 t Abb Zünden des Lasers auf das Atom A. Die von den Atomen ausgestrahlten Wellen stehen in einer festen Phasenbeziehung zur einfallenden Welle und haben als bevorzugte Richtung die Richtung der auslösenden Welle. Die von A 1 ausgestrahlte Welle 1 trifft gleichzeitig mit der auslösenden Welle auf A, d.h. 1 und sind gleichphasig. Der Laser sendet monochromatisches, über große Raumbereiche gleichphasiges (kohärentes) Licht aus. Die Kohärenz des Laserlichts ist von viel größerer Bedeutung als die hohen Energiedichten, die ein gepulster Laser erzeugen kann. 3. Die Lichtquantenhypothese Die Aussagen (3.1.7), (3.1.8) und (3.1.9) können auch durch folgende Hypothese gedeutet werden: Eine elektromagnetische Welle der Frequenz f ist in Portionen der Energie W = h f, (3..1) die sogenannten Lichtteilchen, Lichtquanten oder Photonen, aufgeteilt. Die dynamische Masse eines Photons wäre dann sein Impuls Für elektromagnetische Wellen gilt woraus µ = W c = hf c, (3..) p = µc = W c = hf c. (3..3) c = f λ oder ω = c k (3..4) p = hf c = h λ = π = k (3..5) λ folgt. Für Photonen gelten also die Planck-Relation und die de Broglie-Relation genauso wie für Materieteilchen. m µ = = m = µ 1 β = µ 1 c 1 β c = (3..6) d.h. Photonen haben die Masse m = (3..7) 4
43 3 Wechselwirkung von elektrom. Strahlung mit Materie Aus (3..4) folgt für die Gruppengeschwindigkeit der Photonen v g = dω dk = c (3..8) Licht der Frequenz f besteht aus kleinen Teilchen der Energie W = hf mit dem Impuls p = hf c. (3..9) (Naives Photonenbild) In Materie ist die Lichtgeschwindigkeit kleiner als c und daher können in Materie nach dem naiven Photonenbild überhauptkeine Photonen existieren, da wegen m = auch W = und damit f = gelten würde. Das naive Photonenbild ist also sicher noch keine vollständige physikalische Theorie. 3.3 Der Compton-Effekt 1919 bis 193 untersuchte A.H. Compton die Streuung von Röntgenstrahlung der Frequenz f an freien Elektronen. Als freie Elektronen verwendete er sehr lose an Atome gebundene Elektronen mit einer Ionisierungsenergie A, die sehr klein gegen die Energie W γ der einfallenden Photonen war. Compton fand heraus, dass die Frequenz f der gestreuten Photonen vom Streuwinkel ϕ abhängt. Um eine Formel für die Wellenlänge der gestreuten γ-quanten zu erhalten, benutzen wir das naive Photonenbild, d.h. wir betrachten die Photonen als kleine Teilchen mit der Energie W = hf und dem Impuls p = hf c. Mit der kinetischen Energie W e und dem Impuls p e des Elektrons nach dem Stoß gilt hf ϕ p γ = hf c vorher v = p γ = hf c ε ϕ p e Abb Compton-Streuung p e hf Energiesatz: hf = hf +W e = hf hf = W e (3.3.1) Impulssatz: p γ = p γ + p e = p γ p γ = p e (3.3.) Quadrieren von (3.3.1) und (3.3.) ergibt mit p γ p γ = p γ p γ cosϕ h f +h f h f f cosϕ = p e c (3.3.3) h f +h f h f f = We (3.3.4) (3.3.3) (3.3.4): h f f (1 cosϕ) = p ec We (3.3.5) Mit der Energie-Impuls-Relation folgt p ec = W W = (W W )(W +W ) = W e (W +W e ) (3.3.6) 43
44 Einsetzen von (3.3.6) in (3.3.5): 3 Wechselwirkung von elektrom. Strahlung mit Materie h f f (1 cosϕ) = W W e = W h(f f ) (3.3.7) hf f (1 cosϕ) = W (f f ) (3.3.8) f [hf (1 cosϕ)+w ] = W f (3.3.9) 1 f = hf (1 cosϕ)+w W f λ = c f = hc (1 cosϕ)+ c W f (3.3.1) (3.3.11) λ = hc W (1 cosϕ)+λ (3.3.1) Die Differenz der Wellenlängen von Streustrahlung und einfallender Strahlung ist somit λ = λ λ = h m e c (1 cosϕ) = λ C (1 cosϕ) (3.3.13) mit der Compton-Wellenlänge des Elektrons Ein Photon mit der Wellenlänge λ C hat die Energie Merkregel: λ C = h m e c =, m (3.3.14) W C = hf C = hc λ C = m e c (3.3.15) Die Compton-Wellenlänge eines Teilchens ist gleich der Wellenlänge eines Photons, dessen Energie gleich der Ruhenergie des Teilchens ist. (3.3.16) (3.3.13) stimmt ausgezeichnet mit der Erfahrung überein, d.h. unser Ausgangspunkt der Rechnung, das naive Photonenbild, führt auf die richtige Funktion f (ϕ). Mit der Kenntnis von f bzw. λ in Abhängigkeit von ϕ ist aber der Versuchsausgang noch nicht vollständig beschrieben, da noch nicht bekannt ist, wie viele Photonen in die Richtung zwischen ϕ und ϕ+dϕ gestreut werden. Unser naives Photonenbild gibt uns keine Handhabe zur Berechnung der Intensitätsverteilung I(ϕ) der Streustrahlung. Im Jahre 198 gelang es aber Klein und Nishina, I(ϕ) mit Hilfe der Dirac-Gleichung, einer relativistischen Verallgemeinerung der Schrödingergleichung, zu berechnen. Klein und Nishina verwendeten als Ausgangspunkt ihrer sehr langwierigen Rechnung die quantenmechanische Theorie des Elektrons (Dirac-Gleichung) und die klassische Theorie des elektromagnetischen Feldes (Maxwell); diese Kombination heißt semiklassische Theorie: Schrödinger (bzw. Dirac) + Maxwell = semiklassische Theorie (3.3.13) kann auch mit der semiklassischen Theorie hergeleitet werden, doch übersteigt das den uns gesteckten Rahmen (siehe z.b. Döring, Atomphysik und Quantenmechanik I, S.3-36). 44
45 3 Wechselwirkung von elektrom. Strahlung mit Materie dp = w(ϕ) dϕ sei die Wahrscheinlichkeit, dass ein mit dem Elektron wechselwirkendes Photon in den Winkelbereich zwischen ϕ und ϕ+dϕ gestreut wird. Abb.3.3. zeigt die von Klein und Nishina berechnete Funktion w(ϕ) als Polardiagramm, wobei die Richtung der waagrechten Achse ϕ = entspricht.,4,4,4 Abb.3.3. w(ϕ) Für die Rückstoßenergie des Elektrons gilt nach (3.3.1) W e = hc λ hc ( ) 1 λ = hc λ 1 λ+ λ (3.3.17) Mit (3.3.13) erhält man die Elektronenenergie in Abhängigkeit vom Streuwinkel ϕ des Photons: ( ) 1 W e = hc λ 1 (3.3.18) λ+λ C (1 cosϕ) W e ist maximal, wenn der zweite Bruch in (3.3.18) minimal ist, d.h. für cosϕ = 1: ( ) 1 W e,max = hc λ 1 λ+λ C (3.3.19) Um die Richtung zu bestimmen (ε in Abb.3.3.1), in die die Elektronen davonfliegen, setzen wir den Impulssatz vektoriell an: hf hf c = c cosϕ + p e cosε (3.3.) hf c sinϕ p e sinε p e cosε = hf c hf c cos ϕ (3.3.1) p e sinε = hf sin ϕ c (3.3.) tanε = f sinϕ f f cosϕ (3.3.3) Mit folgt aus (3.3.3) f = c λ = c λ+λ C (1 cosϕ) (3.3.4) tanε = sinϕ f f cosϕ = sinϕ f [λ+λ C (1 cosϕ)] c cosϕ = sinϕ 1 = ) = (1 cosϕ) (1+ λ C λ 1 cos ϕ sinϕ (1+ λ C λ ) (3.3.5) 45
46 3 Wechselwirkung von elektrom. Strahlung mit Materie Mit der trigonometrischen Umformung folgt aus (3.3.5) tan x 1 cosx = 1+cosx = 1 cosx sinx tanε = 1 (1+ λ C λ ) tan ϕ (3.3.6) (3.3.7) Abb zeigt den prinzipiellen Versuchsaufbau und die gemessene Intensität der Streustrahlung für einen festen Streuwinkel ϕ in Abhängigkeit von der Frequenz. Neben der Frequenz f nach der Compton-Formel findet man auch gestreute Photonen mit der Frequenz f der einfallenden Strahlung. Für diese Photonen diente nicht ein einzelnes Elektron, sondern ein vollständiges Atom (bei Gasen) oder sogar der ganze Festkörper als Streupartner. Die Rechnung verläuft in diesem Fall genauso wie bei der Streuung an einem Elektron, im Ergebnis (3.3.13) ist aber die Masse des jeweiligen StreupartnersindieComptonwellenlängeλ C einzusetzen. Da eine Atommasse oder gar die Masse des ganzen Körpers um einige Zehnerpotenzen größer ist als die Elektronenmasse, ist λ C und somit auch λ um diesen Faktor kleiner als die entsprechende Größe bei der Streung am Elektron. Die Frequenz des gestreuten Photons ist also fast gleich f. Die Wahrscheinlichkeit dafür, welcher Kanal der Wechselwirkung vom Photon gewählt wird, hängt davon ab, wie stark das Elektron an das Restatom gebunden ist. Bei Atomen niedriger Ordnungszahl ist die I I f f f f f f ϕ Blende Zähler mit Energiemessung hohe Ordnungszahl niedrige Ordnungszahl Abb Experimentelle Untersuchung der Compton-Streuung Bindung der Elektronen schwächer als bei Atomen hoher Ordnungszahl und damit die Wahrscheinlichkeit für die Streuung am einzelnen Elektron höher. Die Streuung am ganzen Atom oder am Festkörper nennt man auch elastische Streuung, weil sich die Frequenz und damit die Energie des Photons fast nicht ändert. Neben der Compton- Streuung und der elastischen Streuung kann das einfallende Photon auch vom Atom absorbiert werden und seine ganze Energie abgeben (Fotoeffekt, siehe nächstes Kapitel). Bei genügend hoher Energie des Gammaquants können im Feld des Kerns auch neue Teilchen erzeugt werden (Paarerzeugung). Überblick über die wichtigsten Wechselwirkungen von Photonen mit Atomen: f f elastische Streuung: Rückstoßatom und gestreutes Quant Gammaquant auf Atom Compton-Streuung Rückstoßelektron und gestreutes Quant Fotoeffekt: Rückstoßatom und Elektron Paarerzeugung: Rückstoßatom und neue Teilchen 46
47 3.4 Der Fotoeffekt 3 Wechselwirkung von elektrom. Strahlung mit Materie W W Kontinuum W Kontinuum Kontinuum W k W k A hf A hf hf Leitungsband W Leitungsband A Abb Innerer Fotoeffekt Anheben von Elektronen aus dem Valenzband ins Leitungsband. Der elektrische Widerstand sinkt also bei Lichteinfall (Fotowiderstand). Abb.3.4. Äußerer Fotoeffekt Anheben von Elektronen aus dem Leitungsband ins Kontinuum (Ablösen von Elektronen aus dem Metall). A heißt Austrittsarbeit oder Ablösearbeit. Abb Fotoionisation Ablösung eines Elektrons von einem freien Atom. A heißt hier Ionisierungsenergie. Ablösen von Elektronen aus einem Festkörper oder von einem Atom oder das Anheben von Elektronen aus dem Valenzband ins Leitungsband bei einem Leiter oder Halbleiter bezeichnet man als Fotoeffekt, wenn dabei das auslösende Photon seine ganze Energie abgibt (kein gestreutes Photon wie beim Compton-Effekt). Zur Untersuchung des äußeren Fotoeffekts verwendet man eine Fotozelle (siehe Abb.3.4.4): Eine großflächige Cäsiumkathode und ein Leiterring befinden sich in einem evakuierten Glasgefäß. Wird die Kathode mit Licht bestrahlt, treffen die austretenden Elektronen (Fotoelektronen) zum Teil auf den Leiterring und es fließt ein Fotostrom zwischen den Kontakten 1 und. Die Fotozelle ist bei Lichteinfall eine Stromquelle. Cäsiumkathode 1 1 Abb Fotozelle mit Schaltbild Es folgt eine Zusammenstellung einiger Versuche zum Fotoeffekt mit deren Ergebnissen: Eine negativ geladene und fein abgeschmirgelte Zinkplatte (Entfernen der Oxydschicht), die auf ein Elektroskop zum Anzeigen der Ladung gesteckt ist, wird mit dem Licht einer Hg-Lampe bestrahlt: Die Platte entlädt sich. Wird der Versuch mit einer positiv geladenen Platte wiederholt, wird keine Entladung festgestellt. Licht löst Elektronen von Metall ab (Hallwachs-Effekt). (3.4.1) Wird der Abstand der Lichtquelle zu einer Fotozelle verdoppelt, sinkt der Fotostrom auf ein Viertel. Daraus folgt Der Fotostrom und damit die Zahl der abgelösten Elektronen ist zur Intensität des einfallenden Lichtes proportional. (3.4.) Die Messung des Fotostroms mit einem Oszilloskop extrem hoher Zeitauflösung ( t 1 8 s) ergibt: Der Fotostrom setzt praktisch sofort mit der Bestrahlung ein. (3.4.3) 47
48 3 Wechselwirkung von elektrom. Strahlung mit Materie Die maximale kinetische Energie der Fotoelektronen wird mit der Gegenfeldmethode gemessen (siehe Abb.3.4.5): Filter FZ Messverstärker Mit geeigneten Filtern (farbige Gläser) werden der Reihe nach die Wellenlängen des Hg-Spektrums einer Quecksilberdampf-Hochdrucklampe ausge- Hg-Lampe Abb Gegenfeldmethode U I F R + siebt und damit eine Fotozelle bestrahlt. Zwischen die Kathode und die Anode der Fotozelle wird eine Gegenspannung U gelegt, die von den Fotoelektronen überwunden werden muss. Man stellt U so ein, dass der Fotostrom I F gerade verschwindet (U = U ). In diesem Fall erreichen auch die schnellsten und unter dem günstigsten Winkel ausgetretenen Elektronen die Anode nicht mehr. Die maximale kinetische Energie der Fotoelektronen ist also W k = e U. E k [ev] f g f [ 1 14 Hz ] 1 f [ 1 14 Hz ] 8, 6,88 5,5 5,19 W k [ev] 1,45,94,33, Abb Gegenfeldmethode (Versuchsergebnis) Der Versuch mit der Gegenfeldmethode liefert folgende Ergebnisse: Die kinetische Energie hängt nicht von der Intensität, sondern nur von der Frequenz der einfallenden Strahlung ab. Es existiert eine materialabhängige Grenzfrequenz f g ; für Licht mit einer kleineren Frequenz gibt es keine Fotoelektronen. (3.4.4) (3.4.5) Für die kinetische Energie der Fotoelektronen gilt W k = hf A (3.4.6) (Lichtelektrische Gleichung; Einstein, Lenard, 195) Man beachte, dass (3.4.6) vor der Entdeckung der Quantenmechanik gefunden wurde. Mit unserem Kenntnisstand ist diese Gleichung eine triviale Anwendung des Energiesatzes und der Bohr schen Frequenzbedingung, für Einstein hingegen war das Aufstellen dieser Gleichung eine radikale Abkehr von der klassischen Theorie des Lichtes (Maxwell). Für uns ist das in Abb dargestellte Versuchsergebnis eine schöne Bestätigung unserer bisherigen Theorie und eine weitere Methode der experimentellen h-bestimmung (Steigung der Geraden durch die Messwerte). 48
49 3 Wechselwirkung von elektrom. Strahlung mit Materie Außerdem folgt aus dem Versuch die Austrittsarbeit A des verwendeten Kathodenmaterials der Fotozelle untersuchte Chaffee die Winkelabhängigkeit der Intensitätsverteilung der Fotoelektronen. Das Versuchsergebnis (siehe Abb.3.4.8) steht im Widerspruch zu der Verteilung, die man nach dem naiven Photonenbild erwarten würde (siehe Abb.3.4.7). hf I(ϕ) ϕ hf E keine Rückstreuung Abb Naives Photonenbild keine Streuung für ϕ = Abb Semiklassische Theorie Die klassische Physik (Newton und Maxwell) kann das Auftreten von Fotoelektronen erklären (erzwungene Schwingung der Elektronen im Feld der einfallenden Welle), doch wäre die Amplitude der Schwingung und somit auch die Energie des Elektrons von der Amplitude und damit der Intensität des einfallenden Lichtes abhängig (Widerspruch zu (3.4.4)). In der folgenden Tabelle ist zusammengestellt, welche Theorie welches Versuchsergebnis erklärt: Versuch (3.4.1) (3.4.) (3.4.3) (3.4.4) (3.4.5) (3.4.6) I(ϕ) klassisch ja ja nein nein nein nein ja naives Photon ja ja ja ja ja ja nein semiklassisch ja ja ja ja ja ja ja Die Versuche entscheiden eindeutig zugunsten der semiklassischen Theorie! 49
50 3 Wechselwirkung von elektrom. Strahlung mit Materie 3.5 Der Wirkungsquerschnitt Will man z.b. die Wahrscheinlichkeit für das Auftreten des Comptoneffektes in Abhängigkeit von der Wellenlänge der einfallenden Strahlung messen, dann lässt man eine Strahlung der Intensität I und der Wellenlänge λ auf einen Körper, das sogenannte Target (Ziel), fallen und misst, gegebenenfalls in Abhängigkeit von der Richtung, die Intensität der gestreuten Strahlung. Die meisten experimentellen Ergebnisse der Quantenmechanik und der Elementarteilchenphysik werden durch Streuexperimente dieser Art gefunden. N Teilchen im Zustand Z dx N = N +dn Teilchen im Zustand Z N Teilchen, die sich im Zustand Z befinden, durchdringen ein sehr dünnes Target der Fläche A und der Dicke dx. Target dn = dn Teilchen im Zustand Z Abb Streuexperiment : Dichte des Targetmaterials dn : Zahl der Teilchen (Atome, Moleküle) im Target M : Masse der Targetatome dm : Masse des Targets z : Teilchendichte des Targets dm = M dn = dv = Adx (3.5.1) z = dn dv = (3.5.) M Die Wahrscheinlichkeit, dass ein Teilchen beim Durchgang durch das Target vom Zustand Z in den Zustand Z übergeht, ist P = dn (3.5.3) N Zu jedem Atom des Targets denken wir uns eine auf der Flugrichtung der Teilchen senkrecht stehende Querschnittsfläche σ. σ muss nichts mit der geometrischen Fläche des Atoms zu tun haben. Die Wahrscheinlichkeit, dass ein Teilchen beim Durchgang durch das Target mindestens eine der gedachten Querschnittsflächen trifft, ist σ σ σ σ σ σ σ σ P = dn σ A (3.5.4) Abb.3.5. Wirkungsquerschnitt σ heißt Wirkungsquerschnitt dertargetatome fürdenübergangvon Z nach Z,wennP = P gilt, d.h. wenn σ dn A = dn (3.5.5) N Aus (3.5.1) und (3.5.) folgt dn = zdv = zadx und daraus mit (3.5.5) oder dn = σ dn = σzdx (3.5.6) N A dn = N σzdx (3.5.7) 5
51 3 Wechselwirkung von elektrom. Strahlung mit Materie Für ein nicht extrem dünnes Target ist in (3.5.7) N durch N(x) (die Zahl der Teilchen im Zustand Z am Ort x) zu ersetzen. Damit erhält man dn = dn = N(x)σzdx (3.5.8) dx N N N +dn oder dn N = σzdx (3.5.9) x x+dx Abb Lambert sches Gesetz x Integration von (3.5.9) liefert woraus lnn = σzx+c, (3.5.1) N = e σzx+c = C e σzx (3.5.11) folgt. Aus N() = N folgt C = N und damit das Lambert sche Gesetz mit N(x) = N e αx (3.5.1) α = σ z = σ Die Halbwertsdicke x h des Targets ist durch N(x h ) = 1 N definiert. Aus (3.5.1) folgt M (3.5.13) x h = ln α (3.5.14) Im Fall der Absorption bedeutet der Zustand Z, dass das Teilchen nicht mehr vorhanden ist. N ist dann die Zahl der noch vorhandenen Teilchen, α nennt man den Absorptionskoeffizienten und σ heißt in diesem Fall der Absorptionsquerschnitt. Ist der Zustand Z durch das Teilchen wurde gestreut gekennzeichnet, dann nennt man σ den Streuquerschnitt. Das Lambert sche Gesetz gilt nur dann, wenn ein in den Zustand Z versetztes Teilchen nicht mehr in den Zustand Z zurückkehren kann (Alles-oder-nichts-Wechselwirkung). (3.5.1) gilt z.b. für die Absorption von Photonen durch den Fotoeffekt oder die Paarerzeugung und in guter Näherung auch für die Rayleigh- und Compton-Streuung. 51
52 3 Wechselwirkung von elektrom. Strahlung mit Materie 3.6 Die wesentlichen Wechselwirkungen elektromagnetischer Strahlung mit Materie-Überblick Hauptsächlich gibt es vier Arten von Wechselwirkung elektromagnetischer Strahlung mit Materie. Im Folgenden bezeichnet A die Ionisierungsenergie des am schwächsten gebundenen Elektrons, f 1 < f <... < f n sind die Resonanzfrequenzen der beteiligten Atome, m e ist die Ruhmasse des Elektrons, f die Frequenz der einfallenden und f die Frequenz der gestreuten Strahlung. Z sei die Ordnungszahl (Zahl der Elektronen) der beteiligten Atome Kohärente Streuung oder Rayleigh-Streuung (f = f ) Für Wellenlängen, die groß gegen die Abmesseungen eines Atoms sind (λ 1 1 m), d.h. für hf 1 4 ev, kann das elektrische Feld der Welle über den Bereich des Atoms als konstant angesehen werden. Die elastisch an den Kern gebundenen Elektronen schwingen dann im Takt der einfallenden Welle und bilden somit selbst einen schwingenden Dipol, der Licht in alle Richtungen aussendet (Rayleigh-Streuung). Mit dem klassischen Elektronenradius r e = e 4πε m e c (3.6.1) und dem Thomson-Querschnitt σ Th = 8π 3 r e (3.6.) gilt für den Wirkungsquerschnitt der Rayleigh-Streuung außerhalb der Resonanzfrequenzen σ R Z f 4 für f f 1 (3.6.3) σ R = Z σ Th für f n f 1 4 ev (3.6.4) lim σ R = (3.6.5) f Für eine Resonanzfrequenz ist der Wirkungsquerschnitt σ Res = e τ ε m e c, (3.6.6) wobei τ die mittlere Lebensdauer des angeregten Zustands ist. τ liegt in der Größenordnung von 1 8 s. Wegen der endlichen Masse des streuenden Atoms ist f nicht exakt gleich f, sondern etwas kleiner. f berechnet man mit der Comptonformel, wobei die Masse m e des Elektrons durch die Masse M des freien Atoms ersetzt werden muss (Comptoneffekt am ganzen Atom). Die kohärente Streuung an Atomen im Kristall ist die Grundvoraussetzung für die Braggreflexion Comptonstreuung Die klassische Behandlung der Streuung von elektromagnetischen Wellen an freien Elektronen (J.J. Thomson) liefert als Streuquerschnitt den Thomsonquerschnitt (3.6.). Nach der klassischen Rechnung schwingen die Elektronen im Takt der einfallenden Strahlung mit, d.h. es ist f = f. Die korrekte Beschreibung der Streuung an freien Elektronen mit der Quantenmechanik liefert die Comptonformel. Hier gilt näherungsweise für kleine Frequenzen f f. Der Wirkungsquerschnitt für die Comptonstreuung wurde 199 von Klein und Nishina mit Hilfe der Diracgleichung, einer relativistischen Verallgemeinerung der Schrödingergleichung, berechnet: mit σ C = πr e 1 x [(1 4x 8x ) ln(1+x) x 1 (1+x) ] (3.6.7) x = hf m e c (3.6.8) 5
53 Für hf m e c gilt 3 Wechselwirkung von elektrom. Strahlung mit Materie σ C σ Th 1+x, (3.6.9) d.h. σ C geht für kleine Frequenzen in den Thomsonquerschnitt über. Die Comptonformel λ = λ+λ C (1 cosϕ) (3.6.1) und die Formel (3.6.7) von Klein-Nishina gelten exakt nur für wirklich freie Elektronen, in guter Näherung aber auch für gebundene Elektronen, deren Ionisierungsenergie bzw. Austrittsarbeit klein gegen hf ist. Der Wirkungsquerschnitt eines Atoms mit Z Elektronen für Comptonstreuung an Elektronen ist σ C,Atom = Z σ C (3.6.11) σ C,Atom darf nicht mit dem Streuquerschnitt des Comptoneffekts am ganzen Atom (m e durch m Atom ersetzen, Rayleighstreuung) verwechselt werden! Fotoeffekt Für hf > A tritt neben der kohärenten Streuung und der Comptonstreuung als weiterer Kanal der Wechselwirkung noch der Fotoeffekt auf. Der Wirkungsquerschnitt σ F von H-Atomen für den Fotoeffekt kann analytisch berechnet werden. Mit A = 13,6 ev gilt 1 7 σ Th für hf = A σ F (f) ( )7 A 1,5 1 6 (3.6.1) σ Th für A hf m e c hf Für andere Atome ist σ F viel größer, da im Bereich hf A der Wirkungsquerschnitt σ F ungefähr proportional zu Z 5 ist Paarerzeugung Für hf > m e c kann sich ein Photon im Feld eines Kerns (der Kern nimmt Impuls auf) in ein Elektron-Positron-Paar verwandeln. Der Wirkungsquerschnitt für Paarerzeugung ist [ ] π hf Z re m e c für hf m e c [ ( ) σ P (f) = 8 hf 133 Z re ln m e c 19 ] für m e c hf 137 m 4 Z 1 e c (3.6.13) 3 [ ( ) Z re ln 1 ] für hf 137 m e c 4 Z 1 3 Die Berechnung der Wirkungsquerschnitte findet man z.b. in Landau, Lifschitz, Lehrbuch der theoretischen Physik, Bd. IVa. Die heute beste Beschreibung der Wechselwirkung elektromagnetischer Strahlung mit Materie ist die 198 von Dirac begonnene und in den Fünfzigerjahren des zwanzigsten Jahrhunderts von Schwinger, Tomonaga und Feynman vollendete Quantenelektrodynamik (QED). Die QED sagt eine mit der semiklassischen Theorie (Schrödinger und Maxwell) nicht erklärbare Verschiebung der Energieniveaus von Atomen voraus (Lambshift), die 1949 von Kroll, Lamb, Weißkopf und French berechnet wurde ( W 1 6 ev). Z
54 3 Wechselwirkung von elektrom. Strahlung mit Materie σ 1 15 σ Th 1 7 σ Th Rayleigh σ R σ Th Rayleigh σr Fotoeffekt σf Compton σ C Paarerzeugung 1 σ P A m ec hf [ev] Abb Wirkungsquerschnitte für die Streuung von Photonen an H-Atomen t γ A t τ γ A t τ γ e t A e t e + A e γ A γ A γ e γ A γ A f = f x f = f x f < f x x x Rayleigh Resonanzstreuung Compton Fotoeffekt Paarbildung Abb.3.6. Feynman-Diagramme der behandelten Wechselwirkungen 54
55 4 Atommodelle 4.1 Das Atommodell von Rutherford Energiereiche α-teilchen durchdringen leicht die Elektronenhülle eines Atoms und werden erst in Kernnähe spürbar abgelenkt. Rutherford untersuchte 1911 die Streuung von α-teilchen an Goldkernen. Experimentell ermittelte Rutherford die Zahl dn der Teilchen, die in den Winkelbereich zwischen ϕ und ϕ + dϕ gestreut werden im Verhältnis zur Gesamtzahl N der einfallenden α-teilchen. α ϕ Goldfolie Zähler Abb Versuch von Rutherford Denkt man sich um den streuenden Kern K eine Kugelfläche mit dem Radius r, dann entspricht dem Winkelbereich [ϕ, ϕ+dϕ] die Ringfläche πadb (siehe Abb.4.1.). Die Maßzahl dieser Ringfläche für r = 1 nennt man den Raumwinkel dω. Alle einfallenden Teilchen, die eine gewisse Ringfläche dσ um das Streuzentrum treffen, werden in den Raumwinkel dω gestreut. dσ nennt man den differentiellen Wirkungsquerschnitt. Mit s ds dσ K dϕ ϕ r = 1 a dω a = r sinϕ = sinϕ db und erhält man Abb.4.1. Differentieller Wirkungsquerschnitt db = rdϕ = dϕ dω = π sinϕdϕ (4.1.1) Den Abstand s des Streuzentrums von der Flugbahn des noch weit entfernten Teilchens nennt man den Stoßparameter. Damit gilt dσ = πsds (4.1.) Aus der Atomdichte z (Zahl der Atome pro Volumen) des Targetmaterials und der Dicke x des Targets berechnet sich die Fläche σ, die jedem streuenden Atomkern zusteht (A q sei die Querschnittsfläche des einfallenden Teilchenstrahls): Damit gilt σ = A q zv = A q za q x = 1 zx dn N = dσ σ 55 (4.1.3) = zxdσ (4.1.4)
56 4 Atommodelle Aus (4.1.1), (4.1.) und (4.1.4) erhält man (wenn s größer wird, wird ϕ kleiner!) dσ dω = sds sinϕ dϕ = s sinϕ dϕ ds (4.1.5) Mit einer rein klassischen Rechnung (Newton, Coulombkraft), die der Berechnung von Planetenbahnen vollkommen analog ist, erhielt Rutherford folgendes Ergebnisse, die im Anhang zu diesem Kapitel hergeleitet werden: ϕ = arcsinb mit B = 1 ( ) (4.1.6) msv 1+ α Dabei ist m die Masse eines α-teilchens, v die Geschwindigkeit der einfallenden Teilchen in noch großer Entfernung und α = q α q Kern 4πε = e Ze 4πε = Ze πε (4.1.7) Differenzieren von(4.1.6) und Einsetzen in(4.1.5) liefert die berühmte Rutherford sche Streuformel dσ = α dω 4m v 4 (4.1.8) sin 4 ϕ Mit (4.1.4), (4.1.7) und (4.1.8) erhält man endgültig für die Zahl dn der Teilchen, die in den Raumwinkel dω gestreut werden: [ Ze ] dn = N zxdσ = N zx 4πε mv dω sin 4 ϕ (4.1.9) Eine quantenmechanische Rechnung ergibt zufällig die exakt gleiche Streuformel, die Rutherford auf rein klassischem Wege erhalten hat! Rutherford bestimmte experimentell die Zahl dn der in den Raumwinkel dω gestreuten Teilchen und verglich die Messergebnisse mit seiner Formel. Bei Goldkernen stellte er bis zu einer kinetischen Energie der α-teilchen von ungefähr MeV auch für große Streuwinkel Übereinstimmung mit seiner Formel fest. Erst für größere Energien kommen die Teilchen dem Kern zu nahe und die gemachte Annahme der reinen Coulombwechselwirkung ist nicht mehr erfüllt, da die Teilchen dann in den Bereich der Kernkräfte gelangen. Zu einer Abschätzung des Radiuses der Goldkerne gehen wir von einer Rückstreuung (ϕ = 18 ) aus: W kin = W pot = e 79e 4πε r = r 158e 4πε MeV = 1, m Atommodell von Rutherford: Fast die ganze Masse eines Atoms ist im Atomkern mit der Ladung Z e (Z = Ordnungszahl) konzentriert, der einen Durchmesser der Größenordnung 1 14 m aufweist. Die Elektronen befinden sich im Raum um den Kern und gleichen die elektrische Anziehung durch Bewegung (Zentrifugalkraft) aus. Anhang: Herleitung der Rutherfordformel 56
57 4 Atommodelle Die Kraft auf das α-teilchen ist F = α r r 3 mit α = Ze πε (4.1.1) Damit lauten die Bewegungsgleichungen ẍ = αx mr 3 und ÿ = αy mr 3 (4.1.11) Zweimaliges Differenzieren der Beziehung s F α r y ϕ ϑ ϕ Kern x r = x +y (4.1.1) Abb Versuch von Rutherford liefert unter Anwendung der Ketten- und Produktregel Einsetzen von (4.1.11) und in (4.1.13) liefert Mit ṙ +r r = ẋ +ẏ +xẍ+yÿ (4.1.13) v = ẋ +ẏ (4.1.14) r r = v ṙ + α mr (4.1.15) x = r cosϑ und y = r sinϑ (4.1.16) erhält man, wieder unter Anwendung der Ketten- und Produktregel und damit v x = ṙ cosϑ r ϑ sinϑ und v y = ṙ sinϑ+r ϑ cosϑ (4.1.17) v = v x +v y = ṙ +r ϑ (4.1.18) Aus (4.1.15) und (4.1.18) folgt r r = r ϑ + α (4.1.19) mr Mit (4.1.19) haben wir eine erste Bewegungsgleichung des α-teilchens in Polarkoordinaten erhalten. Eine zweite Gleichung liefert uns der Drehimpulssatz. Der Drehimpuls des Teilchens bezüglich des Ursprungs, der wie der Impuls eine Erhaltungsgröße ist, ist definiert durch L = m r v = m (4.1.) xv y yv x Für den Betrag des Drehimpulses erhält man mit (4.1.16) und (4.1.17) L = m (xv y yv x ) = mr ϑ (4.1.1) Der konstante Drehimpuls L kann leicht durch die Anfangsgeschwindigkeit v (r ) und den Stoßparameter s ausgedrückt werden (siehe Abb.4.1.3): L = msv (4.1.) (4.1.19) und (4.1.1) sind die Bewegungsgleichungen in Polarkoordinaten, deren Lösung die Funktionen r(t) und ϑ(t) sind. Um den Ablenkwinkel ϕ zu berechnen brauchen wir aber nicht die volle zeitabhängige Lösung, sondern es genügt uns die Bahngleichung r(ϑ). Dazu rechnen wir die Ableitungen nach der Zeit mit Hilfe der Kettenregel und (4.1.1) in Ableitungen nach ϑ um, die wir im Folgenden mit einem Strich bezeichnen: ṙ = dr dt = dr dϑ dϑ dt = r (4.1.1) ϑ = r L mr (4.1.3) 57
58 4 Atommodelle Um eine leicht lösbare Differentialgleichung zu erhalten, führen wir folgende Substitution aus: r = 1 u bzw. u = 1 r (4.1.4) Damit folgt aus (4.1.1) ϑ = L m u (4.1.5) Mit der Quotienten- und der Kettenregel folgt u = du dϑ = d ( ) 1 = 1 dϑ r r dr dϑ = r r (4.1.6) oder Aus (4.1.3), (4.1.7) und r u = 1 folgt Nochmaliges Differenzieren nach t liefert r = r u = u u (4.1.7) ṙ = L m u (4.1.8) r = L m du dt = L m du dϑ ϑ = L m u u (4.1.9) Einsetzen von (4.1.4), (4.1.9) und (4.1.5) in (4.1.19): ) 1 ( u L m u u = 1 u L u 4 m + αu m oder (4.1.3) u +u = αm L (4.1.31) Wäre die rechte Seite von (4.1.31) Null, dann wäre es die vertraute Schwingungsgleichung. Wie man leicht sieht, ist die Lösung von (4.1.31): u(ϑ) = A cos(ϑ Φ) αm L (4.1.3) mit noch frei wählbaren Konstanten A und Φ. Nach Rücksubstitution erhält man die gesuchte Bahngleichung in Polarkoordinaten: r(ϑ) = 1 A cos(ϑ Φ) αm L (4.1.33) Die Konstante Φ bewirkt eine Drehung der Bahnkurve um den Winkel Φ. Durch geeignete Wahl des Koordinatensystems erreichen wir Φ =. Die Konstante A bestimmen wir mit Hilfe des Energiesatzes. Diepotentielle Energiedesα-Teilchens istu(r) = α r.damitlautetderenergiesatz m v + α r = W = m v = konst. (4.1.34) oder mit (4.1.18) m ( ) ṙ +r ϑ + α r = W (4.1.35) Einsetzen von (4.1.3) und (4.1.5) in (4.1.35): L r mr 4 + L mr + α r = W (4.1.36) 58
59 4 Atommodelle Differenzieren von (4.1.33): r = dr(ϑ) dϑ = Einsetzen von (4.1.37) und (4.1.33) in (4.1.36): Auflösen nach A: W = L A sin ϑ m A sinϑ ( A cosϑ αm ) = r L A sinϑ (4.1.37) + L ( m A cosϑ αm ) +α ( L A cosϑ αm ) L = = L A m α m L (4.1.38) A = ± 1 ( αm mw + L L ) (4.1.39) Mit (4.1.33) und (4.1.39) haben wir die Bahngleichung in Abhängigkeit von der Gesamtenergie W und vom Drehimpuls L gefunden. Diese Lösung gilt nicht nur für die Streuung von α-teilchen an Atomkernen, sondern für alle Wechselwirkungen, deren Kraft einem 1 -Gesetz r gehorcht, insbesondere für die Bahnen von Planeten und Satelliten. Wenn die Masse des Zentralgestirns (Sonne) nicht sehr groß gegen die Masse des Satelliten ist, muss man vorher ins Schwerpunktsystem transformieren. Für Gravitationswechselwirkungen ist α = γmm (4.1.4) v 4 = v 5 = 1,5 4 W = MeV 1 t = s v 3 = 1,3 v = v 1 =,5 α = 1, m = 1 r() = 1 s 1 = 1 s = 5 s 3 = 1 s 4 = s 5 = 3 Einheit: 1 15 m Abb Satellitenbahnen Abb Rutherfordstreuung (numerisch) Es ist üblich, (4.1.33) in der Form mit r(ϑ) = p 1+e cosϑ p = L mα (4.1.41) (4.1.4) 59
60 und der Exzentrizität 4 Atommodelle e = sgn(α) 1+ W L mα (4.1.43) zu schreiben. Für anziehende Kräfte (α < ) gilt folgende Bahnklassifizierung (siehe Abb.4.1.4, die schwere Masse befindet sich im Koordinatenursprung): mα L < W <, 1 < e < : Ellipse (v 1 in Abb.4.1.4) W = mα L, e = : Kreis (Spezialfall der Ellipse) (v in Abb.4.1.4) mα L < W <, < e < 1 : Ellipse (v 3 in Abb.4.1.4) W =, e = 1 : Parabel (v 4 in Abb.4.1.4) W >, e > 1 : Hyperbel (v 5 in Abb.4.1.4) Für eine abstoßende Kraft (α > ) ist die potentielle Energie und damit auch die Gesamtenergie W immer positiv, es gilt e > 1 und die Bahnkurve ist eine Hyperbel (siehe Abb.4.1.5). Es fehlt noch die Berechnung des Ablenkwinkels ϕ. Abb entnimmt man ϕ = π ϑ (4.1.44) ϑ erhält man aus (4.1.41) durch Nullsetzen des Nenners, weil dann r gegen Unendlich geht: ϕ α cosϑ = 1 e (4.1.45) K ϑ ϑ Aus (4.1.44) und (4.1.45) folgt ( ϕ = π arccos 1 ) = e oder mit Hilfe einer Formelsammlung ( ( π arccos 1 )) e Abb Ablenkwinkel s ( ϕ = arcsin 1 ) ( ) 1 = arcsin e e (4.1.46) Zur Herleitung der Streuformel müssen wir ϕ durch den Stoßparameter s ausdrücken. Mit der Geschwindigkeit v des α-teilchens im Unendlichen gilt Mit (4.1.43) und (4.1.47) geht (4.1.46) über in Mit Hilfe von L = mv s und W = m v (4.1.47) 1 ϕ = arcsinb mit B = ( ) (4.1.48) msv 1+ α 1 1 B = 1+ 6 ( ) msv α msv α (4.1.49)
61 4 Atommodelle berechnet sich die Ableitung von (4.1.48) nach s zu dϕ ds = mv ( ( msv ) ) (4.1.5) α 1+ α Einsetzen von (4.1.5) in (4.1.5) ergibt ( Aus (4.1.48) folgt αs dσ dω = Damit kann man sin ϕ umschreiben: ( msv ) ) 1+ α mv sinϕ = αs mv B sinϕ sin ϕ ( msv ) = B und 1+ = 1 α B = 1 sin ϕ sinϕ = sin ϕ cos ϕ = sin ϕ 1 sin ϕ = = sin ϕ 1 B (4.1.49) = sin ϕ B msv = α = msv α sin ϕ (4.1.5) und (4.1.53) in (4.1.51) liefert endgültig die Rutherford sche Streuformel: (4.1.51) (4.1.5) (4.1.53) dσ dω = αs mv sin ϕ msv α sin ϕ = α 4m v 4 1 sin 4 ϕ (4.1.54) oder dσ = α 4m v 4 dω sin 4 ϕ (4.1.55) 61
62 4 Atommodelle Es folgen, ohne Beweis, einige Formeln für Ellipsenbahnen, wenn die Masse M des Zentralgestirns sehr groß gegen die Masse m des Satelliten ist. Das Zentralgestirn befindet sich in einem Brennpunkt der Ellipse (B 1 ), der auch der Ursprung des Koordinatensystems ist. Der sonnenfernste Punkt der Ellipse heißt Aphel (A), der sonnennächste Punkt ist der Perihel (P). a ist die große Halbachse, b die kleine Halbachse. A B a Q b M a e r B 1 ϑ r v P Abb Keplerellipse r(ϑ) = p 1+e cosϑ a = B 1 Q+B Q (4.1.56) r = r() = B 1 P = p 1+e r(π) = B 1 A = p 1 e (4.1.57) a = p 1 e b = p 1 e (4.1.58) p = r v γm e = r v γm 1 (4.1.59) 4. Das Bohr sche Atommodell Das Rutherford sche Atommodell (Newton und Maxwell auf kreisendes Elektron anwenden) liefert keinen Anhaltspunkt für diskrete Energiewerte des Atoms. Wir versuchen daher folgende Modellvorstellung: Das Elektron im H-Atom wird als stehende Materiewelle um den Kern herum beschrieben (siehe Abb.4..1). r n Für die Wellenlänge dieser Materiewelle gilt dann n = 6 n λ = πr n (4..1) Mit der de Broglie-Relation λ = h m e v n Abb.4..1 Stehende Welle um den Kern folgt dann m e v n r n = n (4..) (1. Bohr sches Postulat) Niels Bohr hat dieses Postulat 1913 aufgestellt, um die experimentellen Ergebnisse zu erklären (de Broglie veröffentlichte seine Relation erst 194!!). In Worten lautet das 1. Bohr sche Postulat: Der Bahndrehimpuls L n = m e v n r n des Elektrons kann nur ein ganzzahliges Vielfaches von sein! 6
63 4 Atommodelle Weiter forderte Bohr, dass die Elektronen auf den Bohr schen Bahnen, im Gegensatz zur Maxwell schen Theorie, strahlungsfrei kreisen! Die Bohr sche Frequenzbedingung wird auch als. Bohr sches Postulat bezeichnet. hf = W m W n (4..3) Im Einelektronensystem (z.b. H, He +, Li ++, Be +++ usw.) spielt die elektrische Kraft die Rolle der Zentripetalkraft, d.h. es gilt Ze 4πε r n = m ev n r n (4..4) Auflösen von (4..) nach v n, Einsetzen in (4..4) und Auflösen nach r n liefert Z e r n F e v n r n = 4πε Zm e e n = ε h Zm e e π n (4..5) Abb.4.. Kräfte auf das e Mit r H1 bezeichnen wir den Radius des Wasserstoffatoms für n = 1 (1. Bohr scher Radius): r H1 = ε h m e e π =,59Å (4..6) Damit gilt für ein beliebiges Einelektronensystem mit der Kernladungszahl Z: r n = r H1 Z n =,59Å n (4..7) Z Mit (4..4) erhält man für die potentielle und die kinetische Energie des Elektrons W pot = Ze 4πε r n und W kin = m e v n = 1 Ze (4..8) 4πε r n Die Gesamtenergie des Elektrons auf der n-ten Bahn ist dann W n = W kin +W pot = 1 W pot +W pot = 1 W pot = Ze 8πε r n (4..9) 63
64 4 Atommodelle Mit (4..5) folgt aus (4..9) W Mit folgt W n = m e 8 ( Ze ) ε h 1 n (4..1) C = m ( ) e e 8 =, J = 13,6eV (4..11) ε h W n = Z C 1 n = W 1 n (4..1) Die Ionisierungsenergie eines Einelektronensystems im Grundzustand ist W Ion = W W 1 = Z C = Z 13,6eV (4..13) W 3 W W W 1 Abb.4..3 Energiespektrum Beim Übergang von W m nach W n wird elektromagnetische Strahlung der Wellenlänge λ mn ausgesandt. Es gilt 1 = W ( m W n 1 = Z R λ mn hc n 1 ) m (4..14) mit der Rydbergkonstanten R = C hc = m ee 4 8ε h3 c = 1, m (4..15) Das in R steht für eine unendliche Kernmasse (keine Berücksichtigung der Kernmitbewegung). Es gilt R H R (siehe Aufgaben). 64
65 4 Atommodelle 4.3 Quantenmechanische Atomtheorie Das Bohr sche Atommodell erklärt die Energiewerte von Einelektronensystemen in bester Übereinstimmung mit dem Experiment. Dieses Modell kann aber folgende Eigenschaften der Atome nicht erklären: z z P(x y z) Die dreidimensionale Gestalt Die magnetischen Eigenschaften Die Spektren der Mehrelektronenatome Die Auswahlregeln für erlaubte Übergänge (Spektrallinien zu bestimmten Energiedifferenzen fehlen) Die Feinstruktur (Aufspaltung) der Energieniveaus r ϑ y ϕ x F(x y ) x OF = r sinϑ x = r sinϑ cosϕ y = r sinϑ sinϕ z = r cosϑ Abb Kugelkoordinaten y Schreibt man die dreidimensionale Schrödingergleichung für das H-Atom ( ) m ϕ x + ϕ y + ϕ z +V( r) ϕ( r) = W ϕ( r) (4.3.1) auf Kugelkoordinaten um (siehe Abb.4.3.1), dann erhält man mit der potentiellen Energie V( r) = e 4πε r (4.3.) eine von r, ϑ und ϕ abhängige Lösung, die in der Form ψ(r,ϑ,ϕ) = R(r) Θ(ϑ) Φ(ϕ) (4.3.3) geschrieben werden kann. Die selbstverständlichen Bedingungen lim ψ(r,ϑ,ϕ) = und ψ(r,ϑ+π,ϕ+π) = ψ(r,ϑ,ϕ) (4.3.4) r lassen für die in den Funktionen R, Θ und Φ auftretenden Konstanten n, l und m nur ganze Zahlen mit folgenden Zusatzbedingungen zu: Zu jeder Hauptquantenzahl n kann l die Werte, 1,..., n 1 und zu jedem l kann m die Werte, ±1, ±..., ±l annehmen. n l: n 1 {}}{{}}{{}}{ m:, ±1, ±1, ±, ±1, ±, ±3... {}}{, ±1,..., ±(n 1) Abb.4.3. Quantenzahlen 65
66 4 Atommodelle Zu jedem Wert von l gibt es l+1 verschiedene Werte von m. Die Gesamtzahl der verschiedenen Wellenfunktionen zu einer festen Hauptquantenzahl n ist also (siehe Aufgaben) (n 1) = n (4.3.5) Zu jedem Zustand (n,l,m) gibt es noch zwei Einstellungen des Eigendrehimpulses oder Spins des Elektrons, was durch eine vierte Quantenzahl s beschrieben wird: s s = 1 s = ± 1 (4.3.6) (4.3.6) bedeutet, dass der Spin die Werte ± 1 annehmen kann. s s = 1 Abb Spin Die Energie, die zu einer Wellenfunktion ψ nmls gehört, hängt nur von der Hauptquantenzahl n ab und ist identisch mit den Werten der Bohr schen Theorie. Beim H-Atom gibt es also zu jeder Hauptquantenzahl n genau n verschiedene Zustände mit der gleichen Energie W n. Die verschiedenen Zustände mit gleichem n unterscheiden sich z.b. im Bahndrehimpuls, der im Gegensatz zur Bohr schen Theorie (L = n ) durch L = l(l+1) (4.3.7) gegeben ist. Wolfgang Pauli (Nobelpreis 1945) entdeckte 195 sein berühmtes Ausschließungsprinzip (Pauliprinzip oder Pauliverbot): Im Atom kann jeder Elektronenzustand (n,l,m,s) nur von einem Elektron besetzt sein! Im Mehrelektronenatom sind die Energien zu verschiedenen Zuständen, auch bei gleicher Hauptquantenzahl, i.a. verschieden. Da das Maximum der Aufenthaltswahrscheinlichkeit eines Elektrons mit wachsendem n weiter vom Kern entfernt ist, kommt es zu einem schalenartigen Aufbau der Elektronenhülle eines Atoms. n Bezeichnung der Schale: K L M N O maximale Besetzung (n ): Die Spektren der Alkalimetalle können annähernd durch eine etwas abgewandelte Bohr sche Theorie beschrieben werden (Leuchtelektronenmodell): Die Kernladung wird durch die Elektronen der inneren Schalen teilweise abgeschirmt; man verwendet daher in den Bohr schen Formeln eine effektive Kernladung Z eff < Z: ( 1 1 Zeff λ R mn n 1 ) m (4.3.8) 66
67 4 Atommodelle r in Å Cs Rb, K Xe He Na Ar Kr 1,5 Li H Al Os Ru Ni 1, B Abb Atomradien in Abhängigkeit von der Ordnungszahl Z Z W I in ev 5 He Ne Ar 15 H Kr Xe Rn 1 B 5 Li Al Na K Ga Rb In Cs Tl Abb Ionisierungsenergien in Abhängigkeit von der Ordnungszahl Z Z 67
68 4 Atommodelle Es folgt eine qualitative Erklärung der Größe der Atomradien in Abhängigkeit von der Kernladungszahl Z (siehe Abb.4.3.4). Wir gehen von der vereinfachenden Annahme aus, dass die Elektronen der äußeren Schale tatsächlich weiter außen sind als die Elektronen der inneren Schalen (wir wissen natürlich, dass sich die Aufenthaltswahrscheinlichkeiten der verschiedenen Elektronen überschneiden). Befinden sich n Elektronen in der äußeren Schale, dann sieht ein Elektron der äußeren Schale unter sich eine effektive Kernladung Z eff e, mit dem maximalen Wert äußere Schale ne (Z n)e Z e innere Schalen Z e (Z n) e = n e (4.3.9) Abb Zur effektiven Kernladung Wenn alle anderen Elektronen der äußeren Schale auch noch unter dem betrachteten Elektron sind, dann ist die effektive Kernladung nur noch e: 1 Z eff n (4.3.1) Für ein Alkaliatom ist n = 1 und damit Z eff 1. Mit wachsendem Z wird Z eff zunächst größer und der Atomradius r kleiner. Wird Z noch größer, dann wird die äußere Schale immer mehr gefüllt und Z eff wird wieder kleiner, der Radius wieder größer. Beim Erreichen des nächsten Alkaliatoms wird eine neue Schale begonnen und der Radius steigt sprunghaft an. Der große Sprung bei der Ionisierungsenergie von einem Edelgas zum benachbarten Alkaliatom erklärt sich wie folgt: Beim Alkaliatom ist der Radius groß und Z eff 1, beim Edelgas ist der Radius kleiner und Z eff größer. Wegen (4..9) ist die Ionisierungsenergie W Ion = Z eff e (4.3.11) r n 8πε damit beim Edelgas viel größer als beim benachbarten Alkaliatom. 68
69 4 Atommodelle 4.4 Röntgenspektren Bei einer nicht zu kleinen Beschleunigungsspannung U einer Röntgenröhre tritt zum kontinuierlichen Bremsspektrum (nur von U abhängig) noch ein vom Material der Anode abhängiges charakteristisches Linienspektrum. W. Kossel erklärte 1914 das Auftreten diskreter Linien im Röntgenspektrum mit der Bohr schen Theorie: Ein beschleunigtes Elektron schlägt aus dem Atom ein Elektron einer inneren Schale heraus. Dieses Loch wird von einem Elektron einer äußeren Schale wieder aufgefüllt. Intensität λ λ = hc eu Abb Röntgenemissionsspektrum λ M L K M L N M L K N M L K K Abb.4.4. Beispiel 1 Abb Beispiel Im ersten Beispiel (siehe Abb.4.4.) wird ein Elektron der K-Schale herausgeschlagen und von einem Elektron der M-Schale in einem Sprung wieder aufgefüllt - es wird ein Quant der K β -Linie ausgesendet. Im zweiten Beispiel (siehe Abb.4.4.3) wird ein Elektron der L-Schale herausgeschlagen und von einem Elektron der N-Schale in zwei Sprüngen wieder aufgefüllt - es wirdein Quant der L α - undder M α -Linie ausgesendet. Fehlt einelektronderk-schale,dann sieht einelektron der L-Schale eine kugelsymmetrische Ladungsverteilung der Ladung (Z 1)e (wenn das K-Elektron im Grundzustand ist). Aus (4..15) folgt dann für die Wellenlänge der K α -Linie mit n = 1 und m = das Moseley sche Gesetz O N M L K α β γ δ K-Serie α β γ L-Serie α β M-Serie Abb Diskrete Röntgenlinien 1 λ Kα = 3 4 R (Z 1) (4.4.1) Für beliebige Röntgenlinien folgt analog ( 1 1 R (Z a) λ mn n 1 ) m (4.4.) 69
70 4 Atommodelle mit einer von m und n abhängigen Abschirmkonstanten a. Das Ungefährzeichen wird verwendet, weil die Wechselwirkung zwischen den Elektronen vernachlässigt wird. Für die L α -Linie würde man a 9 erwarten, experimentell erhält man a = 7,4. Springt ein Elektron der M-Schale in ein Loch der K-Schale, wird ein Photon der K β -Linie emittiert. Die Energie dieses Photons ist sicher größer als die Energie eines Photons der K α - Linie, d.h. es gilt λ Kβ < λ Kα. Mit n = 1 und m = 3 folgt aus (4.4.) 1 λ Kβ 8 9 R (Z a) (4.4.3) Auf dem Weg von der M- zur K-Schale sieht das Elektron eine effektive Kernladung von ungefähr Z 9 bis zu Z 1, d.h es gilt sicher a > 1. Mit (4.4.3) und (4.4.1) folgt daraus für die Lage der K β -Linie λ Kβ 8 9 R (Z a) < 8 9 R (Z 1) = λ Kα oder zusammengefasst 7 3 λ K α < λ Kβ < λ Kα (4.4.4) σ K σ σ L W K W W L W WM W L W K W Abb Röntgenabsorptionsspektrum Die linken Diagramme in Abb zeigen den Wirkungsquerschnitt für die Absorption eines Photons durch den Fotoeffekt an einem Elektron einer bestimmten Schale. Die Form der Diagramme folgt aus der Tatsache, dass der Wirkungsquerschnitt für den Fotoeffekt mit wachsender Gammaenergie abnimmt, für Energien kleiner der Ionisierungsenergie aber Null sein muss. Die Überlagerung der Wirkungsquerschnitte für die einzelnen Schalen ergibt den gesamten Wirkungsquerschnitt. 7
71 Inhaltsverzeichnis 1 Materiewellen 1.1 Elektronenbeugung Die Wellenfunktion und ihre physikalische Bedeutung Wellenpakete als Überlagerung ebener Wellen Teilchen als Wellenpakete Die Unbestimmtheitsrelationen Stationäre Zustände 5.1 Die Schrödingergleichung Potentialbarrieren Gebundene Zustände Der Franck-Hertz-Versuch Wechselwirkung von elektrom. Strahlung mit Materie Der Übergang zwischen stationären Zuständen - Spektrallinien Die Lichtquantenhypothese Der Compton-Effekt Der Fotoeffekt Der Wirkungsquerschnitt Die wesentlichen Wechselwirkungen elektromagnetischer Strahlung mit Materie- Überblick Kohärente Streuung oder Rayleigh-Streuung (f = f ) Comptonstreuung Fotoeffekt Paarerzeugung Atommodelle Das Atommodell von Rutherford Das Bohr sche Atommodell Quantenmechanische Atomtheorie Röntgenspektren
Die Schrödingergleichung
 Die Schrödingergleichung Wir werden in dieser Woche die grundlegende Gleichung der Quantenmechanik kennenlernen, die Schrödingergleichung. Sie beschreibt das dynamische Verhalten von Systemen in der Natur.
Die Schrödingergleichung Wir werden in dieser Woche die grundlegende Gleichung der Quantenmechanik kennenlernen, die Schrödingergleichung. Sie beschreibt das dynamische Verhalten von Systemen in der Natur.
Übungen Quantenphysik
 Ue QP 1 Übungen Quantenphysik Kernphysik Historische Entwicklung der Atommodelle Klassische Wellengleichung 5 Schrödinger Gleichung 6 Kastenpotential (Teilchen in einer Box) 8 Teilchen im Potentialtopf
Ue QP 1 Übungen Quantenphysik Kernphysik Historische Entwicklung der Atommodelle Klassische Wellengleichung 5 Schrödinger Gleichung 6 Kastenpotential (Teilchen in einer Box) 8 Teilchen im Potentialtopf
ν und λ ausgedrückt in Energie E und Impuls p
 phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
Martinovsky Nicole. Schwarzmann Tobias. Thaler Michael
 Themen: Unbestimmtheitsrelationen, Materiewellen, Materieteilchen als Welle, Wellenfunktion, Dispersionsrelation, Wellenpaket, Wahrscheinlichkeitsinterpretation, Materie-Quanteninterferenz Martinovsky
Themen: Unbestimmtheitsrelationen, Materiewellen, Materieteilchen als Welle, Wellenfunktion, Dispersionsrelation, Wellenpaket, Wahrscheinlichkeitsinterpretation, Materie-Quanteninterferenz Martinovsky
Die Wellenfunktion ψ(r,t) ist eine komplexe skalare Größe, da keine Polarisation wie bei elektromagnetischen Wellen beobachtet wurde.
 2. Materiewellen und Wellengleichung für freie Teilchen 2.1 Begriff Wellenfunktion Auf Grund des Wellencharakters der Materie können wir den Zustand eines physikalischen Systemes durch eine Wellenfunktion
2. Materiewellen und Wellengleichung für freie Teilchen 2.1 Begriff Wellenfunktion Auf Grund des Wellencharakters der Materie können wir den Zustand eines physikalischen Systemes durch eine Wellenfunktion
1.4. Das freie quantenmechanische Elektron
 1.4. Das freie quantenmechanische Elektron 1.4.3. Dispersionsrelation Damit ist die Basis gelegt, um sich mit den grundlegenden Eigenschaften eines quantenmechanischen Teilchens vertraut zu machen. Die
1.4. Das freie quantenmechanische Elektron 1.4.3. Dispersionsrelation Damit ist die Basis gelegt, um sich mit den grundlegenden Eigenschaften eines quantenmechanischen Teilchens vertraut zu machen. Die
Quantenmechanik I Sommersemester QM Web Page teaching/ss13/qm1.d.html
 Quantenmechanik I Sommersemester 2013 QM Web Page http://einrichtungen.physik.tu-muenchen.de/t30e/ teaching/ss13/qm1.d.html Hinweise Zusätzliche Übung: Aufgrund des großen Andrangs bieten wir eine zusätzliche
Quantenmechanik I Sommersemester 2013 QM Web Page http://einrichtungen.physik.tu-muenchen.de/t30e/ teaching/ss13/qm1.d.html Hinweise Zusätzliche Übung: Aufgrund des großen Andrangs bieten wir eine zusätzliche
Übungen zur Quantentheorie (Lehramt) WS 2006/07
 Übungen zur Quantentheorie Lehramt) WS 2006/07 Lesender: Prof. M. Müller-Preußker Übungen: Dr. J. Käppeli Lösungsbeispiele zur 1. Serie Marcus Petschlies 1 Ebene Wellen 1 1.a) Allgemeine Lösung der Wellengleichung
Übungen zur Quantentheorie Lehramt) WS 2006/07 Lesender: Prof. M. Müller-Preußker Übungen: Dr. J. Käppeli Lösungsbeispiele zur 1. Serie Marcus Petschlies 1 Ebene Wellen 1 1.a) Allgemeine Lösung der Wellengleichung
Ferienkurs Quantenmechanik I WKB-Näherung und Störungstheorie
 Ferienkurs Quantenmechanik I WKB-Näherung und Störungstheorie Sebastian Wild Freitag, 6.. Inhaltsverzeichnis Die WKB-Näherung. Grundlegendes............................. Tunnelwahrscheinlichkeit.......................
Ferienkurs Quantenmechanik I WKB-Näherung und Störungstheorie Sebastian Wild Freitag, 6.. Inhaltsverzeichnis Die WKB-Näherung. Grundlegendes............................. Tunnelwahrscheinlichkeit.......................
1.4. Die Wahrscheinlichkeitsinterpretation
 1.4. Die Wahrscheinlichkeitsinterpretation 1.4.1. Die Heisenbergsche Unschärferelation Wie kann der Welle-Teilchen-Dualismus in der Quantenmechanik interpretiert werden? gibt die Wahrscheinlichkeit an,
1.4. Die Wahrscheinlichkeitsinterpretation 1.4.1. Die Heisenbergsche Unschärferelation Wie kann der Welle-Teilchen-Dualismus in der Quantenmechanik interpretiert werden? gibt die Wahrscheinlichkeit an,
Probestudium der Physik 2011/12
 Probestudium der Physik 2011/12 1 Schwingungen und Wellen: Einführung in die mathematischen Grundlagen 1.1 Die Sinus- und die Kosinusfunktion Die Sinusfunktion lässt sich genauso wie die Kosinusfunktion
Probestudium der Physik 2011/12 1 Schwingungen und Wellen: Einführung in die mathematischen Grundlagen 1.1 Die Sinus- und die Kosinusfunktion Die Sinusfunktion lässt sich genauso wie die Kosinusfunktion
Quantenmechanik. Eine Kurzvorstellung für Nicht-Physiker
 Quantenmechanik Eine Kurzvorstellung für Nicht-Physiker Die Quantenvorstellung Der Ursprung: Hohlraumstrahlung Das Verhalten eines Von Interesse: idealen Absorbers Energiedichte in Abhängigkeit zur Wellenlänge
Quantenmechanik Eine Kurzvorstellung für Nicht-Physiker Die Quantenvorstellung Der Ursprung: Hohlraumstrahlung Das Verhalten eines Von Interesse: idealen Absorbers Energiedichte in Abhängigkeit zur Wellenlänge
Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit. An einigen Beispielen erläutern
 Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit An einigen Beispielen erläutern 5. Das Photon: Welle und Teilchen 5.4. Die Plancksche Strahlungsformel Wichtige Punkte: u( ν, T ) = 8πh c
Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit An einigen Beispielen erläutern 5. Das Photon: Welle und Teilchen 5.4. Die Plancksche Strahlungsformel Wichtige Punkte: u( ν, T ) = 8πh c
1 Die Schrödinger Gleichung
 1 Die Schrödinger Gleichung 1.1 Die Wellenfunktion und ihre Wahrscheinlichkeitsinterpretation Aus den Versuchen der Elektronenbeugung, hat ein Elektron auch Welleneigenschaften. Für freie Elektronen mit
1 Die Schrödinger Gleichung 1.1 Die Wellenfunktion und ihre Wahrscheinlichkeitsinterpretation Aus den Versuchen der Elektronenbeugung, hat ein Elektron auch Welleneigenschaften. Für freie Elektronen mit
WKB-Methode. Jan Kirschbaum
 WKB-Methode Jan Kirschbaum Westfälische Wilhelms-Universität Münster Fachbereich Physik Seminar zur Theorie der Atome, Kerne und kondensierten Materie 1 Einleitung Die WKB-Methode, unabhängig und fast
WKB-Methode Jan Kirschbaum Westfälische Wilhelms-Universität Münster Fachbereich Physik Seminar zur Theorie der Atome, Kerne und kondensierten Materie 1 Einleitung Die WKB-Methode, unabhängig und fast
Durch welchen Schlitz ist das Teilchen geflogen? Beobachtung
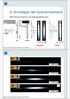 ) Grundlagen der Quantenmechanik Welle-Teilchen-Dualismus: das Doppelspaltexperiment Teilchen Welle Durch welchen Schlitz ist das Teilchen geflogen? Beobachtung Welle-Teilchen-Dualismus: 1) P =... Wahrscheinlichkeitsamplitude
) Grundlagen der Quantenmechanik Welle-Teilchen-Dualismus: das Doppelspaltexperiment Teilchen Welle Durch welchen Schlitz ist das Teilchen geflogen? Beobachtung Welle-Teilchen-Dualismus: 1) P =... Wahrscheinlichkeitsamplitude
VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik
 VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
Der Welle-Teilchen-Dualismus
 Quantenphysik Der Welle-Teilchen-Dualismus Welle-Teilchen-Dualismus http://bluesky.blogg.de/2005/05/03/fachbegriffe-der-modernen-physik-ix/ Welle-Teilchen-Dualismus Alles ist gleichzeitig Welle und Teilchen.
Quantenphysik Der Welle-Teilchen-Dualismus Welle-Teilchen-Dualismus http://bluesky.blogg.de/2005/05/03/fachbegriffe-der-modernen-physik-ix/ Welle-Teilchen-Dualismus Alles ist gleichzeitig Welle und Teilchen.
Vorlesung 23: Roter Faden: Die Schrödingergleichung. (Bedeuting in der Quantenmechanik wie F=ma in der klassischen Mechanik)
 Vorlesung 23: Roter Faden: Die Schrödingergleichung (Bedeuting in der Quantenmechanik wie F=ma in der klassischen Mechanik) Juli 12, 2006 Ausgewählte Kapitel der Physik, Prof. W. de Boer 1 Welle Teilchen
Vorlesung 23: Roter Faden: Die Schrödingergleichung (Bedeuting in der Quantenmechanik wie F=ma in der klassischen Mechanik) Juli 12, 2006 Ausgewählte Kapitel der Physik, Prof. W. de Boer 1 Welle Teilchen
Mathematischer Vorkurs für Physiker WS 2012/13: Vorlesung 1
 TU München Prof. P. Vogl Mathematischer Vorkurs für Physiker WS 2012/13: Vorlesung 1 Komplexe Zahlen Das Auffinden aller Nullstellen von algebraischen Gleichungen ist ein Grundproblem, das in der Physik
TU München Prof. P. Vogl Mathematischer Vorkurs für Physiker WS 2012/13: Vorlesung 1 Komplexe Zahlen Das Auffinden aller Nullstellen von algebraischen Gleichungen ist ein Grundproblem, das in der Physik
Ein Unterrichtsprojekt zur Quantenmechanik am Begabungsstützpunkt
 Ein Unterrichtsprojekt zur Quantenmechanik am Begabungsstützpunkt Andreas Kellerer (BSG Memmingen) Prof. Dr. Reinhold Rückl (Universität Würzburg) Die Rahmenbedingungen: Unterrichtsprojekt für den Kurs
Ein Unterrichtsprojekt zur Quantenmechanik am Begabungsstützpunkt Andreas Kellerer (BSG Memmingen) Prof. Dr. Reinhold Rückl (Universität Würzburg) Die Rahmenbedingungen: Unterrichtsprojekt für den Kurs
5. Kapitel Die De-Broglie-Wellenlänge
 5. Kapitel Die De-Broglie-Wellenlänge 5.1 Lernziele Sie können die De-Broglie-Wellenlänge nachvollziehen und anwenden. Sie kennen den experimentellen Nachweis einer Materiewelle. Sie wissen, dass das Experiment
5. Kapitel Die De-Broglie-Wellenlänge 5.1 Lernziele Sie können die De-Broglie-Wellenlänge nachvollziehen und anwenden. Sie kennen den experimentellen Nachweis einer Materiewelle. Sie wissen, dass das Experiment
Kapitel 8: Gewöhnliche Differentialgleichungen 8.1 Definition, Existenz, Eindeutigkeit von Lösungen Motivation: z.b. Newton 2.
 Kapitel 8: Gewöhnliche Differentialgleichungen 8.1 Definition, Existenz, Eindeutigkeit von Lösungen Motivation: z.b. Newton 2. Gesetz: (enthalten Ableitungen der gesuchten Funktionen) Geschwindigkeit:
Kapitel 8: Gewöhnliche Differentialgleichungen 8.1 Definition, Existenz, Eindeutigkeit von Lösungen Motivation: z.b. Newton 2. Gesetz: (enthalten Ableitungen der gesuchten Funktionen) Geschwindigkeit:
= 6,63 10 J s 8. (die Plancksche Konstante):
 35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
10. Das Wasserstoff-Atom Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
Probestudium der Physik 2011/12
 Probestudium der Physik 2011/12 Karsten Kruse 2. Mechanische Schwingungen und Wellen - Theoretische Betrachtungen 2.1 Der harmonische Oszillator Wir betrachten eine lineare Feder mit der Ruhelänge l 0.
Probestudium der Physik 2011/12 Karsten Kruse 2. Mechanische Schwingungen und Wellen - Theoretische Betrachtungen 2.1 Der harmonische Oszillator Wir betrachten eine lineare Feder mit der Ruhelänge l 0.
Abb.15: Experiment zum Rutherford-Modell
 6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
X.4 Elektromagnetische Wellen im Vakuum
 X.4 Elektromagnetische Wellen im Vakuum 173 X.4 Elektromagnetische Wellen im Vakuum In Abwesenheit von Quellen, ρ el. = 0 j el. = 0, nehmen die Bewegungsgleichungen (X.9) (X.11) für die elektromagnetischen
X.4 Elektromagnetische Wellen im Vakuum 173 X.4 Elektromagnetische Wellen im Vakuum In Abwesenheit von Quellen, ρ el. = 0 j el. = 0, nehmen die Bewegungsgleichungen (X.9) (X.11) für die elektromagnetischen
Grundbausteine des Mikrokosmos (7) Wellen? Teilchen? Beides?
 Grundbausteine des Mikrokosmos (7) Wellen? Teilchen? Beides? Experimentelle Überprüfung der Energieniveaus im Bohr schen Atommodell Absorbierte und emittierte Photonen hν = E m E n Stationäre Elektronenbahnen
Grundbausteine des Mikrokosmos (7) Wellen? Teilchen? Beides? Experimentelle Überprüfung der Energieniveaus im Bohr schen Atommodell Absorbierte und emittierte Photonen hν = E m E n Stationäre Elektronenbahnen
5. Vorlesung Wintersemester
 5. Vorlesung Wintersemester 1 Bewegung mit Stokes scher Reibung Ein dritter Weg, die Bewegungsgleichung bei Stokes scher Reibung zu lösen, ist die 1.1 Separation der Variablen m v = αv (1) Diese Methode
5. Vorlesung Wintersemester 1 Bewegung mit Stokes scher Reibung Ein dritter Weg, die Bewegungsgleichung bei Stokes scher Reibung zu lösen, ist die 1.1 Separation der Variablen m v = αv (1) Diese Methode
Erfüllt eine Funktion f für eine feste positive Zahl p und sämtliche Werte t des Definitionsbereichs die Gleichung
 34 Schwingungen Im Zusammenhang mit Polardarstellungen trifft man häufig auf Funktionen, die Schwingungen beschreiben und deshalb für den Ingenieur von besonderer Wichtigkeit sind Fast alle in der Praxis
34 Schwingungen Im Zusammenhang mit Polardarstellungen trifft man häufig auf Funktionen, die Schwingungen beschreiben und deshalb für den Ingenieur von besonderer Wichtigkeit sind Fast alle in der Praxis
Gewöhnliche Differentialgleichungen am Beispiel des harmonischen Oszillators
 Gewöhnliche Differentialgleichungen am Beispiel des harmonischen Oszillators Horst Laschinsky 12. Oktober 1999 Inhaltsverzeichnis 1 Gewöhnliche lineare homogene Differentialgleichungen 2. Ordnung mit konstanten
Gewöhnliche Differentialgleichungen am Beispiel des harmonischen Oszillators Horst Laschinsky 12. Oktober 1999 Inhaltsverzeichnis 1 Gewöhnliche lineare homogene Differentialgleichungen 2. Ordnung mit konstanten
Wahrscheinlichkeitsrechnung und Quantentheorie
 Physikalische Chemie II: Atombau und chemische Bindung Winter 2013/14 Wahrscheinlichkeitsrechnung und Quantentheorie Messergebnisse können in der Quantenmechanik ganz prinzipiell nur noch mit einer bestimmten
Physikalische Chemie II: Atombau und chemische Bindung Winter 2013/14 Wahrscheinlichkeitsrechnung und Quantentheorie Messergebnisse können in der Quantenmechanik ganz prinzipiell nur noch mit einer bestimmten
VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik
 VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
VL7 VL6. Elemente der Quantenmechanik I 6.1. Schrödingergleichung als Wellengleichung der Materie 6.2. Messungen in der Quantenmechanik VL7. Elemente der Quantenmechanik II 7.1. Wellenpakete als Lösungen
Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke)
 Freie Universität Berlin WS 2006/2007 Fachbereich Physik 0..2006 Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke) Übungsblatt 3: Zentraler Grenzwertsatz, Mikrokanonisches Ensemble, Entropie Aufgabe
Freie Universität Berlin WS 2006/2007 Fachbereich Physik 0..2006 Statistische Physik - Theorie der Wärme (PD Dr. M. Falcke) Übungsblatt 3: Zentraler Grenzwertsatz, Mikrokanonisches Ensemble, Entropie Aufgabe
Die Lösungen der S.-Glg. für das freie Teilchen
 Die Lösungen der S.-Glg. für das freie Teilchen Zeitabhängige S- G l g., ħ ħ x (, (, m i = + Vrt rt Analogie zu den eletromagnetischen Wellen, Materiewellen, intuitives Raten etc. Ansatz f ü r W e l l
Die Lösungen der S.-Glg. für das freie Teilchen Zeitabhängige S- G l g., ħ ħ x (, (, m i = + Vrt rt Analogie zu den eletromagnetischen Wellen, Materiewellen, intuitives Raten etc. Ansatz f ü r W e l l
Der photoelektrische Effekt
 Der photoelektrische Effekt h ν I ph Abnahme der negativen Ladung auf einer Platte bei Beleuchtung mit UV-Strahlung. Lichtinduzierte Elektronenemission (Lenard, 1902). Erklärung durch A. Einstein (1905)
Der photoelektrische Effekt h ν I ph Abnahme der negativen Ladung auf einer Platte bei Beleuchtung mit UV-Strahlung. Lichtinduzierte Elektronenemission (Lenard, 1902). Erklärung durch A. Einstein (1905)
10. Wellenpakete im Vakuum
 ω m. Wellenpakete im Vakuum. Informationsübertragung durch elektromagnetische Wellen Ein wichtiger Anwendungsbereich elektromagnetischer Strahlung ist die Informationsübertragung. Monochromatische ebene
ω m. Wellenpakete im Vakuum. Informationsübertragung durch elektromagnetische Wellen Ein wichtiger Anwendungsbereich elektromagnetischer Strahlung ist die Informationsübertragung. Monochromatische ebene
1. Bestimmen Sie die Phasengeschwindigkeit von Ultraschallwellen in Wasser durch Messung der Wellenlänge und Frequenz stehender Wellen.
 Universität Potsdam Institut für Physik und Astronomie Grundpraktikum 10/015 M Schallwellen Am Beispiel von Ultraschallwellen in Wasser werden Eigenschaften von Longitudinalwellen betrachtet. Im ersten
Universität Potsdam Institut für Physik und Astronomie Grundpraktikum 10/015 M Schallwellen Am Beispiel von Ultraschallwellen in Wasser werden Eigenschaften von Longitudinalwellen betrachtet. Im ersten
16 Elektromagnetische Wellen
 16 Elektromagnetische Wellen In den folgenden Kapiteln werden wir uns verschiedenen zeitabhängigen Phänomenen zuwenden. Zunächst werden wir uns mit elektromagnetischen Wellen beschäftigen und sehen, dass
16 Elektromagnetische Wellen In den folgenden Kapiteln werden wir uns verschiedenen zeitabhängigen Phänomenen zuwenden. Zunächst werden wir uns mit elektromagnetischen Wellen beschäftigen und sehen, dass
9. Vorlesung Wintersemester
 9. Vorlesung Wintersemester 1 Die Phase der angeregten Schwingung Wertebereich: bei der oben abgeleiteten Formel tan φ = β ω ω ω0. (1) ist noch zu sehen, in welchem Bereich der Winkel liegt. Aus der ursprünglichen
9. Vorlesung Wintersemester 1 Die Phase der angeregten Schwingung Wertebereich: bei der oben abgeleiteten Formel tan φ = β ω ω ω0. (1) ist noch zu sehen, in welchem Bereich der Winkel liegt. Aus der ursprünglichen
Klassische Theoretische Physik III (Elektrodynamik)
 WiSe 017/18 Klassische Theoretische Physik III (Elektrodynamik Vorlesung: Prof. Dr. D. Zeppenfeld Übung: Dr. M. Sekulla Übungsblatt 10 Ausgabe: Fr, 1.01.18 Abgabe: Fr, 19.01.17 Besprechung: Mi, 4.01.18
WiSe 017/18 Klassische Theoretische Physik III (Elektrodynamik Vorlesung: Prof. Dr. D. Zeppenfeld Übung: Dr. M. Sekulla Übungsblatt 10 Ausgabe: Fr, 1.01.18 Abgabe: Fr, 19.01.17 Besprechung: Mi, 4.01.18
Vorbereitung. (1) bzw. diskreten Wellenzahlen. λ n = 2L n. k n = nπ L
 Physikalisches Fortgeschrittenenpraktikum Gitterschwingungen Vorbereitung Armin Burgmeier Robert Schittny 1 Theoretische Grundlagen Im Versuch Gitterschwingungen werden die Schwingungen von Atomen in einem
Physikalisches Fortgeschrittenenpraktikum Gitterschwingungen Vorbereitung Armin Burgmeier Robert Schittny 1 Theoretische Grundlagen Im Versuch Gitterschwingungen werden die Schwingungen von Atomen in einem
Bohrsches Atommodell / Linienspektren. Experimentalphysik für Biologen und Chemiker, O. Benson & A. Peters, Humboldt-Universität zu Berlin
 Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Doppelspalt. Abbildung 1: Experimenteller Aufbau zur Beugung am Doppelspalt
 5.10.802 ****** 1 Motivation Beugung am Doppelspalt: Wellen breiten sich nach dem Huygensschen Prinzip aus; ihre Amplituden werden superponiert (überlagert). Der Unterschied der Intensitätsverteilungen
5.10.802 ****** 1 Motivation Beugung am Doppelspalt: Wellen breiten sich nach dem Huygensschen Prinzip aus; ihre Amplituden werden superponiert (überlagert). Der Unterschied der Intensitätsverteilungen
14 Teilchen und Wellen
 14 Teilchen und Wellen 14.1 Teilchencharakter von elektromagnetischen Wellen 1411 14.1.1 Strahlung schwarzer Körper 14.1.2 Der Photoeffekt 14.1.3 Technische Anwendungen 14.2 Wellencharakter von Teilchen
14 Teilchen und Wellen 14.1 Teilchencharakter von elektromagnetischen Wellen 1411 14.1.1 Strahlung schwarzer Körper 14.1.2 Der Photoeffekt 14.1.3 Technische Anwendungen 14.2 Wellencharakter von Teilchen
2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten
 Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Bohm sche Mechanik. Determinismus in der Quantenmechanik. Sven Köppel Mirko Pohland. 9. Juni, Fachbereich 13, Physik
 Determinismus in Quantenmechanik Sven Köppel Mirko Pohland Fachbereich 13, Physik 9. Juni, 2011 Ergebnisse an landläufigen Quantenmechanik ähnlich wie in Thermodynamik wäre es möglich, dass die Quantenmechanik
Determinismus in Quantenmechanik Sven Köppel Mirko Pohland Fachbereich 13, Physik 9. Juni, 2011 Ergebnisse an landläufigen Quantenmechanik ähnlich wie in Thermodynamik wäre es möglich, dass die Quantenmechanik
Differentialgleichungen 2. Ordnung
 Differentialgleichungen 2. Ordnung 1-E1 1-E2 Einführendes Beispiel Freier Fall Viele Geschichten ranken sich um den schiefen Turm von Pisa: Der Legende nach hat der aus Pisa stammende Galileo Galilei bei
Differentialgleichungen 2. Ordnung 1-E1 1-E2 Einführendes Beispiel Freier Fall Viele Geschichten ranken sich um den schiefen Turm von Pisa: Der Legende nach hat der aus Pisa stammende Galileo Galilei bei
2. Quadratische Lagrangefunktionen und Fourierreihe.
 0. Einführung Wir haben gerade das klassische Wirkungsprinzip betrachtet, nachdem wir wissen, dass der dynamische Verlauf eines Teilchens in dem Diagramm die Kurve darstellen soll, die die minimale Wirkung
0. Einführung Wir haben gerade das klassische Wirkungsprinzip betrachtet, nachdem wir wissen, dass der dynamische Verlauf eines Teilchens in dem Diagramm die Kurve darstellen soll, die die minimale Wirkung
Vorlesung 21: Roter Faden: Das Elektron als Welle Heisenbergsche Unsicherheitsrelation. Versuch: Gasentladung
 Vorlesung 21: Roter Faden: Das Elektron als Welle Heisenbergsche Unsicherheitsrelation Versuch: Gasentladung Juli 7, 2006 Ausgewählte Kapitel der Physik, Prof. W. de Boer 1 Erste Experimente mit Elektronen
Vorlesung 21: Roter Faden: Das Elektron als Welle Heisenbergsche Unsicherheitsrelation Versuch: Gasentladung Juli 7, 2006 Ausgewählte Kapitel der Physik, Prof. W. de Boer 1 Erste Experimente mit Elektronen
1 Funktionen und ihre Ableitungen
 1 Funktionen und ihre Ableitungen 1.1 Funktionen Wir nennen eine Grösse y eine Funktion von x, wenn der Wert von y von demjenigen von x abhängt: Zu jedem x wird in eindeutiger Weise ein Wert von y zugeordnet.
1 Funktionen und ihre Ableitungen 1.1 Funktionen Wir nennen eine Grösse y eine Funktion von x, wenn der Wert von y von demjenigen von x abhängt: Zu jedem x wird in eindeutiger Weise ein Wert von y zugeordnet.
WELLEN im VAKUUM. Kapitel 10. B t E = 0 E = B = 0 B. E = 1 c 2 2 E. B = 1 c 2 2 B
 Kapitel 0 WELLE im VAKUUM In den Maxwell-Gleichungen erscheint eine Asymmetrie durch Ladungen, die Quellen des E-Feldes sind und durch freie Ströme, die Ursache für das B-Feld sind. Im Vakuum ist ρ und
Kapitel 0 WELLE im VAKUUM In den Maxwell-Gleichungen erscheint eine Asymmetrie durch Ladungen, die Quellen des E-Feldes sind und durch freie Ströme, die Ursache für das B-Feld sind. Im Vakuum ist ρ und
1.3. DAS COULOMBSCHE GESETZ, ELEKTROSTATISCHES FELD 9
 8 KAPITEL. ELEKTROSTATIK.3 Das Coulombsche Gesetz, elektrostatisches Feld Zur Einführung verschiedener Grundbegriffe betrachten wir zunächst einmal die Kraft, die zwischen zwei Ladungen q an der Position
8 KAPITEL. ELEKTROSTATIK.3 Das Coulombsche Gesetz, elektrostatisches Feld Zur Einführung verschiedener Grundbegriffe betrachten wir zunächst einmal die Kraft, die zwischen zwei Ladungen q an der Position
27. Wärmestrahlung. rmestrahlung, Quantenmechanik
 24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
3 Lineare Differentialgleichungen
 3 Lineare Differentialgleichungen In diesem Kapitel behandeln wir die allgemeine Theorie linearer Differentialgleichungen Sie werden zahlreiche Parallelen zur Theorie linearer Gleichungssysteme feststellen,
3 Lineare Differentialgleichungen In diesem Kapitel behandeln wir die allgemeine Theorie linearer Differentialgleichungen Sie werden zahlreiche Parallelen zur Theorie linearer Gleichungssysteme feststellen,
Fourier-Reihen und Fourier-Transformation
 Fourier-Reihen und Fourier-Transformation Matthias Dreÿdoppel, Martin Koch, Bernhard Kreft 25. Juli 23 Einleitung Im Folgenden sollen dir und die Fouriertransformation erläutert und mit Beispielen unterlegt
Fourier-Reihen und Fourier-Transformation Matthias Dreÿdoppel, Martin Koch, Bernhard Kreft 25. Juli 23 Einleitung Im Folgenden sollen dir und die Fouriertransformation erläutert und mit Beispielen unterlegt
7 Die Hamilton-Jacobi-Theorie
 7 Die Hamilton-Jacobi-Theorie Ausgearbeitet von Rolf Horn und Bernhard Schmitz 7.1 Einleitung Um die Hamilton schen Bewegungsgleichungen q k = H(q, p) p k ṗ k = H(p, q) q k zu vereinfachen, führten wir
7 Die Hamilton-Jacobi-Theorie Ausgearbeitet von Rolf Horn und Bernhard Schmitz 7.1 Einleitung Um die Hamilton schen Bewegungsgleichungen q k = H(q, p) p k ṗ k = H(p, q) q k zu vereinfachen, führten wir
Übungsblatt 6 ( ) mit Lösungen
 1) Wellengleichung Experimentalphysik für Naturwissenschaftler 1 Universität Erlangen Nürnberg WS 014/15 Übungsblatt 6 (09.01.015) mit Lösungen Eine Welle, die sich in positiver x-richtung mit der Geschwindigkeit
1) Wellengleichung Experimentalphysik für Naturwissenschaftler 1 Universität Erlangen Nürnberg WS 014/15 Übungsblatt 6 (09.01.015) mit Lösungen Eine Welle, die sich in positiver x-richtung mit der Geschwindigkeit
6 Gewöhnliche Differentialgleichungen
 6 Gewöhnliche Differentialgleichungen Differentialgleichungen sind Gleichungen in denen nicht nur eine Funktion selbst sondern auch ihre Ableitungen vorkommen. Im einfachsten Fall gibt es eine unabhängige
6 Gewöhnliche Differentialgleichungen Differentialgleichungen sind Gleichungen in denen nicht nur eine Funktion selbst sondern auch ihre Ableitungen vorkommen. Im einfachsten Fall gibt es eine unabhängige
FK Experimentalphysik 3, Lösung 4
 1 Sterne als schwarze Strahler FK Experimentalphysik 3, 4 1 Sterne als schwarze Strahler Betrachten sie folgende Sterne: 1. Einen roten Stern mit einer Oberflächentemperatur von 3000 K 2. einen gelben
1 Sterne als schwarze Strahler FK Experimentalphysik 3, 4 1 Sterne als schwarze Strahler Betrachten sie folgende Sterne: 1. Einen roten Stern mit einer Oberflächentemperatur von 3000 K 2. einen gelben
4. Gleichungen im Frequenzbereich
 Stationäre Geräusche: In der technischen Akustik werden überwiegend stationäre Geräusche untersucht. Stationäre Geräusche sind zusammengesetzt aus harmonischen Schallfeldern p x,t = p x cos t x Im Folgenden
Stationäre Geräusche: In der technischen Akustik werden überwiegend stationäre Geräusche untersucht. Stationäre Geräusche sind zusammengesetzt aus harmonischen Schallfeldern p x,t = p x cos t x Im Folgenden
Mathematik II für Studierende der Informatik. Wirtschaftsinformatik (Analysis und lineare Algebra) im Sommersemester 2016
 und Wirtschaftsinformatik (Analysis und lineare Algebra) im Sommersemester 2016 5. Juni 2016 Definition 5.21 Ist a R, a > 0 und a 1, so bezeichnet man die Umkehrfunktion der Exponentialfunktion x a x als
und Wirtschaftsinformatik (Analysis und lineare Algebra) im Sommersemester 2016 5. Juni 2016 Definition 5.21 Ist a R, a > 0 und a 1, so bezeichnet man die Umkehrfunktion der Exponentialfunktion x a x als
Bellsche Ungleichungen oder existiert Einstein s spukhafte Fernwirkung wirklich?
 Kapitel 1 Bellsche Ungleichungen oder existiert Einstein s spukhafte Fernwirkung wirklich? 1.1 Worum gehts? In vielen Experimenten mit verschiedensten Teilchen ist nun gezeigt worden, dass Verschränkung
Kapitel 1 Bellsche Ungleichungen oder existiert Einstein s spukhafte Fernwirkung wirklich? 1.1 Worum gehts? In vielen Experimenten mit verschiedensten Teilchen ist nun gezeigt worden, dass Verschränkung
Potentialtöpfe und Potentialbarrieren
 Potentialtöpfe und Potentialbarrieren Potentialtopf Potentialbarriere V V -V < V > für x < V ( x = ± V für x a für x > a Der endliche Potentialtopf: Gebundene Lösungen V(x : x > L / V ( x = V : x > L /
Potentialtöpfe und Potentialbarrieren Potentialtopf Potentialbarriere V V -V < V > für x < V ( x = ± V für x a für x > a Der endliche Potentialtopf: Gebundene Lösungen V(x : x > L / V ( x = V : x > L /
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie. Messungen in der Quantenmechanik
 Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
Vorlesung 6: Roter Faden: Schrödingergleichung als Wellengleichung der Materie Messungen in der Quantenmechanik Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Wim de Boer, Karlsruhe
13 Mehrdimensionale Zufallsvariablen Zufallsvektoren
 3 Mehrdimensionale Zufallsvariablen Zufallsvektoren Bisher haben wir uns ausschließlich mit Zufallsexperimenten beschäftigt, bei denen die Beobachtung eines einzigen Merkmals im Vordergrund stand. In diesem
3 Mehrdimensionale Zufallsvariablen Zufallsvektoren Bisher haben wir uns ausschließlich mit Zufallsexperimenten beschäftigt, bei denen die Beobachtung eines einzigen Merkmals im Vordergrund stand. In diesem
Bellsche Ungleichungen oder existiert Einstein s spukhafte Fernwirkung wirklich?
 Kapitel 1 Bellsche Ungleichungen oder existiert Einstein s spukhafte Fernwirkung wirklich? Hier betrachten wir ein Gedankenexperiment, das bereits in unterschiedlichster Weise realisiert wurde, und uns
Kapitel 1 Bellsche Ungleichungen oder existiert Einstein s spukhafte Fernwirkung wirklich? Hier betrachten wir ein Gedankenexperiment, das bereits in unterschiedlichster Weise realisiert wurde, und uns
Übungsblatt 6 ( ) mit Lösungen
 Experimentalphysik für Naturwissenschaftler 1 Universität Erlangen Nürnberg WS 011/1 Übungsblatt 6 (7.01.01) mit Lösungen Vorlesungen: Mo, Mi, jeweils 08:15-09:50 HG Übungen: Fr 08:15-09:45 oder Fr 1:15-13:45
Experimentalphysik für Naturwissenschaftler 1 Universität Erlangen Nürnberg WS 011/1 Übungsblatt 6 (7.01.01) mit Lösungen Vorlesungen: Mo, Mi, jeweils 08:15-09:50 HG Übungen: Fr 08:15-09:45 oder Fr 1:15-13:45
Das Bohrsche Atommodell
 Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
6 Einige Gleichungen der mathematischen Physik
 203 6 Einige Gleichungen der mathematischen Physik Wir haben verschiedene dynamische Gleichungen kennengelernt, die die Bewegung eines physikalischen Systems wir betrachten in diesem Kapitel nur Systeme
203 6 Einige Gleichungen der mathematischen Physik Wir haben verschiedene dynamische Gleichungen kennengelernt, die die Bewegung eines physikalischen Systems wir betrachten in diesem Kapitel nur Systeme
Grundlagen der Physik 2 Schwingungen und Wärmelehre
 (c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 07. 05. 2007 Othmar Marti [email protected] Experimentelle Physik Universität Ulm (c) Ulm University p. 2/1 Wellen in
(c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 07. 05. 2007 Othmar Marti [email protected] Experimentelle Physik Universität Ulm (c) Ulm University p. 2/1 Wellen in
10.7 Moderne Atommodelle
 10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
3.3 Eindimensionale Wellengleichung
 3.3. Eindimensionale Wellengleichung 77 3.3 Eindimensionale Wellengleichung Die Wellengleichung lautet c 2 u(x,t) = 2 u t 2(x,t) für alle x Ω Rn, t R, wobei c > 0 eine Konstante ist. Schauen wir uns diese
3.3. Eindimensionale Wellengleichung 77 3.3 Eindimensionale Wellengleichung Die Wellengleichung lautet c 2 u(x,t) = 2 u t 2(x,t) für alle x Ω Rn, t R, wobei c > 0 eine Konstante ist. Schauen wir uns diese
Übungen Physik VI (Kerne und Teilchen) Sommersemester 2010
 Übungen Physik VI (Kerne und Teilchen) Sommersemester 21 Übungsblatt Nr. 3 Bearbeitung bis 6.5.21 Aufgabe 1: Neutronensterne Im Allgemeinen kann man annehmen, dass die Dichte in Zentrum von Neutronensternen
Übungen Physik VI (Kerne und Teilchen) Sommersemester 21 Übungsblatt Nr. 3 Bearbeitung bis 6.5.21 Aufgabe 1: Neutronensterne Im Allgemeinen kann man annehmen, dass die Dichte in Zentrum von Neutronensternen
,Faltung. Heavisidefunktion σ (t), Diracimpuls δ (t) Anwendungen. 1) Rechteckimpuls. 2) Sprungfunktionen. 3) Schaltvorgänge
 Heavisidefunktion σ (t), Diracimpuls δ (t),faltung Definition Heavisidefunktion, t > 0 σ ( t) = 0, t < 0 Anwendungen ) Rechteckimpuls, t < T r( t) = = σ ( t + T ) σ ( t T ) 0, t > T 2) Sprungfunktionen,
Heavisidefunktion σ (t), Diracimpuls δ (t),faltung Definition Heavisidefunktion, t > 0 σ ( t) = 0, t < 0 Anwendungen ) Rechteckimpuls, t < T r( t) = = σ ( t + T ) σ ( t T ) 0, t > T 2) Sprungfunktionen,
4. Wellenausbreitung
 Motivation: Beim Stab konnten Lösungen der Form gefunden werden. u x,t = f 1 x ct f 2 x ct Diese Lösungen beschreiben die Ausbreitung von Wellen im Stab. Die Funktionen f 1 x und f 2 x werden durch die
Motivation: Beim Stab konnten Lösungen der Form gefunden werden. u x,t = f 1 x ct f 2 x ct Diese Lösungen beschreiben die Ausbreitung von Wellen im Stab. Die Funktionen f 1 x und f 2 x werden durch die
5 Interpolation und Approximation
 5 Interpolation und Approximation Problemstellung: Es soll eine Funktion f(x) approximiert werden, von der die Funktionswerte nur an diskreten Stellen bekannt sind. 5. Das Interpolationspolynom y y = P(x)
5 Interpolation und Approximation Problemstellung: Es soll eine Funktion f(x) approximiert werden, von der die Funktionswerte nur an diskreten Stellen bekannt sind. 5. Das Interpolationspolynom y y = P(x)
10 Teilchen und Wellen. 10.1 Strahlung schwarzer Körper
 10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
Für Geowissenschaftler. EP WS 2009/10 Dünnweber/Faessler
 Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Das Unschärfeprodukt x p in der klassischen Mechanik Seminar zur Theorie der Atome, Kerne und kondensierten Materie. Jonas Lübke
 Das Unschärfeprodukt x p in der klassischen Mechanik Seminar zur Theorie der Atome, Kerne und kondensierten Materie Jonas Lübke 7. November 013 Inhaltsverzeichnis 1 Einführung 1 Beziehung zwischen klassischer
Das Unschärfeprodukt x p in der klassischen Mechanik Seminar zur Theorie der Atome, Kerne und kondensierten Materie Jonas Lübke 7. November 013 Inhaltsverzeichnis 1 Einführung 1 Beziehung zwischen klassischer
8 Das Bohrsche Atommodell
 8 Das Bohrsche Atommodell 1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse,
8 Das Bohrsche Atommodell 1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse,
Die Geschichte der Quantenmechanik
 Die Geschichte der Quantenmechanik Kurt Bräuer Institut für Theoretische Physik 5.04.006 www.kbraeuer.de 1 'Urväter' 5.04.006 www.kbraeuer.de Strahlung schwarzer Körper: Max Plank 1900 Plank'sches Strahlungsgesetz:
Die Geschichte der Quantenmechanik Kurt Bräuer Institut für Theoretische Physik 5.04.006 www.kbraeuer.de 1 'Urväter' 5.04.006 www.kbraeuer.de Strahlung schwarzer Körper: Max Plank 1900 Plank'sches Strahlungsgesetz:
Klassische Theoretische Physik: Elektrodynamik
 Klassische Theoretische Physik: Elektrodynamik Kaustuv Basu (Deutsche Übersetzung: Jens Erler) Argelander-Institut für Astronomie Auf dem Hügel 71 [email protected] Website: www.astro.uni-bonn.de/tp-l
Klassische Theoretische Physik: Elektrodynamik Kaustuv Basu (Deutsche Übersetzung: Jens Erler) Argelander-Institut für Astronomie Auf dem Hügel 71 [email protected] Website: www.astro.uni-bonn.de/tp-l
Wichtige Definitionen und Aussagen
 Wichtige Definitionen und Aussagen Zufallsexperiment, Ergebnis, Ereignis: Unter einem Zufallsexperiment verstehen wir einen Vorgang, dessen Ausgänge sich nicht vorhersagen lassen Die möglichen Ausgänge
Wichtige Definitionen und Aussagen Zufallsexperiment, Ergebnis, Ereignis: Unter einem Zufallsexperiment verstehen wir einen Vorgang, dessen Ausgänge sich nicht vorhersagen lassen Die möglichen Ausgänge
Wellenfunktion und Schrödinger Gleichung
 Kapitel 2 Wellenfunktion und Schrödinger Gleichung Das Ziel ist es, die Begriffe Wellenfunktion, Schrödinger Gleichung und Hamilton Operator anhand von Beispielen einzuführen. 2.1 Wellenfunktion eines
Kapitel 2 Wellenfunktion und Schrödinger Gleichung Das Ziel ist es, die Begriffe Wellenfunktion, Schrödinger Gleichung und Hamilton Operator anhand von Beispielen einzuführen. 2.1 Wellenfunktion eines
WAHRSCHEINLICHKEITSRECHNUNG
 WAHRSCHEINLICHKEITSRECHNUNG Mathematischer Teil In der Wahrscheinlichkeitsrechnung haben wir es mit Zufallsexperimenten zu tun, d.h. Ausgang nicht vorhersagbar. Grundbegriffe Zufallsexperiment und Ergebnisse
WAHRSCHEINLICHKEITSRECHNUNG Mathematischer Teil In der Wahrscheinlichkeitsrechnung haben wir es mit Zufallsexperimenten zu tun, d.h. Ausgang nicht vorhersagbar. Grundbegriffe Zufallsexperiment und Ergebnisse
Teilchen im elektromagnetischen Feld
 Kapitel 5 Teilchen im elektromagnetischen Feld Ausgearbeitet von Klaus Henrich, Mathias Dubke und Thomas Herwig Der erste Schritt zur Lösung eines quantenmechanischen Problems ist gewöhnlich das Aufstellen
Kapitel 5 Teilchen im elektromagnetischen Feld Ausgearbeitet von Klaus Henrich, Mathias Dubke und Thomas Herwig Der erste Schritt zur Lösung eines quantenmechanischen Problems ist gewöhnlich das Aufstellen
Die Macht und Ohnmacht der Quantenwelt
 Die Macht und Ohnmacht der Quantenwelt Prof. Dr. Sebastian Eggert Tag der Physik, TU Kaiserslautern, 5. Dezember 2015 Quantenmechanik heute Quanteninformatik Ultrakalte Quantengase Supraleitung und Vielteilchenphysik
Die Macht und Ohnmacht der Quantenwelt Prof. Dr. Sebastian Eggert Tag der Physik, TU Kaiserslautern, 5. Dezember 2015 Quantenmechanik heute Quanteninformatik Ultrakalte Quantengase Supraleitung und Vielteilchenphysik
7. Materiewellen und Energiequantisierung
 7.1 7. Materiewellen und Energiequantisierung 7.1 Energiequantisierung in Atomen Weisses Licht: kontinuierliches Spektrum, d.h. enthält alle Wellenlängen des sichtbaren Bereichs Anregung von Atomen in
7.1 7. Materiewellen und Energiequantisierung 7.1 Energiequantisierung in Atomen Weisses Licht: kontinuierliches Spektrum, d.h. enthält alle Wellenlängen des sichtbaren Bereichs Anregung von Atomen in
Experimentalphysik II Elektromagnetische Schwingungen und Wellen
 Experimentalphysik II Elektromagnetische Schwingungen und Wellen Ferienkurs Sommersemester 2009 Martina Stadlmeier 10.09.2009 Inhaltsverzeichnis 1 Elektromagnetische Schwingungen 2 1.1 Energieumwandlung
Experimentalphysik II Elektromagnetische Schwingungen und Wellen Ferienkurs Sommersemester 2009 Martina Stadlmeier 10.09.2009 Inhaltsverzeichnis 1 Elektromagnetische Schwingungen 2 1.1 Energieumwandlung
Fourier-Transformation
 Fourier-ransformation Im Folgenden werden die schon bekannten Eigenschaften der Fourier-Reihen zur Darstellung periodischer Funktionenn zusammengefasst und dann auf beliebige Funktionen verallgemeinert.
Fourier-ransformation Im Folgenden werden die schon bekannten Eigenschaften der Fourier-Reihen zur Darstellung periodischer Funktionenn zusammengefasst und dann auf beliebige Funktionen verallgemeinert.
15.5 Stetige Zufallsvariablen
 5.5 Stetige Zufallsvariablen Es gibt auch Zufallsvariable, bei denen jedes Elementarereignis die Wahrscheinlich keit hat. Beispiel: Lebensdauer eines radioaktiven Atoms Die Lebensdauer eines radioaktiven
5.5 Stetige Zufallsvariablen Es gibt auch Zufallsvariable, bei denen jedes Elementarereignis die Wahrscheinlich keit hat. Beispiel: Lebensdauer eines radioaktiven Atoms Die Lebensdauer eines radioaktiven
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale
 Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Wahrscheinlichkeit und Statistik: Zusammenfassung
 HSR Hochschule für Technik Rapperswil Wahrscheinlichkeit und Statistik: Zusammenfassung beinhaltet Teile des Skripts von Herrn Hardy von Lukas Wilhelm lwilhelm.net 12. Januar 2007 Inhaltsverzeichnis 1
HSR Hochschule für Technik Rapperswil Wahrscheinlichkeit und Statistik: Zusammenfassung beinhaltet Teile des Skripts von Herrn Hardy von Lukas Wilhelm lwilhelm.net 12. Januar 2007 Inhaltsverzeichnis 1
Fazit: Wellen haben Teilchencharakter
 Die Vorgeschichte Maxwell 1865 sagt elektromagnetische Wellen vorher Hertz 1886 beobachtet verstärkten Funkenüberschlag unter Lichteinstrahlung Hallwachs 1888 studiert den photoelektrischen Effekt systematisch
Die Vorgeschichte Maxwell 1865 sagt elektromagnetische Wellen vorher Hertz 1886 beobachtet verstärkten Funkenüberschlag unter Lichteinstrahlung Hallwachs 1888 studiert den photoelektrischen Effekt systematisch
