GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN
|
|
|
- Vincent Messner
- vor 7 Jahren
- Abrufe
Transkript
1 53 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu gehören vor allem Temperatur, ph-wert und Ionenstärke des Reaktionsmilieus. Die Geschwindigkeit einer enzymatischen Reaktion ist in bestimmten Grenzen auch von der Konzentration des Substrates [S] abhängig. In der Regel nimmt die Reaktionsgeschwindigkeit mit steigender Substratkonzentration zu, bis bei hohen Konzentrationen ein Sättigungswert (Maximalgeschwindigkeit V max ) erreicht wird. Das Erreichen dieser Maximalgeschwindigkeit ist ein wesentliches Charakteristikum enzymatisch katalysierter Reaktionen. Im einfachsten Fall, in dem nur ein Substrat umgesetzt wird, lässt sich die Abhängigkeit der Reaktionsgeschwindigkeit von der Substratkonzentration mit Hilfe der von Michaelis und Menten angegebenen Gleichung beschreiben: d [ S ] V S max v 0 dt K S m Dabei bedeutet: [S]: V 0 : Substratkonzentration bei Beginn der Reaktion Anfangsgeschwindigkeit der Reaktion bei der entsprechenden Substratkonzentration [S] t: Zeit V max : Maximalgeschwindigkeit der Reaktion, die bei Substratsättigung erreicht wird Beachte: V max ist proportional zur gesamten Enzymkonzentration [E] 0 : V max ~ [E] 0 K m : Michaelis-Konstante; bei dieser Substratkonzentration läuft die Reaktion mit halbmaximaler Geschwindigkeit ab. Oft ist die Michaelis-Konstante ein Maß für die Affinität des Enzyms zum Substrat. Die Ermittlung der Michaelis-Konstante hat eine große praktische Bedeutung für die Beurteilung eines Enzyms und der Wirkungsweise von Enzyminhibitoren.
2 54 Die Bestimmung der Maximalgeschwindigkeit spielt im klinisch-chemischen Labor eine große Rolle. Da die Maximalgeschwindigkeit V max proportional zur Enzymkonzentration ist, lässt sich aus der Maximalgeschwindigkeit die Enzymkonzentration (z.b. im Blut) ermitteln. Die Michaelis-Konstante lässt sich graphisch ermitteln, wenn man die Anfangsgeschwindigkeit der Reaktion bei verschiedenen Substratkonzentrationen unter sonst identischen Bedingungen misst und die Werte V 0 gegen [S] aufträgt (Auftragung nach Michaelis und Menten). Dabei ergibt sich eine Hyperbel, die bei hohen Substratkonzentrationen der Maximalgeschwindigkeit V max zustrebt. Im Bereich hoher Substratkonzentrationen ist also die Reaktionsgeschwindigkeit praktisch unabhängig von der Substratkonzentration, im Bereich niedriger Substratkonzentrationen ist V 0 dagegen stark von der Substratkonzentration abhängig. Aus der Kurve lässt sich die halbmaximale Geschwindigkeit und die zugehörige Substratkonzentration, die der Michaelis-Konstante des Enzyms entspricht, ablesen. S K m wenn v 0 V max 2 Diese Methode zur Bestimmung der Michaelis-Konstante ist jedoch verhältnismäßig ungenau, da sich V max in den wenigsten Fällen eindeutig festlegen lässt. Die graphische Bestimmung wird wesentlich vereinfacht durch eine Auftragung nach Lineweaver und Burk, der eine einfache Umformung der Michaelis-Menten-Gleichung zugrunde liegt: 1 v 0 K m V S max 1 V max Bei einer Auftragung von 1/V 0 gegen 1/[S] erhält man eine Gerade, die die Y-Achse im Punkt 1/V max und die X-Achse im Punkt -1/K m schneidet. Aus diesen Schnittpunkten lassen sich sowohl die Maximalgeschwindigkeit als auch die Michaelis-Konstante bestimmen. Im normalen Stoffwechsel spielt die Hemmung enzymatischer Reaktionen - ebenso wie die Aktivierung - eine bedeutende Rolle bei der Regulation von metabolischen Prozessen. Daneben lassen sich in vielen Fällen Vergiftungserscheinungen oder auch die Wirkung bestimmter Pharmaka auf eine Hemmung spezifischer enzymatischer Reaktionen zurückführen. Grundsätzlich unterscheidet man bei der Hemmung von Enzymen zwischen irreversibler und reversibler Hemmung. Im Gegensatz zur irreversiblen Hemmung kann bei der reversiblen Hemmung der Inhibitor vom Enzym dissoziieren (z.b. durch Verdünnen).
3 55 REVERSIBLE HEMMTYPEN Man unterscheidet drei Hemmtypen: kompetitive Hemmung, nichtkompetitive Hemmung und unkompetitive Hemmung. Bei der kompetitiven Hemmung wird der Inhibitor reversibel am aktiven Zentrum des Enzyms gebunden und verhindert so die Bindung des Substrats. Durch erhöhte Substratkonzentrationen kann der Inhibitor jedoch verdrängt werden, so dass bei sehr hohen Substratkonzentrationen die Maximalgeschwindigkeit der enzymatischen Reaktion erreicht werden kann. Die scheinbare Michaelis-Konstante des Enzyms nimmt dagegen in Anwesenheit des kompetitiven Inhibitors zu. Die Auftragung der Kehrwerte der Geschwindigkeit (1/V 0 ) gegen die Kehrwerte der Substratkonzentration (1/[S]) nach Lineweaver und Burk ergibt eine Gerade, die die Gerade der ungehemmten Reaktion auf der Y-Achse im Punkt 1/V max schneidet. Aus dem Schnittpunkt mit der X-Achse lässt sich die scheinbare (oder auch apparente) Michaelis-Konstante (K m app ) der gehemmten Reaktion errechnen, die mit der Inhibitor-Konstante K i über folgende Formel verknüpft ist: K m I app 1 K i K m Dabei ist [I] die molare Konzentration des Inhibitors. Die Inhibitor-Konstante K i ist ein Maß für die Affinität zwischen Enzym und Inhibitor. Sie gibt diejenige Konzentration des Inhibitors an, bei der die apparente Michaelis-Konstante der gehemmten Reaktion gerade doppelt so groß ist wie die Michaelis-Konstante der ungehemmten Reaktion. Bei der nichtkompetitiven Hemmung wird der Inhibitor nicht am aktiven Zentrum, sondern an einer anderen Stelle des Enzymproteins gebunden. Dadurch wird die Aktivität des Enzyms herabgesetzt oder vollständig unterdrückt. Da in diesem Fall der Inhibitor nicht durch das Substrat vom Enzym verdrängt werden kann, wird selbst bei sehr hohen Substratkonzentrationen die Maximalgeschwindigkeit des Enzyms nicht erreicht. Für den speziellen Fall, dass die Michaelis-Konstante für das Substrat unverändert bleibt, ergibt sich bei der Kehrwertauftragung nach Lineweaver und Burk bei der nichtkompetitiven Hemmung eine Gerade, welche die X-Achse im gleichen Punkt schneidet wie die Gerade der ungehemmten Reaktion. Die Maximalgeschwindigkeit der gehemmten Reaktion lässt sich aus dem Schnittpunkt mit der Y-Achse bestimmen. Die Dissoziationskonstante des Enzym- Inhibitor-Komplexes (K i ) berechnet man mit Hilfe der folgenden Formel: V app V max I 1 K i
4 56 Hierbei ist V app die in Anwesenheit des Inhibitors erhaltene Maximalgeschwindigkeit, [I] die molare Konzentration des Inhibitors und V max die Maximalgeschwindigkeit der ungehemmten Reaktion. K i entspricht der Inhibitorkonzentration, bei der die Maximalgeschwindigkeit der gehemmten Reaktion gerade halb so groß ist wie die Maximalgeschwindigkeit der nicht gehemmten Reaktion. Wird der Inhibitor nur von dem Enzym-Substrat-Komplex und nicht vom freien Enzym gebunden, handelt es sich um eine unkompetitive Hemmung. Bei diesem Hemmtyp wird der Enzym-Substrat-Inhibitor-Komplex nicht oder nur verlangsamt zum Enzym-Produkt-Komplex umgesetzt. In der Auftragung nach Lineweaver und Burk ergibt eine enzymatische Reaktion in Gegenwart eines unkompetitiven Inhibitors eine Gerade, die parallel zur Geraden für die ungehemmte Reaktion verläuft. Die Inhibitorkonstante lässt sich nach folgenden Formeln ermitteln: V app V max oder I m app I 1 K i K K m 1 K i wobei K m app bzw. V app die in Anwesenheit des Inhibitors erhaltene Michaelis-Konstante und Maximalgeschwindigkeit, [I] die molare Konzentration des Inhibitors und K m und V max die entsprechenden Konstanten der ungehemmten Reaktion sind. Ein unkompetitiver Inhibitor reduziert in gleichem Maße sowohl V max als auch K m einer enzymatischen Reaktion. Häufig wird auch das Auftreten von gemischten Hemmtypen beobachtet, die sich nicht eindeutig einer dieser drei Grundarten zuordnen lassen. ALLGEMEINE FRAGESTELLUNGEN Enzyme als Biokatalysatoren; Substratspezifität, Klassifizierung der Enzyme; Grundlagen der Messung einer Reaktionsgeschwindigkeit im optischen Test; Michaelis-Menten-Gleichung; Mechanismen der Hemmung von Enzymen; Interpretation von K m, V max, K i ; Medizinische Bedeutung der Enzyme.
5 57
6 58 ZIELSETZUNG DER EXPERIMENTE 1. Bestimmung der Michaelis-Konstante der Lactatdehydrogenase aus Kaninchen-Skelettmuskeln Die Lactatdehydrogenase (L-Lactat: NAD Oxidoreductase, EC ) (LDH) katalysiert den letzten Schritt der anaeroben Glykolyse LDH CH 3 -CHOH-COO + NAD + CH 3 -CO-COO + NADH + H + L (+) Lactat Pyruvat Das Gleichgewicht dieser Reaktion liegt auf der Seite der Lactatproduktion. Die Gleichgewichtskonstante K (25 C) = Pyruvat NADH H Lactat NAD 12 2,7 10 Unter den Reaktionsbedingungen in diesem Versuch liegt das gesamte Enzym in Form eines LDH-NADH Komplexes vor. Die Michaelis-Konstante K m für Pyruvat beschreibt in diesem Falle die Wechselwirkung zwischen Pyruvat und dem LDH-NADH Komplex. Die Reaktionsgeschwindigkeit wird mit dem photometrischen Test nach Otto Warburg gemessen, wobei der Unterschied im Absorptionsmaximum von NAD + und NADH ausgenutzt wird. Nikotinamid-Adenin-Dinukleotide (NAD) sind als Coenzyme von Dehydrogenasen in der Übertragung von Reduktionsequivalenten beteiligt. Dabei geht die oxidierte Form, NAD +, in die reduzierte Form, NADH, über: RH 2 + NAD + R + NADH + H +
7 59 Bei der Dehydrogenierung wird ein H -Hydridion (1 Proton + 2 Elektronen) auf die C4-Position des Pyridinringes übertragen. Der zweite Substratwasserstoff wird als Proton H + freigesetzt. Dieser Prozess ist schematisch am Beispiel der LDH-Reaktion dargestellt: NADH besitzt neben dem Absorptionsmaximum bei 260 nm ein zusätzliches Maximum bei 340 nm, das der oxidierten Form, dem NAD +, fehlt. In der Praxis wird die Messung statt bei 340 nm oft bei 366 nm durchgeführt, da Wolframdraht-Glühlampen in diesem Bereich benutzt werden können.
8 60 Der Extinktionskoeffizient für NADH beträgt in Abhängigkeit von der Wellenlänge: 340 = 6, (l mol -1 cm -1 ) 366 = 3, (l mol -1 cm -1 ) (Bei Verwendung von zur Berechnung ist neben der verwendeten Wellenlänge die Dimension von unbedingt zu berücksichtigen.) HEMMUNG DER LACTATDEHYDROGENASE DURCH OXAMAT In diesem Versuch wird die Hemmung des Lactatdehydrogenase-NADH Komplexes durch Oxamat untersucht. Substrat ist dabei Pyruvat. Man kann aber auch NADH als Substrat der Lactatdehydrogenase betrachten. Entsprechend könnte auch die Hemmung des Umsatzes von NADH durch Oxamat untersucht werden. Aus rein praktischen Gründen ist dieses Experiment mit den im Praktikum zur Verfügung stehenden Mitteln nicht möglich: Wegen der hohen Affinität von NADH, also dem niedrigen K m -Wert für die Bindung von NADH an Lactatdehydrogenase, müssten die Messungen bei NADH-Konzentrationen durchgeführt werden, die so niedrig sind, dass ein photometrische Bestimmung nicht möglich ist. Bei geeigneter Versuchsanordnung (Messung der NADH- Konzentrationen durch Fluoreszenz) würde sich herausstellen, dass Oxamat nur an den Lactatdehydrogenase NADH Komplex, aber nicht an die Lactatdehydrogenase bindet. Oxamat (Halbamid der Oxalsäure) Fragen: Vergleichen Sie die Struktur des Inhibitors Oxamat mit der Struktur der Substrate Pyruvat und NADH Welchen Hemmtyp erwarten Sie für die Hemmung der Lactatdehydrogenase durch Oxamat a) bezüglich Pyruvat? b) bezüglich NADH?
9 61 VERSUCHSDURCHFÜHRUNG UND VERSUCHSPROTOKOLL Mitbringliste: 30cm langes Lineal, Taschenrechner, Kittel Messung der Reaktionsgeschwindigkeit der LDH-Reaktion in Abhängigkeit von der Pyruvat-Konzentration 1. In Abwesenheit von Oxamat: Pipettierplan A Küvette Nr ml Na-Phosphat-Puffer (Glaskolben) 2,00 2,00 2,00 2,00 2,00 (0,1 mol/l, ph 7.4) ml NADH (gelbes Eppendorf-Gefäß) 0,15 0,15 0,15 0,15 0,15 (5 mmol/l) ml Na-Pyruvat (blaues Eppendorf-Gefäß) (10 mmol/l) 0,02 0,05 0,10 0,20 0,40 ml H 2 O 0,81 0,78 0,73 0,63 0,43 START der Reaktion ml LDH* (rotes Eppendorf-Gefäß) 0,02 0,02 0,02 0,02 0,02 Die Messung erfolgt gegen eine mit 3ml Wasser gefüllte Küvette. Der Küvetteninhalt wird durch dreimaliges Umdrehen der Küvette (bitte vorher mit Parafilm verschließen) gründlich gemischt und die Anfangsextinktion (E 0 ) gemessen. Nach 30 sec wird überprüft, ob E 0 unverändert bleibt. Die Küvette wird aus dem Photometer herausgenommen. Das Enzym (jeweils 0,02 ml) wird in die Küvette pipettiert. Der Küvetteninhalt wird sofort mit Parafilm verschlossen und durch dreimaliges Wenden der Küvette gemischt. Nach Entfernen des Parafilms wird die Küvette in das Photometer eingesetzt. Für einen Zeitraum von 2 min wird in Abständen von 15 sec die Extinktion abgelesen.
10 62 2. In Anwesenheit von Oxamat: Pipettierplan B Küvette Nr ml Na-Phosphat-Puffer (Glaskolben) (0,1 mol/l, ph 7.4) 2,00 2,00 2,00 2,00 2,00 ml NADH (gelbes Eppendorf-Gefäß) (5 mmol/l) ml Na-Pyruvat (blaues Eppendorf-Gefäß) (10 mmol/l) ml Oxamat (grünes Eppendorf-Gefäß) (1 mmol/l) 0,15 0,15 0,15 0,15 0,15 0,02 0,05 0,10 0,20 0,40 0,24 0,24 0,24 0,24 0,24 ml H 2 O 0,57 0,54 0,49 0,39 0,19 START der Reaktion ml LDH* (rotes Eppendorf-Gefäß) 0,02 0,02 0,02 0,02 0,02 Der Küvetteninhalt wird durch dreimaliges Umdrehen der Küvette (bitte vorher mit Parafilm verschließen) gründlich gemischt und die Anfangsextinktion (E 0 ) gemessen. Nach 30 sec wird überprüft, ob E 0 unverändert bleibt. Die Küvette wird aus dem Photometer herausgenommen. Das Enzym (jeweils 0,02 ml) wird in die Küvette pipettiert. Der Küvetteninhalt wird sofort mit Parafilm verschlossen und durch dreimaliges Wenden der Küvette gemischt. Nach Entfernen des Parafilms wird die Küvette in das Photometer eingesetzt. Für einen Zeitraum von 2 min wird in Abständen von 15 sec die Extinktion abgelesen.
11 63 Messergebnisse zu Pipettierplan A Zeit ' Küvette Vor Zugabe von LDH Start durch Zugabe von LDH (0,02 ml/küvette; mischen) Messergebnisse zu Pipettierplan B Zeit ' Küvette Vor Zugabe von LDH Start durch Zugabe von LDH (0,02 ml/küvette; mischen)
12 64 AUSWERTUNG UND FEHLERDISKUSSION Für jede Küvette werden die gemessenen Extinktionen in Abhängigkeit von der Zeit graphisch dargestellt. Die Abweichung von einem linearen Verlauf ist aber innerhalb der ersten Minute gering. Die Messpunkte (ab 15 s.) können verbunden werden. Die Steigungen der Messkurven werden mit Steigungsdreiecken von Hand bestimmt. Die Anfangsgeschwindigkeiten (NADH Verbrauch pro Zeiteinheit) werden mit Hilfe des Lambert-Beer Gesetzes errechnet: E = c d E = ermittelte Extinktionsänderung = molarer Extinktionskoeffizient von NADH bei 366 nm = 3, l mol -1 cm -1 d = Schichtdicke, 1 cm c = Änderung der NADH-Konzentration Für die mit Hilfe des Steigungsdreiecks für ein Zeitintervall von t min ermittelte Anfangsgeschwindigkeit der Reaktion, v 0, ergibt sich dann: v 0 c t E d t E 1-1 mol min 3, t Für t = 1 min folgt daraus: v 0 E 0,30 1 µmol ml 1 min
13 65 Aufgaben: 1. Stellen Sie die Zeitverläufe der Extinktion der Versuche 3 und 8 jeweils in einem Graphen dar. 2. Bestimmen Sie Extinktionsabnahme pro min ab dem Messpunkt 15sec. 3. Stellen Sie die Abhängigkeit der Anfangsgeschwindigkeiten von den Substratkonzentrationen in An- und Abwesenheit des Inhibitors jeweils in einem Graphen nach Michaelis-Menten (Anfangsgeschwindigkeit gegen Substratkonzentration) und Lineweaver-Burk (1/Anfangsgeschwindigkeit gegen 1/Substratkonzentration) dar. Bestimmung der Substratkonzentrationen [S] (Pyruvatkonzentrationen): Die Konzentration der Na-Pyruvat-Lösung beträgt 10 mmol/l (siehe Pipettierplan A und B). Diese Na-Pyruvat-Lösung wird durch das Pipettieren um folgenden Faktor verdünnt: ö ü 3 Folglich beträgt die Konzentration [S] der Na-Pyruvat-Lösung in den einzelnen Küvetten: ö ö ü ö 10 /l 3 4. Ermitteln Sie für die ungehemmte und die gehemmte Reaktion jeweils V max, K m und K m app 5. Welcher Typ der Enzymhemmung durch Oxamat liegt vor? 6. Berechnen Sie mit Hilfe der im Text für den jeweiligen Hemmtyp angegebenen Formel die Inhibitor-Konstante, K i.
14 66 Tabelle Küvette Nr. Extinktionsabnahme pro Minute E min Anfangsgeschwindigkeit E v 0,30* 0 min µmol ml min 1 v 0 ml min µmol Substratkon -zentration [S] (in der Küvette) mmol/ 1 [ S ] mmol * siehe Berechnung
15 BERECHNUNGEN 67
16 68 HÄUFIGSTE FEHLER BEIM EXPERIMENT UND SEINER AUSWERTUNG 1. Experiment - Photometer nicht gemäß der Anleitung am Arbeitsplatz eingestellt - Mangelhafte Pipettierung (Merke: Pipettenspitze soll bei Entnahme aus dem Vorrat und beim Pipettieren in die Küvette schräg aufstehen. Pipetten senkrecht halten, Küvetten schräg! - Durchmischung des Küvetteninhalts vergessen - Ungenaue Ablesung vom Photometer (zu früh oder zu spät) 2. Auswertung - Messpunkte nicht vollständig, unklar oder falsch eingetragen - Dimension nicht angegeben, Koordinatenbezeichnung in Abbildungen ungenügend.
17 SCHLUSSFOLGERUNGEN 69
GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN
 45 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN A. BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu
45 GRUNDLAGEN DER ENZYMKINETIK: MICHAELIS-MENTEN-GLEICHUNG, HEMMTYPEN A. BIOCHEMISCHE GRUNDLAGEN Die katalytischen Eigenschaften eines Enzyms können durch verschiedene Faktoren beeinflusst werden. Dazu
Versuch 03: Enzyme. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
 Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Versuch 03: Enzyme Lactatdehydrogenase I. Der optische Test: Bestimmung von Pyruvat Acetylcholinesterase II. Bestimmung der Serum-Acetylcholinesterase Aktivität: 1. Bestimmung der Acetylcholinesterase-Aktivität
Versuch 4. Enzymkinetik
 Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
Versuch 4 Enzymkinetik Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@mustermann.de X X X Dr. Postina Wird benotet?: Aufgabenstellung Ermittlung der maximalen Reaktionsgeschwindigkeit
Biochemische UE Alkaline Phosphatase.
 Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Lehrstuhl für Physiologische Chemie, Tierärztliche Fakultät, LMU München
 ENZYME II Beispiele für Stoffinhalte aus der Chemie als Grundlage für das Verständnis dieses Teiles: Säurestärke (pk s Wert), Begriff der Katalyse, Massenwirkungsgesetz und Gleichgewichtsverschiebung,
ENZYME II Beispiele für Stoffinhalte aus der Chemie als Grundlage für das Verständnis dieses Teiles: Säurestärke (pk s Wert), Begriff der Katalyse, Massenwirkungsgesetz und Gleichgewichtsverschiebung,
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2
 Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
Vom Molekül zur Zelle Block 3 Seminar / Praktikum 2 Diese Präsentation befindet sich auf der Lehr-Inhalts Seite des Inst f. unter www.meduniwien.ac.at/hp/medizinische-genetik/lehre Helmut Dolznig Inst.
1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S]
![1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S] 1.1. Grundlage aller enzymkinetischen Untersuchungen ist die Michaelis-Menten- Gleichung: V 0 = V max x [S] K m + [S]](/thumbs/58/42178387.jpg) 1.1 ABSHNITT 1: ENZYME Einführung Enzyme sind informationelle Makromoleküle und als solche Instrumente gezielter Prozeßsteuerung. Sie haben eine katalytische und eine kognitive Funktion. Die katalytische
1.1 ABSHNITT 1: ENZYME Einführung Enzyme sind informationelle Makromoleküle und als solche Instrumente gezielter Prozeßsteuerung. Sie haben eine katalytische und eine kognitive Funktion. Die katalytische
Enzymkinetik. PTV.6 Seite 1 von 12 Prof. Dr. M. Brunner M.Eng. Philip Schmit. Praktikum PT. 1 Einleitung. 2 Theoretische Grundlagen
 Seite 1 von 12 Praktikumsvorbereitung 1 Einleitung Die Tatsache, dass man sich abends ein paar Bier genehmigen kann und diese am nächsten Morgen im eigenen Blutkreislauf noch kaum, bzw. nicht mehr nachweisbar
Seite 1 von 12 Praktikumsvorbereitung 1 Einleitung Die Tatsache, dass man sich abends ein paar Bier genehmigen kann und diese am nächsten Morgen im eigenen Blutkreislauf noch kaum, bzw. nicht mehr nachweisbar
Enzymkinetik: Kinetik der alkalischen Phosphatase mit dem Substrat p-nitrophenylphosphat
 Biophysikalisches Praktikum Institut für Biophysik Johann Wolfgang Goethe-Universität Frankfurt am Main Enzymkinetik: Kinetik der alkalischen Phosphatase mit dem Substrat p-nitrophenylphosphat (letzte
Biophysikalisches Praktikum Institut für Biophysik Johann Wolfgang Goethe-Universität Frankfurt am Main Enzymkinetik: Kinetik der alkalischen Phosphatase mit dem Substrat p-nitrophenylphosphat (letzte
Nutzung von Origin in der Enzym-Kinetik
 Nutzung von Origin in der Enzym-Kinetik Ausgangssituation Die Geschwindigkeit einer enzymatischen Reaktionen bei vorgegebener Enzymkonzentration aber verschiedener Substratkonzentration berechnen und grafisch
Nutzung von Origin in der Enzym-Kinetik Ausgangssituation Die Geschwindigkeit einer enzymatischen Reaktionen bei vorgegebener Enzymkonzentration aber verschiedener Substratkonzentration berechnen und grafisch
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb +
![6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb + 6. Fragentyp A Wie berechnet man die ph-werte wässriger Lösungen starker Basen? A) ph = pks - log [HA] / 2 B) ph = 14 + log [OH-] C) ph = 7+ 1/2 pkb +](/thumbs/77/74984433.jpg) 1. Fragentyp D Welche der folgenden Einheiten für den molaren Extinktionskoeffizienten ist/sind korrekt? 1) liter I mol x cm 2) liter I mol 3) cm2 / mmol 4) cm2 / mmol x m1 2. Wie lautet die Henderson-Hasselbalch-Gleichung?
1. Fragentyp D Welche der folgenden Einheiten für den molaren Extinktionskoeffizienten ist/sind korrekt? 1) liter I mol x cm 2) liter I mol 3) cm2 / mmol 4) cm2 / mmol x m1 2. Wie lautet die Henderson-Hasselbalch-Gleichung?
Vertiefendes Seminar zur Vorlesung Biochemie I. Bearbeitung Übungsblatt 6
 Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Versuch 5: Enzyme (Alkalische Phosphatase) (V )
 Versuch 5: Enzyme (Alkalische Phosphatase) (V10 6.03.2012) Lernziele: 1) Reaktionsgeschwindigkeit, Aktivierungsenergie, chemisches Gleichgewicht; 2) Was tun Katalysatoren und Enzyme, 3) Michaelis-Menten
Versuch 5: Enzyme (Alkalische Phosphatase) (V10 6.03.2012) Lernziele: 1) Reaktionsgeschwindigkeit, Aktivierungsenergie, chemisches Gleichgewicht; 2) Was tun Katalysatoren und Enzyme, 3) Michaelis-Menten
Enzymologie 10. Kurs
 Arbeitsgruppe D Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs : Enzymologie Einleitung Enzyme ermöglichen durch ihre katalytische Wirkung viele Reaktionen im Stoffwechsel von Lebewesen.
Arbeitsgruppe D Clara Dees Susanne Duncker Anja Hartmann Kristin Hofmann Kurs : Enzymologie Einleitung Enzyme ermöglichen durch ihre katalytische Wirkung viele Reaktionen im Stoffwechsel von Lebewesen.
Versuch. Übungswoche: Enzyme. Kinetik der Lactat - Dehydrogenase. Enzymkinetik der Lactat Dehydrogenase Peroxidase Nachweis
 Labormethoden der Biologie Vorlesung zur Übung Zellbiologie und Physiologie Übungswoche: Enzyme AG Kudla Leiter: Oliver Batistič Enzymkinetik der Lactat Dehydrogenase Peroxidase Nachweis Versuch Kinetik
Labormethoden der Biologie Vorlesung zur Übung Zellbiologie und Physiologie Übungswoche: Enzyme AG Kudla Leiter: Oliver Batistič Enzymkinetik der Lactat Dehydrogenase Peroxidase Nachweis Versuch Kinetik
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
ENZYMREAKTIONEN. Die Geschwindigkeit einer enzymatischen Reaktion hängt von folgenden Reaktionsbedingungen ab.
 34 3. Probe in den Lichtweg bringen und E ablesen. Wird die Wellenlänge verändert, so muss das Photometer wieder neu geeicht werden, weil die Intensität der Lichtquelle und die Empfindlichkeit der Photozelle
34 3. Probe in den Lichtweg bringen und E ablesen. Wird die Wellenlänge verändert, so muss das Photometer wieder neu geeicht werden, weil die Intensität der Lichtquelle und die Empfindlichkeit der Photozelle
Praktikum. Enzymkinetik am Beispiel der Protease Trypsin
 Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
Praktikum Methoden der molekularen Biowissenschaften Teil 1: Biochemie Enzymkinetik am Beispiel der Protease Trypsin Prof. Walter Nickel Biochemie-Zentrum der Universität Heidelberg Thermodynamische Eigenschaften
Grundlagen der Enzymkinetik und Enzymologie
 Grundlagen der Enzymkinetik und Enzymologie 1. Tag: Bestimmung der Kenngrößen eines Enzyms Biochemische Grundlagen Anfang des 20. Jahrhunderts untersuchte Adrian Brown die Hydrolysegeschwindigkeit von
Grundlagen der Enzymkinetik und Enzymologie 1. Tag: Bestimmung der Kenngrößen eines Enzyms Biochemische Grundlagen Anfang des 20. Jahrhunderts untersuchte Adrian Brown die Hydrolysegeschwindigkeit von
Biochemie-Praktikum: Programm E
 Gruppe Nr. 0 Tübingen, den XXIX. Mai Anno Domini 00 Gero Schwenk, Forian Waker Biochemie-Praktikum: Programm E Versuch : Lactatkonzentration im Serum Enzyme Decies repetita pacebit. Aufgabensteung: Mit
Gruppe Nr. 0 Tübingen, den XXIX. Mai Anno Domini 00 Gero Schwenk, Forian Waker Biochemie-Praktikum: Programm E Versuch : Lactatkonzentration im Serum Enzyme Decies repetita pacebit. Aufgabensteung: Mit
Versuch: Enzyme (LDH)
 Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
GRUNDLAGEN DER ENZYMOLOGIE: AKTIVITÄTS- UND SUBSTRATBESTIMMUNGEN
 55 GRUNDLAGEN DER ENZYMOLOGIE: AKTIVITÄTS- UND SUBSTRATBESTIMMUNGEN BIOCHEMISCHE GRUNDLAGEN In lebenden Organismen katalysieren Enzyme chemische Stoffumwandlungen. Ein Enzym wird durch seine katalytische
55 GRUNDLAGEN DER ENZYMOLOGIE: AKTIVITÄTS- UND SUBSTRATBESTIMMUNGEN BIOCHEMISCHE GRUNDLAGEN In lebenden Organismen katalysieren Enzyme chemische Stoffumwandlungen. Ein Enzym wird durch seine katalytische
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease
 K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease
 K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
K3: Bestimmung der Michaelis-Menten-Kinetik von Urease Einleitung: In diesem Versuch soll die Umsetzung von Harnstoff durch das Enzym Urease beobachtet werden. Fast alle Enzyme sind Proteine, manche bestehen
Enzymkinetik Seite 1. Enzyme. Einführung
 Enzymkinetik Seite 1 Enzyme Einführung In jeder Zelle laufen Hunderte chemischer Reaktionen ab, die (mit wenigen Ausnahmen) alle von hochwirksamen Biokatalysatoren (Enzymen ) beschleunigt und gesteuert
Enzymkinetik Seite 1 Enzyme Einführung In jeder Zelle laufen Hunderte chemischer Reaktionen ab, die (mit wenigen Ausnahmen) alle von hochwirksamen Biokatalysatoren (Enzymen ) beschleunigt und gesteuert
Katalyse. höhere Reaktionsgeschwindigkeit bei derselben Temperatur! Achtung: Gleichgewicht der chemischen Reaktion wird nicht verschoben
 Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
Katalyse Ein Katalysator setzt Aktivierungsenergie einer Reaktion herab, indem er einen anderen Reaktionsweg ermöglicht, so dass der geschwindigkeitsbestimmende Schritt der nicht-katalysierten Reaktion
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail. Mag. Gerald Trutschl
 Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Enzyme (Teil 2) Enzymatische Reaktion, Thermodynamik & Enzyme im Detail Mag. Gerald Trutschl 1 Inhalt 1. Enzym Reaktion im Detail 2. Thermodynamische Reaktion 3. Katalysemechanismen 4. Michaelis-Menten-Konstante
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Biophysikpraktikum. Bestimmung der Enzymkinetik durch Absorptionsmessungen
 Biophysipratium Versuch: Bestimmung der Enzymineti durch Absorptionsmessungen I Ziel des Versuches: Der Versuch gibt eine Einführung in die grundlegenden Prozesse und Parameter der Enzymineti und deren
Biophysipratium Versuch: Bestimmung der Enzymineti durch Absorptionsmessungen I Ziel des Versuches: Der Versuch gibt eine Einführung in die grundlegenden Prozesse und Parameter der Enzymineti und deren
Aktivitätsbestimmung der Laktatdehydrogenase
 Aktivitätsbestimmung der Laktatdehydrogenase Für das Verständnis des Aufbaus von Enzymen und ihrer Wirkung sind Kenntnisse in der Biochemie der Proteine Voraussetzung. Folgende Begriffe sind von Bedeutung:
Aktivitätsbestimmung der Laktatdehydrogenase Für das Verständnis des Aufbaus von Enzymen und ihrer Wirkung sind Kenntnisse in der Biochemie der Proteine Voraussetzung. Folgende Begriffe sind von Bedeutung:
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Enzym-Kinetik (Abb. 1) Das Thema der heutigen Vorlesung ist die Kinetik isolierter und gereinigter Enzyme zum Verständnis ihrer Reaktionsmechanismen.
 1 Enzym-Kinetik (Abb. 1) Das Thema der heutigen Vorlesung ist die Kinetik isolierter und gereinigter Enzyme zum Verständnis ihrer Reaktionsmechanismen. Wie ich schon erwähnte, ist die Geschwindigkeit (V)
1 Enzym-Kinetik (Abb. 1) Das Thema der heutigen Vorlesung ist die Kinetik isolierter und gereinigter Enzyme zum Verständnis ihrer Reaktionsmechanismen. Wie ich schon erwähnte, ist die Geschwindigkeit (V)
Block 3 Vom Molekül zur Zelle Biochemie Seminar & Praktika
 Block 3 Vom Molekül zur Zelle Biochemie Seminar & Praktika Ao. Univ. Prof. Mag. Dr. Georg Weitzer Zentrum für Medizinische Biochemie georg.weitzer@univie.ac.at Medizinische Chemie 1 SEMINAR 2: Auswertung
Block 3 Vom Molekül zur Zelle Biochemie Seminar & Praktika Ao. Univ. Prof. Mag. Dr. Georg Weitzer Zentrum für Medizinische Biochemie georg.weitzer@univie.ac.at Medizinische Chemie 1 SEMINAR 2: Auswertung
Modul 1 Dynamik multidsziplinär
 Dynamik multidisziplinär Diese Lerneinheit befasst sich mit den Grundlagen der Kinetik am Beispiel des enzymatischen Abbaus von Alkohol Zum Verständnis für die Abbaukinetik pseudo-nullter Ordnung! Zur
Dynamik multidisziplinär Diese Lerneinheit befasst sich mit den Grundlagen der Kinetik am Beispiel des enzymatischen Abbaus von Alkohol Zum Verständnis für die Abbaukinetik pseudo-nullter Ordnung! Zur
Enzyme als Biokatalysatoren
 1 Enzymwirkung Enzyme als Biokatalysatoren Versuch: Wasserstoffperoxid wird bei RT mit a) Mn(IV)-oxid und b) Katalase versetzt. Beobachtung: a) Gasentwicklung Glimmspanprobe positiv b) Gasentwicklung Glimmspanprobe
1 Enzymwirkung Enzyme als Biokatalysatoren Versuch: Wasserstoffperoxid wird bei RT mit a) Mn(IV)-oxid und b) Katalase versetzt. Beobachtung: a) Gasentwicklung Glimmspanprobe positiv b) Gasentwicklung Glimmspanprobe
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Einführung. Ablesen von einander zugeordneten Werten
 Einführung Zusammenhänge zwischen Größen wie Temperatur, Geschwindigkeit, Lautstärke, Fahrstrecke, Preis, Einkommen, Steuer etc. werden mit beschrieben. Eine Zuordnung f, die jedem x A genau ein y B zuweist,
Einführung Zusammenhänge zwischen Größen wie Temperatur, Geschwindigkeit, Lautstärke, Fahrstrecke, Preis, Einkommen, Steuer etc. werden mit beschrieben. Eine Zuordnung f, die jedem x A genau ein y B zuweist,
Aufnahme- und Enzymkinetik
 Aufnahme- und Enzymkinetik Kinetik = Verlauf einer Reaktion unter verschiedenen Bedingungen Alle enzym-katalysierten Reaktionen unterliegen Geschwindigkeitsgesetzen Carrier = Enzyme Enzyme sind Biokatalysatoren
Aufnahme- und Enzymkinetik Kinetik = Verlauf einer Reaktion unter verschiedenen Bedingungen Alle enzym-katalysierten Reaktionen unterliegen Geschwindigkeitsgesetzen Carrier = Enzyme Enzyme sind Biokatalysatoren
Versuch 5. Isocitrat-Dehydrogenase
 Versuch 5 Isocitrat-Dehydrogenase Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X PD Dr. Gimpl Einleitung Ziel des Versuches ist es, die Abhängigkeit
Versuch 5 Isocitrat-Dehydrogenase Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X PD Dr. Gimpl Einleitung Ziel des Versuches ist es, die Abhängigkeit
LF - Leitfähigkeit / Überführung
 Verfasser: Matthias Ernst, Tobias Schabel Gruppe: A 11 Betreuer: G. Heusel Datum: 18.11.2005 Aufgabenstellung LF - Leitfähigkeit / Überführung 1) Es sind die Leitfähigkeiten von zwei unbekanten Elektrolyten
Verfasser: Matthias Ernst, Tobias Schabel Gruppe: A 11 Betreuer: G. Heusel Datum: 18.11.2005 Aufgabenstellung LF - Leitfähigkeit / Überführung 1) Es sind die Leitfähigkeiten von zwei unbekanten Elektrolyten
Michaelis-Menten-Gleichung
 Physikalisch-Chemische Praktika Michaelis-Menten-Gleichung Versuch K4 1 Aufgabe Experimentelle Bestimmung der Kinetik der Zersetzung von Harnsto durch Urease. 2 Grundlagen Im Bereich der Biochemie spielen
Physikalisch-Chemische Praktika Michaelis-Menten-Gleichung Versuch K4 1 Aufgabe Experimentelle Bestimmung der Kinetik der Zersetzung von Harnsto durch Urease. 2 Grundlagen Im Bereich der Biochemie spielen
Biochemie-Praktikum Wintersemester 05/06 1. Klausur
 Biochemie-Praktikum Wintersemester 05/06 1. Klausur 01. Welches Verfahren eignet sich am wenigsten zur Trennung von Proteinmolekülen? Ionenaustauschchromatographie Ausschlusschromatographie Papierchromatographie
Biochemie-Praktikum Wintersemester 05/06 1. Klausur 01. Welches Verfahren eignet sich am wenigsten zur Trennung von Proteinmolekülen? Ionenaustauschchromatographie Ausschlusschromatographie Papierchromatographie
Michaelis-Menten-Kinetik
 Michaelis-Menten-Kinetik Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Modellannahmen... 2 2.2 Drei Fälle... 2. Simulationsdiagramm (Typ ), Systemdynamik... 2.4 Dokumentation (Gleichungen, Parameter)...
Michaelis-Menten-Kinetik Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Modellannahmen... 2 2.2 Drei Fälle... 2. Simulationsdiagramm (Typ ), Systemdynamik... 2.4 Dokumentation (Gleichungen, Parameter)...
Enzyme: Grundlegende Konzepte und Kinetik
 Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
Enzyme: Grundlegende Konzepte und Kinetik Enzyme sind Katalysatoren biologischer Systeme Wichtigste Eigenschaften: katalytische Stärke und Spezifität Nahezu alle bekannten Enzyme sind Proteine, es gibt
Inhaltsverzeichnis. 1. Einleitung. 2. Aufgabenstellung. 3. Material, Methoden und Versuchsdurchführung. 4. Ergebnisse. 5.
 Inhaltsverzeichnis 1. Einleitung 1.1. Enzyme 1.2. Enzymaktivität 1.3. Cofaktoren 1.4. Reaktionsgeschwindigkeit 1.5. Enzym-Substrat-Affinität 1.6. Michaelis-Menten 1.7. Lineweaver-Burk 1.8. Enzymhemmung
Inhaltsverzeichnis 1. Einleitung 1.1. Enzyme 1.2. Enzymaktivität 1.3. Cofaktoren 1.4. Reaktionsgeschwindigkeit 1.5. Enzym-Substrat-Affinität 1.6. Michaelis-Menten 1.7. Lineweaver-Burk 1.8. Enzymhemmung
Grundpraktikum Physikalische Chemie. Versuch 16 Kinetischer Salzeffekt
 Grundpraktikum Physikalische Chemie Versuch 16 Kinetischer Salzeffekt Version: März 2016 1. Theorie 1.1. Kinetischer Salzeffekt Eine bimolekulare chemische Reaktion lässt sich mithilfe von Konzepten der
Grundpraktikum Physikalische Chemie Versuch 16 Kinetischer Salzeffekt Version: März 2016 1. Theorie 1.1. Kinetischer Salzeffekt Eine bimolekulare chemische Reaktion lässt sich mithilfe von Konzepten der
Lineare Funktionen. Klasse 8 Aufgabenblatt für Lineare Funktionen Datum: Donnerstag,
 Lineare Funktionen Aufgabe 1: Welche der folgenden Abbildungen stellen eine Funktion dar? Welche Abbildungen stellen eine lineare Funktion dar? Ermittle für die linearen Funktionen eine Funktionsgleichung.
Lineare Funktionen Aufgabe 1: Welche der folgenden Abbildungen stellen eine Funktion dar? Welche Abbildungen stellen eine lineare Funktion dar? Ermittle für die linearen Funktionen eine Funktionsgleichung.
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Versuchsprotokoll: Leitenzyme
 Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Praktikum - Physikalische Chemie I 14. Januar Reaktion 2. Ordnung. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum - Physikalische Chemie I 14. Januar 2016 Reaktion 2. Ordnung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Reaktionsgeschwindigkeit von der Hydrolyse von Essigsäureacetatester
Praktikum - Physikalische Chemie I 14. Januar 2016 Reaktion 2. Ordnung Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Reaktionsgeschwindigkeit von der Hydrolyse von Essigsäureacetatester
Biochemische Labormethoden
 Biochemische Labormethoden, Seite 1 Biochemische Labormethoden Einführung Mit den Versuchen an diesem ersten Praktikumstag sollen Sie wichtige Methoden wiederholen bzw. ergänzen, die Sie bereits im Chemischen
Biochemische Labormethoden, Seite 1 Biochemische Labormethoden Einführung Mit den Versuchen an diesem ersten Praktikumstag sollen Sie wichtige Methoden wiederholen bzw. ergänzen, die Sie bereits im Chemischen
Enzyme. Prof. Dr. Albert Duschl
 Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Enzyme Prof. Dr. Albert Duschl Katalyse Reaktionen laufen normalerweise nicht spontan ab, auch wenn insgesamt dabei Energie gewonnen werden sollte. Es muß zunächst eine Aktivierungsenergie aufgebracht
Enzymatische Katalyse
 VERSUCHSZIEL Die natürliche Braunfärbung einer aufgeschnittenen Kartoffel ist nichts anderes, als die enzymatisch oxydative Umsetzung der darin anwesenden Phenolverbindungen mit Sauerstoff zu Chinonverbindungen.
VERSUCHSZIEL Die natürliche Braunfärbung einer aufgeschnittenen Kartoffel ist nichts anderes, als die enzymatisch oxydative Umsetzung der darin anwesenden Phenolverbindungen mit Sauerstoff zu Chinonverbindungen.
Versuch 5. Kinetik der Kaliumaufnahme durch Getreidewurzeln
 Versuch Kinetik der Kaliumaufnahme durch Getreidewurzeln Till Biskup Matrikelnummer: 67. Juni Aufgaben. Geben Sie die Kaliumkonzentration an, die am Ende der ersten Meßserie im Medium festgestellt wurde.
Versuch Kinetik der Kaliumaufnahme durch Getreidewurzeln Till Biskup Matrikelnummer: 67. Juni Aufgaben. Geben Sie die Kaliumkonzentration an, die am Ende der ersten Meßserie im Medium festgestellt wurde.
Aufgaben zur Enzymatik
 Aufgaben zur Enzymatik Viele dieser Aufgaben wurden in den vergangenen Jahren im Rahmen von Klassenarbeiten und/oder Prüfungen gestellt. 1. Grundlagen 1.1. Die Temperatur wird in einem Enzymversuch mit
Aufgaben zur Enzymatik Viele dieser Aufgaben wurden in den vergangenen Jahren im Rahmen von Klassenarbeiten und/oder Prüfungen gestellt. 1. Grundlagen 1.1. Die Temperatur wird in einem Enzymversuch mit
SOP_018_Glucosebestimmung
 SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
SOP_018_Glucosebestimmung Inhalt Version erstellt am erstellt durch freigegeben durch D Glucosebestimmung in Fermentationsproben 001 11.08.11 Laborpraxis Frank Eiden mittels UV - Test Einsatzgebiet: UV
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Photometrie mit Pyridinnucleotiden
 Photometrie mit Pyridinnucleotiden Grundlagen der Photometrie Photometer-Arten Eppendorf-Photometer Struktur und Funktion des NADH Beispiele des optischen Tests Berechnungsverfahren Biochemie - "Photometrie
Photometrie mit Pyridinnucleotiden Grundlagen der Photometrie Photometer-Arten Eppendorf-Photometer Struktur und Funktion des NADH Beispiele des optischen Tests Berechnungsverfahren Biochemie - "Photometrie
Lineare Funktionen y = m x + n Sekundarstufe I u. II Funktion ist monoton fallend, verläuft vom II. in den IV.
 LINEARE FUNKTIONEN heißt Anstieg oder Steigung heißt y-achsenabschnitt Graphen linearer Funktionen sind stets Geraden Konstante Funktionen Spezialfall Graphen sind waagerechte Geraden (parallel zur x-achse)
LINEARE FUNKTIONEN heißt Anstieg oder Steigung heißt y-achsenabschnitt Graphen linearer Funktionen sind stets Geraden Konstante Funktionen Spezialfall Graphen sind waagerechte Geraden (parallel zur x-achse)
EnzymeLab.
 Das Enzyme Lab ist ein virtuelles Labor in dem enzymatische Reaktionen getestet werden können. Dem Benutzer sollen hier in einfacher Form Prinzipien der Enzymkinetik und die experimentelle Laborarbeit
Das Enzyme Lab ist ein virtuelles Labor in dem enzymatische Reaktionen getestet werden können. Dem Benutzer sollen hier in einfacher Form Prinzipien der Enzymkinetik und die experimentelle Laborarbeit
Versuch: Reaktionskinetik
 Versuch: Reaktionskinetik Befindet sich eine chemische Reaktion im thermodynamischen Gleichgewicht, so lassen sich die Bedingungen für diesen Zustand durch eine energetische Betrachtungsweise mithilfe
Versuch: Reaktionskinetik Befindet sich eine chemische Reaktion im thermodynamischen Gleichgewicht, so lassen sich die Bedingungen für diesen Zustand durch eine energetische Betrachtungsweise mithilfe
2. Theoretischer Hintergrund Enzyme allgemein. 2.2 Aufbau von Enzymen
 Inhaltsverzeichnis 1. Abstract... 2 2. Theoretischer Hintergrund... 3 2.1. Enzyme allgemein... 3 2.2 Aufbau von Enzymen... 3 2.3 Reaktionsgeschwindigkeit... 4 2.4 Enzymkinetik... 4 2.5 Michaelis-Menten-Gleichung...
Inhaltsverzeichnis 1. Abstract... 2 2. Theoretischer Hintergrund... 3 2.1. Enzyme allgemein... 3 2.2 Aufbau von Enzymen... 3 2.3 Reaktionsgeschwindigkeit... 4 2.4 Enzymkinetik... 4 2.5 Michaelis-Menten-Gleichung...
Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung
 Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
Übungsaufgabe 1. Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz
 Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Elektrolytische Leitfähigkeit
 Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
Versuch 6. Leitenzyme
 Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Enzymkinetik. Vorbereitung zum Thema Enzyme, Thermodynamik und Kinetik enzymatischer Reaktionen
 Enzymkinetik Seite 1 Enzymkinetik Einführung In jeder Zelle laufen Hunderte chemischer Reaktionen ab, die (mit wenigen Ausnahmen) alle von hochwirksamen Biokatalysatoren (Enzymen) beschleunigt und gesteuert
Enzymkinetik Seite 1 Enzymkinetik Einführung In jeder Zelle laufen Hunderte chemischer Reaktionen ab, die (mit wenigen Ausnahmen) alle von hochwirksamen Biokatalysatoren (Enzymen) beschleunigt und gesteuert
7 ENZYMKINETIK 7.5 Pre-steady State Kinetik bei schnellen Reaktionen. (t 1 e (k 1[S] 0 +k 2 +k 1. k 1 [S] 0 + k 2 + k 1. t/ms
![7 ENZYMKINETIK 7.5 Pre-steady State Kinetik bei schnellen Reaktionen. (t 1 e (k 1[S] 0 +k 2 +k 1. k 1 [S] 0 + k 2 + k 1. t/ms 7 ENZYMKINETIK 7.5 Pre-steady State Kinetik bei schnellen Reaktionen. (t 1 e (k 1[S] 0 +k 2 +k 1. k 1 [S] 0 + k 2 + k 1. t/ms](/thumbs/97/132715863.jpg) v0(t) [P](t) " & $ " & $ " [P] = v max τ k 2 [S] 0 [E] 0 [S] 0 +(k + k 2 )/k " & " % " $ " # v max " $ & (t e (k [S] 0 +k 2 +k ) )t & # ' ' # " $ & k [S] 0 + k 2 + k t/ms t/ms Bild 5: Allmähliche Annäherung
v0(t) [P](t) " & $ " & $ " [P] = v max τ k 2 [S] 0 [E] 0 [S] 0 +(k + k 2 )/k " & " % " $ " # v max " $ & (t e (k [S] 0 +k 2 +k ) )t & # ' ' # " $ & k [S] 0 + k 2 + k t/ms t/ms Bild 5: Allmähliche Annäherung
1. Ziel des Versuchs. 2. Versuchsaufbau und Durchführung. Dennis Fischer Gruppe 9 Magdalena Boeddinghaus
 Versuch Nr. 7: Lambert-Beersches Gesetz 1. Ziel des Versuchs Ziel des Versuches ist es, die Abhängigkeiten der Absorption eines Stoffes von der Konzentration, der Schichtdicke und der Wellenlänge zu ermitteln.
Versuch Nr. 7: Lambert-Beersches Gesetz 1. Ziel des Versuchs Ziel des Versuches ist es, die Abhängigkeiten der Absorption eines Stoffes von der Konzentration, der Schichtdicke und der Wellenlänge zu ermitteln.
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion:
 Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Versuchsprotokoll Kapitel 6
 Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
Versuchsprotokoll Kapitel 6 Felix, Sebastian, Tobias, Raphael, Joel 1. Semester 21 Inhaltsverzeichnis Einleitung...3 Versuch 6.1...3 Einwaagen und Herstellung der Verdünnungen...3 Photospektrometrisches
1 Michaelis-Menten-Kinetik
 Physikalische Chemie II Lösung 2 9. Dezember 206 Michaelis-Menten-Kinetik. Das Geschwindigkeitsgesetz für die zeitliche Änderung der ES-Konzentration ist durch folgendes Geschwindigkeitsgesetz beschrieben:
Physikalische Chemie II Lösung 2 9. Dezember 206 Michaelis-Menten-Kinetik. Das Geschwindigkeitsgesetz für die zeitliche Änderung der ES-Konzentration ist durch folgendes Geschwindigkeitsgesetz beschrieben:
Säurekonstante des p-nitrophenols
 Säurekonstante des p-nitrophenols Grundlagen Sie bestimmen spektralphotometrisch die Säurekonstante einer schwachen Säure. Voraussetzung dafür ist, dass die undissoziierte Säure in einem anderen Spektralbereich
Säurekonstante des p-nitrophenols Grundlagen Sie bestimmen spektralphotometrisch die Säurekonstante einer schwachen Säure. Voraussetzung dafür ist, dass die undissoziierte Säure in einem anderen Spektralbereich
(a) Lösen Sie die Differentialgleichung unter Verwendung der Mathematica-Funktion DSolve.
 Institut für Physikalische Chemie Methodenkurs Anwendungen von Mathematica und Matlab in der Physikalischen Chemie im WS 205/206 Prof Dr Stefan Weber, Dr Till Biskup Aufgabenblatt zum Teil (Mathematica)
Institut für Physikalische Chemie Methodenkurs Anwendungen von Mathematica und Matlab in der Physikalischen Chemie im WS 205/206 Prof Dr Stefan Weber, Dr Till Biskup Aufgabenblatt zum Teil (Mathematica)
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2
 Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 10. Temperaturabhängigkeit der Reaktionsgeschwindigkeit: Arrhenius-Beziehung Thema In diesem Versuch
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 10. Temperaturabhängigkeit der Reaktionsgeschwindigkeit: Arrhenius-Beziehung Thema In diesem Versuch
Fragen zum Versuch Kinetik:
 Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
Zuordnungen. 2 x g: y = x + 2 h: y = x 1 4
 Zuordnungen Bei Zuordnungen wird jedem vorgegebenen Wert aus einem Bereich ein Wert aus einem anderen Bereich zugeordnet. Zuordnungen können z.b. durch Wertetabellen, Diagramme oder Rechenvorschriften
Zuordnungen Bei Zuordnungen wird jedem vorgegebenen Wert aus einem Bereich ein Wert aus einem anderen Bereich zugeordnet. Zuordnungen können z.b. durch Wertetabellen, Diagramme oder Rechenvorschriften
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
Versuch 412: Photometrische Bestimmung von Phosphatspuren als "Phosphormolybdänblau"
 Instrumentelle Bestimmungsverfahren 131 Versuch 412: Photometrische Bestimmung von Phosphatspuren als "Phosphormolybdänblau" Phosphationen reagieren mit Molybdat MoO 4 in saurer Lösung zur 2 gelben Dodekamolybdatophosphorsäure
Instrumentelle Bestimmungsverfahren 131 Versuch 412: Photometrische Bestimmung von Phosphatspuren als "Phosphormolybdänblau" Phosphationen reagieren mit Molybdat MoO 4 in saurer Lösung zur 2 gelben Dodekamolybdatophosphorsäure
Biochemisches Praktikum 1 ENZYMKINETIK Praktischer Teil
 Biochemisches Praktikum 1 ENZYMKINETIK Praktischer Teil Sicherheitshinweise Enzymkinetik Sicherheitshinweise und Entsorgungsrichtlinien: Alkohol Dehydrogenase, ADH: o Na-Pyrophosphat (Bestandteil des ADH-Puffers)
Biochemisches Praktikum 1 ENZYMKINETIK Praktischer Teil Sicherheitshinweise Enzymkinetik Sicherheitshinweise und Entsorgungsrichtlinien: Alkohol Dehydrogenase, ADH: o Na-Pyrophosphat (Bestandteil des ADH-Puffers)
Physikalische Chemie. LD Handblätter Chemie. Bestimmung der Reaktionsordnung. Malachitgrün mit Natronlauge C4.1.2.2
 SW-2014-06 Physikalische Chemie Reaktionskinetik Reaktionsordnungen LD Handblätter Chemie Bestimmung der Reaktionsordnung der Reaktion von Malachitgrün mit Natronlauge Versuchsziele Den Reaktionsverlauf
SW-2014-06 Physikalische Chemie Reaktionskinetik Reaktionsordnungen LD Handblätter Chemie Bestimmung der Reaktionsordnung der Reaktion von Malachitgrün mit Natronlauge Versuchsziele Den Reaktionsverlauf
Standardabweichung und Variationskoeffizient. Themen. Prinzip. Material TEAS Qualitätskontrolle, Standardabweichung, Variationskoeffizient.
 Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Standardabweichung und TEAS Themen Qualitätskontrolle, Standardabweichung,. Prinzip Die Standardabweichung gibt an, wie hoch die Streuung der Messwerte um den eigenen Mittelwert ist. Sie ist eine statistische
Was ist eine Funktion?
 Lerndomino zum Thema Funktionsbegriff Kopiereen Sie die Seite (damit Sie einen Kontrollbogen haben), schneiden Sie aus der Kopie die "Dominosteine" zeilenweise aus, mischen Sie die "Dominosteine" und verteilen
Lerndomino zum Thema Funktionsbegriff Kopiereen Sie die Seite (damit Sie einen Kontrollbogen haben), schneiden Sie aus der Kopie die "Dominosteine" zeilenweise aus, mischen Sie die "Dominosteine" und verteilen
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL. WiSe 2015/2016. Versuch 6. Adiabatischer Batch-Reaktor
 PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 6 Adiabatischer Batch-Reaktor Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Es wurde der Temperaturverlauf
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 6 Adiabatischer Batch-Reaktor Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Es wurde der Temperaturverlauf
Praktikum Stoffwechselphysiologie
 Praktikum Stoffwechselphysiologie WS 2011/2012 Versuch Gruppe XY Betreuer: Praktikanten: Versuchstag: 1 Inhaltsverzeichnis 1. Einleitung... 3 2. Theorie... 3 2.1 Enzyme... 3 2.1.1 Definition... 3 2.1.2
Praktikum Stoffwechselphysiologie WS 2011/2012 Versuch Gruppe XY Betreuer: Praktikanten: Versuchstag: 1 Inhaltsverzeichnis 1. Einleitung... 3 2. Theorie... 3 2.1 Enzyme... 3 2.1.1 Definition... 3 2.1.2
Universität Ulm Tierphysiologisches Anfängerpraktikum Stoffwechselphysiologie Enzymkinetik
 Universität Ulm Tierphysiologisches Anfängerpraktikum Stoffwechselphysiologie Enzymkinetik Gruppe Name Name Name Datum Inhaltsverzeichnis 1. Theorie.3 1.1. Allgemeines zu Enzymen.3 Enzyme als Biokatalysatoren...3
Universität Ulm Tierphysiologisches Anfängerpraktikum Stoffwechselphysiologie Enzymkinetik Gruppe Name Name Name Datum Inhaltsverzeichnis 1. Theorie.3 1.1. Allgemeines zu Enzymen.3 Enzyme als Biokatalysatoren...3
Aufgabensammlung zum Üben Blatt 1
 Aufgabensammlung zum Üben Blatt 1 Seite 1 Lineare Funktionen ohne Parameter: 1. Die Gerade g ist durch die Punkte A ( 3 4 ) und B( 2 1 ) festgelegt, die Gerade h durch die Punkte C ( 5 3 ) und D ( -2-2
Aufgabensammlung zum Üben Blatt 1 Seite 1 Lineare Funktionen ohne Parameter: 1. Die Gerade g ist durch die Punkte A ( 3 4 ) und B( 2 1 ) festgelegt, die Gerade h durch die Punkte C ( 5 3 ) und D ( -2-2
NAD+/NADH ADH CH 3 CH 2 OH + NAD + CH 3 CHO + NADH + H + Hier unterscheiden sich Ethanol und NAD + in der Tat funktionell nicht.
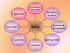 NAD+/NADH NAD + (Nicotinamid-adenin-dinukleotid) ist das häufigste "Coenzym" enzymatischer Redox-reaktionen. Von den Lehrbüchern wird es teils als Coenzym, teils als Cosubstrat eingeordnet. Das erstere
NAD+/NADH NAD + (Nicotinamid-adenin-dinukleotid) ist das häufigste "Coenzym" enzymatischer Redox-reaktionen. Von den Lehrbüchern wird es teils als Coenzym, teils als Cosubstrat eingeordnet. Das erstere
Fachbereich Mathematik und Informatik Wintersemester 2013/14 der Universität Marburg Dr. Helga Lohöfer
 Fachbereich Mathematik und nformatik Wintersemester 23/4 der Universität Marburg Dr. Helga Lohöfer Grundlagen der Mathematik für Biologen - Blatt - Abgabe: Montag, den 2..23, vor der Vorlesung, spätestens4:5
Fachbereich Mathematik und nformatik Wintersemester 23/4 der Universität Marburg Dr. Helga Lohöfer Grundlagen der Mathematik für Biologen - Blatt - Abgabe: Montag, den 2..23, vor der Vorlesung, spätestens4:5
Wachstum von Escherichia coli mit Glucose oder Acetat
 Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 22.1.2005 Wachstum von Escherichia
Johannes Gutenberg-Universität Mainz Institut für Mikrobiologie und Weinforschung FI-Übung: Identifizierung, Wachstum und Regulation (WS 2004/05) Sebastian Lux Datum: 22.1.2005 Wachstum von Escherichia
Gegenstand der letzten Vorlesung
 Gegenstand der letzten Vorlesung Reaktionsgeschwindigkeit Reaktionsordnung Molekularität Reaktion 0., 1.,. Ordnung Reaktion pseudo-erster Ordnung Aktivierungsenergie Temperaturabhängigkeit der Geschwindigkeitskonstanten
Gegenstand der letzten Vorlesung Reaktionsgeschwindigkeit Reaktionsordnung Molekularität Reaktion 0., 1.,. Ordnung Reaktion pseudo-erster Ordnung Aktivierungsenergie Temperaturabhängigkeit der Geschwindigkeitskonstanten
Biochemisches Grundpraktikum
 Institut für Biowissenschaften Lehrstuhl Biochemie Biochemisches Grundpraktikum SS 2017 Laborordnung 2 Erste Hilfe 3 Versuchsvorbereitung und Protokoll 4 Teil 1: Photometrie 5 Quantitative Proteinbestimmung
Institut für Biowissenschaften Lehrstuhl Biochemie Biochemisches Grundpraktikum SS 2017 Laborordnung 2 Erste Hilfe 3 Versuchsvorbereitung und Protokoll 4 Teil 1: Photometrie 5 Quantitative Proteinbestimmung
4.1. Eigenschaften von Enzymen
 4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
 Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
