Aus Strahlenklinik der Friedrich-Alexander-Universität Erlangen-Nürnberg Direktor: Prof. Dr. med. Rainer Fietkau
|
|
|
- Gitta Fiedler
- vor 7 Jahren
- Abrufe
Transkript
1 Aus Strahlenklinik der Friedrich-Alexander-Universität Erlangen-Nürnberg Direktor: Prof. Dr. med. Rainer Fietkau Adenokarzinome mit Lokalisation am gastroösophagealen Übergang: Lymphatisches Metastasierungsmuster als Grundlage für die Definition des Planungszielvolumens bei neoadjuvanter Radiochemotherapie Inaugural-Dissertation zur Erlangung der Doktorwürde der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg vorgelegt von Iris Meier aus Byunjang-Myun, Südkorea
2 2 Gedruckt mit Erlaubnis der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg Dekan: Prof. Dr. med. Dr. h.c. J. Schüttler Referent: PD Dr. med. T. Brunner Koreferent: Prof. Dr. med. S. Merkel Tag der mündlichen Prüfung: 21. Juli 2010
3 3 Inhaltsverzeichnis Inhaltsverzeichnis 3 Zusammenfassung 5 Summary 7 1. Einleitung Anatomie der Speiseröhre und des Magens Klassifikation und Stadieneinteilung von Magen- und 10 Ösophaguskarzinomen 1.3. Tumorstaging Staging mit Computertomographie Staging mit EUS Staging mit PET Klassifikation von AEG-Tumoren Metastasierungsmuster bei AEG-Tumoren Therapie Chirurgische Therapie Adjuvante und neoadjuvante Therapie Adjuvante Therapie Neoadjuvante Therapie Ziele der Studie Material und Methoden Datenerhebung und Patientenzahl Einschlusskriterien Ausschlusskriterien Dissezierte Lymphknotenstationen Statistische Methoden Klassifikation von AEG-Tumoren Planung der 3-dimensionalen Strahlentherapie 26
4 4 3. Ergebnisse Lymphknotenmetastasierungsmuster Allgemeine Verteilung der Lymphknotenmetastasen Spezifische regionale Verteilung der 30 Lymphknotenmetastasen Verteilung der Lymphknotenmetastasen nach 32 Tumorcharakteristik Lymphknotenbefall in mediastinalen und distalen Gebieten Lymphknotenbefall bei den jeweiligen AEG- 36 Tumortypen Mediastinaler Lymphknotenbefall bei AEG-Tumoren, 37 die die Z-Linie überschreiten Lymphknotenbefall distaler Gebiete mit hoher 38 Bedeutung für die Größe des Planungszielvolumens 3.2. Vorschlag für das PTV Pulmonale Strahlenbelastung bei erweiterten PTV Diskussion Schlusswort Literaturverzeichnis Abkürzungsverzeichnis Danksagung Lebenslauf Erklärung der eigenständigen Arbeit 67
5 5 Zusammenfassung Ziel der Studie Regionale Lymphknotenmetastasen bei Adenokarzinomen am ösophagogastrealen Übergang (AEG) sind ein prognostischer Faktor nach einer neoadjuvanten Radiochemotherapie. Ziel dieser Arbeit ist es, die Verteilung von Lymphknotenmetastasen bei AEG-Tumoren unter Berücksichtigung der Tumorlokalisation und des Tumorwachstums in Nachbarregionen zu identifizieren, um adäquate Grenzen für das Bestrahlungs-Planungszielvolumen erstellen zu können. Methodik Bei 326 Patienten mit AEG Tumoren wurde das Metastasierungsmuster von regionalen Lymphknoten anhand von Pathologiebefunden analysiert. Bei den Betroffenen wurde eine radikale Tumorresektion ohne vorausgegangene Therapie durchgeführt. Hierbei wurden mindestens 15 Lymphknoten untersucht. Basierend auf Endoskopie- und Pathologiebefunden wurden die Tumoren in drei AEG-Typen (I-III) klassifiziert. Mit Hilfe des Fisher`s Exact Tests wurden die Lymphknotenmetastasen und die Tumorcharakteristika verglichen. Ergebnisse Bei T2- bis T4-Tumoren waren 81 % der Lymphknoten positiv. AEG-Typ, Tumorgröße, Lymphgefäßeinbrüche und Grading haben einen deutlichen Einfluss auf die Verteilung von Lymphknotenmetastasen. Wir stellten folgende signifikante Korrelationen fest: Eine Tumorinvasion proximal der Z- Linie in den distalen Ösophagus korrelierte bei AEG II/III-Tumoren mit paraösophagealen Lymphknotenmetastasen und das Vorliegen eines
6 6 Tumorstadiums T3- und T4-Tumoren der AEG-Typen II/III korrelierte mit Lymphknotenmetastasen im Bereich der A. splenica und des Milzhilus. Für die Bestrahlungsplanung sollten bei allen AEG I-Tumoren, bei AEG II- Tumoren mit 15 mm Beteiligung oberhalb der Z-Linie im T2- bis T4- Stadium und bei AEG II-Tumoren im T3/T4-Stadium die mittleren und unteren paraösophagealen Lymphknoten mit in das PTV eingeschlossen werden. Andererseits können Lymphknoten im Bereich der A. splenica und des Milzhilus bei T2 AEG-Tumoren, insbesondere bei AEG-Typ I-Tumoren, bei der Therapie ausgespart werden. Das Risiko von postoperativen pulmonalen Komplikationen durch die Behandlung von paraösophagealen Lymphknoten kann anhand eines Dosis-Volumen-Histogramms abgeschätzt werden. Schlussfolgerung Durch ein sorgfältiges prätherapeutisches Staging des Primärtumors kann das Risiko für subklinische Lymphknotenmetastasen prognostiziert werden. Es sollte für die Wahl eines adäquaten radiotherapeutischen Planungszielvolumens herangezogen werden. Die sorgfältig bedachte Wahl des Planungszielvolumens trägt dazu bei, das therapeutische Fenster bei der multimodalen Therapie bei AEG-Tumoren zu maximieren.
7 7 Summary Aim of the study Regional nodal metastasis after neoadjuvant chemoradiation (ypn) of adenocarcinoma of the esophagogastric junction (AEG) has a high impact on the odds of the survival of patients. It is the aim of this study to clarify the lymph node distribution of AEG according to location of the tumor mass and invasion of neighboring areas for the selection of radiotherapy planning target volume (PTV) margins. Methods Patterns of regional spread were analyzed in pathologic reports of 326 primary resected patients with AEG with 15 lymph nodes examined. Tumors were classified into three AEG types (I, II and III) based on endoscopic and pathologic reports. Fisher s exact test was used to compare nodal disease and tumor characteristics. Results Nodes were positive in 81% of T2-4 tumors. AEG type, tumor size, lymphovascular invasion and grading significantly influenced nodal distribution. We assessed the following significant correlations: Marked esophageal invasion of AEG II/III significantly correlates with paraesophageal nodal disease and T3-4 AEG II/III has a significant rate of splenic hilum/artery nodes. For radiotherapy planning the following nodes should be included into the planning target volume (PTV): Middle and lower paraesophageal nodes should be treated in T2-4 AEG I and AEG II with 15 mm involvement above the Z-line, and T3-4 AEG II. The splenic hilum and artery nodes on the other
8 8 hand can be spared in T2 AEG tumors, especially type I tumors. The influence of paraesophageal nodal treatment on the risk of postoperative pulmonary complications can be estimated from dose-volume-histograms. Conclusions Accurate pretherapeutic staging predicts the risk of subclinical nodal disease and should be used to select the appropriate radiotherapeutic planning target volume (PTV). Careful selection of the PTV can be used to maximize the therapeutic window in multimodal therapy for AEG.
9 9 1. Einleitung Die Inzidenz von hoch malignen Adenokarzinomen am ösophagogastrealen Übergang (Adenocarcinoma of the esophagogastric junction = AEG) und am unteren Ösophagus ist in den letzen 40 Jahren dramatisch gestiegen [12; 5]. Jährlich nimmt die Zahl an Neuerkrankungen in den westlichen Ländern um 5-10 % zu [12]. Die AEG-Tumoren werden in drei Gruppen eingeteilt gemäß den Empfehlungen der International Society for Diseases of the Esophagus (ISDE) und der International Gastric Cancer Association (IGCA). Diese Klassifikation wurde von Siewert und Kollegen 1987 eingeführt [47; 49]. Nachdem eine international akzeptierte Klassifikation existiert, ist ein Vergleich von Mortalität, Überleben und verschiedener Therapiemöglichkeiten möglich, und infolgedessen ist die Planung einer multimodalen Therapie so viel einfacher [47]. Die Therapie von AEG- Tumoren ist eine therapeutische Herausforderung, da die Prognose für diese Tumoren nach wie vor schlecht ist. Sogar schon bei kleinen Tumoren (T1 und T2) mit Lymphknotenbefall beträgt die 5-Jahres-Überlebensrate maximal 30 %. Lokal fortgeschrittene Tumoren (T3 und T4) sind beinahe immer mit einem Lymphknotenbefall assoziiert. Die 5-Jahres Überlebensrate bei diesen Patienten ist normalerweise unter 15% [14] Anatomie der Speiseröhre und des Magens Der Ösophagus ist ein cm langer Muskelschlauch, der aus dem Pharynx hervorgeht und an der Kardia endet. Der Ösophagus lässt sich in eine Pars cervicalis, thoracica und abdominalis einteilen [57]. Die Pars cervicalis beginnt in Höhe des Ringknorpels mit dem Ösophagusmund, der in etwa 15 cm von der oberen Zahnreihe entfernt liegt [46], und endet nach ca. 8 cm am oberen Sternumrand, 23 cm aboral. Die Pars thoracica ist etwa 16 cm lang und reicht bis zum Zwerchfell, 39 cm aboral. Der abdominale Teil beginnt unterhalb des Zwerchfells bis zum unteren Ösophagussphinkter und variiert zwischen 0 bis 3 cm je nach Magenfüllung [41; 57]. Der Magenmund,
10 10 die Kardia, liegt also bei 39 bis 42 cm entfernt von der oberen Zahnreihe. Der Ösophagus, der sich aboral über 15 bis 42 cm erstreckt, ist mit Plattenepithel ausgekleidet und geht an der Ora serrata, auch Z-Linie genannt, in das Zylinderepithel der Kardia über. Die Z-Linie liegt 2-3 cm oberhalb der Kardia [4]. Der Magen teilt sich auf in die Pars cardiaca mit dem Magenmund, den Fundus gastricus (ventriculi), Corpus gastricum (ventriculi) und die Pars pylorica mit dem Antrum pyloricum, dem Canalis pyloricus und dem Pylorus [46; 57] Klassifikation und Stadieneinteilung von Magen- und Ösophaguskarzinomen Das T- und N-Stadium der AEG-Ca ist ein entscheidender Faktor für die Überlebensprognose [14, 20], und muss somit bei jedem Patienten ermittelt werden. Die Stadieneinteilung von Ösophagus- und Magen-Ca nach der TNM-Klassifikation und der Stadiengruppierung (UICC 2002) erfolgt wie in Tabelle 1 und 2 dargestellt. Sie kann klinisch (TNM), pathologisch (p-tnm) sowie während oder nach einer multimodalen Therapie (yp-tnm) ermittelt werden. Für AEG-Tumoren existiert keine eigene Klassifikation. Sie werden zu den Magenkarzinomen gezählt, genauer gesagt zu denen der Kardia [63].
11 11 Mit der T-Kategorie wird die Ausdehnung bzw. Endringtiefe des Primärtumors, mit der N-Kategorie das Fehlen, das Vorhandensein und die Ausbreitung von Lymphknotenmetastasen und mit der M-Kategorie das Fehlen oder Vorhandensein von Fernmetastasen klassifiziert [63]. T-Primärtumor Ösophagus Magen TX Primärtumor kann nicht beurteilt werden Primärtumor kann nicht beurteilt werden T0 Kein Anhalt für Primärtumor Kein Anhalt für Primärtumor Tis Carcinoma in situ Carcinoma in situ T1 Tumor infiltriert Lamina propria oder Submucosa Tumor infiltriert Lamina propria oder submucosa T2 Tumor infiltriert Muscularis propria Tumor infiltriert Muscularis propria oder Subserosa T3 Tumor infiltriert Adventitia Tumor penetriert Serosa T4 Tumor infiltriert Nachbarstrukturen Tumor infiltriert Nachbarstrukturen N-Regionäre Ösophagus Magen Lymphknoten NX Regionäre Lymphknoten nicht beurteilbar Regionäre Lymphknoten nicht beurteilbar N0 Keine legionary Lymphknotenmetastasen Keine regionären Lymphknotenmetastasen N1 Regionäre Lymphknotenmetastasen Metastasen in 1-6 regionären Lymphknoten N Metastasen in 7-15 regionären Lymphknoten N Metastasen in >15 regionären Lymphknoten M- Ösophagus Magen Fernmetastasen MX Vorhandensein von Fernmetastasen nicht beurteilbar Vorhandensein von Fernmetastasen nicht beurteilbar M0 Keine Fernmetastasen Keine Fernmetastasen M1 Fernmetastasen Fernmetastasen Tabelle 1: TNM-Klassifikation für Ösophagus- und Magenkarzinome nach UICC 2002
12 12 Durch die UICC-Stadiengruppierung kann die TNM-Klassifikation in verschiedene Stadien eingeteilt werden [63]. Stadiengruppierung Ösophagus Magen Stadium 0 Tis, N0, M0 Tis, N0, M0 Stadium I T1, N0, M Stadium IA T1, N0, M0 Stadium IB T1, N1, M0 T2, N0, M0 Stadium II T1, N2, M0 T2, N1, M0 T3, N0, M0 Stadium IIA T2, N0, M T3, N0, M0 Stadium IIB T1, N1, M T2, N1, M0 Stadium III T3, N1, M Stadium IIIA T2, N2, M0 T3, N1, M0 T4, N0, M0 Stadium IIIB T3, N2, M0 Stadium IV Jedes T, jedes N, M1 T4, N1, M0 T4, N2, M0 T4, N3, M0 Jedes T, N3, M0 jedes T, jedes N, M1 Tabelle 2: UICC-Stadiengruppierung des Ösophagus- und Magen-Ca 2002 Nach einer Histopathologischen Untersuchung des Tumors postoperativ bzw. nach einer endoskopischen Biopsie kann mit Hilfe des Gradings (G) eine Aussage über den Differenzierungsgrad getroffen werden, der eine wichtige Rolle spielt. - G1: gut differenziert - G2: mäßig differenziert - G3: schlecht differenziert - G4: undifferenziert
13 Tumorstaging Informationen über den Lymphknotenstatus der einzelnen Patienten vor einer neoadjuvanten Therapie werden typischer Weise durch die prätherapeutische Bildgebung erhalten, die Genauigkeit dieser ist jedoch begrenzt [43] Staging mit Computertomographie Die gebräuchlichste Methode für das Tumorstaging ist die Computertomographie, welche als Grundlage für die Radiotherapieplanung dient. Mit Hilfe der Computertomographie können der Primärtumor einschließlich Ausbreitung in Nachbarstrukturen, regionale LK-Metastasen und Fernlymphknoten lokalisiert werden. Die Genauigkeit bezüglich des Lymphknotenbefalles ist beim CT-Scanning allerdings niedrig. Das Problem ist, dass durch Metastasen befallene Lymphknoten kaum größer sind als nicht metastasierte (6,7 mm versus 5 mm) und dass nur 12 % von allen befallenen Lymphknoten überhaupt größer sind als 1 cm [43; 52]. Die Computertomographie kann T1-, T2 und T3-Tumoren nicht eindeutig voneinander unterscheiden und damit ist auch eine adäquate Aussage über die Eindringtiefe des Tumors nicht möglich [34; 45] Staging mit EUS Die Endoskopische Ultrasonographie (EUS) ist derzeit das beste bildgebende Verfahren für das Staging von Ösophaguskarzinomen. Zur Bestimmung der Tumorinfiltrationstiefe (T-Kategorie) ist die Endoskopische Ultrasonographie (EUS) derzeit die Methode der Wahl [19; 27; 64]. Die EUS zeigt bei der Bestimmung des T-Stadiums eine Genauigkeit von % und bei der Diagnostik regionalen Lymphknotenmetastasen eine Genauigkeit von % [19; 34; 64] und ist somit bei beiden Parametern der Computertomographie überlegen. Für die Diagnostik von Fernmetastasen ist
14 14 die Computertomographie oder Positronen-Emissions-Tomographie besser geeignet [34; 43; 64]. Beim Staging von AEG-Tumoren ist die Genauigkeit der EUS allerdings aufgrund der anatomischen Verhältnisse am gastroösophagealen Übergang und der größeren Entfernung der abdominellen lymphatischen Metastasen von der Sonde beeinträchtigt Staging mit PET Mit der Positronen-Emissions-Tomographie (PET) können Stoffwechselvorgänge untersucht werden. Bei fast allen malignen Tumoren ist der Glucosemetabolismus erhöht, und kann mit Hilfe von F-18- Fluorodeoxy-glucose (FDG) nachgewiesen werden [21]. In vergangenen Studien wurde beim Staging mit FDG-PET beim Ösophaguskarzinom eine Spezifität von 71-84% aber nur eine Sensitivität von % des regionalen Lymphknotenbefalles ermittelt [21; 42]. Mit FDG-PET ist zwar die Diagnostik des Primärtumors möglich [42], zur Bestimmung des T-Stadiums ist sie ungeeignet [21]. Bei der Identifikation von Fernmetastasen ist die FDG-PET der CT oder auch der Kombination aus CT und EUS überlegen [21; 34; 42].
15 Klassifikation von AEG-Tumoren Die Tumoren am gastroösophagealen Übergang (AEG) werden nach Siewert in drei Typen klassifiziert [47; 48; 49] nach den Empfehlungen der ISDE und der IGCA. Abbildung 1: Klassifikation von AEG-Tumoren [25] 1. AEG-Typ I: distales Ösophagus-Ca bis zu 5 cm oberhalb der Z-Linie 2. AEG-Typ II: echtes Kardia-Ca 3. AEG-Typ III: subkardiales Funduskarzinom bis zu 5 cm unterhalb der Z-Linie Die AEG-Tumoren werden anhand der anatomischen Lage der Tumorhauptmasse definiert und liegen bis zu 5 cm vom gastroösophagealen Übergang entfernt.
16 Metastasierungsmuster bei AEG-Tumoren In vorausgegangenen Studien wurde über einen Lymphknotenbefall in 45 %, 85 % und 100% der Fälle bei T2-, T3- und T4-Tumoren des gastroösphagealen Übergangs nach direkter Lymphknotendissektion berichtet [13] und die prognostische Bedeutung bereits von Mikrometastasen [22]. Ähnlich wie bei Plattenepithel-Ca des Ösophagus [3] ist das Lymphknotenmetastasierungsmuster bei AEG-Tumoren durch eine Tendenz, sich im Wesentlichen in cranio-caudale Richtung auszubreiten charakterisiert und außerdem scheint sie vom AEG-Typ abzuhängen [13]. Zudem zeigte ein aktueller Bericht, dass die Zahl der Lymphknotenmetastasen nach Radiochemotherapie (ypn-status) von prognostischer Bedeutung ist [20] Therapie Chirurgische Therapie Für die chirurgische Resektion von AEG-Tumoren gibt es eine ganze Reihe von verschiedenen Operationsmethoden [37; 39; 44] - abdominothorakale en bloc Ösophagogastrektomie - transhiatale subtotale Ösophagektomie mit Resektion des proximalen Magens - transthorakale en bloc Ösophagektomie mit Resektion des proximalen Magens - totale Gastrektomie mit transhiataler Resektion von dem distalenösophagus - limitierte Resektion des ösophagogastrealen Überganges
17 17 Die geläufigsten Techniken sind beim AEG-Typ I eine transhiatale subtotale Ösophagektomie bzw. transthorakale mit Resektion des proximalen Magens und bei AEG-Typ II/III eine totale Gastrektomie mit transhiataler Resektion des distalen Ösophagus. Die komplette Ösophagogastrektomie sollte heute nicht mehr durchgeführt werden [37; 39; 44] Grundsätzlich ist zu sagen, dass für AEG-Tumoren, die kurativ behandelt werden können, die Behandlung der Wahl die komplette Resektion ist. Es treten jedoch zwei Hauptprobleme auf, wenn der therapeutische Ansatz ausschließlich auf einer chirurgischen Intervention basiert: 1. R0-Resektionen sind bei lokal fortgeschrittener Erkrankung schwierig zu erreichen, insbesondere wenn das Zwerchfell und retroperitoneale Strukturen betroffen sind [39]. 2. Die Rezidivrate lokoregionär und im Bereich der Anastomose liegt nach einer chirurgischen Therapie zwischen 20 % und 40 % [3; 33]. Eine einheitliche Empfehlung für das Ausmaß der Lymphadenektomie gibt es nicht. Eine systematische Lymphknotendissektion wird kontrovers diskutiert, da diese mit einer erhöhten Letalitäts- und Morbiditätsrate einhergeht. In der Vergangenheit wurde in Japan, aber auch in westlichen Ländern eine systematische 2-Feld-Lymphadenektomie mit mediastinaler und abdomineller Lymphadenektomie im Rahmen einer Ösophagektomie bei AEG-Tumoren Typ I und einer D2-Lymphknotendissektion im Rahmen einer Gastrektomie bei AEG-Typ II/III-Tumoren durchgeführt, die derzeit favorisiert wird [17; 33; 37; 53]. Die D2-Lymphadenektomien wurden nach der Japanese Gastric Cancer Association (JGCA) durchgeführt, indem an - N1-Stationen (rechts und links parakardial, kleine Kurvatur, perigastrischen Lymphknoten)
18 18 - N2-Stationen (A. gastrica sinistra, A. hepatica communis, Truncus coeliacus, A. lienalis, Milzhilus) Lymphknoten disseziert wurden [13; 26] Adjuvante und neoadjuvante Therapie Weitere Behandlungsoptionen bei der multimodalen Therapie von Tumoren sind die postoperative adjuvante und die präoperative neoadjuvante Therapie mit Strahlentherapie, Chemotherapie und einer Kombination aus Strahlentherapie und Chemotherapie. Zu Beginn einer Radiotherapie wird nach Tumordiagnostik und Staging zunächst das klinische Zielvolumen geplant. Das klinische Zielvolumen (CTV) umfasst das Tumorvolumen und einen Sicherheitssaum für mikroskopische Tumorausläufer. In der postoperativen Situation wird das ehemalige Tumorbett behandelt, ermittelt an präoperativer Bildgebung, dem Operationsbericht und dem pathohistologischen Bericht. Die Zielvolumina lassen sich in I., II. und III Ordnung unterteilen [28]: - I. Ordnung: Primärtumor mit Sicherheitssaum - II. Ordnung: benachbarte regionäre Lymphknoten mit Sicherheitssaum - III. Ordnung: juxtaregionäre Lymphknoten (N3 nach TNM- Klassifikation) oder Körperhöhlen Um das so genannte Planungszielvolumen (PTV) zu erhalten, wird zu dem klinischen Zielvolumen noch ein Sicherheitssaum für die Veränderungen (z.b. Organverschiebungen, Verschiebungen infolge nicht reproduzierbarer Patientenlagerung), dazu addiert [28]. Die Radiotherapie des Ösophaguskarzinoms kann heute unter anderem mit zwei- bzw. dreidimensionaler konformaler (2 bzw. 3D) Radiotherapie oder mit einem
19 19 relativen neuen Verfahren der intensitätsmodulierten Radiotherapie (IMRT) durchgeführt werden [9]. Oft wird die Radiotherapie durch eine Chemotherapie ergänzt Adjuvante Therapie Das Ziel einer postoperativen adjuvanten Radio- und Chemotherapie ist es, das Rezidivrisiko nach einer kurativen Resektion zu senken, und damit eine Lebensverlängerung zu erreichen. Nachdem die Rezidivrate von AEG- Tumoren zwischen % liegt [3; 33], sollte man meinen, dass die postoperative Radiotherapie bzw. Chemotherapie einen besonderen Stellenwert einnimmt. Dies wird allerdings kontrovers diskutiert, da die postoperative Therapie eine große Belastung für den durch die Operation schon geschwächten Patienten darstellt, so dass diese oft schlecht toleriert wird. Adjuvante Chemotherapie: Die adjuvante Chemotherapie wird nicht nur schlecht vertragen, sondern konnte auch keine Überlebensverlängerung bei AEG Tumoren und Magen-Ca in mehreren randomisierten Studien demonstrieren [11; 17; 29; 35]. Auch in der von Hermans veröffentlichten Metaanalyse konnte keine signifikante Überlegenheit der adjuvanten Chemotherapie gezeigt werden [23]. Adjuvante Radio- und Radiochemotherapie: Im Gegensatz dazu konnte in einer kleinen Studie (n=62) ein positiver Effekt auf das Überleben nach postoperativer Radiotherapie mit und ohne Fluorouracil gezeigt werden [17; 35; 40]. In den Vereinigten Staaten wird die postoperative Radiochemotherapie trotz hoher Toxizität bei AEG-Tumoren favorisiert, basierend auf einer Publikation der Southwest Oncology Group Intergroup study (SWOG 9008/INT-0116) [35]. Es wurden 556 Patienten mit AEG- und Magentumoren über einen Zeitraum von etwa sieben Jahren (8/91 bis 7/98) untersucht. Bei dieser großen randomisierten Untersuchung konnte interessanterweise eine höhere Gesamtüberlebenszeit und ein höheres krankheitsfreies Intervall bei
20 20 postoperativer Chemoradiotherapie mit Fluorouracil und Leucovorin als bei alleiniger chirurgischer Intervention aufgezeigt werden (52 % vs. 41% und 48% vs. 31%) [11; 17; 35] Neoadjuvante Therapie Die R0-Resektion ist für das Überleben der AEG-Tumoren ein entscheidender Faktor, welche theoretisch mit einer präoperativen Therapie erreicht werden könnte. Mit Hilfe der neoadjuvanten Therapie soll nicht nur die Wahrscheinlichkeit einer kurativen Resezierbarkeit gesteigert werden können, sondern auch die frühzeitige Behandlung von Mikrometastasen ermöglicht werden. Aufgrund dessen ist ein neoadjuvantes Behandlungsregime bei auch noch besserer Verträglichkeit einem adjuvanten möglicherweise überlegen [17; 18; 55]. Jedoch ist die neoadjuvante Therapie nach wie vor umstritten, da sich in vergangenen Untersuchungen eine Steigerung der perioperativen Mortalität und Morbidität gezeigt haben [17; 55]. Neoadjuvante Chemotherapie: Es wurde eine ganze Reihe von Versuchen mit neoadjuvanter Chemotherapie auf der Basis von Cisplatin und Fluorouracil (CF) durchgeführt. Zum Teil erhielten die Patienten auch postoperativ Chemotherapie. In der Intergroup 113 Studie wurden 440 Patienten mit Ösophagus-Ca untersucht. Ein Teil der Patienten erhielten präoperativ 3 Kurse CF und postoperativ 2 Kurse. Eine signifikante Veränderung der R0-Resektion, der 2-Jahres-Überlebensrate oder der mittleren Überlebensrate konnte im Vergleich zur alleinigen Operation nicht publiziert werden [29; 30]. Im Gegensatz dazu konnte im MRC-OE2 Versuch (n=802) bei den Patienten die zusätzlich präoperativ mit 2 Kursen CF behandelt wurden, eine Verbesserung der mittleren und der 2-Jahres- Überlebensrate gezeigt werden (16,8 % vs und 34% vs. 43%) [29]. Zudem konnte in einer randomisierten Studie von Cunningham et. al. (MAGIC Trial, n=503) gezeigt werden, dass eine chirurgische Therapie mit perioperativer Chemotherapie, mit jeweils 3 Zyklen Epirubicin, Cisplatin und Fluourouracil (ECF) prä- und postoperativ, der alleinigen Operation
21 21 überlegen ist. Die 5-Jahres-Überlebensrate bei Adeno-Ca des Magens, des gastroösophagealen Übergangs und des unteren Ösophagus war um ca. 13 % höher. Die postoperativen Komplikationen waren in beiden Gruppen in etwa gleich [11; 29]. Insgesamt wurde bei keinen der 3 Studien eine erhöhte Mortalität oder Morbidität bei der auf CF basierender Chemotherapie festgestellt [29]. Zudem wurde in mehreren Studien Fluorouracil, Doxirubicin, Methotrexat (FAMTX) als Chemotherapeutika eingesetzt. Bei dem Einsatz von ECF im Vergleich mit FAMTX zeigten sich bessere Ansprechraten und auch eine höhere Überlebensrate [11; 17; 60]. In einer weiteren Studie wurde bei fortgeschrittenen Magenkarzinomen die bessere Überlebensrate mit Fluorouracil, Cisplatin und Anthrazyclin gezeigt, die bessere Verträglichkeit wurde allerdings mit Epirubicin, Cisplatin und Fluourouracil demonstriert [17; 56]. Neoadjuvante Radio- und Radiochemotherapie: In vergangenen Studien wurde gezeigt, dass bei der multimodalen neoadjuvanten Therapie eine Kombination aus Radio- und Chemotherapie der alleinigen Radiotherapie eindeutig überlegen ist, die systemischen Nebenwirkungen bei einer Radiochemotherapie allerdings zunehmen. Der positive Effekt bei der RCT wird der erhöhten Strahlensensibilität des Tumorgewebes zugeschrieben, die durch die Chemotherapie erreicht wird [2; 24; 29]. Bezüglich der Überlebensrate ist die Datenlage eher schwierig. Es gibt zwar eine ganze Reihe randomisierter Studien, die zum einen aber meist nur eine kleinere Zahl von Patienten untersuchten und zum anderen unterschiedliche Ergebnisse lieferten [15; 29; 55]. In den Metanalysen von Urschel et. al. und Fiorica et. al., die mehrere randomisierte Studien miteinander verglichen haben, konnten aber beide insgesamt einen positiven Effekt der neoadjuvanten RCT im Vergleich zur alleinigen chirurgischen Therapie ausarbeiten [15; 55]. Die postoperative Letalität nahm bei Anwendung von neoadjuvanter RCT bei Ösophaguskarzinomen in vergangenen Phase III Studien allerdings signifikant zu, bei Walsh et. al. um 6% [7; 58] und bei Bosset et. al. sogar um 9,6 % [6; 7]. In mehreren anderen Studien zeigte sich keine eindeutige Erhöhung der postoperativen Sterberate [7]. Noch von
22 22 besonderer Bedeutung ist, dass nach neoadjuvanter Radiochemotherapie die Anzahl der Lymphknotenmetastasen (ypn-status) bei AEG-Tumoren oder Ösophagus-Ca eine prognostische Wertigkeit haben. Die Tumoren von Patienten, die sich einer neoadjuvanten Therapie unterzogen, hatten ein niedrigeres klinisches TNM-Stadium und pathologisches ptnm-stadium als die, die nur operiert wurden [10; 20; 31; 51] Ziele der Studie Die Häufigkeit von Lymphknotenmetastasen bei AEG-Tumoren und die prognostische Bedeutung für die erfolgreiche Behandlung dieser mit Radiochemotherapie haben uns angeregt, die betroffenen Lymphknotenregionen bei AEG-Tumoren zu identifizieren. Sie wurden in Abhängigkeit von den jeweiligen AEG-Typen und anhand des Tumorwachstums in die Nachbarregion hinein bestimmt. Basierend auf diesen Daten beabsichtigen wir ausgesuchte Lymphknotenregionen in das Zielvolumen mit einzuschließen und versuchen durch eine Reduktion des Zielvolumens ohne Ausschluss von Lymphknotenmetastasen, die Verträglichkeit der Therapie zu steigern. Insbesondere die potentielle pulmonale postoperative Morbidität soll dadurch reduziert werden [59].
23 23 2. Material und Methoden 2.1. Datenerhebung und Patientenzahl Eine prospektive systematische Datensammlung des Tumorregisters der chirurgischen Klinik der Universitätsklinik in Erlangen ermöglichte uns pathohistologische Daten für diese Studie zu untersuchen. Hierbei haben wir die Richtlinien der WHO angewendet, um die Histomorphologie zu klassifizieren. Die Originalevaluation der Tumorproben wurde von einem erfahrenen Pathologen oder unter seiner Supervision durchgeführt. Auf der Basis dieser Daten konnten wir einen Datenpool an Adenokarzinomen vom unteren Ösophagus (n=90) und vom proximalen Magen (n=236) ermitteln. Für die Kriterien von AEG-Tumoren orientierten wir uns an den Vorgaben der International Gastric Cancer Association (IGCA) und der International Society for Diseases of the esophagus (ISDE) [49]. Zwischen Januar 1982 und Dezember 2004 wurden in der chirurgischen Klinik der Universitätsklinik Erlangen 326 Patienten behandelt, die für unsere Studie in Frage kamen Einschlusskriterien - Adeno-Ca des gastroösophagealen Übergangs - radikale Tumorresektion - keine neoadjuvante Therapie - systematische regionale Lymphknotendissektion im Rahmen der Tumorresektion - Patienten bei denen mindestens 15 Lymphknoten untersucht worden sind Ausschlusskriterien - Plattenepithel-Ca im Bereich des gastroösophagealen Übergangs - Neoadjuvante Therapie - Palliative Tumorresektion - Patienten ohne positive Lymphknoten
24 Dissezierte Lymphknotenstationen In folgenden Bereichen wurden Lymphknotenstationen disseziert wie in Abbildung 2 dargestellt; nummeriert wurden sie nach der Japanese Classification of Gastric Carcinoma [26]: (1) rechts parakardial (2) links parakardial (3) kleine Kurvatur (4) große Kurvatur (4sb) A. gastroepiploica sinistra (4d) A. gastroepiploica dextra (5) proximal des Pylorus (6) distal des Pylorus (7) A. gastrica sinistra (8) A. hepatica communis (9) Truncus coeliacus (10) Milzhilus (11) A. lienalis (108) mittlere paraösophageale (110) untere paraösophageale Lymphknotenareale, bei denen entweder nur 10 % bei den Patienten disseziert wurden oder die keine Metastasen enthielten, wurden nicht berücksichtigt (n=33 Regionen).
25 sb 6 4d Abb. 2: Dissezierte Lymphknotenstationen, nummeriert nach der Japanese Classification of Gastric Carcinoma [38] 2.3. Statistische Methoden Mit Hilfe von Fisher`s Exact Test wurde untersucht, ob eine Korrelation zwischen Metastasen der Lymphknotenareale und der Tumorcharakteristik besteht. Wenn nicht anders festgelegt, repräsentiert der prozentuale Anteil von Lymphknotenmetastasen das Vorhandensein von durch Tumor befallene Lymphknoten pro Patient, bezogen auf eine bestimmte Lymphknotenregion.
26 26 Das Signifikanzniveau wurde bei p 0.05 festgelegt und unter Berücksichtigung des statistischen Einflusses von multiplem Testen wurde bei p von einem hochsignifikanten Niveau gesprochen. Die statistische Auswertung wurde mit Hilfe von Herrn PD Dr. Thomas Brunner durchgeführt Klassifikation von AEG-Tumoren Anhand von Endoskopie- und Pathologiebefunden wurden die Tumore der Patienten retrospektiv in AEG-Typen I-III eingeteilt, je nach Lage des Tumorzentrums oder der Tumormasse. Die jeweiligen AEG-Typen wurden folgendermaßen definiert: 1.) AEG-Typ I, Adeno-Ca des distalen Ösophagus 2.) AEG-Typ II, Adeno-Ca der Kardia 3.) AEG-Typ III, Adeno-Ca unterhalb der Kardia Nur 57 von 326 Patienten konnten direkt einem der drei Subtypen zugeordnet werden. Bei den restlichen Patienten bestand eine Tumorausdehnung in proximale und/oder distale Gebiete ausgehend von der Tumorhauptmasse. Jegliche Tumorinvasion in benachbarte Regionen wurde separat dokumentiert. Es wurde besonders darauf geachtet, ob eine Tumorausdehnung oberhalb der Z-Linie für Typ II und III bzw. unterhalb der Z-Linie für Typ I bestand Planung der 3-dimensionalen Strahlentherapie Bei acht Patienten mit AEG Typ II-Tumoren wurde eine, wie an anderer Stelle ausführlich beschriebene [8], 3-dimensionale Behandlungsplanung für neoadjuvante Radiochemotherapie durchgeführt. Die in der Literatur beschriebene Planung für Pankreastumoren [8] wurde in Analogie für Tumoren der Kardia modifiziert.
27 27 Die CT-Scans mit intravenösem Kontrast wurden in der portalvenösen Phase und mit einer Schichtdicke von 5 mm durchgeführt. Die Planungszielvolumina 1 und 2 wurden für eine konventionelle Fraktionierung mit einer Einzeldosis von 1,8 Gy bis zu einer Gesamtdosis von 45,0 Gy konturiert. Die Strahlendosis für gefährdete Nachbarorgane wurde auf folgende Maximaldosen limitiert: - Bis zu 20 Gy auf 30% der beiden Lungenvolumina (seitengetrennt) - Bis zu 30 Gy auf 50% des Lebervolumens - Bis zu 20 Gy auf 50% des rechten Nierenvolumens - Bis zu 20 Gy auf 30% des linken Nierenvolumens - Bis zu 40 Gy auf Anteile des Rückenmarks Unterschiedliche proximale Grenzen für das Planungszielvolumen 2 wurden anhand des Lungen-Dosis-Volumen-Histogramms für jeden Behandlungsplan miteinander verglichen, um die postoperativen Lungenkomplikationen abschätzen zu können [59].
28 28 3. Ergebnisse 3.1. Lymphknotenmetastasierungsmuster Allgemeine Verteilung der Lymphknotenmetastasen Insgesamt konnten 326 Patienten mit AEG-Tumoren in die Analyse eingeschlossen werden. Die Patientencharakteristika dieser Patienten sind in Tabelle 3 aufgeführt. Kriterien Rang Patientenzahl Prozent Geschlecht männlich weiblich Alter in Jahren Im Mittel 63 (von 25 bis 84) Operation Ösophagektomie 91 proximale Magenresektion/ 14 ösophageale Resektion Gastrektomie Resektion des Magenstumpfes Grade Keine Angabe pt Ösophagus: 1 (UICC 2002) (n = 90) pn (UICC 2002) Magen: Ösophagus: 0 1 (n = 236) (n = 90) LK untersucht LK positive Magen: Mittel Mittel (n = 236) (von 15 bis 102) 4 (von 0 bis 40)
29 29 Kriterien Rang Patientenzahl Prozent AEG-Typen AEG I AEG II AEG III Stadiengruppierung (UICC 2002) Ösophagus: I IIA IIB III IVA IVB Magen: IA IB II IIIA IIIB IV R-Klassifikation R0 R = = Tabelle 3 Patentencharakteristika (n = 326) Insgesamt war die Inzidenz von regionalen Lymphknotenmetastasen 71 %. Bei 232 von 326 Patienten wurde eine mittlere Anzahl von 37 Lymphknoten (von 15 bis 102 Lymphknoten) histopathologisch untersucht. Bei den genannten 232 Patienten war der Mittelwert von positiven regionalen Lymphknoten n= 4 (von 1 bis 40 befallenen Lymphknoten). Bei 40 von 48 (83.3 %) Patienten im pt1-stadium wurden keine Lymphknotenmetastasen nachgewiesen. In unserer Studie wurden nur die Patienten im T2-T4- Stadium, insgesamt 278, zur weiteren Beurteilung herangezogen. Ein Lymphknotenbefall wurde jeweils bei 81 % der T2-T4-Tumore, bei 78 % der T2 Tumore, bei 86 % der T3-Tumore und bei 90 % der T4-Tumore festgestellt. Im Stadium T2-T4 wurden 111 AEG I-Tumoren, 155 AEG II- Tumoren und 12 AEG III-Tumoren ermittelt.
30 Spezifische regionale Verteilung der Lymphknotenmetastasen Die genaue Lokalisation der Lymphknotenmetastasen wurde in Tabelle 4 dargestellt.
31 31 T2 bis T4 Tumoren (n=278) pt (n=180)* pt3/ (n=98) AEG I (n=111) AEG II/III (n=167) G1, G2 (n=131) G3, G4 (n=147) L0 (n=101) L1 (n=114) <55 mm (*1) (n=135) 55 mm (n=141), x=2 45 mm (*2) (n=140) > 45 mm (n=134), x=4 paraösophageal unten 110 (%) rechts parakardial 1 (%) links parakardial 2 (%) parakardial gesamt 1+2 (%) kleine Kurvatur große Kurvatur linke Arteria gastroepiploica 4sb (%) rechte Arteria gastroepiploica 4d (%) linke Arteria gastrica 7 (%) Truncus coeliacus Milzhilus Arteria lienalis 3 (%) 4s (%) 9 (%) (%) (%) 79/165 91/ / / /236 46/208 35/165 28/190 90/203 36/151 20/136 20/126 (48) (39) (47) (51) (68) (22) (21) (15) (44) (24) 15 (16) 28/96 55/151 73/155 87/ /170 27/157 21/122 13/139 53/136 20/109 6/97 10/89 (11) (29) (36) (47) (50) (71) (17) (17) (9) (39) (18) (6) 51/69 36/83 38/84 51/96 40/66 19/51 14/43 15/51 (39) 37/67 16/42 14/39 10/37 (74) (43) (45) (53) (61) (37) (33) (55) (38) (36) (27) p<0.001 p=0.006 p=0.03 P=0.002 p=0.035 p=0.018 p<0.001 p= /89 (55) 44/99 46/97 61/108 46/76 15/57 11/44 10/55 38/75 17/56 5/36 3/33 (44) (47) (56) (61) (26) (25) (18) (68) (30) (14) (9) 30/76 47/136 65/141 77/ /160 31/151 25/121 18/135 52/128 19/95 15/100 17/93 (39) (35) (46) (48) (71) (21) (21) (13) (41) (20) (15) (18) p= /78 44/119 58/127 72/140 86/130 21/121 14/89 13/112 44/114 16/89 12/77 9/67 (44) (37) (46) (51) (66) (17) (16) (12) (39) (18) (16) (13) 45/87 47/116 53/111 66/129 74/106 25/87 21/76 15/78 46/89 20/62 (32) 8/59 11/59 (52) (41) (48) (51) (70) (29) (28) (19) (52) (14) (19) p=0.063 p=0.085 p=0.066 p= /38 13/56 19/58 21/68 35/70 4/55 3/40 2/50 17/47 5/41 2/29 4/29 (37) (23) (33) (31) (50) (7) (8) (4) (36) (12) (7) (14) 46/21 38/88 52/91 63/107 82/106 31/91 22/67 20/81 36/78 15/56 14/58 9/53 (46) (43) (57) (59) (77) (34) (33) (25) (46) (27) (24) (17) p=0.020 p=0.004 p<0.001 p<0.001 p<0.001 p=0.002 P=0.002 p= /76 42/115 44/112 60/130 64/108 20/83 18/76 11/83 38/97 15/67 2/46 3/48 (38) (37) (39) (46) (59) (24) (24) (13) (39) (22) (4) (6) 50/89 49/119 65/124 76/137 94/126 26/106 17/88 17/106 51/105 20/83 18/89 17/78 (56) (41) (52) (55) (75) (25) (19) (16) (49) (24) (20) (22) p=0.028 p=0.050 p=0.017 p=0.019 p= /88 41/118 46/118 60/135 68/113 15/96 12/75 9/85 43/102 17/73 4/50 3/52 (41) (35) (39) (44) (60) (16) (16) (11) (42) (23) (8) (6) 43/76 50/116 63/117 76/131 90/121 30/110 22/188 18/103 45/98 17/75 16/85 17/74 (57) (43) (54) (58) (74) (27) (12) (17) (46) (23) (19) (23) p=0.042 p=0.026 p=0.028 p=0.025 p=0.062 p=0.012 Tabelle 4: Verteilung der Lymphknotenmetastasen nach Tumorcharakteristika bei 278 Patienten mit T2 bis T4 Tumoren
32 32 In Tabelle 4 werden fehlende Werte bei n Patienten mit x=n definiert. Die Zahlen im Tabellenkopf stellen Lymphknotenregionen entsprechend nach der Japanese Gastric Carcinoma Association dar. Die p-werte, welche mit Hilfe des Fisher s Exact Test ermittelt wurden, ermöglichen einen Vergleich der Metastasierungsmuster nach Tumorcharakteristika. Aus Gründen der Übersichtlichkeit wurden nicht signifikante Werte nicht in die Tabelle aufgenommen, so dass nur Werte bis p< 0.1 ersichtlich sind. Von deutlich signifikanten Werten kann bei p 0.05 gesprochen werden. Die fettgedruckten p-werte in Tabelle 4 sind mit Werten p als hoch signifikant einzustufen. In der Tabelle wird mit (*1) beschrieben, dass das Mittel des maximalen longitudinalen Durchmessers 55 mm und mit (*2), dass das Mittel des maximalen Durchmessers der Infiltrationstiefe 45 mm bei der histopathologischen Messung betrug. Bei Anmerkung (*1) fehlten bei 2 Patienten und bei Anmerkung (*2) bei 4 Patienten die Daten. Die Regionen mit der höchsten Zahl von positiven Lymphknoten lagen an der kleinen Kurvatur und parakardial, gefolgt von den unteren paraösophagealen Lymphknoten und denen die entlang der A. gastrica sinistra lagen. Im gesamten Patientendatenkollektiv waren die Lymphknoten an der A. gastroepiploica sinistra und dextra, an der großen Kurvatur und am Truncus coeliacus nur bei ca. 20 % positiv. Zudem wurden Metastasen im Bereich des Milzhilus und der A. lienalis bei < 20 % ermittelt, gefolgt von Lymphknotenarealen an der A. hepatica communis und am distalen und proximalen Pylorus Verteilung der Lymphknotenmetastasen nach Tumorcharakteristik Routinemäßig verfügbare Tumorcharakteristika vor neoadjuvanter oder definitiver Therapie wie T-Klassifikation, Lymphgefäßeinbrüche, histopathologisches Grading, Tumorlänge und maximale Invasionstiefe wurden in der Absicht analysiert, Unterschiede des nodalen Befalls
33 33 festzustellen, die als Grundlage für die Bestrahlungsplanung elektiver Lymphknotenareale dienen. In den Abbildungen 3A bis 3D wird die Verteilung der Lymphknotenmetastasen nach Tumorcharakteristika graphisch mit Angabe der Prozentzahlen veranschaulicht. Die Prozentsätze an der Y-Achse spiegeln den Anteil der Patienten wieder, die Lymphknotenmetastasen in der jeweiligen Region aufwiesen. Die Anordnung der Lymphknotenregionen an der X-Achse stellen die Gebiete von proximal (links) bis nach distal (rechts) dar. Üblicherweise werden Lymphknotenareale mit in das Bestrahlungsplanungszielvolumen eingeschlossen, die mit einer Wahrscheinlichkeit von 15 % bis 20 % mit Metastasen befallen sind. Um das Metastasierungsmuster in Abbildung 3A bis 3D darzustellen wurden für verschiedene Lymphknotengebiete folgende Abkürzungen verwendet: PÖU= paraösophageal unten, RPC= parakardial rechts, LPC= parakardial links, PC= parakardial gesamt, KKV= kleine Kurvatur, GKV= große Kurvatur, LGE= A. gastroepiploica links, RGE= A. gastroepiploica rechts, TCC= Truncus coeliacus, AHC= A. hepatica communis, LAG= A. gastrica sinistra, ALI= A. lienalis, MH= Milzhilus, crpyl= cranial des Pylorus, cdpyl= caudal des Pylorus. Abbildung 3A: Vergleich Lymphknotenbefall bei T2 und T3/4 Tumoren Die Zahl der befallenen Lymphknoten war bei T3- und T4- Tumoren beinahe gleich mit der bei T2-Tumoren in der juxtatumoralen Region, d. h. parakardial
34 34 und an der kleinen Kurvatur. In allen anderen Regionen stellten wir jedoch bei T3- und T4-Tumoren einen signifikant höheren Lymphknotenbefall als bei T2-Tumoren fest, wie in Abbildung 3A dargestellt. Abbildung 3B: Bedeutung des lymphovaskulären Befalls In Abbildung 3B wird das Metastasierungsmuster unter Berücksichtigung des lymphovaskulären Befalls (L1) und ohne lymphovaskulären Befall (L0) gezeigt. Es ist ersichtlich, dass bei einem lymphovaskulären Befall bei nahezu fast allen Lymphknotenstationen die Rate an Metastasen deutlich angestiegen ist. Abbildung 3C: Bedeutung des Gradings
35 35 In Abbildung 3 C wurden gut differenzierte Tumoren G1/G2 mit schlecht differenzierten Tumoren G3/G4 verglichen. Die schlecht differenzierten Tumoren korrelierten mit einer besonders hohen Rate an Metastasen im Bereich der A. gastroepiploica sinistra, der großen Kurvatur, des Truncus coeliacus und der A. gastrica sinistra. Abbildung 3D: Vergleich Lymphknotenbefall bei AEG I und AEG II/III Bei den AEG-Typ I-Tumoren im Vergleich zu den AEG-Typ II/III-Tumoren zeigte sich eine massive Zunahme an Metastasen bei den unteren paraösophagealen Lymphknoten und an der A. gastrica sinistra, wie in Abbildung 3D dargestellt Lymphknotenbefall in mediastinalen und distalen Gebieten Im folgenden Abschnitt wird spezifisch auf die Lymphknotenmetastasen im Bereich des Mediastinums und in distalen Gebieten eingegangen. In Abbildung 4A wird die Verteilung der Lymphknotenmetastasen paraösophageal unten, der Arteria lienalis und des Milzhilus bei AEG Typ I versus Typ II/III im Stadium pt3/t4 graphisch dargestellt. In Abbildung 4B wurde das Ausmaß der ösophagealen Invasion < 15mm bzw. 15 mm bei AEG II/III veranschaulicht. Bei beiden Abbildungen spiegeln die Prozentsätze
36 36 an der Y-Achse den Anteil der Patienten wieder, die Lymphknotenmetastasen in der jeweiligen Region aufwiesen Mediastinaler Lymphknotenbefall bei den jeweiligen AEG- Tumortypen Für die verschiedenen AEG-Tumortypen wurde die Anzahl von befallenen Lymphknoten im Mediastinum analysiert. AEG-Typ I: bei 12 von 32 Patienten (38 %) zeigten sich Metastasen der mittleren und bei 49 von 89 Patienten der unteren paraösophagealen Lymphknoten (55%). AEG-Typ II/III: bei 30 von 76 Patienten (39 %) zeigte sich ein Befall der unteren paraösophagealen Lymphknoten. Die Anzahl der Lymphknotendissektionen aus der mittleren paraösophagealen Etage war für Type II/III-Tumoren zu gering, um ein aussagekräftiges Ergebnis zu erhalten. Wie oben in Tabelle 4 und Abbildung 3D dargestellt. T3- und T4-Tumore bei AEG-Typen: AEG-Typ I: 36 von 48 Patienten (75 %) zeigten positive Lymphknoten im unteren paraösophagealen Bereich bei T3/T4-Tumoren. AEG-Typ II/III: 15 von 21 Patienten (71 %) zeigten positive Lymphknoten im unteren paraösophagealen Bereich. In Abbildung 4A dargestellt.
37 37 Abbildung 4A: Vergleich pt3/4 Tumoren bei AEG I und AEG II/III Um das Metastasierungsmuster in Abbildung 4A darzustellen wurden für die verschiedenen Lymphknotengebiete folgende Abkürzungen verwendet: PÖU= paraösophageal unten, ALI= A. lienalis, MH= Milzhilus Mediastinaler Lymphknotenbefall bei AEG-Tumoren, die die Z-Linie überschreiten Die AEG Klassifikation ist gemäß der Lokalisation der Tumorhauptmasse definiert. Die Tumorausdehnung in andere Regionen wird allerdings nicht berücksichtigt. Wir haben die Tumorinfiltration in die Nachbarregionen ausgemessen, um mögliche Unterschiede bezüglich des Lymphknotenmetastasierungsmusters ermitteln zu können. Bei AEG II/III-Tumoren waren Tumorinvasionen proximal der Z-Linie in den distalen Ösophagus bei 162 von 167 Patienten (97 %) vorhanden. Die mediane Tumorinvasion in die proximale Richtung betrug 15 mm (3-60 mm). Bei einer proximalen Tumorinvasion kleiner als 15 mm wurden in 16 % der Fälle paraösophageale Lymphknotenmetastasen gefunden und bei einer Tumorausdehnung 15 mm proximal der Z-Linie in den distalen Ösophagus lagen sie bei 47 %. Der eindeutig höhere Lymphknotenbefall an der A. gastrica sinistra mit über 50 % ist vermutlich alleinig dadurch zu erklären, dass größere Tumoren mehr metastasieren. Dasselbe gilt für Metastasen im Bereich der A. lienalis. Weiterhin wurden Tumorinvasionen von AEG I-Tumoren distal der Z-Linie bei
38 38 83 von 111 Patienten gefunden (75 %). In unserer Studie wurde bei diesen Patienten keine höheren Raten an abdominalen Metastasen gefunden (Abbildung 4B). Abbildung 4B: ösophageale Invasion bei AEG II/III Um das Metastasierungsmuster in Abbildung 4B darzustellen wurden für die verschiedenen Lymphknotengebiete folgende Abkürzungen verwendet: PÖU= paraösophageal unten, ALI= A. lienalis, LAG= A. gastrica sinistra Lymphknotenbefall distaler Gebiete mit hoher Bedeutung für die Größe des Planungszielvolumens Bei T2- bis T4-Tumoren wurde eine Ausdehnung der Metastasen bis zu den Lymphknoten des Milzhilus gefunden. Hierbei wurde für AEG Typ I-Tumoren 5 von 36 Patienten (14 %) und für AEG II-Tumoren 15 von 100 Patienten (15 %) ermittelt. Positive Lymphknoten entlang der A. lienalis wurden bei 3 von 33 AEG I-Tumoren (9 %) und bei 17 von 93 AEG II-Tumoren (18 %) gefunden (siehe oben, Tabelle 4 und Abbildung 3D), wohingegen bei AEG Typ I-Tumoren im T3/T4-Stadium kein höherer Lymphknotenbefall der A. lienalis oder des Milzhilus ermittelt werden konnte. Bei AEG II/III-Tumoren konnte allerdings im T3/T4-Stadium eine Ausbreitung bis zum Milzhilus bei 12 von 29 Patienten (41 %) und bis zur A. lienalis bei 9 von 26 Patienten (35 %) entdeckt werden (siehe oben, Abbildung 4A).
39 Vorschlag für das Planungszielvolumen Basierend auf den erhaltenen Ergebnissen kann eine Empfehlung für das Behandlungsvolumen abgeleitet werden (Tabelle 5). Die in Tabelle 5 fettgedruckten Lymphknotenbereiche sollten immer mitbehandelt werden. Mit X werden die Lymphknotenareale gekennzeichnet, die zu > 20% befallen sind, und somit in die Behandlung mit eingeschlossen werden sollten. Mit (X) werden die Lymphknoten gekennzeichnet, die ein Risiko von 15 % haben mit Tumorgewebe infiltriert zu sein. Die mittleren paraösophagealen wurden mit eingeschlossen, wenn die Befallsrate der unteren paraösophagealen >50 % betrug. In Tabelle 5 wird mit (*1) beschrieben, dass das Mittel des maximalen longitudinalen Durchmesser 55 mm und mit (*2), dass das Mittel der maximalen Infiltrationstiefe 45 mm bei der histopathologischen Messung betrug.
40 40 ösophageal Mitte (108) ösophageal unten (110) parakardial gesamt (1+2) kleine Kurvatur (3) große Kurvatur (4s) linke Arteria gastroepiploica (4sb) rechte Arteria gastroepiploica (4d) linke Arteria gastrica (7) Arteria hepatica communis (8a) Truncus coeliacus (9) Milzhilus (10) Arteria lienalis (11) paraaortal links (16a2) T2 bis T4 Tumoren x x x (x) (x) x (x) pt3/4 x x x x x X x x 55 mm (*1) Länge 45 mm (*2) Tiefe x x x x x x x x AEG I x x (x) X AEG II/III (x) (x) (x) x AEG II/III 15 mm Ösophageale Invasion (x) (x) (x) (x) x G3, G4 x x x X (x) (x) L1 (x) x x x X x (x) Tabelle 5: Vorschlag für die elektive Radiotherapie, Planungszielvolumen (PTV2), für Patienten mit T2-T4 Tumoren
41 41 Es gibt keinen einheitlichen Grenzwert für das Risiko von Lymphknotenmetastasen und somit ist es schwierig eine generelle Empfehlung für das PTV auszusprechen. Abhängig von den zu behandelnden Organen, ist oft mit einem Risiko des Lymphknotentbefalls von 10 % bis 20 % zu rechnen. Gehen wir von einem Grenzwert für die Behandlung von 20 % aus, sind demnach die folgenden Lymphknoten in > 20 % befallen, unabhängig von anderen Risikofaktoren und sollten immer in das PTV eingeschlossen werden: - untere paraösophageale Lymphknoten - parakardiale Lymphknoten - Lymphknoten an der kleinen Kurvatur - Lymphknoten an der A. gastrica sinistra. Andererseits korreliert bei den Lymphknoten entlang des Pylorus kein Risikofaktor mit einem relativen Risiko für Tumorbefall von > 20 %. Lediglich bei T3/T4-Tumoren zeigte sich ein Tumorbefall von 15 %. Zwischen diesen Extremen gab es eine ganze Reihe von Lymphknotenarealen, bei denen der Tumorbefall stark von den Risikofaktoren abhing: 1. Lymphgefäßeinbrüche 2. Tumorstadium (T3, T4) 3. Tumorgrading 4. Tumorgröße 5. Tumorausdehnung oberhalb oder unterhalb des Zwerchfells 1. Lymphgefäßeinbrüche Bei Lymphgefäßeinbrüchen wurden > 20 % Metastasen diagnostiziert an der - A. gastroepiploica sinistra und dextra - großen Kurvatur - Truncus coeliacus - Milzhilus
42 42 2. Tumorstadium Bei fortgeschrittenen Tumoren (T3, T4) sollten folgende Lymphknoten mit in die Behandlung einbezogen werden Lymphknoten im Bereich - der A. gastroepiploica sinistra und dextra - der großen Kurvatur - des Truncus coeliacus - des Milzhilus - der A. lienalis - der A. hepatica communis 3. Tumorgrading Schlecht differenzierte Tumoren (G3, G4) korrelierten mit Metastasen bei > 20 % im Bereich - der A. gastroepiploica sinistra - der großen Kurvatur - des Truncus coelicus 4. Tumorgröße Bei einer Tumorlänge von 55 mm oder einer maximalen Wandinfiltrationstiefe von 45 mm sollten die Lymphknoten - der A. splenica - des Milzhilus - der großen Kurvatur in das PTV 2 eingeschlossen werden. 5. Tumoren oberhalb des Zwerchfells Bei Tumoren oberhalb des Zwerchfells und Tumoren, deren Hauptmasse sich unterhalb der Z-Linie befindet, aber ein Wachstum von mindestens 15
Die Klassifikation gilt nur für Karzinome. Histologische Diagnosesicherung
 Magen 59 Magen (ICD-O C16) Regeln zur Klassifikation Die Klassifikation gilt nur für Karzinome. Histologische Diagnosesicherung ist erforderlich. Verfahren zur Bestimmung der T-, N- und M-Kategorien sind:
Magen 59 Magen (ICD-O C16) Regeln zur Klassifikation Die Klassifikation gilt nur für Karzinome. Histologische Diagnosesicherung ist erforderlich. Verfahren zur Bestimmung der T-, N- und M-Kategorien sind:
TNM Klassifikation maligner Tumoren
 UICC International Union Against Cancer TNM Klassifikation maligner Tumoren Bearbeitet von Ch Wittekind, H.-J Meyer, F Bootz, G Wagner Neuausgabe 2005. Taschenbuch. xxii, 225 S. Paperback ISBN 978 3 540
UICC International Union Against Cancer TNM Klassifikation maligner Tumoren Bearbeitet von Ch Wittekind, H.-J Meyer, F Bootz, G Wagner Neuausgabe 2005. Taschenbuch. xxii, 225 S. Paperback ISBN 978 3 540
GI-ONCOLOGY INTERDISZIPLINÄRES UPDATE. Die neue TNM-Klassifikation von Tumoren. des oberen Gastrointestinaltrakts
 GI-ONCOLOGY 2010 6. INTERDISZIPLINÄRES UPDATE Die neue TNM-Klassifikation von Tumoren des oberen Gastrointestinaltrakts Christian Wittekind, Institut für Pathologie des UKL, Liebigstrasse 26, 04103 Leipzig
GI-ONCOLOGY 2010 6. INTERDISZIPLINÄRES UPDATE Die neue TNM-Klassifikation von Tumoren des oberen Gastrointestinaltrakts Christian Wittekind, Institut für Pathologie des UKL, Liebigstrasse 26, 04103 Leipzig
Vorlesungsreihe Onkologie Ösophagus und Magen
 Vorlesungsreihe Onkologie Ösophagus und Magen PD Dr. Michael Heise Klinik für michael.heise@med.uni-jena.de Patientenvorstellung Patientenvorstellung Patientenvorstellung Patientenvorstellung Patientenvorstellung
Vorlesungsreihe Onkologie Ösophagus und Magen PD Dr. Michael Heise Klinik für michael.heise@med.uni-jena.de Patientenvorstellung Patientenvorstellung Patientenvorstellung Patientenvorstellung Patientenvorstellung
Ösophaguskarzinom Ist die Chirurgie beim Adeno- und Plattenepithelkarzinom gleichermaßen noch zeitgemäß?
 Ösophaguskarzinom Ist die Chirurgie beim Adeno- und Plattenepithelkarzinom gleichermaßen noch zeitgemäß? Prof. Dr. Jörg Köninger Klinik für Allgemein- und Viszeralchirurgie Katharinenhospital Klinikum
Ösophaguskarzinom Ist die Chirurgie beim Adeno- und Plattenepithelkarzinom gleichermaßen noch zeitgemäß? Prof. Dr. Jörg Köninger Klinik für Allgemein- und Viszeralchirurgie Katharinenhospital Klinikum
Ösophagustumor (1) Klinisches Krebsregister Kodierhilfe - Stand September Epidemiologie:
 Ösophagustumor (1) Epidemiologie: Der Speiseröhrenkrebs gehört zu den selteneren Krebserkrankungen. Das Robert-Koch-Institut in Berlin gibt für 2002 die Zahl der Neuerkrankungen in Deutschland pro 100
Ösophagustumor (1) Epidemiologie: Der Speiseröhrenkrebs gehört zu den selteneren Krebserkrankungen. Das Robert-Koch-Institut in Berlin gibt für 2002 die Zahl der Neuerkrankungen in Deutschland pro 100
Interdisziplinäre Behandlung der Karzinome des gastroösophagealen Übergangs und der Magenkarzinome
 Interdisziplinäre Behandlung der Karzinome des gastroösophagealen Übergangs und der Magenkarzinome Priv.-Doz. Dr. René Hennig Klinik für Allgemein und Viszeralchirurgie Bad Cannstatt Magenkarzinom & AEG
Interdisziplinäre Behandlung der Karzinome des gastroösophagealen Übergangs und der Magenkarzinome Priv.-Doz. Dr. René Hennig Klinik für Allgemein und Viszeralchirurgie Bad Cannstatt Magenkarzinom & AEG
Was steht in meinem Befund?
 Basiskurs Krebswissen 09.11.2016 Was steht in meinem Befund? (Staging, Grading, TNM, ) Rainer Hamacher, MUW-AKH, Univ. Klinik für Innere Medizin I / Onkologie TNM STAGING & GRADING Tumorstaging (=Staging)
Basiskurs Krebswissen 09.11.2016 Was steht in meinem Befund? (Staging, Grading, TNM, ) Rainer Hamacher, MUW-AKH, Univ. Klinik für Innere Medizin I / Onkologie TNM STAGING & GRADING Tumorstaging (=Staging)
Perioperative Radiochemotherapie beim Magenkarzinomen
 Perioperative Radiochemotherapie beim Magenkarzinomen Frank Zimmermann und Alexandros Papachristofilou Das Magenkarzinom: eine heterogene Erkrankung Lokalisation: Ösophagogastraler 35% Übergang (proximal)
Perioperative Radiochemotherapie beim Magenkarzinomen Frank Zimmermann und Alexandros Papachristofilou Das Magenkarzinom: eine heterogene Erkrankung Lokalisation: Ösophagogastraler 35% Übergang (proximal)
2. Material und Methodik Eigenes Material Tumorausbreitung Tumorklassifikation Qualitätsindikatoren und Referenzbereiche 5
 Referat Ausgehend von der Feststellung des Gesundheitsprogramms des Ministeriums für Arbeit, Soziales und Gesundheit des Landes Sachsen-Anhalt 1997 Sachsen-Anhalt liegt beim Vergleich der allgemeinen Sterblichkeit
Referat Ausgehend von der Feststellung des Gesundheitsprogramms des Ministeriums für Arbeit, Soziales und Gesundheit des Landes Sachsen-Anhalt 1997 Sachsen-Anhalt liegt beim Vergleich der allgemeinen Sterblichkeit
Symptome des Ösophaguskarzinoms
 Symptome des Ösophaguskarzinoms Schluckstörungen (Nahrung bleibt stecken) Gewichtsverlust Schmerzen sind eher selten Rekurrensparese, Horner-Syndrom Ösophagus Ösophaguskarzinom - Diagnostik Endoskopie
Symptome des Ösophaguskarzinoms Schluckstörungen (Nahrung bleibt stecken) Gewichtsverlust Schmerzen sind eher selten Rekurrensparese, Horner-Syndrom Ösophagus Ösophaguskarzinom - Diagnostik Endoskopie
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht N rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016
3 Ergebnisse 3.1 Klinische Befunde Alter und Geschlecht in Abhängigkeit von der Überlebenszeit
 13 3 Ergebnisse 3.1 Klinische Befunde 3.1.1 Alter und Geschlecht in Abhängigkeit von der Überlebenszeit Es wurden die klinischen Daten von 33 Patienten ausgewertet. Es handelte sich um 22 Frauen (66,7
13 3 Ergebnisse 3.1 Klinische Befunde 3.1.1 Alter und Geschlecht in Abhängigkeit von der Überlebenszeit Es wurden die klinischen Daten von 33 Patienten ausgewertet. Es handelte sich um 22 Frauen (66,7
Pathologie und Prognoseparameter. AGO e.v. in der DGGG e.v. sowie in der DKG e.v. Dietmar Schmidt Institut für Pathologie A2,2; Mannheim
 Pathologie und Prognoseparameter Dietmar Schmidt Institut für Pathologie A2,2; Mannheim Endometriales Adenokarzinom Histologische Typen (WHO 2003) Endometrioid Muzinös Serös Klarzellig Undifferenziert
Pathologie und Prognoseparameter Dietmar Schmidt Institut für Pathologie A2,2; Mannheim Endometriales Adenokarzinom Histologische Typen (WHO 2003) Endometrioid Muzinös Serös Klarzellig Undifferenziert
Ab durch die Mitte: Radiotherapie beim Pankreaskarzinom
 Ab durch die Mitte: Radiotherapie beim Pankreaskarzinom Alexandros Papachristofilou Pankreaskarzinom: Eine Herausforderung 0 1 Pankreaskarzinom: Eine Herausforderung 7.8/8.7 = 90% 10.1/10.7 = 94% 0 23.9/110.5
Ab durch die Mitte: Radiotherapie beim Pankreaskarzinom Alexandros Papachristofilou Pankreaskarzinom: Eine Herausforderung 0 1 Pankreaskarzinom: Eine Herausforderung 7.8/8.7 = 90% 10.1/10.7 = 94% 0 23.9/110.5
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen Abteilung Nuklearmedizin
 Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Pathologie, Typisierung, Ausbreitungsstadien
 1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
Zusammenfassung für Radioonkologen
 Preoperative Chemoradiotherapy for Esophageal or Junctional Cancer P. van Hagen, M.C.C.M. Hulshof, J.J.B. van Lanschot, E.W. Steyerberg,, M.I. van Berge Henegouwen, B.P.L. Wijnhoven, D.J. Richel, G.A.P.
Preoperative Chemoradiotherapy for Esophageal or Junctional Cancer P. van Hagen, M.C.C.M. Hulshof, J.J.B. van Lanschot, E.W. Steyerberg,, M.I. van Berge Henegouwen, B.P.L. Wijnhoven, D.J. Richel, G.A.P.
Optimierung der Tumorklassifikation durch klinische Krebsregister: Die pn-kategorie beim Rektumkarzinom
 Optimierung der Tumorklassifikation durch klinische Krebsregister: Die pn-kategorie beim Rektumkarzinom S. Merkel, W. Hohenberger Erlangen 03.04.2003 Merkel Patientengut 1382 Patienten mit Rektumkarzinom
Optimierung der Tumorklassifikation durch klinische Krebsregister: Die pn-kategorie beim Rektumkarzinom S. Merkel, W. Hohenberger Erlangen 03.04.2003 Merkel Patientengut 1382 Patienten mit Rektumkarzinom
Was ist Strahlentherapie?
 Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
SRH Wald-Klinikum Gera ggmbh
 SRH Wald-Klinikum Gera ggmbh PET-CT Bestrahlungsplanung bei Patienten mit Bronchialkarzinom Monat Jahr von Dr. med. J. Pagel Prof. Dr. med. R.P. Baum* Dipl.- Phys. M. Schöpe PD Dr. med. K.-H. Kloetzer
SRH Wald-Klinikum Gera ggmbh PET-CT Bestrahlungsplanung bei Patienten mit Bronchialkarzinom Monat Jahr von Dr. med. J. Pagel Prof. Dr. med. R.P. Baum* Dipl.- Phys. M. Schöpe PD Dr. med. K.-H. Kloetzer
Tumor des Gebärmutterhalses (Zervixtumor) (1)
 Tumor des Gebärmutterhalses (Zervixtumor) (1) Epidemiologie: Die Inzidenz des Zervixkarzinoms wird vom Robert-Koch-Institut für 2004 mit 14,7 pro 100 000 Frauen pro Jahr angegeben (rohe Rate+). Eine Abnahme
Tumor des Gebärmutterhalses (Zervixtumor) (1) Epidemiologie: Die Inzidenz des Zervixkarzinoms wird vom Robert-Koch-Institut für 2004 mit 14,7 pro 100 000 Frauen pro Jahr angegeben (rohe Rate+). Eine Abnahme
Postoperative Bestrahlung nach Mastektomie und brusterhaltender Operation: Vergleich prognostischer Faktoren und Bedeutung des Lokalrezidivs.
 Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. Jürgen Dunst) Postoperative Bestrahlung nach Mastektomie und brusterhaltender
Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. Jürgen Dunst) Postoperative Bestrahlung nach Mastektomie und brusterhaltender
Leitlinie Bronchialkarzinom 2011 IOZ Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009
 Nr 27724 Version 1-0-0 Datum 29.08.11 Seite 1 von 5 Leitlinie Bronchialkarzinom 2011 Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009 Tab.1: Beschreibung der TNM-Parameter
Nr 27724 Version 1-0-0 Datum 29.08.11 Seite 1 von 5 Leitlinie Bronchialkarzinom 2011 Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009 Tab.1: Beschreibung der TNM-Parameter
Chirurgische Therapie des Ösophagus- und Magenkarzinoms Was gibt es Neues? A.H. Hölscher
 Chirurgische Therapie des Ösophagus- und Magenkarzinoms Was gibt es Neues? A.H. Hölscher Wiesbaden, 07. Juli 2012 Was gibt es Neues? Ösophagus Frühkarzinome des Ösophagus Minimal-invasive Ösophagektomie
Chirurgische Therapie des Ösophagus- und Magenkarzinoms Was gibt es Neues? A.H. Hölscher Wiesbaden, 07. Juli 2012 Was gibt es Neues? Ösophagus Frühkarzinome des Ösophagus Minimal-invasive Ösophagektomie
Diagnostik und Therapie primärer und metastasierter Mammakarzinome
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Aktuelle Studie zeigt positive Effekte präoperativer Maßnahmen bei zuvor nicht operablen Tumoren
 Neoadjuvante Therapie bei Pankreaskrebs Aktuelle Studie zeigt positive Effekte präoperativer Maßnahmen bei zuvor nicht operablen Tumoren Patienten mit nicht operablen Pankreastumoren profitieren von einer
Neoadjuvante Therapie bei Pankreaskrebs Aktuelle Studie zeigt positive Effekte präoperativer Maßnahmen bei zuvor nicht operablen Tumoren Patienten mit nicht operablen Pankreastumoren profitieren von einer
Team Prim. Prof. Dr. Wolfgang Eisterer Malignome von Ösophagus, Magen, Dünndarm, Leber und Galle. Aktuelle Aspekte aus der Chirurgischen Onkologie
 Team Prim. Prof. Dr. Wolfgang Eisterer Malignome von Ösophagus, Magen, Dünndarm, Leber und Galle Aktuelle Aspekte aus der Chirurgischen Onkologie Prim. Assoz. Prof. PD Dr. Matthias Zitt Chirurgie, KH Dornbirn
Team Prim. Prof. Dr. Wolfgang Eisterer Malignome von Ösophagus, Magen, Dünndarm, Leber und Galle Aktuelle Aspekte aus der Chirurgischen Onkologie Prim. Assoz. Prof. PD Dr. Matthias Zitt Chirurgie, KH Dornbirn
Adjuvante und neoadjuvante Therapie beim KRK. PD Dr. med. Christian Pox Bremen
 10. addz - Jahrestagung Adjuvante und neoadjuvante Therapie beim KRK PD Dr. med. Christian Pox Bremen S3 Leitlinie Kolorektales Karzinom 2017 Update 2017 Themenkomplex I Themenkomplex II Themenkomplex
10. addz - Jahrestagung Adjuvante und neoadjuvante Therapie beim KRK PD Dr. med. Christian Pox Bremen S3 Leitlinie Kolorektales Karzinom 2017 Update 2017 Themenkomplex I Themenkomplex II Themenkomplex
Statistische Untersuchungen zur onkologischen Qualitätskontrolle anhand von Daten des Brandenburgischen Tumorzentrums
 Aus dem Institut für Pathologie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. S. Hauptmann) Statistische Untersuchungen zur onkologischen Qualitätskontrolle anhand von Daten
Aus dem Institut für Pathologie an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. S. Hauptmann) Statistische Untersuchungen zur onkologischen Qualitätskontrolle anhand von Daten
Ösophagus. 3.2 Ösophaguskarzinom
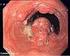 55 3.2 karzinom Das karzinom ist mit einer Inzidenzrate von ca. 8 je 100.000 bzw. 2% aller Krebsneuerkrankungen bei Männern und 2,1 bzw. 0,4% bei Frauen eine seltene Erkrankungsform. 82% der Erkrankten
55 3.2 karzinom Das karzinom ist mit einer Inzidenzrate von ca. 8 je 100.000 bzw. 2% aller Krebsneuerkrankungen bei Männern und 2,1 bzw. 0,4% bei Frauen eine seltene Erkrankungsform. 82% der Erkrankten
Aspekte zur Indikation und Auswahl der Radiotherapie
 Aspekte zur Indikation und Auswahl der Radiotherapie Kurative oder palliative Therapie (medianes Überleben 1 2 Jahre) Zielvolumen Sequenz Neoadjuvant (vor OP) Postoperativ adjuvant Definitiv bei Inoperabilität
Aspekte zur Indikation und Auswahl der Radiotherapie Kurative oder palliative Therapie (medianes Überleben 1 2 Jahre) Zielvolumen Sequenz Neoadjuvant (vor OP) Postoperativ adjuvant Definitiv bei Inoperabilität
2 Material und Methoden 2.1 Patienten
 2 Material und Methoden 2.1 Patienten In der Studie der Ostdeutschen Arbeitsgruppe für Leistungserfassung und Qualitätssicherung in der Chirurgie wurden in dem Zeitraum vom 1.1.1998 bis 31.12.1998 insgesamt
2 Material und Methoden 2.1 Patienten In der Studie der Ostdeutschen Arbeitsgruppe für Leistungserfassung und Qualitätssicherung in der Chirurgie wurden in dem Zeitraum vom 1.1.1998 bis 31.12.1998 insgesamt
Einfluss der Niedrigdosisbelastung (V10) auf das Pneumonitisrisiko bei thorakaler Bestrahlung
 Einfluss der Niedrigdosisbelastung (V10) auf das Pneumonitisrisiko bei thorakaler Bestrahlung M. Becker-Schiebe 1, M. Renz 1, H. Christiansen 2, W. Hoffmann 1 1 Klinik für Radioonkologie und Strahlentherapie
Einfluss der Niedrigdosisbelastung (V10) auf das Pneumonitisrisiko bei thorakaler Bestrahlung M. Becker-Schiebe 1, M. Renz 1, H. Christiansen 2, W. Hoffmann 1 1 Klinik für Radioonkologie und Strahlentherapie
Ösophagogastraler Übergang
 7 Ösophagogastraler Übergang Jörg-Stephan Müller M. Heise (Hrsg.), Viszeralchirurgie Fragen und Antworten, DOI 10.1007/978--642-54761-4_, Springer-Verlag Berlin Heidelberg 2015 7. Welche der folgenden
7 Ösophagogastraler Übergang Jörg-Stephan Müller M. Heise (Hrsg.), Viszeralchirurgie Fragen und Antworten, DOI 10.1007/978--642-54761-4_, Springer-Verlag Berlin Heidelberg 2015 7. Welche der folgenden
Die stereotaktische Bestrahlung von Lungentumoren
 Hypofraktionierung Innovation oder Risiko? Die stereotaktische Bestrahlung von Lungentumoren Frank Zimmermann Institut für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch;
Hypofraktionierung Innovation oder Risiko? Die stereotaktische Bestrahlung von Lungentumoren Frank Zimmermann Institut für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel zimmermannf@uhbs.ch;
Strahlentherapie & Nuklearmedizin. Lungenkarzinom. Prof. Michael Flentje, Heribert Hänscheid, Prof. Andreas Buck
 Strahlentherapie & Nuklearmedizin Lungenkarzinom. Prof. Michael Flentje, Heribert Hänscheid, Prof. Andreas Buck Definitive Radiochemotherapie Gesamtdosis 66 Gy mit Einzeldosis 2 Gy (6.5Wochen) Cisplatin/Vinorelbine
Strahlentherapie & Nuklearmedizin Lungenkarzinom. Prof. Michael Flentje, Heribert Hänscheid, Prof. Andreas Buck Definitive Radiochemotherapie Gesamtdosis 66 Gy mit Einzeldosis 2 Gy (6.5Wochen) Cisplatin/Vinorelbine
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016 männlich
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016 männlich
Tumor des Gebärmutterkörpers (1)
 Tumor des Gebärmutterkörpers (1) Epidemiologie: Das Korpuskarzinom (auch Endometriumkarzinom) ist der häufigste weibliche Genitaltumor. Das Robert-Koch-Institut gibt die Inzidenz in Deutschland für 2004
Tumor des Gebärmutterkörpers (1) Epidemiologie: Das Korpuskarzinom (auch Endometriumkarzinom) ist der häufigste weibliche Genitaltumor. Das Robert-Koch-Institut gibt die Inzidenz in Deutschland für 2004
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015 männlich
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2011-2015 männlich
Klassifikation Tumorstadium
 Klassifikation Tumorstadium Klinische Klassifikation Tumorstadium mit Details, Performance Status Tumorstadien TNM Klassifikation, Staging, G-Grading, Zusätzliche Kennzeichen, C-Faktor, optionale Deskriptoren
Klassifikation Tumorstadium Klinische Klassifikation Tumorstadium mit Details, Performance Status Tumorstadien TNM Klassifikation, Staging, G-Grading, Zusätzliche Kennzeichen, C-Faktor, optionale Deskriptoren
Absolute Neuerkrankungen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016 männlich
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate alterstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016 männlich
Originalarbeit: James et al., N Engl J Med 2012; 366:
 Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Originalarbeit: James et al., N Engl J Med 2012; 366: 1477-1488 Kommentar zur Originalarbeit: Shipley & Zietman N Engl J Med 2012; 366: 1540-41 Meilenstein BC2001-Studie: Design randomisierte Studie mit
Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION
 Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION Thema: Entscheidungskriterien vor radikaler Prostatektomie Eine retrospektive Untersuchung der Daten von 427 Patienten
Aus der Klinik für Urologie des Vivantes Klinikums im Friedrichshain Berlin DISSERTATION Thema: Entscheidungskriterien vor radikaler Prostatektomie Eine retrospektive Untersuchung der Daten von 427 Patienten
Plattenepithelkarzinom des Ösophagus
 Plattenepithelkarzinom des Ösophagus Stand Juni 2017 Obligate Diagnostik Entscheidung Stadium Entscheidung Klinisches Stadium ct1 Seite 2 Anamnese/Klinische Untersuchung ÖGD mit Biopsie/Histologie Endoskopie/EUS
Plattenepithelkarzinom des Ösophagus Stand Juni 2017 Obligate Diagnostik Entscheidung Stadium Entscheidung Klinisches Stadium ct1 Seite 2 Anamnese/Klinische Untersuchung ÖGD mit Biopsie/Histologie Endoskopie/EUS
Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr
 Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr Klinik für Allgemein-, Visceral- und Transplantationschirurgie Charité, Campus Virchow-Klinikum Universitätsmedizin
Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr Klinik für Allgemein-, Visceral- und Transplantationschirurgie Charité, Campus Virchow-Klinikum Universitätsmedizin
Bronchus - Karzinom. Bronchus - Karzinom. 2. Screening. Bronchus Karzinom - Allgemein. 1. Einleitung allgemeine Informationen. 3.
 Bronchus - Karzinom J. Barandun LungenZentrum Hirslanden Zürich Screening Abklärung - Therapie Bronchus - Karzinom 1. Einleitung allgemeine Informationen 2. Screening 3. Abklärung 4. Therapie Bronchus
Bronchus - Karzinom J. Barandun LungenZentrum Hirslanden Zürich Screening Abklärung - Therapie Bronchus - Karzinom 1. Einleitung allgemeine Informationen 2. Screening 3. Abklärung 4. Therapie Bronchus
Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation?
 Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation? H.-S. Hofmann Thoraxchirurgisches Zentrum Universitätsklinikum Regensburg Krankenhaus Barmherzige Brüder Regensburg Problem:
Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation? H.-S. Hofmann Thoraxchirurgisches Zentrum Universitätsklinikum Regensburg Krankenhaus Barmherzige Brüder Regensburg Problem:
1 Einleitung Das Mammakarzinom Epidemiologie Ätiologie Risikofaktoren Protektive Faktoren 3
 Inhaltsverzeichnis 1 Einleitung 1 1.1 Das Mammakarzinom 1 1.1.1 Epidemiologie 1 1.1.2 Ätiologie 2 1.1.2.1 Risikofaktoren 2 1.1.2.2 Protektive Faktoren 3 1.1.3 Prognosefaktoren 4 1.2 Rezeptorstatus 5 1.2.1
Inhaltsverzeichnis 1 Einleitung 1 1.1 Das Mammakarzinom 1 1.1.1 Epidemiologie 1 1.1.2 Ätiologie 2 1.1.2.1 Risikofaktoren 2 1.1.2.2 Protektive Faktoren 3 1.1.3 Prognosefaktoren 4 1.2 Rezeptorstatus 5 1.2.1
Radioonkologie ( ) Therapieoptionen gegen den Krebs. Frank Zimmermann und Mitarbeiter
 Radioonkologie ( 13.1.4.15 ) Therapieoptionen gegen den Krebs Frank Zimmermann und Mitarbeiter Institut für Radioonkologie, Universitätsspital Basel Petersgraben 4, CH 4031 Basel radioonkologie basel Was
Radioonkologie ( 13.1.4.15 ) Therapieoptionen gegen den Krebs Frank Zimmermann und Mitarbeiter Institut für Radioonkologie, Universitätsspital Basel Petersgraben 4, CH 4031 Basel radioonkologie basel Was
Radiochemotherapie des nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT
 Radiochemotherapie des Nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT W. Huhnt Ruppiner Kliniken GmbH, Klinik für Strahlentherapie und Radioonkologie, Neuruppin GLIEDERUNG Einleitung: Überblick
Radiochemotherapie des Nichtkleinzelligen Bronchialkarzinoms mit und ohne IMRT W. Huhnt Ruppiner Kliniken GmbH, Klinik für Strahlentherapie und Radioonkologie, Neuruppin GLIEDERUNG Einleitung: Überblick
Seite Diskussion
 Seite 99 4 Diskussion In der Behandlung lokal fortgeschrittener oder inflammatorischer Mammakarzinome gilt die neoadjuvante Chemotherapie schon lange als Standard. Dass diese Therapieform in Hinblick auf
Seite 99 4 Diskussion In der Behandlung lokal fortgeschrittener oder inflammatorischer Mammakarzinome gilt die neoadjuvante Chemotherapie schon lange als Standard. Dass diese Therapieform in Hinblick auf
Auslegungshinweise Kennzahlenbogen Darm (Stand ) - basierend auf dem Erhebungsbogen vom
 Allgemeine Anmerkungen In dem Dokument Auslegungshinweise Kennzahlenbogen Darm werden weitergehende ErlÄuterungen zu den einzelnen Kennzahlen gemacht. Dieses Dokument befindet sich im Moment in Diskussion
Allgemeine Anmerkungen In dem Dokument Auslegungshinweise Kennzahlenbogen Darm werden weitergehende ErlÄuterungen zu den einzelnen Kennzahlen gemacht. Dieses Dokument befindet sich im Moment in Diskussion
Radio-(Chemo)-Therapie. des Rektumkarzinoms
 Radio-(Chemo)-Therapie des Rektumkarzinoms A. Liebmann 17.01.2012 Häufigkeitsverteilung Tumorausbreitung CT : tiefsitzendes Rektumkarzinom mit pararektaler LK-Metastase Chirurgie des Mesorektums Indikationen
Radio-(Chemo)-Therapie des Rektumkarzinoms A. Liebmann 17.01.2012 Häufigkeitsverteilung Tumorausbreitung CT : tiefsitzendes Rektumkarzinom mit pararektaler LK-Metastase Chirurgie des Mesorektums Indikationen
Verbessert die neue TNM-Klassifikation die Prognoseabschätzung be Tumoren des oberen Gastrointestinaltraktes?
 Aus der Chirurgischen Universitätsklinik Heidelberg Abteilung für Allgemein-,Viszeral-,und Transplantationschirurgie Ärztlicher Direktor. Professor Dr D r h.c. Markus N. Büchler Verbessert die neue TNM-Klassifikation
Aus der Chirurgischen Universitätsklinik Heidelberg Abteilung für Allgemein-,Viszeral-,und Transplantationschirurgie Ärztlicher Direktor. Professor Dr D r h.c. Markus N. Büchler Verbessert die neue TNM-Klassifikation
Magenkrebs (1) Klinisches Krebsregister Kodierhilfe - Stand September Epidemiologie:
 Magenkrebs (1) Epidemiologie: Der Magenkrebs gehört zu den häufigen Krebserkrankungen. Die Inzidenz ist seit 30 Jahren rückläufig, ausgenommen die Tumoren des ösophagogastralen Übergangs, die zunehmen.
Magenkrebs (1) Epidemiologie: Der Magenkrebs gehört zu den häufigen Krebserkrankungen. Die Inzidenz ist seit 30 Jahren rückläufig, ausgenommen die Tumoren des ösophagogastralen Übergangs, die zunehmen.
Strahlentherapie des Endometriumkarzinoms. Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg
 Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Strahlentherapie des Endometriumkarzinoms Aktuelle Studienlage
Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Strahlentherapie des Endometriumkarzinoms Aktuelle Studienlage
Lungentumoren Frank Zimmermann Klinik für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel radioonkologiebasel.
 Lungentumoren Frank Zimmermann Klinik für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel radioonkologiebasel.ch Heutige Lernziele C IM 240 lung carcinoma 2 C SU 94 C RN 4 types of
Lungentumoren Frank Zimmermann Klinik für Radioonkologie Universitätsspital Basel Petersgraben 4 CH 4031 Basel radioonkologiebasel.ch Heutige Lernziele C IM 240 lung carcinoma 2 C SU 94 C RN 4 types of
Verruköses Karzinom des Ösophagus, nicht metastasierend aber infiltrierend
 Verruköses Karzinom des Ösophagus, nicht metastasierend aber infiltrierend Ulrich Peitz, Medizinische Klinik 2, Raphaelsklinik Münster Vieth M, Institut für Pathologie, Klinikum Bayreuth Kuhnen C, Institut
Verruköses Karzinom des Ösophagus, nicht metastasierend aber infiltrierend Ulrich Peitz, Medizinische Klinik 2, Raphaelsklinik Münster Vieth M, Institut für Pathologie, Klinikum Bayreuth Kuhnen C, Institut
3.2 Speiseröhre. Kernaussagen
 ICD-10 C15 Ergebnisse zur 21 3.2 Speiseröhre Kernaussagen Inzidenz und Mortalität: In Deutschland erkrankten nach der tausendwende pro etwa 1.050 und 3.900 an Speiseröhrenkrebs. Seit 1980 waren die Erkrankungs-
ICD-10 C15 Ergebnisse zur 21 3.2 Speiseröhre Kernaussagen Inzidenz und Mortalität: In Deutschland erkrankten nach der tausendwende pro etwa 1.050 und 3.900 an Speiseröhrenkrebs. Seit 1980 waren die Erkrankungs-
Aktuelles zur Pathologie von Pankreastumoren einschließlich neuroendokriner Tumoren
 Aktuelles zur Pathologie von Pankreastumoren einschließlich neuroendokriner Tumoren Prof. Dr. med. Andrea Tannapfel Institut für Pathologie, Ruhr-Universität Bochum Neuroendokrine Tumoren: Einheitliche
Aktuelles zur Pathologie von Pankreastumoren einschließlich neuroendokriner Tumoren Prof. Dr. med. Andrea Tannapfel Institut für Pathologie, Ruhr-Universität Bochum Neuroendokrine Tumoren: Einheitliche
Stellenwert von neoadjuvanten und adjuvanten, perioperativen Therapiestrategien bei gastroösophagealen Tumoren
 Stellenwert von neoadjuvanten und adjuvanten, perioperativen Therapiestrategien bei gastroösophagealen Tumoren Prof. Dr. S.-E. Al-Batran Krankenhaus Nordwest UCT University Cancer Center Frankfurt Offenlegung
Stellenwert von neoadjuvanten und adjuvanten, perioperativen Therapiestrategien bei gastroösophagealen Tumoren Prof. Dr. S.-E. Al-Batran Krankenhaus Nordwest UCT University Cancer Center Frankfurt Offenlegung
Strahlentherapie des Endometriumkarzinoms. Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg
 Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Übersicht Aktuelle Empfehlungen: risikoadaptierter Einsatz der
Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Übersicht Aktuelle Empfehlungen: risikoadaptierter Einsatz der
Harnröhrentumor (1) D09.1 Carcinoma in situ sonstiger und nicht näher bezeichneter Harnorgane
 Harnröhrentumor (1) Epidemiologie: Malignome der Urethra sind sehr selten. Ihre Inzidenz pro 100 000 Einwohner und Jahr wird auf 0,4 bei Männern und 1,5 bei Frauen geschätzt. Frauen sind aufgrund ihrer
Harnröhrentumor (1) Epidemiologie: Malignome der Urethra sind sehr selten. Ihre Inzidenz pro 100 000 Einwohner und Jahr wird auf 0,4 bei Männern und 1,5 bei Frauen geschätzt. Frauen sind aufgrund ihrer
Krebs der großen Speicheldrüsen (1)
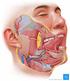 Krebs der großen Speicheldrüsen (1) Epidemiologie: Nur etwa 0,3 % aller Tumoren sind epitheliale Speicheldrüsentumoren mit einer geschätzten Inzidenz von 1-3 pro 100 000 Einwohner pro Jahr. Sie kommen
Krebs der großen Speicheldrüsen (1) Epidemiologie: Nur etwa 0,3 % aller Tumoren sind epitheliale Speicheldrüsentumoren mit einer geschätzten Inzidenz von 1-3 pro 100 000 Einwohner pro Jahr. Sie kommen
So gut wie noch nie und bei jedem Tumortyp: Heilung und Palliation mit perfekter Strahlentherapie
 So gut wie noch nie und bei jedem Tumortyp: Heilung und Palliation mit perfekter Strahlentherapie Klinik für Strahlentherapie und Radioonkologie und MVZ Lörrach Prof. Dr. Frank Zimmermann und Mitarbeiter
So gut wie noch nie und bei jedem Tumortyp: Heilung und Palliation mit perfekter Strahlentherapie Klinik für Strahlentherapie und Radioonkologie und MVZ Lörrach Prof. Dr. Frank Zimmermann und Mitarbeiter
kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ
 WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
D i s s e r t a t i o n. zur Erlangung des akademischen Grades Doktor der Zahnmedizin (Dr. med. dent.)
 Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. D. Vordermark Klinische Untersuchungen der Speicheldrüsenfunktion
Aus der Universitätsklinik und Poliklinik für Strahlentherapie an der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. D. Vordermark Klinische Untersuchungen der Speicheldrüsenfunktion
Rückmeldungen der klinischen Krebsregister an ihre meldenden Ärzte und Institutionen
 Rückmeldungen der klinischen Krebsregister an ihre meldenden Ärzte und Institutionen Klinische Beispiele Modul Kolorektales Karzinom klinikspezifische Rückmeldung regionale Rückmeldung (Benchmarking) bundesweite
Rückmeldungen der klinischen Krebsregister an ihre meldenden Ärzte und Institutionen Klinische Beispiele Modul Kolorektales Karzinom klinikspezifische Rückmeldung regionale Rückmeldung (Benchmarking) bundesweite
Schilddrüsenkrebs (1)
 Schilddrüsenkrebs (1) Epidemiologie: Schilddrüsenkrebs gehört zu den seltenen Tumoren. Die Inzidenzzahlen werden vom Robert-Koch- Institut für Deutschland 4,0 bei Männern und 6,1 bei Frauen pro 100 000
Schilddrüsenkrebs (1) Epidemiologie: Schilddrüsenkrebs gehört zu den seltenen Tumoren. Die Inzidenzzahlen werden vom Robert-Koch- Institut für Deutschland 4,0 bei Männern und 6,1 bei Frauen pro 100 000
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung. Universitäts- Klinikum Jena
 Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN
 DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Analtumor (1) D01.3 Carcinoma in situ des Analkanals und des Anus (ohne Haut)
 Analtumor (1) Epidemiologie: Das Analkarzinom tritt eher selten auf. Insgesamt erkranken in Deutschland pro Jahr 0,5-1,5 pro 100.000 Einwohner daran, mit steigender Tendenz. Frauen sind etwa dreimal so
Analtumor (1) Epidemiologie: Das Analkarzinom tritt eher selten auf. Insgesamt erkranken in Deutschland pro Jahr 0,5-1,5 pro 100.000 Einwohner daran, mit steigender Tendenz. Frauen sind etwa dreimal so
Strahlentherapie bei Lungenkrebs
 Basiskurs Krebswissen Sommer 2018 Strahlentherapie bei Lungenkrebs 1 Joachim Widder, UK Strahlentherapie Lungenkrebs (Bronchuskarzinom) Ursachen, Häufigkeit Histologische (feingewebliche) Typen Stadieneinteilung
Basiskurs Krebswissen Sommer 2018 Strahlentherapie bei Lungenkrebs 1 Joachim Widder, UK Strahlentherapie Lungenkrebs (Bronchuskarzinom) Ursachen, Häufigkeit Histologische (feingewebliche) Typen Stadieneinteilung
Nachsorge und adjuvante Chemotherapie des Dickdarmkarzinoms. Sankt Marien-Hospital Buer
 Nachsorge und adjuvante Chemotherapie des Dickdarmkarzinoms Grundlagen und Ziele Nachsorgemethoden Wertigkeit der Nachsorgetests Stadienadaptierte Nachsorgepläne Adjuvante Chemotherapie Leitliniengemässe
Nachsorge und adjuvante Chemotherapie des Dickdarmkarzinoms Grundlagen und Ziele Nachsorgemethoden Wertigkeit der Nachsorgetests Stadienadaptierte Nachsorgepläne Adjuvante Chemotherapie Leitliniengemässe
Ersetzen fehlender Werte bei der Tumorstadienverteilung nach UICC
 Ersetzen fehlender Werte bei der Tumorstadienverteilung nach UICC Klaus Kraywinkel, A.Katalinic Epidemiologische Krebsregister NRW, Schleswig-Holstein Hintergrund Tumorstadienverteilung in bevölkerungsbezogenen
Ersetzen fehlender Werte bei der Tumorstadienverteilung nach UICC Klaus Kraywinkel, A.Katalinic Epidemiologische Krebsregister NRW, Schleswig-Holstein Hintergrund Tumorstadienverteilung in bevölkerungsbezogenen
Bundesweite Onkologische Qualitätskonferenz - Kolorektales Karzinom-
 Bundesweite Onkologische Qualitätskonferenz - Kolorektales Karzinom- S. Benz, M. Gerken, M. Klinkhammer-Schalke Klink f. Allgemein-, Viszeral und Kinderchirurgie Böblingen-Sindelfingen Tumorzentrum Regensburg
Bundesweite Onkologische Qualitätskonferenz - Kolorektales Karzinom- S. Benz, M. Gerken, M. Klinkhammer-Schalke Klink f. Allgemein-, Viszeral und Kinderchirurgie Böblingen-Sindelfingen Tumorzentrum Regensburg
GRENZBEREICHE VISZERALER CHIRURGIE. Reinhold Függer Allgemein-, Viszeral-, Thorax-, Gefäß- und Transplantationschirurgie, Ordensklinikum Linz
 GRENZBEREICHE VISZERALER CHIRURGIE Reinhold Függer Allgemein-, Viszeral-, Thorax-, Gefäß- und Transplantationschirurgie, Ordensklinikum Linz GRENZEN Innerhalb der Chirurgie: Minimal invasiv konventionell
GRENZBEREICHE VISZERALER CHIRURGIE Reinhold Függer Allgemein-, Viszeral-, Thorax-, Gefäß- und Transplantationschirurgie, Ordensklinikum Linz GRENZEN Innerhalb der Chirurgie: Minimal invasiv konventionell
Thomas G. Wendt Stand 31. Januar 2013
 Thomas G. Wendt Stand 31. Januar 2013 Prätherapeutisch: Posttherapeutisch: FIGO ptnm (UICC) ( Féderation Internationale de Gynécologie et d Obstétrique) TNM (UICC) (UICC= Union International Contre le
Thomas G. Wendt Stand 31. Januar 2013 Prätherapeutisch: Posttherapeutisch: FIGO ptnm (UICC) ( Féderation Internationale de Gynécologie et d Obstétrique) TNM (UICC) (UICC= Union International Contre le
NSCLC: Diagnostik. PD Dr. med. F. Griesinger Abtl. Hämatologie und Onkologie Universität Göttingen
 NSCLC: Diagnostik PD Dr. med. F. Griesinger Abtl. Hämatologie und Onkologie Universität Göttingen Bronchialkarzinom Inzidenz: weltweit Jährliche Alters-bezogene Inzidenz des Bronchial-Karzinoms/100.000
NSCLC: Diagnostik PD Dr. med. F. Griesinger Abtl. Hämatologie und Onkologie Universität Göttingen Bronchialkarzinom Inzidenz: weltweit Jährliche Alters-bezogene Inzidenz des Bronchial-Karzinoms/100.000
Untersuchungen zur Qualität von Diagnostik und Therapieentscheidung bei Patienten mit operablem Nichtkleinzelligem Bronchialkarzinom
 Aus der Universitätsklinik für Innere Medizin II (Direktor: Prof. Dr. med. habil. B. Osten) und dem Institut für Medizinische Epidemiologie, Biometrie und Informatik (Direktor: Prof. Dr. J. Haerting) der
Aus der Universitätsklinik für Innere Medizin II (Direktor: Prof. Dr. med. habil. B. Osten) und dem Institut für Medizinische Epidemiologie, Biometrie und Informatik (Direktor: Prof. Dr. J. Haerting) der
Feedbackbericht. DMP Brustkrebs. der. Gemeinsamen Einrichtung GE-DMP-BK-BB. für die Region Brandenburg
 Feedbackbericht DMP Brustkrebs der Gemeinsamen Einrichtung GE-DMP-BK-BB für die Region Brandenburg Berichtszeitraum 01.01.2010 31.12.2010 Feedback-Bericht DMP Brustkrebs für den Zeitraum vom 01.01.2010
Feedbackbericht DMP Brustkrebs der Gemeinsamen Einrichtung GE-DMP-BK-BB für die Region Brandenburg Berichtszeitraum 01.01.2010 31.12.2010 Feedback-Bericht DMP Brustkrebs für den Zeitraum vom 01.01.2010
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom
 Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Gute Überlebensqualität Trastuzumab beim metastasierten Magenkarzinom München (24. April 2012) - Mit dem monoklonalen Antikörper Trastuzumab (Herceptin ) steht bislang die einzige zielgerichtete Substanz
Innovative Diagnostik des Bronchialkarzinoms. Was leisten die neuen Methoden?
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN II Innovative Diagnostik des Bronchialkarzinoms. Was leisten die neuen Methoden? Christian Schulz Klinik und Poliklinik für Innere Medizin II Universität Regensburg
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN II Innovative Diagnostik des Bronchialkarzinoms. Was leisten die neuen Methoden? Christian Schulz Klinik und Poliklinik für Innere Medizin II Universität Regensburg
Strahlentherapieplanung
 FDG-PET/CT in der Strahlentherapieplanung Viola Duncker-Rohr Klinik für Strahlenheilkunde Universitätsklinikum Freiburg PET in der Strahlentherapie-Planung - Diagnostisch zuverlässige(re) Darstellung der
FDG-PET/CT in der Strahlentherapieplanung Viola Duncker-Rohr Klinik für Strahlenheilkunde Universitätsklinikum Freiburg PET in der Strahlentherapie-Planung - Diagnostisch zuverlässige(re) Darstellung der
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016
Absolute Neuerkrankungszahlen und Neuerkrankungsraten je Einwohner
 Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016
Durchschnittlich erfasste Erkrankungszahlen Zeitraum Geschlecht rohe Rate altersstandardisierte Rate (ESR)* arithm. Alter Jahre medianes Alter Jahre Vergleich medianes Alter Vergleichsquelle 2012-2016
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom
 Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Das Ösophaguskarzinom Diagnostik und interdisziplinäres Therapiekonzept
 Das Ösophaguskarzinom Diagnostik und interdisziplinäres Therapiekonzept von Th. Junginger, I. Gockel, W. Kneist und U. Gönner Ösophaguskarzinome gehören zu den seltenen Tumoren und ihre ungünstige Prognose
Das Ösophaguskarzinom Diagnostik und interdisziplinäres Therapiekonzept von Th. Junginger, I. Gockel, W. Kneist und U. Gönner Ösophaguskarzinome gehören zu den seltenen Tumoren und ihre ungünstige Prognose
Feedbackbericht. DMP Brustkrebs. der. Gemeinsamen Einrichtung GE-DMP-BK-BB. für die Region Brandenburg. Berichtszeitraum
 Feedbackbericht DMP Brustkrebs der Gemeinsamen Einrichtung GE-DMP-BK-BB für die Region Brandenburg Berichtszeitraum 01.01.2011 31.12.2011 DMP Brustkrebs_Feedbackbericht 2011 Feedback-Bericht DMP Brustkrebs
Feedbackbericht DMP Brustkrebs der Gemeinsamen Einrichtung GE-DMP-BK-BB für die Region Brandenburg Berichtszeitraum 01.01.2011 31.12.2011 DMP Brustkrebs_Feedbackbericht 2011 Feedback-Bericht DMP Brustkrebs
7. Tag der Organkrebszentren am Klinikum Dortmund Diagnostisches und therapeutisches Vorgehen beim Ösophaguskarzinom
 7. Tag der Organkrebszentren am Klinikum Dortmund Diagnostisches und therapeutisches Vorgehen beim Ösophaguskarzinom Dr. med. Bernd Kroes, Chirurgische Klinik, Klinikum Dortmund ggmbh Epidemiologie 4-5
7. Tag der Organkrebszentren am Klinikum Dortmund Diagnostisches und therapeutisches Vorgehen beim Ösophaguskarzinom Dr. med. Bernd Kroes, Chirurgische Klinik, Klinikum Dortmund ggmbh Epidemiologie 4-5
Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H.
 Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H. Dralle Gastric-banding als Operationsmethode bei morbider Adipositas
Aus der Klinik für Allgemein-, Viszeral- und Gefäßchirurgie der Martin-Luther-Universität Halle-Wittenberg Direktor: Prof. Dr. med. H. Dralle Gastric-banding als Operationsmethode bei morbider Adipositas
Operative und systemische Therapie des Endometriumkarzinoms
 Operative und systemische Therapie des Endometriumkarzinoms J. Huober Workshop DESO St.Gallen 20./21. Februar 2015 Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen
Operative und systemische Therapie des Endometriumkarzinoms J. Huober Workshop DESO St.Gallen 20./21. Februar 2015 Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen
Tabelle 11: AgNOR- und Zellparameter aller benignen Tumoren
 60 Tumor- Nr. Gesamtfläche Zahl/ Zelle [z/ - Quotient [z/µm²] höchste Zahl [z/nukl.] Kernfläche Nukleolenzahl [NZ/ Nuk.ges. [µm²/ 1 0,080 0,373 4,6 57,73 12,0 48,33 1,0 3,64 2 0,120 0,275 2,3 19,02 3,0
60 Tumor- Nr. Gesamtfläche Zahl/ Zelle [z/ - Quotient [z/µm²] höchste Zahl [z/nukl.] Kernfläche Nukleolenzahl [NZ/ Nuk.ges. [µm²/ 1 0,080 0,373 4,6 57,73 12,0 48,33 1,0 3,64 2 0,120 0,275 2,3 19,02 3,0
