Fluoreszenz. 2.1 Was ist Fluoreszenz? Der Fluoreszenz-Prozess
|
|
|
- Curt Kopp
- vor 6 Jahren
- Abrufe
Transkript
1 2 Fluoreszenz Die konfokale Mikroskopie wurde deshalb eine so erfolgreiche Technik, weil sie insbesondere in der Fluoreszenzmikroskopie eine ganz neue Dimension dem Beobachter zugänglich gemacht hat: nämlich die dritte Dimension. Darum soll hier das Phänomen der Fluoreszenz ausreichend Raum finden, da nicht nur die konfokale Mikroskopie, sondern auch die modernen Super- Hochauflösungsverfahren auf dieser Erscheinung aufbauen. 2.1 Was ist Fluoreszenz? Erste Beschreibungen von Fluoreszenz kennt man aus der Pflanzenwelt und von Mineralien. Zerreibungen stark chlorophyllhaltiger Blätter, wie sie zu pharmazeutischen Zwecken hergestellt werden, zeigen bei starkem Licht am Rand des Glasgefäßes eine rote Färbung. Auch Chininlösung bekannt als Tonic Water ist in der Durchsicht farblos, bekommt in heller Sonne aber einen blau-grünlichen Schimmer. Manche Flussspat-Sorten leuchten farbig, wenn man sie mit UV-Licht bestrahlt; die Farbe wird dabei durch die Verunreinigungen bestimmt. Besonders spektakuläre Fluoreszenz kann man an Uranylmineralien beobachten (Abb. 2.1). Systematisch untersucht wurden diese Erscheinungen erstmals durch G. G. Stokes, der dafür das Wort Fluoreszenz eingeführt hat. Es ist zusammengesetzt aus fluorspar (Flussspat) und luminescence (Leuchten). Stokes fand heraus, dass die Leuchterscheinungen immer mit einer Verschiebung der Wellenlänge einhergehen. UV-Strahlung wird zu blau, gelb oder grün, blaues Licht zu grün oder rot verschoben. Diese Änderung der Farbe nach längeren Wellenlängen (Rotverschiebung) wird daher Stokes-Verschiebung genannt. Wie kommt so etwas zustande? Der Fluoreszenz-Prozess Licht kann auf unterschiedliche Weise mit Materie wechselwirken. Zwei dieser Wechselwirkungen, nämlich die Absorption und die spontane Emission spielen bei der Fluoreszenz eine Rolle. Wenn bei Bestrahlung mit Licht die Springer-Verlag Berlin Heidelberg 2016 R. T. Borlinghaus, Konfokale Mikroskopie in Weiß, DOI / _2
2 30 Konfokale Mikroskopie in Weiß Abb. 2.1 Autunit, ein fluoreszierender Uranglimmer, Ca[UO 2 PO 4 ] 2 10 H 2 O, hier ein Stück aus Portugal. a Aufnahme bei Tageslicht, b Beleuchtung mit einer Schwarzlichtglühlampe und Aufnahme durch einen gelben Langpassfilter. Die Autunitkristalle leuchten aufgrund der UV-angeregten Fluoreszenz hell gelblich-grün Photonen von den Elektronen eines Atoms oder Moleküls eingefangen werden, gehen diese Elektronensysteme in einen höheren Energiezustand über. Die Energiedifferenz entspricht genau der Energie des absorbierten Photons. Da es nur diskrete Energiezustände für die Elektronen gibt, muss das Licht Photonen mit passender Energie enthalten. Daher kommt es, dass Flussspat bei UV-Bestrahlung also mit Photonen hoher Energie leuchtet, aber nicht bei Bestrahlung mit blauem oder grünem Licht. Im Jablonski-Diagramm in Abb. 2.2 werden die Energiezustände durch Abstände in der Vertikalen dargestellt. Sinnbildlich wird bei Absorption das Elektron auf ein höheres Energieniveau gehoben, etwa so, wie man einen Stein vom Boden auf einen Tisch hebt. Auch hier hat der Stein am Ende ja mehr Energie als vorher. Vor der Absorption befinden sich die Moleküle im Grundzustand (G). Durch die Absorption gehen sie in einen angeregten Zustand (A) über. Wie man in der Zeichnung sieht, gibt es jeweils eine ganze Serie von Grundzuständen und angeregten Zuständen. Das hängt mit den Schwingungen der Atome in den Molekülen zusammen: Die Atome können allerlei Formen von Schwingungen gegeneinander ausführen, und auch dazu muss jeweils spezifisch viel Energie aufgenommen werden. Die Energiepakete die Quanten sind aber viel kleiner (deshalb sind diese Schwingungszustände so nahe beieinander). Schwingungsanregungen findet man typischerweise im infraroten Bereich (Wärmeschwingungen). Bei Raumtemperatur befinden sich die allermeisten Moleküle im untersten der Schwingungszustände. Die CARS- Mikroskopie (CARS: coherent anti-stokes Raman scattering) nutzt diese thermischen Schwingungszustände, um Bilder zu erzeugen, die nur von Molekülen mit genau vorgegebenen Schwingungsenergien stammen.
3 2 Fluoreszenz 31 A Absorption Emission (spontan) G Lebensdauer des angeregten Zustandes Abb. 2.2 Energieschema einer fluoreszierenden Spezies. Durch Absorption eines blauen Photons wird das Elektronensystem aus dem Grundzustand G in den angeregten Zustand A gehoben. Beide Zustände haben mehrere Unterzustände, die mit den Wärmebewegungen der Atome im Kristall oder im Molekül korrelieren. Wird das Molekül in einen der höheren Unterzustände angeregt, fällt es sehr schnell in den tiefsten Unterzustand von A und gibt dabei etwas Energie in Form von Wärme ab. Nach einiger Zeit nimmt das Molekül einen der Grundzustände an, wobei die Energiedifferenz in Form von Licht abgegeben wird. Da ein Teil schon als Wärme abgegeben wurde, haben die emittierten Photonen immer eine kleinere Energie als die absorbierten. Da es verschiedene Unterzustände gibt, in die sie zurückfallen können, ist die Energie bei jedem Ereignis unterschiedlich. Man erhält deshalb ein Emissionsspektrum Kommt nun ein passendesphoton dem Molekül ausreichend nahe (im Beispiel: blaues Licht), wird das Photon absorbiert und das Molekül in einen der Schwingungszustände des angeregten Zustandes angehoben (blauer Pfeil in Abb. 2.2), dann sickert das Molekül schnell in den untersten Schwingungszustand (gestrichelter Pfeil) und gibt dabei Wärme ab. Nach einer gewissen Zeit im angeregten Zustand wird die Energie in Form eines Photons wieder abgegeben, und das Molekül nimmt wieder den Grundzustand ein. Der Stein fällt vom Tisch. Dieser Übergang (grüner, gelber und roter Pfeil in Abb. 2.2) kann in irgendeinen der Schwingungszustände des Grundzustandes erfolgen. So wie hier beschrieben, spricht man von spontaner Emission. Es gibt alternativ noch die stimulierte Emission, die bei Lasern und bei der STED-Mikroskopie (STED: stimulated emission depletion) eine zentrale Rollespielt. Nach der Emission sickert auch hier der Zustand wieder in den tiefsten der Schwingungsserie.
4 32 Konfokale Mikroskopie in Weiß Farbenspiele Die Schwingungszustände in den üblichen Fluoreszenzmolekülen weisen eine sehr dichte Folge von Energieniveaus auf. Deshalb ist die Emission nicht eine Schar von einzelnen Linien, sondern mehr oder weniger kontinuierlich. Die Wahrscheinlichkeit, dass ein bestimmter Unterzustand erreicht wird, ist quantenmechanisch festgelegt und nicht für alle Unterzustände gleich. Aus diesem Grund ist die Farbe des emittierten Lichtes durch ein Emissionsspektrum zu beschreiben, das die Intensität in Abhängigkeit von der Wellenlänge anzeigt (Abb. 2.3). Sehr typisch sind ein etwas steilerer Anstieg auf der blauen Seite und eine weniger steile Abnahme im roten Bereich (es gibt natürlich auch Spektren, die völlig anders aussehen). Auf eine kurzwellige Anregung (im Beispiel: blau) erfolgt eine längerwellige Emission (im Beispiel: grün, gelb, rot). Durch das breite Band der möglichen Schwingungszustände in A können unterschiedliche Farben zur Anregung benutzt werden, solange die Photonen eine passende Energie besitzen. Das Farbband, das zur Anregung geeignet ist, ist das Anregungsspektrum (Abb. 2.4). Je wahrscheinlicher die Absorption einer bestimmten Farbe, desto höher ist hier der Wert im Anregungsspektrum. Auch die Emission kann in verschiede- Intensität (Häufigkeit) Energie Wellenlänge (λ) Abb. 2.3 Idealisiertes Emissionsspektrum. Die Anteile der verschiedenen Farben werden durch die Wahrscheinlichkeit eines Übergangs in einen der Unterzustände des Grundzustandes beschrieben. Diese Wahrscheinlichkeit ist eine Eigenschaft des fluoreszierenden Moleküls und quantenmechanisch festgelegt, kann aber durch die molekulare Umgebung beeinflusst werden. In diesem Beispiel ist die Emission von Photonen mit einer Energie sehr häufig, die einer Wellenlänge von etwa 500 nm entspricht. Die Emission wird daher grünlich erscheinen, da dieser Farbanteil am intensivsten ist. Nach Einstein ist die Energie E eines Photons proportional zur Frequenz und damit umgekehrt proportional zur Wellenlänge. So kommt es, dass in üblichen Spektren von links nach rechts die Energie abnimmt
5 2 Fluoreszenz 33 Intensität (Häufigkeit) HO O O COOH Anregungsspektrum Emissionsspektrum δλ Stokes sche Verschiebung Wellenlänge (nm) Abb. 2.4 Anregungsspektrum (blaue Kurve) und Emissionsspektrum (rote Kurve) des Farbstoffes Fluorescein (Strukturformel). Das Anregungsspektrum beschreibt die Wahrscheinlichkeit für die Absorption eines Photons in Abhängigkeit von dessen Energie (Farbe). Das Emissionsspektrum die Wahrscheinlichkeit, welche Energie subsequent abgestrahlt wird. Der Abstand der beiden Maxima wird als Stokes sche Verschiebung bezeichnet ne Schwingungszustände münden, das wird im Emissionsspektrum sichtbar. Die Werte im Emissionsspektrum entsprechen der relativen Helligkeit der abgestrahlten Farbe. Die schon erwähnte Stokes-Verschiebung beschreibt den Abstand der beiden Maxima. Reiner Flussspat ist durchsichtig und fluoresziert nicht. Es sind Verunreinigungen, die anregbare Elektronenzustände bewirken. Wir verstehen jetzt, wasin diesenkristallengeschieht: Nach der Anregung mit dem für uns nicht sichtbaren UV-Licht senden die durch Verunreinigungen entstandenen Stellen sichtbares Licht aus. Im Tonic-Water ist es das Chinin, das UV-Licht absorbiert und gelb-grünes Licht aussendet. Das pflanzliche Chlorophyll absorbiert blaues Licht und fluoresziert tiefrot. Es hat also eine sehr große Stokes- Verschiebung Lebensdauern Die Zeitspanne, die das Molekül im angeregten Zustand verbleibt, ist nicht vorhersagbar. Allerdings kann man eine typische Zeit angeben, so wie die
6 34 Konfokale Mikroskopie in Weiß N 0 N = N 0 *e -t/τ N 0/ 2 N 0/ e 0 t 1/2 τ 2t 1/2 3t 1/2 t Abb. 2.5 Exponentieller Zerfall angeregter Fluoreszenzmoleküle (rote Kurve). Die Fluoreszenz-Lebenszeit ist die charakteristische Zeit, mit der die verbliebene Anzahl der angeregten Zustände N nach einer anfänglichen Anregung eines Ensembles von N 0 Molekülen beschrieben wird. Dieser Zerfall ist vergleichbar mit radioaktivem Zerfall. Die Halbwertszeit t 1/2 ist mit über die Beziehung t 1/2 = ln(2) verknüpft. Ein Beispiel mit N 0 = 8 ist unter dem Graphen skizziert Halbwertszeit bei radioaktiven Substanzen. Diese mittlere Lebensdauer des angeregten Zustandes wird etwas lax als Fluoreszenz-Lebensdauer bezeichnet (Abb. 2.5). Man kann diese Lebensdauern messen und hat damit neben den spektralen Eigenschaften noch einen weiteren Parameter, mit dem man fluoreszierende Farbstoffe ( Fluorochrome ) charakterisieren kann. Die mittlere Lebenszeit hängt stark von der molekularen Umgebung des fluoreszierenden Stoffes ab, deshalb kann man aus Veränderungen der mittleren Lebenszeit auch auf solche Umgebungsparameter schließen. Es sind sogar Systeme entwickelt worden, bei denen ein Fluorochrom mit geeigneten anderen Molekülgruppen chemisch verbunden wurde, sodass eine Änderung beispielsweise einer Metabolitenkonzentration zu lokalen Änderungen der Umgebung des Fluorochroms führt und aus dessen Helligkeitsänderung dann auf die Konzentrationsänderungen des Metaboliten geschlossen werden kann. Misst man die Lebensdauern für jedes Bildelement, dann erhält man ein Lebenszeit-Bild (FLIM: fluorescence lifetime imaging). Weiter kann man auch in der STED-Mikroskopie durch Filterung der Lebenszeiten die Auflösung steuern, da die Intensität des Lichtes für die stimulierte Emission ja direkt die mittlere Lebenszeit beeinflusst.
7 2 Fluoreszenz 35 Fluoreszenz ist in der Natur weit verbreitet, wegen der geringen Intensität fällt sie uns aber meist nicht auf. 2.2 Mikroskopie mit Fluoreszenz Eine Verbindung der Fluoreszenzphänomene mit der Mikroskopie wurde Anfang des 20. Jahrhunderts durch A. Köhler angestoßen, der sich auch mit der fotografischen Dokumentation und mit Beleuchtungskonzepten im Mikroskop ausführlich auseinandergesetzt hat. Zunächst kam nur ultraviolettes Licht zur Anregung zum Einsatz, weshalb auch heute noch gelegentlich von UV-Beleuchtung gesprochen wird, wenn Beleuchtungseinrichtungen zur Fluoreszenz gemeint sind. UV-Anregung macht aber nur noch einen geringen TeilderPraxisaus,undderTrendgehteherzurinfrarotenSeitedesSpektrums. Das hängt einerseits damit zusammen, dass Optik für kürzere Wellenlängen sehr viel schwieriger und komplexer und damit auch teurer ist, und andererseits damit, dass bei längeren Wellenlängen die Streuung im Präparat schnell abnimmt. Mit roterem Licht wirdesalso möglich, viel tieferin inhomogene Präparate hineinzuschauen, das Präparat ist hier durchsichtiger. Aus ähnlichen Gründenbetreibtman Infrarot-Astronomie, um durch Staubwolken hindurch etwa in das Zentrum unseres Milchstraßensystems zu schauen. Die Intensität der Fluoreszenzemission ist in der Regel sehr viel schwächer alsdie des anregenden Lichtes. Typischerweise wenigstens um ein Zehntausendfaches. Deshalb muss bei der Trennung des Fluoreszenzlichtes vom Anregungslicht viel Aufwand betrieben werden, um ein Fluoreszenzbild ohne hellen Hintergrund zu erhalten. Zudem möchte man Schäden am Sensor (Kamera, Photonenvervielfacher, Auge) natürlich vermeiden. Dazu dienen Emissionsfilter. Sie helfen auch bei Mehrfachfluoreszenzfärbungen die Trennung der einzelnen Kanäle zu verbessern. Weitere Bestandteile des Fluoreszenzmikroskops sind Farbteiler für die Auflichtmikroskopie und Anregungsfilter. Letztere sorgen dafür, dass nur Licht im Bereich der Absorption auf das Präparat fallen kann. Alle diese Bauteile werden in den folgenden Abschnitten etwas näher beschrieben. Für die weiße Konfokalmikroskopie sind dort stufenlos einstellbare Elemente eingeführt worden, denen jeweils ein eigener Abschnitt gewidmet ist Leistungsverhältnisse von Anregungslicht und Emissionslicht. In der täglichen Praxis wird oft über mäßige Qualität von Fluoreszenzmessungen geklagt,insbesondere,wenn es sich um Bilder handelt. Daher werden
8 36 Konfokale Mikroskopie in Weiß in Werbebroschüren vorzugsweise sehr helle Beispiele abgebildet das gilt natürlichauchfürdieabb.2.1 in diesem Buch! Manche Geräte nutzen moderne Bildverarbeitungssoftware, um ein mäßiges Bild dennoch vorzeigbar zu machen. IndigitalenKamerasistdas heute kaum noch zu unterbinden und geschieht oft ohne Wissen und Einflussnahme des Benutzers. Im wissenschaftlichen Zusammenhang sind solche Verfälschungen durch Weichzeichnung und Interpolation natürlich völlig unangemessen, denn eine quantitative Auswertung der Intensitäten ist nach solchen Manipulationenin der Regel nicht mehr sinnvoll möglich. Es darf also ruhig etwas rauschen. Um ein Gefühl für die wirklichen Lichtverhältnisse zu bekommen, wollen wir ein Beispiel explizit vorführen, dann wird klar, dass eine Menge Technologie benötigt wird, wenn man ohne verfälschende Rechenverfahren ein brauchbares Bild erzeugen möchte. Wir wählen einen klassischen Fluoreszenzfarbstoff, beispielsweise Fluoreszein (Abb. 2.4). Der Einfachheit halber betrachten wir die Situation in einem konfokalen Mikroskop (Details hierzu folgen im Kap. 3). Was uns interessiert, ist die Intensität der Fluoreszenz, die wir aus dem konfokalen Volumen erhalten, wenn dieses von einer typischen Lichtmenge durchstrahlt wird. Um diese Intensität auszurechnen, benutzen wir das Lambert-Beer sche Gesetz (Abb. 2.6)zurAbsorptionE: E D lg I0 I 1 D " cd: (2.1) Abb. 2.6 Intensitätsabnahme des Anregungslichtes beim Durchgang durch ein absorbierendes Medium. Die Intensität sinkt exponentiell ab. Hier ist die Absorption sehr hoch gewählt. In vielen praktischen Situationen, bei sehr kleinen Konzentrationen, kann man die Abnahme linear annähern I 0 δi I = I 0 *10 -ε λ cd I 1 d
9 2 Fluoreszenz 37 Hier wird die eingestrahlte Intensität I 0 ins Verhältnis gesetzt zur durchgegangenen Intensität I 1 auf der anderen Seite der Messstrecke. Durch Absorption im Präparat ist I 1 kleiner als I 0, und die Differenz entspricht der Energie, die durch Anregung der Moleküle im Lichtweg abgezogen wird. Man findet, dass I 1 exponentiell abnimmt mit der Konzentration c der absorbierenden Spezies und der Schichtdicke d. Die Proportionalitätskonstante " ist abhängig von der Wellenlänge und eine Eigenschaft des absorbierenden Stoffes. Aus historischen Gründen sind die Absorptionskoeffizienten (auch: Extinktionskoeffizienten) meist für den dekadischen Logarithmus und für eine Schichtdicke von 1 cm tabelliert. In grober Näherung liegt der Extinktionskoeffizient für Fluoreszein an seinem Absorptionsmaximum 485 nm bei 10 5 ` cm 1 mol 1. Als Konzentration wählen wir eine einmikromolare Lösung (10 6 Mol ` 1 ), das ist eine typische Situation. Die Schichtdicke d in einem konfokalen Mikroskop können wir näherungsweise mit einem Mikrometer veranschlagen, das sind 10 4 cm und entspricht etwa der Ausdehnung der psf in z-richtung. So bekommen wir für den Term " cd den Wert =10 5. Das Lambert-Beer sche Gesetz lässt sich umschreiben zu: I 1 D I 0 10 " cd: (2.2) Daraus erhält man die Differenz der ein- und ausgestrahlten Intensität: D I 0 I 1 (2.3) D I " cd : (2.4) Und wenn wir die bekannten Zahlen von oben einsetzen, erhalten wir sofort: D 2; : (2.5) I 0 Das Intensitätsverhältnis liegt sehr nahe bei 1, die Intensitäten unterscheiden sich fast nicht. Das Licht wird demnach fast nicht abgeschwächt, weil die Absorption so gering ausfällt. Dieses fast liegt mit 0, in der Größenordnung von 1/ = Allerdings ist genau diese kleine Intensitätsdifferenz die Lichtmenge, die von den Fluoresceinmolekülen absorbiert wurde. Und wenn man nun davon ausgeht, dass alle Moleküle, die ein Photon absorbiert haben, auch ein Fluoreszenzphoton abgeben, dann ist eben 10 5 das Verhältnis des abgestrahlten zum eingestrahlten Anregungslicht. Die Annahme einer so effizienten Umsetzung von Anregung in Fluoreszenz ist für den Farbstoff Fluoreszein gerechtfertigt, da dessen Quantenausbeute nahe bei 1 liegt. Die Quantenausbeute beschreibt das Verhältnis von absorbierten
10 38 Konfokale Mikroskopie in Weiß Photonen zu in Fluoreszenz umgesetzten Photonen. Wir können also grob festhalten, dass die Intensität der Fluoreszenz in einem typischen Fall etwa eine Million Mal schwächer ist als das anregende Licht. Dass nur ein kleiner Teil der emittierten Fluoreszenzphotonen tatsächlich den Detektor erreichen wird, ist dabei noch gar nicht berücksichtigt Durchlicht- und Auflichtfluoreszenz Die ersten Mikroskope für Fluoreszenz waren Geräte, die aus dem Fundus der bis dahin verwendeten Technik umgebaut und für Fluoreszenz vorbereitet wurden. Das heißt, eine Lichtquelle durchstrahlt das Präparat, und man betrachtet auf der anderen Seite das entstandene Bild. Die bis dato benutzten Lichtquellen, nämlich Petroleumlampen, Glühlampen oder die Sonne, konnten für UV-Fluoreszenz nicht ohne Weiteres brauchbare Ergebnisse liefern. Selbst umfangreichere Sammlung und Bündelung des Lichtes führte nicht immer zu befriedigenden Ergebnissen. Daher wurden bald starke elektrische Bogenlampen eingesetzt. Diese Geräte erzeugen sehr hohe Lichtströme, nehmen gewaltige Leistungen im Kilowattbereich auf und müssen gut gekühlt werden. Das größere Problem ist allerdings, dass in einem gewöhnlichen Mikroskop, also einer Durchlichteinrichtung, fast 100 % des eingestrahlten Lichtes im Okular ankommt wie wir in Abschn berechnet haben. Einerseits ist es nicht möglich, das geringe Fluoreszenzlicht gegen diesen Hintergrund wahrzunehmen, auch wenn es eine andere Farbe hat. Andererseits sind gewöhnliche Detektoren für so hohe Lichtintensitäten nicht geeignet. Insbesondere das Auge ist gefährdet und es gab wohl einige Fälle, in denen der Experimentator durch unachtsame Benutzung solcher Einrichtungen erblindet war. Um den extremen Hintergrund zu unterdrücken, muss im Strahlengang auf der Beobachtungsseite ein Filter eingeschaltet werden. Dieser Filter muss das Fluoreszenzlicht möglichst unbehindert passieren lassen, aber das Anregungslicht möglichst vollständig blockieren. Man spricht daher von einem Blockfilter, Sperrfilter oder Emissionsfilter. Vergisst man diesen Blockfilter und schaut ins Mikroskop, ist eine ernsthafte Augenverletzung sehr wahrscheinlich insbesondere, wenn das Licht hohe Anteile des unsichtbaren Ultravioletts enthält. Sowohl der Kontrast als auch die Sicherheit werden wesentlich verbessert, wenn die Beobachtung nicht direkt in die Lichtquelle erfolgt. Das kann erreicht werden, indem mittels eines Strahlteilers die Beleuchtung von der Betrachtung entkoppelt wird (Abb. 2.7). Das Licht zur Beleuchtung wird dabei in einem Winkel gegen die optische Achse des Mikroskops eingekoppelt und strahlt auf dieselbe Seite des Präparates, die anschließend beobachtet wird. Das
11
Bilder Ton Zeit [s] Vorspann
![Bilder Ton Zeit [s] Vorspann Bilder Ton Zeit [s] Vorspann](/thumbs/62/47191146.jpg) Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Gymnasium / Realschule. Atomphysik 2. Klasse / G8. Aufnahme und Abgabe von Energie (Licht)
 Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Fluoreszenz. Abb. 1: Möglicher Versuchsaufbau
 Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Fluoreszenz von Silberclustern
 Fluoreszenz von Silberclustern Unter Fluoreszenz versteht man die Emission von Licht durch Hüllenelektronen, wenn diese aus einem angeregten Zustand (energetisch höher liegend) in einen energetisch niedrigeren
Fluoreszenz von Silberclustern Unter Fluoreszenz versteht man die Emission von Licht durch Hüllenelektronen, wenn diese aus einem angeregten Zustand (energetisch höher liegend) in einen energetisch niedrigeren
SPEKTRALANALYSE. entwickelt um 1860 von: GUSTAV ROBERT KIRCHHOFF ( ; dt. Physiker) + ROBERT WILHELM BUNSEN ( ; dt.
 SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
Mikroskopie II. Szilvia Barkó 2016
 Mikroskopie II. Szilvia Barkó 2016 Zusammenfassung der Vorlesung Fluoreszenzmikroskopie Fluorophoren Aufbau eines Epifluoreszenzmikroskops Konfokalmikroskopie Evaneszentfeldmikroskopie Multiphotonenmikroskopie
Mikroskopie II. Szilvia Barkó 2016 Zusammenfassung der Vorlesung Fluoreszenzmikroskopie Fluorophoren Aufbau eines Epifluoreszenzmikroskops Konfokalmikroskopie Evaneszentfeldmikroskopie Multiphotonenmikroskopie
Photom etrieren Photometrie Fraunhofer sche Linien
 17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002
 Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Fortgeschrittenenpraktikum: Ausarbeitung - Versuch 14 Optische Absorption Durchgeführt am 13. Juni 2002 30. Juli 2002 Gruppe 17 Christoph Moder 2234849 Michael Wack 2234088 Sebastian Mühlbauer 2218723
Lösungen zu den Übungen zur Einführung in die Spektroskopie für Studenten der Biologie (SS 2011)
 Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
Universität Konstanz Fachbereich Biologie Priv.-Doz. Dr. Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Datum: 26.5.211 Lösungen zu den Übungen zur Einführung in die Spektroskopie
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
Medizinische Biophysik Licht in der Medizin. Temperaturstrahlung, Lumineszenz
 V. Lichtemission Medizinische Biophysik Licht in der Medizin. Temperaturstrahlung, Lumineszenz 6. Vorlesung Lichtquellen warmes Licht kaltes Licht kontinuierliches Spektrum Linien- oder Bandenspektrum
V. Lichtemission Medizinische Biophysik Licht in der Medizin. Temperaturstrahlung, Lumineszenz 6. Vorlesung Lichtquellen warmes Licht kaltes Licht kontinuierliches Spektrum Linien- oder Bandenspektrum
Stundenprotokoll vom : Compton Effekt
 Stundenprotokoll vom 9.12.2011: Compton Effekt Zunächst beschäftigten wir uns mit den einzelnen Graphen des Photoeffekts (grün), des Compton-Effekts (gelb) und mit der Paarbildung (blau). Anschließend
Stundenprotokoll vom 9.12.2011: Compton Effekt Zunächst beschäftigten wir uns mit den einzelnen Graphen des Photoeffekts (grün), des Compton-Effekts (gelb) und mit der Paarbildung (blau). Anschließend
K1: Lambert-Beer`sches Gesetz
 K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
K1: Lambert-Beer`sches Gesetz Einleitung In diesem Versuch soll die Entfärbung von Kristallviolett durch atronlauge mittels der Absorptionsspektroskopie untersucht werden. Sowohl die Reaktionskinetik als
Wärmestrahlung. Einfallende Strahlung = absorbierte Strahlung + reflektierte Strahlung
 Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1. Lambert Beer sches Gesetz - Zerfall des Manganoxalations
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 34 Lambert Beer sches Gesetz - Zerfall des Manganoxalations Aufgabe: 1. Bestimmen Sie die Wellenlänge maximaler Absorbanz λ max eines
27. Wärmestrahlung. rmestrahlung, Quantenmechanik
 24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
Kinetik zusammengesetzter Reaktionen
 Kinetik zusammengesetzter Reaktionen Kap. 23 1 PC 2 SS 2016 Kinetik zusammengesetzter Reaktionen Kettenreaktionen Explosionen Polymerisationen Schrittweise Polymerisation Kettenpolymerisation Homogene
Kinetik zusammengesetzter Reaktionen Kap. 23 1 PC 2 SS 2016 Kinetik zusammengesetzter Reaktionen Kettenreaktionen Explosionen Polymerisationen Schrittweise Polymerisation Kettenpolymerisation Homogene
PEITING. Fluoreszenz-Experimente aus der Biologie mit modernen UV-LEDs. ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht
 ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht PEITING Fluoreszenz-Experimente aus der Biologie mit modernen UV-LEDs Oliver Debacher Schule: Jugend forscht 2015 Fluoreszenz-Experimente
ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht PEITING Fluoreszenz-Experimente aus der Biologie mit modernen UV-LEDs Oliver Debacher Schule: Jugend forscht 2015 Fluoreszenz-Experimente
Klausurinformation. Sie dürfen nicht verwenden: Handy, Palm, Laptop u.ae. Weisses Papier, Stifte etc. Proviant, aber keine heiße Suppe u.dgl.
 Klausurinformation Zeit: Mittwoch, 3.Februar, 12:00, Dauer :90 Minuten Ort: Veterinärmediziner: Großer Phys. Hörsaal ( = Hörsaal der Vorlesung) Geowissenschaftler u.a.: Raum A140, Hauptgebäude 1. Stock,
Klausurinformation Zeit: Mittwoch, 3.Februar, 12:00, Dauer :90 Minuten Ort: Veterinärmediziner: Großer Phys. Hörsaal ( = Hörsaal der Vorlesung) Geowissenschaftler u.a.: Raum A140, Hauptgebäude 1. Stock,
23. Vorlesung EP. IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik
 23. Vorlesung EP IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik Strahlung: Stoff der Optik, Wärme-, Elektrizitätslehre u. Quantenphysik Photometrie
23. Vorlesung EP IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik Strahlung: Stoff der Optik, Wärme-, Elektrizitätslehre u. Quantenphysik Photometrie
Fluoreszierende Verbindungen
 Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale
 Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
SCHWEIZER JUGEND FORSCHT. Chemie und Materialwissenschaften
 SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
Raman- Spektroskopie. Natalia Gneiding. 5. Juni 2007
 Raman- Spektroskopie Natalia Gneiding 5. Juni 2007 Inhalt Einleitung Theoretische Grundlagen Raman-Effekt Experimentelle Aspekte Raman-Spektroskopie Zusammenfassung Nobelpreis für Physik 1930 Sir Chandrasekhara
Raman- Spektroskopie Natalia Gneiding 5. Juni 2007 Inhalt Einleitung Theoretische Grundlagen Raman-Effekt Experimentelle Aspekte Raman-Spektroskopie Zusammenfassung Nobelpreis für Physik 1930 Sir Chandrasekhara
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Licht als Teilchenstrahlung
 Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Ausbreitung von elektromagnetischer Strahlung
 Ausbreitung von elektromagnetischer Strahlung E! B Der elektrische Feldvektor und der magnetische Feldvektor stehen senkrecht aufeinander Die elektromagentische Welle ist beschrieben durch x x E = E 0
Ausbreitung von elektromagnetischer Strahlung E! B Der elektrische Feldvektor und der magnetische Feldvektor stehen senkrecht aufeinander Die elektromagentische Welle ist beschrieben durch x x E = E 0
22 Optische Spektroskopie; elektromagnetisches Spektrum
 22 Optische Spektroskopie; elektromagnetisches Spektrum Messung der Wellenlänge von Licht mithilfedes optischen Gitters Versuch: Um das Spektrum einer Lichtquelle, hier einer Kohlenbogenlampe, aufzunehmen
22 Optische Spektroskopie; elektromagnetisches Spektrum Messung der Wellenlänge von Licht mithilfedes optischen Gitters Versuch: Um das Spektrum einer Lichtquelle, hier einer Kohlenbogenlampe, aufzunehmen
Lehrbuchaufgaben Strahlung aus der Atomhülle
 LB S. 89, Aufgabe 1 Die Masse lässt sich mithilfe eines Massenspektrografen bestimmen. Der Radius von Atomen kann z.b. aus einmolekularen Schichten (Ölfleckversuch) oder aus Strukturmodellen (dichtgepackte
LB S. 89, Aufgabe 1 Die Masse lässt sich mithilfe eines Massenspektrografen bestimmen. Der Radius von Atomen kann z.b. aus einmolekularen Schichten (Ölfleckversuch) oder aus Strukturmodellen (dichtgepackte
 Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre?
 Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
Spektren 1 Welche Strahlen werden durch die Erdatmosphäre abgeschirmt? Welche Moleküle beeinflussen wesentlich die Strahlendurchlässigkeit der Atmosphäre? Der UV- und höherenergetische Anteil wird fast
Klausur -Informationen
 Klausur -Informationen Datum: 4.2.2009 Uhrzeit und Ort : 11 25 im großen Physikhörsaal (Tiermediziner) 12 25 ibidem Empore links (Nachzügler Tiermedizin, bitte bei Aufsichtsperson Ankunft melden) 11 25
Klausur -Informationen Datum: 4.2.2009 Uhrzeit und Ort : 11 25 im großen Physikhörsaal (Tiermediziner) 12 25 ibidem Empore links (Nachzügler Tiermedizin, bitte bei Aufsichtsperson Ankunft melden) 11 25
Material 1. Fluoreszenz von Flussspat
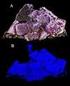 Material 1 Fluoreszenz von Flussspat In der Natur kommt Calcium-Fluorit in Form von Flussspat vor, der im ultravioletten (UV-) Licht eine starke, blaue Fluoreszenz zeigt. Anzumerken ist dabei, dass nicht
Material 1 Fluoreszenz von Flussspat In der Natur kommt Calcium-Fluorit in Form von Flussspat vor, der im ultravioletten (UV-) Licht eine starke, blaue Fluoreszenz zeigt. Anzumerken ist dabei, dass nicht
Optische Eigenschaften fester Stoffe. Licht im neuen Licht Dez 2015
 Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Licht und Materie Optische Eigenschaften fester Stoffe Matthias Laukenmann Den Lernenden muss bereits bekannt sein: Zahlreiche Phänomene lassen sich erklären, wenn man annimmt, dass die von Atomen quantisiert
Aufgaben zum Wasserstoffatom
 Aufgaben zum Wasserstoffatom Hans M. Strauch Kurfürst-Ruprecht-Gymnasium Neustadt/W. Aufgabenarten Darstellung von Zusammenhängen, Abgrenzung von Unterschieden (können u.u. recht offen sein) Beantwortung
Aufgaben zum Wasserstoffatom Hans M. Strauch Kurfürst-Ruprecht-Gymnasium Neustadt/W. Aufgabenarten Darstellung von Zusammenhängen, Abgrenzung von Unterschieden (können u.u. recht offen sein) Beantwortung
Laserlicht Laser. Video: Kohärenz. Taschenlampe. Dieter Suter Physik B Grundlagen
 Dieter Suter - 423 - Physik B2 6.7. Laser 6.7.1. Grundlagen Das Licht eines gewöhnlichen Lasers unterscheidet sich vom Licht einer Glühlampe zunächst dadurch dass es nur eine bestimmte Wellenlänge, resp.
Dieter Suter - 423 - Physik B2 6.7. Laser 6.7.1. Grundlagen Das Licht eines gewöhnlichen Lasers unterscheidet sich vom Licht einer Glühlampe zunächst dadurch dass es nur eine bestimmte Wellenlänge, resp.
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Wellenlängen bei Strahlungsmessungen. im Gebiet der Meteorologie nm nm
 Die Solarstrahlung Die Sonne sendet uns ein breites Frequenzspektrum. Die elektromagnetische Strahlung der Sonne, die am oberen Rand der Erdatmosphäre einfällt, wird als extraterrestrische Sonnenstrahlung
Die Solarstrahlung Die Sonne sendet uns ein breites Frequenzspektrum. Die elektromagnetische Strahlung der Sonne, die am oberen Rand der Erdatmosphäre einfällt, wird als extraterrestrische Sonnenstrahlung
Hochschule Düsseldorf University of Applied Sciences. 04. Oktober 2016 HSD. Solarenergie. Die Sonne
 Solarenergie Die Sonne Wärmestrahlung Wärmestrahlung Lichtentstehung Wärme ist Bewegung der Atome Im Festkörper ist die Bewegung Schwingung Diese Schwingungen können selber Photonen aufnehmen und abgeben
Solarenergie Die Sonne Wärmestrahlung Wärmestrahlung Lichtentstehung Wärme ist Bewegung der Atome Im Festkörper ist die Bewegung Schwingung Diese Schwingungen können selber Photonen aufnehmen und abgeben
Beschreibe die wesentlichen Unterschiede zwischen den einzelnen Anregungsmöglichkeiten.
 Erkläre den Begriff Anregung eines Atoms Unter Anregung eines Atoms versteht man die Zufuhr von Energie an ein Atom, welche dieses vom Grundzustand in einen höheren Energiezustand, auf ein höheres Energieniveau,
Erkläre den Begriff Anregung eines Atoms Unter Anregung eines Atoms versteht man die Zufuhr von Energie an ein Atom, welche dieses vom Grundzustand in einen höheren Energiezustand, auf ein höheres Energieniveau,
32. Lektion. Laser. 40. Röntgenstrahlen und Laser
 32. Lektion Laser 40. Röntgenstrahlen und Laser Lernziel: Kohärentes und monochromatisches Licht kann durch stimulierte Emission erzeugt werden Begriffe Begriffe: Kohärente und inkohärente Strahlung Thermische
32. Lektion Laser 40. Röntgenstrahlen und Laser Lernziel: Kohärentes und monochromatisches Licht kann durch stimulierte Emission erzeugt werden Begriffe Begriffe: Kohärente und inkohärente Strahlung Thermische
Lösungen zu den Aufg. S. 363/4
 Lösungen zu den Aufg. S. 363/4 9/1 Die gemessene Gegenspannung (s. Tab.) entspricht der max. kin. Energie der Photoelektronen; die Energie der Photonen = E kin der Elektronen + Austrittsarbeit ==> h f
Lösungen zu den Aufg. S. 363/4 9/1 Die gemessene Gegenspannung (s. Tab.) entspricht der max. kin. Energie der Photoelektronen; die Energie der Photonen = E kin der Elektronen + Austrittsarbeit ==> h f
5.1. Wellenoptik d 2 E/dx 2 = m 0 e 0 d 2 E/dt 2 Die Welle hat eine Geschwindigkeit von 1/(m 0 e 0 ) 1/2 = 3*10 8 m/s Das ist die
 5. Optik 5.1. Wellenoptik d 2 E/dx 2 = m 0 e 0 d 2 E/dt 2 Die Welle hat eine Geschwindigkeit von 1/(m 0 e 0 ) 1/2 = 3*10 8 m/s Das ist die Lichtgeschwindigkeit! In Materie ergibt sich eine andere Geschwindikeit
5. Optik 5.1. Wellenoptik d 2 E/dx 2 = m 0 e 0 d 2 E/dt 2 Die Welle hat eine Geschwindigkeit von 1/(m 0 e 0 ) 1/2 = 3*10 8 m/s Das ist die Lichtgeschwindigkeit! In Materie ergibt sich eine andere Geschwindikeit
Molekülsymmetrie und Kristallographie
 Optische Aktivität Wie schon im Skriptum 5 erwähnt ist es nicht einfach, aus experimentellen Daten auf die Absolutkonfiguration einer chiralen Verbindung zu schließen. In den meisten Fällen verwendet man
Optische Aktivität Wie schon im Skriptum 5 erwähnt ist es nicht einfach, aus experimentellen Daten auf die Absolutkonfiguration einer chiralen Verbindung zu schließen. In den meisten Fällen verwendet man
Für Geowissenschaftler. EP WS 2009/10 Dünnweber/Faessler
 Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Radioaktiver Zerfall des Atomkernes: α-zerfall
 Radioaktiver Zerfall des Atomkernes: α-zerfall Schwere Atomkerne (hohes Z, hohes N) sind instabil gegen spontanen Zerfall. Die mögliche Emission einzelner Protonen oder einzelner Neutronen ist nicht häufig.
Radioaktiver Zerfall des Atomkernes: α-zerfall Schwere Atomkerne (hohes Z, hohes N) sind instabil gegen spontanen Zerfall. Die mögliche Emission einzelner Protonen oder einzelner Neutronen ist nicht häufig.
Quantenphysik. Albert Einstein Mitbegründer der Quantenphysik. Modellvorstellung eines Quants
 Quantenphysik Albert Einstein Mitbegründer der Quantenphysik Modellvorstellung eines Quants Die Wechselwirkung von Licht und Materie 1888 Wilhelm Hallwachs Bestrahlung von unterschiedlichen Metallplatten
Quantenphysik Albert Einstein Mitbegründer der Quantenphysik Modellvorstellung eines Quants Die Wechselwirkung von Licht und Materie 1888 Wilhelm Hallwachs Bestrahlung von unterschiedlichen Metallplatten
VL 20 VL Mehrelektronensysteme VL Periodensystem VL Röntgenstrahlung
 VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
Versuch Q1. Äußerer Photoeffekt. Sommersemester Daniel Scholz
 Demonstrationspraktikum für Lehramtskandidaten Versuch Q1 Äußerer Photoeffekt Sommersemester 2006 Name: Daniel Scholz Mitarbeiter: Steffen Ravekes EMail: daniel@mehr-davon.de Gruppe: 4 Durchgeführt am:
Demonstrationspraktikum für Lehramtskandidaten Versuch Q1 Äußerer Photoeffekt Sommersemester 2006 Name: Daniel Scholz Mitarbeiter: Steffen Ravekes EMail: daniel@mehr-davon.de Gruppe: 4 Durchgeführt am:
Dieter Suter Physik B3
 Dieter Suter - 421 - Physik B3 9.2 Radioaktivität 9.2.1 Historisches, Grundlagen Die Radioaktivität wurde im Jahre 1896 entdeckt, als Becquerel feststellte, dass Uransalze Strahlen aussenden, welche den
Dieter Suter - 421 - Physik B3 9.2 Radioaktivität 9.2.1 Historisches, Grundlagen Die Radioaktivität wurde im Jahre 1896 entdeckt, als Becquerel feststellte, dass Uransalze Strahlen aussenden, welche den
VL 20 VL Mehrelektronensysteme VL Periodensystem VL Röntgenstrahlung
 VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
VL 20 VL 18 18.1. Mehrelektronensysteme VL 19 19.1. Periodensystem VL 20 20.1. Röntgenstrahlung Wim de Boer, Karlsruhe Atome und Moleküle, 27.06.2013 1 Vorlesung 20: Roter Faden: Röntgenstrahlung Folien
Der lichtelektrische Effekt (Photoeffekt)
 Der lichtelektrische Effekt (Photoeffekt) Versuchsanordnung Zn-Platte, amalgamiert Wulfsches Elektrometer Spannung, ca. 800 V Knappe Erklärung des Versuches Licht löst aus der Zn-Platte Elektronen aus
Der lichtelektrische Effekt (Photoeffekt) Versuchsanordnung Zn-Platte, amalgamiert Wulfsches Elektrometer Spannung, ca. 800 V Knappe Erklärung des Versuches Licht löst aus der Zn-Platte Elektronen aus
Optische Systeme (5. Vorlesung)
 5.1 Optische Systeme (5. Vorlesung) Yousef Nazirizadeh 20.11.2006 Universität Karlsruhe (TH) Inhalte der Vorlesung 5.2 1. Grundlagen der Wellenoptik 2. Abbildende optische Systeme 2.1 Lupe / Mikroskop
5.1 Optische Systeme (5. Vorlesung) Yousef Nazirizadeh 20.11.2006 Universität Karlsruhe (TH) Inhalte der Vorlesung 5.2 1. Grundlagen der Wellenoptik 2. Abbildende optische Systeme 2.1 Lupe / Mikroskop
Photochemische Reaktion
 TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
TU Ilmenau Chemisches Praktikum Versuch Fachgebiet Chemie 1. Aufgabe Photochemische Reaktion V5 Es soll die Reduktion des Eisen(III)-trisoxalats nach Gleichung (1) unter der Einwirkung von Licht untersucht
= 6,63 10 J s 8. (die Plancksche Konstante):
 35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
35 Photonen und Materiefelder 35.1 Das Photon: Teilchen des Lichts Die Quantenphysik: viele Größen treten nur in ganzzahligen Vielfachen von bestimmten kleinsten Beträgen (elementaren Einheiten) auf: diese
(2.65 ev), da sich die beiden Elektronen gegenseitig abstossen.
 phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
Methoden. Spektroskopische Verfahren. Mikroskopische Verfahren. Streuverfahren. Kalorimetrische Verfahren
 Methoden Spektroskopische Verfahren Mikroskopische Verfahren Streuverfahren Kalorimetrische Verfahren Literatur D. Haarer, H.W. Spiess (Hrsg.): Spektroskopie amorpher und kristalliner Festkörper Steinkopf
Methoden Spektroskopische Verfahren Mikroskopische Verfahren Streuverfahren Kalorimetrische Verfahren Literatur D. Haarer, H.W. Spiess (Hrsg.): Spektroskopie amorpher und kristalliner Festkörper Steinkopf
Seminar zum Praktikumsversuch: Optische Spektroskopie. Tilman Zscheckel Otto-Schott-Institut
 Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Seminar zum Praktikumsversuch: Optische Spektroskopie Tilman Zscheckel Otto-Schott-Institut Optische Spektroskopie Definition: - qualitative oder quantitative Analyse, die auf der Wechselwirkung von Licht
Zentralabitur 2012 Physik Schülermaterial Aufgabe I ga Bearbeitungszeit: 220 min
 Thema: Wellen und Quanten Interferenzphänomene werden an unterschiedlichen Strukturen untersucht. In Aufgabe 1 wird zuerst der Spurabstand einer CD bestimmt. Thema der Aufgabe 2 ist eine Strukturuntersuchung
Thema: Wellen und Quanten Interferenzphänomene werden an unterschiedlichen Strukturen untersucht. In Aufgabe 1 wird zuerst der Spurabstand einer CD bestimmt. Thema der Aufgabe 2 ist eine Strukturuntersuchung
Chemistry Department Cologne University. Photochemie 1 PC 2 SS Chemistry Department Cologne University. Photochemie
 Photochemie 1 PC 2 2016 Photochemie 2 PC 2 2016 1 Wichtige photophysikalische Prozesse 3 PC 2 2016 Der Grundzustand Boltzmann Verteilung: Alle Moleküle sind im elektronischen Grundzustand (0) chwingungsgrundzustand
Photochemie 1 PC 2 2016 Photochemie 2 PC 2 2016 1 Wichtige photophysikalische Prozesse 3 PC 2 2016 Der Grundzustand Boltzmann Verteilung: Alle Moleküle sind im elektronischen Grundzustand (0) chwingungsgrundzustand
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
Entwicklung und Anwendungen der hochauflösenden STED-Mikroskopie
 Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/entwicklung-undanwendungen-der-hochaufloesenden-sted-mikroskopie/ Entwicklung und Anwendungen der hochauflösenden
Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/entwicklung-undanwendungen-der-hochaufloesenden-sted-mikroskopie/ Entwicklung und Anwendungen der hochauflösenden
Atommodell. Atommodell nach Bohr und Sommerfeld Für sein neues Atommodell stellte Bohr folgende Postulate auf:
 Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Feldbegriff und Feldlinienbilder. Elektrisches Feld. Magnetisches Feld. Kraft auf Ladungsträger im elektrischen Feld
 Feldbegriff und Feldlinienbilder Elektrisches Feld Als Feld bezeichnet man den Bereich um einen Körper, in dem ohne Berührung eine Kraft wirkt beim elektrischen Feld wirkt die elektrische Kraft. Ein Feld
Feldbegriff und Feldlinienbilder Elektrisches Feld Als Feld bezeichnet man den Bereich um einen Körper, in dem ohne Berührung eine Kraft wirkt beim elektrischen Feld wirkt die elektrische Kraft. Ein Feld
21-1. K=f c I=I0 e f c d
 21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
21-1 Lichtabsorption 1. Vorbereitung : Extinktions- und Absorptionskonstante, mittlere Reichweite, Unterscheidung zwischen stark und schwach absorbierenden Stoffen, Lambert-Beersches Gesetz, Erklärung
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Lösungen zum Niedersachsen Physik Abitur 2012-Grundlegendes Anforderungsniveau Aufgabe II Experimente mit Elektronen
 1 Lösungen zum Niedersachsen Physik Abitur 2012-Grundlegendes Anforderungsniveau Aufgabe II xperimente mit lektronen 1 1.1 U dient zum rwärmen der Glühkathode in der Vakuumröhre. Durch den glühelektrischen
1 Lösungen zum Niedersachsen Physik Abitur 2012-Grundlegendes Anforderungsniveau Aufgabe II xperimente mit lektronen 1 1.1 U dient zum rwärmen der Glühkathode in der Vakuumröhre. Durch den glühelektrischen
10/6/2015. Licht IST FARBIG! DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE. Alle Objekte sind Reflektoren!
 DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE 1 WAS GENAU SIND OPTISCHE AUFHELLER? Optische Aufheller sind chemische Stoffe welche im elektromagnetischen Spektrum Licht
DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE 1 WAS GENAU SIND OPTISCHE AUFHELLER? Optische Aufheller sind chemische Stoffe welche im elektromagnetischen Spektrum Licht
Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves
 Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves 1. Einleitung 2. Optische Grundbegriffe 3. Optische Meßverfahren 3.1 Grundlagen dρ 3.2 Interferometrie, ρ(x,y), dx (x,y) 3.3 Laser-Doppler-Velozimetrie
Vorlesung Messtechnik 2. Hälfte des Semesters Dr. H. Chaves 1. Einleitung 2. Optische Grundbegriffe 3. Optische Meßverfahren 3.1 Grundlagen dρ 3.2 Interferometrie, ρ(x,y), dx (x,y) 3.3 Laser-Doppler-Velozimetrie
43. Strahlenschutz und Dosimetrie. 36. Lektion Wechselwirkung und Reichweite von Strahlung
 43. Strahlenschutz und Dosimetrie 36. Lektion Wechselwirkung und Reichweite von Strahlung Lernziel: Die Wechselwirkung von radioaktiver Strahlung (α,β,γ( α,β,γ) ) ist unterschiedlich. Nur im Fall von α-
43. Strahlenschutz und Dosimetrie 36. Lektion Wechselwirkung und Reichweite von Strahlung Lernziel: Die Wechselwirkung von radioaktiver Strahlung (α,β,γ( α,β,γ) ) ist unterschiedlich. Nur im Fall von α-
Lk Physik in 13/1 2. Klausur aus der Physik Blatt 1 (von 2)
 Blatt 1 (von 2) 1. Leuchtelektronen-Modell des Na-Atoms 5 BE Berechne aus dem experimentellen Wert der Ionisierungsenergie von Natrium, 5, 12 ev, die effektive Kernladungszahl für das Leuchtelektron der
Blatt 1 (von 2) 1. Leuchtelektronen-Modell des Na-Atoms 5 BE Berechne aus dem experimentellen Wert der Ionisierungsenergie von Natrium, 5, 12 ev, die effektive Kernladungszahl für das Leuchtelektron der
Physik 2 (GPh2) am
 Name: Matrikelnummer: Studienfach: Physik 2 (GPh2) am 17.09.2013 Fachbereich Elektrotechnik und Informatik, Fachbereich Mechatronik und Maschinenbau Zugelassene Hilfsmittel zu dieser Klausur: Beiblätter
Name: Matrikelnummer: Studienfach: Physik 2 (GPh2) am 17.09.2013 Fachbereich Elektrotechnik und Informatik, Fachbereich Mechatronik und Maschinenbau Zugelassene Hilfsmittel zu dieser Klausur: Beiblätter
Strahlungsgesetze. Stefan-Boltzmann Gesetz. Wiensches Verschiebungsgesetz. Plancksches Strahlungsgesetz
 Tell me, I will forget Show me, I may remember Involve me, and I will understand Chinesisches Sprichwort Strahlungsgesetze Stefan-Boltzmann Gesetz Wiensches Verschiebungsgesetz Plancksches Strahlungsgesetz
Tell me, I will forget Show me, I may remember Involve me, and I will understand Chinesisches Sprichwort Strahlungsgesetze Stefan-Boltzmann Gesetz Wiensches Verschiebungsgesetz Plancksches Strahlungsgesetz
Das CD-Spektroskop. 15 min
 50 Experimente- Physik / 9.-13. Schulstufe Das CD-Spektroskop 15 min Welche Beleuchtung eignet sich für Innenräume am besten? Seit die Glühlampe aus den Wohnungen verbannt wurde, wird in den Medien über
50 Experimente- Physik / 9.-13. Schulstufe Das CD-Spektroskop 15 min Welche Beleuchtung eignet sich für Innenräume am besten? Seit die Glühlampe aus den Wohnungen verbannt wurde, wird in den Medien über
Physikalische Grundlagen zur Wärmegewinnung aus Sonnenenergie
 7 Physikalische Grundlagen zur Wärmegewinnung aus Sonnenenergie Umwandlung von Licht in Wärme Absorptions- und Emissionsvermögen 7.1 Umwandlung von Licht in Wärme Zur Umwandlung von Solarenergie in Wärme
7 Physikalische Grundlagen zur Wärmegewinnung aus Sonnenenergie Umwandlung von Licht in Wärme Absorptions- und Emissionsvermögen 7.1 Umwandlung von Licht in Wärme Zur Umwandlung von Solarenergie in Wärme
Elemente der Quantenmechanik III 9.1. Schrödingergleichung mit beliebigem Potential 9.2. Harmonischer Oszillator 9.3. Drehimpulsoperator
 VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
Übungsaufgaben zur Optischen Spektroskopie. 1) Nennen Sie drei Arten von elektronischen Übergängen und geben Sie jeweils ein Beispiel an!
 Übungsaufgaben zur Optischen Spektroskopie 1) Nennen Sie drei Arten von elektronischen Übergängen und geben Sie jeweils ein Beispiel an! 2) Welche grundlegenden Arten der Wechselwirkung von Licht mit Materie
Übungsaufgaben zur Optischen Spektroskopie 1) Nennen Sie drei Arten von elektronischen Übergängen und geben Sie jeweils ein Beispiel an! 2) Welche grundlegenden Arten der Wechselwirkung von Licht mit Materie
Zentralabitur 2011 Physik Schülermaterial Aufgabe I ga Bearbeitungszeit: 220 min
 Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Thema: Eigenschaften von Licht Gegenstand der Aufgabe 1 ist die Untersuchung von Licht nach Durchlaufen von Luft bzw. Wasser mit Hilfe eines optischen Gitters. Während in der Aufgabe 2 der äußere lichtelektrische
Einführungsseminar S2 zum Physikalischen Praktikum
 Einführungsseminar S2 zum Physikalischen Praktikum 1. Organisatorisches 2. Unterweisung 3. Demo-Versuch Radioaktiver Zerfall 4. Am Schluss: Unterschriften! Praktischer Strahlenschutz Wechselwirkung von
Einführungsseminar S2 zum Physikalischen Praktikum 1. Organisatorisches 2. Unterweisung 3. Demo-Versuch Radioaktiver Zerfall 4. Am Schluss: Unterschriften! Praktischer Strahlenschutz Wechselwirkung von
Photonik Technische Nutzung von Licht
 Photonik Technische Nutzung von Licht Lichterzeugung und Spektrum Was ist Licht? Quelle: Wikipedia de.wikipedia.org/wiki/elektromagnetische_welle Elektromagnetische Welle Transversalwelle Polarisation
Photonik Technische Nutzung von Licht Lichterzeugung und Spektrum Was ist Licht? Quelle: Wikipedia de.wikipedia.org/wiki/elektromagnetische_welle Elektromagnetische Welle Transversalwelle Polarisation
31. Lektion. Röntgenstrahlen. 40. Röntgenstrahlen und Laser
 31. Lektion Röntgenstrahlen 40. Röntgenstrahlen und Laser Lerhnziel: Röntgenstrahlen entstehen durch Beschleunigung von Elektronen oder durch die Ionisation von inneren Elektronenschalen Begriffe Begriffe:
31. Lektion Röntgenstrahlen 40. Röntgenstrahlen und Laser Lerhnziel: Röntgenstrahlen entstehen durch Beschleunigung von Elektronen oder durch die Ionisation von inneren Elektronenschalen Begriffe Begriffe:
Gibt es myonische Atome?
 Minitest 7 Das Myon it ist ein Elementarteilchen, t das dem Elektron ähnelt, jedoch jd eine deutlich höhere Masse (105,6 MeV/c 2 statt 0,511 MeV/c 2 ) aufweist. Wie das Elektron ist es mit einer Elementarladung
Minitest 7 Das Myon it ist ein Elementarteilchen, t das dem Elektron ähnelt, jedoch jd eine deutlich höhere Masse (105,6 MeV/c 2 statt 0,511 MeV/c 2 ) aufweist. Wie das Elektron ist es mit einer Elementarladung
Konfokale Mikroskopie
 Konfokale Mikroskopie Seminar Laserphysik SoSe 2007 Christine Derks Universität Osnabrück Gliederung 1 Einleitung 2 Konfokales Laser-Scanning-Mikroskop 3 Auflösungsvermögen 4 andere Konfokale Mikroskope
Konfokale Mikroskopie Seminar Laserphysik SoSe 2007 Christine Derks Universität Osnabrück Gliederung 1 Einleitung 2 Konfokales Laser-Scanning-Mikroskop 3 Auflösungsvermögen 4 andere Konfokale Mikroskope
Die Farben des Lichts
 Einen Regenbogen herbeizaubern Ist es möglich, hier im Schülerlabor einen Regenbogen zu erzeugen? Ja Nein Wo und wann hast du schon Regenbögen oder Regenbogenfarben gesehen? Regenbogen in der Natur nach
Einen Regenbogen herbeizaubern Ist es möglich, hier im Schülerlabor einen Regenbogen zu erzeugen? Ja Nein Wo und wann hast du schon Regenbögen oder Regenbogenfarben gesehen? Regenbogen in der Natur nach
Methoden der Durchlichtfluoreszenzmikroskopie
 Methoden der Durchlichtfluoreszenzmikroskopie Gerhard Göke 1. Einführung in die Technik und Problematik Für eine ganze Reihe von Mikroskopen stehen heute Hochleistungs-Mikroskopierleuchten zur Verfügung,
Methoden der Durchlichtfluoreszenzmikroskopie Gerhard Göke 1. Einführung in die Technik und Problematik Für eine ganze Reihe von Mikroskopen stehen heute Hochleistungs-Mikroskopierleuchten zur Verfügung,
CMB Echo des Urknalls. Max Camenzind Februar 2015
 CMB Echo des Urknalls Max Camenzind Februar 2015 Lemaître 1931: Big Bang des expandierenden Universums Big Bang : Photonenhintergrund + Neutrinohintergrund 3-Raum expandiert: dx a(t) dx ; Wellenlängen
CMB Echo des Urknalls Max Camenzind Februar 2015 Lemaître 1931: Big Bang des expandierenden Universums Big Bang : Photonenhintergrund + Neutrinohintergrund 3-Raum expandiert: dx a(t) dx ; Wellenlängen
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
27. Vorlesung EP V. STRAHLUNG, ATOME, KERNE
 27. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 28. Atomphysik, Röntgenstrahlung (Fortsetzung: Röntgenröhre, Röntgenabsorption) 29. Atomkerne, Radioaktivität (Nuklidkarte, α-, β-, γ-aktivität, Dosimetrie)
27. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 28. Atomphysik, Röntgenstrahlung (Fortsetzung: Röntgenröhre, Röntgenabsorption) 29. Atomkerne, Radioaktivität (Nuklidkarte, α-, β-, γ-aktivität, Dosimetrie)
Instrumenten- Optik. Mikroskop
 Instrumenten- Optik Mikroskop Gewerblich-Industrielle Berufsschule Bern Augenoptikerinnen und Augenoptiker Der mechanische Aufbau Die einzelnen mechanischen Bauteile eines Mikroskops bezeichnen und deren
Instrumenten- Optik Mikroskop Gewerblich-Industrielle Berufsschule Bern Augenoptikerinnen und Augenoptiker Der mechanische Aufbau Die einzelnen mechanischen Bauteile eines Mikroskops bezeichnen und deren
Radioaktivität II. Gamma Absorption. (Lehrer AB) Abstract:
 Radioaktivität II Gamma Absorption (Lehrer AB) Abstract: Den SchülerInnen soll der Umgang mit radioaktiven Stoffen nähergebracht werden. Im Rahmen dieses Versuches nehmen die SchülerInnen Messwerte eines
Radioaktivität II Gamma Absorption (Lehrer AB) Abstract: Den SchülerInnen soll der Umgang mit radioaktiven Stoffen nähergebracht werden. Im Rahmen dieses Versuches nehmen die SchülerInnen Messwerte eines
Teil 1 Schwingungsspektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
A. Mechanik (18 Punkte)
 Prof. Dr. A. Hese Prof. Dr. G. v. Oppen Dipl.-Phys. G. Hoheisel Dipl.-Phys. R. Jung Technische Universität Berlin Name: Vorname: Matr. Nr.: Fachbereich: Platz Nr.: Tutor: A. Mechanik (18 Punkte) 1. Wie
Prof. Dr. A. Hese Prof. Dr. G. v. Oppen Dipl.-Phys. G. Hoheisel Dipl.-Phys. R. Jung Technische Universität Berlin Name: Vorname: Matr. Nr.: Fachbereich: Platz Nr.: Tutor: A. Mechanik (18 Punkte) 1. Wie
