Darstellung von Molekülen
|
|
|
- Daniela Hofer
- vor 6 Jahren
- Abrufe
Transkript
1 MM Darstellung von Molekülen Vorlesung II Speicherung von Molekülen in Dateien Dateiformat Referenz Koordinaten SMILES (.smi) Daylight nein MOLfile (.mol) SDfile (.sd) MDL kartesisch (2D,3D) MOL2 (.mol2) Tripos kartesisch (3D) PDB file (.pdb) Protein Databank kartesisch (3D) z-matrix intern 3D SMILES-Referenz Darstellung
2 MM Simplified Molecular Input Line Entry System SMILES ermöglicht die odierung der Molekültopologie als String. Atome werden durch chemische Symbole dargestellt 2. -Atome ergänzen freie Valenzen und werden weggelassen 3. Nachbaratome stehen nebeneinander 4. Einfachbindungen werden nicht explizit angegeben, = und # symbolisieren Doppel- und Dreifachbindungen 5. ( ) symbolisiert Verzweigungen 6. Ein Paar identischer Zahlen an Atomen symbolisiert einen Ringschluß 7. Aromatische Ring werden durch kleine Buchstaben dargestellt 8. Metalle und Metallionen stehen in eckigen Klammern 9. cis- und trans-isomerie wird durch / \ und / / dargestellt zeigen die Drehung gegen bzw. im Uhrzeigersinn von hiralitätszentren an SMILES - Beispiele Formel SMILES Formel SMILES 4 a 2+ [a+2], [a++] 2 5 O O cccccc N O 3 #N (=O)O 2 2 ccc2ccccc2cc O 3 OO - (=O)[O-] 2 N OO F 3 N[@]()(F)(=O)O N[@@](F)()(=O)O 3 3 /=/ F l Br [@](F)(l)Br [@@](F)(Br)l Darstellung 2
3 MM IUPA International hemical Identifier IUPA International hemical Identifier (InhI) Darstellung von Molekülen als standardisierte Zeichenkette codiert werden Konnektivität, Tautomerie, Isotopie, Stereochemie und Formalladung im Gegensatz zu SMILES Strings eindeutig Erzeugung z. B. Mit Pubhem Editor: Zweck Identifizierung in Datenbanken (Pubhem, SciFinder) Beipiel Ethanol InhI=/26O/c-2-3/h3,22,3 Summenformel 26O, Konnektivität startet mit dem Präfix c, Wasserstoffatome (Präfix h ) MOL- und SD-Format MOL-Datei für Essigsäure MOE2006 2D header V O O M END counts line atom block bond block properties block SD-Dateien sind eine Erweiterung der MOL-Dateien zur Darstellung mehrerer Moleküle (Trennung durch eine Zeile mit $$$$ ) Darstellung 3
4 MM AETIAID SMALL AETAID <> AETAID <> AETAID <> AETAID <> AETAID <> O O.3 AETAID <> AETAID <> O O.2 AETAID <> PDB-Format verbreitetes Format für Biopolymere Zeile beginnt mit einem Schlüsselwort für die dann folgenden Daten EADER, TITLE,... SEQRES Beschreibung Primärstruktur ET, ETNAM, FORMUL Angabe von nicht-standadrd Gruppen / Molekülen ELIX, SEET, TURN Sekundärstruktur ATOM, ETATM ONET Atomkoordinaten Bindungen von nicht-standard Gruppen / Molekülen Detaillierte Dokumentation Darstellung 4
5 MM Beispiel für PDB-Format REMARK MININMALE PDB_DATEI ATOM N GLY N+ ATOM 2 GLY ATOM 3 2 GLY ATOM 4 A GLY ATOM 5 GLY ATOM 6 O GLY O ATOM 7 3 GLY ATOM 8 A2 GLY ATOM 9 A3 GLY ATOM 0 N SER N ATOM N SER ATOM 2 A SER ATOM 3 SER ATOM 4 O SER O ATOM 5 B SER ATOM 6 OG SER O ATOM 7 A SER ATOM 8 B2 SER ATOM 9 B3 SER ATOM 20 G SER ATOM 2 OXT SER O- TER 22 SER 2 END Beispiel für PDB-Format Spezifikation von nicht-standard Molekülen RESIDUE 74 5 ONET L4 4 ONET 4 3L4 5 3 ONET ONET ONET ONET ONET ONET 3 O O2 ONET O 2 O ONET O2 ONET O O ONET 2 2 ONET 3 3 ONET 5 5 ONET 6 6 END ET 74 5 ETNAM 74 4-LORO-BENZOI AID FORMUL O2 L Darstellung 5
6 MM Aufbau einer z-matrix Atom Atom 2, Abstand -2, Atom 3, Abstand 2-3, 2, Winkel -2-3, Atom 4, Abstand 3-4, 3, Winkel 2-3-4, 2, Torsionswinkel , Atom 5, Die Atome werden durch ihr chemisches Symbol dargestellt und durchnummeriert. Die relative Position der Atome zu einander wird durch interne Koordinaten beschrieben. Für das. Atom sind keinerlei weitere Angaben erforderlich. Der Ort des Atoms 2 wird durch den Abstand zu Atom definiert. Der Ort des Atoms 3 wird durch den Abstand zu Atom oder 2 und den Winkel -2-3 definiert. Der Ort des Atoms 4 und weiteren Atomen wird durch den Abstand zu einem, den Winkel mit zwei und dem Torsionswinkel mit drei Atomen definiert. Die internen Koordinaten eines jeden Atoms werden immer mit den vorherigen Atomen definiert. Kein Atom darf mehrfach in einer Zeile auftreten WS09/0 Z-Matrix Beispiele Wasser O, ro,, ro,, ao, 2 2 O 3 Methanol O, ro,, ro, 2, ao,, rt,, ao, 2, 80.0, 3, rg,, aog, 2, do, 3, rg,, aog, 2, -do, O Darstellung 6
Daten, Datensammlung, Datenbank
 Daten, Datensammlung, Datenbank Inhalte Molekülstrukturen Spektren Patentinformation Moleküleigenschaften Fachliteratur Verweise Anbieterinformation Preise Implementierung Flatfile Lokale Datenbank www-zugriff
Daten, Datensammlung, Datenbank Inhalte Molekülstrukturen Spektren Patentinformation Moleküleigenschaften Fachliteratur Verweise Anbieterinformation Preise Implementierung Flatfile Lokale Datenbank www-zugriff
2. Übungsblatt. Praktikum Theoretische Chemie. Themenblock - Die Grundlagen. Molekülgeometrie
 Praktikum Theoretische Chemie Universität Regensburg Prof. Martin Schütz, Dr. Denis Usvyat, Thomas Merz Themenblock - Die Grundlagen 1 2. Übungsblatt Molekülgeometrie Kartesische Koordinaten Eine Möglichkeit,
Praktikum Theoretische Chemie Universität Regensburg Prof. Martin Schütz, Dr. Denis Usvyat, Thomas Merz Themenblock - Die Grundlagen 1 2. Übungsblatt Molekülgeometrie Kartesische Koordinaten Eine Möglichkeit,
Klausur zur Vorlesung "Grundzüge der Chemie" für Studierende des Maschinenbaus BITTE AUSFÜLLEN BITTE HALTEN SIE IHREN STUDENTAUSWEIS BEREIT
 1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
Moleküle mit mehr als einem Chiralitätselement
 Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
2. Übungsaufgabe: Geometrieoptimierung, Verwendung der Z-Matrix
 Theoretische Chemie II Übungen am Computer Prof. Bernhard Dick Christian Neiß Uni Regensburg WS 2003/2004 2. Übungsaufgabe: Geometrieoptimierung, Verwendung der Z-Matrix A. Vorbemerkungen: Angabe der Molekülgeometrie
Theoretische Chemie II Übungen am Computer Prof. Bernhard Dick Christian Neiß Uni Regensburg WS 2003/2004 2. Übungsaufgabe: Geometrieoptimierung, Verwendung der Z-Matrix A. Vorbemerkungen: Angabe der Molekülgeometrie
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Structure/Draw: zwischen den Modi wählen (Structure-Modus zum zeichnen von Molekülen, Draw-Modus zum zeichnen von Geräten und Apparaturen)
 Computer im (Chemie-)Unterricht Chemielehrerfortbildung 2007 Sebastian Musli 1) Grundfunktionen von Chemsketch 10.0 Hinweis: In der Version 10.0 mögen einige Buttons ein wenig von den abgedruckten im Design
Computer im (Chemie-)Unterricht Chemielehrerfortbildung 2007 Sebastian Musli 1) Grundfunktionen von Chemsketch 10.0 Hinweis: In der Version 10.0 mögen einige Buttons ein wenig von den abgedruckten im Design
Strukturisomere der Alkane
 Strukturisomere der Alkane Zusammenfassung Bei Alkanen tritt das Phänomen der Strukturisomerie auf. In diesem Artikel werden auf hoffentlich für Oberstufenschüler verständlichem Niveau Algorithmen beschrieben,
Strukturisomere der Alkane Zusammenfassung Bei Alkanen tritt das Phänomen der Strukturisomerie auf. In diesem Artikel werden auf hoffentlich für Oberstufenschüler verständlichem Niveau Algorithmen beschrieben,
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Oktett-Theorie von Lewis
 Oktett-Theorie von Lewis Oktettregel Atome versuchen durch die Nutzung gemeinsamer Elektronenpaare möglichst ein Elektronenoktett zu erlangen. allgemeiner: Edelgasregel Atome streben durch Vereinigung
Oktett-Theorie von Lewis Oktettregel Atome versuchen durch die Nutzung gemeinsamer Elektronenpaare möglichst ein Elektronenoktett zu erlangen. allgemeiner: Edelgasregel Atome streben durch Vereinigung
Einführung in das Molecular Modelling
 Einführung in das Molecular Modelling Darstellung und Bearbeitung dreidimensionaler Molekülstrukturen Berechnung der physikochemischen Eigenschaften Ziel: Einsicht in die molekularen Mechanismen der Arzneistoffwirkung
Einführung in das Molecular Modelling Darstellung und Bearbeitung dreidimensionaler Molekülstrukturen Berechnung der physikochemischen Eigenschaften Ziel: Einsicht in die molekularen Mechanismen der Arzneistoffwirkung
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1
 Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Valenz-Bindungstheorie H 2 : s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie
 Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
JavaScript. Dies ist normales HTML. Hallo Welt! Dies ist JavaScript. Wieder normales HTML.
 JavaScript JavaScript wird direkt in HTML-Dokumente eingebunden. Gib folgende Zeilen mit einem Texteditor (Notepad) ein: (Falls der Editor nicht gefunden wird, öffne im Browser eine Datei mit der Endung
JavaScript JavaScript wird direkt in HTML-Dokumente eingebunden. Gib folgende Zeilen mit einem Texteditor (Notepad) ein: (Falls der Editor nicht gefunden wird, öffne im Browser eine Datei mit der Endung
504 mm. 70 mm 310 mm
 504 mm 380 mm 70 mm 217 mm 217 mm 70 mm 310 mm Mappe Eckig - 1 mm füllhöhe - mit VK (1EM) beschnittenes Endformat: 504 x 380 mm Format mit Randbeschnitt: 508 x 384 mm Stand: 14.11.08 Rillung () 504 mm
504 mm 380 mm 70 mm 217 mm 217 mm 70 mm 310 mm Mappe Eckig - 1 mm füllhöhe - mit VK (1EM) beschnittenes Endformat: 504 x 380 mm Format mit Randbeschnitt: 508 x 384 mm Stand: 14.11.08 Rillung () 504 mm
GI Vektoren
 Vektoren Problem: Beispiel: viele Variablen vom gleichen Typ abspeichern Text ( = viele char-variablen), Ergebnisse einer Meßreihe ( = viele int-variablen) hierfür: Vektoren ( = Arrays = Feld ) = Ansammlung
Vektoren Problem: Beispiel: viele Variablen vom gleichen Typ abspeichern Text ( = viele char-variablen), Ergebnisse einer Meßreihe ( = viele int-variablen) hierfür: Vektoren ( = Arrays = Feld ) = Ansammlung
Grundlagen der Chemie Die Atombindung Kovalente Bindungen
 Die Atombindung Kovalente Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Kovalente Bindungen In einem
Die Atombindung Kovalente Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Kovalente Bindungen In einem
Prof. Dr. Stephen Hashmi, Sommersemester Organische Chemie für Technische Biologen, Organische Chemie für Lehramtskandidaten, Teil 2.
 Prof. Dr. ashmi, Sommersemester 2005 13 IV. Alkane Methan -C 2 - Ethan -C 2 -C 2 - Propan -C 2 -C 2 -C 2 - Butan -C 2 -C 2 -C 2 -C 2 - Pentan -C 2 -C 2 -C 2 -C 2 -C 2 - exan -C 2 -C 2 -C 2 -C 2 -C 2 -C
Prof. Dr. ashmi, Sommersemester 2005 13 IV. Alkane Methan -C 2 - Ethan -C 2 -C 2 - Propan -C 2 -C 2 -C 2 - Butan -C 2 -C 2 -C 2 -C 2 - Pentan -C 2 -C 2 -C 2 -C 2 -C 2 - exan -C 2 -C 2 -C 2 -C 2 -C 2 -C
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. hristoffers, Vorlesung Organische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. inführung 1.1 Atomorbitale Die Atome im Molekülverband werden durch lektronen
Prof. hristoffers, Vorlesung Organische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 1. inführung 1.1 Atomorbitale Die Atome im Molekülverband werden durch lektronen
Klausur : Allgemeine und Anorganische Chemie. Name...Fachrichtung... Matr.-Nr...
 Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
H2 1862 mm. H1 1861 mm
 1747 mm 4157 mm H2 1862 mm H1 1861 mm L1 4418 mm L2 4818 mm H2 2280-2389 mm H1 1922-2020 mm L1 4972 mm L2 5339 mm H3 2670-2789 mm H2 2477-2550 mm L2 5531 mm L3 5981 mm L4 6704 mm H1 2176-2219 mm L1 5205
1747 mm 4157 mm H2 1862 mm H1 1861 mm L1 4418 mm L2 4818 mm H2 2280-2389 mm H1 1922-2020 mm L1 4972 mm L2 5339 mm H3 2670-2789 mm H2 2477-2550 mm L2 5531 mm L3 5981 mm L4 6704 mm H1 2176-2219 mm L1 5205
Chemische Bindung, Molekülbau, Stöchiometrie
 Seminar zum Brückenkurs Chemie 2016 Chemische Bindung, Molekülbau, Stöchiometrie Dr. Jürgen Getzschmann Dresden, 20.09.2016 Zeichnen von Valenzstrichformeln 1. Zeichnen Sie die Strukturformeln der folgenden
Seminar zum Brückenkurs Chemie 2016 Chemische Bindung, Molekülbau, Stöchiometrie Dr. Jürgen Getzschmann Dresden, 20.09.2016 Zeichnen von Valenzstrichformeln 1. Zeichnen Sie die Strukturformeln der folgenden
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Übungsblatt 3: Algorithmen in Java & Grammatiken
 Humboldt-Universität zu Berlin Grundlagen der Programmierung (Vorlesung von Prof. Bothe) Institut für Informatik WS 15/16 Übungsblatt 3: Algorithmen in Java & Grammatiken Abgabe: bis 9:00 Uhr am 30.11.2015
Humboldt-Universität zu Berlin Grundlagen der Programmierung (Vorlesung von Prof. Bothe) Institut für Informatik WS 15/16 Übungsblatt 3: Algorithmen in Java & Grammatiken Abgabe: bis 9:00 Uhr am 30.11.2015
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
Kennsilbe. -an. -en -in. -yl. -ol. -al (VI) -on. (VII) -säure (VIII)
 Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Eine Beschreibung des Programms und der dahinter stehenden Philosophie.
 1 Geschichte Larry Wall schrieb ein Konfigurationsmanagementsystem und benötigte dazu ein Berichtwerkzeug, das mehrere Dateien gleichzeitig öffnen konnte. Awk konnte es damals nicht, daher schrieb er eine
1 Geschichte Larry Wall schrieb ein Konfigurationsmanagementsystem und benötigte dazu ein Berichtwerkzeug, das mehrere Dateien gleichzeitig öffnen konnte. Awk konnte es damals nicht, daher schrieb er eine
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006
 Übungsaufgaben zur Vorlesung hemie für Biologen, WS 2005/2006 Themenbereiche Atombau, chemische Bindung, Stöchiometrie, Aggregatzustände 1. Ergänzen Sie folgende Tabelle: Symbol Z M Protonen eutronen Elektronen
Übungsaufgaben zur Vorlesung hemie für Biologen, WS 2005/2006 Themenbereiche Atombau, chemische Bindung, Stöchiometrie, Aggregatzustände 1. Ergänzen Sie folgende Tabelle: Symbol Z M Protonen eutronen Elektronen
floatchart Flußdiagramme in TEX/L A TEX
 floatchart Flußdiagramme in TEX/L A TEX M. Schollmeyer 9. Februar 2006 floatchart sind eine Sammlung von Definitionen, die das Erstellen von Struktogrammen in TEX/L A TEX ermöglichen. Wenn man an L A TEX
floatchart Flußdiagramme in TEX/L A TEX M. Schollmeyer 9. Februar 2006 floatchart sind eine Sammlung von Definitionen, die das Erstellen von Struktogrammen in TEX/L A TEX ermöglichen. Wenn man an L A TEX
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Inhalt Das Zeichnen von Strukturformeln mit ISIS/Draw
 Inhalt Das Zeichnen von Strukturformeln mit ISIS/Draw 2 A Zeichnen von Strukturen mit Hilfe der Vorlagen und Zeichenwerkzeuge 2 B Vorlagen von den Vorlageseiten verwenden 3 C Zeichnen von Bindungen und
Inhalt Das Zeichnen von Strukturformeln mit ISIS/Draw 2 A Zeichnen von Strukturen mit Hilfe der Vorlagen und Zeichenwerkzeuge 2 B Vorlagen von den Vorlageseiten verwenden 3 C Zeichnen von Bindungen und
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Chiralität in der Natur und synthetisch
 Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Vokabular zur Stereochemie
 Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
Alkene / Additions-, Eliminierungsreaktionen
 2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
MM Kraftfelder. Michael Meyer. Vorlesung III. Kraftfelder
 MM 3.09.013 Kraftfelder Vorlesung III Kraftfelder Ziel Berechnung der potentiellen nergie eines bestimmten Moleküls als Funktion der Atomkoordinaten (potential energy surface). Beschreibung einer ganzen
MM 3.09.013 Kraftfelder Vorlesung III Kraftfelder Ziel Berechnung der potentiellen nergie eines bestimmten Moleküls als Funktion der Atomkoordinaten (potential energy surface). Beschreibung einer ganzen
Grundwissen der 10.Klasse NTG
 Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Arbeitsheft Isomerie Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Grundlagen. Atombindung, Nichtmetalle, Valenzelektronen, Bindende und
 Arbeitsheft Isomerie Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Grundlagen Atombindung, Nichtmetalle, Valenzelektronen, Bindende und 1.1 Verkürzte Schreibweisen 2 Freie Elektronenpaare,
Arbeitsheft Isomerie Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Grundlagen Atombindung, Nichtmetalle, Valenzelektronen, Bindende und 1.1 Verkürzte Schreibweisen 2 Freie Elektronenpaare,
Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3
 Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3 Teil 1: Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben p-orbitale? Skizzieren
Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3 Teil 1: Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben p-orbitale? Skizzieren
Landeshauptstadt Hannover
 Landeshauptstadt Hannover Schulbiologiezentrum 19.81 Stöchiometrie zum Anfassen Reaktionsgleichungen und Energiebilanzen mit Molekülmodellen begreifbar machen November 2015 Herausgeber: Landeshauptstadt
Landeshauptstadt Hannover Schulbiologiezentrum 19.81 Stöchiometrie zum Anfassen Reaktionsgleichungen und Energiebilanzen mit Molekülmodellen begreifbar machen November 2015 Herausgeber: Landeshauptstadt
Vorlesung 5. Alkane. Experimentalchemie, Prof. H. Mayr 20 Achtung Lückentext. Nur als Begleittext zur Vorlesung geeignet. Anzahl C-Atome im n-alkan
 Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
Programme und Skript-Sprache für die Modellierung von Molekülen und die Behandlung ihrer Konformationen
 Diplomarbeit die Modellierung von Molekülen und die Behandlung ihrer Autor: 07.Mai.2002 1 Überblick Motivation und Ziele Modellierung von Molekülen Konzeption Zusammenfassung Ausblick 2 Motivationen und
Diplomarbeit die Modellierung von Molekülen und die Behandlung ihrer Autor: 07.Mai.2002 1 Überblick Motivation und Ziele Modellierung von Molekülen Konzeption Zusammenfassung Ausblick 2 Motivationen und
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Alignment-Verfahren zum Vergleich biologischer Sequenzen
 zum Vergleich biologischer Sequenzen Hans-Joachim Böckenhauer Dennis Komm Volkshochschule Zürich. April Ein biologisches Problem Fragestellung Finde eine Methode zum Vergleich von DNA-Molekülen oder Proteinen
zum Vergleich biologischer Sequenzen Hans-Joachim Böckenhauer Dennis Komm Volkshochschule Zürich. April Ein biologisches Problem Fragestellung Finde eine Methode zum Vergleich von DNA-Molekülen oder Proteinen
Übung Datenstrukturen. Objektorientierung in C++
 Übung Datenstrukturen Objektorientierung in C++ Aufgabe 1a - Farben Schreiben Sie eine Klasse COLOR zur Beschreibung von Farben. Eine Farbe werde hierbei additiv durch ihren Rot-, Grün- und Blauanteil
Übung Datenstrukturen Objektorientierung in C++ Aufgabe 1a - Farben Schreiben Sie eine Klasse COLOR zur Beschreibung von Farben. Eine Farbe werde hierbei additiv durch ihren Rot-, Grün- und Blauanteil
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Repetitorium Informatik (Java)
 Repetitorium Informatik (Java) Tag 6 Lehrstuhl für Informatik 2 (Programmiersysteme) Übersicht 1 Klassen und Objekte Objektorientierung Begrifflichkeiten Deklaration von Klassen Instanzmethoden/-variablen
Repetitorium Informatik (Java) Tag 6 Lehrstuhl für Informatik 2 (Programmiersysteme) Übersicht 1 Klassen und Objekte Objektorientierung Begrifflichkeiten Deklaration von Klassen Instanzmethoden/-variablen
AK Chemie Baukasten Der Schüler als Molekülbaumeister Info X303
 Kategorie Übungen und Tests Übungsmodus ja Testmodus - Schwierigkeitsgrade 2/2 vorwählbare Aufgabenzahl 35 Aktueller Notenstand - Highscore ja Musik zur Belobigung wählbar Spezielle Hilfen: Dr. Atom Steuerung
Kategorie Übungen und Tests Übungsmodus ja Testmodus - Schwierigkeitsgrade 2/2 vorwählbare Aufgabenzahl 35 Aktueller Notenstand - Highscore ja Musik zur Belobigung wählbar Spezielle Hilfen: Dr. Atom Steuerung
Einführung in die Computerlinguistik Einführung in Python (2)
 Einführung in die Computerlinguistik Einführung in Python (2) Dozentin: Wiebke Petersen 11. Foliensatz Wiebke Petersen Einführung CL 1 Kurzwiederholung der letzten Sitzung Textausgabe mit print("text")
Einführung in die Computerlinguistik Einführung in Python (2) Dozentin: Wiebke Petersen 11. Foliensatz Wiebke Petersen Einführung CL 1 Kurzwiederholung der letzten Sitzung Textausgabe mit print("text")
3. Grundregeln für die Java-Programmierung
 3. Grundregeln für die Java-Programmierung Sprachaufbau von Java Programmen Stilistische Konventionen JavaDoc Allgemeine Informatik 2 SS09 Folie 2.1 Allgemeine Vorbemerkung Bei Programmiersprachen sind
3. Grundregeln für die Java-Programmierung Sprachaufbau von Java Programmen Stilistische Konventionen JavaDoc Allgemeine Informatik 2 SS09 Folie 2.1 Allgemeine Vorbemerkung Bei Programmiersprachen sind
Isomerie organischer Verbindungen
 15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
Übungsbeispiele Kapitel Organische Verbindungen
 Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
30. Lektion. Moleküle. Molekülbindung
 30. Lektion Moleküle Molekülbindung Lernziel: Moleküle entstehen aus Atomen falls ihre Wellenfunktionen sich derart überlappen, daß die Gesamtenergie abgesenkt wird. Begriffe Begriffe: Kovalente Bindung
30. Lektion Moleküle Molekülbindung Lernziel: Moleküle entstehen aus Atomen falls ihre Wellenfunktionen sich derart überlappen, daß die Gesamtenergie abgesenkt wird. Begriffe Begriffe: Kovalente Bindung
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
RO-Tutorien 3 / 6 / 12
 RO-Tutorien 3 / 6 / 12 Tutorien zur Vorlesung Rechnerorganisation Christian A. Mandery WOCHE 2 AM 06./07.05.2013 KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft
RO-Tutorien 3 / 6 / 12 Tutorien zur Vorlesung Rechnerorganisation Christian A. Mandery WOCHE 2 AM 06./07.05.2013 KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft
Chiralitätszentrum X X
 hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
1. Zusammenfassung der letzten Vorlesung
 Websiteentwicklung auf Basis vontypo3 TypoScript Unterlagen zur Vorlesung WS 15/16-6- 1. Zusammenfassung der letzten Vorlesung 2. Marker befüllen 3. Bildbearbeitung mit TypoScript 1 Root Seite anlegen
Websiteentwicklung auf Basis vontypo3 TypoScript Unterlagen zur Vorlesung WS 15/16-6- 1. Zusammenfassung der letzten Vorlesung 2. Marker befüllen 3. Bildbearbeitung mit TypoScript 1 Root Seite anlegen
zu große Programme (Bildschirmseite!) zerlegen in (weitgehend) unabhängige Einheiten: Unterprogramme
 Bisher Datentypen: einfach Zahlen, Wahrheitswerte, Zeichenketten zusammengesetzt Arrays (Felder) zur Verwaltung mehrerer zusammengehörender Daten desselben Datentypes eindimensional, mehrdimensional, Array-Grenzen
Bisher Datentypen: einfach Zahlen, Wahrheitswerte, Zeichenketten zusammengesetzt Arrays (Felder) zur Verwaltung mehrerer zusammengehörender Daten desselben Datentypes eindimensional, mehrdimensional, Array-Grenzen
Funktionen: Einleitung
 Funktionen: Einleitung Funktionen sind fundamentale Instrumente der Mathematik zur Beschreibung verschiedener Zusammenhänge. E 1 E 2 E 3 Der Abbildungsbegriff Abb. 1 1: Darstellung einer Abbildung Oft
Funktionen: Einleitung Funktionen sind fundamentale Instrumente der Mathematik zur Beschreibung verschiedener Zusammenhänge. E 1 E 2 E 3 Der Abbildungsbegriff Abb. 1 1: Darstellung einer Abbildung Oft
Atome - Chemische Symbole
 Atome - Chemische Symbole Um zu erklären, dass die Grundstoffe nicht weiter zerlegbar sind, nahm der englische Wissenschaftler John Dalton um 1800 an, dass die chemischen Elemente aus unteilbaren Teilchen
Atome - Chemische Symbole Um zu erklären, dass die Grundstoffe nicht weiter zerlegbar sind, nahm der englische Wissenschaftler John Dalton um 1800 an, dass die chemischen Elemente aus unteilbaren Teilchen
Summenformel Elektronenstrichformel Name Siedepunkt
 Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Zeichnen von Valenzstrichformeln
 Zeichnen von Valenzstrichformeln ür anorganische Salze werden keine Valenzstrichformeln gezeichnet, da hier eine ionische Bindung vorliegt. Die Elektronen werden vollständig übertragen und die Ionen bilden
Zeichnen von Valenzstrichformeln ür anorganische Salze werden keine Valenzstrichformeln gezeichnet, da hier eine ionische Bindung vorliegt. Die Elektronen werden vollständig übertragen und die Ionen bilden
3. Wieviel bindig sind folgende Elemente in kovalenten Bindungen? Einige Elemente können auch verschiedene Bindigkeiten zeigen
 Übungen zur VL Chemie für Biologen und umanbiologen 26. 11.2010 1. ennen Sie mindestens 2 Arten der chemischen Bindungen und geben Sie je 2 Beispielverbindungen dafür an (Strukturformel). 1) Ionische Bindung:
Übungen zur VL Chemie für Biologen und umanbiologen 26. 11.2010 1. ennen Sie mindestens 2 Arten der chemischen Bindungen und geben Sie je 2 Beispielverbindungen dafür an (Strukturformel). 1) Ionische Bindung:
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
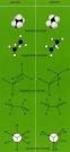 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Proseminar L A TEX Ausarbeitung zum Vortrag L A TEX in der Informatik
 Proseminar L A TEX Ausarbeitung zum Vortrag L A TEX in der Informatik Thilo Ohlemueller Juni 2006 Inhaltsverzeichnis 1 Einführung 2 2 Bäume 2 2.1 Einleitung............................... 2 2.2 Das Paket
Proseminar L A TEX Ausarbeitung zum Vortrag L A TEX in der Informatik Thilo Ohlemueller Juni 2006 Inhaltsverzeichnis 1 Einführung 2 2 Bäume 2 2.1 Einleitung............................... 2 2.2 Das Paket
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Atombindung. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Atombindung Das komplette Material finden Sie hier: School-Scout.de Titel: Atombindungen Reihe: Lernwerkstatt Bestellnummer:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Atombindung Das komplette Material finden Sie hier: School-Scout.de Titel: Atombindungen Reihe: Lernwerkstatt Bestellnummer:
Programmieren I + II Regeln der Code-Formatierung
 Technische Universität Braunschweig Dr. Werner Struckmann Institut für Programmierung und Reaktive Systeme WS 2016/2017, SS 2017 Programmieren I + II Regeln der Code-Formatierung In diesem Dokument finden
Technische Universität Braunschweig Dr. Werner Struckmann Institut für Programmierung und Reaktive Systeme WS 2016/2017, SS 2017 Programmieren I + II Regeln der Code-Formatierung In diesem Dokument finden
In der Quantenchemie versteht man unter core oder deutsch Rumpf den Kern inklusive
 Was ist ein core (Rumpf)? In der Quantenchemie versteht man unter core oder deutsch Rumpf den Kern inklusive innere Elektronenschalen, oder anders gesagt, ein Atom ohne seine Valenzelektronen. In den semiempirischen
Was ist ein core (Rumpf)? In der Quantenchemie versteht man unter core oder deutsch Rumpf den Kern inklusive innere Elektronenschalen, oder anders gesagt, ein Atom ohne seine Valenzelektronen. In den semiempirischen
Organische Chemie für MST 6. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Einstieg in die Informatik mit Java
 Vorlesung vom 18.4.07, Literalkonstanten Übersicht 1 Ganzzahlige Konstanten 2 Gleitkommakonstanten 3 Zeichenkonstanten 4 Zeichenketten 5 Boolsche Konstanten 6 null Referenz Literalkonstanten Literalkonstanten
Vorlesung vom 18.4.07, Literalkonstanten Übersicht 1 Ganzzahlige Konstanten 2 Gleitkommakonstanten 3 Zeichenkonstanten 4 Zeichenketten 5 Boolsche Konstanten 6 null Referenz Literalkonstanten Literalkonstanten
Fragen zum Thema chemische Reaktionen Klasse 4 1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion
 1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion vorliegen? 3. Wie nennt man die Stoffe, die nach der Reaktion vorliegen? 4. Womit wird die Richtung
1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion vorliegen? 3. Wie nennt man die Stoffe, die nach der Reaktion vorliegen? 4. Womit wird die Richtung
Werkzeuge der Informatik UNIX
 Autor: David Mainzer Institut für Informatik 1 Werkzeuge der Informatik UNIX Prof. Dr. Gabriel Zachmann (zach@in.tu-clausthal.de) David Mainzer (dm@tu-clausthal.de) Institut für Informatik 17. Dezember
Autor: David Mainzer Institut für Informatik 1 Werkzeuge der Informatik UNIX Prof. Dr. Gabriel Zachmann (zach@in.tu-clausthal.de) David Mainzer (dm@tu-clausthal.de) Institut für Informatik 17. Dezember
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1
 Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Übersicht. Vorstellung des OO-Paradigmas
 Java, OO und UML Vorstellung des OO-Paradigmas Übersicht Umsetzung des OO-Paradigmas in Java Einführung (seeeeeehr rudimenter) in UML zur graphischen Darstellung von OO Grammatik und Semantik von Java
Java, OO und UML Vorstellung des OO-Paradigmas Übersicht Umsetzung des OO-Paradigmas in Java Einführung (seeeeeehr rudimenter) in UML zur graphischen Darstellung von OO Grammatik und Semantik von Java
Organische Chemie. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie Name: Fachprüfung Vorname: 11. März 2002, 8 00-10 00 h Matr.-Nr.: Raum 204 + 206 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
Organische Chemie Name: Fachprüfung Vorname: 11. März 2002, 8 00-10 00 h Matr.-Nr.: Raum 204 + 206 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
Aufgabenblatt 10 Übungsblatt Stöchiometrie
 Name: Datum: Aufgabenblatt 10 Übungsblatt Stöchiometrie Berechnung von Stoffmengen bei chemischen Reaktionen II _ 20091005 Dr. Hagen Grossholz A1 Zusammenhang zwischen den verschiedenen Größen. Masse m
Name: Datum: Aufgabenblatt 10 Übungsblatt Stöchiometrie Berechnung von Stoffmengen bei chemischen Reaktionen II _ 20091005 Dr. Hagen Grossholz A1 Zusammenhang zwischen den verschiedenen Größen. Masse m
Berechnung eines Röntgen-Pulverdiffraktogramms aus Einkristallstrukturdaten, welche der ICSD entnommen wurden
 Versuch Nr. 3 Berechnung eines Röntgen-Pulverdiffraktogramms aus Einkristallstrukturdaten, welche der ICSD entnommen wurden Einleitung: Im ersten Versuch Ihres Praktikums haben Sie mit Hilfe von Einkristallstrukturdaten
Versuch Nr. 3 Berechnung eines Röntgen-Pulverdiffraktogramms aus Einkristallstrukturdaten, welche der ICSD entnommen wurden Einleitung: Im ersten Versuch Ihres Praktikums haben Sie mit Hilfe von Einkristallstrukturdaten
Organische Chemie. Kapitel 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Organische Verbindungen enthalten Kohlenstoff
 rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
1. Zusammenfassung der letzten Vorlesung
 Websiteentwicklung auf Basis vontypo3 TypoScript Unterlagen zur Vorlesung WS 14/15-6- 1. Zusammenfassung der letzten Vorlesung 2. Marker befüllen 3. Bildbearbeitung mit TypoScript 1 Template anlegen Template
Websiteentwicklung auf Basis vontypo3 TypoScript Unterlagen zur Vorlesung WS 14/15-6- 1. Zusammenfassung der letzten Vorlesung 2. Marker befüllen 3. Bildbearbeitung mit TypoScript 1 Template anlegen Template
Chemie. für die Berufsmaturität. Günter Baars. Chemie. Baars. Unter Mitarbeit von Franz Heini, Markus Isenschmid und Doris Kohler
 www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
Praktikumskurs SCF-Rechnungen
 Praktikumskurs SCF-Rechnungen SCF-1 Lernziele: - Sie können SCF-Rechnungen durchführen (SCF = Self Consistent Field) - Sie verstehen qualitativ was SCF-Rechnungen sind, wo sie relativ zu anderen Methoden
Praktikumskurs SCF-Rechnungen SCF-1 Lernziele: - Sie können SCF-Rechnungen durchführen (SCF = Self Consistent Field) - Sie verstehen qualitativ was SCF-Rechnungen sind, wo sie relativ zu anderen Methoden
Nanotechnologie der Biomoleküle. Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie. Aufbau Struktur Funktion
 anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
Praktikumskurs SCF-Rechnungen
 Praktikumskurs SCF-Rechnungen SCF-1 Lernziele: - Sie können SCF-Rechnungen durchführen (SCF = Self Consistent Field) - Sie verstehen qualitativ was SCF-Rechnungen sind, wo sie relativ zu anderen Methoden
Praktikumskurs SCF-Rechnungen SCF-1 Lernziele: - Sie können SCF-Rechnungen durchführen (SCF = Self Consistent Field) - Sie verstehen qualitativ was SCF-Rechnungen sind, wo sie relativ zu anderen Methoden
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie
 Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Bestimmung der Primärstruktur kleiner Moleküle mittels 1D-NMR-Spektroskopie
 Bestimmung der Primärstruktur kleiner Moleküle mittels 1D-NMR-Spektroskopie Zusammenfassung Mit Hilfe von 1D 1 H- und 13 C-NMR-Spektren und gegebener Summenformel wird die Primärstruktur eines unbekannten
Bestimmung der Primärstruktur kleiner Moleküle mittels 1D-NMR-Spektroskopie Zusammenfassung Mit Hilfe von 1D 1 H- und 13 C-NMR-Spektren und gegebener Summenformel wird die Primärstruktur eines unbekannten
Einführung in die Programmierung mit VBA
 Einführung in die Programmierung mit VBA Vorlesung vom 07. November 2016 Birger Krägelin Inhalt Vom Algorithmus zum Programm Programmiersprachen Programmieren mit VBA in Excel Datentypen und Variablen
Einführung in die Programmierung mit VBA Vorlesung vom 07. November 2016 Birger Krägelin Inhalt Vom Algorithmus zum Programm Programmiersprachen Programmieren mit VBA in Excel Datentypen und Variablen
Chapter 1 : þÿ b e t a t h o m e F i n a n z e n c h a p t e r
 Chapter 1 : þÿ b e t a t h o m e F i n a n z e n c h a p t e r þÿ E s v e r f ü g t d u r c h d i e b e t - a t - h o m e. c o m H o l d i n g L t d. m i t S i t z i n M a l t a ü b e r. 0 1. 0 8. 2 0
Chapter 1 : þÿ b e t a t h o m e F i n a n z e n c h a p t e r þÿ E s v e r f ü g t d u r c h d i e b e t - a t - h o m e. c o m H o l d i n g L t d. m i t S i t z i n M a l t a ü b e r. 0 1. 0 8. 2 0
Grundwissen Chemie Jahrgangsstufe 10 (NTG)
 Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Drehung um einen Punkt um Winkel α.
 Drehung um einen Punkt um Winkel α. Sei A R 2 und α R. Drehung um A um Winkel α ist eine Abbildung D A (α) : R 2 R 2 welche wie folgt definiert ist: D A (α) = T A D 0 (α) T ( A), wobei die Abbildung D
Drehung um einen Punkt um Winkel α. Sei A R 2 und α R. Drehung um A um Winkel α ist eine Abbildung D A (α) : R 2 R 2 welche wie folgt definiert ist: D A (α) = T A D 0 (α) T ( A), wobei die Abbildung D
Importdatei Grobkoordinaten mit Excel erstellen und bearbeiten
 Importdatei Grobkoordinaten mit Excel erstellen und bearbeiten Benutzerhandbuch Datum: 22.01.2016 Version: 1.1 Bearbeiter/in: Christoph Rüfenacht Status: In Arbeit Freigegeben Klassifikation: öffentlich
Importdatei Grobkoordinaten mit Excel erstellen und bearbeiten Benutzerhandbuch Datum: 22.01.2016 Version: 1.1 Bearbeiter/in: Christoph Rüfenacht Status: In Arbeit Freigegeben Klassifikation: öffentlich
