Versuchsprotokoll: Neutralisationsenthalpie
|
|
|
- Kerstin Esser
- vor 7 Jahren
- Abrufe
Transkript
1 Versuchsprotokoll: Neutralisationsenthalpie Patrik Wolfram TId: 0 Alina Heidbüchel TId: 19 Gruppe
2 Inhaltsverzeichnis 1. Einleitung...3. Theorie Durchführung Auswertung Bestimmung der Thermokraft Bestimmung der Wärmekapazität Bestimmung der Stoffmenge in der Lösung Konzentrationsbestimmung der Lösung Bestimmung der Stoffmenge Bestimmung der Verdünnungsenthalpie Bestimmung der Gesamtenthalpie Bestimmung der Neutralisationsenthalpie Ergebnisstabelle Diskussion Fehlerrechnung Fehler auf die Thermokraft Fehler auf die Wärmekapazität Fehler auf die Konzentrationsbestimmung der Lösung Fehler auf die Gesamtenthalpie...1
3 1. Einleitung In dem durchgeführten Experiment findet eine Säure Base Reatkion statt. Es wurden HCl und NaOH verwendet, sodass es sich um eine starke Säure und eine starke Base handelt. Dabei findet folgende Reaktionsgleichung statt: H + + OH - H O Von uns wird dabei die are Reaktionsenthalpie für die Neutralisation einer starken Säure durch eine starke Base bestimmt. Hierzu soll nun der auftretende Enthalpieunterschied bestimmt werden.. Theorie Es findet eine Reaktion einer starken Säure mit einer starken Base statt. Die Hauptreaktion lautet damit: H + + OH - H O (1) Diese Reaktion ist exotherm. Die jeweiligen Kationen bzw. Anionen spielen keine Rolle für die Enthalpieänderung. Im folgenden bezeichnen wir die Enthalpieänderung dieser Reaktion mit Tp H, der Neutralisationsenthalpie. Bei konstantem Druck und konstanter Temperatur gibt diese den Unterschied zwischen der Enthalpie des Wassers und der Summe der Enthalpien der H + und OH - - Ionen an. Zur Messung verwenden wir ein Kalorimeter, welches isotherm (Temperatur konstant) und isobar (Druck konstant) ist. Somit ist nur noch die Verrichtung von Arbeit zugelassen. Aus dem 1. Hauptsatz der Thermodynamik: und der Definition der Enthalpie: folgt: W * : zusätzlich am System verrichtete Arbeit U: innere Energie (extensive Zustandsgröße) Q: frei werdende Wärme du = dw + dq () H = U + p*v (3) H = W * + Q (4) Ist das System thermisch isoliert, sodass kein Wärmeaustausch mit der Umgebung stattfindet ist Q = 0. Für Gleichung (4) folgt damit: H = W * (5) Wir verwenden ein solches, adiabatisches Kalorimeter, welches ein geschlossenes thermisch isoliertes System ist. Die Enthalpiezunahme ist also nach Gleichung (5) gleich der zusätzlich am System verrichtete Arbeit. Wird nun auch keine zusätzliche Arbeit verrichtet (W * = 0), so bleibt die Enthalpie konstant. Es folgt aus Gleichung (5): H = 0 (6) Die ablaufende Neutralisationsreaktion findet unter konstantem Druck statt, aber nicht unter 3
4 konstanter Temperatur. Es tritt also eine Temperaturänderung ein. Die Reaktion geht somit nicht direkt von ihrem Ausgangszustand 1 isotherm isobar in den Endzustand über, sondern zunächst in einen Zustand 3, in dem die Temperatur höher ist als die des Ausgangszustandes. Dieser Verlauf ist in allen Zuständen isobar. Folgendes Schema zeigt diesen Übergang: Quelle: Versuchsbeschreibung Neutralisationsenthalpie, IPC Zunächst geht die Reaktion vom Ausgangszustand 1 in den Zustand 3 über, wobei kein Wärmeaustausch mit der Umgebung stattfindet und ohne Verrichtung zusätzlicher Arbeit. Somit bleibt für diesen Übergang die Enthalpieänderung konstant: H = 0 Vom Zustand 3 geht die Reaktion schließlich in den Zustand über. Es handelt sich bei der Enthalpie um eine Zustandsfunktion, d.h. dass diese zum einen nur von den veränderten Größen abhängt und dass es egal ist auf welchem Weg man zu Zustand gelangt. Somit folgt für die gesuchte Neutralisationsenthalpie: Tp H = - H (7) Um in unserem Fall die Enthalpiedifferenz H zwischen Zustand und Zustand 3 berechnen zu können benötigen wir die Definition der Wärmekapazität bei konstantem Druck C p : C p = H T p Bei der Wärmekapazität des Kalorimeters, welche Wasserwert C W genannt wird, handelt es sich um ein heterogenes System, das aus verschiedenen Teilen mit unterschiedlichen Massen besteht, welche spezifische Wärmekapazitäten besitzen. k: Anzahl der verschiedenen Teile m i : Masse des jeweiligen Teils C pi : Wärmekapazität des jeweiligen Teils (8) k m i C pi (9) i=1 4
5 Wenn man nun Gleichung (8) integriert in den Grenzen von T (Temperatur Zustand ) bis T 3 (Temperatur Zustand 3) so erhält man: T 3 T T 3 dh= H= C W dt (10) T In unserem Versuch können wir die Temperaturabhängigkeit von C W vernachlässigen, sodass man mit Gleichung (10) und Gleichung (7) zu folgender Gleichung kommt: Tp H = - C W *(T 3 T ) = - C W * T (11) Um den Wasserwert bestimmen zu können muss ein Kalibrierversuch durchgeführt werden, wobei zusätzliche Arbeit durch Wärmeenergie dem System zugeführt wird. Die Temperatur steigt dabei von T A auf T E an. Die Temperaturänderung ist somit wie folgt: Und somit folgt aus Gleichung (11) und Gleichung (1): T K = T E T A (1) T E H=W = C W dt=c W T K (13) T A C W = W T K (14) Es ergibt sich für die gesuchte Neutralisationsenthalpie durch Einsetzen in Gleichung (11): TP H= W T T K (15) Um die Temperatur zu messen benutzen wir eine Thermosäule mit einem Eis Wasser Bezugspunkt, wobei die Thermokraft φ der Thermosäule ein Maß für die Temperatur ist: φ = a * T (16) Man kann nun auf den Proportionalitätsfaktir a verzichten, da die Temperaturdifferenzen für den Neutralisationsversuch und den Kalibrierversuch als Quotient eingehen. Man erhält also abschließen für die Neutralisationsenthalpie aus Gleichung (15) und Gleichung (16): Tp H= W φ φ K (17) Fehlerrechnung: Hierzu werden folgende Formeln (PC Skript) angewandt: Mittelwert: x= 1 x n i (18) i=1 Streuung: x = n n i=1 x i x n 1 (19) Gaußsche Fehlerfortpflanzung: f = n df i=1 dx xi i (0) 5
6 3. Durchführung Es werden 17 ml einer HCl Lösung auf 100 ml aufgefüllt, sodass eine HCl Lösung der Konzentration c = bis,5 /l entstand. Zur genauen Bestimmung dieser Konzentration werden zwei Titrationen mit je 10 ml der hergestellten HCl Lösung mit einer 0,5 aren NaOH Maßlösung durchgeführt. Für die Neutralisationsreaktion, zu der die Enthalpie bestimmt werden sollte, werden 0 ml der HCl Lösung verwendet. Mit Hilfe der genauen Konzentration wird die Menge an NaOH Plättchen bestimmt die benötigt wird um die gesamte Säuremenge zu neutralisieren. Es wird ein Überschuss von 10% hinzugegeben. Die Menge NaOH Plättchen wird in das Kalorimeter gegeben und in ca. 00 ml dest. Wasser unter Rühren gelöst. Die Messung der Vorperiode beginnt. Dazu misst man in Zeitabständen von 1 min die Thermokraft. Nach 10 Minuten wird mit Hilfe einer Einlaufpipette 0 ml der Säure hinzugefügt und die Thermokraft weiterhin in Zeitabständen von 1 min gemessen. Zur genauen Bestimmung der Säuremenge wurde die Einlaufpipette mit der Säure gewogen und erneut nach dem Versuch um zu überprüfen wie groß die Säuremenge ist, welche nicht an der Reaktion teilgenommen hat. Abschließend wird an der neutralen Lösung eine Kalibrierung durchgeführt. Dazu wird der Heizstab 35 Sekunden eingeschaltet und der Heizstrom, sowie die Heizspannung gemessen. Es wird weiter 5 min die Thermokraft in Abständen von einer Minute gemessen. Danach wird ein abschließender Verdünnungsversuch durchgeführt. Dazu wird die selbe Menge an Säure verwendet, die Menge an NaOH wird jedoch durch die selbe Menge an dest. Wasser ersetzt. Wie im Versuch zuvor wird nach 10 Minuten Messung der Vorperiode die Säure hinzugegeben und 15 Minuten die Hauptperiode gemessen. Abschließend wird erneut 35s mit dem Heizstab erhitzt und 5 min die Nachperiode aufgenommen. 6
7 4.Auswertung 4.1 Bestimmung der Thermokraft Mit den aufgenommen Messwerten (vgl. Anhang) wurde die Thermokraft gegen die Zeit aufgetragen: 0, Neutralisationsenthalpie 0, , , ,00180 Thermokraft in V 0, , , , , , Zeit (t) in min Abbildung (1): Thermokraft gegen die Zeit 7
8 Die Thermokraft wurde nun wie im Skript dargestellt manuell bestimmt. Es wurden also direkt die φ bestimmt. Dabei ergaben sich die folgenden Werte (vgl. Anhang): Tabelle (1): Differenz der Theromkraft Spannungsdifferenz in V Fehler φ 47,6 µv ±,88µV φ K 60 µv ±,88µV Dabei ergibt sich der Fehler wie folgt: 4. Bestimmung der Wärmekapazität Durch die Definition der Arbeit: W = U*I*t und die aufgenommenen Werte (siehe Anhang) ergeben sich zunächst folgende Mittelwerte: Tabelle (): Aufgenommene Messwerte Heizstab Spannung [V] Stromstärke [ma] Zeit [s] Mittelwerte 9,67 376,33 35 Durch die Ablesegenauigkeit und die schwankenden Messwerte ergeben sich auf die errechneten Mittelwerte die folgenden Fehler: Tabelle (3): Messwerte des Heizstabes Zeit (t) in s Spannung in V Stromstärke in ma 35 s±0,5 s 9,67 V±1V 376,33 ma±1 ma Somit lässt sich die geleistete elektrische Arbeit errechnen: W = 9,67 V * 376,33 ma * 35 s = 305,093 kg m kg m A s 3 = 305,093 A s s = 305,093 J 8
9 4.3 Bestimmung der Stoffmenge in der Lösung Konzentrationsbestimmung der Lösung Es ist nötig die Konzentration der Lösung zu bestimmen um später die are Neutralisationsenthalpie berechnen zu können. Unsere hergestellte Lösung bestand aus 17 ml konz. Salzsäure, welche auf 100 ml mit dest. Wasser aufgefüllt wurde. Anschließend wurden 10 ml von dieser Lösung mit 0,5 arer NaOH Lösung titriert, wobei Phenolrot als Indikator diente. Es ergaben sich dadurch die folgenden Werte: Titration Verbrauch NaOH in ml 1 39,8 40,4 Mittelwert 40, Bestimmung der Stoffmenge Während des Versuches nimmt nicht die gesamte Säurestoffmenge am Versuch teil, denn es verbleibt ein geringer Rest in dem Glasröhrchen. Deshalb muss dieses vor dem Versuch und nach dem Versuch gewogen werden. Durch die Massendifferenz und die vom Assistenten mitgeteilte Dichte: ρ = 1,19 kg/l = 1,19 g/ml können die folgenden Werte ermittelt werden: Verdünnung Neutralisation m (Glasrohr) befüllt 111,713 g 111,55 g m (Glasrohr) leer 91,575 g 88,334 g m 0,138 g 3,18 g Volumen 16,93 ml 19,511 ml Mol 33,931 m 39,10 m (Hierbei ist der Fehler auf die Stoffmenge zu vernachlässigen, da die Auswirkung eher gering ist.) 4.4 Bestimmung der Verdünnungsenthalpie Möchte man bei diesem Versuch später die Neutralisationsenthalpie berechnen, so muss dort miteinbezogen werden, dass auch die Verdünnung einer Säure eine Enthalpiedifferenz bewirkt. Deshalb muss die Verdünnungsenthalpie von der Gesamtenthalpie abgezogen werden um die Neutralisationsenthalpie zu erhalten. Durch die Gleichung (11) und der berechneten Wärmekapazität des Wasserwertes folgt: H verd. = kj 50,418 0, J mv= 50, , mv= 88,988 J mv mv Dazu wurde φ verd = 0, mv wie im Teil zuvor per Hand bestimmt. Wir haben in Absprache mit unserem Assistenten die Kurve der Verdünnungsenthalpie unserer Komitonen verwendet, da 9
10 bei uns der erste Sprung kaum zu erkennen war (siehe Anhang). Für den zweiten Sprung haben wir schließlich nicht mehr den Wert per Hand bestimmt, sondern den zweiten Wert von unserer Neutralisationsenthalpie verwendet. Dies durften wir so machen, da wir bei der Neutralisation, wie bei der Verdünnung die gleiche Zeitspanne aufgeheizt haben. Dieses Vorgehen wurde so mit dem Assistenten abgesprochen und die errechneten Werte wurden vorgezeigt. Der Fehler von φ verd wird gemäß des Maßstabes als 1*10-9 V angenommen. Es ergibt sich somit für die Rechnung: H verd. = 50,418 kj mv 0, mv± V = 88,988 J±0,050 J Somit ergibt sich für die are Verdünnungsenthalpie: H verd = 88,988 J n 33,931 m = 6,646 J 4.5 Bestimmung der Gesamtenthalpie Man bestimmt durch die Gleichung (17) die Neutralisationsenthalpie und führt nach Gleichung (0) eine Gaußsche Fehlerfortpflanzung durch. H ges = W T T K 305,093 J 47,6µV = = 399,907 J 60µV H ge s= φ φ W W K φ φ φ W K φ K φ K =185,608 J => H ges = 399,907 J±185,608 J Somit ergibt sich die are Gesamtenthalpie unter Vernachlässigung des Fehlers auf die Stoffmenge (siehe oben): H ges 399,907 J±185,608 J = = 7079,038 n 33,931 m J ±5470,16 J 4.6 Bestimmung der Neutralisationsenthalpie Durch das Diagramm und Gleichung (7) folgt: Tp/ H= ges/ H verd/ H = 68106,39 Es bleibt bei der Addition der Fehler der Gesamtenthalpie enthalten. J ±5470,16 J 5. Ergebnisstabelle Messgröße Wert Fehler 10
11 Molare Neutralisationsenthalpie ( Tp/ H) 68106,39 J Molare Verdünnungsenthalpie ( verd/ H) 6,646 J Molare Gesamtenthalpie ( ges/ H) 7079,038 J ±5470,16 J Wird vernachlässigt ±5470,16 J 6. Diskussion Wenn man nun die Fehler und Messwerte im Detail betrachtet, so fällt auf, dass die Fehler sehr unterschiedliche Auswertung auf das Endergebnis haben. Der Fehler der Verdünnungsenthalpie kann beispielsweise im Vergleich zu dem der Gesamtenthalpie vernachlässigt werden. Ebenso der Fehler auf die Stoffmenge. Die Gesamtenthalpie hat augenscheinlich einen sehr großen Fehler. Dieser lässt sich jedoch auf den Fehler der zugeführten Wärme (stark schwankende Werte) und den Fehler der grafischen Bestimmung per Hand zurückführen. Ein Fehler von ca. 7,7% ist dabei noch im Toleranzbereich. Selbst genaueres Arbeiten würde keinen Effekt auf diesen Fehler haben, da dieser, wie erwähnt, größtenteils von der zugeführten Wärme abhängt. 7. Fehlerrechnung 7.1 Fehler auf die Thermokraft Auf die Bestimmung der jeweiligen Werte für φ ergibt sich aus der Ungenauigkeit durch die Anpassnung der Geraden und Senkrechten ein Fehler. Dieser wird für jeden Wert mit ± µv abgeschätzt, damit die niedrigsten und höchsten Grenzen der möglichen Fehler betrachtet werden. Mit: φ = φ - φ 1 (analog für φ K ) folgt durch Gaußsche Fehlerfortpflanzung (Gleichung 0): φ = φ1 φ = ±µv ±µv = 8µV =±,88µV Somit ist der Fehler auf φ und φ K,88 µv. 7. Fehler auf die Wärmekapazität Wie bei der Thermokraft lässt sich auch hier durch Gaußsche Fehlerfortpflanzung ein Fehler berechnen: = dw W du U dw di I dw dt t = 305,093 J 9,67 V 1V 305,093 J 0,37633 A 0,001 A 305,093 J 0,5 s =±45,888 J 35 s => W = 305,093 J ±45,888 J 11
12 Somit lässt sich direkt der Wasserwert bestimmen. Mit den Gleichungen (14) und (16) folgt: C W = W = 305,093 J kj =50,418 φ K V mv Wie bereits erläutert lässt sich auch auf C W der Fehler bestimmen: = dc W CW dw W dc W d φ φk = K 50,418 kj 50,418 kj mv mv ±45,888 J 305,093 J V ±, V =±,4964 kj mv => C W =50,418 kj kj ±,4964 mv mv 7.3 Fehler auf die Konzentrationsbestimmung der Lösung V = 39,8 ml 40,1 ml 40,4 ml 40,1 ml =±0,446 ml 1 => V = 40,1 ml ± 0,446 ml Durch das Volumen ergibt sich nun auch folgende Konzentration der Säure mit Fehler (durch Gaußsche Fehlerfortpflanzung): c HCl = Mit erneuter Fehlerfortpflanzung: 0,5 40,1 ml c NaOH V NaOH l = V HCl 10 ml c =,005 l ±0,446 ml =0,011 40,1 ml l => c HCl =,005 ±0,011 l l =,005 l 7.4 Fehler auf die Gesamtenthalpie H ge s= φ φ W W K φ φ φ W K φ K φ K =185,608 J 1
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 6 Kalorimetrie Aufgabe: Mittels eines Flüssigkeitskalorimeters ist a) die Neutralisationsenthalpie von säure b) die ösungsenthalpie
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 6 Kalorimetrie Aufgabe: Mittels eines Flüssigkeitskalorimeters ist a) die Neutralisationsenthalpie von säure b) die ösungsenthalpie
PCG Grundpraktikum Versuch 4 Neutralisationswärme Multiple Choice Test
 PCG Grundpraktikum Versuch 4 Neutralisationswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Neutralisationswärme wird dieses Vorgespräch durch einen
PCG Grundpraktikum Versuch 4 Neutralisationswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Neutralisationswärme wird dieses Vorgespräch durch einen
Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung
 Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
1.1 V 1 Überprüfung des Satzes von Hess mit der Reaktion von Calcium und Salzsäure
 1.1 V 1 Überprüfung des Satzes von Hess mit der Reaktion von Calcium und Salzsäure In diesem Versuch soll der Satz von Hess (die umgesetzte Wärmemenge ist bei einer chemischen Reaktion unabhängig vom Weg)
1.1 V 1 Überprüfung des Satzes von Hess mit der Reaktion von Calcium und Salzsäure In diesem Versuch soll der Satz von Hess (die umgesetzte Wärmemenge ist bei einer chemischen Reaktion unabhängig vom Weg)
Protokoll zum Versuch 3.1
 Grundpraktikum Physikalische Chemie Studiengang: Chemie-Ingenieurwesen Technische Universität München SS 2003 Protokoll zum Versuch 3.1 Kalorimetrie Gruppe 3 Kim Langbein Oliver Gobin 11 April 2003 Inhaltsverzeichnis
Grundpraktikum Physikalische Chemie Studiengang: Chemie-Ingenieurwesen Technische Universität München SS 2003 Protokoll zum Versuch 3.1 Kalorimetrie Gruppe 3 Kim Langbein Oliver Gobin 11 April 2003 Inhaltsverzeichnis
T5 - Hydratations- und Neutralisationsenthalpie
 T5 - Hydratations- und Neutralisationsenthalpie Aufgaben: 1. Messung der molaren integralen Lösungsenthalpie von Natriumhydrogenphosphat Na 2 HPO 4, Natriumhydrogenphosphat-dihydrat Na 2 HPO 4 2H 2 O,
T5 - Hydratations- und Neutralisationsenthalpie Aufgaben: 1. Messung der molaren integralen Lösungsenthalpie von Natriumhydrogenphosphat Na 2 HPO 4, Natriumhydrogenphosphat-dihydrat Na 2 HPO 4 2H 2 O,
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test
 PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
PCG Grundpraktikum Versuch 5 Lösungswärme Multiple Choice Test 1. Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Lösungswärme wird dieses Vorgespräch durch einen Multiple Choice
Der Zustand eines Systems ist durch Zustandsgrößen charakterisiert.
 Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
ADIABATISCHE KALORIMETRIE
 VERSUCH 6 ADIABATISCHE KALORIMETRIE Thema Kalorimetrische Bestimmung von Lösungs- und Neutralisationswärmen Grundlagen Literatur 1. Hauptsatz der Thermodynamik adiabatische Kalorimetrie Lösungs-, Neutralisations-,
VERSUCH 6 ADIABATISCHE KALORIMETRIE Thema Kalorimetrische Bestimmung von Lösungs- und Neutralisationswärmen Grundlagen Literatur 1. Hauptsatz der Thermodynamik adiabatische Kalorimetrie Lösungs-, Neutralisations-,
Verbrennungsenergie und Bildungsenthalpie
 Praktikum Physikalische Chemie I 1. Januar 2016 Verbrennungsenergie und Bildungsenthalpie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Bildungsenthalpie von Salicylsäure wurde
Praktikum Physikalische Chemie I 1. Januar 2016 Verbrennungsenergie und Bildungsenthalpie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 Aufgabenstellung Die Bildungsenthalpie von Salicylsäure wurde
PC-Grundpraktikum Versuch 7: Adiabatische Kalorimetrie vom Gruppe 2 (Johannes Martin und Christina Sauermann)
 PC-Grundpraktikum Versuch 7: Adiabatische alorimetrie vom 22.11.1999 Gruppe 2 (ohannes Martin und Christina Sauermann) 1 Versuch 7: Adiabatischen alorimetrie 1.Theorie Temperaturänderungen im Zusammenhang
PC-Grundpraktikum Versuch 7: Adiabatische alorimetrie vom 22.11.1999 Gruppe 2 (ohannes Martin und Christina Sauermann) 1 Versuch 7: Adiabatischen alorimetrie 1.Theorie Temperaturänderungen im Zusammenhang
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
TD 3: Neutralisationswärme
 TD 3: Neutralisationswärme Theoretische Einleitung Chemische Umsetzungen sind stets von einer Energieänderung begleitet, wobei der umgesetzte Energiebetrag entweder vom System aufgenommen (endotherme Reaktion)
TD 3: Neutralisationswärme Theoretische Einleitung Chemische Umsetzungen sind stets von einer Energieänderung begleitet, wobei der umgesetzte Energiebetrag entweder vom System aufgenommen (endotherme Reaktion)
Versuch Nr.53. Messung kalorischer Größen (Spezifische Wärmen)
 Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Physikalische Grundlagen und Aufgabenstellung
 Inhaltsverzeichnis Physikalische Grundlagen und Aufgabenstellung... 2 Versuchsziel... 2 Versuchsbeschreibung... 2 Elektrische Methode... 2 Mischungsmethode... 2 Messwerte... 2 Elektrische Methode... 2
Inhaltsverzeichnis Physikalische Grundlagen und Aufgabenstellung... 2 Versuchsziel... 2 Versuchsbeschreibung... 2 Elektrische Methode... 2 Mischungsmethode... 2 Messwerte... 2 Elektrische Methode... 2
Chemie Klausur
 Chemie Klausur 12.1 1 21. Oktober 2002 Aufgaben Aufgabe 1 1.1. Definiere: Innere Energie, Enthalpieänderung, Volumenarbeit, Standard-Bildungsenthalpie, molare Standard- Bildungsenthalpie. 4 VP 1.2. Stelle
Chemie Klausur 12.1 1 21. Oktober 2002 Aufgaben Aufgabe 1 1.1. Definiere: Innere Energie, Enthalpieänderung, Volumenarbeit, Standard-Bildungsenthalpie, molare Standard- Bildungsenthalpie. 4 VP 1.2. Stelle
Whitekalorimeter. Wärmekapazitätsbestimmung verschiedener Materialien. Dominik Büchler 5HL. Betreuer: Mag. Dr. Per Federspiel
 Dominik Büchler Physikalisch chemisches Laboratorium Betreuer: Mag. Dr. Per Federspiel 5HL Whitekalorimeter sbestimmung verschiedener Materialien Note: Datum: Unterschrift: Whitekalorimetrie Seite 1 von
Dominik Büchler Physikalisch chemisches Laboratorium Betreuer: Mag. Dr. Per Federspiel 5HL Whitekalorimeter sbestimmung verschiedener Materialien Note: Datum: Unterschrift: Whitekalorimetrie Seite 1 von
T1: Wärmekapazität eines Kalorimeters
 Grundpraktikum T1: Wärmekapazität eines Kalorimeters Autor: Partner: Versuchsdatum: Versuchsplatz: Abgabedatum: Inhaltsverzeichnis 1 Physikalische Grundlagen und Aufgabenstellung 2 2 Messwerte und Auswertung
Grundpraktikum T1: Wärmekapazität eines Kalorimeters Autor: Partner: Versuchsdatum: Versuchsplatz: Abgabedatum: Inhaltsverzeichnis 1 Physikalische Grundlagen und Aufgabenstellung 2 2 Messwerte und Auswertung
Praktikum Physik. Protokoll zum Versuch 5: Spezifische Wärme. Durchgeführt am Gruppe X
 Praktikum Physik Protokoll zum Versuch 5: Spezifische Wärme Durchgeführt am 10.11.2011 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
Praktikum Physik Protokoll zum Versuch 5: Spezifische Wärme Durchgeführt am 10.11.2011 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuer: Wir bestätigen hiermit, dass wir das
PHYSIKALISCHES PRAKTIKUM FÜR ANFÄNGER LGyGe. W 3 - Kalorimetrie
 10.08.2008 PHYSIKALISCHES PRAKTIKUM FÜR ANFÄNGER LGyGe Versuch: W 3 - Kalorimetrie 1. Grundlagen Definition und Einheit von Wärme und Temperatur; Wärmekapazität (spezifische und molare); Regel von Dulong
10.08.2008 PHYSIKALISCHES PRAKTIKUM FÜR ANFÄNGER LGyGe Versuch: W 3 - Kalorimetrie 1. Grundlagen Definition und Einheit von Wärme und Temperatur; Wärmekapazität (spezifische und molare); Regel von Dulong
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
PCI (Biol./Pharm.) Thermodyn. Musterlösung Übung 5 H.P. Lüthi / R. Riek HS Musterlösung Übung 5
 Musterlösung Übung 5 ufgabe 1: Enthalpieänderungen bei Phasenübergängen Es ist hilfreich, zuerst ein Diagramm wie das folgende zu konstruieren: (Die gesuchten Werte sind in den umrandeten oxen.) sub X
Musterlösung Übung 5 ufgabe 1: Enthalpieänderungen bei Phasenübergängen Es ist hilfreich, zuerst ein Diagramm wie das folgende zu konstruieren: (Die gesuchten Werte sind in den umrandeten oxen.) sub X
Musterlösung zu Übung 7
 PCI Thermodynamik G. eschke FS 011 Musterlösung zu Übung 7 (8. April 011) Aufgabe 1 (a) Die Shomate-Gleichung (Script (153)) lautet: C p (gas, T ) A + BT + CT + DT 3 + E T (1) Für das Kohlenstoffmonooxid
PCI Thermodynamik G. eschke FS 011 Musterlösung zu Übung 7 (8. April 011) Aufgabe 1 (a) Die Shomate-Gleichung (Script (153)) lautet: C p (gas, T ) A + BT + CT + DT 3 + E T (1) Für das Kohlenstoffmonooxid
Spezifische Wärme fester Körper
 1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
Übung 2. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Gefahrenstoffe. Styroporkalorimeter, Magnetrührer, digitales Thermometer, Stativ und Stativmaterial
 1.1 V 3 Lösungswärme von Salzen Dieser Versuch zeigt dass beim Lösen von Salzen Wärme freigesetzt wird. Es soll jeweils die emperaturdifferenz beim Lösen verschiedener Salze bestimmt werden und anschließend
1.1 V 3 Lösungswärme von Salzen Dieser Versuch zeigt dass beim Lösen von Salzen Wärme freigesetzt wird. Es soll jeweils die emperaturdifferenz beim Lösen verschiedener Salze bestimmt werden und anschließend
(b) Schritt I: freie adiabatische Expansion, also ist δw = 0, δq = 0 und damit T 2 = T 1. Folglich ist nach 1. Hauptsatz auch U = 0.
 3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
1 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure
 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure 1 1 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure Der Satz von Hess besagt, dass die Wärmemenge
V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure 1 1 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure Der Satz von Hess besagt, dass die Wärmemenge
Thermodynamik. Kapitel 4. Nicolas Thomas
 Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
Protokoll zum Versuch: Elektrisches Wärmeäquivalent
 Protokoll zum Versuch: Elektrisches Wärmeäquivalent Nils Brüdigam Fabian Schmid-Michels Universität Bielefeld Wintersemester 2006/2007 Grundpraktikum I 07.12.2006 Inhaltsverzeichnis 1 Ziel 2 2 Theorie
Protokoll zum Versuch: Elektrisches Wärmeäquivalent Nils Brüdigam Fabian Schmid-Michels Universität Bielefeld Wintersemester 2006/2007 Grundpraktikum I 07.12.2006 Inhaltsverzeichnis 1 Ziel 2 2 Theorie
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludigs-Universität Freiburg Lösungen zum 4. Übungsblatt zur orlesung Physikalische Chemie I SS 00 Prof. Dr. Bartsch 4. (6 Punkte) In einem Behälter mit der Grundfläche
Institut für Physikalische Chemie Albert-Ludigs-Universität Freiburg Lösungen zum 4. Übungsblatt zur orlesung Physikalische Chemie I SS 00 Prof. Dr. Bartsch 4. (6 Punkte) In einem Behälter mit der Grundfläche
Spezische Wärme von Festkörpern
 Spezische Wärme von Festkörpern Praktikumsversuch am 11.05.2011 Gruppe: 18 Thomas Himmelbauer Daniel Weiss Abgegeben am: 18.05.2011 Inhaltsverzeichnis 1 Einleitung 2 2 Vorbemerkung zur Fehlerrechnung 2
Spezische Wärme von Festkörpern Praktikumsversuch am 11.05.2011 Gruppe: 18 Thomas Himmelbauer Daniel Weiss Abgegeben am: 18.05.2011 Inhaltsverzeichnis 1 Einleitung 2 2 Vorbemerkung zur Fehlerrechnung 2
Stickstoff kann als ideales Gas betrachtet werden mit einer spezifischen Gaskonstante von R N2 = 0,297 kj
 Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Spezifische Wärmekapazität fester Körper
 Version: 14. Oktober 2005 Spezifische Wärmekapazität fester Körper Stichworte Wärmemenge, spezifische Wärme, Schmelzwärme, Wärmekapazität, Wasserwert, Siedepunkt, innere Energie, Energiesatz, Hauptsätze
Version: 14. Oktober 2005 Spezifische Wärmekapazität fester Körper Stichworte Wärmemenge, spezifische Wärme, Schmelzwärme, Wärmekapazität, Wasserwert, Siedepunkt, innere Energie, Energiesatz, Hauptsätze
Thermo Dynamik. Mechanische Bewegung (= Arbeit) Wärme (aus Reaktion) maximale Umsetzung
 Thermo Dynamik Wärme (aus Reaktion) Mechanische Bewegung (= Arbeit) maximale Umsetzung Aussagen der Thermodynamik: Quantifizieren von: Enthalpie-Änderungen Entropie-Änderungen Arbeit, maximale (Gibbs Energie)
Thermo Dynamik Wärme (aus Reaktion) Mechanische Bewegung (= Arbeit) maximale Umsetzung Aussagen der Thermodynamik: Quantifizieren von: Enthalpie-Änderungen Entropie-Änderungen Arbeit, maximale (Gibbs Energie)
Klausur Technische Chemie SS 2008 Prof. M. Schönhoff // PD Dr. C. Cramer-Kellers Klausur zur Vorlesung
 Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
Versuchsprotokoll: Konduktometrische Titration und Potentiometrische Titration
 Versuchsprotokoll: Konduktometrische Titration und Potentiometrische Titration Patrik Wolfram TId: 0 Alina Heidbüchel TId: 9 Gruppe 0 05.05.3 Inhaltsverzeichnis. Konduktometrische Titration...3. Einleitung...3.
Versuchsprotokoll: Konduktometrische Titration und Potentiometrische Titration Patrik Wolfram TId: 0 Alina Heidbüchel TId: 9 Gruppe 0 05.05.3 Inhaltsverzeichnis. Konduktometrische Titration...3. Einleitung...3.
E3: Potentiometrische Titration
 Theoretische Grundlagen Als potentiometrische Titration bezeichnet man ein Analyseverfahren, bei dem durch Messung der Gleichgewichtsspannung einer galvanischen Kette auf die Menge des zu titrierenden
Theoretische Grundlagen Als potentiometrische Titration bezeichnet man ein Analyseverfahren, bei dem durch Messung der Gleichgewichtsspannung einer galvanischen Kette auf die Menge des zu titrierenden
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
2.2 Spezifische und latente Wärmen
 1 Einleitung Physikalisches Praktikum für Anfänger - Teil 1 Gruppe 2 Wärmelehre 2.2 Spezifische und latente Wärmen Die spezifische Wärme von Wasser gibt an, wieviel Energie man zu 1 kg Wasser zuführen
1 Einleitung Physikalisches Praktikum für Anfänger - Teil 1 Gruppe 2 Wärmelehre 2.2 Spezifische und latente Wärmen Die spezifische Wärme von Wasser gibt an, wieviel Energie man zu 1 kg Wasser zuführen
Kalorimetrische Untersuchung verschiedener Enthalpieformen anhand von Oxalsäure, atronlauge, Essigsäure, Kaliumchlorid und Wasser
 Kalorimetrische Untersuchung verschiedener Enthalpieformen anhand von Oxalsäure, atronlauge, Essigsäure, Kaliumchlorid und Wasser Lisa Kamber, D-CHAB, 1. Semester kamberl@student.ethz.ch Jorge Ferreiro,
Kalorimetrische Untersuchung verschiedener Enthalpieformen anhand von Oxalsäure, atronlauge, Essigsäure, Kaliumchlorid und Wasser Lisa Kamber, D-CHAB, 1. Semester kamberl@student.ethz.ch Jorge Ferreiro,
Lösungswärme von Salzen
 Lösungswärme von Salzen In diesem Versuch wird die Lösungswärme von zwei Salzen, Calciumchlorid und Calciumchlorid-Hexahydrat ermittelt. Dabei wird die Temperaturänderung beim Lösen des Salzes kalorimetrisch
Lösungswärme von Salzen In diesem Versuch wird die Lösungswärme von zwei Salzen, Calciumchlorid und Calciumchlorid-Hexahydrat ermittelt. Dabei wird die Temperaturänderung beim Lösen des Salzes kalorimetrisch
Physik 2 Hydrologen et al., SoSe 2013 Lösungen 3. Übung (KW 19/20) Carnot-Wärmekraftmaschine )
 3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
Lehrbuch der Thermodynamik
 Ulrich Nickel Lehrbuch der Thermodynamik Eine verständliche Einführung Ж HANSER Carl Hanser Verlag München Wien VII Inhaltsverzeichnis 1 GRUNDBEGRIFFE DER THERMODYNAMIK 1 Einführung 1 Systeme 3 offene
Ulrich Nickel Lehrbuch der Thermodynamik Eine verständliche Einführung Ж HANSER Carl Hanser Verlag München Wien VII Inhaltsverzeichnis 1 GRUNDBEGRIFFE DER THERMODYNAMIK 1 Einführung 1 Systeme 3 offene
3 Der 1. Hauptsatz der Thermodynamik
 3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Gefahrenstoffe. 2 Bechergläser (230 ml), Bürette, Magnetrührer, Trichter, Rührschwein, Pipette, Stativ, Muffe, ph-meter
 1.1 V1 Titration von Cola In diesem Versuch wird die in Cola enthaltene Phosphorsäure mittels Säure-Base-Titration titriert und bestimmt. Ebenfalls wird mit den erhaltenen Werten gerechnet um das chemische
1.1 V1 Titration von Cola In diesem Versuch wird die in Cola enthaltene Phosphorsäure mittels Säure-Base-Titration titriert und bestimmt. Ebenfalls wird mit den erhaltenen Werten gerechnet um das chemische
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL. WiSe 2015/2016. Versuch 6. Adiabatischer Batch-Reaktor
 PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 6 Adiabatischer Batch-Reaktor Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Es wurde der Temperaturverlauf
PRAKTIKUM DER TECHNISCHEN CHEMIE I PRAKTIKUMSPROTOKOLL WiSe 2015/2016 Versuch 6 Adiabatischer Batch-Reaktor Rami Saoudi (356563) Guido Petri (364477) Gruppe 29 1. EINFÜHRUNG Es wurde der Temperaturverlauf
2 Grundbegriffe der Thermodynamik
 2 Grundbegriffe der Thermodynamik 2.1 Thermodynamische Systeme (TDS) Aufteilung zwischen System und Umgebung (= Rest der Welt) führt zu einer Klassifikation der Systeme nach Art der Aufteilung: Dazu: adiabatisch
2 Grundbegriffe der Thermodynamik 2.1 Thermodynamische Systeme (TDS) Aufteilung zwischen System und Umgebung (= Rest der Welt) führt zu einer Klassifikation der Systeme nach Art der Aufteilung: Dazu: adiabatisch
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
G1 pk S -Wert Bestimmung der Essigsäure
 G1 pk S -Wert Bestimmung der Essigsäure Bürette Rührer, Rührfisch ph-meter mit Einstabmesskette Stativ Becherglas Essigsäure H: 226, 314 P: 210, 260, 280.1+3, 303+361+353, 304+340, 305+351+338, 310 Phenolphthalein
G1 pk S -Wert Bestimmung der Essigsäure Bürette Rührer, Rührfisch ph-meter mit Einstabmesskette Stativ Becherglas Essigsäure H: 226, 314 P: 210, 260, 280.1+3, 303+361+353, 304+340, 305+351+338, 310 Phenolphthalein
Protokoll Grundpraktikum: F5 Dichte fester Körper
 Protokoll Grundpraktikum: F5 Dichte fester Körper Sebastian Pfitzner 6. Februar 013 Durchführung: Sebastian Pfitzner (553983), Jannis Schürmer (5589) Arbeitsplatz: 4 Betreuer: Anicó Kulow Versuchsdatum:
Protokoll Grundpraktikum: F5 Dichte fester Körper Sebastian Pfitzner 6. Februar 013 Durchführung: Sebastian Pfitzner (553983), Jannis Schürmer (5589) Arbeitsplatz: 4 Betreuer: Anicó Kulow Versuchsdatum:
Bestimmung der Wärmekapazitäten mit dem Erwärmungskalorimeter
 Bestimmung der Wärmekapazitäten mit dem Erwärmungskalorimeter 1.1 Durchführung In einem Stromkreis sind neben dem Netzgerät auch ein Amperemeter, Voltmeter und ein Kalorimeter miteingebunden. Auf einer
Bestimmung der Wärmekapazitäten mit dem Erwärmungskalorimeter 1.1 Durchführung In einem Stromkreis sind neben dem Netzgerät auch ein Amperemeter, Voltmeter und ein Kalorimeter miteingebunden. Auf einer
Bevor man sich an diesen Hauptsatz heranwagt, muss man sich über einige Begriffe klar sein. Dazu gehört zunächst die Energie.
 Thermodynamik 1 1.Hauptsatz der Thermodynamik Bevor man sich an diesen Hauptsatz heranwagt, muss man sich über einige Begriffe klar sein. Dazu gehört zunächst die Energie. Energie ist die Fähigkeit Arbeit
Thermodynamik 1 1.Hauptsatz der Thermodynamik Bevor man sich an diesen Hauptsatz heranwagt, muss man sich über einige Begriffe klar sein. Dazu gehört zunächst die Energie. Energie ist die Fähigkeit Arbeit
Festkörper - System steht unter Atmosphärendruck gemessenen Wärmen erhalten Index p : - isoliert
 Kalorimetrie Mit Hilfe der Kalorimetrie können die spezifischen Wärmekapazitäten für Festkörper, Flüssigkeiten und Gase bestimmt werden. Kalorische Grundgleichung: ΔQ = c m ΔT Festkörper - System steht
Kalorimetrie Mit Hilfe der Kalorimetrie können die spezifischen Wärmekapazitäten für Festkörper, Flüssigkeiten und Gase bestimmt werden. Kalorische Grundgleichung: ΔQ = c m ΔT Festkörper - System steht
1. Ziel des Versuchs. 2. Theorie. Dennis Fischer Gruppe 9 Magdalena Boeddinghaus
 Versuch Nr. 1: Joule - Thomson - Effekt 1. Ziel des Versuchs In diesem Versuch soll der Joule - Thomson - oeffizient für CO und N bestimmt werden.. Theorie Einfache Zustandsgleichungen gegeben das reale
Versuch Nr. 1: Joule - Thomson - Effekt 1. Ziel des Versuchs In diesem Versuch soll der Joule - Thomson - oeffizient für CO und N bestimmt werden.. Theorie Einfache Zustandsgleichungen gegeben das reale
Auswertung. C16: elektrische Leitung in Halbleitern
 Auswertung zum Versuch C16: elektrische Leitung in Halbleitern Alexander FufaeV Partner: Jule Heier Gruppe 434 Einleitung In diesem Versuch sollen wir die elektrische Leitung in Halbleitern untersuchen.
Auswertung zum Versuch C16: elektrische Leitung in Halbleitern Alexander FufaeV Partner: Jule Heier Gruppe 434 Einleitung In diesem Versuch sollen wir die elektrische Leitung in Halbleitern untersuchen.
E1: Bestimmung der Dissoziationskonstante einer schwachen Säure durch Messung der elektrischen Leitfähigkeit der Elektrolytlösung
 Versuch E1/E2 1 Versuch E1/E2 E1: Bestimmung der Dissoziationskonstante einer schwachen Säure durch Messung der elektrischen Leitfähigkeit der Elektrolytlösung E2: Konduktometrische Titration I Aufgabenstellung
Versuch E1/E2 1 Versuch E1/E2 E1: Bestimmung der Dissoziationskonstante einer schwachen Säure durch Messung der elektrischen Leitfähigkeit der Elektrolytlösung E2: Konduktometrische Titration I Aufgabenstellung
3. Berechnung der molaren Verbrennungsenthalpie. 4. Berechnung der Standardreaktionsenthalpie für die Hydrierung von Phthalsäureanhydrid
 Verbrennungswärme Aufgaben: 1. Ermittlung der Wärmekapazität des Kalorimeters durch Verbrennen einer Eichsubstanz. 2. Bestimmung der spezifischen Verbrennungswärmen von Phthalsäureanhydrid und Tetrahydrophthalsäureanhydrid.
Verbrennungswärme Aufgaben: 1. Ermittlung der Wärmekapazität des Kalorimeters durch Verbrennen einer Eichsubstanz. 2. Bestimmung der spezifischen Verbrennungswärmen von Phthalsäureanhydrid und Tetrahydrophthalsäureanhydrid.
4.1.2 Quantitative Definition durch Wärmekapazitäten
 4 Energie Aus moderner (mikroskopischer Sicht ist klar, daß die Summe U der kinetischen Energien der Moleküle eines Gases (und ggf. ihrer Wechselwirkungsenergien eine thd. Zustandsgröße des Gases ist,
4 Energie Aus moderner (mikroskopischer Sicht ist klar, daß die Summe U der kinetischen Energien der Moleküle eines Gases (und ggf. ihrer Wechselwirkungsenergien eine thd. Zustandsgröße des Gases ist,
Anleitung zum Physikpraktikum für Oberstufenlehrpersonen Einführungsversuch (EV) Herbstsemester Physik-Institut der Universität Zürich
 Anleitung zum Physikpraktikum für Oberstufenlehrpersonen Einführungsversuch (EV) Herbstsemester 2017 Physik-Institut der Universität Zürich Inhaltsverzeichnis 1 Einführungsversuch (EV) 11 11 Einleitung
Anleitung zum Physikpraktikum für Oberstufenlehrpersonen Einführungsversuch (EV) Herbstsemester 2017 Physik-Institut der Universität Zürich Inhaltsverzeichnis 1 Einführungsversuch (EV) 11 11 Einleitung
Bernhard Härder. Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik W/ WESTAR.P WISSENSCHAFTEN. Skripte, Lehrbücher Band 2
 Bernhard Härder Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik Skripte, Lehrbücher Band 2 W/ WESTAR.P WISSENSCHAFTEN Inhaltsverzeichnis Vorwort zur ersten Auflage Vorwort zur
Bernhard Härder Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik Skripte, Lehrbücher Band 2 W/ WESTAR.P WISSENSCHAFTEN Inhaltsverzeichnis Vorwort zur ersten Auflage Vorwort zur
PC-Übung Nr.3 vom
 PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
m T 1 0.5kg 8.6K = 7535 m T 2 0.5kg 10.4K = 6923 J
 3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
3 Lösungen Lösung zu 39. Zugeführte Energie ro Schritt E W h 36kJ..5l Wasser nähern wir mit der Masse.5kg an. mol Wasser hat eine Masse von 8g. Also sind in dem Behälter 28.78mol Wasser. Aus den beiden
Schülervorbereitungsseminar an der Rheinischen Friedrich-Wilhelms- Universität Bonn für die Chemieolympiade Teil 3: Physikalische Chemie
 Prof. Dr. Robert Glaum Institut für Anorganische Chemie Gerhard-Domagk-Straße 1 D-53121 Bonn (Germany) Tel. +49 228 / 73 53 53 Fax. +49 228 / 73 56 60 e-mail: rglaum @uni-bonn.de Schülervorbereitungsseminar
Prof. Dr. Robert Glaum Institut für Anorganische Chemie Gerhard-Domagk-Straße 1 D-53121 Bonn (Germany) Tel. +49 228 / 73 53 53 Fax. +49 228 / 73 56 60 e-mail: rglaum @uni-bonn.de Schülervorbereitungsseminar
Fachhochschule Flensburg. Die spezifische Wärmekapazität fester Körper
 Name : Fachhochschule Flensburg Fachbereich Technik Institut für Physik und Werkstoffe Name: Versuch-Nr: W4 Die spezifische Wärmekapazität fester Körper Gliederung: Seite Einleitung 1 Berechnung 1 Versuchsbeschreibung
Name : Fachhochschule Flensburg Fachbereich Technik Institut für Physik und Werkstoffe Name: Versuch-Nr: W4 Die spezifische Wärmekapazität fester Körper Gliederung: Seite Einleitung 1 Berechnung 1 Versuchsbeschreibung
Korrektur Versuchsprotokoll: Atomabsorptions- und Atomemissionsspektroskopie
 Korrektur Versuchsprotokoll: Atomabsorptions- und Atomemissionsspektroskopie Patrik Wolfram TId: 20 Alina Heidbüchel TId: 19 Gruppe 10 21.04.13 1 Durchführung Beide Geräte wurden zu Beginn durch bereits
Korrektur Versuchsprotokoll: Atomabsorptions- und Atomemissionsspektroskopie Patrik Wolfram TId: 20 Alina Heidbüchel TId: 19 Gruppe 10 21.04.13 1 Durchführung Beide Geräte wurden zu Beginn durch bereits
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
T6 - Verbrennungswärmen
 T6 - Verbrennungswärmen 1. Problemstellung: Die molaren Standardbildungs- und Standardverbrennungsenthalpien und V ür n-exan und Cyclohexan, zweier verwandter Strukturen, sind zu bestimmen. Die unterschiedlichen
T6 - Verbrennungswärmen 1. Problemstellung: Die molaren Standardbildungs- und Standardverbrennungsenthalpien und V ür n-exan und Cyclohexan, zweier verwandter Strukturen, sind zu bestimmen. Die unterschiedlichen
Säure-Base Titrationen
 Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 2,
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
Grundpraktikum A T7 Spezifische Wärmekapazität idealer Gase
 Mathematisch-Naturwissenschaftliche Fakultät Institut für Physik Grundpraktikum A T7 Spezifische Wärmekapazität idealer Gase 16.6.217 Studenten: Tim Will Betreuer: Raum: Messplatz: M. NEW14-2.15 Links
Mathematisch-Naturwissenschaftliche Fakultät Institut für Physik Grundpraktikum A T7 Spezifische Wärmekapazität idealer Gase 16.6.217 Studenten: Tim Will Betreuer: Raum: Messplatz: M. NEW14-2.15 Links
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Musterlösung Übung 3
 Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
Auswertung. B04: Spezifische Wärme
 Auswertung zum Versuch B04: Spezifische Wärme Alexander FufaeV Partner: Jule Heier Gruppe 254 Inhaltsverzeichnis 2. Bestimmung der Wärmekapazität C1 des blauen Dewargefäßes... 3 3. Bestimmung der Schmelzwärme
Auswertung zum Versuch B04: Spezifische Wärme Alexander FufaeV Partner: Jule Heier Gruppe 254 Inhaltsverzeichnis 2. Bestimmung der Wärmekapazität C1 des blauen Dewargefäßes... 3 3. Bestimmung der Schmelzwärme
C Metallkristalle. Allgemeine Chemie 60. Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4. Tabelle 7: weiter Strukturtypen. kubisch innenzentriert KZ = 8
 Allgemeine Chemie 60 Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4 Tabelle 7: weiter Strukturtypen C Metallkristalle kubisch primitiv KZ = 6 kubisch innenzentriert KZ = 8 kubisch flächenzentriert, kubisch dichteste
Allgemeine Chemie 60 Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4 Tabelle 7: weiter Strukturtypen C Metallkristalle kubisch primitiv KZ = 6 kubisch innenzentriert KZ = 8 kubisch flächenzentriert, kubisch dichteste
Inhaltsverzeichnis. 1. Chemische Grundbegriffe...9
 sverzeichnis 3 1. Chemische Grundbegriffe...9 1.1. Sinn und Zweck dieser Lehreinheit... 9 1.2. Das Wesen der Naturwissenschaften... 10 1.3. Stoffe und Körper...12 1.4. Physikalische und chemische Vorgänge...
sverzeichnis 3 1. Chemische Grundbegriffe...9 1.1. Sinn und Zweck dieser Lehreinheit... 9 1.2. Das Wesen der Naturwissenschaften... 10 1.3. Stoffe und Körper...12 1.4. Physikalische und chemische Vorgänge...
Gasthermometer. durchgeführt am von Matthias Dräger, Alexander Narweleit und Fabian Pirzer
 Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum
 Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum Tobias Schabel Datum des Praktikumstags: 02.12.2005 Matthias Ernst Protokoll-Datum: 12/20/2005 Gruppe A-11 11. Versuch: Schmelzdiagramm Assistent:
Praktikumsprotokoll Physikalisch-Chemisches Anfängerpraktikum Tobias Schabel Datum des Praktikumstags: 02.12.2005 Matthias Ernst Protokoll-Datum: 12/20/2005 Gruppe A-11 11. Versuch: Schmelzdiagramm Assistent:
Thermodynamik I Klausur 1
 Aufgabenteil / 100 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
Aufgabenteil / 100 Minuten Name: Vorname: Matr.-Nr.: Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern abgegeben werden. Nicht nachvollziehbare
Versuchsprotokoll Grundpraktikum Analytische Chemie WS 09/10. V2/3: Coulometrie. Coulometrische Titration von Ascorbinsäure
 Versuchsprotokoll Grundpraktikum Analytische Chemie WS 09/10 V2/3: Coulometrie Coulometrische Titration von Ascorbinsäure Versuchsdurchführung: 01.03.2010 Protokollabgabe: 03.03.2010 durchgeführt von:
Versuchsprotokoll Grundpraktikum Analytische Chemie WS 09/10 V2/3: Coulometrie Coulometrische Titration von Ascorbinsäure Versuchsdurchführung: 01.03.2010 Protokollabgabe: 03.03.2010 durchgeführt von:
TU-München, Musterlösung. Experimentalphysik II - Ferienkurs Andreas Schindewolf
 TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
ST Der Stirling-Motor als Wärmekraftmaschine
 ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
PN 1 Einführung in die Experimentalphysik für Chemiker und Biologen
 PN 1 Einführung in die Experimentalphysik für Chemiker und Biologen 26.1.2007 Paul Koza, Nadja Regner, Thorben Cordes, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 1 Einführung in die Experimentalphysik für Chemiker und Biologen 26.1.2007 Paul Koza, Nadja Regner, Thorben Cordes, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Formel X Leistungskurs Physik 2001/2002
 Versuchsaufbau: Messkolben Schlauch PI Barometer TI 1 U-Rohr-Manometer Wasser 500 ml Luft Pyknometer 2 Bild 1: Versuchsaufbau Wasserbad mit Thermostat Gegeben: - Länge der Schläuche insgesamt: 61,5 cm
Versuchsaufbau: Messkolben Schlauch PI Barometer TI 1 U-Rohr-Manometer Wasser 500 ml Luft Pyknometer 2 Bild 1: Versuchsaufbau Wasserbad mit Thermostat Gegeben: - Länge der Schläuche insgesamt: 61,5 cm
Neutralisationsenthalpie in Wasser
 Übungen in physikalischer Chemie für B. Sc.-Studierende Versuch Nr.: S11 Version 2018 (090318) Kurzbezeichnung: Neutralisation Neutralisationsenthalpie in Wasser Aufgabenstellung Mit einem Kalorimeter
Übungen in physikalischer Chemie für B. Sc.-Studierende Versuch Nr.: S11 Version 2018 (090318) Kurzbezeichnung: Neutralisation Neutralisationsenthalpie in Wasser Aufgabenstellung Mit einem Kalorimeter
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Übungsaufgaben Chemie Nr. 3
 Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Übungsaufgaben Chemie Nr. 3 22) Wie hoch ist die Molarität der jeweiligen Lösungen, wenn die angegebene Substanzmenge in Wasser gelöst und auf 200 ml aufgefüllt wurde? a) 58.44g NaCl (Kochsalz) b) 100
Grundpraktikum T7 spezifische Wärmekapazität idealer Gase
 Grundpraktikum T7 spezifische Wärmekapazität idealer Gase Julien Kluge 11. Mai 2015 Student: Julien Kluge (564513) Partner: Emily Albert (564536) Betreuer: Maximilian Kockert Raum: 215 Messplatz: 2 (Clément-Desormes
Grundpraktikum T7 spezifische Wärmekapazität idealer Gase Julien Kluge 11. Mai 2015 Student: Julien Kluge (564513) Partner: Emily Albert (564536) Betreuer: Maximilian Kockert Raum: 215 Messplatz: 2 (Clément-Desormes
Stirling-Maschine (STI)
 TUM Anfängerpraktikum für Physiker II Wintersemester 26/27 Stirling-Maschine (STI) Inhaltsverzeichnis 5. Dezember 26 1. Einleitung...2 2. Thermodynamische Kreisprozesse...2 3. Versuchsdurchführung...3
TUM Anfängerpraktikum für Physiker II Wintersemester 26/27 Stirling-Maschine (STI) Inhaltsverzeichnis 5. Dezember 26 1. Einleitung...2 2. Thermodynamische Kreisprozesse...2 3. Versuchsdurchführung...3
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan
 Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
Physik 4 Praktikum Auswertung Zustandsdiagramm Ethan Von J.W., I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Zustandsgleichung....... 2 2.2. Koexistenzgebiet........ 3 2.3. Kritischer
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
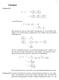 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
Übungen zu Experimentalphysik 2 für MSE
 Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
Essigsäure färbt ph-papier rot. Natronlauge färbt ph-papier blau
 5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
Hauptsatz der Thermodynamik
 0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
