Responsibility Split. <Studie XXX>
|
|
|
- Gerd Holtzer
- vor 8 Jahren
- Abrufe
Transkript
1 Responsibility Split <Studie > Der Responsibility Split listet alle wesentlichen Tätigkeiten im Rahmen der klinischen Studie und deren Zuordnung zu den Kooperationspartnern auf. Er gliedert sich chronologisch in die Abschnitte Vorbereitung, Durchführung und Abschluss. Die Kreuze markieren die Verantwortlichkeiten / Zuständigkeiten für die jeweilige Aufgabe. Punkte, die für die jeweilige Studie voraussichtlich nicht zum Tragen kommen, werden als nicht zutreffend ( n.z. ) gekennzeichnet. Dabei markiert die Stelle, an der das n.z. gesetzt wird, die entsprechende Verantwortlichkeit/Zuständigkeit, falls die Punkte während des Studienverlaufs doch zum Tragen kommen. In solchen Fällen sind ggf. Kosten neu zu kalkulieren. Der Responsibility Split enthält nicht nur Aufgaben, die in der Verantwortlichkeit des ZKS Köln bzw. des IMSIE liegen. Die Zuordnung von Aufgabenbereichen zu anderen beteiligten Institutionen ist für diese nicht bindend, sondern dient zur Abgrenzung der vom ZKS Köln bzw. dem IMSIE zu übernehmenden Aufgaben. ResponsibilitySplit_V3-28.doc 1/10
2 Hinweise zum Dokument Der Responsibility Split ist ein Kerndokument für die Projektplanung und dient der Transparenz. Er wird zur Unterstützung bei den Absprachen zur Kooperations- und Finanzplanung herangezogen. In der finalisierten Version wird er Angebotsbestandteil und ist damit vertragsrelevant. Generell sollten im Responsibility Split alle relevanten Aufgaben auftauchen, soweit sie im Rahmen der Projektplanung absehbar sind. Die Kreuze markieren dabei die Verantwortlichkeit / Zuständigkeit für die jeweilige Aufgabe. Wird eine Aufgabe arbeitsteilig durchgeführt, sollte die Art der Aufteilung möglichst eindeutig gekennzeichnet werden. Punkte, die für die jeweilige Studie voraussichtlich nicht zum Tragen kommen, sollten als nicht zutreffend ( n.z. ) gekennzeichnet werden. Alternativ, wenn dies als sinnvoller erachtet wird, kann die entsprechende Zeile gelöscht werden. Aufgabenbereiche (grau unterlegt und mit Hauptnummern gekennzeichnet), die in allen Einzelpunkten von einer Partei übernommen werden, können anhand der Kapitelüberschrift (grau unterlegt) zugeordnet werden. In diesem Fall können alle Unterpunkte gelöscht werden. Ggf. ist es sinnvoll, diese zu belassen, insbesondere falls Detailpunkte unterschiedlich zugeordnet werden können (z.b. Randomisierung Einordnung wäre bei Statistik oder DM möglich). Die Vorgaben, die in dieser Vorlage bereits enthalten sind, dienen als Orientierung, welche Aufgaben in vielen Fällen sinnvollerweise von der mit Kreuz gekennzeichneten Partei übernommen werden können. Diese Aufteilung ist im konkreten Fall im Einzelnen zu prüfen und ggf. zu korrigieren (Tätigkeiten ggf. aufteilen, ergänzen, Zuordnung ändern). Hierbei sollte insbesondere die Erfahrung der jeweiligen Partei mit der Durchführung der einzelnen Aufgabe und auch generell mit der Durchführung von klinischen Studien berücksichtigt werden, außerdem die Zuordnung der übrigen Aufgaben. Es kann sinnvoll sein, weitere beteiligte Partner in zusätzlichen Spalten abzubilden (diese können ggf. zusammenfassend dargestellt werden). Die Zuständigkeiten bzw. die Übernahme der entsprechenden Aufgaben müssen mit den genannten Parteien abgesprochen sein. Dazu müssen die Kooperationspartner in geeigneter Weise in die Planung involviert werden. Auch wenn eine Aufgabe von einer Partei verantwortlich übernommen wird, kann dies bedeuten, dass eine andere Partei Unterlagen oder Informationen beisteuern muss, damit die Aufgabe durchgeführt werden kann (so müssen die Prüfer, deren Stellvertreter, und die Mitglieder der Prüfgruppe beispielsweise ihre Lebensläufe (CVs) und weitere Unterlagen bereitstellen, wenn das ZKS Köln den Ethikantrag einer Studie vorbereitet bzw. für die Dokumentation der Qualifikation der Prüfgruppen verantwortlich ist). Beispieltexte, die Studienspezifisch anzupassen sind, sind blau gehalten, ergänzende Kommentare (in der Regel Bearbeitungshinweise für den Projektmanager des ZKS) grün. ResponsibilitySplit_V3-28.doc 2/10
3 1. Allgemein 1.1. Medizinische Studienleitung: Studienplanung, Konzeption Design und Behandlung; inhaltliche / medizinische Verantwortung und Überwachung der Studie, Betreuung der Prüfzentren für medizinische Fachfragen (Clinical Project Management) 1.2. Generelles Projektmanagement: Organisatorische Überwachung der Studie, Beratung zu Studienfragen, Betreuung der Prüfzentren für organisatorische Rückfragen, Projektsteuerung und -Controlling 1.3. Freigabe der Studie 1.4. Freigabe der Prüfzentren (Rekrutierungsbeginn) 1.5. Vorzeitige Beendigung / Aussetzung der Studie 1.6. Schließen der Prüfzentren (Sicherheitsgründe, schwerwiegende Gesetzes- / GCP-Verstöße) 1.7. ZKS-interne Koordination (Koordination der beteiligten Abteilungen, interne Meetings, interne Qualitätssicherung) 1.8. Klinik-interne Koordination (Koordination der beteiligten Abteilungen, interne Meetings, interne Qualitätssicherung) Studienvorbereitung 2. Studienplanung 2.1. GCP-Beratung, Beratung zu Sponsor-Pflichten und -Verantwortlichkeiten 2.2. Beratung zur Studienplanung, Regularien, Studiendesign, -Konzeption und -Organisation (Konzeption Monitoring incl. Risikoabschätzung, Datenmanagement, Studiendesign, Ablaufplanung etc.) 2.3. Klärung der regulatorischen Rahmenbedingungen der Studie (Relevanz von AMG, MPG, BfS, BOpSt etc.) 2.4. Rekrutierung von Prüfzentren, Planung der Patientenrekrutierung, Auswahl qualifizierter Prüfer und erforderlichen Personals, Definition der Anforderungen an Prüfer/Stellvertreter/Prüfgruppe 2.5. Medizinische Schulung ZKS-Personal (Einführung in den medizinischen Hintergrund, spezifische Aspekte der Indikation / Therapie) 3. Studiendokumente / Medical Writing 3.1. Erstellung des Prüfplans 3.2. Unterstützung bei der Erstellung oder Review des Prüfplans (Methodik) 3.3. Unterstützung bei der Erstellung oder Review des Prüfplans (Statistik) 3.4. Einbindung Gesundheitsökonomie oder weitere bei der Erstellung des Prüfplans 3.5. Erstellung der Patienteninformation / Informed Consent 3.6. Unterstützung bei der Erstellung oder Review der Patienteninformation / Informed Consent 3.7. Erstellung weiterer Dokumente (z.b. Patiententagebuch, Anzeigen, Flyer etc.) 3.8. Unterstützung bei der Erstellung oder Review weiterer Dokumente (ggf. nennen) 3.9. Übersetzung Studiendokumente (Prüfplan, Informed Consent etc.) Entwurf / Entwicklung / Layout (e)crf einschließlich (S)AE-Dokumentation Unterstützung bei der Erstellung des (e)crf (Itemliste), Review des (e)crf Organisation von Lizenzen (für Patientenfragebögen o.ä.) Organisation Druck CRF, weitere Dokumente ResponsibilitySplit_V3-28.doc 3/10
4 3.14. Versand CRF Entwicklung TMF, ISF (Registerstruktur / Inhaltsverzeichnis, ggf. kommentiert, def. relevanter Dokumente) inkl. ausgelagerter Abschnitte des TMF (TBF, TPF, etc.) (der TMF und der ISF sollten durch den Projektmanager entwickelt/vorbereitet werden, der das volle PM durchführt, ggf. also durch die Klinik) Pflege / Verwaltung Original TMF (TSF und TCF) Pflege / Verwaltung ausgelagerter Abschnitt Biometrie (TBF) / Datenmanagement / Prüfmedikation (TPF) / des Original TMF (Abschnitte ggf. ergänzen und auf mehrere Zeilen verteilen, ggf. nur Ergänzung im Text, das Pflege durch Apotheke etc. erfolgt) Pflege / Verwaltung Qualifikationsunterlagen der Prüfgruppe im Original TMF / ISF Vorbereitung ISF (inkl. Zusammenstellung aller notwendigen Unterlagen), Versand ISF Pflege / Verwaltung ISF 4. Prozesse 4.1. Prozessplanung und Erstellung Manual Monitoring 4.2. Prozessplanung und Erstellung Manual Datenmanagement, Definition automatisierte und manuelle Plausibilitätsprüfungen 4.3. Prozessplanung und Erstellung Manual Zentrale Qualitätskontrolle (bei zentraler Qualitätskontrolle) 4.4. Prozessplanung und Erstellung Manual Safety- Management (SAE, SUSAR, DSUR) 4.5. Prozessplanung und Erstellung Manual, ggf. Schulung Randomisierung 4.6. Prozessplanung und ggf. Erstellung Manual DMSC (für Safety-Überwachung und ggf. Überwachung der Datenqualität und ggf. Bewertung von Zwischenauswertungen etc.; incl. Absprachen hinsichtl. zus. Exporte, Datencleaning / Monitoringrelevanz, relevante Daten (z.b. nur SAEs) etc.) 4.7. Prozessplanung und Erstellung Manual Einteilung Studienpopulationen für ITT:PP (Blind Review Board, Definition und Dokumentation major / minor protocol violations, Fehleinschlüsse etc.) 4.8. Prozessplanung und Organisation Zwischen- und Endauswertung (Datenmanagement, SAE-Management, Monitoring, Statistik etc.) 4.9. Prozessplanung und Organisation, ggf. Erstellung Manual Studienmedikation / Apotheke / Lohnhersteller, (Verblindung, Handhabung, Ausgabe / Dokumentation, Lagerung, Vernichtung der Studienmedikation; einschl. Schnittstellen zur Randomisierung) Prozessplanung und Erstellung Manual Labor Prozessplanung und Erstellung Manual - ggf. weitere Prozessplanung und Erstellung klin. Manuals (Diagnostik (z.b. Radiologie), Behandlung und ggf. weitere); klinisches Input für Prozesse Datenmanagement (Plausibilitätsprüfungen), Monitoring (SDV-Eckdaten), SAE- Management und ggf. weitere Unterstützung bei der Erstellung von Manuals, Review von Manuals (Manuals auflisten, ggf in mehreren Zeilen) 5. Administration 5.1. Abschluss Patientenversicherung und ggf. Wege- Unfallversicherung Erstellung und Einreichung Ethikantrag und Behördenanträge 5.2. (EUDRA-CT, BOB, BfS, ggf. weitere) (incl. Amend- ments) ResponsibilitySplit_V3-28.doc 4/10
5 5.3. Unterstützung bei der Erstellung oder Review Ethikantrag und Behördenanträge (EUDRA-CT, BOB, BfS, ggf. weitere) 5.4. Durchführung Anzeige lokale Behörden 5.5. Geldgeber: Verhandlungen, Vertrag oder Antragstellung 5.6. Unterstützung bei Geldgeber-Verhandlungen, -Antrag, - Vertrag 5.7. Antrag auf Übernahme der Sponsorschaft durch die Uni Köln, Vertragsmanagement Sponsorvertrag, Einreichung aller Amendments beim Sponsor Uni Köln Vertragsmanagement - Prüfzentrums-Verträge, - interne Kooperationsvereinbarung(en) / Kooperationsvertrag, ggf. weitere Parteien: Kooperationspartner, Gremien, Auftragnehmer (z.b. Lohnhersteller, Labor, Apotheke, DMSC, ggf. externe Monitore, ggf. weitere) 5.9. Unterstützung bei Vertragsmanagement (Verträge nennen) Finanzverwaltung / Rechnungswesen: Prozessplanung / Organisation / Überwachung (Zeitpunkte / Kriterien / Milestones für Prüfer-Honorar, ggf. DMSC, weitere) Abrechnung Behörden-/Ethikgebühren, Prüfzentren- Fallpauschalen etc. (ggf. spezifizieren; klären, wo die Mittel verwaltet werden (ZKS-Konto, Klinik-Konto oder Zugriffsberechtigung ZKS auf Klinik-Konto)) Registrierung der Studie bei ClinicalTrials / CurrentControlledTrials oder anderem adäquaten Register einschließlich Pflege (bei klinischen Prüfungen mit Arzneimitteln, die mit Erwachsenen in den Phasen II bis IV und mit Kindern und Jugendlichen der Phasen I bis IV durchgeführt werden, optional, da die Studie bereits über EudraCT (EU-CTR: öffentlich zugänglich ist) Eingabe und Pflege der Studiendaten im SMS 6. Studienmedikation / Medizinprodukt (ggf. auf Angebot der Apotheke bzw. des (Lohn)herstellers verweisen, ggf. anpassen z.b. für Medizinprodukt) 6.1. Erstellung Investigators Brochure / Bereitstellung Fachinformation / Erstellung Handbuch des klinischen Prüfers 6.2. Prüfung der Aktualität der Investigators Brochure / Fachinformation / Handbuch des klinischen Prüfers, Bereitstellung aktueller Investigators Brochure / Fachinformation / Handbuch des klinischen Prüfers an die Prüfer Organisation Herstellung, Packaging & Labeling, ggf. weitere (Stabilitätsprüfungen, Umlabelling, Reserven für 6.3. Multicenterstudien, lange Studiendauern / Austausch / Rücknahme abgelaufener Medikation / Medizinprodukt etc.); ggf. in mehreren Zeilen aufführen 6.4. Organisation Versand und Tracking Studienmedikation / Medizinprodukt (Dokumentation von Lieferung und Empfang, Prüfen des Bestands in den Zentren und Nach- Versand regelmäßig oder bei Bedarf, Rücknahme / Austausch abgelaufener Med. etc.) 6.5. Organisation Drug Accountability (Dokumentation der Ausgabe / Rücknahme der Studienmedikation / des Medizinprodukts an den Patienten / Probanden) 6.6. Organisation Rücknahme / Vernichtung Rest- Studienmedikation / -Medizinprodukt nach Ende der Studie 7. Labor 7.1. Betreuung Prüfzentren, ggf. Laborpersonal ResponsibilitySplit_V3-28.doc 5/10
6 7.2. Organisation / Durchführung Laboranalysen 7.3. Organisation Versand, Tracking Probennahme- / Versandmaterial 7.4. Organisation Versand, Tracking Laborproben Studiendurchführung 8. Laufendes Projektmanagement, Regulatorisches, Allgemeines 8.1. Zwischenberichte / Reports / Stellungnahmen an den Geldgeber 8.2. Unterstützung bei der Erstellung oder Review Zwischenberichte / Reports / Stellungnahmen an den Geldgeber 8.3. Erstellung Meldungen zu Unterbrechung / Abbruch an Prüfzentren, zuständige EK, zuständige Behörden innerhalb von 15 Tagen 8.4. Unterstützung bei der Erstellung oder Review Meldungen zu Unterbrechung / Abbruch an Prüfzentren, EK, Behörden 8.5. Nachmeldung von Prüfern/Stellvertretern (Anzahl festlegen und entspr. kalkulieren) Organisation Meetings (Vorbereitung / Durchführung / Abrechnungen / Protokolle) - Prüfarzttreffen Leitungsgruppentreffen (Steering Committee) - DMSC / Safety-Meetings - Blind Review Board-Meetings - weitere Meetings (nennen) 8.7. Prüfung und Bewertung Monitoring-Berichte auf Handlungsbedarf, Lösungsvorschläge, ggf. Intervention im Zentrum bzw. Eskalation an LKP oder Sponsor, Absprache for-cause-monitoring 8.8. Prüfung und Bewertung Reports zur Zentralen Qualitätskontrolle (Reports zentraler Qualitätsparameter, Ergänzung des Vor-Ort-Monitorings), ggf. Lösungsvorschläge zu spezifischen Problemen, ggf. Intervention im Zentrum bzw. Eskalation an LKP oder Sponsor 8.9. Erstellung regelmäßiger Newsletter o.ä. (Umfang und Frequenz definieren) Erstellung von Veröffentlichungen (z.b. Veröffentlichung des Prüfplans in BMC, siehe Website Management (ggf. Form / Umfang ausführen, z.b. Einpflegen von Prüfplan und Protokollen auf der Studienwebsite) Amendments (Anzahl festlegen und entspr. kalkulieren) Unterstützung bei der Erstellung / Review von Amendments 9. Studienassistenz 9.1. Studienassistenz 10. SAE-Management / Safety AMG Festlegungen zum SAE-Management (SAE-Formular, Data Lock Point); ggf. Absprache mit dem Hersteller der Studienmedikation (Pharmafirma) Schulung der Prüfzentren zum SAE Management (Notwendigkeit mit SAE-Management-Abteilung klären (bei MPG oft notwendig); telefonisch, per Internet oder vor Ort; Ort in den Annahmen zum Angebot angeben, ggf. Reisekosten / -zeiten kalkulieren ) SAE-Meldung (Initial und Follow-Up: Dokumentation und direkte Meldung an SAE-Management) SAE-Bearbeitung (Überprüfung, Queries, Nachverfolgung) SAE Zweit-Bewertung, Narratives für SUSARs ResponsibilitySplit_V3-28.doc 6/10
7 10.6. Vorbereitung SAE-Datenbank; Erfassung der SAEs ; MedDRA-Kodierung der SAEs Datenabgleich mit Studiendaten, SAE-Reconciliation (für DMSC-Meetings, DSUR oder ggf. weitere) (geplante Anzahl der Zeitpunkte in den Annahmen zum Angebot angeben und entsprechend kalkulieren) SAE Reporting an DMSC, Pharmafirma, ggf. weitere SUSAR Reporting an Behörden, Ethikkommissionen, LKP (innerhalb von 7 bzw. 15 Tagen), DMSC, Pharmafirma SUSAR Reporting an Prüfzentren (innerhalb von 7 bzw. 15 Tagen), inkl. SUSARs aus anderen Studien desselben Sponsors mit demselben Medikament/Wirkstoff (Medikament oder Wirkstoff, je nachdem was im Prüfplan defi- niert ist) SUSAR Reporting an LKPs von Studien desselben Sponsors mit demselben Medikament/Wirkstoff (innerhalb von 7 bzw. 15 Tagen) SAE Jahresbericht(e), (kalkulierte Anzahl angeben) Aufbereitung der Daten (Line-Listings of SAEs, Cumulative Summary Tabulation of SAEs) Erstellung der DSUR-Vorlage (inkl. Appendices 5, 6) Erstellung des DSUR Unterstützung bei der Erstellung oder Review des / der DSUR Einreichung des DSUR bei EK und Behörde Regelmäßige Prüfung Nutzen-Risiko-Verhältnis (Literaturrecherche, Fachinfo- / IB-Aktualisierung, SAE-Monitoring) Unverzügliche Information aller betroffenen Prüfer, Institutionen, der zuständigen Behörden und evtl. von beteiligten Firmen über alle Ergebnisse, die sich negativ auf die Prüfungsteilnehmer auswirken, die Durchführung der Studie beeinflussen oder die Entscheidung der Ethikkommission, die Studie fortzusetzen, ändern könnten 11. SAE-Management / Safety MPG ( 20-23a) Vorbereitung zum SAE-Management (Manual, etc.) Schulung der Prüfzentren zum SAE Management (Notwendigkeit mit SAE-Management-Abteilung klären; telefonisch, per Internet oder vor Ort; Ort in den Annahmen zum Angebot angeben, ggf. Reisekosten / -zeiten kalkulieren ) SAE-Meldung (Initial, Follow-Up- und Abschlussmeldung: Dokumentation und direkte Meldung an SAE- Management) Erfassung der SAEs (Trackingliste) SAE-Bearbeitung (Überprüfung, Queries, Nachverfolgung) SAE Sponsor-Bewertung SAE Reporting an weitere Vertragspartner (DMSC, Hersteller) Prüfung des Nutzen-Risiko-Verhältnis und Einleitung und Durchführung von eigenverantwortlichen korrektiven Maßnahmen, ggf. Erstellung einer erneuten Risikobewertung auf Anforderung des BfArM Weiterleitung von Informationen über eigenverantwortliche korrektive Maßnahmen und/oder Risikobewertungen an die BOB und die EK Unverzügliche Information aller betroffenen Prüfärzte, Institutionen, der zuständigen Behörden und evtl. von beteiligten Firmen über alle Ergebnisse, die sich negativ auf die Prüfungsteilnehmer auswirken, die Durchführung der Studie beeinflussen oder die Entscheidung der Ethikkommission, die Studie fortzusetzen, ändern könnten ResponsibilitySplit_V3-28.doc 7/10
8 12. SAE-Management / Safety MPG ( 23b) Vorbereitung zum SAE-Management (Formulare, Manual, etc.) Festlegungen der SAE-Meldeprozesse mit der zuständigen EK (SAE-Liste für die Meldung an die EK) Schulung der Prüfzentren zum SAE Management (Notwendigkeit mit SAE-Management-Abteilung klären; telefonisch, per Internet oder vor Ort; Ort in den Annahmen zum Angebot angeben, ggf. Reisekosten / -zeiten kalkulieren ) SAE-Meldung analog der Forderungen im EK-Votum (Dokumentation und direkte Meldung an SAE-Management) Vorkommnis-Meldung (Dokumentation und direkte Meldung an SAE-Management) SAE- und Vorkommnis-Erfassung und Bearbeitung (Überprüfung, Queries, Nachverfolgung, Tracking) SAE Reporting an weitere Vertragspartner (DMSC, Hersteller) Unverzügliche Information aller betroffenen Prüfärzte, Institutionen, der zuständigen Behörden, und evtl. von beteiligten Firmen über alle Ergebnisse, die sich negativ auf die Prüfungsteilnehmer auswirken, die Durchführung der Studie beeinflussen oder die Entscheidung der Ethikkommission, die Studie fortzusetzen, ändern könnten 13. Monitoring Monitortreffen, Monitorschulung Monitoring Koordination Monitoring-Dokumentation / -Berichte Auswahlbesuche / Site Selection Visit Initiierungsbesuche / Initiation Visits Regelbesuche / Regular Visits, risikoadaptiert (Source Data Verification, Prüfung ISF) Zentrales regelmäßiges Monitoring (telefonische und schriftliche Nachfragen) Abschlussbesuche / Close Out Visits (Source Data Verification, Abschlussprüfung ISF) 14. Datenmanagement Studiendatenbankdesign / -entwicklung, Dokumentation und Validierung Datenbank Administration / Änderungen und Pflege Studiendatenbank; (bei RDE / externer Dateneingabe:) User- Administration Studiendatenbank Erstellung und Pflege Dateneingabe-Anleitung; (bei RDE / externer Dateneingabe:) Datenbankschulung Review, Test und Abnahme der Datenbank Help Desk Studiendatenbank für externe Eingeber / Monitore / Datenmanager Zentraler Randomisierungsdienst (ALEA (wird vom IMSIE aufgesetzt + betreut) / Bearbeitung von Randomisierungsanfragen, Anfragen kommen über Fax/ /Telefon) Help Desk für zentralen Randomisierungsdienst (first level support i.d.r. durch ZKS) CRF Tracking (entfällt bei RDE / externer Dateneingabe) und Dateneingabe (Einfach, doppelt, second look, RDE: online-eingabe durch Prüfzentrum), Doppeldaten- Abgleich (excl. Textfelder) (entfällt bei RDE) MedDRA-Codierung für AEs, Medical History, ggf. weitere Datenprüfung (Plausibilitätsprüfungen und Queries / Discrepancies) Behebung der Datenfehler (Beantwortung von Queries / Discrepancies) ResponsibilitySplit_V3-28.doc 8/10
9 Datenexport(e) (MACRO-Format) für - Newsletter - SAE-Reconciliation DMSC-Meetings - Zwischenauswertungen - ggf. weitere (jew. Frequenzen angeben) Datenbank-Updates, Anpassungen der Datenbank (Anzahl geplant) Schließen der Datenbank, Formatieren der Datenexporte und Abschluss-Datenexport (MACRO-Format); Vorbereitung der Datenbank für die Archivierung Erstellung Übersichts-Reports (Rekrutierungsverlauf, Übersicht Serious Adverse Events, ) (Reports müssen berechnet werden (kein Standard!); Frequenz ggf. auch für Newsletter berücksichtigen) Programmierungen und Erstellung der Berichte für die zentrale Qualitätssicherung (bei zentraler Qualitätskontrolle) Mahnwesen für ausstehende CRF-Dokumentation und Queries (bei zentraler Qualitätskontrolle) 15. Statistik (ggf. an Angebot Statistik anpassen bzw. verweisen) Statistische Beratung Fallzahlkalkulation Erstellung Randomisierungsliste, Erstellung Randomisierungsumschläge, Programmierung und Administration Online-Randomisierung Erstellung Notfallumschläge (für Notfall-Entblindung) Entwicklung statistischer Analyseplan Durchführung Zwischenauswertungen Erstellung statistische Zwischenberichte Bewertung Zwischenauswertungen, Empfehlung zur Studienfortführung Durchführung Endauswertung Erstellung statistischer Kurzabschlussbericht Abschluss 16. Berichte / Medical Writing, Archivierung Erstellung Kurzabschlussbericht (Falls ein umfassender Abschlussbericht entsprechend ICH E3 erstellt werden soll: hier angeben und in der Kalkulation entsprechend berücksichtigen, entsprechend auch für Statistik 12.9) Unterstützung bei der Erstellung oder Review Abschlussbericht Behördlicher / Ethikkommissions-Studienabschluss (Abmeldung, Meldung der Ergebnisse, Einreichung Abschlussbericht gemäß AMG 42b) Erstellung Publikation Mitarbeit oder Unterstützung Publikation Zusammenführung aller Abschnitte des Original TMF, abschließende Prüfung vor Archivierung Archivierung Original TMF ResponsibilitySplit_V3-28.doc 9/10
10 Abkürzungen Kooperationspartner: ZKS: Zentrum für Klinische Studien der Universität zu Köln IMSIE: Institut für Medizinische Statistik, Informatik und Epidemiologie der Universität zu Köln Klinik: Klinik der Universität zu Köln / LKP / Prüfzentren Weitere Abkürzungen: AE: Adverse Event ALEA: Online Randomisierungstool AMG: Arzneimittelgesetz BfArM: Bundesinstitut für Arzneimittel und Medizinprodukte BfS: Bundesamt für Strahlenschutz BOB: Bundesoberbehörde BOpSt: Bundesopiumstelle CRF: Case Report Form DM: Datenmanagement DMSC: Data Montoring and Safety Committee DSUR: Development Safety Update Report ecrf: elektronisches Case Report Form EK: Ethikkommission GCP: Good Clinical Practice Guideline IB: Investigator Brochure ISF: Investigator Site File ITT: intention to treat LKP: Leiter klinische Prüfung MACRO: Datenmanagementtool für klinische Studien MedDRA: Medical Dictionary for Regulatory Activities MPG: Medizinproduktgesetz PP: per protocol RDE: Remote Data Entry SAE: Serious Adverse Event SDV: Source Data Verification SMS: Site Management System SUSAR: Suspected Unexpected Serious Adverse Reaction TBF: Trial Biometrician File TCF: Trial Center File (zentrumsspezifischer Abschnitt des TMF) TMF: Trial Master File TPF: Trial Pharmacist File TSF: Trial Sponsor File (sponsorspezifischer Abschnitt des TMF) ResponsibilitySplit_V3-28.doc 10/10
Monitoring. Lucia Kacina. CTU Bern
 Monitoring Lucia Kacina CTU Bern Themen Einverständniserklärung Protokoll & Dokumentation (e)crf-einträge: Dos & Don ts Monitoringvisiten: Teilnehmer & Ablauf Monitoring: Aufgaben des Zentrums Monitoring
Monitoring Lucia Kacina CTU Bern Themen Einverständniserklärung Protokoll & Dokumentation (e)crf-einträge: Dos & Don ts Monitoringvisiten: Teilnehmer & Ablauf Monitoring: Aufgaben des Zentrums Monitoring
CoCStom. Inhalt. 1. Monitoring und Query-Prozess. 2. SAE-Meldeweg. 3. Vorstellung des Investigator Site File (ISF) 21./22.11.
 Prospective randomized multicentre investigator initiated study: Randomised trial comparing completeness of adjuvant chemotherapy after early versus late diverting stoma closure in low anterior resection
Prospective randomized multicentre investigator initiated study: Randomised trial comparing completeness of adjuvant chemotherapy after early versus late diverting stoma closure in low anterior resection
GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG
 GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG Kursleiter: Prof. Dr. Richard F. Schlenk Datum: 2. Schulungstag: 15.10.2014 Name Vorname Anleitung Tragen
GCP-Schulung für Prüfer/Stellvertreter/Mitglieder der Prüfgruppe für klinische Prüfungen nach AMG Kursleiter: Prof. Dr. Richard F. Schlenk Datum: 2. Schulungstag: 15.10.2014 Name Vorname Anleitung Tragen
Wir beraten Sie. Wir unterstützen Sie. Wir schaffen Lösungen. Wir bringen Qualität. Wir beraten Sie. Wir unterstützen Sie. Wir schaffen Lösungen
 Was bedeutet es, ein Redaktionssystem einzuführen? Vorgehensmodell für die Einführung eines Redaktionssystems Die Bedeutung Fast alle Arbeitsabläufe in der Abteilung werden sich verändern Die inhaltliche
Was bedeutet es, ein Redaktionssystem einzuführen? Vorgehensmodell für die Einführung eines Redaktionssystems Die Bedeutung Fast alle Arbeitsabläufe in der Abteilung werden sich verändern Die inhaltliche
Strukturen zur Übernahme der Sponsorfunktion- Gut schlafen trotz Sponsorverantwortung!
 Strukturen zur Übernahme der Sponsorfunktion- Gut schlafen trotz Sponsorverantwortung! Dr. Christine Georgias Qualitätssicherung für klinische Prüfungen Forschungsdekanat der Medizinischen Fakultät Sponsor
Strukturen zur Übernahme der Sponsorfunktion- Gut schlafen trotz Sponsorverantwortung! Dr. Christine Georgias Qualitätssicherung für klinische Prüfungen Forschungsdekanat der Medizinischen Fakultät Sponsor
Was ist eine gute Klinische Studie - die Sicht der Statistik. Peter Martus Institut für Biometrie und Klinische Epidemiologie
 Was ist eine gute Klinische Studie - die Sicht der Statistik Peter Martus Institut für Biometrie und Klinische Epidemiologie Historisches Beispiel James Lind (1716-1794) entwickelte 1747 als britischer
Was ist eine gute Klinische Studie - die Sicht der Statistik Peter Martus Institut für Biometrie und Klinische Epidemiologie Historisches Beispiel James Lind (1716-1794) entwickelte 1747 als britischer
ZKS Köln 06.09.2010. Adaptiertes Monitoring ADAMON: Risk analysis and risk adapted on-site monitoring in non-commercial clinical trials
 ZKS Köln Zentrale Unterstützung des Monitoring in klinischen Studien Standardisierte Prozesse zur Risiko- Identifizierung und Reduktion bei adaptierten Monitoring-Strategien Urs Harnischmacher, Claudia
ZKS Köln Zentrale Unterstützung des Monitoring in klinischen Studien Standardisierte Prozesse zur Risiko- Identifizierung und Reduktion bei adaptierten Monitoring-Strategien Urs Harnischmacher, Claudia
Das Gesamtkonzept für die Durchführung. nicht-interventioneller Studien
 Das Gesamtkonzept für die Durchführung nicht-interventioneller Studien Software und Organisation aus einer Hand - Speziell zugeschnitten auf die Anforderungen einer nicht-interventionellen Studie. StudyARCHIVE
Das Gesamtkonzept für die Durchführung nicht-interventioneller Studien Software und Organisation aus einer Hand - Speziell zugeschnitten auf die Anforderungen einer nicht-interventionellen Studie. StudyARCHIVE
Monitoring und Datenmanagement: Eine Beziehung mit Tücken und großen Chancen Ansichten eines Monitors Katharina Thorn Vorsitzende DVMD e.v.
 Monitoring und Datenmanagement: Eine Beziehung mit Tücken und großen Chancen Ansichten eines Monitors Katharina Thorn Vorsitzende DVMD e.v. DVMD-Tagung 2015 / Ulm / K. Thorn Das Datenmanagement wird pro
Monitoring und Datenmanagement: Eine Beziehung mit Tücken und großen Chancen Ansichten eines Monitors Katharina Thorn Vorsitzende DVMD e.v. DVMD-Tagung 2015 / Ulm / K. Thorn Das Datenmanagement wird pro
Fragen und Antworten
 Fragen und Antworten im Umgang mit dem elektronischen Abfallnachweisverfahren eanv in Bezug auf die ZKS-Abfall -Allgemeine Fragen- www.zks-abfall.de Stand: 19.05.2010 Einleitung Auf den folgenden Seiten
Fragen und Antworten im Umgang mit dem elektronischen Abfallnachweisverfahren eanv in Bezug auf die ZKS-Abfall -Allgemeine Fragen- www.zks-abfall.de Stand: 19.05.2010 Einleitung Auf den folgenden Seiten
Qualitätsrisikomanagement in der klinischen Forschung:
 Qualitätsrisikomanagement in der klinischen Forschung: Methoden zur Gewährleistung der Patientensicherheit und der Datenvalidität bei adaptierten Monitoring-Strategien Jochen Dreß, Urs Harnischmacher,
Qualitätsrisikomanagement in der klinischen Forschung: Methoden zur Gewährleistung der Patientensicherheit und der Datenvalidität bei adaptierten Monitoring-Strategien Jochen Dreß, Urs Harnischmacher,
QualiPRO. Internetbasierte Datenbank für studienspezifische QualifikationsPROfile von Prüfstellen und Prüfern. Schulung I - Basisanwendungen
 QualiPRO Internetbasierte Datenbank für studienspezifische QualifikationsPROfile von Prüfstellen und Prüfern 1 QualiPRO - Funktionen Vorteile I: Kostenlose Mitgliedschaft Standortunabhängig, da browserbasiert
QualiPRO Internetbasierte Datenbank für studienspezifische QualifikationsPROfile von Prüfstellen und Prüfern 1 QualiPRO - Funktionen Vorteile I: Kostenlose Mitgliedschaft Standortunabhängig, da browserbasiert
Dok.-Nr.: Seite 1 von 6
 Logo Apotheke Planung, Durchführung und Dokumentation von QM-Audits Standardarbeitsanweisung (SOP) Standort des Originals: Dok.-Nr.: Seite 1 von 6 Nummer der vorliegenden Verfaßt durch Freigabe durch Apothekenleitung
Logo Apotheke Planung, Durchführung und Dokumentation von QM-Audits Standardarbeitsanweisung (SOP) Standort des Originals: Dok.-Nr.: Seite 1 von 6 Nummer der vorliegenden Verfaßt durch Freigabe durch Apothekenleitung
Document Management. Überblick DM 1.5.300
 Document Management Überblick - 1 - OMNITRACKER Document Management im Überblick Unternehmensweite, zentrale Dokumentenverwaltung mit dem OMNITRACKER Document Management: Qualitätssicherung der Geschäftsprozesse
Document Management Überblick - 1 - OMNITRACKER Document Management im Überblick Unternehmensweite, zentrale Dokumentenverwaltung mit dem OMNITRACKER Document Management: Qualitätssicherung der Geschäftsprozesse
!"#$%&'()*& +,-&',.-)/,.012-34151"/46!1
 !"#$%&'()*& +,-&',.-)/,.012-34151"/46!1 111111111111111111111111111111111111117/8'1#9.:&1+$+;1"0),)*.01
!"#$%&'()*& +,-&',.-)/,.012-34151"/46!1 111111111111111111111111111111111111117/8'1#9.:&1+$+;1"0),)*.01
Kostenstellen verwalten. Tipps & Tricks
 Tipps & Tricks INHALT SEITE 1.1 Kostenstellen erstellen 3 13 1.3 Zugriffsberechtigungen überprüfen 30 2 1.1 Kostenstellen erstellen Mein Profil 3 1.1 Kostenstellen erstellen Kostenstelle(n) verwalten 4
Tipps & Tricks INHALT SEITE 1.1 Kostenstellen erstellen 3 13 1.3 Zugriffsberechtigungen überprüfen 30 2 1.1 Kostenstellen erstellen Mein Profil 3 1.1 Kostenstellen erstellen Kostenstelle(n) verwalten 4
MIT NEUEN FACHTHEMEN
 ZUM UMGANG MIT Version: 1.0 Datum: 15.10.2012 INHALTSVERZEICHNIS 1 EINLEITUNG... 3 1.1 Ziel und Zweck... 3 1.2 Anwendungsbereich... 3 1.3 Entwicklung und Fortführung... 3 2 DOKUMENTE... 4 2.1 Formular
ZUM UMGANG MIT Version: 1.0 Datum: 15.10.2012 INHALTSVERZEICHNIS 1 EINLEITUNG... 3 1.1 Ziel und Zweck... 3 1.2 Anwendungsbereich... 3 1.3 Entwicklung und Fortführung... 3 2 DOKUMENTE... 4 2.1 Formular
Handbuch ZfEditor Stand 24.08.2012
 Handbuch ZfEditor Stand 24.08.2012 Inhaltsverzeichnis Einführung... 1 Ansprechpartner... 1 Installation und Update... 1 Installation... 1 Update... 2 Bedienung des ZfEditors... 2 Aufruf... 2 Auswahl Gemeinde,
Handbuch ZfEditor Stand 24.08.2012 Inhaltsverzeichnis Einführung... 1 Ansprechpartner... 1 Installation und Update... 1 Installation... 1 Update... 2 Bedienung des ZfEditors... 2 Aufruf... 2 Auswahl Gemeinde,
CHECKLISTE für KRANKENANSTALTEN
 CHECKLISTE für KRANKENANSTALTEN 12 Schritte zur nutritionday Teilnahme (nd.h) 6 Monate bis 1 Woche vor nutritionday 1 2 3 4 5 6 7 8 9 10 11 12 Registrieren und Kodes bestellen Beachten Sie nationale Richtlinien
CHECKLISTE für KRANKENANSTALTEN 12 Schritte zur nutritionday Teilnahme (nd.h) 6 Monate bis 1 Woche vor nutritionday 1 2 3 4 5 6 7 8 9 10 11 12 Registrieren und Kodes bestellen Beachten Sie nationale Richtlinien
Hinweise zum elektronischen Meldeformular
 BASG / AGES Institut Überwachung Traisengasse 5, 1200 Wien, Österreich Hinweise zum elektronischen Meldeformular Das Bundesamt für Sicherheit im Gesundheitswesen (BASG) hat gemeinsam mit dem BfArM ein
BASG / AGES Institut Überwachung Traisengasse 5, 1200 Wien, Österreich Hinweise zum elektronischen Meldeformular Das Bundesamt für Sicherheit im Gesundheitswesen (BASG) hat gemeinsam mit dem BfArM ein
Kontenaktualisierung in Lexware buchhalter
 Kontenaktualisierung in Lexware buchhalter Inhalt 1. Kontenaktualisierung durchführen... 1 1.1. Willkommen... 1 1.2. Prüflauf... 1 1.3. Status... 2 1.4. Neue Konten... 3 1.5. Nicht bebuchte Konten... 4
Kontenaktualisierung in Lexware buchhalter Inhalt 1. Kontenaktualisierung durchführen... 1 1.1. Willkommen... 1 1.2. Prüflauf... 1 1.3. Status... 2 1.4. Neue Konten... 3 1.5. Nicht bebuchte Konten... 4
Anleitung zum Login. über die Mediteam- Homepage und zur Pflege von Praxisnachrichten
 Anleitung zum Login über die Mediteam- Homepage und zur Pflege von Praxisnachrichten Stand: 18.Dezember 2013 1. Was ist der Mediteam-Login? Alle Mediteam-Mitglieder können kostenfrei einen Login beantragen.
Anleitung zum Login über die Mediteam- Homepage und zur Pflege von Praxisnachrichten Stand: 18.Dezember 2013 1. Was ist der Mediteam-Login? Alle Mediteam-Mitglieder können kostenfrei einen Login beantragen.
Serviceanweisung Austausch Globalsign Ausstellerzertifikate
 Serviceanweisung Austausch Globalsign Ausstellerzertifikate Version: Stand: 1.0 03.03.2014 Leipziger Straße 110, 04425 Taucha Tel.: +49 34298 4878-10 Fax.: +49 34298 4878-11 Internet: www.procilon.de E-Mail:
Serviceanweisung Austausch Globalsign Ausstellerzertifikate Version: Stand: 1.0 03.03.2014 Leipziger Straße 110, 04425 Taucha Tel.: +49 34298 4878-10 Fax.: +49 34298 4878-11 Internet: www.procilon.de E-Mail:
Lexware eservice personal - Nutzung ab Januar 2014
 Lexware eservice personal - Nutzung ab Januar 2014 Sie möchten sich von den vielen Vorteilen überzeugen und Lexware eservice personal ab 2014 nutzen. Wie können Sie sich registrieren und welche Funktionen
Lexware eservice personal - Nutzung ab Januar 2014 Sie möchten sich von den vielen Vorteilen überzeugen und Lexware eservice personal ab 2014 nutzen. Wie können Sie sich registrieren und welche Funktionen
IT-Controlling als notwendiges Instrument für die Leitung eines Krankenhauses. Dr. Bernd Schütze, Gesellschaft für klinische Dienstleistungen
 IT-Controlling als notwendiges Instrument für die Leitung eines Krankenhauses Dr. Bernd Schütze, Gesellschaft für klinische Dienstleistungen IT-Controlling...... oder die Frage: Welche IT-Leistungen sollen
IT-Controlling als notwendiges Instrument für die Leitung eines Krankenhauses Dr. Bernd Schütze, Gesellschaft für klinische Dienstleistungen IT-Controlling...... oder die Frage: Welche IT-Leistungen sollen
E-Mail Kampagnen mit Maildog
 E-Mail Kampagnen mit Maildog Dokumentversion 2.0 1 E-Mail Marketing leicht gemacht Das Maildog Newslettersystem bietet alles um erfolgreiche Newsletterkampagnen durchzuführen. Newsletter erstellen Erstellen
E-Mail Kampagnen mit Maildog Dokumentversion 2.0 1 E-Mail Marketing leicht gemacht Das Maildog Newslettersystem bietet alles um erfolgreiche Newsletterkampagnen durchzuführen. Newsletter erstellen Erstellen
Registrierung am Elterninformationssysytem: ClaXss Infoline
 elektronisches ElternInformationsSystem (EIS) Klicken Sie auf das Logo oder geben Sie in Ihrem Browser folgende Adresse ein: https://kommunalersprien.schule-eltern.info/infoline/claxss Diese Anleitung
elektronisches ElternInformationsSystem (EIS) Klicken Sie auf das Logo oder geben Sie in Ihrem Browser folgende Adresse ein: https://kommunalersprien.schule-eltern.info/infoline/claxss Diese Anleitung
PowerPoint 2010 Mit Folienmastern arbeiten
 PP.002, Version 1.1 07.04.2015 Kurzanleitung PowerPoint 2010 Mit Folienmastern arbeiten Der Folienmaster ist die Vorlage für sämtliche Folien einer Präsentation. Er bestimmt das Design, die Farben, die
PP.002, Version 1.1 07.04.2015 Kurzanleitung PowerPoint 2010 Mit Folienmastern arbeiten Der Folienmaster ist die Vorlage für sämtliche Folien einer Präsentation. Er bestimmt das Design, die Farben, die
Evaluation eines stichprobenartigen Monitorings bei Therapieoptimierungsstudien Ulrike Zettelmeyer
 internet: www.lymphome.de email: lymphome@medizin.uni-koeln.de Evaluation eines stichprobenartigen Monitorings bei Therapieoptimierungsstudien Ulrike Zettelmeyer Gliederung Deutsche Hodgkin Studiengruppe
internet: www.lymphome.de email: lymphome@medizin.uni-koeln.de Evaluation eines stichprobenartigen Monitorings bei Therapieoptimierungsstudien Ulrike Zettelmeyer Gliederung Deutsche Hodgkin Studiengruppe
Hinweise zum elektronischen Meldeformular
 Paul-Ehrlich-Institut Postfach 63207 Langen Jochen Halbauer Referat Pharmakovigilanz 2 Tel. +49 (0) 6103 77 3114 Fax +49 (0) 6103 77 1268 E-Mail pharmakovigilanz2@pei.de 22.06.2015 Hinweise zum elektronischen
Paul-Ehrlich-Institut Postfach 63207 Langen Jochen Halbauer Referat Pharmakovigilanz 2 Tel. +49 (0) 6103 77 3114 Fax +49 (0) 6103 77 1268 E-Mail pharmakovigilanz2@pei.de 22.06.2015 Hinweise zum elektronischen
Vorlagen im Online Banking. Anlegen von Vorlagen
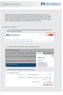 Vorlagen im Online Banking Beiträge werden üblicherweise regelmäßig wiederkehrend eingezogen. Daher ist es sinnvoll, die Lastschriften mit den Bankdaten der Mitglieder als sogenannte Vorlagen anzulegen.
Vorlagen im Online Banking Beiträge werden üblicherweise regelmäßig wiederkehrend eingezogen. Daher ist es sinnvoll, die Lastschriften mit den Bankdaten der Mitglieder als sogenannte Vorlagen anzulegen.
Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Wiederholungsverordnung
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Stand der Revision: 13.11.2013
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Information und Beratung des Patienten bei der Abgabe von Arzneimitteln Erst- und Stand der Revision: 13.11.2013
KOOPERATIVES E-CRM ZERMATT.
 KOOPERATIVES E-CRM ZERMATT. AUSGANGSLAGE. E-Mail-Marketing (bzw. Newsletter-Marketing) ist aufgrund der hohen Reichweite und Akzeptanz bei den Kunden sowie der geringen Kosten ein sehr nützliches Marketinginstrument
KOOPERATIVES E-CRM ZERMATT. AUSGANGSLAGE. E-Mail-Marketing (bzw. Newsletter-Marketing) ist aufgrund der hohen Reichweite und Akzeptanz bei den Kunden sowie der geringen Kosten ein sehr nützliches Marketinginstrument
BASISWISSEN PHARMAKOVIGILANZ I - VII
 BASISWISSEN PHARMAKOVIGILANZ I - VII 24. Februar 17. März 14. April 5. Mai 2. Juni 23. Juni 2015 Gesetzliche und regulatorische Grundlagen ( Wo steht das? ) Veränderungen und Konsequenzen ( Vom Stufenplanbeauftragten
BASISWISSEN PHARMAKOVIGILANZ I - VII 24. Februar 17. März 14. April 5. Mai 2. Juni 23. Juni 2015 Gesetzliche und regulatorische Grundlagen ( Wo steht das? ) Veränderungen und Konsequenzen ( Vom Stufenplanbeauftragten
Techniken des klinischen Monitorings souverän beherrschen lernen
 Seminar-Workshop Intensivkurs Monitoring Techniken des klinischen Monitorings souverän beherrschen lernen in Kooperation mit Dienstag + Mittwoch, 27. + 28. November 2012 Ihre Referenten Dipl.-Biol. Robert
Seminar-Workshop Intensivkurs Monitoring Techniken des klinischen Monitorings souverän beherrschen lernen in Kooperation mit Dienstag + Mittwoch, 27. + 28. November 2012 Ihre Referenten Dipl.-Biol. Robert
Kurzanleitung Kredit über Santander Bank
 HANDBUCH Kurzanleitung Kredit über Santander Bank Anleitung für Tech Data eshop Partner CGX AG Weinbergstr. 48d CH-8623 Wetzikon Inhaltsverzeichnis 1 Allgemeines... 3 1.1 Was wird der Bank vom Shop übergeben?...3
HANDBUCH Kurzanleitung Kredit über Santander Bank Anleitung für Tech Data eshop Partner CGX AG Weinbergstr. 48d CH-8623 Wetzikon Inhaltsverzeichnis 1 Allgemeines... 3 1.1 Was wird der Bank vom Shop übergeben?...3
AZK 1- Freistil. Der Dialog "Arbeitszeitkonten" Grundsätzliches zum Dialog "Arbeitszeitkonten"
 AZK 1- Freistil Nur bei Bedarf werden dafür gekennzeichnete Lohnbestandteile (Stundenzahl und Stundensatz) zwischen dem aktuellen Bruttolohnjournal und dem AZK ausgetauscht. Das Ansparen und das Auszahlen
AZK 1- Freistil Nur bei Bedarf werden dafür gekennzeichnete Lohnbestandteile (Stundenzahl und Stundensatz) zwischen dem aktuellen Bruttolohnjournal und dem AZK ausgetauscht. Das Ansparen und das Auszahlen
IMPLEMENTIERUNG VON GOOD PRACTICE ZUR REDUZIERUNG VON MEDIKATIONSFEHLERN IN SPITÄLERN
 IMPLEMENTIERUNG VON GOOD PRACTICE ZUR REDUZIERUNG VON MEDIKATIONSFEHLERN IN SPITÄLERN Zusammenfassende Beschreibung des Good practice -Beispieles Check der Medikation bei Aufnahme und Entlassung Im gegenständlichen
IMPLEMENTIERUNG VON GOOD PRACTICE ZUR REDUZIERUNG VON MEDIKATIONSFEHLERN IN SPITÄLERN Zusammenfassende Beschreibung des Good practice -Beispieles Check der Medikation bei Aufnahme und Entlassung Im gegenständlichen
Dokumentation von Patientendaten in klinischen Studien
 Dokumentation von Patientendaten in klinischen Studien ZKS Kolloquium, 16. November 2010 Dorothee Arenz Stellvertretende Leiterin des Medizinischen Bereichs BMBF 01KN0706 Vorlage für eine SOP Standard
Dokumentation von Patientendaten in klinischen Studien ZKS Kolloquium, 16. November 2010 Dorothee Arenz Stellvertretende Leiterin des Medizinischen Bereichs BMBF 01KN0706 Vorlage für eine SOP Standard
Microsoft Access 2013 Navigationsformular (Musterlösung)
 Hochschulrechenzentrum Justus-Liebig-Universität Gießen Microsoft Access 2013 Navigationsformular (Musterlösung) Musterlösung zum Navigationsformular (Access 2013) Seite 1 von 5 Inhaltsverzeichnis Vorbemerkung...
Hochschulrechenzentrum Justus-Liebig-Universität Gießen Microsoft Access 2013 Navigationsformular (Musterlösung) Musterlösung zum Navigationsformular (Access 2013) Seite 1 von 5 Inhaltsverzeichnis Vorbemerkung...
Anleitung zur Bearbeitung von Prüferkommentaren in der Nachreichung
 Anleitung zur Bearbeitung von Prüferkommentaren in der Nachreichung Inhalt 1. Schritt Prüferkommentare... 1 2. Schritt Prüferkommentar kommentieren... 4 3. Schritt Nachweisdokumente hochladen... 6 4. Schritt
Anleitung zur Bearbeitung von Prüferkommentaren in der Nachreichung Inhalt 1. Schritt Prüferkommentare... 1 2. Schritt Prüferkommentar kommentieren... 4 3. Schritt Nachweisdokumente hochladen... 6 4. Schritt
GSM: Airgap Update. Inhalt. Einleitung
 Copyright 2009-2015 Greenbone Networks GmbH Herkunft und aktuellste Version dieses Dokuments: www.greenbone.net/learningcenter/airgap.de.html GSM: Airgap Update Inhalt Vorbereitung des Airgap-Masters Vorbereitung
Copyright 2009-2015 Greenbone Networks GmbH Herkunft und aktuellste Version dieses Dokuments: www.greenbone.net/learningcenter/airgap.de.html GSM: Airgap Update Inhalt Vorbereitung des Airgap-Masters Vorbereitung
Dokumentinformationen
 Dokumentinformationen Art des Dokuments Autoren Organisation Status Dr. Olaf Heimbürger Bundesamt für Kartographie und Geodäsie (BKG), Betrieb GDI-DE abgestimmt Version 1.0 erstellt am 16.02.2015 zuletzt
Dokumentinformationen Art des Dokuments Autoren Organisation Status Dr. Olaf Heimbürger Bundesamt für Kartographie und Geodäsie (BKG), Betrieb GDI-DE abgestimmt Version 1.0 erstellt am 16.02.2015 zuletzt
Änderungen mit dem Humanforschungsgesetz Neue Vorlagen
 Departement Klinische Forschung Clinical Trial Unit Änderungen mit dem Humanforschungsgesetz Neue Vorlagen HFG News 3 Astrid Mattes 09. Januar 2014 -Seite 5 revidiert am 24.01.2014- Werkzeug zur Risikoklassifizierung
Departement Klinische Forschung Clinical Trial Unit Änderungen mit dem Humanforschungsgesetz Neue Vorlagen HFG News 3 Astrid Mattes 09. Januar 2014 -Seite 5 revidiert am 24.01.2014- Werkzeug zur Risikoklassifizierung
Prozessbewertung und -verbesserung nach ITIL im Kontext des betrieblichen Informationsmanagements. von Stephanie Wilke am 14.08.08
 Prozessbewertung und -verbesserung nach ITIL im Kontext des betrieblichen Informationsmanagements von Stephanie Wilke am 14.08.08 Überblick Einleitung Was ist ITIL? Gegenüberstellung der Prozesse Neuer
Prozessbewertung und -verbesserung nach ITIL im Kontext des betrieblichen Informationsmanagements von Stephanie Wilke am 14.08.08 Überblick Einleitung Was ist ITIL? Gegenüberstellung der Prozesse Neuer
Alle alltäglichen Aufgaben können auch über das Frontend durchgeführt werden, das in den anderen Anleitungen erläutert wird.
 Der Admin-Bereich im Backend Achtung: Diese Anleitung gibt nur einen groben Überblick über die häufigsten Aufgaben im Backend-Bereich. Sollten Sie sich nicht sicher sein, was genau Sie gerade tun, dann
Der Admin-Bereich im Backend Achtung: Diese Anleitung gibt nur einen groben Überblick über die häufigsten Aufgaben im Backend-Bereich. Sollten Sie sich nicht sicher sein, was genau Sie gerade tun, dann
Investigator Initiated Trials
 Investigator Initiated Trials Die Universität in der Rolle des Sponsors nach AMG - Rechtliche Aspekte - Alexander May, LL.M. Seite 1 Überblick Rechtliche Rahmenbedingungen 12. AMG-Novelle Der Sponsor und
Investigator Initiated Trials Die Universität in der Rolle des Sponsors nach AMG - Rechtliche Aspekte - Alexander May, LL.M. Seite 1 Überblick Rechtliche Rahmenbedingungen 12. AMG-Novelle Der Sponsor und
Erstellung von Prozessbeschreibungen. PB 4.2-1: Erstellung von Prozessbeschreibungen
 Seite 1 von 9 PB 4.2-1: Erstellung von Prozessbeschreibungen 1 Ziel und Zweck Durch Prozessbeschreibungen werden die einzelnen Prozesse des Qualitätshandbuchs detaillierter beschrieben. Sie werden für
Seite 1 von 9 PB 4.2-1: Erstellung von Prozessbeschreibungen 1 Ziel und Zweck Durch Prozessbeschreibungen werden die einzelnen Prozesse des Qualitätshandbuchs detaillierter beschrieben. Sie werden für
Datenübernahme von HKO 5.9 zur. Advolux Kanzleisoftware
 Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
DOKUMENTATION PASY. Patientendaten verwalten
 DOKUMENTATION PASY Patientendaten verwalten PASY ist ein Programm zur einfachen und zuverlässigen Verwaltung von Patientendaten. Sämtliche elektronisch gespeicherten Dokumente sind sofort verfügbar. Neue
DOKUMENTATION PASY Patientendaten verwalten PASY ist ein Programm zur einfachen und zuverlässigen Verwaltung von Patientendaten. Sämtliche elektronisch gespeicherten Dokumente sind sofort verfügbar. Neue
Wir empfehlen Ihnen eine zeitnahe Bewerbung, da in jedem Halbjahr nur eine limitierte Anzahl an Bündnissen bewilligt werden können.
 Ich bin ein LeseHeld Bewerbungsformular zur Teilnahme am Leselernförderprojekt des Borromäusverein e.v. im Rahmen des Programms Kultur macht stark. Bündnisse für Bildung des Bundesministeriums für Bildung
Ich bin ein LeseHeld Bewerbungsformular zur Teilnahme am Leselernförderprojekt des Borromäusverein e.v. im Rahmen des Programms Kultur macht stark. Bündnisse für Bildung des Bundesministeriums für Bildung
Agile Vorgehensmodelle in der Softwareentwicklung: Scrum
 C A R L V O N O S S I E T Z K Y Agile Vorgehensmodelle in der Softwareentwicklung: Scrum Johannes Diemke Vortrag im Rahmen der Projektgruppe Oldenburger Robot Soccer Team im Wintersemester 2009/2010 Was
C A R L V O N O S S I E T Z K Y Agile Vorgehensmodelle in der Softwareentwicklung: Scrum Johannes Diemke Vortrag im Rahmen der Projektgruppe Oldenburger Robot Soccer Team im Wintersemester 2009/2010 Was
Grundlagen für die Durchführung klinischer Studien Nadine Röthling 05.11.2014, Praxistag Study Nurse
 SOPs für Prüfzentren Grundlagen für die Durchführung klinischer Studien Nadine Röthling 05.11.2014, Praxistag Study Nurse Standard Operating Procedures eilt nicht unbedingt der Ruf voraus, ein interessantes
SOPs für Prüfzentren Grundlagen für die Durchführung klinischer Studien Nadine Röthling 05.11.2014, Praxistag Study Nurse Standard Operating Procedures eilt nicht unbedingt der Ruf voraus, ein interessantes
GE Capital Equipment Financing. GE Capital Leasing-Tool Schulungsunterlagen
 GE Capital Equipment Financing GE Capital Leasing-Tool Schulungsunterlagen Sie befinden sich im ALSO Online-Shop (2 Objekte liegen in Ihrem Merkzettel) Wechsel vom ALSO Online-Shop zum GE Capital Leasingantrag:
GE Capital Equipment Financing GE Capital Leasing-Tool Schulungsunterlagen Sie befinden sich im ALSO Online-Shop (2 Objekte liegen in Ihrem Merkzettel) Wechsel vom ALSO Online-Shop zum GE Capital Leasingantrag:
Anleitung für die Lohnmeldung via ELM-Standard mittels PartnerWeb
 Ausgleichskasse Gewerbe St. Gallen Lindenstrasse 137 Postfach 245 9016 St. Gallen Telefon 071 282 29 29 Telefax 071 282 29 30 info@ahv-gewerbe.ch www.ahv-gewerbe.ch Anleitung für die Lohnmeldung via ELM-Standard
Ausgleichskasse Gewerbe St. Gallen Lindenstrasse 137 Postfach 245 9016 St. Gallen Telefon 071 282 29 29 Telefax 071 282 29 30 info@ahv-gewerbe.ch www.ahv-gewerbe.ch Anleitung für die Lohnmeldung via ELM-Standard
Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt?
 DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
Übungsbeispiele für die mündliche Prüfung
 Übungsbeispiele für die mündliche Prüfung Nr. Frage: 71-02m Welche Verantwortung und Befugnis hat der Beauftragte der Leitung? 5.5.2 Leitungsmitglied; sicherstellen, dass die für das Qualitätsmanagementsystem
Übungsbeispiele für die mündliche Prüfung Nr. Frage: 71-02m Welche Verantwortung und Befugnis hat der Beauftragte der Leitung? 5.5.2 Leitungsmitglied; sicherstellen, dass die für das Qualitätsmanagementsystem
Handbuch ECDL 2003 Basic Modul 5: Datenbank Grundlagen von relationalen Datenbanken
 Handbuch ECDL 2003 Basic Modul 5: Datenbank Grundlagen von relationalen Datenbanken Dateiname: ecdl5_01_00_documentation_standard.doc Speicherdatum: 14.02.2005 ECDL 2003 Basic Modul 5 Datenbank - Grundlagen
Handbuch ECDL 2003 Basic Modul 5: Datenbank Grundlagen von relationalen Datenbanken Dateiname: ecdl5_01_00_documentation_standard.doc Speicherdatum: 14.02.2005 ECDL 2003 Basic Modul 5 Datenbank - Grundlagen
Medizintechnik und Informationstechnologie im Krankenhaus. Dr. Andreas Zimolong
 Medizintechnik und Informationstechnologie im Krankenhaus Dr. Andreas Zimolong DIN EN 80001-1:2011 Anwendung des Risikomanagements für IT-Netzwerke, die Medizinprodukte beinhalten Teil 1: Aufgaben, Verantwortlichkeiten
Medizintechnik und Informationstechnologie im Krankenhaus Dr. Andreas Zimolong DIN EN 80001-1:2011 Anwendung des Risikomanagements für IT-Netzwerke, die Medizinprodukte beinhalten Teil 1: Aufgaben, Verantwortlichkeiten
Eigenen WSUS Server mit dem UNI WSUS Server Synchronisieren
 Verwaltungsdirektion Informatikdienste Eigenen WSUS Server mit dem UNI WSUS Server Synchronisieren Inhaltsverzeichnis Einleitung... 3 Installation WSUS Server... 4 Dokumente... 4 Step by Step Installation...
Verwaltungsdirektion Informatikdienste Eigenen WSUS Server mit dem UNI WSUS Server Synchronisieren Inhaltsverzeichnis Einleitung... 3 Installation WSUS Server... 4 Dokumente... 4 Step by Step Installation...
Anleitung für den Euroweb-Newsletter
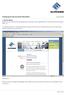 1. Die Anmeldung Begeben Sie sich auf der Euroweb Homepage (www.euroweb.de) in den Support-Bereich und wählen dort den Punkt Newsletter aus. Im Folgenden öffnet sich in dem Browserfenster die Seite, auf
1. Die Anmeldung Begeben Sie sich auf der Euroweb Homepage (www.euroweb.de) in den Support-Bereich und wählen dort den Punkt Newsletter aus. Im Folgenden öffnet sich in dem Browserfenster die Seite, auf
Anwenderdokumentation Prüfung nach dem Heilmittelkatalog
 Ausgabe August 2008 Anwenderdokumentation Prüfung nach dem Heilmittelkatalog 1 Einleitung... 2 2 Stammdateneinstellungen... 3 2.1 Zuordnung der Heilmittel... 3 3 Prüfung einer Verordnung... 7 3.1 Vorgehensweise
Ausgabe August 2008 Anwenderdokumentation Prüfung nach dem Heilmittelkatalog 1 Einleitung... 2 2 Stammdateneinstellungen... 3 2.1 Zuordnung der Heilmittel... 3 3 Prüfung einer Verordnung... 7 3.1 Vorgehensweise
Anleitung E-Mail - Archivierung
 Anleitung E-Mail - Archivierung Aufgrund unserer langjährigen Erfahrung, wissen wir um viele Kundenprobleme in der Bedienung von IKT-Produkten. Um solche Probleme bei der Nutzung der Net4You Produkte zu
Anleitung E-Mail - Archivierung Aufgrund unserer langjährigen Erfahrung, wissen wir um viele Kundenprobleme in der Bedienung von IKT-Produkten. Um solche Probleme bei der Nutzung der Net4You Produkte zu
Externe Archivierung von Studiendokumenten ein Überblick
 Externe Archivierung von Studiendokumenten ein Überblick Lars Pester Tutor Study Nurse ZKS Köln BMBF 01KN0706 Hintergrund Teil 1 Archivierungsmöglichkeiten am Klinikum erschöpft ZKS Köln übernimmt Verantwortung
Externe Archivierung von Studiendokumenten ein Überblick Lars Pester Tutor Study Nurse ZKS Köln BMBF 01KN0706 Hintergrund Teil 1 Archivierungsmöglichkeiten am Klinikum erschöpft ZKS Köln übernimmt Verantwortung
ABES/Objects: Dokumentation AGH mit em@w
 1 für Arbeitsgelegeneheiten Über wird ein ganzheitlicher standardisierter Prozess- und Kommunikationsablauf bezüglich 1 angeboten. Anmeldung der Teilnehmerin, des Teilnehmers Mitteilung von Datenänderungen
1 für Arbeitsgelegeneheiten Über wird ein ganzheitlicher standardisierter Prozess- und Kommunikationsablauf bezüglich 1 angeboten. Anmeldung der Teilnehmerin, des Teilnehmers Mitteilung von Datenänderungen
1 Formale Grundlagen -._,.'.,,/,.^'T.,^,'^/ '" ',,
 Vorwort 9 Zu den Verfasserinnen 11 Danksagungen 12 Einleitung 13 Abkürzungen 15 Glossar ^...... 17 ' '"' lh?--- - :;,'.' - v.$%&'';.-0 >.,;.; ; 1 Formale Grundlagen -._,.'.,,/,.^'T.,^,'^/ '" ',, 7.7 Arzneimittelgesetz
Vorwort 9 Zu den Verfasserinnen 11 Danksagungen 12 Einleitung 13 Abkürzungen 15 Glossar ^...... 17 ' '"' lh?--- - :;,'.' - v.$%&'';.-0 >.,;.; ; 1 Formale Grundlagen -._,.'.,,/,.^'T.,^,'^/ '" ',, 7.7 Arzneimittelgesetz
Seriendruck mit der Codex-Software
 Seriendruck mit der Codex-Software Seriendruck mit der Codex-Software Erstellen der Seriendruck-Datei in Windach Sie können aus der Adressverwaltung von Windach eine sogenannte Seriendruck-Datei erstellen,
Seriendruck mit der Codex-Software Seriendruck mit der Codex-Software Erstellen der Seriendruck-Datei in Windach Sie können aus der Adressverwaltung von Windach eine sogenannte Seriendruck-Datei erstellen,
Standard Inhaltsverzeichnis für Testvorschrift
 Standard Inhaltsverzeichnis für Testvorschrift Inhaltsverzeichnis 1. Zweck, Veranlassung... 1 2. Allgemeines... 1 2.1 Zweck der Testvorschrift... 1 2.2 Freigabe und Änderungen... 1 2.3 Prinzipien... 2
Standard Inhaltsverzeichnis für Testvorschrift Inhaltsverzeichnis 1. Zweck, Veranlassung... 1 2. Allgemeines... 1 2.1 Zweck der Testvorschrift... 1 2.2 Freigabe und Änderungen... 1 2.3 Prinzipien... 2
Dokumentenlenkung - Pflicht oder Kür-
 Dokumentenlenkung - Pflicht oder Kür- - QM-Sprengel Württemberg - Sunhild Klöss Stabsabteilung Projekt- und Qualitätsmanagement Klinikum Heidenheim Themenübersicht Forderungen der DIN EN ISO 9001 Was muss
Dokumentenlenkung - Pflicht oder Kür- - QM-Sprengel Württemberg - Sunhild Klöss Stabsabteilung Projekt- und Qualitätsmanagement Klinikum Heidenheim Themenübersicht Forderungen der DIN EN ISO 9001 Was muss
Projektmanagement. Einleitung. Beginn. Was ist Projektmanagement? In dieser Dokumentation erfahren Sie Folgendes:
 Projektmanagement Link http://promana.edulearning.at/projektleitung.html Einleitung Was ist Projektmanagement? In dieser Dokumentation erfahren Sie Folgendes: Definition des Begriffs Projekt" Kriterien
Projektmanagement Link http://promana.edulearning.at/projektleitung.html Einleitung Was ist Projektmanagement? In dieser Dokumentation erfahren Sie Folgendes: Definition des Begriffs Projekt" Kriterien
Seite 20-21 Wo finde ich die Landingpage Auswahl? Seite 22-24 Wie aktiviere ich eine Landingpage? Seite
 Gesamte Anleitung Dashboard Seite 2-3 Meine Kontakte Seite 4-5 Wie lege ich eine neue Gruppe an bzw. ändere den Namen? Seite 6-7 Wie lege ich einen neuen Kontakt an? Seite 8-9 Wie ordne ich Kunden einem
Gesamte Anleitung Dashboard Seite 2-3 Meine Kontakte Seite 4-5 Wie lege ich eine neue Gruppe an bzw. ändere den Namen? Seite 6-7 Wie lege ich einen neuen Kontakt an? Seite 8-9 Wie ordne ich Kunden einem
CERTQUA-Servicecenter Nahtlose IT-Anbindung per Schnittstelle
 CERTQUA-Servicecenter Nahtlose IT-Anbindung per Bequeme Maßnahmenverwaltung mit automatischem Datenaustausch Bequem Manuelle Dateneingabe entfällt Sicher Verschlüsselter Datentransfer Zeitsparend Schnelle
CERTQUA-Servicecenter Nahtlose IT-Anbindung per Bequeme Maßnahmenverwaltung mit automatischem Datenaustausch Bequem Manuelle Dateneingabe entfällt Sicher Verschlüsselter Datentransfer Zeitsparend Schnelle
Elektronische Unterstützung der Antragsstellung in Erasmus+ www.eu.daad.de/datenbanken
 Elektronische Unterstützung der Antragsstellung in Erasmus+ www.eu.daad.de/datenbanken 1 Schritte zum Mobilitätsantrag Beantragung der ECHE (Erasmus Charter for Higher Education 2014-2020) Registrierung
Elektronische Unterstützung der Antragsstellung in Erasmus+ www.eu.daad.de/datenbanken 1 Schritte zum Mobilitätsantrag Beantragung der ECHE (Erasmus Charter for Higher Education 2014-2020) Registrierung
Maintenance & Re-Zertifizierung
 Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
1. Einführung. 2. Weitere Konten anlegen
 1. Einführung In orgamax stehen Ihnen die gängigsten Konten des Kontenrahmens SKR03 und SKR04 zur Verfügung. Damit sind im Normalfall alle Konten abgedeckt, die Sie zur Verbuchung benötigen. Eine ausführliche
1. Einführung In orgamax stehen Ihnen die gängigsten Konten des Kontenrahmens SKR03 und SKR04 zur Verfügung. Damit sind im Normalfall alle Konten abgedeckt, die Sie zur Verbuchung benötigen. Eine ausführliche
Updateanleitung für SFirm 3.1
 Updateanleitung für SFirm 3.1 Vorab einige Informationen über das bevorstehende Update Bei der neuen Version 3.1 von SFirm handelt es sich um eine eigenständige Installation, beide Versionen sind komplett
Updateanleitung für SFirm 3.1 Vorab einige Informationen über das bevorstehende Update Bei der neuen Version 3.1 von SFirm handelt es sich um eine eigenständige Installation, beide Versionen sind komplett
Handbuch. NAFI Online-Spezial. Kunden- / Datenverwaltung. 1. Auflage. (Stand: 24.09.2014)
 Handbuch NAFI Online-Spezial 1. Auflage (Stand: 24.09.2014) Copyright 2016 by NAFI GmbH Unerlaubte Vervielfältigungen sind untersagt! Inhaltsangabe Einleitung... 3 Kundenauswahl... 3 Kunde hinzufügen...
Handbuch NAFI Online-Spezial 1. Auflage (Stand: 24.09.2014) Copyright 2016 by NAFI GmbH Unerlaubte Vervielfältigungen sind untersagt! Inhaltsangabe Einleitung... 3 Kundenauswahl... 3 Kunde hinzufügen...
Projektmanagement in der Spieleentwicklung
 Projektmanagement in der Spieleentwicklung Inhalt 1. Warum brauche ich ein Projekt-Management? 2. Die Charaktere des Projektmanagement - Mastermind - Producer - Projektleiter 3. Schnittstellen definieren
Projektmanagement in der Spieleentwicklung Inhalt 1. Warum brauche ich ein Projekt-Management? 2. Die Charaktere des Projektmanagement - Mastermind - Producer - Projektleiter 3. Schnittstellen definieren
Kurzanleitung. Zuordnung eines Moodle-Kurses in TUMonline
 Kurzanleitung Zuordnung eines Moodle-Kurses in TUMonline Inhalt 1 Allgemeine Informationen... 2 2 Kategorie elearning zuordnen... 2 3 Wo ist die Kategorie nach der Zuteilung zu finden?... 4 4 Wann wird
Kurzanleitung Zuordnung eines Moodle-Kurses in TUMonline Inhalt 1 Allgemeine Informationen... 2 2 Kategorie elearning zuordnen... 2 3 Wo ist die Kategorie nach der Zuteilung zu finden?... 4 4 Wann wird
Herzlich willkommen zur Einführungsveranstaltung Elektronische Pensenmeldung
 Herzlich willkommen zur Einführungsveranstaltung Elektronische Pensenmeldung #620 985 1 Themen Generelles zum Projekt Elektronische Pensenmeldung aktuelle Version Einführung Support für die Schulleiter
Herzlich willkommen zur Einführungsveranstaltung Elektronische Pensenmeldung #620 985 1 Themen Generelles zum Projekt Elektronische Pensenmeldung aktuelle Version Einführung Support für die Schulleiter
Wichtige Hinweise zu den neuen Orientierungshilfen der Architekten-/Objektplanerverträge
 Wichtige Hinweise zu den neuen Orientierungshilfen der Architekten-/Objektplanerverträge Ab der Version forma 5.5 handelt es sich bei den Orientierungshilfen der Architekten-/Objektplanerverträge nicht
Wichtige Hinweise zu den neuen Orientierungshilfen der Architekten-/Objektplanerverträge Ab der Version forma 5.5 handelt es sich bei den Orientierungshilfen der Architekten-/Objektplanerverträge nicht
Qualitätsmanagement-Handbuch. 1.7 Projektmanagement
 Seite 1 von 5 Erstellt: Geprüft: Freigegeben: Dr. Christine Reimann Datum: Datum: Datum: Inhaltsverzeichnis Nr. Element-Abschnitt Seite 1 Ziel und Zweck 2 2 Geltungsbereich / Verantwortung 2 3 Vorgehen
Seite 1 von 5 Erstellt: Geprüft: Freigegeben: Dr. Christine Reimann Datum: Datum: Datum: Inhaltsverzeichnis Nr. Element-Abschnitt Seite 1 Ziel und Zweck 2 2 Geltungsbereich / Verantwortung 2 3 Vorgehen
SAP Cloud Solutions. Key-User-Support der All for One Steeb
 SAP Cloud Solutions Key-User-Support der All for One Steeb Der stetige Wandel Wie wir aus Erfahrung wissen, sind IT-Projekte niemals fertig. Auch nach Abschluss der Einführungsprojekte mit den SAP Cloud
SAP Cloud Solutions Key-User-Support der All for One Steeb Der stetige Wandel Wie wir aus Erfahrung wissen, sind IT-Projekte niemals fertig. Auch nach Abschluss der Einführungsprojekte mit den SAP Cloud
Dokumentation für Inventur
 Dokumentation für Inventur dvc Computing, Software Service GmbH Kapitel 1 - Lagerstand merken Allgemein: Die Inventur wird im Programm AFL Lager Inventurprogramme aufgerufen. Für die Durchführung der Inventur
Dokumentation für Inventur dvc Computing, Software Service GmbH Kapitel 1 - Lagerstand merken Allgemein: Die Inventur wird im Programm AFL Lager Inventurprogramme aufgerufen. Für die Durchführung der Inventur
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
Umzug der abfallwirtschaftlichen Nummern /Kündigung
 Umzug der abfallwirtschaftlichen Nummern /Kündigung Um sich bei ebegleitschein abzumelden/ zu kündigen sind folgende Schritte notwendig: Schritt 1: Sie erteilen bifa Umweltinstitut GmbH den Auftrag, Ihre
Umzug der abfallwirtschaftlichen Nummern /Kündigung Um sich bei ebegleitschein abzumelden/ zu kündigen sind folgende Schritte notwendig: Schritt 1: Sie erteilen bifa Umweltinstitut GmbH den Auftrag, Ihre
Anleitung öffentlicher Zugang einrichten
 TRK-DashBoard Anleitung öffentlicher Zugang einrichten Manual für Kunden VERSION DATUM AUTOR DATEINAME 1.0 8. SEPTEMBER 2011 HRR ANLEITUNG_OEFFENTLICHER_ZUGANG_DASHBOARD_V10 INHALT 1 ALLGEMEINE INFORMATIONEN...
TRK-DashBoard Anleitung öffentlicher Zugang einrichten Manual für Kunden VERSION DATUM AUTOR DATEINAME 1.0 8. SEPTEMBER 2011 HRR ANLEITUNG_OEFFENTLICHER_ZUGANG_DASHBOARD_V10 INHALT 1 ALLGEMEINE INFORMATIONEN...
Regulatorische Anforderungen an die Entwicklung von Medizinprodukten
 Regulatorische Anforderungen an die Entwicklung von Medizinprodukten Alexander Fink, Metecon GmbH Institut für Medizintechnik Reutlingen University Alteburgstraße 150 D-72762 Reutlingen Reutlingen, 04.03.2015
Regulatorische Anforderungen an die Entwicklung von Medizinprodukten Alexander Fink, Metecon GmbH Institut für Medizintechnik Reutlingen University Alteburgstraße 150 D-72762 Reutlingen Reutlingen, 04.03.2015
Version: Version 0.01.00-2014-04-22
 Version: Version 0.01.00-2014-04-22 Inhaltsverzeichnis Vorwort... iii 1. Modul "Projektverwaltung"... 1 1.1. Benutzergruppen und Rechte... 1 1.2. Projekt erstellen... 1 1.3. Projekte auflisten und bearbeiten...
Version: Version 0.01.00-2014-04-22 Inhaltsverzeichnis Vorwort... iii 1. Modul "Projektverwaltung"... 1 1.1. Benutzergruppen und Rechte... 1 1.2. Projekt erstellen... 1 1.3. Projekte auflisten und bearbeiten...
K. Hartmann-Consulting. Schulungsunterlage Outlook 2013 Kompakt Teil 1
 K. Hartmann-Consulting Schulungsunterlage Outlook 03 Kompakt Teil Inhaltsverzeichnis Outlook... 4. Das Menüband... 4. Die Oberfläche im Überblick... 4.. Ordner hinzufügen... 5.. Ordner zu den Favoriten
K. Hartmann-Consulting Schulungsunterlage Outlook 03 Kompakt Teil Inhaltsverzeichnis Outlook... 4. Das Menüband... 4. Die Oberfläche im Überblick... 4.. Ordner hinzufügen... 5.. Ordner zu den Favoriten
Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers -
 Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers - Priv.-Doz. Dr. A. Erhardt Klinik für Gastroenterologie, Hepatologie und Infektiologie Heinrich-Heine-Universität
Auswirkungen der 12. AMG- Novelle auf wissenschaftsgesteuerte Studien die Sicht eines Klinikers - Priv.-Doz. Dr. A. Erhardt Klinik für Gastroenterologie, Hepatologie und Infektiologie Heinrich-Heine-Universität
Faktura. IT.S FAIR Faktura. Handbuch. Dauner Str.12, D-41236 Mönchengladbach, Hotline: 0900/1 296 607 (1,30 /Min)
 IT.S FAIR Faktura Handbuch Dauner Str.12, D-41236 Mönchengladbach, Hotline: 0900/1 296 607 (1,30 /Min) 1. Inhalt 1. Inhalt... 2 2. Wie lege ich einen Kontakt an?... 3 3. Wie erstelle ich eine Aktion für
IT.S FAIR Faktura Handbuch Dauner Str.12, D-41236 Mönchengladbach, Hotline: 0900/1 296 607 (1,30 /Min) 1. Inhalt 1. Inhalt... 2 2. Wie lege ich einen Kontakt an?... 3 3. Wie erstelle ich eine Aktion für
HTBVIEWER INBETRIEBNAHME
 HTBVIEWER INBETRIEBNAHME Vorbereitungen und Systemvoraussetzungen... 1 Systemvoraussetzungen... 1 Betriebssystem... 1 Vorbereitungen... 1 Installation und Inbetriebnahme... 1 Installation... 1 Assistenten
HTBVIEWER INBETRIEBNAHME Vorbereitungen und Systemvoraussetzungen... 1 Systemvoraussetzungen... 1 Betriebssystem... 1 Vorbereitungen... 1 Installation und Inbetriebnahme... 1 Installation... 1 Assistenten
Programm für lebenslanges Lernen 2007 2013. Kick-off-Meeting GRUNDTVIG Lernpartnerschaften. Bonn, 08.10.2013. NA beim BIBB
 Programm für lebenslanges Lernen 2007 2013 Kick-off-Meeting GRUNDTVIG Lernpartnerschaften Bonn, 08.10.2013 Was erwartet Sie heute? 1. Vertrag und Finanzierung 2. Abrechnung und Berichte 3. Verbreitung
Programm für lebenslanges Lernen 2007 2013 Kick-off-Meeting GRUNDTVIG Lernpartnerschaften Bonn, 08.10.2013 Was erwartet Sie heute? 1. Vertrag und Finanzierung 2. Abrechnung und Berichte 3. Verbreitung
Quickstep Server Update
 Quickstep Server Update Übersicht Was wird aktualisiert Update einspielen intersales stellt das Quickstep Entwicklungs- und Ablaufsystem auf eine aktuelle Version um. Hierfür ist es erforderlich, Ihre
Quickstep Server Update Übersicht Was wird aktualisiert Update einspielen intersales stellt das Quickstep Entwicklungs- und Ablaufsystem auf eine aktuelle Version um. Hierfür ist es erforderlich, Ihre
4.1 Wie bediene ich das Webportal?
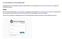 4.1 Wie bediene ich das Webportal? Die Bedienung ist durch ein Redaktionssystem sehr einfach möglich. Das Tutorial zeigt Ihnen wie Sie SMS-News und Top-News erstellen und veröffentlichen können. Schritt
4.1 Wie bediene ich das Webportal? Die Bedienung ist durch ein Redaktionssystem sehr einfach möglich. Das Tutorial zeigt Ihnen wie Sie SMS-News und Top-News erstellen und veröffentlichen können. Schritt
Informationssicherheit als Outsourcing Kandidat
 Informationssicherheit als Outsourcing Kandidat aus Kundenprojekten Frankfurt 16.06.2015 Thomas Freund Senior Security Consultant / ISO 27001 Lead Auditor Agenda Informationssicherheit Outsourcing Kandidat
Informationssicherheit als Outsourcing Kandidat aus Kundenprojekten Frankfurt 16.06.2015 Thomas Freund Senior Security Consultant / ISO 27001 Lead Auditor Agenda Informationssicherheit Outsourcing Kandidat
Web-Kürzel. Krishna Tateneni Yves Arrouye Deutsche Übersetzung: Stefan Winter
 Krishna Tateneni Yves Arrouye Deutsche Übersetzung: Stefan Winter 2 Inhaltsverzeichnis 1 Web-Kürzel 4 1.1 Einführung.......................................... 4 1.2 Web-Kürzel.........................................
Krishna Tateneni Yves Arrouye Deutsche Übersetzung: Stefan Winter 2 Inhaltsverzeichnis 1 Web-Kürzel 4 1.1 Einführung.......................................... 4 1.2 Web-Kürzel.........................................
Lexware professional und premium setzen bis einschließlich Version 2012 den Sybase SQL-Datenbankserver
 Eine Firewall für Lexware professional oder premium konfigurieren Inhaltsverzeichnis: 1. Allgemein... 1 2. Einstellungen... 1 3. Die Firewall von Windows 7 und Windows 2008 Server... 2 4. Die Firewall
Eine Firewall für Lexware professional oder premium konfigurieren Inhaltsverzeichnis: 1. Allgemein... 1 2. Einstellungen... 1 3. Die Firewall von Windows 7 und Windows 2008 Server... 2 4. Die Firewall
