ATOMPHYSIK. Gábor Talián Univ. Pécs, Institut für Biophysik September 2016
|
|
|
- Leon Meissner
- vor 6 Jahren
- Abrufe
Transkript
1 ATOMPHYSIK Gábor Talián Univ. Pécs, Institut für Biophysik September 2016
2 PRÜFUNGSTHEMA Die Temperaturstrahlung. Das plancksche Wirkungsquantum. Derphotoelektrische Effekt. Experimentelle Beobachtungen und Erklärung des Phänomens. Die Einstein-Gleichung. Lehrbuch: S.
3 Ende XIX-en Jahrhunderts Aufbau von Physik grundsätzlich beendet. Erkannte Zusammenhänge und Konstanten müssen nur genauer gemacht werden: Im XX-en Jahrhundert wird es die Physik der fünften Stelle nach dem Komma sein.
4 Das klassische physikalische Modell Physik beruht sich auf den Gesetzen der herkömmlichen Mechanik, den Maxwell-Gleichungen in Elektromagnetischen Erscheinungen und der statistischen Verteilung von Energie in thermodynamischen Systemen. Die Bewegungsparameter und die Position der Körper von den größten (wie Sternen und Planeten) bis ab den kleinsten (?) ist theoretisch beliebig genau in jedem Moment zu berechnen. Die Eigenschaften eines Systems sind in jedem zustand eindeutig bestimmt und können in den nachkommenden Zuständen ebenso erkannt und vorhergesagt werden.
5 Einige winzige, unangenehme Wolken auf dem klaren Himmel der Physik Radioaktivität Schwarzkörperstrahlung Photoelektrischer Effekt Linienspektrum von Elementen (H) Spezifische Wärme der Gase Konstanz der Lichtgeschwindichkeit Sie waren aber erwartet bald erklärt und in das klassische Modell gefügt zu werden.
6 Die Grundstruktur der Materie: Gibt es Atome? Leukipp, Demokrit atomos(ατομος) unteilbar Dalton (1803) Stoffe bestehen aus unteilbaren Atomen Atome können nicht geschöpft oder zerstört werden Die Atome eines Elementes sind gleich Die Atome verschiedener Elemente unterscheiden sich nur in Größe und Masse in Verbindungen mischen sich die Atome nach konstanten Proportionen (wie ganze Zahlen) Massenerhaltung Biliardkugel-Modell
7 Mendelejev - periodisches System J.J.Thomson (1897) Entdeckung des Elektrons, Einheit von negativer elektrischer Ladung Es entsteht aus jedem Element (Metall im Kathodenstrahlrohr) Seine Masse ist ~1800-fach weniger als die des leichtesten Elements (H) Das Atom kann nicht unteilbar bzw. der kleinste Baustein des Stoffes sein! Rosinenkuchenmodell (1904) Ludwig Boltzmann Er beging Selbstmord in 1906 (!), weil seine Kollegen ihm nicht abnehmen wollten, dass es Atome wirklich gibt. (heute: Einzelne Atome können mit Rastertunnelmikroskop untersucht - gesehen -werden.)
8 PROBLEM I. : SCHWARZKÖRPERSTRAHLUNG Problemstellung: Körper können EM Strahlung aufnehmen und abgeben. Wie kann das Ausstrahlungsspektrum des schwarzen Körpers erklärt werden?
9 Schwarzkörperstrahlung 5,67 10 Stefan-Bolzmann Konstante Wilhelm Wien, Ludwig Boltzmann, Jozef Stefan,
10 Schwarzkörperstrahlung Die große Tragödie der Wissenschaft -die Erledigung einer wunderschönen Hypothese durch eine häßliche Tatsache Thomas Huxley 6, Max Planck,
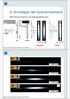
11 der photoelektrische Effekt U Albert Einstein,
12 PRÜFUNGSTHEMA Der Rutherford-Versuch. Das rutherfordsche Atommodell. Diebohrschen Postulate. Das bohrsche Atommodell. Das Teilchen-Welle Modell von de Broglie. Der Franck-Hertz Versuch. Lehrbuch: S.
13 PROBLEM II. LINIENSPEKTRUM VOM WASSERSTOFF Problemstellung: Das Absorptions- oder Emissionsspektrum des Wasserstoffs besteht aus diskreten Linien mit bestimmten Positionen bezüglich des kontinuierlichem weißem Lichtspektrum. Es bedeutet, dass der Wasserstoff kann Photonen nur mit gewissen Wellenlängen/Energien aufnehmen oder aussenden. Warum ist es so?
14 Das Spektrum vom Wasserstoff 121,57 n m 102,57 n m 656,3 n m 97,25 n m 94,97 n m 93,78 n m 93,07 n m 92,62 n m 91,1 n m 486,1 n m 434 n m 410,2 n m 397 n m 388,9 n m 365 n m 1875 n m 1282 n m 4050 n m 1094 n m 1005 n m 955 n m 820 n m Johannes Rydberg, n m 2170 n m 1460 n m infrarot sichtbar Wellenlänge (nm) ultraviolett Johann Balmer,
15 der Versuch von Rutherford Ernest Rutherford, Es war so ziemlich das unglaublichste Ereignis, das mir je in meinem Leben widerfahren ist. Es war so unglaublich, wie wenn man eine 15-Zoll-Granate auf ein Stück Seidenpapier abgefeuert hatte, und diese wäre zurückgeprallt und hätte den Schützen getroffen
16 das Planetenmodell im Wasserstoffatom das Elektron umkreist den Atomkern Zentripetalkraft = elektrische Kraft (bei anderen Elementen: Wechselwirkung zwischen den Elektronen Dreikörperproblem, usw. ) r m v F Klassische Physik kann die Stabilität des Atoms nicht erklären
17 bohrsche Postulate Postulat: ein Grundsatz bezeichnet für eine Theorie oder ein formales System, der keine neuen Terme einführt, aber nicht aus den gegebenen Definitionen abgeleitet werden kann. Ein Postulat gilt als Axiom, wenn sich aus ihm andere Theorien des Systems oder der Alltagserfahrung herleiten lassen, deren Geltung bereits bekannt ist oder beschlossen wurde. Niels Bohr,
18 1. Elektronen bewegen sich um den Atomkern auf Kreisbahnen nach den Gesetzen der klassischen Physik. Die Energie eines Elektrons im AtomkannnurdiskreteWerte(E n )annehmen. 2. Jede Energieabgabe oder -aufnahme des Elektrons kann nur durch Übergänge zwischen den stabilen Bahnen in Quanten erfolgen, die der Differenz von zwei erlaubten Bahnenenergien entsprechen. 3. Nur wenige stabile Atombahnen des Elektrons um den Atomkern existieren, wo es keine Energie verliert. Die Bahnen müssen die folgende Quantenbedingung erfüllen: 2 Die Gesamtenergie der Bahn ist die Summe der potentiellen und der kinetischen Energie. Elektronen in nicht erlaubten Positionen müssen sich sofort auf die energetisch nächst niedrige stabile Bahn begeben, und die Überschußenergie wird als EM Welle abgestrahlt.
19 Nur ganz bestimmte Drehimpulse sind erlaubt: L r m v Teilchen als Welle Louis de Broglie, Kann das man auf alle Teilchen anwenden? Ein Elektronmit 100V Beschleunigung (v = 5.9*10 6 m/s) / Ein geworfener Baseball (v = 40 m/s, m = 0.15 kg) (Atomkern: m)
20 ELEKTRON: STOFF oder WELLE? Experiment: Davisson, Germer 1926, Nobelpreis 1937
21 L r m v Kreislauf:
22 Die rydbergsche Konstante
23 Der Franck-Hertz Versuch (1913) James Franck, Gustav Hertz,
24 PRÜFUNGSTHEMA Das quantenmechanische Atommodell, Wellenfunktion. Quantenzahlen Der Stern-Gerlach und Eintein-de Haas Versuch. Die heisenbergsche Unschärferelation. Lehrbuch: 6-18 S.
25 PROBLEM III. DIE WELLENNATUR DES ELEKTRONS Problemstellung: Wie kann etwas sowohl ein Teilchen als auch eine Welle sein? Was ist die wellende physikalische Größe in dem Elektron? Erwin Schrödinger,
26 de-broglie-wellenlänge h λ = = p h 2m E
27 Quantenzahlen l ist die Nebenquantenzahl 1 2 m (m l ) ist die magnetische Quantenzahl 2 Z-komponent des Drehimpulses in einem magnetischen Feld Spin: Eigendrehimpuls s ist die Spinquantenzahl 1 / 2 2 Z-komponent des Drehimpulses in einem magnetischen Feld m s ist die magnetische Spinquantenzahl /
28 Stern -GerlachVersuch Otto Stern, Walter Gerlach,
29 Einstein -de Haas Versuch Wander Johannes de Haas, )
30
31 Elektronenbahnen
32
33
34 heisenbergsche Unschärferelation p x h/4π = ħ/2 Werner Heisenberg, Impuls Ort Plancksche Konstante h h h x p x 2 y p y 2 z p z 2 h t E 2 Zwei komplementäre Zustände (hier: Impuls und Ort) lassen sich nie mit beliebiger Genauigkeit messen
35 Zentrale Unterschiede von klassicher und quantenmechanischer Sicht Klassische Theorien (Newtonsche Mechanik, Maxwell Elektrodynamik) Deterministisch aus maximaler Beobachtung eindeutig auf Zukunft und Vergangenheit schliessen Teilchen: Orts&Impuls&Zeit Punkte Quantenmechanik Indeterministisch nur wirklichscheinlichkeitsaussagen Teilchen: Wellenfunktion Realität lokal d.h. räumlich entfernte Teilchen sind nur über Kräfte verknüpft, Lichtgeschwindigkeit Realität nichtlokal auch weitentferne Teilchen sind verschränkt (Überlichtgeschwindigkeit) Kontinuierlich: Energie und Drehimpuls kann jeden Wert annehmen Gequantelt: Energie und Drehimpuls haben nur diskrete Werte
36
37 PHYSIKALISCHE KONSTANTEN Symbol und Formel Zahlwert Größenordnung und Maßeinheit Lichtgeschwindigkeit in Vakuum Bemerkung c 0, c 2, m s 1 wirklich fundamental Gravitationskonstante G 6, m 3 kg 1 s 2 wirklich fundamental h Plancksche Konstante 6, J s wirklich 4, ev s fundamental Elementarladung e 1, C Masse des Elektrons in Ruhe wirklich fundamental? vielleicht nicht 10 9, kg Nichtwirklich fundamental; m e kann errechnet 0, MeV werden in Prinzip Masse des Protons in Ruhe m p 1, u fundamental; kann errechnet 1, kg Nichtwirklich 938,271998(38) MeV werden in Prinzip Symbol und Formel Zahlwert N A 6, (47) Größenordnung und Maßeinheit Konstante von Avogadro Faradaysche Konstante mol 1 Nichtwirklich fundamental mehr F = e N A 96485,3415(39) C mol 1 fundamental Nichtwirklich mehr Universale Gaskonstante R 8,314472(15) J mol 1 K 1 fundamental Nichtwirklich mehr Boltzmannsche Konstante k = R/N A 1, J K 1 wirklich fundamental 8, ev K 1 Magnetische Permeabilität in Vakuum µ 0 = 1/ 0 c 2 12, V s A 1 m 1 Nichtwirklich fundamental Elektrische Susceptibilität in Vakuum Bemerkung 0 = 1/µ 0 c 2 8, A s V 1 m 1 Nichtwirklich fundamental
38 DANKE FÜR IHRE AUFMERKSAMKEIT
39 Ψ= Wellenfunktion Die sich ausbreitende physikalische Grösse in Materienwellen, die alle messbaren Informationen über das Teilchen enthält Das Elektron wird durch die Wellenfunktion repräsentiert (Ort, Zeit), wobei ψ*ψ(= ψ 2 ) die Wahrscheinlichkeitsdichte für das Auffinden des Teilchens am gegebenen Ort und Zeitpunkt bedeutet. ψ 2 (Aufenthaltswahrscheinlichkeitsdichte) über den ganzen Raum summiert ist 1, weil die Wahrscheinlichkeit für das Auffinden eines existierenden Teilchens 1 sein muss. Ψ ist eine stetige Funktion. Die Wellenfunktion wird in der Schrödingergleichung zur Berechnungen von Energie oder des Wahrscheinlichsten Werts einer Variablen benutzt. Ψist für ein freies Teilchen eine Sinuswelle, mit einem exakt bestimmten Impuls und einem unbestimmten Ort (siehe später). Die Wellenfunktion beschreibt das gebundene Elektron in drei Dimensionen, somit ist sie für den Wasserstoff Kugelsymmetrisch. Mit Hilfe der Wellenfunktion spielt die Schrödingergleichung die Rolle der Newtonschen Gesetze von klassischer Mechanik in atomaren und subatomaren Systemen. Sie macht Vorhersagungen über das Verhalten eines dynamischen Systems und die Wahrscheinlichkeit von möglichen Ereignissen und Ausgängen. Kein einzelner Ausgang ist strikt festgelegt, für eine grosse Anzahl an Ereignissen jedoch sagt die Schrödingergleichung die präzise Verteilung der Ergebnisse voraus.
40 Wichtigere Quellen
41
SS 2015 Supplement to Experimental Physics 2 (LB-Technik) Prof. E. Resconi
 Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
Atommodell führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen.
 Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
10 Teilchen und Wellen. 10.1 Strahlung schwarzer Körper
 10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
10 Teilchen und Wellen Teilchen: m, V, p, r, E, lokalisierbar Wellen: l, f, p, E, unendlich ausgedehnt (harmonische Welle) Unterscheidung: Wellen interferieren 10.1 Strahlung schwarzer Körper JEDER Körper
Abb.15: Experiment zum Rutherford-Modell
 6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
Elemente der Quantenmechanik III 9.1. Schrödingergleichung mit beliebigem Potential 9.2. Harmonischer Oszillator 9.3. Drehimpulsoperator
 VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten
 Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Übungen Quantenphysik
 Ue QP 1 Übungen Quantenphysik Kernphysik Historische Entwicklung der Atommodelle Klassische Wellengleichung 5 Schrödinger Gleichung 6 Kastenpotential (Teilchen in einer Box) 8 Teilchen im Potentialtopf
Ue QP 1 Übungen Quantenphysik Kernphysik Historische Entwicklung der Atommodelle Klassische Wellengleichung 5 Schrödinger Gleichung 6 Kastenpotential (Teilchen in einer Box) 8 Teilchen im Potentialtopf
10. Das Wasserstoff-Atom Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Ein schwarzer Körper und seine Strahlung
 Quantenphysik 1. Hohlraumstrahlung und Lichtquanten 2. Max Planck Leben und Persönlichkeit 3. Das Bohrsche Atommodell 4. Niels Bohr Leben und Persönlichkeit 5. Wellenmechanik 6. Doppelspaltexperiment mit
Quantenphysik 1. Hohlraumstrahlung und Lichtquanten 2. Max Planck Leben und Persönlichkeit 3. Das Bohrsche Atommodell 4. Niels Bohr Leben und Persönlichkeit 5. Wellenmechanik 6. Doppelspaltexperiment mit
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Grundbausteine des Mikrokosmos (6) Vom Planetenmodell der Atome zum Bohrschen Atommodell
 Grundbausteine des Mikrokosmos (6) Vom Planetenmodell der Atome zum Bohrschen Atommodell 1900: Entdeckung einer neuen Naturkonstanten: Plancksches Wirkungsquantum Was sind Naturkonstanten und welche Bedeutung
Grundbausteine des Mikrokosmos (6) Vom Planetenmodell der Atome zum Bohrschen Atommodell 1900: Entdeckung einer neuen Naturkonstanten: Plancksches Wirkungsquantum Was sind Naturkonstanten und welche Bedeutung
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Atomphysik NWA Klasse 9
 Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
22. Wärmestrahlung. rmestrahlung, Quantenmechanik
 22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
Wiederholung der letzten Vorlesungsstunde: Das (wellen-) quantenchemische Atommodell Orbitalmodell Beschreibung atomarer Teilchen (Elektronen) durch Wellenfunktionen, Wellen, Wellenlänge, Frequenz, Amplitude,
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
ν und λ ausgedrückt in Energie E und Impuls p
 phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
phys4.011 Page 1 8.3 Die Schrödinger-Gleichung die grundlegende Gleichung der Quantenmechanik (in den bis jetzt diskutierten Fällen) eine Wellengleichung für Materiewellen (gilt aber auch allgemeiner)
1 Physikalische Hintergrunde: Teilchen oder Welle?
 Skript zur 1. Vorlesung Quantenmechanik, Montag den 11. April, 2011. 1 Physikalische Hintergrunde: Teilchen oder Welle? 1.1 Geschichtliches: Warum Quantenmechanik? Bis 1900: klassische Physik Newtonsche
Skript zur 1. Vorlesung Quantenmechanik, Montag den 11. April, 2011. 1 Physikalische Hintergrunde: Teilchen oder Welle? 1.1 Geschichtliches: Warum Quantenmechanik? Bis 1900: klassische Physik Newtonsche
Grundbausteine des Mikrokosmos (7) Wellen? Teilchen? Beides?
 Grundbausteine des Mikrokosmos (7) Wellen? Teilchen? Beides? Experimentelle Überprüfung der Energieniveaus im Bohr schen Atommodell Absorbierte und emittierte Photonen hν = E m E n Stationäre Elektronenbahnen
Grundbausteine des Mikrokosmos (7) Wellen? Teilchen? Beides? Experimentelle Überprüfung der Energieniveaus im Bohr schen Atommodell Absorbierte und emittierte Photonen hν = E m E n Stationäre Elektronenbahnen
Der Welle-Teilchen-Dualismus
 Quantenphysik Der Welle-Teilchen-Dualismus Welle-Teilchen-Dualismus http://bluesky.blogg.de/2005/05/03/fachbegriffe-der-modernen-physik-ix/ Welle-Teilchen-Dualismus Alles ist gleichzeitig Welle und Teilchen.
Quantenphysik Der Welle-Teilchen-Dualismus Welle-Teilchen-Dualismus http://bluesky.blogg.de/2005/05/03/fachbegriffe-der-modernen-physik-ix/ Welle-Teilchen-Dualismus Alles ist gleichzeitig Welle und Teilchen.
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
8.2 Aufbau der Atome. auch bei der Entdeckung der Kathodenstrahlen schienen die Ladungsträger aus den Atomen herauszukommen.
 Dieter Suter - 404 - Physik B3 8.2 Aufbau der Atome 8.2.1 Grundlagen Wenn man Atome als Bausteine der Materie i- dentifiziert hat stellt sich sofort die Frage, woraus denn die Atome bestehen. Dabei besteht
Dieter Suter - 404 - Physik B3 8.2 Aufbau der Atome 8.2.1 Grundlagen Wenn man Atome als Bausteine der Materie i- dentifiziert hat stellt sich sofort die Frage, woraus denn die Atome bestehen. Dabei besteht
8 Das Bohrsche Atommodell. 8. Das Bohrsche Atommodell
 1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse, Isotopie 4. Atomkern und Hülle:
1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse, Isotopie 4. Atomkern und Hülle:
10.7 Moderne Atommodelle
 10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale
 Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Einführung in die Quantenphysik
 Einführung in die Quantenphysik Klassische Optik Der lichtelektrische Effekt Effekte elektromagnetischer Strahlung Kopenhagen-Interpretation Elektronen Quantenphysik und klassische Physik Atomphysik Klassische
Einführung in die Quantenphysik Klassische Optik Der lichtelektrische Effekt Effekte elektromagnetischer Strahlung Kopenhagen-Interpretation Elektronen Quantenphysik und klassische Physik Atomphysik Klassische
Klassische Mechanik. Elektrodynamik. Thermodynamik. Der Stand der Physik am Beginn des 20. Jahrhunderts. Relativitätstheorie?
 Der Stand der Physik am Beginn des 20. Jahrhunderts Klassische Mechanik Newton-Axiome Relativitätstheorie? Maxwell-Gleichungen ok Elektrodynamik Thermodynamik Hauptsätze der Therm. Quantentheorie S.Alexandrova
Der Stand der Physik am Beginn des 20. Jahrhunderts Klassische Mechanik Newton-Axiome Relativitätstheorie? Maxwell-Gleichungen ok Elektrodynamik Thermodynamik Hauptsätze der Therm. Quantentheorie S.Alexandrova
Atome und ihre Eigenschaften
 Atome und ihre Eigenschaften Vom Atomkern zum Atom - von der Kernphysik zur Chemie Die Chemie beginnt dort, wo die Temperaturen soweit gefallen sind, daß die positiv geladenen Atomkerne freie Elektronen
Atome und ihre Eigenschaften Vom Atomkern zum Atom - von der Kernphysik zur Chemie Die Chemie beginnt dort, wo die Temperaturen soweit gefallen sind, daß die positiv geladenen Atomkerne freie Elektronen
Die Macht und Ohnmacht der Quantenwelt
 Die Macht und Ohnmacht der Quantenwelt Prof. Dr. Sebastian Eggert Tag der Physik, TU Kaiserslautern, 5. Dezember 2015 Quantenmechanik heute Quanteninformatik Ultrakalte Quantengase Supraleitung und Vielteilchenphysik
Die Macht und Ohnmacht der Quantenwelt Prof. Dr. Sebastian Eggert Tag der Physik, TU Kaiserslautern, 5. Dezember 2015 Quantenmechanik heute Quanteninformatik Ultrakalte Quantengase Supraleitung und Vielteilchenphysik
Joseph J. Thomson ( ) Nobelpreis 1906
 Joseph J. Thomson (1856 1940) Nobelpreis 1906 Atome Kathoden & Kanalstrahlen Experimenteller Befund von Wiechert, Kaufmann & Thomson 1897: Kathodenstrahlen: Elektrisch negativ geladen. Magnetisch leicht
Joseph J. Thomson (1856 1940) Nobelpreis 1906 Atome Kathoden & Kanalstrahlen Experimenteller Befund von Wiechert, Kaufmann & Thomson 1897: Kathodenstrahlen: Elektrisch negativ geladen. Magnetisch leicht
Thema heute: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Das Bohrsche Atommodell
 Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
Das Bohrsche Atommodell Auf ein Elektron, welches im elektrischen Feld eines Atomkerns kreist wirkt ein magnetisches Feld. Der Abstand zum Atomkern ist das Ergebnis, der elektrostatischen Coulomb-Anziehung
27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus
 26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
Atommodell. Atommodell nach Bohr und Sommerfeld Für sein neues Atommodell stellte Bohr folgende Postulate auf:
 Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Die Welt der Quanten Murmeln oder Wellen? Max Camenzind Senioren Uni WS2013
 Die Welt der Quanten Murmeln oder Wellen? Max Camenzind Senioren Uni Würzburg @ WS2013 Die Krise des mechanischen Weltbildes und die Gründerväter der modernen Physik. Elektromagnetische Strahlung Maxwell,
Die Welt der Quanten Murmeln oder Wellen? Max Camenzind Senioren Uni Würzburg @ WS2013 Die Krise des mechanischen Weltbildes und die Gründerväter der modernen Physik. Elektromagnetische Strahlung Maxwell,
5.3 Ausblick: Eine weitreichende Anwendung der Planckschen Strahlungsformel
 Eberhard Müller: Interdisziplinärer Zugang zu den Grundlagen der Quantentheorie: Beginn der Quantentheorie 5.3 Ausblick: Eine weitreichende Anwendung der Planckschen Strahlungsformel Bei der Entwicklung
Eberhard Müller: Interdisziplinärer Zugang zu den Grundlagen der Quantentheorie: Beginn der Quantentheorie 5.3 Ausblick: Eine weitreichende Anwendung der Planckschen Strahlungsformel Bei der Entwicklung
Entwicklung der Atommodelle
 Entwicklung der Atommodelle Entwicklung der Atommodelle Demokrit 460 v Chr. Nur scheinbar hat ein Ding eine Farbe, nur scheinbar ist es süß oder bitter; in Wirklichkeit gibt es nur Atome im leeren Raum.
Entwicklung der Atommodelle Entwicklung der Atommodelle Demokrit 460 v Chr. Nur scheinbar hat ein Ding eine Farbe, nur scheinbar ist es süß oder bitter; in Wirklichkeit gibt es nur Atome im leeren Raum.
lichen auf sehr engem Raum konzentriert ist und die positive Ladung trägt
 lichen auf sehr engem Raum konzentriert ist und die positive Ladung trägt Kanalstrahlexperimente hatten schwere, positiv geladene Teilchen beim Wasserstoff nachgewiesen Aufgrund von Streuexperimenten postulierte
lichen auf sehr engem Raum konzentriert ist und die positive Ladung trägt Kanalstrahlexperimente hatten schwere, positiv geladene Teilchen beim Wasserstoff nachgewiesen Aufgrund von Streuexperimenten postulierte
Für Geowissenschaftler. EP WS 2009/10 Dünnweber/Faessler
 Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Fazit: Wellen haben Teilchencharakter
 Die Vorgeschichte Maxwell 1865 sagt elektromagnetische Wellen vorher Hertz 1886 beobachtet verstärkten Funkenüberschlag unter Lichteinstrahlung Hallwachs 1888 studiert den photoelektrischen Effekt systematisch
Die Vorgeschichte Maxwell 1865 sagt elektromagnetische Wellen vorher Hertz 1886 beobachtet verstärkten Funkenüberschlag unter Lichteinstrahlung Hallwachs 1888 studiert den photoelektrischen Effekt systematisch
Die seltsame Welt der Quanten
 Saturday Morning Physics Die seltsame Welt der Quanten Wie spielt Gott sein Würfelspiel? 12. 11. 2005 Gernot Alber und Gerhard Birkl Institut für Angewandte Physik Technische Universität Darmstadt gernot.alber@physik.tu-darmstadt.de
Saturday Morning Physics Die seltsame Welt der Quanten Wie spielt Gott sein Würfelspiel? 12. 11. 2005 Gernot Alber und Gerhard Birkl Institut für Angewandte Physik Technische Universität Darmstadt gernot.alber@physik.tu-darmstadt.de
Quantenmechanik. Eine Kurzvorstellung für Nicht-Physiker
 Quantenmechanik Eine Kurzvorstellung für Nicht-Physiker Die Quantenvorstellung Der Ursprung: Hohlraumstrahlung Das Verhalten eines Von Interesse: idealen Absorbers Energiedichte in Abhängigkeit zur Wellenlänge
Quantenmechanik Eine Kurzvorstellung für Nicht-Physiker Die Quantenvorstellung Der Ursprung: Hohlraumstrahlung Das Verhalten eines Von Interesse: idealen Absorbers Energiedichte in Abhängigkeit zur Wellenlänge
Einleitung Das Rutherford sche Atommodell Das Bohr sche Atommodell. Atommodelle [HERR] Q34 LK Physik. 25. September 2015
![Einleitung Das Rutherford sche Atommodell Das Bohr sche Atommodell. Atommodelle [HERR] Q34 LK Physik. 25. September 2015 Einleitung Das Rutherford sche Atommodell Das Bohr sche Atommodell. Atommodelle [HERR] Q34 LK Physik. 25. September 2015](/thumbs/49/25189684.jpg) Q34 LK Physik 25. September 2015 Geschichte Antike Vorstellung von Leukipp und Demokrit (5. Jahrh. v. Chr.); Begründung des Atomismus (atomos, griech. unteilbar). Anfang des 19. Jahrh. leitet Dalton aus
Q34 LK Physik 25. September 2015 Geschichte Antike Vorstellung von Leukipp und Demokrit (5. Jahrh. v. Chr.); Begründung des Atomismus (atomos, griech. unteilbar). Anfang des 19. Jahrh. leitet Dalton aus
Inhaltsverzeichnis. Einleitung 1
 Inhaltsverzeichnis Einleitung 1 1 Licht und Materie 7 Was ist eigentlich Licht? 8 Aber was schwingt da wie? 9 Was sind Frequenz und Wellenlänge des Lichts? 11 Was ist eigentlich Materie? 12 Woraus besteht
Inhaltsverzeichnis Einleitung 1 1 Licht und Materie 7 Was ist eigentlich Licht? 8 Aber was schwingt da wie? 9 Was sind Frequenz und Wellenlänge des Lichts? 11 Was ist eigentlich Materie? 12 Woraus besteht
Atombau, Elektronenkonfiguration und das Orbitalmodell:
 Bohrsches Atommodell: Atombau, Elektronenkonfiguration und das Orbitalmodell: Nachdem Rutherford mit seinem Streuversuch bewiesen hatte, dass sich im Kern die gesamte Masse befindet und der Kern zudem
Bohrsches Atommodell: Atombau, Elektronenkonfiguration und das Orbitalmodell: Nachdem Rutherford mit seinem Streuversuch bewiesen hatte, dass sich im Kern die gesamte Masse befindet und der Kern zudem
Atome - Moleküle - Kerne
 Atome - Moleküle - Kerne Band I Atomphysik Von Univ.-Professor Dr. Gerd Otter und Akad.-Direktor Dr. Raimund Honecker III. Physikalisches Institut der Rheinisch-Westfälischen Technischen Hochschule Aachen
Atome - Moleküle - Kerne Band I Atomphysik Von Univ.-Professor Dr. Gerd Otter und Akad.-Direktor Dr. Raimund Honecker III. Physikalisches Institut der Rheinisch-Westfälischen Technischen Hochschule Aachen
Das Rutherfordsche Atommodelle
 Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
27. Wärmestrahlung. rmestrahlung, Quantenmechanik
 24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
24. Vorlesung EP 27. Wärmestrahlung rmestrahlung, Quantenmechanik V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik Photometrie Plancksches Strahlungsgesetz Welle/Teilchen Dualismus für Strahlung
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Rätsel in der Welt der Quanten. Leipziger Gespräche zur Mathematik Sächsische Akademie der Wissenschaften
 Rätsel in der Welt der Quanten Leipziger Gespräche zur Mathematik Sächsische Akademie der Wissenschaften 1. Februar 2012 Die Klassische Physik Bewegung von Objekten Lichtwellen Bewegung von Objekten Newtonsche
Rätsel in der Welt der Quanten Leipziger Gespräche zur Mathematik Sächsische Akademie der Wissenschaften 1. Februar 2012 Die Klassische Physik Bewegung von Objekten Lichtwellen Bewegung von Objekten Newtonsche
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Fachschule für f. r Technik. Dipl.FL. D.Strache FST UH
 . FST UH Ein Atommodell ist eine Vorstellung von den kleinsten Teilen der Stoffe. Lange Zeit gab es keine experimentellen Hinweise für die Existenz kleinster Teilchen, sondern lediglich die intuitive Ablehnung
. FST UH Ein Atommodell ist eine Vorstellung von den kleinsten Teilen der Stoffe. Lange Zeit gab es keine experimentellen Hinweise für die Existenz kleinster Teilchen, sondern lediglich die intuitive Ablehnung
1. Auf dem Weg zur Quantentheorie Grundlegende Experimente und Erkenntnisse
 1. Auf dem Weg zur Quantentheorie Grundlegende Experimente und Erkenntnisse 1.1. Theorie der Wärmestrahlung Plancksche Strahlenhypothese Untersuchungen der Hohlraumstrahlung vor 1900 zeigten, dass das
1. Auf dem Weg zur Quantentheorie Grundlegende Experimente und Erkenntnisse 1.1. Theorie der Wärmestrahlung Plancksche Strahlenhypothese Untersuchungen der Hohlraumstrahlung vor 1900 zeigten, dass das
Die Geschichte der Quantenmechanik
 Die Geschichte der Quantenmechanik Kurt Bräuer Institut für Theoretische Physik 5.04.006 www.kbraeuer.de 1 'Urväter' 5.04.006 www.kbraeuer.de Strahlung schwarzer Körper: Max Plank 1900 Plank'sches Strahlungsgesetz:
Die Geschichte der Quantenmechanik Kurt Bräuer Institut für Theoretische Physik 5.04.006 www.kbraeuer.de 1 'Urväter' 5.04.006 www.kbraeuer.de Strahlung schwarzer Körper: Max Plank 1900 Plank'sches Strahlungsgesetz:
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
Struktur des Atomkerns
 Struktur des Atomkerns den 6 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Struktur des Atomkerns. Die Eigenschaften des Kernkraftes. Bindungsenergie. Massendefekt. Tröpfchenmodell und Schallmodell. Magische
Struktur des Atomkerns den 6 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Struktur des Atomkerns. Die Eigenschaften des Kernkraftes. Bindungsenergie. Massendefekt. Tröpfchenmodell und Schallmodell. Magische
Aufbau von Atomen. Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem
 Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Probeklausur zu Physikalische Chemie II für Lehramt
 Department Chemie Dr. Don C. Lamb http://www.cup.uni-muenchen.de/pc/lamb Probeklausur zu Physikalische Chemie II für Lehramt Zur Bearbeitung der Klausur ist nur der freie Platz dieser vor Ihnen liegenden
Department Chemie Dr. Don C. Lamb http://www.cup.uni-muenchen.de/pc/lamb Probeklausur zu Physikalische Chemie II für Lehramt Zur Bearbeitung der Klausur ist nur der freie Platz dieser vor Ihnen liegenden
Grundbausteine des Mikrokosmos (5) Die Entdeckung des Wirkungsquantums
 Grundbausteine des Mikrokosmos (5) Die Entdeckung des Wirkungsquantums Ein weiterer Zugang zur Physik der Atome, der sich als fundamental erweisen sollte, ergab sich aus der Analyse der elektromagnetischen
Grundbausteine des Mikrokosmos (5) Die Entdeckung des Wirkungsquantums Ein weiterer Zugang zur Physik der Atome, der sich als fundamental erweisen sollte, ergab sich aus der Analyse der elektromagnetischen
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Bohrsches Atommodell / Linienspektren. Experimentalphysik für Biologen und Chemiker, O. Benson & A. Peters, Humboldt-Universität zu Berlin
 Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen Mechanik).
 phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
phys4.017 Page 1 10.4.2 Bahndrehimpuls des Elektrons: Einheit des Drehimpuls: Der Bahndrehimpuls des Elektrons ist quantisiert. Der Gesamtbahndrehimpuls ist eine Erhaltungsgrösse (genau wie in der klassischen
14 Teilchen und Wellen
 14 Teilchen und Wellen 14.1 Teilchencharakter von elektromagnetischen Wellen 1411 14.1.1 Strahlung schwarzer Körper 14.1.2 Der Photoeffekt 14.1.3 Technische Anwendungen 14.2 Wellencharakter von Teilchen
14 Teilchen und Wellen 14.1 Teilchencharakter von elektromagnetischen Wellen 1411 14.1.1 Strahlung schwarzer Körper 14.1.2 Der Photoeffekt 14.1.3 Technische Anwendungen 14.2 Wellencharakter von Teilchen
12.8 Eigenschaften von elektronischen Übergängen. Übergangsfrequenz
 phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
Strahlenschutzkurs für Mediziner
 Strahlenschutzkurs für Mediziner von Uwe G. Schröder, Beate S. Schröder 2. akt. Aufl. Thieme 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 139112 4 Zu Inhaltsverzeichnis schnell und portofrei
Strahlenschutzkurs für Mediziner von Uwe G. Schröder, Beate S. Schröder 2. akt. Aufl. Thieme 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 13 139112 4 Zu Inhaltsverzeichnis schnell und portofrei
Festkörperelektronik 2008 Übungsblatt 1
 Lichttechnisches Institut Universität Karlsruhe (TH) Prof. Dr. rer. nat. Uli Lemmer Dipl.-Phys. Alexander Colsmann Engesserstraße 13 76131 Karlsruhe Festkörperelektronik 1. Übungsblatt 17. April 2008 Dozent:
Lichttechnisches Institut Universität Karlsruhe (TH) Prof. Dr. rer. nat. Uli Lemmer Dipl.-Phys. Alexander Colsmann Engesserstraße 13 76131 Karlsruhe Festkörperelektronik 1. Übungsblatt 17. April 2008 Dozent:
4. Quantenmechanik. Offene Fragen am Ende des 19. Jahrhunderts:
 4. Quantenmechanik Offene Fragen am Ende des 19. Jahrhunderts: - Strahlungsspektrum schwarzer Körper (z.b. der Sonne) - Merkwürdigkeiten beim lichtelektrische Effekt (Photoeffekt) - Aufbau der Atome -
4. Quantenmechanik Offene Fragen am Ende des 19. Jahrhunderts: - Strahlungsspektrum schwarzer Körper (z.b. der Sonne) - Merkwürdigkeiten beim lichtelektrische Effekt (Photoeffekt) - Aufbau der Atome -
Vom Doppelspalt zum Quantencomputer
 Vom Doppelspalt zum Quantencomputer Aktuelle Physik in der Schule Herbert Rubin Aufbau der Lerneinheit Vorstellungen von Licht Huygens Newton Young 1704 1678 1804 Linienspektren Äusserer Photoeffekt Hallwachs-Effekt
Vom Doppelspalt zum Quantencomputer Aktuelle Physik in der Schule Herbert Rubin Aufbau der Lerneinheit Vorstellungen von Licht Huygens Newton Young 1704 1678 1804 Linienspektren Äusserer Photoeffekt Hallwachs-Effekt
Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4)
 Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4) Gesetzmäßigkeiten in der Anordnung der Spektrallinien eines Stoffes? Wasserstoff Johann Jacob Balmer 1825-1898 A=364.4 nm n ganzzahlig > 2 Eine
Sterne 16 Sternspektroskopie und Spektralanalyse (Teil 4) Gesetzmäßigkeiten in der Anordnung der Spektrallinien eines Stoffes? Wasserstoff Johann Jacob Balmer 1825-1898 A=364.4 nm n ganzzahlig > 2 Eine
Vorstellungen über den Bau der Materie
 Atombau Die Welt des ganz Kleinen Vorstellungen über den Bau der Materie Demokrit denkt sich das Unteilbare, das Atom Dalton entwirft ein Atommodell Rutherford formuliert das Kern-Hüllenmodell Bohr spricht
Atombau Die Welt des ganz Kleinen Vorstellungen über den Bau der Materie Demokrit denkt sich das Unteilbare, das Atom Dalton entwirft ein Atommodell Rutherford formuliert das Kern-Hüllenmodell Bohr spricht
Der Stern-Gerlach-Versuch
 Der Stern-Gerlach-Versuch Lukas Mazur Physik Fakultät Universität Bielefeld Physikalisches Proseminar, 08.05.2013 1 Einleitung 2 Wichtige Personen 3 Motivation 4 Das Stern-Gerlach-Experiment 5 Pauli-Prinzip
Der Stern-Gerlach-Versuch Lukas Mazur Physik Fakultät Universität Bielefeld Physikalisches Proseminar, 08.05.2013 1 Einleitung 2 Wichtige Personen 3 Motivation 4 Das Stern-Gerlach-Experiment 5 Pauli-Prinzip
Die Wellenfunktion ψ(r,t) ist eine komplexe skalare Größe, da keine Polarisation wie bei elektromagnetischen Wellen beobachtet wurde.
 2. Materiewellen und Wellengleichung für freie Teilchen 2.1 Begriff Wellenfunktion Auf Grund des Wellencharakters der Materie können wir den Zustand eines physikalischen Systemes durch eine Wellenfunktion
2. Materiewellen und Wellengleichung für freie Teilchen 2.1 Begriff Wellenfunktion Auf Grund des Wellencharakters der Materie können wir den Zustand eines physikalischen Systemes durch eine Wellenfunktion
Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit. An einigen Beispielen erläutern
 Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit An einigen Beispielen erläutern 5. Das Photon: Welle und Teilchen 5.4. Die Plancksche Strahlungsformel Wichtige Punkte: u( ν, T ) = 8πh c
Vortragsthema: Die Unschärferelationen Ort/Impuls Energie/Zeit An einigen Beispielen erläutern 5. Das Photon: Welle und Teilchen 5.4. Die Plancksche Strahlungsformel Wichtige Punkte: u( ν, T ) = 8πh c
Atomphysik für Studierende des Lehramtes
 Atomphysik für Studierende des Lehramtes Teil 3 Grenzen der atomistischen Beschreibung der kinetischen Gastheorie Die spezifische Wärmekapazität gibt an, welche Wärmemenge einem Stoff pro Kilogramm zugeführt
Atomphysik für Studierende des Lehramtes Teil 3 Grenzen der atomistischen Beschreibung der kinetischen Gastheorie Die spezifische Wärmekapazität gibt an, welche Wärmemenge einem Stoff pro Kilogramm zugeführt
Moderne Physik. von Paul A.Tipler und Ralph A. Liewellyn
 Moderne Physik von Paul A.Tipler und Ralph A. Liewellyn Aus dem Englischen von Dr. Anna Schleitzer Bearbeitet von Prof. Dr. Gerd Czycholl Prof. Dr. Cornelius Noack Prof. Dr. Udo Strohbusch 2., verbesserte
Moderne Physik von Paul A.Tipler und Ralph A. Liewellyn Aus dem Englischen von Dr. Anna Schleitzer Bearbeitet von Prof. Dr. Gerd Czycholl Prof. Dr. Cornelius Noack Prof. Dr. Udo Strohbusch 2., verbesserte
Die Welt der Teilchen
 Die Welt der Teilchen Prof. André Schöning Physikalisches Institut Universität Heidelberg 1 Blick in die Tiefe des Universums 2 Blick in die Tiefe des Universums RAUM 3 Blick in die Tiefe des Universums
Die Welt der Teilchen Prof. André Schöning Physikalisches Institut Universität Heidelberg 1 Blick in die Tiefe des Universums 2 Blick in die Tiefe des Universums RAUM 3 Blick in die Tiefe des Universums
9. Atomphysik und Quantenphysik 9.0 Atom (historisch)
 9. Atomphysik und Quantenphysik 9.0 Atom (historisch) Atom: átomos (gr.) unteilbar. 5-4 Jh. v. Chr.: Demokrit und sein Lehrer Leukippos von Millet entwickeln Theorie der Atome Fragment 125 aus den Schriften
9. Atomphysik und Quantenphysik 9.0 Atom (historisch) Atom: átomos (gr.) unteilbar. 5-4 Jh. v. Chr.: Demokrit und sein Lehrer Leukippos von Millet entwickeln Theorie der Atome Fragment 125 aus den Schriften
VI. Quantenphysik. VI.1 Ursprünge der Quantenphysik, Atomphysik. Physik für Mediziner 1
 VI. Quantenphysik VI.1 Ursprünge der Quantenphysik, Atomphysik Physik für Mediziner 1 Mikroskopische Welt Physik für Mediziner 2 Strahlung des Schwarzen Körpers Schwarzer Körper: eintretendes Licht im
VI. Quantenphysik VI.1 Ursprünge der Quantenphysik, Atomphysik Physik für Mediziner 1 Mikroskopische Welt Physik für Mediziner 2 Strahlung des Schwarzen Körpers Schwarzer Körper: eintretendes Licht im
2 Elektrostatik. 2.1 Coulomb-Kraft und elektrische Ladung. 2.1 Coulomb-Kraft und elektrische Ladung
 2.1 Coulomb-Kraft und elektrische Ladung 2 Elektrostatik 2.1 Coulomb-Kraft und elektrische Ladung Abb. 2.1 Durch Reiben verschiedener Stoffe aneinander verbleiben Elektronen der Atomhüllen überwiegend
2.1 Coulomb-Kraft und elektrische Ladung 2 Elektrostatik 2.1 Coulomb-Kraft und elektrische Ladung Abb. 2.1 Durch Reiben verschiedener Stoffe aneinander verbleiben Elektronen der Atomhüllen überwiegend
4. Aufbau der Elektronenhülle 4.1. Grundlagen 4.2. Bohrsches Atommodell 4.3. Grundlagen der Quantenmechanik 4.4. Quantenzahlen 4.5.
 4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches Atommodell 4.3. Grundlagen der Quantenmechanik 4.4. Quantenzahlen 4.5. Atomorbitale 4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches
4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches Atommodell 4.3. Grundlagen der Quantenmechanik 4.4. Quantenzahlen 4.5. Atomorbitale 4. Aufbau der Elektronenhülle 4.. Grundlagen 4.. Bohrsches
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwörter von der letten Vorlesung können Sie sich noch erinnern? Elektronmikroskopie Die Energie eines Elektrons in einer Elektronenfalle En π = ml n Photonenabsorption & Photonenemission
An welche Stichwörter von der letten Vorlesung können Sie sich noch erinnern? Elektronmikroskopie Die Energie eines Elektrons in einer Elektronenfalle En π = ml n Photonenabsorption & Photonenemission
Von der kosmischen Hintergrundstrahlung zur Heisenbergschen Unbestimmtheitsrelation. eine Einführung in die Quantenmechanik
 Von der kosmischen Hintergrundstrahlung zur Heisenbergschen Unbestimmtheitsrelation eine Einführung in die Quantenmechanik 1) Die Hohlraumstrahlung: Geburt der Quantenmechanik Die kosmische Hintergrundstrahlung
Von der kosmischen Hintergrundstrahlung zur Heisenbergschen Unbestimmtheitsrelation eine Einführung in die Quantenmechanik 1) Die Hohlraumstrahlung: Geburt der Quantenmechanik Die kosmische Hintergrundstrahlung
2. Max Planck und das Wirkungsquantum h
 2. Max Planck und das Wirkungsquantum h Frequenzverteilung eines schwarzen Strahlers Am 6. Dezember 1900, dem 'Geburtsdatum' der modernen Physik, hatte Max Planck endlich die Antwort auf eine Frage gefunden,
2. Max Planck und das Wirkungsquantum h Frequenzverteilung eines schwarzen Strahlers Am 6. Dezember 1900, dem 'Geburtsdatum' der modernen Physik, hatte Max Planck endlich die Antwort auf eine Frage gefunden,
Festkörperelektronik 4. Übung
 Festkörperelektronik 4. Übung Felix Glöckler 23. Juni 2006 1 Übersicht Themen heute: Feedback Spin Drehimpuls Wasserstoffatom, Bohr vs. Schrödinger Wasserstoffmolekülion, kovalente Bindung Elektronen in
Festkörperelektronik 4. Übung Felix Glöckler 23. Juni 2006 1 Übersicht Themen heute: Feedback Spin Drehimpuls Wasserstoffatom, Bohr vs. Schrödinger Wasserstoffmolekülion, kovalente Bindung Elektronen in
Durch welchen Schlitz ist das Teilchen geflogen? Beobachtung
 ) Grundlagen der Quantenmechanik Welle-Teilchen-Dualismus: das Doppelspaltexperiment Teilchen Welle Durch welchen Schlitz ist das Teilchen geflogen? Beobachtung Welle-Teilchen-Dualismus: 1) P =... Wahrscheinlichkeitsamplitude
) Grundlagen der Quantenmechanik Welle-Teilchen-Dualismus: das Doppelspaltexperiment Teilchen Welle Durch welchen Schlitz ist das Teilchen geflogen? Beobachtung Welle-Teilchen-Dualismus: 1) P =... Wahrscheinlichkeitsamplitude
9. Das Wasserstoff-Atom. 9.1 Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 09. Wasserstoff-Atom Page 1 9. Das Wasserstoff-Atom 9.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
09. Wasserstoff-Atom Page 1 9. Das Wasserstoff-Atom 9.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Fundamentale Physikalische Konstanten - Gesamtliste Relativer Größe Symbol Wert Einheit Fehler
 UNIVERSELLE KONSTANTEN Vakuumlichtgeschwindigkeit c, c 0 299 792 458 m s 1 (exact) Magnetische Feldkonstante des Vakuums µ 0 4π 10 7 N A 2 (exact) =12.566 370 614... 10 7 N A 2 (exact) Elektrische Feldkonstante
UNIVERSELLE KONSTANTEN Vakuumlichtgeschwindigkeit c, c 0 299 792 458 m s 1 (exact) Magnetische Feldkonstante des Vakuums µ 0 4π 10 7 N A 2 (exact) =12.566 370 614... 10 7 N A 2 (exact) Elektrische Feldkonstante
23. Vorlesung EP. IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik
 23. Vorlesung EP IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik Strahlung: Stoff der Optik, Wärme-, Elektrizitätslehre u. Quantenphysik Photometrie
23. Vorlesung EP IV Optik 26. Beugung (Wellenoptik) V Strahlung, Atome, Kerne 27. Wärmestrahlung und Quantenmechanik Strahlung: Stoff der Optik, Wärme-, Elektrizitätslehre u. Quantenphysik Photometrie
3. Feinstruktur von Alkalispektren: Die gelbe D-Linie des Na ist ein Dublett, sollte aber nur eine Linie sein.
 13. Der Spin Experimentelle Fakten: 2. Normaler Zeeman-Effekt ist die Ausnahme: Meist sieht man den anormalen Zeeman-Effekt (Aufspaltung beobachtet, für die es keine normale Erklärung gab wegen Spin).
13. Der Spin Experimentelle Fakten: 2. Normaler Zeeman-Effekt ist die Ausnahme: Meist sieht man den anormalen Zeeman-Effekt (Aufspaltung beobachtet, für die es keine normale Erklärung gab wegen Spin).
Nawi 2AHMI Atommodelle I Glavas, Jakovljevic, Josipovic
 e -1. Teil Das Wort Atom kommt aus dem Griechischen atomos und bedeutet unteilbar ; unteilbarer Urstoff. Ein Atom ist der kleinste Baustein eines chemischen Grundstoffes oder Elements, der ohne Verlust
e -1. Teil Das Wort Atom kommt aus dem Griechischen atomos und bedeutet unteilbar ; unteilbarer Urstoff. Ein Atom ist der kleinste Baustein eines chemischen Grundstoffes oder Elements, der ohne Verlust
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Das quantenmechanische Atommodell
 Ende 93 konzipierte de Broglie seine grundlegenden Ideen über die Dualität von Welle und Korpuskel. Albert Einstein hatte schon 905 von den korpuskularen Eigenschaften des Lichtes gesprochen; de Broglie
Ende 93 konzipierte de Broglie seine grundlegenden Ideen über die Dualität von Welle und Korpuskel. Albert Einstein hatte schon 905 von den korpuskularen Eigenschaften des Lichtes gesprochen; de Broglie
Elemente der Quantenmechanik III 9.1. Schrödingergleichung mit beliebigem Potential 9.2. Harmonischer Oszillator 9.3. Drehimpulsoperator
 VL 9 VL8. VL9. Das Wasserstoffatom in der Klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren des
VL 9 VL8. VL9. Das Wasserstoffatom in der Klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren des
FK Experimentalphysik 3, Lösung 4
 1 Sterne als schwarze Strahler FK Experimentalphysik 3, 4 1 Sterne als schwarze Strahler Betrachten sie folgende Sterne: 1. Einen roten Stern mit einer Oberflächentemperatur von 3000 K 2. einen gelben
1 Sterne als schwarze Strahler FK Experimentalphysik 3, 4 1 Sterne als schwarze Strahler Betrachten sie folgende Sterne: 1. Einen roten Stern mit einer Oberflächentemperatur von 3000 K 2. einen gelben
Hallwachs-Experiment. Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe
 Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Entdeckung von Proton, Neutron, Elektron sowie (Elektron-)Neutrino
 Entdeckung von Proton, Neutron, Elektron sowie (Elektron-)Neutrino Wintersemester 2014/15 Li Jiaqi 11.11.2014 Chronik der mikroskopischen Welt 17-18 Jahrhundert: Begriffe des Atoms benutzen, die chemischen
Entdeckung von Proton, Neutron, Elektron sowie (Elektron-)Neutrino Wintersemester 2014/15 Li Jiaqi 11.11.2014 Chronik der mikroskopischen Welt 17-18 Jahrhundert: Begriffe des Atoms benutzen, die chemischen
Quantenphysik. Teil 3: PRAKTISCHE AKTIVITÄTEN
 Praktische Aktivität: Messung der Planck-Konstante mit LEDs 1 Quantenphysik Die Physik der sehr kleinen Teilchen mit großartigen Anwendungsmöglichkeiten Teil 3: PRAKTISCHE AKTIVITÄTEN Messung der Planck-Konstante
Praktische Aktivität: Messung der Planck-Konstante mit LEDs 1 Quantenphysik Die Physik der sehr kleinen Teilchen mit großartigen Anwendungsmöglichkeiten Teil 3: PRAKTISCHE AKTIVITÄTEN Messung der Planck-Konstante
