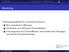
N k H nk ( α k Q k )e α k
|
|
|
- Eike Baum
- vor 5 Jahren
- Abrufe
Transkript
1 6 AUSWAHLREGELN Gesamt-Schwingungsustandsfunktionen Für die Auswahlregeln der Übergänge wischen den Schwingungsniveaus müssen die Smmetrien der ugehörigen Gesamt-Schwingungsustandsfunktionen betrachtet werden. Diese seten sich aus den Lösungsfunktionen des eindimensionalen harmonischen sillators usammen(siehe TC I): ψ = NH n ( αx)e α 2 x2 Durch die Entkopplung der Bewegungsgleichungen (6.13) lassen sich die 3N 6 Normalschwingungen jeweils als quasi eindimensionale harmonische sillatoren betrachten. Die Bewegungskoordinate jeder einelnen Normalschwingung ist die ugehörige Normalkoordinate Q k. Für die Kerne als Bosonen gelten nicht die Pauli-Postulate, die u Slaterdeterminanten als elektronische Gesamtustandsfunktionen geführt hatten (siehe TC I). Die Gesamt-Schwingungsustandsfunktion lässt sich daher als einelnes Produkt aller eindimensionalen Schwingungsfunktionen beschreiben. Φ n = 3N 6 k N k H nk ( α k Q k )e α k 2 Q 2 k Dabei ist die Konstante α k = 2π h λk, N k ist ein Normierungsfaktor, H nk sind die Hermite-Polnome; für die fundamentalen Anregungen werden nur H 0 = 1 und H 1 = 2 α k Q k benötigt. Die n k sind die Schwingungsquantenahlen n für jede Normalschwingung Q k. n k = 0 beschreibt den Grundustand ψ k0, n k = 1 den ersten angeregten Zustand ψ k1 Die verkürte Schreibweise Φ 0 für die Gesamtschwingungs-Grundustandsfunktion bedeutet, dass alle Quantenahlen null sind: n k = 0,k = 1,...,3N 6 Eine alternative Schreibweise gibt expliit die Quantenahlen aller Normalschwingungen an (was nur für kleine Ssteme praktikabel ist). Beispiel H 2 : Φ 0 = φ 000 Bei fundamentalen Anregungen Φ k ist genau eine Quantenahl eins statt null: n k = 1,n j = 0,j = 1,...,3N 6 k. In der alternativen Schreibweise werden die n k nach den ugehörigen Wellenahlen ν ke geordnet. Beispiel H 2 : Φ 1 = φ 100,Φ 2 = φ 010,Φ 3 = φ 001 Höhere Anregungen einer Normalschwingung, also.b. φ 020, haben in den experimentellen Spektren umeist geringe Intensitäten. Kombinationen von fundamentalen Anregungen verschiedener Normalschwingungen, also.b. φ 110, spielen in den Spektren besonders dann eine Rolle, wenn das entsprechende (Kombinations-)Schwingungsniveau in der Nähe einer fundamentalen Anregung liegt. In diesem Fall kann es u einer sogenannten Fermi-Resonan kommen, einer Koppelung der beiden Schwingungen. Die Gesamtwellenfunktion für den Schwingungsgrundustand kann nun expliit angegeben werden: Φ 0 = k 2 k N k e α k Q 2 Da im fundamental angeregten Schwingungsustand Φ k nur eine Quantenahl von Null verschieden ist, und das entsprechende Hermitepolnom ein Produkt aus einer Konstanten 2 α k und der Normalkoordinate Q k ist, ergibt sich der folgende Zusammenhang wischen Φ 0 und Φ k Auswahlregeln für die fundamentalen Anregungen Φ k = Φ 0 2 α k Q k (6.15) Analog u optischen Übergängen ist die Übergangswahrscheinlichkeit Φ 0 Φ k in der IR- bw. Raman- Spektroskopie proportional u Φ 0 Â Φ k 2, wobei  der jeweilige Übergangsoperator ist.
2 6 AUSWAHLREGELN 79 Dies ergibt sich wiederum nach einer Näherung des Lichts als Dipolstrahlung im Rahmen der eitabhängigen Störungstheorie (siehe Abschnitt 6.3). Die Franck-Condon-Näherung, bei der der Übergangsoperator nur auf die elektronische Wellenfunktion angewendet wird, gilt hier nicht, da nur Übergänge wischen Schwingungsuständen desselben elektronischen Zustands betrachtet werden. AusderGruppentheorieergibtsichanalogudenoptischenAnregungen,dassdasÜbergangsintegral Φ 0 Â Φ k nur dann von Null verschieden sein kann, wenn seine irreduible Darstellung Γ Φ0 Â Φ k totalsmmetrisch ist. Nur so ist gewährleistet, dass sich der Wert des Integrals nicht durch S ändert. Die irreduible Darstellung des Integrals ergibt sich als direktes Produkt der irreduiblen Darstellungen des Grundustandes, des Anregungsoperators und der angeregten Zustandsfunktion. Es muss also geprüft werden: Γ Φ0 ΓÂ Γ Φk? = Γ1 Aufgrund der Produktdarstellung (6.15) von Φ k vereinfacht sich das direkte Produkt u ΓÂ Γ Qk da Φ 0 Φ 0 stets totalsmmetrisch ist (oder im mehrdimensionalen Fall Γ 1 enthält). Die Übergangsoperatoren der beiden spektroskopischen Methoden sind nicht identisch. x Da in der IR-Spektroskopie ein direkter Übergang Φ 0 Φ k stattfindet, ist  der Dipoloperator r = (in atomaren Einheiten). In der Raman-Spektroskopie finden wei Übergange statt. Der Übergangsoperator ist deshalb quadratisch in r, allerdings nicht als Skalar- sondern als Tensorprodukt r r T. Es resultiert der Polarisierbarkeitstensor, der alle Kombinationen der kartesischen Koordinaten x 2,x,x, 2,, 2 enthält. Als Basis der irreduiblen Darstellungen der Charaktertabellen können auch Linearkombinationen dieser Funktionen auftreten. Verkürte Prüfungen: Da die direkten Produkte ΓÂ Γ Qk nur dann die totalsmmetrische Darstellung enthalten können, wenn Γ = Γ Qk gilt, brauchen nur folgende Vergleiche durchgeführt werden: Γ Qk Γ Qk = Γ x oder Γ oder Γ = Schwingung ist IR-aktiv = Γ x 2 oder... oder Γ 2 = Schwingung ist Raman-aktiv Zur Bestimmung der irreduiblen Darstellungen der Normalschwingungen muss wie folgt vorgegangen werden: Bestimmung von Γ Qk a) Transformation der lokalen Auslenkungsvektoren q i oderξ i durch S der Punktgruppe (hier kann analog u den p x,p,p -Atomorbitalen bei der Konstruktion von SMs vorgegangen werden). Sofern nur die irreduiblen Darstellungen gesucht werden, kann die Gesamt-Transformationsmatrix (Dimension 3N 3N) vereinfacht werden: Nur Atome a tragen ur Spur der TM bei, die durch Smmetrieoperation nicht bewegt werden (invariant sind). b) Für diese ortsfesten Atome a können die Spuren der lokalen Transformationsmatrien analtisch bestimmt werden:
3 6 AUSWAHLREGELN 80 C () ϕ = S () ϕ = σ x = i = E = cosϕ sinϕ 0 sinϕ cosϕ 0 χ a = 2cosϕ+1 analog für C (x),c () cosϕ sinϕ 0 sinϕ cosϕ 0 χ a = 2cosϕ 1 analog für S (x),s () χ a = 1 analog für σ x,σ χ a = χ a = DiereduibleDarstellunginderBasisder3N AuslenkungskoordinatenΓ Q ergibtsichalssummeüberalleχ a : Eine alternative Vorgehensweise ist N χ Q (Â) = χ a (Â) = N aχ a (Â) a=1 χ Q (Â) = N a(χ x (Â) χ(â) χ(â)) wobei N a die Anahl der invarianten Atome unter der Smmetrieoperation (Â) ist Separation von Rotation und Translation Aus der Gesamtdarstellung Γ Q müssen im nächsten Schritt die Freiheitsgrade der Translation Q trans und der Rotation Q rot eliminiert werden, um die reinen Schwingungsdarstellungen u erhalten. Dabei gilt: Translationen transformieren wie x,, Rotationen transformieren wie R x,r,r Daher wird die Separation wie folgt durchgeführt: Γ vib = Γ Q Γ x Γ Γ Γ Rx Γ R Γ R
4 6 AUSWAHLREGELN 81 Beispiel 66: Bestimmung der irreduiblen Darstellungen der Normalschwingungen von H 2 χ Q (E) = H 1 H 2 {}}{{}}{{}}{ = 9 χ Q (C 2 ) = = 1 nur ist ortsfest χ Q (σ x ) = = 1 nur ist ortsfest χ Q (σ ) = = 3 Daraus ergibt sich: Γ Q = (9, 1,1,3) = 3A 1 A 2 2B 1 3B 2 Γ Qtrans = A 1 B 1 B 2 Γ Qrot = A 2 B 1 B 2 Γ Qvib = 2A 1 B 2 IR-aktiv: Γ = A 1,Γ x = B 1, Raman-aktiv: Γ x 2 = Γ 2 = Γ 2 = A 1,Γ = B 2 = Alle H 2 -Schwingungen sind IR- und Ramanaktiv Im Allgemeinen lassen sich aber.b. verschiedene Isomere eines Moleküls durch die unterschiedliche Anahl IR- und Ramanaktiver Normalschwingungen unterscheiden (siehe Übung). Mit Hilfe der Normalkoordinaten lässt sich die eitabhängige Bewegung der Atomkerne im Molekül beschreiben: Q k (t) = 3N i C ik q i (t) = A k sin(2πν k t) Dabei lassen sich die massegewichteten Auslenkungskoordinaten q(t) als Vielfache lokaler Einheitsvektoren in x,, -Richtung interpretieren. Die Funktionswerte ändern sich eitlich sinusförmig (gemäß der Lösung der Newtonschen Bewegungsgleichungen) wischen q e x,, und + q e x,,. Die Bewegungsrichtung jedes Atoms ergibt sich durch Superposition dreier q i mit den Beiträgen C ik. Es ist dabei anschaulicher, anstelle der q i die lokalen Einheitsvektoren der Auslenkungen in x,,,-richtung u betrachten, die im Folgenden kur als x i, i, i beeichnet werden. Dies soll konkret für das Wassermolekül vorgestellt werden: 3N i C ik e i
5 6 AUSWAHLREGELN 82 Beispiel 67: Lokale Komponenten der Normalschwingungen von H H 1 H Resultierende Bewegungsrichtungen in Q 1 (links) und lokale kartesische Einheitsvektoren (rechts) Berechnete Koeffiienten C ik aus einer quantenchemischen Rechnung: x x x Q 1 : C 11 C 12 C 13 C 14 C 15 C 16 C 17 C 18 C 19 0,0 0,4 +0,6 0,0 +0,4 +0,6 0,0 0,0 0,1 : C 11 C 12 C 13 C 14 C 15 C 16 C 17 C 18 C 19 0,0 0,6 0,4 0,0 0,6 +0,4 0,0 +0,1 0,0 Die Normalschwingungen sind an die Smmetrie des Moleküls adaptiert. Das lässt sich konkret durch Anwendung der S der PG auf die Auslenkungsvektoren eigen: Beispielsweise geht für unter C () 2 der Richtungspfeil an H 1 in den negativen Richtungspfeil von H 2 über: E Q3 C () 2 σ x Q3 σ Q3 Γ Q3 = (1, 1, 1,1) = B 2
6 6 AUSWAHLREGELN 83 Expliite Transformation der Auslenkungskoordinaten Zur Bestimmung der irreduiblen Darstellungen der Normalschwingungen reicht es aus, die Spuren der TM u bestimmen (siehe Beispiel 66). Sollen die Normalschwingungen jedoch (qualitativ) konstruiert werden, müssen alle 3N lokalen Auslenkungsvektoren expliit mit allen S der PG transformiert werden. Beispiel 68: Lokale Auslenkungskoordinaten von H 2 x x1 H 1 x2 H Die Resultate der Transformationen lassen sich tabellarisch usammenfassen: Beispiele für die vollständigen 9 9-TM: E C () 2 σ x σ x 1 x 1 x 2 +x 2 x x 2 x 2 x 1 +x 1 x x 3 x 3 x 3 +x 3 x E = C 2 = Im Allgemeinen werden diese Matrien nicht benötigt. Für C 2 ist aber u erkennen, warum nur ortsfeste Atome ur Spur der TM beitragen.
7 6 AUSWAHLREGELN Konstruktion von smmetrieadaptierten Normalschwingungen In Analogie ur Konstruktion von Smmetrieorbitalen (siehe Abschnitt 5.11) werden die smmetrieadaptierten Normalschwingungen durch Anwendung der Projektionsoperatoren auf die Auslenkungskoordinaten erhalten. Dau ist es vorteilhaft, die Wirkung der S tabellarisch usammenufassen (siehe Beispiel 68). Beispiel 69: Konstruktion von B 2 -Normalschwingungen für H 2 In der Punktgruppe C 2v ergibt sich.b. der Projektionsoperator ˆP B2 u 1 4 (1E 1C 2 1σ x +1σ ). Mit der Tabelle aus Beispiel 68 ergibt sich ˆP B2 x 1 = 0 ˆP B2 1 = 1 2 ( ) ˆP B2 1 = 1 2 ( 1 2 ) ˆP B2 x 2 = 0 ˆP B2 2 = 1 2 ( ) ˆP B2 2 = 1 2 ( 2 1 ) ˆP B2 x 3 = 0 ˆP B2 3 = 3 ˆP B2 3 = 0 Die Ergebnisse für ( 1, 2 ) und ( 1, 2 ) sind jeweils linear abhängig. Auch hier lässt sich die Konstruktion linear abhängiger Projektionen dadurch vermeiden, wenn die Projektionsoperatoren nur auf die Koordinaten eines der smmetrieäquivalenten Atome (H 1 oder H 2 ) angewendet werden. Es werden somit drei von Null verschiedene Projektionen erhalten, in Übereinstimmung mit der Ausreduktion von Γ Q (siehe Beispiel 66). Daraus lassen sich drei Linearkombinationen bilden, die in diesem Fall u einer Rotation ( ), einer Translation ( ) und der B 2 -Normalschwingung ( 1 2 ( )+ 1 2 ( 2 2 ) 3 ) gehören. Diese stimmt qualitativ mit der quantenchemisch berechneten Normalschwingung (siehe Beispiel 65) überein: H 1 H Smmetrieanalse von gegebenen Normalschwingungen Analog ur Smmetriebestimmung von vorgegebenen Molekülorbitalen (siehe Abschnitt 5.12) lassen sich die irreduiblen Darstellungen von vorgegebenen Normalschwingungen (in Form der Koeffiienten oder als Abbildungen) bestimmen. Daher soll die Vorgehensweise hier nicht erneut im Detail beschrieben werden. Besonders einfach ist hier die Smmetriebestimmung von bestimmten Streckschwingungen. Dau müssen die entsprechenden Bindungen mit den S der PG transformiert werden. Nach Ausreduktion der reduiblen Darstellung ergeben sich die irreduiblen Darstellungen der entsprechenden smmetrischen und antismmetrischen Streckschwingungen.
In den vorigen Abschnitten wurden die globalen kartesischen Koordinaten der Atome eines Moleküls transformiert.
 4 MATRXDARSTELLUNG VON SYMMETREOPERATONEN 33 4.8 Lokale Koordinatenachsen m Gegensat um globalen Koordinatensstem, das für das gesamte Molekül gilt, sind lokale Koordinatenachsen individuell für jedes
4 MATRXDARSTELLUNG VON SYMMETREOPERATONEN 33 4.8 Lokale Koordinatenachsen m Gegensat um globalen Koordinatensstem, das für das gesamte Molekül gilt, sind lokale Koordinatenachsen individuell für jedes
Theoretische Chemie II. (Gruppentheorie)
 Theoretische Chemie II (Gruppentheorie) Modul BCh 4.4 Sommersemester 2016 i Vorwort Dieses Skript enthält die wesentlichen Inhalte, mathematischen Formeln und Abbildungen der Vorlesung Theoretische Chemie
Theoretische Chemie II (Gruppentheorie) Modul BCh 4.4 Sommersemester 2016 i Vorwort Dieses Skript enthält die wesentlichen Inhalte, mathematischen Formeln und Abbildungen der Vorlesung Theoretische Chemie
9. Moleküle. 9.1 Wasserstoff-Molekül Ion H Wasserstoff-Molekül H Schwerere Moleküle 9.4 Angeregte Moleküle. Physik IV SS
 9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
Klausur zur Vorlesung Symmetrie in Chemie und Spektroskopie
 Klausur zur Vorlesung Symmetrie in Chemie und Spektroskopie Zulässige Hilfsmittel: Charakterentafeln, Schema Hierarchie der Punktgruppen SS 6 Prof. Dr. B. Dick Aufgabe 1 (15P): Finden Sie die Punktgruppe
Klausur zur Vorlesung Symmetrie in Chemie und Spektroskopie Zulässige Hilfsmittel: Charakterentafeln, Schema Hierarchie der Punktgruppen SS 6 Prof. Dr. B. Dick Aufgabe 1 (15P): Finden Sie die Punktgruppe
Anorganische Chemie III
 Seminar zur Vorlesung Anorganische Chemie III Wintersemester 2015/16 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah # Darstellungen für
Seminar zur Vorlesung Anorganische Chemie III Wintersemester 2015/16 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah # Darstellungen für
3D-Transformationen. Kapitel Translation Skalierung
 Kapitel 3 3D-Transformationen Wie im weidimensionalen Fall, werden die Definitionspunkte der Objekte als Spaltenvektoren mit homogener Koordinate geschrieben. Die notwendigen Transformationen werden wieder
Kapitel 3 3D-Transformationen Wie im weidimensionalen Fall, werden die Definitionspunkte der Objekte als Spaltenvektoren mit homogener Koordinate geschrieben. Die notwendigen Transformationen werden wieder
9 WOODWARD-HOFFMANN-REGELN 92
 9 WOODWARD-HOFFMANN-REGELN 92 Die SMOs des Reaktanden und der Produkte (die nach Idealisierung nicht mehr unterschieden werden) müssen konstruiert und nach ihrer Knotenstruktur energetisch klassifiziert
9 WOODWARD-HOFFMANN-REGELN 92 Die SMOs des Reaktanden und der Produkte (die nach Idealisierung nicht mehr unterschieden werden) müssen konstruiert und nach ihrer Knotenstruktur energetisch klassifiziert
Schwingungsspektroskopie
 In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
In N atomigen Molekülen haben wir 3N 5 (linear) bzw. 3N 6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm wird zu einer komplizierten
7.3 Lorentz Transformation
 26 KAPITEL 7. SPEZIELLE RELATIVITÄTSTHEORIE 7.3 Lorent Transformation In diesem Abschnitt sollen die Transformationen im 4-dimensionalen Minkowski Raum betrachtet werden. Dabei wollen wir uns auf solche
26 KAPITEL 7. SPEZIELLE RELATIVITÄTSTHEORIE 7.3 Lorent Transformation In diesem Abschnitt sollen die Transformationen im 4-dimensionalen Minkowski Raum betrachtet werden. Dabei wollen wir uns auf solche
Schwingungen (Vibrationen) zweiatomiger Moleküle
 Schwingungen (Vibrationen) zweiatomiger Moleküle Das Molekülpotential ist die Potentialkurve für die Schwingung H 2 Molekül 0.0 2.5 4 5 6 H( 1s) + H( 3l ) Energie in ev 5.0 7.5 H( 1s) + H( 2l ) H( 1s)
Schwingungen (Vibrationen) zweiatomiger Moleküle Das Molekülpotential ist die Potentialkurve für die Schwingung H 2 Molekül 0.0 2.5 4 5 6 H( 1s) + H( 3l ) Energie in ev 5.0 7.5 H( 1s) + H( 2l ) H( 1s)
Übungen zur Vorlesung Physikalische Chemie 2 (B. Sc.) Lösungsvorschlag zu Blatt 12
 Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Theoretical Biophysics - Quantum Theory and Molecular Dynamics. 13. Vorlesung. Pawel Romanczuk WS 2016/17
 Theoretical Biophysics - Quantum Theory and Molecular Dynamics 13. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Variationsrechnung LCAO-Verfahren am Beispiel
Theoretical Biophysics - Quantum Theory and Molecular Dynamics 13. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Variationsrechnung LCAO-Verfahren am Beispiel
Schwingungsspektroskopie
 Schwingungsspektroskopie In N-atomigen Molekülen haben wir 3N-5 (linear) bzw. 3N-6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm
Schwingungsspektroskopie In N-atomigen Molekülen haben wir 3N-5 (linear) bzw. 3N-6 (nichtlinear) Freiheitsgrade der Schwingung, welche die Position der Atome relativ zueinander beschreiben. Der Potentialterm
Protokoll zum Versuch Infrarot-Spektren mehratomiger Gase
 Protokoll zum Versuch Infrarot-Spektren mehratomiger Gase. Versuchsziel / Experimentelles In diesem Versuch wird ein Infrarot-Spektrum von CO im Bereich der Wellenzahlen ν von 6000 bis 400 cm- mit einer
Protokoll zum Versuch Infrarot-Spektren mehratomiger Gase. Versuchsziel / Experimentelles In diesem Versuch wird ein Infrarot-Spektrum von CO im Bereich der Wellenzahlen ν von 6000 bis 400 cm- mit einer
Gruppentheorie ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD. Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE
 ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
: Quantenmechanische Lösung H + 2. Molekülion und. Aufstellen der Schrödingergleichung für das H + 2
 H + 2 Die molekulare Bindung : Quantenmechanische Lösung Aufstellen der Schrödingergleichung für das H + 2 Molekülion und Lösung Wichtige Einschränkung: Die Kerne sind festgehalten H Ψ(r) = E Ψ(r) (11)
H + 2 Die molekulare Bindung : Quantenmechanische Lösung Aufstellen der Schrödingergleichung für das H + 2 Molekülion und Lösung Wichtige Einschränkung: Die Kerne sind festgehalten H Ψ(r) = E Ψ(r) (11)
Vorlesung 21. Identische Teilchen und das Pauli-Prinzip
 Vorlesung 1 Identische Teilchen und das Pauli-Prinzip Identische Teilchen: Jede Art von Teilchen in der Natur definieren wir durch ihre Eigenschaften, z.b. Massen, Spins, Ladungen usw. Das bedeutet, dass
Vorlesung 1 Identische Teilchen und das Pauli-Prinzip Identische Teilchen: Jede Art von Teilchen in der Natur definieren wir durch ihre Eigenschaften, z.b. Massen, Spins, Ladungen usw. Das bedeutet, dass
5 Kinematik der Rotation (Drehbewegungen) 6 Dynamik der Translation
 Inhalt 1 4 Kinematik der Translation 4.1 Koordinatensysteme 4. Elementare Bewegungen 5 Kinematik der Rotation (Drehbewegungen) 6 Dynamik der Translation 6.1 Die Newton sche Aiome 6.1.1 Erstes Newton sches
Inhalt 1 4 Kinematik der Translation 4.1 Koordinatensysteme 4. Elementare Bewegungen 5 Kinematik der Rotation (Drehbewegungen) 6 Dynamik der Translation 6.1 Die Newton sche Aiome 6.1.1 Erstes Newton sches
3D-Transformationen. Kapitel Translation Skalierung
 Kapitel 13 3D-Transformationen Wie im weidimensionalen Fall, werden die Definitionspunkte der Objekte als Spaltenvektoren mit homogener Koordinate geschrieben. Die notwendigen Transformationen werden wieder
Kapitel 13 3D-Transformationen Wie im weidimensionalen Fall, werden die Definitionspunkte der Objekte als Spaltenvektoren mit homogener Koordinate geschrieben. Die notwendigen Transformationen werden wieder
Dynamik von Molekülen. Rotationen und Schwingungen von Molekülen
 Rotationen und Schwingungen von Molekülen Schwingungen und Rotationen Bis jetzt haben wir immer den Fall betrachtet, daß die Kerne fest sind Was geschieht nun, wenn sich die Kerne bewegen können? Zwei
Rotationen und Schwingungen von Molekülen Schwingungen und Rotationen Bis jetzt haben wir immer den Fall betrachtet, daß die Kerne fest sind Was geschieht nun, wenn sich die Kerne bewegen können? Zwei
z n z m e 2 WW-Kern-Kern H = H k + H e + H ek
 2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
Quantenzahlen. A B z. Einführung in die Struktur der Materie 67
 Quantenzahlen Wir haben uns bis jetzt nur mit dem Grundzustand des H + 2 Moleküls beschäftigt Wie sieht es aus mit angeregten Zuständen wie z.b. 2p Zuständen im H Atom? Bezeichnung der Molekülorbitale
Quantenzahlen Wir haben uns bis jetzt nur mit dem Grundzustand des H + 2 Moleküls beschäftigt Wie sieht es aus mit angeregten Zuständen wie z.b. 2p Zuständen im H Atom? Bezeichnung der Molekülorbitale
Viele wichtige Operationen können als lineare Abbildungen interpretiert werden. Beispielsweise beschreibt die lineare Abbildung
 Kapitel 3 Lineare Abbildungen Lineare Abbildungen sind eine natürliche Klasse von Abbildungen zwischen zwei Vektorräumen, denn sie vertragen sich per definitionem mit der Struktur linearer Räume Viele
Kapitel 3 Lineare Abbildungen Lineare Abbildungen sind eine natürliche Klasse von Abbildungen zwischen zwei Vektorräumen, denn sie vertragen sich per definitionem mit der Struktur linearer Räume Viele
4.1. Vektorräume und lineare Abbildungen
 4.1. Vektorräume und lineare Abbildungen Mengen von Abbildungen Für beliebige Mengen X und Y bezeichnet Y X die Menge aller Abbildungen von X nach Y (Reihenfolge beachten!) Die Bezeichnungsweise erklärt
4.1. Vektorräume und lineare Abbildungen Mengen von Abbildungen Für beliebige Mengen X und Y bezeichnet Y X die Menge aller Abbildungen von X nach Y (Reihenfolge beachten!) Die Bezeichnungsweise erklärt
Gliederung. Potentialenergieflächen für chemische Reaktionen. und konische Durchschneidungen. 1 Born-Oppenheimer-Näherung
 Gliederung Potentialenergieflächen für chemische Reaktionen 1 2 adiabatische und diabatische Potentialflächen 3 Kreuzungsverbot für Potentialflächen, nicht-adiabatische Übergänge und konische Durchschneidungen
Gliederung Potentialenergieflächen für chemische Reaktionen 1 2 adiabatische und diabatische Potentialflächen 3 Kreuzungsverbot für Potentialflächen, nicht-adiabatische Übergänge und konische Durchschneidungen
Lösung der harmonischen Oszillator-Gleichung
 Lösung der harmonischen Oszillator-Gleichung Lucas Kunz 8. Dezember 016 Inhaltsverzeichnis 1 Physikalische Herleitung 1.1 Gravitation................................... 1. Reibung.....................................
Lösung der harmonischen Oszillator-Gleichung Lucas Kunz 8. Dezember 016 Inhaltsverzeichnis 1 Physikalische Herleitung 1.1 Gravitation................................... 1. Reibung.....................................
Da Atome viele ununterscheidbare Elektronen besitzen, sind ihre Zustände durch interelektronische Coulomb- und Austausch-Wechselwirkungen bestimmt.
 12 Moleküle Slide 267 Vorbemerkungen Da Atome viele ununterscheidbare Elektronen besitzen, sind ihre Zustände durch interelektronische Coulomb- und Austausch-Wechselwirkungen bestimmt. Je 2 Elektronen
12 Moleküle Slide 267 Vorbemerkungen Da Atome viele ununterscheidbare Elektronen besitzen, sind ihre Zustände durch interelektronische Coulomb- und Austausch-Wechselwirkungen bestimmt. Je 2 Elektronen
Vorlesung Statistische Mechanik: N-Teilchensystem
 Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Virialentwicklung Die Berechnung der Zustandssumme bei realen Gasen ist nicht mehr exakt durchführbar. Eine Möglichkeit, die Wechselwirkung in realen Gasen systematisch mitzunehmen ist, eine Entwicklung
Das H + 2 -Molekülion
 Das Näherungen für das elektronische Problem und Kernbewegungen 7. Dezember 2011 Schrödinger-Gleichung des s Abbildung: Arthur Beiser; Atome, Moleküle, Festkörper; Vieweg, Braunschweig 1983 ( K/E 2 2 +
Das Näherungen für das elektronische Problem und Kernbewegungen 7. Dezember 2011 Schrödinger-Gleichung des s Abbildung: Arthur Beiser; Atome, Moleküle, Festkörper; Vieweg, Braunschweig 1983 ( K/E 2 2 +
(a) Transformation auf die generalisierten Koordinaten (= Kugelkoordinaten): ẏ = l cos(θ) θ sin(ϕ) + l sin(θ) cos(ϕ) ϕ.
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Theoretische Physik B - Lösungen SS 10 Prof. Dr. Aleander Shnirman Blatt 5 Dr. Boris Narozhny, Dr. Holger Schmidt 11.05.010
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Theoretische Physik B - Lösungen SS 10 Prof. Dr. Aleander Shnirman Blatt 5 Dr. Boris Narozhny, Dr. Holger Schmidt 11.05.010
4 Matrixdarstellung von Symmetrieoperationen
 4 MATRIXDARSTELLUNG VON SYMMETRIEOPERATIONEN 4 Konsistenz der minimalen Symmetrieanalyse: fehlende Symmetrieelemente? Beispiel 3: Punktgruppe D h Im Schema (3.1) wird die Punktgruppe D h durch Auffinden
4 MATRIXDARSTELLUNG VON SYMMETRIEOPERATIONEN 4 Konsistenz der minimalen Symmetrieanalyse: fehlende Symmetrieelemente? Beispiel 3: Punktgruppe D h Im Schema (3.1) wird die Punktgruppe D h durch Auffinden
Eigenwerte und Eigenvektoren
 Vortrag Gmnasium Birkenfeld Von der mathematischen Spielerei zur technischen Anwendung Vortrag Gmnasium Birkenfeld. Vektoren und Matrizen Wir betrachten einen Punkt P (, ) in der Ebene eines rechtwinklig
Vortrag Gmnasium Birkenfeld Von der mathematischen Spielerei zur technischen Anwendung Vortrag Gmnasium Birkenfeld. Vektoren und Matrizen Wir betrachten einen Punkt P (, ) in der Ebene eines rechtwinklig
Symmetrie und Anwendungen
 PC II Kinetik und Struktur Kapitel 6 Symmetrie und Anwendungen Symmetrie von Schwingungen und Orbitalen, Klassifizierung von Molekülschwingungen Auswahlregeln: erlaubte verbotene Übergänge IR-, Raman-,
PC II Kinetik und Struktur Kapitel 6 Symmetrie und Anwendungen Symmetrie von Schwingungen und Orbitalen, Klassifizierung von Molekülschwingungen Auswahlregeln: erlaubte verbotene Übergänge IR-, Raman-,
Molekulare Kerndynamik. Grundlagen
 Grundlagen Bei der Bestimmung der elektronischen Struktur von Molekülen haben wir bis jetzt den Fall betrachtet, daß die Kerne fest sind. Lösung der elektronischen Schrödingergleichung in einem festen
Grundlagen Bei der Bestimmung der elektronischen Struktur von Molekülen haben wir bis jetzt den Fall betrachtet, daß die Kerne fest sind. Lösung der elektronischen Schrödingergleichung in einem festen
Einige Lösungsvorschläge für die Klausur zur Vorlesung
 Prof Klaus Mohnke Institut für Mathematik Einige Lösungsvorschläge für die Klausur zur Vorlesung Lineare Algebra und analtische Geometrie II* - SS 7 Aufgabe Im R mit dem Standardskalarprodukt ist die folgende
Prof Klaus Mohnke Institut für Mathematik Einige Lösungsvorschläge für die Klausur zur Vorlesung Lineare Algebra und analtische Geometrie II* - SS 7 Aufgabe Im R mit dem Standardskalarprodukt ist die folgende
Skript zur 19. Vorlesung Quantenmechanik, Freitag den 24. Juni, 2011.
 Skript ur 19. Vorlesung Quantenmechanik, Freitag den 4. Juni, 011. 13.5 Weitere Eigenschaften des Spin 1/ 1. Die Zustände und sind war Eigenustände der -Komponente ŝ des Spin- Operators s, sie stellen
Skript ur 19. Vorlesung Quantenmechanik, Freitag den 4. Juni, 011. 13.5 Weitere Eigenschaften des Spin 1/ 1. Die Zustände und sind war Eigenustände der -Komponente ŝ des Spin- Operators s, sie stellen
(6.29) Z X. Die standardnormalverteilte Zufallvariable Z, Z ~ N(0,1), weist den Erwartungswert (6.30) E(Z) = 0 und die Varianz (6.31) V(Z) = 1 auf.
 Standardnormalverteilung Da die arameter μ und σ beliebige reelle Zahlenwerte bw. beliebige positive reelle Zahlenwerte (σ >0) annehmen können, gibt es unendlich viele Normalverteilungen. Die Dichtefunktion
Standardnormalverteilung Da die arameter μ und σ beliebige reelle Zahlenwerte bw. beliebige positive reelle Zahlenwerte (σ >0) annehmen können, gibt es unendlich viele Normalverteilungen. Die Dichtefunktion
Darstellungstheorie. Vortag von Heiko Fischer - Proseminar QM
 Darstellungstheorie Vortag von Heiko Fischer - Proseminar QM Wir haben uns in den vergangenen Vorträgen intensiv mit den Eigenschaften abstrakter Gruppen beschäftigt. Im physikalischen Kontext sind Gruppen
Darstellungstheorie Vortag von Heiko Fischer - Proseminar QM Wir haben uns in den vergangenen Vorträgen intensiv mit den Eigenschaften abstrakter Gruppen beschäftigt. Im physikalischen Kontext sind Gruppen
Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt
 Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
Atom- und Molekülbau Ein Lehrbuch für Studierende der Chemie im 2. Studienabschnitt Von Peter C. Schmidt und Konrad G. Weil 147 Abbildungen, 19 Tabellen Georg Thieme Verlag Stuttgart New York 1982 Vorwort
1 Lagrange-Formalismus
 Lagrange-Formalismus SS 4 In der gestrigen Vorlesung haben wir die Beschreibung eines physikalischen Systems mit Hilfe der Newton schen Axiome kennen gelernt. Oft ist es aber nicht so einfach die Kraftbilanz
Lagrange-Formalismus SS 4 In der gestrigen Vorlesung haben wir die Beschreibung eines physikalischen Systems mit Hilfe der Newton schen Axiome kennen gelernt. Oft ist es aber nicht so einfach die Kraftbilanz
Mathematik II Frühjahrssemester 2013
 Mathematik II Frühjahrssemester 213 Prof. Dr. Erich Walter Farkas Kapitel 7: Lineare Algebra Kapitel 7.5: Eigenwerte und Eigenvektoren einer quadratischen Matrix Prof. Dr. Erich Walter Farkas Mathematik
Mathematik II Frühjahrssemester 213 Prof. Dr. Erich Walter Farkas Kapitel 7: Lineare Algebra Kapitel 7.5: Eigenwerte und Eigenvektoren einer quadratischen Matrix Prof. Dr. Erich Walter Farkas Mathematik
4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration
 g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
Anwendungsorientierte Mathematik für ingenieurwissenschaftliche Fachrichtungen
 Anwendungsorientierte Mathematik für ingenieurwissenschaftliche Fachrichtungen Band : Gleichungen und Differentialgleichungen Bearbeitet von Rudolf Taschner 1. Auflage 014. Buch. 314 S. Hardcover ISBN
Anwendungsorientierte Mathematik für ingenieurwissenschaftliche Fachrichtungen Band : Gleichungen und Differentialgleichungen Bearbeitet von Rudolf Taschner 1. Auflage 014. Buch. 314 S. Hardcover ISBN
PC2: Spektroskopie Störungsrechnung
 PC: Spektroskopie Störungsrechnung (neu überarbeitet im SS 014, nach: Wedler-Freund, Physikalische Chemie) Wir betrachten ein System aus quantenchemischen Zuständen m, n, zwischen denen durch die Absorption
PC: Spektroskopie Störungsrechnung (neu überarbeitet im SS 014, nach: Wedler-Freund, Physikalische Chemie) Wir betrachten ein System aus quantenchemischen Zuständen m, n, zwischen denen durch die Absorption
3 Elektronengas-Modell und Polyene
 3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
Die Gruppe der affinen Abbildungen A
 H. Burkhardt, Institut für Informatik, Universität Freiburg ME-I, Kap. 2b 1 Die Gruppe der affinen Abbildungen A Die Gruppe der affinen Abbildungen entsteht durch Wahl einer beliebigen regulären Matrix
H. Burkhardt, Institut für Informatik, Universität Freiburg ME-I, Kap. 2b 1 Die Gruppe der affinen Abbildungen A Die Gruppe der affinen Abbildungen entsteht durch Wahl einer beliebigen regulären Matrix
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
4 Lineare Abbildungen
 17. November 2008 34 4 Lineare Abbildungen 4.1 Lineare Abbildung: Eine Funktion f : R n R m heißt lineare Abbildung von R n nach R m, wenn für alle x 1, x 2 und alle α R gilt f(αx 1 ) = αf(x 1 ) f(x 1
17. November 2008 34 4 Lineare Abbildungen 4.1 Lineare Abbildung: Eine Funktion f : R n R m heißt lineare Abbildung von R n nach R m, wenn für alle x 1, x 2 und alle α R gilt f(αx 1 ) = αf(x 1 ) f(x 1
Theoretische Biophysikalische Chemie
 Theoretische Biophysikalische Chemie Thermochemie (und Schwingungsspektroskopie) Christoph Jacob DFG-CENTRUM FÜR FUNKTIONELLE NANOSTRUKTUREN 0 KIT 17.12.2012 Universität deschristoph Landes Baden-Württemberg
Theoretische Biophysikalische Chemie Thermochemie (und Schwingungsspektroskopie) Christoph Jacob DFG-CENTRUM FÜR FUNKTIONELLE NANOSTRUKTUREN 0 KIT 17.12.2012 Universität deschristoph Landes Baden-Württemberg
Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten oder in Festkörpern vor.
 phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
phys4.025 Page 1 13. Moleküle Nur eine kleine Anzahl von Elementen kommt natürlich in Form von einzelnen Atomen vor. Die meisten Elemente liegen in gebundener Form als einzelne Moleküle, in Flüssigkeiten
Chemische Bindung zweiatomiger Moleküle
 Die Born Oppenheimer Näherung vernachlässigt Elektronenimpulse gegenüber Kernimpulsen und erlaubt die Gesamtwellenfunktion als ein Produkt aus einer Kernwellenfunktion F q ( R) und der einer Elektronenwellenfunktion
Die Born Oppenheimer Näherung vernachlässigt Elektronenimpulse gegenüber Kernimpulsen und erlaubt die Gesamtwellenfunktion als ein Produkt aus einer Kernwellenfunktion F q ( R) und der einer Elektronenwellenfunktion
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Theoretische Mechanik
 Prof. Dr. R. Ketzmerick/Dr. R. Schumann Technische Universität Dresden Institut für Theoretische Physik Sommersemester 2008 Theoretische Mechanik 9. Übung 9.1 d alembertsches Prinzip: Flaschenzug Wir betrachten
Prof. Dr. R. Ketzmerick/Dr. R. Schumann Technische Universität Dresden Institut für Theoretische Physik Sommersemester 2008 Theoretische Mechanik 9. Übung 9.1 d alembertsches Prinzip: Flaschenzug Wir betrachten
ANWENDUNG DER GRUPPENTHEORIE IN DER QUANTENMECHANIK
 M. I. PETRASCHEN E. D. TRIFONOW ANWENDUNG DER GRUPPENTHEORIE IN DER QUANTENMECHANIK In deutscher Sprache herausgegeben von Prof. Dr. rer. nat. habil. ARMIN UHLMANN Leipzig Mit 22 Abbildungen und 16 Tabellen
M. I. PETRASCHEN E. D. TRIFONOW ANWENDUNG DER GRUPPENTHEORIE IN DER QUANTENMECHANIK In deutscher Sprache herausgegeben von Prof. Dr. rer. nat. habil. ARMIN UHLMANN Leipzig Mit 22 Abbildungen und 16 Tabellen
11. Quantenchemische Methoden
 Computeranwendung in der Chemie Informatik für Chemiker(innen) 11. Quantenchemische Methoden Jens Döbler 2004 "Computer in der Chemie", WS 2003-04, Humboldt-Universität VL11 Folie 1 Grundlagen Moleküle
Computeranwendung in der Chemie Informatik für Chemiker(innen) 11. Quantenchemische Methoden Jens Döbler 2004 "Computer in der Chemie", WS 2003-04, Humboldt-Universität VL11 Folie 1 Grundlagen Moleküle
Mathematik II Frühlingsemester 2015 Kapitel 8: Lineare Algebra 8.5 Eigenwerte und Eigenvektoren
 Mathematik II Frühlingsemester 215 Kapitel 8: Lineare Algebra 8.5 Eigenwerte und Eigenvektoren www.math.ethz.ch/education/bachelor/lectures/fs215/other/mathematik2 biol Prof. Dr. Erich Walter Farkas http://www.math.ethz.ch/
Mathematik II Frühlingsemester 215 Kapitel 8: Lineare Algebra 8.5 Eigenwerte und Eigenvektoren www.math.ethz.ch/education/bachelor/lectures/fs215/other/mathematik2 biol Prof. Dr. Erich Walter Farkas http://www.math.ethz.ch/
Lösungsvorschlag Übung 9
 Lösungsvorschlag Übung 9 Aufgabe 1: Wellenfunktion und Aufenthaltswahrscheinlichkeit a Die Wahrscheinlichkeitsdichte ist eine Wahrscheinlichkeit pro Volumenelement. Die Wahrscheinlichkeit selbst ist eine
Lösungsvorschlag Übung 9 Aufgabe 1: Wellenfunktion und Aufenthaltswahrscheinlichkeit a Die Wahrscheinlichkeitsdichte ist eine Wahrscheinlichkeit pro Volumenelement. Die Wahrscheinlichkeit selbst ist eine
Darstellungstheorie I
 Darstellungstheorie I Vortrag im Rahmen des Proseminars: Gruppentheorie und Quantenmechanik von Prof. Dr. Jan Louis und Dr. Robert Richter Universität Hamburg Jan Oliver Rieger 8. November 2012 1 1 Grundlegende
Darstellungstheorie I Vortrag im Rahmen des Proseminars: Gruppentheorie und Quantenmechanik von Prof. Dr. Jan Louis und Dr. Robert Richter Universität Hamburg Jan Oliver Rieger 8. November 2012 1 1 Grundlegende
Grundlagen der Gruppentheorie
 Grundlaen der Gruppentheorie Eine Gruppe G besteht entsprechend ihrer Ordnun aus Elementen a, b, c,..., zwischen denen eine Multiplikationsoperation so definiert ist, 1. dass das Produkt beliebi zweier
Grundlaen der Gruppentheorie Eine Gruppe G besteht entsprechend ihrer Ordnun aus Elementen a, b, c,..., zwischen denen eine Multiplikationsoperation so definiert ist, 1. dass das Produkt beliebi zweier
Blatt 11.1: Fourier-Integrale, Differentialgleichungen
 Fakultät für Physik R: Rechenmethoden für Physiker, WiSe 204/5 Dozent: Jan von Delft Übungen: Benedikt Bruognolo, Katharina Stadler http://homepages.physik.uni-muenchen.de/~vondelft/lehre/4t0/ Blatt.:
Fakultät für Physik R: Rechenmethoden für Physiker, WiSe 204/5 Dozent: Jan von Delft Übungen: Benedikt Bruognolo, Katharina Stadler http://homepages.physik.uni-muenchen.de/~vondelft/lehre/4t0/ Blatt.:
Übungen zur Quantentheorie der Viel-Teilchen-Systeme
 Übungen ur Quantentheorie der Viel-Teilchen-Systeme Frank ssenberger, Andreas Linscheid, Kai Schmit 5. Juni 2008 Aufgabe 2 a Wir betrachten ein System von lektronen in einem Band. Die nergie des System
Übungen ur Quantentheorie der Viel-Teilchen-Systeme Frank ssenberger, Andreas Linscheid, Kai Schmit 5. Juni 2008 Aufgabe 2 a Wir betrachten ein System von lektronen in einem Band. Die nergie des System
5 Elektronengas-Modell und Polyene
 5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
7 Die Hamilton-Jacobi-Theorie
 7 Die Hamilton-Jacobi-Theorie Ausgearbeitet von Rolf Horn und Bernhard Schmitz 7.1 Einleitung Um die Hamilton schen Bewegungsgleichungen q k = H(q, p) p k ṗ k = H(p, q) q k zu vereinfachen, führten wir
7 Die Hamilton-Jacobi-Theorie Ausgearbeitet von Rolf Horn und Bernhard Schmitz 7.1 Einleitung Um die Hamilton schen Bewegungsgleichungen q k = H(q, p) p k ṗ k = H(p, q) q k zu vereinfachen, führten wir
WAS FEHLT? STATISCHE KORRELATION UND VOLLE KONFIGURATIONSWECHSELWIRKUNG
 31 besetzen als die β Elektronen. Wenn man dies in der Variation der Wellenfunktion zulässt, also den Satz der Orbitale verdoppelt und α und β Orbitale gleichzeitig optimiert, so ist i. A. die Energie
31 besetzen als die β Elektronen. Wenn man dies in der Variation der Wellenfunktion zulässt, also den Satz der Orbitale verdoppelt und α und β Orbitale gleichzeitig optimiert, so ist i. A. die Energie
Probestudium der Physik 2011/12
 Probestudium der Physik 2011/12 Karsten Kruse 2. Mechanische Schwingungen und Wellen - Theoretische Betrachtungen 2.1 Der harmonische Oszillator Wir betrachten eine lineare Feder mit der Ruhelänge l 0.
Probestudium der Physik 2011/12 Karsten Kruse 2. Mechanische Schwingungen und Wellen - Theoretische Betrachtungen 2.1 Der harmonische Oszillator Wir betrachten eine lineare Feder mit der Ruhelänge l 0.
Moleküle und Wärmestatistik
 Moleküle und Wärmestatistik Musterlösung.08.008 Molekülbindung Ein Molekül bestehe aus zwei Atomkernen A und B und zwei Elektronen. a) Wie lautet der Ansatz für die symmetrische Wellenfunktion in der Molekülorbitalnäherung?
Moleküle und Wärmestatistik Musterlösung.08.008 Molekülbindung Ein Molekül bestehe aus zwei Atomkernen A und B und zwei Elektronen. a) Wie lautet der Ansatz für die symmetrische Wellenfunktion in der Molekülorbitalnäherung?
3. Kreisbewegung. Punkte auf einem Rad Zahnräder, Getriebe Drehkran Turbinen, Hubschrauberrotor
 3. Kreisbewegung Ein wichtiger technischer Sonderfall ist die Bewegung auf einer Kreisbahn. Dabei hat der Punkt zu jedem Zeitpunkt den gleichen Abstand vom Kreismittelpunkt. Beispiele: Punkte auf einem
3. Kreisbewegung Ein wichtiger technischer Sonderfall ist die Bewegung auf einer Kreisbahn. Dabei hat der Punkt zu jedem Zeitpunkt den gleichen Abstand vom Kreismittelpunkt. Beispiele: Punkte auf einem
Computergrafik Sommersemester 2004 Übungen
 Sommersemester 4 Freiwillige Zusatzübung Aufgabe 6: Transformationen im zweidimensionalen aum Berechnen Sie die Transformationsmatri, die eine Szene zuerst um 3 Grad um den Ursprung dreht und anschließend
Sommersemester 4 Freiwillige Zusatzübung Aufgabe 6: Transformationen im zweidimensionalen aum Berechnen Sie die Transformationsmatri, die eine Szene zuerst um 3 Grad um den Ursprung dreht und anschließend
Prof. D. Salamon Funktionentheorie ETH Zürich MATH, PHYS 3. November Musterlösungen 6
 Prof. D. Salamon Funktionentheorie ETH Zürich MATH, PHYS 3. November 009 Musterlösungen 6. Sei B r := { C < r} und f : C C durch 3 + definiert. Welches ist der grösste Wert von r so dass f Br injektiv
Prof. D. Salamon Funktionentheorie ETH Zürich MATH, PHYS 3. November 009 Musterlösungen 6. Sei B r := { C < r} und f : C C durch 3 + definiert. Welches ist der grösste Wert von r so dass f Br injektiv
Aufgabe 2: Quantenmechanisches Modell für pseudolineare Polyene
 Lösungsvorschlag Übung 10 Aufgabe 1: Ein Teilchen im eindimensionalen Kasten a Die Energiedifferenz zwischen zwei aufeinanderfolgenden Energie-Eigenwerten ist E n,n+1 = E n+1 E n ml n + 1 n 1.1 n + 1.
Lösungsvorschlag Übung 10 Aufgabe 1: Ein Teilchen im eindimensionalen Kasten a Die Energiedifferenz zwischen zwei aufeinanderfolgenden Energie-Eigenwerten ist E n,n+1 = E n+1 E n ml n + 1 n 1.1 n + 1.
Übungen zur Vorlesung Theoretische Chemie II Übungsblatt 1 SoSe 2015 Lösungen Ĥ Ψ = E Ψ (1) c b
 Übungen zur Vorlesung Theoretische Chemie II Übungsblatt SoSe 205 Lösungen. H 2 + Molekülion a) Konstruieren Sie die Schrödingergleichung in Matrixdarstellung. Zunächst geht man von der stationären Schrödinger-Gleichung
Übungen zur Vorlesung Theoretische Chemie II Übungsblatt SoSe 205 Lösungen. H 2 + Molekülion a) Konstruieren Sie die Schrödingergleichung in Matrixdarstellung. Zunächst geht man von der stationären Schrödinger-Gleichung
Einführung Vektoralgebra VEKTORRECHNUNG. Prof. Dr. Dan Eugen Ulmet. Hochschule Esslingen. October 6, 2007
 Hochschule Esslingen October 6, 2007 Overview Einführung 1 Einführung 2 Was sind Vektoren? Vektoren werden geometrisch definiert als Pfeilklassen: Strecken mit gleichem Betrag, gleicher Richtung und Orientierung.
Hochschule Esslingen October 6, 2007 Overview Einführung 1 Einführung 2 Was sind Vektoren? Vektoren werden geometrisch definiert als Pfeilklassen: Strecken mit gleichem Betrag, gleicher Richtung und Orientierung.
Mathematik I+II Frühlingsemester 2019 Kapitel 8: Lineare Algebra 8.5 Eigenwerte und Eigenvektoren
 Mathematik I+II Frühlingsemester 219 Kapitel 8: Lineare Algebra 8.5 Eigenwerte und Eigenvektoren Prof. Dr. Erich Walter Farkas http://www.math.ethz.ch/ farkas 1 / 46 8. Lineare Algebra: 5. Eigenwerte und
Mathematik I+II Frühlingsemester 219 Kapitel 8: Lineare Algebra 8.5 Eigenwerte und Eigenvektoren Prof. Dr. Erich Walter Farkas http://www.math.ethz.ch/ farkas 1 / 46 8. Lineare Algebra: 5. Eigenwerte und
TC1 Grundlagen der Theoretischen Chemie
 TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Konstantin Falahati (k.falahati@yahoo.com) Jan von Cosel (jvcosel@theochem.uni-frankfurt.de)
TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Konstantin Falahati (k.falahati@yahoo.com) Jan von Cosel (jvcosel@theochem.uni-frankfurt.de)
Prüfung zur Vorlesung Mathematik I/II
 Dr. A. Caspar ETH Zürich, August 08 D-BIOL, D-CHAB, D-HEST Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle 3 4 5 Total Vollständigkeit
Dr. A. Caspar ETH Zürich, August 08 D-BIOL, D-CHAB, D-HEST Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle 3 4 5 Total Vollständigkeit
7 Zwei- und Dreidimensionale Probleme in kartesischen Koordinaten
 7 Zwei- und Dreidimensionale Probleme in kartesischen Koordinaten 7.1 Das Teilchen im -Dimensionalen Kasten Slide 119 Das Teilchen im Kasten Das Teilchen soll sich zwischen = 0 und = L und = 0 und = L
7 Zwei- und Dreidimensionale Probleme in kartesischen Koordinaten 7.1 Das Teilchen im -Dimensionalen Kasten Slide 119 Das Teilchen im Kasten Das Teilchen soll sich zwischen = 0 und = L und = 0 und = L
Einführung in die Schwingungsspektroskopie
 Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
2. Linear Combination of Atomic Orbitals
 . Linear Combination of Atomi Orbitals Molekülorbitale werden mit ilfe des Variationsansatzes erhalten. Beispiel: -atomiges Molekül Atom, ϕ Atom, ϕ amilton-operator: Orthonormierung: ˆ ϕ El. Atom ϕ = =
. Linear Combination of Atomi Orbitals Molekülorbitale werden mit ilfe des Variationsansatzes erhalten. Beispiel: -atomiges Molekül Atom, ϕ Atom, ϕ amilton-operator: Orthonormierung: ˆ ϕ El. Atom ϕ = =
VL 24 VL Homonukleare Moleküle VL Heteronukleare Moleküle VL Molekülschwingungen
 VL 24 VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle VL 24 24.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 17.07.2012 1 Zum Mitnehmen Moleküle: Rotation und
VL 24 VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle VL 24 24.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 17.07.2012 1 Zum Mitnehmen Moleküle: Rotation und
O ist gegenüber C 2. invariant. Allgemein bezeichnet man mit C n. ist symmetrisch gegenüber, das JCl Ion gegenüber C 4
 107 KAPITEL J Symmetrien 1. Einleitung a) Warum Symmetriebetrachtungen? Je komplizierter die Probleme, desto mehr spielen Symmetriebetrachtungen eine Rolle. Die Symmetriebetrachtungen in der Molekülphysik
107 KAPITEL J Symmetrien 1. Einleitung a) Warum Symmetriebetrachtungen? Je komplizierter die Probleme, desto mehr spielen Symmetriebetrachtungen eine Rolle. Die Symmetriebetrachtungen in der Molekülphysik
(2.65 ev), da sich die beiden Elektronen gegenseitig abstossen.
 phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
phys4.026 Page 1 13.8 Das Wasserstoff-Molekül Wie im Fall des H2 + Moleküls führen im H2 Molekül symmetrische Wellenfunktionen zu bindenden Zuständen, wohingegen anti-symmetrische Wellenfunktionen zu anti-bindenden
2.9 Gedämpfter Harmonischer Oszillator
 72 KAPITEL 2. DYNAMIK EINES MASSENPUNKTES 2.9 Gedämpfter Harmonischer Oszillator In diesem Abschnitt wollen wir die Bewegung eines Massenpunktes betrachten, der sich in einer Raumrichtung x in einer Harmonischen
72 KAPITEL 2. DYNAMIK EINES MASSENPUNKTES 2.9 Gedämpfter Harmonischer Oszillator In diesem Abschnitt wollen wir die Bewegung eines Massenpunktes betrachten, der sich in einer Raumrichtung x in einer Harmonischen
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Ballaufgabe. David Reichenbacher. 8. November 2015
 Ballaufgabe David Reichenbacher 8. November 2015 Hausaufgabe aus der Vorlesung Höhere Mathematik für die Fachrichtung Physik Dozent: Dr. Ioannis Anapolitanos Dieses Dokument beinhaltet einen Lösungsvorschlag
Ballaufgabe David Reichenbacher 8. November 2015 Hausaufgabe aus der Vorlesung Höhere Mathematik für die Fachrichtung Physik Dozent: Dr. Ioannis Anapolitanos Dieses Dokument beinhaltet einen Lösungsvorschlag
Übungen zu Physik 2 für Maschinenwesen
 Physikdepartment E13 SS 011 Übungen zu Physik für Maschinenwesen Prof. Dr. Peter Müller-Buschbaum, Dr. Eva M. Herzig, Dr. Volker Körstgens, David Magerl, Markus Schindler, Moritz v. Sivers Vorlesung 1.07.011,
Physikdepartment E13 SS 011 Übungen zu Physik für Maschinenwesen Prof. Dr. Peter Müller-Buschbaum, Dr. Eva M. Herzig, Dr. Volker Körstgens, David Magerl, Markus Schindler, Moritz v. Sivers Vorlesung 1.07.011,
Symmetrie und Struktur
 Symmetrie und Struktur Eine Einführung in die Gruppentheorie Von Prof. Sidney RA. Kettle University of East Anglia, Norwich Aus dem Englischen übersetzt von Dr. Elke Buchholz, Aachen Mit 167 Bildern und
Symmetrie und Struktur Eine Einführung in die Gruppentheorie Von Prof. Sidney RA. Kettle University of East Anglia, Norwich Aus dem Englischen übersetzt von Dr. Elke Buchholz, Aachen Mit 167 Bildern und
3 Koordinatentransformationen
 8 MATHEMATISCHE GRUNDLAGEN DER COMPUTERGEOMETRIE 3 Koordinatentransformationen Für die Darstellung von dreidimensionalen Objekten wird grundsätlich eine Reihe von Transformationen ausgeführt, die von den
8 MATHEMATISCHE GRUNDLAGEN DER COMPUTERGEOMETRIE 3 Koordinatentransformationen Für die Darstellung von dreidimensionalen Objekten wird grundsätlich eine Reihe von Transformationen ausgeführt, die von den
Differenzengleichungen, Z - Transformation
 Differenengleichungen, Z - Transformation In diesem Kapitel wollen wir eine weitere Transformation, die Z-Transformation behandeln. Mit Hilfe der Z-Transformation können lineare Differenengleichungen (DFG
Differenengleichungen, Z - Transformation In diesem Kapitel wollen wir eine weitere Transformation, die Z-Transformation behandeln. Mit Hilfe der Z-Transformation können lineare Differenengleichungen (DFG
Probestudium der Physik 2011/12
 Probestudium der Physik 2011/12 1 Schwingungen und Wellen: Einführung in die mathematischen Grundlagen 1.1 Die Sinus- und die Kosinusfunktion Die Sinusfunktion lässt sich genauso wie die Kosinusfunktion
Probestudium der Physik 2011/12 1 Schwingungen und Wellen: Einführung in die mathematischen Grundlagen 1.1 Die Sinus- und die Kosinusfunktion Die Sinusfunktion lässt sich genauso wie die Kosinusfunktion
Lösungen zu Übungsblatt 1
 Maike Tormählen Übung 1, 11.4.213 Lösungen zu Übungsblatt 1 Aufgabe 1: Large Extra Dimensions & lanck-länge Die Newtonsche Gravitation ist hinreichend, um fundamentale Größen wie die lanck- Länge in diversen
Maike Tormählen Übung 1, 11.4.213 Lösungen zu Übungsblatt 1 Aufgabe 1: Large Extra Dimensions & lanck-länge Die Newtonsche Gravitation ist hinreichend, um fundamentale Größen wie die lanck- Länge in diversen
k m = 2 f (Frequenz) k = 2 m gilt näherungsweise für alle Schwingungen, falls die Auslenkungen klein genug sind (ähnliches Potential ähnliche Kraft)
 8. Der lineare harmonische Oszillator (1D) klass.: E = k m = f (Frequenz) x k = m U = k x = m x m größer -> ω kleiner (deuterierte Moleküle) gilt näherungsweise für alle Schwingungen, falls die Auslenkungen
8. Der lineare harmonische Oszillator (1D) klass.: E = k m = f (Frequenz) x k = m U = k x = m x m größer -> ω kleiner (deuterierte Moleküle) gilt näherungsweise für alle Schwingungen, falls die Auslenkungen
ART 5. Kontravarianter und kovarianter Vierervektor
 ART 5. Kontravarianter und kovarianter Vierervektor Wolfgang Lange. Oktober 205 B. Mathematische Hilfsmittel für die Aufstellung allgemein kovarianter Gleichungen. Über 5. Kontravarianter und kovarianter
ART 5. Kontravarianter und kovarianter Vierervektor Wolfgang Lange. Oktober 205 B. Mathematische Hilfsmittel für die Aufstellung allgemein kovarianter Gleichungen. Über 5. Kontravarianter und kovarianter
TC1 Grundlagen der Theoretischen Chemie
 TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Sarah Römer (roemer@em.uni-frankfurt.de) Simona Scheit (simona.scheit@googlemail.com) Juanma
TC1 Grundlagen der Theoretischen Chemie Irene Burghardt (burghardt@chemie.uni-frankfurt.de) Praktikumsbetreuung: Sarah Römer (roemer@em.uni-frankfurt.de) Simona Scheit (simona.scheit@googlemail.com) Juanma
T2 Quantenmechanik Lösungen 4
 T2 Quantenmechanik Lösungen 4 LMU München, WS 17/18 4.1. Lösungen der Schrödinger-Gleichung Beweisen Sie die folgenden Aussagen. Prof. D. Lüst / Dr. A. Schmi-May version: 06. 11. a) Die Separationskonstante
T2 Quantenmechanik Lösungen 4 LMU München, WS 17/18 4.1. Lösungen der Schrödinger-Gleichung Beweisen Sie die folgenden Aussagen. Prof. D. Lüst / Dr. A. Schmi-May version: 06. 11. a) Die Separationskonstante
11. April Institut für Theoretische Physik. Das Toda-Gitter: periodische Lösungen. Daniel Westerfeld. Motivation. Vorbereitungen.
 Toda- Institut für Theoretische Physik 11. April 2012 Überblick Toda- 1 2 3 Toda- Toda- Betrachte eindimensionale Kette N identischer Teilchen. Wechselwirkung nur zwischen Nachbarn = Bewegungsgleichung:
Toda- Institut für Theoretische Physik 11. April 2012 Überblick Toda- 1 2 3 Toda- Toda- Betrachte eindimensionale Kette N identischer Teilchen. Wechselwirkung nur zwischen Nachbarn = Bewegungsgleichung:
Kapitel 7: Elektronische Spektroskopie
 Kapitel 7: Elektronische Spektroskopie Übersicht: 7.1 Drehimpuls-Kopplungshierarchien in Molekülen: Hundsche Fälle 7.2 Auswahlregeln für rovibronische Übergänge 7.3 Das Franck-Condon-Prinzip 7.4 Zerfall
Kapitel 7: Elektronische Spektroskopie Übersicht: 7.1 Drehimpuls-Kopplungshierarchien in Molekülen: Hundsche Fälle 7.2 Auswahlregeln für rovibronische Übergänge 7.3 Das Franck-Condon-Prinzip 7.4 Zerfall
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm.
 Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
Cluster-Struktur in Kernen. Cluster: Aus mehr als einem Nukleon zusammengesetzten und identifizierbarem Subsystem
 Cluster-Struktur in Kernen Cluster: Aus mehr als einem Nukleon zusammengesetzten und identifizierbarem Subsystem Die Struktur von 11 Li Beim Aufbruch von 11 Li wird nicht nur ein Neutron herausgeschlagen
Cluster-Struktur in Kernen Cluster: Aus mehr als einem Nukleon zusammengesetzten und identifizierbarem Subsystem Die Struktur von 11 Li Beim Aufbruch von 11 Li wird nicht nur ein Neutron herausgeschlagen
