Mittlere Ringe aus Alprenolol und Oxprenolol
|
|
|
- Rudolf Hauer
- vor 7 Jahren
- Abrufe
Transkript
1 Institut für Pharmazeutische Chemie der Technischen Universität Braunschweig, Germany Mittlere Ringe aus Alprenolol und Oxprenolol K. Görlitzer, A. Lorenz Herrn Prof. Dr. Dr. h.c. G. Zinner mit den besten Wünschen zum 80. Geburtstag gewidmet Eingegangen am 22. Dezember 2003, angenommen am 20. Januar 2004 Prof. Dr. K. Görlitzer, Institut für Pharmazeutische Chemie, Beethovenstraße 55, D Braunschweig Pharmazie 58: (2004) Aus den b-blockern 1 wurden die N-Allyl-Derivate 2 dargestellt und diese zu den Estern 5 acetyliert. Durch Ringschlussmetathese (RCM) von 5a und 5b mit Grubbs-Katalysator in Gegenwart von Titantetraisopropylat wurden das 1,5-Benzoxazacycloundecin 6a und das 1,10,5-Benzodioxazacyclododecin 7a isoliert. Alkalische Hydrolyse lieferte die Alkohole 6b und 7b. Medium sized rings from alprenolol and oxprenolol The N-allyl derivatives 2 formed from the b-blockers 1, were acetylated to give the esters 5. The 1,5- benzoxazacycloundecine 6a and the 1,10,5-benzodioxazacyclododecine 7a were isolated by ring closing metathesis (RCM) of 5a and 5b, respectively, using Grubbs catalyst in the presence of titanium tetraisopropanolate. Alkaline hydrolysis yielded the alcohols 6b and 7b. 1. Einleitung Ausgehend vom b-rezeptorenblocker Propranolol gelangte man durch formale Cyclisierung der N-Alkylaminoethanol-Funktion unter Bildung eines Morpholin-Rings zum Antidepressivum Viloxazin (Mallion et al. 1972). Uns interessierten mittlere Ringe, bei denen die Seitenketten von Alprenolol und Oxprenolol entweder über die alkoholische Hydroxyl- oder die NH-Gruppe verknüpft sind. Als mittlere Ringe werden Ringsysteme mit 8 12 Gliedern bezeichnet, die im Gegensatz zu 5 7-gliedrigen sowie großen Ringen relativ schwierig darzustellen sind und eine größere Ringspannung aufweisen (Falbe und Regitz 1991). Durch Fixierung der ursprünglichen Seitenketten zu einem mittleren Ring unter Beibehaltung einer konformativen Rest-Flexibilität ist mit einer Ønderung des Wirkprofils zu rechnen. 2. Untersuchungen, Ergebnisse und Diskussion Eine wichtige Methode zur Synthese mittlerer Ringe ist der Ringschluss durch Olefinmetathese (RCM) (Ivin 1983). Als Edukte kamen die N- und O-Allylierungsprodukte von 1 in Betracht. Durch Erhitzen von Alprenolol (1a) mit Kalium-tert-butylat in Tetrahydrofuran (THF) wurde die Allyl-Gruppe zum mit dem Aromaten konjugierten Propenyl-Derivat 1c isomerisiert. Die Reaktion der b-blocker 1 mit Allylbromid und Natriumhydrid in THF unter Zusatz von N,N-Dimethylpropylenharnstoff (DMPU) führte zu einem Gemisch der N-Mono- und N,O-Diallylierungsprodukte 2 und 4. Die selektive N-Alkylierung zu 2 gelang mit Allylbromid und Kaliumcarbonat in Aceton. Dagegen konnte die O-Allylierung zu 3 nur mittels Kalium-tert-butylat in THF und Auftrennung des erhaltenen N-, O- und N,O-allylierten Gemisches mit sehr schlechter Ausbeute realisiert werden. Bei Alprenolol erfolgte gleichzeitig Isomerisierung der 2-Allyl- zur 2-Propenyl-Funktion. Ausgehend von Oxprenolol konnte auch das N,O-Diallyl-Produkt 4 rein isoliert werden. Die Makrocyclisierung sowohl der N-Allyl-Verbindungen 2 als auch der O-Allyl-Derivate 3 durch RCM mittels Benzyliden-bis(tricyclohexylphosphin)-rutheniumdichlorid (Grubbs Katalysator) in stark verdünnter Dichlormethan- Lösung misslang. Da sich weitere polare funktionelle Gruppen im Edukt günstig für die RCM auswirken (Fürstner und Langemann 1997), wurde die Hydroxyl- Gruppe von 2 mit Acetylchlorid und Triethylamin zum Ester 5 umgesetzt. Nach Zusatz der Lewis-Säure Titan(IV)-tetraisopropylat und Grubbs Katalysator (Fürstner 1999) trat unter Ethen-Eliminierung Cyclisierung von 13a zum benzoanellierten 11-Ring 6a und bei 5b RCM zum 12-Ring 7a ein. Während die Ausbeute beim 11-Ring 6a nur 24 % betrug, ließ sie sich bei der Darstellung des 12- Rings 7a auf 48 % verdoppeln. Die gelungene Cyclisierung zu den mittleren Ringen 6a und 7a wird neben dem jeweiligen Molpeak im Massenspektrum durch die beiden Pharmazie 59 (2004)
2 verbliebenen olefinischen Protonen im 1 H NMR-Spektrum belegt. Die cyclische Doppelbindung weist (E)-Konfiguration auf, wie die große Kopplungskonstante (J 15 Hz) beweist. Dies wird durch die 13 C NMR-Spektren bestätigt, in denen weiterhin nur ein Signalsatz registriert wird. Die alkalische Hydrolyse der Ester 6a und 7a lieferte die Alkohole 6b und 7b. Die RCM von 5c zum benzoanellierten 10-Ring unter gleichen Bedingungen lieferte nur das Edukt. Weiterhin wurde versucht, aus Alprenolol (1a) und Oxprenolol (1b) die zu 5 isomeren N-Acetyl-O-allyl-Derivate darzustellen und mittels RCM einen 10-Ring bzw. 11- Ring zu synthetisieren. Hierzu wurden die b-blocker 1 mit überschüssigem Acetanhydrid in Pyridin umgesetzt und ein Produktgemisch erhalten. Das 1 H NMR-Spektrum zeigt 4 Resonanzsignale für Methyl-Protonen von Acetyl- Gruppen, was auf das Vorliegen von N-Acetyl-, O-Acetylund N,O-Diacetyl-Verbindungen schließen lässt. Durch Reaktion der b-blocker 1 mit äquimolaren Mengen Acetylchlorid und Triethylamin in Diethylether bei 0 C wurden die N-Acetyl-Verbindungen 8 erhalten. Der Plan, aus den N-Acetyl-O-allyl-Derivaten 9 durch RCM mit Grubbs Katalysator und Titan(IV)-tetraisopropylat die mittleren Ringe 10 und 11 zu synthetisieren, ließ sich jedoch nicht umsetzen. Aus den Amiden 8 konnten nach Deprotonierung der Hydroxylfunktion mit Natriumhydrid oder Kalium-tert-butylat und Reaktion mit Allylbromid weder durch Katalysatoren wie 4-Dimethylaminopyridin (DMAP) oder DMPU noch durch Erhitzen die N- Acetyl-O-allyl-Derivate 9 dargestellt werden. Unerwarteterweise führte auch die Acetylierung von 3 mit Acetanhydrid und Pyridin zu einem nicht trennbaren Produktgemisch. 3. Experimenteller Teil 3.1. Allgemeine Angaben Vgl. Görlitzer, Lorenz (2004). Schema Pharmazie 59 (2004) 10
3 Schema (RS)-1-[Allyl(isopropyl)amino]-3-(2-allylphenoxy)propan-2-ol (2a) 1.0 g (4 mmol) Alprenolol wird in 20 ml Aceton gelöst. Nach Zugabe von 1.0 g (7.2 mmol) K 2 CO 3 wird für 1 1 / 2 h unter Rückfluss erhitzt. Den auf RT abgekühlten Reaktionsansatz versetzt man mit 0.38 ml (4.4 mmol) Allylbromid und lässt für 3 h unter Rückfluss rühren. Man filtriert den Niederschlag und zieht das Lösemittel i. Vak. ab. Ausbeute: 1.07 g (92 %). Farbloses Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.98 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.07 (d, J ¼ 6.7 Hz, 3 H, CHCH 3 ), 2.60 (d, J ¼ 4.0 Hz, 2 H, NCH 2 ), 3.03 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.08 (dd, J ¼ 14.3 Hz, J ¼ 7.2 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.21 (dd, J ¼ 14.3 Hz, J ¼ 5.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.40 (d, J ¼ 6.6 Hz, 2 H, ArCH 2 ), 3.97 (d, J ¼ 6.0 Hz, 2 H, OCH 2 ), 4.00 (dt, J ¼ 6.0 Hz, J ¼ 3.9 Hz, 1 H, CHOH), 5.02 (dd, J ¼ 16.8 Hz, J ¼ 1.3 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.05 (dd, J ¼ 10.1 Hz, J ¼ 1.8 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.11 (dd, J ¼ 10.1 Hz, J ¼ 1.3 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.20 (dd, J ¼ 17.1 Hz, J ¼ 1.6 Hz, 1H, NCH 2 CH¼CH 2 ), 5.82 (dddd, J ¼ 17.1 Hz, J ¼ 10.1 Hz, J ¼ 7.1 Hz, J ¼ 5.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 6.00 (ddt, J ¼ 16.8 Hz, J ¼ 10.1 Hz, J ¼ 6.6 Hz, 1 H, ArCH 2 CH¼CH 2 ), 6.85 (dd, J ¼ 7.9 Hz, J ¼ 1.0 Hz, 1H, 6-H), 6.90 (ddd, J ¼ 7.4 Hz, J ¼ 7.4 Hz, J ¼ 1.0 Hz, 1 H, 4-H), 7.13 (dd, J ¼ 7.4 Hz, J ¼ 1.6 Hz, 1 H, 3-H), 7.17 (ddd, J ¼ 7.8 Hz, J ¼ 7.7 Hz, J ¼ 1.6 Hz, 1 H, 5-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (ArCH 2 ), (NCH), (NCH 2 ), (NCH 2 CH¼CH 2 ), (CHOH), (OCH 2 ), (C-6), (ArCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-4), (C-5), (C-2), (C-3), (NCH 2 CH¼CH 2 ), (ArCH 2 CH¼CH 2 ), (C-1). MS (EI): m/z (%) ¼ 289 [M] þ. (1), 112 (100). IR (KBr): ~n (cm 1 ) ¼ 3436 (OH), 1639 (C¼C), 1600 (C¼C). HPLC (1): t s ¼ 4.27 min (RS)-1-[Allyl(isopropyl)amino]-3-{2-(allyloxy)phenoxy}propan-2-ol (2b) 1.0 g (3.8 mmol) Oxprenolol wird in 20 ml wasserfreiem Aceton gelöst. Nach Zugabe von 1.0 g (7.2 mmol) K 2 CO 3 wird für 1 1 / 2 h unter Rückfluss erhitzt. Den auf RT abgekühlten Reaktionsansatz versetzt man mit 0.36 ml (4.2 mmol) Allylbromid und lässt für 3 h unter Rückfluss rühren. Man filtriert den Niederschlag ab und zieht das Lösemittel i. Vak. ab. Ausbeute: 1.1 g (96 %). Farbloses Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.98 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.05 (d, J ¼ 6.7 Hz, 3 H, CHCH 3 ), 2.59 (d, J ¼ 7.4 Hz, 2 H, NCH 2 ), 3.02 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.08 (dd, J ¼ 14.6 Hz, J ¼ 7.3 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.20 (dd, J ¼ 14.6 Hz, J ¼ 5.6 Hz, 1 H, NCH 2 CH¼CH 2 ), 4.01 (dt, J ¼ 7.4 Hz, J ¼ 3.6 Hz, 1 H, CHOH), 4.02 (d, J ¼ 3.6 Hz, 2 H, OCH 2 ), 4.57 (d, J ¼ 5.2 Hz, 2 H, ArOCH 2 CH¼CH 2 ), 5.09 (dd, J ¼ 10.1 Hz, J ¼ 1.4 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.17 (dd, J ¼ 17.2 Hz, J ¼ 1.6 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.26 (dd, J ¼ 10.5 Hz, J ¼ 1.4 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.42 (dd, J ¼ 17.2 Hz, J ¼ 1.6 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.81 (dddd, J ¼ 17.2 Hz, J ¼ 10.1 Hz, J ¼ 7.0 Hz, J ¼ 5.7 Hz, 1 H, NCH 2 CH¼CH 2 ), 6.07 (ddt, J ¼ 17.2 Hz, J ¼ 10.5 Hz, J ¼ 5.3 Hz, 1 H, ArOCH 2 CH¼CH 2 ), (m, 4H, Aromat). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (NCH), (NCH 2 ), (NCH 2 CH¼CH 2 ), (CHOH), (ArOCH 2 CH¼CH 2 ), (OCH 2 ), (C-3), (C-6), (NCH 2 CH¼CH 2 ), (ArOCH 2 CH¼CH 2 ), (C-4), (C-5), (ArOCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-1), (C-2). MS (EI): m/z (%) ¼ 305 [M] þ. (2), 112 (100). IR (KBr): ~n (cm 1 ) ¼ 3426 (OH), 1630 (C¼C), 1592 (C¼C). HPLC (1): t s ¼ 5.89 min. C 18 H 27 NO 3 (305.4) 3.4. (E)-(RS)-1-Isopropylamino-3-[2-(prop-1-en-1-yl)phenoxy]propan-2-ol (1c) 1.0 g (4 mmol) Alprenolol wird in 20 ml trockenem THF gelöst. Zu dieser Lösung gibt man 0.8 g (7.2 mmol) t-buok und rührt für 1 1 / 2 h bei C. Danach werden der Niederschlag filtriert und das Lösemittel i. Vak. eingeengt. Der Rückstand wird mittels FC unter Verwendung von EtOAc/ Et 2 NH (9 : 1) als Eluent gereinigt. Ausbeute: 0.96 g (96 %). Schmp. 79 C (CH 2 Cl 2 /Et 2 O). 1 H NMR (CDCl 3 ): d (ppm) ¼ 1.08 (d, J ¼ 6.3 Hz, 3 H, CHCH 3 ), 1.10 (d, J ¼ 6.3 Hz, 3 H, CHCH 3 ), 1.89 (dd, J ¼ 6.6 Hz, J ¼ 1.7 Hz, 3 H, CH¼CHCH 3 ), 2.76 (dd, J ¼ 12.1 Hz, J ¼ 7.3 Hz, 1 H, NCH 2 ), 2.83 (quint, 1 H, NH), 2.91 (dd, J ¼ 12.1 Hz, J ¼ 3.8 Hz, 1 H, NCH 2 ), (m c, 1 H, NCH), 3.96 (dd, J ¼ 9.3 Hz, J ¼ 4.9 Hz, 1 H, OCH 2 ), 4.01 (dd, J ¼ 9.3 Hz, J ¼ 5.3 Hz, 1 H, OCH 2 ), (m, 1 H, CHOH), 6.22 (dq, J ¼ 15.9 Hz, J ¼ 6.6 Hz, CH¼CHCH 3 ), 6.69 (dq, J ¼ 15.9 Hz, J ¼ 1.7 Hz, 1 H, CH¼CHCH 3 ), 6.84 (dd, J ¼ 8.2 Hz, J ¼ 0.9 Hz, 1 H, 6-H), 6.91 (ddd, J ¼ 8.1 Hz, J ¼ 7.6 Hz, J ¼ 0.7 Hz, 1 H, 4-H), 7.15 (ddd, J ¼ 8.2 Hz, J ¼ 7.6 Hz, J ¼ 1.7 Hz, 1 H, 5-H), 7.39 (dd, J ¼ 7.6 Hz, J ¼ 1.6 Hz, 1 H, 3-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ Pharmazie 59 (2004)
4 (CH¼CHCH 3 ), (CHCH 3 ), (CHCH 3 ), (NCH), (NCH 2 ), (CHOH), (OCH 2 ), (C-6), (C-4), (CH¼CHCH 3 ), (C-3), (CH¼CHCH 3 ), (C-2), (C-5), (C-1) MS (EI): m/z (%) ¼ 249 [M] þ. (4), 72 (100). IR (KBr): ~n (cm 1 ) ¼ 3399 (OH), 3040 (NH), 1600 (C¼C). HPLC (1): t s ¼ 1.97 min. C 15 H 23 NO 2 (249.3) 3.5. (E)-(RS)-1-[Allyl(isopropyl)amino]-3-[2-(prop-1-en-1-yl)- phenoxy]propan-2-ol (2c) 0.48 g (1.9 mmol) 1c werden in 10 ml wasserfreiem Aceton gelöst. Nach Zugabe von g (3.4 mmol) K 2 CO 3 wird für 1 1 / 2 h unter Rückfluss erhitzt. Den auf RT abgekühlten Reaktionsansatz versetzt man mit 0.18 ml (2.1 mmol) Allylbromid und lässt für 1 d unter Rückfluss rühren. Man filtriert den Niederschlag und zieht das Lösemittel i. Vak. ab. Ausbeute: 0.31 g (55 %). Hellgelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.99 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.09 (d, J ¼ 6.7 Hz, 3 H, CHCH 3 ), 1.89 (dd, J ¼ 6.6 Hz, J ¼ 1.7 Hz, 3 H, CH¼CHCH 3 ), 2.62 (dd, J ¼ 11.9 Hz, J ¼ 3.3 Hz, 1 H, NCH 2 ), 2.67 (dd, J ¼ 11.7 Hz, J ¼ 7.5 Hz, 1 H, NCH 2 ), 3.06 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.11 (dd, J ¼ 14.2 Hz, J ¼ 7.2 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.23 (dd, J ¼ 14.2 Hz, J ¼ 5.5 Hz, 1 H, NCH 2 CH¼CH 2 ), (m, 1 H, CHOH), 3.98 (d, J ¼ 6.8 Hz, 2 H, OCH 2 ), 5.12 (dd, J ¼ 10.1 Hz, J ¼ 1.3 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.19 (dd, J ¼ 17.1 Hz, J ¼ 1.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.83 (dddd, J ¼ 17.2 Hz, J ¼ 10.1 Hz, J ¼ 7.2 Hz, J ¼ 5.5 Hz, 1 H, NCH 2 CH=CH 2 ), 6.23 (dq, J ¼ 15.9 Hz, J ¼ 6.6 Hz, 1 H, CH¼CHCH 3 ), 6.71 (dq, J ¼ 15.9 Hz, J ¼ 1.7 Hz, 1 H, CH¼CHCH 3 ), 6.85 (dd, J ¼ 8.2 Hz, J ¼ 0.9 Hz, 1 H, 6-H), 6.90 (ddd, J ¼ 7.6 Hz, J ¼ 7.5 Hz, J ¼ 0.7 Hz, 1 H, 4-H), 7.15 (ddd, J ¼ 8.2 Hz, J ¼ 7.4 Hz, J ¼ 1.7 Hz, 1 H, 5-H), 7.39 (dd, J ¼ 7.6 Hz, J ¼ 1.6 Hz, 1 H, 3- H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CH¼CHCH 3 ), (CHCH 3 ), (NCH), (NCH 2 ), (NCH 2 CH¼CH 2 ), (CHOH), (OCH 2 ), (C-6), (NCH 2 CH¼CH 2 ), (C-4), (CH¼CHCH 3 ), (CH¼CHCH 3 ), (C-3), (C-2), (C-5), NCH 2 CH¼CH 2 ), (C-1). MS (EI): m/z (%) ¼ 289 [M] þ. (1), 112 (100). IR (KBr): ~n (cm 1 ) ¼ 3401 (OH), 1644 (C¼C), 1597 (C¼C). HPLC (1): t s ¼ 4.64 min (RS)-2-(Allyloxy)-3-(2-allylphenoxy)-N-isopropyl-1-propanamin (3a) (2 mmol) Allylbromid dazu getropft.. Nach 3 h Rühren bei RT wird der Eluent gereinigt. Ausbeute: 0.04 g (7 %). Farbloses Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 1.06 (d, J ¼ 6.2 Hz, 3 H, CHCH 3 ), 1.07 (d, J ¼ 6.2 Hz, 3 H, CHCH 3 ), 2.76 (dd, J ¼ 12.1 Hz, J ¼ 3.4 Hz, 1 H, NCH 2 ), 2.82 (sept, J ¼ 6.2 Hz, 1 H, NCH), 2.90 (dd, J ¼ 12.0 Hz, J ¼ 4.0 Hz, 1 H, NCH 2 ), 3.39 (d, J ¼ 6.2 Hz, 2 H, ArCH 2 ), 3.89 (dddd, J ¼ 5.2 Hz, J ¼ 5.0 Hz, J ¼ 4.0 Hz, J ¼ 3.5 Hz, 1 H, CHO), 3.99 (dd, J ¼ 9.7 Hz, J ¼ 5.0 Hz, 1 H, OCH 2 ), 4.07 (dd, J ¼ 9.7 Hz, J ¼ 5.4 Hz, 1 H, OCH 2 ), 4.14 (dd, J ¼ 12.6 Hz, J ¼ 5.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 4.25 (dd, J ¼ 12.6 Hz, J ¼ 5.6 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.01 (dd, J ¼ 16.9 Hz, J ¼ 1.8 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.05 (dd, J ¼ 10.2 Hz, J ¼ 1.8 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.18 (dd, J ¼ 10.4 Hz, J ¼ 1.5 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.30 (dd, J ¼ 17.2 Hz, J ¼ 1.6 Hz, 1 H, OCH 2 CH=CH 2 ), 5.94 (dddd, J ¼ 17.3 Hz, J ¼ 10.5 Hz, J ¼ 5.8 Hz, J ¼ 5.6 Hz, 1 H, OCH 2 CH¼CH 2 ), 6.00 (ddt, J ¼ 16.9 Hz, J ¼ 10.2 Hz, J ¼ 6.6 Hz, 1 H, ArCH 2 CH¼CH 2 ), 6.84 (d, J ¼ 8.1 Hz, 1 H, 6-H), 6.90 (ddd, J ¼ 8.3 Hz, J ¼ 7.4 Hz, J ¼ 0.9 Hz, 1 H, 4-H), 7.14 (ddd, J ¼ 7.6 Hz, J ¼ 1.6 Hz, 1 H, 5-H), 7.18 (dd, J ¼ 7.9 Hz, J ¼ 7.7 Hz, J ¼ 1.6 Hz, 1H, 3-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (ArCH 2 ), (NCH), (NCH 2 ), (OCH 2 CH¼CH 2 ), (OCH 2 ), (CHO), (C-6), (ArCH 2 CH¼CH 2 ), (OCH 2 CH¼CH 2 ), (C-4), (C-5), (C-2), (C-3), (OCH 2 CH¼CH 2 ), (ArCH 2 CH¼CH 2 ), (C-1). MS (EI): m/z (%) ¼ 289 [M] þ. (2), 72 (100). IR (KBr): ~n (cm 1 ) ¼ 1639 (C¼C), 1601 (C¼C). HPLC (1): t s ¼ 2.25 min (RS)-2-(Allyloxy)-3-[2-(allyloxy)phenoxy]-N-isopropyl-1-propanamin (3b) 0.55 g (2.1 mmol) Oxprenolol werden in 10 ml wasserfreiem THF gelöst. Nach Zugabe von 0.42 g (3.8 mmol) t-buok wird für 1 1 / 2 h bei C gerührt. Den auf RT abgekühlten Reaktionsansatz versetzt man mit 0.18 ml (2.1 mmol) Allylbromid und lässt für 1 d bei RT rühren. Man filtriert den Niederschlag ab und zieht das Lösemittel i. Vak. ab. Der Rückstand wird mittels FC unter Verwendung von EtOAc/Et 2 NH (9 : 1) als Eluent gereinigt. Ausbeute: 0.05 g (8 %). Farbloses Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 1.06 (d, J ¼ 6.2 Hz, 6H, CH(CH 3 ) 2 ), 2.79 (dd, J ¼ 12.1 Hz, J ¼ 9.4 Hz, 1 H, NCH 2 ), 2.80 (sept, J ¼ 6.2 Hz, 1 H, NCH), 2.90 (dd, J ¼ 12.1 Hz, J ¼ 4.2 Hz, 1 H, NCH 2 ), (m c, 1 H, CHO), 4.05 (dd, J ¼ 9.9 Hz, J ¼ 5.0 Hz, 1 H, OCH 2 ), 4.11 (dd, J ¼ 9.9 Hz, J ¼ 5.8 Hz, 1 H, OCH 2 ), 4.16 (dd, J ¼ 12.7 Hz, J ¼ 5.8 Hz, 1 H, OCH 2 CH¼CH 2 ), 4.29 (dd, J ¼ 12.7 Hz, J ¼ 5.6 Hz, 1 H, OCH 2 CH¼CH 2 ), 4.56 (d, J ¼ 5.2 Hz, 2 H, ArOCH 2 CH¼CH 2 ), 5.17 (dd, J ¼ 10.4 Hz, J ¼ 1.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.25 (dd, J ¼ 10.6 Hz, J ¼ 1.5 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.29 (dd, J ¼ 17.3 Hz, J ¼ 1.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.41 (dd, J ¼ 17.2 Hz, J ¼ 1.6 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.95 (dddd, J ¼ 17.1 Hz, J ¼ 10.4 Hz, J ¼ 5.7 Hz, J ¼ 4.8 Hz, 1 H, OCH 2 CH¼CH 2 ), 6.06 (ddt, J ¼ 17.2 Hz, J ¼ 10.5 Hz, J ¼ 5.3 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 6.90 (dd, J ¼ 8.6 Hz, J ¼ 2.6 Hz, 1 H, 6-H), 6.91 (ddd, J ¼ 6.2 Hz, J ¼ 5.4 Hz, J ¼ 2.4 Hz, 1 H, 4-H), 6.96 (dd, J ¼ 5.3 Hz, J ¼ 1.7 Hz, 1 H, 3-H), 6.98 (ddd, J ¼ 8.4 Hz, J ¼ 6.3 Hz, J ¼ 1.7 Hz, 1 H, 5-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (NCH), (NCH 2 ), (ArOCH 2 CH¼CH2), (OCH 2 ), (OCH 2 CH¼CH 2 ), (CHO), (C-3), (C-6), (OCH 2 CH¼CH 2 ), (ArOCH 2 CH¼CH 2 ), (C-4), (C-5), (ArOCH 2 CH¼CH 2 ), (OCH 2 CH¼CH 2 ), (C-1), (C-2). MS (EI): m/z (%) ¼ 305 [M] þ. (10), 72 (100). IR (NaCl): ~n (cm 1 ) ¼ 2965 (NH), 1669 (C=C), 1592 (C=C). HPLC (1): t s ¼ 4.55 min. C 18 H 27 NO 3 (305.4) 3.8. (RS)-2-(Allyloxy)-N-isopropyl-3-{2-[1-propenyl]phenoxy}-1-propanamin (3c) (2 mmol) Allylbromid dazu getropft. Nach 3 h Rühren bei RT wird der Eluent gereinigt. Ausbeute: 0.03 g (5 %). Farbloses Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 1.07 (d, J ¼ 5.9 Hz, 3 H, CHCH 3 ), 1.08 (d, J ¼ 5.9 Hz, 3 H, CHCH 3 ), 1.88 (dd, J ¼ 6.6 Hz, J ¼ 1.7 Hz, 3 H, CH¼CHCH 3 ), 2.78 (dd, J ¼ 12.1 Hz, J ¼ 7.4 Hz, 1 H, NCH 2 ), 2.80 (sept, J ¼ 6.2 Hz, 1 H, NCH), 2.92 (dd, J ¼ 12.1 Hz, J ¼ 4.0 Hz, 1 H, NCH 2 ), (m c, 1H, OCH), 4.01 (dd, J ¼ 9.7 Hz, J ¼ 5.1 Hz, 1 H, OCH 2 ), 4.08 (dd, J ¼ 9.7 Hz, J ¼ 5.1 Hz, 1 H, OCH 2 ), 4.15 (dd, J ¼ 12.7 Hz, J ¼ 5.8 Hz, 1H, OCH 2 CH¼CH 2 ), 4.25 (dd, J ¼ 12.7 Hz, J ¼ 5.6 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.19 (dd, J ¼ 10.4 Hz, J ¼ 1.4 Hz, 1 H, CH¼CH 2 ), 5.30 (dd, J ¼ 17.2 Hz, J ¼ 1.6 Hz, 1 H, CH¼CH 2 ), 5.96 (dddd, J ¼ 17.2 Hz, J ¼ 10.4 Hz, J ¼ 5.7 Hz, J ¼ 5.7 Hz, 1 H, CH¼CH 2 ), 6.22 (dq, J ¼ 15.9 Hz, J ¼ 6.6 Hz, 1 H, CH¼CHCH 3 ), 6.71 (dq, J ¼ 15.9 Hz, J ¼ 1.7 Hz, 1 H, CH¼CHCH 3 ), 6.80 (d, J ¼ 8.2 Hz, 1 H, 6-H), 6.90 (t, J ¼ 7.5 Hz, J ¼ 7.3 Hz, 1 H, 4-H), 7.15 (ddd, J ¼ 8.2 Hz, J ¼ 7.4 Hz, J ¼ 1.7 Hz, 1 H, 5-H), 7.39 (dd, J ¼ 7.6 Hz, J ¼ 1.6 Hz, 1 H, 3-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CH¼CHCH 3 ), (CHCH 3 ), (CHCH 3 ), (NCH), (NCH 2 ), (OCH 2 CH¼CH 2 ), (OCH 2 ), (CHO), (C-6), (CH¼CH 2 ), (C-4), (CH¼CHCH 3 ), (C-3, CH¼CHCH 3 ), (C-2), (C-5), (CH¼CH 2 ), (C-1). MS (EI): m/z (%) ¼ 289 [M] þ. (26), 134 (100). IR (KBr): ~n (cm 1 ) ¼ 3041 (NH), 1642 (C¼C), 1597 (C¼C). HPLC (1): t s ¼ 2.67 min (RS)-N-[2-(Allyloxy)-3-(2-allylphenoxy)propyl]-N-isopropylprop-2-en- 1-amin (4a) (2 mmol) Allylbromid dazu getropft. Nach 3 h Rühren bei RT wird der Eluent gereinigt. Ausbeute: 0.05 g (7 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.96 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 0.99 (d, J ¼ 6.7 Hz, 3 H, CHCH 3 ), 2.55 (dd, J ¼ 13.7 Hz, J ¼ 5.4 Hz, 1 H, NCH 2 ), 2.64 (dd, J ¼ 13.7 Hz, J ¼ 7.4 Hz, 1 H, NCH 2 ), 2.97 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.10 (dd, J ¼ 14.4 Hz, J ¼ 6.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.15 (dd, J ¼ 14.4 Hz, J ¼ 6.0 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.41 (d, J ¼ 6.6 Hz, 2 H, ArCH 2 ), 3.75 (dddd, J ¼ 7.2 Hz, J ¼ 6.0 Hz, J ¼ 5.4 Hz, J ¼ 2.3 Hz, 1 H, CHO), 3.99 (dd, J ¼ 9.9 Hz, J ¼ 6.2 Hz, 1 H, OCH 2 ), 4.16 (dd, J ¼ 9.9 Hz, J ¼ 2.5 Hz, 1 H, OCH 2 ), 4.18 (dd, J ¼ 12.9 Hz, J ¼ 2.7 Hz, 1H, OCH 2 CH¼CH 2 ), 4.22 (dd, J ¼ 12.8 Hz, J ¼ 1.4 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.06 (dd, J ¼ 17.0 Hz, J ¼ 1.8 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.08 (dd, J ¼ 10.3 Hz, J ¼ 1.7 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.10 (dd, J ¼ 10.2 Hz, J ¼ 1.7 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.16 (dd, J ¼ 17.2 Hz, J ¼ 1.6 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.17 (dd, J ¼ 10.2 Hz, J ¼ 1.6 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.28 (dd, J ¼ 17.2 Hz, J ¼ 1.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.81 (dddd, J ¼ 17.0 Hz, J ¼ 10.3 Hz, J ¼ 6.5 Hz, J ¼ 6.2 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.92 (dddd, J ¼ 17.5 Hz, J ¼ 10.4 Hz, J ¼ 2.7 Hz, J ¼ 1.1 Hz, 1 H, OCH 2 CH¼CH 2 ), 6.00 (ddt, J ¼ 16.8 Hz, J ¼ 10.0 Hz, J ¼ 6.7 Hz, 1 H, ArCH 2 CH¼CH 2 ), 6.86 (dd, J ¼ 8.1 Hz, J ¼ 0.9 Hz, 1 H, 6-H), 6.89 (ddd, J ¼ 8.1 Hz, J ¼ 7.4 Hz, J ¼ 1.2 Hz, 1 H, 4-H), 7.13 (dd, 766 Pharmazie 59 (2004) 10
5 J ¼ 7.2 Hz, J ¼ 1.6 Hz, 1 H, 3-H), 7.16 (ddd, J ¼ 7.9 Hz, J ¼ 7.7 Hz, J ¼ 1.7 Hz, 1 H, 5-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (ArCH 2 ), (NCH 2 ), (NCH), (NCH 2 CH¼CH 2 ), (OCH 2 CH¼CH 2 ), (OCH 2 ), (CHO), (C-6), (ArCH 2 CH¼CH 2 ), (OCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-4), (C-5), (C-2), (C-3), (OCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (ArCH 2 CH¼CH 2 ), (C-1). MS (EI): m/z (%) ¼ 329 [M] þ. (1), 112 (100). IR (KBr): ~n (cm 1 ) ¼ 1639 (C¼C), 1600 (C¼C). HPLC (1): t s ¼ min. C 21 H 31 NO 2 (329.5) (RS)-N-{2-(Allyloxy)-3-[2-(allyloxy)phenoxy]propyl}-N-isopropylprop-2-en-1-amin (4b) 1.0 g (3.8 mmol) Oxprenolol wird in 20 ml wasserfreiem THF gelöst. Nach Zugabe von 0.29 g (12 mmol) NaH erhitzt man für 5 min bei ca. 70 C und lässt dann auf RT abkühlen. Danach gibt man 0.71 ml (8.3 mmol) Allylbromid und 4 ml DMPU zu dem Reaktionsansatz und erhitzt für 2 h unter Rückfluss. Der Niederschlag wird abfiltriert, die Lösung in ca. 50 ml H 2 O gegossen und anschließend mit Et 2 O ausgeschüttelt. Die vereinigten organischen Phasen werden über Na 2 SO 4 getrocknet und das Lösemittel i. Vak. eingeengt. Der Rückstand wird mittels FC unter Verwendung von EtOAc/Et 2 NH (9 : 1) als Eluent gereinigt. Ausbeute: 0.34 g (26 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.96 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 0.99 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 2.54 (dd, J ¼ 13.7 Hz, J ¼ 5.4 Hz, 1 H, NCH 2 ), 2.62 (dd, J ¼ 13.7 Hz, J ¼ 7.4 Hz, 1 H, NCH 2 ), 2.97 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.10 (dd, J ¼ 14.3 Hz, J ¼ 6.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.15 (dd, J ¼ 14.3 Hz, J ¼ 5.9 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.81 (dddd, J ¼ 7.2 Hz, J ¼ 5.5 Hz, J ¼ 5.4 Hz, J ¼ 5.2 Hz, 1 H, CHO), 3.99 (dd, J ¼ 10.1 Hz, J ¼ 6.7 Hz, 1 H, OCH 2 ), 4.19 (dd, J ¼ 12.8 Hz, J ¼ 5.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 4.24 (dd, J ¼ 10.1 Hz, J ¼ 3.4 Hz, 1 H, OCH 2 ), 4.28 (dd, J ¼ 12.8 Hz, J ¼ 5.2 Hz, 1 H, OCH 2 CH¼CH 2 ), 4.56 (d, J ¼ 5.3 Hz, 2 H, ArOCH 2 CH¼CH 2 ), 5.04 (dd, J ¼ 10.1 Hz, J ¼ 1.8 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.13 (dd, J ¼ 10.4 Hz, J ¼ 1.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.15 (dd, J ¼ 17.2 Hz, J ¼ 1.8 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.24 (dd, J ¼ 10.7 Hz, J ¼ 1.6 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.29 (dd, J ¼ 17.3 Hz, J ¼ 1.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.41 (dd, J ¼ 17.3 Hz, J ¼ 1.6 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.80 (dddd, J ¼ 17.2 Hz, J ¼ 10.1 Hz, J ¼ 6.4 Hz, J ¼ 6.1 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.93 (dddd, J ¼ 17.2 Hz, J ¼ 10.4 Hz, J ¼ 5.6 Hz, J ¼ 5.5 Hz, 1 H, OCH 2 CH¼CH 2 ), 6.06 (ddt, J ¼ 17.2 Hz, J ¼ 10.5 Hz, J ¼ 5.3 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 6.85 (dd, J ¼ 5.7 Hz, J ¼ 2.0 Hz, 1 H, 6-H), 6.88 (ddd, J ¼ 6.0 Hz, J ¼ 5.8 Hz, J ¼ 2.0 Hz, 1 H, 4-H), 6.90 (dd, J ¼ 5.7 Hz, J ¼ 2.7 Hz, 1 H, 3-H), 6.92 (ddd, J ¼ 6.0 Hz, J ¼ 5.8 Hz, J ¼ 2.5 Hz, 1 H, 5-H). 13 CNMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (NCH 2 ), (NCH), (NCH 2 CH¼CH 2 ), (ArOCH 2 CH¼CH 2 ), (OCH 2 ), (OCH 2 CH¼CH 2 ), (CHO), (C-3), (C-6), NCH 2 CH¼CH 2 ), (OCH 2 CH¼CH 2 ), (ArOCH 2 CH¼CH 2 ), (C-4), (C-5), (ArOCH 2 CH¼CH 2 ), (OCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-1), (C-2). MS (EI): m/z (%) ¼ 345 [M] þ. (1), 112 (100). IR (KBr): ~n (cm 1 ) ¼ 1640 (C¼C), 1593 (C¼C). HPLC (1): t s ¼ 7.46 min. C 21 H 31 NO 3 (345.5) (RS)-N-(2-(Allyloxy)-3-{2-[(1E)-1-propenyl]phenoxy}propyl)-N-isopropylprop-2-en-1-amin (4c) (2 mmol) Allylbromid dazu getropft. Nach 3 h Rühren bei RT wird der Eluent gereinigt. Ausbeute: 0.05 g (7 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.97 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 0.99 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.88 (dd, J ¼ 6.6 Hz, J ¼ 1.7 Hz, 3 H, CH¼CHCH 3 ), 2.56 (dd, J ¼ 13.7 Hz, J ¼ 5.5 Hz, 1 H, NCH 2 ), 2.65 (dd, J ¼ 13.7 Hz, J ¼ 7.2 Hz, 1 H, NCH 2 ), 2.98 (sept, J ¼ 6.6 Hz, 1H, NCH), 3.15 (dd, J ¼ 14.3 Hz, J ¼ 4.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.16 (dd, J ¼ 14.3 Hz, J ¼ 4.7 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.77 (dddd, J ¼ 7.2 Hz, J ¼ 6.0 Hz, J ¼ 5.8 Hz, J ¼ 5.5 Hz, 1 H, CHO), 3.98 (dd, J ¼ 10.0 Hz, J ¼ 6.2 Hz, 1 H, OCH 2 ), 4.15 (dd, J ¼ 10.1 Hz, J ¼ 6.5 Hz, 1 H, OCH 2 ), 4.18 (dd, J ¼ 12.6 Hz, J ¼ 1.3 Hz, 1 H, OCH 2 CH¼CH 2 ), 4.20 (dd, J ¼ 12.2 Hz, J ¼ 1.5 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.05 (dd, J ¼ 10.1 Hz, J ¼ 1.8 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.16 (dd, J ¼ 17.3 Hz, J ¼ 1.6 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.17 (dd, J ¼ 10.2 Hz, J ¼ 1.6 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.29 (dd, J ¼ 17.2 Hz, J ¼ 1.7 Hz, 1 H, OCH 2 CH¼CH 2 ), 5.81 (dddd, J ¼ 17.1 Hz, J ¼ 10.2 Hz, J ¼ 4.3 Hz, J ¼ 4.1 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.94 (dddd, J ¼ 17.2 Hz, J ¼ 10.4 Hz, J ¼ 1.2 Hz, J ¼ 0.6 Hz, 1 H, OCH 2 CH¼CH 2 ), 6.22 (dq, J ¼ 15.9 Hz, J ¼ 6.6 Hz, 1 H, CH¼CHCH 3 ), 6.74 (dq, J ¼ 15.9 Hz, J ¼ 1.7 Hz, 1 H, CH¼CHCH 3 ), 6.87 (ddd, J ¼ 8.2 Hz, J ¼ 7.6 Hz, J ¼ 0.7 Hz, 1 H, 4-H), 6.89 (dd, J ¼ 7.4 Hz, J ¼ 0.9 Hz, 1 H, 6-H), 7.13 (ddd, J ¼ 8.0 Hz, J ¼ 7.6 Hz, J ¼ 1.7 Hz, 1 H, 5-H), 7.38 (dd, J ¼ 7.6 Hz, J ¼ 1.6 Hz, 1 H, 3-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CH¼CHCH 3 ), (CH(CH 3 ) 2 ), (NCH 2 ), (NCH), (NCH 2 CH¼CH 2 ), (OCH 2 ), (OCH 2 CH¼CH 2 ), (CHO), (C-6), (OCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-4), (CH¼CHCH 3 ), (CH¼CHCH 3 ), (C-3), (C-2), (C-5), (OCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-1). MS (EI): m/z (%) ¼ 329 [M] þ. (2), 112 (100). IR (KBr): ~n (cm 1 ) ¼ 1643 (C¼C), 1597 (C¼C). HPLC (1): t s ¼ 9.42 min. C 21 H 31 NO 2 (329.5) (RS)-2-[Allyl(isopropyl)amino]-1-[(2-allylphenoxy)methyl]ethylacetat (5a) 0.52 g (1.8 mmol) 2a werden in 10 ml Et 2 O gelöst. Zu dieser Lösung gibt man 0.13 ml (1.8 mmol) Et 3 N und 0.14 ml (2.0 mmol) Acetylchlorid und lässt bei RT 2 1 / 2 hrühren. Anschließend filtriert man den Niederschlag ab und zieht das Lösemittel i. Vak. ab. Ausbeute: 0.55 g (92 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.97 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 0.97 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 2.05 (s, 3 H, COCH 3 ), 2.60 (dd, J ¼ 13.6 Hz, J ¼ 6.0 Hz, 1 H, NCH 2 ), 2.72 (dd, J ¼ 13.6 Hz, J ¼ 7.4 Hz, 1 H, NCH 2 ), 2.98 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.10 (dd, J ¼ 14.4 Hz, J ¼ 6.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.16 (dd, J ¼ 14.4 Hz, J ¼ 6.0 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.38 (d, J ¼ 6.7 Hz, 2 H, ArCH 2 CH¼CH 2 ), 4.08 (dd, J ¼ 10.2 Hz, J ¼ 5.5 Hz, 1 H, OCH 2 ), 4.16 (dd, J ¼ 10.2 Hz, J ¼ 3.4 Hz, 1 H, OCH 2 ), 5.01 (dd, J ¼ 10.0 Hz, J ¼ 1.9 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.02 (dd, J ¼ 16.4 Hz, J ¼ 1.7 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.05 (dd, J ¼ 10.1 Hz, J ¼ 1.8 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.15 (dd, J ¼ 17.1 Hz, J ¼ 1.6 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.21 (dddd, J ¼ 7.3 Hz, J ¼ 5.8 Hz, J ¼ 5.6 Hz, J ¼ 3.4 Hz, 1 H, CHO), 5.80 (dddd, J ¼ 17.1 Hz, J ¼ 10.2 Hz, J ¼ 6.8 Hz, J ¼ 6.1 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.98 (ddt, J ¼ 16.7 Hz, J ¼ 10.0 Hz, J ¼ 6.7 Hz, 1 H, ArCH 2 CH¼CH 2 ), 6.82 (dd, J ¼ 7.7 Hz, J ¼ 0.9 Hz, 1 H, 6-H), 6.90 (ddd, J ¼ 7.4 Hz, J ¼ 7.4 Hz, J ¼ 0.9 Hz, 1 H, 4-H), 7.13 (dd, J ¼ 7.3 Hz, J ¼ 1.6 Hz, 1 H, 3-H), 7.17 (ddd, J ¼ 7.7 Hz, J ¼ 7.3 Hz, J ¼ 1.6 Hz, 1 H, 5-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (COCH 3 ), (ArCH 2 ), (NCH 2 ), (NCH), (NCH 2 CH¼CH 2 ), (OCH 2 ), (CHO), (C- 6), (ArCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-4), (C-5), (C-2), (C-3), (NCH 2 CH¼CH 2 ), (ArCH 2 CH¼CH 2 ), (C-1), (CO). MS (EI): m/z (%) ¼ 331 [M] þ. (2), 112 (100). IR (KBr): ~n (cm 1 ) ¼ 1745 (CO), 1638 (C¼C), 1601 (C¼C). HPLC (1):t s ¼ 7.32 min. C 20 H 29 NO 3 (331.4) (RS)-2-[Allyl(isopropyl)amino]-1-{[2-(allyloxy)phenoxy]methyl}- ethylacetat (5b) 1.1 g (3.6 mmol) 2b werden in 20 ml Et 2 O gelöst. Zu dieser Lösung gibt man 0.27 ml (3.6 mmol) Et 3 N und 0.28 ml (4 mmol) Acetylchlorid und lässt bei RT 2 1 / 2 hrühren. Anschließend filtriert man den Niederschlag ab und zieht das Lösemittel i. Vak. ab. Ausbeute: 0.94 g (75 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.96 (d, J ¼ 6.3 Hz, 3 H, CHCH 3 ), 0.97 (d, J ¼ 6.4 Hz, 3 H, CHCH 3 ), 2.04 (s, 3 H, COCH 3 ), 2.60 (dd, J ¼ 13.6 Hz, J ¼ 6.0 Hz, 1 H, NCH 2 ), 2.72 (dd, J ¼ 13.6 Hz, J ¼ 7.4 Hz, 1 H, NCH 2 ), 2.97 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.10 (dd, J ¼ 14.5 Hz, J ¼ 6.5 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.16 (dd, J ¼ 14.5 Hz, J ¼ 6.0 Hz, 1 H, NCH 2 CH¼CH 2 ), 4.12 (dd, J ¼ 10.6 Hz, J ¼ 5.8 Hz, 1 H, OCH 2 ), 4.25 (dd, J ¼ 10.6 Hz, J ¼ 3.3 Hz, 1 H, OCH 2 ), 4.56 (d, J ¼ 5.2 Hz, 2 H, ArOCH 2 CH¼CH 2 ), 5.04 (dd, J ¼ 10.1 Hz, J ¼ 1.9 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.15 (dd, J ¼ 17.2 Hz, J ¼ 1.8 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.20 (dddd, J ¼ 7.4 Hz, J ¼ 5.9 Hz, J ¼ 5.8 Hz, J ¼ 3.4 Hz, 1 H, CHO), 5.25 (dd, J ¼ 10.5 Hz, J ¼ 1.5 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.42 (dd, J ¼ 17.3 Hz, J ¼ 1.7 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.79 (dddd, J ¼ 17.2 Hz, J ¼ 10.1 Hz, J ¼ 6.4 Hz, J ¼ 6.1 Hz, 1 H, NCH 2 CH¼CH 2 ), 6.06 (ddt, J ¼ 17.2 Hz, J ¼ 10.4 Hz, J ¼ 5.2 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 6.90 (dd, J ¼ 6.3 Hz, J ¼ 1.7 Hz, 1 H, 6-H), 6.91 (ddd, J ¼ 6.3 Hz, J ¼ 5.2 Hz, J ¼ 1.7 Hz, 1 H, 4-H), 6.92 (dd, J ¼ 6.2 Hz, J ¼ 1.9 Hz, 1 H, 3-H), 6.94 (ddd, J ¼ 6.3 Hz, J ¼ 5.1 Hz, J ¼ 2.0 Hz, 1 H, 5-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (COCH 3 ), (NCH 2 ), (NCH), (NCH 2 CH¼CH 2 ), (ArOCH 2 CH¼CH 2 ), (OCH 2 ), (CHO), (C-3), (C-6), (NCH 2 CH¼CH 2 ), (ArOCH 2 CH¼CH 2 ), (C-4), (C-5), (ArOCH 2 CH¼CH 2 ), (NCH 2 CH¼CH 2 ), (C-1), (C-2), (CO). MS (EI): m/z (%) ¼ 347 [M] þ. (26), 112 (100). IR (NaCl): ~n (cm 1 ) ¼ 1731 (CO), 1644 (C¼C), 1592 (C¼C). HPLC (1): t s ¼ 6.88 min. C 20 H 29 NO 4 (347.4) (E)-(RS)-2-[Allyl(isopropyl)amino]-1-[2-(prop-1-en-1-yl)phenoxy]- methylethylacetat (5c) 0.38 g (1.3 mmol) 2c werden in 10 ml Et 2 O gelöst. Zu dieser Lösung gibt man 0.1 ml (1.3 mmol) Et 3 N und 0.1 ml (1.4 mmol) Acetylchlorid und lässt bei RT 1 d rühren. Anschließend filtriert man den Niederschlag ab Pharmazie 59 (2004)
6 und zieht das Lösemittel i. Vak. ab. Ausbeute: 0.3 g (68 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.97 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 0.98 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.89 (dd, J ¼ 6.6 Hz, J ¼ 1.7 Hz, 3 H, CH¼CHCH 3 ), 2.06 (s, 3 H, COCH 3 ), 2.62 (dd, J ¼ 13.6 Hz, J ¼ 6.1 Hz, 1 H, NCH 2 ), 2.72 (dd, J ¼ 13.6 Hz, J ¼ 7.2 Hz, 1 H, NCH 2 ), 2.98 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.10 (dd, J ¼ 14.4 Hz, J ¼ 6.4 Hz, 1 H, NCH 2 CH¼CH 2 ), 3.16 (dd, J ¼ 14.4 Hz, J ¼ 6.0 Hz, 1 H, NCH 2 CH¼CH 2 ), 4.10 (dd, J ¼ 10.2 Hz, J ¼ 5.7 Hz, 1 H, OCH 2 ), 4.18 (dd, J ¼ 10.2 Hz, J ¼ 3.5 Hz, 1 H, OCH 2 ), 5.05 (dd, J ¼ 10.1 Hz, J ¼ 1.9 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.16 (dd, J ¼ 17.2 Hz, J ¼ 1.8 Hz, 1 H, NCH 2 CH¼CH 2 ), 5.23 (dddd, J ¼ 7.1 Hz, J ¼ 6.0 Hz, J ¼ 5.6 Hz, J ¼ 3.5 Hz, 1 H, CHO), 5.79 (dddd, J ¼ 17.1 Hz, J ¼ 10.1 Hz, J ¼ 6.5 Hz, J ¼ 6.2 Hz, 1 H, NCH 2 CH¼CH 2 ), 6.23 (dq, J ¼ 15.9 Hz, J ¼ 6.6 Hz, 1 H, CH¼CHCH 3 ), 6.68 (dq, J ¼ 15.9 Hz, J ¼ 1.7 Hz, 1 H, CH¼CHCH 3 ), 6.83 (dd, J ¼ 8.2 Hz, J ¼ 0.9 Hz, 1 H, 6-H), 6.89 (ddd, J ¼ 7.5 Hz, J ¼ 7.5 Hz, J ¼ 0.5 Hz, 1 H, 4-H), 7.14 (ddd, J ¼ 8.2 Hz, J ¼ 7.4 Hz, J ¼ 1.7 Hz, 1 H, 5-H), 7.38 (dd, J ¼ 7.7 Hz, J ¼ 1.7 Hz, 1 H, 3-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (CH¼CHCH 3 ), (COCH 3 ), (NCH 2 ), (NCH), (NCH 2 CH¼CH 2 ), (OCH 2 ), (CHO), (C-6), (NCH 2 CH¼CH 2 ), (C- 4), (CH¼CHCH 3 ), (CH¼CHCH 3 ), (C-3), (C-2), (C-5), (NCH 2 CH¼CH 2 ), (C-1), (CO). MS (EI): m/z (%) ¼ 331 [M þ. (4), 112 (100). IR (NaCl): ~n (cm 1 ) ¼ 1741 (CO), 1642 (C¼C), 1597 (C¼C). HPLC (1): t s ¼ 7.06 min. C 20 H 29 NO 3 (331.4) (7E)-5-Isopropyl-2,3,4,5,6,9-hexahydro-1,5-benzoxazacycloundecin- 3-ylacetat (6a) 0.55 g (1.7 mmol) 5a werden in 1.02 l wasserfreiem CH 2 Cl 2 gelöst. Nach Zugabe von 0.30 ml (1.0 mmol) Titan(IV)-tetraisopropylat unter N 2 wird 1 h unter Rückfluss erhitzt. Dann werden 100 mg (0.1 mmol) Benzylidenbis(tricyclohexylphosphin)dichlorruthenium (Grubbs Katalysator), gelöst in 5mlCH 2 Cl 2, zugetropft und weiter unter Rückfluss und N 2 erhitzt. Nach 3 d wird der Katalysator abgesaugt und das Lösemittel i. Vak. eingeengt. Der Rückstand wird mittels FC unter Verwendung von n-hexan/etoac (3 : 1) als Eluent gereinigt. Ausbeute: 0.12 g (24 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.98 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.04 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 2.1 (s, 3 H, COCH 3 ), 2.55 (dd, J ¼ 14.2 Hz, J ¼ 4.8 Hz, 1 H, 4-H), 2.81 (dd, J ¼ 14.4 Hz, J ¼ 4.7 Hz, 1 H, 6-H), 2.92 (sept., J ¼ 6.6 Hz, 1 H, NCH), 2.69 (dd, J ¼ 14.1 Hz, J ¼ 7.8 Hz, 1 H, 4-H), 3.09 (dd, J ¼ 14.4 Hz, J ¼ 10.2 Hz, 1 H, 6-H), 3.31 (dd, J ¼ 17.1 Hz, J ¼ 4.4 Hz, 1 H, 9-H), 3.50 (dd, J ¼ 17.1 Hz, J ¼ 5.4 Hz, 1 H, 9-H), 4.08 (dd, J ¼ 10.0 Hz, J ¼ 2.3 Hz, 1 H, 2-H), 4.19 (dd, J ¼ 10.0 Hz, J ¼ 4.8 Hz, 1 H, 2-H), 4.87 (dddd, J ¼ 7.5 Hz, J ¼ 5 Hz, J ¼ 4.8 Hz, J ¼ 2.4 Hz, 1 H, 3-H), 5.13 (ddd, J ¼ 14.5 Hz, J ¼ 5.0 Hz, J ¼ 4.7 Hz, 1 H, 8-H), 5.70 (ddd, J ¼ 15.7 Hz, J ¼ 9.7 Hz, J ¼ 4.8 Hz, 1 H, 7-H), 6.92 (dd, J ¼ 7.6 Hz, J ¼ 1.1 Hz, 1 H, 11- H), 6.93 (d, J ¼ 7.8 Hz, 1 H, 13-H), 7.11 (dd, J ¼ 7.6 Hz, J ¼ 1.6 Hz, 1 H, 10-H), 7.21 (ddd, J ¼ 7.8 Hz, J ¼ 7.8 Hz, J ¼ 1.7 Hz, 1 H, 12-H). 13 CNMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (COCH 3 ), (C-9), (C-4), (C-6), (NCH), (C-2), (C- 3), (C-13), (C-11), (C-12), (C-9a), (C- 8), (C-10), (C-7), (C-13a), (CO). MS (EI): m/z (%) ¼ 303 [M] þ. (11), 146 (100). IR (KBr): ~n (cm 1 ) ¼ 1738 (C¼O), 1600 (C¼C). HPLC (1): t s ¼ 6.68 min. C 18 H 25 NO 3 (303.4) (7E)-5-Isopropyl-2,3,4,5,6,9-hexahydro-1,10,5-benzodioxazacyclododecin-3-ylacetat (7a) 0.5 g (1.4 mmol) 5b werden in 880 ml wasserfreiem CH 2 Cl 2 gelöst. Nach Zugabe von 0.13 ml (0.42 mmol) Titan(IV)-tetraisopropylat unter N 2 wird 1 h unter Rückfluss erhitzt. Dann werden 42 mg (0.042 mmol) Benzylidenbis(tricyclohexylphosphin)dichlorruthenium (Grubbs Katalysator), gelöst in 5mlCH 2 Cl 2, zugetropft und weiter unter Rückfluss und N 2 erhitzt. Nach 3 d wird der Katalysator abgesaugt und das Lösemittel i. Vak. eingeengt. Der Rückstand wird mittels FC unter Verwendung von n-hexan / EtOAc (3 : 1) als Eluent gereinigt. Ausbeute: 0.22 g (48 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 0.99 (d, J ¼ 6.9 Hz, 3H, CHCH 3 ), 1.01 (d, J ¼ 6.9 Hz, 3 H, CHCH 3 ), 2.08 (s, 3 H, COCH 3 ), 2.56 (dd, J ¼ 13.3 Hz, J ¼ 4.6 Hz, 1 H, 6- H), 2.66 (dd, J ¼ 12.5 Hz, J ¼ 8.5 Hz, 1 H, 4-H), 2.96 (sept, 1 H, NCH), 3.04 (dd, J ¼ 12.5 Hz, J ¼ 5.1 Hz, 1 H, 4-H), 3.17 (dd, J ¼ 13.3 Hz, J ¼ 9.4 Hz, 1 H, 6-H), 4.10 (dd, J ¼ 10.0 Hz, J ¼ 2.5 Hz, 1 H, 2-H), 4.15 (dd, J ¼ 10.0 Hz, J ¼ 3.6 Hz, 1 H, 2-H), 4.17 (dd, J ¼ 12.2 Hz, J ¼ 6.2 Hz, 1 H, 9-H), 4.65 (dd, J ¼ 12.1 Hz, J ¼ 6.5 Hz, 1 H, 9-H), 5.04 (dddd, J ¼ 8.3 Hz, J ¼ 5.6 Hz, J ¼ 3.8 Hz, J ¼ 2.6 Hz, 1 H, 3-H), 5.53 (ddd, J ¼ 15.3 Hz, J ¼ 10.0 Hz, J ¼ 5.2 Hz, 1 H, 7-H), 5.96 (ddd, J ¼ 15.2 Hz, J ¼ 7.3 Hz, J ¼ 6.9 Hz, 1 H, 8-H), 6.93 (dd, J ¼ 7.5 Hz, J ¼ 1.6 Hz, 1 H, 14-H), 6.93 (ddd, J ¼ 8.2 Hz, J ¼ 7.8 Hz, J ¼ 1.5 Hz, 1 H, 12-H), 7.05 (ddd, J ¼ 8.2 Hz, J ¼ 7.2 Hz, J ¼ 1.7 Hz, 1 H, 13-H), 7.10 (dd, J ¼ 7.8 Hz, J ¼ 1.6 Hz, 1 H, 11-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (COCH 3 ), (C-4), (C-6), (NCH), (C-2), (C-3), (C-9), (C-12), (C-13), (C-14), (C-11), (C-7), (C-8), (C-14a), (C-10a), (CO). MS (EI): m/z (%) ¼ 319[M] þ. (6), 110 (100). IR (KBr): ~n (cm 1 ) ¼ 1734 (C¼O), 1593 (C¼C). HPLC (1): t s ¼ 6.22 min. C 18 H 25 NO 4 (319.4) (7E)-5-Isopropyl-2,3,4,5,6,9-hexahydro-1,5-benzoxazacycloundecin- 3-ol (6b) 0.12 g (0.4 mmol) 6a werden zu einer Lösung von 0.03 g (0.5 mmol) KOH in 0.5 ml H 2 O und 5 ml EtOH (96 %) gegeben. Man lässt 2 h bei Raumtemperatur stehen. Danach neutralisiert man den Reaktionsansatz mit verd. HCl und extrahiert mit 3 15 ml CHCl 3, trocknet über Na 2 SO 4 und zieht das Lösemittel i. Vak. ab. Ausbeute: 0.08 g (80 %). Gelbes Úl. 1 HNMR (CDCl 3 ): d (ppm) ¼ 1.12 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.16 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 2.53 (dd, J ¼ 14.2 Hz, J ¼ 4.9 Hz, 1 H, 4-H), 2.92 (dd, J ¼ 14.3 Hz, J ¼ 4.7 Hz, 1 H, 6-H), 3.09 (sept, J ¼ 6.6 Hz, 1 H, NCH), 3.17 (dd, J ¼ 14.2 Hz, J ¼ 7.1 Hz, 1 H, 4-H), 3.26 (dd, J ¼ 14.1 Hz, J ¼ 9.7 Hz, 1 H, 6-H), (m, 1 H, 9-H), (m, 1 H, 9-H), 3.88 (dddd, J ¼ 7.2 Hz, J ¼ 5.5 Hz, J ¼ 4.8 Hz, J ¼ 2.4 Hz, 1 H, 3-H), 4.08 (dd, J ¼ 10.0 Hz, J ¼ 2.3 Hz, 1 H, 2-H), 4.21 (dd, J ¼ 10.1 Hz, J ¼ 4.7 Hz, 1 H, 2-H), (m, 1 H, 8-H), (m, 1 H, 7-H), 6.86 (ddd, J ¼ 8.2 Hz, J ¼ 7.4 Hz, J ¼ 0.9 Hz, 1 H, 11-H), 6.94 (dd, J ¼ 7.4 Hz, J ¼ 1.0 Hz, 1 H, 13-H), 7.11 (dd, J ¼ 7.4 Hz, J ¼ 1.7 Hz, 1 H, 10-H), 7.20 (ddd, J ¼ 7.8 Hz, J ¼ 7.6 Hz, J ¼ 1.8 Hz, 1 H, 12-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (C-9), (C-4), (NCH), (C-6), (C-2), (C-3), (C-13), (C-11), (C-12), (C-9a), (C-8), (C-10), (C-7), (C-13a). MS (EI): m/z (%) ¼ 261 [M] þ. (5), 217 (100). IR (NaCl): ~n (cm 1 ) ¼ 3329 (OH), 1600 (C¼C). HPLC (1): t s ¼ 4.73 min. C 16 H 23 NO 2 (261.4) (7E)-5-Isopropyl-2,3,4,5,6,9-hexahydro-1,10,5-benzodioxazacyclododecin-3-ol (7b) 0.16 g (0.5 mmol) 7a werden zu einer Lösung von 0.03 g (0.5 mmol) KOH in 0.5 ml H 2 O und 5 ml EtOH (96 %) gegeben. Man lässt 2 h bei RT stehen. Danach neutralisiert man den Reaktionsansatz mit verd. HCl und extrahiert mit 3 15 ml CHCl 3, trocknet über Na 2 SO 4 und zieht das Lösemittel i. Vak. ab. Ausbeute: 0.11 g (77 %). Gelbes Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 1.02 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.05 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 2.74 (dd, J ¼ 13.5 Hz, J ¼ 3.5 Hz, 1 H, 4-H), 2.89 (dd, J ¼ 13.3 Hz, J ¼ 7.4 Hz, 1 H, 4-H), 2.98 (sept, J ¼ 6.8 Hz, 1 H, NCH), 3.01 (dd, J ¼ 12.4 Hz, J ¼ 1.8 Hz, 1 H, 6-H), 3.05 (dd, J ¼ 12.4 Hz, J ¼ 6.7 Hz, 1 H, 6-H), 3.81 (dddd, J ¼ 7.3 Hz, J ¼ 3.8 Hz, J ¼ 3.4 Hz, J ¼ 1.8 Hz, 1 H, 3-H), 3.97 (dd, J ¼ 10.2 Hz, J ¼ 1.8 Hz, 1 H, 2-H), 4.31 (dd, J ¼ 10.1 Hz, J ¼ 3.7 Hz, 1 H, 2-H), 4.32 (dd, J ¼ 12.2 Hz, J ¼ 6.8 Hz, 1 H, 9-H), 4.55 (dd, J ¼ 12.2 Hz, J ¼ 6.9 Hz, 1 H, 9-H), 5.61 (ddd, J ¼ 15.3 Hz, J ¼ 6.7 Hz, J ¼ 1.8 Hz, 1 H, 7-H), 5.91 (ddd, J ¼ 15.4 Hz, J ¼ 7.0 Hz, J ¼ 6.9 Hz, 1 H, 8-H), 6.87 (dd, J ¼ 6.7 Hz, J ¼ 2.3 Hz, 1 H, 14-H), 6.95 (ddd, J ¼ 8.3 Hz, J ¼ 7.5 Hz, J ¼ 2.2 Hz, 1 H, 12-H), 7.04 (ddd, J ¼ 8.2 Hz, J ¼ 6.7 Hz, J ¼ 1.7 Hz, 1 H, 13-H), 7.09 (dd, J ¼ 7.6 Hz, J ¼ 1.6 Hz, 1 H, 11-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (C-4), (C-6), (NCH), (C-3), (C-2), (C-9), (C-12), (C-13), (C-14), (C-11), (C-7), (C-8), (C-14a), (C- 10a). MS (EI): m/z (%) ¼ 277 [M] þ. (3), 110 (100). IR (KBr): ~n (cm 1 ) ¼ 3400 (OH), 1594 (C¼C). HPLC (1): t s ¼ 4.49 min. C 16 H 23 NO 3 (277.4) (RS)-N-[3-(2-Allylphenoxy)-2-hydroxypropyl]-N-isopropylacetamid (8a) 1.0 g (4 mmol) Alprenolol wird in 20 ml Et 2 O gelöst. Die Lösung wird in Eiswasser auf 0 10 C gekühlt. Nach Zugabe von 0.30 ml (4 mmol) Et 3 N und 0.28 ml (4 mmol) Acetylchlorid lässt man den Reaktionsansatz unter Eiswasserkühlung für 20 min stehen. Danach filtriert man den Niederschlag ab und zieht das Lösemittel i. Vak. ab. Ausbeute: 0.92 g (79 %). Farbloses Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 1.21 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.28 (d, J ¼ 6.7 Hz, 3 H, CHCH 3 ), 2.20 (s, 3 H, COCH 3 ), 3.39 (d, J ¼ 6.3 Hz, 2 H, ArCH 2 CH¼CH 2 ), 3.45 (dd, J ¼ 14.7 Hz, J ¼ 1.6 Hz, 1 H, NCH 2 ), 3.65 (dd, J ¼ 14.7 Hz, J ¼ 8.2 Hz, 1 H, NCH 2 ), 3.84 (sept, J ¼ 6.6 Hz, 1 H, NCH), 4.05 (d, J ¼ 6.1 Hz, 2 H, OCH 2 ), 4.06 (ddt, J ¼ 8.4 Hz, J ¼ 6.2 Hz, J ¼ 1.6 Hz, 1 H, CHOH), 5.01 (dd, J ¼ 16.8 Hz, J ¼ 1.7 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.04 (dd, J ¼ 10.0 Hz, J ¼ 1.7 Hz, 1 H, ArCH 2 CH¼CH 2 ), 5.52 (breiter Peak, 1 H, OH), 5.99 (ddt, J ¼ 16.6 Hz, J ¼ 10.3 Hz, J ¼ 6.3 Hz, 1 H, ArCH 2 CH¼CH 2 ), 6.88 (dd, J ¼ 8.1 Hz, J ¼ 0.9 Hz, 1 H, 6-H), 6.92 (ddd, J ¼ 7.4 Hz, J ¼ 7.4 Hz, J ¼ 0.9 Hz, 1 H, 4-H), 7.14 (dd, J ¼ 7.4 Hz, J ¼ 1.6 Hz, 1 H, 3-H), 7.20 (ddd, J ¼ 7.9 Hz, J ¼ 7.7 Hz, J ¼ 1.7 Hz, 1 H, 5-H). 13 C NMR (CDCl 3 ): d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (COCH 3 ), (ArCH 2 ), (NCH 2 ), (NCH), (OCH 2 ), (CHOH), (C-6), (ArCH 2 CH¼CH 2 ), (C-4), (C-5), (C-2), Pharmazie 59 (2004) 10
7 (C-3), (ArCH 2 CH¼CH 2 ), (C-1), (CO). MS (EI): m/z (%) ¼ 291 [M] þ. (2), 158 (100). IR (KBr): ~n (cm 1 ) ¼ 3450 (OH), 1617 (NCO), 1597 (C¼C). HPLC (1): t s ¼ 3.90 min. C 17 H 25 NO 3 (291.4) (RS)-N-{3-[2-(Allyloxy)phenoxy]-2-hydroxypropyl}-N-isopropylacetamid (8b) 1.0 g (3.8 mmol) Oxprenolol wird in 20 ml Et 2 O gelöst. Die Lösung wird in Eiswasser auf 0 10 C gekühlt. Nach Zugabe von 0.29 ml (3.8 mmol) Et 3 N und 0.27 ml (3.8 mmol) Acetylchlorid lässt man den Reaktionsansatz unter Eiswasserkühlung für 20 min stehen. Danach filtriert man den Niederschlag ab und zieht das Lösemittel i. Vak. ab. Ausbeute: 1.0 g (86 %). Farbloses Úl. 1 H NMR (CDCl 3 ): d (ppm) ¼ 1.20 (d, J ¼ 6.6 Hz, 3 H, CHCH 3 ), 1.30 (d, J ¼ 6.7 Hz, 3 H, CHCH 3 ), 2.19 (s, 3 H, COCH 3 ), 3.55 (dd, J ¼ 14.7 Hz, J ¼ 3.0 Hz, 1 H, NCH 2 ), 3.60 (dd, J ¼ 14.7 Hz, J ¼ 6.8 Hz, 1 H, NCH 2 ), 3.81 (dd, J ¼ 8.9 Hz, J ¼ 3.6 Hz, 1 H, OCH 2 ), 4.03 (sept, J ¼ 6.6 Hz, 1 H, NCH), 4.04 (dddd, J ¼ 6.8 Hz, J ¼ 4.5 Hz, J ¼ 3.8 Hz, J ¼ 2.8 Hz, 1 H, CHOH), 4.13 (dd, J ¼ 9.1 Hz, J ¼ 4.4 Hz, 1 H, OCH 2 ), 4.55 (d, J ¼ 5.6 Hz, ArOCH 2 CH¼CH 2 ), 5.26 (dd, J ¼ 10.5 Hz, J ¼ 1.4 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.40 (dd, J ¼ 17.2 Hz, J ¼ 1.6 Hz, 1 H, ArOCH 2 CH¼CH 2 ), 5.60 (s, br., 1 H, OH), 6.06 (ddt, J ¼ 17.2 Hz, J ¼ 10.7 Hz, J ¼ 5.5 Hz, 1 H, ArOCH 2 CH=CH 2 ), 6.87 (dd, J ¼ 6.9 Hz, J ¼ 2.4 Hz, 1 H, 6-H), 6.88 (ddd, J ¼ 8.3 Hz, J ¼ 5.6 Hz, J ¼ 2.7 Hz, 1 H, 4-H), 6.91 (dd, J ¼ 5.6 Hz, J ¼ 1.8 Hz, 1 H, 3-H), 6.94 (ddd, J ¼ 8.5 Hz, J ¼ 6.9 Hz, J ¼ 1.8 Hz, 1 H, 5-H). 13 C NMR (CDCl 3 ) þ DEPT: d (ppm) ¼ (CHCH 3 ), (CHCH 3 ), (COCH 3 ), (NCH 2 ), (NCH), (ArOCH 2 CH¼CH 2 ), (OCH 2 ), (CHOH), (C-3), (C-6), (ArOCH 2 CH¼CH 2 ), (C-4), (C-5), (ArOCH 2 CH¼CH 2 ), (C-2, C-1), (COCH 3 ). MS (EI): m/z (%) ¼ 307 [M] þ. (2), 158 (100). IR (KBr): ~n ¼ 3350 (OH), 1615 (CO), 1607 (C¼C). HPLC (1): t s ¼ 4.04 min. C 17 H 25 NO 4 (307.4) Für die großzügige kostenlose Ûberlassung der Arzneistoffe danken wir AstraZeneca (Alprenololhydrochlorid) und Novartis Pharma (Oxprenololhydrochlorid). Literatur Falbe J, Regitz M (1991) Römpp Chemielexikon, Thieme-Verlag, Stuttgart, Fürstner A, Langemann K (1997) Macrocycles by ring-closing metathesis. Synthesis: Fürstner A (1999) Venturing into catalysis based natural product synthesis. Synlett: Görlitzer K, Lorenz A (2004) Zur bromometrischen Bestimmung von Alprenolol und Oxprenolol. Pharmazie 59: Ivin KJ (1983) Olefin metathesis. Academic Press, London. Mallion KB, Todd AH, Turner RW, Bainbridge JG, Greenwood DT, Medinaveitia J, Somerville AR, Whittle BA (1972) 2-(2-Ethoxyphenoxymethyl)tetrahydro-1,4-oxazine hydrochloride, a potential psychotropic agent. Nature 238: Pharmazie 59 (2004)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten C H 3 H 33. Br 22 25
 2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
5 Chemisch-experimenteller Teil
 5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
2017 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid
 217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
Darstellung von Chelidamsäure (gekürzte Version)
 CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
4 Experimenteller Teil
 4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
Organisch-chemisches Praktikum Wintersemester 2005/06. 1-Phenyl-propan-1-ol. Stephan Steinmann
 Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
5001 Nitrierung von Phenol zu 2-Nitrophenol und 4-Nitrophenol
 00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von Acetessigsäureethylester
 Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
4002 Synthese von Benzil aus Benzoin
 4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
Experimenteller Teil
 II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid
 4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid
 1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
3002 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure
 32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b
 3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
4010 Synthese von p-methoxyacetophenon aus Anisol
 4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
3021 Oxidation von Anthracen zu Anthrachinon
 xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
1024 Eliminierung von Wasser aus 4-Hydroxy-4-methyl-2- pentanon
 0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren Brombutanen
 1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NO 2 Rühren mit Magnetrührer, Extrahieren, Ausschütteln, Abrotieren, Umkristallisieren, Abfiltrieren,
 1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
Mustervorschrift 2.3.1
 Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
3012 Synthese von Adamantylidenadamantan aus Adamantanon
 Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
5009 Synthese von Kupferphthalocyanin
 P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13
 Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff -
 hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
Chloro(triphenylphosphin)gold(I)
 raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013
 Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
4009 Synthese von Adipinsäure aus Cyclohexen
 4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
6011 Hippursäure aus Glycin und Benzoylchlorid
 P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
3011 Synthese von erythro-9,10-dihydroxystearinsäure aus Ölsäure
 311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
- 2 - Das folgende retrosynthetische Schema erwies sich als geeignet, die gewünschte Zielverbindung darzustellen. TEG. Abbildung 1
 - 1 - Protokoll ynthese von 4(3)-[4-(triethylenglykolmethylether)-3,5-dimetylphenyl]- cyclohepta-2,4,6-trienyl-[n-(triethylenglykolmethylether)-n- (methyl)-anilin] N rganisch-chemisches Fortgeschrittenenpraktikum
- 1 - Protokoll ynthese von 4(3)-[4-(triethylenglykolmethylether)-3,5-dimetylphenyl]- cyclohepta-2,4,6-trienyl-[n-(triethylenglykolmethylether)-n- (methyl)-anilin] N rganisch-chemisches Fortgeschrittenenpraktikum
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol
 3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
Aufgabe 1: (18 Punkte)
 Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
Benzol-d. Illumina-Chemie.de - Artikel
 Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
3 Experimenteller Teil
 Experimenteller Teil: Allgemeines 116 3 Experimenteller Teil 3.1 Allgemeines 3.1.1 Präparative Methoden 3.1.1.1 Arbeiten unter Schutzgas Alle metallorganischen Umsetzungen und sämtliche Reaktionen unter
Experimenteller Teil: Allgemeines 116 3 Experimenteller Teil 3.1 Allgemeines 3.1.1 Präparative Methoden 3.1.1.1 Arbeiten unter Schutzgas Alle metallorganischen Umsetzungen und sämtliche Reaktionen unter
Synthese 1 Herstellung von. Cyclohex-3-en-1,1-diyldimethanol
 Organisch-Chemisches Praktikum 1 (OCP 1) HS 10/11 Assistenten: Daniel Fankhauser, Lorenz Urner Synthese 1 Herstellung von Cyclohex-3-en-1,1-diyldimethanol Bastian Vögeli Versuch: 21./22. Oktober 2010 1
Organisch-Chemisches Praktikum 1 (OCP 1) HS 10/11 Assistenten: Daniel Fankhauser, Lorenz Urner Synthese 1 Herstellung von Cyclohex-3-en-1,1-diyldimethanol Bastian Vögeli Versuch: 21./22. Oktober 2010 1
Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)-
 Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid
 NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
Erste Klausur zur Vorlesung Grundlagen der Organischen Chemie
 Prof. Dr. Jens Christoffers 14. Februar 2011 Universität Oldenburg Erste Klausur zur Vorlesung Grundlagen der Organischen Chemie für Studierende der Chemie (Fach-Bachelor und Zwei-Fächer-Bachelor, Wert:
Prof. Dr. Jens Christoffers 14. Februar 2011 Universität Oldenburg Erste Klausur zur Vorlesung Grundlagen der Organischen Chemie für Studierende der Chemie (Fach-Bachelor und Zwei-Fächer-Bachelor, Wert:
2023 Reduktion von D-(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b).
 23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
Versuchsprotokoll. Versuch 2.5 B: Brom-Addition an Cholesterol und Brom-Eliminierung N - NaI
 Matrikelnr.: 242232 Organischchemisches Grundpraktikum Versuchsprotokoll Versuch 2.5 B: omaddition an Cholesterol und omeliminierung Reaktionsgleichung: 2 3 3 O ai O 386,7 g/mol 606,6 g/mol C 3 COO Literatur:
Matrikelnr.: 242232 Organischchemisches Grundpraktikum Versuchsprotokoll Versuch 2.5 B: omaddition an Cholesterol und omeliminierung Reaktionsgleichung: 2 3 3 O ai O 386,7 g/mol 606,6 g/mol C 3 COO Literatur:
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
Spektroskopiemodul II. H-NMR und 13 C-NMR
 Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von tert-butylchlorid (2-Chloro-2-methylpropan)
 Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Gruppenpräparat im Organisch-Chemischen Praktikum II
 Gruppenpräparat im rganisch-chemischen Praktikum II WS 2007/2008 Versuch 6.2.3 Philipp Bissinger Alexander Damme Yvonne Göbel Inhaltsverzeichnis 1. Einleitung 2. Darstellungsmethoden 2.1 Darstellung von
Gruppenpräparat im rganisch-chemischen Praktikum II WS 2007/2008 Versuch 6.2.3 Philipp Bissinger Alexander Damme Yvonne Göbel Inhaltsverzeichnis 1. Einleitung 2. Darstellungsmethoden 2.1 Darstellung von
Synthese von Dibenzalaceton (DBA) (1,5-Bisphenylpenta-1E,4E-dien-3-on)
 Praktikum rganische Chemie I Zürich, 08.01.2006 529-0229-00L (für Biol./arm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Dibenzalaceton (DBA)
Praktikum rganische Chemie I Zürich, 08.01.2006 529-0229-00L (für Biol./arm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Dibenzalaceton (DBA)
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b).
 2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Klausur OC1 (BA-Studiengang) 2. Wiederholung :00 16:00 Uhr N2. Name: Punkte: Matrikel Nr. Note:
 Klausur OC1 (BA-Studiengang) 2. Wiederholung 12.04.2012 13:00 16:00 Uhr N2 PIN: Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Klausur OC1 (BA-Studiengang) 2. Wiederholung 12.04.2012 13:00 16:00 Uhr N2 PIN: Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Übungen LÖSUNGEN
 Übungen 24.01.2012 - LÖSUNGEN Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Maximale Punktezahl: 20 Aufgabe 1.1 (5 Punkte) Zeichnen Sie die Strukturformeln der folgenden
Übungen 24.01.2012 - LÖSUNGEN Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Maximale Punktezahl: 20 Aufgabe 1.1 (5 Punkte) Zeichnen Sie die Strukturformeln der folgenden
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Übungen zur Spektroskopie 2
 Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Titration von Metallorganylen und Darstellung der dazu benötigten
 Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
(R)-(S)-PPFA. (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3. PPh 2
![(R)-(S)-PPFA. (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3. PPh 2 (R)-(S)-PPFA. (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3. PPh 2](/thumbs/30/14148963.jpg) (R)-(S)-PPFA (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3 NMe 2 Fe PPh 2 Abstract Mit (R)-N,N-Dimethylferrocenylethylamin wird eine Enantiomerenanreicherung durchgeführt und dann
(R)-(S)-PPFA (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3 NMe 2 Fe PPh 2 Abstract Mit (R)-N,N-Dimethylferrocenylethylamin wird eine Enantiomerenanreicherung durchgeführt und dann
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
Abbauprodukte von Amiloridhydrochlorid
 Seientia Pharmaeeutiea (Sei. Pharm.) 72, 109-120 (2004) 109 Österreiehisehe Apotheker-Verlagsgesellsehaft m.b.h., Wien, Printed in Austria Abbauprodukte von Amiloridhydrochlorid Klaus Görlitzer * 1, Silke
Seientia Pharmaeeutiea (Sei. Pharm.) 72, 109-120 (2004) 109 Österreiehisehe Apotheker-Verlagsgesellsehaft m.b.h., Wien, Printed in Austria Abbauprodukte von Amiloridhydrochlorid Klaus Görlitzer * 1, Silke
4. Experimenteller Teil
 . Experimenteller Teil.. Material und Methoden... Analytik... H-MR-Spektroskopie Sämtliche Substanzen wurden mit Spektrometern des Typs AC 0 oder AC 0 und in besonderen Fällen mit einem AMX 00 der Firma
. Experimenteller Teil.. Material und Methoden... Analytik... H-MR-Spektroskopie Sämtliche Substanzen wurden mit Spektrometern des Typs AC 0 oder AC 0 und in besonderen Fällen mit einem AMX 00 der Firma
Synthese von P,P-, S,S-, P,P -, P,N- und P,S- Liganden, ihrer Komplexe und mögliche Anwendung in der Katalyse. Band 2
 1 5. Experimenteller Teil Synthese von P,P-, S,S-, P,P -, P,N- und P,S- Liganden, ihrer Komplexe und mögliche Anwendung in der Katalyse Band 2 Dissertation zur Erlangung des akademischen Grades Doktor
1 5. Experimenteller Teil Synthese von P,P-, S,S-, P,P -, P,N- und P,S- Liganden, ihrer Komplexe und mögliche Anwendung in der Katalyse Band 2 Dissertation zur Erlangung des akademischen Grades Doktor
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 2. Klausur OC1 (BA-Studiengang) PIN: 12.03.2014 13:00 16:00 Uhr N2 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
2. Klausur OC1 (BA-Studiengang) PIN: 12.03.2014 13:00 16:00 Uhr N2 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid
 NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
Aufgabe S. 2/a (2 Punkte) Wodurch können Sie Cyclopenten von Benzol unterscheiden?
 14-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
14-1 2 Zur Punktevergabe bei multiple choice-aufgaben: Meist gibt es 5 Antwortmöglichkeiten, und 2 Punkte können pro Aufgabe erreicht werden. Pro falscher Antwort (Kreuz zu viel, aber auch fehlend) wird
2. Wiederholungsklausur OC1 (BA-Studiengang) :00 16:00 Uhr M1 C-Bau. Name: Punkte: Matrikel Nr. Note:
 2. Wiederholungsklausur C1 (BA-Studiengang) PI: 07.04.2011 13:00 16:00 Uhr M1 C-Bau ame: Punkte: Matrikel r. ote: otenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
2. Wiederholungsklausur C1 (BA-Studiengang) PI: 07.04.2011 13:00 16:00 Uhr M1 C-Bau ame: Punkte: Matrikel r. ote: otenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Dimethyl(S)-2-(1-phenylallyl)malonat
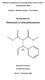 Praktikum in Organischer und Anorganischer Chemie OACP 2 Herbstsemester 2008 Assistenz : Michelle Flückiger / Tina Osswald Synthesebericht Dimethyl(S)-2-(1-phenylallyl)malonat Ehrenmann Janosch D CHAB,
Praktikum in Organischer und Anorganischer Chemie OACP 2 Herbstsemester 2008 Assistenz : Michelle Flückiger / Tina Osswald Synthesebericht Dimethyl(S)-2-(1-phenylallyl)malonat Ehrenmann Janosch D CHAB,
8 Experimenteller Teil
 8 8.1 Synthese 8.1.1 Material 8.1.1.1 Geräte Klassische Chromatographie Als Reaktionskontrolle wurde die Dünnschichtchromatographie mit Kieselgel-Fertigfolien der Firma Merck Typ 60 F254 eingesetzt. Die
8 8.1 Synthese 8.1.1 Material 8.1.1.1 Geräte Klassische Chromatographie Als Reaktionskontrolle wurde die Dünnschichtchromatographie mit Kieselgel-Fertigfolien der Firma Merck Typ 60 F254 eingesetzt. Die
Synthese von DOC (2,5-Dimethoxy-4-chloramphetamin)
 T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether)
 Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Organisch chemisches Praktikum II
 18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol
 Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von cis- und trans-stilben
 28. April 2008 eifer Manuel raktikum in Organischer Chemie (OC 1) Frühjahrssemester 2008 529-0230-00L eifer Manuel Synthese von cis- und trans-stilben Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich
28. April 2008 eifer Manuel raktikum in Organischer Chemie (OC 1) Frühjahrssemester 2008 529-0230-00L eifer Manuel Synthese von cis- und trans-stilben Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich
Schriftliche Prüfung BSc Frühling 2008
 Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Präparat 1: Darstellung von Essigsäurebutylester
 hristina Sauermann 1 - A- Praktikum Präparat 1: Darstellung von Essigsäurebutylester 3 3 ( 2 ) 3 2 S 4 (konz.) in l 3 3 4 9 Essigsäure Butanol Essigsäurebutylester ( 2 4 2 ) ( 4 10 ) ( 6 12 2 ) M = 60,05
hristina Sauermann 1 - A- Praktikum Präparat 1: Darstellung von Essigsäurebutylester 3 3 ( 2 ) 3 2 S 4 (konz.) in l 3 3 4 9 Essigsäure Butanol Essigsäurebutylester ( 2 4 2 ) ( 4 10 ) ( 6 12 2 ) M = 60,05
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 317. Band, Heft 5, Seite 43 47 Verlag Chemie GmbH, Weinheim (Bergstr.) Synthese der Pyrrolizidine (± )-Tussilagin und (± )-Isotussilagin Erhard Röder*, Helmut Wiedenfeld
Sonderdruck aus Archiv der Pharmazie 317. Band, Heft 5, Seite 43 47 Verlag Chemie GmbH, Weinheim (Bergstr.) Synthese der Pyrrolizidine (± )-Tussilagin und (± )-Isotussilagin Erhard Röder*, Helmut Wiedenfeld
