3 Experimenteller Teil
|
|
|
- Hetty Richter
- vor 8 Jahren
- Abrufe
Transkript
1 Experimenteller Teil: Allgemeines Experimenteller Teil 3.1 Allgemeines Präparative Methoden Arbeiten unter Schutzgas Alle metallorganischen Umsetzungen und sämtliche Reaktionen unter Luft- und / oder Feuchtigkeitsausschluß werden in absoluten Lösungsmitteln durchgeführt. Die benötigten Glasapparaturen werden im Ölpumpenvakuum ausgeheizt und im Strom trockenen Argons der Fa. Linde belüftet. Lösungsmittel und Reagentien werden gegebenfalls durch Injektionsspritzen in die Apparaturen eingebracht. Sofern nicht anders angegeben, werden alle Reaktionsansätze magnetisch gerührt Chemikalien und Lösungsmittel Die Chemikalien werden von den Firmen Acros, Aldrich, Avocado, Fluka, Lancaster, Merck, Sigma und insbesondere durch großzügige Spenden von der Firma Schering bezogen. Molsieb, Zinkchlorid und Kalium-t-butylat werden im Hochvakuum bei 200 C ausgeheizt und unter Argon aufbewahrt. Bei Verwendung absoluter Amine (Triethylamin, Diisopropylamin, Hünig- Base etc.) werden diese über Calciumhydrid getrocknet und abdestilliert. Sonstige Reagentien werden in der Regel vor Gebrauch destilliert. Die für die Reaktionen und Reinigungen benötigten Lösungsmittel werden bei Bedarf nach Routinevorschriften gereinigt, getrocknet und destilliert. Acetonitril wird über Phosphorpentoxid unter Rückfluß gekocht und von Kaliumcarbonat abdestilliert. Chloroform wird über einer mit basischem Aluminiumoxid der Aktivitätsstufe 1 beschickte Säule getrocknet und destilliert. Diethylether wird über Kaliumhydroxid vorgetrocknet, über atrium mit Benzophenon als Indikator unter Rückfluß gekocht und abdestilliert. Essigsäureethylester wird über Phosphorpentoxid unter Rückfluß gekocht und abdestilliert. Methylenchlorid wird über einer mit basischem Aluminiumoxid der Aktivitätsstufe 1 beschickte Säule getrocknet, über Calciumhydrid unter Rückfluß gekocht und abdestilliert. Tetrahydrofuran wird über Kaliumhydroxid vorgetrocknet, über atrium mit Benzophenon als Indikator unter Rückfluß gekocht und abdestilliert. Toluol wird über atrium unter Rückfluß gekocht und abdestilliert.
2 Experimenteller Teil: Allgemeines Chromatographie Der Reaktionsfortschritt wird mittels analytischer Dünnschichtchromatographie verfolgt. Dazu werden kieselgelbeschichtete Aluminiumfolien der Fa. Merck mit UV-Indikator verwendet. Als Laufmittel werden meist Lösungsmittelgemische aus n-hexan, Essigsäureethylester und Methanol benutzt. eben der UV-Auslöschung wird mit folgenden Sprühreagentien gearbeitet: inhydrin-reagenz: 200 mg inhydrin in 100 ml Ethanol (Entwicklung im Heißluftstrom) KMn 4 -Reagenz: 0.05%ige wässrige Lösung von KMn 4 Anisaldehyd-Reagenz: 1 ml Anisaldehyd und 2 ml konz. Schwefelsäure in 100 ml Eisessig (Entwicklung im Heißluftstrom) Schlittlers-Reagenz: 3 ml wässrige 10%ige H 2 PtCl 6 -Lösung, 97 ml Wasser und 100 ml wässrige 6%ige Kaliumiodid-Lösung Bromkresolgrün-Reagenz: 40 mg Bromkresolgrün, 100 ml Ethanol und 0.1 m atronlauge bis zur Blaufärbung der Lösung Cer-Reagenz: 2 g Ce(S 4 ) 2, 5 g Phosphormolybdänsäure und 16 ml konz. Schwefelsäure, mit Wasser auf 200 ml auffüllen (Entwicklung im Heißluftstrom) Die präparative Säulenchromatographie wird über Kieselgel 60 der Fa. Merck durchgeführt. Als Laufmittel werden meist Gemische aus n-hexan und Essigsäureethylester verwendet. Die analytische und präparative HPLC wird durchgeführt auf Geräten der Firmen Knauer (Modulsystem aus Pumpe, Säule, IR- und UV-Detektor und Schreiber), Waters-Millipore (Injektionssystem U6K9) und Milton-Roy (Integrator CI-10). Für die analytische HPLC wird eine Knauer-Säule (4x 125 mm) gepackt mit 5 µm ucleosil 50 und für die präparative HPLC eine Knauer-Säule (32x 250 mm oder 65x 300 mm) gepackt mit 7 µm ucleosil 50 verwendet. Als Eluens werden Lösungsmittelgemische aus n-hexan, Essigsäureethylester und Isopropanol verwendet Analytik MR-Spektroskopie Alle 1 H- und 13 C-MR-Spektren werden in Lösung unter Verwendung von Tetramethylsilan bzw. Deuterochloroform als internen Standard an den Geräten AM 270, AC 250 und AMX 500 der Fa. Bruker vermessen. Die Auswertung der 1 H-MR-Spektren erfolgt nach 1. rdnung; für die Multiplizitäten der Spin-Spin-Kopplungen werden folgende Kürzel verwendet: s = Singulett, d= Dublett, dd = Doppeldublett, t = Triplett, dt = Doppeltriplett, q = Quartett, m = Multiplett, b = breit. In einigen Fällen wird die Zuordnung der Protonen mit Hilfe eines 1 H, 1 H-CSY vorgenommen. Die Konfiguration der Doppelbindungen wird durch Messung von E-Differenzspektren bestimmt. Alle 13 C-MR-Spektren werden 1 H-Breitband-entkoppelt. Als Fehlerbreite für die chemische Verschiebung bzw. für die Kopplungskonstanten müssen 0.02 ppm bzw. 0.5 Hz berücksichtigt werden.
3 Experimenteller Teil: Allgemeines Massenspektroskopie Die massenspektroskopischen Untersuchungen werden mit Geräten der Fa. Varian (MAT 711 bzw. MAT 112 S) durchgeführt. Angegeben sind Elektronenanregungsenergie, Art der Ionisation (Elektronenstoßionisation = EI, Fast Atom Bombardement = FAB) und die Temperatur der Ionenquelle. Den Werten der physikalischen Massen-Ladungsverhältnisse der Molekülund Fragmentkationen bzw. der Radikalkationen folgt in Klammern die relative Intensität (%). Hochauflösende Massenspektren werden von den Molpeaks (M) bzw. charakteristischen Fragmenten angefertigt und in einem computergestützten Verfahren mit den entsprechenden Summenformeln verglichen IR-Spektroskopie Alle Infrarotspektren werden an einem FT-IR-Interferometer-System 5 SXC (icolet) der Fa. Perkin-Elmer in KBr-Presslingen oder als Film auf solchen gemessen. Die Angabe der Schwingungsbanden erfolgt nach fallender Wellenzahl 1/λ (cm -1 ). Die Banden werden mit s = stark, m = mittel, w = schwach und b = breit gekennzeichnet Elementaranalysen Sämtliche Elementaranalysen werden mit einem Perkin-Elmer 240 Elementar Analyser angefertigt. Aufgrund der hohen Viskosität mancher Öle sind Abweichungen von den theoretischen Werten möglich Polarimetrie Alle spezifischen Drehwerte werden bei Raumtemperatur auf einem Gerät der Fa. Perkin- Elmer (Typ P241) im monochromatischen Licht der atrium-d-linie (γ = nm) aufgenommen. Die Probenlösungen werden durch Einwaage von mg Substanz auf 1 bzw. 2 ml Lösungsmittel hergestellt und in einer Küvette der Schichtdicke d = 1 dm gemessen Schmelzpunktbestimmung Die Schmelzpunkte werden mit dem Gerät SMP 20 der Fa. Büchi gemessen und sind unkorrigiert angegeben.
4 Experimenteller Teil: Synthese der Reagentien Synthese der Reagentien Dimethylphthalimidomethylphosphonat (30) H P Me Me g -Hydroxymethylphthalimid (28, 282 mmol) werden in 150 ml Toluol suspendiert und vorsichtig mit 30.6 g Phosphortribromid versetzt. Man rückflussiert 2 h, saugt anschließend vom iederschlag ab, engt die Mutterlauge im Vakuum ein und läßt im Kühlschrank auskristallisieren. ach Abfiltrieren der Kristalle wird die Mutterlauge erneut eingeengt und in den Kühlschrank gestellt. Es wird erneut abfiltriert und im Hochvakuum getrocknet. Man erhält insgesamt 55.9 g -Brommethylphthalimid 29 (233 mmol 83%). Dieses wird in 95 ml Xylol gelöst und unter Argon vorsichtig mit 31.8 g Trimethylphosphit versetzt. Es wird vorsichtig bis zur einsetzenden Gasentwicklung erwärmt, ehe man 5 h rückflussiert. Im Vakuum wird das Volumen auf die Hälfte eingeengt und der Rückstand in den Kühlschrank gestellt. Die Kristalle werden abgesaugt und mit Toluol umkristallisiert. Man erhält 35.4 g elfenbeinfarbiges Produkt 30 (132 mmol 57%). -Brommethylphthalimid 29: Smp.: C (Lit.: C) 1 H-MR (CDCl 3 ; 250 MHz): δ = 5.48 (s, 2H; CH 2 ), 7.80, 7.94 (2x m, 4H; Phth CH) ppm. Dimethylphthalimidomethylphosphonat (30): Smp.: C (Lit.: C) 1 H-MR (CDCl 3 ; 250 MHz): δ = 3.82 (d, J = 11.9 Hz, 6H; CH 3 ), 4.12 (d, J = 10.8 Hz, 2H; CH 2 ), 7.74, 7.87 (2x m, 4H; Phth CH) ppm.
5 Experimenteller Teil: Synthese der Reagentien Diazomethylphosphonsäuredimethylester (27) P Me Me 2 P Me Me g Dimethylphthalimidomethylphosphonat (30, 54.3 mmol) werden in ml Methanol gelöst und bei Raumtemperatur mit 2.2 ml 80%ige Hydrazin-Hydrat-Lösung versetzt. ach 45 h werden 5.4 ml Essigsäure hinzugegeben, und es wird vom iederschlag abgesaugt. Aus dem Filtrat wird im Vakuum das Solvens entfernt, worauf der Rückstand in 13.6 ml Essigsäure gelöst wird. Unter Eiskühlung tropft man 5.9 g atriumnitrit in 13.6 ml Wasser hinzu. Anschließend wird vorsichtig mit 14.4 g atriumcarbonat basisch gestellt. Man verdünnt mit 54.3 ml Eiswasser und extrahiert dreimal mit Methylenchlorid. ach Trocknen der organischen Phase über atriumsulfat wird abgesaugt und das Lösungsmittel entfernt. Man erhält 6.1 g Diazophosphonat 27 (40.7 mmol 75%), welches ohne weitere Reinigung umgesetzt wird. 1 H-MR (CDCl 3 ; 250 MHz): δ = 2.12 (s, 1H; CH), (m, 6H; CH 3 ) ppm Diazoessigsäureethylester (81) HCl H 2 Et 2 Et Zu einer Lösung von 0.25 g atriumacetat in 100 ml Wasser werden 50.0 g Glycinethylester- Hydrochlorid (82, 0.36 mol) und 37.5 g atriumnitrit gegeben. Zu der klaren Lösung gibt man 0.25 ml 10%ige Schwefelsäure und 25 ml Diethylether und läßt 15 min reagieren. ach Phasentrennung wird die wässrige Phase erneut mit 0.25 ml 10%ige Schwefelsäure und 25 ml Diethylether versetzt. Es wird 15 min gerührt, ehe die Phasen wieder getrennt werden. Dieses wird solange wiederholt, bis bei der Zugabe von Schwefelsäure braune Dämpfe entstehen. Die vereinigten organischen Phasen werden mit atriumhydrogencarbonat-lösung gewaschen und über Calciumchlorid getrocknet. Es wird vom Feststoff abgesaugt und das Lösungsmittel im Vakuum entfernt. Das Rohöl wird durch Destillation im Vakuum gereinigt (bei Überhitzung, Säure- oder Schwermetallspuren besteht Explosionsgefahr). Man erhält 23.8 g Diazoessigsäureethylester (81, 0.21 mol 58%). Sdp.: 55 C / 33 mbar
6 Experimenteller Teil: Synthese der Reagentien H-MR (CDCl 3 ; 250 MHz): δ = 1.26 (t, J = 7.0 Hz, 3H; Et CH 3 ), 4.22 (q, J = 7.0 Hz, 2H; Et CH 2 ), 4.78 (s, 1H; H 2) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (Et CH 3 ), (C 2), (Et CH 2 ), (C 1) ppm ,2-Methylendioxyphenyltributylstannan (68) Br SnBu Zu einer Lösung von 10.0 g 4-Brom-1,2-methylendioxybenzol (67, 49.8 mmol) in 100 ml abs. THF werden unter Argon bei 78 C 34.2 ml n-buli-lösung (1.1 eq.; 1.6 m in n-hexan) getropft. ach 1 h werden 22.3 ml Tributylstannylchlorid (1.5 eq.) hinzugegeben. Man läßt 2 h bei 78 C reagieren und gibt anschließend auf 100 ml ges. Ammoniumchlorid-Lösung. ach Phasentrennung wird die wässrige Phase dreimal mit 150 ml Diethylether extrahiert. Die vereinigten organischen Phasen werden über Magnesiumsulfat getrocknet. Anschließend wird vom Feststoff abgesaugt und das Solvens im Vakuum entfernt. Das Rohöl wird durch Destillation im Hochvakuum gereinigt. Man erhält 16.8 g eronylstannan 68 (40.9 mmol 82%). Sdp.: C / 0.02 mbar 1 H-MR (CDCl 3 ; 250 MHz): δ = 0.92 (t, J = 7.0 Hz, 9H; Bu CH 3 ), 1.06, 1.40, 1.56 (3x m, 18H; Bu CH 2 ), 5.96 (s, 2H; CH 2 ), (m, 3H; CH) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = 9.73 (3C; Bu CH 2 ), (3C; Bu CH 3 ), 27.35, (6C; Bu CH 2 ), ( CH 2 ), , , (3C; CH), , , (3C; C) ppm.
7 Experimenteller Teil: Synthese der Reagentien Tributyltrimethylsilylethinylstannan (69) TMS TMS H SnBu Zu einer Lösung von 1.64 g Trimethylsilylacetylen (70, 16.7 mmol) in 33.4 ml abs. THF werden unter Argon bei 78 C 11.5 ml n-buli-lösung (1.1 eq.; 1.6 m in n-hexan) getropft. ach 1 h werden 4.95 ml Tributylstannylchlorid (1.1 eq.) hinzugegeben. Man läßt 2 h bei 78 C reagieren und gibt anschließend auf 30 ml ges. Ammoniumchlorid-Lösung. Die wässrige Phase wird dreimal mit 100 ml Diethylether extrahiert. ach Trocknen der organischen Phase über Magnesiumsulfat wird vom Feststoff abgesaugt und das Solvens im Vakuum entfernt. Das Rohöl wird durch Kugelrohrdestillation im Hochvakuum gereinigt. Man erhält 6.3 g Alkinylstannan 69 (16.3 mmol 98%). Sdp.: C / 0.05 mbar (Lit.: 89 C / 0.36 mbar) 1 H-MR (CDCl 3 ; 250 MHz): δ = 0.22 (s, 9H; Si CH 3 ), , 1.36, 1.60 (3x m, 27H; Bu CH 2, Bu CH 3 ) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = 0.22 (3C; Si CH 3 ), 8.73, (6C; Bu CH 2 ), (3C; Bu CH 3 ), (3C; Bu CH 2 ), , (2C; Alkin C) ppm Tris(dibenzylidenaceton)dipalladium-Chloroform (64) PdCl 2 Pd (dba) 2 Pd 2 (dba) 3 -CHCl g Dibenzylidenaceton und 3.7 g atriumacetat werden in 150 ml Methanol gelöst und auf 50 C erhitzt. Es wird 1.0 g Palladiumdichlorid (65, 5.64 mmol) hinzugegeben und 4 h bei 40 C gerührt. ach Abkühlen auf RT wird der entstandene iederschlag abgesaugt, mit Wasser und Aceton gewaschen und im Hochvakuum getrocknet. Dieser wird bei 50 C in 120 ml Chloroform gelöst. ach 5 min wird vom ungelösten Bis-(dibenzylidenaceton)-Palladium (66) abgesaugt, welches in weiteren Ansätzen erneut eingesetzt wird. Aus dem Filtrat erhält man durch Zugabe von 170 ml Diethylether violette adeln, welche abfltriert und zweimal mit 10 ml Diethylether gewaschen werden. ach Trocknen im Hochvakuum erhält man 1.8 g Palladiumdibenzylidenaceton-Chloroform (64, 1.74 mmol 62%).
8 Experimenteller Teil: Synthese der Reagentien Acetoxyacetaldehyd (147) Ac Ac Ac g Z-1,4-Diacetoxy-2-buten (148, 17.4 mmol) werden in 26.2 ml Wasser gelöst und mit 8.2 g atriumperiodat und 8.3 ml smiumtetroxid-lösung (0.042 m in t-butanol, 2 mol%) versetzt. ach 4 h wird vom iederschlag abfiltriert. Das Filtrat wird dreimal mit Tetrachlorkohlenstoff gewaschen und mit 34.8 ml kaltem Aceton versetzt. Erneut wird vom iederschlag abfiltriert und das Lösungsmittel im Vakuum bei 30 C entfernt (mit Argon belüften). Der Rückstand wird in Methylenchlorid aufgenommen und über Magnesiumsulfat getrocknet. Anschließend wird vom Feststoff abfiltriert und das Lösungsmittel im Vakuum bei 30 C entfernt. Man erhält 2.89 g 2-Acetoxyacetaldehyd (147, 28.3 mmol 81%), welcher ohne weitere Reinigung umgesetzt wird. 1 H-MR (CDCl 3 ; 250 MHz): δ = 2.20 (s, 3H; Ac CH 3 ), 4.67 (s, 2H; H 2), 9.60 (s, 1H; H 1) ppm ,2-Diethoxyacetaldehyd (152) H Zu einer Lösung von 1.37 ml xalylchlorid (2.1 eq.) in 14.9 ml Methylenchlorid werden unter Argon bei 65 C 1.59 ml Dimethylsulfoxid (3 eq.) in 7.5 ml Methylenchlorid getropft. ach 30 min gibt man 1.0 g Glykolaldehyddiethylacetal (153, 7.45 mmol) in 14.9 ml Methylenchlorid hinzu und läßt 1 h bei 65 C reagieren. Anschließend werden 5.2 ml Triethylamin (5.0 eq.) zugetropft. ach 15 min läßt man 2 h auf 0 C auftauend reagieren. Das Lösungsmittel wird im Vakuum bei 30 C entfernt (mit Argon belüften) und der Rückstand in Diethylether aufgenommen. Anschließend wird von den ungelösten Salzen abfiltriert und das Lösungsmittel erneut im Vakuum bei 30 C entfernt. Man erhält 1.33 g Diethoxyacetaldehyd (152, mmol 68%), welcher ohne weitere Reinigung umgesetzt wird. 1 H-MR (CDCl 3 ; 270 MHz): δ = 1.23 (m, 6H; Et CH 3 ), 3.66 (m, 4H; Et CH 2 ), 4.57 (s, 1H; H 2), 9.47 (s, 1H; H 1) ppm.
9 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette Synthesen zum Aufbau der Seitenkette Asparaginsäuresysteme (2S)--t-Butyloxycarbonylasparaginsäure (3) H 2 HBC H H H H 1 3 Eine Lösung von 9.8 g Di-t-butyldicarbonat in 28 ml Dioxan wird bei 0 C zu 5.0 g L-Asparaginsäure (1, 37.6 mmol) in 115 ml 1 m atronlauge getropft. Man läßt über acht auf Raumtemperatur kommend reagieren. achdem das Volumen im Vakuum auf die Hälfte eingeengt wurde, stellt man mit 1 m Kaliumhydrogensulfat-Lösung den ph-wert auf 2-3 ein. ach Extrahieren mit EE und Trocknen der organischen Phase über Magnesiumsulfat wird abgesaugt. Man entfernt das Solvens im Vakuum und erhält 8.4 g Produkt 3 (30.0 mmol 96%). 1 H-MR (d 6 -DMS; 250 MHz): δ = 1.38 (s, 9H; BC CH 3 ), (m, 2H; H 3), 4.22 (m, 1H; H 2), 6.99 (d, J = 10.0 Hz, 1H; H), (bs, 2H; CH) ppm. 13 C-MR, DEPT (d 6 -DMS; 63 MHz): δ = (3C; BC CH 3 ), (C 3), (C 2), (BC C), (BC C), , (2C; C 1, C 4) ppm. MS (80 ev, FAB neg.): m/e = 465 (4.7), 233 (12.9), 232 (100), 158 (97.1), 132 (8.5), 115 (35.3), 114 (23.1), 73 (8.0), 42 (11.3) (2S)--t-Butyloxycarbonylasparaginsäureanhydrid (4) HBC HBC H H g L-BC-Asparaginsäure (3, 26.7 mmol) werden bei Raumtemperatur mit 21.2 ml Acetanhydrid versetzt. Man läßt über acht reagieren und fügt dann Diethylether / n-hexan (1:1)
10 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette 125 zum Auskristallisieren hinzu. Die Kristalle werden abgesaugt und mit Diethylether gewaschen. Die Mutterlauge wird im Vakuum eingeengt und erneut mit Diethylether / n-hexan (1:1) versetzt. ach Absaugen der Kristalle und Trocknen im Vakuum erhält man insgesamt 3.2 g Anhydrid 4 (14.9 mmol 56%). 1 H-MR (CD 3 D; 250 MHz): δ = 1.42 (s, 9H; BC CH 3 ), 2.92 (dd, J 1 = 6.3 Hz, J 2 = 20.0 Hz, 1H; H A 3), 3.20 (m, 1H; H B 3), 4.54 (m, 1H; H 2), 7.49 (bd, J = 7.5 Hz, 1H; H) ppm. 13 C-MR, DEPT (CD 3 D; 63 MHz): δ = (3C; BC CH 3 ), 37.13, (C 3), 51.35, (C 2), (BC C), (BC C), , (2C; C 1, C 4) ppm (3S)-3-(-t-Butyloxycarbonylamido)-γ-butyrolacton (5) HBC HBC 4 5 Zu einer Suspension von 0.19 g atriumborhydrid (2.2 eq.) in 18.6 ml abs. THF werden bei 0 C unter Argon 2.0 g BC-Asparaginsäureanhydrid 4 (9.29 mmol) in 18.6 ml abs. THF getropft. Man läßt 4 h auf Raumtemperatur kommend reagieren. Anschließend wird der ph- Wert mit 25%iger Salzsäure vorsichtig auf 2-3 eingestellt. Das Volumen wird am Rotationsverdampfer bis auf ein Viertel eingeengt und danach achtmal mit 30 ml Diethylether extrahiert. Aus den vereinigten organischen Phasen wird das Lösungsmittel entfernt. Der Rückstand wird in 50 ml Toluol aufgenommen und mit p-toluolsulfonsäure versetzt, bis ein ph-wert von 2.5 eingestellt ist. Es wird 4 h an einem Wasserabscheider rückflussiert. Anschließend läßt man langsam abkühlen und entfernt das Solvens im Vakuum. Das Rohprodukt wird säulenchromatographisch gereinigt (2:1 n-hexan / EE). Man erhält 1.3 g BC-Butyrolacton 5 (6.46 mmol 70%) in Form eines elfenbeinfarbenden Feststoffs. 1 H-MR (CDCl 3 ; 250 MHz): δ = 1.45 (s, 9H; BC CH 3 ), 2.49 (dd, J 1 = 3.8 Hz, J 2 = 17.5 Hz, 1H; H A 2), 2.87 (dd, J 1 = 7.5 Hz, J 2 = 17.5 Hz, 1H; H B 2), 4.24 (m, 1H; H 3), 4.51 (m, 2H; H 4), 5.27 (bs, 1H; H) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (3C; BC CH 3 ), (C 2), (C 3), (C 4), (BC C), (BC C), (C 1) ppm. IR (KBr, Pille): 1/λ = 3527 (w), 3322 (s), 2982 (m), 2933 (m), 1768 (s), 1686 (s), 1543 (s), 1171 (s), 1083 (m), 1009 (m), 963 (m) cm -1.
11 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette Serinsysteme L--t-Butyloxycarbonylserin (8) H HBC H 2 H H H 2 8 Zu einer Lösung von 5 g L-Serin (2, 47.5 mmol) in 147 ml 1 m atronlauge werden bei 0 C 13.0 g Di-t-butyldicarbonat in 35 ml Dioxan getropft. Man läßt über acht auf Raumtemperatur kommend reagieren. Anschließend wird das Volumen im Vakuum auf die Hälfte eingeengt und mit 1 m Kaliumhydrogensulfat-Lösung der ph-wert auf 2-3 eingestellt. ach Extrahieren mit EE und Entfernen des Lösungsmittels der organischen Phase im Vakuum erhält man 9.4 g BC-Serin 8 (45.8 mmol 96%), welches ohne weitere Reinigung eingesetzt wird. 1 H-MR (CDCl 3 ; 250 MHz): δ = 1.48 (s, 9H; BC CH 3 ), 3.85 (bm, 1H; H A 3), 4.05 (bm, 1H; H B 3), 4.24, 4.39 (2x bs, 1H; H 2), 5.86 (bd, J = 8.8 Hz, 1H; H), 6.92 (bs, 1H; H), (bs, 1H; CH) ppm (2S)-2-(-t-Butyloxycarbonylamido)-β-propiolacton (7) H HBC H HBC 8 7 Zu einer Lösung von 27.8 g Triphenylphosphin in 270 ml abs. Acetonitril und 30 ml abs. THF werden unter Argon bei 55 C 17.0 ml Diethylazodicarboxylat getropft. ach 30 Minuten werden 19.5 g L-BC-Serin 8 (95.0 mmol) in 270 ml abs. Acetonitril und 30 ml abs. THF zugetropft. Es wird 1 h bei 55 C gerührt, anschließend wird das Kältebad entfernt und weitere 2 h gerührt. Das Lösungsmittel wird im Vakuum entfernt und der Rückstand in wenig EE aufgenommen. Durch Zugabe von vier Volumenanteilen n-hexan entsteht ein weißer iederschlag von Triphenylphosphinoxid, von dem abfiltriert wird. Das Lösungsmittel wird erneut im Vakuum entfernt und das Rohöl durch Säulenchromatographie gereinigt (4:1 n-hexan / EE). Man erhält 10.0 g Propiolacton 7 (53.4 mmol 56%). 1 H-MR (CDCl 3 ; 270 MHz): δ = 1.45 (s, 9H, BC CH 3 ), 4.44 (m, 2H; H 3), 5.11 (m, 1H; H 2), 5.34 (bd, 1H; H) ppm.
12 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (3C; BC CH 3 ), (C 2), (C 3), (BC C), (BC C), (C 1) ppm. MS (70 ev, EI, 80 C): m/e = 172 (0.7), 87 (5.2), 59 (49.2), 58 (5.2), 57 (100), 56 (5.1), 44 (2.7), 43 (9.3), 41 (15.7), 39 (2.7). IR (KBr, Pille): 1/λ = 3361 (s), 3013 (m), 2980 (m), 1846 (s), 1680 (s), 1532 (s), 1369 (s), 1162 (s), 889 (s), 619 (m) cm (2S)-2-(-t-Butyloxycarbonylamido)-4-methyl-4-pentensäure (9) HBC 7 HBC H 9 In einem Schlenkkolben werden unter Argon 0.57 g getrocknete Magnesiumspäne (10 eq.) mit wenig abs. THF bedeckt. Hierzu werden 1.90 ml 2-Brompropen (10 eq.) getropft, zuerst ohne Rührer und konzentriert, bis die Reaktion anspringt und anschließend unter Rühren mit 32 ml abs. THF verdünnt. Bei zu starker exothermer Reaktion wird vorsichtig mit einem Eisbad gekühlt. Man läßt über acht reagieren. Diese trübe Lösung wird bei 23 C zu einer Suspension aus 0.40 g β-lacton 7 (2.14 mmol) und 83 mg Kupfer-(Ι)-bromid-Dimethylsulfid-Komplex (0.2 eq.) in 18.9 ml abs. THF und 0.9 ml Dimethylsulfid getropft. ach 2 h bei 23 C hat sich das Edukt komplett umgesetzt (DC-Kontrolle mit EE zeigt einen basischen Startfleck). Es wird mit 10%iger Citronensäure gewaschen (anschließend färbt Startfleck mit Bromkresol gelb). ach Phasentrennung wird die wässrige Phase dreimal mit EE extrahiert. Das Lösungsmittel der vereinigten organischen Phase wird im Vakuum entfernt und der Rückstand in gesättigter atriumhydrogencarbonat-lösung aufgenommen. Es wird mit 1:1 n-hexan / EE gewaschen. ach Ansäuern (ph 2.5) wird erneut dreimal mit EE extrahiert. Anschließend werden die Phasen getrennt und das Lösungsmittel der organischen Phase im Vakuum entfernt. Man erhält 0.18 g BC-Amidopentensäure 9 (0.79 mmol 37%), welche wegen des amphiphilen Charakters nur schwer zu reinigen ist. 1 H-MR (CDCl 3 ; 270 MHz): δ = 1.44 (s, 9H, BC CH 3 ), 1.76 (s, 3H; 4-CH 3 ), 2.37 (m, 1H; H A 3), 2.56 (m, 1H; H B 3), 3.66 (m, 1H; H A 5), 4.35 (m, 1H; H 2), (m, 2H; H B 5, H), (bs, 1H; CH) ppm.
13 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette L--t-Butyloxycarbonylserinmethylester (11) HBC HBC H H H Me g BC-Serin 8 (45.8 mmol) werden in 130 ml Diethylether gelöst und auf 0 C gekühlt. Unter Rühren gibt man portionsweise 1.4 eq. frisch hergestelltes Diazomethan in Diethylether hinzu und läßt über acht reagieren. Man setzt das überschüssige Diazomethan mit wenig Eisessig um und wäscht mit halbgesättigter atriumhydrogencarbonat-lösung. ach Trocknen der organischen Phase über Magnesiumsulfat wird abgesaugt und das Solvens im Vakuum entfernt. Man erhält 8.6 g Serinester 11 (39.3 mmol 86%), welcher ohne weitere Reinigung umgesetzt wird. 1 H-MR (CDCl 3 ; 250 MHz): δ = 1.48 (s, 9H; BC CH 3 ), 3.36 (bs, 1H; H), 3.77 (s, 3H; CH 3 ), (m, 2H; H 3), 4.37 (bs, 1H; H 2), 5.68 (bd, J = 8.8 Hz, 1H; H) ppm. 13 C-MR (CDCl 3 ; 63 MHz): δ = (3C; BC CH 3 ), (C 2), ( CH 3 ), (C 3), (BC C), (BC C), (C 1) ppm L-Serinmethylester-Hydrochlorid (14) H H 2 H 2 HCl H H Me 2 14 Zu einer Suspension von 20.0 g L-Serin (2, 190 mmol) in 200 ml Methanol werden unter Eiskühlung langsam 21.4 ml Thionylchlorid getropft. ach Abklingen der stark exothermen Reaktion wird 2 h rückflussiert. Das Lösungsmittel wird abdestilliert, der Rückstand in 100 ml Methanol aufgenommen und mit 70 ml Diethylether versetzt. Man läßt über acht im Kühlschrank auskristallisieren, ehe das Hydrochlorid 14 abfiltriert und mit Diethylether gewaschen wird. Die Mutterlauge wird erneut mit Diethylether versetzt, und nach erfolgter Auskristallisation wird wieder das Hydrochlorid 14 abfiltriert und mit Diethylether gewaschen. Das vereinigte Produkt wird im Hochvakuum über Phosphorpentoxid getrocknet, und man erhält 29.4 g L-Serinmethylester-Hydrochlorid (14, 189 mmol 99%). 1 H-MR (d 6 -DMS; 250 MHz): δ = 3.76 (s, 3H; CH 3 ), 3.85 (s, 2H; H 3), 4.09 (m, 1H; H 2), 5.64 (bs, 1H; H), 8.64 (bs, J = 8.8 Hz, 3H; H 3 + ) ppm.
14 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette C-MR (d 6 -DMS; 63 MHz): δ = 53.05, (2C; C 2, CH 3 ), (C 3), (C 1) ppm L--Triphenylmethylserinmethylester (17) H 2 HCl HTr H Me H Me Eine Suspension von 64.2 g L-Serinmethylester-Hydrochlorid (14, 413 mmol) und 126 ml Triethylamin in 825 ml Methylenchlorid wird unter Eiskühlung mit 127 g Triphenylmethylchlorid versetzt. Man läßt über acht auf Raumtemperatur kommend reagieren. Anschließend wird mit 350 ml 10%iger Citronensäure gewaschen. ach Phasentrennung wird die organische Phase mit 300 ml Wasser gewaschen. Die vereinigten wässrigen Phasen werden dreimal mit 300 ml Diethylether extrahiert. Anschließend wird die organische Phase über Magnesiumsulfat getrocknet. Der Feststoff wird abgesaugt und das Lösungsmittel im Vakuum entfernt. Man erhält 150 g Tritylserinester 17, welcher ohne weitere Reinigung umgesetzt wird. 1 H-MR (CDCl 3 ; 250 MHz): δ = 2.31, 2.96 (2x bs, 2H; H, H), 3.28 (s, 3H; CH 3 ), 3.55 (m, 2H; H 3), 3.72 (m, 1H; H 2), (m, 15H; Trityl CH) ppm (2S)-2,3-(-Triphenylmethylepimino)-propansäuremethylester (16) H HTr Me Tr Me Zu einer Lösung von 150 g Tritylserinester 17 (413 mmol) und 126 ml Triethylamin in 826 ml abs. THF werden bei 0 C 35.2 ml Methansulfonsäurechlorid (1.1 eq.) getropft. Man läßt auf Raumtemperatur kommend 2 h reagieren. Anschließend wird mit 400 ml 10%iger Citronensäure gewaschen. ach Phasentrennung wird die wässrige Phase dreimal mit 300 ml EE extrahiert und die vereinigte organische Phase über Magnesiumsulfat getrocknet. Der Feststoff wird abgesaugt und das Solvens im Vakuum entfernt. Das Mesylat 18 (250 g 413 mmol) wird in 826 ml abs. THF gelöst und mit 127 ml Triethylamin (2.2 eq.) versetzt. Es wird 3 Tage rückflussiert (DC-Kontrolle). Anschließend wird das Volumen am Rotationsverdampfer auf ein Viertel eingeengt. Man nimmt in Diethylether auf
15 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette 130 und wäscht mit 350 ml 10%iger Citronensäure und 300 ml 1 m atriumhydrogencarbonat-lösung. ach Phasentrennung wird die wässrige Phase dreimal mit 300 ml Diethylether extrahiert. Anschließend wird das Solvens der organischen Phase im Vakuum entfernt. Das Rohöl wird in 1:1 Diethylether / EE aufgenommen und mit n-hexan versetzt. Die Kristalle werden abfiltriert, und man erhält g Tritylaziridinester 16 (357 mmol 86%). (2S)-3-Methansulfonyloxy-2-triphenylmethylaminopropansäuremethylester (18): 1 H-MR (CDCl 3 ; 250 MHz): δ = 2.90 (bs, 1H; H), 2.98 (s, 3H; Ms CH 3 ), 3.26 (s, 3H; CH 3 ), 3.66 (m, 1H; H 2), 4.26 (dd, J 1 = 5.5 Hz, J 2 = 10.0 Hz, 1H; H A 3), 4.44 (dd, J 1 = 4.8 Hz, J 2 = 10.0 Hz, 1H; H B 3), (m, 15H; Trityl CH), ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (Ms CH 3 ), 51.73, (2C; C 2, CH 3 ), (C 3), (Trityl C), (15; Trityl CH), (3C; Trityl C), (C 1) ppm. Tritylaziridinester 16: 1 H-MR (CDCl 3 ; 250 MHz): δ = 1.44 (dd, J 1 = 1.7 Hz, J 2 = 6.1 Hz, 1H; H A 3), 1.91 (dd, J 1 = 3.0 Hz, J 2 = 6.1 Hz, 1H; H 2), 2.28 (m, 1H; H B 3), 3.76 (s, 3H; CH 3 ), (m, 15H, Trityl CH) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (C 3), (C 2), ( CH 3 ), (Trityl C), (15C; Trityl CH), (3C; Trityl C), (C 1) ppm. MS (70 ev, EI, 120 C): m/e = 343 (M, 0.1), 342 (0.1), 312 (0.2), 284 (0.1), 260 (10.6), 244 (20.5), 243 (100), 183 (19.8), 165 (23.5), 105 (15.8). [α] D 20 = 83.4 (c = 0.95; CHCl 3 ) (4R/S,6S)-2,4-Dimethyl-6,7-(-triphenylmethylepimino)-1-hepten-5-on (19) Tr Me Tr CH 3 CH Zu einer Lösung von 1.1 g Tritylaziridinmethylester 16 (3.20 mmol) in 28.7 ml abs. THF werden 0.17 g Kupfer-(Ι)-bromid-Dimethylsulfid-Komplex und 1.4 ml Dimethylsulfid gegeben. Unter Argon werden bei 15 C 10.7 ml frisch hergestellte Isopropenylmagnesiumbromid-
16 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette 131 Lösung (ca. 0.6 m in THF, 2 eq.) zugetropft. Man läßt über acht auf Raumtemperatur kommend reagieren. Da nach DC-Kontrolle noch deutlich Edukt vorhanden ist, wird wieder auf 15 C gekühlt und erneut 10.7 ml Isopropenylmagnesiumbromid-Lösung zugetropft. ach 4 h ist kein Edukt mehr erkennbar (DC-Kontrolle). Es wird 2 h mit 30 ml gesättigter Ammoniumchlorid-Lösung gerührt. ach Phasentrennung wird die wässrige Phase viermal mit Diethylether extrahiert. Anschließend werden die vereinigten organischen Phasen über Magnesiumsulfat getrocknet. Es wird vom Feststoff abgesaugt und das Lösungsmittel im Vakuum entfernt. Das Rohprodukt wird durch Säulenchromatographie gereinigt (12:1 n-hexan / EE). Man erhält 0.59 g Heptenon 19 (1.49 mmol 47%) und 0.08 g Edukt 16 (0.23 mmol 7%). 1 H-MR (CDCl 3 ; 250 MHz): δ = 1.06 (m, 3H; CH 3 ), 1.45 (m, 1H; H A 7), 1.71 (s, 3H; CH 3 ), 1.95 (m, 1H; H A 3), 2.05 (m, 1H; H 6), 2.22 (bs, 1H; H B 7), 2.33 (m, 1H; H B 3), 2.98 (m, 1H; H 4), (m, 2H; H 1), (m, 15H, Trityl CH) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = 16.10, 16.61, 22.15, (2C; CH 3 ), 29.75, (C 7), (C 6), 40.40, (C 3), 41.60, (C 4), (Trityl C), , (C 1), (15C; Trityl CH), , 142,72 (C 2), (3C; Trityl C), (C 5) ppm. MS (70 ev, EI, 130 C): m/e = 318 (0.3), 276 (1.7), 244 (23.1), 243 (100), 165 (19.0), 123 (16.9), 109 (17.2), 83 (17.6), 71 (65.7), 43 (22.7). IR (KBr, Film): 1/λ = 3058 (m), 3021 (w), 2970 (m), 2932 (m), 1715 (s), 1648 (w), 1595 (w), 1489 (s), 1448 (s), 708 (s) cm -1. EA: C 28 H 29 ber.: C / H = gef.: C / H = (2S)-2,3-(-t-Butyloxycarbonylepimido)-propansäuremethylester (12) Tr Me BC Me g Tritylaziridinester 16 (5.82 mmol) werden in 21.6 ml Chloroform gelöst und auf 10 C gekühlt. ach Zugabe von 5.0 ml abs. Methanol versetzt man mit 9.9 ml TFA und läßt 2 h bei 10 C reagieren. Das Lösungsmittel wird sorgfältig im Vakuum entfernt und der Rückstand in 20.0 ml Methylenchlorid aufgenommen. Mit 0.81 ml Triethylamin und 0.71 g DMAP wird basisch gestellt, ehe bei 0 C 2.54 g Di-t-butyldicarbonat zugetropft werden. Es wird 1 h bei 0 C gerührt, anschließend weitere 18 h bei RT. Das Lösungsmittel wird im Vakuum entfernt und das Rohprodukt säulenchromatographisch gereinigt (6:1 n-hexan / EE). Man erhält 0.71 g BC-Aziridinester 12 (3.53 mmol 61%).
17 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette H-MR (CDCl 3 ; 270 MHz): δ = 1.36 (s, 9H, BC CH 3 ), 2.33 (dd, J 1 = 1.2 Hz, J 2 = 5.5 Hz, 1H; H A 3), 2.44 (dd, J 1 = 1.2 Hz, J 2 = 3.5 Hz, 1H; H B 3), 2.97 (dd, J 1 = 3.5 Hz, J 2 = 5.5 Hz, 1H; H 2), 3.69 (s, 3H; CH 3 ) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (3C; BC CH 3 ), (C 3), (C 2), ( CH 3 ), (BC C), (BC C), (C 1) ppm. MS (70 ev, EI, 40 C): m/e = 186 (3.1), 142 (5.9), 128 (11.0), 102 (7.1), 101 (8.5), 86 (18.1), 59 (8.5), 57 (100), 41 (16.4), 29 (8.1). IR (KBr, Film): 1/λ = 3004 (w), 2980 (m), 2936 (w), 1748 (s), 1727 (s), 1370 (s), 1330 (s), 1157 (s), 853 (m), 801 (m) cm -1. EA: C 9 H 15 4 ber.: C / H = 7.15 gef.: C / H = 7.42 [α] D 20 = 69.9 (c = 2.32; CHCl 3 ) (-t-Butyloxycarbonylamido)-2-propensäuremethylester (13) BC Me HBC Me Zu einer Lösung von 0.31 ml 2-Brompropen (4 eq.) in 8.7 ml abs. THF werden unter Argon bei 78 C 2.5 ml t-buli-lösung (1.4 m in n-pentan) getropft. ach 1 h bei 78 C wird diese Lösung zu 0.36 g Kupfer-(Ι)-bromid-Dimethylsulfid-Komplex (2 eq.) in 4.4 ml abs. THF getropft. Es wird 30 min gerührt, ehe bei 78 C 0.17 g BC-Aziridinester 12 (0.84 mmol) in 2.1 ml abs. THF zugetropft werden. Man läßt über acht auf Raumtemperatur kommend reagieren. ach DC-Kontrolle (kein Eduktfleck vorhanden) wird mit 15 ml Ammoniumchlorid- Lösung gewaschen. Anschließend werden die Phasen getrennt und die wässrige Phase fünfmal mit Diethylether extrahiert. Die organische Phase wird über Magnesiumsulfat getrocknet, anschließend wird vom Feststoff abgesaugt und das Lösungsmittel im Vakuum entfernt. Das Rohprodukt wird säulenchromatographisch gereinigt (5:1 n-hexan / EE). Man erhält 0.13 g Acrylester 13 (0.65 mmol 77%) als einzig identifizierbares Produkt. 1 H-MR (CDCl 3 ; 270 MHz): δ = 1.42 (s, 9H, BC CH 3 ), 3.76 (s, 3H; CH 3 ), 5.66 (s, 1H; H A 3), 6.09 (s, 1H; H B 3), 6.96 (bs, 1H; H) ppm. 13 C-MR (CDCl 3 ; 68 MHz): δ = (3C; BC CH 3 ), ( CH 3 ), (BC C), (C 3), (C 2), (BC C), (C 1) ppm.
18 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette 133 MS (70 ev, EI, 200 C): m/e = 201 (M, 0.5), 101 (6.5), 59 (33.4), 58 (8.4), 57 (100), 43 (16.9), 42 (11.6), 41 (57.1), 39 (16.0), 31 (19.1). IR (KBr, Film): 1/λ = 3422 (s), 3005 (s), 2979 (s), 2933 (s), 1748 (s), 1730 (s), 1160 (s), 757 (m) cm -1. Hochauflösende MS: Molpeak (C 9 H 15 4 ) ber.: gef.: (2S)-2,3-(-t-Butyloxycarbonylisopropylidenazoxy)-propansäuremethylester (22) HBC BC H Me Me Eine Lösung von 8.6 g Serinester 11 (39.3 mmol) in 137 ml abs. Toluol wird mit 9.9 ml DMP und 116 mg p-toluolsulfonsäure-dihydrat versetzt. Man rückflussiert 30 min und destilliert anschließend 100 ml Solvens ab. ach Zugabe von 3.4 ml DMP und 46 ml abs. Toluol wird erneut 30 min rückflussiert. Man wäscht mit atriumhydrogencarbonat-lösung, extrahiert dreimal mit Diethylether und trocknet die organische Phase über Magnesiumsulfat. ach Absaugen vom Feststoff wird das Solvens im Vakuum entfernt. Das Rohöl wird durch Vakuumdestillation gereinigt, und man erhält 6.6 g Garnerester 22 (25.5 mmol 65%). Sdp.: C / 1.1 mbar (Lit.: C / 2.7 mbar). 1 H-MR (CDCl 3 ; 250 MHz): δ = 1.42, 1.51 (2x s, 9H; BC CH 3 ), (4x s, 6H; Acetonid CH 3 ), 3.76 (s, 3H; CH 3 ), (m, 2H; H 3), 4.40, 4.51 (2x dd, J 1 = 3.0 Hz, J 2 = 7.0 Hz, 1H; H 2) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (2C; Acetonid CH 3 ), 28.13, (3C; BC CH 3 ), 52.17, (C 2), 59.06, ( CH 3 ), 65.87, (C 3), 80.18, (BC C), 94.27, (Ketal C), (BC C), , (C 1) ppm. [α] D 20 = 54.3 (c = 2.15; CHCl 3 ).
19 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette (2S)-2,3-(-t-Butyloxycarbonylisopropylidenazoxy)-propanal (23) BC BC Me H g Garnermethylester 22 (22.3 mmol) werden unter Argon in 35.2 ml abs. Toluol gelöst. Bei 78 C tropft man 37.3 ml DIBAH-Lösung (1.2 m in Toluol) hinzu und läßt 2 h reagieren. ach Versetzen mit 10.2 ml kaltem Methanol wird die Suspension in 170 ml eisgekühlter 1 m Salzsäure gegeben. Es wird dreimal mit EE extrahiert und die organische Phase über Magnesiumsulfat getrocknet. ach Absaugen und Entfernen des Solvens im Vakuum erhält man 5.6 g Aldehyd 23, welcher durch Vakuumdestillation gereinigt wird. Man erhält 4.0 g Garneraldehyd 23 (17.5 mmol 79%). Sdp.: 93 C / 0.13 mbar 1 H-MR (CDCl 3 ; 250 MHz): δ = (m, 15H; Acetonid CH 3, BC CH 3 ), (m, 2H; H 3), 4.20, 4.36 (2x bs, 1H; H 2), 9.56, 9.63 (2x s, 1H; H 1) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = (2C; Acetonid CH 3 ), (3C; BC CH 3 ), 63.36, (C 3), (C 2), 80.96, (BC C), 94.25, (Ketal C), (BC C), (C 1) ppm. [α] D 20 = 83.8 (c = 1.12; CHCl 3 ) (3R)-3,4-(-t-Butyloxycarbonylisopropylidenazoxy)-1,1-dibrom-1-buten (24) BC BC H CBr Eine Suspension aus 26.5 g Triphenylphosphin und 6.6 g Zink in 255 ml abs. Methylenchlorid wird bei 0 C vorsichtig mit 33.4 g Tetrabrommethan versetzt. Man läßt 18 h auf Raumtemperatur kommend reagieren, ehe bei 0 C 9.1 g Garneraldehyd 23 (39.7 mmol) in 80 ml Methylenchlorid zugetropft werden. ach 18 h gibt man 500 ml n-hexan hinzu, wobei sich ein dunkelbrauner Schleim absetzt, von dem anschließend abdekantiert wird. Der Sumpf wird in 100 ml Methylenchlorid gelöst und erneut mit 500 ml n-hexan versetzt. Man dekantiert wieder
20 Experimenteller Teil: Synthesen zum Aufbau der Seitenkette 135 vom Rückstand ab und wiederholt diese Prozedur ein zweites Mal. Das Solvens der Methylenchlorid-Phase wird im Vakuum entfernt und das erhaltene Rohöl säulenchromatographisch gereinigt (10:1 n-hexan / EE), wobei man 11.5 g Dibromid 24 (29.9 mmol 75%) erhält. 1 H-MR (CDCl 3 ; 250 MHz): δ = (m, 15H; Acetonid CH 3, BC CH 3 ), (m, 1H; H A 4), 4.08 (dd, J 1 = 6.3 Hz, J 2 = 8.8 Hz, 1H; H B 4), (m, 1H; H 3), 6.43 (bd, J = 7.5 Hz, 1H; H 2) ppm. 13 C-MR, DEPT (CDCl 3 ; 63 MHz): δ = 23.79, (2C; Acetonid CH 3 ), (3C; BC CH 3 ), (C 3), (C 4), (BC C), (Ketal C), (C 1), (C 2), (BC C) ppm. MS (70 ev, EI, 60 C): m/e = 385 (M, 2.2), 370 (1.8), 329 (18.0), 316 (25.6), 314 (54.0), 312 (30.1), 270 (28.3), 144 (18.5), 57 (100), 41 (24.2). IR (KBr, Film): 1/λ = 2979 (m), 2934 (w), 2873 (w), 1703 (s), 1477 (w), 1456 (w), 1378 (s), 1366 (s), 1253 (m), 855 (m) cm (3R)-3,4-(-t-Butyloxycarbonylisopropylidenazoxy)-1-butin (25) Methode A: BC CBr 2 BC g Vinyldibromid 24 (11.1 mmol) werden in 52 ml abs. THF gelöst und unter Argon auf 78 C gekühlt. Man tropft 17.9 ml n-buli-lösung (1.6 m in n-hexan) hinzu und läßt 2 h reagieren. Es wird mit Wasser gewaschen und die wässrige Phase dreimal mit Diethylether extrahiert. ach Entfernen des Solvens der organischen Phase im Vakuum wird das Rohöl säulenchromatographisch (20:1 n-hexan / EE) gereinigt, und man erhält 1.2 g Garneralkin 25 (5.4 mmol 49%) und geringe Mengen C4-verlängertes Garnerbutylalkin 26.
Titration von Metallorganylen und Darstellung der dazu benötigten
 Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
2. Herstellung der α,β-ungesättigten Kupplungskomponenten C H 3 H 33. Br 22 25
 2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
5 Chemisch-experimenteller Teil
 5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
Organisch-Chemisches Grundpraktikum. trans-1,2-cyclohexandiol
 rganischhemisches Grundpraktikum Präparat 06: trans1,2yclohexandiol Gliederung: I. Literatur... 1 II. Präparateigenschaften... 1 III. Stöchiometrische Reaktionsgleichung... 1 IV. Reaktionsmechanismus...
rganischhemisches Grundpraktikum Präparat 06: trans1,2yclohexandiol Gliederung: I. Literatur... 1 II. Präparateigenschaften... 1 III. Stöchiometrische Reaktionsgleichung... 1 IV. Reaktionsmechanismus...
2017 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid
 217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
O 3a O 3 (98.1) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.3 [4+2]-Cycloaddition von Cyclopentadien mit Maleinsäureanhydrid zum endobzw. exo-bicyclo[2.2.1]hept-5-en-2,3-dicarbonsäureanhydrid (3, Umwandlung in das exo-addukt 3b C 5 6 (66.1) + C 4 2 3 (98.1)
3.4.3 [4+2]-Cycloaddition von Cyclopentadien mit Maleinsäureanhydrid zum endobzw. exo-bicyclo[2.2.1]hept-5-en-2,3-dicarbonsäureanhydrid (3, Umwandlung in das exo-addukt 3b C 5 6 (66.1) + C 4 2 3 (98.1)
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
4002 Synthese von Benzil aus Benzoin
 4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
NO 2 Rühren mit Magnetrührer, Extrahieren, Ausschütteln, Abrotieren, Umkristallisieren, Abfiltrieren,
 1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von DOC (2,5-Dimethoxy-4-chloramphetamin)
 T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
3021 Oxidation von Anthracen zu Anthrachinon
 xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Organisch-chemisches Praktikum Wintersemester 2005/06. 1-Phenyl-propan-1-ol. Stephan Steinmann
 Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Mustervorschrift 2.3.1
 Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
4009 Synthese von Adipinsäure aus Cyclohexen
 4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
Experimenteller Teil
 II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie
 HPLC 1 Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie 1. Aufgabe In diesem Versuch werden die Retentionszeiten der Substanzen Acetylsalicylsäure (ASS)
HPLC 1 Skript zum Praktikum Instrumentelle Analytik der Universität Heidelberg im 4. Fachsemester Pharmazie 1. Aufgabe In diesem Versuch werden die Retentionszeiten der Substanzen Acetylsalicylsäure (ASS)
4. Experimenteller Teil
 . Experimenteller Teil.. Material und Methoden... Analytik... H-MR-Spektroskopie Sämtliche Substanzen wurden mit Spektrometern des Typs AC 0 oder AC 0 und in besonderen Fällen mit einem AMX 00 der Firma
. Experimenteller Teil.. Material und Methoden... Analytik... H-MR-Spektroskopie Sämtliche Substanzen wurden mit Spektrometern des Typs AC 0 oder AC 0 und in besonderen Fällen mit einem AMX 00 der Firma
3011 Synthese von erythro-9,10-dihydroxystearinsäure aus Ölsäure
 311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
Protokoll zur Übung Ölanalyse
 Protokoll zur Übung Ölanalyse im Rahmen des Praktikums Betreuender Assistent Univ.Ass. Dipl.-Ing. Martin Schwentenwein Verfasser des Protokolls: Daniel Bomze 0726183 1 Theoretischer Hintergrund 1.1 Aufgabenstellung
Protokoll zur Übung Ölanalyse im Rahmen des Praktikums Betreuender Assistent Univ.Ass. Dipl.-Ing. Martin Schwentenwein Verfasser des Protokolls: Daniel Bomze 0726183 1 Theoretischer Hintergrund 1.1 Aufgabenstellung
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH)
 Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Extraktion. Arbeitstechnik der Extraktion
 1 Extraktion Die heute vielfach angewandte Trennung durch Extraktion basiert auf der unterschiedlichen Löslichkeit bestimmter Verbindungen in zwei nicht (od. begrenzt) mischbaren Lösungsmittel. (Das Lösungsmittesystem
1 Extraktion Die heute vielfach angewandte Trennung durch Extraktion basiert auf der unterschiedlichen Löslichkeit bestimmter Verbindungen in zwei nicht (od. begrenzt) mischbaren Lösungsmittel. (Das Lösungsmittesystem
Fachbereich Chemie. der Philipps-Universität Marburg
 Fachbereich Chemie der Philipps-Universität Marburg Skriptum zu den Versuchen Moderne präparative Methoden der organischen Chemie (1. Auflage, April 2004) Versuch 1: (AK Schrader) Enantioselektive Michael-Addition
Fachbereich Chemie der Philipps-Universität Marburg Skriptum zu den Versuchen Moderne präparative Methoden der organischen Chemie (1. Auflage, April 2004) Versuch 1: (AK Schrader) Enantioselektive Michael-Addition
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008
 Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
Biochemisches Grundpraktikum
 Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
c C 2 K = c A 2 c B 2mol /l 2 0,5mol /l 2 4 mol /l K =4l /mol
 Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
Dünnschichtchromatographie. - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie
 Dünnschichtchromatographie - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie Dünnschichtchromatographie (DC) Trennmethode mit vielen Vorteilen gegenüber klassischen Verfahren (Destillation,
Dünnschichtchromatographie - ein kurzes Reptitorium für das 7. bzw. 8. Semester Pharmazie Dünnschichtchromatographie (DC) Trennmethode mit vielen Vorteilen gegenüber klassischen Verfahren (Destillation,
6011 Hippursäure aus Glycin und Benzoylchlorid
 P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
3012 Synthese von Adamantylidenadamantan aus Adamantanon
 Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse
 Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Klausur WS 03/04. 1 Schutzgruppen 10
 Institut für rganische Chemie rganisch-chemisches Fortgeschrittenenpraktikum http://www.chm.tu-dresden.de/organik/hierse/c_fp.htm Name: Erfolgreiche Teilnahme am Praktikum: WS Erfolgreiche Teilnahme am
Institut für rganische Chemie rganisch-chemisches Fortgeschrittenenpraktikum http://www.chm.tu-dresden.de/organik/hierse/c_fp.htm Name: Erfolgreiche Teilnahme am Praktikum: WS Erfolgreiche Teilnahme am
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on)
 6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
Ein Puffer ist eine Mischung aus einer schwachen Säure/Base und ihrer Korrespondierenden Base/Säure.
 2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
Benzol-d. Illumina-Chemie.de - Artikel
 Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
3002 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure
 32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
(R)-(S)-PPFA. (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3. PPh 2
![(R)-(S)-PPFA. (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3. PPh 2 (R)-(S)-PPFA. (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3. PPh 2](/thumbs/30/14148963.jpg) (R)-(S)-PPFA (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3 NMe 2 Fe PPh 2 Abstract Mit (R)-N,N-Dimethylferrocenylethylamin wird eine Enantiomerenanreicherung durchgeführt und dann
(R)-(S)-PPFA (R)-1-N,N-Dimethyl-[(S)-2-(diphenylphosphino)ferrocenyl]ethylamin CH 3 NMe 2 Fe PPh 2 Abstract Mit (R)-N,N-Dimethylferrocenylethylamin wird eine Enantiomerenanreicherung durchgeführt und dann
Schlussbericht. Studienwoche Chemie und Materialwissenschaften 2014
 Schlussbericht Studienwoche Chemie und Materialwissenschaften 2014 Zum Projekt Synthese des künstlichen Süßstoffes Aspartam und qualitativer Nachweis der Verbindung in ausgewählten Produkten Betreut von
Schlussbericht Studienwoche Chemie und Materialwissenschaften 2014 Zum Projekt Synthese des künstlichen Süßstoffes Aspartam und qualitativer Nachweis der Verbindung in ausgewählten Produkten Betreut von
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
Bestimmung des Stickstoffgehalts von Erde
 Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol
 3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Säure-Base-Reaktion. Versuch 5.1 5.2. Neutralisation, Gehaltsbestimmungen und Titrationskurven
 Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
ÖAB Report. Monographie Sulfadimidin-Natrium. Betreff: A. Mayrhofer, 23.05.2013 ------------------------------------------------------
 BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report Betreff: Monographie Sulfadimidin-Natrium VORWORT Die Basis-Monographie Sulfadimidin ist in der Ph. Eur. enthalten und wurde kürzlich
BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report Betreff: Monographie Sulfadimidin-Natrium VORWORT Die Basis-Monographie Sulfadimidin ist in der Ph. Eur. enthalten und wurde kürzlich
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3.3 Entparaffinierung durch Extraktion. Aufbau. Gefahren. Aufbau. Naturwissenschaften - Chemie - Organische Chemie - 3 Erdöl
 Naturwissenschaften - Chemie - Organische Chemie - 3 Erdöl (P77400) 3.3 Entparaffinierung durch Extraktion Experiment von: seb Gedruckt: 7.03.204 4:55:40 intertess (Version 3.2 B24, Export 2000) Aufbau
Naturwissenschaften - Chemie - Organische Chemie - 3 Erdöl (P77400) 3.3 Entparaffinierung durch Extraktion Experiment von: seb Gedruckt: 7.03.204 4:55:40 intertess (Version 3.2 B24, Export 2000) Aufbau
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
Synthese von Acetessigsäureethylester
 Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Meisterwurz. Imperatoriae Radix. Radix Imperatoriae
 ÖAB xxxx/xxx Meisterwurz Imperatoriae Radix Radix Imperatoriae Definition Das ganze oder geschnittene, getrocknete Rhizom und die Wurzel von Peucedanum ostruthium (L.) KCH. Gehalt: mindestens 0,40 Prozent
ÖAB xxxx/xxx Meisterwurz Imperatoriae Radix Radix Imperatoriae Definition Das ganze oder geschnittene, getrocknete Rhizom und die Wurzel von Peucedanum ostruthium (L.) KCH. Gehalt: mindestens 0,40 Prozent
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Kap.7 ph-wert und ph-indikatoren
 Der ph-wert und ph-indikatoren Kapitel 7 Übung 6.1: Berechnung der Konzentration von Wasser in Wasser Wieviel mol H2O sind in 1 L H2O? M(H2O)= 18.01528 g/mol 1 L(H2O)= 00g H2O n= m/m= 00g/ 18.01528 g/mol
Der ph-wert und ph-indikatoren Kapitel 7 Übung 6.1: Berechnung der Konzentration von Wasser in Wasser Wieviel mol H2O sind in 1 L H2O? M(H2O)= 18.01528 g/mol 1 L(H2O)= 00g H2O n= m/m= 00g/ 18.01528 g/mol
Organisch chemisches Praktikum II
 18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid
 4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid
 NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
Laborprotokoll. Trennung von Chlorophyll a und Chlorophyll b mittels Säulenchromatographie
 Laborprotokoll Trennung von Chlorophyll a und Chlorophyll b mittels Säulenchromatographie Cédric Birrer (E46) Michel Rickhaus (E45) Anna-Caterina Senn (E44) Juni 2007 Inhaltsverzeichnis 1 Versuchsziel...
Laborprotokoll Trennung von Chlorophyll a und Chlorophyll b mittels Säulenchromatographie Cédric Birrer (E46) Michel Rickhaus (E45) Anna-Caterina Senn (E44) Juni 2007 Inhaltsverzeichnis 1 Versuchsziel...
Anorganisches Praktikum 1. Semester. FB Chemieingenieurwesen. Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften
 Anorganisches Praktikum 1. Semester FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften 1 Gravimetrie Bestimmung von Nickel Sie erhalten eine Lösung, die 0.1-0.2g
Anorganisches Praktikum 1. Semester FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften 1 Gravimetrie Bestimmung von Nickel Sie erhalten eine Lösung, die 0.1-0.2g
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon)
 1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
4. Quantitative Bestimmung von Eisen(II) durch Redoxtitration mit Kaliumpermanganat
 Redoxtitration 29. Quantitative Bestimmung von Eisen(II) durch Redoxtitration mit Kaliumpermanganat Einleitung Eisen ist das mit Abstand wichtigste Gebrauchsmetall. Aufgrund seines elektrochemisch sehr
Redoxtitration 29. Quantitative Bestimmung von Eisen(II) durch Redoxtitration mit Kaliumpermanganat Einleitung Eisen ist das mit Abstand wichtigste Gebrauchsmetall. Aufgrund seines elektrochemisch sehr
Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle Reaktion: Saccharose
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle Reaktion: Saccharose
Als Grundlage für die Revision wird die Monographie gemäß HELV. mit folgendem Änderungsvorschlag herangezogen:
 !!! NEE ÖAB-MONOGAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
!!! NEE ÖAB-MONOGAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
Versuch: Siedediagramm eines binären Gemisches
 Versuch: Siedediagramm eines binären Gemisches Aufgaben - Kalibriermessungen Bestimmen Sie experimentell den Brechungsindex einer gegebenen Mischung bei unterschiedlicher Zusammensetzung. - Theoretische
Versuch: Siedediagramm eines binären Gemisches Aufgaben - Kalibriermessungen Bestimmen Sie experimentell den Brechungsindex einer gegebenen Mischung bei unterschiedlicher Zusammensetzung. - Theoretische
Abgestufte Lernhilfen
 Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
4 Experimenteller Teil
 4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
Lernzirkel WAS Station 1 Herstellung von Seife aus Kokosfett
 Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Synthesevorschriften für die Grundpräparate
 Laborübungen aus rganischer Chemie Institut für Chemie, Synthesevorschriften für die Grundpräparate Acetanilid ß-Aminocrotonsäure-ethylester A-1. Acetanilid Reaktionstyp: Aminolyse eines Carbonsäurederivats
Laborübungen aus rganischer Chemie Institut für Chemie, Synthesevorschriften für die Grundpräparate Acetanilid ß-Aminocrotonsäure-ethylester A-1. Acetanilid Reaktionstyp: Aminolyse eines Carbonsäurederivats
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
SKRIPT ZUM INTEGRIERTEN SYNTHESEPRAKTIKUM
 Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Organisches Praktikum I - SS 2006 Assistentin: Gabi Marti. Synthese von. Isobutylacetat. Zürich, Balzers & Eschen, Mai 2005
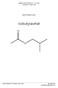 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
Experiment Isolierung, Aktivität und Hemmung der Carboanhydrase
 Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Baldriantinktur, etherische Valerianae tinctura aetherea
 Baldriantinktur, etherische Valerianae tinctura aetherea ÖAB 2009/048 Definition Baldriantinktur, etherische, wird aus Etheralkohol (Ether + Ethanol: 1 + 3 V/V) und Baldrianwurzel (Valerianae radix) hergestellt.
Baldriantinktur, etherische Valerianae tinctura aetherea ÖAB 2009/048 Definition Baldriantinktur, etherische, wird aus Etheralkohol (Ether + Ethanol: 1 + 3 V/V) und Baldrianwurzel (Valerianae radix) hergestellt.
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Protokoll des Versuches 7: Umwandlung von elektrischer Energie in Wärmeenergie
 Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 7: Umwandlung von elektrischer Energie in ärmeenergie Verantwortlicher
Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 7: Umwandlung von elektrischer Energie in ärmeenergie Verantwortlicher
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
Darstellung von Chelidamsäure (gekürzte Version)
 CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol
 1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
merken!!! 29,22 g NaCl abwiegen, in einem Becher mit etwa 800 ml Wasser lösen, dann im Messzylinder auf 1000 ml auffüllen.
 Das ABC der Stöchiometrie Lösungen aus Feststoffen Molare Lösungen herstellen (m = M c V) Beispiel 1: 1 L einer 500 mm NaCl-Lösung herstellen. Masse: Volumen: Stoffmenge: Dichte: m (kg) V (L) n (mol) (kg/l)
Das ABC der Stöchiometrie Lösungen aus Feststoffen Molare Lösungen herstellen (m = M c V) Beispiel 1: 1 L einer 500 mm NaCl-Lösung herstellen. Masse: Volumen: Stoffmenge: Dichte: m (kg) V (L) n (mol) (kg/l)
